Предпосылки создания изобретения
Область техники, к которой относится изобретение
Некоторые аспекты настоящего изобретения относятся к способам лечения психоневрологических расстройств, боли и других расстройств соединениями, которые модулируют активность мускариновых рецепторов, в частности, подтипов М1, причем посредством этого модулируется неврональная активность, связанная с развитием психоневрологических расстройств. Аспекты изобретения также относятся к соединениям, селективно взаимодействующим с данным подтипом рецепторов, и способам идентификации указанных соединений.
Описание уровня техники
Мускариновые холинергические рецепторы опосредуют действие нейротрансмиттера ацетилхолина в центральной и периферической нервных системах, желудочно-кишечной системе, сердце, эндокринных железах, легких и других тканях. Мускариновые рецепторы играют центральную роль в центральной нервной системе в отношении когнитивных функций, а также в периферической нервной парасимпатической нервной системе. Идентифицированы пять различных подтипов мускариновых рецепторов m1-m5. Подтип m1 является преобладающим подтипом, обнаруженным в коре головного мозга, и, как полагают, участвует в регуляции когнитивных функций; подтип m2 является преобладающим подтипом, обнаруженным в сердце, и, как полагают, участвует в регуляции частоты сердечных сокращений; полагают, что m3 участвует в стимуляции желудочно-кишечного тракта и мочевых путей, а также в потоотделении и слюноотделении; m4 присутствует в головном мозге и может участвовать в локомоции; и m5 присутствует в головном мозге и может участвовать в некоторых функциях центральной нервной системы, связанных с дофаминергической системой.
Состояния, связанные с когнитивным ухудшением, такие как болезнь Альцгеймера, сопровождаются потерей ацетилхолина в головном мозге. Полагают, что это является результатом дегенерации холинергических нейронов в базальном переднем мозге, которые иннервируют области ассоциативной зоны, и гиппокампе, участвующем в более критических процессах.
Усилия для повышения уровней ацетилхолина фокусировались на повышении уровней холина - предшественника для синтеза ацетилхолина и на блокировке ацетилхолинэстеразы (AChE) - фермента, который метаболизирует ацетилхолин. Введение холина или фосфатидилхолина не стало достаточно успешным. Ингибиторы AChE показывают некоторую лечебную эффективность, но могут вызывать холинергическое побочное действие из-за стимуляции периферического ацетилхолина, в том числе, абдоминальные судороги, тошноту, рвоту, диарею, анорексию, потерю массы, миопатию и депрессию. Побочное действие на желудочно-кишечный тракт наблюдали у примерно трети пациентов, которых лечили. Кроме того, также обнаружено, что некоторые ингибиторы AChE, такие как такрин, вызывают существенную гепатотоксичность с повышением содержания трансаминаз в печени, наблюдаемым у примерно 30% пациентов. Вредное действие ингибиторов AChE ограничивает их клиническую применимость.
Также обнаружено, что известные агонисты мускариновых m1, такие как ареколин, являются слабыми агонистами подтипа m2, а также m3, и не очень эффективны при лечении когнитивного нарушения, наиболее вероятно, из-за ограничения дозы побочным действием.
Существует потребность в соединениях, усиливающих передачу сигнала или действие ацетилхолина в головном мозге. Конкретно, существует потребность в мускариновых агонистах, активных в отношении различных подтипов мускариновых рецепторов в центральной и периферической нервной системе. Кроме того, существует потребность в более высокоселективных мускариновых агонистах, таких как m1- или m4-селективные средства, как в качестве фармакологических инструментов, так и в качестве лечебных средств.
Сущность изобретения
Изобретение относится к соединению формулы I, II или XV


или его фармацевтически приемлемой соли, сложному эфиру, амиду или пролекарству, где в указанных формулах А выбирают из группы, состоящей из
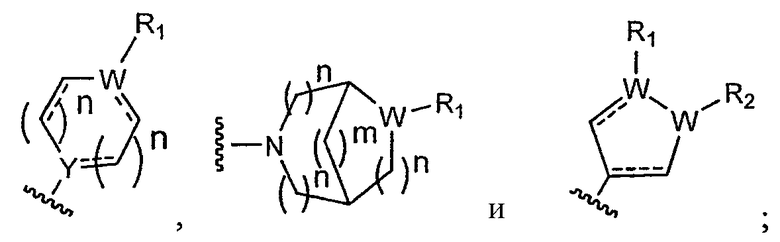
Х представляет собой азот, СН или СН2; X' представляет собой С или СН, где, когда X' представляет собой С, существует двойная связь между Х и X', и, когда X' представляет собой СН, существует простая связь между Х и X'; каждый Y выбирают, по отдельности, из группы, состоящей из азота, кислорода или СН; каждый W выбирают, по отдельности, из группы, состоящей из азота, СН, кислорода или серы; каждый n выбирают, по отдельности, из группы, состоящей из 0, 1, 2, 3 и 4; m выбирают из группы, состоящей из 1, 2 и 3; каждый R1, по отдельности, отсутствует или его, по отдельности, выбирают из группы, состоящей из водорода, галогена, амина, необязательно замещенного С1-20алкила, необязательно замещенного С3-8циклоалкила, необязательно замещенного С2-20алкенила, необязательно замещенного С2-20алкинила, необязательно замещенного С1-20алкоксиалкила и необязательно замещенного арила и арилалкила; L отсутствует или его выбирают из группы, состоящей из -NH(CH2)n- и -(CH2)n-; a, b, c и d выбирают, каждый независимо, из группы, состоящей из углерода, азота, кислорода и серы, или каждый из них, независимо, отсутствует, при условии, что присутствуют, по меньшей мере, три из a, b, c или d, при условии, что, по меньшей мере, один из a, b, c или d представляет собой атом углерода, и при условии, что два соседних из a, b, c или d оба не являются атомами кислорода или атомами серы; e, f, g и h выбирают, каждый независимо, из группы, состоящей из углерода, азота, кислорода и серы, или каждый из них, независимо, отсутствует, при условии, что присутствуют, по меньшей мере, три из e, f, g или h, при условии, что, по меньшей мере, один из e, f, g или h представляет собой атом углерода, и при условии, что два соседних из e, f, g или h оба не являются атомами кислорода или атомами серы; R2, R3, R4 и R5 выбирают, каждый независимо, из группы, состоящей из водорода, галогена, необязательно замещенного С1-6алкила, необязательно замещенного С1-6алкилокси, необязательно замещенного С2-6алкенила, необязательно замещенного С2-6алкинила, необязательно замещенного С1-6алкоксиалкила, необязательно замещенного С1-6алкилтио, пергалогеналкила, CN, COR10, CONHR10, NHCONHR10, SO2NHR10, SO2R10, OSO2R10, гетероалкила, NO2, NHCOR10, или R2 и R3, или R3 и R4, или R4 и R5, взятые вместе и вместе с атомами углерода кольца, к которым они присоединены, образуют пятичленное или шестичленное циклоалкильное, гетероциклильное или гетероарильное кольцо или шестичленную арильную группу; R6, R7, R8 и R9 выбирают, каждый независимо, из группы, состоящей из водорода, галогена, необязательно замещенного С1-6алкила, необязательно замещенного С1-6алкилокси, необязательно замещенного С2-6алкенила, необязательно замещенного С2-6алкинила, необязательно замещенного С1-6алкоксиалкила, необязательно замещенного С1-6алкилтио, пергалогеналкила, CN, COR10, CONHR10, NHCONHR10, SO2NHR10, SO2R10, OSO2R10, гетероалкила, NO2, NHCOR10, или R6 и R7, или R7 и R8, или R8 и R9, взятые вместе и вместе с атомами углерода кольца, к которым они присоединены, образуют пятичленное или шестичленное циклоалкильное, гетероциклильное или гетероарильное кольцо или шестичленную арильную группу; Z выбирают из группы, состоящей из NR11, кислорода, серы и СН2; R10 выбирают из группы, состоящей из водорода, необязательно замещенного С1-6алкила, необязательно замещенного С3-8циклоалкила, необязательно замещенного С2-6алкенила, необязательно замещенного С2-6алкинила, необязательно замещенного арила, необязательно замещенного арилалкила и пергалогеналкила; и R11 выбирают из группы, состоящей из водорода, необязательно замещенного С1-6алкила, необязательно замещенного С3-8циклоалкила, необязательно замещенного С2-6алкенила, необязательно замещенного С2-6алкинила и необязательно замещенного арилалкила; R12 и R13 выбирают, по отдельности, из группы, состоящей из водорода, галогена, необязательно замещенного С1-6алкила, необязательно замещенного С1-6алкилокси, необязательно замещенного С2-6алкенила, необязательно замещенного С2-6алкинила, необязательно замещенного С1-6алкоксиалкила, необязательно замещенного С1-6алкилтио, пергалогеналкила, CN, COR10, CONHR10, NHCONHR10, SO2NHR10, SO2R10, OSO2R10, гетероалкила, NO2, NHCOR10, или R12 и R13, взятые вместе и вместе с атомами углерода кольца, к которым они присоединены, образуют пятичленное или шестичленное циклоалкильное, гетероциклильное или гетероарильное кольцо или шестичленную арильную группу; и любая связь, представленная пунктирной и сплошной линией, представляет связь, выбранную из группы, состоящей из простой углерод-углеродной связи и двойной углерод-углеродной связи; при условии, что соединение формулы I или XV не является клозапином или N-десметилклозапином.
В некоторых вариантах осуществления соединение имеет структуру, представленную формулами III или IV
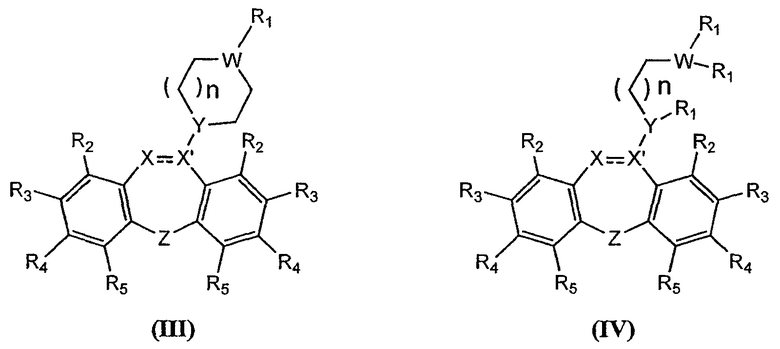 .
.
В некоторых вариантах осуществления соединение выбирают из группы, состоящей из
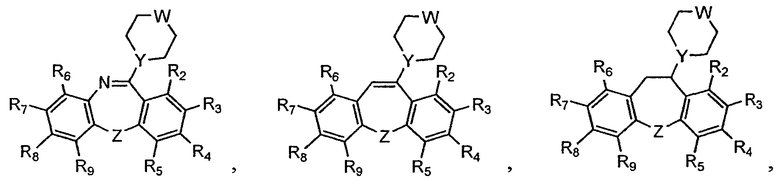

В некоторых вариантах осуществления соединение выбирают из группы, состоящей из
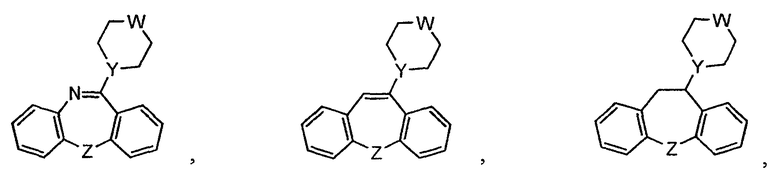

В некоторых вариантах осуществления ни один из a, b, c или d не отсутствует. В некоторых вариантах осуществления ни один из е, f, g или h не отсутствует. В некоторых вариантах осуществления a, b, c и d являются атомом углерода. В некоторых вариантах осуществления е, f, g и h являются атомом углерода. В некоторых вариантах осуществления R2 выбирают из группы, состоящей из водорода, галогена, необязательно замещенного С1-6алкила и необязательно замещенного С1-6алкилокси. В некоторых вариантах осуществления алкил выбирают из группы, состоящей из метила, этила, пропила, изопропила, бутила, втор-бутила и трет-бутила. В некоторых вариантах осуществления алкилокси выбирают из группы, состоящей из метокси, этокси, пропокси, изопропокси, бутокси, втор-бутокси и трет-бутокси. В некоторых вариантах осуществления галоген выбирают из группы, состоящей из фтора, хлора и брома. В некоторых вариантах осуществления R2 выбирают из группы, состоящей из водорода, метила, метокси и хлора. В некоторых вариантах осуществления R3 выбирают из группы, состоящей из водорода, галогена, необязательно замещенного С1-6алкила, необязательно замещенного С1-6алкилокси и NO2. В некоторых вариантах осуществления алкил выбирают из группы, состоящей из метила, этила, пропила, изопропила, бутила, втор-бутила и трет-бутила. В некоторых вариантах осуществления алкилокси выбирают из группы, состоящей из метокси, этокси, пропокси, изопропокси, бутокси, втор-бутокси и трет-бутокси. В некоторых вариантах осуществления галоген выбирают из группы, состоящей из хлора, брома и иода. В некоторых вариантах осуществления R3 выбирают из группы, состоящей из водорода, метила, метокси, хлора, брома, иода и NO2. В некоторых вариантах осуществления R4 выбирают из группы, состоящей из водорода, галогена, необязательно замещенного С1-6алкила, пергалогеналкила, SO2R10 и NO2. В некоторых вариантах осуществления алкил выбирают из группы, состоящей из метила, этила, пропила, изопропила, бутила, втор-бутила и трет-бутила. В некоторых вариантах осуществления пергалогеналкил представляет собой перфторалкил. В некоторых вариантах осуществления пергалогеналкил представляет собой трифторметил. В некоторых вариантах осуществления галоген выбирают из группы, состоящей из фтора, хлора и брома. В некоторых вариантах осуществления R10 представляет собой водород или необязательно замещенный С1-6алкил, где в некоторых вариантах осуществления алкил выбирают из группы, состоящей из метила, этила, пропила, изопропила, бутила, втор-бутила и трет-бутила. В некоторых вариантах осуществления R4 выбирают из группы, состоящей из водорода, метила, фтора, хлора, брома, трифторметила, SO2СН3 и NO2. В некоторых вариантах осуществления R5 выбирают из группы, состоящей из водорода, галогена и необязательно замещенного С1-6алкила, где в некоторых вариантах осуществления алкил выбирают из группы, состоящей из метила, этила, пропила, изопропила, бутила, втор-бутила и трет-бутила, и где в некоторых вариантах осуществления галоген выбирают из группы, состоящей из фтора, хлора и брома. В некоторых вариантах осуществления R5 представляет собой водород или хлор. В некоторых вариантах осуществления R6 представляет собой водород или необязательно замещенный С1-6алкил. В некоторых вариантах осуществления R6 представляет собой водород. В некоторых вариантах осуществления R7 выбирают из группы, состоящей из водорода, галогена, необязательно замещенного С1-6алкила, пергалогеналкила, CN, SO2R10 и NO2, где в некоторых вариантах осуществления алкил выбирают из группы, состоящей из метила, этила, пропила, изопропила, бутила, втор-бутила и трет-бутила; где в некоторых вариантах осуществления галоген выбирают из группы, состоящей из фтора, хлора и брома; где в некоторых вариантах осуществления пергалогеналкил представляет собой перфторалкил; где в некоторых вариантах осуществления перфторалкил представляет собой трифторметил. В некоторых вариантах осуществления R10 представляет собой водород или необязательно замещенный С1-6алкил, где в некоторых вариантах осуществления алкил выбирают из группы, состоящей из метила, этила, пропила, изопропила, бутила, втор-бутила и трет-бутила. В некоторых вариантах осуществления R7 выбирают из группы, состоящей из водорода, метила, хлора, трифторметила, SO2СН3, CN и NO2. В некоторых вариантах осуществления R8 выбирают из группы, состоящей из водорода, галогена, необязательно замещенного С1-6алкила, где в некоторых вариантах осуществления алкил выбирают из группы, состоящей из метила, этила, пропила, изопропила, бутила, втор-бутила и трет-бутила, и где в некоторых вариантах осуществления галоген выбирают из группы, состоящей из фтора, хлора и брома. В некоторых вариантах осуществления R8 выбирают из группы, состоящей из водорода, хлора и брома. В некоторых вариантах осуществления R9 выбирают из группы, состоящей из водорода, галогена, необязательно замещенного С1-6алкила и пергалогеналкила; где в некоторых вариантах осуществления алкил выбирают из группы, состоящей из метила, этила, пропила, изопропила, бутила, втор-бутила и трет-бутила; где в некоторых вариантах осуществления галоген выбирают из группы, состоящей из фтора, хлора и брома; где в некоторых вариантах осуществления пергалогеналкил представляет собой перфторалкил; где в некоторых вариантах осуществления перфторалкил представляет собой трифторметил. В некоторых вариантах осуществления R9 выбирают из группы, состоящей из водорода, хлора, метила и трифторметила. В некоторых вариантах осуществления R1 выбирают из группы, состоящей из водорода, необязательно замещенного С1-6алкила и необязательно замещенного арила, где в некоторых вариантах осуществления алкил выбирают из группы, состоящей из метила, этила, пропила, изопропила, бутила, втор-бутила и трет-бутила. В некоторых вариантах осуществления R1 представляет собой водород. В некоторых вариантах осуществления Х представляет собой азот. В некоторых вариантах осуществления Y представляет собой NH. В некоторых вариантах осуществления L отсутствует или его выбирают из группы, состоящей из -NHCH2-, -NH- и -СН2-. В некоторых вариантах осуществления А выбирают из группы, состоящей из
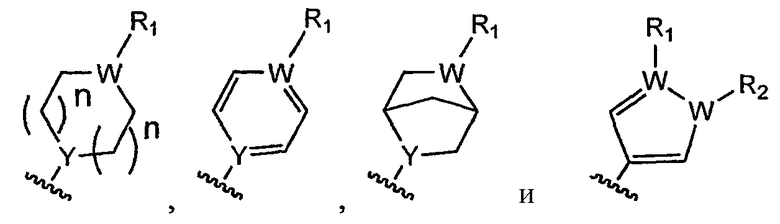
и n выбирают из группы, состоящей из 0, 1 и 2.
Данное изобретение также относится к способу получения соединения формулы V или VI

включающему взаимодействие соединения формулы VII
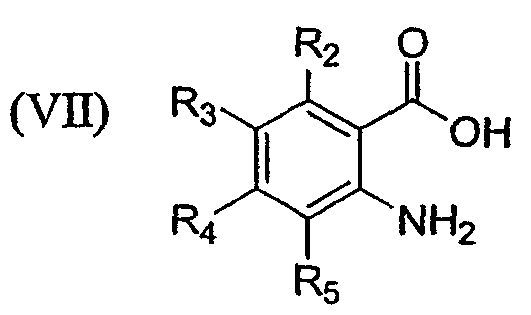
с соединением формулы VIII
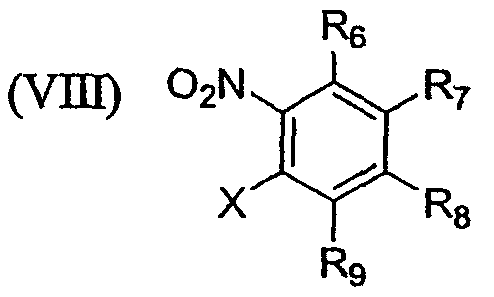
с образованием конденсированного циклического соединения формулы IX
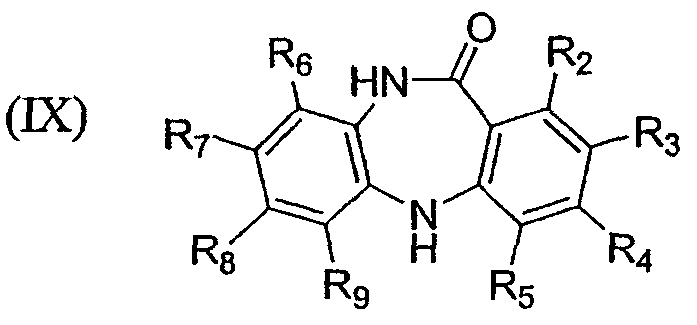
и взаимодействие соединения формулы IX с соединением формулы Х

с образованием соединения формулы V, где Х представляет собой галоген; R1 выбирают из группы, состоящей из водорода, необязательно замещенного С1-6алкила, необязательно замещенного С3-8циклоалкила, необязательно замещенного С2-6алкенила, необязательно замещенного С2-6алкинила, необязательно замещенного С1-6алкоксиалкила и необязательно замещенного арила и арилалкила; R2, R3, R4 и R5 выбирают, каждый независимо, из группы, состоящей из водорода, галогена, необязательно замещенного С1-6алкила, необязательно замещенного С1-6алкилокси, необязательно замещенного С2-6алкенила, необязательно замещенного С2-6алкинила, необязательно замещенного С1-6алкоксиалкила, необязательно замещенного С1-6алкилтио, пергалогеналкила, CN, COR10, CONHR10, NHCONHR10, SO2NHR10, SO2R10, OSO2R10, гетероалкила, NO2, NHCOR10, или R2 и R3, или R3 и R4, или R4 и R5, взятые вместе и вместе с атомами углерода кольца, к которым они присоединены, образуют пятичленное или шестичленное циклоалкильное, гетероциклильное или гетероарильное кольцо или шестичленную арильную группу; R6, R7, R8 и R9 выбирают, каждый независимо, из группы, состоящей из водорода, галогена, необязательно замещенного С1-6алкила, необязательно замещенного С1-6алкилокси, необязательно замещенного С2-6алкенила, необязательно замещенного С2-6алкинила, необязательно замещенного С1-6алкоксиалкила, необязательно замещенного С1-6алкилтио, пергалогеналкила, CN, COR10, CONHR10, NHCONHR10, SO2NHR10, SO2R10, OSO2R10, гетероалкила, NO2, NHCOR10, или R6 и R7, или R7 и R8, или R8 и R9, взятые вместе и вместе с атомами углерода кольца, к которым они присоединены, образуют пятичленное или шестичленное циклоалкильное, гетероциклильное или гетероарильное кольцо или шестичленную арильную группу.
Данное изобретение также относится к комбинаторной библиотеке из, по меньшей мере, 220 соединений дибензо[b,e][1,4]диазепин[a,d]циклогептена, которые можно получить взаимодействием соединения формулы VII

с соединением формулы VIII

и соединением формулы Х

где Х представляет собой галоген; R1 выбирают из группы, состоящей из водорода, необязательно замещенного С1-6алкила, необязательно замещенного С3-8циклоалкила, необязательно замещенного С2-6алкенила, необязательно замещенного С2-6алкинила, необязательно замещенного С1-6алкоксиалкила и необязательно замещенного арила и арилалкила; R2, R3, R4 и R5 выбирают, каждый независимо, из группы, состоящей из водорода, галогена, необязательно замещенного С1-6алкила, необязательно замещенного С1-6алкилокси, необязательно замещенного С2-6алкенила, необязательно замещенного С2-6алкинила, необязательно замещенного С1-6алкоксиалкила, необязательно замещенного С1-6алкилтио, пергалогеналкила, CN, COR10, CONHR10, NHCONHR10, SO2NHR10, SO2R10, OSO2R10, гетероалкила, NO2, NHCOR10, или R2 и R3, или R3 и R4, или R4 и R5, взятые вместе и вместе с атомами углерода кольца, к которым они присоединены, образуют пятичленное или шестичленное циклоалкильное, гетероциклильное или гетероарильное кольцо или шестичленную арильную группу; R6, R7, R8 и R9 выбирают, каждый независимо, из группы, состоящей из водорода, галогена, необязательно замещенного С1-6алкила, необязательно замещенного С1-6алкилокси, необязательно замещенного С2-6алкенила, необязательно замещенного С2-6алкинила, необязательно замещенного С1-6алкоксиалкила, необязательно замещенного С1-6алкилтио, пергалогеналкила, CN, COR10, CONHR10, NHCONHR10, SO2NHR10, SO2R10, OSO2R10, гетероалкила, NO2, NHCOR10, или R6 и R7, или R7 и R8, или R8 и R9, взятые вместе и вместе с атомами углерода кольца, к которым они присоединены, образуют пятичленное или шестичленное циклоалкильное, гетероциклильное или гетероарильное кольцо или шестичленную арильную группу.
Данное изобретение также относится к комбинаторной библиотеке из, по меньшей мере, 220 соединений дибензо[b,e][1,4]диазепин[a,d]циклогептена, которые можно получить взаимодействием соединения формулы VII

с соединением формулы VIII

и соединением формулы Х
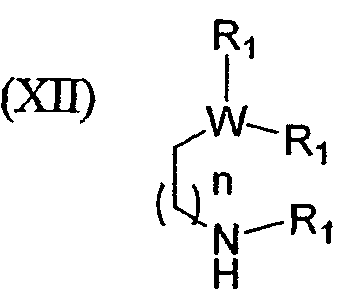
где Х представляет собой галоген; R1 выбирают из группы, состоящей из водорода, необязательно замещенного С1-6алкила, необязательно замещенного С3-8циклоалкила, необязательно замещенного С2-6алкенила, необязательно замещенного С2-6алкинила, необязательно замещенного С1-6алкоксиалкила и необязательно замещенного арила и арилалкила; R2, R3, R4 и R5 выбирают, каждый независимо, из группы, состоящей из водорода, галогена, необязательно замещенного С1-6алкила, необязательно замещенного С1-6алкилокси, необязательно замещенного С2-6алкенила, необязательно замещенного С2-6алкинила, необязательно замещенного С1-6алкоксиалкила, необязательно замещенного С1-6алкилтио, пергалогеналкила, CN, COR10, CONHR10, NHCONHR10, SO2NHR10, SO2R10, OSO2R10, гетероалкила, NO2, NHCOR10, или R2 и R3, или R3 и R4, или R4 и R5, взятые вместе и вместе с атомами углерода кольца, к которым они присоединены, образуют пятичленное или шестичленное циклоалкильное, гетероциклильное или гетероарильное кольцо или шестичленную арильную группу; R6, R7, R8 и R9 выбирают, каждый независимо, из группы, состоящей из водорода, галогена, необязательно замещенного С1-6алкила, необязательно замещенного С1-6алкилокси, необязательно замещенного С2-6алкенила, необязательно замещенного С2-6алкинила, необязательно замещенного С1-6алкоксиалкила, необязательно замещенного С1-6алкилтио, пергалогеналкила, CN, COR10, CONHR10, NHCONHR10, SO2NHR10, SO2R10, OSO2R10, гетероалкила, NO2, NHCOR10, или R6 и R7, или R7 и R8, или R8 и R9, взятые вместе и вместе с атомами углерода кольца, к которым они присоединены, образуют пятичленное или шестичленное циклоалкильное, гетероциклильное или гетероарильное кольцо или шестичленную арильную группу.
Данное изобретение также относится к фармацевтической композиции, содержащей физиологически приемлемый носитель, разбавитель или эксципиент или их сочетание и соединение формулы I, II или XV.
Данное изобретение также относится к способу лечения психоневрологического расстройства, включающему введение пациенту терапевтически эффективного количества соединения формулы I, II или XV.
Данное изобретение также относится к способу лечения психоневрологического расстройства, включающему контактирование терапевтически эффективного количества соединения формулы I, II или XV с пациентом.
Данное изобретение также относится к фармацевтической композиции, содержащей соединение формулы I, II или XV и психоневрологическое средство. В некоторых вариантах осуществления психоневрологическое средство выбирают из группы, состоящей из селективного ингибитора повторного поглощения серотонина, ингибитора повторного поглощения норэпинефрина, агониста дофамина, антагониста мускариновых рецепторов, антипсихотического средства, антагониста серотонина 2А и обратного агониста серотонина 2А. В некоторых вариантах осуществления антипсихотическое средство выбирают из группы, состоящей из фенотиазина, фенилбутилпиперадина, дебензапина, бензизоксидила и соли лития. В некоторых вариантах осуществления фенотиазин выбирают из группы, состоящей из хлорпромазина (Thorazine®), мезоридазина (Serentil®), прохлорперазина (Compazine®) и тиоридазина (Mellaril®). В некоторых вариантах осуществления фенилбутилпиперадины выбирают из группы, состоящей из галоперидола (Haldol®) и пимозида (Orap®). В некоторых вариантах осуществления дебензапин выбирают из группы, состоящей из клозапина (Clozaril®), локсапина (Loxitane®), оланзапина (Zyprexa®) и кветиапина (Seroquel®). В некоторых вариантах осуществления бензизоксидил выбирают из группы, состоящей из респеридона (Resperidal®) и ципразидона (Geodon®). В некоторых вариантах осуществления соль лития представляет собой карбонат лития. В некоторых вариантах осуществления антипсихотическое средство выбирают из группы, состоящей из Clozaril, Compazine, Etrafon, Geodon, Haldol, Inapsine, Loxitane, Mellaril, Moban, Navane, Orap, Permitil, Prolixin, Phenergan, Reglan, Risperdal, Serentil, Seroquel, Stelazine, Taractan, Thorazine, Triavil, Trilafon и Zyprexa. В некоторых вариантах осуществления селективный ингибитор повторного поглощения серотонина выбирают из группы, состоящей из флуоксетина, флувоксамина, сертралина, пароксетина, циталопрама, эсциталопрама, сибутрамина, дулоксетина и венлафаксина, и их фармацевтически приемлемых солей и пролекарств. В некоторых вариантах осуществления ингибитор повторного поглощения норэпинефрина выбирают из группы, состоящей из тионизоксетина и ребоксетина. В некоторых вариантах осуществления агонист допамина выбирают из группы, состоящей из суматриптана, альмотриптана, наратриптана, фроватриптана, ризатриптана, зомитриптана, каберголина, амантадина, лизурида, перголида, ропинирола, прамипексола и бромокриптина. В некоторых вариантах осуществления обратный агонист серотонина 2А представляет собой соединение формулы XIII или его родственный аналог.
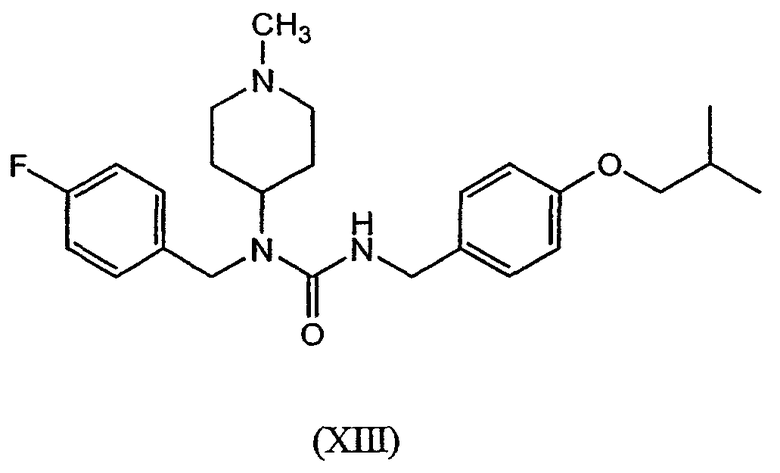
В некоторых вариантах осуществления антагонист серотонина 2А представляет собой соединение формулы XIV или его родственный аналог.
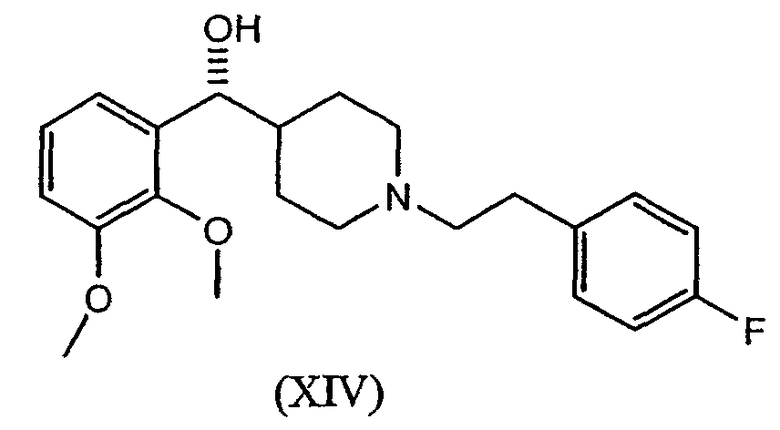 .
.
Данное изобретение также относится к способу лечения психоневрологического расстройства у пациента, включающему введение пациенту терапевтически эффективного количества фармацевтической композиции, содержащей соединение формулы I, II или XV и психоневрологическое средство.
Данное изобретение также относится к способу лечения психоневрологического расстройства у пациента, включающему введение пациенту терапевтически эффективного количества соединения формулы I, II или XV и терапевтически эффективного количества психоневрологического средства. В некоторых вариантах осуществления стадия введения включает введение соединения формулы I, II или XV и психоневрологического средства почти одновременно. В других вариантах осуществления стадия введения включает введение сначала одного активного начала из числа соединения формулы I, II или XV и психоневрологического средства и затем введение другого активного начала из числа соединения формулы I, II или XV и психоневрологического средства. В некоторых вариантах осуществления психоневрологическое расстройство выбирают из группы, состоящей из шизофрении и родственных идиопатических психозов, тревоги, расстройств сна, расстройств аппетита, аффективных расстройств, таких как большая депрессия, биполярное расстройство и депрессия с психотическими признаками, и синдрома Туретта, психозов, вызванных лекарственными средствами, психозов, вторичных по отношению к психоневрологическим расстройствам, таких как болезнь Альцгеймера или болезнь Гентингтона.
Подробное описание предпочтительных вариантов осуществления
В первом аспекте настоящее изобретение относится к соединению формулы I, II или XV


или его фармацевтически приемлемой соли, сложному эфиру, амиду или пролекарству, где в указанных формулах
А выбирают из группы, состоящей из

Х представляет собой азот, СН или СН2;
X' представляет собой С или СН, где, когда X' представляет собой С, существует двойная связь между Х и X', и, когда X' представляет собой СН, существует простая связь между Х и X';
каждый Y выбирают, по отдельности, из группы, состоящей из азота, кислорода или СН;
каждый W выбирают, по отдельности, из группы, состоящей из азота, СН, кислорода или серы;
каждый n выбирают, по отдельности, из группы, состоящей из 0, 1, 2, 3 и 4;
m выбирают из группы, состоящей из 1, 2 и 3;
каждый R1, по отдельности, отсутствует или его выбирают, по отдельности, из группы, состоящей из водорода, галогена, амина, необязательно замещенного С1-20алкила, необязательно замещенного С3-8циклоалкила, необязательно замещенного С2-20алкенила, необязательно замещенного С2-20алкинила, необязательно замещенного С1-20алкоксиалкила и необязательно замещенного арила и арилалкила;
L отсутствует или его выбирают из группы, состоящей из -H(CH2)n- и -(CH2)n-;
a, b, c и d выбирают, каждый независимо, из группы, состоящей из углерода, азота, кислорода и серы, или каждый из них, независимо, отсутствует,
при условии, что присутствуют, по меньшей мере, три из a, b, c или d,
при условии, что, по меньшей мере, один из a, b, c или d представляет собой атом углерода, и
при условии, что два соседних из a, b, c или d оба не являются атомами кислорода или атомами серы;
e, f, g и h выбирают, каждый независимо, из группы, состоящей из углерода, азота, кислорода и серы, или каждый из них, независимо, отсутствует,
при условии, что присутствуют, по меньшей мере, три из e, f, g или h,
при условии, что, по меньшей мере, один из e, f, g или h представляет собой атом углерода, и
при условии, что два соседних из e, f, g или h оба не являются атомами кислорода или атомами серы;
R2, R3, R4 и R5 выбирают, каждый независимо, из группы, состоящей из водорода, галогена, необязательно замещенного С1-6алкила, необязательно замещенного С1-6алкилокси, необязательно замещенного С2-6алкенила, необязательно замещенного С2-6алкинила, необязательно замещенного С1-6алкоксиалкила, необязательно замещенного С1-6алкилтио, пергалогеналкила, CN, COR10, CONHR10, NHCONHR10, SO2NHR10, SO2R10, OSO2R10, гетероалкила, NO2, NHCOR10,
или R2 и R3, или R3 и R4, или R4 и R5, взятые вместе и вместе с атомами углерода кольца, к которым они присоединены, образуют пятичленное или шестичленное циклоалкильное, гетероциклильное или гетероарильное кольцо или шестичленную арильную группу;
R6, R7, R8 и R9 выбирают, каждый независимо, из группы, состоящей из водорода, галогена, необязательно замещенного С1-6алкила, необязательно замещенного С1-6алкилокси, необязательно замещенного С2-6алкенила, необязательно замещенного С2-6алкинила, необязательно замещенного С1-6алкоксиалкила, необязательно замещенного С1-6алкилтио, пергалогеналкила, CN, COR10, CONHR10, NHCONHR10, SO2NHR10, SO2R10, OSO2R10, гетероалкила, NO2, NHCOR10,
или R6 и R7, или R7 и R8, или R8 и R9, взятые вместе и вместе с атомами углерода кольца, к которым они присоединены, образуют пятичленное или шестичленное циклоалкильное, гетероциклильное или гетероарильное кольцо или шестичленную арильную группу;
Z выбирают из группы, состоящей из NR11, кислорода, серы и СН2;
R10 выбирают из группы, состоящей из водорода, необязательно замещенного С1-6алкила, необязательно замещенного С3-8циклоалкила, необязательно замещенного С2-6алкенила, необязательно замещенного С2-6алкинила, необязательно замещенного арила, необязательно замещенного арилалкила и пергалогеналкила;
R11 выбирают из группы, состоящей из водорода, необязательно замещенного С1-6алкила, необязательно замещенного С3-8циклоалкила, необязательно замещенного С2-6алкенила, необязательно замещенного С2-6алкинила и необязательно замещенного арилалкила;
R12 и R13 выбирают, по отдельности, из группы, состоящей из водорода, галогена, необязательно замещенного С1-6алкила, необязательно замещенного С1-6алкилокси, необязательно замещенного С2-6алкенила, необязательно замещенного С2-6алкинила, необязательно замещенного С1-6алкоксиалкила, необязательно замещенного С1-6алкилтио, пергалогеналкила, CN, COR10, CONHR10, NHCONHR10, SO2NHR10, SO2R10, OSO2R10, гетероалкила, NO2, NHCOR10,
или R12 и R13, взятые вместе и вместе с атомами углерода кольца, к которым они присоединены, образуют пятичленное или шестичленное циклоалкильное, гетероциклильное или гетероарильное кольцо или шестичленную арильную группу.
Связи, представленные пунктирной и сплошной линией, представляют связь, выбранную из группы, состоящей из простой углерод-углеродной связи и двойной углерод-углеродной связи. Пунктирная связь между Х и X' в формулах I, II и XV указывает, что Х и X' могут соединяться или простой или двойной связью.
В некоторых вариантах осуществления соединение формулы I и XV не включает клозапин или N-десметилклозапин, структура которых показана ниже
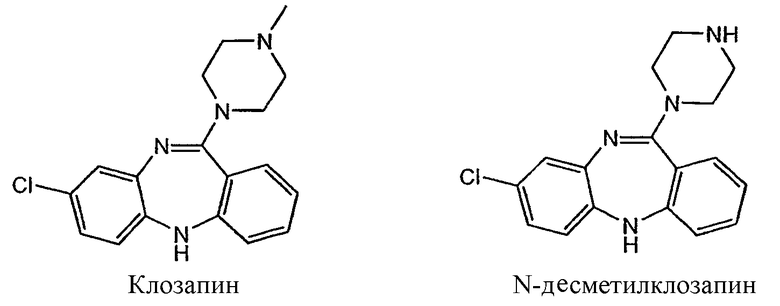
В некоторых вариантах осуществления в соединениях формулы I и XV Y представляет собой азот или СН. В других вариантах осуществления в соединениях формулы II Y представляет собой азот, кислород или СН.
Термин "фармацевтически приемлемая соль" относится к форме соединения, которая не вызывает существенного раздражения в организме, в который ее вводят, и не аннулирует биологическую активность и свойства соединения. Фармацевтические соли можно получить взаимодействием соединения изобретения с неорганическими кислотами, такими как хлористоводородная кислота, бромистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота, метансульфоновая кислота, этансульфоновая кислота, п-толуолсульфоновая кислота, салициловая кислота и т.п. Фармацевтические соли также можно получить взаимодействием соединения изобретения с основанием с образованием такой соли, как аммониевая соль, соль щелочного металла, такая как натриевая или калиевая соль, соль щелочноземельного металла, такая как кальциевая или магниевая соль, соль органического основания, такого как дициклогексиламин, N-метил-D-глюкамин, трис(гидроксиметил)метиламин, и солей с аминокислотами, такими как аргинин, лизин и т.п.
Термин "сложный эфир" относится к химической группе формулы -(R)n-COOR', где R и R' выбирают, независимо, из группы, состоящей из алкила, циклоалкила, арила, гетероарила (связанного через циклический атом углерода) и гетероалициклической группы (связанной через циклический атом углерода), и где n равен 0 или 1.
"Амид" представляет собой химическую группу формулы -(R)n-C(O)NHR' или -(R)n-NHC(O)R', где R и R', независимо, выбирают из группы, состоящей из алкила, циклоалкила, арила, гетероарила (связанного через циклический атом углерода) и гетероалициклической группы (связанной через циклический атом углерода), и где n равен 0 или 1. Амид также может представлять собой остаток аминокислоты или молекулы пептида, присоединенный к молекуле настоящего изобретения, причем посредством этого образуется пролекарство.
Любую боковую цепь соединений настоящего изобретения, содержащую амино, гидрокси или карбоксильную группу, можно этерифицировать или амидировать. Методики и конкретные группы, используемые для достижения такого конечного результата, известны специалистам в данной области и могут быть легко найдены в литературных источниках, таких как Greene and Wuts, Protective Groups in Organic Synthesis, 3rd Ed., John Wiley & Sons, New York, NY, 1999, включенная в данное описание посредством ссылки.
Термин "пролекарство" относится к средству, которое превращается в исходное лекарственное средство in vivo. Пролекарства часто применяют, поскольку, в некоторых случаях, их можно легче ввести, чем исходное лекарственное средство. Они могут быть, например, биодоступными при пероральном введении, в то время как исходное средство недоступно. Пролекарство также может иметь улучшенную растворимость в фармацевтических композициях по сравнению с исходным лекарственным средством. Примером пролекарства, без ограничения, может быть соединение настоящего изобретения, которое вводят в виде сложного эфира ("пролекарство") для облегчения прохождения клеточной мембраны, где растворимость в воде пагубна для подвижности, но которое затем метаболически гидролизуется до карбоновой кислоты - активного начала сразу внутри клетки, где растворимость в воде благоприятна. Другим примером пролекарства может являться короткий пептид (полиаминокислота), связанный с кислотной группой, где пептид метаболизируется с образованием активного начала.
Термин "ароматическая" относится к ароматической группе, содержащей, по меньшей мере, одно кольцо с системой конъюгированных пи-электронов, и включает как карбоциклические арильные (например, фенильные), так и гетероциклические арильные группы (например, пиридин). Термин включает моноциклические или конденсированные полициклические (т.е. циклы, имеющие общие пары атомов углерода) группы. Термин "карбоциклическое" относится к соединению, содержащему одну или несколько ковалентно замкнутых циклических структур и атомы которого, образующие основу кольца, все являются атомами углерода. Таким образом, термин устанавливает отличие карбоциклических колец от гетероциклических, в которых основа кольца содержит, по меньшей мере, один атом, который отличается от атома углерода. Термин "гетероароматическая" относится к ароматической группе, которая содержит, по меньшей мере, одно гетероциклическое кольцо.
Используемый в данном описании термин "алкил" относится к алифатической углеводородной группе. Алкильная группа может являться "насыщенной алкильной" группой, что означает, что она не содержит какой-либо алкеновой или алкиновой группы. Алкильная группа также может являться "ненасыщенной алкильной" группой, что означает, что она содержит, по меньшей мере, одну алкеновую или алкиновую группу. Определение "алкеновая" относится к группе, содержащей, по меньшей мере, два атома углерода и, по меньшей мере, одну двойную углерод-углеродную связь, и определение "алкиновая" относится к группе, содержащей, по меньшей мере, два атома углерода и, по меньшей мере, одну тройную углерод-углеродную связь. Алкильная группа, насыщенная или ненасыщенная, может быть разветвленной, линейной или циклической.
Алкильная группа может содержать 1-20 атомов углерода (при любом появлении числовой интервал, такой как "1-20", относится к любому целому числу в данном интервале; например, "1-20 атомов углерода" означает, что алкильная группа может состоять из 1 атома углерода, 2 атомов углерода, 3 атомов углерода и т.д., до и включая 20 атомов углерода, хотя такое определение также включает появление термина "алкил", где числовой интервал не обозначен). Алкильная группа также может представлять собой алкил среднего размера с 1-10 атомами углерода. Алкильная группа также может представлять собой низший алкил с 1-5 атомами углерода. Алкильная группа в соединениях изобретения может обозначаться как "(С1-С4)алкил" или подобным образом. Только в качестве примера, обозначение "(С1-С4)алкил" показывает, что в алкильной цепи содержится от одного до четырех атомов углерода, т.е. алкильную цепь выбирают из группы, состоящей из метила, этила, пропила, изопропила, н-бутила, изобутила, втор-бутила и трет-бутила.
Алкильная группа может быть замещенной или незамещенной. Когда алкильная группа является замещенной, замещающая(ие) группа(ы) представляет(ют) собой одну или несколько групп, выбранных, по отдельности и независимо, из числа циклоалкила, арила, гетероарила, гетероалициклической группы, гидрокси, алкокси, арилокси, меркапто, алкилтио, арилтио, циано, галогена, карбонила, тиокарбонила, О-карбамила, N-карбамила, О-тиокарбамила, N-тиокарбамила, С-амидо, N-амидо, S-сульфонамидо, N-сульфонамидо, С-карбокси, О-карбокси, изоцианато, тиоцианато, изотиоцианато, нитро, силила, тригалогенметансульфонила и амино, включая моно-, ди- и тризамещенные аминогруппы, и их производных, содержащих защитные группы. Типичными алкильными группами являются, но не ограничиваются перечисленным, метил, этил, пропил, изопропил, бутил, изобутил, третичный бутил, пентил, гексил, этенил, пропенил, бутенил, циклопропил, циклобутил, циклопентил, циклогексил и т.п. Когда заместитель описан как "необязательно замещенный", такой заместитель может быть замещен одним из вышеуказанных заместителей.
Заместитель "R", появляющийся как таковой и без числового обозначения, относится к заместителю, выбранному из группы, состоящей из алкила, циклоалкила, арила, гетероарила (связанного через атом углерода кольца) и гетероалициклической группы (связанной через атом углерода кольца).
Группой "О-карбокси" называется группа RC(=O)O-, где R имеет значения, указанные в данном описании.
Группой "С-карбокси" называется группа -C(=O)OR, где R имеет значения, указанные в данном описании.
"Ацетильной" группой называется группа -С(=О)СН3.
"Тригалогенметансульфонильной" группой называется группа Х3CS(=O)2-, где Х представляет собой галоген.
Группой "циано" называется группа -CN.
Группой "изоцианато" называется группа -NCO.
Группой "тиоцианато" называется группа -СNS.
Группой "изотиоцианато" называется группа -NСS.
"Сульфинильной" группой называется группа -S(=O)-R, где R имеет значения, указанные в данном описании.
Группой "S-сульфонамидо" называется группа -S(=O)2NR, где R имеет значения, указанные в данном описании.
Группой "N-сульфонамидо" называется группа RS(=O)2NH-, где R имеет значения, указанные в данном описании.
Группой "тригалогенметансульфонамидо" называется группа X3CS(=O)2NR-, где Х и R имеют значения, указанные в данном описании.
"О-карбамильной" группой называется группа -ОС(=О)-NR, где R имеет значения, указанные в данном описании.
"N-карбамильной" группой называется группа RОС(=О)NН-, где R имеет значения, указанные в данном описании.
"О-тиокарбамильной" группой называется группа -ОС(=S)-NR, где R имеет значения, указанные в данном описании.
"N-тиокарбамильной" группой называется группа RОС(=S)NН-, где R имеет значения, указанные в данном описании.
Группой "С-амидо" называется группа -С(=О)-NR2, где R имеет значения, указанные в данном описании.
Группой "N-амидо" называется группа RС(=О)-NH-, где R имеет значения, указанные в данном описании.
Термин "пергалогеналкил" относится к алкильной группе, где все атомы водорода заменены атомами галогена.
Термин "ацилалкил" относится к группе RC(=O)R', где R имеет значения, указанные в данном описании, и R' представляет собой двухвалентную алкиленовую группу. Примеры ацилалкила, без ограничений, могут включать СН3С(=О)СН2-, СН3С(=О)СН2СН2-, СН3СН2С(=О)СН2СН2-, СН3С(=О)СН2СН2СН2- и подобные группы.
Если не указано иное, то, когда полагают, что заместитель является "необязательно замещенным", это означает, что заместитель представляет собой группу, которая может быть замещена одной или несколькими группами, по отдельности и независимо, выбранными из числа циклоалкила, арила, гетероарила, гетероалициклической группы, гидрокси, алкокси, арилокси, меркапто, алкилтио, арилтио, циано, галогена, карбонила, тиокарбонила, О-карбамила, N-карбамила, О-тиокарбамила, N-тиокарбамила, С-амидо, N-амидо, S-сульфонамидо, N-сульфонамидо, С-карбокси, О-карбокси, изоцианато, тиоцианато, изотиоцианато, нитро, силила, тригалогенметансульфонила и амино, включая моно- и дизамещенные аминогруппы, и их производных, содержащих защитные группы. Защитные группы, которые могут образовывать защищенные производные вышеуказанных заместителей, известны специалистам в данной области, и их можно найти в ссылках, таких как цитированная выше Greene and Wuts.
В настоящем контексте предполагается, что термин "циклоалкил" перекрывает трех-, четырех-, пяти-, шести-, семи- и восьмичленные или с большим числом членов кольца, содержащие только атомы углерода. Циклоалкил, необязательно, может содержать одну или несколько ненасыщенных связей, однако расположенных таким образом, что система ароматических пи-электронов не возникает. Несколькими примерами "циклоалкила" являются карбоциклы циклопропана, циклобутана, циклопентана, циклопентена, циклопентадиена, циклогексана, циклогексена, 1,3-циклогексадиена, 1,4-циклогексадиена, циклогептана или циклогептена.
Подразумевается, что термин "гетероциклил" означает трех-, четырех-, пяти-, шести-, семи- и восьмичленные или с большим числом членов кольца, где указанное кольцо составляют атомы углерода вместе с 1-3 гетероатомами. Гетероциклил, необязательно, может содержать одну или несколько ненасыщенных связей, однако расположенных таким образом, что система ароматических пи-электронов не возникает. Гетероатомы выбирают, независимо, из числа атомов кислорода, серы и азота.
Гетероциклил также может содержать одну или несколько карбонильных или тиокарбонильных функциональных групп, так что данное определение включает оксосистемы и тиосистемы, такие как лактамы, лактоны, циклические имиды, циклические тиоимиды, циклические карбаматы и подобные системы.
Гетероциклильные кольца также могут, необязательно, быть конденсированы с арильными кольцами, так что данное определение включает бициклические структуры. Конкретно такие конденсированные гетероциклильные группы имеют одну общую связь с необязательно замещенным бензольным кольцом. Примерами бензоконденсированных гетероциклильных групп являются, но не ограничиваются перечисленным, циклические структуры бензимидазолидинона, тетрагидрохинолина и метилендиоксибензола.
Некоторые примеры "гетероциклилов" включают, но не ограничиваются перечисленным, тетрагидротиопиран, 4Н-пиран, тетрагидропиран, пиперидин, 1,3-диоксин, 1,3-диоксан, 1,4-диоксин, 1,4-диоксан, пиперазин, 1,3-оксатиан, 1,4-оксатиин, 1,4-оксатиан, тетрагидро-1,4-тиазин, 2Н-1,2-оксазин, малеимид, сукцинимид, барбитуровую кислоту, тиобарбитуровую кислоту, диоксопиперазин, гидантоин, дигидроурацил, морфолин, триоксан, гексагидро-1,3,5-триазин, тетрагидротиофен, тетрагидрофуран, пирролин, пирролидин, пирролидон, пирролидион, пиразолин, пиразолидин, имидазолин, имидазолидин, 1,3-диоксол, 1,3-диоксолан, 1,3-дитиол, 1,3-дитиолан, изоксазолин, изоксазолидин, оксазолин, оксазолидин, оксазолидинон, тиазолин, тиазолидин и 1,3-оксатиолан. Связь с гетероциклом может находиться в положении гетероатома или осуществляться через атом углерода гетероцикла или, в случае бензоконденсированных производных, через атом углерода бензольного кольца.
В настоящем контексте подразумевается, что термин "арил" означает карбоциклическое ароматическое кольцо или систему колец. Кроме того, термин "арил" включает конденсированные циклические системы, где, по меньшей мере, два арильных кольца или, по меньшей мере, один арил и, по меньшей мере, один С3-8циклоалкил имеют в общем распоряжении, по меньшей мере, одну химическую связь. Некоторые примеры "арильных" колец включают необязательно замещенный фенил, нафталенил, фенантренил, антраценил, тетралинил, флуоренил, инденил и инданил. Термин "арил" относится к ароматическим, включая, например, бензольные группы, присоединенные через один из образующих кольцо атомов углерода и, необязательно, содержащие один или несколько заместителей, выбранных из гетероциклила, гетероарила, галогена, гидрокси, амино, циано, нитро, алкиламидо, ацила, С1-6алкокси, С1-6алкила, С1-6-гидроксиалкила, С1-6-аминоалкила, С1-6алкиламино, алкилсульфенила, алкилсульфинила, алкилсульфонила, сульфамоила или трифторметила. Арильная группа может быть замещена в пара- и/или метаположениях. В других вариантах осуществления арильная группа может быть замещена в ортоположении. Характерные примеры арильных групп включают, но не ограничиваются перечисленным, фенил, 3-галогенфенил, 4-галогенфенил, 3-гидроксифенил, 4-гидроксифенил, 3-аминофенил, 4-аминофенил, 3-метилфенил, 4-метилфенил, 3-метоксифенил, 4-метоксифенил, 4-трифторметоксифенил, 3-цианофенил, 4-цианофенил, диметилфенил, нафтил, гидроксинафтил, гидроксиметилфенил, трифторметилфенил, алкоксифенил, 4-морфолин-4-илфенил, 4-пирролидин-1-илфенил, 4-пиразолилфенил, 4-триазолилфенил и 4-(2-оксопирролидин-1-ил)фенил.
В контексте настоящего изобретения подразумевается, что термин "гетероарил" означает гетероциклическую ароматическую группу, где один или несколько атомов углерода в ароматическом кольце заменены одним или несколькими гетероатомами, выбранными из группы, состоящей из атомов азота, серы, фосфора и кислорода.
Кроме того, в контексте настоящего изобретения термин "гетероарил" относится к конденсированным циклическим системам, где, по меньшей мере, одно арильное кольцо и, по меньшей мере, одно гетероарильное кольцо, по меньшей мере, два гетероарильных кольца, по меньшей мере, одно гетероарильное кольцо и, по меньшей мере, одно гетероциклильное кольцо или, по меньшей мере, одно гетероарильное кольцо и, по меньшей мере, одно циклоалкильное кольцо имеют в общем распоряжении, по меньшей мере, одну химическую связь.
Подразумевается, что термин "гетероарил" относится к ароматическим С3-8циклическим группам, также содержащим один атом кислорода или серы или до четырех атомов азота, или сочетание одного атома кислорода или серы и до двух атомов азота, и их замещенным, а также бензо- и пиридоконденсированным производным, например, соединенным через один из атомов углерода, образующих кольцо. Гетероарильные группы могут содержать один или несколько заместителей, выбранных из галогена, гидрокси, амино, циано, нитро, алкиламино, ацила, С1-6алкокси, С1-6алкила, С1-6гидроксиалкила, С1-6аминоалкила, С1-6алкиламино, алкилсульфенила, алкилсульфинила, алкилсульфонила, сульфамоила или трифторметила. В некоторых вариантах осуществления гетероарильные группы могут представлять собой пяти- и шестичленные ароматические гетероциклические системы, содержащие 0, 1 или 2 заместителя, которые могут быть одинаковыми или отличаться один от другого, выбранных из заместителей, перечисленных выше. Характерными примерами гетероарильных групп являются, но не ограничиваются перечисленным, группы, образованные из незамещенных и моно- или дизамещенных производных фурана, бензофурана, тиофена, бензотиофена, пиррола, пиридина, индола, оксазола, бензоксазола, изоксазола, бензизоксазола, тиазола, бензотиазола, изотиазола, имидазола, бензимидазола, пиразола, индазола, тетразола, хинолина, изохинолина, пиридазина, пиримидина, пурина и пиразина, фуразана, 1,2,3-оксадиазола, 1,2,3-тиадиазола, 1,2,4-тиадиазола, триазола, бензотриазола, птеридина, феноксазола, оксадиазола, бензопиразола, хинолизина, циннолина, фталазина, хиназолина и хиноксалина. В некоторых вариантах осуществления заместителями являются галоген, гидрокси, циано, О-С1-6алкил, С1-6алкил, гидроксиС1-6алкил и аминоС1-6алкил.
В некоторых вариантах осуществления, раскрываемых в данном описании, соединение выбирают из следующих структур


где R1-R9, W, Y и Z имеют значения, указанные в данном описании.
В некоторых других вариантах осуществления, раскрываемых в данном описании, соединение выбирают из следующих структур


где R1, W, Y и Z имеют значения, указанные в данном описании.
В некоторых вариантах осуществления, раскрываемых в данном описании, соединение имеет структуру, представленную формулой III или формулой IV

где R1-R5, W, X, X', Y и Z имеют значения, указанные в данном описании.
В некоторых вариантах осуществления ни один из a, b, c или d не отсутствует, и образованное при этом кольцо является шестичленным кольцом. В других вариантах осуществления ни один из e, f, g или h не отсутствует, и, следовательно, образованное при этом кольцо является шестичленным кольцом. В некоторых вариантах осуществления a, b, c и d являются атомами углерода, и образованное при этом кольцо является необязательно замещенным фенильным кольцом. В других вариантах осуществления e, f, g и h являются атомами углерода, которые, подобным образом, образуют необязательно замещенное фенильное кольцо.
В некоторых вариантах осуществления R2 может быть выбран из группы, состоящей из водорода, галогена, необязательно замещенного С1-6алкила и необязательно замещенного С1-6алкилокси. В некоторых вариантах осуществления алкил может быть выбран из группы, состоящей из метила, этила, пропила, изопропила, бутила, втор-бутила и трет-бутила. В других вариантах осуществления алкилокси может быть выбран из группы, состоящей из метокси, этокси, пропокси, изопропокси, бутокси, втор-бутокси и трет-бутокси. В других вариантах осуществления галоген может быть выбран из группы, состоящей из фтора, хлора и брома. В некоторых вариантах осуществления R2 может быть выбран из группы, состоящей из водорода, метила, метокси и хлора.
В некоторых вариантах осуществления R3 может быть выбран из группы, состоящей из водорода, галогена, необязательно замещенного С1-6алкила, необязательно замещенного С1-6алкилокси и NO2. Алкильная группа может быть выбрана из группы, состоящей из метила, этила, пропила, изопропила, бутила, втор-бутила и трет-бутила, в то время как алкокси может быть выбран из группы, состоящей из метокси, этокси, пропокси, изопропокси, бутокси, втор-бутокси и трет-бутокси. В других вариантах осуществления галоген может быть выбран из группы, состоящей из хлора, брома и иода. В других вариантах осуществления R3 может быть выбран из группы, состоящей из водорода, метила, метокси, хлора, брома, иода и NO2.
В некоторых вариантах осуществления R4 может быть выбран из группы, состоящей из водорода, галогена, необязательно замещенного С1-6алкила, пергалогеналкила, SO2R10 и NO2. В некоторых вариантах осуществления алкил может быть выбран из группы, состоящей из метила, этила, пропила, изопропила, бутила, втор-бутила и трет-бутила. В других вариантах осуществления пергалогеналкил может представлять собой перфторалкил, который в некоторых вариантах осуществления может представлять собой трифторметил. В других вариантах осуществления галоген может быть выбран из группы, состоящей из фтора, хлора и брома. Когда R4 представляет собой SO2R10, R10 может представлять собой водород или необязательно замещенный С1-6алкил, который может быть выбран из группы, состоящей из метила, этила, пропила, изопропила, бутила, втор-бутила и трет-бутила. В некоторых вариантах осуществления R4 может быть выбран из группы, состоящей из водорода, метила, фтора, хлора, брома, трифторметила, SO2CH3 и NO2.
В некоторых вариантах осуществления R5 может быть выбран из группы, состоящей из водорода, галогена и необязательно замещенного С1-6алкила. Алкил может быть выбран из группы, состоящей из метила, этила, пропила, изопропила, бутила, втор-бутила и трет-бутила, в то время как галоген может быть выбран из группы, состоящей из фтора, хлора и брома. В некоторых вариантах осуществления R5 может представлять собой водород или хлор.
В некоторых вариантах осуществления R6 может представлять собой водород или необязательно замещенный С1-6алкил. Алкил может быть выбран из группы, состоящей из метила, этила, пропила, изопропила, бутила, втор-бутила и трет-бутила. В некоторых вариантах осуществления R6 может представлять собой водород.
В некоторых вариантах осуществления R7 может быть выбран из группы, состоящей из водорода, галогена, необязательно замещенного С1-6алкила, пергалогеналкила, CN, SO2R10 и NO2. Алкил может быть выбран из группы, состоящей из метила, этила, пропила, изопропила, бутила, втор-бутила и трет-бутила, в то время как галоген может быть выбран из группы, состоящей из фтора, хлора и брома. В некоторых вариантах осуществления пергалогеналкил представляет собой перфторалкил, который в некоторых вариантах осуществления может представлять собой трифторметил. В вариантах осуществления, в которых R7 может представлять собой SO2R10, R10 может представлять собой водород или необязательно замещенный С1-6алкил, который может быть выбран из группы, состоящей из метила, этила, пропила, изопропила, бутила, втор-бутила и трет-бутила. В некоторых вариантах осуществления R7 может быть выбран из группы, состоящей из водорода, метила, хлора, трифторметила, SO2CH3, CN и NO2.
В некоторых вариантах осуществления R8 может быть выбран из группы, состоящей из водорода, галогена и необязательно замещенного С1-6алкила, где алкил может быть выбран из группы, состоящей из метила, этила, пропила, изопропила, бутила, втор-бутила и трет-бутила. Галоген может быть выбран из группы, состоящей из фтора, хлора и брома. В некоторых вариантах осуществления R8 может быть выбран из группы, состоящей из водорода, хлора и брома.
Варианты осуществления настоящего изобретения включают варианты, в которых R9 может быть выбран из группы, состоящей из водорода, галогена, необязательно замещенного С1-6алкила и пергалогеналкила. Алкил может быть выбран из группы, состоящей из метила, этила, пропила, изопропила, бутила, втор-бутила и трет-бутила. Галоген может быть выбран из группы, состоящей из фтора, хлора и брома. Пергалогеналкил может представлять собой перфторалкил, который в некоторых вариантах осуществления может представлять собой трифторметил. В некоторых вариантах осуществления R9 может быть выбран из группы, состоящей из водорода, хлора, метила и трифторметила.
В некоторых вариантах осуществления R1 может быть выбран из группы, состоящей из водорода, необязательно замещенного С1-6алкила и необязательно замещенного арила. Алкил может быть выбран из группы, состоящей из метила, этила, пропила, изопропила, бутила, втор-бутила и трет-бутила, в то время как арил может представлять собой фенил или нафтил. В других вариантах осуществления R1 может представлять собой гетероарил. В некоторых вариантах осуществления R1 может представлять собой водород. В некоторых вариантах осуществления R1 отсутствует.
В некоторых вариантах осуществления Х может представлять собой азот. В других вариантах осуществления Y может представлять собой NH, и W может представлять собой азот или СН.
В некоторых вариантах осуществления соединения формулы I или формулы XV L отсутствует или его выбирают из группы, состоящей из -NHCH2-, -NH- и -СН2-. В некоторых вариантах осуществления соединения формулы I или формулы XV А выбирают из группы, состоящей из

где n выбирают из группы, состоящей из 0, 1 и 2.
Некоторыми вариантами осуществления соединений формулы I, формулы II или формулы XV являются:
2,7-дихлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
2-хлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
2,8-дихлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
8-бром-2-хлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
2-хлор-11-(пиперазин-1-ил)-8-трифторметил-5Н-дибензо[b,e][1,4]диазепин,
6-хлор-11-(пиперазин-1-ил)-8-трифторметил-5Н-дибензо[b,e][1,4]диазепин,
7-хлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
8-бром-1-хлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
8-бром-2-метил-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
4,8-дихлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
8-хлор-2-метил-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
8-хлор-2-фтор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
3,8-дихлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
2-бром-8-хлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
3,7-дихлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
8-бром-3-хлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
3-хлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
3-хлор-11-(пиперазин-1-ил)-8-трифторметил-5Н-дибензо[b,e][1,4]диазепин,
7-хлор-2-метил-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
2-метил-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
2-метил-11-(пиперазин-1-ил)-8-трифторметил-5Н-дибензо[b,e][1,4]диазепин,
8-хлор-4-метил-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
1,8-дихлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
8-бром-5-метил-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
7,8-дихлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
11-(пиперазин-1-ил)-8-трифторметил-5Н-дибензо[b,e][1,4]диазепин,
11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
8-фтор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин-8-карбонитрил,
8-бром-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
8-метил-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
3-фтор-6-пиперазин-1-ил-11Н-дибензо[b,e]азепин,
2-(трифторметансульфонилокси)-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
2-(трифторметансульфонилокси)-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]оксазепин,
8-хлор-2-(трифторметансульфонилокси)-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
8-(трифторметансульфонилокси)-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
11-(пиперазин-1-ил)дибензо[b,f][1,4]тиазепин,
11-(пиперазин-1-ил)-2,3-дигидро-1,4-бензодиоксино[6,7-b][1,4]бензотиазепин,
8-хлор-11-[1,4]диазепин-1-ил-5Н-дибензо[b,e][1,4]диазепин,
N'-(8-хлор-5Н-дибензо[b,e][1,4]диазепин-11-ил)-N,N-диметилэтан-1,2-диамин,
N'-(8-хлор-5Н-дибензо[b,e][1,4]диазепин-11-ил)-N,N-диэтилэтан-1,2-диамин,
8-хлор-11-(4-метил[1,4]диазепам-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
8-хлор-2-метокси-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
N'-(5Н-дибензо[b,e][1,4]диазепин-11-ил)-N,N-диметилэтан-1,2-диамин,
11-[1,4]диазепам-1-ил-5Н-дибензо[b,e][1,4]диазепин,
N'-(8-фтор-5Н-дибензо[b,e][1,4]диазепин-11-ил)-N,N-диметилэтан-1,2-диамин,
8-фтор-11-[1,4]диазепам-1-ил-5Н-дибензо[b,e][1,4]диазепин,
N'-(8-хлор-5Н-дибензо[b,e][1,4]диазепин-11-ил)-N-метилэтан-1,2-диамин,
8-хлор-11-(транс-2,5-диметилпиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
8-хлор-11-(3,5-диметилпиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
8-хлор-11-(3-метилпиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
8-хлор-11-(3-фенилпиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
8-хлор-5-метил-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
8-хлор-5-бензил-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
8-иод-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
2-иод-8-хлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
8-фенил-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
8-хлор-11-(пиперидин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
8-хлор-11-(морфолин-4-ил)-5Н-дибензо[b,e][1,4]диазепин,
5-аллил-8-хлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
6-хлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин,
8-хлор-5-пиперазин-1-ил-11Н-бензо[b]пиридо[2,3-e][1,4]диазепин,
2-хлор-10-пиперазин-1-ил-5Н-дибензо[b,f]азепин,
8-хлор-11-(пиперазин-1-ил)дибензо[b,f][1,4]тиазепин,
8-хлор-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
8-хлор-11-(4-метилпиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
3-хлор-6-пиперазин-1-ил-11Н-дибензо[b,е]азепин,
8-бром-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
7-хлор-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
8-хлор-3-метокси-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
8-бром-3-метокси-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
3-метокси-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
7-хлор-3-метокси-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
8-хлор-4-метил-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
8-бром-4-метил-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
4-метил-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
2-бром-8-хлор-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
2,8-дибром-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
2-бром-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
2-бром-7-хлор-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
11-(пиперазин-1-ил)-8-трифторметилдибензо[b,f][1,4]оксазепин,
4-метил-11-(пиперазин-1-ил)-8-трифторметилдибензо[b,f][1,4]оксазепин,
8-фтор-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
8-фтор-3-метокси-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
8-фтор-4-метил-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
2-бром-8-фтор-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
8-метил-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
3-метокси-8-метил-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
4,8-диметил-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
3-метокси-11-(пиперазин-1-ил)-8-трифторметилдибензо[b,f][1,4]оксазепин,
2-бром-11-(пиперазин-1-ил)-8-трифторметилдибензо[b,f][1,4]оксазепин,
6-хлор-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
2-бром-8-метил-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
7-хлор-4-метил-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
8-фенил-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
8-хлор-11-(пиперидин-4-ил)-5Н-дибензо[b,е][1,4]диазепин,
5-бензил-8-хлор-11-(пиперидин-4-ил)-5Н-дибензо[b,е][1,4]диазепин,
8-бром-5,10-дигидродибензо[b,е][1,4]диазепин-11-он,
5,10-дигидродибензо[b,е][1,4]диазепин-11-он,
8-фтор-5,10-дигидродибензо[b,е][1,4]диазепин-11-он,
8,5-дихлор-5Н-дибензо[b,е][1,4]диазепин,
8-хлор-11-метилсульфанил-5Н-дибензо[b,е][1,4]диазепин,
(8-хлор-5Н-дибензо[b,е][1,4]диазепин-11-ил)-(S)-1-пирролидин-2-илметиламин,
1-(8-хлор-5Н-дибензо[b,е][1,4]диазепин-11-ил)пиперидин-4-иламин,
1-(8-хлор-5Н-дибензо[b,е][1,4]диазепин-11-ил)пирролидин-3-иламин,
(8-хлор-5Н-дибензо[b,е][1,4]диазепин-11-ил)-(R)-1-пирролидин-2-илметиламин,
(8-хлор-5Н-дибензо[b,е][1,4]диазепин-11-ил)пирролидин-3-иламин,
8-хлор-11-(2,5-диазабицикло[2,2,1]гепт-2-ил)-5Н-дибензо[b,е][1,4]диазепин,
ацетидин-3-ил-(8-хлор-5Н-дибензо[b,е][1,4]диазепин-11-ил)амин,
7-бром-4-(пиперазин-1-ил)-2,3-дигидро-1Н-бензо[b][1,4]диазепин,
7-бром-2-метил(пиперазин-1-ил)-2,3-дигидро-1Н-бензо[b][1,4]диазепин,
7-бром-2-фенил-4-(пиперазин-1-ил)-2,3-дигидро-1Н-бензо[b][1,4]диазепин,
7-бром-10-(пиперазин-1-ил)-1,2,3,3а,4,10а-гексагидробензо[b]циклопента[e][1,4]диазепин,
8-хлор-11-(4-фторбензил)-5Н-дибензо[b,е][1,4]диазепин,
8-хлор-11-(4-фторфенил)-5Н-дибензо[b,е][1,4]диазепин,
8-хлор-11-(4-нонилфенил)-5Н-дибензо[b,е][1,4]диазепин,
8-хлор-11-(пиридин-4-ил)-5Н-дибензо[b,е][1,4]диазепин и
8-хлор-11-(1Н-пиразол-4-ил)-5Н-дибензо[b,е][1,4]диазепин.
В другом аспекте настоящее изобретение относится к способу получения соединения формулы V или формулы VI

включающему
взаимодействие соединения формулы VII

с соединением формулы VIII

с образованием конденсированного циклического соединения формулы IX

и взаимодействие соединения формулы IX с соединением формулы Х

с образованием соединения формулы V или VI;
где Х представляет собой галоген, и R1-R9 имеют значения, указанные в данном описании. В некоторых вариантах осуществления соединение формулы V, синтезированное согласно описываемому способу, представляет собой клозапин, в то время как в других вариантах осуществления соединение представляет собой N-десметилклозапин. В некоторых других вариантах осуществления соединение формулы V, синтезированное согласно описываемому способу, не является клозапином или N-десметилклозапином.
Согласно данному аспекту схемы 1 и 2 отображают синтез некоторых соединений, раскрываемых в данном описании. Первый ряд стадий получения промежуточного лактама описан, среди прочего, Liao et al., в J. Med. Chem., 1997, 40, 4146-4153. Последняя стадия описана, например, Liao et al., в J. Med. Chem., 1999, 42, 2235-2244. Обе указанные ссылки включены в данное описание посредством ссылок, включая чертежи.
Схема 1
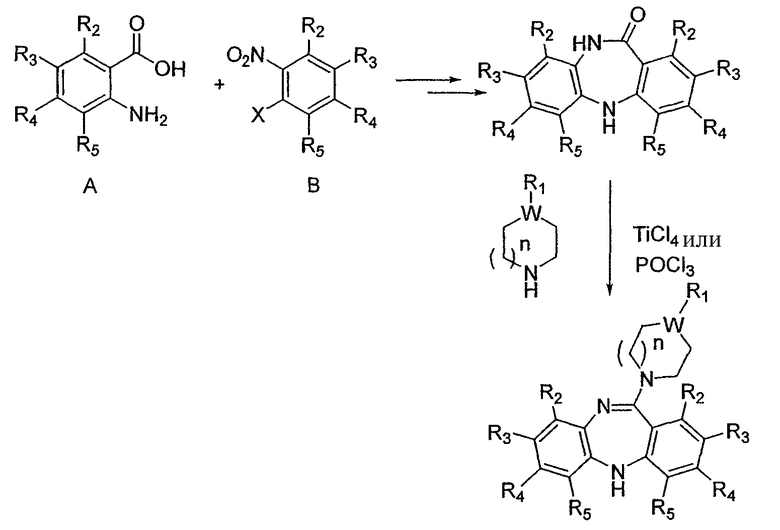
Схема 2
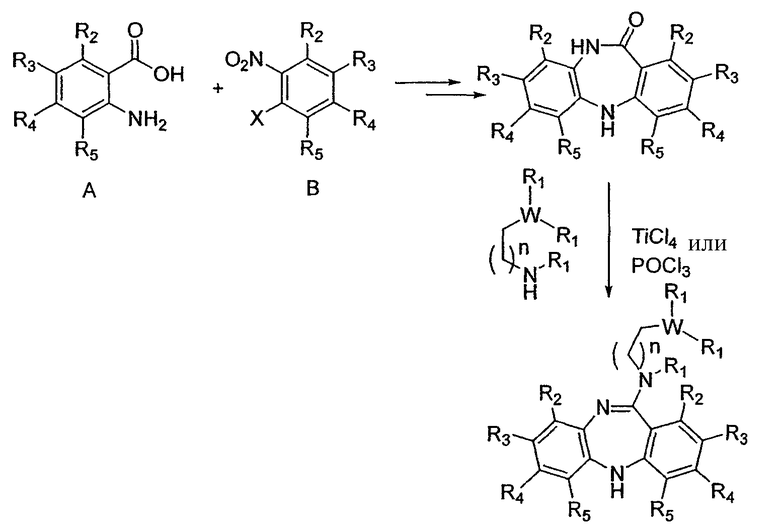
В некоторых вариантах осуществления изобретения строительные блоки А и В выбирают, но не ограничиваются указанным, из числа:
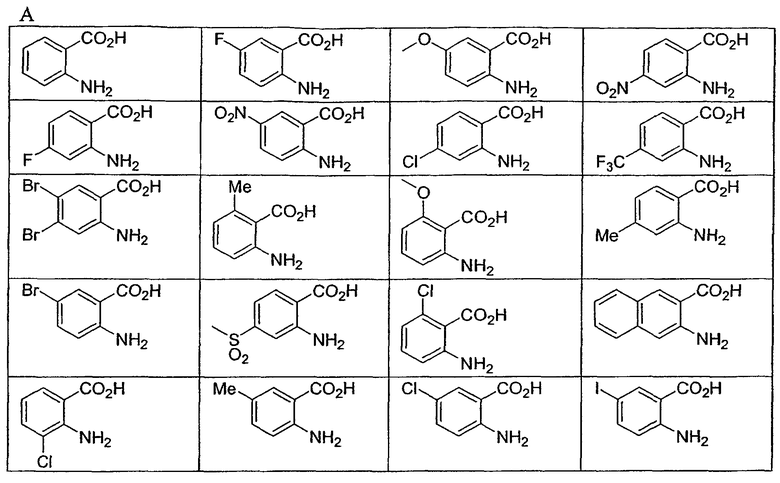
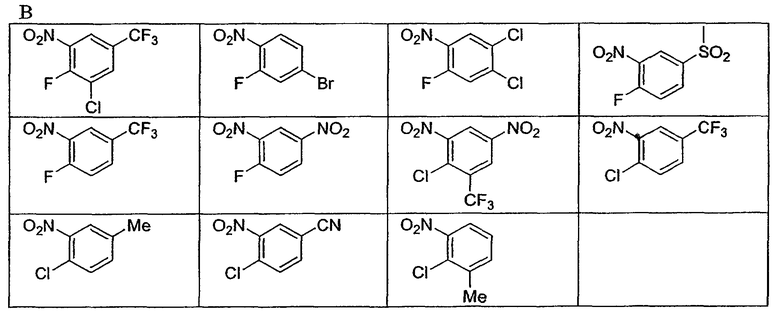
В другом аспекте настоящее изобретение относится к комбинаторной библиотеке из, по меньшей мере, 10, или, по меньшей мере, 30, или, по меньшей мере, 50, или, по меньшей мере, 100, или, по меньшей мере, 200, или, по меньшей мере, 220 соединений дибензо[b,e][1,4]диазепина, которые могут быть получены взаимодействием соединения формулы VII

с соединением формулы VIII

и соединением формулы XI

где Х представляет собой галоген; W представляет собой азот, СН, кислород или серу; n равен 1, 2, 3 или 4, и R1-R9 имеют значения, указанные в данном описании. В некоторых вариантах осуществления комбинаторная библиотека включает клозапин и/или N-десметилклозапин. В некоторых других вариантах осуществления комбинаторная библиотека не включает клозапин или N-десметилклозапин.
В другом аспекте настоящее изобретение относится к комбинаторной библиотеке из, по меньшей мере, 10, или, по меньшей мере, 30, или, по меньшей мере, 50, или, по меньшей мере, 100, или, по меньшей мере, 200, или, по меньшей мере, 220 соединений дибензо[b,e][1,4]диазепина, которые могут быть получены взаимодействием соединения формулы VII

с соединением формулы VIII

и соединением формулы XII

где Х представляет собой галоген; W представляет собой азот, СН, кислород или серу; n равен 1, 2, 3 или 4, и R1-R9 имеют значения, указанные в данном описании.
Используемый в данном описании термин "комбинаторная библиотека" относится ко всем соединениям, полученным взаимодействием каждого соединения одной группы с соединением в каждой из других групп в наборе из нескольких групп соединений. В контексте настоящего изобретения набор состоит из трех групп, где одна группа представляет все соединения формулы VII, вторая группа представляет все соединения формулы VIII и третья группа представляет все соединения формулы Х. Каждое соединение формулы VII можно подвергнуть взаимодействию с любым и каждым соединением формулы VIII и любым и каждым соединением формулы Х для того, чтобы получить замещенное соединение формулы V или VI. Все соединения, входящие в объем формулы V или VI, полученные таким путем, входят в объем настоящего изобретения. Также в объем настоящего изобретения входят комбинаторные библиотеки меньшего размера, полученные взаимодействием некоторых или всех соединений формулы VII с некоторыми или всеми соединениями формулы VIII и некоторыми или всеми соединениями формулы Х.
В некоторых вариантах осуществления соединения формул I, II или XV, раскрытые и описанные в данном описании, могут обладать способностью модулировать активность мускаринового рецептора.
Термин "модулировать" относится к способности соединения, раскрываемого в данном описании, изменять функцию мускаринового рецептора. Модулятор может активировать мускариновый рецептор, может активировать или ингибировать активность мускаринового рецептора в зависимости от концентрации соединения, воздействующего на мускариновый рецептор, или может ингибировать активность мускаринового рецептора. Термин "модулировать" также относится к изменению функции мускаринового рецептора путем повышения или снижения вероятности того, что между мускариновым рецептором и природным партнером по связыванию образуется комплекс. Модулятор может увеличивать вероятность того, что такой комплекс между мускариновым рецептором и природным партнером по связыванию образуется, может увеличивать или уменьшать вероятность того, что комплекс образуется между мускариновым рецептором и природным партнером по связыванию в зависимости от концентрации соединения, воздействующего на мускариновый рецептор, и может уменьшать вероятность того, что между мускариновым рецептором и природным партнером по связыванию образуется комплекс. В некоторых вариантах осуществления модуляцию мускаринового рецептора можно оценить с использованием технологии отбора и амплификации рецепторов (Receptor Selection and Amplification) (R-SAT), как описано в патенте США № 5707798, включенном в данное описание посредством ссылки.
Термин "активировать" относится к усилению клеточной функции мускаринового рецептора. Термин "ингибировать" относится к ослаблению клеточной функции мускаринового рецептора. Функцией мускаринового рецептора может являться взаимодействие с природным партнером по связыванию или каталитическая активность.
Термин "введение контактирования", используемый в данном описании, относится к приведению соединения, раскрываемого в данном описании, и мускаринового рецептора-мишени в такое состояние, что соединение может воздействовать на активность мускаринового рецептора или непосредственно, т.е. взаимодействуя с самим мускариновым рецептором, или косвенно, т.е. взаимодействуя с другой молекулой, от которой зависит активность мускаринового рецептора. Такое "контактирование" можно осуществить в пробирке, чашке Петри или подобным образом. В пробирке в контактировании могут участвовать только соединение и представляющий интерес мускариновый рецептор или могут участвовать целые клетки. Клетки также могут поддерживаться или расти в чашках для культивирования клеток и контактировать с соединением в таком окружении. В данном контексте способность определенного соединения воздействовать на мускариновый рецептор, связанный с расстройством, т.е. IC50 соединения, можно определить до попытки применения соединения in vivo с более сложными живыми организмами. Для клеток вне организма существует несколько хорошо известных специалистам в данной области способов контактирования мускариновых рецепторов с соединениями, в том числе, прямая микроинъекция клеток и несколько методов трансмембранного переноса, и другие методы. Термин "контактирование" также может относиться к приведению соединения, раскрываемого в данном описании, в контакт с мускариновым рецептором-мишенью in vivo. Таким образом, если соединение, раскрываемое в данном описании, или его пролекарство вводят в организм и соединение соединяется с мускариновым рецептором в организме, такое контактирование входит в объем настоящего изобретения.
В некоторых вариантах осуществления соединение формул I, II или XV может являться агонистом указанного рецептора, в то время как в других вариантах осуществления соединение может являться антагонистом указанного рецептора. Соединение, которое является частичным агонистом, в некоторых случаях может являться частичным активатором рецептора, в то время как в других случаях может являться частичным ингибитором функции рецептора. Еще в некоторых условиях соединение может являться тканеспецифическим модулятором, в то время как в других условиях соединение может быть генспецифическим модулятором.
Некоторые соединения, раскрываемые в данном описании, могут существовать в виде стереоизомеров, включая оптические изомеры. В объем настоящего изобретения входят все стереоизомеры и рацемические смеси таких стереоизомеров, а также отдельные энантиомеры, которые можно разделить согласно способам, хорошо известным специалистам в данной области.
В другом аспекте настоящее изобретение относится к фармацевтической композиции, содержащей физиологически приемлемый носитель, разбавитель или эксципиент или их сочетание и соединение формулы I, II или XV.
Термин "фармацевтическая композиция" относится к смеси соединения изобретения с другими химическими компонентами, такими как разбавители или носители. Фармацевтическая композиция облегчает введение соединения в организм. В данной области существует множество методов введения соединения, такие как пероральное введение, инъекция, в виде аэрозоля, парентеральное и местное введение, и другие методы. Фармацевтическую композицию также можно получить взаимодействием соединений с неорганическими или органическими кислотами, такими как хлористоводородная кислота, бромистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота, метансульфоновая кислота, этансульфоновая кислота, п-толуолсульфоновая кислота, салициловая кислота и т.п.
Термин "носитель" относится к химическому соединению, которое облегчает внедрение соединения в клетки или ткани. Например, диметилсульфоксид (ДМСО) является обычно используемым носителем, так как он облегчает поглощение многих органических соединений в клетках или тканях организма.
Термин "разбавитель" относится к химическому соединению, разведенному в воде, которое будет растворять нужное соединение, а также стабилизировать биологически активную форму соединения. В данной области в качестве разбавителей используют соли, растворенные в забуференных растворах. Одним из обычно используемых забуференных растворов является забуференный фосфатом физиологический раствор, поскольку он имитирует солевые состояния крови человека. Так как буферные соли могут регулировать рН раствора в низких концентрациях, забуференный разбавитель редко изменяет биологическую активность соединения.
Термин "физиологически приемлемый" относится к носителю или разбавителю, который не препятствует биологической активности и свойствам соединения.
Фармацевтические композиции, описанные в данном описании, можно вводить больному человеку per se или в фармацевтических композициях, в которых они смешаны с другими активными ингредиентами, как при комбинированной терапии, или с подходящими носителями или эксципиентом(ами). Способы получения и введения соединений настоящего изобретения можно найти в "Remington's Pharmaceutical Sciences", Mack Publishing Co., Easton, PA, 18th edition, 1990.
Подходящие способы введения могут включать, например, пероральное, ректальное, трансмукозное или интестинальное введение; парентеральную доставку, включая внутримышечные, подкожные, внутривенные и интрамедуллярные инъекции, а также интратекальные, прямые интравентрикулярные, интраперитонеальные, интраназальные или интраокулярные инъекции.
Альтернативно, соединение можно вводить местно, а не системно, например, инъекцией соединения непосредственно в ренальную или кардиальную область, часто, в композиции депо или с замедленным высвобождением. Кроме того, лекарственное средство можно вводить в нацеленной системе доставки лекарственного средства, например в липосоме с покрытием из тканеспецифических антител. Липосомы будут направляться и селективно поглощаться определенным органом.
Фармацевтические композиции настоящего изобретения можно получить способом, известным самим по себе, например обычными способами смешивания, растворения, грануляции, изготовления драже, растирания в порошок, эмульгирования, инкапсулирования, улавливания и таблетирования.
Таким образом, фармацевтические композиции для применения согласно настоящему изобретению можно получить обычными способами с использованием одного или нескольких физиологически приемлемых носителей, содержащих эксципиенты и вспомогательные вещества, облегчающие переработку активных соединений в препараты, которые можно использовать фармацевтически. Конкретная композиция зависит от выбранного способа введения. Любой из хорошо известных способов, носителей и эксципиентов можно использовать как подходящий и как общепринятый в данной области, см., например, Remington's Pharmaceutical Sciences, цит. выше.
Для инъекции средства по изобретению можно получить в виде водных растворов, предпочтительно, в физиологически совместимых буферах, таких как раствор Хэнкса, раствор Рингера или забуференный физиологический раствор. Для трансмукозного введения в композиции используют смачивающие вещества, соответствующие барьеру, через который происходит проникновение. Такие смачивающие вещества, как правило, известны в данной области.
Для перорального введения соединения можно ввести в композиции, просто объединив активные соединения с фармацевтически приемлемыми носителями, хорошо известными в данной области. Такие носители способствуют введению соединений в композиции в виде таблеток, пилюль, драже, капсул, жидкостей, гелей, сиропов, взвесей, суспензий и т.п., для перорального приема пациентом, которого подвергают лечению. Фармацевтические препараты для перорального применения можно получить, смешивая один или несколько твердых эксципиентов с фармацевтической комбинацией изобретения, необязательно, измельчая полученную смесь и перерабатывая смесь в гранулы после добавления подходящих вспомогательных веществ, при необходимости, для получения ядер таблеток или драже. Подходящими эксципиентами являются, в частности, наполнители, такие как сахара, в том числе, лактоза, сахароза, маннит или сорбит; целлюлозные препараты, такие как, например, кукурузный крахмал, пшеничный крахмал, рисовый крахмал, картофельный крахмал, желатин, трагакантовая камедь, метилцеллюлоза, гидроксипропилметилцеллюлоза, натрийкарбоксиметилцеллюлоза и/или поливинилпирролидон (PVP). При необходимости, можно добавить дезинтегрирующие вещества, такие как сшитый поливинилпирролидон, агар или альгиновая кислота или ее соль, такая как альгинат натрия.
На ядра наносят подходящие покрытия. Для такой цели можно использовать концентрированные растворы сахара, которые, необязательно, могут содержать аравийскую камедь, тальк, поливинилпирролидон, карбополгель, полиэтиленгликоль и/или диоксид титана, растворы глазури и подходящие органические растворители или смеси растворителей. В покрытия таблеток или драже можно добавить красители или пигменты для идентификации или характеризации различных комбинаций доз активных соединений.
Фармацевтические препараты, которые можно применять перорально, включают составные капсулы, изготовленные из желатина, а также мягкие сплошные капсулы, изготовленные из желатина и пластификатора, такого как глицерин или сорбит. Составные капсулы могут содержать активные ингредиенты в смеси с наполнителем, таким как лактоза, связующими веществами, такими как крахмалы, и/или смазывающими веществами, такими как тальк или стеарат магния, и, необязательно, стабилизаторами. В мягких капсулах активные соединения могут быть растворены или суспендированы в подходящих жидкостях, таких как жирные масла, жидкий парафин или жидкие полиэтиленгликоли. Кроме того, могут быть добавлены стабилизаторы. Все композиции для перорального введения должны находиться в дозировках, подходящих для такого введения.
Для трансбуккального введения композиции могут принимать форму таблеток или лепешек, полученных обычными способами.
Для введения ингаляцией соединения для применения согласно настоящему изобретению обычно доставляют в форме аэрозольного спрея, поступающего из упаковок под давлением или ингалятора с применением подходящего пропеллента, например дихлордифторметана, трихлорфторметана, дихлортетрафторэтана, диоксида углерода или другого подходящего газа. В случае аэрозоля, находящегося под давлением, единичную дозу можно определить с помощью клапана для доставки отмеренного количества. Капсулы и картриджи из, например, желатина для применения в ингаляторе или инсуффляторе можно получить в композициях, содержащих смесь порошка соединения и подходящей порошковой основы, такой как лактоза или крахмал.
Соединения можно ввести в композиции для парентерального введения инъекцией, например инъекцией ударной дозы вещества, или непрерывной инфузией. Композиции для инъекции можно представить в единичной дозированной форме, например, в ампулах или многодозовых емкостях с добавлением консерванта. Композиции могут принимать такие формы, как суспензии, растворы или эмульсии в масляных или водных средах, и могут содержать вещества для получения композиций, такие как суспендирующие, стабилизирующие и/или диспергирующие вещества.
Фармацевтические композиции для парентерального введения включают водные растворы активных соединений в водорастворимой форме. Кроме того, можно получить суспензии активных соединений в виде подходящих масляных суспензий для инъекций. Подходящие липофильные растворители или среды включают жировые масла, такие как сезамовое масло, или синтетические эфиры жирных кислот, такие как этилолеат или триглицериды, или липосомы. Водные суспензии для инъекций могут содержать вещества, повышающие вязкость суспензии, такие как натрийкарбоксиметилцеллюлоза, сорбит или декстран. Необязательно, суспензия также может содержать подходящие стабилизаторы или вещества, повышающие растворимость соединений, для получения высококонцентрированных растворов.
Альтернативно, активный ингредиент может находиться в форме порошка для получения состава с подходящей средой, например стерильной апирогенной водой, перед применением.
Соединения также можно ввести в состав ректальных композиций, таких как суппозитории или удерживающие клизмы, например, содержащие обычные основы для суппозиториев, такие как масло какао или другие глицериды.
Кроме композиций, описанных выше, соединения также можно ввести в состав препаратов-депо. Такие препараты длительного действия можно вводить имплантацией (например, подкожно или внутримышечно) или внутримышечной инъекцией. Так, например, соединения можно ввести в композиции с подходящими полимерными или гидрофобными веществами (например, в виде эмульсии в приемлемом масле), или ионообменными смолами, или в виде умеренно растворимых производных, например в виде умеренно растворимой соли.
Фармацевтическим носителем для гидрофобных соединений изобретения является система сорастворителей, содержащая бензиловый спирт, неполярное поверхностно-активное вещество, смешивающийся с водой органический полимер и водную фазу. Обычная используемая система сорастворителей представляет собой систему сорастворителей VPD, которая представляет собой 3%, мас./об., раствор бензилового спирта, 8%, мас./об., раствор неполярного поверхностно-активного вещества полисорбата 80™ и 65%, мас./об., раствор полиэтиленгликоля 300, полученный в абсолютном этаноле. Естественно, пропорции в системе сорастворителей могут значительно изменяться, не нарушая ее характеристик растворимости и токсичности. Кроме того, идентичность компонентов сорастворителя может изменяться: например, вместо полисорбата 80™ можно использовать другие малотоксичные неполярные поверхностно-активные вещества; может изменяться размер фракции полиэтиленгликоля; полиэтиленгликоль можно заменить другими биосовместимыми полимерами, например поливинилпирролидоном; и другие сахара или полисахариды могут заменить декстрозу.
Альтернативно, можно использовать другие системы доставки для гидрофобных фармацевтических соединений. Липосомы и эмульсии являются хорошо известными примерами сред или носителей для гидрофобных лекарственных средств. Также можно использовать некоторые органические растворители, такие как диметилсульфоксид, хотя, как правило, возможным последствием является большая токсичность. Кроме того, соединения можно доставлять с использованием систем с замедленным высвобождением, таких как полупроницаемые матрицы твердых гидрофобных полимеров, содержащие лечебное средство. Различные материалы для систем с замедленным высвобождением разработаны и хорошо известны специалистам в данной области. Капсулы с замедленным высвобождением могут, в зависимости от их химической природы, высвобождать соединения в течение нескольких недель на протяжении более 100 дней. В зависимости от химической природы и биологической устойчивости лечебного реагента можно использовать другие стратегии для стабилизации белков.
Многие соединения, используемые в фармацевтических комбинациях изобретения, могут предоставляться в виде солей с фармацевтически совместимыми противоионами. Фармацевтически совместимые соли могут быть образованы со многими кислотами, включая хлористоводородную, серную, уксусную, молочную, винную, яблочную, янтарную и другие кислоты. Соли имеют тенденцию быть более растворимыми в водных или других протонных растворителях, чем соответствующие формы свободных кислот или оснований.
Фармацевтические композиции, подходящие для применения в настоящем изобретении, включают композиции, в которых активные ингредиенты содержатся в количестве, эффективном для достижения поставленной цели. Конкретнее, терапевтически эффективное количество означает количество соединения, эффективное для предупреждения, облегчения или устранения симптомов заболевания или продления жизнеспособности субъекта, которого подвергают лечению. Определение терапевтически эффективного количества вполне могут осуществить специалисты в данной области, в особенности, в свете данного детального описания.
Конкретный состав, способ введения и дозировку фармацевтических композиций настоящего изобретения каждый лечащий врач может выбрать с учетом состояния пациента (см., например, Fingl et al., 1975, "The Pharmacological Basis of Therapeutics", Ch. 1, p.1). Конкретно, интервал доз композиции, вводимой пациенту, может составлять от примерно 0,5 до 1000 мг/кг массы тела пациента. Дозировка может быть однократной или вводиться два или большее число раз курсом из одного или нескольких дней, как это требуется данному пациенту. Следует отметить, что почти для всех конкретных соединений, указанных в настоящем описании, установлены дозировки для людей для лечения, по меньшей мере, некоторого состояния. Так, в большинстве случаев в настоящем изобретении будут использоваться те же дозировки или дозировки, которые находятся в интервале от примерно 0,1% до 500%, предпочтительнее, от примерно 25% до примерно 250%, от дозировки, установленной для людей. Если дозировка для людей не установлена, как будет в случае вновь разработанных фармацевтических соединений, подходящую дозировку можно вывести из величин ED50 или ID50 или других соответствующих величин, полученных в исследованиях in vitro или in vivo, установленных исследованиями токсичности и эффективности на животных.
Хотя точная дозировка будет определяться на основании действия лекарственного средства, в большинстве случаев можно сделать некоторое обобщение относительно дозировки. Схема ежесуточного приема для взрослого человека может составлять, например, пероральную дозу от 0,1 мг до 500 мг каждого ингредиента, предпочтительно, от 1 мг до 250 мг, например 5-200 мг, или внутривенную, подкожную или внутримышечную дозу каждого ингредиента от 0,01 мг до 100 мг, предпочтительно, от 0,1 мг до 60 мг, например 1-40 мг каждого ингредиента фармацевтических композиций настоящего изобретения или его фармацевтически приемлемой соли в расчете на свободное основание, причем композицию вводят 1-4 раза в сутки. Альтернативно, композиции изобретения можно вводить непрерывной внутривенной инфузией, предпочтительно, при дозе каждого ингредиента до 400 мг в сутки. Таким образом, общая суточная дозировка при пероральном введении каждого ингредиента конкретно будет находиться в интервале от 1 до 2000 мг, и общая суточная дозировка при парентеральном введении конкретно будет находиться в интервале от 0,1 до 400 мг. Подходящим будет являться введение соединений на протяжении непрерывного лечения, например, в течение недели или более, или в течение месяцев или лет.
Количество доз и интервал можно подобрать индивидуально для обеспечения в плазме уровней активного начала, которые достаточны для поддержания модулирующего действия или минимальной эффективной концентрации (МЕС). МЕС будет изменяться для каждого соединения, но ее можно оценить из данных, полученных in vitro. Дозировки, необходимые для достижения МЕС, будут зависеть от индивидуальных особенностей и способа введения. Однако для определения концентраций в плазме можно использовать анализы методом ВЭЖХ или биологические анализы.
Дозировочные интервалы также можно определить с использованием величины МЕС. Композиции следует вводить с использованием схемы, которая поддерживает уровни в плазме выше МЕС в течение 10-90% времени, предпочтительно - 30-90% и наиболее предпочтительно - 50-90%.
В случаях местного введения или селективного поглощения эффективная местная концентрация лекарственного средства может не соотноситься с концентрацией в плазме.
Вводимое количество композиции будет, естественно, зависеть от особенностей субъекта, которого подвергают лечению, массы субъекта, тяжести заболевания, способа введения и предписаний лечащего врача.
Композиции, при необходимости, можно предоставлять в упаковке или распределительном устройстве, которые могут содержать одну или несколько единичных дозированных форм, содержащих активный ингредиент. Упаковка, например, может состоять из металлической фольги или пластиковой пленки, как, например, блистерная упаковка. К упаковке или распределительному устройству могут прилагаться инструкции по введению. К упаковке или распределительному устройству также может прилагаться извещение, закрепленное на упаковке, в форме, предписанной государственным органом, регулирующим производство, применение или продажу фармацевтических препаратов, в котором отражается одобрение органа формы лекарственного средства для применения в медицине или ветеринарии. Такое извещение, например, может представлять собой этикетку, содержащую одобрение Управления U.S. Food and Drug на лекарственные средства или на вложенный продукт. Композиции, содержащие соединение изобретения в составе с совместимым фармацевтическим носителем, также могут быть получены, помещены в соответствующую упаковку и снабжены этикеткой для лечения указанного состояния.
В другом аспекте настоящее изобретение относится к способу лечения психоневрологического расстройства у пациента, включающему введение указанному пациенту терапевтически эффективного количества соединения формулы I или II. В некоторых вариантах осуществления психоневрологическое расстройство выбирают из группы, состоящей из шизофрении и родственных идиопатических психозов, тревоги, расстройств сна, расстройств аппетита, аффективных расстройств, таких как большая депрессия, биполярное расстройство и депрессия с психотическими признаками, и синдрома Туретта, психозов, вызванных лекарственными средствами, психозов, вторичных по отношению к психоневрологическим расстройствам, таким как болезнь Альцгеймера или болезнь Гентингтона.
В некоторых вариантах осуществления соединение формулы I или XV представляет собой клозапин, в то время как в других вариантах осуществления соединение представляет собой N-десметилклозапин. В некоторых других вариантах осуществления соединение формулы I или XV не является клозапином или N-десметилклозапином.
В еще одном аспекте настоящее изобретение относится к способу лечения психоневрологического расстройства у пациента, включающему контактирование терапевтически эффективного количества соединения формулы I, II или XV с указанным пациентом.
В некоторых вариантах осуществления настоящее изобретение относится к фармацевтической композиции, содержащей соединение формулы I, II или XV и психоневрологическое средство. Используемый в данном описании термин "психоневрологическое средство" относится к соединению или комбинации соединений, воздействующей на нейроны головного мозга или непосредственно или косвенно, или воздействующей на сигнал, передаваемый нейронам головного мозга. Следовательно, психоневрологические средства могут воздействовать на психическое состояние человека, такое как настроение человека, перцепция, ноцицепция, познание, живость ума, память и т.д. В некоторых вариантах осуществления психоневрологическое средство можно выбрать из группы, состоящей из селективного ингибитора повторного поглощения серотонина, ингибитора повторного поглощения норэпинефрина, агониста дофамина, антипсихотического средства, антагониста серотонина 2А и обратного агониста серотонина 2А.
В некоторых вариантах осуществления антипсихотическое средство можно выбрать из группы, состоящей из фенотиазина, фенилбутилпиперадина, дебензапина, бензизоксидила и соли лития. Фенотиазиновую группу соединений можно выбрать из группы, состоящей из хлорпромазина (Thorazine®), мезоридазина (Serentil®), прохлорперазина (Compazine®) и тиоридазина (Mellaril®). Фенилбутилпиперадиновую группу соединений можно выбрать из группы, состоящей из галоперидола (Haldol®) и пимозида (Orap®). Дебензапиновую группу соединений можно выбрать из группы, состоящей из клозапина (Clozaril®), локсапина (Loxitane®), оланзапина (Zyprexa®) и кветиапина (Seroquel®). Бензизоксидиловую группу соединений можно выбрать из группы, состоящей из респеридона (Resperidal®) и ципразидона (Geodon®). Соль лития может представлять собой карбонат лития. В некоторых вариантах осуществления антипсихотическое средство можно выбрать из группы, состоящей из арипипразола (Abilify), клозапина, Clozaril, Compazine, Etrafon, Geodon, Haldol, Inapsine, Loxitane, Mellaril, Moban, Navane, оланзапина (Zyprexa), Orap, Permitil, Prolixin, Phenergan, кветиапина (Seroquelа), Reglan, Risperdal, Serentil, Seroquel, Stelazine, Taractan, Thorazine, Triavil, Triaflon и Zyprexa или их фармацевтически приемлемых солей.
В некоторых вариантах осуществления селективный ингибитор повторного поглощения серотонина выбирают из группы, состоящей из флуоксетина, флувоксамина, сертралина, пароксетина, циталопрама, эсциталопрама, сибутрамина, дулоксетина и венлафаксина и их фармацевтически приемлемых солей и пролекарств.
В некоторых вариантах осуществления ингибитор повторного поглощения норэпинефрина выбирают из группы, состоящей из тионизоксетина и ребоксетина.
В других вариантах осуществления агонист допамина выбирают из группы, состоящей из суматриптана, альмотриптана, наратриптана, фроватриптана, ризатриптана, зомитриптана, каберголина, амантадина, лизурида, перголида, ропинирола, прамипексола и бромокриптина.
В другом варианте осуществления обратный агонист серотонина 2А представляет собой АСР-103 или его аналог. АСР-103 является обозначением соединения формулы XIII

В другом воплощении антагонист серотонина 2А представляет собой М 110907 или его аналог. М 110907 является обозначением соединения формулы XIV

В другом аспекте настоящее изобретение относится к способу лечения психоневрологического расстройства у пациента, включающему введение указанному пациенту терапевтически эффективного количества фармацевтической композиции, содержащей соединения формулы I, II или XV и психоневрологическое средство. В еще одном аспекте настоящее изобретение относится к способу лечения психоневрологического расстройства у пациента, включающему введение указанному пациенту терапевтически эффективного количества соединения формулы I, II или XV и терапевтически эффективного количества психоневрологического средства.
В некоторых вариантах осуществления пациентом является млекопитающее. Млекопитающее может быть выбрано из группы, состоящей из мышей, крыс, кроликов, морских свинок, собак, кошек, овец, коз, коров, приматов, таких как обезьяны, шимпанзе и человекообразные обезьяны, и людей. В некоторых вариантах осуществления пациентом является человек.
В некоторых вариантах осуществления стадия введения в вышеуказанных способах включает введение указанного соединения формулы I, II или XV и указанного психоневрологического средства почти одновременно. К таким вариантам осуществления относятся варианты, в которых соединение формулы I или II и психоневрологическое средство находятся в одной и той же предназначенной для введения композиции, т.е. в одной таблетке, пилюле или капсуле, или в одном растворе для внутривенной инъекции, или в одном растворе, который можно пить, или в одном препарате драже или пэтче, содержащих оба соединения. Варианты осуществления также включают воплощения, в которых каждое соединение находится в отдельной предназначенной для введения композиции, но пациенту назначен прием таких отдельных композиций почти одновременно, т.е. одну пилюлю принимают сразу же после другой или одну инъекцию одного соединения делают сразу же после инъекции другого соединения и т.д.
В других вариантах осуществления стадия введения включает введение сначала одного активного начала из числа соединения формулы I, II или XV и психоневрологического средства, а затем введение другого активного начала из числа соединения формулы I, II или XV и психоневрологического средства. В таких вариантах осуществления пациенту может быть введена композиция, содержащая одно из соединений, и затем через некоторое время в несколько минут или несколько часов введена другая композиция, содержащая одно другое соединение. К таким вариантам осуществления также относятся варианты, в которых композицию, содержащую одно из соединений, пациенту вводят обычным или непрерывным способом, причем в то же время он время от времени получает композицию, содержащую другое соединение.
В некоторых вариантах осуществления психоневрологическое расстройство, которое подвергают лечению способами и соединениями настоящего изобретения, выбирают из группы, состоящей из шизофрении и родственных идиопатических психозов, тревоги, расстройств сна, расстройств аппетита, аффективных расстройств, таких как большая депрессия, биполярное расстройство и депрессия с психотическими признаками, и синдрома Туретта, психозов, вызванных лекарственными средствами, и психозов, вторичных по отношению к психоневрологическим расстройствам, таким как болезнь Альцгеймера или Гентингтона.
Примеры
Пример 1. Общая методика 1 (ОМ1)
Смесь аминобензойной кислоты (1 экв.), 2-фторнитробензола (3 экв.) и Cs2CO3 (3 экв.) в ДМФА нагревают при 140оС в течение 1 часа и затем оставляют при комнатной температуре. Смесь разбавляют водой и промывают EtOAc (2×).
К водной фазе добавляют EtOH и Na2S2O4 (5 экв.) и полученную смесь перемешивают в течение 1 часа. К смеси добавляют хлористоводородную кислоту (2М), затем водную фазу экстрагируют EtOAc (3×) и объединенные органические фазы концентрируют.
Остаток растворяют в CH2Cl2, добавляют гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида (3 экв.), полученную смесь перемешивают при комнатной температуре в течение 1 часа и затем концентрируют. Остаток разбавляют EtOAc, промывают водным раствором NaOH (2М) и концентрируют.
Остаток растворяют в диоксане и при 50°С добавляют к смеси TiCl4 (1,1 экв., 1М раствор в толуоле) и пиперазина (5 экв.) в диоксане. Полученную смесь перемешивают при 100°С в течение ночи и затем оставляют при комнатной температуре. К смеси добавляют хлористоводородную кислоту (2М) до тех пор, пока раствор не станет кислым, и затем водную фазу экстрагируют EtOAc (2×). К водной фазе добавляют водный раствор NaOH (2М) до тех пор, пока раствор не станет щелочным и полученную суспензию экстрагируют EtOAc (3×). Объединенные органические фазы концентрируют и остаток очищают ВЭЖХ.
Пример 2. 2,7-Дихлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (166JO85F1)

4-Хлор-2-фторнитробензол (263 мг, 1,5 ммоль) и 2-амино-5-хлорбензойную кислоту (86 мг, 0,5 ммоль) подвергают взаимодействию согласно ОМ1 и получают 6,1 мг указанного в заголовке соединения (166JO85F1). МС (ESI) 347 (MH+). Чистота для МН+ (УФ/МС) 100/85.
Пример 3. 2-Хлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (166JO85F6)
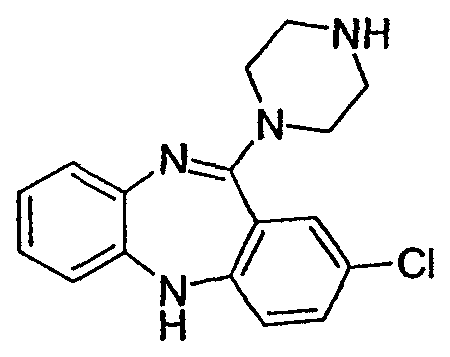
2-Фторнитробензол (212 мг, 1,5 ммоль) и 2-амино-5-хлорбензойную кислоту (86 мг, 0,5 ммоль) подвергают взаимодействию согласно ОМ1 и получают 5,3 мг указанного в заголовке соединения (166JO85F6). МС (ESI) 313 (MH+). Чистота для МН+ (УФ/МС) 100/95.
Пример 4. 2,8-Дихлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (166JO85F2)

5-Хлор-2-фторнитробензол (263 мг, 1,5 ммоль) и 2-амино-5-хлорбензойную кислоту (86 мг, 0,5 ммоль) подвергают взаимодействию согласно ОМ1 и получают 4,8 мг указанного в заголовке соединения (166JO85F2). МС (ESI) 347 (MH+). Чистота для МН+ (УФ/МС) 99/99.
Пример 5. 8-Бром-2-хлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (166JO85F3)

5-Бром-2-фторнитробензол (330 мг, 1,5 ммоль) и 2-амино-5-хлорбензойную кислоту (86 мг, 0,5 ммоль) подвергают взаимодействию согласно ОМ1 и получают 8,0 мг указанного в заголовке соединения (166JO85F3). МС (ESI) 391 (MH+). Чистота для МН+ (УФ/МС) 100/96.
Пример 6. 2-Хлор-11-(пиперазин-1-ил)-8-трифторметил-5Н-дибензо[b,e][1,4]диазепин (166JO85F7)

4-Фтор-3-нитробензотрифторид (314 мг, 1,5 ммоль) и 2-амино-5-хлорбензойную кислоту (86 мг, 0,5 ммоль) подвергают взаимодействию согласно ОМ1 и получают 0,3 мг указанного в заголовке соединения (166JO85F7). МС (ESI) 381 (MH+). Чистота для МН+ (УФ/МС) 100/95.
Пример 7. 6-Хлор-11-(пиперазин-1-ил)-8-трифторметил-5Н-дибензо[b,e][1,4]диазепин (189JO77В)
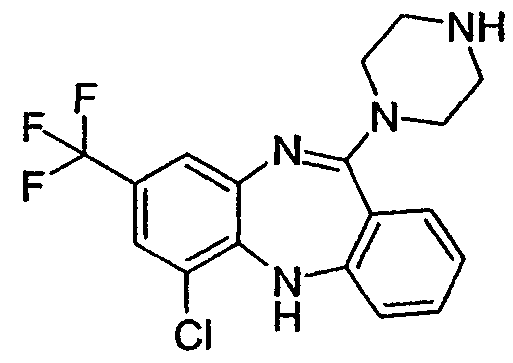
3-Хлор-4-фтор-5-нитробензотрифторид (366 мг, 1,5 ммоль) и 2-аминобензойную кислоту (69 мг, 0,5 ммоль) подвергают взаимодействию согласно ОМ1 и получают 28 мг указанного в заголовке соединения (189JO77В). МС (ESI) 381 (MH+). Чистота для МН+ (УФ/МС) 99/100.
Пример 8. 7-Хлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE35В)

4-Хлор-2-фторнитробензол (528 мг, 3,0 ммоль) и 2-аминобензойную кислоту (138 мг, 1,0 ммоль) подвергают взаимодействию согласно ОМ1 и получают 5,0 мг указанного в заголовке соединения (160FE35В). МС (ESI) 313 (MH+). Чистота для МН+ (УФ/МС) 99/86.
Пример 9. 8-Бром-1-хлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE36А)
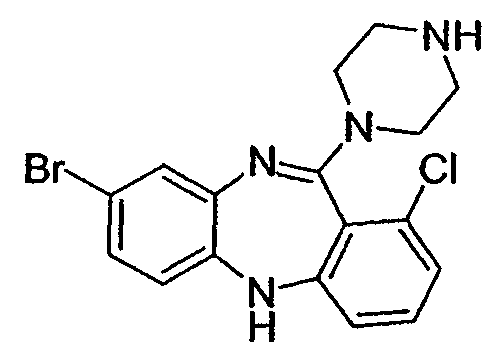
5-Бром-2-фторнитробензол (660 мг, 3,0 ммоль) и 2-амино-6-хлорбензойную кислоту (172 мг, 1,0 ммоль) подвергают взаимодействию согласно ОМ1 и получают 5,0 мг указанного в заголовке соединения (160FE36А). МС (ESI) 391 (MH+). Чистота для МН+ (УФ/МС) 94/87.
Пример 10. 8-Бром-2-метил-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE40С)
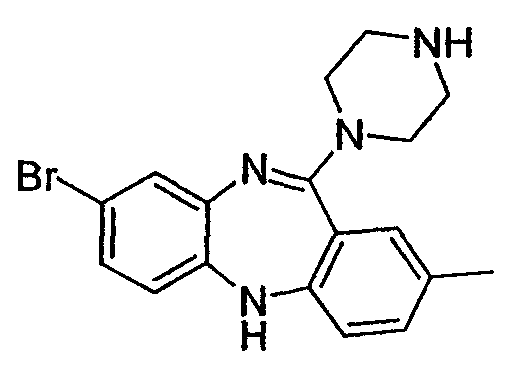
5-Бром-2-фторнитробензол (660 мг, 3,0 ммоль) и 2-амино-5-метилбензойную кислоту (152 мг, 1,0 ммоль) подвергают взаимодействию согласно ОМ1 и получают 7,9 мг указанного в заголовке соединения (160FE40С). МС (ESI) 371 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 11. 4,8-Дихлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE41А)
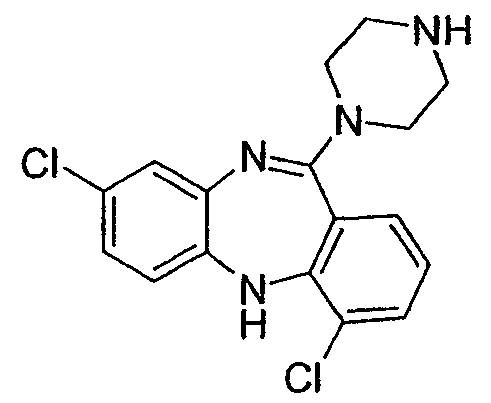
5-Хлор-2-фторнитробензол (527 мг, 3,0 ммоль) и 2-амино-3-хлорбензойную кислоту (172 мг, 1,0 ммоль) подвергают взаимодействию согласно ОМ1 и получают 4,6 мг указанного в заголовке соединения (160FE41А). МС (ESI) 347 (MH+). Чистота для МН+ (УФ/МС) 95/70.
Пример 12. 8-Хлор-2-метил-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE41В)

5-Хлор-2-фторнитробензол (527 мг, 3,0 ммоль) и 2-амино-5-метилбензойную кислоту (151 мг, 1,0 ммоль) подвергают взаимодействию согласно ОМ1 и получают 7,1 мг указанного в заголовке соединения (160FE41В). МС (ESI) 327 (MH+). Чистота для МН+ (УФ/МС) 100/94.
Пример 13. 8-Хлор-2-фтор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE42А-F3)
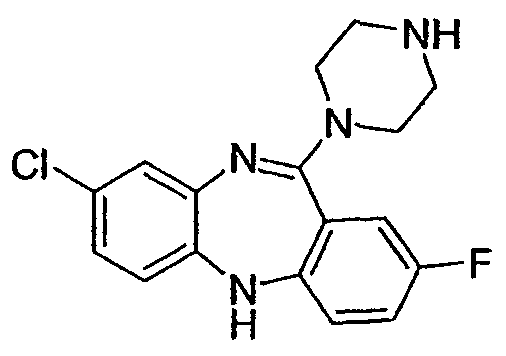
5-Хлор-2-фторнитробензол (264 мг, 1,5 ммоль) и 2-амино-5-фторбензойную кислоту (78 мг, 0,5 ммоль) подвергают взаимодействию согласно ОМ1 и получают 21 мг указанного в заголовке соединения (160FE42А-F3). МС (ESI) 331 (MH+). Чистота для МН+ (УФ/МС) 99/98.
Пример 14. 3,8-Дихлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE42В-F4)
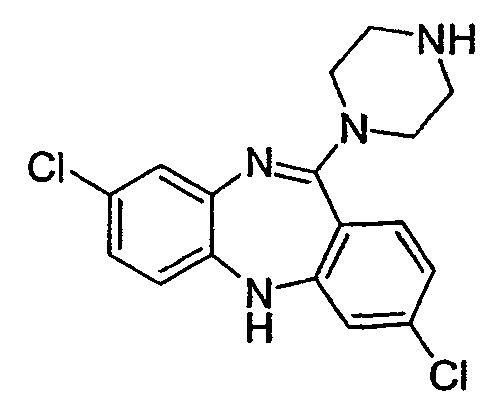
5-Хлор-2-фторнитробензол (264 мг, 1,5 ммоль) и 2-амино-4-хлорбензойную кислоту (86 мг, 0,5 ммоль) подвергают взаимодействию согласно ОМ1 и получают 9,4 мг указанного в заголовке соединения (160FE42В-F4). МС (ESI) 347 (MH+). Чистота для МН+ (УФ/МС) 99/97.
Пример 15. 2-Бром-8-хлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE43А-F6)
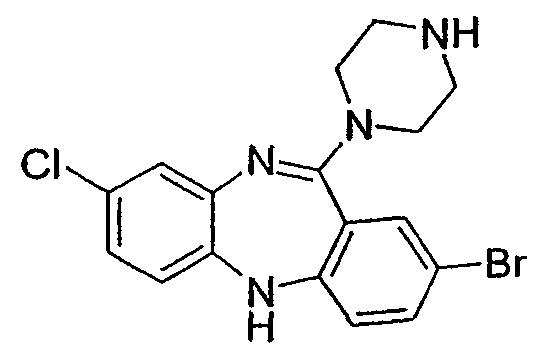
5-Хлор-2-фторнитробензол (528 мг, 3,0 ммоль) и 2-амино-5-бромбензойную кислоту (216 мг, 1,0 ммоль) подвергают взаимодействию согласно ОМ1 и получают 20 мг указанного в заголовке соединения (160FE43А-F6). МС (ESI) 391 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 16. 3,7-Дихлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE58D1)
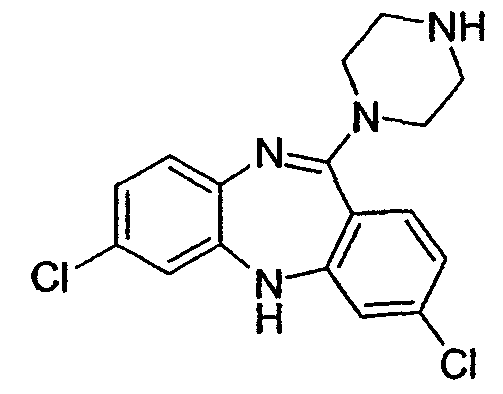
4-Хлор-2-фторнитробензол (263 мг, 1,5 ммоль) и 2-амино-4-хлорбензойную кислоту (86 мг, 0,5 ммоль) подвергают взаимодействию согласно ОМ1 и получают 3,1 мг указанного в заголовке соединения (160FE58D1). МС (ESI) 347 (MH+). Чистота для МН+ (УФ/МС) 63/83.
Пример 17. 8-Бром-3-хлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE58D3)

5-Бром-2-фторнитробензол (330 мг, 1,5 ммоль) и 2-амино-4-хлорбензойную кислоту (86 мг, 0,5 ммоль) подвергают взаимодействию согласно ОМ1 и получают 1,1 мг указанного в заголовке соединения (160FE58D3). МС (ESI) 391 (MH+). Чистота для МН+ (УФ/МС) 90/85.
Пример 18. 3-Хлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE58D6)

2-Фторнитробензол (212 мг, 1,5 ммоль) и 2-амино-4-хлорбензойную кислоту (86 мг, 0,5 ммоль) подвергают взаимодействию согласно ОМ1 и получают 2,2 мг указанного в заголовке соединения (160FE58D6). МС (ESI) 313 (MH+). Чистота для МН+ (УФ/МС) 90/100.
Пример 19. 3-Хлор-11-(пиперазин-1-ил)-8-трифторметил-5Н-дибензо[b,e][1,4]диазепин (160FE58D7)
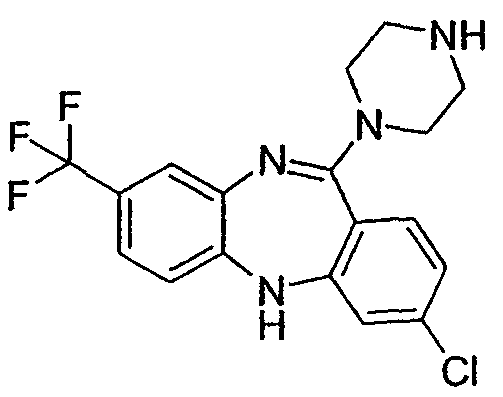
4-Фтор-3-нитробензотрифторид (314 мг, 1,5 ммоль) и 2-амино-4-хлорбензойную кислоту (86 мг, 0,5 ммоль) подвергают взаимодействию согласно ОМ1 и получают 2,0 мг указанного в заголовке соединения (160FE58D7). МС (ESI) 313 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 20. 7-Хлор-2-метил-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE58Е1)
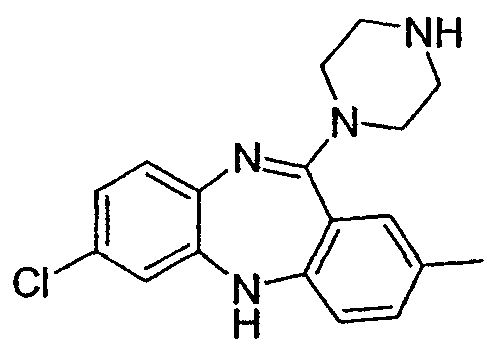
4-Хлор-2-фторнитробензол (263 мг, 1,5 ммоль) и 2-амино-5-метилбензойную кислоту (76 мг, 0,5 ммоль) подвергают взаимодействию согласно ОМ1 и получают 1,1 мг указанного в заголовке соединения (160FE58Е1). МС (ESI) 327 (MH+). Чистота для МН+ (УФ/МС) 100/90.
Пример 21. 2-Метил-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE58Е6)
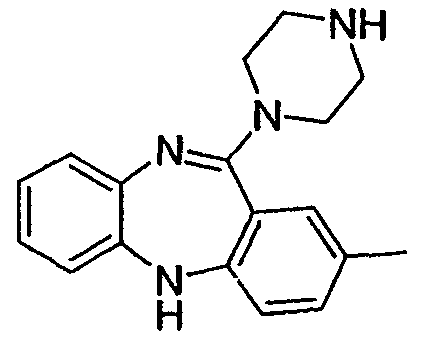
4-Фторнитробензол (212 мг, 1,5 ммоль) и 2-амино-5-метилбензойную кислоту (76 мг, 0,5 ммоль) подвергают взаимодействию согласно ОМ1 и получают 6,8 мг указанного в заголовке соединения (160FE58Е6). МС (ESI) 293 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 22. 2-Метил-11-(пиперазин-1-ил)-8-трифторметил-5Н-дибензо[b,e][1,4]диазепин (160FE58Е7)

4-Фтор-3-нитробензотрифторид (314 мг, 1,5 ммоль) и 2-амино-5-метилбензойную кислоту (76 мг, 0,5 ммоль) подвергают взаимодействию согласно ОМ1 и получают 1,2 мг указанного в заголовке соединения (160FE58Е7). МС (ESI) 361 (MH+). Чистота для МН+ (УФ/МС) 100/85.
Пример 23. 8-Хлор-4-метил-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE74С)
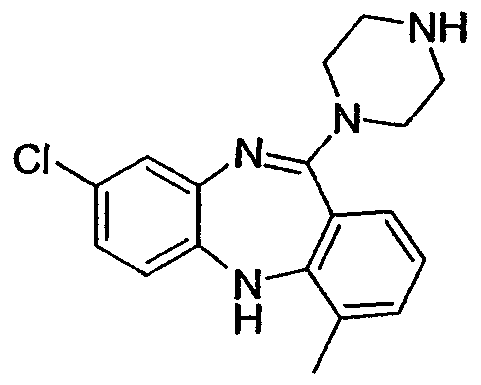
5-Хлор-2-фторнитробензол (1,06 г, 6,0 ммоль) и 2-амино-3-метилбензойную кислоту (302 мг, 2,0 ммоль) подвергают взаимодействию согласно ОМ1 и получают 4,8 мг указанного в заголовке соединения (160FE74С). МС (ESI) 327 (MH+). Чистота для МН+ (УФ/МС) 97/90.
Пример 24. 1,8-Дихлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (203FE03)

5-Хлор-2-фторнитробензол (1,06 г, 6,0 ммоль) и 2-амино-6-хлорбензойную кислоту (343 мг, 2,0 ммоль) подвергают взаимодействию согласно ОМ1 и получают 3,1 мг указанного в заголовке соединения (203FE03). МС (ESI) 347 (MH+). Чистота для МН+ (УФ/МС) 100/99.
Пример 25. 8-Бром-5-метил-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (166JO32)
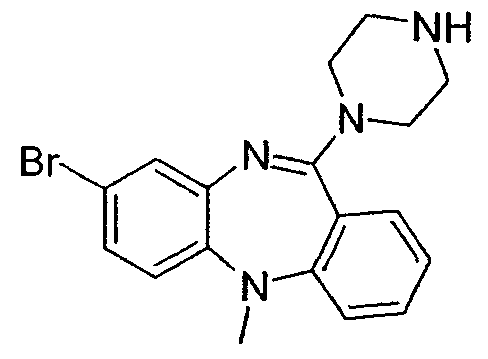
5-Бром-2-фторнитробензол (580 мг, 2,6 ммоль) и N-метилантраниловую кислоту (200 мг, 1,3 ммоль) подвергают взаимодействию согласно ОМ1 и получают 1,6 мг указанного в заголовке соединения (166JO32). МС (ESI) 371 (MH+). Чистота для МН+ (УФ/МС) 90/74.
Пример 26. Общая методика 2 (ОМ2)
Смесь аминобензойной кислоты (1 экв.), 2-фторнитробензола (3 экв.) или 2-хлорнитробензола (3 экв.) и Cs2CO3 (3 экв.) в ДМФА нагревают при 140°С в течение 1 часа и затем оставляют при комнатной температуре. Смесь разбавляют водой и промывают EtOAc (2×).
К водной фазе добавляют EtOH и Na2S2O4 (5 экв.) и полученную смесь перемешивают в течение 1 часа. К смеси добавляют хлористоводородную кислоту (2М), затем водную фазу экстрагируют EtOAc (3×) и объединенные органические фазы концентрируют.
Остаток растворяют в ксилоле и полученную смесь перемешивают при 130°С в течение ночи. Смесь разбавляют EtOAc, промывают насыщенным водным раствором NaHCO3, сушат (Na2SO4) и концентрируют.
Остаток растворяют в диоксане и при 50°С добавляют к смеси TiCl4 (1,1 экв., 1М раствор в толуоле) и пиперазина (5 экв.) в диоксане. Полученную смесь перемешивают при 100°С в течение ночи и затем оставляют при комнатной температуре. К смеси добавляют хлористоводородную кислоту (2М) до тех пор, пока раствор не станет кислым, и затем водную фазу экстрагируют EtOAc (2×). К водной фазе добавляют водный раствор NaOH (2М) до тех пор, пока раствор не станет щелочным и полученную суспензию экстрагируют EtOAc (3×). Объединенные органические фазы концентрируют и остаток очищают ВЭЖХ.
Пример 27. 7,8-Дихлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (166JO28)

1,2-Дихлор-4-фтор-5-нитробензол (1,26 г, 6,0 ммоль) и 2-аминобензойную кислоту (274 мг, 2 ммоль) подвергают взаимодействию согласно ОМ2 и получают 16 мг указанного в заголовке соединения (166JO28). МС (ESI) 347 (MH+). Чистота для МН+ (УФ/МС) 99/96.
Пример 28. 11-(Пиперазин-1-ил)-8-трифторметил-5Н-дибензо[b,e][1,4]диазепин (166JO23)

4-Фтор-3-нитробензотрифторид (1,25 г, 6 ммоль) и 2-аминобензойную кислоту (274 мг, 2 ммоль) подвергают взаимодействию согласно ОМ2 и получают 12 мг указанного в заголовке соединения (166JO23). МС (ESI) 347 (MH+). Чистота для МН+ (УФ/МС) 81/98.
Пример 29. 11-(Пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE19А)

2-Фторнитробензол (847 мг, 6,0 ммоль) и 2-аминобензойную кислоту (274 мг, 2 ммоль) подвергают взаимодействию согласно ОМ2 и получают 16 мг указанного в заголовке соединения (160FE19А). МС (ESI) 279 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 30. 8-Фтор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE19С)

2,5-Дифторнитробензол (955 мг, 6,0 ммоль) и 2-аминобензойную кислоту (274 мг, 2 ммоль) подвергают взаимодействию согласно ОМ2 и получают 8,9 мг указанного в заголовке соединения (160FE19С). МС (ESI) 297 (MH+). Чистота для МН+ (УФ/МС) 99/97.
Пример 31. 11-(Пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин-8-карбонитрил (160FE19D)

4-Хлор-3-нитробензол (1,10 г, 6,0 ммоль) и 2-аминобензойную кислоту (274 мг, 2 ммоль) подвергают взаимодействию согласно ОМ2 и получают 4,7 мг указанного в заголовке соединения (160FE19D). МС (ESI) 304 (MH+). Чистота для МН+ (УФ/МС) 100/86.
Пример 32. 8-Бром-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE19Е)
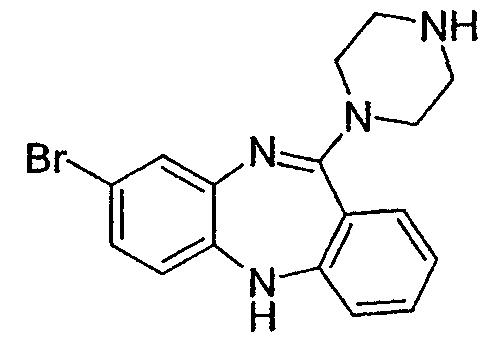
5-Бром-2-фторнитробензол (1,32 г, 6,0 ммоль) и 2-аминобензойную кислоту (274 мг, 2 ммоль) подвергают взаимодействию согласно ОМ2 и получают 15 мг указанного в заголовке соединения (160FE19Е). МС (ESI) 357 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 33. 8-Метил-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE19F)
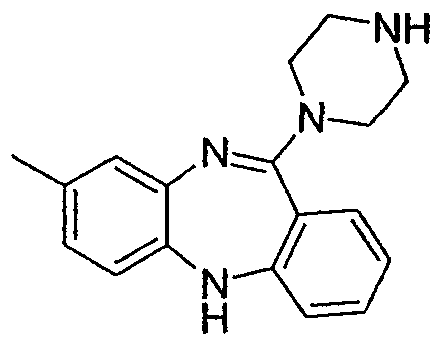
4-Хлор-3-нитротолуол (1,03 г, 6,0 ммоль) и 2-аминобензойную кислоту (274 мг, 2 ммоль) подвергают взаимодействию согласно ОМ2 и получают 1,6 мг указанного в заголовке соединения (160FE19F). МС (ESI) 293 (MH+). Чистота для МН+ (УФ/МС) 70/70.
Пример 34. Общая методика 3 (ОМ3)
К производному N-метилпиперазина (0,1 ммоль), растворенному в ТГФ (2 мл), при 10°С добавляют 1-хлорэтилхлорформиат (17 мг, 0,12 ммоль). Затем полученную смесь кипятят с обратным холодильником в течение 18 часов. Температуру снижают и удаляют ТГФ при пониженном давлении. Затем к оставшемуся маслу добавляют метанол и смесь встряхивают при 65°С в течение 2 часов. Метанол удаляют при пониженном давлении и оставшийся неочищенный продукт реакции очищают ВЭЖХ.
Пример 35. 3-Фтор-6-пиперазин-1-ил-11Н-дибензо[b,e]азепин (160FE02)
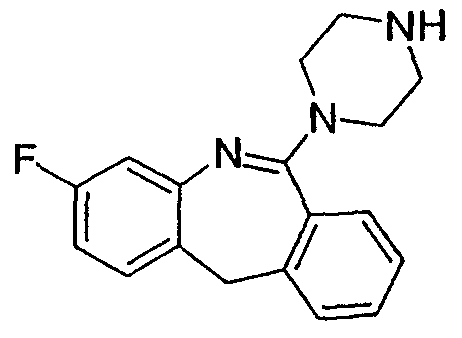
3-Фтор-6-(4-метилпиперазин-1-ил)-11Н-дибензо[b,e]азепин (31 мг, 0,1 ммоль) подвергают взаимодействию согласно ОМ3 и получают 8 мг указанного в заголовке соединения, выделенного в виде соли оксалата (160FE02). МС (ESI) 296 (MH+). Чистота для МН+ (УФ/МС) 99/100.
Пример 36. 2-(Трифторметансульфонилокси)-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE13А)

2-(Трифторметансульфонилокси)-11-(4-метилпиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (39 мг, 0,1 ммоль) подвергают взаимодействию согласно ОМ3 и получают 3,0 мг указанного в заголовке соединения (160FE13А). МС (ESI) 427 (MH+). Чистота для МН+ (УФ/МС) 95/98.
Пример 37. 2-(Трифторметансульфонилокси)-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]оксазепин (160FE13В)

2-(Трифторметансульфонилокси)-11-(4-метилпиперазин-1-ил)-5Н-дибензо[b,e][1,4]оксазепин (39 мг, 0,1 ммоль) подвергают взаимодействию согласно ОМ3 и получают 11 мг указанного в заголовке соединения (160FE13В). МС (ESI) 428 (MH+). Чистота для МН+ (УФ/МС) 98/100.
Пример 38. 8-Хлор-2-(трифторметансульфонилокси)-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE13С)

8-Хлор-2-(трифторметансульфонилокси)-11-(4-метилпиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (42 мг, 0,1 ммоль) подвергают взаимодействию согласно ОМ3 и получают 3,2 мг указанного в заголовке соединения (160FE13С). МС (ESI) 461 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 39. 8-(Трифторметансульфонилокси)-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE13D)

8-(Трифторметансульфонилокси)-11-(4-метилпиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (39 мг, 0,1 ммоль) подвергают взаимодействию согласно ОМ3 и получают 2,2 мг указанного в заголовке соединения (160FE13D). МС (ESI) 427 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 40. Общая методика 4 (ОМ4)
К смеси TiCl4 (1,1 экв., 1М раствор в толуоле) и амина (0,5 ммоль) в диоксане при 50°С или к смеси TiCl4 (2,2 экв., 1М раствор в толуоле) и амина (1,0 ммоль) в диоксане при 50°С добавляют смесь соответствующего лактама (0,1 ммоль) в диоксане. Полученную смесь перемешивают при 100°С в течение ночи и затем оставляют при комнатной температуре. К водной смеси добавляют хлористоводородную кислоту (3 мл, 2М) и затем водную фазу экстрагируют EtOAc (2×4 мл). К водной фазе добавляют водный раствор NaOH (6 мл, 2М) и полученную суспензию экстрагируют EtOAc (3×3 мл). Объединенные органические фазы концентрируют и остаток очищают ВЭЖХ.
Пример 41. 11-(Пиперазин-1-ил)-дибензо[b,f][1,4]тиазепин (160FE17А)

10Н-Дибензо[b,f][1,4]тиазепин-11-он (23 мг, 0,1 ммоль) и пиперазин (43 мг, 0,5 ммоль) подвергают взаимодействию согласно ОМ4 и получают 3,1 мг указанного в заголовке соединения (160FE17А). МС (ESI) 296 (MH+). Чистота для МН+ (УФ/МС) 97/90.
Пример 42. 11-(Пиперазин-1-ил)-2,3-дигидро-1,4-бензодиоксино[6,7-b][1,4]бензотиазепин (160FE17В)

2,3-Дигидро-1,4-бензодиоксино[6,7-b][1,4]бензотиазепин-11(12Н)-он (29 мг, 0,1 ммоль) и пиперазин (43 мг, 0,5 ммоль) подвергают взаимодействию согласно ОМ4 и получают 1,9 мг указанного в заголовке соединения (160FE17В). МС (ESI) 354 (MH+). Чистота для МН+ (УФ/МС) 99/95.
Пример 43. 8-Хлор-11-[1,4]диазепам-1-ил-5Н-дибензо[b,e][1,4]диазепин (160FE16А)

8-Хлор-5,10-дигидродибензо[b,e][1,4]диазепин-11-он (25 мг, 0,1 ммоль) и гомопиперазин (50 мг, 0,5 ммоль) подвергают взаимодействию согласно ОМ4 и получают 12 мг указанного в заголовке соединения (160FE16А). МС (ESI) 327 (MH+). Чистота для МН+ (УФ/МС) 99/93.
Пример 44. N'-(8-Хлор-5Н-дибензо[b,e][1,4]диазепин-11-ил)-N,N-диметилэтан-1,2-диамин (160FE16D)

8-Хлор-5,10-дигидродибензо[b,e][1,4]диазепин-11-он (25 мг, 0,1 ммоль) и N,N-диметилэтилендиамин (44 мг, 0,5 ммоль) подвергают взаимодействию согласно ОМ4 и получают 20 мг указанного в заголовке соединения (160FE16D). МС (ESI) 315 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 45. N'-(8-Хлор-5Н-дибензо[b,e][1,4]диазепин-11-ил)-N,N-диэтилэтан-1,2-диамин (160FE16Е)

8-Хлор-5,10-дигидродибензо[b,e][1,4]диазепин-11-он (25 мг, 0,1 ммоль) и N,N-диэтилэтилендиамин (58 мг, 0,5 ммоль) подвергают взаимодействию согласно ОМ4 и получают 3,9 мг указанного в заголовке соединения (160FE16Е). МС (ESI) 343 (MH+). Чистота для МН+ (УФ/МС) 99/94.
Пример 46. 8-Хлор-11-(4-метил[1,4]диазепам-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE16F)
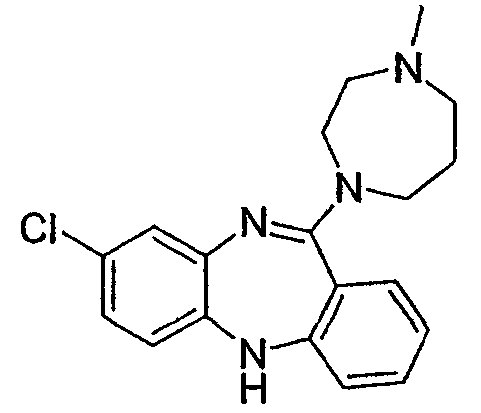
8-Хлор-5,10-дигидродибензо[b,e][1,4]диазепин-11-он (25 мг, 0,1 ммоль) и 1-метилгомопиперазин (57 мг, 0,5 ммоль) подвергают взаимодействию согласно ОМ4 и получают 5,7 мг указанного в заголовке соединения (160FE16F). МС (ESI) 341 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 47. 8-Хлор-2-метокси-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE20А)
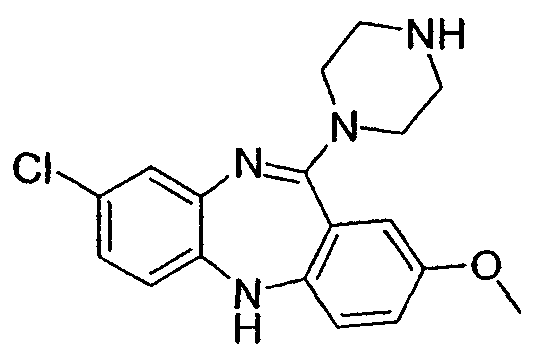
8-Хлор-2-метокси-5,10-дигидродибензо[b,e][1,4]диазепин-11-он (28 мг, 0,1 ммоль) и пиперазин (86 мг, 1,0 ммоль) подвергают взаимодействию согласно ОМ4 и получают 19 мг указанного в заголовке соединения (160FE20А). МС (ESI) 342 (MH+). Чистота для МН+ (УФ/МС) 99/100.
Пример 48. N'-(5Н-Дибензо[b,e][1,4]диазепин-11-ил)-N,N-диметилэтан-1,2-диамин (160FE20В)

5,10-Дигидродибензо[b,e][1,4]диазепин-11-он (160FE15A) (21 мг, 0,1 ммоль) и N,N-диметилэтилендиамин (88 мг, 1,0 ммоль) подвергают взаимодействию согласно ОМ4 и получают 7,6 мг указанного в заголовке соединения (160FE20В). МС (ESI) 281 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 49. 11-[1,4]Диазепам-1-ил-5Н-дибензо[b,e][1,4]диазепин (160FE20С)
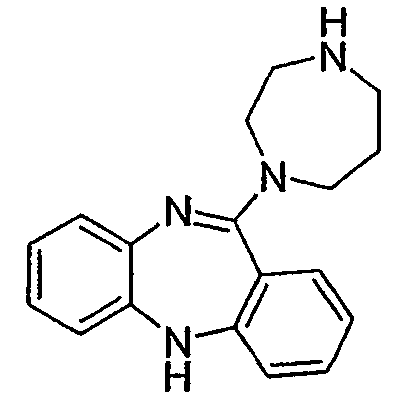
5,10-Дигидродибензо[b,e][1,4]диазепин-11-он (160FE15A) (21 мг, 0,1 ммоль) и гомопиперазин (100 мг, 1,0 ммоль) подвергают взаимодействию согласно ОМ4 и получают 12 мг указанного в заголовке соединения (160FE20С). МС (ESI) 293 (MH+). Чистота для МН+ (УФ/МС) 95/95.
Пример 50. N'-(8-Фтор-5Н-дибензо[b,e][1,4]диазепин-11-ил)-N,N-диметилэтан-1,2-диамин (160FE20D)

8-Фтор-5,10-дигидродибензо[b,e][1,4]диазепин-11-он (160FE15С) (23 мг, 0,1 ммоль) и N,N-диметилэтилендиамин (88 мг, 1,0 ммоль) подвергают взаимодействию согласно ОМ4 и получают 11 мг указанного в заголовке соединения (160FE20D). МС (ESI) 299 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 51. 8-Фтор-11-[1,4]диазепам-1-ил-5Н-дибензо[b,e][1,4]диазепин (160FE20Е)
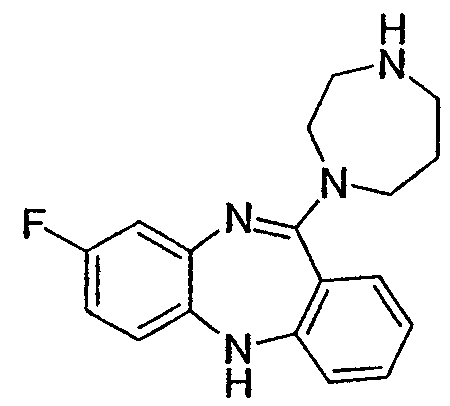
8-Фтор-5,10-дигидродибензо[b,e][1,4]диазепин-11-он (160FE15С) (23 мг, 0,1 ммоль) и гомопиперазин (100 мг, 1,0 ммоль) подвергают взаимодействию согласно ОМ4 и получают 19 мг указанного в заголовке соединения (160FE20Е). МС (ESI) 311 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 52. N'-(8-Хлор-5Н-дибензо[b,e][1,4]диазепин-11-ил)-N-метилэтан-1,2-диамин (160FE22)

8-Хлор-5,10-дигидродибензо[b,e][1,4]диазепин-11-он (25 мг, 0,1 ммоль) и N-метилэтилендиамин (74 мг, 1,0 ммоль) подвергают взаимодействию согласно ОМ4 и получают 7,6 мг указанного в заголовке соединения (160FE22). МС (ESI) 301 (MH+). Чистота для МН+ (УФ/МС) 92/83.
Пример 53. 8-Хлор-11-(транс-2,5-диметилпиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE33А)
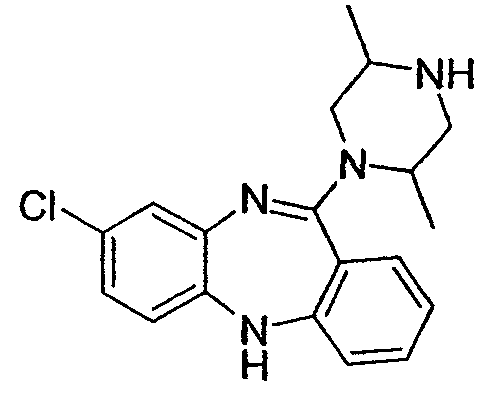
8-Хлор-5,10-дигидродибензо[b,e][1,4]диазепин-11-он (25 мг, 0,1 ммоль) и транс-2,5-диметилпиперазин (114 мг, 1,0 ммоль) подвергают взаимодействию согласно ОМ4 и получают 1,9 мг указанного в заголовке соединения (160FE33А). МС (ESI) 341 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 54. 8-Хлор-11-(3,5-диметилпиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE33В)

8-Хлор-5,10-дигидродибензо[b,e][1,4]диазепин-11-он (25 мг, 0,1 ммоль) и 2,6-диметилпиперазин (114 мг, 1,0 ммоль) подвергают взаимодействию согласно ОМ4 и получают 18 мг указанного в заголовке соединения (160FE33В). МС (ESI) 341 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 55. 8-Хлор-11-(3-метилпиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE38)

8-Хлор-5,10-дигидродибензо[b,e][1,4]диазепин-11-он (25 мг, 0,1 ммоль) и 2-метилпиперазин (100 мг, 1,0 ммоль) подвергают взаимодействию согласно ОМ4 и получают 30 мг указанного в заголовке соединения (160FE38). МС (ESI) 327 (MH+). Чистота для МН+ (УФ/МС) 100/89.
Пример 56. 8-Хлор-11-(3-фенилпиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE45)

8-Хлор-5,10-дигидродибензо[b,e][1,4]диазепин-11-он (25 мг, 0,1 ммоль) и 2-фенилпиперазин (162 мг, 1,0 ммоль) подвергают взаимодействию согласно ОМ4 и получают 27 мг указанного в заголовке соединения (160FE45). МС (ESI) 389 (MH+). Чистота для МН+ (УФ/МС) 100/89.
Пример 57. 8-Хлор-5-метил-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (189JO25А)

К смеси 8,5-дихлор-5Н-дибензо[b,e][1,4]диазепина (160FЕ64) (50 мг, 0,19 ммоль) и толуола (1,5 мл) в ДМФА (0,5 мл) добавляют NaH (12 мг, 0,29 ммоль, 60% в минеральном масле). Затем добавляют MeI (24 мкл, 0,38 ммоль). Полученную смесь перемешивают в течение 1 часа и затем реакцию гасят, добавляя насыщенный водный раствор NaHCO3 (2 мл). Смесь экстрагируют диэтиловым эфиром, объединенные органические фазы сушат (Na2SO4) и концентрируют. Остаток растворяют в толуоле (2,0 мл), добавляют пиперазин (98 мг, 1,1 ммоль) и полученную смесь перемешивают при 100°С в течение 1 часа. Затем к смеси добавляют хлористоводородную кислоту (1 мл, 2М) и EtOAc (2 мл). Фазы разделяют, водную фазу экстрагируют EtOAc (2 мл) и затем добавляют водный раствор NaOH (2 мл, 2М). Щелочную водную фазу экстрагируют EtOAc (3×2 мл), объединенные органические фазы сушат (Na2SO4) и концентрируют. Остаток растворяют в ДМФА, очищают ВЭЖХ и получают 34 мг указанного в заголовке соединения (189JO25А). МС (ESI) 327 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 58. 8-Хлор-5-бензил-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (160FE46-PIPBN)
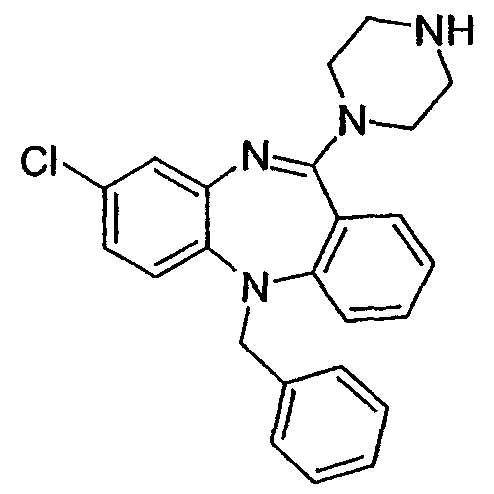
8,5-Дихлор-5Н-дибензо[b,e][1,4]диазепин (160FЕ46) (51 мг, 0,20 ммоль) и бензилбромид (68 мг, 0,4 ммоль) подвергают взаимодействию так, как описано в примере 57, и получают 8,4 мг указанного в заголовке соединения (160FE46-PIPBN). МС (ESI) 403 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 59. 8-Иод-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (166JO38)
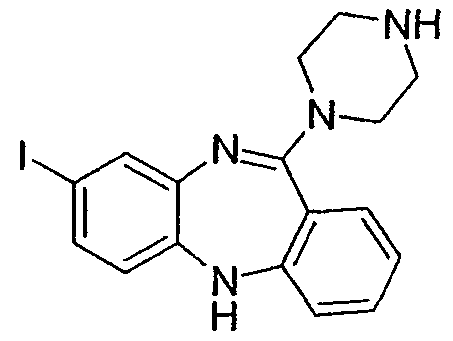
Смесь 8-бром-5,10-дигидродибензо[b,e][1,4]диазепин-11-она (166JO31) (60 мг, 0,21 ммоль), NaI (62 мг, 0,42 ммоль), N,N-диметилэтилендиамина (2,2 мкл, 0,021 ммоль) и CuI (2 мг, 0,42 ммоль) в диоксане (1 мл) нагревают в закрытой пробирке в течение 3 суток. Реакционную смесь охлаждают до комнатной температуры, затем смесь вносят в колонку с ионообменной смолой SCX-2, продукт реакции элюируют CH2Cl2 и получают 49 мг промежуточного 8-иодлактама. Промежуточный иодлактам (20 мг, 0,060 ммоль) в диоксане (1 мл) при 50°С добавляют к смеси TiCl4 (0,13 мл, 0,13 ммоль, 1М раствор в толуоле) и пиперазина (0,051 г, 0,60 ммоль) в диоксане. Полученную смесь перемешивают при 100°С в течение ночи и затем оставляют при комнатной температуре. К смеси добавляют хлористоводородную кислоту (3 мл, 2М) и затем водную фазу экстрагируют EtOAc (2×4 мл). К водной фазе добавляют водный раствор NaOH (6 мл, 2М) и полученную суспензию экстрагируют EtOAc (3×3 мл). Объединенные органические фазы концентрируют. Остаток очищают ВЭЖХ и получают 4,1 мг указанного в заголовке соединения (166JO38). МС (ESI) 405 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 60. 2-Иод-8-хлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (166JO54)

2-Бром-8-хлор-5,10-дигидродибензо[b,e][1,4]диазепин-11-он (промежуточное соединение по методике ОМ1) (30 мг, 0,09 ммоль) подвергают взаимодействию так, как описано в примере 59, и получают 7,0 мг указанного в заголовке соединения (166JO54). МС (ESI) 439 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 61. 8-Фенил-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (189JO53)

К смеси 8-бром-5,10-дигидродибензо[b,e][1,4]диазепин-11-она (166JO31) (30 мг, 0,12 ммоль), бензолбороновой кислоты (18 мг, 0,15 ммоль) и К2СО3 (34 мг, 0,24 ммоль) в обескислороженной смеси толуол/EtOH/H2O (1,5 мл) добавляют тетракис(трифенилфосфин)палладий(0) (каталитическое количество) и полученную смесь перемешивают при 80°С в течение ночи. Смесь разбавляют EtOAc, промывают насыщенным водным раствором NaHCO3, сушат (Na2SO4), концентрируют и получают неочищенный 8-фениллактам. Промежуточный фениллактам в диоксане (1 мл) при 50°С добавляют к смеси TiCl4 (0,24 мл, 0,24 ммоль, 1М раствор в толуоле) и пиперазина (0,103 г, 1,2 ммоль) в диоксане. Полученную смесь перемешивают при 100°С в течение ночи и затем оставляют при комнатной температуре. К смеси добавляют хлористоводородную кислоту (3 мл, 2М) и затем водную фазу экстрагируют EtOAc (2×4 мл). К водной фазе добавляют водный раствор NaOH (6 мл, 2М) и полученную суспензию экстрагируют EtOAc (3×3 мл). Объединенные органические фазы вносят в колонку с ионообменной смолой SCX-2. Колонку промывают МеОН, затем продукт реакции элюируют NH3 (7н. раствор в МеОН), концентрируют, остаток очищают ВЭЖХ и получают 16 мг указанного в заголовке соединения (189JO53). МС (ESI) 355 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 62. 8-Хлор-11-(пиперидин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (166JO69А)

К неочищенному 8-хлор-11-метилсульфанил-5Н-дибензо[b,e][1,4]диазепину (166JO50) (90 мг, чистота 50%, 0,218 ммоль) в пиридине (2 мл) добавляют пиперидин (37 мг, 0,44 ммоль) и полученную смесь нагревают в закрытой пробирке при 160°С в течение 10 ч. Смесь концентрируют, остаток подвергают флэш-хроматографии (SiO2, гептан:EtOAc, 8:1-6:1) и получают 12 мг указанного в заголовке соединения (166JO69А). МС (ESI) 312 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 63. 8-Хлор-11-(морфолин-4-ил)-5Н-дибензо[b,e][1,4]диазепин (166JO69В)

Неочищенный 8-хлор-11-метилсульфанил-5Н-дибензо[b,e][1,4]диазепин (166JO50) (90 мг, чистота 50%, 0,218 ммоль) и морфолин подвергают взаимодействию, как описано в примере 62, и получают 11 мг указанного в заголовке соединения (166JO69В). МС (ESI) 314 (MH+). Чистота для МН+ (УФ/МС) 100/98.
Пример 64. 5-Аллил-8-хлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (166JO68)
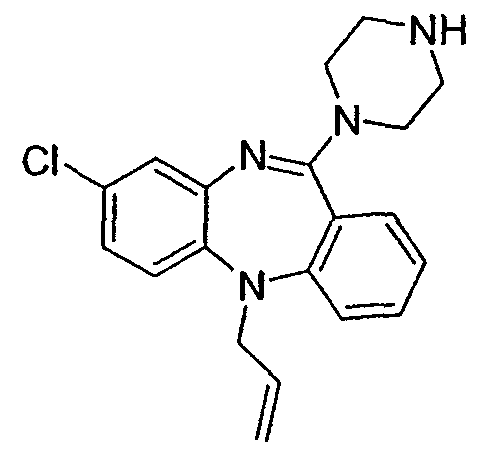
К смеси 8-хлор-5,10-дигидродибензо[b,e][1,4]диазепин-11-она (500 мг, 2,0 ммоль) и диоксана (10 мл) добавляют К-трет-OВu (343 мг, 3,1 ммоль), полученную смесь перемешивают при 60°С в течение 1 часа, затем охлаждают до комнатной температуры, добавляют п-метоксибензилхлорид (0,42 мл, 3,1 ммоль) и полученную смесь перемешивают при 40°С в течение 2 ч. Реакцию гасят, добавляя МеОН (2 мл). Смесь разбавляют CH2Cl2, промывают насыщенным водным раствором NaHCO3, сушат (Na2SO4), концентрируют, остаток подвергают флэш-хроматографии (SiO2, гептан:EtOAc, 4:1-3:1) и получают промежуточный п-метоксибензилзащищенный лактам (732 мг), чистота 85%, который используют на следующей стадии без дополнительной очистки.
К смеси п-метоксибензилзащищенного лактама (100 мг, 0,27 ммоль) и ДМФА (2 мл) добавляют NaH (16 мг, 0,41 ммоль, 60% в минеральном масле), полученную смесь нагревают до 60°С и затем оставляют при комнатной температуре. Добавляют аллилбромид (36 мкл, 0,41 ммоль), полученную смесь перемешивают при комнатной температуре в течение 3 часов, затем разбавляют CH2Cl2, промывают насыщенным водным раствором NaHCO3, сушат (Na2SO4), концентрируют, остаток подвергают флэш-хроматографии (SiO2, гептан:EtOAc, 8:1-4:1) и концентрируют. Остаток растворяют в трифторуксусной кислоте (4 мл), полученную смесь перемешивают при комнатной температуре в течение ночи и затем при 45°С в течение 2 часов. Смесь концентрируют, остаток подвергают хроматографии (SiO2, гептан:EtOAc, 8:1-4:1) и концентрируют. Остаток растворяют в толуоле (2 мл) и добавляют N,N-диметиланилин (48 мкл, 0,38 ммоль) и POCl3 (35 мкл, 0,38 ммоль). Полученную смесь перемешивают при 100°С в течение 2 часов и затем концентрируют. Остаток растворяют в диоксане, добавляют пиперазин (65 мг, 0,76 ммоль) и полученную смесь перемешивают при 100°С в течение 3 часов. К смеси добавляют хлористоводородную кислоту (3 мл, 2М) и затем водную фазу экстрагируют EtOAc (2×4 мл). К водной фазе добавляют водный раствор NaOH (6 мл, 2М) и полученную суспензию экстрагируют EtOAc (3×3 мл). Объединенные органические фазы концентрируют. Остаток очищают ВЭЖХ и получают 17 мг указанного в заголовке соединения (166JO68). МС (ESI) 353 (MH+). Чистота для МН+ (УФ/МС) 99/88.
Пример 65. 6-Хлор-11-(пиперазин-1-ил)-5Н-дибензо[b,e][1,4]диазепин (189JO68)
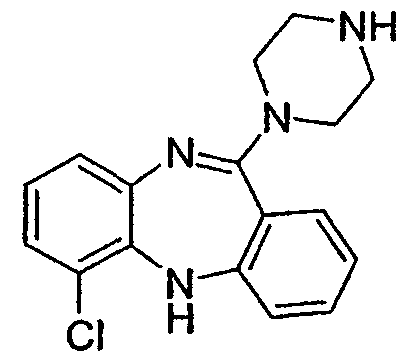
Смесь метил-2-аминобензоата (454 мг, 3,0 ммоль), 3-хлор-2-фторнитробензола (352 мг, 2 ммоль) и Cs2CO3 (0,78 г, 2,4 ммоль) в ДМФА (4 мл) перемешивают при 140°С в течение 2 часов.
Смесь разбавляют EtOAc, промывают 2М водным раствором NaОH (2×5 мл), сушат (Na2SO4), концентрируют, остаток подвергают флэш-хроматографии (SiO2, система толуол:гептан:EtOAc) и концентрируют. Остаток растворяют в ТГФ (10 мл), добавляют 1М водный раствор LiOH (5 мл), полученную смесь перемешивают при 80°С в течение 1 часа и затем оставляют при комнатной температуре. Добавляют 2М хлористоводородную кислоту до рН 2. Водную фазу экстрагируют EtOAc (2×4 мл). К водной фазе добавляют водный раствор NaOH (6 мл, 2М) и полученную суспензию экстрагируют EtOAc (3×). Объединенные органические фазы сушат (Na2SO4) и концентрируют. Остаток растворяют в EtOH, добавляют смесь К2СО3 (1,38 г, 10 ммоль) и Na2S2O4 (1,74 г, 10 ммоль) в воде и полученную смесь перемешивают в течение 1 часа. Смесь разбавляют водой, промывают 2М водным раствором NaОH (2×5 мл), затем сушат (Na2SO4) и концентрируют.
Остаток растворяют в CH2Cl2 и добавляют гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида (307 мг, 1,6 ммоль). Полученную смесь перемешивают при комнатной температуре в течение 1 часа. Смесь разбавляют EtOAc, промывают насыщенным водным раствором NaHCO3, сушат (Na2SO4), концентрируют, остаток подвергают флэш-хроматографии (SiO2, гептан:EtOAc, 2:1) и получают промежуточный лактам.
Промежуточный лактам растворяют в диоксане и при 50°С добавляют к смеси TiCl4 (0,19 мл, 0,19 ммоль, 1М раствор в толуоле) и пиперазина (73 мг, 0,85 ммоль) в диоксане. Полученную смесь перемешивают при 100°С в течение ночи и затем оставляют при комнатной температуре. К смеси добавляют хлористоводородную кислоту (1 мл, 2М) и затем водную фазу экстрагируют EtOAc (2×1 мл). К водной фазе добавляют водный раствор NaOH (2 мл, 2М) и полученную суспензию экстрагируют EtOAc (3×1 мл). Объединенные органические фазы концентрируют, остаток очищают ВЭЖХ и получают 9,8 мг указанного в заголовке соединения (189JO68). МС (ESI) 313 (MH+). Чистота для МН+ (УФ/МС) 100/98.
Пример 66. 8-Хлор-5-пиперазин-1-ил-11Н-бензо[b]пиридо[2,3-e][1,4]диазепин (166JO63)

К смеси 5-хлор-2-нитроанилина (345 мг, 2 ммоль) и пиридина (162 мкл, 2 ммоль) в диоксане добавляют 1-хлорникотинилхлорид (352 мг, 2 ммоль) и полученную смесь перемешивают при комнатной температуре в течение 2 ч. Смесь разбавляют CH2Cl2, промывают насыщенным водным раствором NaHCO3, сушат (Na2SO4), концентрируют, остаток кристаллизуют из МеОН и получают 271 мг промежуточного диариламина. К смеси промежуточного диариламина (100 мг, 0,32 ммоль) и EtOH (0,5 мл) добавляют смесь К2СО3 (220 мг, 1,6 ммоль) и Na2S2O4 (278 мг, 1,6 ммоль) в воде (0,5 мл) и полученную смесь перемешивают в течение 1 часа при комнатной температуре. Смесь концентрируют, остаток растворяют в EtOAc/H2O и слои разделяют. Органическую фазу сушат (Na2SO4) и концентрируют. Остаток растворяют в ксилоле и нагревают при 130°С в течение ночи, затем разбавляют EtOAc, промывают насыщенным водным раствором NaHCO3, сушат (Na2SO4), концентрируют, остаток подвергают флэш-хроматографии (SiO2, гептан:EtOAc) и получают промежуточный лактам. Промежуточный лактам растворяют в диоксане и при 50°С добавляют к смеси TiCl4 (187 мкл, 0,187 ммоль, 1М раствор в толуоле) и пиперазина (73 мг, 0,85 ммоль) в диоксане. Полученную смесь перемешивают при 100°С в течение ночи и затем оставляют при комнатной температуре. К смеси добавляют хлористоводородную кислоту (1 мл, 2М) и затем водную фазу экстрагируют EtOAc (2×2 мл). К водной фазе добавляют водный раствор NaOH (2 мл, 2М) и полученную суспензию экстрагируют EtOAc (3×1 мл). Объединенные органические фазы концентрируют, остаток очищают ВЭЖХ и получают 20 мг указанного в заголовке соединения (166JO63). МС (ESI) 314 (MH+). Чистота для МН+ (УФ/МС) 100/99.
Пример 67. 2-Хлор-10-пиперазин-1-ил-5Н-дибензо[b,f]азепин (189JO39)

К смеси 2-хлор-5-(4-метоксибензил)-5,11-дигидродибензо[b,f]азепин-11-она (189JO27) (150 мг, 0,41 ммоль) и CH2Cl2 (10 мл) в атмосфере Ar при -75°С добавляют TiCl4 (0,60 мл, 0,60 ммоль, 1М раствор в толуоле) и полученную смесь перемешивают в течение 1 часа. Смесь разбавляют насыщенным водным раствором NH4Cl и CH2Cl2, оставляют при комнатной температуре и разделяют фазы. Водную фазу экстрагируют CH2Cl2 (1×10 мл), объединенные органические фазы сушат (Na2SO4) и концентрируют и получают неочищенный продукт реакции, содержащий защитную группу (90 мг, 90%), который используют на следующей стадии без дополнительной очистки.
К раствору TiCl4 (0,18 мл, 0,18 ммоль, 1М раствор в толуоле) и пиперазина (283 мг, 3,3 ммоль) в диоксане (4 мл) при 50°С добавляют неочищенный продукт, содержащий защитную группу (80 мг, 0,33 ммоль), и полученную суспензию перемешивают при 100°С в течение 1,5 часа. Смесь оставляют при комнатной температуре, затем ее разбавляют EtOAc, промывают насыщенным водным раствором NaHCO3, сушат (Na2SO4), концентрируют, остаток подвергают флэш-хроматографии (Al2О3, CH2Cl2:MeOH, 1:0-25:1) и получают 64 мг (63%) указанного в заголовке соединения (189JO39). МС (ESI) 312 (MH+). Чистота для МН+ (УФ/МС) 97/95.
Пример 68. 8-Хлор-11-(пиперазин-1-ил)дибензо[b,f][1,4]тиазепин (189JO16)

К смеси 8-хлор-10Н-дибензо[b,f][1,4]тиазепин-11-она (189JO13) (38 мг, 0,15 ммоль) и N,N-диметиланилина (46 мкл, 0,36 ммоль) в толуоле добавляют POCl3 (27 мкл, 0,29 ммоль), полученную смесь перемешивают в течение 2 часов при 100°С и затем концентрируют. Добавляют толуол (2 мл) и пиперазин (62 мг, 0,73 ммоль), полученную смесь перемешивают при 100°С в течение 3 часов и затем оставляют при комнатной температуре. К смеси добавляют хлористоводородную кислоту (1 мл, 2М) и затем водную фазу экстрагируют EtOAс (2×2 мл). К водной фазе добавляют водный раствор NaOH (3 мл, 2М) и полученную смесь экстрагируют EtOAc (3×3 мл). Объединенные органические фазы концентрируют, остаток очищают ВЭЖХ и получают 6,6 мг указанного в заголовке соединения (189JO16). МС (ESI) 330 (MH+). Чистота для МН+ (УФ/МС) 99/98.
Пример 69. 8-Хлор-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин (189JO31)

Смесь 8-хлор-10Н-дибензо[b,f][1,4]оксазепин-11-она (189JO29С) (17 мг, 0,069 ммоль) и 2,4-бис(4-метоксифенил)-1,3-дитиа-2,4-дифосфетан-2,4-дисульфида (16 мг, 0,040 ммоль) в толуоле (2 мл) нагревают в закрытой пробирке с использованием микроволновой печи (130°С, 20 минут). Реакционную смесь охлаждают до комнатной температуры, добавляют MeI (18 мкл, 0,29 ммоль) и полученную смесь нагревают в закрытой пробирке с использованием микроволновой печи (120°С, 20 минут). Смесь концентрируют, остаток растворяют в пиридине (2 мл) и добавляют пиперазин (25 мг, 0,29 ммоль). Полученную смесь нагревают в закрытой пробирке при 130°С в течение ночи и затем с использованием микроволновой печи (160°С, 30 минут). Смесь концентрируют, разбавляют EtOAc и промывают водой. Органическую фазу вносят в колонку с ионообменной смолой SCX-2. Колонку промывают МеОН, затем продукт реакции элюируют NH3 (7н. раствор в МеОН) и получают 9,0 мг (57%) указанного в заголовке соединения (189JO31). МС (ESI) 314 (MH+). Чистота для МН+ (УФ/МС) 92/100.
Пример 70. 8-Хлор-11-(4-метилпиперидин-1-ил)дибензо[b,f][1,4]оксазепин (189JO47)
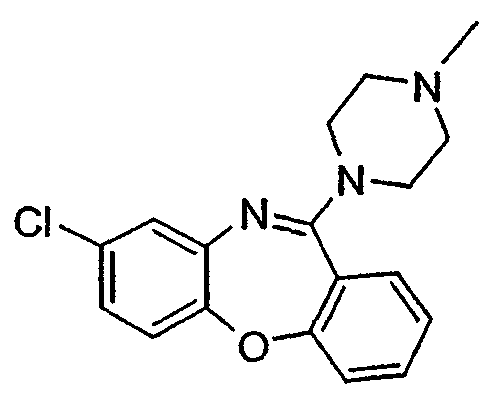
Смесь 8-хлор-10Н-дибензо[b,f][1,4]оксазепин-11-она (189JO29С) (30 мг, 0,069 ммоль) и 2,4-бис(4-метоксифенил)-1,3-дитиа-2,4-дифосфетан-2,4-дисульфида (29 мг, 0,040 ммоль) в толуоле (2 мл) нагревают в закрытой пробирке с использованием микроволновой печи (130°С, 20 минут). Реакционную смесь охлаждают до комнатной температуры, добавляют MeI (38 мкл, 0,29 ммоль) и полученную смесь нагревают в закрытой пробирке с использованием микроволновой печи (120°С, 20 минут). Смесь концентрируют, остаток растворяют в пиридине (2 мл) и добавляют пиперазин (24 мг, 0,29 ммоль). Полученную смесь нагревают в закрытой пробирке при 130°С в течение ночи и затем нагревают с использованием микроволновой печи (160°С, 30 минут). Смесь концентрируют, разбавляют EtOAc и промывают водой. Органическую фазу сушат (Na2SO4), концентрируют, подвергают флэш-хроматографии (SiO2, толуол:EtOAc:MeOH, 4:2:0 - 2:2:1) и получают 8,9 мг указанного в заголовке соединения (189JO47). МС (ESI) 328 (MH+). Чистота для МН+ (УФ/МС) 98/93.
Пример 71. 3-Хлор-6-пиперазин-1-ил-11Н-дибензо[b,е]азепин (189JO60)

3-Хлор-5,11-дигидродибензо[b,е]азепин-6-он (189JO59) (25 мг, 0,1 ммоль) и пиперазин подвергают взаимодействию согласно ОМ4 и получают 2,2 мг указанного в заголовке соединения (189JO60). МС (ESI) 312 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 72. Общая методика 5 (ОМ5)
Смесь метилового эфира аминобензойной кислоты (2,0 ммоль), 2-фторнитробензола (1,0 ммоль) и Cs2CO3 (0,65 г, 2,0 ммоль) в ДМФА (4 мл) перемешивают при 40°С в течение 2 ч. Смесь разбавляют EtOAc (10 мл) и промывают 2М водным раствором NaOH (2×5 мл).
К фазе EtOAc добавляют EtOH, Н2О, К2СО3 (0,69 г, 5 ммоль) и Na2S2O4 (0,87 г, 5 ммоль) и полученную смесь энергично перемешивают в течение 1 часа. Водную фазу удаляют, органическую фазу промывают 1М водным раствором NaOH (2×5 мл) и затем концентрируют.
Остаток растворяют в ДМФА (1 мл), добавляют толуол (4 мл) и NaH (60 мг, 1,5 ммоль, 60% в минеральном масле), полученную смесь перемешивают при 80°С в течение ночи и затем реакцию гасят, добавляя насыщенный водный раствор NH4Cl. Полученную смесь разбавляют EtOAc, промывают 2М водным раствором NaOH (2×5 мл), сушат (Na2SO4) и концентрируют. Остаток растворяют в диоксане и при 50°С добавляют к смеси TiCl4 (1,1 мл, 1,1 ммоль, 1М раствор в толуоле) и пиперазина (0,41 г, 5 ммоль) в диоксане. Полученную смесь перемешивают при 100°С в течение ночи и затем оставляют при комнатной температуре. К смеси добавляют хлористоводородную кислоту (3 мл, 2М) и затем водную фазу экстрагируют EtOAc (2×4 мл). К водной фазе добавляют водный раствор NaOH (6 мл, 2М) и полученную суспензию экстрагируют EtOAc (3×3 мл). Объединенные органические фазы сушат (Na2SO4), концентрируют и остаток очищают ВЭЖХ.
Пример 73. 8-Бром-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин (189JO48А)
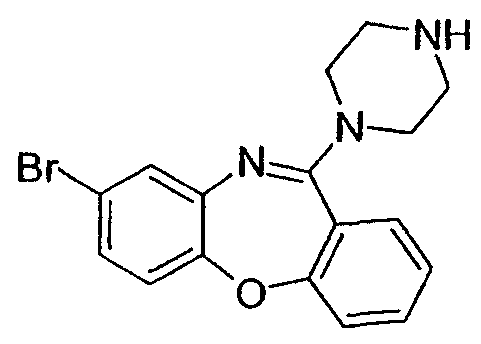
5-Бром-2-фторнитробензол (220 мг, 1 ммоль) и метил-2-гидроксибензоат (304 мг, 2 ммоль) подвергают взаимодействию согласно ОМ5 и получают 36 мг указанного в заголовке соединения (189JO48А). МС (ESI) 358 (MH+). Чистота для МН+ (УФ/МС) 96/82.
Пример 74. 11-(Пиперазин-1-ил)дибензо[b,f][1,4]оксазепин (189JO48В)

2-Фторнитробензол (141 мг, 1 ммоль) и метил-2-гидроксибензоат (304 мг, 2 ммоль) подвергают взаимодействию согласно ОМ5 и получают 5,2 мг указанного в заголовке соединения (189JO48В). МС (ESI) 280 (MH+). Чистота для МН+ (УФ/МС) 99/99.
Пример 75. 7-Хлор-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин (189JO50А)

4-Хлор-2-фторнитробензол (175 мг, 1 ммоль) и метил-2-гидроксибензоат (304 мг, 2 ммоль) подвергают взаимодействию согласно ОМ5 и получают 17 мг указанного в заголовке соединения (189JO50А). МС (ESI) 314 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 76. 8-Хлор-3-метокси-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин (189JO50В)

5-Хлор-2-фторнитробензол (175 мг, 1 ммоль) и метил-2-гидрокси-4-метоксибензоат (364 мг, 2 ммоль) подвергают взаимодействию согласно ОМ5 и получают 6,8 мг указанного в заголовке соединения (189JO50В). МС (ESI) 344 (MH+). Чистота для МН+ (УФ/МС) 94/86.
Пример 77. 8-Бром-3-метокси-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин (189JO50D)
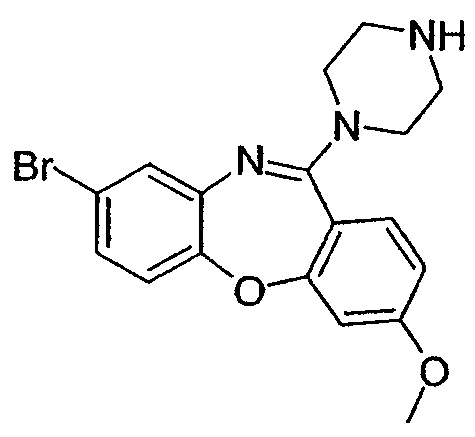
5-Бром-2-фторнитробензол (220 мг, 1 ммоль) и метил-2-гидрокси-4-метоксибензоат (364 мг, 2 ммоль) подвергают взаимодействию согласно ОМ5 и получают 14 мг указанного в заголовке соединения (189JO50D). МС (ESI) 388 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 78. 3-Метокси-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин (189JO50Е)
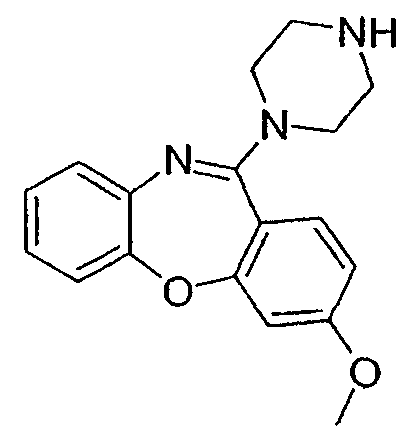
2-Фторнитробензол (141 мг, 1 ммоль) и метил-2-гидрокси-4-метоксибензоат (364 мг, 2 ммоль) подвергают взаимодействию согласно ОМ5 и получают 33 мг указанного в заголовке соединения (189JO50Е). МС (ESI) 310 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 79. 7-Хлор-3-метокси-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин (189JO50F)

4-Хлор-2-фторнитробензол (175 мг, 1 ммоль) и метил-2-гидрокси-4-метоксибензоат (364 мг, 2 ммоль) подвергают взаимодействию согласно ОМ5 и получают 6,7 мг указанного в заголовке соединения (189JO50F). МС (ESI) 344 (MH+). Чистота для МН+ (УФ/МС) 98/96.
Пример 80. 8-Хлор-4-метил-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин (189JO50Н)

5-Хлор-2-фторнитробензол (175 мг, 1 ммоль) и метил-2-гидрокси-3-метилбензоат (332 мг, 2 ммоль) подвергают взаимодействию согласно ОМ5 и получают 34 мг указанного в заголовке соединения (189JO50Н). МС (ESI) 328 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 81. 8-Бром-4-метил-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин (189JO51А)

5-Бром-2-фторнитробензол (220 мг, 1 ммоль) и метил-2-гидрокси-3-метилбензоат (332 мг, 2 ммоль) подвергают взаимодействию согласно ОМ5 и получают 20 мг указанного в заголовке соединения (189JO51А). МС (ESI) 372 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 82. 4-Метил-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин (189JO51В)

2-Фторнитробензол (141 мг, 1 ммоль) и метил-2-гидрокси-3-метилбензоат (332 мг, 2 ммоль) подвергают взаимодействию согласно ОМ5 и получают 1,8 мг указанного в заголовке соединения (189JO51В). МС (ESI) 294 (MH+). Чистота для МН+ (УФ/МС) 99/98.
Пример 83. 2-Бром-8-хлор-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин (189JO51D)
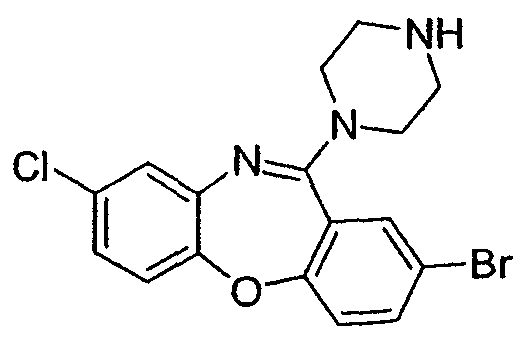
5-Хлор-2-фторнитробензол (175 мг, 1 ммоль) и метил-5-бром-2-гидроксибензоат (462 мг, 2 ммоль) подвергают взаимодействию согласно ОМ5 и получают 21 мг указанного в заголовке соединения (189JO51D). МС (ESI) 392 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 84. 2,8-Дибром-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин (189JO51Е)
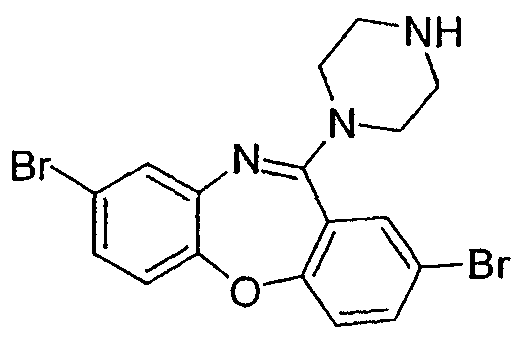
5-Бром-2-фторнитробензол (220 мг, 1 ммоль) и метил-5-бром-2-гидроксибензоат (462 мг, 2 ммоль) подвергают взаимодействию согласно ОМ5 и получают 0,7 мг указанного в заголовке соединения (189JO51Е). МС (ESI) 436 (MH+). Чистота для МН+ (УФ/МС) 94/99.
Пример 85. 2-Бром-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин (189JO51F)
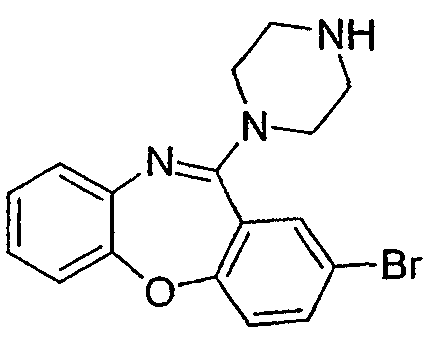
2-Фторнитробензол (142 мг, 1 ммоль) и метил-5-бром-2-гидроксибензоат (462 мг, 2 ммоль) подвергают взаимодействию согласно ОМ5 и получают 10 мг указанного в заголовке соединения (189JO51F). МС (ESI) 358 (MH+). Чистота для МН+ (УФ/МС) 95/99.
Пример 86. 2-Бром-7-хлор-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин (189JO51G)

4-Хлор-2-фторнитробензол (175 мг, 1 ммоль) и метил-5-бром-2-гидроксибензоат (462 мг, 2 ммоль) подвергают взаимодействию согласно ОМ5 и получают 17 мг указанного в заголовке соединения (189JO51G). МС (ESI) 392 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 87. 11-(Пиперазин-1-ил)-8-трифторметилдибензо[b,f][1,4]оксазепин (189JO54А)

2-Фтор-3-нитробензотрифторид (209 мг, 1 ммоль) и метил-2-гидроксибензоат (304 мг, 2 ммоль) подвергают взаимодействию согласно ОМ5 и получают 19 мг указанного в заголовке соединения (189JO54А). МС (ESI) 348 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 88. 4-Метил-11-(пиперазин-1-ил)-8-трифторметилдибензо[b,f][1,4]оксазепин (189JO54С)

2-Фтор-3-нитробензотрифторид (209 мг, 1 ммоль) и метил-2-гидрокси-3-метилбензоат (332 мг, 2 ммоль) подвергают взаимодействию согласно ОМ5 и получают 15 мг указанного в заголовке соединения (189JO54С). МС (ESI) 362 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 89. 8-Фтор-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин (189JO54Е)

2,5-Дифторнитробензол (159 мг, 1 ммоль) и метил-2-гидроксибензоат (304 мг, 2 ммоль) подвергают взаимодействию согласно ОМ5 и получают 14 мг указанного в заголовке соединения (189JO54Е). МС (ESI) 298 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 90. 8-Фтор-3-метокси-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин (189JO54F)
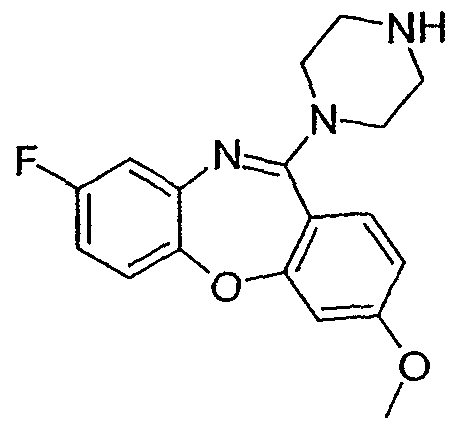
2,5-Дифторнитробензол (159 мг, 1 ммоль) и метил-2-гидрокси-4-метоксибензоат (364 мг, 2 ммоль) подвергают взаимодействию согласно ОМ5 и получают 9,8 мг указанного в заголовке соединения (189JO54F). МС (ESI) 328 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 91. 8-Фтор-4-метил-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин (189JO54G)
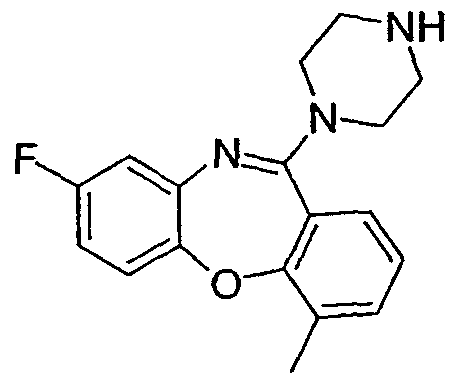
2,5-Дифторнитробензол (159 мг, 1 ммоль) и 2-гидрокси-3-метилбензоат (332 мг, 2 ммоль) подвергают взаимодействию согласно ОМ5 и получают 9,8 мг указанного в заголовке соединения (189JO54G). МС (ESI) 312 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 92. 2-Бром-8-фтор-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин (189JO54Н)

2,5-Дифторнитробензол (159 мг, 1 ммоль) и метил-5-бром-2-гидроксибензоат (462 мг, 2 ммоль) подвергают взаимодействию согласно ОМ5 и получают 11 мг указанного в заголовке соединения (189JO54Н). МС (ESI) 376 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 93. 8-Метил-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин (189JO58А)

4-Фтор-3-нитробензол (155 мг, 1 ммоль) и метил-2-гидроксибензоат (304 мг, 2 ммоль) подвергают взаимодействию согласно ОМ5 и получают 24 мг указанного в заголовке соединения (189JO58А). МС (ESI) 294 (MH+). Чистота для МН+ (УФ/МС) 100/98.
Пример 94. 3-Метокси-8-метил-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин (189JO58В)

4-Фтор-3-нитробензол (155 мг, 1 ммоль) и метил-2-гидрокси-4-метоксибензоат (364 мг, 2 ммоль) подвергают взаимодействию согласно ОМ5 и получают 27 мг указанного в заголовке соединения (189JO58В). МС (ESI) 324 (MH+). Чистота для МН+ (УФ/МС) 100/98.
Пример 95. 4,8-Диметил-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин (189JO58С)

4-Фтор-3-нитробензол (155 мг, 1 ммоль) и метил-2-гидрокси-3-метилбензоат (332 мг, 2 ммоль) подвергают взаимодействию согласно ОМ5 и получают 24 мг указанного в заголовке соединения (189JO58С). МС (ESI) 308 (MH+). Чистота для МН+ (УФ/МС) 100/98.
Пример 96. 3-Метокси-11-(пиперазин-1-ил)-8-трифторметилдибензо[b,f][1,4]оксазепин (189JO62А)

4-Фтор-3-нитробензотрифторид (209 мг, 1 ммоль) и метил-2-гидрокси-4-метоксибензоат (364 мг, 2 ммоль) подвергают взаимодействию согласно ОМ5 и получают 12 мг указанного в заголовке соединения (189JO62А). МС (ESI) 378 (MH+). Чистота для МН+ (УФ/МС) 100/95.
Пример 97. 2-Бром-11-(пиперазин-1-ил)-8-трифторметилдибензо[b,f][1,4]оксазепин (189JO62В)
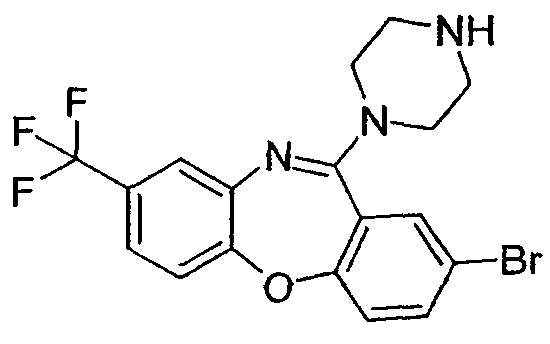
2-Фтор-3-нитробензотрифторид (209 мг, 1 ммоль) и метил-5-бром-2-гидроксибензоат (462 мг, 2 ммоль) подвергают взаимодействию согласно ОМ5 и получают 11 мг указанного в заголовке соединения (189JO62В). МС (ESI) 426 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 98. 6-Хлор-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин (189JO69)

3-Хлор-2-фторнитробензол (352 мг, 2 ммоль) и метил-2-гидроксибензоат (453 мг, 3 ммоль) подвергают взаимодействию согласно ОМ5 и получают 57 мг указанного в заголовке соединения (189JO69). МС (ESI) 314 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 99. Общая методика 6 (ОМ6)
Смесь метилового эфира аминобензойной кислоты (1,0 ммоль), 2-фторнитробензола (0,5 ммоль) и Cs2CO3 (0,33 г, 1,0 ммоль) в ДМФА (3 мл) перемешивают при 40°С в течение 2 ч. Смесь разбавляют EtOAc (10 мл) и промывают 2М водным раствором NaOH (2×5 мл), сушат (Na2SO4), концентрируют, остаток подвергают флэш-хроматографии (SiO2, система толуол:гептан:EtOAc) и концентрируют. Остаток растворяют в ТГФ (4 мл), добавляют 1М водный раствор LiOH (3 мл), полученную смесь перемешивают при 80°С в течение 1 часа и затем оставляют при комнатной температуре. Добавляют 2М хлористоводородную кислоту до тех пор, пока рН не достигнет 2. Водную фазу экстрагируют EtOAc (3×). Объединенные органические фазы сушат (Na2SO4) и концентрируют. Остаток растворяют в EtOH, добавляют смесь К2СО3 (0,359 г, 2,55 ммоль) и Na2S2O4 (0,44 г, 2,5 ммоль) в воде и полученную смесь перемешивают в течение 1 часа. Смесь разбавляют водой, промывают 1М водным раствором NaOH (2×5 мл) и затем сушат (Na2SO4) и концентрируют.
Остаток растворяют в CH3CN и добавляют гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида (143 мг, 0,75 ммоль), гидрат гидроксибензотриазола (160 мг, 0,75 ммоль), триэтиламин (311 мкл, 2,25 ммоль) и N,N-диметиламинопиридин (каталитическое количество). Полученную смесь нагревают в закрытой пробирке с использованием микроволновой печи (140°С, 10 мин). Смесь разбавляют EtOAc, промывают насыщенным водным раствором NaHCO3, сушат (Na2SO4) и концентрируют. Остаток растворяют в диоксане и при 50°С добавляют к смеси TiCl4 (0,55 мл, 0,55 ммоль, 1М раствор в толуоле) и пиперазина (0,22 г, 2,5 ммоль) в диоксане. Полученную смесь перемешивают при 100°С в течение ночи и затем оставляют при комнатной температуре. К смеси добавляют хлористоводородную кислоту (3 мл, 2М) и затем водную фазу экстрагируют EtOAc (2×4 мл). К водной фазе добавляют водный раствор NaOH (6 мл, 2М) и полученную суспензию экстрагируют EtOAc (3×3 мл). Объединенные органические фазы концентрируют и остаток очищают ВЭЖХ.
Пример 100. 8-Бром-8-метил-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин (189JO63А)

4-Фтор-3-нитротолуол (78 мг, 0,5 ммоль) и метил-5-бром-2-гидроксибензоат (231 мг, 1 ммоль) подвергают взаимодействию согласно ОМ6 и получают 13 мг указанного в заголовке соединения (189JO63А). МС (ESI) 372 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 101. 7-Хлор-4-метил-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин (189JO63В)
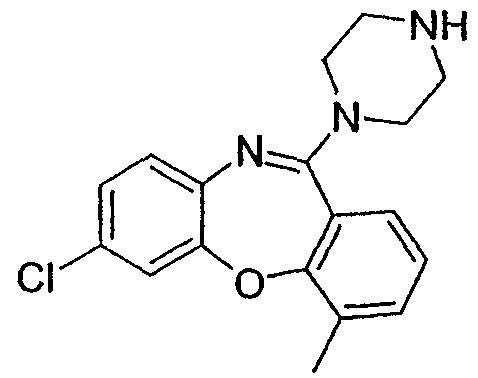
4-Хлор-2-фторнитробензол (88 мг, 0,5 ммоль) и метил-2-гидрокси-3-метилбензоат (166 мг, 1 ммоль) подвергают взаимодействию согласно ОМ6 и получают 24 мг указанного в заголовке соединения (189JO63В). МС (ESI) 328 (MH+). Чистота для МН+ (УФ/МС) 100/100.
Пример 102. 8-Фенил-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин (189JO64)
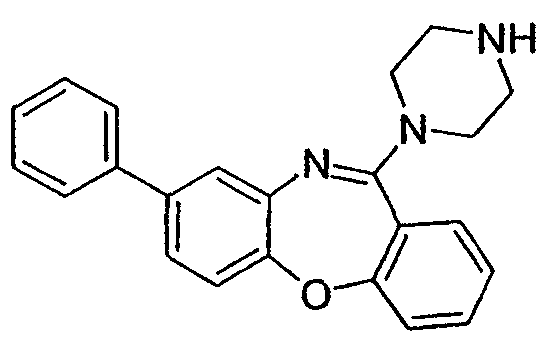
К смеси 8-бром-10Н-дибензо[b,f][1,4]оксазепин-11-она (189JO56) (30 мг, 0,12 ммоль), бензолбороновой кислоты (18 мг, 0,15 ммоль) и К2СО3 (34 мг, 0,24 ммоль) в обескислороженной смеси толуол/EtOH/H2O (1,5 мл) добавляют тетракис(трифенилфосфин)палладий(0) (каталитическое количество) и полученную смесь нагревают в закрытой пробирке с использованием микроволновой печи (140°С, 15 мин). Смесь разбавляют EtOAc, промывают насыщенным водным раствором NaHCO3, сушат (Na2SO4), концентрируют и получают неочищенный 8-фениллактам. Смесь промежуточного 8-фениллактама и диоксана (1 мл) при 50°С добавляют к смеси TiCl4 (0,27 мл, 0,27 ммоль, 1М раствор в толуоле) и пиперазина (0,103 г, 1,2 ммоль) в диоксане. Полученную смесь перемешивают при 100°С в течение ночи и затем оставляют при комнатной температуре. К смеси добавляют хлористоводородную кислоту (3 мл, 2М) и затем водную фазу экстрагируют EtOAc (2×4 мл). К водной фазе добавляют водный раствор NaOH (6 мл, 2М) и полученную суспензию экстрагируют EtOAc (3×3 мл). Объединенные органические фазы вносят в колонку с ионообменной смолой SCX-2. Колонку промывают МеОН, затем продукт реакции элюируют NH3 (7н. раствор в МеОН), раствор концентрируют, остаток очищают ВЭЖХ и получают 16 мг указанного в заголовке соединения (189JO64). МС (ESI) 356 (MH+). Чистота для МН+ (УФ/МС) 100/99.
Пример 103. 8-Хлор-11-(пиперидин-4-ил)-5Н-дибензо[b,е][1,4]диазепин (160FE67А)
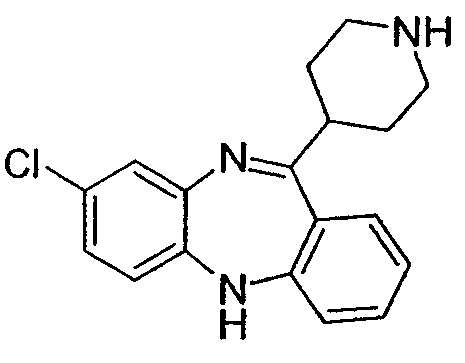
К раствору 8,5-дихлор-5Н-дибензо[b,е][1,4]диазепина (160FE64) (106 мг, 0,4 ммоль) и PdCl2(PPh3)2 (18 мг, 0,04 ммоль) в сухом ТГФ (2 мл) при 50°С добавляют 4-CBZ-пиперидилцинкиодид (полученный из 4-CBZ-пиперидилиодида (345 мг, 1,0 ммоль) с использованием металлического цинка и дибромэтана) (0,8 ммоль). Реакционную смесь встряхивают в течение 16 ч и затем реакцию гасят, добавляя водный насыщенный раствор NH4Cl. Полученную смесь дважды экстрагируют эфиром, объединенные эфирные фазы промывают рассолом и сушат (Na2SO4). Фильтрование с последующим концентрированием органической фазы при пониженном давлении дают неочищенный продукт реакции. К неочищенному продукту, растворенному в CH2Cl2 (1 мл), при -30°С добавляют BBr3 (100 мкл). Затем температуру реакционной смеси постепенно поднимают до 0°С. ТСХ показывает полное превращение исходного вещества, и к реакционной смеси последовательно добавляют Et3N, H2O и EtOAc. Органическую фазу промывают рассолом и сушат (Na2SO4). Фильтрование с последующим концентрированием при пониженном давлении дают неочищенный продукт реакции, который очищают ВЭЖХ и получают 2,3 мг указанного в заголовке соединения (160FE67А). МС (ESI) 312 (MH+). Чистота для МН+ (УФ/МС) 99/96.
Пример 104. 5-Бензил-8-хлор-11-(пиперидин-4-ил)-5Н-дибензо[b,е][1,4]диазепин (160FE67В)
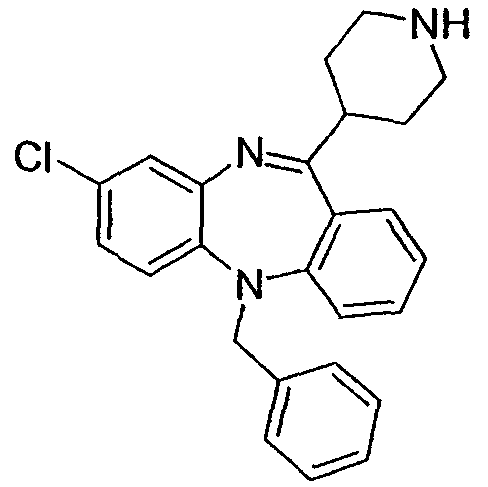
Названное в заголовке соединение (4,4 мг) выделяют как побочный продукт синтеза в примере 102. МС (ESI) 402 (MH+). Чистота для МН+ (УФ/МС) 85/87.
Пример 105. Общая методика 7 (ОМ7)
Смесь 2-аминобензойной кислоты (1 экв.), 2-фторнитробензола (2 экв. или 3 экв.) и К2СО3 (3 экв.) в ДМФА нагревают при 100°С в течение 2 часов и затем оставляют при комнатной температуре. Органическую фазу экстрагируют 0,1М водным раствором NaOH (3×). Объединенные водные фазы подкисляют 4М хлористоводородной кислотой и экстрагируют EtOAc (3×). Объединенные органические фазы сушат (Na2SO4) и концентрируют. Остаток растворяют в EtOH, добавляют раствор К2СО3 (5 экв.) и Na2S2O4 (5 экв.) в воде и полученную смесь перемешивают в течение 1 часа. Смесь концентрируют и остаток растворяют в EtOAc. Смесь подкисляют хлористоводородной кислотой (2М), затем водную фазу экстрагируют EtOAc (3×) и объединенные органические фазы концентрируют.
Остаток растворяют в ксилоле и полученную смесь перемешивают при 130°С в течение ночи. Смесь разбавляют EtOAc, промывают насыщенным водным раствором NaHCO3, сушат (Na2SO4), концентрируют и остаток подвергают флэш-хроматографии (SiO2, система гептан:EtOAc).
Пример 106. 8-Бром-5,10-дигидродибензо[b,е][1,4]диазепин-11-он (166JO31)
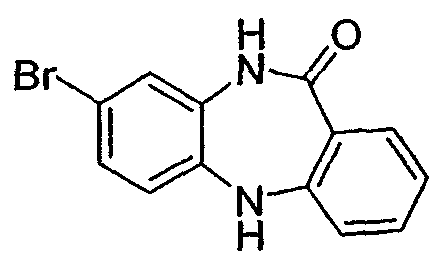
5-Бром-2-фторнитробензол (1,6 г, 7,4 ммоль) и 2-аминобензойную кислоту (0,50 г, 3,6 ммоль) подвергают взаимодействию согласно ОМ7 и получают 331 мг указанного в заголовке соединения (166JO31). МС (ESI) 289 (MH+). Чистота для МН+ (УФ) 93%.
Пример 107. 5,10-Дигидродибензо[b,е][1,4]диазепин-11-он (160FE15А)
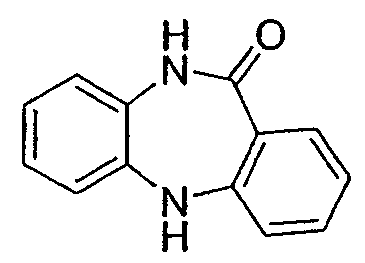
2-Фторнитробензол (847 мг, 6 ммоль) и 2-аминобензойную кислоту (274 мг, 2,0 ммоль) подвергают взаимодействию согласно ОМ7 и получают 130 мг указанного в заголовке соединения (160FE15А).
Пример 108. 8-Фтор-5,10-дигидродибензо[b,е][1,4]диазепин-11-он (160FE15С)
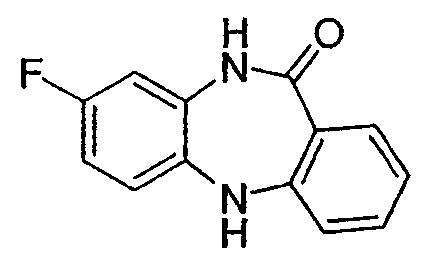
2,4-Дифторнитробензол (0,96 г, 6 ммоль) и 2-аминобензойную кислоту (274 мг, 2,0 ммоль) подвергают взаимодействию согласно ОМ7 и получают 100 мг указанного в заголовке соединения (160FE15С).
Пример 109. 8,5-Дихлор-5Н-дибензо[b,е][1,4]диазепин (160FE64)
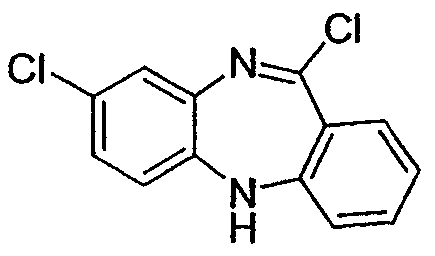
К смеси 8-хлор-5,10-дигидродибензо[b,е][1,4]диазепин-11-она (2,45 г, 10 ммоль) и сухого толуола (20 мл) добавляют N,N-диметиланилин (5,1 мл, 40 ммоль) и оксихлорид фосфора (2,8 мл, 30 ммоль). Смесь встряхивают при 95°С в течение 2 ч. Затем температуру снижают и избыток N,N-диметиланилина и оксихлорида фосфора удаляют при пониженном давлении с использованием масляного насоса. Оставшееся масло растворяют в диоксане (20 мл) и добавляют водный раствор Na2CO3 (10 мл, 2М). Двухфазную смесь встряхивают при 80°С в течение 30 мин. Затем температуру снижают и к реакционной смеси добавляют эфир. Эфирную фазу промывают насыщенным водным раствором NaCl, сушат (Na2SO4) и, наконец, концентрируют при пониженном давлении. Полученное масло кристаллизуется при стоянии при комнатной температуре. Перекристаллизация (гептан-эфир) дает 1,8 г (69%) указанного в заголовке соединения (160FE64).
1H ЯМР (CDCl3) δ 7,61 (дд, 1H, J=1,4, 7,8 Гц), 7,31 (дт, 1H, J=1,5, 8,0 Гц), 7,15 (д, 1H, J=2,5 Гц), 7,02 (м, 2H), 6,66 (дд, 1H, J=1,0, 7,8 Гц), 6,58 (д, 1H, J=8,4 Гц), 4,94 (уш.с, 1H). 13C ЯМР (CDCl3) δ 157,2, 152,4, 140,3, 138,9, 134,0, 131,9, 129,7, 128,5, 128,0, 127,0, 123,5, 121,0, 119,8.
Пример 110. 8-Хлор-11-метилсульфанил-5Н-дибензо[b,е][1,4]диазепин (166JO50)
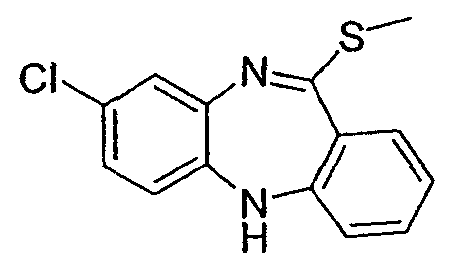
Смесь 8-хлор-5,10-дигидродибензо[b,е][1,4]диазепин-11-она (500 мг, 2,05 ммоль) и 2,4-бис(4-метоксифенил)-1,3-дитиа-2,4-дифосфетан-2,4-дисульфида (480 мг, 1,19 ммоль) в толуоле (4 мл) нагревают в закрытой пробирке в микроволновой печи (120°С, 30 минут). Смесь хроматографируют (SiO2, гептан:EtOAc, 2:1) и получают 599 мг промежуточного тиолактама. К смеси промежуточного тиолактама и ТГФ (10 мл) добавляют MeI (633 мкл, 10,3 ммоль) и полученную смесь кипятят с обратным холодильником в течение 4 ч. Смесь концентрируют и получают 610 мг неочищенного указанного в заголовке соединения (166JO50) (чистота 59%).
Пример 111. N,N-Диэтил(2-бромбензил)амид (189JO10)

К смеси 2-бромбензоилхлорида (3,5 г, 16 ммоль) и CH2Cl2 (50 мл) при 0°С добавляют по каплям диэтиламин (3,2 мл, 32 ммоль) и полученную смесь оставляют при комнатной температуре. Через 30 минут добавляют воду, смесь разбавляют CH2Cl2, промывают насыщенным водным раствором NaHCO3 и насыщенным водным раствором NH4Cl, сушат (Na2SO4), концентрируют и получают 3,9 г (95%) указанного в заголовке соединения (189JO10).
1H ЯМР (CDCl3) δ 7,54 (м, 1H), 7,32 (м, 1H), 7,22 (м, 2H), 3,79 (м, 1H), 3,33 (м, 1H), 3,13 (м, 2H), 1,26 (т, 3H, J=7,2 Гц), 1,05 (т, 3H, J=7,0 Гц). 13C ЯМР (CDC13) δ 168,5, 139,0, 132,8, 130,0, 127,61, 127,59, 119,3, 42,8, 39,0, 14,0, 12,6.
Пример 112. 2-[(4-Хлор-2-метилфенил)(4-метоксибензил)амино]-N,N-диэтилбензамид (189JO26)

К смеси N,N-диэтил(2-бромбензил)амида (189JO10) (1,41 г, 5,50 ммоль) и 4-хлор-2-метиланилина (1,01 г, 7,15 ммоль) в обескислороженном толуоле (14 мл) добавляют NaO-трет-Bu (0,74 г, 7,7 ммоль), рац-BINAP (110 мг, 0,17 ммоль) и Pd(OAc)2 (18 мг, 0,08 ммоль) и полученную смесь перемешивают в атмосфере Ar в течение 14 ч при 80°С. Смесь фильтруют через целит, концентрируют и остаток подвергают флэш-хроматографии (SiO2, гептан:EtOAc, 10:1-4:1), что дает промежуточный кетон без защитной группы (1,50 г), содержащий примерно 15% примесей.
Смесь, содержащую промежуточное соединение, растворяют в ДМФА (20 мл). Добавляют п-метоксибензилхлорид (0,90 мл, 6,6 ммоль) и затем по частям добавляют NaH (0,23 г, 5,6 ммоль, 60% в минеральном масле). Полученную смесь перемешивают при комнатной температуре в течение 1 часа и затем реакцию гасят, добавляя насыщенный водный раствор NaHCO3. Смесь разбавляют EtOAc, промывают насыщенным водным раствором NaHCO3, сушат (Na2SO4), концентрируют, остаток подвергают флэш-хроматографии (SiO2, толуол:EtOAc, 10:1) и получают 1,66 г (68%) указанного в заголовке соединения (189JO26).
1H ЯМР (CDCl3) δ 7,35 (м, 2H), 7,20 (м, 1H), 7,09-6,99 (м, 4H), 6,91 (м, 2H), 6,80(м, 2H), 4,84-4,54 (Abq, 2H, J=16,2 Гц), 3,74 (с, 3H), 3,18 (т, 2Н), 3,03 (м, 1H), 2,48 (м, 1H), 2,17 (с, 3H), 1,01 (т, 3H, J=7,2 Гц), 0,97 (т, 3H, J=7,0 Гц). 13C ЯМР (CDCl3) δ 169,6, 158,7, 146,53, 146,51, 137,0, 131,3, 130,9, 130,4, 129,6, 129,3, 128,7, 127,8, 127,4, 126,3, 122,8, 121,4, 114,0, 57,1, 55,3, 43,3, 39,0, 19,1, 13,9, 12,9. MC (ESI) 437 (MH+).
Пример 113. 2-Хлор-5-(4-метоксибензил)-5,11-дигидродибензо[b,f]азепин-11-он (189JO27)

К смеси диизопропиламина (1,09 мл, 7,8 ммоль) и N,N,N,N-тетраметилендиамина (1,17 мл, 7,8 ммоль) в сухом ТГФ (19 мл) при -20°С добавляют н-BuLi (5,54 мл, 1,4М раствор в гексане) и полученную смесь перемешивают при -20°С в течение 5 минут. Затем добавляют смесь 2-[(4-хлор-2-метилфенил)(4-метоксибензил)амино]-N,N-диэтилбензамида (189JO26) (1,36 г, 3,1 ммоль) и сухого ТГФ (38 мл) и полученную смесь перемешивают при -20°С в течение 4 ч. Реакцию гасят, добавляя насыщенный водный раствор NH4Cl. Смесь разбавляют EtOAc, промывают водой, сушат (Na2SO4), концентрируют, остаток подвергают флэш-хроматографии (SiO2, толуол:гептан, 7:1-1:0) и получают 665 мг (59%) указанного в заголовке соединения (189JO27).
1H ЯМР (CDCl3) δ 8,15 (дд, 1H, J=1,8, 8,0 Гц), 7,43 (м, 1H), 7,24 (м, 4H), 7,17 (д, 1H, J=8,6 Гц), 7,12 (дд, 1H, J=2,4, 8,6 Гц), 7,00 (дт, 1H, J=0,8, 7,0 Гц), 6,81 (м, 2H), 5,09 (с, 2H), 4,00 (с, 2H), 3,75 (с, 3H). 13C ЯМР (CDC13) δ 190,3, 159,1, 149,5, 146,2, 134,1, 132,4, 131,3, 131,1, 129,1, 129,0, 128,6, 127,3, 126,4, 123,4, 121,0, 118,5, 114,2, 55,5, 19,3. MC (ESI) 364 (MH+).
Пример 114. Метиловый эфир 2-(4-хлор-2-нитрофенилсульфанил)бензойной кислоты (189JO09)
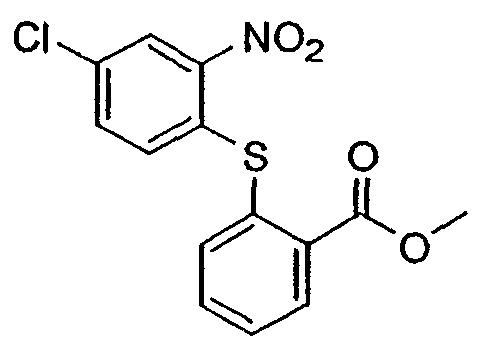
К смеси 5-хлор-2-нитрофторбензола (176 мг, 1 ммоль) и метилтиосалицилата (275 мкл, 2 ммоль) в ДМФА (5 мл) добавляют Cs2CO3 (652 мг, 2 ммоль) и полученную смесь перемешивают при комнатной температуре в течение 2 ч. Смесь разбавляют CH2Cl2, промывают водой, сушат (Na2SO4), концентрируют, остаток подвергают флэш-хроматографии (SiO2, гептан:толуол, 1:10-1:4) и получают 300 мг (92%) указанного в заголовке соединения (189JO09).
1H ЯМР (CDCl3) δ 8,15 (д, 1H, J=2,4 Гц), 7,94 (м, 1H), 7,53-7,46 (м, 3H), 7,34 (дд, 1H, 2,4, 8,6 Гц), 6,95 (д, 1H, J=8,8 Гц), 3,82 (с, 3H).
Пример 115. Метиловый эфир 2-(2-амино-4-хлорфенилсульфанил)бензойной кислоты (189JO11)
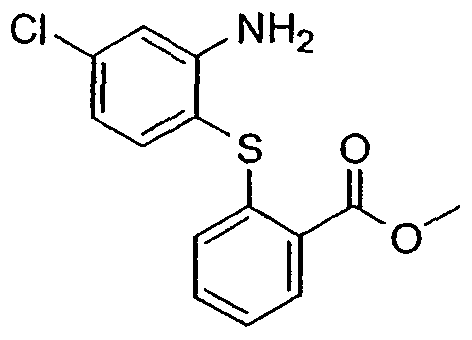
К смеси метилового эфира 2-(4-хлор-2-нитрофенилсульфанил)бензойной кислоты (189JO09) (232 мг, 0,72 ммоль) и EtOH (5 мл) добавляют SnCl2·2H2O (812 мг, 3,6 ммоль), полученную смесь перемешивают при 80°С в течение 2 ч и затем концентрируют. Остаток обрабатывают льдом и затем добавляют Na2CO3 до тех пор, пока рН не достигнет 10. Добавляют EtOAc и взвесь фильтруют через целит. Фазу EtOAc промывают водой и рассолом, сушат (Na2SO4), концентрируют и получают 149 мг (70%) указанного в заголовке соединения (189JO11).
1H ЯМР (CDCl3) δ 8,02 (дд, 1H, J=1,6, 7,8 Гц), 7,39 (д, 1H, J=8,2 Гц), 7,29 (м, 1H), 7,15 (дт, 1H, J=1,2, 7,8 Гц), 6,87 (д, 1H, J=2,2 Гц), 6,80 (дд, 1H, J=2,2, 8,2 Гц), 6,76 (дд, 1H, J=1,2, 8,0 Гц), 3,96 (с, 3H).
Пример 116. 8-Хлор-10Н-дибензо[b,f][1,4]тиазепин-11-он (189JO13)
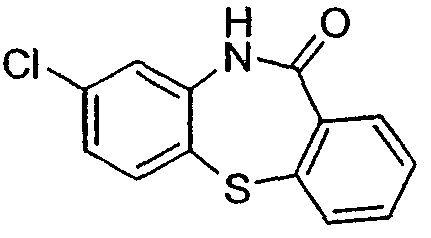
Смесь метилового эфира 2-(2-амино-4-хлорфенилсульфанил)бензойной кислоты (189JO11) (149 мг, 0,51 ммоль) и AlMe3 (355 мкл, 0,71 ммоль, 2М раствор в толуоле) в CH2Cl2 (3 мл) перемешивают при температуре окружающей среды в течение шести суток и затем осторожно добавляют воду. Смесь разбавляют CH2Cl2 и подкисляют 2М хлористоводородной кислотой. Органическую фазу отделяют, сушат (Na2SO4), концентрируют, остаток подвергают флэш-хроматографии (гептан:EtOAc, 5:1-3:1) и получают 38 мг (29%) указанного в заголовке соединения (189JO13). МС (ESI) 262 (MH)+.
Пример 117. Метиловый эфир 2-(хлор-2-нитрофенокси)бензойной кислоты (189JO29А)

К смеси 5-хлор-2-нитрофторбензола (352 мг, 2 ммоль) и метил-2-гидроксибензоата (0,52 мл, 4 ммоль) в ДМФА (6 мл) добавляют Cs2CO3 (1,30 г, 4 ммоль) и полученную смесь перемешивают при комнатной температуре в течение 2 ч. Смесь разбавляют CH2Cl2, промывают водой, сушат (Na2SO4), концентрируют, остаток подвергают флэш-хроматографии (SiO2, гептан:EtOAc, 10:1-4:1) и получают 505 мг (82%) указанного в заголовке соединения (189JO29А).
1H ЯМР (CDCl3) δ 8,02 (дд, 1H, J=1,8, 7,8 Гц), 7,96 (д, 1H, J=1,9 Гц), 7,59 (дт, 1H, J=2,0, 7,6 Гц), 7,39 (дд, 1H, J=2,5, 9,0 Гц), 7,24 (дт, 1H, J=1,2, 7,6 Гц), 7,13 (дд, 1H, J=1,2, 8,0 Гц), 6,74 (д, 1H, J=9,0 Гц), 3,77 (с, 3H).
Пример 118. 8-Хлор-10Н-дибензо[b,f][1,4]оксазепин-11-он (189JO29С)
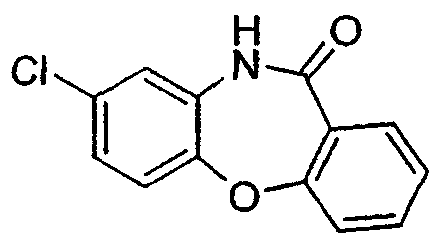
К раствору метилового эфира 2-(хлор-2-нитрофенокси)бензойной кислоты (189JO29А) (505 мг, 1,64 ммоль) в EtOAc (20 мл) добавляют Pd (каталитическое количество, 5% на угле), полученную смесь гидрируют (Н2, 1 атм) в течение 48 ч, затем фильтруют через целит и концентрируют. Остаток растворяют в толуоле (6 мл) и добавляют NaH (160 мг, 4,0 ммоль, 60% в минеральном масле). Полученную смесь перемешивают при 80°С в течение ночи и затем реакцию гасят, добавляя насыщенный водный раствор NH4Cl. Полученную смесь разбавляют EtOAc, промывают водой, сушат (Na2SO4), концентрируют, остаток подвергают флэш-хроматографии (SiO2, толуол:EtOAc, 4:1) и получают 171 мг (42%) указанного в заголовке соединения (189JO29С).
1H ЯМР (CDCl3) δ 8,12 (уш.с, 1H), 7,95 (дд, 1H, J=1,8, 8,0 Гц), 7,54 (дт, 1H, J=1,8, 8,0 Гц), 7,29-7,19 (м, 3H), 7,08 (дд, 1H, J=2,3, 8,6 Гц), 7,04 (д, 1H, J=2,3 Гц). MC (ESI) 246 (MH+).
Пример 119. 3-Хлор-5,11-дигидродибензо[b,е]азепин-6-он (189JO59)

К смеси 5-хлор-2-метилфенилизоцианата (100 мкл, 0,73 ммоль) и CCl4 (2 мл) добавляют сульфурилхлорид (118 мкл, 0,88 ммоль) и 2,2'-азобис(изобутиронитрил) (каталитическое количество) и полученную смесь кипятят с обратным холодильником в течение 20 ч. Смесь оставляют при комнатной температуре, затем разбавляют CH2Cl2, промывают насыщенным водным раствором NaHCO3, сушат (Na2SO4) и концентрируют. Смесь растворяют в бензоле (2 мл) и добавляют смесь AlCl3 (160 мг, 1,2 ммоль) и бензола (1 мл). Полученную смесь перемешивают при 80°С в течение 4 ч и затем оставляют при комнатной температуре. Смесь фильтруют через короткую колонку (SiO2, гептан:EtOAc, 1:1) и получают 25 мг (14%) указанного в заголовке соединения (189JO59).
1H ЯМР (CDCl3) δ 8,18 (уш.с, 1H), 7,92 (дд, 1H, J=1,2, 7,8 Гц), 7,46 (дт, 1H, J=1,4, 7,4 Гц), 7,34 (дт, 1H, J=1,2, 7,4 Гц), 7,23 (м, 2H), 7,07 (м, 2H), 3,92 (с, 2H). MC (ESI) 244 (MH+).
Пример 120. 8-Бром-10Н-дибензо[b,f][1,4]оксазепин-11-он (189JO56)
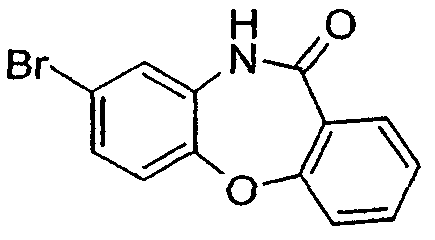
Смесь метил-2-гидроксибензоата (1,0 мл, 10,0 ммоль), 5-бром-2-фторнитробензола (0,62 мл, 5,0 ммоль) и Cs2CO3 (3,3 г, 10,0 ммоль) в ДМФА (12 мл) перемешивают при 40°С в течение 2 ч. Смесь разбавляют EtOAc и промывают 1М водным раствором NaOH. К фазе EtOAc добавляют EtOH, H2O, K2CO3 (2,8 г, 20 ммоль) и Na2S2O4 (3,5 г, 20 ммоль) и полученную смесь энергично перемешивают в течение 1 часа. Водную фазу удаляют, органическую фазу промывают 1М водным раствором NaOH и затем концентрируют. Остаток растворяют в ДМФА (1 мл), затем добавляют толуол (4 мл) и NaH (60 мг, 1,5 ммоль, 60% в минеральном масле), полученную смесь перемешивают при 80°С в течение ночи и затем реакцию гасят, добавляя насыщенный водный раствор NH4Cl. Полученную смесь разбавляют EtOAc, промывают 2М водным раствором NaOH, сушат (Na2SO4), концентрируют, фильтруют через короткую колонку с SiO2, концентрируют, остаток кристаллизуют из смеси гептан:EtOAc и получают 130 мг указанного в заголовке соединения (189JO56). МС (ESI) 290 (MH)+. Чистота для МН+ (УФ/МС) 100/100.
Пример 121. Общая методика 8 (ОМ8)
К 8-хлор-11-метилсульфанил-5Н-дибензо[b,е][1,4]диазепину (166JO50) (чистота 50%, 1 экв.) в пиридине добавляют диамин с защитной ВОС-группой (1,8 экв.). Полученную смесь нагревают в закрытой пробирке при 110°С в течение 66 ч. Смесь концентрируют и затем разбавляют смесью CH2Cl2:трифторуксусная кислота (соотношение 2:1). Полученную смесь перемешивают при температуре окружающей среды в течение ночи и затем концентрируют. Остаток растворяют в CH2Cl2 и промывают насыщенным водным раствором NaHCO3. Органическую фазу вносят в колонку с ионообменной смолой SCX-2. Колонку промывают МеОН, затем продукт реакции элюируют NH3 (7н. раствор в МеОН), концентрируют и очищают ВЭЖХ.
Пример 122. (8-Хлор-5Н-дибензо[b,е][1,4]диазепин-11-ил)-(S)-1-пирролидин-2-илметиламин (166JO51)
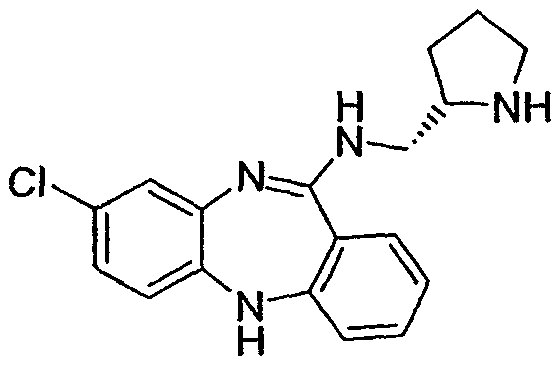
8-Хлор-11-метилсульфанил-5Н-дибензо[b,е][1,4]диазепин (166JO50) (50 мг, 0,11 ммоль) и (S)-(2-аминометил)-1-N-(трет-бутоксикарбониламино)пирролидин (39 мг, 0,2 ммоль) подвергают взаимодействию согласно ОМ8 и получают 3,0 мг указанного в заголовке соединения (166JO51). МС (ESI) 327 (MH)+. Чистота для МН+ (УФ/МС) 100/92.
Пример 123. 1-(8-Хлор-5Н-дибензо[b,е][1,4]диазепин-11-ил)пиперидин-4-иламин (166JO55)

8-Хлор-11-метилсульфанил-5Н-дибензо[b,е][1,4]диазепин (166JO50) (50 мг, 0,11 ммоль) и 4-(трет-бутоксикарбониламино)аминопиперидин (39 мг, 0,2 ммоль) подвергают взаимодействию согласно ОМ8 и получают 6,5 мг указанного в заголовке соединения (166JO55). МС (ESI) 327 (MH)+. Чистота для МН+ (УФ/МС) 100/99.
Пример 124. 1-(8-Хлор-5Н-дибензо[b,е][1,4]диазепин-11-ил)пирролидин-3-иламин (166JO64)
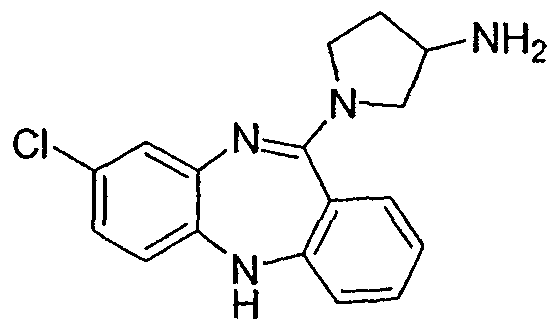
8-Хлор-11-метилсульфанил-5Н-дибензо[b,е][1,4]диазепин (166JO50) (100 мг, 0,22 ммоль) и 3-(трет-бутоксикарбониламино)пирролидин (73 мг, 0,4 ммоль) подвергают взаимодействию согласно ОМ8 и получают 8,1 мг указанного в заголовке соединения (166JO64). МС (ESI) 313 (MH)+. Чистота для МН+ (УФ/МС) 100/94.
Пример 125. (8-Хлор-5Н-дибензо[b,е][1,4]диазепин-11-ил)-(R)-1-пирролидин-2-илметиламин (166JO70)
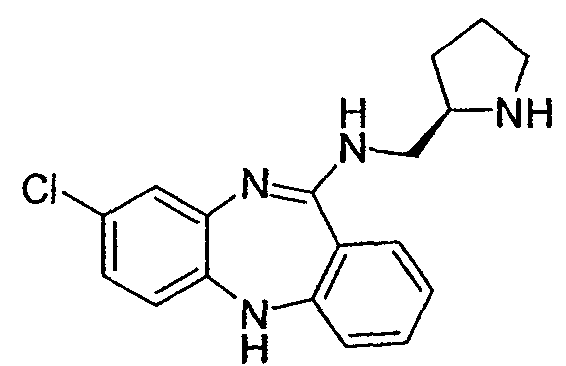
8-Хлор-11-метилсульфанил-5Н-дибензо[b,е][1,4]диазепин (166JO50) (100 мг, 0,22 ммоль) и (R)-(2-аминометил)-1-N-(трет-бутоксикарбониламино)пирролидин (78 мг, 0,4 ммоль) подвергают взаимодействию согласно ОМ8 и получают 7,6 мг указанного в заголовке соединения (166JO70). МС (ESI) 327 (MH)+. Чистота для МН+ (УФ/МС) 100/90.
Пример 126. (8-Хлор-5Н-дибензо[b,е][1,4]диазепин-11-ил)пирролидин-3-иламин (166JO74)
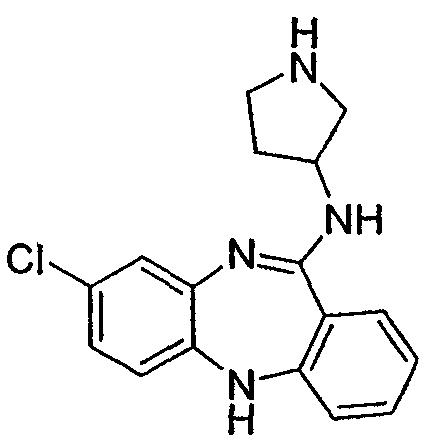
8-Хлор-11-метилсульфанил-5Н-дибензо[b,е][1,4]диазепин (166JO50) (100 мг, 0,22 ммоль) и 3-амино-1-N-(трет-бутоксикарбониламино)пирролидин (73 мг, 0,4 ммоль) подвергают взаимодействию согласно ОМ8 и получают 7,7 мг указанного в заголовке соединения (166JO74). МС (ESI) 313 (MH)+. Чистота для МН+ (УФ/МС) 100/90.
Пример 127. 8-Хлор-11-(2,5-диазабицикло[2,2,1]гепт-2-ил)-5Н-дибензо[b,е][1,4]диазепин (166JO39-2)

8-Хлор-11-метилсульфанил-5Н-дибензо[b,е][1,4]диазепин (166JO50) (50 мг, 0,11 ммоль) и N-(трет-бутоксикарбониламино)-2,5-диазабицикло[2,2,1]гептан (34 мг, 0,2 ммоль) подвергают взаимодействию согласно ОМ8 и получают 15 мг указанного в заголовке соединения (166JO39-2). МС (ESI) 324 (MH)+. Чистота для МН+ (УФ/МС) 93/100.
Пример 128. Ацетидин-3-ил-(8-хлор-5Н-дибензо[b,е][1,4]диазепин-11-ил)амин (166JO65)

К 8,5-дихлор-5Н-дибензо[b,е][1,4]диазепину (160FE64) (30 мг, 0,11 ммоль) в диоксане добавляют трет-бутиловый эфир 3-аминоазетидин-1-карбоновой кислоты (59 мг, 0,34 ммоль) и Cs2CO3 (74 мг, 0,23 ммоль) и полученную смесь нагревают в закрытой пробирке с использованием микроволновой печи (170°С, 40 минут). Смесь разбавляют EtOAc, промывают водой, сушат (Na2SO4) и концентрируют. Остаток растворяют в CH2Cl2 (2 мл) и добавляют трифторуксусную кислоту (1 мл). Полученную смесь перемешивают при температуре окружающей среды в течение ночи и затем концентрируют. Остаток растворяют в CH2Cl2 и промывают насыщенным водным раствором NaHCO3. Органическую фазу вносят в колонку с ионообменной смолой SCX-2. Колонку промывают МеОН, затем продукт реакции элюируют NH3 (7н. раствор в МеОН), концентрируют, очищают ВЭЖХ и получают 16 мг указанного в заголовке соединения (166JO65). МС (ESI) 299 (MH)+. Чистота для МН+ (УФ/МС) 97/90.
Пример 129. Общая методика 9 (ОМ9)
Смесь 3-аминометилового эфира (1 экв.), 5-бром-2-фторнитробензола (1 экв.) и К2СО3 (4 экв.) в ДМФА нагревают при 60°С в течение 1 часа и затем оставляют при комнатной температуре. Смесь разбавляют CH2Cl2 и промывают насыщенным водным раствором NH4Cl, сушат (Na2SO4) и концентрируют. Остаток растворяют в EtOH, добавляют смесь К2СО3 (5 экв.) и Na2S2O4 (5 экв.) в воде и полученную смесь энергично перемешивают в течение 1 часа. Водную фазу экстрагируют EtOAc (3×), объединенные органические фазы сушат (Na2SO4) и концентрируют.
Остаток растворяют в CH3CN, добавляют H2SO4 (10 об.%, 98%) и полученную смесь перемешивают при 80°С в течение 1 часа. Смесь разбавляют CH2Cl2, промывают насыщенным водным раствором NaHCO3, сушат (Na2SO4), концентрируют, остаток подвергают флэш-хроматографии (SiO2, система гептан:EtOAc), концентрируют и получают промежуточный лактам.
Остаток растворяют в диоксане и при 50°С добавляют к смеси TiCl4 (1,1 экв., 1М раствор в толуоле) и пиперазина (5 экв.) в диоксане. Полученную смесь перемешивают при 100°С в течение ночи и затем оставляют при комнатной температуре. К смеси добавляют хлористоводородную кислоту (2М) до тех пор, пока раствор не станет кислым, и затем водную фазу экстрагируют EtOAc (2×). К водной фазе добавляют водный раствор NaOH (2М) до тех пор, пока раствор не станет щелочным, и полученную суспензию экстрагируют EtOAc (3×). Объединенные органические фазы концентрируют и остаток подвергают флэш-хроматографии система (SiO2, CH2Cl2:MeOH, NH3 (7н. раствор в МеОН)).
Пример 130. 7-Бром-4-(пиперазин-1-ил)-2,3-дигидро-1Н-бензо[b][1,4]диазепин (166JO47)

5-Бром-2-фторнитробензол (440 мг, 2,0 ммоль) и гидрохлорид метил-3-аминопропионата (920 мг, 3,0 ммоль) подвергают взаимодействию согласно ОМ9 и получают 4,0 мг указанного в заголовке соединения (166JO47). МС (ESI) 309 (MH)+. Чистота для МН+ (УФ/МС) 100/100.
Пример 131. 7-Бром-2-метил(пиперазин-1-ил)-2,3-дигидро-1Н-бензо[b][1,4]диазепин (166JO95)

5-Бром-2-фторнитробензол (440 мг, 2,0 ммоль) и метил-3-аминобутират (787 мг, 3,0 ммоль) подвергают взаимодействию согласно ОМ9 и получают 12 мг указанного в заголовке соединения (166JO95). МС (ESI) 323 (MH)+. Чистота для МН+ (УФ/МС) 100/100.
Пример 132. 7-Бром-2-фенил-4-(пиперазин-1-ил)-2,3-дигидро-1Н-бензо[b][1,4]диазепин (189JO20)
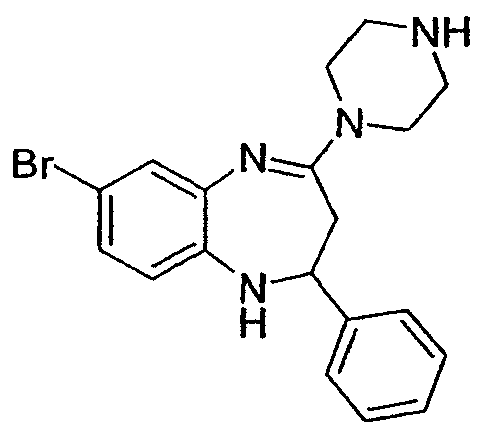
5-Бром-2-фторнитробензол (440 мг, 2,0 ммоль) и гидрохлорид этил-3-амино-3-фенилпропионата (394 мг, 1,5 ммоль) подвергают взаимодействию согласно ОМ9 и получают 9,8 мг указанного в заголовке соединения (189JO20). МС (ESI) 385 (MH)+. Чистота для МН+ (УФ/МС) 97/88.
Пример 133. 7-Бром-10-(пиперазин-1-ил)-1,2,3,3а,4,10а-гексагидробензо[b]циклопента[e][1,4]диазепин (166JO46)

5-Бром-2-фторнитробензол (110 мг, 0,5 ммоль) и гидрохлорид цис-2-амино-1-циклопентанкарбоновой кислоты (138 мг, 0,75 ммоль) подвергают взаимодействию согласно ОМ9 и получают 3,0 мг указанного в заголовке соединения (166JO46). МС (ESI) 349 (MH)+. Чистота для МН+ (УФ/МС) 99/88.
Пример 134. Общая методика 10 (ОМ10)
К раствору 8,5-дихлор-5Н-дибензо[b,е][1,4]диазепина (160FE64) (53 мг, 0,2 ммоль) и PdCl2(PPh3)2 (9 мг, 0,02 ммоль) в сухом ТГФ (1 мл) при комнатной температуре добавляют цинковый реагент (0,4 ммоль). Реакционную смесь встряхивают до полной конверсии (1-16 ч, ТСХ) и затем реакцию гасят, добавляя водный насыщенный раствор NH4Cl. Полученную смесь дважды экстрагируют эфиром, объединенные эфирные фазы промывают рассолом и сушат над Na2SO4. Фильтрование с последующим концентрированием органической фазы при пониженном давлении дают неочищенный продукт реакции, который очищают с использованием колоночной хроматографии (система гептан:EtOAc).
Пример 135. 8-Хлор-11-(4-фторбензил)-5Н-дибензо[b,е][1,4]диазепин (160FE59)
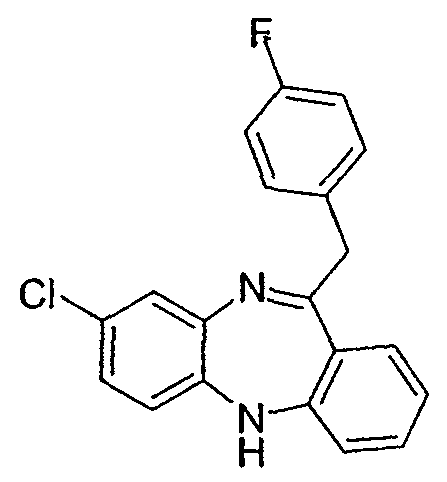
4-Фтробензилцинкхлорид (0,8 мл, 0,5М раствор в ТГФ, 0,4 ммоль) и 8,5-дихлор-5Н-дибензо[b,е][1,4]диазепин (160FE64) (53 мг, 0,2 ммоль) подвергают взаимодействию согласно ОМ10 и получают 52 мг указанного в заголовке соединения (160FE59). МС (ESI) 337 (MH)+. Чистота для МН+ (УФ/МС) 90/90.
Пример 136. 8-Хлор-11-(4-фторбензил)-5Н-дибензо[b,е][1,4]диазепин (160FE70)
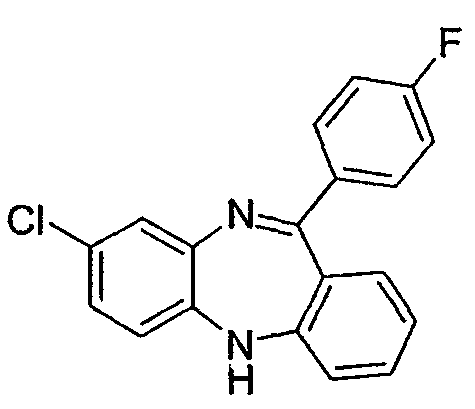
4-Фторбензилцинкхлорид (0,5 мл, 0,5М раствор в ТГФ, 0,4 ммоль) и 8,5-дихлор-5Н-дибензо[b,е][1,4]диазепин (160FE64) (26 мг, 0,1 ммоль) подвергают взаимодействию согласно ОМ10 и получают 23 мг указанного в заголовке соединения (160FE70). МС (ESI) 323 (MH)+. Чистота для МН+ (УФ/МС) 98/100.
Пример 137. Общая методика 11 (ОМ11)
К раствору 8,5-дихлор-5Н-дибензо[b,е][1,4]диазепина (160FE64) (53 мг, 0,2 ммоль), Pd(PPh3)4 (10 мг) и соответствующего реагента бороновой кислоты (0,12 ммоль) в диоксане (3 мл) при комнатной температуре добавляют водный раствор Na2CO3 (1 мл, 1М). Затем смесь встряхивают при 80°С до полной конверсии имидоилхлорида (ТСХ). Температуру понижают и к реакционной смеси добавляют эфир и Н2О. Эфирную фазу промывают рассолом и сушат над Na2SO4. Фильтрование с последующим концентрированием органической фазы при пониженном давлении дают неочищенный продукт реакции, который очищают с использованием колоночной хроматографии (система гептан:EtOAc).
Пример 138. 8-Хлор-11-(4-нонилфенил)-5Н-дибензо[b,е][1,4]диазепин (160FE63)

4-Нонилфенилбороновую кислоту (30 мг, 0,12 ммоль) и 8,5-дихлор-5Н-дибензо[b,е][1,4]диазепин (160FE64) (26 мг, 0,1 ммоль) подвергают взаимодействию согласно ОМ11 и получают 25 мг указанного в заголовке соединения (160FE63). МС (ESI) 431 (MH)+. Чистота для МН+ (УФ/МС) 85/85.
Пример 139. 8-Хлор-11-(пиридин-4-ил)-5Н-дибензо[b,е][1,4]диазепин (160FE69А)
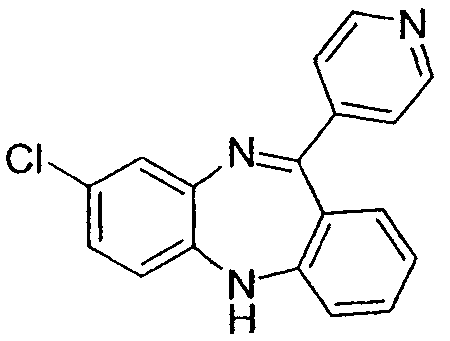
4-Пиридил-4-бороновую кислоту (14 мг, 0,12 ммоль) и 8,5-дихлор-5Н-дибензо[b,е][1,4]диазепин (160FE64) (26 мг, 0,1 ммоль) подвергают взаимодействию согласно ОМ11 и получают 9,3 мг указанного в заголовке соединения (160FE69А). МС (ESI) 306 (MH)+. Чистота для МН+ (УФ/МС) 98/95.
Пример 140. 8-Хлор-11-(1Н-пиразол-4-ил)-5Н-дибензо[b,е][1,4]диазепин (160FE59)

4-(4,4,5,5,-Тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразол (22 мг, 0,1 ммоль) и 8,5-дихлор-5Н-дибензо[b,е][1,4]диазепин (160FE64) (26 мг, 0,1 ммоль) подвергают взаимодействию согласно ОМ11 и получают 8,7 мг указанного в заголовке соединения (160FE59). МС (ESI) 295 (MH)+. Чистота для МН+ (УФ/МС) 95/100.
Пример 141. Проведение функционального скрининга
Некоторые соединения, раскрытые в данном описании, оценивают на активность в отношении мускариновых рецепторов с использованием технологии отбора и амплификации рецепторов (R-SAT), описанной в патенте США № 5707798, включенном в данное описание посредством ссылки. Эффективность (эфф) и активность (выраженная в виде рЕС50) таких соединений в отношении рецепторов М1, М2 и М3 представлены в табл.1.
| название | год | авторы | номер документа |
|---|---|---|---|
| НЕСТЕРОИДНЫЕ МОДУЛЯТОРЫ РЕЦЕПТОРА ПРОГЕСТЕРОНА | 2003 |
|
RU2309155C2 |
| СОДЕРЖАЩАЯ ПРОИЗВОДНОЕ С ТРЕМЯ КОНДЕНСИРОВАННЫМИ КОЛЬЦАМИ СОЛЬ ИЛИ КРИСТАЛЛИЧЕСКАЯ ФОРМА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2020 |
|
RU2835105C1 |
| ЗАМЕЩЕННЫЕ ПИРРОЛЫ, АКТИВНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗ | 2013 |
|
RU2666538C2 |
| ПРОИЗВОДНЫЕ 2-ИМИНОПИРРОЛИДИНА | 2002 |
|
RU2270192C2 |
| ПРОИЗВОДНЫЕ 5H-ДИБЕНЗО[b, e][1, 4]ДИАЗЕПИНА И ИХ ПРИМЕНЕНИЕ | 2010 |
|
RU2441867C2 |
| БИЦИКЛИЧЕСКИЕ ПИРИДИНЫ И АНАЛОГИ В КАЧЕСТВЕ МОДУЛЯТОРОВ СИРТУИНА | 2010 |
|
RU2550821C2 |
| Способ получения производных триазолазепина | 1973 |
|
SU475777A3 |
| ПРОИЗВОДНЫЕ АЗЕПИНОИНДОЛА В КАЧЕСТВЕ ФАРМАЦЕВТИЧЕСКИХ СРЕДСТВ | 2004 |
|
RU2423363C2 |
| ПРОИЗВОДНЫЕ 1,2-ДИ(ЦИКЛО)ЗАМЕЩЕННОГО БЕНЗОЛА | 2004 |
|
RU2340602C2 |
| ИНГИБИТОР, СОДЕРЖАЩИЙ ТРИЦИКЛИЧЕСКОЕ ПРОИЗВОДНОЕ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ | 2019 |
|
RU2800543C2 |
Настоящее изобретение относится к соединению, имеющему структуру, представленную формулой I, или его фармацевтически приемлемой соли, сложному эфиру или амиду, где А имеет структуру  , где каждая связь в А, представленная пунктирной и сплошной линией, представляет углерод-углеродную простую связь; каждый из а, b, с и d представляет собой атом углерода; каждый из е, f, g и h представляет собой атом углерода; Х представляет собой азот; X' представляет собой С; L отсутствует; каждый n равен 1; Y представляет собой азот; W представляет собой азот; R1 представляет собой водород; каждый из R2, R3 и R4 представляет собой атом водорода; каждый из R6, R8 и R9 представляет собой атом водорода; R5 выбирают из группы, состоящей из галогена, C1-6алкила, необязательно замещенного гидроксигруппой, и C1-6алкокси; R7 выбирают из группы, состоящей из галогена, C1-6алкила и пергалогеналкила; Z выбирают из группы, состоящей из NR11, кислорода и CH2; R11 представляет собой водород; и каждая связь в формуле I, представленная пунктирной и сплошной линией, представляет углерод-углеродную двойную связь. Также изобретение относится к способу синтеза соединения формулы V, фармацевтической композиции на основе соединения формулы I, способам лечения психоневрологического расстройства, фармацевтической композиции, содержащей соединение формулы I и психоневрологическое средство. Технический результат: получены новые соединения, полезные для модуляции активности мускаринового рецептора. 9 н. и 28 з.п. ф-лы, 1 табл.
, где каждая связь в А, представленная пунктирной и сплошной линией, представляет углерод-углеродную простую связь; каждый из а, b, с и d представляет собой атом углерода; каждый из е, f, g и h представляет собой атом углерода; Х представляет собой азот; X' представляет собой С; L отсутствует; каждый n равен 1; Y представляет собой азот; W представляет собой азот; R1 представляет собой водород; каждый из R2, R3 и R4 представляет собой атом водорода; каждый из R6, R8 и R9 представляет собой атом водорода; R5 выбирают из группы, состоящей из галогена, C1-6алкила, необязательно замещенного гидроксигруппой, и C1-6алкокси; R7 выбирают из группы, состоящей из галогена, C1-6алкила и пергалогеналкила; Z выбирают из группы, состоящей из NR11, кислорода и CH2; R11 представляет собой водород; и каждая связь в формуле I, представленная пунктирной и сплошной линией, представляет углерод-углеродную двойную связь. Также изобретение относится к способу синтеза соединения формулы V, фармацевтической композиции на основе соединения формулы I, способам лечения психоневрологического расстройства, фармацевтической композиции, содержащей соединение формулы I и психоневрологическое средство. Технический результат: получены новые соединения, полезные для модуляции активности мускаринового рецептора. 9 н. и 28 з.п. ф-лы, 1 табл.
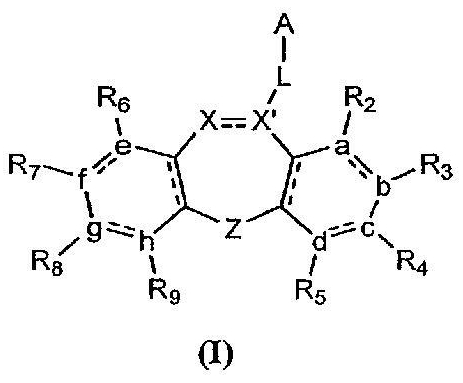
1. Соединение, имеющее структуру, представленную формулой I

или его фармацевтически приемлемая соль, сложный эфир или амид,
где А имеет структуру
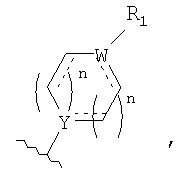
где каждая связь в А, представленная пунктирной и сплошной линией, представляет углерод-углеродную простую связь;
каждый из а, b, с и d представляет собой атом углерода;
каждый из е, f, g и h представляет собой атом углерода;
Х представляет собой азот;
X' представляет собой С;
L отсутствует;
каждый n равен 1;
Y представляет собой азот;
W представляет собой азот;
R1 представляет собой водород;
каждый из R2, R3 и R4 представляет собой атом водорода;
каждый из R6, R8 и R9 представляет собой атом водорода;
R5 выбирают из группы, состоящей из галогена, C1-6алкила, необязательно замещенного гидроксигруппой, и C1-6алкокси;
R7 выбирают из группы, состоящей из галогена, C1-6алкила и пергалогеналкила;
Z выбирают из группы, состоящей из NR11, кислорода и СН2;
R11 представляет собой водород; и
каждая связь в формуле I, представленная пунктирной и сплошной линией, представляет углерод-углеродную двойную связь.
2. Соединение по п.1, где R5 выбирают из группы, состоящей из галогена и C1-6алкила, необязательно замещенного гидроксигруппой.
3. Соединение по п.2, где указанный алкил выбирают из группы, состоящей из метила, этила, пропила, изопропила, бутила, втор-бутила и трет-бутила.
4. Соединение по п.2, где указанный галоген выбирают из группы, состоящей из фтора, хлора и брома.
5. Соединение по п.1, где R5 представляет собой хлор.
6. Соединение по п.1, где указанный алкил в R7 выбирают из группы, состоящей из метила, этила, пропила, изопропила, бутила, втор-бутила и трет-бутила.
7. Соединение по п.1, где указанный галоген в R7 выбирают из группы, состоящей из фтора, хлора и брома.
8. Соединение по п.1, где указанный пергалогеналкил в R7 представляет собой перфторалкил.
9. Соединение по п.8, где указанный перфторалкил представляет собой трифторметил.
10. Соединение по п.1, где R7 выбирают из группы, состоящей из метила, хлора и трифторметила.
11. Соединение по п.1, выбранное из группы, в которую входят
4,8-дихлор-11-(пиперазин-1-ил)-5Н-дибензо[b,е][1,4]диазепин,
8-хлор-4-метил-11-(пиперазин-1-ил)-5Н-дибензо[b,е][1,4]диазепин,
8-хлор-4-метил-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
8-бром-4-метил-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
4-метил-11-(пиперазин-1-ил)-8-трифторметилдибензо[b,f][1,4]оксазепин,
8-фтор-4-метил-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин,
4,8-диметил-11-(пиперазин-1-ил)дибензо[b,f][1,4]оксазепин.
12. Способ синтеза соединения формулы V

включающий взаимодействие соединения формулы VII
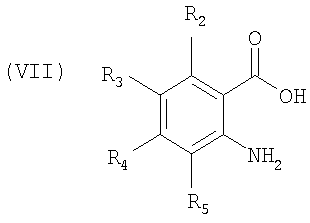
с соединением формулы VIII
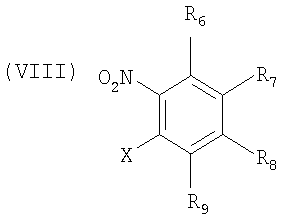
с образованием конденсированного циклического соединения формулы IX

и взаимодействие соединения формулы IX с соединением формулы Х
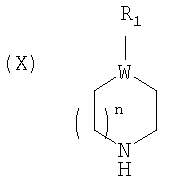
с образованием соединения формулы V;
где Х представляет собой галоген;
W представляет собой азот;
R1 представляет собой водород;
каждый из R2, R3 и R4 представляет собой атом водорода;
каждый из R6, R8 и R9 представляет собой атом водорода;
R5 выбирают из группы, состоящей из галогена, C1-6алкила, необязательно замещенного гидроксигруппой, и C1-6алкокси; и
R7 выбирают из группы, состоящей из галогена, С1-6алкила и пергалогеналкила.
13. Фармацевтическая композиция для модуляции активности мускаринового рецептора, содержащая физиологически приемлемый носитель, разбавитель или эксципиент или их комбинацию и соединение по п.1.
14. Способ лечения психоневрологического расстройства у пациента, включающий введение указанному пациенту терапевтически эффективного количества соединения по п.1.
15. Способ лечения психоневрологического расстройства у пациента, включающий контактирование терапевтически эффективного количества соединения по п.1 с указанным пациентом.
16. Фармацевтическая композиция, содержащая соединение по п.1 и психоневрологическое средство.
17. Композиция по п.16, где указанное психоневрологическое средство выбирают из группы, состоящей из селективного ингибитора повторного поглощения серотонина, ингибитора повторного поглощения норэпинефрина, агониста допамина, антагониста мускаринового рецептора, антипсихотического средства, антагониста серотонина 2А и обратного агониста серотонина 2А.
18. Композиция по п.17, где указанное антипсихотическое средство выбирают из группы, состоящей из фенотиазина, фенилбутилпиперидина, дебензапина, бензизоксидила и соли лития.
19. Композиция по п.18, где указанный фенотиазин выбирают из группы, состоящей из хлорпромазина (Thorazine®), мезоридазина (Serentil®), прохлорперазина (Compazine®) и тиоридазина (Mellaril®).
20. Композиция по п.18, где указанный фенилбутилпиперидин выбирают из группы, состоящей из галоперидола (Haldol®) и пимозида (Оvар®).
21. Композиция по п.18, где указанный дебензапин выбирают из группы, состоящей из клозапина (Clozaril®), локсапина (Loxitane®), оланзапина (Zyprexa®) и кветиапина (Seroquel®).
22. Композиция по п.18, где указанный бензизоксидил выбирают из группы, состоящей из рисперидона (Resperidal®) и ципразидона (Geodon®).
23. Композиция по п.18, где указанная соль лития представляет собой карбонат лития.
24. Композиция по п.17, где указанное антипсихотическое средство выбирают из группы, состоящей из Clozaril, Compazine, Etrafon (Triavil), Geodon, Haldol, Inapsine, Loxitane, Mellaril, Moban, Navane, Orap, Permitil, Prolixin, Phenergan, Reglan, Risperdal, Serentil, Seroquel, Stelazine, Taractan, Thorazine, Trilafon и Zyprexa.
25. Композиция по п.17, где указанный селективный ингибитор повторного поглощения серотонина выбирают из группы, состоящей из флуоксетина, флувоксамина, сертралина, пароксетина, циталопрама, эсциталопрама, сибутрамина, дулоксетина и венлафаксина, и их фармацевтически приемлемых солей или пролекарств.
26. Композиция по п.17, где указанный ингибитор повторного поглощения норэпинефрина выбирают из группы, состоящей из тионизоксетина и ребоксетина.
27. Композиция по п.17, где указанный агонист допамина выбирают из группы, состоящей из суматриптана, альмотриптана, наратриптана, фроватриптана, ризатриптана, зомитриптана, каберголина, амантадина, лизурида, перголида, ропинирола, прамипексола и бромокриптина.
28. Композиция по п.17, где указанный антагонист серотонина 2А представляет собой соединение формулы XIV или его родственный аналог
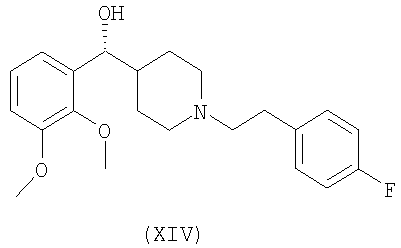
29. Способ лечения психоневрологического расстройства у пациента, включающий введение указанному пациенту терапевтически эффективного количества композиции по п.16.
30. Способ лечения психоневрологического расстройства у пациента, включающий введение указанному пациенту терапевтически эффективного количества соединения по п.1 и терапевтически эффективного количества психоневрологического средства.
31. Способ по п.30, где стадия указанного введения включает введение указанного соединения по п.1 и указанного психоневрологического средства почти одновременно.
32. Способ по п.30, где стадия указанного введения включает введение сначала одного указанного соединения по п.1 и указанного психоневрологического средства и затем введение другого активного указанного соединения по п.1 и указанного психоневрологического средства.
33. Способ по п.30, где указанное психоневрологическое расстройство выбирают из группы, состоящей из шизофрении и родственных идиопатических психозов, тревоги, расстройств сна, расстройств аппетита, аффективных расстройств, таких как большая депрессия, биполярное расстройство и депрессия с психотическими признаками, и синдрома Туретта, психозов, вызванных лекарственными средствами, психозов, вторичных по отношению к психоневрологическим расстройствам, таких как болезнь Альцгеймера или болезнь Гентингтона.
34. Соединение по п.1 для применения при лечении психоневрологического расстройства.
35. Композиция по п.16 для применения при лечении психоневрологического расстройства.
36. Композиция, содержащая соединение по п.1 и психоневрологическое средство, для применения при лечении психоневрологического расстройства.
37. Композиция по п.36, где указанное психоневрологическое расстройство выбирают из группы, состоящей из шизофрении и родственных идиопатических психозов, тревоги, расстройств сна, расстройств аппетита, аффективных расстройств, таких как большая депрессия, биполярное расстройство и депрессия с психотическими признаками, и синдрома Туретта, психозов, вызванных лекарственными средствами, психозов, вторичных по отношению к психоневрологическим расстройствам, таких как болезнь Альцгеймера или болезнь Гентингтона.
| Приспособление в пере для письма с целью увеличения на нем запаса чернил и уменьшения скорости их высыхания | 1917 |
|
SU96A1 |
| Домовый номерной фонарь, служащий одновременно для указания названия улицы и номера дома и для освещения прилежащего участка улицы | 1917 |
|
SU93A1 |
| Способ получения 8-хлор-11-/4-метилпиперазино/-5н-дибензо/в,е,//1,4-/диазепина | 1979 |
|
SU920055A1 |
| SU 1713245 A1, 27.02.1996. | |||
Авторы
Даты
2010-07-10—Публикация
2004-12-21—Подача