Изобретение относится к области газофазной очистки этан-этиленовой фракции (ЭЭФ) пирогаза от примеси ацетилена, в частности к способам приготовления катализаторов очистки методом селективного гидрирования.
Известен способ приготовления палладиевого катализатора на алюмооксидном носителе для селективного гидрирования ацетилена в ЭЭФ, включающий подготовку носителя, нагрев носителя и водного раствора хлорида палладия, пропитку носителя раствором, удаления растворителя из носителя и восстановление металла. Подготовку носителя ведут предварительной прокалкой при 600-800°С, пропиткой раствором нитрата бария Ва(NO3)2 и удалением растворителя - воды в течение 4 ч при 120°С и прокалкой при 1073-1123К. Удаление растворителя из носителя ведут при температуре 373К с последующей прокалкой при 395К. Восстановления металла ведут в токе водорода при температуре 450-475К [1]. На этом катализаторе при температуре 343К, объемной скорости подачи газовой смеси 3000-9000 ч-1 ацетилен, содержащийся в количестве 0,8 об.%, гидрируется полностью.
Недостатками способа являются: большие затраты энергии на удаление растворителя, низкая дисперсность частиц активных центров и широкий диапазон разброса по размерам частиц, как на поверхности, так и в объеме носителя, что ухудшает селективность и ведет к образованию «зеленого масла», снижающего срок непрерывной работы катализатора между регенерациями.
Известен способ приготовления катализатора на алюмооксидном носителе для селективного гидрирования ацетилена в ЭЭФ, включающий подготовку носителя, нагрев носителя и смеси водных растворов хлорида палладия и нитрата хрома, пропитку носителя смесью растворов, удаление растворителя из носителя. Удаление растворителя из носителя ведут при температурах 298-473К либо на открытом воздухе, либо под вакуумом с последующей прокалкой при 973-1173К. Восстановления металла ведут в токе водорода при температуре 450-475К [2].
В процессе гидрирования ацетилена катализатор, полученный данным способом, обеспечивает селективность 75-78%, активность 80% при давлении 3,4-34 МПа, температуре 323-473К и объемной скорости исходной газовой смеси 50-10000 ч-1.
Недостатками данного способа приготовления палладиевого катализатора являются использование токсичного элемента хрома в качестве модификатора катализатора, энергоемких стадий удаления растворителя и прокалки катализатора, получение катализатора с невысокой селективностью, работающего при достаточно высоких температурах, при которых происходит образование "зеленого масла" за счет реакций полимеризации ацетилена и этилена на активных центрах.
Наиболее близким по технической сущности и количеству совпадающих признаков является способ приготовления палладиевого катализатора на алюмооксидном носителе для селективного гидрирования ацетилена в этан-этиленовой фракции, включающий подготовку носителя, нагрев носителя и раствора металлорганического комплекса палладия, пропитку носителя раствором, удаление растворителя из носителя и восстановление металла [3]. В качестве палладийсодержащего раствора используют раствор аминного комплекса палладия в этаноламине в смеси с полиэтиленоксидом, процесс пропитки проводят при 68-70°С, а удаление растворителя ведут в течение 1-2 ч при 363-373К и восстановление - в течение 2-3 ч при 393-403К и 4-5 ч при 413-418К. Недостатками данного способа приготовления палладиевого катализатора являются наличие длительной и энергоемкой стадии удаления растворителя, низкая дисперсность частиц активных центров и широкий диапазон разброса по размерам частиц, как на поверхности, так и в объеме носителя.
Задачей изобретения, во-первых, является обеспечение высокой дисперсности частиц активных центров в узком диапазоне разброса по размерам частиц, как на поверхности, так и в объеме носителя, что позволит повысить активность, селективность катализатора и увеличить срок его непрерывной работы между стадиями регенерации, во-вторых, снижение энергозатратности приготовления катализатора за счет значительного сокращения длительности стадии удаления растворителя. В предлагаемом способе удаление растворителя - СО2 производится простым сбросом давления.
Задача достигается тем, что способ приготовления палладиевого катализатора на алюмооксидном носителе для селективного гидрирования ацетилена в этан-этиленовой фракции, включающий подготовку носителя, нагрев носителя и раствора металлорганического комплекса палладия, пропитку носителя раствором, удаление растворителя из носителя и восстановление металла, согласно изобретению, ведут при 1,0≤Т/Ткр≤1,2 и 1,3≤Р/Ркр≤5,6 растворенным в диоксиде углерода бензонитрильным, либо стирольным, либо циклогексановым комплексом хлорида палладия, удаление растворителя из носителя ведут простым сбросом давления до Р<Ркр, а восстановление металла ведут в токе водорода при температуре 450-475К, где Т - температура, К; Р - давление, МПа; Ткр - критическая температура растворителя, К; Ркр - критическое давление растворителя.
Вещества, которые при нормальных параметрах состояния (Т~273 К, Р~0,1 МПа) являются газами в сверхкритическом состоянии (сверхкритические флюиды), становятся сильными растворителями, обладающими уникальными свойствами. В окрестности критической точки проявляется резкая аномалия всех термодинамических и транспортных свойств растворителя. Так, динамическая вязкость сверхкритических флюидов менее чем на порядок превосходит аналогичный показатель обычных газов (~100 µП), и это имеет место в ситуации, когда плотность сверхкритических флюидов (~300÷800 кг/м3) как минимум на два порядка превышает плотность последних (~1 кг/м3). Коэффициент диффузии в сверхкритических флюидах при условии бесконечного разбавления по величине на 1÷2 порядка превосходит аналогичный показатель для жидкостей. По сравнению с жидкими растворителями сверхкритические флюиды имеют более низкое значение коэффициента поверхностного натяжения. Все эти свойства сверхкритических флюидов позволяют значительно увеличить скорость пропитки пористых структур различными растворами.
Процессы, использующие сверхкритические флюидные среды, проводятся при небольших температурах. Так, критическая температура наиболее распространенного флюида - углекислого газа 304К.
Энергозатратность процесса пропитки носителя определяется растворимостью металлорганического комплекса палладия в сверхкритическом растворителе. Результаты растворимости бензонитрильного, стирольного и циклокесенового комплексов палладия в диоксиде углерода при различных температурах и давлениях приведены в табл. 1-3. Как видно из таблиц, зависимость растворимости от давления при всех исследованных температурах носит экстремальный характер. Отсюда для каждой температуры исследования можно определить максимальное значение растворимости металлорганического комплекса в диоксиде углерода. Если проводить процесс пропитки носителя при параметрах состояния, соответствующих максимуму растворимости, то энергозатратность этого процесса будет минимальной. Для промышленной реализации процесса пропитки носителя раствором металлоорганического комплекса в диоксиде углерода оптимальной является область параметров состояния 1,0≤Т/Ткр≤1,2 и 1,3≤Р/Ркр≤5,6.
При Т≥Ткр и Р≥Ркр способ пропитки носителя раствором металлоорганического комплекса также осуществим, однако затраты энергии для осуществления способа будут выше. Так, например, при пропитке носителя раствором металлоорганического комплекса в диоксиде углерода при температуре 318,15К и давлении Р/Ркр>5,6 (Р>42 МПа) необходимо затратить энергии в 4 и более раза больше, чем при той же температуре, но давлении 25 МПа.
Предлагаемый способ может быть применен для изготовления катализаторов гидрирования жиров (органических жирных кислот), непредельных алифатических углеводородов, пропадиена, метилацетилена, диеновых углеводородов, олефиновых улеводородов и др.
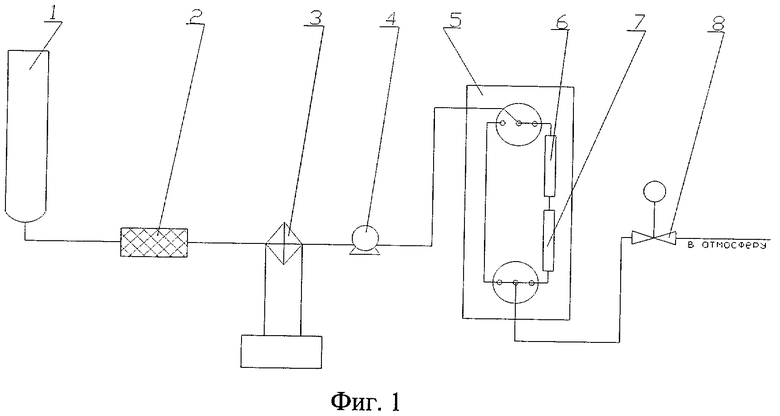
На фиг. 1 приведена установка по исследованию растворимости и пропитки носителя, где 1 - баллон с CO2, 2 - фильтр-осушитель, 3 - холодильный агрегат, 4 - насос, 5 - термостат, 6, 7 - ячейки, 8 - регулятор давления.
На следующих примерах описан способ приготовления палладиевого катализатора на алюмооксидном носителе для селективного гидрирования ацетилена в этан-этиленовой фракции.
Пример 1
Алюмооксидный носитель массой 4 г прокаливается в печи при температуре 820К в течение 3 часов для удаления паров влаги и примесей, находящихся в порах носителя. В ячейку 6 (фиг. 1) помещается бензонитрильный комплекс хлорида палладия массой 2,5 г, а в ячейку 7 (фиг. 1) - носитель. Газ, проходя через первую ячейку, растворяет в себе комплекс, и поступает во вторую ячейку, в которой носитель сорбирует в себя комплекс из раствора. Процесс пропитки проводился в течение 15 часов. Массовый расход газа 0,4 г/мин, температура 328,15К, давление от 25 до 30 МПа. Восстановление металла из комплекса, нанесённого на носитель, проводится при температуре около 470К в токе водорода при объемной скорости подачи водорода 30 мл/мин. В результате получается катализатор с палладия 0,022 % (масс).
Пример 2
Катализатор готовят аналогично примеру 1, только в ячейку 6 помещен стирольный комплекс хлорида палладия. В результате получается катализатор с палладия 0,15 % (масс).
Пример 3
Катализатор готовят аналогично примеру 1, только в ячейку 6 помещен циклогексеновый комплекс хлорида палладия. В результате получается катализатор с палладия 0,04% (масс).
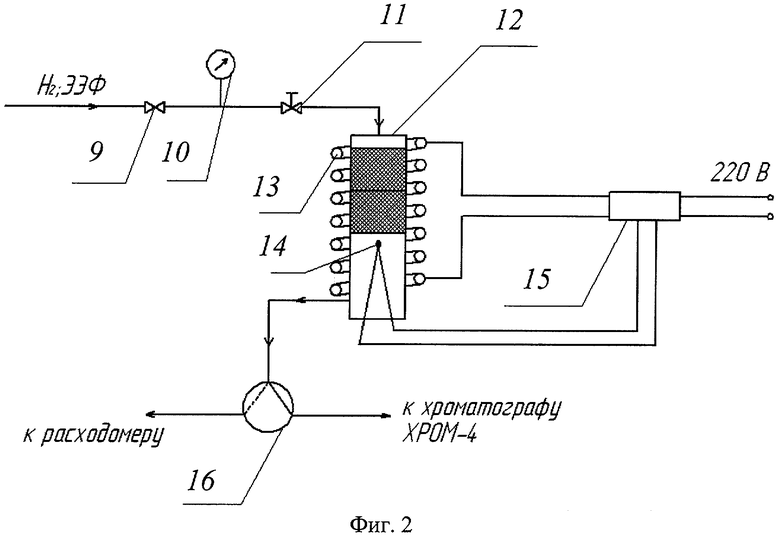
Анализ катализаторов осуществлён на микрокаталитической экспериментальной установке проточного типа действия. На фиг. 2 приведена схема экспериментальной установки по определению активности и селективности полученных катализаторов, где 9 - игольчатый вентиль, 10 - манометр марки МТИ, 11 - вентиль тонкой регулировки, 12 - реактор, 13 - электропечь, 14 - термопара, 15 - терморегулятор, 16 - трехходовой кран. Данная установка используется как для предварительной обработки катализатора (восстановление водородом), так и для дальнейшего испытания этого катализатора на активность и селективность при очистке этан-этиленовой фракции от примесей ацетилена. 0,5 см3 катализатора с размером частиц 0,2-0,5 мм загружается в среднюю часть реактора 12, под которым размещается спай измерительной и регулирующей термопары 14 терморегулятора 15. Кроме того, для дополнительного обогрева поступающего газового потока над слоем катализатора засыпается слой инертного носителя (размолотое кварцевое стекло или фарфор с размером частиц 0,2-0,5 мм).
Восстановление проводится при температуре около 470К в токе водорода, который мы устанавливаем при помощи вентилей 9 и 11 и замеряем на выходе пленочным расходомером, при установленной объемной скорости подачи водорода и включенном нагреве печи. Восстановление заканчивается за 2 часа. Далее снижают температуру в реакторе 12 до температуры, выбранной для проведения эксперимента, после чего подачу водорода прекращают и начинают подачу этан-этиленовой фракции следующего состава, об.%: C1 - 0,22; С2 (этан) - 13,11; С2 (этилен) - 80,99; С2 (ацетилен) - 1,05; Н2 - 4,73 с требуемой объемной скоростью подачи. Состав ЭЭФ определён на заводе «Оргсинтез». Анализ ЭЭФ после реактора проводили на хроматографе «ХРОМ-4» с пламенным ионизационным детектором.
Результаты испытания активности катализатора, пропитанного бензонитрильным комплексом, в сравнении с образцами, приготовленными из воды и бензола по традиционной методике, представлены в табл.4, где:
образец 1 приготовлен из водного раствора хлорида палладия, содержание палладия 0,022 мас.%;
образец 2 приготовлен из раствора бензонитрильного комплекса палладия в бензоле, содержание палладия 0,022 мас.%;
образец 3 приготовлен из раствора бензонитрильного комплекса палладия в сверхкритическом диоксиде углерода, содержание палладия 0,022 мас.%;
Результаты испытания показали, что селективность гидрирования ацетилена в ЭЭФ на катализаторе, приготовленном по предложенному способу, выше, чем на катализаторе, приготовленном по способу [3], 88-92% против 83-85% при одинаковых условиях процесса гидрирования.
На электронном микроскопе-микроанализаторе марки ЭММА-4 исследован разброс размеров частичек палладия на поверхности и в сколе гранулы носителя. Установлено, что при пропитке носителя по предлагаемому способу (примеры 1-3) получаются катализаторы:
- С узким диапазоном разброса размера частиц активного металла, который составляет 3±1 нм (90% частиц). У катализатора приготовленного по способу [3] разброс размера частиц активного металла составляет 3÷3000 нм (90% частиц).
- С высокой дисперсностью распределения частиц активного металла, так на поверхности и объеме носителя в среднем в 100 раз больше частиц активного металла, чем у катализатора, приготовленного по способу [3].
Источники информации
1. А.с. СССР N 871377, опубл. 1992 по классу B01J 23/44.
2. Пат. США N 4551443, опубл. 1985.
3. Патент (РФ) 2161535, опубл. 10.01.2001 по классам B01J 37/02, B01J 23/44, B01J 23/63.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПАЛЛАДИЕВОГО КАТАЛИЗАТОРА ГИДРИРОВАНИЯ АЦЕТИЛЕНА | 2015 |
|
RU2572787C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ПАЛЛАДИЕВОГО КАТАЛИЗАТОРА | 1998 |
|
RU2161535C2 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА ДЛЯ ГИДРИРОВАНИЯ АЦЕТИЛЕНА В ЭТАН-ЭТИЛЕНОВОЙ ФРАКЦИИ | 1991 |
|
RU2053018C1 |
| Способ изготовления катализатора селективного гидрирования ЭЭФ | 2021 |
|
RU2772011C1 |
| СПОСОБ ОЧИСТКИ ПОРИСТОЙ МАТРИЦЫ ОТ ЖИДКИХ И ТВЕРДЫХ ОТЛОЖЕНИЙ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2006 |
|
RU2348447C2 |
| Катализатор жидкофазного селективного гидрирования ацетиленовых углеводородов и способ его получения | 2020 |
|
RU2738233C1 |
| Катализатор, способ его приготовления и способ одностадийной переработки возобновляемого растительного сырья для получения экологически чистых компонентов моторных топлив | 2019 |
|
RU2699364C1 |
| КАТАЛИЗАТОР ГИДРИРОВАНИЯ АЦЕТИЛЕНА В ЭТАН-ЭТИЛЕНОВОЙ ФРАКЦИИ | 1998 |
|
RU2145519C1 |
| КАТАЛИТИЧЕСКАЯ СИСТЕМА ДЛЯ СЕЛЕКТИВНОГО ГИДРИРОВАНИЯ ЭТАН-ЭТИЛЕНОВОЙ ФРАКЦИИ ПИРОЛИЗА НЕФТЕПРОДУКТОВ | 1999 |
|
RU2152252C1 |
| СПОСОБ ОЧИСТКИ ТОПЛИВНОГО КОЛЛЕКТОРА С ФОРСУНКАМИ КАМЕРЫ СГОРАНИЯ ГАЗОТУРБИННОГО ДВИГАТЕЛЯ ОТ ПРОДУКТОВ КОКСОВАНИЯ ТОПЛИВА | 2014 |
|
RU2561367C1 |
Изобретение относится к способам приготовления катализаторов очистки этан-этиленовой фракции пирогаза от примеси ацетилена методом селективного гидрирования. Описан способ приготовления палладиевого катализатора на алюмооксидном носителе для селективного гидрирования ацетилена в этан-этиленовой фракции, включающий подготовку носителя, нагрев носителя и раствора металлорганического комплекса палладия, пропитку носителя раствором, удаление растворителя из носителя и восстановление металла, отличающийся тем, что нагрев и пропитку ведут при 1,0≤Т/Ткр≤1,2 и 1,3≤Р/Ркр≤5,6 растворенным в диоксиде углерода бензонитрильным, либо стирольным, либо циклогексановым комплексом хлорида палладия, удаление растворителя из носителя ведут простым сбросом давления до Р<Ркр, а восстановление в токе водорода при температуре около 470К, где Т - температура, К; Р - давление, МПа; Ткр - критическая температура растворителя; Ркр - критическое давление растворителя. Технический эффект - получен высокодисперсный катализатор, обладающий повышенной активностью, селективностью катализатора с увеличенным сроком его непрерывной работы между стадиями регенерации, при этом способ получения характеризуется снижением энергозатрат на приготовление катализатора за счет значительного сокращения длительности стадии удаления растворителя. 4 табл., 2 ил.
Способ приготовления палладиевого катализатора на алюмооксидном носителе для селективного гидрирования ацетилена в этан-этиленовой фракции, включающий подготовку носителя, нагрев носителя и раствора металлорганического комплекса палладия, пропитку носителя раствором, удаление растворителя из носителя и восстановление металла, отличающийся тем, что нагрев и пропитку ведут при 1,0≤Т/Ткр≤1,2 и 1,3≤Р/Ркр≤5,6 растворенным в диоксиде углерода бензонитрильным, либо стирольным, либо циклогексановым комплексом хлорида палладия, удаление растворителя из носителя ведут простым сбросом давления до Р<Ркр, а восстановление в токе водорода при температуре около 470 К, где Т - температура, К; Р - давление, МПа; Ткр - критическая температура растворителя; Ркр - критическое давление растворителя.
| СПОСОБ ПРИГОТОВЛЕНИЯ ПАЛЛАДИЕВОГО КАТАЛИЗАТОРА | 1998 |
|
RU2161535C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЛЮМОПАЛЛАДИЕВОГО КАТАЛИЗАТОРА | 2001 |
|
RU2199392C1 |
| КАТАЛИТИЧЕСКАЯ СИСТЕМА ДЛЯ СЕЛЕКТИВНОГО ГИДРИРОВАНИЯ ЭТАН-ЭТИЛЕНОВОЙ ФРАКЦИИ ПИРОЛИЗА НЕФТЕПРОДУКТОВ | 1999 |
|
RU2152252C1 |
| DE 19757990 А1, 02.07.1998 | |||
| WO 2003033136 R4, 24.04.2003 | |||
| ВЛАЖНАЯ САЛФЕТКА ИЛИ ТОНКИЙ ГИГИЕНИЧЕСКИЙ МАТЕРИАЛ, КОТОРЫЕ МОЖНО СПУСКАТЬ В КАНАЛИЗАЦИЮ | 2009 |
|
RU2519994C2 |
Авторы
Даты
2010-07-20—Публикация
2008-12-26—Подача