Изобретение относится к технологии получения ди-(β-хлорэтил)формаля, являющегося основным сырьем при синтезе полисульфидных олигомеров (тиоколов), характеризующихся способностью к холодной вулканизации с получением уникальных по своим свойствам герметиков.
Известен способ получения ди-(β-хлорэтил)формаля путем конденсации этиленхлоргидрина с формальдегидом в присутствии кислых катализаторов по реакции
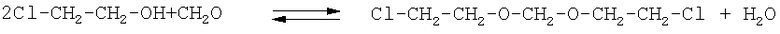
Для смещения данной равновесной системы в сторону образования целевого продукта используют водоотнимающие средства, такие как: сульфат натрия, хлорид кальция (Ю.В.Поконова. Галоидэфиры. Изд-во «Химия», М.-Л., 1966, с.20-21) или концентрированную серную кислоту (Химическая промышленность, т.84, №2, 2007, с.97-100). Однако применение серной кислоты в технологии получения ди-(β-хлорэтил)формаля сопряжено с образованием значительного количества отходов - разбавленной серной кислоты, загрязненной органическими примесями и поэтому трудно утилизируемой. Использование в качестве водоотнимающего средства хлорида кальция приводит к сложному аппаратурному оформлению процесса, а также к значительным потерям целевого продукта с отработанным хлоридом кальция.
К более современным приемам удаления воды из реакционной смеси синтеза ди-(β-хлорэтил)формаля относится ее отгонка в виде азеотропной смеси с подходящим разделяющим агентом, например дихлорэтаном, диизопропиловым эфиром, нитрометаном (С.К.Огородников. Формальдегид. Изд-во «Химия», Л., 1984, с.199) или этиленхлоргидрином, взятым для реакции в стехиометрическом избытке (J.Orlowski, H.Czerwinska, L.Klar. Przem. Chem., 1957, 13, №9, 520-523, Д.М.Винокуров, «Известия высших учебных заведений. Химия и химическая технология», 1961, 4, №6, 988-991).
Известен способ (Патент РФ №2143419, заявл 07.07.98, оп. 27.12.99) получения ди-(β-хлорэтил)формаля путем взаимодействия 1-хлорметил-2'-хлорэтилового эфира с окисью этилена в присутствии каталитического количества хлорида цинка при температуре от минус 10 до плюс 10°С с выходом целевого продукта 99%. Но 1-хлорметил-2'-хлорэтиловый эфир относится к классу высокотоксичных соединений. Кроме того, при проведении синтеза ди-(β-хлорэтил)формаля из данного эфира и окиси этилена, отличающегося выделением значительного количества тепла, была отмечена возможность локальных перегревов реакционной массы, сопровождающихся образованием полимеров окиси этилена.
Наиболее близок к заявляемому способу получения ди-(β-хлорэтил)формаля метод, используемый в патенте (Патент ФРГ №4214847, заявл. 05.05.92, оп. 11.11.93) и заключающийся во взаимодействии параформальдегида - полимерной формы формальдегида (ФА) и этиленхлоргидрина (ЭХГ), взятых в мольном соотношении ФА:ЭХГ, равном 1:(2,7÷6), предпочтительно 1:(3÷4,5), в присутствии концентрированной соляной кислоты. Роль азеотропообразующего средства в данном способе осуществляет этиленхлоргидрин, взятый на синтез в большом избытке. Поскольку соляная кислота вносит с собой в реакционную систему воду, ингибирующую процесс конденсации этиленхлоргидрина с формальдегидом, то авторы достигают высокой степени превращения исходных реагентов в целевой продукт 98-99% и высоких выходов ди-(β-хлорэтил)формаля - 98% (по ФА) и 97% (по ЭХГ) за счет значительного количества избыточного этиленхлоргидрина и высоких температур синтеза - 80-125°С. Поскольку вывод реакционной воды из системы осуществляется за счет избыточного этиленхлоргидрина, то данный способ получения ди-(β-хлорэтил)формаля характеризуется большими потерями исходного сырья (этиленхлоргидрина), составляющими по массе не менее 10% от массы получаемого целевого продукта. Кроме того, в данном технологическом процессе необходима специальная стадия отделения возвратного этиленхлоргидрина от реакционной воды, которая в описании патента не упоминается.
Задачей предлагаемого изобретения является увеличение выхода ди-(β-хлорэтил)формаля, повышение селективности процесса по целевому продукту и уменьшение потерь сырьевых компонентов.
Авторы предлагают получать ди-(β-хлорэтил)формаль путем взаимодействия этиленхлоргидрина (ЭХГ) с параформальдегидом (ФА) в присутствии кислотного катализатора - безводного хлористого водорода (HCl). Синтез ди-(β-хлорэтил)формаля протекает в две стадии. Вначале проводят растворение параформальдегида в предварительно закисленном хлористым водородом этиленхлоргидрине при температуре 40-60°С и выдерживают реакционную смесь при температуре 40-85°С в течение 20-30 мин. Концентрация хлористого водорода в реакционной смеси в диапазоне 0,3-1,0 мас.%. Мольное соотношение ЭХГ:ФА соответствует (2,25÷2,7):1, преимущественно 2,6:1. Общая продолжительность первой стадии синтеза не превышает 40 мин. Выход ди-(β-хлорэтил)формаля по окончании первой стадии синтеза составляет от 80 до 90,2%. Селективность по целевому продукту от 95,8 до 99,7% (по формальдегиду) и от 98,0 до 99,8% (по ЭХГ).
Предлагаемые условия уже на первой стадии синтеза обеспечивают высокую конверсию исходных реагентов (не менее 80%) при одновременно высокой селективности процесса по целевому продукту и незначительному образованию побочных олигомерных формалей.
Для достижения в заявленном способе выходов целевого ди-(β-хлорэтил)формаля вторую стадию синтеза осуществляют с одновременной отгонкой реакционной воды в виде азеотропной смеси с добавленным для этой цели 1,2-дихлорэтаном (ДХЭ) в количестве 2,04 моля на 1 моль получаемого ди-(β-хлорэтил)формаля. Отгонку азеотропной смеси ДХЭ-H2O от реакционной массы проводят на колонне ректификации при атмосферном давлении и температуре куба колонны 84-95°С, верха - 72-85°С. 1,2-Дихлорэтан загружают в куб колонны ректификации или полностью из расчета 201,73 г (2,04 моля) на 1 моль получаемого ди-(β-хлорэтил)формаля, или сначала загружают одну треть необходимого количества 1,2-дихлорэтана, а остальной 1,2-дихлорэтан дозируют в куб колонны непрерывно в ходе всего процесса отгонки реакционной воды. По окончании второй стадии синтеза выход ди-(β-хлорэтил)формаля достигает 95,0-99,6% при одновременно высокой селективности процесса по целевому продукту, составляющей 97,0-99,7% (по формальдегиду) и 98,5-99,8% (по ЭХГ). Отогнанная азеотропная смесь ДХЭ-H2O с примесями ЭХГ, HCl и формальдегида расслаивается на органический - дихлорэтановый слой, который возвращают в рецикл на последующую операцию получения ди-(β-хлорэтил)формаля, и на водный слой.
Полученный после отгонки реакционной воды кубовый остаток с содержанием ди-(β-хлорэтил)формаля в среднем 80% (остальное - в основном избыточный ЭХГ) подвергают ректификации под вакуумом (Рост = 230 мм рт.ст.). После отгонки избыточного ЭХГ ди-(β-хлорэтил)формаль, содержащий олигомерные формали в количестве 0,32-1,73 мас.%, используют для синтеза тиоколов.
Отогнанный ЭХГ возвращают в рецикл на первую стадию синтеза ди-(β-хлорэтил)формаля.
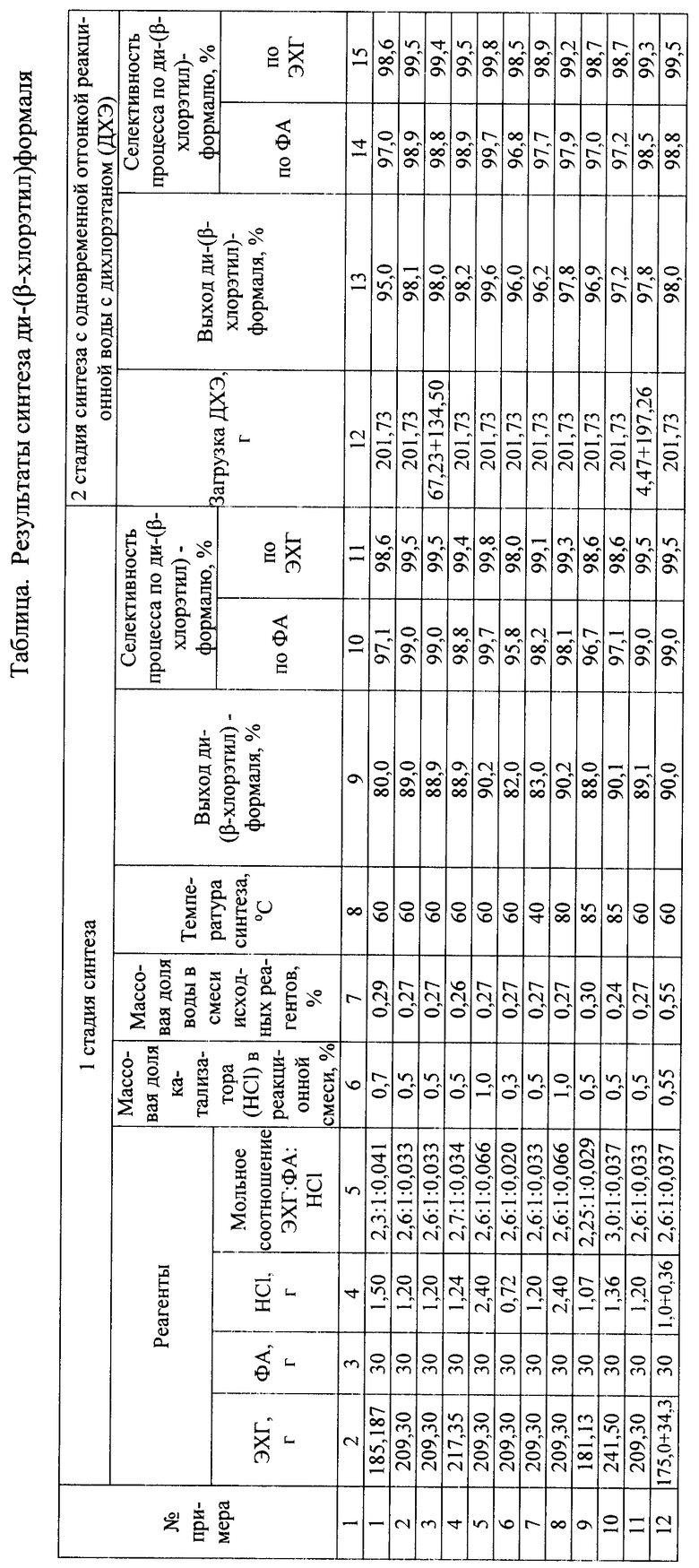
Получение ди-(β-хлорэтил)формаля по предлагаемому способу иллюстрируется примерами 1-12, условия проведения синтеза и отгонки и результаты приведены в таблице.
Пример 1. В стеклянный реактор, снабженный мешалкой, обратным холодильником, термометром и тубусом для загрузки исходных компонентов и отбора проб реакционной массы на анализ, загружают 185,187 г (2,3 моля) этиленхлоргидрина (содержащего в своем составе 0,037 г H2O), предварительно закисленного газообразным хлористым водородом. Масса растворенного в ЭХГ хлористого водорода составляет 1,5 г. Содержимое реактора нагревают с помощью водяной бани до температуры 60°С и загружают 30,597 г параформальдегида, содержащего в своем составе 0,597 г Н2О в виде примеси. Массовая доля катализатора (хлористого водорода) в суммарной массе загруженных исходных реагентов (ЭХГ и формальдегид) составляет 0,7%. Реакционную смесь выдерживают при температуре 60°С и при перемешивании в течение 30 мин.
Массовая доля ди-(β-хлорэтил)формаля в реакционной смеси по истечении указанного времени составляет 63,7%, что соответствует образованию 80% целевого продукта от теоретически возможного. Селективность процесса по ди-(β-хлорэтил)формалю составляет 97,1% (по израсходованному формальдегиду), 98,6% (по израсходованному ЭХГ).
Полученную на первой стадии синтеза реакционную массу переносят в куб ректификационной колонны эффективностью 5 т.т., куда загружают также 201,73 г (161 мл) ДХЭ в качестве азеотропообразователя для отгонки реакционной воды. Азеотропную смесь ДХЭ-H2O отгоняют при атмосферном давлении и при температуре куба колонны 84-95°С, верха - 72-85°С. Общая масса отогнанной жидкости составляет 230,2 г, при расслоении которой получают 210,75 г органического (ди-хлорэтанового слоя) и 19,45 г водного слоя. Продолжительность разгонки 45 минут.
Состав полученного дихлорэтанового слоя, мас.%:
Состав водного слоя, мас.%:
В кубе колонны после отделения реакционной воды осталось 188,81 г ди-(β-хлор-этил)формаля - сырца, содержащего в своем составе, мас.%:
где T1 и Т2 - гомологи ди-(β-хлорэтил)формаля, имеющие формулу:
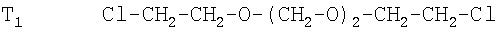
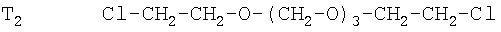
Выход ди-(β-хлорэтил)формаля после отгонки реакционной воды составляет 95% от теоретического. Селективность всего процесса получения целевого продукта, рассчитанная по израсходованному формальдегиду, составляет 97%, по израсходованному этиленхлоргидрину - 98,6%.
Остаточный этиленхлоргидрин и другие легкокипящие примеси (формальдегид, ДХЭ, HCl, Н2О) удаляют от ди-(β-хлорэтил)формаля - сырца отгонкой на колонне ректификации под вакуумом (остаточное давление - 230 мм рт.ст.) при температуре куба колонны 112-130°С, верха - 84-90°С. Масса отогнанной фракции составляет 21,46 г. Состав, мас.%:
Жидкость, оставшаяся в кубе колонны и представляющая собой товарный ди-(β-хлорэтил)формаль массой 167,35 г, имеет следующий состав, мас.%:
Методом простой отгонки под вакуумом можно получить ди-(β-хлорэтил)формаль улучшенного качества с содержанием основного вещества не менее 99 мас.%.
Пример 2. Синтез ди-(β-хлорэтил)формаля выполняют, как в примере 1, но при мольном соотношении ЭХГ:ФА, равном 2,6:1, в присутствии 0,5 мас.% хлористого водорода при температуре 60°С. Выход ди-(β-хлорэтил)формаля на первой стадии синтеза составляет 89% от теоретического. Селективность по целевому продукту - 99% (по формальдегиду) и 99,5% (по ЭХГ). После второй стадии синтеза с отгонкой реакционной воды в смеси с ДХЭ, добавленным в том же количестве, как и в примере 1, получают 211,43 г ди-(β-хлорэтил)формаля - сырца, содержащего 80,27% основного вещества (остальное - остаточный ЭХГ и другие примеси). Выход ди-(β-хлорэтил)формаля на этой стадии составляет 98,1%. Суммарное содержание формалей - гомологов в ди-(β-хлорэтил)формале - сырце составляет 0,51%. Селективность процесса по целевому продукту - 98,9% (по формальдегиду) и 99,5% (по ЭХГ). После расслоения отогнанной на второй стадии синтеза азеотропной смеси получают 212,11 г органического (дихлорэтанового) слоя, содержащего 93% ДХЭ (197,26 г) и подлежащего возврату в цикл на стадию отгонки реакционной воды при проведении другой операции синтеза ди-(β-хлорэтил)формаля. В результате отделения остаточного ЭХГ от полученного ди-(β-хлорэтил)формаля - сырца отгонкой на колонне ректификации при давлении 230 мм рт.ст., температуре куба колонны 112-129°С, верха 84-90°С получают 170,53 г ди-(β-хлорэтил)формаля технического, содержание основного вещества в котором составляет 98,69%, а суммарная концентрация формалей - гомологов 0,62%. Отогнанная на колонне ректификации фракция остаточного этиленхлоргидрина в количестве 40,9 г, содержащая 83,86% ЭХГ (34,3 г), подлежит возврату в цикл на последующие операции синтеза ди-(β-хлорэтил)формаля для замены части загружаемого в реактор исходного ЭХГ.
Пример 3. Синтез ди-(β-хлорэтил)формаля выполняют, как в примере 2, но для отгонки реакционной воды в куб колонны ректификации загружают сначала третью часть (от расчетного количества) азеотропообразователя - ДХЭ 67,23 г (53,7 мл), остальную массу ДХЭ - 134,5 г (107,3 мл) подают в куб колонны непрерывно в процессе отгонки азеотропной смеси. Отгонку смеси ДХЭ-H2O и остаточного ДХЭ проводят в течение 1 часа при атмосферном давлении при температуре куба колонны в диапазоне 89-95°С, верха - 72-85°С. В результате получают 211,38 г ди-(β-хлорэтил)формаля - сырца, содержащего 80,21% основного вещества (169,54 г). Выход целевого продукта составляет 98%. Селективность процесса по ди-(β-хлорэтил)формалю 98,8% (по формальдегиду) и 99,4% (по ЭХГ).
Пример 4-10. Синтез ди-(β-хлорэтил)формаля выполняют в условиях примера 1.
Пример 11. Синтез ди-(β-хлорэтил)формаля выполняют в условиях примера 1. В качестве азеотропообразователя для отгонки реакционной воды используют возвратный ДХЭ в количестве 212,11 г, полученный при проведении синтеза в примере 2, с добавлением 4,47 г свежего ДХЭ. Возвратный ДХЭ содержит в своем составе 93% (197,26 г) основного вещества, остальное: ЭХГ - 6,76%, H2O - 0,19%, HCl - 0,05%. По окончании отгонки реакционной воды с ДХЭ, проводимой аналогично примеру 1, выход ди-(β-хлорэтил)формаля составляет 97,8% при селективности, рассчитанной по израсходованному формальдегиду, 98,5%, по ЭХГ - 99,3%. Полученный после расслоения отогнанной азеотропной смеси дихлорэтановый слой (212,62 г), имеющий следующий состав, мас.%: ДХЭ - 92,63, ЭХГ - 7,11, Н2О - 0,21, HCl - 0,05, может быть снова возвращен в рецикл.
Пример 12. Синтез ди-(β-хлорэтил)формаля выполняют в условиях примера 1, но используют одновременно с чистым ЭХГ (175,0 г) возвратный этиленхлоргидрин в количестве 40,9 г, отогнанный от ди-(β-хлорэтил)формаля - сырца в примере 2 и содержащий в своем составе 83,86% (34,3 г) ЭХГ, остальное, мас.%: ФА - 0,22, ДХЭ - 9,85, ди-(β-хлорэтил)формаль - 3,45, H2O - 1,74 и HCl - 0,88 (0,36 г). Присутствующий в возвратном этиленхлоргидрине хлористый водород заменяет часть катализатора, поэтому на предварительное закисление исходного этиленхлоргидрина расходуют меньшее количество газообразного хлористого водорода - 1,0 г. Суммарное содержание катализатора в реакционной смеси составляет 0,55 мас.%. В результате последующей ректификации полученного в количестве 214,22 г ди-(β-хлорэтил)формаля - сырца, проводимой с целью выделения ди-(β-хлорэтил)формаля технического, отгоняют остаточный этиленхлоргидрин и другие легкокипящие примеси под вакуумом (Рост=230 мм рт.ст.) при температурном режиме, аналогичном примеру 1. Отгон, составивший 42,64 г, содержащий ЭХГ в количестве 82,86%, остальное, мас.%: формальдегид - 0,26, ДХЭ - 10,39, ди-(β-хлорэтил)формаль - 3,68, H2O - 1,88, HCl - 0,94, может быть возвращен в рецикл на следующие операции синтеза ди-(β-хлорэтил)формаля.
Состав ди-(β-хлорэтил)формаля технического, полученного в результате ректификации, следующий, мас.%:
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ТРЕТ-БУТИЛГИПОХЛОРИТА | 2010 |
|
RU2446146C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1,2-ДИХЛОРЭТАНА ИЛИ 1,2-ТРИХЛОРЭТАНА | 1988 |
|
SU1832672A1 |
| СПОСОБ ВАКУУМНОЙ РЕКТИФИКАЦИИ ЭТИЛЕНХЛОРГИДРИНА | 2004 |
|
RU2277082C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,2'-ДИХЛОРДИЭТИЛФОРМАЛЯ | 2013 |
|
RU2522332C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,2-ДИХЛОРЭТАНА | 1992 |
|
RU2072974C1 |
| СПОСОБ ВЫДЕЛЕНИЯ 1-(2-ХЛОРЭТИЛ)ПИРИДИНИЙТЕТРАХЛОРФЕРРАТА ИЗ РЕАКЦИОННОЙ МАССЫ, ПОЛУЧЕННОЙ ХЛОРИРОВАНИЕМ ЭТИЛЕНА ХЛОРОМ В ПРИСУТСТВИИ 1-(2-ХЛОРЭТИЛ)ПИРИДИНИЙТЕТРАХЛОРФЕРРАТА В КАЧЕСТВЕ КАТАЛИЗАТОРА | 1991 |
|
RU2035446C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИСУЛЬФИДА | 2014 |
|
RU2662433C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭТРИОЛА | 2014 |
|
RU2560156C1 |
| СПОСОБ ОЧИСТКИ ДИХЛОРЭТАНА ОТ ХЛОРОПРЕНА | 1992 |
|
RU2061668C1 |
| Способ переработки высококипящих побочных продуктов процесса получения этриола | 2016 |
|
RU2616004C1 |
Изобретение относится к способу получения ди-(β-хлорэтил)формаля, который является основным сырьем при синтезе полисульфидных олигомеров (тиоколов), обладающих способностью к холодной вулканизации с получением уникальных по своим свойствам герметиков. Способ заключается во взаимодействии этиленхлоргидрина с формальдегидом при мольном соотношении (2,25-2,7):1, в присутствии сухого газообразного хлористого водорода в качестве кислотного катализатора, с последующей азеотропной отгонкой реакционной воды в присутствии 1,2-дихлорэтана, в качестве разделяющего агента. Способ позволяет получить целевой продукт с высоким выходом и селективностью. 5 з.п. ф-лы, 1 табл.
1. Способ получения ди-(β-хлорэтил)формаля путем взаимодействия этиленхлоргидрина с формальдегидом в присутствии кислотного катализатора, отличающийся тем, что процесс взаимодействия этиленхлоргидрина с формальдегидом проводят при мольном соотношении (2,25-2,7):1, в присутствии сухого газообразного хлористого водорода в качестве катализатора, с последующей азеотропной отгонкой реакционной воды в присутствии 1,2-дихлорэтана в качестве разделяющего агента.
2. Способ по п.1, отличающийся тем, что сухой газообразный хлористый водород используют в количестве 0,3-1,0 мас.%.
3. Способ по п.1, отличающийся тем, что 1,2-дихлорэтан подают для отгонки реакционной воды полностью.
4. Способ по п.1, отличающийся тем, что 1,2-дихлорэтан подают для отгонки реакционной воды сначала не менее трети от общего количества, а остальной 1,2-дихлорэтан подают непрерывно в ходе всего процесса отгонки реакционной воды.
5. Способ по п.1, отличающийся тем, что после отгонки реакционной воды осуществляют отгонку остаточного этиленхлоргидрина, который возвращают на стадию синтеза.
6. Способ по п.1, отличающийся тем, что 1,2-дихлорэтан после азеотропной отгонки и последующего отделения от слоя воды возвращают в цикл.
| DE 4214847 A1, 11.11.1993 | |||
| КУКУШКИНА Т.Е | |||
| и др | |||
| Перспективное направление в производстве продуктов на основе этиленхлоргидрина | |||
| Пятая Нижегородская сессия молодых ученых | |||
| Нижний Новгород, 2000 | |||
| Сборник тезисов докладов | |||
| Н.Новгород, ИПФ РАН, 2000, с.175-176 | |||
| DE 19601281 A1, 17.07.1997 | |||
| US 4613411 А, 23.09.1986 | |||
| JP 9151341 A, 27.06.1991. |
Авторы
Даты
2010-09-10—Публикация
2008-12-01—Подача