Изобретение относится к органической химии, конкретно - к динитрилам замещенных фталевых кислот общей формулы I:
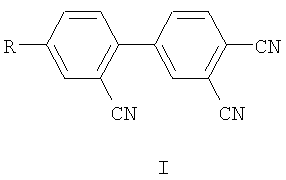
где R=NO2 (Ia), NH2 (Iб), NHCOCH3 (Iв),
которые могут использоваться в качестве промежуточных соединений в синтезе фталоцианинов и их комплексов, перспективных для применения в технике, химической технологии, медицине и др. [Phthalocyanines: Properties and Applications, Eds. C.C.Leznoff, A.B.P.Lever, Vols. 1-4, 1989-1996, VCH, N.Y.; P.Erk and H.Hengelsberg, in Porphyrin Handbook, Eds E.Kadish, K.M.Smith and R.Guilard, Academic Press, New York, 2003, 19, p.105].
В настоящее время известно большое количество соединений, применяемых в качестве исходных полупродуктов для получения фталоцианинов. Однако для обеспечения нужд новой техники требуется синтез новых фталоцианинов различного строения и исходных соединений для их получения. Перспективными в этом отношении представляются арилзамещенные фталонитрилы благодаря широким возможностям структурных преобразований арильного фрагмента с получением разнообразных полезных для получаемых на их основе фталоцианинов свойств.
Ближайшими аналогами новых соединений являются 4-(Х-фенил)фталонитрилы, где X=пара-Cl Br, СН3 (С.А.Михаленко, Е.А.Лукьянец, ЖОХ, 1969, 39, №9, 2129), мета-CF3 (S.Vagin, M.Hanack, Eur. J. Org. Chem, 2004, 600), пара-N(CH3)2 [T.Sigimori, J.Nojima, T.Ozawa, M.Handa, K.Kasuga, Chem. Lett, 2004, 33, 1014]. Общим недостатком этих аналогов является то, что присутствующие в фенильном фрагменте заместители предоставляют весьма ограниченные возможности дальнейших преобразований этого фрагмента для целенаправленного синтеза фталоцианинов с заданными свойствами. Эта ограниченность может быть преодолена введением в фенильный фрагмент таких заместителей, как нитро- и аминогруппа, которые подвержены разнообразным модификациям как таковые, а аминогруппа как сильный электронодонорный заместитель активирует бензольное кольцо для дальнейших преобразований с помощью реакций электрофильного замещения и всевозможных гетероциклизаций.
Задачей технического решения является создание нового соединения, которое может найти применение в качестве промежуточного в синтезе различных фталоцианинов.
Поставленная задача решается новыми соединениями общей формулы I:
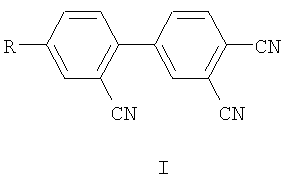
где R=NO2 (Ia), NH2 (Iб), NHCOCH3 (Iв)
как потенциальных исходных соединений в синтезе соответствующих замещенных фталоцианинов, а также полупродуктов при получении других замещенных фталонитрилов и производных фталевых кислот с использованием известных реакций по нитро-, амино- и ацетиламиногруппе. Дополнительные возможности в этом отношении предоставляют находящиеся в орто-положении к фенильному радикалу нитрильные группы.
Эти соединения получают в результате осуществления следующей последовательности реакций: нитрование известного 2,3',4'-трицианодифенила формулы II [Е.В.Пантелеева, Т.А.Ваганова, Е.А.Лукьянец, В.Д.Штейнгарц, ЖОрХ, 2006, 42, 1301-1309.]
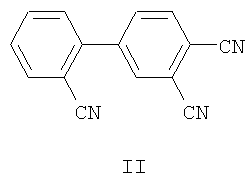
концентрированной азотной кислотой с образованием 4-нитро-2,3',4'-трицианодифенила (выход технического продукта 86%, аналитически чистого - 50%); восстановление соответствующего нитродифенила до 4-амино-2,3'4'-трицианодифенила; N-Ацетилирование 4-амино-2,3',4'-трицианодифенила. Нитрование проводят при выдерживании 2,3',4'-трицианодифенила в концентрированной азотной кислоте при комнатной температуре в течение 87 часов, в том числе при перемешивании 24 часа. 4-Нитро-2,3',4'-трицианодифенил восстанавливают до 4-амино-2,3',4'-трицианодифенила цинком при кипячении в смеси водного изопропилового спирта с ацетоном в присутствии уксусной кислоты в течение 25 часов (выход 67%, СОВ 95%). N-Ацетилирование 4-амино-2,3',4'-трицианодифенила осуществляют действием уксусного ангидрида при 100°С (выход 57%).
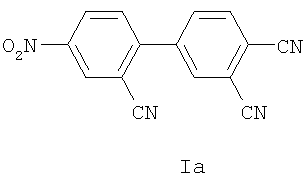
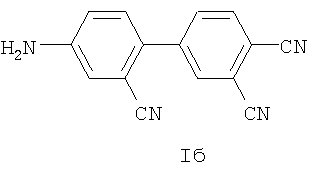
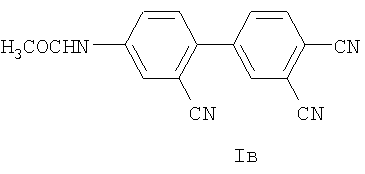
В ИК спектре соединений Iа и Iб присутствуют полосы, характерные для соответствующих функциональных групп: 1530 см-1 и 1353 см-1 (NO2), 2228-2235 см-1 (C≡N), 3468 см-1 и 3383 см-1 (NH2).
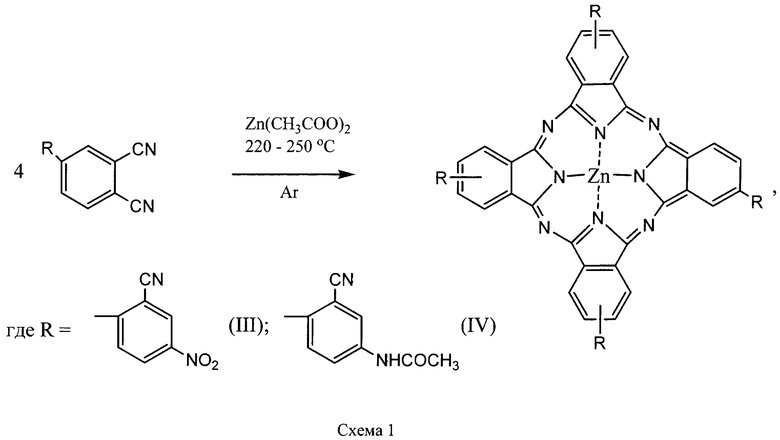
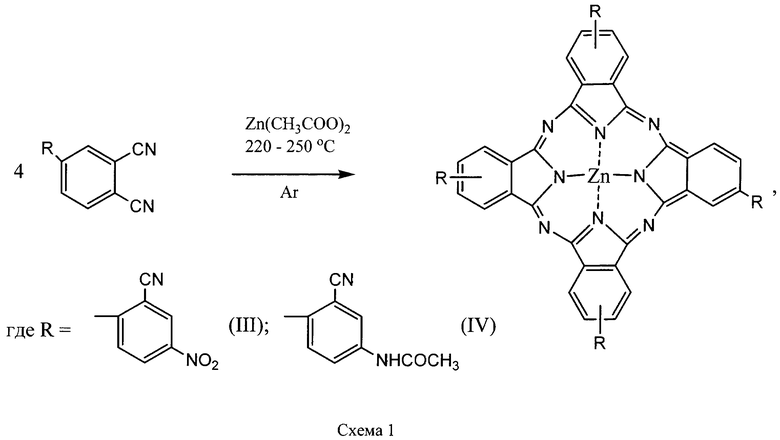
Применимость заявляемых соединений для синтеза фталоцианинов иллюстрируется получением фталоцианиновых комплексов цинка из 4-нитро-2,3',4'-трицианодифенила и 4-ацетиламино-2,3',4'-трицианодифенила, получаемого ацетилированием 4-амино-2,3',4'-трицианодифенила, что является примером использования аминогруппы для модификации соединения с целью придания ему свойств, необходимых для применения в качестве «строительного блока» при сборке фталоцианинового остова. Тетра-(2-циано-4-нитрофенил)фталоцианин цинка и тетра-(2-циано-4-ацетиламино)фталоцианин цинка получены в реакциях 4-нитро-2,3',4'-трицианодифенила и 4-ацетиламино-2,3',4'-трициандифенила, соответственно, с ацетатом цинка по схеме 1.
Изобретение иллюстрируется следующими примерами.
Пример 1. Получение 4-нитро-2,3',4'-трицианодифенила. В плоскодонную колбу емкостью 50 мл, снабженную магнитной мешалкой и хлоркальциевой трубкой, помещают 30 мл концентрированной азотной кислоты (d=1.5 г/см3). Смесь охлаждают до 0°C и при перемешивании вносят 1.77 г 2,3',4'-трицианодифенила, полученного по методике [Е.В.Пантелеева, Т.А.Ваганова, Е.А.Лукьянец, В.Д.Штейнгарц, ЖОрХ, 2006, 42, 1301-1309]. Дают смеси нагреться до комнатной температуры и выдерживают 87 ч с периодическим перемешиванием (~24 ч.). Реакционную массу выливают на 400 г измельченного льда. Осадок отделяют на плотном тканевом фильтре, промывают водой до pH 6 и сушат на воздухе. Получают 1.82 г мелких кристаллов бледно-желтого цвета, содержание основного вещества по данным хромато-масс-спектрометрии составляет 92% (выход 86%), т.пл. 180-181°C.
Кипячением сырого продукта в этиловом спирте (60 мл) с последующим фильтрованием и повторением процедуры со свежей порцией спирта (30 мл) получают 1.2 г индивидуального 4-нитро-2,3',4'-трицианодифенила (выход 50%), т.пл. 198-199°C. ИК спектр, KBr, ν, см-1: 1530 и 1353 см-1 (NO2), 2235 (C≡N), 3043-3097 (СНаром). Спектр ЯМР 1Н (300 МГц, DMCOd6 δ, м.д.): 8.02 д.д (1Н, Н6 JHH oрто 8,5;
JHH пара≤0.8 Гц,), 8.26 д.д (1H, Н6' JHH орто 8,0; JHH мета 1.2 Гц,), 8.39 д.д (1H, Н5' JHH орто 8,0; JHH пара≤0.8 Гц,), 8.54 д (1Н, Н2' JHH мета 1.2 Гц,), 8.64 д.д (1Н, Н5 JHH орто 8,5; JHH мета 2.2 Гц,), 8.94 д.д (1H, Н3 JHH мета 2.2; JHH пара≤0.8 Гц). ЯМР13C (200 МГц) в DMCOd6: δ, м.д.=147.7 (С4), 146.4 (С1), 141.1 (С1'), 134.4 (С6'), 134.4 (С5'), 134.4 (С2'), 132.1 (С6), 128.9 (С5), 128.2 (С3), 116.2 (С3'или С4'), 115.6 (C≡N), 115.5 (C≡N), 115.3 (C≡N), 115.6 (С4'или С3'), 112.2 (С2) м.д. Найдено: М 274.05214. C15H6N4O2. Вычислено: М 274.04907.
Пример 2. Получение 4-амино-2,3',4'-трицианодифенила. К смеси 5.94 г цинковой пыли, 2.86 г ледяной уксусной кислоты, 1.70 г воды, 20 мл изопропилового спирта и 10 мл ацетона при перемешивании добавляют 1.82 г 4-нитро-2,3',4'-трицианодифенила (СОВ 92%) и выдерживают 25 ч при кипячении с обратным холодильником. Горячую массу фильтруют через бумажный фильтр, остаток на фильтре промывают кипящим изопропиловым спиртом (3×50 мл). Из объединенного фильтрата удаляют растворитель на ротационном испарителе, остаток переносят на тканевый фильтр и последовательно промывают 0.1 М водным раствором поташа, затем водой до pH 6, сушат на воздухе до постоянного веса. Продукт из остатка (4.54 г) экстрагируют хлористым метиленом, после удаления которого из экстракта получают 1.08 г светло-желтых кристаллов, содержащих по данным ПМР 95% целевого амина с т.пл. 278-279°C (выход 67%). Возгонкой (240-260°C/10 мм рт.ст.) получают 4-амино-2,3',4'-трицианодифенил, т.пл. 284-285°C. ИК-спектр, KBr, ν, см-1: 3468 и 3383 (NH2), 2228 (C≡N). Спектр ЯМР 1Н (400 МГц, (CD3)2CO δ, м.д.): 7.06 д.д (1H, Н5, JHH орто 8.6; JHH мета 2.5 Гц), 7.12 д (1Н, Н3, JHH мета 2.5 Гц), 7.44 д (1H, Н6, JHH орто 8.6 Гц), 8.07 д.д (1Н, Н6' JHH орто 8.2; JHH мета 1.8 Гц), 8.16 д (1H, Н5' JHH орто 8.2; JHH пара 0.5 Гц), 8.21 д (1H, Н2' JHH мета 1.8; JHH пара 0.5 Гц), 5.81 с (2Н, NH2). ЯМР 13C (300 МГц) в DMCOd6: δ, м.д. 150.1 (С4), 143.6 (С1'), 134.1 (С5'), 133.4 (С6'), 133.3 (С2'), 131.5 (С1), 126.7 (С6), 118.6 (С5), 118.3 (С3), 117.5 и (С3'), 116.0 (C≡N), 115.8 (C≡N), 115.0 (C≡N), 112.7 (С4'), 110.5 (С2). Найдено: M+ 244.07517. C15H8N4. Вычислено: 244.07489. Найдено: С 73.21; Н 3.12; N 22.66. Вычислено: С 73.75; Н 3.31; N 22.94.
Пример 3. Получение 4-ацетиламино-2,3',4'-трицианодифенила. Раствор 4-амино-2,3',4'-трициандифенила (0.050 г) и уксусного ангидрида (0.220 г) в ДМСО (1.5 мл) выдерживали 10 ч при 100°C в атмосфере аргона, затем охлаждали и добавляли воду (8 мл). Осадок отделяли фильтрованием, промывали водой (2 мл) и сушили на воздухе, выход - 0.034 г (57%). Спектр ЯМР 1Н (300 МГц, CD3COCD3/DMCOd6: δ, м.д.): 7.68 д (1Н, Н6, JHH орто 8.5 Гц), 7.97 д (1Н, Н5, 5 JHH орто 8.5 Гц), 8.15 д.д (1H, Н6', JHH орто 8.2; JHH мета 1.6 Гц), 8.23 д (1Н, Н5' JHH орто 8.2 Гц), 8.28 уш. с (1H, Н3), 8.32 д (1H, Н2', JHH мета 1.6 Гц), 10.34 уш. с (1Н, NH), 2.12 с (3Н, СН3). ЯМР 13C (300 МГц, CD3COCD3/DMCOd6: δ, м.д.) 169.2 (С=O), 143.1, 141.0, 134.8, 134.2, 133.9, 133.8, 131.0, 123.5, 123.2, 117.7, 115.6, 115.5, 115.4, 114.6, 111.0, 23.6 (СН3). Найдено: M-H+ 285.0770. C17H9N4O. Вычислено: 285.0776.
Пример 4. Получение тетра-(2-циано-4-нитрофенил)фталоцианина цинка.
Смесь 4-нитро-2,3',4'-трицианодифенила (0.053 г) и Zn(CH3COO)2H2O (0.012 г) выдерживают 1 ч при 220-240°C в атмосфере аргона, охлаждают, промывают водой (3 мл), этанолом (3 мл), диэтиловым эфиром (1.5 мл) и очищают остаток методом ТСХ (силикагель, ДМФА/этанол, объемное соотношение - от 1/2 до 1/0), элюирование осуществляют три раза, выход - 0.033 г (62%). Полученный темно-зеленый порошок слабо растворим в ДМФА и ДМСО, нерастворим в спирте, эфире, хлороформе. ИК спектр, KBr, ν, см-1: 2231 (C≡N), 1526 и 1351 (NO2). УФ спектр, ДМСО: lg λмакс, нм
(lg ε) 350 (0.49), 650 (0.45), 685 (0.43). Спектр ЯМР 1Н (300 МГц, DMCOd6, δ, м.д.): 8.2-9.6. Масс-спектр, m/z для аддукта с Сl-: найдено: 1195.088. C60H24N16O8ZnCl, вычислено: 1195.094.
Пример 5. Получение тетра-(2-циано-4-ацетиламино)фталоцианина цинка.
Смесь 4-ацетиламино-2,3',4'-трициандифенила (0.030 г) и Zn(CH3COO)2H2O (0.006 г) выдерживают 1 ч при 230-250°C в атмосфере аргона, охлаждают и очищают методом ТСХ (силикагель, ДМФА/диэтиловый эфир, объемное соотношение от 1/4 до 1/0), элюирование осуществляют четыре раза, выход - 0.035 г (38%). Полученный синий порошок хорошо растворим в ДМФА и ДМСО, нерастворим в спирте, эфире, хлороформе. ИК-спектр, КВг, ν, см-1: 2225 (C≡N). УФ спектр, ДМСО: lg λмакс, нм
(lg ε) 276 (1.31), 355 (1.09), 648 (0.63), 648 (0.63) 688 (0.92). Спектр ЯМР 1Н (300 МГц, DMCOd6, δ, м.д.): 10.5 уш. с, 10.4 уш. с, 8.8-9.5 (4Н, NH); 6.8-8.7 (24Н, СН); 1.9-2.4 (12Н, СН3). Масс-спектр, m/z для аддукта с Cl-: найдено: 1243.222. C68H40N16O4ZnCl, вычислено: 1243.240.
Таким образом, синтезированы новые производные фталонитрила, которые могут быть использованы в синтезе различных, в том числе новых фталоцианинов.
| название | год | авторы | номер документа |
|---|---|---|---|
| АЗОСОЕДИНЕНИЯ НА ОСНОВЕ 4-АМИНО-2,3',4'-ТРИЦИАНОДИФЕНИЛА | 2011 |
|
RU2479573C1 |
| Замещенные [(3-нитро-1Н-1,2,4-триазол-1-ил)-NNO-азокси]фуразаны и способ их получения | 2020 |
|
RU2747110C1 |
| 16-(1,2,4-ОКСАДИАЗОЛ-3-ИЛ)-15,16-ЭПОКСИЛАБДАНОИДЫ, ОБЛАДАЮЩИЕ ЦИТОТОКСИЧЕСКОЙ АКТИВНОСТЬЮ ПО ОТНОШЕНИЮ К ОПУХОЛЕВЫМ КЛЕТКАМ ЧЕЛОВЕКА | 2011 |
|
RU2473550C1 |
| СПОСОБ ПОЛУЧЕНИЯ СЛОЖНЫХ ЭФИРОВ 4-(3,4-ДИАМИНОФЕНОКСИ)БЕНЗОЙНОЙ КИСЛОТЫ | 2009 |
|
RU2409555C1 |
| Замещенные [(3,4-динитро-1H-пиразол-1-ил)-NNO-азокси]фуразаны и способ их получения | 2020 |
|
RU2756321C1 |
| Способ совместного получения 1-(2-амино-4-R-фенил)- и 2-(2-амино-4-R-фенил)бензотриазолов | 2023 |
|
RU2825731C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРГИДРАТА 1,3-БИС(3,4-ДИАМИНОФЕНОКСИ)БЕНЗОЛА | 2010 |
|
RU2439052C1 |
| Способ получения гидрохлорида 2-(1,2,3-тиадиазол-4-ил)бензиламина | 2023 |
|
RU2825395C1 |
| Способ синтеза 1-(2-амино-4-нитрофенил)-2-R-бензимидазолов | 2024 |
|
RU2825732C1 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛА, ИСПОЛЬЗУЕМЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗЫ | 2001 |
|
RU2340611C2 |
Изобретение относится к органической химии, а именно к производным 2,3',4'-трицианодифенила общей формулы I:
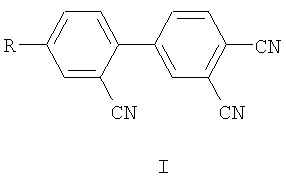
где R=NO2 (Ia), NH2 (Iб), NHCOCH3 (Iв).
Технический результат - получение новых соединений, которые могут найти применение в синтезе соответствующих замещенных фталоцианинов. 1 ил.
Производные 2,3',4'-трицианодифенила общей формулы I
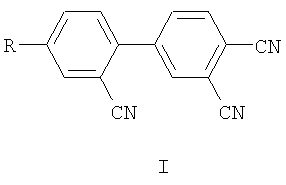
где R=NO2 (Ia), NH2 (Iб), NHCOCH3 (Iв).
| SIGIMORI T | |||
| et al | |||
| Chem | |||
| Lett | |||
| Способ сопряжения брусьев в срубах | 1921 |
|
SU33A1 |
| Способ получения 4-алкокси-4 цианодифенилов | 1976 |
|
SU608800A1 |
| Способ получения 4-(N @ ,N @ -диметилгидразино)-1,5,5-трицианоциклопентенов | 1988 |
|
SU1583410A1 |
Авторы
Даты
2010-09-10—Публикация
2009-03-05—Подача