Текст описания приведен в факсимильном виде.





































































































| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ И ФАРМАКОЛОГИЧЕСКИЕ КОМПОЗИЦИИ ДЛЯ ЗАЖИВЛЕНИЯ РАН | 2004 |
|
RU2392959C1 |
| СПОСОБЫ И ФАРМАКОЛОГИЧЕСКИЕ КОМПОЗИЦИИ ДЛЯ ЗАЖИВЛЕНИЯ РАН | 2004 |
|
RU2491952C2 |
| СПОСОБЫ И ФАРМАКОЛОГИЧЕСКИЕ КОМПОЗИЦИИ ДЛЯ ЗАЖИВЛЕНИЯ РАН | 2004 |
|
RU2359694C2 |
| ИНДОЛИЛМАЛЕИМИДНЫЕ ПРОИЗВОДНЫЕ | 2005 |
|
RU2373201C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ УСКОРЕНИЯ ЗАЖИВЛЕНИЯ РАН | 2004 |
|
RU2358753C2 |
| ПРИМЕНЕНИЕ АДИПОЦИТОВ, ПРЕАДИПОЦИТОВ И СТВОЛОВЫХ КЛЕТОК ДЛЯ ИНДУКЦИИ ИЛИ УСКОРЕНИЯ ЗАЖИВЛЕНИЯ РАНЫ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ИХ | 2009 |
|
RU2419441C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ОТНОСЯЩИЕСЯ СПОСОБЫ | 2008 |
|
RU2502520C2 |
| СПОСОБЫ РЕГУЛЯЦИИ МЕДИАТОРОВ ВОСПАЛЕНИЯ И ПЕПТИДЫ, ИСПОЛЬЗУЕМЫЕ В НИХ | 2007 |
|
RU2429004C2 |
| СПОСОБ ИДЕНТИФИКАЦИИ ИНГИБИТОРОВ ИЛИ АГОНИСТОВ ПРОТЕИНКИНАЗЫ IRS | 2004 |
|
RU2340898C2 |
| МАКРОГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ | 2001 |
|
RU2275373C2 |

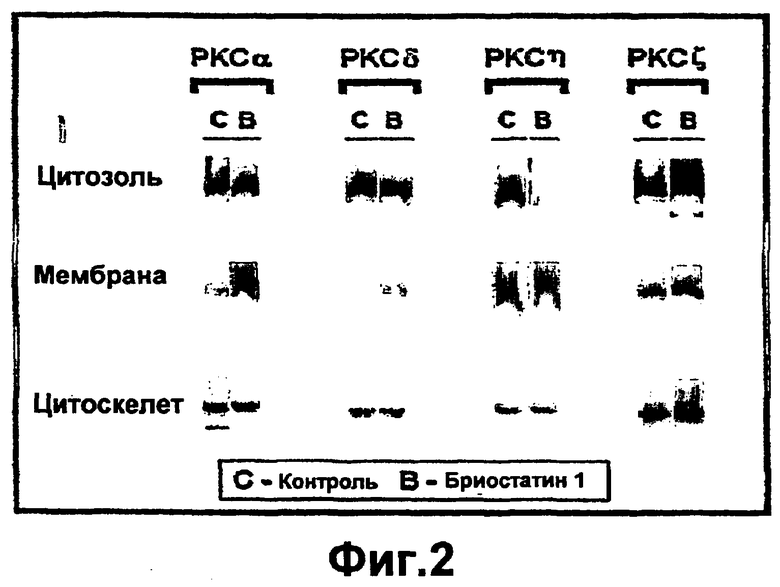


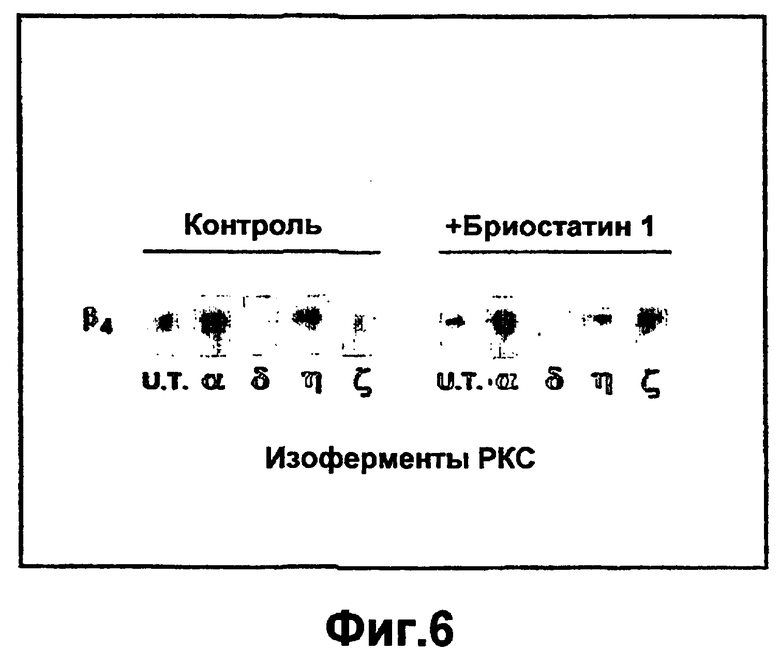









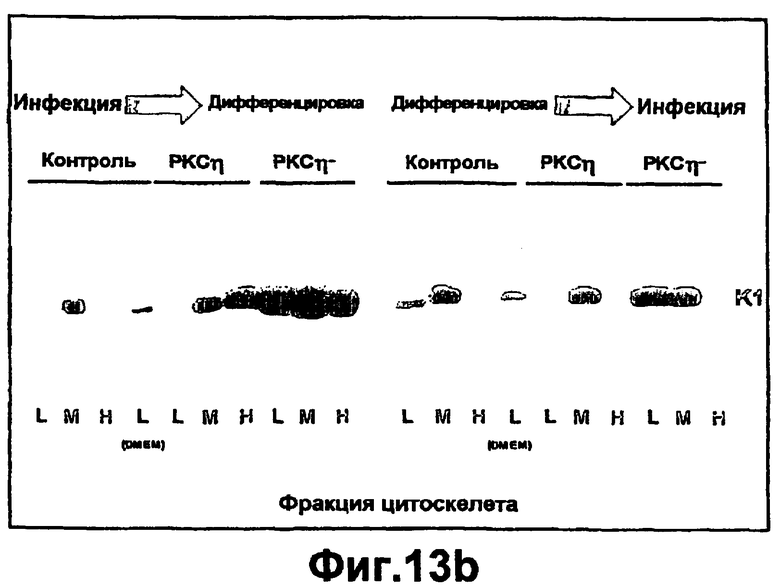


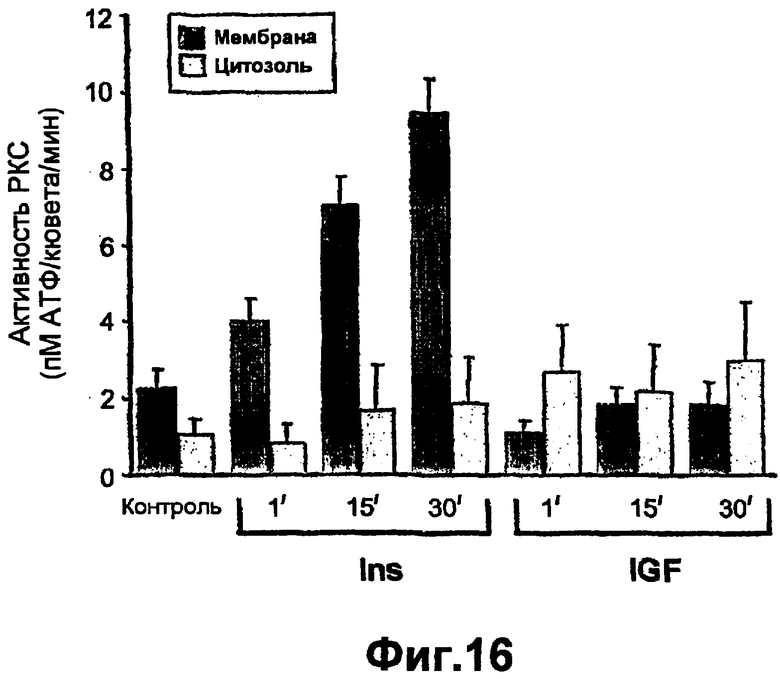
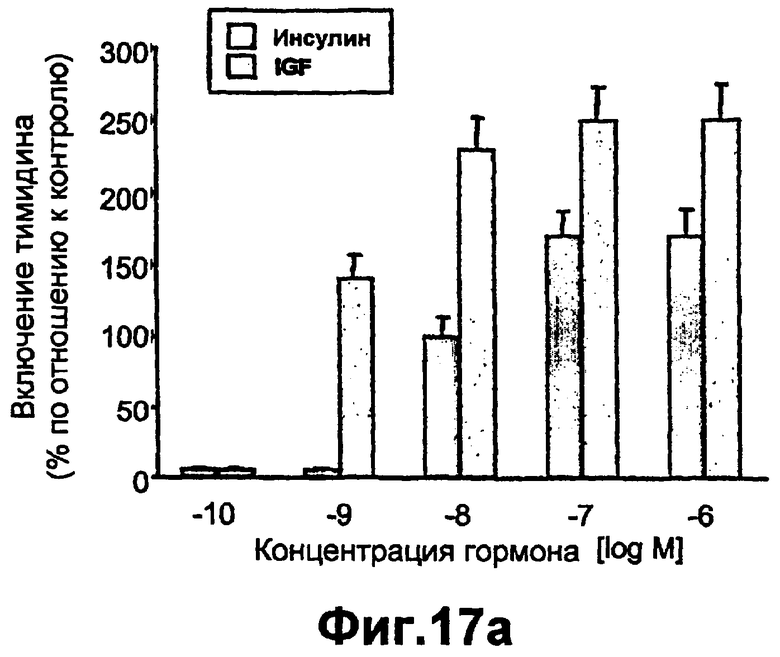


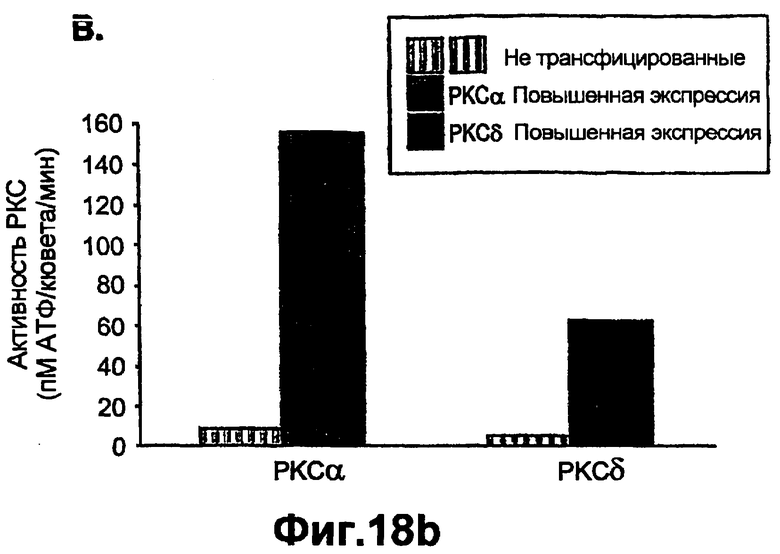




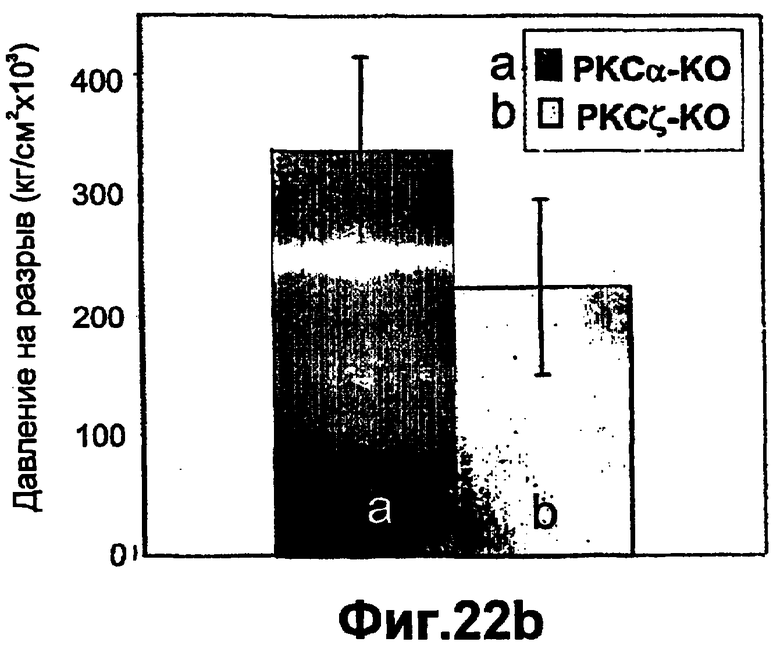


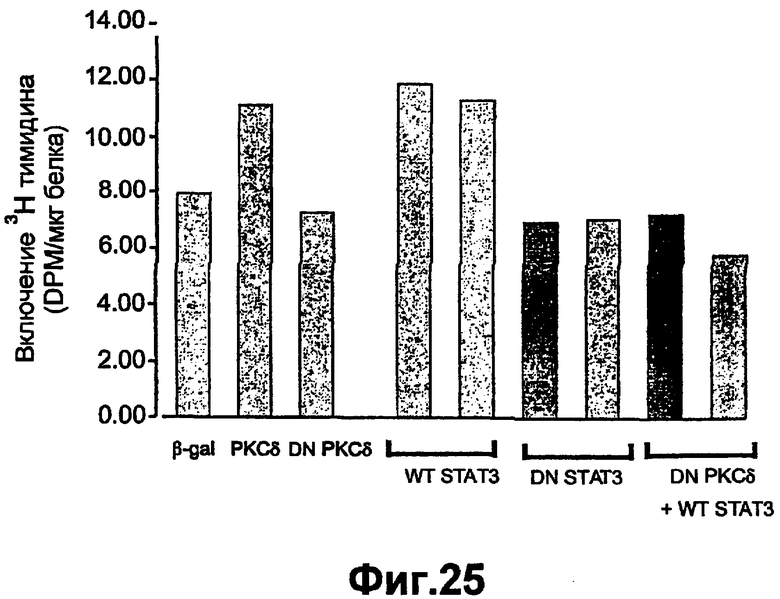

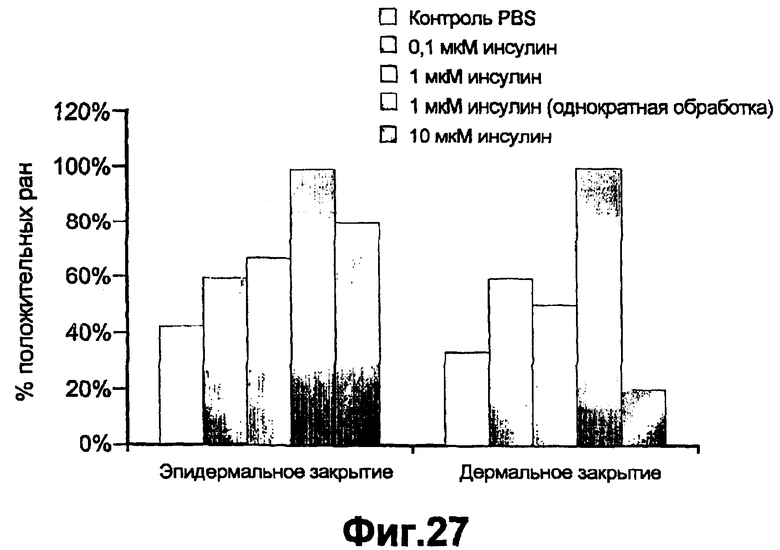
































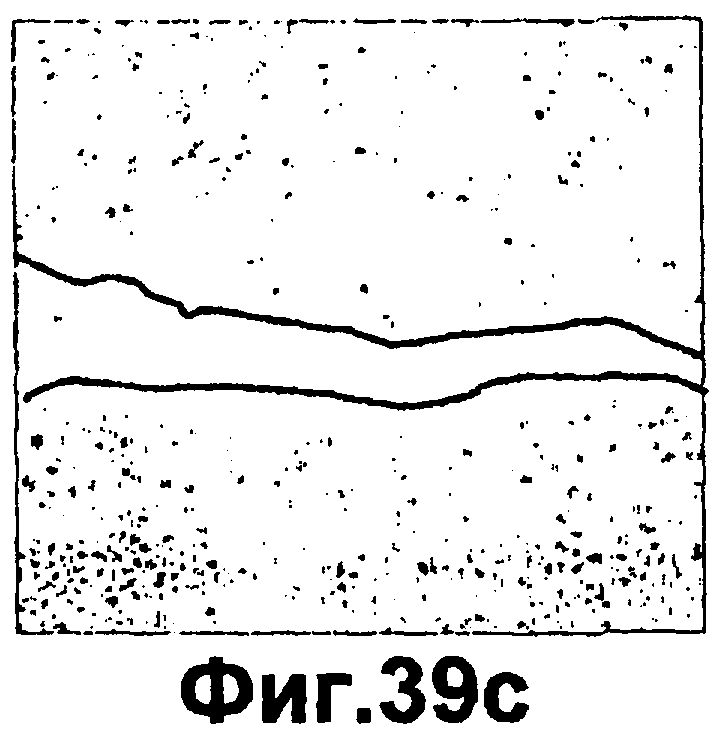

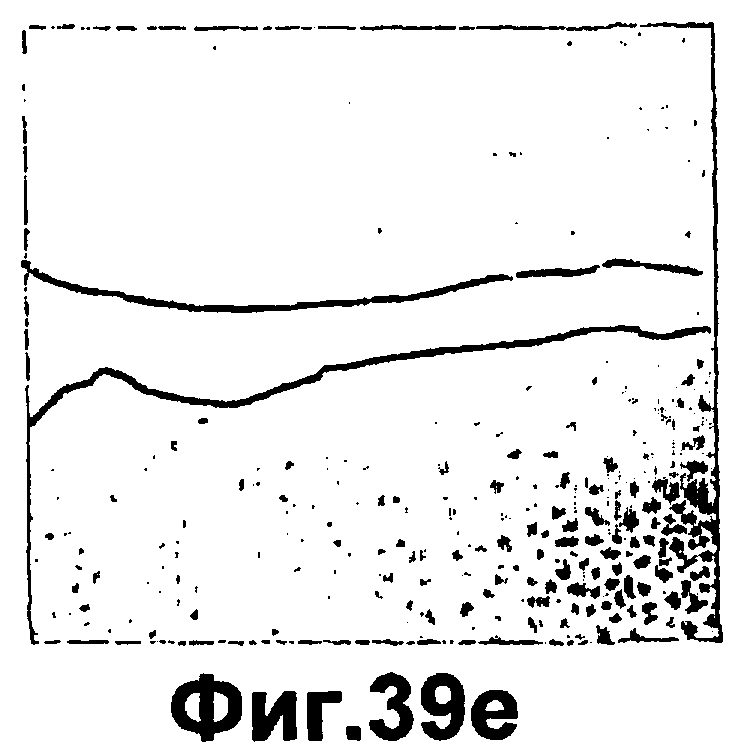
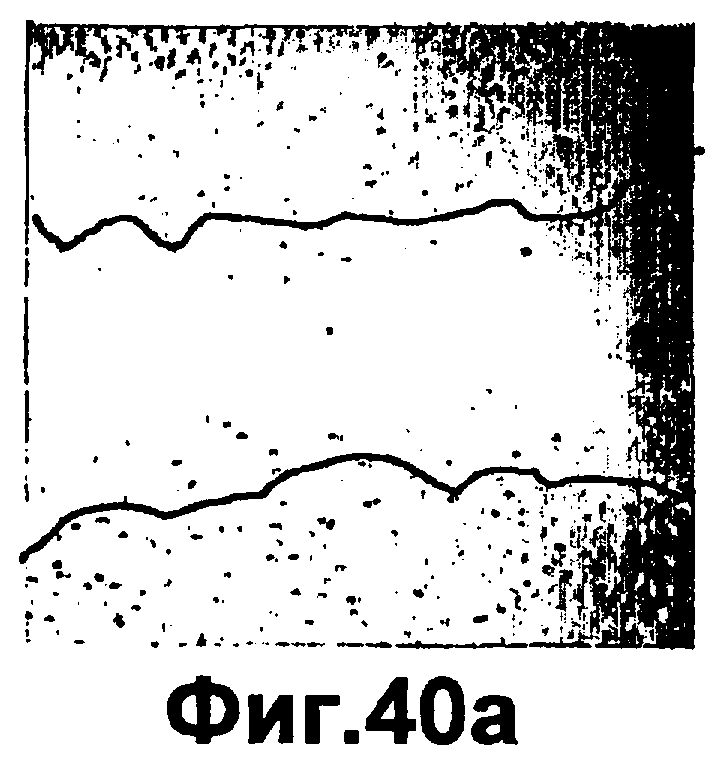




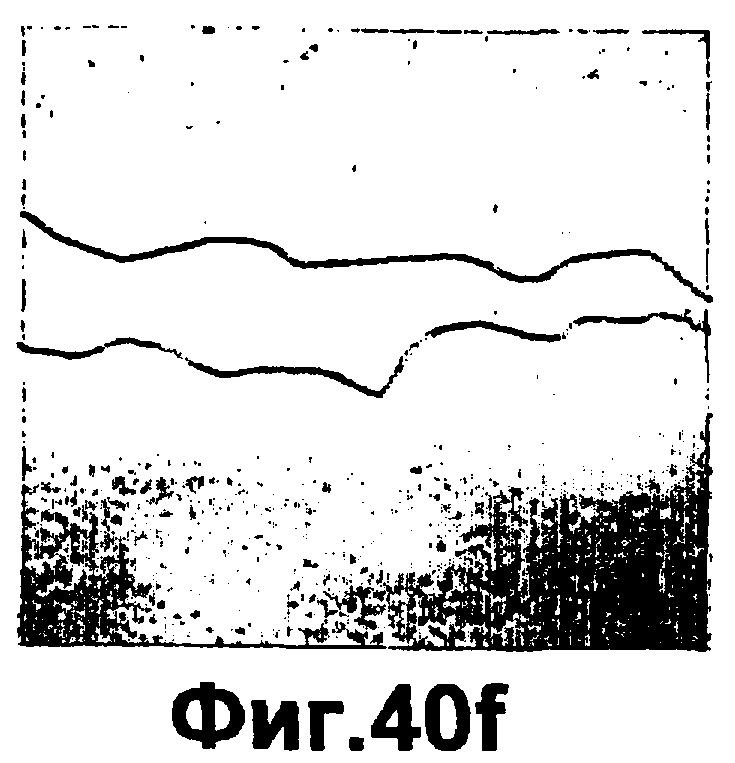




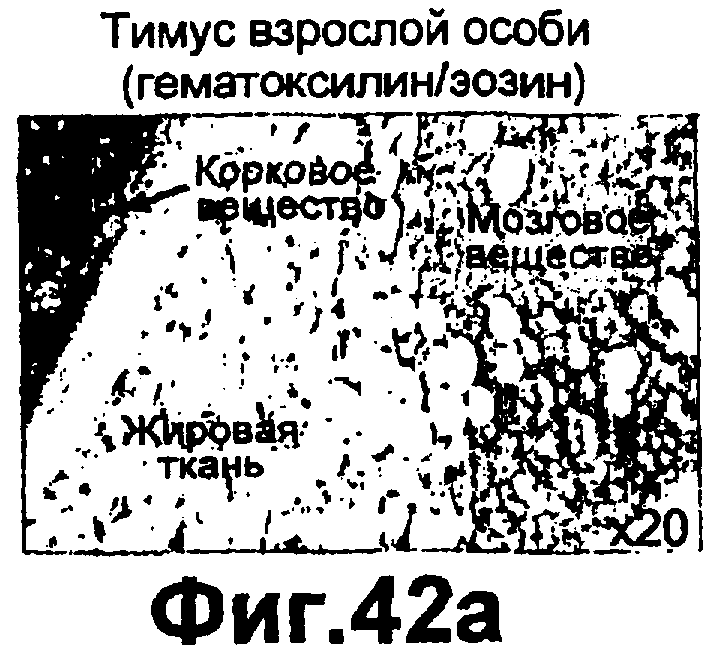







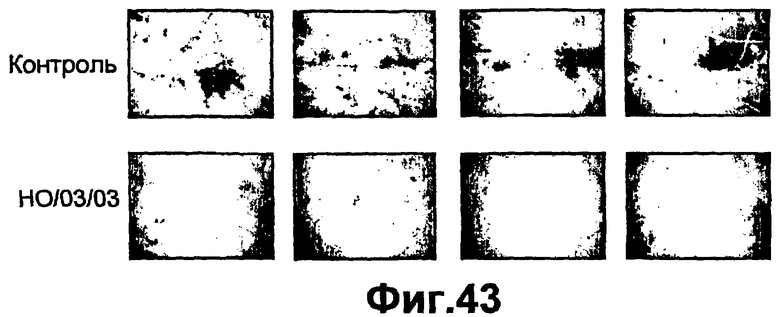
Группа изобретений относится к медицине и может быть использована при лечении ран эпителия различного генеза. Для этого в рану вводят средство, вызывающее модуляцию экспрессии и/или активности одной изоформы РКС и терапевтически эффективное количество одного дополнительного средства, выбранного из группы, состоящей из инсулина, фактора роста, адипокина, РКС RACK и GW9662. Предложены и соответствующие фармацевтические композиции для введения в рану, содержащие помимо терапевтически эффективных количеств необходимых веществ фармацевтически приемлемый носитель. Изобретения позволяют обеспечить ускорение процессов заживления ран эпителия за счет выявленного синергического действия указанных веществ. 5 н. и 55 з.п. ф-лы, 43 ил., 10 табл.
1. Способ индукции процесса заживления раны эпителия, включающий введение в рану терапевтически эффективного количества инсулина и, по меньшей мере, одного дополнительного средства, обладающего синергическим действием с указанным инсулином, для индукции процесса заживления раны эпителия.
2. Способ по п.1, где указанный инсулин является рекомбинантным или имеет природное происхождение.
3. Способ по п.1, где указанное терапевтически эффективное количество инсулина включает концентрацию инсулина, находящуюся в диапазоне от 0,1 до 10 мкМ.
4. Способ по п.1, где указанное, по меньшей мере, одно дополнительное средство представляет собой ингибитор РКСα, фактор роста или РКСδ RACK.
5. Способ по п.4, где указанное дополнительное средство представляет собой ингибитор РКСα.
6. Способ по п.4, где указанное дополнительное средство представляет собой ингибитор РКС N-миристоилированный пептид псевдосубстрата РКСα.
7. Способ по п.4, где указанный фактор роста представляет собой PDGF, EGF, TGFβ, KGF, ECGF и IGF1.
8. Способ по любому из пп.1-7, где указанная рана эпителия выбрана из группы, состоящей из язвы, раны, связанной с диабетом, ожога, солнечного ожога, застарелой раны кожи, изъязвленной раны роговицы, раны при воспалительном заболевании желудочно-кишечного тракта, раны при воспалительном заболевании кишечника, раны при болезни Крона, язвенном колите, геморрое, раны при буллезном эпидермолизе, кожно-нарывной раны, псориатической раны, раны кожи животного, диабетической раны животного, раны при ретинопатии, раны полости рта (мукозит), раны вагинальной слизистой оболочки, раны при заболевании десны, рваной раны, раны хирургического разреза и послеоперационной спаечной раны.
9. Способ по п.8, где указанная язва выбрана из группы, состоящей из диабетической язвы, пролежня, венозной язвы, язвы желудка и язвы, связанной с ВИЧ.
10. Способ по любому из пп.1-7, где указанный инсулин и, по меньшей мере, одно из дополнительных средств содержатся в фармацевтической композиции, адаптированной для местного применения.
11. Способ по п.10, где указанная фармацевтическая композиция выбрана из группы, состоящей из водного раствора, геля, крема, пасты, примочки, аэрозоля, суспензии, порошка, коллоидного раствора, бальзама и мази.
12. Способ по п.11, где указанная фармацевтическая композиция включает твердую основу.
13. Способ индукции процесса заживления раны эпителия, включающий модуляцию экспрессии и/или активности, по меньшей мере, одной изоформы РКС в колонизирующих область раны эпителия дермальных клетках и введение в указанные дермальные клетки терапевтически эффективного количества, по меньшей мере, одного дополнительного средства, выбранного из группы, состоящей из инсулина, фактора роста, адипокина, РКС RACK и GW9662 с тем, чтобы таким образом ускорить процесс заживления раны эпителия.
14. Способ по п.13, где указанные дермальные клетки представляют собой фибробласты или кератиноциты.
15. Способ по п.14, где указанная изоформа РКС выбрана из группы, состоящей из РКСα, РКСβ, РКСδ, РКСε, РКСη и РКСζ.
16. Способ по п.14, где указанный фактор роста выбран из группы, состоящей из IL-6, KGF и TNFα, а указанный адипокин представляет собой адипсин или адипонектин.
17. Способ по п.13, где экспрессия и/или активность указанной изоформы РКС ингибирована.
18. Способ по п.17, где ингибирование указанной изоформы РКС достигают посредством молекулы малой интерферирующей РНК (миРНК) или посредством инфекции указанных дермальных клеток аденовирусной конструкцией с доминантно-негативной РКС.
19. Способ по п.13, где экспрессия и/или активность указанной изоформы РКС активирована.
20. Способ по п.19, где активации указанной изоформы РКС достигают посредством инфекции указанных дермальных клеток аденовирусной конструкцией с изоформой РКС дикого типа.
21. Способ по п.18, где указанная изоформа РКС представляет собой РКСα, а указанное дополнительное средство представляет собой инсулин, TNFα, адипсин или РКСδ RACK.
22. Способ по п.18, где указанная изоформа РКС представляет собой РКСβ, а указанное дополнительное средство представляет собой инсулин, KGF, IL-6 или GW9662.
23. Способ по п.18, где указанная изоформа РКС представляет собой РКСζ, а указанное дополнительное средство представляет собой инсулин, IL-6, TNFα, KGF или адипонектин.
24. Способ по п.20, где указанная изоформа РКС представляет собой РКСδ, а указанное дополнительное средство представляет собой адипсин.
25. Способ по п.13, включающий введение в указанные дермальные клетки терапевтически эффективных количеств вещества, способного модулировать экспрессию и/или активность, по меньшей мере, одной указанной изоформы РКС и указанного дополнительного средства.
26. Способ по п.25, где указанное вещество представляет собой ингибитор РКСα, предпочтительно N-миристоилированный пептид псевдосубстрата РКСα.
27. Способ по п.26, где указанное дополнительное средство представляет собой инсулин.
28. Способ по п.27, включающий введение в указанные дермальные клетки терапевтически эффективных количеств N-миристоилированного пептида псевдосубстрата РКСα и инсулина.
29. Способ по п.25, где указанное вещество представляет собой ингибитор РКСβ; ингибитор РКСη, предпочтительно N-миристоилированный пептид псевдосубстрата РКСη или ингибитор РКСζ, предпочтительно N-миристоилированный пептид псевдосубстрата РКСζ.
30. Способ по п.25, где указанное вещество представляет собой активатор РКСδ, предпочтительно инсулин или РКСδ RACK.
31. Способ по любому из пп.13-30, где указанная рана эпителия выбрана из группы, состоящей из язвы, раны, связанной с диабетом, ожога, солнечного ожога, застарелой раны кожи, изъязвленной раны роговицы, раны при воспалительном заболевании желудочно-кишечного тракта, раны при воспалительном заболевании кишечника, раны при болезни Крона, язвенном колите, геморрое, раны при буллезном эпидермолизе, кожно-нарывной раны, псориатической раны, раны кожи животного, диабетической раны животного, раны при ретинопатии, раны полости рта (мукозит), раны вагинальной слизистой оболочки, раны при заболевании десны, рваной раны, раны хирургического разреза и послеоперационной спаечной раны.
32. Способ по п.31, где указанная язва выбрана из группы, состоящей из диабетической язвы, пролежня, венозной язвы, язвы желудка и язвы, связанной с ВИЧ.
33. Способ по любому из пп.25-30, где указанное вещество и дополнительное средство содержатся в фармацевтическом носителе, адаптированном для местного применения.
34. Способ по п.33, где указанная фармацевтическая композиция выбрана из группы, состоящей из водного раствора, геля, крема, пасты, примочки, аэрозоля, суспензии, порошка, коллоидного раствора, бальзама и мази.
35 Способ по п.34, где указанная фармацевтическая композиция включает твердую основу.
36. Фармацевтическая композиция для местного применения для индукции процесса заживления раны эпителия, содержащая терапевтически эффективные количества инсулина и, по меньшей мере, одно дополнительное средство, обладающее синергическим действием с указанным инсулином, и фармацевтически приемлемый носитель.
37. Фармацевтическая композиция по п.36, где указанный инсулин является рекомбинантным или имеет природное происхождение.
38. Фармацевтическая композиция по п.36, где указанное терапевтически эффективное количество инсулина включает концентрацию инсулина, находящуюся в диапазоне от 0,1 до 10 мкМ.
39. Фармацевтическая композиция по п.36, где указанное, по меньшей мере, одно дополнительное средство представляет собой ингибитор РКСα, фактор роста или РКСδ RACK.
40. Фармацевтическая композиция по п.39, где указанное дополнительное средство представляет собой ингибитор РКСα.
41. Фармацевтическая композиция по п.39, где указанное дополнительное средство представляет собой ингибитор РКСα N-миристоилированный пептид псевдосубстрата РКСα.
42. Фармацевтическая композиция по п.39, где указанный фактор роста представляет собой PDGF, EGF, TGFβ, KGF, ECGF и IGF1.
43. Фармацевтическая композиция для местного применения для индукции процесса заживления раны эпителия, содержащая терапевтически эффективные количества вещества, способного к модуляции экспрессии и/или активности, по меньшей мере, одной изоформы РКС и, по меньшей мере, одно дополнительное средство, выбранное из группы, состоящей из инсулина, фактора роста, адипокина, РКС RACK и GW9662, и фармацевтически приемлемый носитель.
44. Фармацевтическая композиция по п.43, где указанная изоформа РКС выбрана из группы, состоящей из РКСα, РКСβ, РКСδ, РКСε, РКСη и РКСζ.
45. Фармацевтическая композиция по п.44, где указанный фактор роста выбран из группы, состоящей из IL-6, KGF и TNFα, а указанный адипокин представляет собой адипсин или адипонектин.
46. Фармацевтическая композиция по п.43, где указанное вещество представляет собой ингибитор изоформы РКС.
47. Фармацевтическая композиция по п.46, где указанный ингибитор изоформы РКС представляет собой ингибитор РКСα, предпочтительно N-миристоилированный пептид псевдосубстрата РКСα.
48. Фармацевтическая композиция по п.46, где указанный ингибитор изоформы РКС представляет собой ингибитор РКСη, предпочтительно N-миристоилированный пептид псевдосубстрата РКСη; или ингибитор РКСζ, предпочтительно N-миристоилированный пептид псевдосубстрата РКСζ.
49. Фармацевтическая композиция по п.46, где указанный ингибитор изоформы РКС представляет собой ингибитор РКСα N-миристоилированный пептид псевдосубстрата РКСα, а указанное дополнительное средство представляет собой инсулин.
50. Фармацевтическая композиция по п.43, где указанное вещество представляет собой активатор изоформы РКС, предпочтительно активатор РКСδ, такой как инсулин или РКСδ RACK.
51. Фармацевтическая композиция индукции процесса заживления раны эпителия, содержащая терапевтически эффективное количество вещества для ингибирования экспрессии или активации, по меньшей мере, одной изоформы РКС, адипокина и фармацевтически приемлемого носителя.
52. Фармацевтическая композиция по п.51, где указанный адипокин представляет собой адипсин или адипонектин.
53. Фармацевтическая композиция по п.51, где указанная изоформа РКС выбрана из группы, состоящей из РКСα, РКСβ, РКСδ, РКСε, РКСη и РКСζ.
54. Фармацевтическая композиция по п.51, где указанное вещество представляет собой ингибитор РКСα.
55. Фармацевтическая композиция по п.51, где указанное вещество представляет собой ингибитор РКСη, предпочтительно N-миристоилированный пептид псевдосубстрата РКСη или ингибитор РКСζ, предпочтительно N-миристоилированный пептид псевдосубстрата РКСζ.
56. Фармацевтическая композиция по п.51, где указанная фармацевтическая композиция включает твердую основу.
57. Фармацевтическая композиция по п.51, где указанный фармацевтически приемлемый носитель разработан для местного применения указанной фармацевтической композиции.
58. Фармацевтическая композиция по п.51, где указанный адипокин представляет собой адипсин.
59. Фармацевтическая композиция по п.51, где указанный адипокин представляет собой адипонектин.
60. Фармацевтическая композиция по п.51, где указанное вещество представляет собой N-миристоилированный пептид псевдосубстрата РКСα.
| US 5591709 A, 07.01.1997 | |||
| ЗАМЕНИТЕЛЬ ЖИВОЙ КОЖИ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СПОСОБ ОБРАБОТКИ ПОВРЕЖДЕНИЙ ЖИВОЙ КОЖИ | 1993 |
|
RU2104039C1 |
| КОМПОЗИЦИИ, СПОСОБЫ СТИМУЛЯЦИИ ЗАЖИВЛЕНИЙ | 1989 |
|
RU2115410C1 |
| ЩИПЦЫ ДЛЯ ОБРЕЗАНИЯ РОГОВ У КРУПНОГО РОГАТОГО СКОТА | 0 |
|
SU209639A1 |
| JP 7316066 A, 05.12.1995, реферат | |||
| US 2002127564 A1, 12.09.2002, реферат, кол.29, 30, 49, 50 | |||
| УСТАНОВКА ДЛЯ ИСПЫТАНИЯ РАБОЧИХ КОЛЕС ТУРБОМАШИНЫ НА ПРОЧНОСТЬ | 1992 |
|
RU2051352C1 |
| Дж.Ф.Лейкок и др | |||
| Основы эндокринологии | |||
| - М.: Медицина, 2000, с.359-368 | |||
| JAMESON J | |||
| et al | |||
| A role for skin gammadelta Т cells in wound repair., Science, 2002 Apr 26; 296(5568):747-9, реферат. | |||
Авторы
Даты
2010-11-27—Публикация
2008-09-29—Подача