Изобретение относится к биотехнологии, генетической инженерии и касается получения мультикопийного плазмидного вектора для интеграции и экспрессии генов.
Одним из наиболее распространенных способов повышения количества целевого продукта при его получении путем микробиологического синтеза является внесение гена, ответственного за синтез продуцируемого вещества в клетку штамма-реципиента и получение целевого продукта путем культивирования сконструированного рекомбинантного штамма. Как правило, для внесения гена в клетку штамма-реципиента используют вектор, содержащий, в частности, экспрессионную кассету (промотор, терминатор транскрипции, селективный маркер) и сайт интеграции.
Известен мультикопийный экспрессионный вектор pNB268 [ATCC 69355] для экспрессии генов в хромосому дрожжей Yarrowia lipolytica, содержащий промотор гена щелочной протеазы XPR2, селективный маркер LEU2, гомологичный участок для интеграции в заданный локус XPR.
Известен (www.invitrogen.com) мультикопийный экспрессионный вектор pPIC9 для экспрессии генов в хромосому дрожжей Pichia pastoris, который содержит в своем составе сильный индуцибильный промотор 5' АОХ1, терминатор транскрипции 3' АОХ1, селективный маркер HIS4, сайт интеграции 3' АОХ1 и ά-амилазный сигнальный пептид. Однако индуктором экспрессии клонируемого гена в данном случае является метанол, что осложняет его технологическое использование.
Для экспрессии генов, кодирующих нетоксичные для Pichia pastoris белки, предложен конститутивный экспрессионный плазмидный вектор pGAPZάA (www.invitrogen.com), содержащий в своем составе промотор GAP, терминатор транскрипции 3' АОХ1, селективный маркер зеоцин, сайт интеграции 3' АОХ1 и ά-амилазный сигнальный пептид. Однако штаммы, полученные при использовании вектора pGAPZάA, как правило, не обладают высокой продуктивностью, что, возможно, связано с низким числом копий сайта интеграции АОХ1 на хромосоме дрожжей Pichia pastoris.
Задачей заявляемого изобретения является расширение арсенала рекомбинантных плазмид для экспрессии в дрожжах Pichia pastoris гена, кодирующего фосфолипазу и рекомбинантных штаммов дрожжей Pichia pastoris, продуцирующих фосфолипазу.
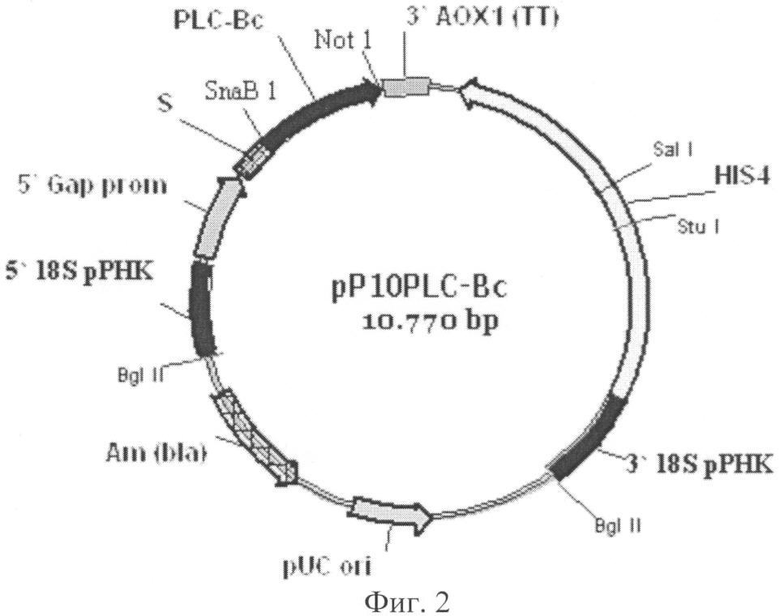
Поставленная задача решена путем конструирования рекомбинантной плазмиды pP10PLC-Bc для экспрессии в дрожжах Pichia pastoris гена из Bacillus cereus, ответственного за синтез фермента фосфолипазы С PLC-Bc. Сконструированная плазмида имеет размер 10770 п.о. и состоит из следующих элементов (фиг.2):
1) фрагмент 5' 18S рРНК: 1-269 п.о.;
2) промотор GAP: 270-1026 п.о.;
3) ά-амилазный сигнальный пептид: 1029-1295 п.о.;
4) ген фосфолипазы PLC-Bc; 1304-2054 п.о.;
5) терминатор транскрипции 3' АОХ1: 2088-2421 п.о.;
6) HIS4 ORF: 3279-5813 п.o.;
7) фрагмент 3' 18S рРНК: 6085-6774 п.о.;
8) pUC ori: 7974-8648 п.o.;
9) ген резистентности к ампициллину: 9448-10308 п.о.
Задача решена также путем конструирования штамма Pichia pastoris-PLC-Bc-1 ВКПМ Y-3359 - продуцента фосфолипазы С PLC-Bc.
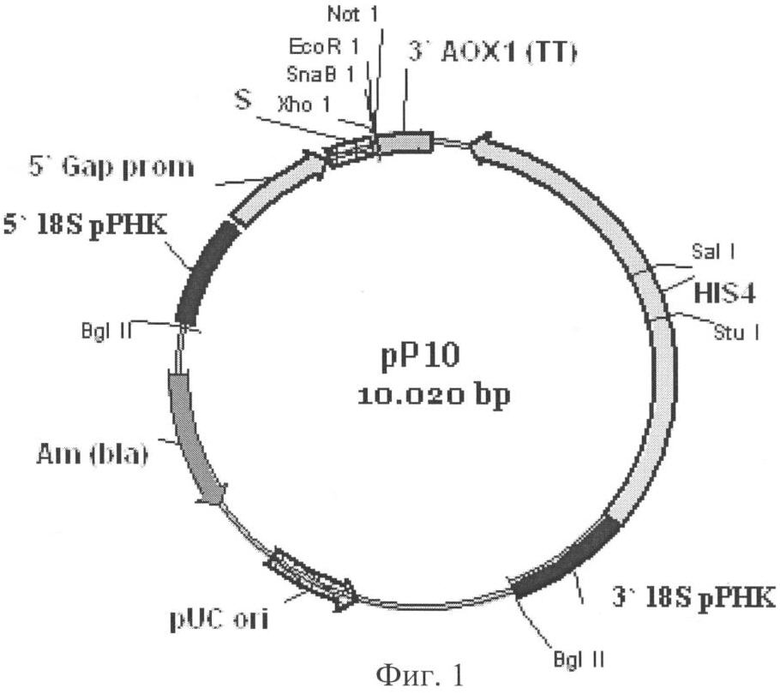
Для получения рекомбинантной плазмиды используют вектор рР10, который в качестве сайта интеграции содержит последовательность ДНК, кодирующую область 18S рРНК, в качестве селективного маркера для отбора трансформантов в клетках E.coli содержит селективный маркер bla, в качестве сайта начала репликации содержит pUC ori, в состав экспрессионной кассеты входит промотор GAP, терминатор транскрипции АОХ1, селективный маркер HIS4, а в качестве сигнального пептида вектор содержит ά-амилазный сигнальный пептид. Вектор рР10 (фиг.1) конструируют следующим образом.
Фрагменты ДНК, кодирующие промотор GAP и область 18S рРНК, амплифицируют полимеразной цепной реакцией. Амплифицированную последовательность GAP промотора по тупым концам лигируют в вектор pPIC9 (Invitrogen), из которого по сайтам BglII и BamHI предварительно вырезают последовательность 5' АОХ1 промотора. Получают вектор pPIC9G.
Амплифицированную последовательность гена, кодирующего область 18S рРНК по тупым концам лигируют в вектор pGEM5Zf(-) (Promega), предварительно расщепленный рестриктазами по сайтам EcoRV и HincII, и получают вектор pNS4, который далее расщепляют рестриктазой по сайту Eco147I и лигируют с фрагментом ДНК, кодирующим экспрессионную кассету из pPIC9G, который предварительно расщепляют рестриктазой PaeI и затупляют.
Сконструированный вектор рР10 используют далее для получения рекомбинантных плазмид, предназначенных для экспрессии генов целевых белков в дрожжах Pichia pastoris.
Важной генетической характеристикой вектора рР10 является набор фрагментов ДНК определенных размеров, который образуется в ходе полимеразной цепной реакции, проведенной с использованием специально подобранных селективных праймеров, сконструированных на основе его нуклеотидной последовательности.
Данная характеристика может быть использована для идентификации штаммов, полученных на основе данного вектора.
Рекомбинантные плазмиды конструируют путем встраивания гетерологичного гена в вектор рР10 по сайтам NotI или SnaB1 с использованием традиционных методов.
Штамм Pichia pastoris-PLC-Bc-1 - продуцент фосфолипазы С PLC-Bc получают путем трансформации клеток Pichia pastoris GS115 (his4) ВКПМ Y2837 рекомбинантной плазмидой pP10-PLC-Bc. Трансформанты отбирают на минимальной среде М9 [T.Maniatis et.al., Molecular Cloning, A laboratory Manual, Cold Spring Harbor Laboratory, 390, 1982] по способности к росту без источника гистидина.
У отобранных трансформантов определяют активность фосфолипазы по модифицированному методу Куриоки [Biotecnology Letters 26, 1475-1479, 2004] и отбирают клон, обладающий максимальной фосфолипазной активностью.
Штамм Pichia pastoris PLC-Bc-1 - продуцент фосфолипазы С PLC-Bc депонирован во Всероссийской Коллекции Промышленных Микроорганизмов (ВКПМ) и имеет регистрационный номер ВКПМ Y-3359.
Клетки хранят в глицерине при температуре -70°С или в лиофильно-высушенном виде при температуре +4°С.
Штамм характеризуется следующими признаками.
Морфологические признаки.
При росте на среде «Malt agar» [The yeast of toponomic study. Ed. N.J.W.Kreger-van Rij, Amsterdam, Elsevier Sci. Publ. B.V., 1984, p.421] в течение 48 часов при температуре 30°С клетки образуют гладкие, круглые колонии с матовой поверхностью светло-кремового цвета.
При росте на среде «Malt extract» [The yeast of toponomic study. Ed. N.J.W.Kreger-van Rij, Amsterdam, Elsevier Sci. Publ.B.V., 1984, p.421] в течение 48 часов при температуре 30°С клетки образуют интенсивную ровную суспензию. Культура имеет характерный запах дрожжей.
На среде «Malt agar» после 3-х дней культивирования культура при температуре 30°С образует клетки округлой, слегка овальной формы, размером 5-10 мкм, часть клеток имеет на поверхности почки или соединена с дочерними клетками.
Культуральные признаки.
Клетки хорошо растут на полной органической среде YEPD следующего состава (мас.%): пептон - 2, дрожжевой экстракт - 1, глюкоза - 2 (или глицерин - 1), вода - остальное, а также на минимальной среде М9 и других синтетических средах для дрожжей, содержащих в качестве источника углерода глюкозу или глицерин.
Клетки штамма отличаются слабым ростом на средах, содержащих в качестве источника углерода метанол.
Физиолого-биохимические признаки.
Клетки растут при температуре от 4 до 37°С. Оптимальной температурой выращивания является 30°С.
Оптимум рН для роста составляет 4,5-6,5.
В качестве источника углерода клетки используют глюкозу, глицерин, метанол. В качестве источника азота - минеральные соли в аммонийной форме, аминокислоты, мочевину.
Клетки способны к аэробному и анаэробному росту.
Штамм не нуждается в гистидине для своего роста.
Изобретение проиллюстрировано следующими чертежами.
Фиг.1 Схема вектора рР10.
Фиг.2 Схема рекомбинантной плазмиды pP10PLC-Bc.
Пример 1. Конструирование вектора рР10.
Вектор pPIC9 (Invitrogen, № К171001) расщепляют ферментами рестрикции BglII и BamHI в буфере 2Х Tangoтм (yellow) (Fermentas) для удаления последовательности, кодирующей 5' АОХ1 промотор. Реакцию проводят в течение 1 часа при 37°С и останавливают прогреванием при 65°С в течение 10 мин. BglII - BamHI фрагмент вектора рРIС9 (7052 п.о.) выделяют электроэлюированием из 1% агарозного геля и дефосфорилируют бактериальной щелочной фосфатазой.
Из штамма Pichia pastoris GS115 (his4) ВКПМ Y2837 фенольным методом [T.Maniatis et. al., Molecular Cloning, A laboratory Manual, Cold Spring Harbor Laboratory, v.3, 1982] выделяют хромосомную ДНК, которая служит матрицей для синтеза GAP промотора. Последовательность, кодирующая GAP промотор, амплифицируют методом ПЦР. Для ПЦР-синтеза используют праймеры, сконструированные на основе нуклеотидной последовательности, кодирующей GAP промотор (23-SI, 29-SI):
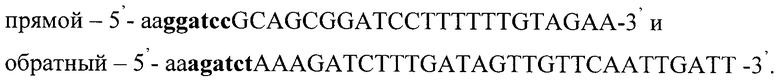
На 5'-конце каждого праймера находится сайт рестрикции для эндонуклеазы, образующей липкие концы: BamHI для прямого праймера и BglII - для обратного (в приведенных последовательностях выделены жирным шрифтом).
Для проведения полимеразной цепной реакции используют 100 мкл реакционной смеси, содержащей 0,5 нг ДНК-матрицы, 1 мкМ праймера 23-SI, 1 мкМ праймера 29-SI, 2,5 ед. Tag-полимеразы в 10 мкл 10× Tag-буфера, 1,5 мМ MgCl2, 0,8 мМ dNTP. Реакцию осуществляют по следующей схеме: 94°С - денатурирование (1 мин), 59°С - отжиг (1 мин), 72°С - полимеризация (1 мин). Всего проводят 30 циклов амплификации. Амплифицированный фрагмент ДНК очищают при помощи «DNA extraction KIT» (Fermentas).
Полученный таким образом ПЦР-амплификат гидролизуют эндонуклеазами рестрикции BglII и BamHI, очищают в агарозном геле и лигируют с BglII - BamHI фрагментом вектора pPIC9 (7052 п.о.), используя ДНК-лигазу фага Т4.
Лигазной смесью трансформируют компетентные клетки E.coli C600, приготовленные накануне обработкой хлористым кальцием. После стандартной процедуры трансформации (0°С - 40 мин, 42°С - 2 мин, 0°С - 5 мин) клетки разводят в 10 раз средой LB (Т.Маниатис, Э.Фрич, Дж.Сэмбрук. Молекулярное клонирование. М.: Мир, 1984, 84), подращивают в течение одного часа и высевают на агар LB, содержащий ампициллин в концентрации 50 мкг/мл. Посевы инкубируют при 37°С.
На следующие сутки выросшие ампициллинрезистентные колонии тестируют с помощью вышеприведенных праймеров и отбирают позитивные клоны, из которых выделяют плазмидную ДНК по стандартной методике (Т.Маниатис, Э.Фрич, Дж.Сэмбрук. Молекулярное клонирование. М.: Мир, 1984, 89). Выделенные плазмидные ДНК гидролизуют эндонуклеазами рестрикции BglII и BamHI и проверяют на наличие вставок, соответствующих последовательности, кодирующей GAP промотор. Из клонов, плазмидная ДНК которых содержит последовательность, кодирующую GAP промотор, выделяют вектор pPIC9G.
Хромосомальная ДНК, выделенная из штамма Pichia pastoris GS 115 (his4) ВКПМ Y2837, как описано выше, служит матрицей для ПЦР-синтеза фрагмента последовательности, кодирующей область 18S рРНК. Для амплификации используют праймеры, сконструированные на основе нуклеотидной последовательности, кодирующей область 18S рРНК (NS1, NS2):
прямой - 5'-GTAGTCTATGCTTGTCTC-3' и
обратный - 5'-CTTCCGTCAATTCCTTTAAG-3'.
Условия, при которых проводят полимеразную цепную реакцию, описаны выше.
Полученный ПЦР-амплификат очищают в агарозном геле и лигируют (используя ДНК-лигазу фагаТ4) с вектором pGEM5Zf(-), который предварительно расщепляют рестриктазами по сайтам EcoRV и HincII.
Лигазной смесью трансформируют компетентные клетки E.coli C600, как описано выше. Отбирают ампициллинрезистентный клон, выделяют из него плазмиду, проверяют ее на наличие вставок методом ПЦР, используя вышеописанные праймеры. Получают новый плазмидный вектор pNS4.
Вектор pPIC9G расщепляют эндонуклеазой рестрикции PaeI, липкие концы превращают в тупые с помощью Pfu полимеразы и из агарозного геля вырезают фрагмент длиной 3889 п.о. Вырезанный фрагмент очищают при помощи «DNA extraction KIT» и лигируют с вектором pNS4, предварительно расщепленным эндонуклеазой рестрикции Есо 147I.
Лигазной смесью трансформируют компетентные клетки E.coli C600, как описано выше. Отбирают ампициллинрезистентные клоны, выделяют из них плазмидную ДНК, проверяют ее на наличие вставляемого фрагмента методом ПЦР, используя все вышеописанные праймеры. Получают вектор рР10 (фиг.1).
На основе нуклеотидной последовательности вектора рР10 конструируют праймеры, которые используют для генетической характеристики полученного вектора:
прямой (N1) - 5'-GTAGTCATATGCTTGTCTC-3' и
обратный (N2) - 5'-AAAGATCTTTGATAGTTGTTCAATTGATT-3';
прямой (N3) - 5'-AGGCCCCGTGGCCGGGGGACT-3' и
обратный (N4) - 5'-CTTCCGTCAATTCCTTTAAG-3'.
Полимеразную реакцию проводят, как описано выше, используя в качестве праймеров пары N1, N2 и N3, N4.
Размер полученных в результате ПЦР фрагментов определяют гельэлектрофоретически с использованием красителя (бромистый этидий) [Т.Маниатис, Э.Фрич, Дж.Сэмбрук. Молекулярное клонирование. М.: Мир, 1984, 84].
При использовании праймеров N1 и N2 в ходе полимеразной цепной реакции нарабатывается фрагмент размером 2300 пар нуклеотидов, а при использовании праймеров N3 и N4 - фрагмент размером 380 пар нуклеотидов.
Размер образующихся фрагментов ДНК является индивидуальной характеристикой заявляемого вектора и позволяет идентифицировать штаммы, полученные с использованием вектора рР10.
Пример 2. Конструирование рекомбинантной плазмиды pP10PLC-Bc.
Из штамма Bacillus cereus ATCC 14579 фенольным методом выделяют хромосомную ДНК, которая служит матрицей для синтеза гена фосфолипазы С PLC-Вс.
Последовательность, кодирующую ген фосфолипазы С PLC-Bc, амплифицируют методом ПЦР. Для ПЦР-синтеза используют праймеры, сконструированные на основе нуклеотидной последовательности, кодирующей ген фосфолипазы С PLC-Bc (Plcl, Plc2). На 5'-конце каждого праймера внесен сайт рестрикции для эндонуклеазы Есо 47III для прямого праймера и Not 1 - для обратного (в приведенных последовательностях выделены жирным шрифтом):
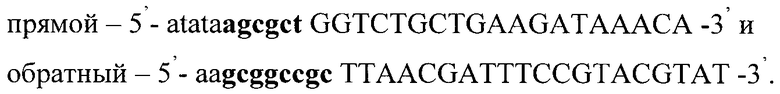
Для проведения полимеразной цепной реакции используют 100 мкл реакционной смеси, содержащей 0,5 нг ДНК-матрицы, 1 мкМ праймера Plc1, 1 мкМ праймера Plc2, 2,5 ед. Tag-полимеразы 10 мкл 10× Tag-буфера, 1,5 мМ MgCl2, 0,8 мМ dNTP. Реакцию осуществляют по следующей схеме: 94°С - денатурирование (1 мин), 59°C - отжиг (1 мин), 72°С - полимеризация (1 мин). Всего проводят 30 циклов амплификации. Амплифицированный фрагмент ДНК очищают при помощи «DNA extraction KIT».
Полученный таким образом ПЦР-амплификат гидролизуют эндонуклеазами рестрикции Есо 47III и Notl (Fermentas), очищают в агарозном геле и лигируют с вектором рР10, расщепленным ферментами рестрикции по сайтам SnaB 1-Not 1, используя ДНК-лигазу фага Т4.
Лигазной смесью трансформируют компетентные клетки E.coli C600, как описано в примере 1.
Отбор трансформантов, выделение плазмидной ДНК и гидролиз осуществляют, как описано в примере 1, с использованием праймеров Р1с1 и Р1с2 и эндонуклеаз рестрикции Eco 47III и Not 1. Получают новую рекомбинантную плазмиду pP10PLC-Вс (фиг.4).
Плазмиду pP10PLC-Bc гидролизуют рестриктазой Bgl II, электроэлюируют в 1% агарозном геле и используют ее для трансформации клеток дрожжей, как описано в примере 3.
Пример 3. Получение штамма дрожжей Pichia pastoris PLC-Bc-1 ВКПМ Y-3359 - продуцента фосфолипазы С PLC-Bc.
Для получения штамма дрожжей Pichia pastoris PLC-Bc-1 - продуцента фосфолипазы С PLC-Bc, клетки дрожжей штамма GS115 (his4) ВКПМ Y-2837 трансформируют плазмидой pP10PLC-Bc.
1 мл ночной культуры клеток дрожжей Pichia pastoris Y-2837 выращивают в 100 мл среды YEPD при 30°С до достижения культурой оптической плотности, соответствующей 2 ед. поглощения при длине волны 600 нм. Клетки дважды промывают стерильной водой, после чего суспендируют в 0,3 мл 100 мМ раствора ацетата лития и инкубируют при 30°С в течение 30 мин. К 50 мкл полученной суспензии клеток добавляют 1 мкг плазмидной ДНК, 50 мкг ДНК спермы лосося, предварительно денатурированной нагреванием (10 мин при 100°С), и 0,3 мл раствора 100 мМ ацетата лития, содержащего 40% полиэтиленгликоля 4000. Далее пробу инкубируют 30 мин при 30°С и 20 минут при 42°С, помещают на 15 секунд в ледяную баню и центрифугируют 10 секунд при 10000 об/мин. Клетки суспендируют в 1 мл стерильной воды и высевают на твердую среду М9 с добавлением 0,3 об.% микроэлементов. Клоны трансформантов выращивают 3 суток.
Полученные трансформанты высевают в жидкую среду YEPD и выращивают при 30°С до стационарной фазы роста в течение 2 суток. Далее клетки осаждают центрифугированием при 10000 об/мин в течение 5 минут, отбирают 100 мкл супернатанта и определяют фосфолипазную активность по накоплению в реакционной среде пара-нитрофенола, детектируемого методом Куриоки. Одна единица активности фермента соответствует количеству фермента, которое разлагает 1 мкмоль паранитрофенилфосфатидилхолина за 1 минуту. Активность фермента измеряют при помощи спектрофотометра при длине волны 410 нм.
Трансформант, показавший наибольшую активность фосфолипазы С PLC-Bc в культуральной жидкости заложен на хранение и депонирован как Pichia pastoris ВКПМ Y-3359.
Для доказательства наличия вектора рР10 в геноме полученного штамма дрожжей Pichia pastoris PLC-Bc-1 используют генетическую характеристику, основанную на получении фрагментов ДНК заданного размера. Фрагменты нарабатываются в ходе полимеразной цепной реакции с использованием праймеров N1, N2, N3 и N4 (пример 1).
При использовании праймеров N1 и N2 нарабатывается фрагмент ДНК размером 2300 пар нуклеотидов, при использовании праймеров N3 и N4 - фрагмент ДНК размером 380 пар нуклеотидов.
Пример 4. Синтез фосфолипазы С PLC-Bc штаммом Pichia pastoris PLC-Bc-1 ВКПМ Y-3359.
Посевную культуру штамма-продуцента PLC-Bc-1 ВКПМ Y-3359 выращивают в 5 мл жидкой среды YEPD при 30°С в течение ночи. Полученной ночной культурой инокулируют колбу Эрленмейера, объемом 750 мл, содержащую 100 мл среды YEPD, в соотношении 1:100. Культуру инкубируют при 30°С и интенсивном встряхивании до достижения стационарной фазы в течение 2 суток. Клетки осаждают центрифугированием при 10000 об/мин в течение 5 минут, супернатант переносят в другую емкость, отбирают аликвоту объемом 100 мкл и определяют фосфолипазную активность, как описано в примере 3.
Фосфолипазная активность составляет 200 ед/мл культуральной жидкости.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНТЕГРАТИВНЫЙ ПЛАЗМИДНЫЙ ВЕКТОР ДЛЯ ЭКСПРЕССИИ ГЕНОВ В ДРОЖЖАХ | 2008 |
|
RU2388823C1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДА ДЛЯ ЭКСПРЕССИИ В ДРОЖЖАХ PICHIA PASTORIS ГЕНА ФИТАЗЫ (ВАРИАНТЫ), ШТАММ ДРОЖЖЕЙ PICHIA PASTORIS - ПРОДУЦЕНТ ФИТАЗЫ (ВАРИАНТЫ) | 2009 |
|
RU2409670C1 |
| Способ получения штамма-продуцента фосфолипазы А2 Komagataella phaffii (Pichia pastoris) YIB Δleu2_PLA2S | 2020 |
|
RU2746817C1 |
| Способ получения ферментного препарата фосфолипазы А2 с применением рекомбинантного штамма-продуцента Pichia pastoris X-33/ pPICZαA-PhoA2-StV | 2018 |
|
RU2676321C1 |
| Трансформант дрожжей Pichia pastoris, продуцирующий бета-глюканазу | 2019 |
|
RU2720914C1 |
| МУТАНТНАЯ РЕКОМБИНАНТНАЯ ТЕРМОСТАБИЛЬНАЯ ФИТАЗА (ВАРИАНТЫ), ФРАГМЕНТ ДНК, КОДИРУЮЩИЙ УКАЗАННУЮ ФИТАЗУ (ВАРИАНТЫ), ШТАММ Pichia pastoris - ПРОДУЦЕНТ УКАЗАННОЙ ФИТАЗЫ (ВАРИАНТЫ) | 2009 |
|
RU2472855C2 |
| Трансформант дрожжей Pichia pastoris, продуцирующий ксиланазу | 2019 |
|
RU2714113C1 |
| Рекомбинантный штамм дрожжей Pichia pastoris с увеличенной продукцией фитазы Escherichia coli | 2019 |
|
RU2737623C1 |
| ПРИМЕНЕНИЕ ШТАММА ДРОЖЖЕЙ Komagataella pastoris В КАЧЕСТВЕ РЕЦИПИЕНТА ДЛЯ КОНСТРУИРОВАНИЯ ПРОДУЦЕНТОВ ЦЕЛЕВОГО БЕЛКА | 2013 |
|
RU2522479C1 |
| ИНТЕГРАЦИОННЫЙ ВЕКТОР ДЛЯ МНОГОКОПИЙНОЙ ИНТЕГРАЦИИ ГЕНОВ В 18SpPHK ДРОЖЖЕЙ Pichia pastoris | 2020 |
|
RU2752904C1 |
Изобретение относится к биотехнологии и относится к рекомбинантной плазмиде pP10PLC-Bc для экспрессии в дрожжах Pichia pastoris гена фосфолипазы. Изобретение относится также к рекомбинантному штамму дрожжей Pichia pastoris PLC-Bc-1 ВКПМ Y-3359 - продуценту фосфолипазы. Изобретение позволяет расширить арсенал средств для получения фосфолипазы. 2 н.п. ф-лы, 2 ил.
1. Рекомбинантная плазмида pP10PLC-Вс для экспрессии гена фосфолипазы С РLС-Вс в дрожжах Pichia pastoris, имеющая размер 10770 п.о. и состоящая из элементов:
1. фрагмент 5' 18S рРНК: 1-269 п.о.;
2. промотор GAP: 270-1026 п.о.;
3. ά-амилазный сигнальный пептид; 1029-1295 п.о.;
4. ген фосфолипазы С PLC-BC: 1304-2054 п.о.;
5. терминатор транскрипции 3' АОХ1: 2088-2421 п.о.;
6. HIS4 ORF: 3279-5813 п.о.;
7. фрагмент 3' 18S рРНК: 6085-6774 п.о.;
8. pUC ori: 7974-8648 п.о.;
9. ген резистентности к ампициллину: 9448-10308 п.о.
2. Штамм дрожжей Pichia pastoris PLC-Bc-1 ВКПМ Y-3359 - продуцент фосфолипазы С PLC-Bc.
| СПОСОБ МОНТАЖА ОСЕВОГО НАГНЕТАТЕЛЬНОГО ВЕНТИЛЯТОРА | 1999 |
|
RU2156890C1 |
| Способ волочения микропроволоки и устройство для его осуществления | 1987 |
|
SU1650304A1 |
| Устройство для автоматического регулирования плотности известкового молока | 1927 |
|
SU8607A1 |
| Способ получения фосфолипазы | 1976 |
|
SU644827A1 |
Авторы
Даты
2011-01-20—Публикация
2009-07-10—Подача