Изобретение относится к нетривиальным методам анализа смесей физиологически активных тритерпеновых гликозидов, которые могут быть использованы в химико-фармацевтической и пищевой промышленности для контроля качества биопрепаратов и биологически активных добавок к пище на их основе.
Анализ методов, применяемых для определения степени сульфатирования гликозидных препаратов, показал следующее. Обычно используют химические методы анализа, которые позволяют оценить содержание сульфатных групп в процентах [Archer Е.Е. // Analyst, 1956. V.81, N 960, р.181-182; Gassner К. // Anal. Chem. 1956, V.152, N 6, p.420-424]. Однако эти методы имеют существенный недостаток. При значениях этого показателя, немного превышающих теоретически рассчитанные показатели, не возможно по данным анализа установить, является ли это превышение следствием присутствия примесей дисульфатированных гликозидов (что допустимо), следствием присутствия трисульфатированных гликозидов (что недопустимо, при их содержании выше 9%) или же в препарате имеются примеси и тех, и других соединений (что также недопустимо при их совместном содержании выше 20%). С помощью химического анализа невозможно даже приблизительно оценить количественное содержание таких примесей.
Еще одним методом анализа, который обычно используют, является тонкослойная хроматография. В самом деле, ди- и трисульфатированные примеси можно обнаружить с помощью тонкослойной хроматографии. Однако этот метод является качественным и не позволяет судить о количественном содержании таких примесей в исследуемых препаратах.
В настоящее время единственным методом оценки количественного содержания сульфатных групп является жидкостная хроматография [Кошелева Л.П., Глебко Л.И. Химия природн. Соединений. 1977, №4, С.500-502; Авилов С.А., Стоник В.А., Калиновский А.И. Химия природн. соединений. 1990, №6, С.787-792]. Метод заключается в разделении компонентов смеси на соответствующей хроматографической колонке с последующим концентрированием элюата и взвешиванием полученных фракций. К недостаткам этого метода следует отнести трудоемкость, длительность процедуры, не всегда полное разделение соответствующих фракций и низкую точность результатов из-за частичной необратимой сорбции некоторых компонентов смеси на твердой фазе.
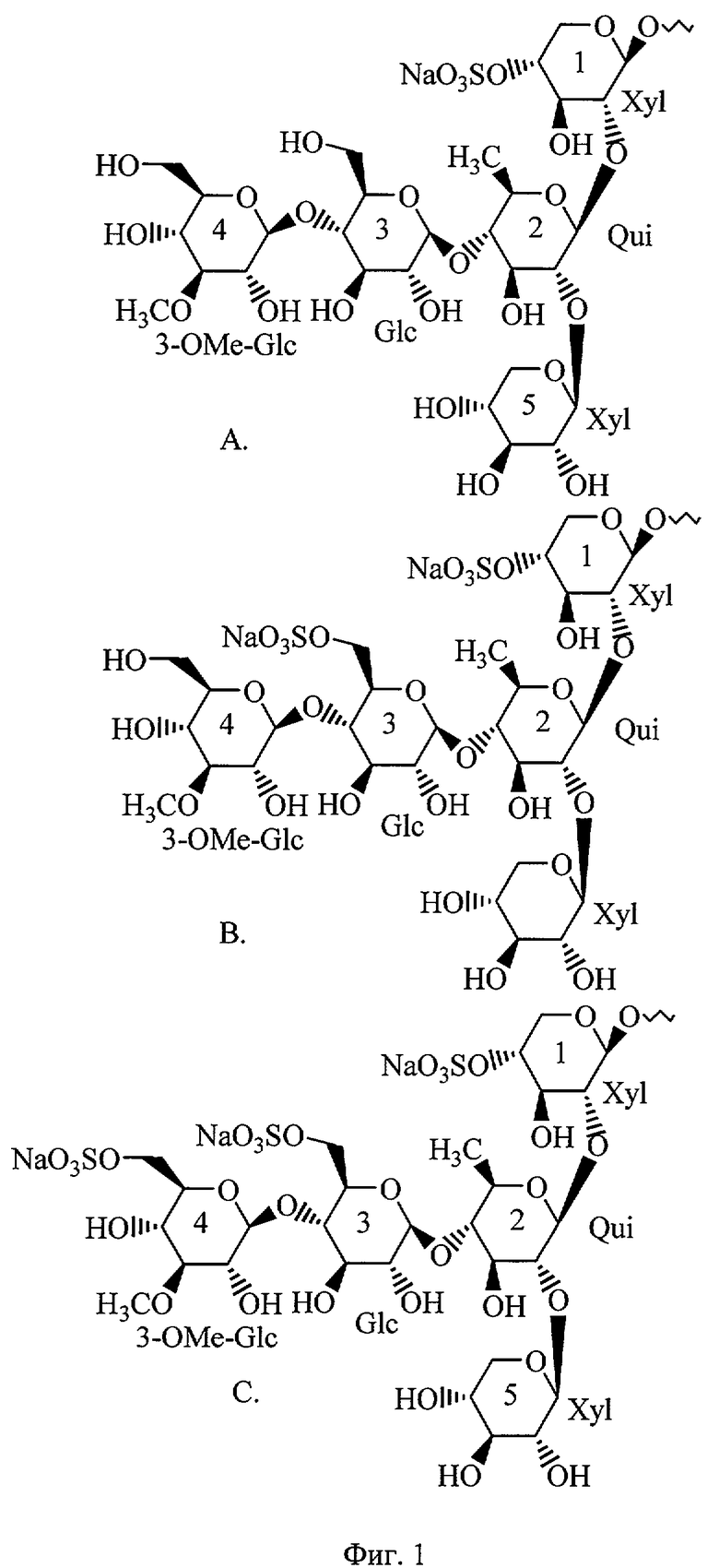
Известно, что съедобные голотурии рода Cucumaria, в частности Cucumaria japonica и родственных видов, содержат исключительно сложные смеси физиологически активных тритерпеновых гликозидов, отличающиеся друг от друга, прежде всего, степенью сульфатирования углеводных цепей (фиг.1). Все эти гликозиды можно разделить на три группы: 1) моносульфатированные гликозиды, проявляющие иммуностимулирующие свойства; 2) дисульфатированные гликозиды, не активные в отношении иммунной системы; и 3) трисульфатированные гликозиды, обладающие иммуносупрессорными свойствами. Таким образом, моно- и трисульфатированные гликозиды из этих беспозвоночных проявляют антагонистические действия в отношении иммунной системы человека и животных.
Фракция моносульфатированных гликозидов является биологически активной субстанцией иммуностимулирующего препарата Кумазид, предложенного для коррекции иммунодефицитных состояний человека [RU 2271820 C1, 20.03.2006]. Даже очень низкие концентрации этих сравнительно малополярных гликозидов из Cucumaria japonica после их перорального введения увеличивают активность макрофагов, число антитела-образующих клеток и эффективность вакцинирования [Aminin DL et al. J. Med. Food. 2001, V.4, N 3, P.125-131; Agafonova IG et al., J. Agr. Food Chem., 2003, V51, P. 6982-6986]. Однако присутствие в кумазиде и других препаратах этой серии примесей трисульфатированных гликозидов значительно ухудшает их качество, а при высоких концентрациях этих веществ (более 10-15%) может полностью нивилировать их положительное действие и даже ухудшить состояние больных с иммунодефицитами, получающих такие препараты. Поэтому определение содержания трисульфатированных гликозидов в препаратах, полученных из голотурий рода Cucumaria, является принципиально важным и устанавливает качественные характеристики таких препаратов. При отсутствии трисульфатированных соединений в них их качество является высоким, при наличии таких примесей - оно тем ниже, чем больше трисульфатированных гликозидов в таких препаратах. В кумазиде такие примеси должны отсутствовать или не превышать 9%.
Задача настоящего изобретения - разработка способа определения относительного содержания моно-, ди- и трисульфатированных гликозидов в препаратах, полученных из голотурий.
Поставленная задача решена применением двумерной ЯМР-спектроскопии для определения соотношения моно-, ди- и трисульфатированных гликозидов в препаратах из голотурий. В доступной патентной и другой научно-технической литературе не обнаружено использование данного метода для решения указанной задачи изобретения.
Основным преимуществом заявляемого способа перед известным является возможность анализа смеси гликозидов без их предварительного разделения на моно-, ди- и трисульфатированные гликозиды. Заявляемый способ основан на использовании эксперимента HSQC (Heteronuclar Single Quantum Coherence) из арсенала методов спектроскопии двумерного ядерного магнитного резонанса (ЯМР). Как показано в работе J.Cavangh, W.R.Fairbroter, A.G.Palmer lll, N.J.Shelton. Protein NMR Spectroscopy. Principles and Practice. Academic Press. 1996, p.420, относительная интенсивность резонанса спина I (протон) в InS (S - углерод 13C) - спиновой системе в базовом HSQC-эксперименте (с использованием двойного INEPT (Insensitive Nuclei Enhaced by Polarization Transfer) зависит от величины τ2 (временная задержка между 180° и 90° импульсами) и имеет значения 0.87 и 0.86 для n=1 и n=2 соответственно при компромиссном значении 2τ2=1/(3 1JIS) (J - константа спин-спинового взаимодействия протона I и углерода S, для 1JCH=135 Гц, 2τ2=2.5 мс).
Таким образом, для количественного анализа требуется измерить относительные объемы соответствующих кросс-пиков в двумерном HSQC-спектре, снятом с учетом вышеприведенного обсуждения параметров съемки. Для успешного анализа необходимо разделение кросс-пиков в измерениях F1 (химические сдвиги углеродов) и F2 (химические сдвиги протонов) (см ниже).
Тритерпеновые гликозиды (кукумариозиды) имеют весьма характерные спектры [Авилов С.А., Стоник В.А., Калиновский А.И. Химия природн. соединений. 1990. №6. С.787-792. Drozdova О.А., Avilov S.A., Kalinin V.L, Kalinovsky A.I., Stonik V.A. Riguera R., Jimenez C. Liebigs Ann. 1997, P.2351-2356. Дроздова O.A., Авилов C.A. Калиновский A.M., Стоник В.А., Мильгром Ю.М., Рашкес Я.В. Химия природн. соединений. 1993, №3, С.369-374].
Анализ всех известных структур тритерпеновых гликозидов из голотурий голотурий рода Cucumaria, показал, что все моносульфатированные гликозиды содержат сульфат при C1 4 (1 - номер моносахарида в углеводной цепи, во всех случаях это β-ксилоза, 4 - положение сульфатной группы в моносахаридном кольце). В спектрах дисульфатированных гликозидов имеются дополнительные сигналы, обусловленные наличием еще одной сульфатной группы при C-6 в глюкозном остатке, а в трисульфатированных соединениях - два набора таких сигналов, поскольку в этих соединениях сульфатные группы находятся при C-6 двух глюкозных остатков. Во всех изученных нами спектрах (более 20 соединений) протоны при углеродных атомах, несущих сульфатные группы, резонировали при 5.19-5.10 м.д. (H1 4) и 5.30-4.70 м.д. (H3,4,5 6), а соответствующие углеродные атомы, соединенные с сульфатами, - при 75.6-76.1 м.д. (ксилозные остатки) и 66.9-68.0 м.д. (глюкозные остатки). Таким образом, эти сигналы были разделимы в обоих измерениях в спектрах, снятых в растворе дейтеропиридина (C5D5N) и воды (D2O) 4:1.
Примеры углеводных цепей моно-, ди- и трисульфатированных соединений, принадлежащих к этой группе соединений, даны на фиг.1.
Таким образом, установленные ранее закономерности сульфатирования для этой группы соединений показывают, что в дисульфатированных производных имеется одна метиленовая группа, соединенная с сульфатом, а в трисульфатированных производных - две таких группы. Соответственно наличие двух сигналов таких групп в ЯМР-спектрах указывает на присутствие трисульфатированных гликозидов и позволяет, таким образом, быстро выполнить качественный анализ, показывающий, имеются или нет примеси таких соединений в исследуемых образцах. Для количественного анализа необходимо использовать сравнительные интенсивности сигналов, химический сдвиг, которых изменился за счет соседства сульфатных групп, а в двумерных спектрах - абсолютные объемы кросс-пиков.
В таблице приведены абсолютные объемы кросс-пиков (в условных единицах) из рутинных HSQC-спектров чистых образцов гликозидов голотурий различного строения, полученных при значении τ2=1.8 мс.
На фиг.2(а-г) приведены частичные HSQC-спектры представителей этих групп соединений.
рия
[2] A.S.Antonov, S.A.Avilov, A.I.Kalinovsky, S.D.Anastyuk, P.S.Dmitrenok, E.V.Evtushenko, V.I.Kalinin, A.A.Smirnov, S.Taboada, M.Ballesteros, CAvila, V.A.Stonik. Journal of Natural Prodacts. 2008, V.71, P.1677-1685.
[3] A.S.Silchenko, S.A.Avilov, A.I.Kalinovsky, P.S.Dmitrenok, V.I.Kalinin, J.Morre, M.L.Deinzer, C.Woodword, P.D.Collin. Canadian Journal of Chemistry. 2007, V.85, P.626-636.
*, **, *** Гликозиды, не вошедшие в публикацию [3].
Как следует из таблицы, средняя точность определения составляет 7% для первой группы соединений, и 8.2% и 11.2% для второй и третьей групп соответственно. Такой разброс данных может быть связан как с процессами спиновой релаксации при прохождении импульсной последовательности, которые не учитывались в нашем анализе, так и с различиями в других параметрах съемки спектров. Кроме того, точность определения будет зависеть от соотношения сигнал/шум в двумерном спектре и от надлежащего выбора других параметров съемки спектра.
Изобретение иллюстрируется следующим примером конкретного выполнения.
Пример. На анализ поступил образец препарата кумазид, представляющий собой смесь высокополярных гликозидов, полученную из голотурии Cucumaria japonica. Известно, что гликозиды этой голотурии являются сульфатированными, разветвленными и принадлежат в основном к моносульфатированным гликозидам пентаозидам [Avilov S.A., Kalinin V.I., Smirnov A.V. Biochem. Syst. Ecol. 2004, V.32, Р.735-745]. Они все сульфатированы по положению C1 4. Требовалось установить в них процентное содержание гликозидов, дополнительно сульфатированных и по положениям C3 6 и C4 6, поскольку они снижали биологическую активность препарата. Диагностическая часть HSQC-спектра 5 мг смеси, снятого в течение 12 часов в C5D5N, приведена на фиг.2г.
Кросс-пик при 76.0 м.д/5.07 м.д. содержит сигнал H1 4 от всех трех форм гликозидов (объемная интенсивность 6.89 условных единиц - 100%). Кросс-пик при 68 м.д./5.20 м.д. содержит сигнал от двух протонов при C6 от трисульфатированных форм и сигнал от одного протона при C6 от дисульфатированных форм (объемная интенсивность 1.97). Кросс-пик при 68 м.д./4.50 м.д. содержит по одному сигналу протонов при C6 от трисульфатированных и дисульфатированных форм (объемная интенсивность 1.42). Из уравнений:
T+D+M=6.89, 2T+D=1.97, T+D=1.42,
получаем, что содержание трисульфатированных гликозидов составляет 8±1%, дисульфатированных 12.6±2%. Ошибку берем из табличных данных (таблица 1) по родственным гликозидам (Cucumaria frondosa).
Хроматографический анализ дал суммарное значение содержания трисульфатированных и дисульфатированных гликозидов 15%, что удовлетворительно согласуется с полученными нами значениями.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИММУНОМОДУЛИРУЮЩЕЕ СРЕДСТВО "КУМАЗИД" И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ | 2004 |
|
RU2271820C1 |
| СРЕДСТВО, СТИМУЛИРУЮЩЕЕ КЛЕТОЧНЫЙ ИММУНИТЕТ МЛЕКОПИТАЮЩИХ | 2009 |
|
RU2415863C1 |
| СРЕДСТВО, ИНГИБИРУЮЩЕЕ МНОЖЕСТВЕННУЮ ЛЕКАРСТВЕННУЮ УСТОЙЧИВОСТЬ ОПУХОЛЕВЫХ КЛЕТОК | 2012 |
|
RU2494742C1 |
| СПОСОБ ПЕРЕРАБОТКИ ДАЛЬНЕВОСТОЧНОЙ КУКУМАРИИ Cucumaria japonica И БИОЛОГИЧЕСКИ АКТИВНЫЙ ПРОДУКТ, ПОЛУЧАЕМЫЙ ЭТИМ СПОСОБОМ | 2009 |
|
RU2426453C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФРОНДОЗИДА А И СПОСОБ СТИМУЛИРОВАНИЯ ИММУННОЙ СИСТЕМЫ МЛЕКОПИТАЮЩИХ | 2005 |
|
RU2339644C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ | 2001 |
|
RU2184556C1 |
| ВОДКА ОСОБАЯ | 2014 |
|
RU2562100C1 |
| СПОСОБ ПОВЫШЕНИЯ ПОЛОВОЙ АКТИВНОСТИ (ПОТЕНЦИИ) ЧЕЛОВЕКА И ЖИВОТНЫХ | 2001 |
|
RU2210377C1 |
| ФРАКЦИЯ КЕРАТАНСУЛЬФАТОЛИГОСАХАРИДОВ И СОДЕРЖАЩИЙ ЕЕ ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ | 1995 |
|
RU2173154C2 |
| Биологически активная добавка из голотурии и способ её получения | 2021 |
|
RU2755312C1 |
Использование: для определения относительного содержания сульфатированных форм гликозидов в препаратах из голотурий. Сущность: заключается в том, что определение проводят без разделения смеси гликозидов из данных ЯМР-эксперимента HSQC и при значении параметра τ2 (временная задержка между 180° и 90° импульсами), определяемого из соотношения 2τ2=1/(31JCH), где 1JCH - константа спин-спинового взаимодействия между замещенным углеродом и его протоном, затем измеряют объемные интенсивности соответствующих протонам при замещенных углеродах кросс-пиков, и из получившихся значений вычисляют процентное содержание компонентов смеси путем составления и решения системы линейных уравнений. Технический результат: обеспечение возможности анализа смеси гликозидов без их предварительного разделения на моно-, ди- и трисульфатированные гликозиды. 2 ил., 1 табл.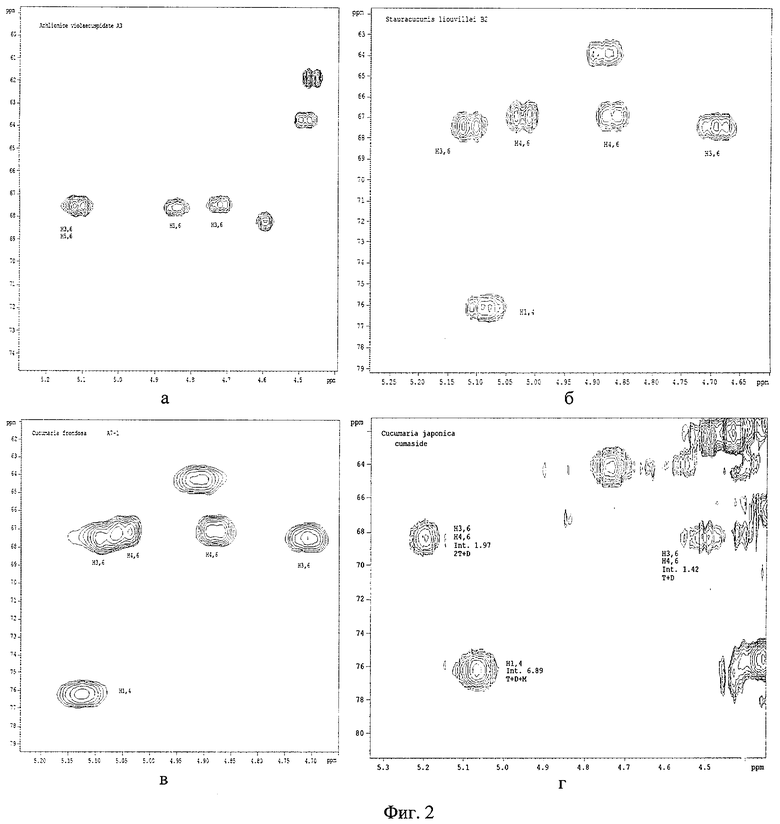
Способ определения относительного содержания сульфатированных форм гликозидов в препаратах из голотурий, характеризующийся тем, что определение проводят без разделения смеси гликозидов из данных ЯМР-эксперимента HSQC и при значении параметра τ2 (временная задержка между 180° и 90° импульсами), определяемого из соотношения
2τ2=1/(31JCH),
где 1JCH - константа спин-спинового взаимодействия между замещенным углеродом и его протоном, затем измеряют объемные интенсивности соответствующих протонам при замещенных углеродах кросс-пиков и из получившихся значений вычисляют процентное содержание компонентов смеси путем составления и решения системы линейных уравнений.
| Archer Е.Е., Analyst, 1956, V.81, №960, р.181, 182 Gassner К., Anal | |||
| Chem., 1956, V.152, №6, p.420-424 | |||
| Способ количественного определения флавонол-3-гликозидов | 1987 |
|
SU1483339A1 |
| Способ определения кислых гликозидаз в ткани печени | 1985 |
|
SU1320750A1 |
| JP 4066099 A, 02.03.1992 | |||
| JP 4066096 A, 02.03.1992. | |||
Авторы
Даты
2011-01-27—Публикация
2009-11-18—Подача