Область изобретения
Настоящее изобретение относится к пиперидинилпиперазинам, применимым в качестве селективных ингибиторов хемокиновых рецепторов, в особенности рецепторов CCR5, к фармацевтическим композициям, содержащим соединения, соответствующие настоящему изобретению, и к способам лечения с применением соединений, соответствующих настоящему изобретению. Настоящее изобретение также относится к применению комбинации одного или более соединений, соответствующих настоящему изобретению, и одного или более противовирусных или других средств, применимых для лечения вируса иммунодефицита человека (ВИЧ). Настоящее изобретение также относится к применению соединения, соответствующего настоящему изобретению, по отдельности или в комбинации с другим средством, для лечения отторжения цельного органа, реакции "трансплантат против хозяина", артрита, ревматоидного артрита, воспалительной болезни кишечника, атонического дерматита, псориаза, астмы, аллергий или рассеянного склероза.
Предшествующий уровень
Глобальный кризис здравоохранения, вызванный ВИЧ, возбудителем синдрома приобретенного иммунодефицита (СПИД), не вызывает сомнения. Хотя последние достижения в фармакотерапии позволяют успешно замедлять развитие СПИД, все же необходим более безопасный, более эффективный способ борьбы с этим вирусом.
Имеются данные о том, что ген CCR5 (СС хемокинового рецептора 5) участвует в резистентности по отношению к инфекции ВИЧ. Инфекция ВИЧ начинается с присоединения вируса к мембране клетки-мишени путем взаимодействия с клеточным рецептором CD4 и молекулой вторичного хемокинового рецептора и развивается путем репликации и диссеминации инфицированных клеток в крови и других тканях. Существуют различные хемокиновые рецепторы, но для макрофаго-тропического ВИЧ, который считается главным патогенным штаммом, реплицирующимся на начальных стадиях инфицирования, главным хемокиновым рецептором, необходимым для проникновения ВИЧ в клетку, является CCR5. Поэтому создание помех взаимодействию между вирусным рецептором CCR5 и ВИЧ может блокировать проникновение ВИЧ в клетку. Настоящее изобретение относится к небольшим молекулам, которые являются антагонистами CCR5.
Имеются данные о том, что рецепторы CCR5 опосредуют перенос клеток при воспалительных заболеваниях, таких как артрит, ревматоидный артрит, атонический дерматит, псориаз, астма и аллергии. Предполагается, что ингибирование таких рецепторов полезно для лечения таких заболеваний и для лечения других воспалительных заболеваний или патологических состояний, таких как воспалительная болезнь кишечника, рассеянный склероз, отторжения цельного органа и реакция "трансплантат против хозяина".
Производные пиперидина, которые являются антагонистами мускарина, применимыми для лечения нарушений познавательной способности, таких как болезнь Альцгеймера, раскрыты в патентах US 5883096, 6037352, 5889006, 5952349 и 5977138.
Соединения, применимые в качестве антагонистов рецептора CCR5, раскрыты в патентах US 6387930; 6602885 и 6391865, публикациях РСТ WO 2000/66558, WO 2000/66559, WO 02/079194, WO 03/69252, WO 03/020716, WO 04/056770, публикации европейского патента ЕР 1421075 и в публикациях патентов US 2004/0092745 и US 2004/0092551 и в предварительной заявке US 60/516954, поданной 3 ноября 2003 г.
В публикации РСТ WO 2002/081449, опубликованной 17 октября 2002 г. (R.Albert et al.), раскрыты некоторые производные бипиперидинила, применимые в качестве ингибиторов хемокиновых рецепторов. A-M.Vandamme et al., Antiviral Chemistry & Chemotherapy, 9:187-203 (1998) описали современные клинические лечения инфекции ВИЧ-1 у человека, включающие комбинации по меньшей мере трех лекарственных средств, или так называемую высокоактивную антиретровирусную терапию ("ВААРВТ"). ВААРВТ включает различные комбинации нуклеозидных ингибиторов обратной транскриптазы ("НИОТ"), ненуклеозидных ингибиторов обратной транскриптазы ("ННИОТ") и ингибиторов протеазы ВИЧ ("ИП"). Для поддающихся лечению и не принимавших лекарственных средств пациентов ВААРВТ эффективно уменьшает смертность и ослабляет прогрессирование ВИЧ-1 в СПИД. Однако эти методики лечения с использованием нескольких лекарственных средств не уничтожают ВИЧ-1 и длительное лечение обычно приводит к множественной лекарственной устойчивости. Поэтому приоритетной является разработка новых лекарственных средств для лучшего лечения инфекции ВИЧ-1.
Краткое содержание изобретения
Настоящее изобретение относится к новому классу соединений в качестве антагонистов рецептора CCR5, к способам получения таких соединений, к фармацевтическим композициям, содержащим одно или более таких соединений и к способам лечения, предупреждения или облегчения протекания одного или большего количества заболеваний, связанных с рецептором CCR5.
В одном варианте осуществления настоящее изобретение относится к соединению, описываемому структурной формулой IA:
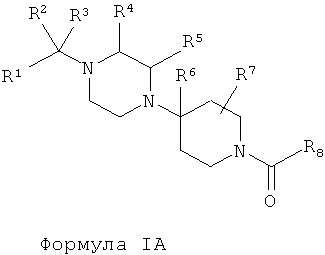
или его фармацевтически приемлемой соли, сольвату или сложному эфиру; в которой:
R1 выбран из группы, включающей R9-фенил, R9-пиридил, R9-тиофенил, R9-нафтил и
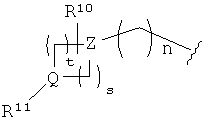
R2 выбран из группы, включающей Н и алкил;
R3 выбран из группы, включающей Н, алкил, алкоксиалкил-, циклоалкил, циклоалкилалкил-, R9-арил, R9-арилалкил-, R9-гетероарил и R9-гетероарилалкил-;
или R2 и R3 совместно означают =O, =N(OR12) или =N-N(R13)(R14);
R4, R5, R6 и R7 независимо выбраны из группы, включающей Н и алкил;
R8 выбран из группы, включающей
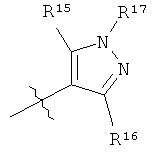
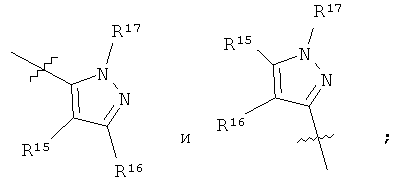
R9 означает 1, 2 или 3 заместителя, независимо выбранных из группы, включающей Н, галоген, алкил, алкоксигруппу, -CF3, -OCF3, СН3С(О)-, -CN, CH3S(O2)-, CF3S(O2)-, -N(R18)(R19);
R10 выбран из группы, включающей Н и алкил;
R11 выбран из группы, включающей Н, алкил, фторалкил-, R9-арилалкил-, R9-гетероарил-, алкил, алкил-S(O2)-, циклоалкил-S(O2)-, фторалкил-S(O2)-, R9-арил-S(O2)-, R9-гетероарил-S(O2)-, N(R18)(R19)-S(O2)-, алкил-С(О)-, циклоалкил-С(О)-, фторалкил-С(О)-, R9-арил-С(О)-, алкил-NH-C(O)- и R9-арил-NH-C(O)-;
R12 означает Н, алкил, фторалкил-, циклоалкилалкил-, гидроксиалкил-, алкил-O-алкил-, алкил-O-С(O)-алкил- или N(R18)(R19)-C(O)-алкил-;
R13 и R14 независимо выбраны из группы, включающей Н, алкил и циклоалкил, или R13 и R14 совместно означают (С2-С6)алкилен и образуют кольцо с атомом азота, к которому, как показано, они присоединены;
R15 и R16 независимо выбраны из группы, включающей алкил, галоген, -NR18R19, -ОН, -CF3, -ОСН3, -O-ацил и -OCF3;
R17 выбран из группы, включающей R20O-, H2N- и R20R21N-;
R18 и R19 независимо выбраны из группы, включающей Н и алкил;
R20 выбран из группы, включающей алкил, галогеналкил циклоалкил, гетероциклил, аралкил, алкиларил, арил и гетероарил;
R21 выбран из группы, включающей Н, алкил, фторалкил-, R9-арилалкил-, R9-гетероарил-, алкил, алкил-S(O2)-, циклоалкил-S(O2)-, фторалкил-S(O2)-, R9-арил-S(O2)-, R9-гетероарил-S(O2)-, N(R18)(R19)-S(O2)-, алкил-С(О)-, циклоалкил-С(О)-, фторалкил-С(О)-, R9-арил-С(О)-, алкил-NH-C(O)- и R9-арил-NH-C(O)-;
Q и Z независимо выбраны из группы, включающей СН и N;
n равно 0, 1, 2, 3 или 4;
s равно 0, 1, 2, 3 или 4; и
t равно 1, 2, 3 или 4;
при условии, что если n равно 0, то Z означает СН.
В другом варианте осуществления настоящее изобретение относится к соединению в выделенной и очищенной форме, указанное соединение описывается структурной формулой IB:
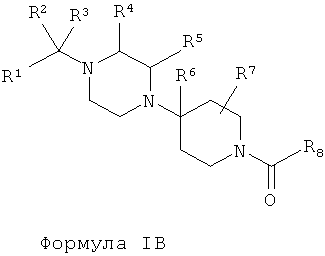
или к его фармацевтически приемлемой соли, сольвату или сложному эфиру; в которой:
R1 выбран из группы, включающей R9-фенил, R9-пиридил, R9-тиофенил, R9-нафтил и
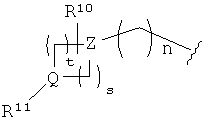
R2 выбран из группы, включающей Н и алкил;
R3 выбран из группы, включающей Н, алкил, алкоксиалкил-, циклоалкил, циклоалкилалкил-, R9-арил, R9-арилалкил-, R9-гетероарил и R9-гетероарилалкил-; или R2 и R3 совместно означают =O, =NOR12, или =N-N(R13)(R14);
R4, R5, R6 и R7 независимо выбраны из группы, включающей Н и алкил;
R8 выбран из группы, включающей
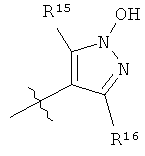
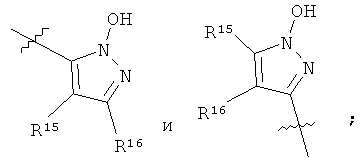
R9 означает 1, 2 или 3 заместителя, независимо выбранных из группы, включающей Н, галоген, алкил, алкоксигруппу, -СF3, -OCF3, СН3С(О)-, -CN, CH3S(O2)-, CF3S(O2)-, -N(R18)(R19);
R10 выбран из группы, включающей Н и алкил;
R11 выбран из группы, включающей Н, алкил, фторалкил-, R9-арилалкил-, R9-гетероарил-, алкил, алкил-S(O2)-, циклоалкил-S(O2)-, фторалкил-S(O2)-, R9-арил-S(O2)-, R9-гетероарил-S(O2)-, N(R18)(R19)-S(O2)-, алкил-С(О)-, циклоалкил-С(О)-, фторалкил-С(О)-, R9-арил-С(О)-, алкил-NH-C(O)- и R9-арил-NH-C(O)-;
R12 означает Н, алкил, фторалкил-, циклоалкилалкил-, гидроксиалкил-, алкил-O-алкил-, алкил-O-С(O)-алкил- или N(R17)(R18)-C(O)-алкил-;
R13 и R14 независимо выбраны из группы, включающей Н, алкил и циклоалкил, или R13 и R14 совместно означают (С2-С6)алкил и образуют кольцо с атомом азота, к которому, как показано, они присоединены;
R15 и R16 независимо выбраны из группы, включающей алкил, галоген, -NR17R18, -ОН, -CF3, -ОСН3, -O-ацил и -OCF3;
R17 и R18 независимо выбраны из группы, включающей Н и алкил;
Q и Z независимо выбраны из группы, включающей СН и N;
n равно 0, 1, 2, 3 или 4;
s равно 0, 1, 2, 3 или 4;
и t равно 1, 2, 3 или 4;
при условии, что если n равно 0, то Z означает СН.
Соединения формулы IA или формулы IB можно применять в качестве ингибиторов CCR5 и для лечения и предупреждения заболеваний, связанных с CCR5 и вирусом иммунодефицита человека.
Подробное описание изобретения
В одном варианте осуществления настоящее изобретение относится к пиперидинилпиперазинам, которые описываются структурной формулой IA или IB, или к их фармацевтически приемлемым солям, сольватам или сложным эфирам, в которой различные фрагменты являются такими, как описано выше.
В другом варианте осуществления в структурной формуле IA,
R2 выбран из группы, включающей Н и (С1-С6)алкил;
R3 выбран из группы, включающей Н, (С1-С6) алкил, (С1-С6)алкокси(С1-С6)алкил-, (С3-С10)циклоалкил, (С3-С10)циклоалкил(С1-С6)алкил-, R9-арил, R9-арил(C1-С6)алкил-, R9-гетероарил и R9-гетероарил(С1-С6)алкил-;
или R2 и R3 совместно означают =O, =N(OR12) или =N-N(R13)(R14);
R4, R5, R6 и R7 независимо выбраны из группы, включающей Н и (С1-С6)алкил;
R8 выбран из группы, включающей

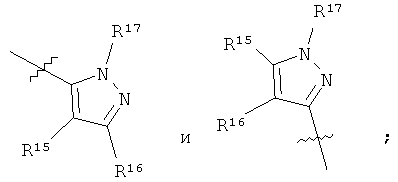
R9 означает 1, 2 или 3 заместителя, независимо выбранных из группы, включающей Н, галоген, (С1-С6)алкил, (С1-С6)алкоксигруппу, -CF3, -OCF3, СН3С(О)-, -CN, CH3S(O2)-, CF3S(O2)-, -N(R18)(R19);
R10 выбран из группы, включающей Н и (С1-С6)алкил;
R11 выбран из группы, включающей Н, (С1-С6)алкил, фтор(С1-С6)алкил-, R9-арил(С1-С6)алкил-, R9-гетероарил-, (С1-С6)алкил, (С1-С6)алкил-S(O2)-, (С3-С6)циклоалкил-S(O2)-, фтор(С1-С6)алкил-S(O2)-, R9-арил-S(O2)-, R9-гетероарил-S(O2)-, N(R18)(R19)-S(O2)-, (С1-С6)алкил-С(O)-, (С3-С6)циклоалкил-С(О)-, фтор(С1-С6)алкил-С(О)-, R9-арил-С(О)-, (С1-С6)алкил-NН-С(O)- и R9-арил-NH-C(O)-;
R12 означает Н, (С1-С6)алкил, фтор(С1-С6)алкил-, (С3-С10)циклоалкил(С1-С6)алкил-, гидрокси(С1-С6)алкил-, (С1-С6)алкил-O-(С2-С6)алкил-, (С1-С6)алкил-O-С(O)-(C1-С6)алкил- или N(R18)(R19)-C(O)-(С1-С6)алкил-;
R13 и R14 независимо выбраны из группы, включающей Н, (С1-С6)алкил и (С3-С10)циклоалкил, или R13 и R14 совместно означают (С2-С6)алкил и образуют кольцо с атомом азота, к которому, как показано, они присоединены;
R15 и R16 независимо выбраны из группы, включающей (С1-С6)алкил, галоген, -NR18R19, -OH, -CF3, -ОСН3, -O-ацил и -OCF3;
R17 выбран из группы, включающей R20O-, H2N- и R20R21N-;
R18 и R19 независимо выбраны из группы, включающей Н и (С1-С6)алкил;
R20 выбран из группы, включающей (С1-С6)алкил, галоген(С1-С6)алкил, (С3-С10)циклоалкил, гетероциклил, арил(С1-С6)алкил, (С1-С6)алкиларил, арил и гетероарил;
R21 выбран из группы, включающей Н, (С1-С6)алкил, фтор-(С1-С6)алкил-, R9-арил(С1-С6)алкил-, R9-гетероарил-, (С1-С6)алкил, (С1-С6)алкил-S(O2)-, цикло(С3-С6)алкил-S(O2)-, фтор(С1-С6)алкил-S(O2)-, R9-арил-S(O2)-, R9-гетероарил-S(O2)-, N(R18)(R19)-S(O2)-, (С1-С6)алкил-С(O)-, (С3-С6)циклоалкил-С(О)-, фтор(С1-С6)алкил-С(O)-, R9-арил-С(О)-, (C1-C6)алкил-NH-C(O)- и R9-арил-NH-C(O)-;
Q и Z независимо выбраны из группы, включающей СН и N;
n равно 0, 1, 2, 3 или 4;
s равно 0, 1, 2, 3 или 4; и
t равно 1, 2, 3 или 4;
при условии, что если n равно 0, то Z означает СН.
В другом варианте осуществления в соединении, описываемом структурной формулой IB,
R2 выбран из группы, включающей Н и (С1-С6)алкил;
R3 выбран из группы, включающей Н, (С1-С6)алкил, (С1-С6)алкокси(С1-С6)алкил-, (С3-С10)циклоалкил, (С3-С10)циклоалкил(С1-С6)алкил-, R9-арил, R9-арил(C1-С6)алкил-, R9-гетероарил и R9-гетероарил(С1-С6)алкил-;
или R2 и R3 совместно означают =O, =N(OR12) или =N-N(R13)(R14);
R4, R5, R6 и R7 независимо выбраны из группы, включающей Н и (С1-С6)алкил;
R8 выбран из группы, включающей
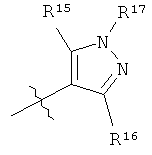

R9 означает 1, 2 или 3 заместителя, независимо выбранных из группы, включающей Н, галоген, (С1-С6)алкил, (С1-С6)алкоксигруппу, -CF3, -OCF3, СН3С(О)-, -CN, CH3S(O2)-, CF3S(O2)-, -N(R18)(R19);
R10 выбран из группы, включающей Н и (С1-С6)алкил;
R11 выбран из группы, включающей Н, (С1-С6)алкил, фтор(С1-С6)алкил-, R9-арил(С1-С6)алкил-, R9-гетероарил-, (С1-С6)алкил, (С1-С6)алкил-S(O2)-, (С3-С6) циклоалкил-S(O2)-, фтор(С1-С6)алкил-S(O2)-, R9-арил-S(O2)-, R9-гетероарил-S(O2)-, N(R17)(R18)-S(O2)-, (С1-С6)алкил-С(O)-, (С3-С6)циклоалкил-С(О)-, фтор(С1-С6)алкил-С(О)-, R9-арил-С(О)-, (C1-C6)алкил-NH-C(O)- и R9-арил-NH-C(O)-;
R12 означает Н, (С1-С6)алкил, фтор(С1-С6)алкил-, (С3-С10)циклоалкил(С1-С6)алкил-, гидрокси(С1-С6)алкил-, (С1-С6)алкил-O-(С2-С6)алкил-, (С1-С6)алкил-O-С(O)- (С1-С6)алкил- или N(R17)(R18)-C(O)-(С1-С6)алкил-;
R13 и R14 независимо выбраны из группы, включающей Н, (С1-С6)алкил и (С3-С10)циклоалкил, или R13 и R14 совместно означают (С2-С6)алкил и образуют кольцо с атомом азота, к которому, как показано, они присоединены;
R15 и R16 независимо выбраны из группы, включающей (С1-С6)алкил, галоген, -NR17R18, -ОН, -CF3, -ОСН3, -O-ацил и -OCF3;
R17 и R18 независимо выбраны из группы, включающей Н и (С1-С6)алкил;
Q и Z независимо выбраны из группы, включающей СН и N;
n равно 0, 1, 2, 3 или 4;
s равно 0, 1, 2, 3 или 4;
и t равно 1, 2, 3 или 4;
при условии, что если n равно 0, то Z означает СН.
В другом варианте осуществления в соединениях, описываемых структурной формулой IA или IB, R1 означает R9-фенил.
В другом варианте осуществления в соединениях, описываемых структурной формулой IA или IB, R1 означает
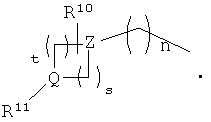
В другом варианте осуществления в структурной формуле IA или IB, в которой R1 означает
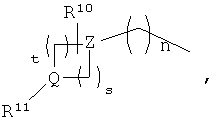
Z означает СН, и Q означает N.
В другом варианте осуществления в структурной формуле IA или IB, R2 означает водород, и R3 выбран из группы, включающей (С1-С6)алкил, (С1-С6)алкокси(С1-С6)алкил- и R9-арил.
При использовании в настоящем изобретении структурные формулы IA, IB и IC являются одинаковыми за исключением значений заместителя R8 в указанных формулах.
Выше и во всем описании приведенные ниже термины, если не указано иное, обладают приведенными ниже значениями.
"Пациент" включает людей и животных.
"Млекопитающее" означает людей и других млекопитающих.
"Алкил" означает алифатическую углеводородную группу, которая может быть линейной или разветвленной и содержать примерно от 1 до примерно 20 атомов углерода в цепи. Предпочтительные алкильные группы содержат примерно от 1 до примерно 12 атомов углерода в цепи. Более предпочтительные алкильные группы содержат от примерно 1 до примерно 6 атомов углерода в цепи. "Разветвленная" означает, что к линейной алкильной цепи присоединена одна или большее количество алкильных групп, таких как метил, этил или пропил. "Низший алкил" означает группу, содержащую от 1 до примерно 6 атомов углерода в цепи, которая может быть линейной или разветвленной. Алкильная группа может быть незамещенной или необязательно замещенной одним или большим количеством заместителей, которые могут быть одинаковыми или разными, причем каждый заместитель независимо выбран из группы, включающей галоген, алкил, арил, циклоалкил, цианогруппу, гидроксигруппу, алкоксигруппу, алкилтиогруппу, аминогруппу, -NH(алкил), -NH(циклоалкил), -N(алкил)2, карбокси и -С(O)O-алкил. Неограничивающие примеры подходящих алкильных групп включают метильную, этильную, н-пропильную, изопропильную и трет-бутильную. Если это применимо, то термин "алкил" также включает двухвалентный алкил, т.е. "алкиленовую" группу, полученную отщеплением атома водорода от алкильной группы. Примеры алкиленовых групп включают метиленовую (-СН2-), этиленовую (-СН2СН2-), пропиленовую (-С3Н6-) и аналогичные, включая, если это применимо, структуры с линейной и разветвленной цепью.
"Алкенил" означает алифатическую углеводородную группу, содержащую, по меньшей мере, одну углерод-углеродную двойную связь и которая может быть линейной или разветвленной и содержит от примерно 2 до примерно 15 атомов углерода в цепи. Предпочтительные алкенильные группы содержат от примерно 2 до примерно 12 атомов углерода в цепи; и более предпочтительно - от примерно 2 до примерно 6 атомов углерода в цепи. "Разветвленная" означает, что одна или большее количество низших алкильных групп, таких как метильная, этильная или пропильная, присоединены к линейной алкенильной цепи. "Низший алкенил" содержит от примерно 2 до примерно 6 атомов углерода в цепи, которая может быть линейной или разветвленной. Термин "замещенный алкенил" означает, что алкинильная группа может содержать один или большее количество заместителей, которые могут быть одинаковыми или разными, причем каждый заместитель независимо выбран из группы, включающей галоген, алкил, арил, циклоалкил, цианогруппу, алкоксигруппу и -S(алкил). Неограничивающие примеры подходящих алкенильных групп включают этенил, пропенил, н-бутенил, 3-метилбут-2-енил, н-пентенил, октенил и деценил.
"Алкинил" означает алифатическую углеводородную группу, содержащую не менее одной углерод-углеродной тройной связи, и которая может быть линейной или разветвленной и содержать от примерно 2 до примерно 15 атомов углерода в цепи. Предпочтительные алкинильные группы содержат от примерно 2 до примерно 12 атомов углерода в цепи; а более предпочтительно - от примерно 2 до примерно 4 атомов углерода в цепи. "Разветвленная" означает, что к линейной алкинильной цепи присоединена одна или большее количество низших алкильных групп, таких как метил, этил или пропил. "Низший алкинил" означает группу, содержащую от 2 до примерно 6 атомов углерода в цепи, которая может быть линейной или разветвленной. Неограничивающие примеры алкенильных групп включают: этинильную, пропинильную, 2-бутинильную и 3-метилбутинильную. Алкинильная группа может быть незамещенной или необязательно замещенной одним или большим количеством заместителей, которые могут быть одинаковыми или разными, причем каждый заместитель независимо выбран из группы, включающей алкил, арил и циклоалкил.
"Арил" означает ароматическую моноциклическую или полициклическую кольцевую систему, включающую от примерно 6 до примерно 14 атомов углерода, предпочтительно - от примерно 6 до примерно 10 атомов углерода. Арильная группа необязательно может быть замещена одним или большим количеством "заместителей кольцевой системы", которые могут быть одинаковыми или разными и являются такими, как определено в настоящем изобретении. Неограничивающие примеры подходящих арильных групп включают фенильную и нафтильную.
"Гетероарил" означает ароматическую моноциклическую или полициклическую кольцевую систему, содержащую от примерно 5 до примерно 14 циклических атомов, предпочтительно - от примерно 5 до примерно 10 циклических атомов, в которой один или большее количество атомов кольцевой системы представляет собой элемент, не являющийся углеродом, например азот, кислород или серу, поодиночке или в комбинации. Предпочтительные гетероарилы содержат от примерно 5 до примерно 6 циклических атомов. "Гетероарил" необязательно может быть замещен одним или большим количеством "заместителей кольцевой системы", которые могут быть одинаковыми или разными и являются такими, как определено в настоящем изобретении. Приставка аза-, окса- или тиа- перед названием гетероциклильной системы означает, что в качестве циклического атома содержится не менее одного атома азота, кислорода или серы соответственно. Атом азота гетероарила необязательно может быть окислен с образованием соответствующего N-оксида. Неограничивающие примеры подходящих гетероарилов включают пиридил, пиразинил, фуранил, тиенил, пиримидинил, пиридон (включая N-замещенные пиридоны), изоксазолил, изотиазолил, оксазолил, тиазолил, пиразолил, фуразанил, пирролил, пиразолил, триазолил, 1,2,4-тиадиазолил, пиразинил, пиридазинил, хиноксалинил, фталазинил, оксиндолил, имидазо[1,2-а]пиридинил, имидазо[2,1-b]тиазолил, бензофуразанил, индолил, азаиндолил, бензимидазолил, бензотиенил, хинолинил, имидазолил, тиенопиридил, хиназолинил, тиенопиримидил, пирролопиридил, имидазопиридил, изохинолинил, бензоазоиндолил, 1,2,4-триазинил, бензотиазолил, тетразолил и т.п. Термин "гетероарил" также относится к частично насыщенным гетероарильным фрагментам, таким как, например, тетрагидроизохинолил, тетрагидрохинолил и т.п.
«Аралкил» или "Арилалкил" означает арилалкильную группу, в которой арил и алкил являются такими, как определено выше. Предпочтительные аралкилы включают низшую алкильную группу. Неограничивающие примеры подходящих аралкильных групп включают бензильную, 2-фенетильную и нафталинилметильную. Связь с основным фрагментом осуществляется через алкил.
"Алкиларил" означает алкиларильную группу, в которой алкил и арил являются такими, как определено выше. Предпочтительные алкиларилы включают низшую алкильную группу. Неограничивающим примером подходящих алкиларильных групп является толил. Связь с основным фрагментом осуществляется через арил.
"Циклоалкил" означает неароматическую моно- или полициклическую кольцевую систему, содержащую от примерно 3 до примерно 10 атомов углерода, предпочтительно - от примерно 5 до примерно 10 атомов углерода. Предпочтительные циклоалкильные кольца содержат от примерно 5 до примерно 7 кольцевых атомов. Циклоалкил необязательно может быть замещен одним или несколькими "заместителями кольцевой системы", которые могут быть одинаковыми или разными и являются такими, как определено выше. Неограничивающие примеры подходящих моноциклических циклоалкилов включают циклопропил, циклопентил, циклогексил, циклогептил и т.п. Неограничивающие примеры подходящих полициклических циклоалкилов включают 1-декалинил, норборнил, адамантил и т.п., а также частично насыщенные системы, такие как, например, инданил, тетрагидронафтил и т.п.
"Галоген" означает фтор, хлор, бром или йод. Предпочтительными галогенами являются фтор, хлор и бром.
"Заместитель кольцевой системы" означает заместитель, присоединенный к ароматической или неароматической кольцевой системе, который, например, замещает имеющийся в кольцевой системе водород. Заместители кольцевой системы могут быть одинаковыми или разными, причем каждый независимо выбран из группы, включающей алкил, алкенил, алкинил, арил, гетероарил, аралкил, алкиларил, гетероаралкил, гетероарилалкенил, гетероарилалкинил, алкилгетероарил, гидроксигруппу, гидроксиалкил, алкоксигруппу, арилоксигруппу, аралкоксигруппу, ацил, ароил, галоген, нитрогруппу, цианогруппу, карбоксил, алкоксикарбонил, арилоксикарбонил, аралкоксикарбонил, алкилсульфонил, арилсульфонил, гетероарилсульфонил, алкилтиогруппу, арилтиогруппу, гетероарилтиогруппу, аралкилтиогруппу, гетероаралкилтиогруппу, циклоалкил, гетероциклил, -C(=N-CN)-NH2, -C(=NH)-NH2, -C(=NH)-NH(алкил), Y1Y2N-, Y1Y2N-алкил-, Y1Y2NC(O)-, Y1Y2NSO2- и -SO2NY1Y2, в которых Y1 и Y2 могут быть одинаковыми или разными и независимо выбраны из группы, включающей водород, алкил, арил, циклоалкил и арилалкил. "Заместитель кольцевой системы" также может означать один фрагмент, который одновременно замещает два доступных атома водорода у двух соседних атомов углерода (один Н у каждого атома углерода) кольцевой системы. Примерами таких фрагментов являются метилендиоксигруппа, этилендиоксигруппа, -С(СН3)2- и т.п., которые образуют фрагменты, такие как, например:
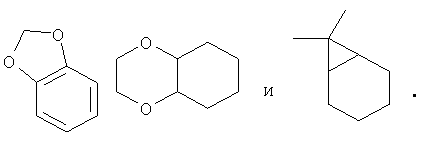
"Гетероциклил" означает неароматическую насыщенную моноциклическую или полициклическую кольцевую систему, содержащую от примерно 3 до примерно 10 атомов в кольце, предпочтительно - от примерно 5 до примерно 10 атомов в кольце, в которой один или несколько атомов кольцевой системы представляет собой элемент, не являющийся углеродом, например азот, кислород или серу, по отдельности или в комбинации. В кольцевой системе не имеется соседних атомов кислорода и/или серы. Предпочтительные гетероциклилы содержат от примерно 5 до примерно 6 атомов в кольце. Приставка аза-, окса- или тиа- перед названием гетероциклильной системы означает, что в качестве атома кольца содержится не менее одного атома азота, кислорода или серы соответственно. Любая группа - NH в гетероциклильном кольце может находиться в защищенном виде, таком как, например, в виде группы -N(Boc), -N(CBz), -N(Tos) и т.п.; такая защита также считается частью настоящего изобретения. Гетероциклил может быть необязательно замещен одним или несколькими "заместителями кольцевой системы", которые могут быть одинаковыми или разными, и являются такими, как определено выше. Атом азота или серы гетероциклила необязательно может быть окислен с образованием соответствующего N-оксида, S-оксида или S,S-диоксида. Неограничивающие примеры моноциклических гетероциклильных колец включают пиперидил, пирролидинил, пиперазинил, морфолинил, тиоморфолинил, тиазолидинил, 1,4-диоксанил, тетрагидрофуранил, тетрагидротиофенил, лактам, лактон и т.п.
Следует отметить, что в содержащих гетероатом кольцевых системах, соответствующих настоящему изобретению, не имеется гидроксильных групп у атомов углерода, соседних с N, О и S, а также не имеется групп N или S у атомов углерода, соседних с другим гетероатомом. Таким образом, например, в кольце:
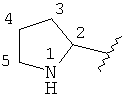
отсутствуют группы -ОН, присоединенные непосредственно к атомам углерода, отмеченным цифрами 2 и 5.
Также следует отметить, что таутомерные формы, такие как, например, фрагменты:
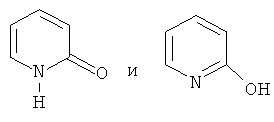
в некоторых вариантах осуществления настоящего изобретения считаются эквивалентными.
"Алкинилалкил" означает алкинилалкильную группу, в которой алкинил и алкил являются такими, как определено выше. Предпочтительные алкинилалкилы содержат низшую алкинильную и низшую алкильную группы. Связь с основным фрагментом осуществляется через алкил. Неограничивающие примеры подходящих алкинилалкильных групп включают пропаргилметил.
"Гетероаралкил" означает гетероаралкильную группу, в которой гетероарил и алкил являются такими, как определено выше. Предпочтительные гетероаралкилы содержат низшую алкильную группу. Неограничивающие примеры подходящих аралкильных групп включают пиридилметил и хинолин-3-илметил. Связь с основным фрагментом осуществляется через алкил.
"Гидроксиалкил" означает группу НО-алкил-, в которой алкил является таким, как определено выше. Предпочтительный гидроксиалкил содержит низший алкил. Неограничивающие примеры подходящих гидроксиалкильных групп включают гидроксиметил и 2-гидроксиэтил.
"Ацил" означает Н-С(О)-, алкил-С(О)- или циклоалкил-С(O)-группу, в которой разные группы являются такими, как описано ранее. Связь с основным фрагментом осуществляется через карбонильную группу. Предпочтительные ацилы содержат низший алкил. Неограничивающие примеры подходящих ацильных групп включают формил, ацетил и пропаноил.
"Ароил" означает группу арил-С(О)-, в которой арильная группа является такой, как описано выше. Связь с основным фрагментом осуществляется через карбонил. Неограничивающие примеры подходящих групп включают бензоил и 1-нафтоил.
"Алкоксигруппа" означает группу алкил-O-, в которой алкильная группа является такой, как описано выше. Неограничивающие примеры подходящих алкоксигрупп включают метоксигруппу, этоксигруппу, н-пропоксигруппу, изопропоксигруппу и н-бутоксигруппу. Связь с основным фрагментом осуществляется через эфирный атом кислорода.
"Арилоксигруппа" означает группу арил-O-, в которой арильная группа является такой, как описано выше. Неограничивающие примеры подходящих арилоксигрупп включают феноксигруппу и нафтоксигруппу. Связь с основным фрагментом осуществляется через эфирный атом кислорода.
"Аралкилоксигруппа" означает группу аралкил-O-, в которой аралкилгруппа является такой, как описано выше. Неограничивающие примеры подходящих аралкилоксигрупп включают бензилоксигруппу и 1- и 2-нафталенметоксигруппу. Связь с основным фрагментом осуществляется через эфирный атом кислорода.
"Алкилтиогруппа" означает группу алкил-S-, в которой алкильная группа является такой, как описано выше. Неограничивающие примеры подходящих алкилтиогрупп включают метилтиогруппу и этилтиогруппу. Связь с основным фрагментом осуществляется через атом серы.
"Арилтиогруппа" означает группу арил-S-, в которой арильная группа является такой, как описано выше. Неограничивающие примеры подходящих арилтиогрупп включают фенилтиогруппу и нафтилтиогруппу. Связь с основным фрагментом осуществляется через атом серы.
"Аралкилтиогруппа" означает группу аралкил-S-, в которой аралкильная группа является такой, как описано выше. Неограничивающим примером подходящей аралкилтиогруппы является бензилтиогруппа. Связь с основным фрагментом осуществляется через атом серы.
"Алкоксикарбонил" означает группу алкил-O-СО-. Неограничивающие примеры подходящих алкоксикарбонильных групп включают метоксикарбонил и этоксикарбонил. Связь с основным фрагментом осуществляется через карбонил.
"Арилоксикарбонил" означает группу арил-О-С(О)-, Неограничивающие примеры подходящих арилоксикарбонильных групп включают феноксикарбонил и нафтоксикарбонил. Связь с основным фрагментом осуществляется через карбонил.
"Аралкоксикарбонил" означает группу аралкил-О-С(О)-, Неограничивающим примером подходящей аралкоксикарбонильной группы является бензилоксикарбонил. Связь с основным фрагментом осуществляется через карбонил.
"Алкилсульфонил" означает группу алкил-S(O2)-. Предпочтительными группами являются такие, в которых алкильными группами является низший алкил. Связь с основным фрагментом осуществляется через сульфонил.
"Арилсульфонил" означает группу арил-S(O2)-. Связь с основным фрагментом осуществляется через сульфонил.
Термин "замещенный" означает, что один или большее количество атомов водорода указанного атома заменены с выбором из указанной группы при условии, что в имеющейся ситуации нормальная валентность указанного атома не превышена и что замещение приводит к стабильному соединению. Комбинации заместителей и/или параметров допустимы только в случае, если такие комбинации приводят к стабильным соединениям. Под "стабильным соединением" или "стабильной структурой" понимается соединение, которое является достаточно прочным, чтобы выдержать выделение из реакционной смеси до пригодной к использованию степени чистоты, и пригодным для включения в эффективный терапевтический препарат.
Термин "необязательно замещенный" означает необязательное замещение указанными группами, радикалами или фрагментами.
Термин "выделенное" или "в выделенной форме" применительно к соединению относится к физическому состоянию указанного соединения после выделения в результате осуществления синтеза или из натурального источника, или их комбинации. Термин "очищенное" или "в очищенной форме" применительно к соединению относится к физическому состоянию указанного соединения после получения с помощью способа или способов очистки, описанных в настоящем изобретении или хорошо известных специалисту в данной области техники, при достаточной чистоте, охарактеризованной стандартными способами анализа, описанными в настоящем изобретении или хорошо известными специалисту в данной области техники.
Также следует отметить, что в тексте, на схемах, в примерах и таблицах, приведенных в настоящем изобретении, подразумевается, что любой углеродный атом, а также гетероатом с ненасыщенными валентностями обладает атомом (атомами) водорода, достаточными для насыщения валентностей.
Если функциональная группа в соединении названа "обладающей защитной группой", это означает, что эта группа находится в модифицированной форме для исключения нежелательных побочных реакций по месту защиты в случае, когда соединение вводят в реакцию. Подходящие защитные группы должны быть известны специалистам с общей подготовкой в данной области техники и описаны в стандартных учебниках, таких как, например, Т.W.Greene et al., Protective Groups in Organic Synthesis (1991), Wiley, New York, который включен в настоящее изобретение для ссылки.
Если какая-либо переменная (например, арил, гетероцикл, R2 и т.п.) в любом компоненте или в формуле I встречается более одного раза, то в каждом случае ее определение не зависит от ее определения в любом другом случае.
При использовании в настоящем изобретении подразумевается, что термин "композиция" охватывает продукт, включающий указанные ингредиенты в указанных количествах, а также любой продукт, который образуется, прямо или косвенно, из комбинации указанных ингредиентов в указанных количествах.
Настоящее изобретение также включает пролекарства и сольваты соединений, соответствующих настоящему изобретению. При использовании в настоящем изобретении термин "пролекарство" означает соединение, которое является предшественником лекарственного средства, которое после введения субъекту подвергается химическим превращениям вследствие протекания метаболических или химических процессов с образованием соединения формулы I или его соли и/или сольвата. Обсуждение пролекарств приведено в публикациях Т.Higuchi and V.Stella. Pro-drugs as Novel Delivery Systems (1987) 14 of the A.C.S. Symposium Series, и Bioreversible Carriers in Drug Design, (1987) Edward B. Roche, ed., American Pharmaceutical Association and Pergamon Press, которые включены в настоящее изобретение в качестве ссылки.
"Сольват" означает физическую ассоциацию соединения, соответствующего настоящему изобретению, с одной или большим количеством молекул растворителя. Эта физическая ассоциация включает разные количества ионных и ковалентных связей, включая водородную связь. В некоторых случаях сольват пригоден для выделения, например когда одна или большее количество молекул растворителя включены в кристаллическую решетку кристаллического твердого вещества. "Сольват" включает и растворенную фазу, и способные к выделению сольваты. Неограничивающие примеры подходящих сольватов включают этаноляты, метаноляты и т.п. "Гидрат" является сольватом, в котором молекулой растворителя является H2O.
Фармацевтически приемлемые сложные эфиры соединений, соответствующих настоящему изобретению, включают следующие группы: (1) эфиры карбоновых кислот, полученные этерификацией гидроксигрупп, в которых некарбонильный фрагмент участка карбоновой кислоты эфирной группы выбран из группы, включающей алкил с линейной или разветвленной цепью (например, ацетил, н-пропил, трет-бутил или н-бутил), алкоксиалкил (например, метоксиметил), аралкил (например, бензил), арилоксиалкил (например, феноксиметил), арил (например, фенил, необязательно замещенный, например, галогеном, С1-4алкилом или С1-4алкоксигруппой или аминогруппой); (2) сульфонатные эфиры, такие как алкил- или аралкилсульфонил (например, метансульфонил); (3) эфиры аминокислот (например, L-валил или L-изолейцил); (4) фосфонатные эфиры и (5) моно-, ди- или трифосфатные эфиры. Фосфатные эфиры могут быть дополнительно этерифицированы, например, С1-20спиртом или его реакционноспособным производным или 2,3-ди(С6-24)ацилглицерином.
Подразумевается, что "эффективное количество" или "терапевтически эффективное количество" описывает количество соединения или композиции, соответствующей настоящему изобретению, эффективное для подавления заболеваний, указанных выше, и тем самым приводящее к необходимому терапевтическому, облегчающему течение заболевания, подавляющему заболевание или предупредительному воздействию.
Соединения формулы IA или IB могут образовывать соли, которые также входят в объем настоящего изобретения. Если не указано иного, то следует понимать, что ссылка на соединение формулы I означает включение ссылки на его соли. При использовании в настоящем изобретении термин "соль (соли)" означает кислые соли, образованные неорганическими и/или органическими кислотами, а также основные соли, образованные неорганическими и/или органическими основаниями. Кроме того, если соединение формулы I содержит и основной фрагмент, такой как (без наложения ограничений) пиридин или имидазол, и кислотный фрагмент, такой как (без наложения ограничений) карбоновая кислота, то могут образоваться цвиттерионы ("внутренние соли") и при использовании в настоящем изобретении они включены в содержание термина "соль (соли)". Предпочтительны фармацевтически приемлемые (т.е. нетоксичные, физиологически приемлемые) соли, хотя применимы и другие соли. Соли соединений формулы I могут образовываться, например, с помощью реакции соединения формулы I с количеством кислоты или основания, таким как эквивалентное количество, в среде, такой как среда, в которой соль осаждается, или в водной среде с последующей лиофилизацией.
Типичные соли присоединения кислоты включают ацетаты, аскорбаты, бензоаты, бензолсульфонаты, бисульфаты, бораты, бутираты, цитраты, камфораты, камфорсульфонаты, фумараты, гидрохлориды, гидробромиды, гидройодиды, лактаты, малеаты, метансульфонаты, нафталинсульфонаты, нитраты, оксалаты, фосфаты, пропионаты, сукцинаты, сульфаты, тартраты, тиоцианаты, толуолсульфонаты (также известные под названием тозилатов) и т.п. Кроме того, рассматриваются кислоты, которые обычно считаются подходящими для образования фармацевтически пригодных солей из основных фармацевтических соединений, например, см. публикации Р. Stahl et al, Camille G. (eds.) Handbook of Pharmaceutical Salts. Properties, Selection and Use. (2002) Zurich: Wiley-VCH; S. Berge et al, Journal of Pharmactutical Sciences (1977) 66(1) 1-19; P. Gould, International J. of Pharmaceutics (1986) 33 201-217; Anderson et al, Practice of Medicinal Chemistry(1996), Academic Press, New York; и The Orange Book (Food & Drug Administration, Washington, D.C. on their website). Эти описания включены в настоящее изобретение в качестве ссылки.
Типичные основные соли включают соли аммония, соли щелочных металлов, такие как соли натрия, лития и калия, соли щелочноземельных металлов, такие как соли кальция и магния, соли с органическим основаниями (например, органическими аминами), такими как дициклогексиламины, трет-бутиламины, и соли с аминокислотами, такими как аргинин, лизин и т.п. Основные азотсодержащие группы могут быть превращены в четвертичные группы с помощью таких соединений, как галогениды низших алкилов (например, метил-, этил- и бутилхлориды, -бромиды и -йодиды), диалкилсульфаты (например, диметил-, диэтил- и дибутилсульфаты), галогениды с длинными цепями (например, децил-, лаурил- и стеарилхлориды, -бромиды и -йодиды), аралкилгалогениды (например, бензил- и фенетилбромиды) и др.
В объеме настоящего изобретения подразумевается, что все такие кислые и основные соли являются фармацевтически приемлемыми солями, и для задач настоящего изобретения все кислотные и основные соли считаются эквивалентными свободным формам соответствующих соединений.
Одно или большее количество соединений, соответствующих настоящему изобретению, также может существовать в виде сольвата или может быть необязательно превращено в него. Получение сольватов является известным. Так, например, М.Caira et al, J. Pharmaceutical Sci., 93(3). 601-611 (2004) описали получение сольватов противогрибкового средства флуконазола с этилацетатом, а также с водой. Аналогичное получение сольватов, гемисольвата, гидратов и т.п. описаны в Е.С. van Tender et al, AAPS PharmSciTech., 5(1), article 12 (2004); и A.L.Bingham et al, Chem. Commun., 603-604 (2001). Типичная неограниичивающая методика включает растворение соединения, соответствующего настоящему изобретению, в необходимом количестве соответствующего растворителя (органического, или воды или их смесей) при температуре, большей температуры окружающей среды, и охлаждение раствора со скоростью, достаточной для образования кристаллов, которые затем выделяют по стандартным методикам. Аналитические методики, такие как, нарпимер, ИК-спектроскопия, показывают наличие растворителя (или воды) в кристаллах сольвата (или гидрата).
Соединения формулы IA, формулы IB и их соли, сольваты, сложные эфиры и пролекарства могут существовать в своих таутомерных формах (например, в виде простого амидо- или иминоэфира). Подразумевается, что все такие таутомерные формы являются частью настоящего изобретения.
В объем настоящего изобретения входят все стереоизомеры (например, геометрические изомеры, оптические изомеры и т.п.) соединений, соответствующих настоящему изобретению (включая изомеры солей, сольватов, сложных эфиров и пролекарств этих соединений, а также соли и сольваты и сложные эфиры пролекарств), такие как те, которые могут существовать вследствие наличия асимметрических атомов углерода в различных заместителях, включая энантиомерные формы (которые могут существовать даже при отсутствии асимметрических атомов углерода), поворотные изомерные формы, атропоизомерные и диастереоизомерные формы, а также позиционные изомеры (такие как, например, 4-пиридил и 3-пиридил). Отдельные стереоизомеры соединений, соответствующих настоящему изобретению, могут, например, в основном не содержать других изомеров или могут быть смешаны, например, как рацематы, или со всеми другими, или с другими выбранными стереоизомерами. Хиральные центры, соответствующие настоящему изобретению, могут обладать S- или R-конфигурацией в соответствии с определением, приведенным в IUPAC 1974 Recommendations. Подразумевается, что при использовании терминов "соль", "сольват", "сложный эфир", "пролекарство" и т.п. они в равной степени применимы к соли, сольвату, сложному эфиру и пролекарству энантиомеров, стереоизомеров, поворотных изомеров, таутомеров, позиционных изомеров, рацематов и пролекарств соединений, соответствующих настоящему изобретению.
Полиморфные формы соединений формулы IA и IB и солей, сольватов, сложных эфиров и пролекарств соединений формулы I считаются включенными в настоящее изобретение.
Соединения формулы IA и IB можно использовать в качестве ингибиторов CCR5 и для лечения и предупреждения заболеваний, связанных с CCR5 и вирусом иммунодефицита человека. Их можно использовать для лечения, предупреждения и/или облегчения протекания заболеваний, таких как, например, синдром приобретенного иммунодефицита ("СПИД"), отторжения цельного органа, реакция "трансплантат против хозяина", артрит, ревматоидный артрит, воспалительная болезнь кишечника, атонический дерматит, псориаз, астма, аллергии или рассеянный склероз. Таким образом, в одном варианте осуществления настоящее изобретение относится к фармацевтической композиции, предназначенной для лечения инфекции ВИЧ, включающей одно или большее количество соединений формулы IA или формулы IB.
В еще одном варианте осуществления настоящее изобретение относится к способу лечения инфекции, вызванной вирусом иммунодефицита человека, включающему введение пациенту, нуждающемуся в таком лечении, терапевтически эффективного количества одного или большего количества соединений формулы IA или IB. В другом варианте осуществления настоящее изобретение относится к способу лечения отторжения цельного органа, реакции "трансплантат против хозяина", артрита, ревматоидного артрита, воспалительной болезни кишечника, атопического дерматита, псориаза, астмы, аллергий или рассеянного склероза, включающему введение пациенту, нуждающемуся в таком лечении, терапевтически эффективного количества одного или более соединений формулы IA или IB.
В еще одном варианте осуществления настоящее изобретение относится к способу лечения инфекции, вызванной вирусом иммунодефицита человека, включающему введение пациенту, нуждающемуся в таком лечении, одного или более соединений формулы IA или IB в комбинации с одним или большим количеством противовирусных или других средств, применимых для лечения. В другом варианте осуществления настоящее изобретение относится к способу лечения отторжения цельного органа, реакции "трансплантат против хозяина", артрита, ревматоидного артрита, воспалительной болезни кишечника, атонического дерматита, псориаза, астмы или аллергий, включающему введение пациенту, нуждающемуся в таком лечении, одного или большего количества соединений формулы IA или IB в комбинации с одним или большим количеством противовирусных или других средств, применимых для лечения. CCR5 и противовирусные или другие средства, которые являются компонентами комбинации, можно вводить в одной дозированной форме или по отдельности. В объем настоящего изобретения также входит набор, включающий отдельные дозированные формы активных средств.
Неограниченные примеры таких комбинированных средств включают нуклеозидные и нуклеотидные ингибиторы обратной транскриптазы ("НИОТ"), ненуклеозидные ингибиторы обратной транскриптазы ("ННИОТ"), ингибиторы протеазы ("ИП"), другие противовирусные средства, анти-ВИЧ лекарственные средства и т.п.
Термин "нуклеозидные и нуклеотидные ингибиторы обратной транскриптазы" ("НИОТ") при использовании в настоящем изобретении означает нуклеозиды и нуклеотиды и их аналоги, которые ингибируют активность обратной транскриптазы ВИЧ-1, т.е. фермента, который катализирует превращение вирусной геномной РНК ВИЧ-1 в провирусную ДНК ВИЧ-1.
Типичные подходящие НИОТ включают зидовудин (AZT), выпускающийся под торговым названием RETROVIR компанией Glaxo-Wellcome Inc., Research Triangle, NC 27709; диданозин (ddl), выпускающийся под торговым названием VIDEX компанией Bristol-Myers Squibb Co., Princeton, NJ 08543; залцитабин (ddC), выпускающийся под торговым названием HIVID компанией Roche Pharmaceuticals, Nutley, NJ 07110; ставудин (d4T), выпускающийся под торговым названием ZERIT компанией Bristol-Myers Squibb Co., Princeton, NJ 08543; ламивудин (3ТС), выпускающийся под торговым названием EPIVIR компанией Glaxo-Wellcome Research Triangle, NC 27709; абакавир (1592U89), раскрытый в WO 96/30025 и выпускающийся под торговым названием ZIAGEN компанией Glaxo-Wellcome Research Triangle, NC 27709; адефовир дипивоксил [бис(РОМ)-РМЕА], выпускающийся под торговым названием PREVON компанией Gilead Sciences, Foster City, CA 94404; лобукавир (BMS-180194), нуклеозидный ингибитор обратной транскриптазы, раскрытый в ЕР-0358154 и ЕР-0736533 и разрабатывающийся компанией Bristol-Myers Squibb, Princeton, NJ 08543; BCH-10652, ингибитор обратной транскриптазы (в виде рацемической смеси ВСН-10618 и ВСН-10619), разрабатывающийся компанией Biochem Pharma, Laval, Quebec H7V, 4A7, Canada; эмитрицитабин [(-)-FTC], лицензия на который выдана Emory University в соответствии с патентом US №5814639, и разрабатывающийся компанией Triangle Pharmaceuticals, Durham, NC 27707; бета-L-FD4 (также обозначаемый как бета-L-D4C и обладающий названием бета-L-2',3'-диклеокси-5-фторцитидена), лицензия на который выдана Yale University компании Vion Pharmaceuticals, New Haven CT 06511; DAPD, пуриновый нуклеозид, (-)-бета-D-2,6-диаминопуриндиоксолан, раскрытый в ЕР-0656778, лицензия на который выдана Emory University и University of Georgia компании Triangle Pharmaceuticals, Durham, NC 27707; и лоденозин (FddA), 9-(2, 3-дидеокси-2-фтор-b-D-трео-пентофуранозил)аденин, стабильный по отношению к воздействию кислот ингибитор обратной транскриптазы, открытый компанией NIH и разрабатывающийся компанией U.S. Bioscience Inc., West Conshohocken, PA 19428.
Термин "ненуклеозидные ингибиторы обратной транскриптазы" при использовании в настоящем изобретении означает ненуклеозиды, которые ингибируют активность обратной транскриптазы ВИЧ-1.
Типичные подходящие ННИОТ включают невирапин (BI-RG-587), выпускающийся под торговым названием VIRAMUNE компанией Boehringer Ingeheim, изготовителем для компании Roxane Laboratories, Columbus, ОН 43216; делавирадин (ВНАР, U-90152), выпускающийся под торговым названием RESCRIPTOR компанией Pharmacia & Upjohn Co., Bridgewater NJ 08807; эфавиренц (DMP-266), бензоксазин-2-он, раскрытый в W094/03440 и выпускающийся под торговым названием SUSTIVA компанией DuPont Pharmaceutical Co., Wilmington. DE 19880-0723; PNU-142721, фуропиридинтиопиримид, разрабатывающийся компанией Pharmacia and Upjohn, Bridgewater NJ 08807; AG-1549 (ранее Shionogi # S-1153); 5-(3,5-дихлорфенил)-тио-4-изопропил-1 -(4-пиридил)метил-1Н-имидазол-2-илметилкарбонат, раскрытый в WO 96/10019 и клинические исследования которого проводит компания Agouron Pharmaceuticals, Inc., LaJolla CA 92037-1020; MKC-442 (1-(этоксиметил)-5-(1-метилэтил)-6-(фенилметил)-(2,4(1Н,3Н)-пиримидиндион), открытый компанией Mitsubishi Chemical Co. и разрабатывающийся компанией Triangle Pharmaceuticals, Durham, NC 27707; и (+)-каланолид A (NSC-675451) и В, производные кумарина, раскрытые в выданном фирме NIH патенте US No. 5489697, лицензия на который выдана компании Med Chem Research, которая совместно с компанией Vita-Invest разрабатывает (+) каланолид А в качестве препарата для перорального введения.
Термин "ингибитор протеазы" ("ИП") при использовании в настоящем изобретении означает ингибиторы протеазы ВИЧ-1, фермент, необходимый для протеолитического расщепления полипротеиновых предшественников вирусов (например, вирусных полипротеинов GAG и GAG Pol) на индивидуальные функциональные протеины, обнаруживающиеся у инфекционном ВИЧ-1. Ингибиторы протеазы ВИЧ включают соединения, обладающие пептидомиметической структурой, большой молекулярной массой (7600 Да) и обладающие преимущественно пептидными свойствами, например CRIXIVAN (выпускающийся компанией Merck), а также непептидные ингибиторы протеазы, например VIRACEPT (выпускающийся компанией Agouron).
Типичные подходящие ИП включают саквинавир (Ro 31-8959), выпускающийся в капсулах из твердого желатина под торговым названием INVIRASE и капсулах из мягкого желатина под торговым названием RORTOVASE компанией Roche Pharmaceuticals, Nutley, NJ 07110-1199; ритонавир (АВТ-538), выпускающийся под торговым названием NORVIR компанией Abbott Laboratories, Abbott Park, IL 60064; индинавир (МК-639), выпускающийся под торговым названием CRIXIVAN компанией Merck & Co., Inc., West Point, PA 19486-0004; нелфнавир (AG-1343), выпускающийся под торговым названием VIRACEPT компанией Agouron Pharmaceuticals, Inc., LaJolla CA 92037-1020; ампренавир (141W94), торговое название AGENERASE, непептидный ингибитор протеазы, разрабатывающийся компанией Vertex Pharmaceuticals, Inc., Cambridge, MA 02139-4211 и выпускающийся компанией Glaxo-Wellcome, Research Triangle, NC, в соответствии с программой расширенного доступа к лекарственным средствам; лазинавир (BMS-234475), выпускающийся компанией Bristol-Myers Squibb, Princeton, NJ 08543 (впервые открытый компанией Novartis, Basel, Switzerland (CGP-61755); DMP-450, циклическая мочевина, открытая компанией Dupont и разрабатывающаяся компанией Triangle Pharmaceuticals; BMS-2322623, азапептид, разрабатывающийся компанией Bristol-Myers Squibb, Princeton, NJ 08543, в качестве ВИЧ-1 ИП 2-го поколения; АВТ-378, разрабатывающийся компанией Abbott, Abbott Park, IL 60064; и AG-1549, активный при пероральном введении имидазолкарбамат, открытый компанией Shionogi (Shionogi #S-1153) и разрабатывающийся компанией Agouron Pharmaceuticals, Inc., LaJolla CA 92037-1020.
Другие противовирусные средства включают гидроксимочевину, рибавирин, IL-2, IL-12, пентафузид и Yissum Project No. 11607. Гидроксимочевина (Droxia), ингибитор рибонуклеозидтрифосфатредуктазы, т.е. фермента, участвующего в активации Т-клеток, была открыта NCI и разрабатывается компанией Bristoi-Myers Squibb; при доклинических исследованиях показано, что она оказывает синергетическое воздействие на активность диданозина, и она исследована со ставудином. IL-2 раскрыли Ajinomoto EP-0142268, Takeda EP-0176299 и компания Chiron в патентах US №№ RE 33653, 4530787, 4569790, 4604377, 4748234, 4752585 и 4949314, и он выпускается под торговым названием PROLEUKIN (алдеслейкин) Chiron Corp., Emeryville, CA 94608-2997 в виде лиофилизированного порошка для внутривенного вливания или подкожного введения после восстановления и разбавления водой; для подкожного введения предпочтительна доза, составляющая от примерно 1 до примерно 20 млн МЕ/сутки, для подкожного введения более предпочтительна доза, составляющая примерно 15 млн МЕ/сутки, предпочтительно подкожное введение. IL-12 раскрыт в WO 96/25171 и выпускается компаниями Roche Pharmaceuticals, Nutley, NJ 07110-1199 и American Home Products, Madison, NJ 07940; вводится в дозах, составляющих от примерно 0,5 до примерно 10 мкг/кг/сутки, предпочтительно подкожное введение. Пентафузид (DP-178, Т-20, состоящий из 36 аминокислотных остатков синтетический пептид, раскрыт в патенте US №№5464933, лицензия на который выдана Duke University компании Trimeris, которая разрабатывает пентафузид совместно с Duke University; пентафузид воздействует путем ингибирования слияния ВИЧ-1 с мембранами-мишенями. Пентафузид (3-100 мг/сутки) выпускается для непрерывного подкожного вливания или инъекции совместно с эфавиренцем и двумя ИП для пациентов, обладающих положительной реакцией на ВИЧ-1 и невосприимчивых по отношению к комбинированной терапии с применением 3 средств; предпочтительно применять 100 мг/сутки. Yissum Project No. 11607, синтетический белок на основе белка ВИЧ-1 Vif, проходит доклинические исследования в компании Yissum Research Development Co., Jerusalem 91042, Israel. Рибавирин, 1-β-D-рибофуранозил-1Н-1,2,4-триазол-3-карбоксамид, выпускается компанией ICN Pharmaceuticals, Inc., Costa Mesa, CA; его получение и содержащий его препарат описаны в патенте US №4211771.
Термин "анти-ВИЧ-1 терапия" при использовании в настоящем изобретении означает любое анти-ВИЧ-1 лекарственное средство, для которого обнаружена применимость для лечения инфекции ВИЧ-1 у людей при использовании в качестве единственного средства или в качестве компонента при методиках комбинированной терапии с применением нескольких лекарственных средств, в особенности комбинированной терапии ВААРТ с применением 3 и 4 лекарственных средств. Типичные подходящие известные анти-ВИЧ-1 терапии включают, но не ограничиваются только ими, терапии с применением нескольких лекарственных средств, такие как включающие (i) не менее трех анти-ВИЧ-1 лекарственных средств, выбранных из группы, включающей два НИОТ, один ИП, второй ИП и один ННИОТ; и (ii) не менее двух анти-ВИЧ-1 лекарственных средств, выбранных из группы, включающей различные ННИОТ и ИП. Типичные подходящие методики ВААРТ - комбинированная терапия с применением нескольких лекарственных средств, включают:
(а) методики комбинированной терапии с применением 3 лекарственных средств, таких как два НИОТ и один ИП; или (b) два НИОТ и один ННИОТ; и (с) методики комбинированной терапии с применением 4 лекарственных препаратов, таких как два НИОТ, один ИП и второй ИП или один ННИОТ. При лечении интактных пациентов предпочтительно начинать анти-ВИЧ-1 лечения с комбинированной терапии с применением 3 лекарственных средств; если отсутствует непереносимость ИП, то предпочтительно применять два НИОТ и один ИП. Важно соблюдение режима лечения. Каждые 3-6 месяцев необходимо проводить мониторинг содержания в плазме CD4+ и ВИЧ-1-РНК. Если вирусная нагрузка устанавливается на постоянном уровне, то можно добавить четвертое лекарственное средство, например один ИП или один ННИОТ.
В приведенной ниже таблице описаны дополнительные типичные терапии:
АНТИ-ВИЧ-1 КОМБИНИРОВАННЫЕ ТЕРАПИИ С ПРИМЕНЕНИЕМ НЕСКОЛЬКИХ ЛЕКАРСТВЕННЫХ СРЕДСТВ
А. Комбинированные терапии с применением 3 средств
1. Два НИОТ1 + один ИП2
2. Два НИОТ1 + один ННИОТ3
В. Комбинированные терапии с применением 4 средств4
Два НИОТ + один ИП + второй ИП или один ННИОТ
С. АЛЬТЕРНАТИВЫ:5
Два НИОТ1
Один НИОТ5 + один ИП2
Два ИП6 + один НИОТ7 или ННИОТ3
Один ИП2 + один НИОТ7 + один ННИОТ3
ПРИМЕЧАНИЯ К ТАБЛИЦЕ
1. Одно из следующих: зидовудин + ламивудин; зидовудин + диданозин; ставудин + ламивудин; ставудин + диданозин; зидовудин + альцитабин.
2. Индинавир, нелфинавир, ритонавир или саквинавир капсулы из мягкого желатина.
3. Невирапин или делавирдин.
4. См. А-М.Vandamne et al Antiviral Chemistry & Chemotherapy 9:187 стр.193-197 и фиг.1+2.
5. Альтернативные режимы предназначены для пациентов, которые не способны соблюдают рекомендованный режим из-за проблем комплаентности и токсичности, и для тех, для которых рекомендованный режим не приводит к положительным результатам лечения или приводит к рецидивам. Комбинации двух нуклеозидов для многих пациентов могут привести к резистентности по отношению к ВИЧ и к неудаче лечения.
6. Большая часть данных получена при использовании саквинавира и ритонавира (каждый вводят по 400 мг два раза в сутки).
7. Зидовудин, ставудин или диданозин.
В другом варианте осуществления настоящее изобретение относится к способу установления того, вводили ли пациенту соединение формулы
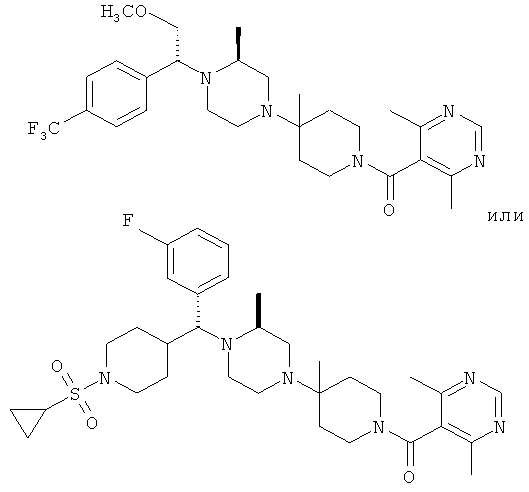
способ включает стадию выявления наличия соединения, описываемого структурной формулой IB, в пробе плазмы, мочи, желчи или фекалий, взятой у пациента.
В другом варианте осуществления настоящее изобретение относится к способу получения соединения, описываемого структурной формулой IC:
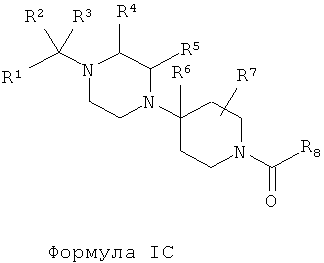
или его фармацевтически приемлемой соли, сольвата или сложного эфира; в которой:
R1 выбран из группы, включающей R9-фенил, R9-пиридил, R9-тиофенил, R9-нафтил и
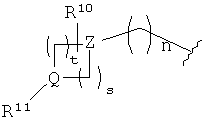 ,
,
R2 выбран из группы, включающей Н и алкил;
R3 выбран из группы, включающей Н, алкил, алкоксиалкил-, циклоалкил, циклоалкилалкил-, R9-арил, R9-арилалкил-, R9-гетероарил и R9-гетероарилалкил-;
или R2 и R3 совместно означают =O, =N(OR12) или =N-N(R13)(R14);
R4, R5, R6 и R7 независимо выбраны из группы, включающей Н и алкил;
R8 выбран из группы, включающей


R9 означает 1, 2 или 3 заместителя, независимо выбранных из группы, включающей Н, галоген, алкил, алкоксигруппу, -CF3, -OCF3, СН3С(О)-, -CN, CH3S(O2)-, CF3S(O2)-, -N(R18)(R19);
R10 выбран из группы, включающей Н и алкил;
R11 выбран из группы, включающей Н, алкил, фторалкил-, R9-арилалкил-, R9-гетероарил-, алкил, алкил-S(O2)-, циклоалкил-S(O2)-, фторалкил-S(O2)-, R9-арил-S(O2)-, R9-гетероарил-S(O2)-, N(R18)(R19)-S(O2)-, алкил-С(О)-, циклоалкил-С(О)-, фторалкил-С(О)-, R9-арил-С(О)-, алкил-NH-С(О)- и R9-арил-NH-C(O)-;
R12 означает Н, алкил, фторалкил-, циклоалкилалкил-, гидроксиалкил-, алкил-O-алкил-, алкил-O-С(O)-алкил- или N(R18)(R19)-С(O)-алкил-;
R13 и R14 независимо выбраны из группы, включающей Н, алкил и циклоалкил, или R13 и R14 совместно означают (С2-С6)алкилен и образуют кольцо с атомом азота, к которому, как показано, они присоединены;
R15 и R16 независимо выбраны из группы, включающей алкил, галоген, -NR18R19, -ОН, -CF3, -ОСН3, -O-ацил и -OCF3;
R17 выбран из группы, включающей R20O-, и R20R21N-;
R18 и R19 независимо выбраны из группы, включающей Н и алкил;
R20 выбран из группы, включающей Н, алкил, галогеналкил циклоалкил, гетероциклил, аралкил, алкиларил, арил и гетероарил;
R21 выбран из группы, включающей Н, алкил, фторалкил-, R9-арилалкил-, R9-гетероарил-, алкил, алкил-S(O2)-, циклоалкил-S(O2)-, фторалкил-S(O2)-, R9-арил-S(O2)-, R9-гетероарил-S(O2)-, N(R18)(R19)-S(O2)-, алкил-С(О)-, циклоалкил-С(О)-, фторалкил-С(О)-, R9-арил-С(О)-, алкил-NH-C(O)- и R9-арил-NH-C(O)-;
Q и Z независимо выбраны из группы, включающей СН и N;
n равно 0, 1, 2, 3 или 4;
s равно 0, 1, 2, 3 или 4; и
t равно 1, 2, 3 или 4;
при условии, что, если n равно 0, то Z означает СН;
включающий реакцию амина формулы
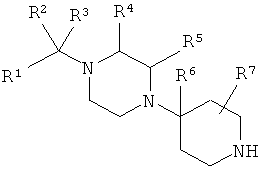
с карбоновой кислотой формулы R8COOH или хлорангидридом кислоты формулы R8C(O)Cl; в которой R1-R8 являются такими, как указано для формулы I.
В одном варианте осуществления указанного выше способа R2 выбран из группы, включающей Н и (С1-С6)алкил;
R3 выбран из группы, включающей Н, (С1-С6)алкил, (С1-С6)алкокси(С1-С6)алкил-, (С3-С10)циклоалкил, (С3-С10)циклоалкил(С1-С6)алкил-, R9-арил, R9-арил(C1-С6)алкил-, R9-гетероарил, и R9-гетероарил(С1-С6)алкил-;
или R2 и R3 совместно означают =O, =N(OR12) или =N-N(R13)(R14);
R4, R5, R6 и R7 независимо выбраны из группы, включающей Н и (С1-С6)алкил;
R8 выбран из группы, включающей


R9 означает 1, 2 или 3 заместителя, независимо выбранных из группы, включающей Н, галоген, (С1-С6)алкил, (С1-С6)алкоксигруппу, -CF3, -OCF3, СН3С(О)-, -CN, CH3S(O2)-, CF3S(O2)-, -N(R18)(R19);
R10 выбран из группы, включающей Н и (С1-С6)алкил;
R11 выбран из группы, включающей Н, (С1-С6)алкил, фтор(С1-С6)алкил-, R9-арил(С1-С6)алкил-, R9-гетероарил-, (С1-С6)алкил, (С1-С6)алкил-S(O2)-, (С3-С6)циклоалкил-S(O2)-, фтор(С1-С6)алкил-S(O2)-, R9-арил-S(O2)-, R9-гетероарил-S(O2)-, N(R18)(R19)-S(O2)-, (С1-С6)алкил-С(O)-, (С3-С6)циклоалкил-С(О)-, фтор(С1-С6)алкил-С(О)-, R9-арил-С(О)-, (С1-С6)алкил-NH-С(O)- и R9-арил-NH-C(O)-;
R12 означает Н, (C1-C6)алкил, фтор(С1-С6)алкил-, (С3-С10)циклоалкил(С1-С6)алкил-, гидрокси(С1-С6)алкил-, (С1-С6)алкил-O-(С2-С6)алкил-, (C1-C6)алкил-O-C(O)- (C1 С6)алкил- или N(R18)(R19)-C(O)- (С1-С6)алкил-;
R13 и R14 независимо выбраны из группы, включающей Н, (С1-С6)алкил и (С3-С10)циклоалкил, или R13 и R14 совместно означают (С2-С6)алкил и образуют кольцо с атомом азота, к которому, как показано, они присоединены;
R15 и R16 независимо выбраны из группы, включающей (С1-С6)алкил, галоген, -NR18R19, -OH, -CF3, -ОСН3, -O-ацил и -OCF3;
R17 выбран из группы, включающей R20O и R20R21N-;
R18 и R19 независимо выбраны из группы, включающей Н и (С1-С6)алкил;
R20 выбран из группы, включающей Н, (С1-С6)алкил, галоген(С1-С6)алкил, (С3-С10)циклоалкил, гетероциклил, арил(С1-С6)алкил, (С1-С6)алкиларил, арил и гетероарил;
R21 выбран из группы, включающей Н, (С1-С6)алкил, фтор-(С1-С6)алкил-, R9-арил(С1-С6)алкил-, R9-гетероарил-, (С1-С6)алкил, (С1-С6)алкил-S(O2)-, цикло(С3-С6)алкил-S(O2)-, фтор(С1-С6)алкил-S(O2)-, R9-арил-S(O2)-, R9-гетероарил-S(O2)-, N(R18)(R19)-S(O2)-, (С1-С6)алкил-С(O)-, (С3-С6)циклоалкил-С(О)-, фтор(С1-С6)алкил-С(O)-, R9-арил-С(О)-, (C1-C6)алкил-NH-C(O)- и R9-арил-NH-C(O)-;
Q и Z независимо выбраны из группы, включающей СН и N;
n равно 0, 1, 2, 3 или 4;
s равно 0, 1, 2, 3 или 4;
и t равно 1, 2, 3 или 4;
при условии, что если n равно 0, то Z означает СН.
В другом варианте осуществления указанного выше способа реакцию амина с карбоновой кислотой или хлорангидридом кислоты проводят в присутствии одного или большего количества связывающих агентов амидирования, таких как 1-гидроксибензотриазол (ГОБТ) и 1-(3-диметиламинопропил)-3-этилкарбодиимид гидрохлорид (ЭДГ).
В другом варианте осуществления настоящее изобретение относится к соединениям, приведенным в таблице 1. В таблице 1 также показаны масс-спектроскопические данные (МСВР - масс-спектроскопия высокого разрешения) для этих соединений.
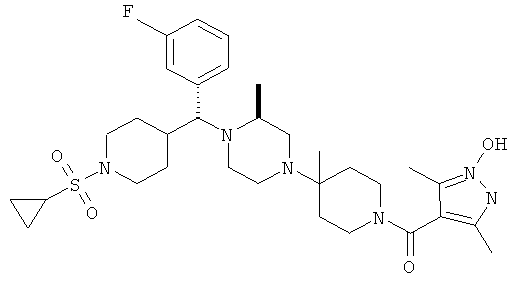
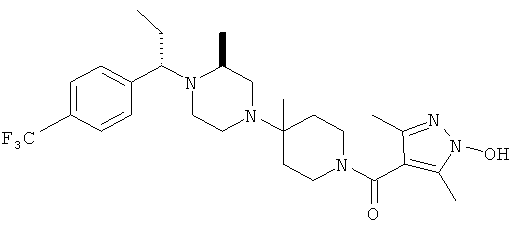
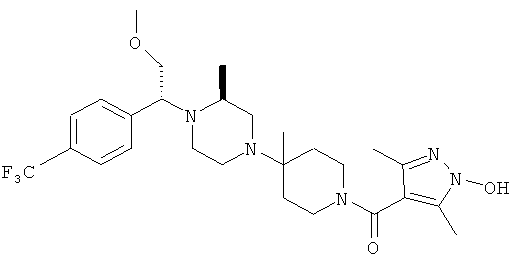
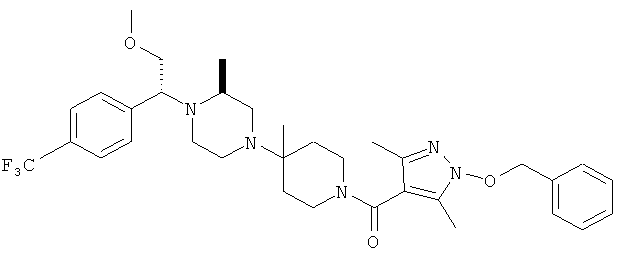
Ниже в таблице 2 также приведены данные по активности (IC50 в наномолях, нМ) для соединений, приведенных в таблице 1, полученные с помощью исследования репликации люциферазы, описанного в следующем разделе настоящей заявки.
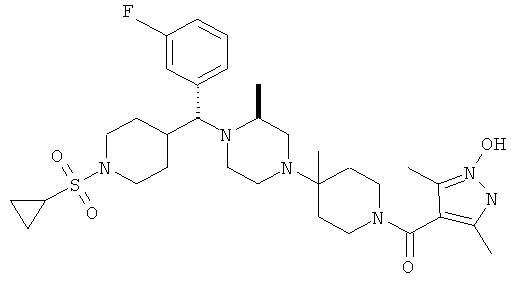
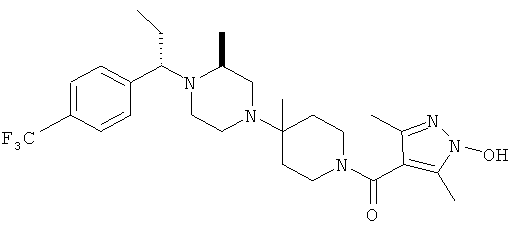
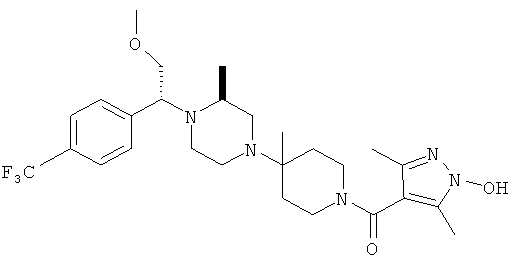

Соединения, соответствующие настоящему изобретению, являются особенно полезными для применения в качестве антагонистов CCR5.
Соединения, соответствующие настоящему изобретению, можно получить по методикам, известным в данной области техники, или по методикам, описанным в приведенных ниже примерах. Приведенные ниже схемы получения и примеры не следует рассматривать в качестве ограничивающих объем настоящего изобретения. Для специалистов в данной области техники должны быть очевидны альтернативные пути и аналогичные структуры, соответствующие объему настоящего изобретения.
Приведенные ниже растворители и реагенты в настоящем изобретении могут быть обозначены указанными аббревиатурами: тетрагидрофуран (ТГФ); этанол (ЕtOН); метанол (МеОН); уксусная кислота (НОАс или АсОН); этилацетат (EtOAc); N,N-диметилформамид (ДМФ); трифторуксусная кислота (ТФК); трифторуксусный ангидрид (ТФУА); 1-гидроксибензотриазол (ГОБТ); м-хлорпербензойная кислота (МХПБА); триэтиламин (Et3N); диэтиловый эфир (Et2O); трет-бутоксикарбонил (ВОС); 1,8-диазабицикло[5.4.0]ундец-7-ен (ДБУ); диметилсульфоксид (ДМСО); п-толуолсульфоновая кислота (п-ТСК); бис(триметилсилил)-амид калия (KHMDA); 4-диметиламинопиридин (ДМАП); N,N,N-диизопропилэтиламин (ДИПЭА); Alloc: аллилоксикарбамат; MeCN: ацетонитрил; и 1-(3-диметиламинопропил)-3-этилкарбодиимид гидрохлорид (ЭДГ). КТ означает комнатную температуру.
Соединения, соответствующие настоящему изобретению, можно получить при стандартных условиях связывания амина с карбоновой кислотой (R8CO2H) (или хлорангидридом карбоновой кислоты, R8C(O)Cl) (схема 1). Типичные примеры приведены ниже.
Схема 1
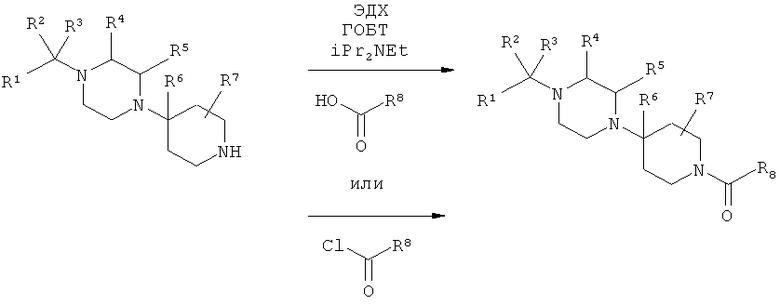
Пример 1
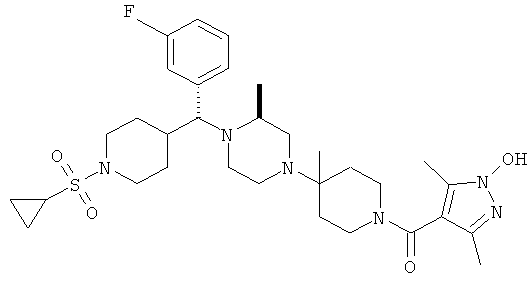
Стадия 1
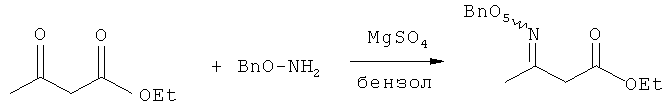
Этилацетоацетат (7,5 г, 58 ммоль) и O-бензилгидроксиламин (7,1 г, 58 ммоль) и MgSO4 (5 г) разбавляют бензолом и перемешивают при 25°С в течение 24 ч. Фильтрование и концентрирование дает оксим.
Стадия 2
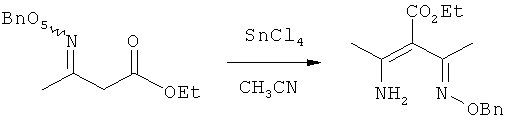
Оксим (1,0 г, 4,25 ммоль) разбавляют с помощью CH3CN (8 мл) и охлаждают до 0°С. К раствору при 0°С по каплям прибавляют SnCl4 (4,3 мл, 1,0 М в CH2Cl2). Раствор перемешивают при 0°С в течение 1 ч. Раствор нейтрализуют насыщенным раствором Na2CO3 (вод.). Смесь экстрагируют с помощью EtOAc. Объединенные органические слои промывают рассолом и сушат (MgSO4). Фильтрование и концентрирование дает бесцветное масло. Очистка с помощью флэш-хроматографии (3/1 гексаны/EtOAc, SiO2) дает 415 мг (35%) енамида в виде бесцветного масла.
Стадия 3
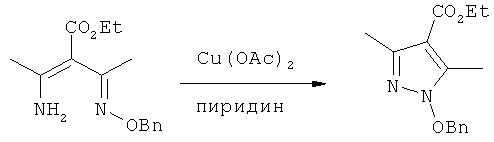
Енамид (415 мг, 1,5 ммоль) и Cu(ОАс)2 (400 мг) разбавляют пиридином. Смесь нагревают при 100°С в течение 4 ч. Раствор охлаждают и концентрируют. Остаток подвергают распределению между EtOAc и 10% NH4OH (вод.) Водный слой экстрагируют с помощью EtOAc. Объединенные органические слои промывают рассолом и сушат (MgSO4). Фильтрование и концентрирование дает коричневое масло. Очистка с помощью флэш-хроматографии (9/1 гексаны/EtOAc, SlO2) дает 330 мг (80%) пиразола в виде бесцветного масла.
Стадия 4
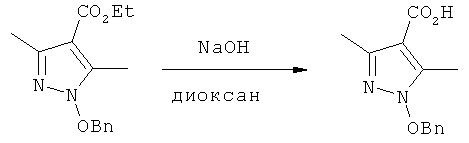
Сложный эфир (545 мг, 1,99 ммоль) и 1 н. NaOH (вод.) разбавляют смесью диоксан/EtOH. Раствор нагревают при 75°С в течение 24 ч. Раствор концентрируют. Раствор подкисляют с помощью 1 М HCl (вод.) (рН=2-3). Образовавшийся белый осадок собирают и сушат в высоком вакууме. Получают кислоту в виде белого порошкообразного вещества (314 мг, 64%). 1Н ЯМР (CDCl3, 400 МГц) δ 2,07 (s, 3Н), 2,46 (s, 3 Н), 5,26 (s, 2Н), 7,25-7,37 (m, 5Н). МСВР рассчитано для C13H15O3N (MH+) 247,1083. Найдено: 247,1089.
Стадия 5
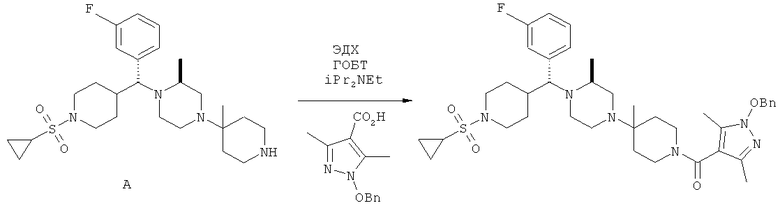
Пиперидин А (синтез А см. ниже; 122 мг, 0,24 ммоль), ЭДГ (56 мг, 0,29 ммоль), ГОБТ (40 мг, 0,29 ммоль), iPr2NEt (93 мг, 0,73 ммоль) и кислоту (61 мг, 0,24 ммоль) разбавляют с помощью CH3CN. Раствор перемешивают при 25°С в течение 18 ч. Раствор концентрируют. Остаток подвергают распределению между EtOAc и 1 н. NaOH (вод.). Водный слой экстрагируют с помощью EtOAc. Объединенные EtOAc слои промывают рассолом и сушат (MgSO4). Фильтрование и концентрированно дает желтое масло. Очистка с помощью препаративной тонкослойной хроматографии 15/1 CH2Cl2/метанол, SiO2 дает амид в виде бесцветного масла (166 мг, 95%). МС низкого разрешения (МН+) 721.
Стадия 6
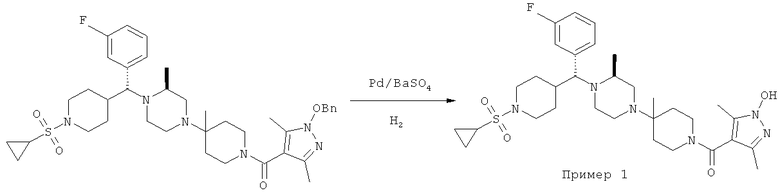
O-Бензиловый эфир (135 мг, 0,19 ммоль) и Pd/BaSO4 (40 мг) разбавляют с помощью МеОН. Смесь помещают в аппарат Парра и подают H2 под давлением 10 фунт-сила/дюйм2. Смесь встряхивают при 25°С в течение 30 мин. Фильтрование дает желтое масло. Очистка с помощью препаративной тонкослойной хроматографии (15/1 CH2Cl2/метанол, SiO2) дает 79 мг (67%) соединения примера 1 (первое соединение в таблице 1) в виде бесцветного масла. Т. пл. (2 НCl): 214-215°С, МСВР рассчитано для C32H48O4N6FS (MH+): 631,3442. Найдено: 631,3433.
Синтез пиперидина А
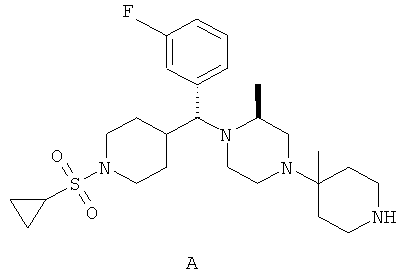
Стадия 1
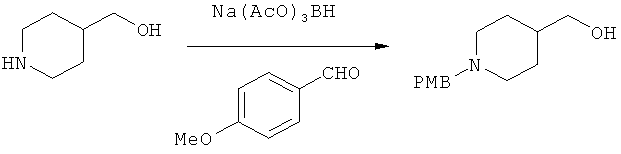
4-Пиперидинметанол (10 г), п-анисовый альдегид (13 мл) и Na(AcO)3BH (22 г) разбавляют с помощью CH2Cl2 (250 мл) и перемешивают при 25°С (19 ч). Раствор разбавляют с помощью CH2Cl2 и промывают с помощью 1 н. NaOH (вод.). Водный слой экстрагируют с помощью CH2Cl2. Объединенные органические слои сушат (Na2SO4), фильтруют и концентрируют и получают желтое масло. Остаток разбавляют с помощью Et2O и промывают с помощью 1 М HCl (вод.). Водный кислый слой экстрагируют с помощью Et2O. Кислый слой охлаждают до 0°С и подщелачивают путем прибавления гранул NaOH (рН 10-12). Смесь экстрагируют с помощью CH2Cl2. Объединенные органические слои сушат (Na2SO4), фильтруют и концентрируют и получают спирт (18,4 г, 90%) в виде густого масла.
Стадия 2
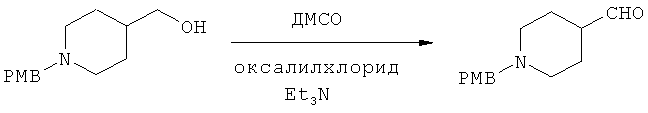
ДМСО (7,2 мл) разбавляют с помощью CH2Cl2 (200 мл), и полученный раствор охлаждают до -40°С (CO2/CH3CN). К раствору при -40°С (механическая мешалка) по каплям прибавляют оксалилхлорид (8,9 мл) в CH2Cl2 (15 мл). После прибавления раствор перемешивают при -40°С в течение 30 мин. К раствору при -40°С прибавляют спирт (18,4 г) в CH2Cl2 (40 мл). После прибавления полученный раствор перемешивают при -40°С в течение 30 мин. К раствору при -40°С прибавляют триэтиламин (33 мл), и в это время образуется осадок. Смесь перемешивают при -40°С в течение 15 мин и затем при 25°С в течение 45 мин. Раствор разбавляют с помощью CH2Cl2 и промывают с помощью 1 н. NaOH (вод.). Водный слой экстрагируют с помощью CH2Cl2. Объединенные органические слои сушат (Na2SO4), фильтруют и концентрируют и получают альдегид в виде желтого масла (17,7 г, 97%).
Стадия 3
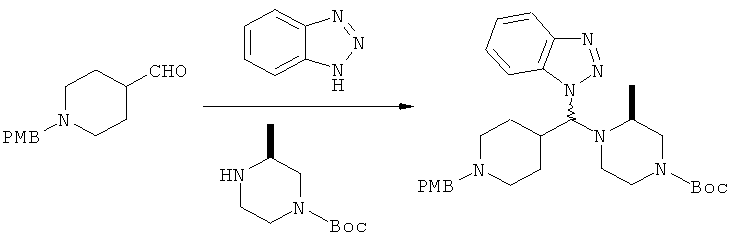
Альдегид (11,3 г), (S)-N-Вос-метилпиперазин (9,7 г) и бензотриазол (5,7 г) разбавляют бензолом (350 мл) и нагревают с азеотропным удалением H2O (ловушка Дина-Старка) в течение 4,75 ч. Раствор охлаждают и концентрируют. Аддукт бензотриазола используют на следующей стадии.
Стадия 4
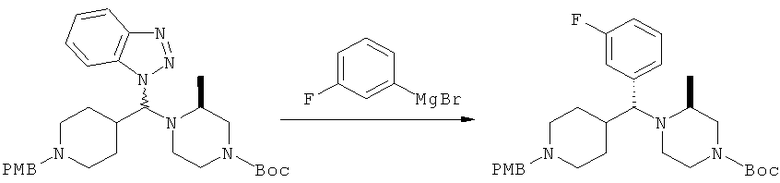
Неочищенный аддукт бензотриазола, полученный на предыдущей стадии (48 ммоль), разбавляют сухим ТГФ (200 мл). Раствор охлаждают до 0°С. К раствору при 0°С прибавляют 3-фторфенилмагнийбромид (290 мл 0,5 М раствора в ТГФ). Полученную коричневую гетерогенную смесь нагревают при 25°С и перемешивают при этой температуре в течение 5 ч. Реакцию медленно гасят с помощью 25 мас.% цитрата натрия и смесь концентрируют на роторном испарителе. Остаток разделяют между EtOAc и 25 мас.% цитратом натрия. Водный слой экстрагируют с помощью EtOAc. Объединенные органические слои промывают рассолом и сушат (Na2SO4). Фильтрование и концентрирование дает желтое масло. Двукратная очистка с помощью флэш-хроматографии (1-й раз: 2/1 гексаны/ацетон, 2-й раз: 4/1 гексаны/ацетон) дает 17,8 г (72%) искомого пиперазина в виде бесцветного масла.
Стадия 5
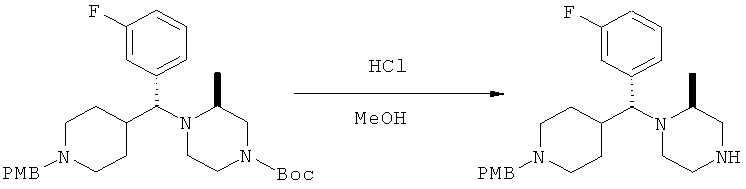
Вос-пиперазин (750 мг) и 3 мл 4,0 М HCl в диоксане разбавляют в МеОН и перемешивают при 25°С (16 ч). Раствор концентрируют. Остаток разделяют между CH2Cl2 и 1 н. NaOH (вод.). Водный слой экстрагируют с помощью CH2Cl2. Объединенные органические слои сушат (MgSO4). Фильтрование и концентрирование дает 582 мг (97%) пиперазина в виде желтого вспененного вещества.
Стадия 6
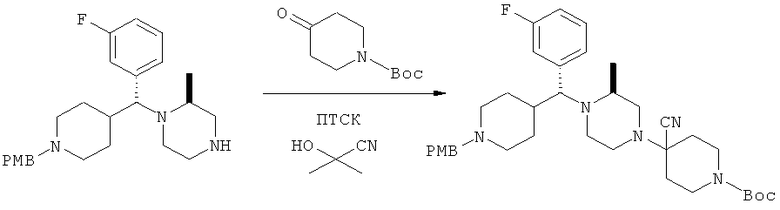
Пиперазин (582 мг), N-Boc-4-пиперидон (281 мг) и п-толуолсульфоновую кислоту (3 мг) разбавляют толуолом и кипятят с обратным холодильником с азеотропным удалением H2O (ловушка Дина-Старка, температура масляной бани = 150°С) в течение 2,5 ч. Раствор охлаждают и прибавляют циангидрин ацетона (0,2 мл). Раствор кипятят с обратным холодильником в течение еще 3 ч. Раствор охлаждают. Цианоамин в толуоле используют на следующей стадии.
Стадия 7
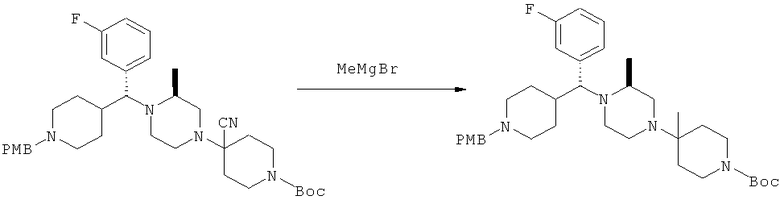
Толуольный раствор цианоамина, полученный выше (1,4 ммоль), разбавляют с помощью ТГФ и к раствору прибавляют MeMgBr (2,4 мл 3,0 М раствора в Et2O). Полученный раствор перемешивают при 25°С в течение 18 ч. Смесь гасят с помощью 25 мас.% цитрата натрия. Смесь экстрагируют с помощью EtOAc. Объединенные органические слои промывают рассолом и сушат (MgSO4). Фильтрование и концентрированно дает 887 мг метилированного пиперидина (100% в пересчете на исходный пиперазин на стадии 6).
Стадия 8
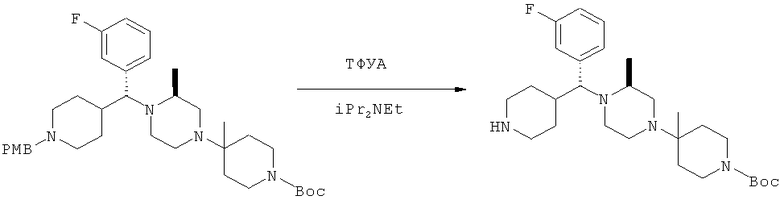
Содержащий защитную группу РМВ пиперидин (887 мг) и iPr2NEt (0,5 мл) разбавляют в CH2Cl2. Прибавляют трифторуксусный ангидрид (0,3 мл) и раствор перемешивают при 25°С в течение 1 ч. Раствор концентрируют и остаток разбавляют смесью МеОН/1 н. NaOH (вод.). Раствор нагревают при 75°С в течение 3 ч. Раствор охлаждают и концентрируют. Остаток распределяют между CH2Cl2 и 1 н. NaOH (вод.). Водный слой экстрагируют с помощью CH2Cl2. Объединенные органические слои сушат (MgSO4), фильтруют и концентрируют и получают пиперидин в виде желтого масла. Это вещество используют непосредственно на следующей стадии.
Стадия 9
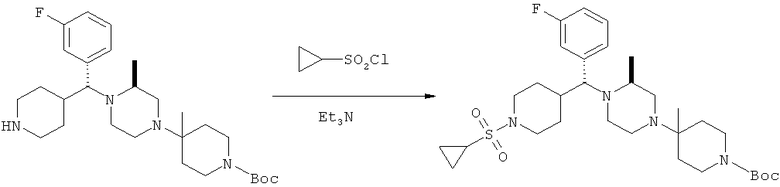
Пиперидин, полученный на стадии 8 (1,46 ммоль), и Et3N (0,45 мл) разбавляют с помощью CH2Cl2 и охлаждают до 0°С. Прибавляют циклопропилсульфонилхлорид (230 мг) и полученный раствор перемешивают при 25°С (2,5 ч). Раствор разбавляют с помощью CH2Cl2 и промывают с помощью 1 н. NaOH (вод.). Водный слой экстрагируют с помощью CH2Cl2. Объединенные органические слои сушат (MgSO4), фильтруют и концентрируют. Остаток очищают с помощью флэш-хроматографии (3/1 гексаны/ацетон, SiO2) и получают 693 мг (80% от цианоамина стадии 6) в виде желтого масла.
Стадия 10
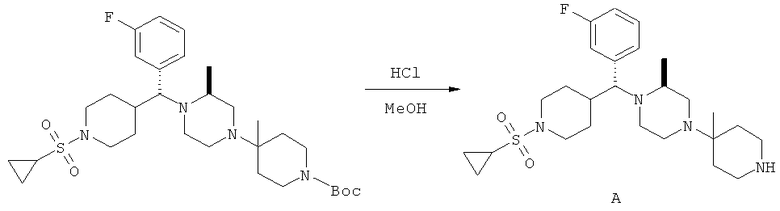
Вос-пиперидин (693 мг) разбавляют с помощью МеОН. Прибавляют 4,0 М HCl в диоксане (2,5 мл) и полученный раствор перемешивают при 25°С (18 ч). Раствор концентрируют. Остаток распределяют между 1 М HCl (вод.) и Et2O. Водный слой экстрагируют с помощью Et2O. Водный слой охлаждают и подщелачивают путем прибавления гранул NaOH (pH=10-12). Смесь экстрагируют с помощью CH2Cl2.
Объединенные слои CH2Cl2, сушат (MgSO4), фильтруют и концентрируют и получают 419 мг (62%) пиперидина А в виде желтого вспененного вещества.
Остальные соединения, приведенные в таблице 1, получают по аналогичным методикам и с использованием соответствующих реагентов.
При изготовлении фармацевтических композиций из соединений, описанных в настоящем изобретении, инертные, фармацевтически приемлемые носители могут быть твердыми или жидкими. К твердым формам препаратов относятся порошки, таблетки, диспергирующиеся гранулы, капсулы, облаток и суппозитории. Порошки и таблетки могут содержать от примерно 5 до примерно 95% активного ингредиента. Подходящие твердые носители известны в данной области техники, например карбонат магния, стеарат магния, тальк, сахар и лактоза. Таблетки, порошки, облатки и капсулы можно использовать в качестве твердых дозированных форм, пригодных для перорального введения. Примеры фармацевтически приемлемых носителей и способов изготовления различных композиций приведены в публикации A. Gennaro (ed.), Remington's Pharmaceutical Sciences, 18th Edition, (1990), Mack Publishing Co., Easton, Pennsylvania.
Жидкие формы препаратов включают растворы, суспензии и эмульсии, например, не ограничиваясь ими, водные или водно-пропиленгликолевые растворы для парентеральных инъекций или прибавление подсластителей и замутнителей в растворы, суспензии и эмульсии для перорального введения. К жидким формам композиций также могут относиться растворы для внутриназального введения.
Аэрозольные препараты, пригодные для ингаляции, могут включать растворы и твердые вещества в порошкообразной форме, которые могут сочетаться с фармацевтически приемлемым носителем, таким как сжатый инертный газ, например азот.
В объем настоящего изобретения также включены твердые формы препаратов, которые предназначены для превращения в жидкие формы препаратов, предназначенных для перорального или парентерального введения, которое выполняется незадолго до использования. Такие жидкие формы включают растворы, суспензии и эмульсии.
Соединения, соответствующие настоящему изобретению, также можно вводить чрескожно. Чрескожные композиции могут представлять собой кремы, лосьоны, аэрозоли и/или эмульсии, и они могут быть включены в матричный пластырь чрескожного воздействия или пластырь резервуарного типа, которые обычно используется в данной области техники для такой цели.
Соединения, соответствующие настоящему изобретению, также можно вводить перорально, внутривенно, назально или подкожно.
Предпочтительно вводить соединение перорально.
Предпочтительно, чтобы фармацевтический препарат находился в виде разовой дозированной формы. В такой форме препараты разделяются на разовые дозы подходящей величины, содержащие терапевтически эффективное количество соединения формулы IA или IB.
Количество активного соединения, содержащегося в разовой дозе препарата, в соответствии с конкретным случаем применения обычно может меняться или регулироваться в диапазоне от примерно 10 до примерно 500 мг, предпочтительно - от примерно 25 до примерно 300 мг, более предпочтительно - от примерно 50 до примерно 250 мг и наиболее предпочтительно - от примерно 55 до примерно 200 мг.
Реальная использующаяся доза соединения, соответствующего настоящему изобретению, может меняться в зависимости от требований пациента и тяжести подвергающегося лечению патологического состояния. Определение надлежащего дозировочного режима для конкретного случая осуществляет специалист в данной области техники. Для удобства полную суточную дозу можно разделять и вводить порциями в течение дня в соответствии с необходимостью.
Количество и частота введения соединений, соответствующих настоящему изобретению, и/или их фармацевтически приемлемых солей будет регулироваться в соответствии с решением лечащего врача, учитывающего такие факторы, как возраст, состояние и массу пациента, а также тяжесть симптомов при лечении. Типичный рекомендованный суточный дозировочный режим для перорального введения может включать введение от примерно 100 до примерно 300 мг/сутки, предпочтительно - от 150 до 250 мг/сутки, более предпочтительно - примерно 200 мг/сутки, вводимых в виде двух - четырех разделенных доз.
Дозы и режимы введения НИОТ, ННИОТ, ИП и других средств, применяющихся в комбинации с соединениями, соответствующими настоящему изобретению, определяет лечащий врач с учетом утвержденных к применению доз и режимов введения, указанных на листке-вкладыше или установленных в протоколах, с учетом возраста, пола и состояния пациента и тяжести подвергающегося лечению патологического состояния.
В предпочтительном варианте осуществления соединение, соответствующее настоящему изобретению, можно применять для лечения вируса иммунодефицита человека путем введения пациенту, нуждающемуся в таком лечении, терапевтически эффективного количества одного или большего количества соединений формулы IA или IB, предпочтительно - в комбинации с одним или большим количеством фармацевтически приемлемых носителей. Одно или большее количество, предпочтительно - от 1 до 4 противовирусных средств, применимых при анти-ВИЧ-1 терапии, можно применять в комбинации с соединением, соответствующим настоящему изобретению. Противовирусное средство или средства можно комбинировать с одним или большим количеством соединений, соответствующих настоящему изобретению, в одной дозированной форме. Одно или большее количество соединений, соответствующих настоящему изобретению, и противовирусное средство или средства можно вводить в любом порядке, например последовательно, одновременно, по отдельности и т.п. Количества таких активных средств при такой комбинированной терапии могут быть разными (вводимые количества) или одинаковыми (вводимые количества). В одной и той же дозированной форме различные активные средства также могут содержаться в фиксированных количествах, например 10 мг соединения по пункту 1 формулы изобретения и 10 мг противовирусного средства в одной таблетке. Иллюстрацией такой "одной таблетки" является, например, антихолестериновый препарат VYTORIN® (выпускающийся фирмой Merck Schering-Plough Pharmaceutical, Kenilworth, New Jersey).
Противовирусные средства, предназначенные для применения в комбинации с соединением, соответствующим настоящему изобретению, включают нуклеозидные и нуклеотидные ингибиторы обратной транскриптазы, ненуклеозидные ингибиторы обратной транскриптазы, ингибиторы протеазы и другие противовирусные средства, указанные ниже и не относящиеся к указанным классам. Конкретные примеры противовирусных средств включают, но не ограничиваются только ими, зидовудин, ламивудин, залцитабин, диданозин, ставудин, абакавир, адефовир дипивоксил, лобукавир, ВСН-10652, эмитрицитабин, бета-L-FD4, DAPD, лоденозин, невирапин, делавиридин, эфавиренц, PNU-142721, AG-1549, МКС-442, (+)-каланолид А и В, саквинавир, индинавир, ритонавир, нелфинавир, лазинавир, DMP-450, BMS-2322623, АВТ-378, ампренавир, гидроксимочевину, рибавирин, IL-2, IL-12, пентафузид, Yissum No. 11607 и AG-1549. В частности, комбинации, известные, как ВААРТ, предполагается применять в комбинации с соединением, соответствующим настоящему изобретению.
При комбинированном лечении более чем одним активным средством, при котором активные средства находятся в отдельных дозированных формах, активные средства можно вводить по отдельности или одновременно. Кроме того, введение одного элемента можно проводить до, одновременно или после введения другого средства.
В другом варианте осуществления настоящее изобретение относится к способу лечения отторжения цельного органа, реакции "трансплантат против хозяина", артрита, ревматоидного артрита, воспалительной болезни кишечника, атонического дерматита, псориаза, астмы, аллергий или рассеянного склероза, включающему введение пациенту, нуждающемуся в таком лечении, терапевтически эффективного количества одного или большего количества соединений формулы IA или IB, предпочтительно - в комбинации с одним или большим количеством фармацевтически приемлемых носителей. В другом варианте осуществления способ лечения отторжения цельного органа, реакции "трансплантат против хозяина", ревматоидного артрита, воспалительной болезни кишечника или рассеянного склероза дополнительно включает введение одного или большего количества других средств, применимых для лечения указанных заболеваний, в комбинации с одним или большим количеством соединений формулы IA или IB.
Средствами, известными и применяющимися для лечения ревматоидного артрита, отторжения трансплантата и реакции "трансплантат против хозяина", воспалительной болезни кишечника и рассеянного склероза, которые можно вводить в комбинации с соединением, соответствующим настоящему изобретению, являются следующие.
Отторжения цельного органа и реакция "трансплантат против хозяина": иммуносупрессанты, такие как циклоспорин и интерлейкин-10 (IL-10), такролимус, антилимфоцитарный глобулин, антитела ОКТ-3 и стероиды.
Воспалительная болезнь кишечника: IL-10 (см. US 5368854), стероиды и азулфидин.
Ревматоидный артрит: метотрексат, азатиоприн, циклофосфамид, стероиды и микофенолят мотефил.
Рассеянный склероз: интерферон-бета, интерферон-альфа и стероиды.
В другом варианте осуществления настоящее изобретение относится к набору, включающему помещенную в отдельные контейнеры в одной упаковке фармацевтическую композицию, предназначенную для применения в комбинации для лечения инфекции вирусом иммунодефицита человека. В одном контейнере находится фармацевтическая композиция, включающая одно или большее количество соединений формулы IA или IB на одном или более фармацевтически приемлемых носителях, и в отдельных контейнерах находится одна или большее количество фармацевтических композиций, включающих эффективное количество одного или большего количества противовирусных средств или других средств, применимых для лечения инфекции вирусом иммунодефицита человека, на одном или более фармацевтически приемлемых носителях.
Задача терапии ВИЧ-1, соответствующей настоящему изобретению, является снижение вирусной нагрузки ВИЧ-1-РНК ниже предела обнаружения. "Предел обнаружения ВИЧ-1-РНК" в настоящем изобретении означает присутствие в 1 мл плазмы пациента от менее примерно 200 до менее примерно 50 копий ВИЧ-1-РНК, где данное количество измерено с помощью количественной ПЦР методологии с использованием обратной транскриптазой, проводимой в течение множества циклов. ВИЧ-1-РНК в настоящем изобретении предпочтительно определять с помощью методологии Amplicor -1 Monitor 1.5 (разработанной компанией Roche Diagnostics) или Nuclisens HIV-1 QT-1.
Исследования, применяющиеся для изучения антагонистической активности CCR5, а также ингибирующего воздействия на репликацию ВИЧ, подробно описаны в заявке на патент № IN01481K. Описанные ниже исследования используют для изучения антагонистической активности CCR5 и ингибирующего воздействия на репликацию ВИЧ соединений, соответствующих настоящему изобретению.
Исследование хемотаксиса. Исследование хемотаксиса представляет собой функциональное исследование, которое сравнительно характеризует агонистичекие и антагонистичексие характеристики исследуемых соединений. В исследовании определяют способность мышиных клеток неадгезивной линии, экспрессирующих CCR5 (BaF-550) человека, проходить через мембрану в ответ на исследуемые соединения или натуральные лиганды (т.е. RANTES, MIP-1β). Клетки проходят через проницаемую мембрану к соединениям, обладающим агонистической активностью. Соединения, которые являются антагонистами, не только не могут вызвать хемотаксис, но и способны подавлять перемещение клеток в ответ на воздействие известных лигандов CCR5. С помощью исследования хемотаксиса также определяют активность соединений, соответствующих настоящему изобретению.
Методика исследования хемотаксиса. Клетки Ba/F3-hCCR5 клона 550 (a.k.a. B550) выращивают в RPMI-1640, к которой прибавлены 10% фетальной бычьей сыворотки (ФБС), 1 × Pen-Strep, 1 × Glutamax, 1 × HEPES, 1 × 2-меркаптоэтанол и mIL-3 при концентрации 1 мкг/л. Все реагенты для культур тканей получают от компании Invitrogen (Carlsbad, California), если не указано иное. ФБС получают от компании Gemini Bio-Products, Woodland, California. Мышиный IL-3 получают от компании R and D Systems, Миннеаполис, Миннесота.
MIP-1β(hMIP-1β) человека получают от компании R and D Systems и при исследовании используют при конечной концентрации, равной 1 нМ. Соединения восстанавливают в ДМСО и разводят в среде для исследования хемотаксиса от 0,1 нМ до 1000 нМ (конечные концентрации).
Для проведения исследования клетки дважды промывают в среде RPMI 1640 без исследуемых компонентов и затем при подходящих концентрациях суспендируют в среде для исследования. Среда для исследования содержит 10% среды Ba/F3 в RPMI 1640. Конечное содержание клеток для исследования составляет примерно 2,5×106 клеток/мл. Хемотаксис проводят с использованием 96-луночной системы ChemoTx system® с фильтрами, обладающими порами размером 5 мкм (NeuroProbe, Inc., Gaithersburg, Maryland, Cat. #: 101-5).
Соединения используют для исследования антагонизма при хемотаксисе в соответствии с инструкциями изготовителя. Вкратце, методика заключается в следующем: каждое соединение смешивают с hMIP-1β и примерно 29 мкл смеси помещают в нижние лунки 96-луночной системы ChemoTx system. Сверху помещают сетчатый фильтр и 25 мкл клеток, смешанных с соединением при подходящей концентрации, помещают на фильтр. Объеденные планшеты инкубируют в течение 2 ч при 37°С в камере с влажной атмосферой. После инкубации клетки счищают и систему планшетов центрифугируют в течение 5 мин при 1000 оборотах/мин в центрифуге ЕС Centra-8R. Сетчатый фильтр удаляют и планшет ChemoTx переворачивают на 96-луночный планшет с воронками. Систему планшетов центрифугируют в течение 5 мин при 1000 оборотах/мин. Объем лунок доводят до 100 мкл, добавляя в них среду, и планшеты выдерживают в течение примерно 20 мин. Количество переместившихся клеток определяют с помощью системы люминесцентного анализа Cell Titer Glo Luminescent Assay компании Promega (Madison, Wisconsin) и люминометра для микропланшетов TROPIX TR717 (РЕ Appiied Biosystems, Boston, Massachusetts)) в соответствии с инструкциями изготовителя.
ИССЛЕДОВАНИЕ РЕПЛИКАЦИИ ЛЮЦИФЕРАЗЫ.
Плазмиды, кодирующие полноразмерный геном ВИЧ-1 pNL-4-Luc с петлей gp 120 V-3, замененной на Bgl II фрагмент ВИЧ-1 ADA, YU-2 или Н×В (ADA-Luc-FL, YU-2-Luc-FL и H×B-Luc-FL) получают у д-ра Susan Pontow (Washington University, St. Louis МО). Исходные культуры компетентного для репликации люциферазы репортерного вируса получают путем трансфекции плазмид в клетки 293Т с использованием реагентов для трансфицирования Superfect (Qiagen) или Mirus. Исходные культуры вирусов собирают через 48 ч после трансфицирования и для определения продуцирования люциферазы титруют на клетках U87-CCR5 или C×CR4. Клетки U87-CD4-CCR5 (104/лунка) помещают в 96-луночные культуральные планшеты и инкубируют в течение ночи. Среды удаляют и заменяют на 50 мкл свежей культуральной среды (МДСИ (модифицированная по способу Дульбекко среда Игла), 10% ФТС (фетальная телячья сыворотка)) и 50 мкл соединения, разведенного в культуральной среде. Клетки инкубируют с соединением при 37°С в течение 1 ч. Образовавшуюся надосадочную жидкость удаляют и заменяют на 20 мкл среды, содержащей соединение и инфицируют таким же объемом разведенной или неразведенной вирусной культуры при 37°С в течение 3-4 ч. Клетки один раз промывают с помощью МДСИ и прибавляют 200 мкл среды, содержащей соединение. Культуры инкубируют в течение 3 дней, клетки подвергают лизису в люциферазном буфере для лизиса (Promega, Madison, WI) и переносят в планшеты Immulon (Dynex Technoiogies, Chantilly VA). К лизатам прибавляют равный объем субстрата люциферазы (Promega, Madison WI) и планшеты сразу же считывают с помощью люминометра Wallac. Концентрации, приводящие к ингибированию на 50 и 90%, определяют с помощью программного обеспечения GraphPad PRISM.
Хотя настоящее изобретение описано с помощью приведенных выше конкретных вариантов осуществления, для специалистов с общей подготовкой в данной области техники должны быть очевидны их многочисленные альтернативы, модификации и изменения. Подразумевается, что все такие альтернативы, модификации и изменения входят в сущность и объем настоящего изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ПИПЕРАЗИНА, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, ИХ СОДЕРЖАЩИЕ, И ПРИМЕНЕНИЕ В КАЧЕСТВЕ АНТАГОНИСТОВ CCR5 | 2000 |
|
RU2299206C9 |
| ПРОИЗВОДНЫЕ ПИПЕРИДИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И ПРИМЕНЕНИЕ | 2002 |
|
RU2316553C2 |
| АНАЛОГИ БЕНЗОХИНОНСОДЕРЖАЩИХ АНСАМИЦИНОВ (ВАРИАНТЫ), СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ (ВАРИАНТЫ) И СПОСОБ ЛЕЧЕНИЯ РАКА (ВАРИАНТЫ) | 2004 |
|
RU2484086C9 |
| КОМБИНАЦИИ АКТИВАТОРА (АКТИВАТОРОВ) РЕЦЕПТОРА, АКТИВИРУЕМОГО ПРОЛИФЕРАТОРОМ ПЕРОКСИСОМ (РАПП), И ИНГИБИТОРА (ИНГИБИТОРОВ) ВСАСЫВАНИЯ СТЕРИНА И ЛЕЧЕНИЕ ЗАБОЛЕВАНИЙ СОСУДОВ | 2008 |
|
RU2483724C2 |
| АНТАГОНИСТЫ РЕЦЕПТОРА ТРОМБИНА | 2005 |
|
RU2408594C2 |
| ЗАМЕЩЕННЫЕ БИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, ФАРМКОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ ИНГИБИРОВАНИЯ | 1998 |
|
RU2204557C2 |
| СПОСОБ ЛЕЧЕНИЯ ПОРАЖЕНИЙ, АССОЦИИРОВАННЫХ С ВОЗДЕЙСТВИЕМ АЛКИЛИРУЮЩИХ ВЕЩЕСТВ | 2009 |
|
RU2506083C2 |
| ПРОИЗВОДНЫЕ, ИМЕЮЩИЕ АКТИВНОСТЬ АГОНИСТОВ PPAR-РЕЦЕПТОРОВ | 2006 |
|
RU2415846C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ ИНГИБИТОРЫ АСПАРТИЛПРОТЕАЗЫ | 2004 |
|
RU2405774C9 |
| ПРОИЗВОДНЫЕ БИПИПЕРИДИНА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2002 |
|
RU2296751C2 |
Изобретение относится к соединениям, описываемых структурной формулой
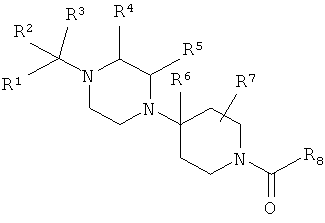
в которой: R1 выбран из группы, включающей R9-фенил и 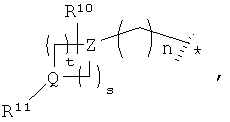 R2 выбран из группы, включающей Н и (С1-С6)-алкил; R3 выбран из группы, включающей (С1-С6)-алкил, (С1-С6)-алкокси-(С1-С6)-алкил- и R9-(C6-С10)-арил; R4, R5, R6 и R7 независимо выбраны из группы, включающей Н и (С1-С6)-алкил; R8 выбран из группы, включающей
R2 выбран из группы, включающей Н и (С1-С6)-алкил; R3 выбран из группы, включающей (С1-С6)-алкил, (С1-С6)-алкокси-(С1-С6)-алкил- и R9-(C6-С10)-арил; R4, R5, R6 и R7 независимо выбраны из группы, включающей Н и (С1-С6)-алкил; R8 выбран из группы, включающей
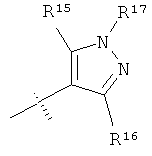
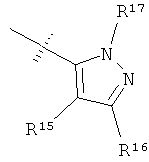 и
и 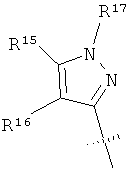 ; R9 означает 1, 2 или 3 заместителя, независимо выбранных из группы, включающей Н, галоген и -CF3; R10 выбран из группы, включающей Н и (С1-С6)-алкил; R11 является (С3-С10)-циклоалкил-S(O2)-; R15 и R16 независимо являются (С1-С6)-алкилом; R17 является R20O-; R20 выбран из группы, включающей Н и (С1-С6)-алкил-(С6-С10)-арил; Q является N; Z является СН; n равно 0; s равно 2; и t равно 2. Изобретение также относится к фармацевтической композиции, обладающей свойствами ингибитора хемокинового рецептора, на основе этих соединений. Технический результат - получены новые соединения и фармацевтическая композиция на их основе, которые могут найти применение в медицине для лечения инфекции вируса иммунодефицита человека (ВИЧ). 4 н. и 4 з.п. ф-лы, 2 табл.
; R9 означает 1, 2 или 3 заместителя, независимо выбранных из группы, включающей Н, галоген и -CF3; R10 выбран из группы, включающей Н и (С1-С6)-алкил; R11 является (С3-С10)-циклоалкил-S(O2)-; R15 и R16 независимо являются (С1-С6)-алкилом; R17 является R20O-; R20 выбран из группы, включающей Н и (С1-С6)-алкил-(С6-С10)-арил; Q является N; Z является СН; n равно 0; s равно 2; и t равно 2. Изобретение также относится к фармацевтической композиции, обладающей свойствами ингибитора хемокинового рецептора, на основе этих соединений. Технический результат - получены новые соединения и фармацевтическая композиция на их основе, которые могут найти применение в медицине для лечения инфекции вируса иммунодефицита человека (ВИЧ). 4 н. и 4 з.п. ф-лы, 2 табл.
1. Соединение, описываемое структурной формулой IA:
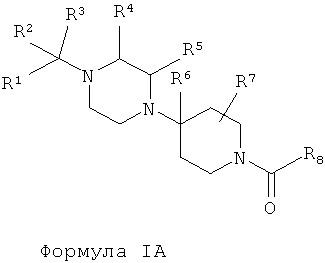
или его фармацевтически приемлемая соль; в которой:
R1 выбран из группы, включающей R9-фенил, и
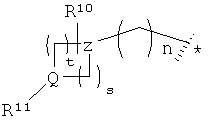
R2 выбран из группы, включающей Н и (С1-С6)-алкил;
R3 выбран из группы, включающей (С1-С6)-алкил, (С1-С6)-алкокси-(С1-С6)-алкил- и R9-(C6-C10)-арил;
R4, R5, R6 и R7 независимо выбраны из группы, включающей Н и (C1-С6)-алкил;
R8 выбран из группы, включающей
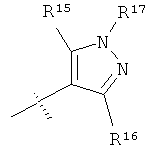
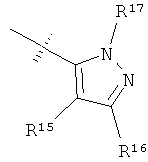 и
и 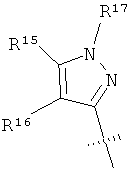 ;
;
R9 означает 1, 2 или 3 заместителя, независимо выбранных из группы, включающей Н, галоген и -CF3;
R10 выбран из группы, включающей Н и (С1-С6)-алкил;
R11 является (С3-С10)-циклоалкил-S(O2)-;
R15 и R16 независимо являются (С1-С6)-алкилом;
R17 является R20O-;
R20 выбран из группы, включающей Н, и (С1-С6)-алкил-(С6-С10)-арил;
Q является N;
Z является СН;
n равно 0;
s равно 2; и
t равно 2.
2. Соединение, описываемое структурной формулой IB:
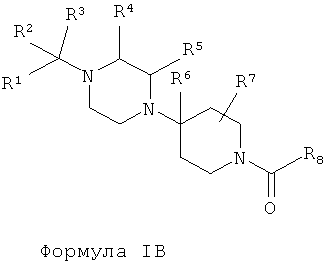
или его фармацевтически приемлемая соль; в которой:
R1 выбран из группы, включающей R9-фенил и
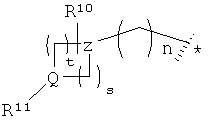
R2 выбран из группы, включающей Н и (С1-С6)-алкил;
R3 выбран из группы, включающей (С1-С6)-алкил, (С1-С6)-алкокси-(С1-С6)-алкил-, R9-(С6-С10)-арил;
R4, R5, R6 и R7 независимо выбраны из группы, включающей Н и (С1-С6)-алкил;
R8 выбран из группы, включающей
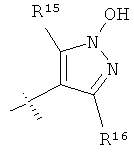
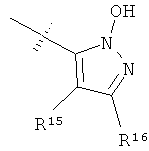 и
и 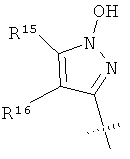 ;
;
R9 означает 1, 2 или 3 заместителя, независимо выбранных из группы, включающей Н, галоген и -CF3;
R10 выбран из группы, включающей Н и (С1-С6)-алкил;
R11 является (С3-С10)-циклоалкил-S(O2)-;
R15 и R16 независимо являются (С1-С6)-алкилом;
Q является N;
Z является СН;
n равно 0;
s равно 2; и t равно 2;
в выделенной и очищенной форме.
3. Соединение по п.1 или 3, представленное формулой
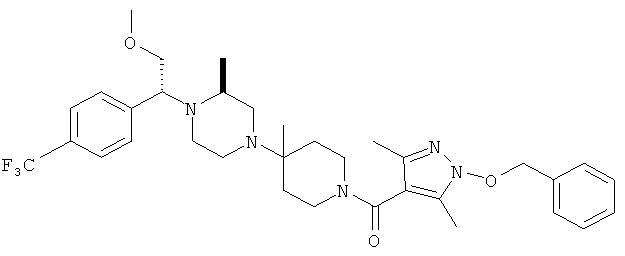
или его фармацевтически приемлемая соль.
4. Соединение по п.1 или 3, выбранное из группы, включающей
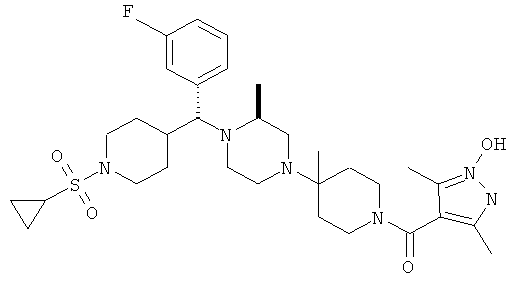
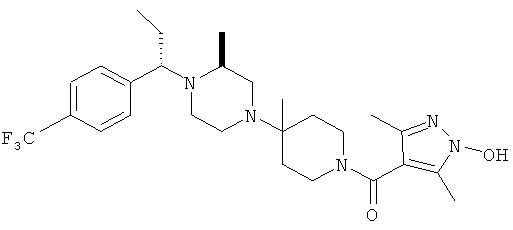
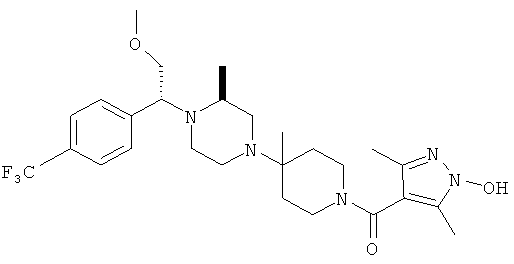
или его фармацевтически приемлемая соль.
5. Фармацевтическая композиция, обладающая свойствами ингибитора хемокинового рецептора, включающая терапевтически эффективное количество, по меньшей мере, одного соединения по п.1 или 3 в комбинации, по меньшей мере, с одним фармацевтически приемлемым носителем.
6. Применение соединения по п.1 или 2 или его фармацевтически приемлемой соли для приготовления лекарственного средства для ингибирования репликации вируса иммунодефицита человека.
7. Применение по п.6, в котором лекарственное средство вводят перорально, внутривенно или подкожно.
8. Применение по п.6, в котором дополнительно вводят одно или более противовирусных средств, применимых для лечения инфекции вирусом иммунодефицита человека.
| Способ флотации | 1944 |
|
SU66558A1 |
| WO 2004056770 A2, 08.07.2004 | |||
| RU 2001132635 A, 10.07.2003. | |||
Авторы
Даты
2011-02-10—Публикация
2006-02-21—Подача