Текст описания приведен в факсимильном виде.








































































































































































































































| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛА ПРОТИВ TENB2, СКОНСТРУИРОВАННЫЕ С ЦИСТЕИНОМ, И КОНЪЮГАТЫ АНТИТЕЛО - ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2008 |
|
RU2505544C2 |
| АНТИ-CD79b АНТИТЕЛА И ИММУНОКОНЪЮГАТЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2009 |
|
RU2553566C2 |
| АНТИТЕЛА И ИММУНОКОНЪЮГАТЫ, ВИЗУАЛИЗИРУЕМЫЕ ПРИ ПОМОЩИ ИММУНО-ПОЗИТРОН-ЭМИССИОННОЙ ТОМОГРАФИИ, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2011 |
|
RU2613886C2 |
| АНТИ-CD79b АНТИТЕЛА И ИММУНОКОНЪЮГАТЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2008 |
|
RU2511410C2 |
| АНТИТЕЛА И ИММУНОКОНЪЮГАТЫ И ИХ ПРИМЕНЕНИЯ | 2007 |
|
RU2436796C9 |
| МУЛЬТИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА, АНАЛОГИ АНТИТЕЛ, КОМПОЗИЦИИ И СПОСОБЫ | 2010 |
|
RU2580038C2 |
| ПЕПТИДОМИМЕТИЧЕСКИЕ СОЕДИНЕНИЯ И ИХ КОНЪЮГАТЫ АНТИТЕЛ С ЛЕКАРСТВЕННЫМИ СРЕДСТВАМИ | 2014 |
|
RU2689388C1 |
| ПОЛУЧЕННЫЕ С ПОМОЩЬЮ ГЕННОЙ ИНЖЕНЕРИИ АНТИТЕЛА С ЦИСТЕИНОВЫМИ ЗАМЕНАМИ И ИХ КОНЪЮГАТЫ | 2011 |
|
RU2755066C2 |
| МОДИФИЦИРОВАННЫЕ АНТИТЕЛА, С КОТОРЫМИ СВЯЗАН МОТИВ, ВКЛЮЧАЮЩИЙ ОСТАТОК ЦИСТЕИНА, КОНЪЮГАТЫ ЭТИХ МОДИФИЦИРОВАННЫХ АНТИТЕЛ С ЛЕКАРСТВЕННЫМИ ВЕЩЕСТВАМИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2013 |
|
RU2582259C2 |
| АНТИ-CD79b АНТИТЕЛА И ИММУНОКОНЪЮГАТЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2791984C2 |















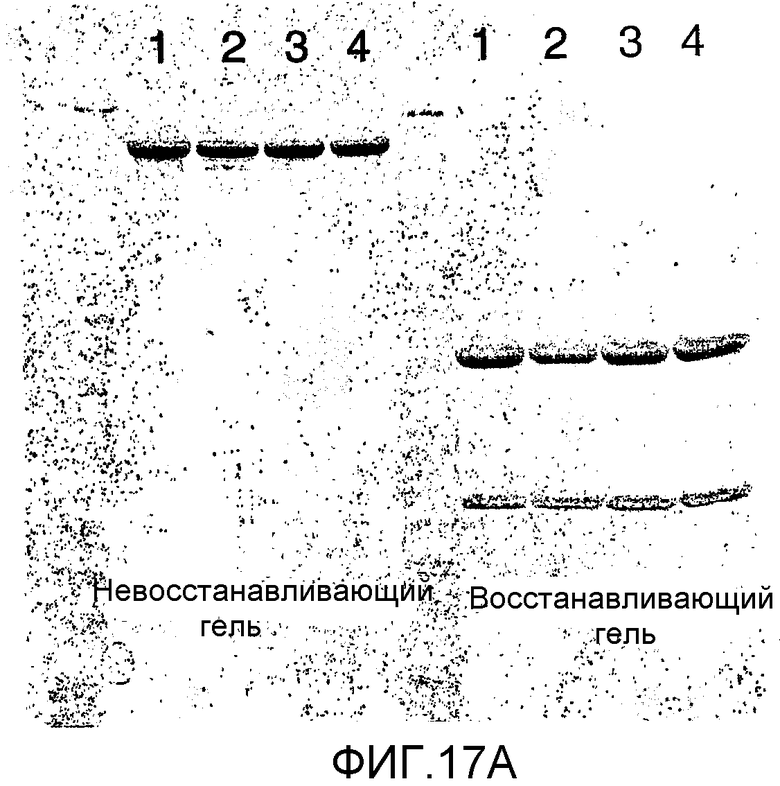
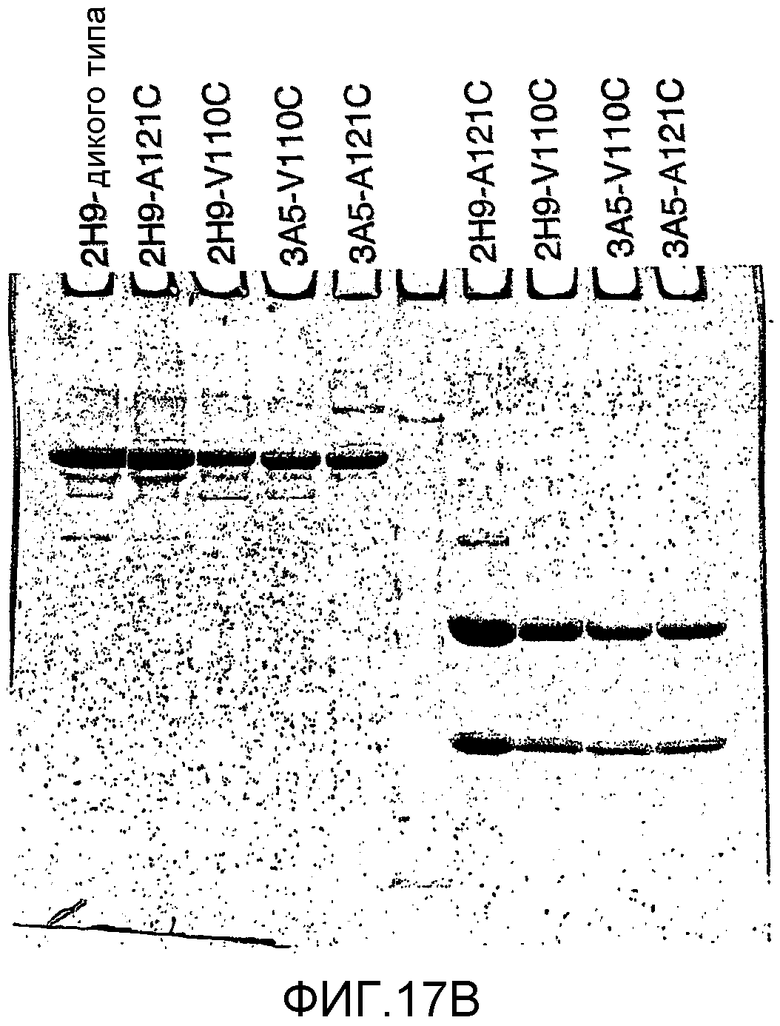



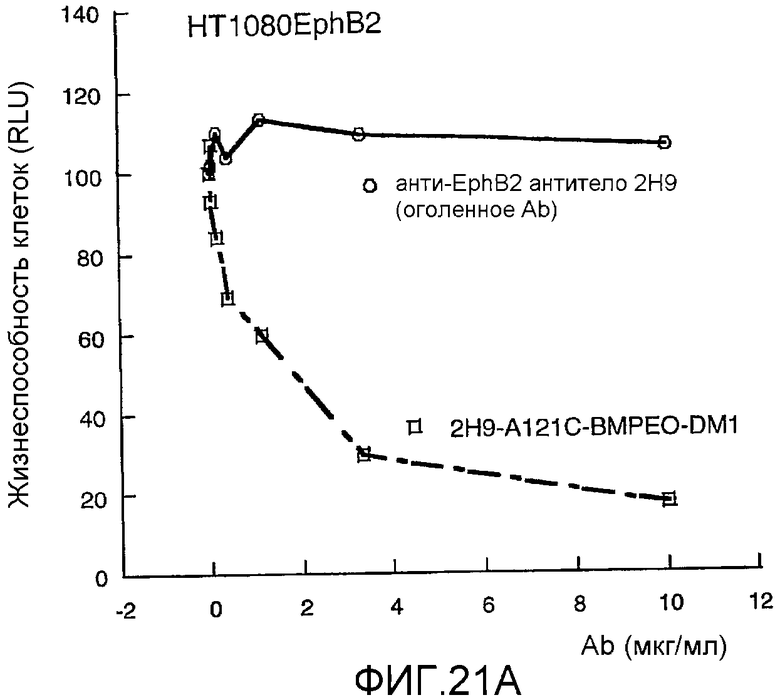
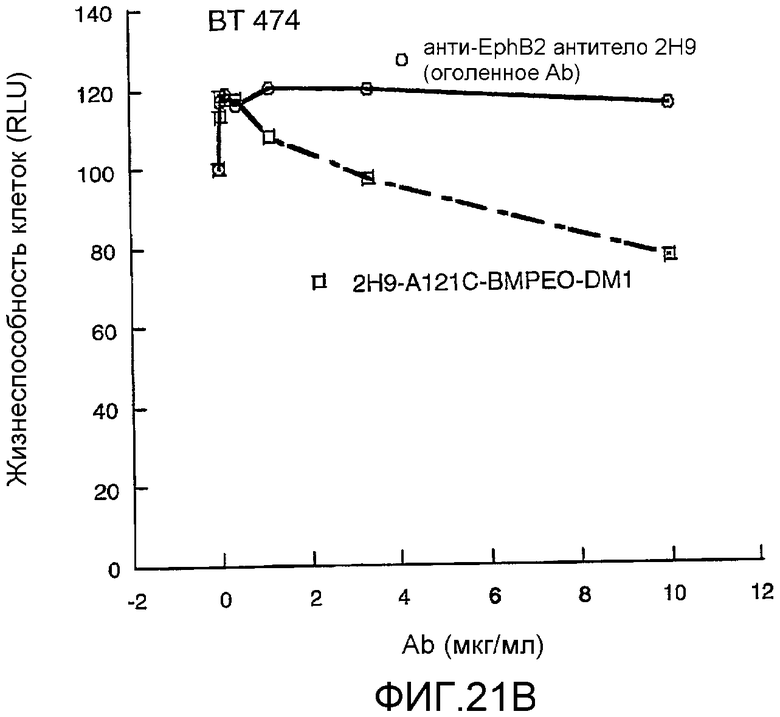




Изобретение относится к биотехнологии. Были сконструированы антитела путем замены одной или нескольких аминокислот родительского антитела высокореактивными цистеиновыми аминокислотными остатками, не являющимися перекрестносшитыми. Описанные антитела были конъюгированы с одной или несколькими молекулами лекарственного средства (D) посредством линкера (L), в результате чего были получены конъюгаты, имеющие формулу: Ab-(L-D)p, где p равно 1-4. Также описано диагностическое и терапевтическое применение соединений в фармацевтических композициях. Изобретение может быть использовано в целях in vitro, in situ и in vivo диагностики или обработки клеток млекопитающих или лечения ассоциированных с ними патологических состояний. 7 н. и 44 з.п. ф-лы, 25 ил., 7 табл.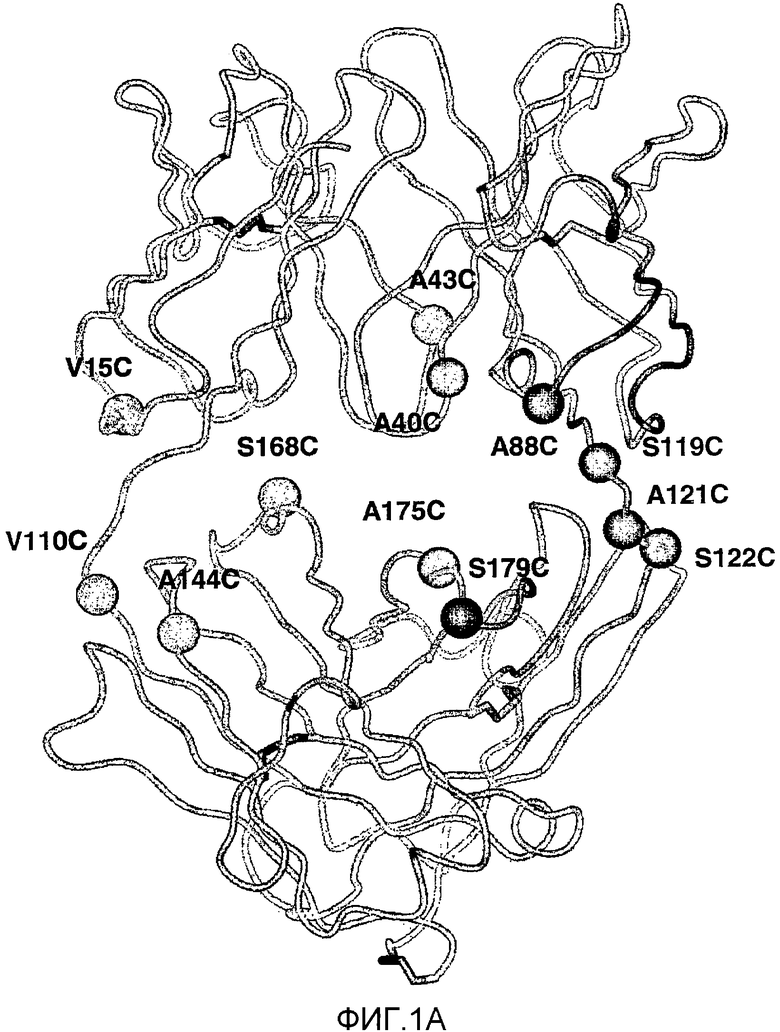
1. Сконструированное антитело с цистеиновыми заменами, предназначенное для конъюгирования с химиотерапевтическими лекарственными средствами, токсинами, аффинными лигандами и детектируемыми метками,
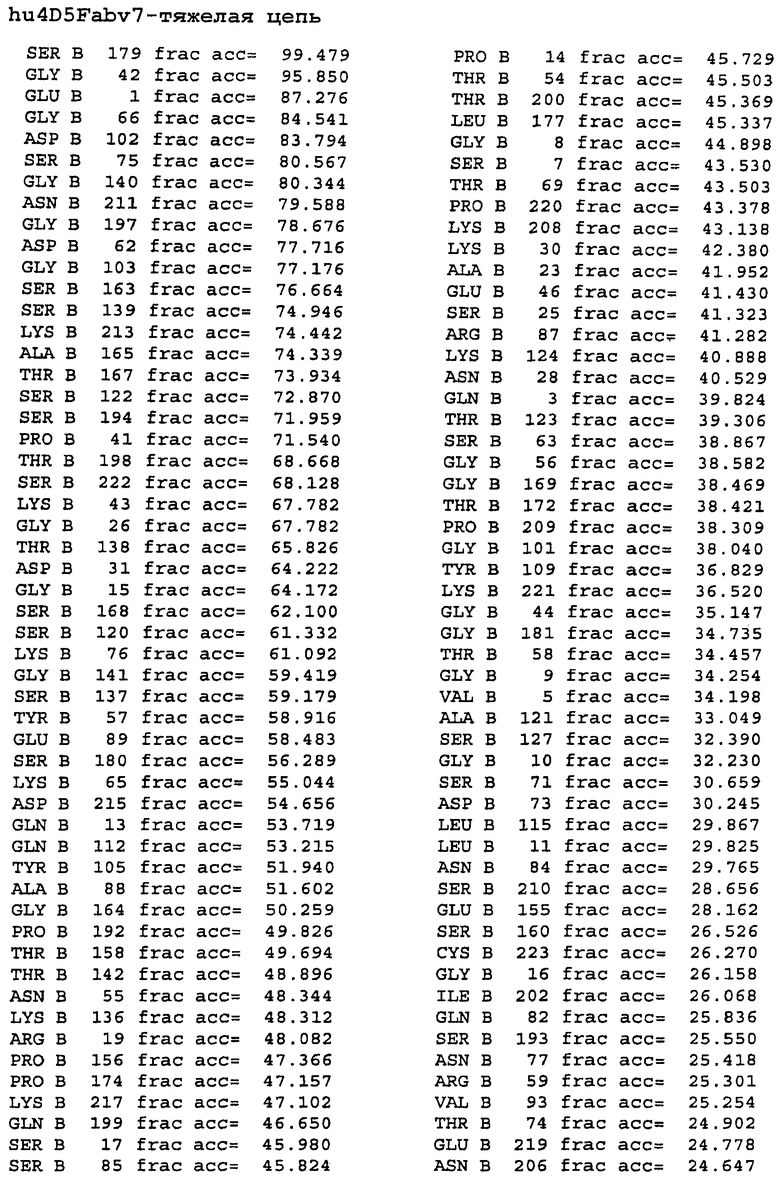
содержащее один или несколько свободных цистеиновых остатков с величиной тиоловой реактивности в пределах от 0,6 до 1,0 и последовательность в тяжелой цепи, выбранную из SEQ ID NO: 11, 12, 13 и 15:
или последовательность в легкой цепи, выбранную из SEQ ID NO: 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 45 и 46;
где указанное сконструированное антитело с цистеиновыми заменами получают способом, включающим замену одного или нескольких аминокислотных остатков родительского антитела свободным цистеиновым остатком, где родительское антитело селективно связывается с антигеном, а сконструированное антитело с цистеиновыми заменами селективно связывается с тем же антигеном, что и родительское антитело.
2. Сконструированное антитело с цистеиновыми заменами по п.1, полученное способом, включающим:
(i) мутагенез последовательности нуклеиновой кислоты, кодирующей сконструированное антитело с цистеиновыми заменами;
(ii) экспрессию сконструированного антитела с цистеиновыми заменами и
(iii) выделение и очистку сконструированного антитела с цистеиновыми заменами.
3. Сконструированное антитело с цистеиновыми заменами по п.2, полученное способом, дополнительно включающим:
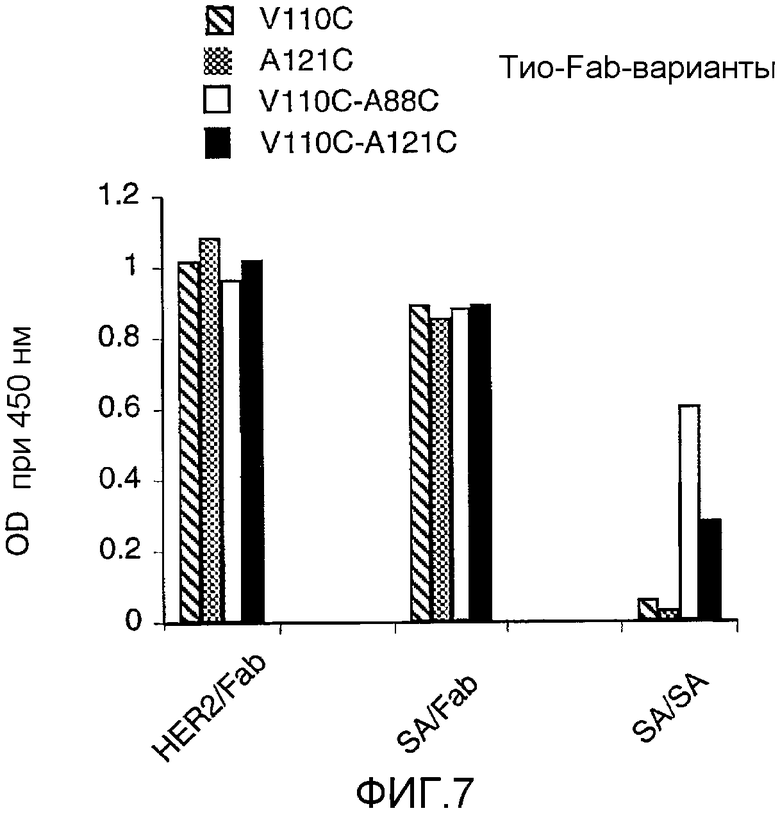
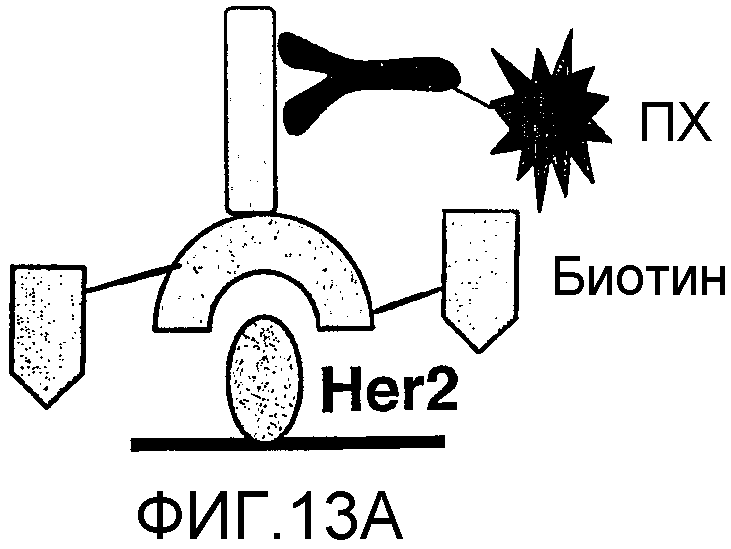
(i) взаимодействие сконструированного антитела с цистеиновыми заменами с реагентом, обладающим аффинностью по отношению к реакционноспособному тиолу, с получением аффинно-меченного сконструированного антитела с цистеиновыми заменами; и
(ii) определение уровня связывания указанного аффинно-меченного сконструированного антитела с цистеиновыми заменами со средой для захвата.
4. Сконструированное антитело с цистеиновыми заменами по п.3, где указанный реагент, обладающий аффинностью в отношении реакционноспособного тиола, содержит биотиновую молекулу и малеимидную молекулу.
5. Сконструированное антитело с цистеиновыми заменами по п.3, где указанная среда для захвата содержит стрептавидин.
6. Сконструированное антитело с цистеиновыми заменами по п.1, где родительским антителом является слитый белок, содержащий альбумин-связывающий пептид (АВР), выбранный из SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4 и SEQ ID NO: 5.
7. Сконструированное антитело с цистеиновыми заменами по п.1, где родительское антитело выбрано из моноклонального антитела, биспецифического антитела, химерного антитела, антитела человека, гуманизированного антитела и фрагмента антитела.
8. Сконструированное антитело с цистеиновыми заменами по п.7, где родительское антитело выбрано из huMAb4D5-8 (трастузумаб), анти-EphB2R антитела и анти-MUC16 антитела.
9. Сконструированное антитело с цистеиновыми заменами по п.1, содержащее аминокислотную последовательность, выбранную из SEQ ID NO: 6, SEQ ID NO: 7, SEQ ID NO: 8, SEQ ID NO: 28 и SEQ ID NO: 39.
10. Сконструированное антитело с цистеиновыми заменами по п.1, где родительским антителом является интактное антитело, выбранное из IgA, IgD, IgE, IgG и IgM.
11. Сконструированное антитело с цистеиновыми заменами по п.10, где IgG выбран из подклассов IgG1, IgG2, IgG3, и IgG4.
12. Сконструированное антитело с цистеиновыми заменами по п.1, где сконструированное антитело с цистеиновыми заменами или родительское антитело связывается с одним или несколькими рецепторами (1)-(36), а именно:
(1) BMPR1B (рецептор белка морфогенеза кости типа IB);
(2) E16 (LAT1, SLC7A5);
(3) STEAP1 (шестидоменный трансмембранный эпителиальный антиген предстательной железы);
(4) 0772P (CA125, MUC16);
(5) MPF (MPF, MSLN, SMR, мегакариоцитарный потенцирующий фактор, мезотелин);
(6) Napi3b (NAPI-3B, NPTIIb, SLC34A2, член 2 семейства растворимых носителей 34 (фосфат натрия), натрий-зависимый фосфат-переносящий белок 3b типа II);
(7) Sema 5b (FLJ10372, KIAA1445, Mm.42015, SEMA5B, SEMAG, семафорин 5b Hlog, сема-домен, семидоменные повторы тромбоспондина (типа 1 и подобный типу 1), трансмембранный домен (ТМ) и короткий цитоплазматический домен (семафорин) 5B);
(8) PSCA hlg (2700050C12Rik, C530008O16Rik, кДНК RIKEN 2700050C12, кДНК гена RIKEN 2700050С12);
(9) ETBR (рецептор эндотелина типа В);
(10) MSG783 (RNF124, гипотетический белок FLJ20315);
(11) STEAP2 (HGNC_8639, IPCA-1, PCANAP1, STAMP1, STEAP2, STMP, ген 1, ассоциированный с раком предстательной железы, белок 1, ассоциированный с раком предстательной железы, шестидоменный трансмембранный эпителиальный антиген предстательной железы 2, шестидоменный трансмембранный белок предстательной железы);
(12) TrpM4 (BR22450, FLJ20041, TRPM4, TRPM4B, рецептор, быстрый потенциал-зависимый катионный канал, член 4 подсемейства М);
(13) CRIPTO (CR, CR1, CRGF, CRIPTO, TDGF1, фактор роста, происходящий от тератокарциномы);
(14) CD21 (CR2 (рецептор комплемента 2) или C3DR (C3d/рецептор вируса Эпштейна-Барра) или Hs.73792);
(15) CD79b (CD79B, CD79p, IGb (бета-белок, связанный с иммуноглобулином), В29);
(16) FcRH2 (IFGP4, IRTA4, SPAP1A (фосфатазный якорный белок 1a, содержащий домен SH2), SPAP1B, SPAP1C);
(17) HER2;
(18) NCA;
(19) MDP;
(20) IL20Rα;
(21) Brevican;
(22) EphB2R;
(23) ASLG659;
(24) PSCA;
(25) GEDA;
(26) BAFF-R (рецептор фактора активации В-клеток, рецептор 3 BlyS, BR3);
(27) CD22 (СВ22-В-изоформа В-клеточного рецептора);
(28) CD79a (CD79A, CD79α, связанный с иммуноглобулином альфа-белок, В-клетко-специфический белок, который ковалентно взаимодействует с Ig бета (CD79B) и образует комплекс с молекулами IgM на поверхности клеток, передает сигнал, участвующий в дифференцировке В-клеток);
(29) CXCR5 (рецептор 1 лимфомы Беркитта, связанный с G-белком рецептор, который активируется хемокином CXCL13, обеспечивает миграцию лимфоцитов и гуморальную защиту, а также играет определенную роль в инфицировании вирусом ВИЧ-2, и, вероятно, в развитии СПИДа, лимфомы, миеломы и лейкоза);
(30) HLA-DOB (бета-субъединица молекулы МНС класса II (антиген 1а), которая связывается с пептидами и презентирует их CD4+-T-лимфоцитам);
(31) Р2Х5 (ионный канал, открываемый лигандом пуринергического рецептора Р2Х5; ионный канал, открываемый внеклеточным АТР, может участвовать в синаптической передаче и в нейрогенезе, а его дефицит может играть определенную роль в патофизиологии идиопатической дисфункции мочевого пузыря);
(32) CD72 (антиген CD72 линии В-клеточной дифференцировки, Lyb-2);
(33) LY64 (лимфоцитарный антиген 64 (RP105), мембранный белок семейства богатых лейцином повторов (LRR) типа I, который регулирует активацию и апоптоз В-клеток, и потеря его функции ассоциируется с прогрессированием заболевания у пациентов с системной красной волчанкой);
(34) FcRH1 (Fc-рецептор-подобный белок 1, предполагаемый рецептор для Fc-домена иммуноглобулина, который содержит Ig-подобные домены типа С2 и домены ITAM, может играть определенную роль в дифференцировке В-лимфоцитов);
(35) IRTA2 (ассоциированный с транслокацией рецептор суперсемейства иммуноглобулина 2, предполагаемый иммунорецептор, который, возможно, играет определенную роль в развитии В-клеток и лимфомагенезе; в некоторых злокачественных В-клетках наблюдается нарушение регуляции гена посредством транслокации); и
(36) TENB2 (предполагаемый трансмембранный протеогликан, родственный семейству факторов роста EGF/герегулинов и фоллистатину).
13. Сконструированное антитело с цистеиновыми заменами по п.1, где антитело ковалентно связано с меткой для захвата, с детектируемой меткой или с твердой подложкой.
14. Сконструированное антитело с цистеиновыми заменами по п.13, где указанное антитело ковалентно связано с детектируемой меткой, являющейся флуоресцентным красителем, выбранным из красителей типа флуоресцеина и родамина; данзила; лиссамина; цианина; фикоэритрина; техасского красного и их аналогов.
15. Сконструированное антитело с цистеиновыми заменами по п.13, где указанное антитело ковалентно связано с радионуклидной детектируемой меткой, выбранной из 3H, 11С, 14С, 18F, 32P, 35S, 64Cu, 68Ga, 86Y, 99Tc, 111In, 123I, 124I, 125I, 131I, 133Xe, 177Lu, 211At и 213Bi.
16. Сконструированное антитело с цистеиновыми заменами по п.13, где указанное антитело ковалентно связано с детектируемой меткой посредством хелатообразующего лиганда, выбранного из DOTA, DOTP, DOTMA, DTPA и ТЕТА.
17. Сконструированное антитело с цистеиновыми заменами, предназначенное для конъюгирования с химиотерапевтическими лекарственными средствами, токсинами, аффинными лигандами и детектируемыми метками,
содержащее сводный цистеиновый остаток с величиной тиоловой реактивности в пределах от 0,6 до 1,0, и указанный свободный цистеиновый остаток расположен в тяжелой цепи в положении, выбранном из 112, 113, 114, и 168, в соответствии с нумерацией по Кабату;
где сконструированное антитело с цистеиновыми заменами получают способом, включающим замену одного или нескольких аминокислотных остатков родительского антитела свободным цистеиновым остатком, где родительское антитело селективно связывается с антигеном, а сконструированное антитело с цистеиновыми заменами селективно связывается с тем же антигеном, что и родительское антитело.
18. Сконструированное антитело с цистеиновыми заменами, предназначенное для конъюгирования с химиотерапевтическими лекарственными средствами, токсинами, аффинными лигандами и детектируемыми метками,
содержащее свободный цистеиновый остаток с величиной тиоловой реактивности в пределах от 0,6 до 1,0; и одну или несколько последовательностей в тяжелой цепи, выбранных из SEQ ID NO: 11, 12, 13 и 15:
где сконструированное антитело с цистеиновыми заменами получают способом, включающим замену одного или нескольких аминокислотных остатков родительского антитела свободным цистеиновым остатком, где родительское антитело селективно связывается с антигеном, а сконструированное антитело с цистеиновыми заменами селективно связывается с тем же антигеном, что и родительское антитело.
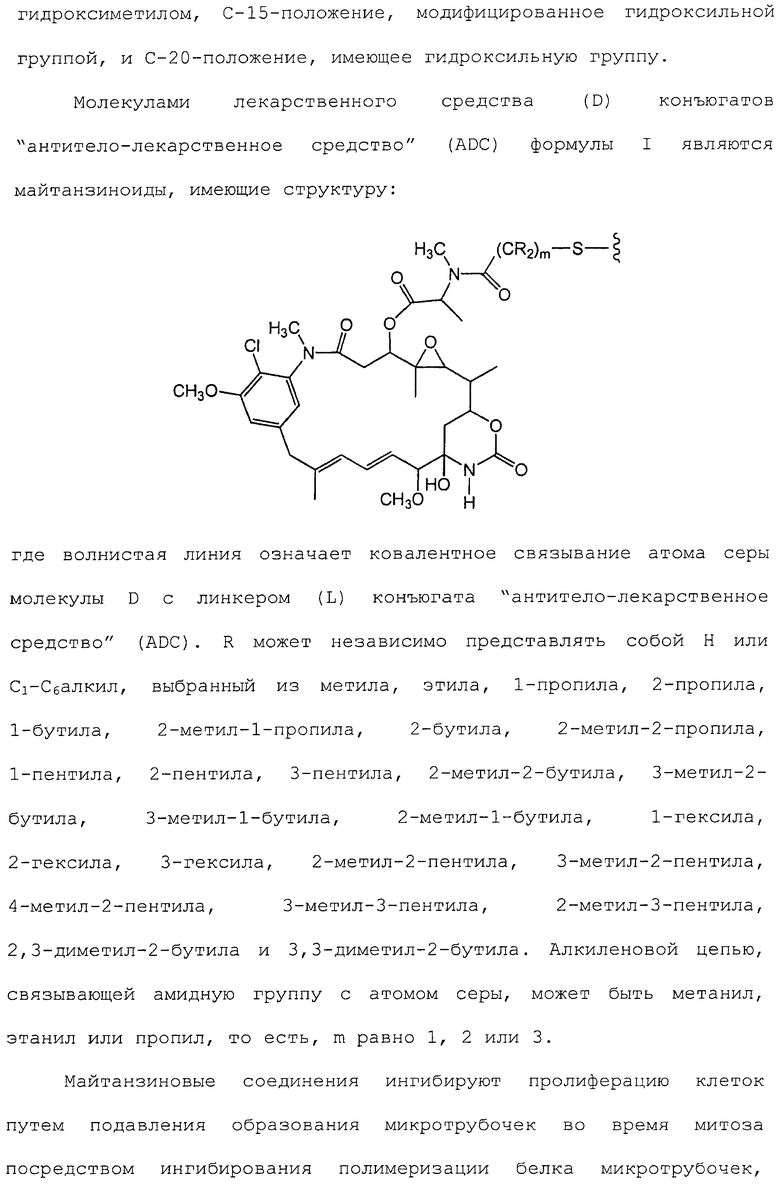
19. Соединение-конъюгат "антитело-лекарственное средство", содержащее сконструированное антитело с цистеиновыми заменами (Ab) по любому из пп.1-18, содержащее свободный цистеиновый остаток с величиной тиоловой реактивности в пределах от 0,6 до 1,0; и лекарственное средство (D), выбранное из майтанзиноида, ауристатина, доластатина, калихеамицина, где сконструированное антитело с цистеиновыми заменами присоединено к молекуле D через один или несколько свободных цистеиновых остатков посредством линкерной группы (L); причем соединение имеет формулу I:
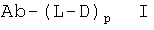
где p равно 1, 2, 3 или 4; и где сконструированное антитело с цистеиновыми заменами получают способом, включающим замену одного или нескольких аминокислотных остатков родительского антитела одним или несколькими свободными цистеиновыми остатками, где родительское антитело селективно связывается с антигеном, а сконструированное антитело с цистеиновыми заменами селективно связывается с тем же антигеном, что и родительское антитело.
20. Соединение-конъюгат "антитело-лекарственное средство" по п.19, где свободный цистеиновый остаток расположен в тяжелой цепи в положении, выбранном из 112, 113, 114, и 168, в соответствии с нумерацией по Кабату.
21. Соединение-конъюгат "антитело-лекарственное средство" по п.19, содержащее одну или несколько последовательностей в тяжелой цепи, выбранных из SEQ ID NO: 11, 12, 13 и 15:
22. Соединение-конъюгат "антитело-лекарственное средство" по п.19, где сконструированное антитело с цистеиновыми заменами получают способом, включающим:
(a) замену одного или нескольких аминокислотных остатков родительского антитела цистеином и
(b) определение реакционной способности тиоловой группы сконструированного антитела с цистеиновыми заменами путем проведения взаимодействия сконструированного антитела с цистеиновыми заменами с реагентом, взаимодействующим с тиолом;
где сконструированное антитело с цистеиновыми заменами более активно реагирует с реагентом, взаимодействующим с тиолом, по сравнению с родительским антителом.
23. Соединение-конъюгат "антитело-лекарственное средство" по п.19, которое дополнительно содержит последовательность альбумин-связывающего пептида (АВР), выбранную из SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4 и SEQ ID NO: 5.
24. Соединение-конъюгат "антитело-лекарственное средство" по п.19, где сконструированное антитело с цистеиновыми заменами связывается с рецептором ErbB, выбранным из EGFR, HER2, HER3 и HER4.
25. Соединение-конъюгат "антитело-лекарственное средство" по п.19, где сконструированное антитело с цистеиновыми заменами связывается с одним или несколькими рецепторами (1)-(36), такими как:
(1) BMPR1B (рецептор белка морфогенеза кости типа IB);
(2) E16 (LAT1, SLC7A5);
(3) STEAP1 (шестидоменный трансмембранный эпителиальный антиген предстательной железы);
(4) 0772P (CA125, MUC16);
(5) MPF (MPF, MSLN, SMR, мегакариоцитарный потенцирующий фактор, мезотелин);
(6) Napi3b (NAPI-3B, NPTIIb, SLC34A2, член 2 семейства растворимых носителей 34 (фосфат натрия), натрий-зависимый фосфат-переносящий белок 3b типа II);
(7) Sema 5b (FLJ10372, KIAA1445, Mm.42015, SEMA5B, SEMAG, семафорин 5b Hlog, сема-домен, семидоменные повторы тромбоспондина (типа 1 и подобный типу 1), трансмембранный домен (ТМ) и короткий цитоплазматический домен (семафорин) 5B);
(8) PSCA hlg (2700050C12Rik, C53 0008016Rik, кДНК RIKEN 2700050С12, кДНК гена RIKEN 2700050C12);
(9) ETBR (рецептор эндотелина типа В);
(10) MSG783 (RNF124, гипотетический белок FLJ20315);
(11) STEAP2 (HGNC_8639, IPCA-1, PCANAP1, STAMP1, STEAP2, STMP, ген 1, ассоциированный с раком предстательной железы, белок 1, ассоциированный с раком предстательной железы, шестидоменный трансмембранный эпителиальный антиген предстательной железы 2, шестидоменный трансмембранный белок предстательной железы);
(12) TrpM4 (BR22450, FLJ20041, TRPM4, TRPM4B, рецептор, быстрый потенциал-зависимый катионный канал, член 4 подсемейства М);
(13) CRIPTO (CR, CR1, CRGF, CRIPTO, TDGF1, фактор роста, происходящий от тератокарциномы);
(14) CD21 (CR2 (рецептор комплемента 2) или C3DR (C3d/рецептор вируса Эпштейна-Барра) или Hs.73792);
(15) CD79b (CD79B, CD79β, IGb (бета-белок, связанный с иммуноглобулином), В29);
(16) FcRH2 (IFGP4, IRTA4, SPAP1A (фосфатазный якорный белок 1a, содержащий домен SH2), SPAP1B, SPAP1C);
(17) HER2;
(18) NCA;
(19) MDP;
(20) IL20Rα;
(21) Brevican;
(22) EphB2R;
(23) ASLG659;
(24) PSCA;
(25) GEDA;
(26) BAFF-R (рецептор фактора активации В-клеток, рецептор 3 BlyS, BR3);
(27) CD22 (СП22-В-изоформа В-клеточного рецептора);
(28) CD79a (CD79A, CD79α, связанный с иммуноглобулином альфа- белок, В-клеткоспецифический белок, который ковалентно взаимодействует с Ig бета (CD79B) и образует комплекс с молекулами IgM на поверхности клеток, передавая сигнал, участвующий в дифференцировке В-клеток);
(29) CXCR5 (рецептор 1 лимфомы Беркитта, связанный с G-белком рецептор, который активируется хемокином CXCL13, обеспечивает миграцию лимфоцитов и гуморальную защиту, а также играет определенную роль в инфицировании вирусом ВИЧ-2, и, вероятно, в развитии СПИДа, лимфомы, миеломы и лейкоза);
(30) HLA-DOB (бета-субъединица молекулы МНС класса II (антиген Ia), которая связывается с пептидами и презентирует их CD4+-T-лимфоцитам);
(31) Р2Х5 (ионный канал, открываемый лигандом пуринергического рецептора Р2Х5; ионный канал, открываемый внеклеточным АТР, может участвовать в синаптической передаче и в нейрогенезе, а его дефицит может играть определенную роль в патофизиологии идиопатической дисфункции мочевого пузыря);
(32) CD72 (антиген CD72 линии В-клеточной дифференцировки, Lyb-2);
(33) LY64 (лимфоцитарный антиген 64 (RP105), мембранный белок семейства богатых лейцином повторов (LRR) типа I, который регулирует активацию и апоптоз В-клеток, и потеря его функции ассоциируется с прогрессированием заболевания у пациентов с системной красной волчанкой);
(34) FcRH1 (Fc-рецептор-подобный белок 1, предполагаемый рецептор для Fc-домена иммуноглобулина, который содержит Ig-подобные домены типа С2 и домены ITAM, может играть определенную роль в дифференцировке В-лимфоцитов);
(35) IRTA2 (ассоциированный с транслокацией рецептор суперсемейства иммуноглобулина 2, предполагаемый иммунорецептор, который, возможно, играет определенную роль в развитии В-клеток и лимфомагенезе; в некоторых злокачественных В-клетках наблюдается нарушение регуляции гена посредством транслокации); и
(36) TENB2 (предполагаемый трансмембранный протеогликан, родственный семейству факторов роста EGF/герегулинов и фоллистатину).
26. Соединение-конъюгат "антитело-лекарственное средство" по п.19, где p равно 1 или 2.
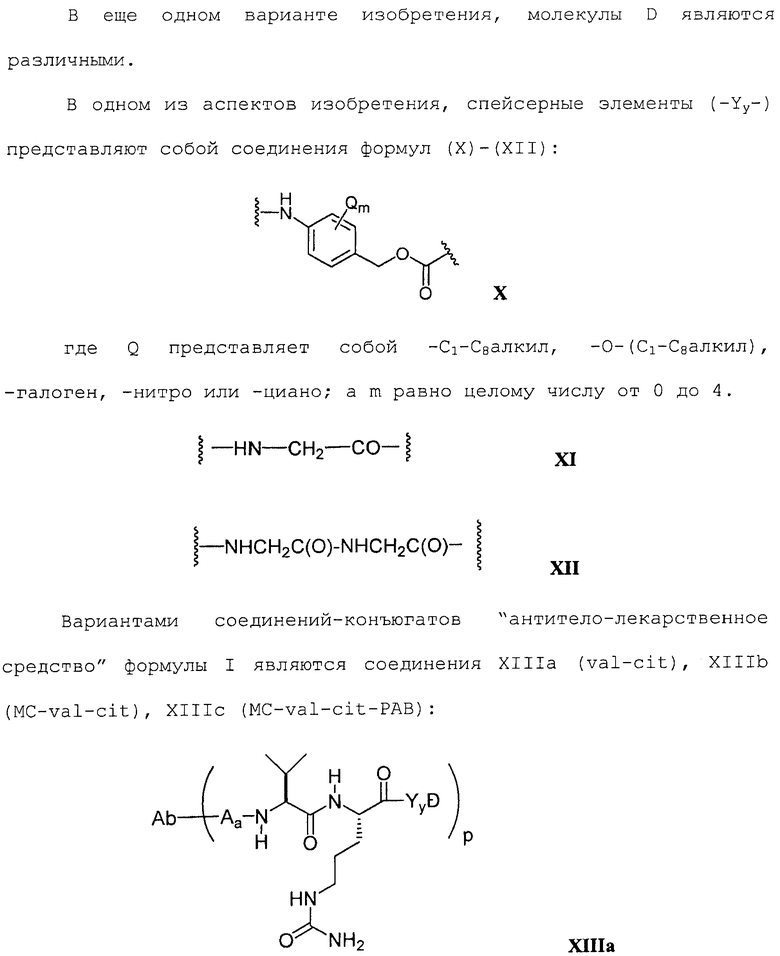
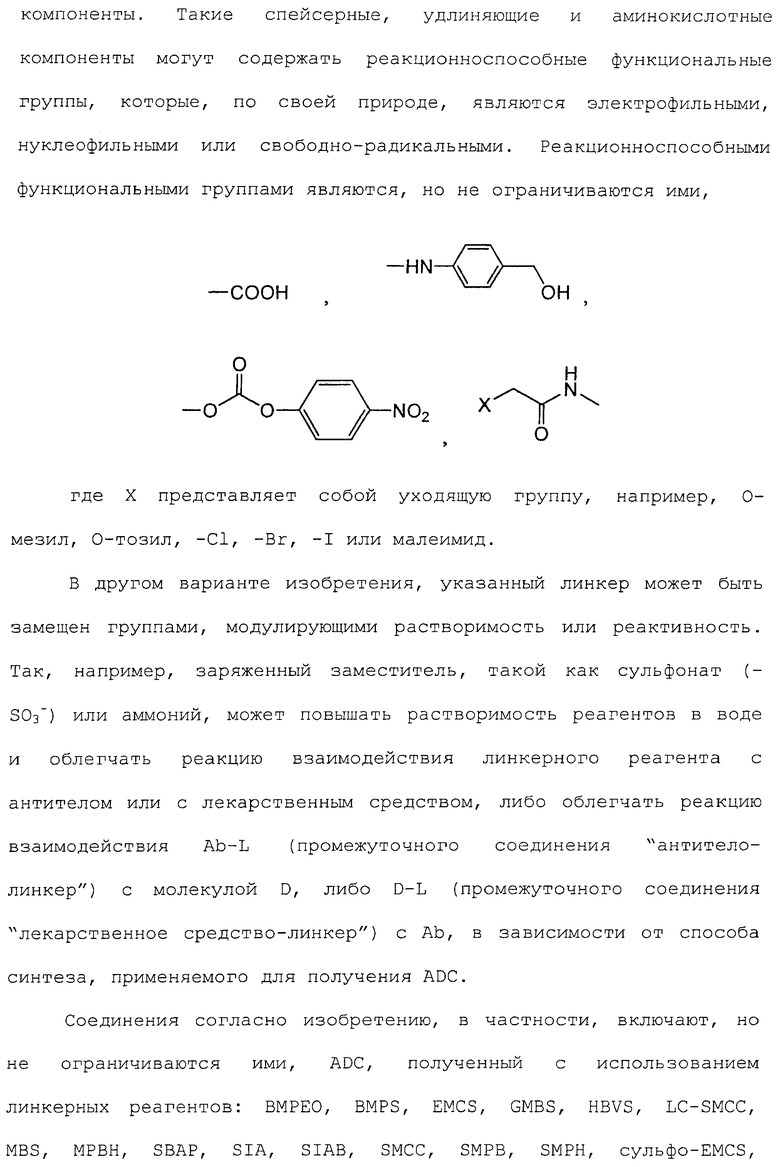
27. Соединение-конъюгат "антитело-лекарственное средство" по п.19, где L имеет формулу:
 ,
,
где А представляет собой удлиняющий компонент, ковалентно присоединенный к тиолу сконструированного антитела с цистеиновыми заменами (Ab);
а равно 0 или 1;
каждый W независимо представляет собой аминокислоту;
w независимо представляет собой целое число от 0 до 12;
Y означает спейсерный компонент, ковалентно связанный с молекулой лекарственного средства; и
у равно 0, 1 или 2.
28. Соединение-конъюгат "антитело-лекарственное средство" по п.27, имеющее формулу:

где РАВ представляет собой пара-аминобензилкарбамоил, a R17 представляет собой двухвалентный радикал, выбранный из (СН2)r, С3-C8 карбоциклила, -O-(СН2)r, арилена, (СН2)r-арилена, арилен-(СН2)r-, (CH2)r-(C3-C8-карбоциклила), (С3-С8-карбоциклил)-(СН2)r-, -(С3-C8- гетероциклила), (СН2)r-(C3-С8-гетероциклила), (C3-C8 гетероциклил)-(СН2)r, -(CH2)rC(O)NRb(CH2)r, -(СН2СН2О)r-, -(CH2CH2O)r-СН2-, -(CH2)rC(O)NRb(CH2CH2O)r-, -(CH2)rC(O)NRb(CH2CH2O)r-CH2-, -(CH2CH2O)rC(O)NRb(CH2CH2O)r-, -(CH2CH2O)rC(O)NRb(CH2CH2O)r-CH2- и -(CH2CH2O)rC(O)NRb(CH2)r-, где Rb представляет собой Н, C1-С6алкил, фенил или бензил, а r независимо представляет собой целое число от 1 от 10.
29. Соединение-конъюгат "антитело-лекарственное средство" по п.28, где Ww представляет собой валин-цитруллин.
30. Соединение-конъюгат "антитело-лекарственное средство" по п.28, где R17 представляет собой (СН2)5 или (СН2)2.
31. Соединение-конъюгат "антитело-лекарственное средство" по п.28, имеющее формулу:

32. Соединение-конъюгат "антитело-лекарственное средство" по п.31, где R17 представляет собой (СН2)5 или (CH2)2.
33. Соединение-конъюгат "антитело-лекарственное средство" по п.28, имеющее формулу:

34. Соединение-конъюгат "антитело-лекарственное средство" по п.19, где L образован из линкерного реагента SMCC или ВМРЕО.
35. Соединение-конъюгат "антитело-лекарственное средство" по п.19, где молекула лекарственного средства D выбрана из ингибитора микротубулина, ингибитора митоза, ингибитора топоизомеразы и ДНК- интеркалирующего агента.
36. Соединение-конъюгат "антитело-лекарственное средство" по п.19, где молекула лекарственного средства D выбрана из майтанзиноида, ауристатина, доластатина и калихеамицина.
37. Соединение-конъюгат "антитело-лекарственное средство" по п.19, где D представляет собой ММАЕ со структурой:
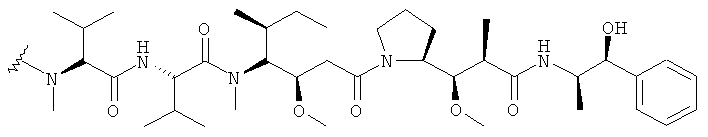 ,
,
где волнистая линия указывает на сайт присоединения к линкеру L.
38. Соединение-конъюгат "антитело-лекарственное средство" по п.19, где
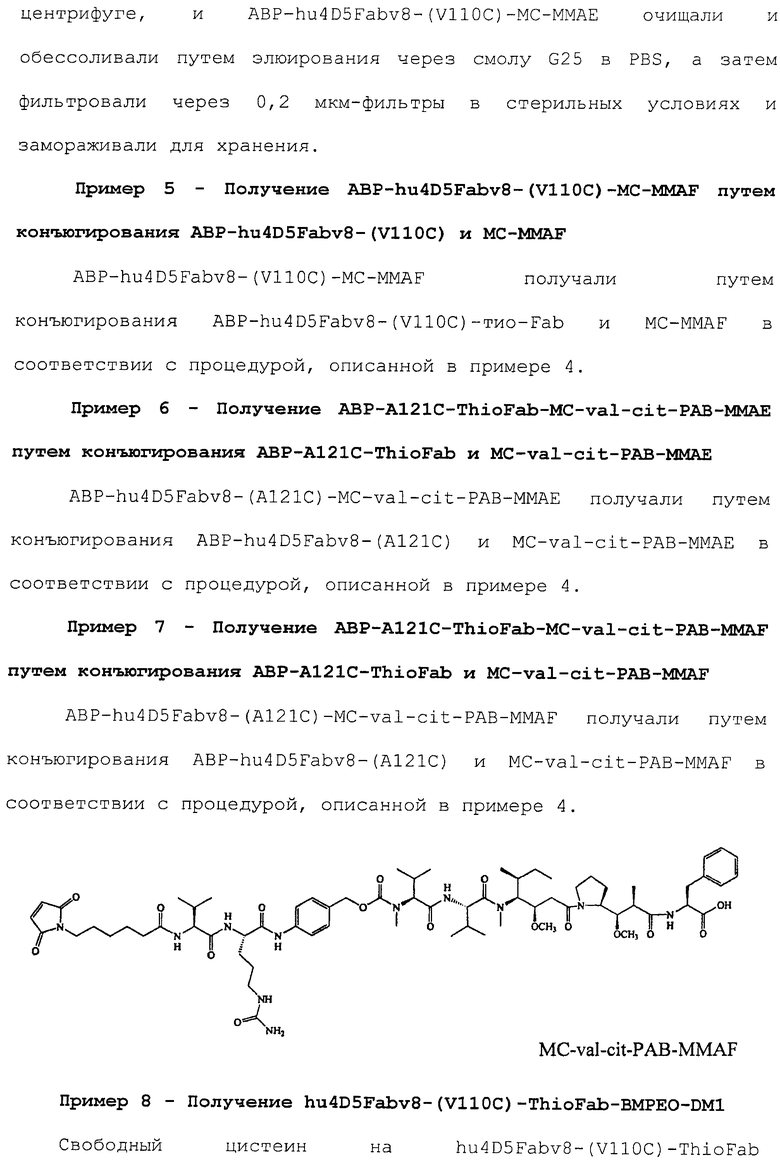
D представляет собой MMAF со структурой:
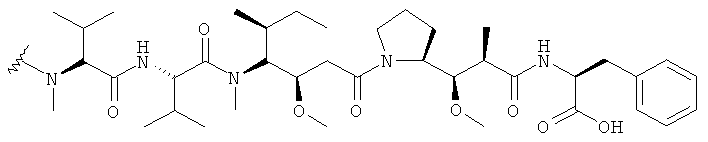 ,
,
где волнистая линия указывает на сайт присоединения к линкеру L.
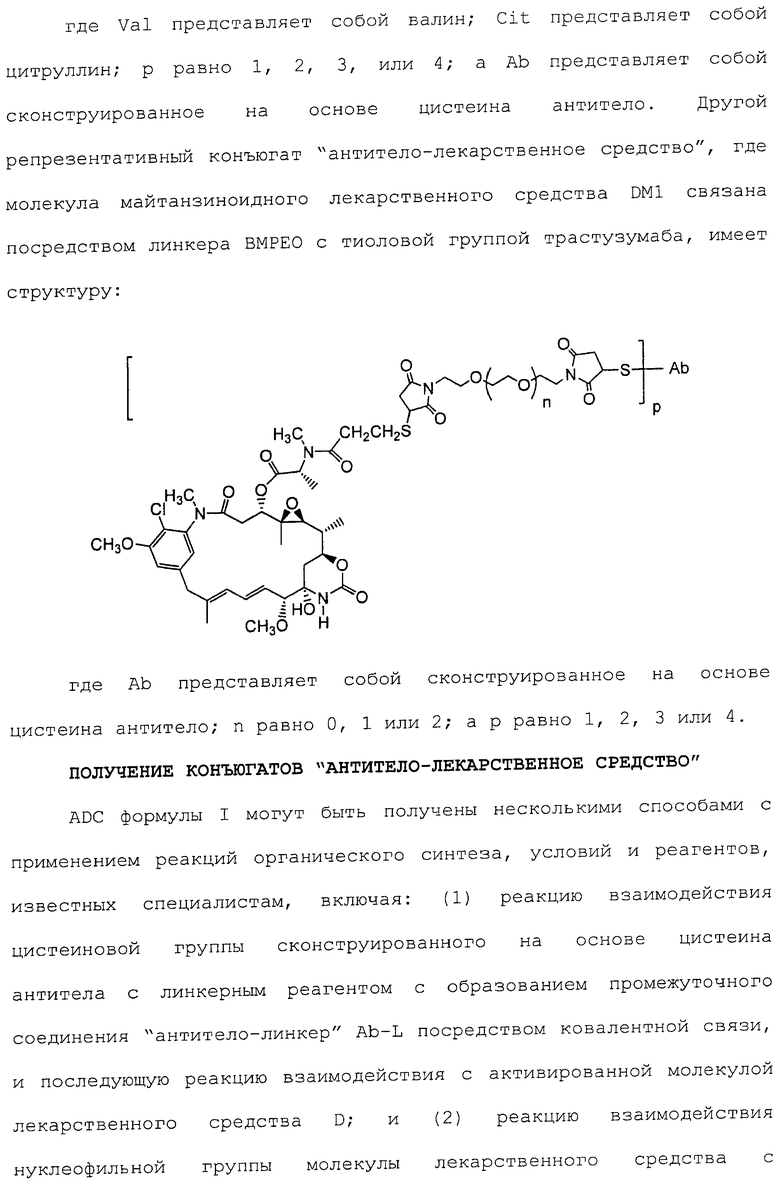
39. Соединение-конъюгат "антитело-лекарственное средство по п.19, где D представляет собой DM1 со структурой:
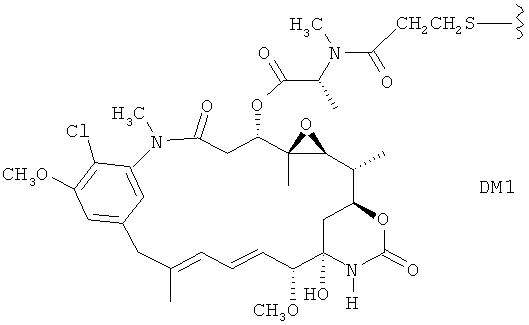
или DM4 со структурой:

где волнистая линия указывает на сайт присоединения к линкеру L.
40. Соединение-конъюгат "антитело-лекарственное средство" по п.19, где указанное родительское антитело выбрано из моноклонального антитела, биспецифического антитела, химерного антитела, человеческого антитела, гуманизованного антитела и фрагмента антитела.
41. Соединение-конъюгат "антитело-лекарственное средство" по п.19, где родительским антителом является huMAb4D5-8 (трастузумаб), анти-ErbB2 антитело, анти-EphB2R антитело, анти-CD22 антитело, анти-MUC16 антитело.
42. Соединение-конъюгат "антитело-лекарственное средство" по п.19, где указанным родительским антителом является интактное антитело, выбранное из IgA, IgD, IgE, IgG и IgM.
43. Соединение-конъюгат "антитело-лекарственное средство" по п.42, где IgG выбран из подклассов IgG1, IgG2, IgG3 и IgG4.
44. Соединение-конъюгат "антитело-лекарственное средство" по п.19, имеющий структуру:

где n равно 0, 1, или 2; и
Ab представляет собой сконструированное антитело с цистеиновыми заменами.
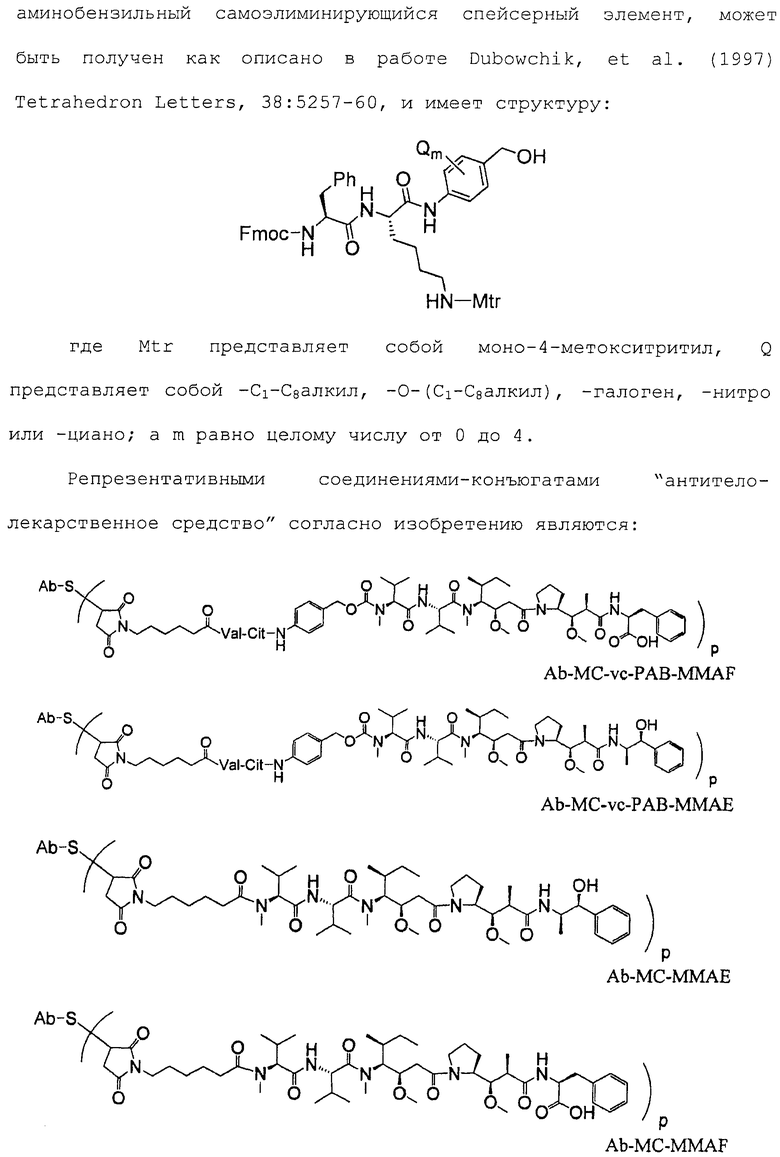
45. Соединение-конъюгат "антитело-лекарственное средство" по п.19, выбранное из следующих структур:
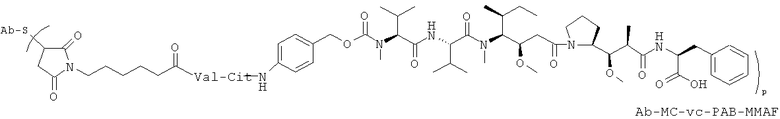
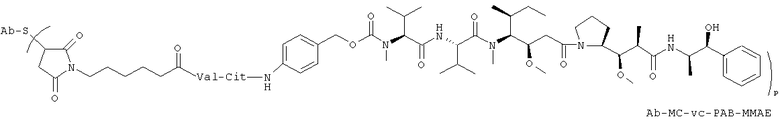

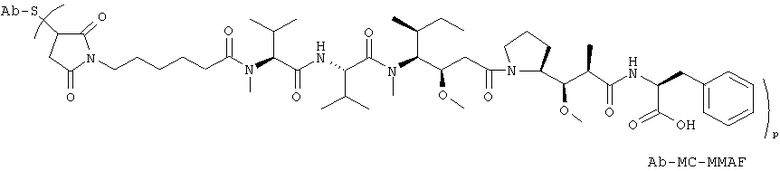
где Val представляет собой валин, и
Cit представляет собой цитруллин.
46. Соединение-конъюгат "антитело-лекарственное средство", предназначенное для конъюгирования с химиотерапевтическими лекарственными средствами, токсинами, аффинными лигандами и детектируемыми метками,
выбранное из следующих структур:


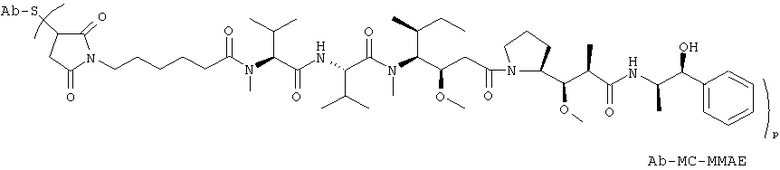

где Val представляет собой валин;
Cit представляет собой цитруллин;
p равно 1, 2, 3 или 4; и
Ab представляет собой антитело по любому из пп.1-18.
47. Соединение-конъюгат "антитело-лекарственное средство" по п.19, используемое для лечения рака.
48. Фармацевтическая композиции, использующаяся в качестве иммуноконъюгата, содержащая соединение-конъюгат "антитело-лекарственное средство" по п.19 или его фармацевтически приемлемую соль, и фармацевтически приемлемый разбавитель, носитель или наполнитель.
49. Фармацевтическая композиция по п.48, которая дополнительно содержит терапевтически эффективное количество дополнительного химиотерапевтического средства.
50. Промышленное изделие, содержащее:
соединение-конъюгат "антитело-лекарственное средство" по п.19,
контейнер и
вкладыш, вложенный в контейнер, или этикетку на упаковке, указывающий, что соединение может быть использовано для лечения рака.
51. Конъюгат антитело-лекарственное средство по п.19, содержащее одну или несколько последовательностей в легкой цепи, выбранных из SEQ ID NO: 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 45 и 46:
SLASASCGDRVT (EQ ID NO: 17)
QKPGKCPKLLI (SEQ ID NO: 18)
EIKRTCAAPSV (SEQ ID NO: 19)
TCAAPCVFIFPP (SEQ ID NO: 20)
FIFPPCDEQLK (SEQ ID NO: 21)
DEQLKCGTASV (SEQ ID NO: 22)
FYPRECKVQWK (SEQ ID NO: 23)
WKVDNCLQSGN (SEQ ID NO: 24)
ALQSGCSQESV (SEQ ID NO: 25)
VTEQDCKDSTY (SEQ ID NO: 26)
GLSSPCTKSFN (SEQ ID NO: 27)
FLSVSCGGRVT (SEQ ID NO: 45)
QKPGNCPRLLI (SEQ ID NO: 46).
| RENARD M et al: "Deriving topological constraints from functional data for the design of reagentless fluorescent immunosensors" J Mol Biol | |||
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРИРОДНОГО ГУМАНИЗИРОВАННОГО АНТИТЕЛА | 1998 |
|
RU2221809C2 |
Авторы
Даты
2011-02-27—Публикация
2005-09-22—Подача