Изобретение относится к медицине, конкретно к фармакологии, и касается противоопухолевых средств.
Известен биологически активный стильбен, выделенный из винограда - резвератрол, который ингибирует инициирование, развитие и прогрессию канцерогенного процесса [Kim S., Min S.Y., Lee S.K., Cho W.-J. (2003) Chem. Pharm. Bull. V.51 N.5. P.16-521]. Экспериментально доказано, что резвератрол вызывает апоптоз у трудноизлечиваемых раковых клеток простаты (РС-3 и DU145) [Gill С. et. al. (2007) The Prostate. V.67. I.15. P.1641-1653]. Считается, что использование резвератрола может быть одним из самых эффективных способов, с помощью которого можно увеличить чувствительность опухолевых клеток простаты к химиотерапии, поскольку он не токсичен и эффективен даже при низких концентрациях, что было подтверждено экспериментально на животных. Резвератрол детоксифицирует канцерогенные вещества и стимулирует генетические механизмы, включающие апоптоз раковых клеток.
Известны изофлавоноиды, выделенные из сои, такие как даидзеин и генистеин, проявляющие противоопухолевые свойства [Jian L. (2009) Mol Nutr Food Res. V.53. P.217-226]. Экспериментально был подтвержден ингибирующий эффект генистеина на рост клеток рака молочной железы, таких как MDA-MB-231, MDA-MB-435, МКФ 7 и раковых клеток простаты РС3 и LNCaP. Он также эффективен против раковых клеток легкого Н460 и Н322 и некоторых видов лейкоза [Sarkar F.H., Li Y. (2003) Cancer Investigation. V.21. N.5. P.744-757; Sarkar F.H., Li Y. (2002) Cancer Metastas. Rev. V.21, N.3. P.265-280; Tominaga Y., Wang A., Wang R.-H., Wang X., Cao L., Deng С.-Х. (2007) Cell Death Differ. V.14. N.3. P.472-479; Chen W.-F, Huang M.-H, Tzang C.-H, Yang M, Wong M.-S. (2003) Biochim. Biophys. Acta. V.1638. N.2. P.187-196].
Прототипом заявляемого средства является растительный компонент - изофлавоноид генистеин, который в сочетании с 5-фтороурацилом способствует индуцированию клеточного апоптоза клеток рака толстой кишки НТ-29 [Фазлул X., Саркар и Ивей Ли, Cancer Res., 2006; 66: (7), April 1, review].
Задачей изобретения является расширение арсенала противоопухолевых средств.
Поставленная задача достигается применением сухого экстракта ядровой древесины маакии амурской в качестве противоопухолевого средства в отношении клеток рака кишечника НТ-29 и DLD-1.
Средство представляет собой высушенный под вакуумом спиртовой экстракт, полученный из измельченной ядровой древесины этого растения, и состоит из растительных полифенолов, обладающих гепатозащитным действием [RU Патент №2104027 C1, 10.02.1998].
Сухой экстракт ядровой древесины маакии амурской зарегистрирован в качестве субстанции (Р №003309/01 от 12.04.2004 г.) для приготовления лекарственного средства «Максар® таблетки, покрытые оболочкой, 60 мг» (Р №003294/01 от 12.04.2004 г.), применяемого для лечения хронических гепатитов [RU 2175237 С2, 27.10.2001].
Известно применение препарата маакии амурской экстракт сухой в качестве гемореологического и антитромбоцитарного средства [RU 2342944 C1, 10.01.2009].
Использование сухого экстракта ядровой древесины маакии амурской в качестве противоопухолевого средства в отношении клеток рака кишечника в доступной патентной и другой научно-технической литературе не описано. Это новое свойство известного препарата явным образом не вытекает из уровня техники. Сухой экстракт ядровой древесины маакии амурской может выпускаться в лекарственной форме и в виде биологически активных добавок для лечения и профилактики заболеваний рака кишечника.
Новые свойства сухого экстракта ядровой древесины маакии амурской были найдены экспериментальным путем.
Изобретение иллюстрируется следующими чертежами.
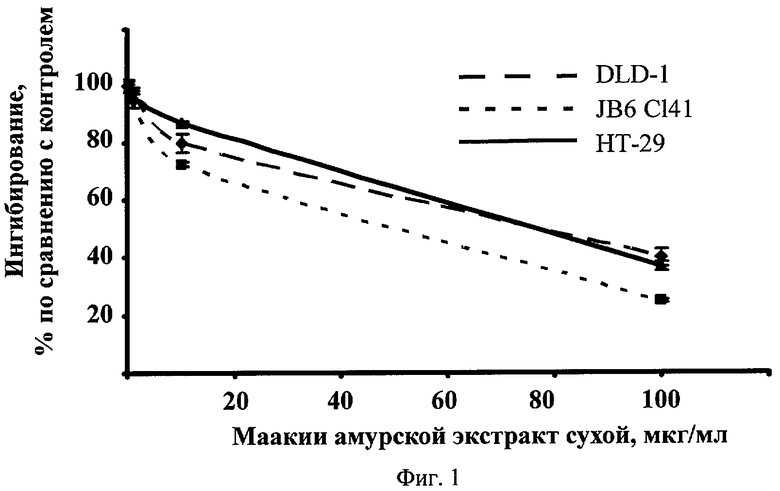
Фиг.1. Жизнеспособность DLD-1 и НТ-29 клеток, обработанных сухим экстрактом ядровой древесины маакии амурской.
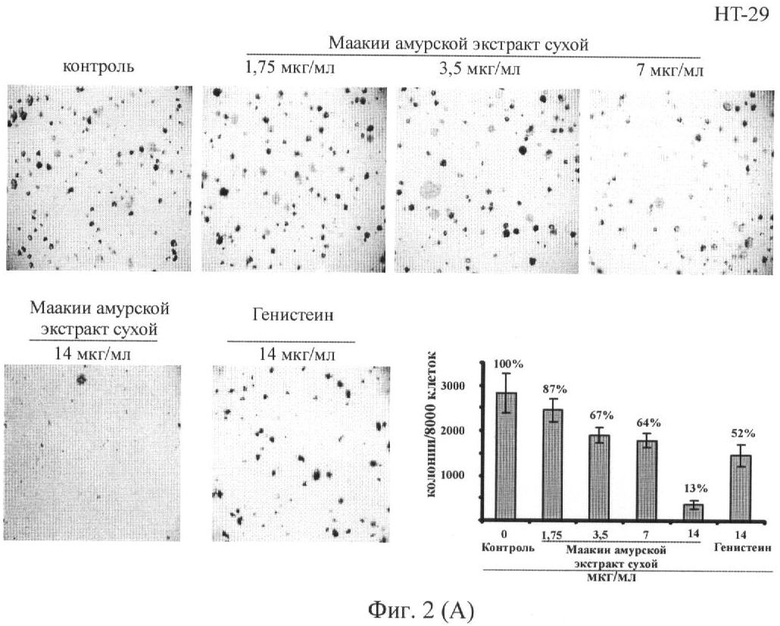
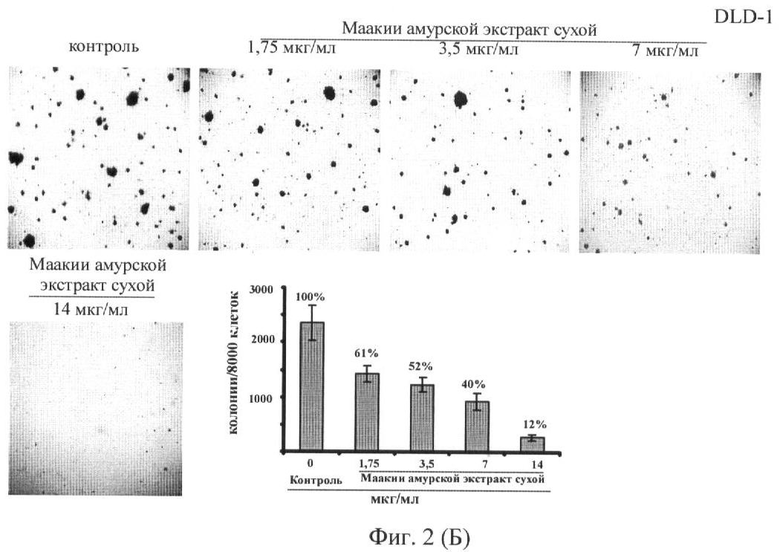
Фиг.2. Ингибирующее действие сухого экстракта ядровой древесины маакии амурской на рост колоний клеток рака кишечника человека НТ-29 (А) и DLD-1 (Б). Колонии клеток рака кишечника человека были оценены с использованием обратимого микроскопа и Motic Image Plus программы. Графические данные, представленные на фигурах, проиллюстрированы имиджами.
Применение сухого экстракта ядровой древесины маакии амурской в качестве средства, обладающего противоопухолевым действием в отношении клеток рака кишечника, иллюстрируется экспериментом.
В эксперименте использовали клеточные линии JB6 С141 (нормальные клетки кожи мышей, АТСС # CRL-2010), НТ-29 (клетки рака кишечника человека, АТСС # НТВ-38), DLD-1 (клетки рака кишечника человека, АТСС # CCL-221) и RPMI-7951 (клетки меланомы кожи человека, АТСС # НТВ-66) из американской коллекции культур (АТСС, США) и питательные среды McCoy, RPMI 1640, MEM, BME.
Культивирование клеток. Нормальные клетки кожи мышей JB6 С141 культивировали в инкубаторе при 37°С и 5% CO2 в среде MEM с добавлением 5% FBS. Клетки рака кишечника человека НТ-29 и DLD-1 культивировали в инкубаторе при 37°С и 5% СО2 в среде МсСоу с добавлением 10% FBS и RPMI 1640 с добавлением 10% FBS, соответственно. Клетки рака кишечника человека RPMI 7951 культивировали в инкубаторе при 37°С, 5% СО2 в среде MEM с добавлением 10% FBS. Все среды содержали 2 мМ L-глутамина, 100 ед/л пенициллина и 100 мкг/л стрептомицина.
Статистическая обработка данных проведена с использованием t-критерия Стъюдента в условиях заданной доверительной вероятности, равной 95% [программа SigmaPlot 2000, версия 6, (SPSS Inc., USA)].
Пример 1. Определение цитотоксичности заявляемого средства.
Для оценки цитотоксичности были использованы нормальные клетки кожи мышей JB6 С141, опухолевые клетки НТ-19, DLD-1 (рак кишечника человека), RPMI-7951 (меланома человека) и применен MTS-метод. Клетки (1×104/мл) рассеивали в 96-луночные планшеты и культивировали в 200 мкл соответствующей среды в инкубаторе при температуре 37°С в течение 24 часов. Затем клетки обрабатывали веществами различной концентрации и инкубировали в течение 24 часов. После инкубации в лунки добавляли по 15 мкл 3-(4,5-диметилтиазол-2-ил)-5-(3-карбоксиметоксифенил)-2-(4-сульфофенил)-2Н-тетразолия (MTS-реагент) и помещали в инкубатор (37°С) на 4 часа. MTS-метод основан на свойстве живых клеток трансформировать MTS-реагент в формазан. Количество образовавшегося формазана пропорционально количеству оставшихся в живых клеток после воздействия вещества и определяется спектрофотометрически при 492 нм. Оптическую плотность измеряли на спектрофотометре «Bio-Tek Instruments» (США).
Концентрации, при которых заявляемое средство проявило цитотоксичность, были следующие: 28 мкг/мл, 52 мкг/мл и 73 мкг/мл для клеток JB6 С141, DLD-1 и НТ-19, соответственно. Оно не проявило цитотоксичность для клеток RPMI-7951 в концентрации до 100 мкг/мл.
Пример 2. Определение способности заявляемого средства ингибировать рост колоний клеток рака кишечника человека и меланомы человека (метод мягкого агара).
Метод мягкого агара основан на том, что раковые клетки, находящиеся в неприкрепленном состоянии в толще мягкого агара дают рост клеточных колоний, тогда как вещества, обладающие антиопухолевым действием, ингибируют рост клеточных колоний. Эксперимент был выполнен на клетках рака кишечника НТ-29, DLD-1, как описано Colburn с некоторыми модификациями [Colburn, N.H. et. al. (1981) Proc Natl Acad Sci USA V.78. I.11. P.6912-6916]. Все вещества были растворены в диметилсульфоксиде (ДМСО), в качестве контроля для обработки клеток использовали ДМСО. Клетки рака кишечника человека НТ-29, DLD-1 и меланомы кожи человека RPMI-7951 (2,4×104 клеток/мл) были обработаны экстрактами веществ в концентрации до 7 мкг/мл в 1 мл 0,33% ВМЕ агара поверх 3,5 мл 0,5% ВМЕ агара, содержащего экстракты веществ в концентрации до 7 мкг/мл. Клетки были культивированы при 37°С, 5% CO2 в течение 30 дней. Колонии клеток были оценены с использованием обратимого микроскопа (Motic AE 20, China) и Motic Image Plus программы (China). Для каждого вещества были выполнены два независимых эксперимента с тремя образцами для каждой концентрации.
Для определения действия заявляемого средства на рост колоний клеток рака кишечника человека и меланомы кожи человека в мягком агаре были выбраны концентрации до 7 мкг/мл, поскольку средство при концентрации 14 мкг/мл ингибировало рост колоний клеток НТ-29 и DLD-1 практически на 90%. Следует отметить, что при исследованных концентрациях (до 7 мкг/мл) не наблюдалось ингибирование роста колоний клеток меланомы кожи человека RPMI-7951, что указывает на избирательное действие сухого экстракта ядровой древесины маакии амурской по отношению к клеткам рака кишечника человека.
Результаты показывают, что под действием заявляемого средства в исследованном интервале концентрации происходит ингибирование роста колоний клеток рака кишечника человека DLD-1 и НТ-29 по сравнению с контролем. Ингибирование роста колоний на 50% для клеток DLD-1 и НТ-29 происходит при концентрациях 4,1 и 8,8 мкг/мл соответственно. Ингибирование роста колоний клеток рака кишечника человека НТ-29 под действием генистеина и сухого экстракта ядровой древесины маакии амурской при концентрации 14 мкг/мл составляет 48% и 87%, соответственно. Эти результаты указывают на то, что заявляемое средство обладает более сильным противоопухолевым действием по отношению к клеткам рака кишечника человека по сравнению с генистеином.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНГИБИТОР ПРОТЕИНКИНАЗЫ ТОРК С НАПРАВЛЕННЫМ ХЕМОПРЕВЕНТИВНЫМ ДЕЙСТВИЕМ IN VITRO | 2014 |
|
RU2566268C1 |
| ГЕПАТОПРОТЕКТОРНОЕ СРЕДСТВО | 2003 |
|
RU2244553C1 |
| СРЕДСТВО, ПРЕДОТВРАЩАЮЩЕЕ ТРАНСФОРМАЦИЮ НОРМАЛЬНЫХ КЛЕТОК МЛЕКОПИТАЮЩИХ В ОПУХОЛЕВЫЕ | 2010 |
|
RU2429840C1 |
| Средство, обладающее противовирусным действием в отношении герпесвируса человека I типа и энтеровируса В | 2022 |
|
RU2798659C1 |
| АНТИКЛИМАКТЕРИЧЕСКОЕ СРЕДСТВО | 2009 |
|
RU2398592C1 |
| СРЕДСТВО, ПРЕДОТВРАЩАЮЩЕЕ ТРАНСФОРМАЦИЮ НОРМАЛЬНЫХ КЛЕТОК МЛЕКОПИТАЮЩИХ В ОПУХОЛЕВЫЕ | 2010 |
|
RU2429839C1 |
| Средство, обладающее противовирусным действием в отношении коронавируса SARS-CoV-2 | 2022 |
|
RU2788762C1 |
| Способ получения полифенольного комплекса из ядровой древесины маакии амурской | 2023 |
|
RU2822249C1 |
| ТЕРАПЕВТИЧЕСКИЕ ХИНОНЫ | 2005 |
|
RU2411229C2 |
| ГЕПАТОПРОТЕКТИВНОЕ СРЕДСТВО | 2011 |
|
RU2454243C1 |
Изобретение относится к химико-фармацевтической промышленности, а именно к созданию средства, обладающего противоопухолевой активностью. В качестве средства, обладающего противоопухолевой активностью в отношении клеток рака кишечника НТ-29 и DLD-1, применяют сухой экстракт ядровой древесины маакии амурской. Средство расширяет арсенал противоопухолевых средств, активных в отношении клеток рака кишечника НТ-29 и DLD-1. 3 ил.
Применение сухого экстракта ядровой древесины маакии амурской в качестве противоопухолевого средства в отношении клеток рака кишечника НТ-29 и DLD-1.
| Фазлул X., Саркар и Ивей Ли | |||
| Использование хемопревентивных агентов в целях повышения эффективности терапии рака // Cancer Res., 2006; 66: (7), April 1, review | |||
| СПОСОБ ПОЛУЧЕНИЯ РАСТИТЕЛЬНЫХ ПОЛИФЕНОЛОВ, ОБЛАДАЮЩИХ ГЕПАТОЗАЩИТНЫМ ДЕЙСТВИЕМ | 1996 |
|
RU2104027C1 |
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКИХ ГЕПАТИТОВ | 1998 |
|
RU2175237C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ГЕМОРЕОЛОГИЧЕСКОЙ И АНТИТРОМБОЦИТАРНОЙ АКТИВНОСТЬЮ | 2007 |
|
RU2342944C1 |
| ФИТОКОМПЛЕКС, ОБЛАДАЮЩИЙ АНТИОКСИДАНТНОЙ АКТИВНОСТЬЮ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2001 |
|
RU2188031C1 |
Авторы
Даты
2011-03-27—Публикация
2009-12-01—Подача