Изобретение относится к медицине, конкретно к онкологии, и касается веществ, обладающих способностью предотвращать злокачественное пререрождение нормальных клеток млекопитающих (в том числе человека) в опухолевые.
Проблема опухолевых заболеваний является одной из острейших проблем современного здравоохранения. Рак (злокачественные опухолевые заболевания) является одной из основных причин смерти в мире. По данным ВОЗ в настоящее время на онкологию приходится 13% от общего числа смертей. За последние 25 лет заболеваемость раком выросла в 1,5-2,0 раза, а к 2030 году по прогнозам вырастет еще втрое, причем особенно тревожно положение в развитых странах. Для различных разновидностей рака характерна одна общая черта - эти болезни чрезвычайно трудно излечить. Следует признать, что лечение онкологических заболеваний в настоящее время высоко затратно и сравнительно малоэффективно. В то же время считается, что до 40% случаев заболевания раком можно предотвратить с помощью здорового рациона питания, физической активности и воздержания от употребления табака. Профилактика может включать употребление различных продуктов и биопрепаратов, содержащих вещества, предотвращающие перерождение нормальных клеток в раковые.
Противоопухолевые хемопревентивные вещества - это обычно природные вторичные метаболиты или их синтетические аналоги, которые ингибируют трансформацию нормальных клеток в прораковые или тормозят прогрессию прораковых клеток в раковые [Hong W.K., Sporn М.В. (1997) Recent advances in chemoprevention of cancer. Science 278:1073-1077; Sporn M.B. (1976) Approaches to prevention of epithelial cancer during the preneoplastic period. Cancer Res 36:2699-2702; Umar A, Viner J.L., Hawk E.T. (2001) The future of colon cancer prevention. Ann NY Acad Sci 952:88-108].
Следовательно, эффективное канцер-превентивное вещество должно вклиниваться в процесс канцерогенеза с тем, чтобы уничтожить прораковые клетки до того, как они трансформируются в раковые [Wattenberg L.W. (1995) What are the critical attributes for cancer chemopreventive agents? Ann NY Acad Sci 768:73-81; Smith T.J., Hong J-Y, Wang Z-Y, Yang C-S (1995) How can carcinogenesis be inhibited? Ann NY Acad Sci 768:82-90; Kelloff G.J., Crowell J.A., Steele V.E., Lubet R.A., Boone C.W., Malone W.A., et al. (1999) Progress in cancer chemoprevention. Ann NY Acad Sci 889:1-13].
Некоторые противораковые хемопревентивные вещества, к примеру ретиноиды и антиэстрогены, оказывают цитостатическое действие на трансформированные клетки путем воздействия на клеточную пролиферацию или дифференциацию [Hong W.K., Sporn М.В. (1997) Recent advances in chemoprevention of cancer. Science 278:1073-1077; Wattenberg L.W. (1995) What are the critical attributes for cancer chemopreventive agents? Ann N.Y Acad Sci 768:73-81; Kelloff G.J., Crowell J.A., Steele V.E., Lubet R.A., Boone C.W., Malone W.A., et al. (1999) Progress in cancer chemoprevention. Ann NY Acad Sci 889:1-13]. Такие вещества должны в течение долгого времени вводиться в организм людей, подверженных повышенному риску раковых заболеваний. В этом случае токсичность веществ, в течение долгого времени вводимых в организм, а также возможность развития резистентности к ним могут ограничить возможность использования данных хемопревентивных веществ [Wattenberg L.W. (1995) What are the critical attributes for cancer chemopreventive agents? Ann NY Acad Sci 768:73-81]. Альтернативный подход заключается в поиске веществ, которые быстро удаляют прораковые клетки путем индукции в них апоптоза.
Публикуются данные о все увеличивающемся числе хемопревентивных противораковых веществ, которые стимулируют апоптоз прораковых и раковых клеток in vitro и in vivo [Gupta S, Hastak K, Ahmad N, Lewin J.S., Mukhtar H (2001) Inhibition of prostate carcinogenesis in TRAMP mice by oral infusion of green tea polyphenols. Proc Natl Acad Sci USA 98:10350-10355; Lu Y-P, Lou Y-R, Li X-H, Xie J-G, Brash D., Huang M-T, et al. (2000) Stimulatory effect of oral administration of green tea or caffeine on ultraviolet light-induced increases in epidermal wild-type p53, p21 (WAFI/CIPI), and apoptotic sunburn cells in SKH-1 mice. Cancer Res 60:4785-4791; Lu Y-P, Lou Y-R, Li X-H, Xie J-G, Yen P, Huang M-T, Conney A.H. (1997) Inhibitory effect of black tea on the growth of established skin tumors in mice: effects on tumor size, apoptosis, mitosis and bromodeoxyuridine incorporation into DNA. Carcinogenesis 18:2163-2169; Samaha H.S., Kelloff G.J., Steele V., Rao C.V., Reddy B.S. (1997) Modulation of apoptosis by sulindac, curcumin, phenylethyl-3-methylcaffeate and 6-phenylhexyl isothiocyanate apoptotic index as a biomarker in colon cancer chemoprevention and promotion. Cancer Res 57:1301-1305; Yang K., Lamprecht S.A., Liu Y, Shinozaki H., Fan K., Leung D., et al. (2000) Chemoprevention studies on the flavonoids quercetin and rutin in normal and azoxymethane-treated mouse colon. Carcinogenesis 21:1655-1660; Tanaka Т., Kohno H., Sakata K., Yamada Y, Hirose Y, Sugie S., et al. (2002) Modifying effects of dietary capsaicin and rotenone on 4-nitroquinoline-l-oxide-induced rat tongue carcinogenesis. Carcinogenesis 23:1361 -1367].
При использовании такого подхода долговременный прием хемопревентивных веществ становится ненужным, что снижает риск проявления токсического эффекта данных препаратов или развития резистентности по отношению к ним [Wattenberg L.W. (1995) What are the critical attributes for cancer chemopreventive agents? Ann NY Acad Sci 768:73-81; Smith T.J., Hong J-Y, Wang Z-Y, Yang C-S (1995) How can carcinogenesis be inhibited? Ann NY Acad Sci 768:82-90; Kelloff G.J., Crowell J.A., Steele V.E., Lubet R.A., Boone C.W., Malone W.A., et al. (1999) Progress in cancer chemoprevention. Ann NY Acad Sci 889:1-13].
Широко известными хемопревентивными веществами, предотвращающими перерождение нормальных клеток в опухолевые, являются полифенолы из зеленого чая, флавоноиды из ягод, ресвератрол из красного винограда, капсаицин из перца, куркумин из тропического растения куркума и многие другие [Lu Y-P, Lou Y-R, Li XH, Xie J-G, Brash D, Huang M-T, et al. (2000) Stimulatory effect of oral administration of green tea or caffeine on ultraviolet light-induced increases in epidermal wild-type p53, p21 (WAFI/CIPI), and apoptotic sunburn cells in SKH-1 mice. Cancer Res 60:4785-4791; Samaha H.S., Kelloff G.J., Steele V, Rao C.V., Reddy B.S. (1997) Modulation of apoptosis by sulindac, curcumin, phenylethyl-3-methylcaffeate and 6-phenylhexyl isothiocyanate apoptotic index as a biomarker in colon cancer chemoprevention and promotion. Cancer Res 57:1301-1305; Yang K., Lamprecht S.A., Liu Y, Shinozaki H., Fan K., Leung D., et al. (2000) Chemoprevention studies on the flavonoids quercetin and rutin in normal and azoxymethane-treated mouse colon. Carcinogenesis 21:1655-1660; Tanaka Т., Kohno H., Sakata K., Yamada Y, Hirose Y, Sugie S., et al. (2002) Modifying effects of dietary capsaicin and rotenone on 4-nitroquinoline-l-oxide-induced rat tongue carcinogenesis. Carcinogenesis 23:1361-1367].
В качестве веществ, предупреждающих злокачественное перерождение нормальных клеток, в последнее время все большее внимание привлекают морские природные соединения и их синтетические аналоги и производные, которые способны вызывать апоптоз трансформированных и раковых клеток.
Впервые ааптамин (1) был выделен группой японских исследователей в 1982 году из тропической губки Aaptos aaptos как компонент, отвечающий за α-адреноблокирующую активность водно-метанольного экстракта этой губки. Ааптамин (1) выделен в виде гидрохлорида и представлял собой ярко-желтые кристаллы tпл=110~113°C. По химической структуре соединение представляет собой производное 1Н-бензо[dе]-1,6-нафтиридина [Nakamura Н., Kobayashi J., Ohizumi Y. Isolation and structure of aaptamine, a novel heteroaromatic substance possessing α-blocking activity from the sea sponge Aaptos aaptos. // Tetrahedron Lett. 1982. V.23, №52. P.5555-5558].
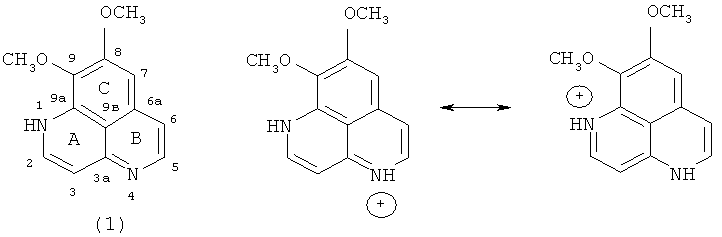
Ааптамин (1) и его протонированная форма
В 1987 году та же группа японских исследователей сообщила о выделении из губки Aaptos aaptos двух новых соединений - 9-деметилоксиааптамина (2) и 9-деметилааптамина (3) и синтезе частично гидрированного производного ааптамина - дигидроааптамина (4) [Nakamura Н., Kobayashi J., Ohizumi Н., Hirata Y. (1987) Aaptamines. Novel benzo[de][1,6]naphthyridines from the Okinawan marine sponge, Aaptos aaptos. J. Chem. Soc. Perkin Trans. 1987. V.14, №1. P.173-176].
В 1988 году был выделен изоааптамин (5) [Федореев С.А.., Прокофьева Н.Г., Денисенко В.А., Ребачук Н.М. Цитотоксическая активность ааптаминов из морских губок семейства Suberitidae. // Хим.-фармацевт. журн. 1988. №8. С.943-946], а в 2002 году - 4-метилааптамин (6) [Coutinho A.F., Chanas В., Souza Т.Е., Frugrulhetti I., Epifanio R.de A. Anti HSV-1 alkaloids from a feeding deterrent marine sponge of the genus Aaptos. // Heterocycles. 2002. V.57, №7. P.1265-1272].
В 2003 году было выделено еще одно производное, диметилкеталь 9-деметилоксиааптамина (7) [Calcut L., Longeon A., Mourabit A., Guyot М., Bourguet-Kondracki М. L. Novel alkaloids of the aaptamine class from an Indonesian marine sponge of the genus Xestopongia. // Tetrahedron. 2003. V.59, №34. P.6539-6544].
В 2004 году были выделены бисдеметилааптамин (8) и первый сульфатированный ааптамин - бисдеметилааптамин-9-О-сульфат (9) [Herlt A., Mander L., Rombang W., Rumampuk R., Soemitro S., Steglich W., Tarigan P., von Nussbaum F. Alkaloids from marine organisms. Part 8: Isolation of bisdemethylaaptamine and bisdemethylaaptamine-9-O-sulfate from an Indonesian Aaptos sp.marine sponge. // Tetrahedron. 2004. V.60, №29. P.6101-6104].
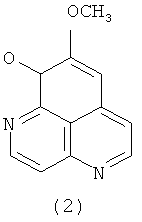
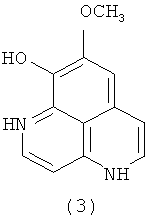
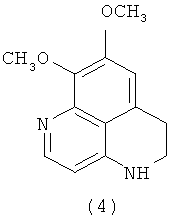
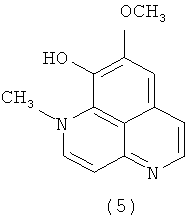
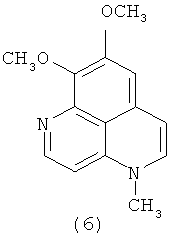
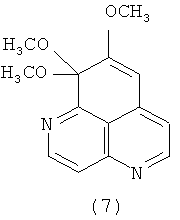
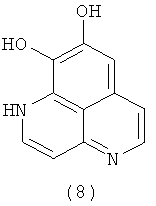

Также в литературе имеются сообщения о тетрациклических производных ааптамина (10)-(13) [Calcut L., Longeon A., Mourabit A., Guyot М., Bourguet-Kondracki М. L. Novel alkaloids of the aaptamine class from an Indonesian marine sponge of the genus Xestopongia. // Tetrahedron. 2003. V.59, №34. P.6539-6544] и его структурном изомере, ааптазине (14) [Rudi A., Kashman Y. Aaptasine - a new cytotoxic 5,8-diazabenz[cd]azulene alkaloid from the Red Sea sponge Aaptos aaptos. // Tetrahedron Lett. 1993. V.34, №29. P.4683-4684].
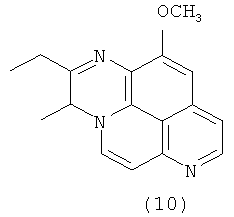

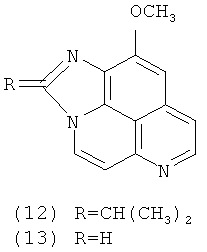
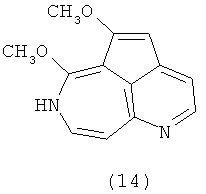
Ааптамин и его производные являются таксономическим маркером отряда Hadromerida [Bergquist P.R., Cambie R.C., Kernan M.R. Chemistry of sponges. 14. Aaptamine, a taxonomic marker for sponges of the order Hadromerida. // Bioch. Syst. Ecol. 1991. V.19, №4. P.289-290] и обладают цитотоксической, противомикробной, противовирусной, противогрибковой и антиоксидантной активностью. Так, наиболее сильной цитотоксической и противомикробной активностью из всех известных производных ааптамина обладает 9-деметилоксиааптамин (2), для которого IC50 (inhibition concentration) по отношению к клеткам HeLa (рак шейки матки) составила 4,09 мкМ a MIC (minimum inhibitory concentration) против Staphylococcus aureus составила 14,71 мкМ, против Bacillus subtilis - 29,38 мкМ, против Proteus vulgaris - 58,76 мкМ. В то же время деметилааптамин (3) по своим аналогичным свойствам был приблизительно в 2 раза менее активен [Nakamura Н., Kobayashi J., Ohizumi Н., Hirata Y. (1987) Aaptamines. Novel benzo[de][1,6]naphthyridines from the Okinawan marine sponge, Aaptos aaptos. J. Chem. Soc. Perkin Trans. 1987. V.14, №1 P.173-176]. 4-Метилааптамин (6) в концентрации 8,3 мкМ и 9-деметилоксиааптамин (2) в концентрации 9,4 мкМ способны ингибировать рост вируса герпеса HSV-1 в зараженных клетках на 80% и 78% соответственно [Coutinho A.F., Chanas В., Souza Т.Е., Frugrulhetti I., Epifanio R.de A. Anti HSV-1 alkaloids from a feeding deterrent marine sponge of the genus Aaptos. // Heterocycles. 2002. V.57, №7. P.1265-1272]. Ааптамин (1) и его производные показали цитотоксическую активность in vitro против мышиных опухолевых клеток Р-388 (лейкемия), а также человеческих опухолевых клеток KB 16 (эпидермоидная карцинома), А549 (аденокарцинома легких) и НТ-29 (аденокарцинома кишечника) [Shen Y, Lin Т., Sheu J., Duh С. Structures and Cytotoxicity Relationship of Isoaaptamine and Aaptamine derivatives. // J. Nat. Prod. - 1999. - V.62, №9. P.1264-1267].
Также было установлено, что наличие гидроксильной группы в положении 9 усиливает цитотоксические свойства соединения, а ацилирование этого положения приводит к снижению цитотоксических свойств. Так, при замене водорода 9-ОН гидроксильной группы изоааптамина (5) на остаток карбоновой кислоты с различной длиной цепи, с образованием 9-ацилизоааптаминов (15)-(26), цитотоксическая активность резко падает [Shen Y, Lin Т., Sheu J., Duh С. Structures and Cytotoxicity Relationship of Isoaaptamine and Aaptamine derivatives. // J. Nat. Prod. - 1999. - V.62, №9. P.1264-1267]. При этом с ростом длины цепи карбоновой кислоты закономерного изменения активности не наблюдается (таблица 1).
Также было показано, что гидрирование кольца В приводит к снижению цитотоксичности, как в случае полученного синтетически дигидроааптамина (4) [Shen Y, Lin Т., Sheu J., Duh С. Structures and Cytotoxicity Relationship of Isoaaptamine and Aaptamine derivatives. // J. Nat. Prod. - 1999. - V.62, №9. P.1264-1267]. При изомеризации скелета, как это можно видеть для ааптазина (14), цитотоксичность также резко понижается (таблица 1).
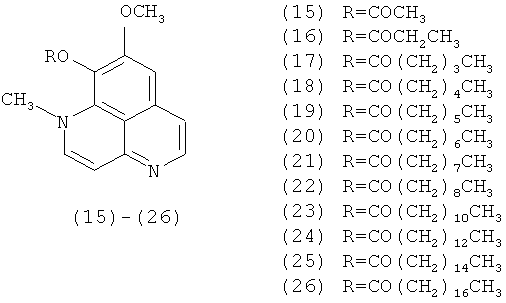
В 2003 году было проведено исследование некоторых антибактериальных (против грамм-положительных бактерий S. aureus, грамм-отрицательных бактерий Е. coli и V. Anguillarum), противогрибковых (против С. tropicalis) и цитотоксических (против клеток KB) свойств ааптамина (1), 9-деметилоксиааптамина (2), изоааптамина (5), диметилкеталя 9-деметилоксиааптамина (7) и тетрациклических производных ааптамина (10)-(13) [Calcut L., Longeon A., Mourabit A., Guyot М., Bourguet-Kondracki M.L. Novel alkaloids of the aaptamine class from an Indonesian marine sponge of the genus Xestopongia. // Tetrahedron. 2003. V.59, №34. P.6539-6544]. Показано, что при замыкании четвертого цикла соединения цитотоксичность резко снижается (таблица 2).
Цитотоксическая активность ааптамина (1), 9-деметилоксиааптамина (2) и изоааптамина (5) также была исследована по отношению к опухолевым клеткам лейкемии (Р388), рака яичника (OVCAR-3), рака центральной нервной системы (SF-295), рака почки (А498), рака легкого (NCI-H460), рака кишечника (KM20L2) и меланомы (SK-MEL-5) [Pettit G.R., Hoffmann Н., McNulty J., Higgs K.C., Murphy A., Molloy D.J., Herald D.L., Williams M.D., Pettit R.K., Doubek D.L., Hooper J.N. A., Albright L., Jean M., Schmidt J. M, Chapuis J., Tackett L.P. Antineoplastic agents. 380. Isolation and X-ray crystal structure determination of isoaaptamine from the Republic of Singapore Hymeniacidon sp.and conversion to the phosphate prodrug hystatin 1. // J. Nat. Prod. 2004. V.67, №3. P.506-509; Pettit G R., Hoffmann H., Herald D.L., McNulty J., Murphy A., Higgs K.C., Hamel E., Lewin N.E., Pearce L.V., Blumberg P.M., Pettit R.K., Knight J. C. Antineoplastic agents 491. Synthetic conversion of aaptamine to isoaaptamine, 9-demethylaaptamine, and 4-methylaaptamine. // J. Org. Chem. - 2004. V.69, №7. P.2251-2256]. Результаты представлены в таблице 3.
Была также установлена цитотоксическая активность 9-деметилоксиааптамина (2) для клеток лейкемии Р388, равная IC50=7,55 мкМ [Longley R.E., McConnell O.L., Essich Е., Harmody D. Evaluation of marine sponge metabolites for cytotoxicity and signal transduction activity. // J. Nat. Prod. 1993. V.56, №6, P.915-920]. Кроме того, ааптамин (1) показал сильную антиоксидантную активность в экспериментах с использованием 2,2-дифенил-1-пикрилгидразил радикала (DPPH) и относительно слабую в опыте с 2',7'-дихлородигидрофлуоресцеин диацетатом (DCFH-DA) [Takamatsu S. Marine natural products as novel antioxidant prototypes. // J. Nat. Prod. 2003. V.66, №5. P.605-608].
В последней по времени из опубликованных статей, касающихся структуры и биологической активности производных ааптамина, были приведены структуры двух новых производных ааптамина, 3-фенетиламино-9-деметилоксиаапамина (27) и 3-изопентиламино-9-деметилоксиааптамина (28) [Shaari К., Ling К.С., Rashid Z.M., Jean Т.P., Abas R, Raof S.M., Zainal Z., Lajis N.H., Mohamad H., Ali A.M. Cytotoxic aaptamines from Malaysian Aaptos aaptos. // Mar. Drugs. 2009. V.7. P.1-8].
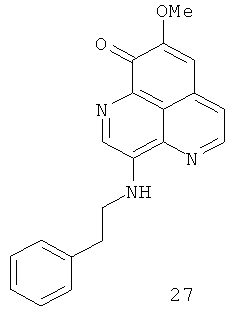
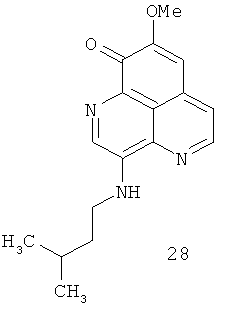
Для этих соединений, а также для ааптамина (1) была сообщена цитотоксическая активность по отношению к клеткам лимфобластической лейкемии CEM-SS. Так, для соединения (27) IC50=5.3 мкг/мл, для (28) IC50=6.7 мкг/мл и для ааптамина IC50=15.0 мкг/мл.
Механизм биологического действия ааптамина и его производных на клетки мало изучен. Установлено, что ааптамин и некоторые его производные способны нарушать проницаемость цитоплазматической мембраны, чем, возможно, и обусловлен его цитотоксический эффект [Федореев С.А., Прокофьева Н.Г., Денисенко В.А., Ребачук Н.М. Цитотоксическая активность ааптаминов из морских губок семейства Suberitidae. // Хим.-фармацевт. журн. 1988. №8. С.943-946]. Также известно, что ааптамин способен индуцировать экспрессию белка р21, ингибитора циклин-зависимой киназы, ответственного за остановку клеточного цикла [Aoki S., Kong D., Suna H., Sowa Y., Sakai T, Setiawan A., Kobayashi M. Aaptamine, a spongean alkaloid, activates p21 promoter in a p53-independent manner. // Biochem. Biophys. Res. Commun. 2006. V.342, №1. P.101-106] и ингибировать активность протеин-киназы РКС [Patil A. D., et al., Aaptamines as protein kinase С inhibitors, PCT Int. App.; WO 95/0584, 1995].
В литературе также были опубликованы различные подходы к синтезу ааптамина и его производных [Pettit G.R., Hoffmann Н., Herald D.L., Blumberg P.M., Hamel E., Schmidt J.M., Chang Y, Pettit R.K., Lewin N.E., Pearce L.V. Antineoplastic agents. 499. Synthesis of hystatin 2 and related lH-benzo[de][l,6]-naphthyridinium salts from aaptamine. // J. Med. Chem. 2004. V.47, №7. P.1775-1782; Walz A.J., Sundberg R.J. Synthesis of 8-methoxy-1-methyl-lH-benzo[de][l,6]naphthyridin-9-ol (isoaaptamine) and analogues. // J. Org. Chem. 2000. V.65, №23. P.8001-8010].
Опубликован также американский патент, в котором описаны выделение, установление структуры изоааптамина (5) и его химическая конверсия в родственные соединения, «которые, по-видимому, обладают антимикробными и/или противораковыми свойствами» [US 2005/0187240 Al, pub. Date: Aug. 25, 2005; Inventors: Pettit G.R., Herald D.L., Hoffman H. Aaptamine and isoaaptamine and strucrural modifications thereof].
Из уровня техники известно применение ааптамина и его аналогов, а именно 9-деметилоксиааптамина (2) и изоааптамина (5) к лечению уже имеющихся раковых заболеваний [WO 95/05824 A1, 02.03.1995], в том числе к преодолению так называемого «drug resistance», когда уже имеющаяся раковая опухоль сопротивляется применяемым лекарственным средствам, при этом говорится об именно опухолевых клетках (target neoplastic cells) как цели применения патентуемых производных ааптамина.
Известны раково-профилактические свойства ааптамина [Дышловой С.А. Создание биологически активной добавки с канцерпревентивными свойствами на основе ааптамина. 1 Far-Eastern International Symposium on life Sciences. Молодежная секция «Актуальные проблемы химии и биологии». Материалы. Часть II, кокурс «У.М.Н.И.К.». Владивосток, 2008, с.22-25]. Однако недостаток ааптамина заключается в том, что он обладает сравнительно высокой цитотоксической активностью по отношению к нормальным клеткам млекопитающих.
Задача изобретения - расширение арсенала средств и фармацевтических композиций на основе аналогов ааптамина, способных избирательно предотвращать злокачественное перерождение нормальных клеток млекопитающих в опухолевые.
Задача решена созданием средства, предотвращающего трансформацию нормальных клеток млекопитающих в опухолевые, представляющее собой 3-N-морфолинил-9-деметилоксиааптамин (29).
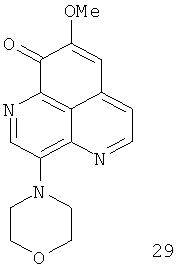
Задача решена также применением 9-деметилоксиааптамина (2), изоааптамина (5), 3-фенетиламино-9-деметилоксиааптамина (27) или 3-изопентиламино-9-деметилоксиааптамина (28) в качестве средства, предотвращающего трансформацию нормальных клеток млекопитающих в опухолевые.
Назначение 9-деметилоксиааптамина (2), изоааптамина (5), 3-фенетиламино-9-деметилоксиааптамина (27) и 3-изопентиламино-9-деметилоксиааптамина (28) в качестве средств, обладающих способностью предотвращать злокачественное перерождение нормальных клеток млекопитающих в опухолевые, в доступной патентной и другой научно-технической литературе не обнаружено.
Новое производное ааптамина, 3-N-морфолинил-9-деметилоксиааптамин (29), наряду с ранее известными 9-деметилоксиааптамином (2), изоааптамином (5), 3-фенетиламино-9-деметилоксиааптамином (27) и 3-изопентиламино-9-деметилоксиааптамином (28) выделены из собранной у побережья Вьетнама морской губки Aaptos sp. Эти соединения могут быть получены также путем химического синтеза.
Процесс выделения ааптаминовых производных из губок является стандартной процедурой, описанной, к примеру, Shaari К. и соавторами [Shaari К., Ling К.С., Rashid Z.M., Jean T.P, Abas F., Raof S.M., Zainal Z., Lajis N.H., Mohamad H., Ali A.M. Cytotoxic aaptamines from Malaysian Aaptos aaptos. // Mar. Drugs. 2009. V.7. P.1-8].
Сущность способа заключается в следующем: животных измельчают и экстрагируют метанолом (или этанолом); экстракт упаривают на роторном испарителе до полного испарения спиртовой составляющей и из оставшегося водного слоя удаляют липиды и неполярные вещества путем экстракции гексаном. Водный слой обессоливают путем хроматографии на колонке с тефлоновым порошком или другим гидрофобным носителем, уравновешенным в воде. Неорганические соли вымывают с колонки водой, а фракцию, содержащую ааптаминовые производные, смывают 10-20%-ным этанолом в воде. После упаривания досуха на роторном испарителе фракцию наносят на колонку с силикагелем; элюент - хлороформ с добавлением возрастающих количеств этанола. В результате, как правило, выделяют в чистом виде ааптамин (1), 9-деметил(оксиа)аптамин (2), изоааптамин (5) и смеси других ааптаминовых производных. Полученные смеси производных ааптамина разделяют методом жидкостной хроматографии высокого давления (ЖХВД) с применением силикагельных или обращенно-фазовых колонок. Так мы разделяли смесь, содержащую ааптамины 27-29, методом ЖХВД на обращенно-фазовой колонке YMC-Pack ODS-A (10×250 мм), используя 60% метанол в качестве элюента. При этом новое производное ааптамина, 3-N-морфолинил-9-деметилоксиааптамин (29), и его аналоги 3-фенетиламино-9-деметилоксиааптамин (27) и 3-изопентиламино-9-деметилоксиааптамин (28) были получены в чистом виде.
Задача решена также применением 3-N-морфолинил-9-деметилоксиааптамина (29) или 9-деметилоксиааптамина (2) или изоааптамина (5) или 3-фенетиламино-9-деметилоксиааптамина (27) или 3-изопентиламино-9-деметилоксиааптамина (28) для приготовления фармацевтической композиции, предотвращающей трансформацию нормальных клеток млекопитающих в опухолевые.
Фармацевтические композиции, предотвращающие трансформацию нормальных клеток млекопитающих в опухолевые, получают смешивая эффективное количество 3-N-морфолинил-9-деметилоксиааптамина (29) или его аналогов 9-деметилоксиааптамина (2), изоааптамина (5), 3-фенетиламино-9-деметилоксиааптамина (27) и 3-изопентиламино-9-деметилоксиааптамина (28) с традиционными фармацевтически или фармакологически приемлемыми наполнителями. Выражение «фармацевтически или фармакологически приемлемый» обозначает молекулярные компоненты и композиции, которые не вызывают негативных, аллергических или иных нежелательных реакций при введении их животному или человеку. Природа наполнителя зависит от способа введения. Например, если желательным является пероральное введение, то может быть выбран твердый наполнитель, тогда как для внутривенного введения может быть использован жидкий солевой раствор.
Технический результат, обеспечиваемый изобретением, заключается в способности 3-N-морфолинил-9-деметилоксиааптамина (29), 9-деметилоксиааптамина (2), изоааптамина (5), 3-фенетиламино-9-деметилоксиааптамина (27) и 3-изопентиламино-9-деметилоксиааптамина (28) предотвращать трансформацию нормальных клеток в опухолевые, а также в возможности использования этих веществ для приготовления фармацевтических композиций, предотвращающих трансформацию нормальных клеток млекопитающих в опухолевые. 3-N-морфолинил-9-деметилоксиааптамин (29) и его аналоги 9-деметилоксиааптамин (2), изоааптамин (5), 3-фенетиламино-9-деметилоксиааптамин (27) и 3-изопентиламино-9-деметилоксиааптамин (28) оказывают раково-превентивное действие в нецитотоксических для нормальных клеток концентрациях, что значительно снижает риск токсического действия на организм при длительном его применении.
Изобретение расширяет арсенал средств и фармацевтических композиций, предотвращающих трансформацию нормальных клеток млекопитающих в опухолевые.
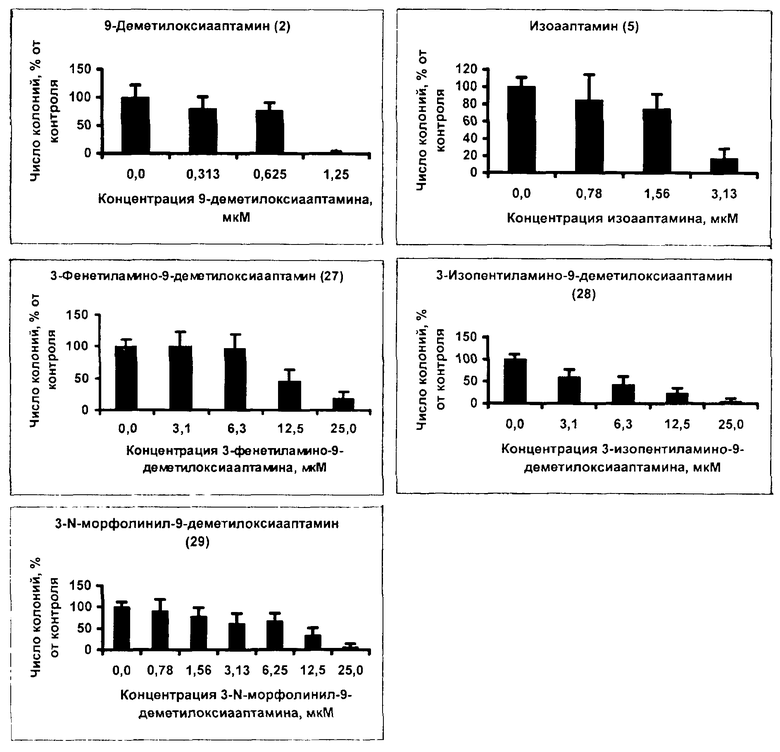
На чертеже представлено ингибирование 3-N-морфолинил-9-деметилоксиааптамином (29) и его аналогами 9-деметилоксиааптамином (2), изоааптамином (5), 3-фенетиламино-9-деметилоксиааптамином (27) и 3-изопентиламино-9-деметилоксиааптамином (28) EGF-индуцированной опухолевой трансформации мышиных эпителиальных клеток JB6 P+ C141.
Изобретение иллюстрируется примерами конкретного выполнения.
Пример 1. Выделение и установление структуры нового аналога ааптамина, 3-N-морфолинил-9-деметилоксиааптамина (29), а также ранее известных 9-деметилоксиааптамина (2), изоааптамина (5), 3-фенетиламино-9-деметилоксиааптамина (27) и 3-изопентиламино-9-деметилоксиааптамина (28).
I. Материалы и методы.
1. Приборы.
1Н и 13С ЯМР спектры регистрировали на спектрометре Bruker DRX-500 (Германия) при 500 и 125 МГц соответственно с тетраметилсиланом в качестве внутреннего стандарта. ИК-спектры регистрировали на спектрометре Bruker Vector 22 (Германия) и УФ-спектры - на спектрометре Shimadzu UV-1601 (Япония). Масс-спектр высокого разрешения получали на масс-спектрометре Agilent 6510 Q-TOF (Agilent, США). Простую колоночную хроматографию проводили с использованием сорбентов Полихром-1 (тефлоновый порошок, Biolar, Latvia) и силикагель КСК (50-100 микрон, Россия). Для тонкослойной хроматографии использовали силикагельные пластинки 4.5×6.0 cm (5-17 µm, Sorbfil, Россия). Жидкостную хроматографию высокого давления выполняли на хроматографе Agilent 1100 (Agilent, США), снабженном рефрактометрическим детектором и колонкой YMC-Pack ODS-A (10×250 mm).
2. Животные.
Губки Aaptos sp.были собраны водолазным методом в течение 30-й научной экспедиции на борту НИС «Академик Опарин» в январе 2005 г. у побережья Вьетнама (бухта Ванг Фонг, глубина 5-10 м, координаты места сбора 12°35'68''N, 109°18'62''E). Образец губки хранится в коллекции, находящейся в ТИБОХ ДВО РАН (Владивосток, Россия).
3. Экстракция и выделение.
Губка (сухой вес 500 г) была проэкстрагирована этанолом немедленно после сбора. Этанольный экстракт после упаривания под вакуумом досуха был заново растворен в системе EtOH-Н2О (5:1) и экстрагирован гексаном. Водно-этанольный слой после упаривания был помещен на колонку с полихромом-1. Колонку элюировали сначала водой, а затем 10% этанолом. После упаривания досуха на роторном испарителе фракцию, элюированную 10% этанолом, хроматографировали на колонке с силикагелем; элюент - хлороформ с добавлением возрастающих количеств этанола. В результате выделили в чистом виде ааптамин (1, 160 мг, 0,03% от сухого веса губки), 9-деметилоксиаапатмин (2, 80 мг, 0,015% от сухого веса губки), изоааптамин (5, 98 мг, 0,023% от сухого веса губки) и смесь алакалоидов 27-29. Полученную смесь производных ааптамина разделяли методом жидкостной хроматографии высокого давления (ЖХВД) с применением обращенно-фазовой колонки YMC-Pack ODS-A (10×250 мм), используя 60% метанол в качестве элюента. При этом все три производных (27, 5 мг, 0,001%; 28, 7 мг, 0,0014%; 29, 15 мг, 0,003%), одно из которых (29) оказалось новым по структуре, были получены в чистом виде.
4. Спектральные данные выделенных веществ (27-29).
3-N-Морфолинил-9-деметилоксиааптамин (29)
Оранжевый аморфный порошок.
ИК-спектр (CHCl3), 1652, 1620, 1505, 1109 см-1.
УФ-спектр (λmax) (EtOH) нм (log ε): 249 (3,89), 280 (3.66).
1Н ЯМР (500 MГz, CD3OD): Таблица 4.
13С ЯМР (125 MГz CD3OD): Таблица 4.
HRESI-MS: m/z [M+H]+ вычислено для C16H15N3O3: 298,1186; найдено: 298,1185.
3-Фенетиламино-9-деметилоксиааптамин (27).
Оранжевый аморфный порошок.
УФ-спектр (λmax) (EtOH) нм (log ε): 246 (3,15), 280 (2,99).
HRESI-MS: m/z [M+H]+ вычислено для C20H17N3O2: 332,1394; найдено: 332,1381.
ЯМР спектры аналогичны опубликованным [Shaari К., Ling К.С., Rashid Z.M., Jean Т.Р., Abas F, Raof S.M., Zainal Z., Lajis N.Н., Mohamad Н., Ali A.M. Cytotoxic aaptamines from Malaysian Aaptos aaptos. // Mar. Drugs. 2009. V.7. P.1-8].
3-Изопентиламино-9-деметилоксиааптамин (28).
Оранжевый аморфный порошок.
УФ-спектр (λmax) (EtOH) нм (log ε): 244 (3,41), 279 (3,23).
HRESI-MS: m/z [M+H]+ вычислено для C17H19N3O2: 298,1550; найдено: 298,1549.
ЯМР спектры аналогичны опубликованным [Shaari К., Ling K.C., Rashid Z.M., Jean Т.Р, Abas F., Raof S.M., Zainal Z., Lajis N.H., Mohamad Н., Ali A.M. Cytotoxic aaptamines from Malaysian Aaptos aaptos. // Mar. Drugs. 2009. V.7. P.1-8].
5. Химическое превращение 3-N-Морфолинил-9-деметилоксиааптамина (29) в ааптамин (1).
К суспензии 29 (5 мг) в смеси ацетонитрила (10 мл) и воды (1 мл) был добавлен трехкратный (моль/моль) избыток Na2S2O4. Полученную смесь перемешивали в течение 30 мин при комнатной температуре. Затем к смеси добавили 1 мл насыщенного раствора NaHCO3. Через 10 мин добавили избыток диазометана в Et2O и смесь перемешивали в течение 1 часа. Затем реакционную смесь разбавили водой (10 мл) и экстрагировали этилацетатом (3×5 мл). Объединенные органические слои сушили над безводным Na2SO4, концентрировали под вакуумом и очищали колоночной хроматографией на силикагеле (CHCl3: МеОН, 3:1), растворили в метаноле и подкислили HCl. Полученный ааптамина гидрохлорид идентифицировали с помощью сравнения данных ЯМР спектров с литературными [Nakamura H., Kobayashi J., Ohizumi H. (1982) Isolation and structure of aaptamine, a novel heteroaromatic substance possessing α-blocking activity from the sea sponge Aaptos aaptos. Tetrahedron Letters, 23, 5555-5558].
II. Результаты выделения и установления структуры нового аналога ааптамина - 3-N-морфолинил-9-деметилоксиааптамина (29), а также ранее известных 9-деметилоксиааптамина (2), изоааптамина (5), 3-фенетиламино-9-деметилоксиааптамина (27) и 3-изопентиламино-9-деметилоксиааптамина (28) и их обсуждение.
В продолжение изучения противораковой и канцер-превентивной активности морских природных соединений нами был изучен этанольный экстракт губки, принадлежащей к роду Aaptos (семейство Suberitidae, отряд Hadromerida), собранной у берегов Вьетнама в течение научной экспедиции на борту НИС «Академик Опарин». Этот экстракт показал цитотоксическую активность против клеток лейкемии человека HL-60. С помощью хроматографических методов из данного экстракта нами был выделен новый алкалоид ааптаминового ряда - 3-N-морфолинил-9-деметилоксиааптамин (29), наряду с ранее известными 9-деметилоксиааптамином (2), изоааптамином (5), 3-фенетиламино-9-деметилоксиааптамином (27) и 3-изопентиламино-9-деметилокси-ааптамином (28). Структуры известных алкалоидов 2, 5, 27, 28 были определены на основе спектральных данных (УФ, ИК, 1D и 2D ЯМР) и при сравнении их с ранее опубликованными данными [Nakamura H., Kobayashi J., Ohizumi H. (1982) Isolation and structure of aaptamine, a novel heteroaromatic substance possessing α-blocking activity from the sea sponge Aaptos aaptos. Tetrahedron Letters, 23, 5555-5558; Nakamura H., Kobayashi J., Ohizumi H., Hirata Y. (1987) Aaptamines. Novel benzo[de] [1.6] naphthyridines from the Okinawan marine sponge, Aaptos aaptos. Journal of the Chemical Society, Perkin Transactions 1, 14, 173-176; Fedoreev S.A., Prokofeva N.G., Denisenko V.A., Rebachuk N.M. (1988) Cytotoxic activities of aaptamines from marine sponges of the family Suberitidae. Khimiko-Farmatsevticheskii Zhurnal, 24, 943-947 (in Russian); Shaari K, Ling K.C., Rashid Z.M., Jean T.P., Abas F., Raof S.M., Zainal Z., Lajis N.H., Mohamad H., Ali A.M. (2009) Cytotoxic aaptamines from Malaysian Aaptos aaptos. Marine Drugs, 7, 1-8].
Новый аналог ааптамина, 3-N-морфолинил-9-деметилоксиааптамин (29), был выделен в виде аморфного вещества оранжевого цвета. Его молекулярная формула C16H15N3O3 была определена на основе масс-спектра высокого разрешения HRESI-MS, в котором был ион [М+Н]+ при m/z 298,1185; Δ 0,1 ppm. В ИК-спектре присутствовала полоса поглощения при 1652 см-1, принадлежащая карбонильной группе хиноидного типа. Все ЯМР-данные (таблица 4) свидетельствовали о том, что данное вещество принадлежит к ряду бензо[де][1,6]-нафтиридинов и структурно родственно 9-деметилоксиааптамину (2), хотя нельзя было исключить его принадлежность и к ряду бензо[де][1,8]-нафтиридинов (30).
Схема химической реакции превращения 3-N-морфолинил-9-деметилоксиааптамина (29) в ааптамин

Однако превращение выделенного соединения 29 в ааптамин (1) после восстановления с помощью Na2S2O4 с последующей обработкой диазометаном исключило структуру 30 и подтвердило, что соединение 29 имеет ту же скелетную систему, что и 9-деметилоксиааптамин (2).
Наряду с характерными для ааптамина сигналами, в 1Н- и 13С ЯМР спектрах вещества 29 присутствовали сигналы четырех дополнительных метиленовых групп, связанных с гетероатомами: δH 3.96 (2Н, м), 3.96 (2Н, м), 4.12 (2Н, м), 4.12 (2Н, м); δC 52.4, 52.4, 67.9, 67.9.
1H-1H COSY корреляция H2-2' и Н2-3', а также Н2-4' и Н2-5', НМВС кросс-пики H-2'/C-3', С-5' и Н-3'/С-2', С-4', а также молекулярная формула указывали на присутствие морфолинильного фрагмента в структуре соединения 29.
На основании вышеуказанных доказательств структура вновь выделенного алкалоида была установлена как 3-N-морфолинил-9-деметилоксиааптамин (29). Насколько нам известно, это первый случай обнаружения морфолинильного фрагмента в структуре морского природного соединения.
Пример 2. Исследование биологической активности 9-деметилоксиааптамина (2), изоааптамина (5), 3-N-морфолинил-9-деметилоксиааптамина (29), 3-фенетиламино-9-деметилоксиааптамина (27) и 3-изопентиламино-9-деметилоксиааптамина (28).
I. Материалы и методы.
1. Принятые сокращения.
EGF - Epidermal growth factor (эпидермальный фактор роста)
FBS - Fetal bovine serum (сыворотка бычьих эмбрионов)
HPLC - High performance liquid chromatography (высокоэффективная жидкостная хроматография)
IC50 - Inhibition concentration 50% (концентрация, вызывающая гибель 50% клеток)
INCC50 - Inhibition of number of colonies concentration 50% (концентрация, ингибирующая злокачественную трансформацию 50% клеток)
PBS - Phosphate-buffered saline (фосфатно-солевой буфер)
ТРА - 12-O-Tetradecanoylphorbol-13-acetate (12-O-тетрадеканоилфорбол-13-ацетат)
мкМ - микромоль/литр
мМ - миллимоль/литр
М - моль/литр
мкл - микролитр
мл - миллилитр
SD - стандартное отклонение
PBS - фосфатно-солевой буферный раствор
ВМЕ - basal medium Eagle (питательная среда Игла для культивирования клеток млекопитающих)
RPMI, DMEM, MEM - питательные среды для культивирования клеток млекопитающих, изготовленные на основе среды Игла ВМЕ
МТТ - 3-(4,5-диметилтиазолил)-2,5-дифенилтетразолиум бромид (реагент для определения цитотоксичности)
MTS - 5-(3-Карбоксиметоксифенил)-2-(4,5-диметилтиазолил)-3-(4-сульфофенил) тетразолиум, внутренняя соль (реагент для определения цитотоксичности)
2. Клеточные культуры.
Мышиные эпителиальные клетки JB6 P+ Cl41, а также опухолевые клетки человека, HeLa (рак шейки матки), ТНР-1 (лейкемия, моноциты), HL-60 (лейкемия, промиелоциты), SNU-C4 (рак кишечника), SK-MEL-28 (меланома), MDA-MB-231 (рак молочной железы), Neuro 2a (нейробластома) из коллекции АТСС, Rockville, MD, США выращивались в инкубаторе Sanyo MCO-15AC в монослое для прикрепленных (линии JB6 Р+ С141, SK-MEL-28, HeLa, SNU-C4, MDA-MB-231, Neuro2a) или в суспензии для неприкрепленных клеток (линии ТНР-1 и HL-60) при 37°С и в атмосфере 5% CO2.
Для клеток линий JB6 P+ С141 и SK-MEL-28 использовалась среда MEM, содержащая 5% FBS, 2 mM раствора L-глутамина и 15 мкг/мл гентамицина.
Для клеток линий SK-MEL-28 и Neuro 2a использовалась среда MEM, содержащая 10% FBS, 2 mM раствора L-глутамина и 15 мкг/мл гентамицина.
Для клеток линий HeLa, ТНР-1, HL-60, SNU-C4 использовалась среда RPMI-1640, содержащая 10% FBS, 2 mM раствора L-глутамина и 15 мкг/мл гентамицина.
Для клеток линии MDA-MB-231 использовалась среда DMEM, содержащая 10% FBS, 2 mM раствора L-глутамина и 15 мкг/мл гентамицина.
3. Приготовление растворов веществ.
Базовые (стоковые) растворы 9-деметилоксиааптамина (2), изоааптамина (5), 3-N-морфолинил-9-деметилоксиааптамина (29), 3-фенетиламино-9-деметилоксиааптамина (27) и 3-изопентиламино-9-деметилокси-ааптамина (28) с концентрацией веществ 20 мМ готовили в системе EtOH: Н2О=1: 1, из которого получали растворы нужной концентрации разбавлением в культуральной среде. Содержание этанола в разбавленных растворах не превышало 0,5% во всех опытах.
4. Метод определения канцерпревентивной (предупреждающей злокачественное перерождение клеток) активности веществ (метод мягкого агара).
Эксперименты по изучению противоопухолевого профилактического эффекта исследуемых веществ проводили методом мягкого агара в шестилуночных планшетах [Nakamura Y., Colburn N.H., Cindhart T.D. Role of reactive oxygen in tumor promotion: implication of superoxide anion in promotion of neoplastic transformations in JB-6 cells by TPA. // Carcinogenesis. 1985. V.6, №2. P.229-235]. Метод основан на способности мышиных эпидермальных JB6 Р+ C141 клеток (8×103 кл/мл) перерождаться в опухолевые под действием активирующего их эпидермального фактора роста (EGF), взятого в концентрации 10 нг/мл, и, как следствие, образовывать колонии. Клетки, не обработанные эпидермальным фактором роста, колоний в мягком агаре не образуют. Методика рассчитана на приготовление 1 контрольного и 5 экспериментальных 6-луночных планшетов с мягким агаром. Всего за один эксперимент можно исследовать 10 различных концентраций (каждая в трипликате) одного или нескольких веществ:
А. Приготовление Agar Mix: В стерильной бутыли объемом 250 мл смешивали 18 мл PBS, 18 мл FBS, 100 мкл раствора гентамицин-сульфата с концентрацией 10 мг/мл (раствор в PBS), 2 мл 0,2 М раствора L-глутамина в PBS и 70 мл среды 2×ВМЕ. Смесь перемешивали и помещали в водяную баню (45°С) на 20 мин. Затем к смеси добавляли 72 мл разогретого до 50°С 1,25% раствора агара в воде (специально очищена для работы с клеточными культурами) и получали таким образом 180 мл смеси Agar Mix.
Б. Приготовление Agar Bottom: 180 мл смеси Agar Mix поделили на 2 части: 60 мл и 120 мл, каждая в стерильной бутыли объемом 250 мл. К 120 мл смеси Agar Mix добавили 60 мкл раствора EGF с концентрацией 20 мкг/мл в PBS и получили таким образом 120 мл смеси Agar Bottom. Обе смеси 120 мл Agar Bottom и 60 мл Agar Mix помещали в водяную баню (45°С).
В. Подготовка контрольного планшета (Bottom): В первые 3 лунки контрольного 6-луночного планшета добавляли по 3 мл Agar Mix (без EGF), в оставшиеся 3 лунки - по 3 мл Agar Bottom (с EGF). Для застывания растворов в лунках оставляли планшет на 30 мин при комнатной температуре.
Г. Подготовка экспериментальных планшетов с веществами: В стерильные пробирки объемом 15 мл помещали рассчитанные объемы растворов исследуемых веществ так, чтобы получить требуемые концентрации в расчете на 10 мл конечного раствора, по одной пробирке на одну концентрацию одного вещества. Затем в каждую пробирку добавляли по 10 мл Agar Bottom (с EGF), перемешивали с помощью пипетки. Из каждой пробирки добавляли по 3 мл полученных растворов веществ с одной и той же концентрацией в 3 лунки одного из приготовленных 6-луночных планшетов. Для застывания растворов в лунках оставили планшеты на 30 мин при комнатной температуре.
Д. Подготовка JB6 Р+ С141 клеток: Из бутыли, в которой выращивались JB6 P+ С141 клетки, с помощью пипетки Пастера удаляли клеточную среду, затем клетки промывали 5 мл PBS и добавляли 2 мл 0,25% раствор трипсина в PBS. Затем клетки с раствором трипсина инкубировались в течение 5 минут при 37°С в атмосфере 5% CO2, полученную суспензию клеток осторожно перемешивали с помощью пипетки, после чего в бутыль с клетками добавляли 8 мл соответствующей клеточной среды и суспензию снова перемешивали. Открепившиеся в процессе трипсинизации клетки переносили в стерильную пробирку и центрифугировали при 1000 об/мин в течение 10 мин. Далее с помощью пипетки Пастера удаляли супернатант и добавляли 5 мл среды 1×BME-10%FBS. После перемешивания считали концентрацию клеток в получившейся суспензии с помощью камеры Горяева. Далее путем смешивания необходимых объемов полученной суспензии клеток и среды 1×BME-10%FBS готовили 20 мл клеточной суспензии с концентрацией клеток 2,4×10 кл/мл.
Е. Подготовка контрольного планшета (Тор): Из оставшихся 51 мл Agar Mix отбирали в стерильную бутыль 30 мл раствора и добавляли в них 23 мкл 20 мкг/мл раствора EGF в PBS, получили таким образом 30 мл Agar Mix+EGF. Далее в первые 3 лунки 6-луночного контрольного планшета поверх застывшего Agar Mix (без EGF) добавляли по 1 мл предварительно приготовленной смеси: 1,2 мл клеточной суспензии JB6 Р+ С141 клеток и 2,4 мл Agar Mix (без EGF), получая, таким образом, 3 готовых лунки с 0% контролем. Во вторые 3 лунки (с Agar Bottom) 6-луночного контрольного планшета поверх застывшего Agar Bottom добавляли по 1 мл предварительно приготовленной смеси 2,4 мл Agar Mix+EGF и 1,2 мл клеточной суспензии JB6 P+ С141 клеток, получая, таким образом, 3 готовых лунки со 100% контролем. После этого планшет помещали в инкубатор и инкубировали в течение 7 суток при 37°С в атмосфере 5% CO2.
Ж. Подготовка экспериментальных планшетов: В стерильные пробирки помещали необходимые объемы растворов исследуемых веществ (исходя из исследуемого диапазона концентраций) в расчете на 3,6 мл конечного раствора, по одной пробирке на одну концентрацию одного вещества. Затем в каждую пробирку добавляли по 2,4 мл Agar Mix+EGF и 1,2 мл клеточной суспензии JB6 P+ С141 клеток, перемешивали и добавляли по 1 мл полученной смеси в соответствующие лунки 6-луночных планшетов поверх застывшего раствора веществ в Agar Bottom. После этого планшет помещали в инкубатор и инкубировали в течение 7 суток при 37°С в атмосфере 5% CO2. Полученная концентрация клеток в верхнем слое лунок всех планшетов равна 2,4×104×1,2/(1,2+2,4)=8×103 кл/мл. Концентрация агара в лунках в нижнем слое равна 1,25%×72/180=0,5%. Концентрация агара в лунках в верхнем слое равна (1,25%×72/180)×1,2/(1,2+2,4)=0.33%.
З. Получение результатов: После инкубации в течение 7 дней колонии живых клеток в лунках контрольного и экспериментальных планшетов были подсчитаны с помощью микроскопа Olympus (Япония). Количество колоний на чертеже показано в процентном отношении к количеству колоний в лунках со 100% контролем. Для каждого исследуемого вещества были проведены два независимых эксперимента.
5. Определение цитотоксической активности MTS методом.
Для определения цитотоксической активности веществ использовали стандартный MTS-метод (усовершенствованная модификация МТТ-метода) [Barltrop J.A., Owen T.C., Cory A.H., Cory J.G. 5-(3-Carboxymethoxyphenyl)-2-(4,5-dimethylthiazolyl)-3-(4-sulfophenyl) tetrazolium, inner sault (MTS) and related analogs of 3-(4,5-dimethylthiazolyl)-2,5-diphenyltetrazolium bromide (MTT) reducing to purple water-soluble formazans as cell-viability indicators. // Bioorg. Med. Chem. Lett. 1991. №11. P.611-614]. Метод основан на способности живых клеток перерабатывать MTS-реагент (желтая окраска, λmax=382 нм) в формазан (красная окраска, λmax=492 нм).
Схема переработки MTS-реагента живыми (метаболитически-активными) клетками в формазан
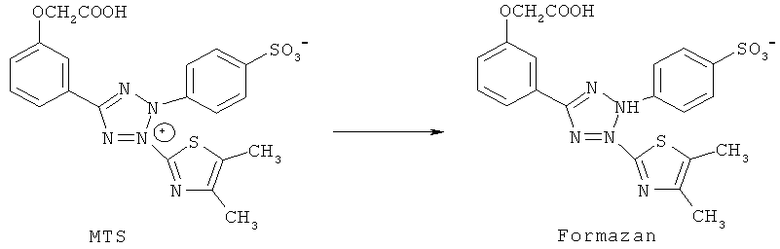
Описание метода:
А. Приготовление планшета с клетками: Для прикрепленных клеток из бутыли, в которой выращивали клетки, с помощью пипетки Пастера удаляли клеточную среду, затем клетки промывали 5 мл PBS и добавляли 2 мл 0,25% раствора трипсина в PBS. Затем клетки с раствором трипсина инкубировали в течение 5 минут при 37°С в атмосфере 5% CO2, после этого осторожно перемешивали с помощью пипетки и к полученной суспензии клеток добавляли 8 мл соответствующей клеточной среды. Открепившиеся в процессе трипсинизации клетки переносили в пробирку и центрифугировали при 1000 об/мин в течение 10 мин. Далее с помощью пипетки Пастера удаляли супернатант и добавляли 5 мл соответствующей среды. После перемешивания считали концентрацию клеток в получившейся суспензии с помощью камеры Горяева.
Для неприкрепленных клеток клеточную суспензию (без предварительной обработки трипсином) центрифугировали при 1000 об/мин в течение 10 мин. Далее с помощью пипетки Пастера удаляли супернатант и добавляли 5 мл соответствующей среды. После перемешивания считали концентрацию клеток в получившейся суспензии с помощью камеры Горяева. Далее путем смешивания необходимых объемов полученной суспензии клеток и соответствующей среды готовили клеточную суспензию с концентрацией - 6×105 кл/мл для прикрепленных и 12×105 кл/мл для неприкрепленных клеток - для загрузки в планшет.
Далее клетки высевали в 96-луночный планшет в лунки В1-H12 по 50 мкл клеточной суспензии на 1 лунку для неприкрепленных клеток и по 100 мкл клеточной суспензии на 1 лунку для прикрепленных клеток. Таким образом, количество клеток на 1 лунку в обоих случаях составляло 6000 клеток. В лунки А1-А12 добавляли соответствующую среду без клеток - по 50 мкл при приготовлении планшета с неприкрепленными клетками и по 100 мкл в случае прикрепленных клеток.
Планшеты инкубировали при 37°С в атмосфере 5% CO2 в течение 1 суток.
Б. Приготовление веществ: На аналитических весах брали навеску исследуемого вещества и растворяли ее в необходимом объеме системы EtOH:H2O=1:1 так, чтобы концентрация вещества в полученном растворе была 20 мМ. Далее приготавливали растворы веществ соответствующих концентраций в соответствующей питательной среде.
В. Загрузка веществ в планшет: В случае прикрепленных клеток из всех лунок с помощью пипетки Пастера удаляли клеточную среду и в лунки С1-H12 помещали приготовленные ранее растворы с исследуемыми веществами по 100 мкл в каждую лунку, по 3 лунки с одной и той же концентрацией вещества. В лунки В1-В12 и A1-А12 добавляли по 100 мкл соответствующей среды без веществ (эти лунки служат в качестве контрольных).
Для неприкрепленных клеток к 50 мкл уже имеющейся в каждой лунке клеточной суспензии добавляли еще 50 мкл раствора исследуемого вещества в соответствующей среде. Таким образом, концентрация вещества в клеточной среде уменьшалась в 2 раза по сравнению с исходной, что необходимо учитывать при приготовлении растворов веществ в среде до загрузки их на планшет. В лунки В1-В12 и А1-А12 добавляли по 50 мкл соответствующей среды без веществ. После этого планшеты инкубировали при 37°С в атмосфере 5% СО2 в течение 1 суток.
Г. Получение результатов: По завершении инкубирования в каждую лунку добавляли по 20 мкл MTS-реагента. Затем планшеты инкубировали при 37°С в атмосфере 5% CO2 еще в течение 2 часов. После чего оптическую плотность среды в каждой лунке регистрировали с помощью спектрофотометрического планшетного ридера при 492 нм (интенсивность поглощения, обусловленного наличием формазана) и 690 нм (результат использовали в качестве фонового показателя). Интенсивность окраски формазана при 492 нм прямо пропорциональна количеству оставшихся живых (метаболически-активных) клеток [Barltrop J.A., Owen Т.С., Соrу А.Н., Cory J.G. 5-(3-Carboxymethoxyphenyl)-2-(4,5-dimethylthiazolyl)-3-(4-sulfophenyl) tetrazolium, inner sault (MTS) and related analogs of 3-(4,5-dimethylthiazolyl)-2,5-diphenyltetrazolium bromide (MTT) reducing to purple water-soluble formazans as cell-viability indicators. // Bioorg. Med. Chem. Lett. 1991. №11. P.611-614]. Для определения цитотоксической активности веществ использовали также соответствующие спектрофотометрические показатели контрольных лунок на планшете: лунок с нулевым контролем (A1-А12), в которые не высевали клетки и не добавляли вещества, но добавляли MTS-реагент, и лунок со 100%-ным контролем (В1-В12), в которые высевали клетки в том же количестве, что и в экспериментальные, не добавляли вещества, но также добавляли MTS-реагент.
Д. Обработка результатов: Для вычисления количества живых клеток, оставшихся в экспериментальных лунках:
1. Из значения интенсивности поглощения среды при 492 нм в каждой лунке вычитали значение интенсивности поглощения среды при 690 нм в соответствующей лунке.
2. Находили среднее значение полученных в пункте 1 результатов для лунок с нулевым контролем и вычитали его из значений, полученных в пункте 1 для всех остальных лунок.
3. Вычисляли среднее значение полученных в пункте 2 результатов для лунок со 100%-ным контролем, IK.
4. Вычисляли количество живых клеток в каждой экспериментальной лунке (N), в процентах по сравнению с контрольными лунками, по формуле:
N=(IЭ/IK)x100%,
где IЭ - это интенсивность поглощения среды в каждой экспериментальной лунке, полученная в пункте 2;
IK - среднее значение полученных в пункте 3 результатов для лунок со 100%-ным контролем.
Для каждого из исследуемых веществ было проведено два независимых эксперимента.
Данную формулу использовали для вычисления цитотоксической активности двух из полученных соединений: 9-деметилоксиааптамина (2) и изоааптамина (5). Интенсивная красная окраска растворов 3-фенетиламино-9-деметилоксиааптамина (27), 3-изопентиламино-9-деметилоксиааптамина (28) и нового производного ааптамина, 3-N-морфолинил-9-деметилоксиааптамина (29), мешала определению цитотоксической активности этих соединений. Так, при регистрации спектрофотометрических показателей содержащейся в экспериментальной лунке среды окраска растворов веществ 27-29 суммировалась с окраской выработанного живыми клетками формазана, что в значительной мере увеличивало интенсивность поглощения при 492 нм и завышало итоговое вычисленное количество живых клеток. Поэтому непосредственно перед добавлением MTS-реагента при 492 нм регистрировали поглощение содержащейся в экспериментальных лунках среды с помощью того же планшетного ридера. Эти показания прибора затем вычитали из соответствующих показаний, полученных после обработки соответствующих лунок MTS-реагентом.
II. Результаты исследования биологической активности 9-деметилоксиааптамина (2), изоааптамина (5), 3-N-морфолинил-9-деметилоксиааптамина (29), 3-фенетиламино-9-деметилоксиааптамина (27) и 3-изопентиламино-9-деметилокси-ааптамина (28) и их обсуждение.
1. Противоопухолевая профилактическая (предупреждающая злокачественное перерождение клеток) активность.
К канцерпревентивным веществам относятся природные метаболиты или их синтетические аналоги, которые ингибируют трансформацию нормальных клеток в прораковые или прогрессию прораковых клеток в опухолевые. Следовательно, эффективное канцерпревентивное вещество должно вмешиваться в процесс канцерогенеза и тем или иным образом нейтрализовывать прораковые клетки, не давая им превратиться в опухолевые. Для исследования 9-деметилоксиааптамина (2), изоааптамина (5), 3-N-морфолинил-9-деметилоксиааптамина (29), 3-фенетиламино-9-деметилоксиааптамина (27) и 3-изопентиламино-9-деметилоксиааптамина (28) на канцерпревентивную активность мы использовали широко применяемый метод мягкого агара, мышиные эпителиальные JB6 Р+ С141 клетки, а также эпидермальный фактор роста (EGF) в качестве промотора опухолевой трансформации JB6 P+ С141 клеток [Colburn N.H., Former B.F., Nelson K.A., Yuspa S.H. Tumour promoter induces anchorage independence irreversibly. //Nature. 1979. V.281. P.589-591; Dong Z., Birrer M.J., Watts R.G., Matrisian L.M., Colburn N.H. Blocking of tumor promoter-induced AP-1 activity inhibits induced transformation in JB6 mouse epidermal cells. // Proc. Natl. Acad. Sci. USA. 1994. V.91, №2. P.609-613; Dong Z., Watts S.G., Sun Y., Colburn N.H. Progressive elevation of AP-1 activity during preneoplastic-to-neoplastic progression as modeled in mouse JB6 cell variants. // Int. J. Oncol. 1995. V.7. P.359-364; Strickland J., Sun Y., Dong Z., Colburn N.H. Grafting assay distinguishes promotion sensitive from promotion resistant JB6 cells. // Carcinogenesis. 1997. V.18. P.1135-1138]. Система клональных генетических вариантов JB6 клеток, которая включает в себя чувствительные к трансформации (Р+) и нечувствительные (Р-), а также трансформированные JB6 С141 клетки, широко используется в поиске канцерпревентивных веществ и изучении их свойства на молекулярном уровне. Различные типы JB6 клеток находятся на различных стадиях процесса их преобразования от пренеопластического до неопластического состояния и от ранней до поздней стадий такого преобразования [Colburn N.H., Wendel E., Srinivas L. Responses of preneoplastic epidermal cells to tumor promoters and growth factors: Use of promoter-resistant variants for mechanism studies. // J.Cell. Biochem. 1982. V.18, №3. P.261-270; Huang С., Ma W., Young M.R., Colburn N., Dong Z. Shortage of mitogen-activated protein kinase is responsible for resistance to AP-1 transactivation and transformation in mouse JB6 cells. // Proc. Natl. Acad. Sci. USA. 1998. V.95, №1. P.156-161; Bernstein L.R., Colburn N.H. AP1/jun function is differentially induced in promotion-sensitive and resistant JB6 cells. // Science. 1989. V.244, №4904. P.566-569].
JB6 P+ С141 клетки трансформируются после их обработки промоторами злокачественной трансформации, такими как EGF или ТРА. В процессе такой трансформации происходит активирование ядерного фактора транскрипции АР-1, который регулирует транскрипцию различных генов, ответственных за процессы воспаления, пролиферации и метастазирования [Dong Z., Birrer M.J., Watts R.G., Matrisian L.M., Colburn N.H. Blocking of tumor promoter-induced AP-1 activity inhibits induced transformation in JB6 mouse epidermal cells. // Proc. Natl. Acad. Sci. USA. 1994. V.91, №2. P.609-613; Huang С., Ma Y., Dawson M.I., Rincon M., Flavell R.A., Dong Z. Blocking activator protein - 1 activity, but not activating retinoic acid response element, is required for the antitumor promotion effect of retinoic acid. // Proc. Natl. Acad. Sci. USA. 1997. V.94, №11. P.5826-5830].
Полученные результаты доза-зависимого ингибирования 9-деметилоксиааптамином (2), изоааптамином (5), 3-N-морфолинил-9-деметилоксиааптамином (29), 3-фенетиламино-9-деметилоксиааптамином (27) и 3-изопентиламино-9-деметилокси-ааптамином (28) опухолевой трансформации JB6 Р+ C141 клеток отражены на чертеже, как количество колоний трансформированных JB6 P+ С141 клеток в процентах от контроля в зависимости от концентрации исследуемого вещества (диаграммы получены с помощью программы Microsoft Excel).
На основании этих данных с помощью компьютерных программ Microsoft Excel и Statistica 6.0 были произведены расчеты концентраций (INCC50), при которых исследуемые вещества ингибируют опухолевую трансформацию 50% клеток JB6 P+ С141. Результаты расчетов INCC50 показаны в таблице 5.
Таким образом, проведенные эксперименты показали, что 9-деметилоксиааптамин (2), изоааптамин (5), 3-фенетиламино-9-деметилоксиааптамин (27), 3-изопентиламино-9-деметилоксиааптамин (28) и 3-N-морфолинил-9-деметилоксиааптамин (29) способны ингибировать опухолевую трансформацию JB6 Р+ С141 клеток в концентрациях меньше цитотоксических (IC50) для той же клеточной линии в 10, 9, 10, 10 и 10 раз соответственно. Это говорит о возможности использования этих соединений в качестве средств профилактики раковых заболеваний.
2. Противоопухолевая цитотоксическая активность.
Цитотоксическая активность для 9-деметилоксиааптамина (2), изоааптамина (5), 3-N-морфолинил-9-деметилоксиааптамина (29), 3-фенетиламино-9-деметилоксиааптамина (27) и 3-изопентиламино-9-деметилокси-ааптамина (28) по отношению к семи линиям опухолевых и нормальных клеток человека и мыши была изучена MTS-методом. Результаты представлены в таблицах 6-10 в виде количества живых клеток определенной линии в зависимости от концентрации исследуемого вещества в среде.
Для каждого значения, отражающего процент живых клеток относительно контроля, указано стандартное отклонение от среднего. Астериск (*) указывает на результат, статистически достоверно отличающийся от контроля, р<0.05 (Манн-Уитни U-тест).
Для каждого значения, отражающего процент живых клеток относительно контроля, указано стандартное отклонение от среднего. Астериск (*) указывает на результат, статистически достоверно отличающийся от контроля, р<0.05 (Манн-Уитни U-тест).
Для каждого значения, отражающего процент живых клеток относительно контроля, указано стандартное отклонение от среднего. Астериск (*) указывает на результат, статистически достоверно отличающийся от контроля, р<0.05 (Манн-Уитни U-тест).
Для каждого значения, отражающего процент живых клеток относительно контроля, указано стандартное отклонение от среднего. Астериск (*) указывает на результат, статистически достоверно отличающийся от контроля, р<0.05 (Манн-Уитни U-тест).
Для каждого значения, отражающего процент живых клеток относительно контроля, указано стандартное отклонение от среднего. Астериск (*) указывает на результат, статистически достоверно отличающийся от контроля, р<0.05 (Манн-Уитни U-тест).
На основании данных, приведенных в таблицах 6-8, и с помощью компьютерных программ Microsoft Excel и Statistica 6.0 были произведены расчеты IC50 (концентрация исследуемого вещества, при которой гибнет 50% исследуемых клеток) по отношению к каждой исследованной клеточной линии. Полученные значения IC50 также представлены в таблицах 6-8.
Необходимо отметить, что цитотоксическая активность 9-деметилоксиааптамина (2), изоааптамина (5), 3-N-морфолинил-9-деметилоксиааптамина (29), 3-фенетиламино-9-деметилоксиааптамина (27) и 3-изопентиламино-9-деметилоксиааптамина (28) по отношению к приведенным в таблицах 6-10 клеточным линиям ранее не изучалась и приводится впервые.
Приготовление фармацевтических композиций.
Пример 3. 9-Деметилоксиааптамин (2) в эффективном количестве смешивают с соответствующим количеством смеси крахмала и гипса и прессуют в таблетку.
Пример 4. Фармацевтическую композицию готовят, как описано в примере 3, но в качестве активного компонента используют изоааптамин (5) в эффективном количестве, а в качестве наполнителя - смесь сорбита и стеарата кальция.
Пример 5. Фармацевтическую композицию готовят, как описано в примере 4, но в качестве активного компонента используют 3-фенетиламино-9-деметилоксиааптамин (27).
Пример 6. 3-Изопентиламино-9-деметилоксиааптамин (28) в эффективных концентрациях растворяют в соответствующем количестве физраствора.
Пример 7. Фармацевтическую композицию готовят, как описано в примере 6, но в качестве активного компонента используют 3-N-морфолинил-9-деметилоксиааптамин (29).
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО, ПРЕДОТВРАЩАЮЩЕЕ ТРАНСФОРМАЦИЮ НОРМАЛЬНЫХ КЛЕТОК МЛЕКОПИТАЮЩИХ В ОПУХОЛЕВЫЕ | 2010 |
|
RU2429839C1 |
| ГЛИКОЗИДНЫЕ ПРОИЗВОДНЫЕ 1,2-ДИТИОЛ-3-ТИОНА ИЛИ 1,2-ДИТИОЛ-3-ОНА И ЛЕКАРСТВЕННЫЕ СРЕДСТВА НА ИХ ОСНОВЕ | 2013 |
|
RU2534525C9 |
| СРЕДСТВО, ВОЗДЕЙСТВУЮЩЕЕ НА АКТИВНОСТЬ НЕКОТОРЫХ ЯДЕРНЫХ ФАКТОРОВ ТРАНСКРИПЦИИ | 2011 |
|
RU2457840C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2414920C1 |
| ТЕРАПЕВТИЧЕСКИЕ ХИНОНЫ | 2005 |
|
RU2411229C2 |
| Пептид, проявляющий антибактериальные и противоопухолевые свойства | 2019 |
|
RU2702661C1 |
| ПЕПТИД, ОБЛАДАЮЩИЙ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2017 |
|
RU2658781C1 |
| Клеточная линия рака молочной железы человека BrCCh4e | 2019 |
|
RU2717654C1 |
| ЦИТОТОКСИЧЕСКАЯ И ПРОТИВОВИРУСНАЯ АКТИВНОСТЬ 3-АЦИЛОКСИМЕТИЛ-3-ОКСО-1-ЦИАНО-2,3-СЕКО-2-НОР-ТРИТЕРПЕНОИДОВ | 2018 |
|
RU2686100C1 |
| МОНОЯДЕРНЫЕ ДИНИТРОЗИЛЬНЫЕ КОМПЛЕКСЫ ЖЕЛЕЗА, СПОСОБ ПОЛУЧЕНИЯ МОНОЯДЕРНЫХ ДИНИТРОЗИЛЬНЫХ КОМПЛЕКСОВ ЖЕЛЕЗА, ДОНОР МОНООКСИДА АЗОТА, ПРИМЕНЕНИЕ МОНОЯДЕРНОГО ДИНИТРОЗИЛЬНОГО КОМПЛЕКСА ЖЕЛЕЗА В КАЧЕСТВЕ ПРОТИВООПУХОЛЕВОГО ЛЕКАРСТВЕННОГО СРЕДСТВА | 2011 |
|
RU2494104C2 |
Группа изобретений относится к медицине, конкретно к онкологии, и касается веществ, предотвращающих злокачественное перерождение нормальных клеток млекопитающих (в том числе человека) в опухолевые. Из губки Aaptos sp. получен аналог ааптамина, а именно 3-N-морфолинил-9-деметилоксиааптамин, обладающий способностью предотвращать трансформацию нормальных клеток млекопитающих в опухолевые. Предложено применение 3-N-морфолинил-9-деметилоксиааптамина, а также его аналогов 9-деметилоксиааптамина, изоааптамина, 3-фенетиламино-9-деметилоксиааптамина и 3-изопентиламино-9-деметилоксиааптамина в качестве подобных средств. Эти вещества также применяют для приготовления фармацевтических композиций, предотвращающих трансформацию нормальных клеток млекопитающих в опухолевые. 3-N-морфолинил-9-деметилоксиааптамин и его аналоги оказывают раково-профилактическое действие в нетоксических для нормальных клеток концентрациях, что значительно снижает риск токсического действия на организм при длительном их применении. 3 н.п. ф-лы, 1 ил., 10 табл.
1. Средство, предотвращающее трансформацию нормальных клеток млекопитающих в опухолевые, представляющее собой 3-N-морфолинил-9-деметилоксиааптамин.
2. Применение 9-деметилоксиааптамина, или изоааптамина, или 3-фенетиламино-9-деметилоксиааптамина, или 3-изопентиламино-9-деметилоксиааптамина в качестве средства, предотвращающего трансформацию нормальных клеток млекопитающих в опухолевые.
3. Применение 3-N-морфолинил-9-деметилоксиааптамина, или 9-деметилоксиааптамина, или изоааптамина, или 3-фенетиламино-9-деметилоксиааптамина, или 3-изопентиламино-9-деметилоксиааптамина для приготовления фармацевтической композиции, предотвращающей трансформацию нормальных клеток млекопитающих в опухолевые.
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
| ДЫШЛОВОЙ С.А | |||
| Создание биологически-активной добавки с канцерпревентивными свойствами на основе ааптамина | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Молодежная секция "Актуальные проблемы химии и биологии" | |||
| Материалы | |||
| Часть II, конкурс "У.М.Н.И.К." - Владивосток: 2008, с.22-25 | |||
| [он-лайн] [Найдено | |||
Авторы
Даты
2011-09-27—Публикация
2010-01-22—Подача