Изобретение относится к биотехнологии, в частности к рекомбинантной плазмидной ДНК, кодирующей фрагмент онкофетального белка человека, обладающего сродством к рецептору альфа-фетопротеина (АФП) и подвергающегося рецептор-опосредованному эндоцитозу.
Известны очищенные и выделенные последовательности ДНК, имеющие активность по повышению продуцирования белка, характеризующиеся тем, что последовательности ДНК включает в себя, по меньшей мере, один элемент изогнутой ДНК и, по меньшей мере, один участок связывания ДНК-связывающего белка [RU 2375078, С2, A61K 39/395, 10.12.2009].
Недостатком этого решения является относительно узкая область применения.
Наиболее близким по своей сущности к предложенному является очищенная и выделенная последовательность ДНК, имеющая активность по повышению продуцирования белка, представляющая собой а) последовательность ДНК, характеризующуюся нуклеотидной последовательностью MAR, выбранной из группы, включающей SEQ ID NO: 24-27, комплементарной ей последовательностью, ее частью, содержащей, по меньшей мере, 70% нуклеотидов в длину; или b) последовательность ДНК, характеризующуюся тем, что она, по существу, соответствует элементу или фрагменту cLysMAR, включающему, по меньшей мере, одну область, выбранную из В-, K- и F-областей [RU 2375450, С2, C12N 15/11, 10.12.2009].
Недостатком этого решения является относительно узкая область применения, поскольку известная ДНК не обладает свойствами рекомбинантной плазмидной ДНК, кодирующей фрагмент альфа-фетопротеина человека, обладающего сродством к рецептору АФП и подвергающегося рецептор-опосредованному эндоцитозу.
Кроме того, продукт, получаемый при реализации известного технического решения, обладает потенциальной возможностью загрязнения вирусами человека.
Требуемый результат заключается в уменьшении возможности загрязнения конечного продукта вирусами человека и расширении области применения за счет создания бактериального штамма-продуцента рекомбинантного фрагмента альфа-фетопротеина человека, что позволяет, в свою очередь, получать свободный от загрязнений вирусами человека целевой белок с высоким уровнем выхода.
Требуемый результат достигается тем, что бактериальный штамм-продуцент отличается тем, что клетки штамма несут плазмиду с геном, кодирующим целевой фрагмент альфа-фетопотеина человека.
Кроме того, требуемый технический результат достигается тем, что в качестве клеток штамма, несущих плазмиду с геном, кодирующим целевой фрагмент альфа-фетопротеина человека, используют клетки штамма BL21 (DE3).
Кроме того, требуемый технический результат достигается тем, что в качестве плазмиды с геном, кодирующим целевой фрагмент альфа-фетопротеина человека, используют плазмиду рЕТ 11 с клонированным в нее геном, кодирующим целевой фрагмент альфа-фетопротеина человека.
Кроме того, требуемый технический результат достигается тем, что ген, кодирующий целевой фрагмент альфа-фетопротеина человека с 404 аминокислоты по 609 аминокислоту, содержит тандем из двух редких кодонов AGG AGG, кодирующих остатки аргининов.
Кроме того, требуемый технический результат достигается тем, что в качестве тандема из двух редких кодонов, кодирующего остатки аргининов, используются изоакцепторные кодоны, кодирующие остатки аргинина.
Кроме того, требуемый технический результат достигается тем, что в качестве тандема изоакцепторных кодонов, кодирующих остатки аргининов, используется тандем CGT CGC.
Кроме того, требуемый технический результат достигается тем, что уровень продукции целевого белка бактериальным штаммом-продуцентом рекомбинантного фрагмента альфа-фетопротеина составляет не менее 100 мг на литр культуры клеток или 100 мг на 1 грамм биомассы клеток.
На чертежах представлены:
на фиг.1 - нуклеотидная последовательность АФП;
на фиг.2 - амплификация фрагментов гена;
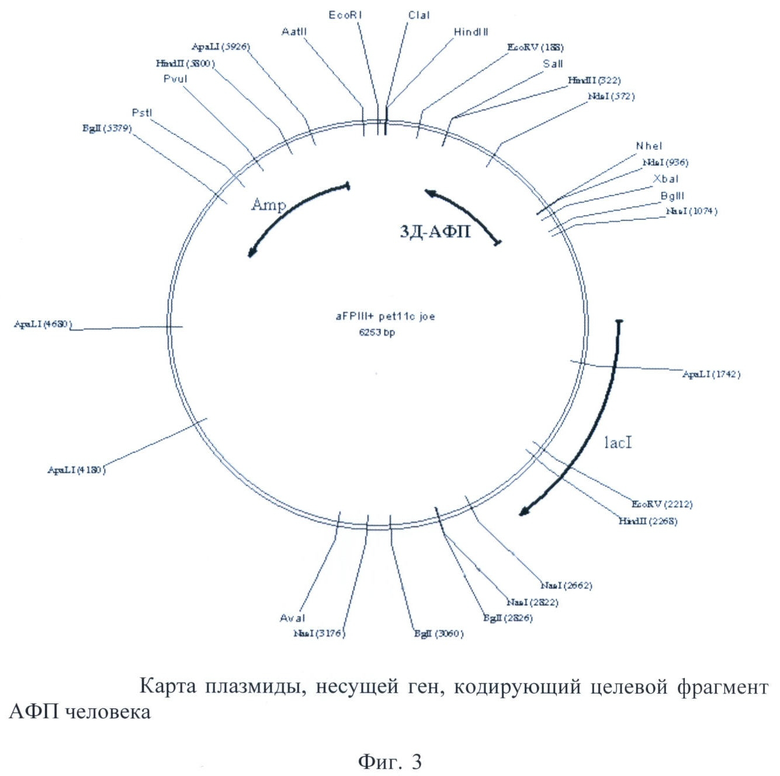
на фиг.3 - карта плазмиды;
на фиг.4 - нуклеотидная последовательность конструктора;
на фиг.5 - аминокислотная последовательность полученного продукта;
на фиг.6 - анализ наличия целевого белка;
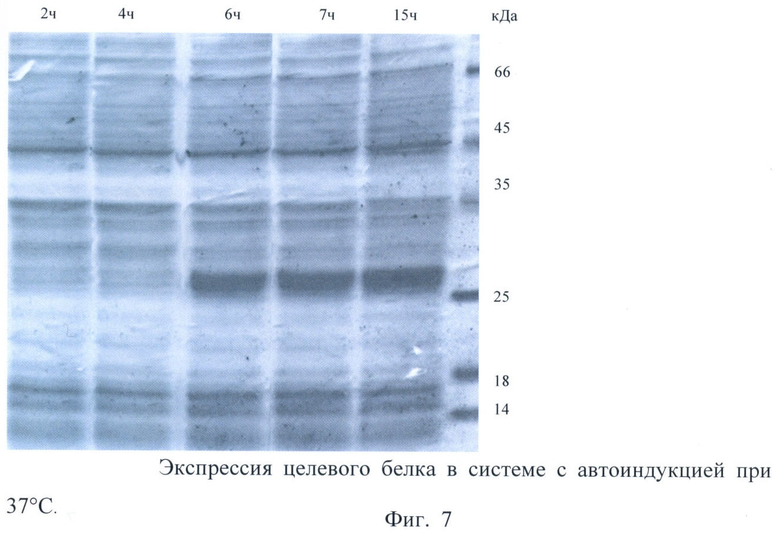
на фиг.7 - электрофоретический анализ клеточного белка.
Получение бактериального штамма-продуцента рекомбинантного фрагмента альфа-фетопротеина человека (АФП) производилось следующим образом.
Известно, что в первую очередь на уровень экспрессии в бактериальных клетках влияет наличие редких кодонов, расположенных друг за другом. В нуклеотидной последовательности АФП присутствует тандем из двух редких кодонов AGG, кодирующих остатки аргининов - Arg508 и Arg509 (фиг.1).
Было выявлено, что замена таких тандемов аргинина обеспечивает значительное увеличение уровня экспрессии. Был получен фрагмент гена АФП, соответствующего целевому фрагменту (404-609 аминокислотные остатки), при этом была произведена замена указанного тандема AGG AGG на кодоны аргинина CGT CGC, оптимальные для E.coli. Замену проводили амплификацией фрагментов гена, как указано на фиг.2.
Для пцр-амплификации использовали следующие праймеры:
1-5′ CCGTAGCTAGCATGTACATCCAGGAGAGCCAAGC 3′
2-5′ CGCCAACCGTCGCCCATGCTTCAGCAGCTTGG 3′
3-5′ GGCGACGGTTGGCGTATGAAGAAGTGCAGCACTGG 3′
4- ′AAGAATGTCGACTTAGTGATGGTGATGGTGATGGTGCTCT TCAGCAAAGCAGACTT 3′
Пцр-амплификацию проводили в стандартных условиях с термостабильной Tag полимеразой. Для реакции проводили 30 циклов. Использовалась температура 72°С для проведения амплификации, 51°С для отжига праймеров и 95°С для разделения цепей ДНК.
При модификации гена был также уничтожен сайт рестрикции NdeI для удобства последующей работы. Указанные модификации гена не приводили к заменам в аминокислотной последовательности белка. Кроме этого к 3′-концу гена была добавлена последовательность, кодирующая 7 гистидиновых остатков для последующей аффинной очистки белка, и введены сайты рестрикции NheI и SalI для клонирования гена.
Модифицированный ген АФП клонировали в плазмиду рЕТ11с по сайтам рестрикции NheI и SalI для дальнейшей аналитической экспрессии в E.coli.
Процедура клонирования состояла из следующих этапов:
1. Амплифицированный фрагмент гена АФП и плазмиду рЕТ11с (по отдельности) последовательно обрабатывали рестриктазами NheI и SalI.
2. Полученные фрагмент гена АФП и плазмиду рЕТ11с подвергали электрофоретическому разделению в агарозном геле и далее вырезали кусочки геля, содержащие указанные фрагменты ДНК. В этом случае для визуализации полос ДНК использовалось ультрафиолетовое освещение трансиллюминатора с длиной волны 365 нм, т.к. она не вызывает повреждений ДНК.
3. Ген и плазмиду выделяли из геля и подвергали реакции лигирования. Для этого их смешивали в буфере для лигирования в весовом соотношении 1:1, добавляли Т4 ДНК лигазу и инкубировали при комнатной температуре в течение 2±0,5 часов.
4. Проводили трансформацию клеток E.coli штамма МС1061 аликвотой лигированной смеси. Для этого к 20±5 мкл лигированной смеси добавляли 200±30 мкл свежеприготовленных компетентных клеток. После инкубации клетки высевали на агаризованную среду LB с ампициллином в концентрации 100 мкг/мл в чашках Петри и инкубировали 15±2 часов при температуре 37°С.
5. Выросшие колонии клеток проверяли на наличие гена АФП амплификацией со специфическими праймерами к указанному гену.
6. Колонии E.coli, несущие ген целевого белка, выращивали на жидкой питательной среде LB с ампициллином в пробирках в течение 15±2 часов при температуре 37°С при постоянном покачивании в качалке. Полученную биомассу собирали центрифугированием в микропробирках 1.5 мл.
7. Выделяли плазмиду из полученной биомассы методом щелочного лизиса.
8. Подтверждение наличия гена АФП в плазмиде проводили с помощью рестрикционного анализа по сайтам клонирования NheI и SalI. Карта плазмиды представлена на фиг.3.
Для проверки полученного конструкта pAFP11D3 было проведено определение его нуклеотидной последовательности (фиг.4). Было подтверждено наличие внесенных нуклеотидных замен в ген АФП для оптимизации его кодонов, что, как указано выше, не приводит к замене в аминокислотной последовательности. Аминокислотная последовательность полученного продукта представлена на фиг 5.
Экспрессия рекомбинантного белка с химическим индуктором.
Полученную плазмиду, содержащую фрагмент гена АФП, трансформировали в клетки E.coli штамма BL21DE3 (E.coli В F- dcm ompT hsdS(rB- mB-) gal λ(DE3)). Для этого к 200 мкл свежеприготовленных компетентных клеток добавляли 0,5 мкл плазмиды в концентрации 0,2 мкг/ мкл. После инкубации клетки высевали на агаризованную среду LB с ампициллином в концентрации 100 мкг/мл в чашках Петри и инкубировали 15 часов при температуре 37°С.
Выросшие колонии клеток проверяли на наличие фрагмента гена АФП амплификацией со специфическими праймерами к указанному гену.
Колонии E.coli, несущие ген целевого белка, выращивали на жидкой питательной среде LB с ампициллином в пробирках в течение 15±2 часов при температуре 37°С при постоянном покачивании в качалке. Полученную биомассу собирали центрифугированием в микропробирках 1,5 мл.
Выделяли плазмиду из полученной биомассы методом щелочного лизиса.
Подтверждение наличия гена АФП в плазмиде проводили с помощью рестрикционного анализа по сайтам клонирования NheI и SalI.
Проводили аналитическую экспрессию целевого белка с использованием химического индуктора. Для этого колонии E.coli, несущие ген целевого белка, выращивали на жидкой питательной среде LB с ампициллином в пробирках в течение 15±2 часов при температуре 37°С при постоянном покачивании в качалке. Добавляли 0,5 мл в колбы объемом 250 мл, содержащие 50 мл жидкой среды LB с ампициллином. Растили при температуре 37°С при постоянном покачивании до оптической плотности 0.5±0.1 (OD600) (время инкубации составляло от 1.5 до 2.5 часов). Затем добавляли химический индуктор - 0.4 мМ ИПТГ (изопропил-β-D-тиогалактопиранозид) и наращивали далее в течение 3 часов. Биомассу собирали центрифугированием в пластиковых пробирках на 50 мл (центрифуга ОПН-8, 4.000 об/мин 8 минут).
Проводили электрофоретический анализ клеточного белка в полиакриламидном геле в денатурирующих условиях. Для этого к аликвоте клеток 10 мг добавляли 40 мкл воды, перемешивали на встряхивателе и добавляли 40 мкл 2х буфера для образцов для белкового денатурирующего электрофореза. Образец прогревали при 95°С в течение 4 минут и наносили на денатурирующий гель с концентрацией акриламида 12%. После проведения электрофоретического разделения гель промывали дистиллированной водой, после чего окрашивали краской, содержащей краситель Кумасси. Избыток краски отмывали раствором, содержащим этанол и уксусную кислоту.
Анализ наличия целевого белка проводили визуально, сравнивая набор клеточных белков в неиндуцированных клетках и клетках, индуцированных ИПТГ (фиг.6). Для определения молекулярной массы полученного целевого белка использовали набор белков с известными молекулярными весами.
Проводили анализ количества целевого белка по отношению к общему клеточному белку. Для этого гель сканировали на сканере Epson 1660 Photo. Полученное изображение обрабатывали с помощью программы Onedscan.
Проводили анализ распределения целевого белка между фракцией растворимых белков и тельцами включения (агрегированной формой белка). Для этого к аликвоте клеток (40 мг) добавляли 200 мкл буфера PBS с 300 mМ NaCl, ингибитором протеаз AEBSF и лизоцимом до конечной концентрации 2.5 мг/ мл. После 10 минут инкубации во льду в суспензию добавляли по 0.2 мкл ДНКазы и РНКазы в концентрации 10 мг/мл и 1 единица/мл, соответственно, и дополнительно инкубировали 30 минут во льду. После этого добавляли 10% Тритон X100 до конечной концентрации 1%. Лизат клеток подвергали центрифугированию в микропробирках 1.5 мл при скорости 13000 об/мин 10 минут при температуре 4°С. Супернатант и осадок разделяли и анализировали белковый состав с помощью акриламидного геля в денатурирующих условиях. Целевой белок практически полностью обнаруживается в осадке, т.е. во фракции нерастворимых белков, также называемых тельцами включения.
Результаты экспрессии (фиг.6) показывают высокий уровень синтеза целевого белка, целевой белок составляет не менее 25% от общего клеточного белка (в среднем составляет 30-35%).
Экспрессия целевого фрагмента АФП в E.coli методом автоиндукции.
Суть подхода состоит в использовании сред роста, позволяющих достичь достаточно высоких плотностей культуры клеток при наращивании. Кроме этого среды роста подбираются таким образом, что при начальном наращивании до высоких плотностей lac-промотор, индуцирующий синтез Т7 полимеразы (а значит и синтез целевого белка), находится в репрессированном состоянии. На поздних же стадиях роста lac-промотор индуцируется под воздействием лактозы, входящей в состав сред.
Плазмиду, содержащую фрагмент гена АФП, трансформировали в клетки E.coli штамма BL21DE3, как описано выше. Выросшие колонии клеток проверяли на наличие фрагмента гена амплификацией со специфическими праймерами.
100-200 колоний E.coli, несущих ген целевого белка, добавляли к 200 мл жидкой питательной среды ТВ с 200 мкг/мл ампициллина и растили в колбах на 1 л в течение 18-24 часов при температуре 37°С при постоянном покачивании в качалке. Указанные условия являются оптимальными для исследуемого штамма по среде роста, температуре и времени инкубации. Оптическая плотность культуры к моменту завершения инкубации составляла не менее 10 о.е. OD600 и, как правило, была около 12 о.е.
Полученную биомассу собирали центрифугированием в центрифужных пробирках на роторе JA14 центрифуга J2-21 Beckman при 7000 об/мин в течение 10 минут.
Проводили электрофоретический анализ клеточного белка в полиакриламидном геле в денатурирующих условиях (фиг.7).
Анализ наличия целевого белка проводили визуально, сравнивая набор клеточных белков в неиндуцированных клетках и клетках после автоиндукции. Для определения молекулярной массы полученного целевого белка использовали набор белков с известными молекулярными весами.
Проводили анализ количества целевого белка по отношению к общему клеточному белку. Выход целевого белка от общего клеточного белка по результатам денситометрии электрофоретического разделения суммарного препарата белков в среднем составляет 30-35%.
Проводили анализ распределения целевого белка между фракцией растворимых белков и тельцами включения (агрегированной формой белка). Целевой белок практически полностью обнаруживается в осадке, т.е. во фракции нерастворимых белков, также называемых тельцами включения.
Система с автоиндукцией позволяет достигать существенно большей оптической плотности клеток, чем экспрессия в среде LB с индуктором. При этом экспрессия начинается достаточно поздно, на поздней логарифмической стадии роста клеток, по-видимому, экспрессия целевого белка начинается при достижении оптической плотности культуры примерно 7.
Характеристика полученного штамма-продуцента.
Конечный продукт представляет собой штамм-продуцент целевого белка, фрагмента АФП, в клетках E.coli, который характеризуется тем, что:
Представлен грамотрицательными палочками, дающими на агаризованной питательной среде с ампициллином слабовыпуклые колонии диаметром (2±0.5)мм серого цвета, гладкие, с ровным краем.
Имеет тельца включения, представляющие собой гибридный белок, имеющий последовательность, соответствующую району предполагаемого целевого фрагмента АФП человека. В оптимальных условиях экспрессии по данным SDS-электрофореза на долю гибридного белка приходится не менее 25% от общего клеточного белка. Продукция целевого белка составляет не менее 170-200 мг с 1 литра культуры или 20-25 мг/1 гр биомассы.
Клетки содержат плазмиду, характеризующуюся соответствующей рестриктной картой, где между сайтами рестрикции NheI и SalI встроена нуклеотидная последовательность, кодирующая целевой гибридный белок. Экспрессия белка регулируется Т7-промотором и может быть индуцирована как с помощью химического индуктора ИПТГ, так и с помощью эффекта автоиндукции.
Таким образом, благодаря проведенному усовершенствованию достигнут требуемый технический результат, поскольку получен бактериальный штамм-продуцент рекомбинантного фрагмента альфа-фетопротеина человека, который практически свободен от загрязнений вирусами человека.




Изобретение относится к биотехнологии, в частности к рекомбинантной продукции онкофетальных белков человека, и может быть использовано для получения фрагмента с 404 по 609 аминокислоту альфа-фетопротеина человека. Путем трансформации клеток Escherichia coli штамма BL21(DE3) плазмидной ДНК pAFP11D3 получают штамм Escherichia coli BL21(DE3)/pAFP11D3 - продуцент фрагмента с 404 по 609 аминокислоту альфа-фетопротеина человека. Изобретение позволяет уменьшить возможность загрязнения вирусами человека при получении рекомбинантным путем указанного фрагмента альфа-фетопротеина, обладающего сродством к рецептору альфа-фетопротеина (АФП) и подвергающегося рецептор-опосредованному эндоцитозу. 1 з.п. ф-лы, 7 ил.
1. Штамм Escherichia coli BL21(DE3)/pAFP11D3 - продуцент фрагмента с 404 по 609 аминокислоту альфа-фетопротеина человека, полученный путем трансформации клеток Escherichia coli штамма BL21(DE3) плазмидной ДНК pAFP11D3, которая имеет физическую карту, изображенную на фиг.3, и характеризуется нуклеотидной последовательностью, показанной на фиг.4.
2. Штамм Escherichia coli BL21(DE3)/pAFP11D3 - продуцент фрагмента с 404 по 609 аминокислоту альфа-фетопротеина человека по п.1, в котором уровень продукции целевого белка составляет не менее 100 мг на литр культуры клеток или 100 мг на 1 грамм биомассы клеток.
| ПРОТИВООПУХОЛЕВЫЙ ПЕПТИДНЫЙ ПРЕПАРАТ НА ОСНОВЕ ФРАГМЕНТА АЛЬФА-ФЕТОПРОТЕИНА, ЕГО КОНЪЮГАТ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ ГОРМОНЗАВИСИМЫХ ОПУХОЛЕЙ | 2005 |
|
RU2285537C1 |
| WO 2008072895 А1, 19.06.2008 | |||
| ДНК, ПОВЫШАЮЩАЯ ПРОДУЦИРОВАНИЕ БЕЛКА, И ЕЕ ПРИМЕНЕНИЕ | 2004 |
|
RU2375450C2 |
Авторы
Даты
2011-06-27—Публикация
2010-02-16—Подача