Настоящее изобретение относится к новым производным бензазепина, обладающим фармакологической активностью, к способам их получения, к композициям, содержащим данные соединения, и к их применению для лечения неврологических и психиатрических нарушений.
В JP 2001226269 и WO 00/23437 (Takeda Chem. Ind. Ltd) описывается ряд производных бензазепина, которые заявляются как средства для лечения ожирения. В DE 2207430, US 4210749, FR 2171879 (Pennwalt Corp.) и GB 1268243 (Wallace and Tiernan Inc.) описывается ряд производных бензазепина в качестве антагонистов наркотиков (таких как морфин или кодеин), а также антигистаминные и антихолинергические средства. В WO 02/14513 (Takeda Chem. Ind. Ltd) описывается ряд производных бензазепина с активностью GPR12 как средства для лечения синдрома нарушения внимания, нарколепсии или беспокойства. В WO 02/02530 (Takeda Chem. Ind. Ltd) описывается ряд производных бензазепина как антагонистов GPR14 как средства для лечения гипертонии, атеросклероза и инфаркта миокарда. В WO 01/03680 (Isis Innovation Ltd) описывается ряд производных бензазепина, которые заявляются как эффективные средства, использующиеся при получении клеток для трансплантации, а также для подавления таких заболеваний, как диабет. В WO 00/21951 (SmithKline Beecham pic) раскрывается ряд производных тетрагидробензазепина как модуляторов рецепторов допамина D3 в качестве антипсихотических средств. В WO 01/87834 (Takeda Chem. Ind Ltd) описывается ряд производных бензазепина как антагонистов MCH, которые заявляются как средства для лечения ожирения. В WO 02/15934 (Takeda Chem. Ind. Ltd) описывается ряд производных бензазепина как антагонистов рецепторов уротензина II, которые заявляются как средства для лечения нейродегенеративных заболеваний.
Рецептор гистамина H3 преимущественно экспрессируется в центральной нервной системе млекопитающих (CNS), в периферических тканях он экспрессируется на минимальном уровне, за исключением некоторых симпатических нервов (Leurs et al. (1998), Trends Pharmacol. Sci. 19, 177-183). Активация рецепторов H3 под действием селективных агонистов или гистамина приводит к ингибированию высвобождения нейромедиаторов из ряда различных популяций нервных клеток, в том числе из гистаминергических и холинергических нейронов (Schlicker et al. (1994), Fundam. Clin. Pharmacol. 8, 128-137). Кроме того, исследования in vitro и in vivo показали, что антагонисты H3 могут способствовать высвобождению нейромедиаторов из таких участков мозга, как кора головного мозга и гиппокамп, которые имеют отношение к познавательной способности (Onodera et al. (1998), In: The Histamine H3 receptor, ed Leurs and Timmerman, pp. 255-267, Elsevier Science B. V.). Кроме того, в ряде публикаций было продемонстрировано, что антагонисты H3 (например, тиоперамид, клобенпропит, ципроксифан и GT-2331) улучшают познавательную способность у кроличьих моделей, в том числе, выполнение следующих тестов: задачи пятикратного выбора, распознавания объекта, приподнятого крестообразного лабиринта, обнаружения новой задачи и пассивного уклонения (Giovanni et al. (1999), Behav. Brain Res. 104, 147-155). Приведенные данные позволяют предположить, что новые антагонисты H3 и/или обратные агонисты, например ряд соединений настоящего изобретения, можно использовать для лечения ухудшения познавательной способности при таких неврологических заболеваниях, как болезнь Альцгеймера и родственные нейродегенеративные нарушения.
В первом аспекте настоящее изобретение предлагает соединение формулы (I) или его фармацевтически приемлемую соль:
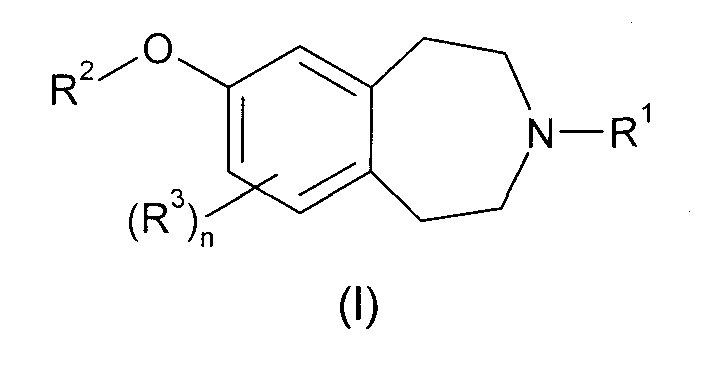
где R1 обозначает -C3-7 циклоалкил, необязательно замещенный C1-3 алкилом;
R2 обозначает водород, -C1-6алкил, -X-C3-8циклоалкил, -X-арил, -X-гетероциклил, -X-гетероарил, -X-C3-8циклоалкил-Y-C3-8циклоалкил, -X-C3-8циклоалкил-Y-арил, -X-C3-8циклоалкил-Y-гетероарил, -X-C3-8циклоалкил-Y-гетероциклил, -X-арил-Y-C3--8циклоалкил, -X-арил-Y-арил, -X-арил-Y-гетероарил, -X-арил-Y-гетероциклил, -X-гетероарил-Y-C3-8циклоалкил, -X-гетероарил-Y-арил, -X-гетероарил-Y-гетероарил, -X-гетероарил-Y-гетероциклил, -X-гетероциклил-Y-C3-8циклоалкил, -X-гетероциклил-Y-арил, -X-гетероциклил-Y-гетероарил, -X-гетероциклил-Y-гетероциклил;
X обозначает связь или C1-6алкил;
Y обозначает связь, C1-6алкил, CO, COC2-6алкенил, О или SO2;
R3 обозначает галоген, C1-6алкил, C1-6алкокси, циано, амино или трифторметил;
n обозначает 0, 1 или 2;
где указанные алкильные, циклоалкильные, арильные, гетероарильные и гетероциклические группы R2 могут быть необязательно замещены одним или несколькими заместителями (например, 1, 2 или 3), которые могут быть одинаковыми или разными и которые могут быть выбраны из группы, состоящей из галогена, гидрокси, циано, нитро, =O, трифторметила, трифторметокси, фторметокси, дифторметокси, C1-6алкила, пентафторэтила, C1-6алкокси, арилС1-6алкокси, C1-6алкилтио, C1-6алкоксиС1-6алкила, C3-7циклоалкилС1-6алкокси, C1-6алканоила, C1-6алкоксикарбонила, C1-6алкилсульфонила, C1-6алкилсульфинила, C1-6алкилсульфонилокси, C1-6алкилсульфонилС1-6алкила, сульфонила, арилсульфонила, арилсульфонилокси, арилсульфонилС1-6алкила, арилокси, C1-6алкилсульфонамидо, C1-6алкиламино, C1-6алкиламидо, -R4, -CO2R4, -COR4, C1-6алкилсульфонамидоС1-6алкила, C1-6алкиламидоС1-6алкила, арилсульфонамидо, арилкарбоксамидо, арилсульфонамидоС1-6алкила, арилкарбоксамидоС1-6алкила, ароила, ароилС1-6алкила, арилС1-6алканоила или группы -NR5R6, -C1-6алкил-NR5R6, -C3-8циклоалкил-NR5R6, -CONR5R6, -NR5COR6, -NR5SO2R6, -OCONR5R6, -NR5CO2R6, -NR4CO2NR5R6 или -SO2NR5R6 (где R4, R5 и R6 независимо обозначают водород, C1-6алкил, C3-8циклоалкил, C1-6алкил-C3-8циклоалкил, арил, гетероциклил или гетероарил, или -NR5R6 может обозначать гетероциклическую группу, содержащую атом азота, где указанные группы R4, R5 и R6 могут быть необязательно замещены одним или несколькими заместителями (например, 1, 2 или 3), которые могут быть одинаковыми или разными и которые могут быть выбраны из группы, состоящей из галогена, гидрокси, C1-6алкила, C1-6алкокси, циано, амино, =O или трифторметила);
или их сольватов.
В одном конкретном воплощении настоящего изобретения предлагается соединение формулы (I), как определено выше, где
R2 обозначает -C1-6алкил, -X-C3-8циклоалкил, -X-арил, -X-гетероциклил, -X-гетероарил, -X-C3-8циклоалкил-Y-C3-8циклоалкил, -X-C3-8циклоалкил-Y-арил, -X-C3-8циклоалкил-Y-гетероарил, -X- C3-8циклоалкил-Y-гетероциклил, -X-арил-Y-C3-8циклоалкил, -X-арил-Y-арил, -X-арил-Y-гетероарил, -X-арил-Y-гетероциклил, -X-гетероарил-Y-C3-8циклоалкил, -X-гетероарил-Y-арил, -X-гетероарил-Y-гетероарил, -X-гетероарил-Y-гетероциклил, -X-гетероциклил-Y-C3-8циклоалкил, -X-гетероциклил-Y-арил, -X-гетероциклил-Y-гетероарил, -X-гетероциклил-Y-гетероциклил;
Y обозначает связь, C1-6алкил, CO, O или SO2; и
R4, R5 и R6 независимо обозначают водород, C1-6алкил, -C3-8циклоалкил, арил, гетероциклил или гетероарил, или -NR5R6 может обозначать гетероциклическую группу, содержащую атом азота.
Особо можно упомянуть соединения формулы (I), где R2 обозначает -X-гетероциклил, -X-гетероциклил-Y-C3-8циклоалкил, -X-гетероциклил-Y-арил, -X-гетероциклил-Y-гетероарил или -X-гетероциклил-Y-гетероциклил, а указанные гетероциклические группы соединены с X через атом углерода.
Алкильные группы, присутствующие отдельно или в составе другой группы, могут быть линейными или разветвленными, группы алкокси и алканоил интерпретируют так же. Более предпочтительно, алкильные фрагменты представляют собой C1-4алкил, например метил или этил. Термин "галоген" используется в описании, если не указано иначе, для определения группы, выбранной из фтора, хлора, брома или иода.
Термин "арил" включает моноциклические карбоциклические ароматические кольца (например, фенил) и бициклические карбоциклические ароматические кольца (например, нафтил) или карбоциклические бензоконденсированные кольца (например, C3-8циклоалкил, конденсированный с фенильным циклом, такой как дигидроинденил или тетрагидронафталинил).
Подразумевается, что термин "гетероциклил" обозначает 4-7-членный моноциклический насыщенный или частично ненасыщенный алифатический цикл или 4-7-членный насыщенный или частично ненасыщенный алифатический цикл, конденсированный с бензольным циклом, содержащим от 1 до 3 гетероатомов, выбранных из кислорода, азота или серы. Подходящие примеры таких моноциклических колец включают в себя пирролидинил, пиперидинил, пиперазинил, морфолинил, тиоморфолинил, тетрагидрофуранил, тетрагидропиранил, диазепанил, азепанил, имидазолидинил, изотиазолидинил, оксазолидинил, пирролидинон и тетрагидрооксазепинил. Подходящие примеры бензоконденсированных гетероциклических колец включают в себя индолинил, изоиндолинил, бензодиоксолил, дигидроизоиндол, дигидробензофуранил, дигидробензотиопиранил и дигидроизохинолинил.
Подразумевается, что термин "гетероциклил, содержащий атом азота" относится к любой гетероциклической группе, как определено выше, которая содержит атом азота.
Подразумевается, что термин "гетероарил" обозначает 5-7-членное моноциклическое ароматическое или конденсированное 8-11-членное бициклическое ароматическое кольцо, содержащее от 1 до 3 гетероатомов, выбранных из кислорода, азота и серы. Подходящие примеры таких моноциклических ароматических циклов включают в себя тиенил, фурил, пирролил, триазолил, имидазолил, оксазолил, тиазолил, оксадиазолил, изотиазолил, изоксазолил, тиадиазолил, пиразолил, пиримидил, пиридазинил, пиразинил, пиридил и тетрагидропиранил.
Подходящие примеры таких конденсированных ароматических циклов включают в себя бензоконденсированные ароматические циклы, такие как хинолинил, изохинолинил, хиназолинил, хиноксалинил, циннолинил, нафтиридинил, индолил, индазолил, фуропиридинил, пирролопиридинил, бензофуранил, бензотиенил, бензимидазолил, бензоксазолил, бензизоксазолил, бензотиазолил, бензизотиазолил, бензоксадиазолил, бензотиадиазолил и т. п.
Предпочтительно R1 обозначает незамещенный -C3-7циклоалкил (например, циклобутил, циклопентил или циклогексил). Также предпочтительно, если R1 обозначает -C3-7циклоалкил (например, циклопентил), замещенный C1-3алкильной (например, метильной) группой.
Наиболее предпочтительно R1 обозначает незамещенный циклобутил или циклопентил, особенно незамещенный циклобутил.
Предпочтительно R2 обозначает
водород;
-C1-6алкил (например, метил или пропил), необязательно замещенный группой -CO2R4 или -CONR5R6;
-X-C3-8циклоалкил-Y-гетероциклил (например, -X-циклогексил-Y-морфолинил);
-X-арил (например, -X-фенил), необязательно замещенный одним или двумя атомами галогена (например, фтора, иода или хлора), группами C1-6алкил (например, метил), C1-6алкокси (например, метокси), -CO2R4,-CONR5R6, -NR5COR6, -SO2NR5R6 или циано;
-X-арил-Y-гетероциклил (например, -X-фенил-Y-пиперазинил, -X-фенил-Y-пирролидинил или -X-фенил-Y-морфолинил), необязательно замещенный одним или двумя =O, атомами галогена (например, фтора) или группами R4;
-X-гетероарил (например, -X-пиридинил, -X-пиразинил, -X-пиримидинил, -X-пиридазинил, -X-хинолинил, -X-пирролопиридинил, -X-фуропиридинил, -X-нафтиридинил, -X-тиазолил или -X-тиенил), необязательно замещенный одним или двумя атомами галогена (например, брома или иода), группами C1-6алкил (например, метил), C1-6алкокси (например, метокси или этокси), циано, нитро, -OR4, -COR4, -CO2R4, -NR5R6, -NR5COR6, -CONR5R6 или =O;
-X-гетероарил-Y-арил (например, -X-пиразинил-Y-фенил), необязательно замещенный группой C1-6алкилсульфонил (например, -SO2Me) или -NR5COR6;
-X-гетероарил-Y-гетероарил (например, -X-пиридинил-Y-пиразолил, -X-пиридинил-Y-оксадиазолил, -X-пиридинил-Y-оксазолил или -X-пиридинил-Y-пиразинил), необязательно замещенный группой C1-6алкил (например, метил);
-X-гетероарил-Y-гетероциклил (например, -X-пиридинил-Y-морфолинил, -X-пиридинил-Y-пирролидинил, -X-пиридинил-Y-пиперидинил, -X-пиридинил-Y-тиоморфолинил, -X-пиридинил-Y-тетрагидропиранил, -X-пиридинил-Y-имидазолидинил, -X-пиридинил-Y-тетрагидрооксазепинил, -X-пиридинил-Y-азетидинил, -X-пиридинил-Y-оксазолидинил, -X-пиридинил-Y-изотиазолидинил, -X-пиразинил-Y-морфолинил, -X-пиразинил-Y-пиперидинил, -X-пиразинил-Y-пирролидинил, -X-пиразинил-Y-тиоморфолинил, -X-пиразинил-Y-оксазолидинил, -X-пиразинил-Y-азетидинил, -X-пиразинил-Y-тетрагидропиранил или -X-пиридазинил-Y-морфолинил), необязательно замещенный одной или двумя группами =О, C1-6алкил (например, метил), -OR4 или галоген (например, хлор или бром);
-X-гетероциклил (например, -X-пиперидинил или -X-пирролидинил), необязательно замещенный группой C1-6алкилсульфонил (например, -SO2Me), C1-6алкоксикарбонил (например, -CO-CH2CH2OMe), -CO2R4, -COR4 или -COR5R6;
-X-гетероциклил-Y-арил (например, -X-пиперидинил-Y-фенил или -X-пирролидинил-Y-фенил), необязательно замещенный группой галоген (например, фтор), циано, C1-6алкилсульфонил (например, -SO2Me), R4 или -CONR5R6;
-X-гетероциклил-Y-гетероциклил (например, -X-пиперидинил-Y-тетрагидропиранил, -X-пирролидинил-Y-тетрагидропиранил, -X-пиперидинил-Y-дигидробензофуранил, -X-пирролидинил-Y-морфолинил, -X-пиперидинил-Y-морфолинил, -X-пиперидинил-Y-тиоморфолинил, -X-пиперидинил-Y-дигидроизоиндол, -X-пиперидинил-Y-пиперазинил, -X-пиперидинил-Y-пирролидинил, -X-пиперидинил-Y-пиперидинил или -X-пиперидинил-Y-дигидробензотиопиранил), необязательно замещенный одной или двумя группами =O или R4;
-X-гетероциклил-Y-C3-8циклоалкил (например, -X-пиперидинил-Y-циклогексил, -X-пиперидинил-Y-циклопропил, -X-пиперидинил-Y-циклобутил или -X-пиперидинил-Y-циклопентил) или
-X-гетероциклил-Y-гетероарил (например, -X-пиперидинил-Y-изохинолинил, -X-пиперидинил-Y-хинолинил, -X-пиперидинил-Y-изоксазолил, -X-пиперидинил-Y-бензотиазолил, -X-пиперидинил-Y-тиофенил, -X-пиперидинил-Y-фуранил, -X-пиперидинил-Y-пиразинил, -X-пиперидинил-Y-пиридил), необязательно замещенный одной или двумя группами C1-6алкил (например, метил), =O, циано или -CONR5R6.
Предпочтительно X обозначает связь или -CH2-, наиболее предпочтительно X обозначает связь.
Предпочтительно Y обозначает связь, CO, SO2 или -CO-CH=CH-, наиболее предпочтительно Y обозначает связь или CO, особенно связь.
Предпочтительно R4 обозначает водород, C1-6алкил (например, метил, этил или трет-бутил), -C1-6алкил-C3-8циклоалкил (например, -CH2-циклопропил), арил (например, фенил, необязательно замещенный атомом галогена (например, фтора)), гетероциклил (например, морфолинил) или гетероарил (например, пиридинил или пиразинил), необязательно замещенный группой галоген (например, фтор) или C1-6алкокси (например, метокси).
Предпочтительно R5 и R6 независимо обозначают водород, C1-6алкил (например, метил, этил, изопропил или пропил), -С3-8циклоалкил (например, циклобутил или циклопентил), -C1-6алкил-C3-8циклоалкил (например, -CH2-циклопропил), гетероциклил (например, пирролидинил, пиперидинил, морфолинил или тетрагидропиранил) или арил (например, фенил), необязательно замещенный группой галоген (например, фтор), циано или C1-6алкокси (например, метокси), или -NR5R6 обозначает гетероциклическую группу, содержащую азот (например, азетидинил, морфолинил, пирролидинил или пиперидинил), необязательно замещенную одной или двумя группами =O.
Более предпочтительно R5 и R6 независимо обозначают водород, C1-6 алкил (например, метил или этил), -C3-8циклоалкил (например, циклобутил или циклопентил) или -C1-6алкил-C3-8циклоалкил (например, -CH2-циклопропил).
Особенно предпочтительно R2 обозначает
водород;
-C1-6алкил (например, метил или пропил), необязательно замещенный группой -CO2R4 (например, -CO2Et или - CO2H) или -CONR5R6 (например, -CON(Me)2, -CON(H)(Me), -CON(H)(циклопентил), -CON(H)(фенил), -CO-пирролидинил, -CO-пиперидинил или -CO-морфолинил);
-X-C3-8циклоалкил-Y-гетероциклил (например, -циклогексил-CO-морфолинил);
-X-арил (например, -фенил или -CH2-фенил), необязательно замещенный одной или двумя группами галоген (например, фтор, иод или хлор), C1-6алкил (например, метил), C1-6алкокси (например, метокси), -CO2R4 (например, -CO2H или -CO2Me), -CONR5R6 (например, -CON(H)(Me), -CON(Et)2 (необязательно замещенной метоксигруппой), -CON(Me)(Pr) замещенной цианогруппой) или -CON(H)(-CH2-циклопропил), -NR5COR6 (например, -NHCOMe), -SO2NR5R6 (например, -SO2N(Et)2) или циано;
-X-арил-Y-гетероциклил (например, -фенилпирролидинил, -фенил-CO-пирролидинил, -фенил-CO-морфолинил, -фенил-SO2-морфолинил, -CH2-фенил-CO-пирролидинил, -CH2-фенил-CO-морфолинил или -CH2-фенил-CO-пиперазинил), необязательно замещенный одной или двумя группами =O, галоген (например, фтор) или R4 (например, фенил (необязательно замещенный атомом фтора) или пиридил);
-X-гетероарил (например, -пиридинил, -CH2-пиридинил, -пиразинил, -пиримидинил, -пиридазинил, -хинолинил, -CH2-хинолинил, -пирролопиридинил, -фуропиридинил, -нафтиридинил, -тиазолил или -тиенил), необязательно замещенный одной или двумя группами галоген (например, бром или иод), C1-6алкил (например, метил), C1-6алкокси (например, метокси или этокси), циано, нитро, -OR4 (например, гидрокси), -CO2R4 (например, CO2H или CO2Me), -COR4 (например, COMe), -NR5R6 (например, -NH2 или -N(H)(Me)), -NR5COR6 (например, NHCOMe, NHCO-i-Pr, -NHCO-пирролидинил, -NHCO-пиперидинил, -NHCO-морфолинил или -NHCO-тетрагидропиранил), -CONR5R6 (например, -CONH2, -CON(Me)2, -CON(Me)(Et), -CON(H)(Me), -CON(H)(i-Pr), -CON(Et)2 (необязательно замещенной метоксигруппой), -CON(H)(Et) (необязательно замещенной метоксигруппой), -CON(H)(-СН2циклопропил), -CON(H)(циклобутил), -CON(H)(циклопентил), -CON(H)(циклопропил) или -CON(H)(тетрагидропиранил)) или =O;
-X-гетероарил-Y-арил (например, -пиразинилфенил), необязательно замещенный группой C1-6алкилсульфонил (например, -SO2Me) или -NR5COR6 (например, -NHCOMe);
-X-гетероарил-Y-гетероарил (например, -пиридинилпиразолил, -пиридинилоксадиазолил, -пиридинилоксазолил или -пиридинилпиразинил), необязательно замещенный группой C1-6алкил (например, метил);
-X-гетероарил-Y-гетероциклил (например, -пиридинил-CO-морфолинил, -пиридинил-CO-пирролидинил, -пиридинил-CO-пиперидинил, -пиридинил-CO-тиоморфолинил, -пиридинилимидазолидинил, -пиридинил-CO-тетрагидрооксазепинил, -пиридинил-CO-азетидинил, -пиридинилоксазолидинил, -пиридинилизотиазолидинил, -пиразинилморфолинил, -пиразинил-CO-морфолинил, -пиразинил-CO-пиперидинил, -пиразинил-CO-пирролидинил, -пиразинилтиоморфолинил, -пиразинилоксазолидинил, -пиразинил-CO-азетидинил, -пиразинилпиперидинил, -пиразинилпирролидинил, -пиридинилпирролидинил, -пиридинилпиперидинил, -пиридинил-SO2-морфолинил или -пиридазинил-CO-морфолинил), необязательно замещенный одной или двумя группами =O, C1-6алкил (например, метил), -OR4 (например, гидрокси) или галоген (например, хлор или бром);
-X-гетероциклил (например, -пиперидинил, -CH2-пиперидинил, -пирролидинил или -CH2-пирролидинил), необязательно замещенный группой C1-6 алкилсульфонил (например, -SO2Me), C1-6 алкоксикарбонил (например, -CO-CH2CH2OMe), -CO2R4 (например, -CO2-t-Bu)-COR4 (например, -COCH2-циклопропил) или -COR5R6 (например, -CON(i-Pr)2, -CON(Et)2, -CON(i-Pr)(Et) (замещенный метоксильной группой), -CON(H)(i-Pr) или -CON(H)(4-фторфенил);
-X-гетероциклил-Y-арил (например, -пиперидинил-CO-фенил, -пирролидинил-CO-фенил, -пиперидинил-CO-CH=CH-фенил, -пиперидинил-SO2-фенил, пирролидинил-SO2-фенил, -CH2-пиперидинил-CO-фенил, -CH2-пирролидинил-CO-фенил, -CH2-пиперидинил-SO2-фенил или -CH2-пирролидинил-SO2-фенил), необязательно замещенный группой галоген (например, фтор), циано, C1-6алкилсульфонил (например, -SO2Me), R4 (например, фенил или морфолинил) или -CONR5R6 (например, -CO-пирролидинил, замещенный группой =O);
-X-гетероциклил-Y-гетероциклил (например, -пиперидинил-CO-тетрагидропиранил, -CH2-пиперидинил-CO-тетрагидропиранил, пирролидинил-CO-тетрагидропиранил, CH2-пирролидинил-CO-тетрагидропиранил, пиперидинил-CO-дигидробензофуранил, пирролидинил-CO-морфолинил,-CH2-пирролидинил-CO-морфолинил, -пиперидинил-CO-морфолинил, CH2-пиперидинил-CO-морфолинил, пиперидинил-CO-тиоморфолинил, пиперидинил-CO-дигидроизоиндол, пиперидинил-CO-пиперазинил, пиперидинил-CO-пирролидинил, пиперидинил-CO-пиперидинил или пиперидинил-CO-дигидробензотиопиранил), необязательно замещенный одной или двумя группами =O, или R4 (например, пиразинил);
-X-гетероциклил-Y-C3-8циклоалкил (например, -пиперидинил-CO-циклогексил, -пиперидинил-CO-циклопропил, -пиперидинил-CO-циклобутил или -пиперидинил-CO-циклопентил);
или -X-гетероциклил-Y-гетероарил (например, -пиперидинил-CO-изохинолинил, -пиперидинил-CO-хинолинил, -пиперидинил-CO-изоксазолил, -пиперидинил-SO2-изоксазолил, -пиперидинил-CO-бензотиазолил, -пиперидинил-CO-тиофенил, -пиперидинил-CO-фуранил, -пиперидинил-CO-пиразинил, -пиперидинилпиразинил, -пиперидинил-CO-пиридинил или -пиперидинилпиридинил), необязательно замещенный одной или двумя группами C1-6алкил (например, метил), =O, циано или -CONR5R6 (например, -CON(H)(Me), -CON(H)(-СН2циклопропил), -CO-азетидинил или -CO-морфолинил).
Более предпочтительно, R2 обозначает
-X-арил (например, фенил), необязательно замещенный группой CONR5R6;
-X-арил-Y-гетероциклил (например, -X-фенил-Y-морфолинил или -X-фенил-Y-пирролидинил);
-X-гетероарил (например, пиразинил или пиридинил), необязательно замещенный группой CONR5R6;
-X-гетероарил-Y-гетероциклил (например, -X-пиридинил-Y-морфолинил, -X-пиридинил-Y-пирролидинил, -X-пиридинил-Y-пиперидинил, -X-пиридинил-Y-тиоморфолинил, -X-пиразинил-Y-морфолинил, -X-пиразинил-Y-пиперидинил или -X-пиразинил-Y-пирролидинил), необязательно замещенный одной или двумя группами =O; или
-X-гетероциклил-Y-гетероциклил (например, -X-пиперидинил-Y-тетрагидропиранил, -X-пиперидинил-Y-морфолинил или -X-пирролидинил-Y-морфолинил).
Еще более предпочтительно R2 обозначает
-X-арил (например, -фенил или -CH2-фенил), необязательно замещенный одной или двумя группами галоген (например, фтор, иод или хлор), C1-6алкил (например, метил), C1-6алкокси (например, метокси), -CO2R4 (например, -CO2H или -CO2Me), -CONR5R6 (например, -CON(H)(Me), -CON(Et)2 (необязательно замещенный метоксильной группой), -CON(Me)(Et), замещенный цианогруппой) или -CON(H)(-CH2-циклопропил), -NR5COR6 (например, -NHCOMe), -SO2NR5R6 (например, -SO2N(Et)2) или циано;
-X-арил-Y-гетероциклил (например, -фенилпирролидинил, -фенил-CO-пирролидинил, -фенил-CO-морфолинил, -фенил-SO2-морфолинил, -CH2-фенил-CO-пирролидинил, -CH2-фенил-CO-морфолинил или -CH2-фенил-CO-пиперазинил), необязательно замещенный одной или двумя группами =O, галоген (например, фтор) или R4 (например, фенил (необязательно замещенный атомом фтора) или пиридил);
-X-гетероарил (например, -пиридинил, -CH2-пиридинил, -пиразинил, -пиримидинил, -пиридазинил, -хинолинил, -CH2-хинолинил, -пирролопиридинил, -фуропиридинил, -нафтиридинил, -тиазолил или -тиенил), необязательно замещенный одной или двумя группами галоген (например, бром или иод), C1-6алкил (например, метил), C1-6алкокси (например, метокси или этокси), циано, нитро, -OR4 (например, гидрокси), -CO2R4 (например, CO2H или CO2Me), -COR4 (например, COMe), -NR5R6 (например, -NH2 или -N(H)(Me)), -NR5COR6 (например, NHCOMe, NHCO-i-Pr, -NHCO-пирролидинил, -NHCO-пиперидинил, -NHCO-морфолинил или -NHCO-тетрагидропиранил), -CONR5R6 (например, -CONH2, -CON(Me)2, -CON(Me)(Et), -CON(H)(Me), -CON(H)(i-Pr), -CON(Et)2 (необязательно замещенный метоксильной группой), -CON(H)(Et) (необязательно замещенный метоксильной группой), -CON(H)(-CH2-циклопропил), -CON(H)(циклобутил), -CON(H)(циклопентил), -CON(H)(циклопропил) или -CON(H)(тетрагидропиранил)) или =O;
-X-гетероарил-Y-гетероциклил (например, -пиридинил-CO-морфолинил, -пиридинил-CO-пирролидинил, -пиридинил-CO-пиперидинил, -пиридинил-CO-тиоморфолинил, -пиридинилимидазолидинил, -пиридинил-CO-тетрагидрооксазепинил, -пиридинил-CO-азетидинил, -пиридинилоксазолидинил, -пиридинилизотиазолидинил, -пиразинилморфолинил, -пиразинил-CO-морфолинил, -пиразинил-CO-пиперидинил, -пиразинил-CO-пирролидинил, -пиразинилтиоморфолинил, -пиразинилоксазолидинил, -пиразинил-CO-азетидинил, -пиразинилпиперидинил, -пиразинилпирролидинил, -пиридинилпирролидинил, -пиридинилпиперидинил, -пиридинил-SO2-морфолинил или -пиридазинил-CO-морфолинил), необязательно замещенный одной или двумя группами =O, C1-6алкил (например, метил), -OR4 (например, гидрокси) или галоген (например, хлор или бром); или
-X-гетероциклил-Y-гетероциклил (например, -пиперидинил-CO-тетрагидропиранил, -CH2-пиперидинил-CO-тетрагидропиранил, -пирролидинил-CO-тетрагидропиранил, -CH2-пирролидинил-CO-тетрагидропиранил, -пиперидинил-CO-дигидробензофуранил, -пирролидинил-CO-морфолинил, -CH2-пирролидинил-CO-морфолинил, -пиперидинил-CO-морфолинил, -CH2-пиперидинил-CO-морфолинил, -пиперидинил-CO-тиоморфолинил, -пиперидинил-CO-дигидроизоиндол, -пиперидинил-CO-пиперазинил, -пиперидинил-CO-пирролидинил, -пиперидинил-CO-пиперидинил или -пиперидинил-CO-дигидробензотиопиранил), необязательно замещенный одной или двумя группами =O или R4 (например, пиразинил).
Наиболее предпочтительно R2 обозначает
-X-арил (например, -фенил), необязательно замещенный одной или двумя группами галоген (например, фтор), C1-6алкокси (например, метокси), -CONR5R6 (например, -CON(H)(Me)), -NR5COR6 (например, -NHCOMe) или циано;
-X-арил-Y-гетероциклил (например, -фенилпирролидинил), необязательно замещенный одной или двумя группами =O или галоген (например, фтор);
незамещенный -X-гетероциклил-Y-гетероциклил (например, -пиперидинил-CO-морфолинил);
-X-гетероарил (например, -2-пиридинил или -2-пиразинил), необязательно замещенный группой -CONR5R6 (например, CON(H)(Me)); или
-X-гетероарил-Y-гетероциклил (например, -2-пиридинил-N-пирролидинил), где указанная гетероциклическая группа необязательно замещена группой =O (например, -2-пиридинил-N-пирролидинон).
Особенно предпочтительно R2 обозначает -X-гетероарил (например, -2-пиридинил), замещенный группой -CONR5R6 (например, 4-метиламинокарбонилпиридин-2-ил).
Предпочтительно n обозначает 0 или 1, более предпочтительно 0.
Если n обозначает 1, R3 предпочтительно обозначает атом галогена (например, иод) или цианогруппу.
Предпочтительные соединения данного изобретения включают в себя примеры E1-E288, как показано ниже, или их фармацевтически приемлемые соли.
Более предпочтительные соединения данного изобретения включают в себя
метиламид 5-(3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илокси)пиразин-2-карбоновой кислоты; и
1-{6-[(3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-пиридинил}-2-пирролидон
или их фармацевтически приемлемые соли.
Особенно предпочтительным соединением данного изобретения является 6-(3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илокси)-N-метилникотинамид или его фармацевтически приемлемая соль.
Соединения формулы (I) могут образовывать кислотно-аддитивные соли с традиционными фармацевтически приемлемыми кислотами, такими как малеиновая, хлористоводородная, бромистоводородная, фосфорная, уксусная, фумаровая, салициловая, серная, лимонная, молочная, миндальная, виннокаменная и метансульфоновая. Таким образом, соли, сольваты и гидраты соединений формулы (I) составляют аспект данного изобретения.
Некоторые соединения формулы (I) могут существовать в стереоизомерных формах. Следует понимать, что данное изобретение охватывает все геометрические и оптические изомеры данных соединений, а также их смеси, включая рацематы. Таутомеры также составляют аспект данного изобретения.
Настоящее изобретение также предлагает способ получения соединения формулы (I) или его фармацевтически приемлемой соли, данный способ включает в себя
(a) взаимодействие соединения формулы (II)
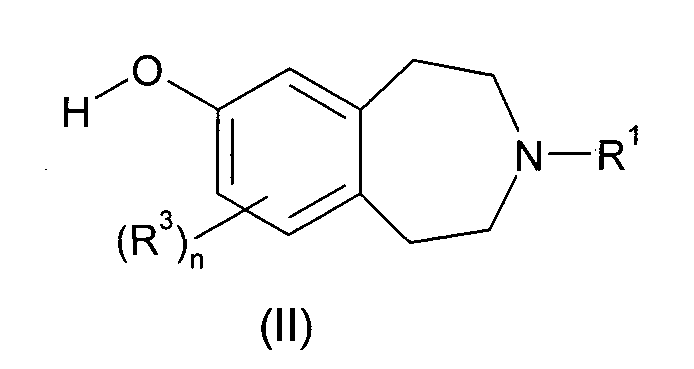
где R1, R3 и n такие, как определено выше, с соединением формулы R2'-L1, где R2' такой, как определено выше для R2, или представляет собой группу, которая способна превратиться в R2, а L1 обозначает подходящую уходящую группу, такую как атом галогена (например, бром или иод) или необязательно активированная гидроксильная группа;
(b) взаимодействие соединения формулы (III)
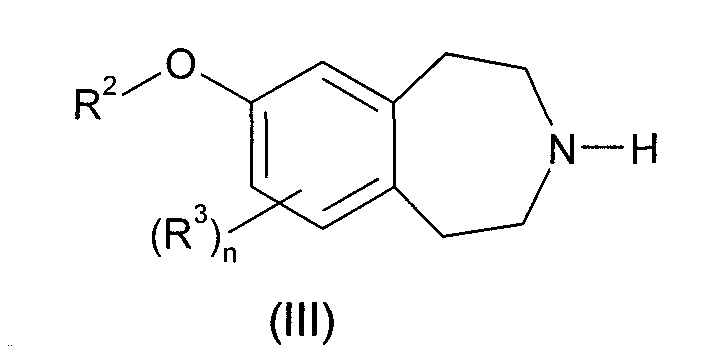
где R2, R3 и n такие, как определено выше, с соединением формулы R1'-L2, где R1' такой, как определено выше для R1, или представляет собой группу, которая способна превратиться в R1, а L2 обозначает подходящую уходящую группу, такую как атом галогена (например, бром, иод или тозилат); или
(c) взаимодействие соединения формулы (III), как определено выше, с кетоном формулы R1'=O, где R1' такой, как определено выше для R1, или представляет собой группу, которая способна превратиться в R1; или
(d) удаление защитной группы с защищенного соединения формулы (I) и
(e) взаимопревращение в другие соединения формулы (I).
Если уходящая группа L1 присоединена к атому углерода в состоянии sp3-гибридизации, например, если R2'-L1 обозначает алкилгалогенид, процесс (a), как правило, включает в себя применение подходящего основания, такого как карбонат калия, в подходящем растворителе, таком как 2-бутанон, необязательно в присутствии катализатора, такого как иодид калия, при подходящей температуре, такой как температура кипения с обратным холодильником.
Если уходящая группа L1 присоединена к атому углерода в состоянии sp2-гибридизации, например, если R2'-L1 обозначает арилгалогенид, процесс (a), как правило, включает в себя применение соли меди (I), такой как иодид меди (I), в присутствии такого основания, как гидрид натрия, в подходящем растворителе, таком как пиридин, при подходящей температуре, такой как температура кипения с обратным холодильником.
Если уходящая группа L1 присоединена к активированному атому углерода в состоянии sp2-гибридизации, например, если R2'-L1 обозначает гетероарилгалогенид, такой как 2-хлорпиридин или 2-хлорпиразин, процесс (a), как правило, включает в себя применение подходящего основания, такого как гидрид натрия, в подходящем растворителе, таком как диметилформамид или диметилсульфоксид, при подходящей температуре. Альтернативно можно использовать трет-бутоксид калия в трет-бутаноле при подходящей температуре.
Если уходящая группа L1 присоединена к активированному атому углерода в состоянии sp2-гибридизации, например, если R2'-L1 обозначает арилгалогенид, такой как 3,4-дифторбензонитрил, процесс (a), как правило, включает в себя применение подходящего основания, карбоната калия, в подходящем растворителе, таком как диметилсульфоксид, при подходящей температуре.
Если L1 обозначает гидроксильную группу, присоединенную к атому углерода в состоянии sp3-гибридизации, например, если R2'-L1 обозначает спирт, процесс (a), как правило, включает в себя применение фосфина, такого как трифенилфосфин, в подходящем растворителе, таком как тетрагидрофуран, с последующим добавлением азодикарбоксилата, такого как диэтилазодикарбоксилат, при подходящей температуре, такой как комнатная температура.
Процесс (b), как правило, включает применение подходящего основания, такого как карбонат калия, в подходящем растворителе, таком как 2-бутанон, необязательно в присутствии катализатора, такого как иодид калия, при подходящей температуре, такой как температура кипения с обратным холодильником.
Процесс (c), как правило, включает применение восстанавливающих условий (таких как обработка боргидридом, например, триацетоксиборгидридом натрия), необязательно в присутствии кислоты, такой как уксусная кислота, в подходящем растворителе, таком как дихлорметан, при подходящей температуре, такой как комнатная температура.
Что касается процесса (d), примеры защитных групп и способы их удаления можно найти в T. W. Greene 'Protective Groups in Organic Synthesis' (J. Wiley and Sons, 1991). Подходящие защитные группы для аминогруппы включают в себя сульфонил (например, тозил), ацил (например, ацетил, 2',2',2'-трихлорэтоксикарбонил, бензилоксикарбонил или трет-бутоксикарбонил) и арилалкил (например, бензил), которые можно удалить гидролизом (например, используя такую кислоту, как хлористоводородная в диоксане, или трифторуксусная в дихлорметане), или восстановлением (например, гидрированием бензильной группы, или, в случае 2',2',2'-трихлорэтоксикарбонильной группы, восстановлением цинком в уксусной кислоте) соответственно. Другие подходящие защитные группы для аминогруппы включают в себя трифторацетил (-COCF3), который можно удалить гидролизом, катализируемым основанием, или с использованием в качестве твердой фазы смолы с иммобилизованной бензильной группой, такой как смола Merrifield, связанная с 2,6-диметоксибензильной группой (линкер Ellman), которую можно удалить кислым гидролизом, например, с помощью трифторуксусной кислоты.
Процесс (e) можно проводить с использованием традиционных методов взаимопревращения, таких как эпимеризация, окисление, восстановление, алкилирование, нуклеофильное или электрофильное замещение в ароматическом ядре, гидролиз сложного эфира, образование амидной связи или реакции сочетания, опосредованные переходным металлом. Примеры реакций сочетания, катализируемых переходными металлами и используемых в качестве способов взаимопревращения, включают в себя следующие: катализируемые палладием реакции сочетания электрофилов, таких как арилгалогениды, с металлорганическими реагентами, например борными кислотами (реакции перекрестного сочетания Сузуки (Suzuki)); катализируемые палладием реакции аминирования и амидирования органических электрофилов, таких как арилгалогениды, проводимые с использованием таких нуклеофилов, как амины и амиды; катализируемые медью реакции амидирования органических электрофилов (таких как арилгалогениды), проводимые с использованием таких нуклеофилов, как амиды; и катализируемые медью реакции сочетания фенолов с борными кислотами.
Соединения формул (II) и (III) можно получить по следующей схеме:
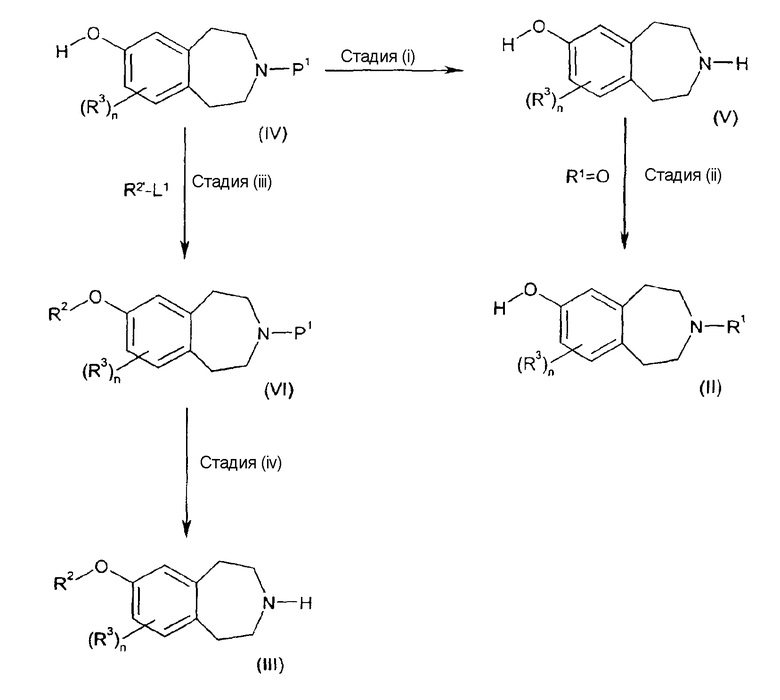
где R1, R2, R2', R3, n и L1 такие, как определено выше, а P1 обозначает подходящую защитную группу, такую как Boc.
Стадия (i), как правило, включает в себя реакцию удаления защитной группы, например если P1 обозначает Boc, реакция удаления защитной группы включает в себя взаимодействие соединения формулы (IV) с кислотой, например хлористоводородной кислотой в диоксане или трифторуксусной кислотой в дихлорметане.
Стадию (ii) можно проводить в восстанавливающих условиях, как описано для процесса (c).
Стадию (iii) можно проводить по способу, описанному для процесса (a).
Стадия (iv), как правило, включает в себя реакцию удаления защитной группы с получением соединения формулы (III) и может проводиться в соответствии со способом стадии (i).
Соединения формулы (VI), где R2 обозначает -X-арил, -X-гетероарил, -X-арил-Y-C3-8циклоалкил, -X-арил-Y-арил, -X-арил-Y-гетероарил, -X-арил-Y-гетероциклил, -X-гетероарил-Y-C3-8циклоалкил, -X-гетероарил-Y-арил, -X-гетероарил-Y-гетероарил или -X-гетероарил-Y-гетероциклил, а X обозначает связь, могут быть также получены по следующей схеме:
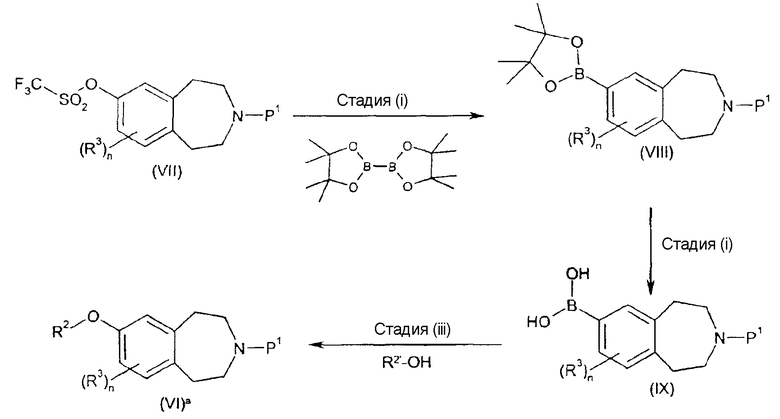
где R2, R2', R3 и n такие, как определено выше, а P1 обозначает подходящую защитную группу, такую как Boc.
Стадию (i) можно проводить в условиях перекрестного сочетания, катализируемого палладием, например, с использованием в качестве каталитической системы комплекса бис(дифенилфосфино)ферроцендихлорпалладия(II) и
1,1'-бис(дифенилфосфино)ферроцена, в сочетании с подходящим основанием, таким как ацетат калия, в подходящем растворителе, например в диоксане, при подходящей температуре, например при температуре кипения с обратным холодильником.
Стадию (ii) можно проводить в окисляющих условиях, например, с использованием периодата натрия в присутствии ацетата аммония, в подходящей системе растворителей, такой как ацетон и вода, при подходящей температуре, например при комнатной температуре.
Стадию (iii) можно проводить в присутствии соли меди, например ацетата меди, в сочетании с подходящим основанием, таким как триэтиламин, с использованием молекулярных сит, в подходящем растворителе, например дихлорметане, при подходящей температуре, например при комнатной температуре.
Соединения формулы (IV) можно получить по способу, приведенному в описании 3 WO 02/40471.
Соединения формулы (VII) можно получить по способу, описанному в Bioorg. Med. Chem. Lett.; 10; 22; 2000; 2553-2556.
Соединения формулы (I) и их фармацевтически приемлемые соли обладают сродством к рецептору гистамина H3, являются антагонистами и/или обратными агонистами указанного рецептора и предположительно могут применяться для лечения неврологических заболеваний, включающих в себя болезнь Альцгеймера, деменцию, старческое расстройство памяти, легкое ухудшение познавательной способности, нарушение познавательной способности, эпилепсию, невропатическую боль, воспалительную боль, мигрень, болезнь Паркинсона, рассеянный склероз, удар и нарушение сна, включая нарколепсию; психиатрических заболеваний, включающих шизофрению (особенно нарушение познавательной способности при шизофрении), синдром дефицита внимания с гиперактивностью, депрессию и привыкание; а также других заболеваний, включающих ожирение, астму, аллергический ринит, заложенность носа, хроническое обструктивное заболевание легких и желудочно-кишечные заболевания.
Следовательно, данное изобретение также относится к соединению формулы (I) или его фармацевтически приемлемой соли для применения в качестве терапевтического средства для лечения или профилактики вышеуказанных заболеваний, особенно нарушения познавательной способности при таких заболеваниях, как болезнь Альцгеймера и родственные нейродегенеративные нарушения.
Далее, данное изобретение относится к способу лечения или профилактики вышеуказанных заболеваний у млекопитающих, в том числе у людей, который включает в себя введение пациенту терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли.
В другом аспекте данное изобретение относится к применению соединения формулы (I) или его фармацевтически приемлемой соли в производстве лекарственного средства для лечения вышеуказанных заболеваний.
Для применения в терапевтических целях соединения формулы (I) обычно вводят в состав стандартной фармацевтической композиции. Такие композиции можно получить с помощью стандартных методов.
Следовательно, настоящее изобретение также относится к фармацевтической композиции для лечения вышеуказанных заболеваний, которая содержит соединение формулы (I) или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель.
Далее, настоящее изобретение относится к фармацевтической композиции, которая содержит соединение формулы (I) или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель.
Соединения формулы (I) можно использовать в комбинации с другими терапевтическими средствами, например с антагонистами гистамина H1, или с медикаментами, заявленными как средства для облегчения или симптоматического лечения болезни Альцгеймера. Подходящими примерами упомянутых других терапевтических средств могут служить средства, которые, как известно, изменяют холинергическую передачу, такие как антагонисты 5-HT6, мускариновые агонисты M1, мускариновые антагонисты M2 или ингибиторы ацетилхолинестеразы. Если соединения используются в комбинации с другими терапевтическими средствами, их можно вводить последовательно или одновременно любым подходящим способом.
Таким образом, в следующем аспекте данное изобретение относится к комбинации соединения формулы (I) или его фармацевтически приемлемого производного с другим терапевтическим средством или другими терапевтическими средствами.
Упомянутые выше комбинации удобно использовать в виде фармацевтической композиции, и, следовательно, фармацевтические композиции, содержащие указанную выше комбинацию вместе с фармацевтически приемлемым носителем или наполнителем, составляют следующий аспект данного изобретения. Отдельные компоненты таких сочетаний можно вводить последовательно или одновременно в разных фармацевтических композициях или в одной фармацевтической композиции.
Если соединение формулы (I) или его фармацевтически приемлемое производное используется в сочетании с другим терапевтическим средством, активным против того же заболевания, доза каждого соединения может отличаться от дозы, используемой в случае применения одного соединения. Специалисты в данной области могут легко определить нужную дозу.
Фармацевтическую композицию данного изобретения, которую можно получить путем смешивания, обычно при температуре окружающей среды и атмосферном давлении, как правило, модифицируют для перорального, парентерального или ректального введения, и, как таковая, она может находиться в виде таблеток, капсул, жидких препаратов для перорального применения, порошков, гранул, пастилок, порошков для разбавления, растворов или суспензий для инъекций или инфузий или свечей. Как правило, предпочтительными являются композиции для перорального введения.
Таблетки и капсулы для перорального введения могут находиться в виде стандартной лекарственной формы и могут содержать традиционные наполнители, такие как связующие средства, наполнители, смазывающие средства, используемые для получения таблеток, дезинтегрирующие средства и приемлемые увлажняющие средства. Таблетки могут быть покрыты в соответствии со способами, хорошо известными в обычной фармацевтической практике.
Жидкие препараты для перорального применения могут находиться в виде, например, водных или масляных суспензий, растворов, эмульсий, сиропов или эликсиров, или они могут находиться в виде сухого продукта для разбавления водой или другой подходящей средой перед применением. Такие жидкие препараты могут содержать традиционные добавки, такие как суспендирующие средства, эмульгирующие средства, неводные среды (которые могут содержать пищевые масла), консерванты и, при желании, традиционные ароматизаторы или красители.
Жидкие стандартные лекарственные формы для парентерального введения получают, используя соединение данного изобретения или его фармацевтически приемлемую соль и стерильную среду. В зависимости от используемых среды и концентрации соединение может быть либо суспендированным, либо растворенным в среде. При получении растворов соединение можно растворить с получением раствора для инъекции, который стерилизуют с помощью фильтра, затем наполняют им подходящие флаконы или ампулы и герметично закрывают их. Предпочтительно в среде растворяют вспомогательные средства, такие как местные анестезирующие средства, консерванты и забуферивающие средства. Для увеличения стабильности после заполнения флаконов и удаления воды под вакуумом композицию можно заморозить. Суспензии для парентерального введения получают по существу таким же способом, за исключением того, что соединение не растворяют, а суспендируют в среде, и стерилизацию нельзя проводить путем фильтрации. Соединение можно стерилизовать путем воздействия этиленоксида перед суспендированием в стерильной среде. Чтобы обеспечить однородное распределение соединения, предпочтительно в состав композиции вводят поверхностно-активное вещество или увлажняющее средство.
Композиция может содержать от 0,1% до 99% по массе, предпочтительно от 10 до 60% по массе активного вещества, в зависимости от способа введения. Доза соединения, используемого для лечения вышеупомянутых заболеваний, как правило, варьируется в зависимости от тяжести заболевания, массы пациента и других факторов. Однако, в общем случае, подходящие разовые дозы могут составлять от 0,05 до 1000 мг, более предпочтительно от 1,0 до 200 мг, причем такие разовые дозы можно вводить более одного раза в день, например два или три раза в день. Такое лечение может продолжаться несколько недель или месяцев.
Нижеследующие описания и примеры иллюстрируют получение соединений данного изобретения.
Описание 1
Трет-бутиловый эфир 7-бензилокси-1,2,4,5-тетрагидробензо[d]азепин-3-карбоновой кислоты (D1)
Трет-бутиловый эфир 7-гидрокси-1,2,4,5-тетрагидробензо[d]азепин-3-карбоновой кислоты (PCT Int. Appl. (2002), WO 02/40471) (790 мг, 3 ммоль), карбонат калия (1,24 г, 9 ммоль) и катализатор иодид калия суспендируют в 2-бутаноне (20 мл). Добавляют бензилбромид (536 мкл, 4,5 ммоль) и смесь нагревают с обратным холодильником 24 часа. Твердые вещества фильтруют и затем промывают ацетоном. Фильтрат концентрируют в вакууме и неочищенное масло очищают колоночной хроматографией, элюируя смесью этилацетата и гексана (1:4), получая указанное в заголовке соединение (D1) (1,06 г, 100%), 1H ЯМР (CDCl3) 7,44 (5H, м), 7,03 (1H, д, J=8,1 Гц), 6,77 (1H, с), 6,74 (1H, дд, J=8,1 и 2,4 Гц), 3,49 (4H, м), 2,84 (4H, м), 1,48 (9H, с).
Описание 2
7-Бензилокси-1,2,4,5-тетрагидробензо[d]азепин (D2)
Трет-бутиловый эфир 7-бензилокси-1,2,4,5-тетрагидробензо[d]азепин-3-карбоновой кислоты (D1) (1,06 г, 3 ммоль) растворяют в дихлорметане (15 мл) и обрабатывают трифторуксусной кислотой (15 мл). Раствор перемешивают при комнатной температуре 2 часа, концентрируют в вакууме и затем дважды упаривают с дихлорметаном. Остаток растворяют в метаноле, наносят на ионообменную колонку SCX (Varian bond-elute, 10 г) и промывают сначала метанолом, затем смесью 0,880 аммиак/метанол. Объединенные основные фракции упаривают в вакууме и остаток очищают колоночной хроматографией, элюируя смесью 0,880 аммиак:этанол:дихлорметан (1:9:90), получая указанное в заголовке соединение (D2) (702 мг, 93%), МС (ES+) m/e 254 [M+H]+.
Описание 3
Трет-бутиловый эфир 7-(4-метоксикарбонилбензилокси)-1,2,4,5-тетрагидробензо[d]азепин-3-карбоновой кислоты (D3)
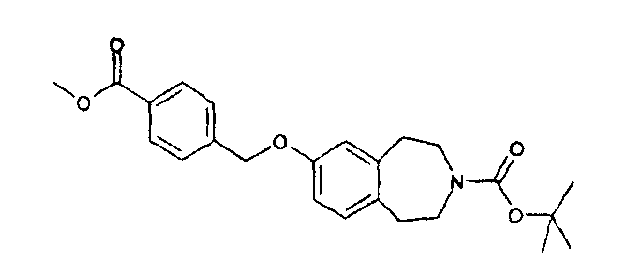
Трет-бутиловый эфир 7-гидрокси-1,2,4,5-тетрагидробензо[d]азепин-3-карбоновой кислоты (WO 02/40471) (5,27 г, 20,0 ммоль), карбонат калия (8,30 г, 60,0 ммоль) и катализатор иодид калия суспендируют в бутаноне (100 мл). Добавляют по каплям метил 4-(бромметил)бензоат (5,5 г, 24,0 ммоль), растворенный в бутаноне (50 мл), после чего реакционную смесь перемешивают с обратным холодильником в течение 24 часов. Реакционную смесь охлаждают, твердые вещества фильтруют и затем промывают ацетоном. Фильтрат концентрируют в вакууме и неочищенную смесь очищают колоночной хроматографией, элюируя смесью этилацетат:гексан (1:4), и получают указанное в заголовке соединение (D3). МС (ES+) m/e 344[(M+H)-CO2 tBu]+.
Описание 4
Метиловый эфир 4-(2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илоксиметил)бензойной кислоты (D4)
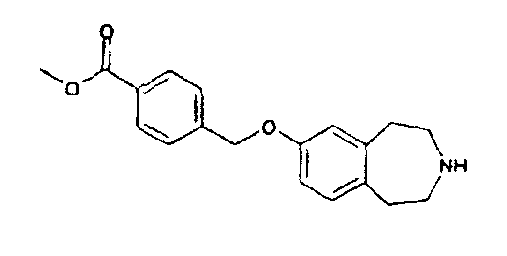
Трет-бутиловый эфир 7-(4-метоксикарбонилбензилокси)-1,2,4,5-тетрагидробензо[d]азепин-3-карбоновой кислоты (D3) (6,35 г) растворяют в дихлорметане (30 мл) и обрабатывают трифторуксусной кислотой (30 мл). Раствор перемешивают при комнатной температуре 2 часа, концентрируют в вакууме и затем дважды упаривают с дихлорметаном. Остаток растворяют в дихлорметане и промывают 10% водным раствором гидроксида натрия, водой и насыщенным соляным раствором. Органический слой сушат над сульфатом магния, фильтруют и концентрируют в вакууме, получая указанное в заголовке соединение (D4).
Описание 5
1-(6-Хлорпиридин-3-ил)-1-морфолин-4-илметанон (D5)

Морфолин (0,2 мл, 2,2 ммоль) добавляют к перемешиваемому раствору 6-хлорникотиноилхлорида (250 мг, 1,4 ммоль) в дихлорметане (10 мл). Через 2 часа реакционную смесь оставляют охлаждаться, неочищенную смесь наносят на ионообменный картридж SCX (Varian bond-elute, 10 г) и промывают метанолом. Метанольные фракции концентрируют в вакууме, получая указанное в заголовке соединение (D5).
Описания 6-31
Соединения описаний 6-31 (D6-D31) получают по способу описания 5 (D5) из соответствующих арилгалогенидов и аминов, указанных в таблице, и используют их без дополнительной характеристики:
метиламин
Описание 32
5-Бром-2-(1-пиперидинил)пиримидин (D32)
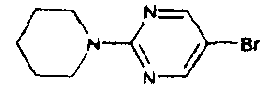
Пиперидин (5,1 мл, 51,6 ммоль) добавляют к перемешиваемому раствору 5-бром-2-хлорпиримидина (5 г, 25,8 ммоль) и триэтиламина (9,0 мл, 64,5 ммоль) в толуоле (30 мл). После перемешивания при комнатной температуре в течение 24 часов реакционную смесь разбавляют этилацетатом и промывают 2N раствором хлористоводородной кислоты, насыщенным соляным раствором и сушат (сульфат магния). Органический слой фильтруют, концентрируют в вакууме, полученный остаток очищают колоночной хроматографией, элюируя этилацетатом, и получают указанное в заголовке соединение (D32).
Описания 33-35
Соединения описаний 33-35 (D33-D35) получают по способу описания 32 (D32), заменяя пиперидин на соответствующий амин, указанный в таблице:
Описания 36-37
Соединения описаний 36-37 (D36-D37) получают по способу описания 5 (D5), заменяя морфолин на соответствующий амин, указанный в таблице:
Описание 38
5-Бром-2-пиримидинкарбонитрил (D38)
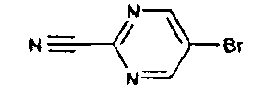
Цианид натрия (2,30 г, 46,6 ммоль) растворяют в диметилформамиде (60 мл) и обрабатывают 5-бром-2-хлорпиримидином (6,0 г, 31,1 ммоль). Полученную смесь перемешивают при комнатной температуре 18 часов, разбавляют водой и экстрагируют дихлорметаном. Дихлорметановые экстракты объединяют, промывают водой, сушат (сульфат магния), фильтруют и концентрируют в вакууме. Неочищенный продукт очищают колоночной хроматографией, элюируя смесью этилацетат:гексан (1:4), и получают указанное в заголовке соединение (D38).
Описание 39
1,1-Диметилэтил 7-({5-[(метиламино)карбонил]-2-пиридинил}окси)-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилат (D39)
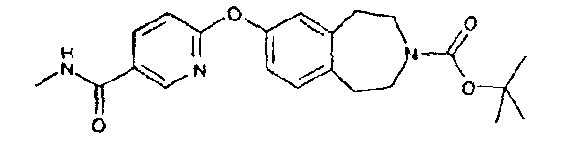
Трет-бутиловый эфир 7-гидрокси-1,2,4,5-тетрагидробензо[d]азепин-3-карбоновой кислоты (PCT Int. Appl. (2002), WO 02/40471) (8,7 г, 33 ммоль) растворяют в трет-бутаноле и обрабатывают трет-бутоксидом калия (4 г, 36 ммоль). После перемешивания в течение 30 минут при комнатной температуре добавляют 6-хлор-N-метилникотинамид (D10) (5,1 г, 30 ммоль) и реакционную смесь перемешивают при температуре кипения с обратным холодильником 20 часов. Реакционную смесь охлаждают до комнатной температуры и концентрируют в вакууме. К неочищенному остатку добавляют воду со льдом, что приводит к выпадению осадка, который собирают фильтрацией. Твердый осадок растворяют в этилацетате, промывают насыщенным соляным раствором и сушат (сульфат магния). Органический слой фильтруют, концентрируют в вакууме, полученный остаток очищают колоночной хроматографией, элюируя смесью этилацетат:гексан (1:1), и получают указанное в заголовке соединение (D39). 1H ЯМР (CDCl3) 8,52 (1H, д, J=2,4), 8,12 (1H, дд, J=8,8), 7,16 (1H, м), 6,95-6,81 (3H, м), 6,02 (1H, ушир.), 3,57 (4H, ушир.), 3,02 (3H, д, J=2,4), 2,89 (4H, ушир.), 1,49 (9H, с).
Описание 40
N-Метил-6-(2,3,4,5-тетрагидро-1H-3-бензазепин-7-илокси)-3-пиридинкарбоксамид (D40)
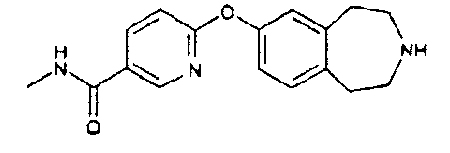
1,1-Диметилэтил 7-({5-[(метиламино)карбонил]-2-пиридинил}окси)-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилат (D39) (3,98 г, 10 ммоль) растворяют в диоксане (40 мл) и обрабатывают 4M раствором хлористого водорода в диоксане (35 мл). Реакционную смесь оставляют перемешиваться при комнатной температуре в течение 6 часов и затем концентрируют в вакууме, получая указанное в заголовке соединение (D40); MS (ES+) m/e 298 [M+H]+.
Описание 41
1,1-Диметилэтил 7-гидрокси-8-иод-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилат (D41)
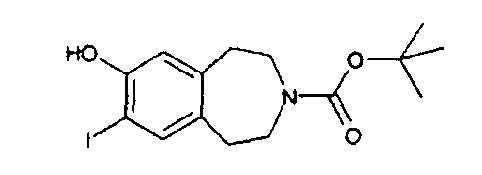
Раствор трет-бутилового эфира 7-гидрокси-1,2,4,5-тетрагидро-3H-бензо[d]азепин-3-карбоновой кислоты (PCT Int. Appl. (2002), WO 02/40471) (5,2 г, 20 ммоль) в 33% метиламине в этаноле (30 мл) перемешивают при 0°C. Раствор иодида натрия (4,6 г, 30 ммоль) и иода (5,2 г, 20 ммоль) в воде (30 мл) добавляют ниже поверхности реакционной смеси. После перемешивания при 0°C в течение 1 часа смесь концентрируют в вакууме. Остаток разбавляют этилацетатом и водой. Органический слой отделяют, промывают водой и насыщенным соляным раствором. Органический слой сушат над сульфатом магния, фильтруют и концентрируют в вакууме, получая указанное в заголовке соединение (D41); (7,0 г, 90%), 1H ЯМР (d6-ДМСО) 10,0 (1H, ушир.с), 7,41 (1H, с), 6,65 (1H, с), 3,40 (4H, м), 2,70 (4H, м), 1,40 (9H, с).
Описание 42
1,1-Диметилэтил 7-иод-8-({5-[(метиламино)карбонил]-2-пиридинил}окси)-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилат (D42)
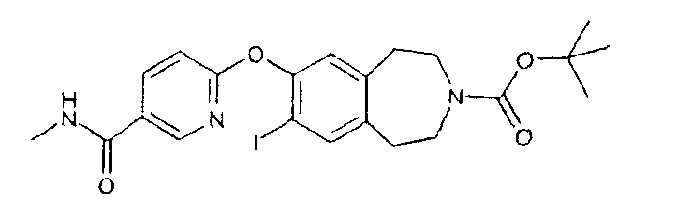
Гидрид натрия (60% дисперсия в минеральном масле, 240 мг, 6 ммоль) добавляют к перемешиваемому раствору 1,1-диметилэтил 7-гидрокси-8-иод-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилат (D41) (1,94 г, 5 ммоль) в диметилсульфоксиде (10 мл). Через 10 минут добавляют 6-хлор-N-метилникотинамид (D10) (850 мг, 5 ммоль) и реакционную смесь нагревают до 100°C в течение 20 часов. После охлаждения до комнатной температуры реакционную смесь разбавляют водой и дихлорметаном. Органический слой отделяют, промывают водой и насыщенным соляным раствором, сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Остаток очищают колоночной хроматографией (1:1 этилацетат:гексаны), получая указанный в заголовке продукт (D42).
Описание 43
N-Метил-6-(8-иод-2,3,4,5-тетрагидро-1H-3-бензазепин-7-илокси)-3-пиридинкарбоксамид (D43)
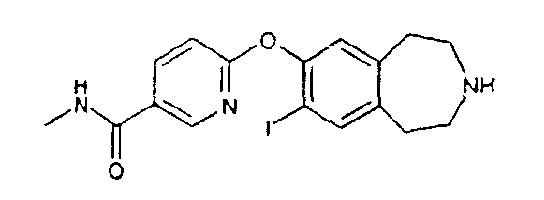
Соединение описания 43 (D43) получают из 1,1-диметилэтил 7-иод-8-({5-[(метиламино)карбонил]-2-пиридинил}окси)-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилата (D42) по способу описания 2 (D2); МС (ES+) m/e 424[M+H]+.
Описание 44
1,1-Диметилэтил 7-иод-8-[(фенилметил)окси]-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилат (D44)
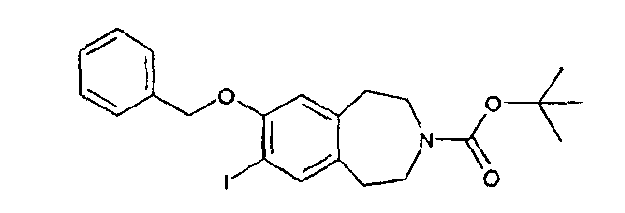
Гидрид натрия (60% дисперсия в минеральном масле, 576 мг, 14,4 ммоль) добавляют к перемешиваемому раствору 1,1-диметилэтил 7-гидрокси-8-иод-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилата (D41) (4,67 г, 12 ммоль) в диметилформамиде (30 мл). Через 15 минут добавляют бензилбромид (2,04 г, 1,4 мл, 12 ммоль) и смесь перемешивают 2 часа. Смесь разбавляют водой и этилацетатом, органический слой отделяют, промывают водой и насыщенным соляным раствором, сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Остаток очищают колоночной хроматографией, элюируя смесью этилацетат:гексаны (1:10), и получают указанный в заголовке продукт (D44).
Описание 45
7-Иод-8-[(фенилметил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепин (D45)
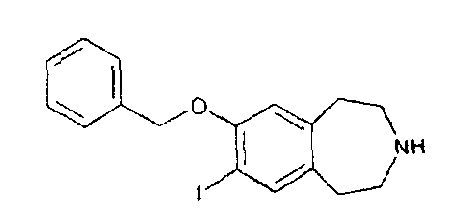
Соединение описания D45 (D45) получают из 1,1-диметилэтил 7-иод-8-[(фенилметил)окси]-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилата (D44) по способу описания 2 (D2); МС (ES+) m/e 380 [M+H]+.
Описание 46
1-(3-Хлор-2-пиразинил)-2-пирролидинон (D46)
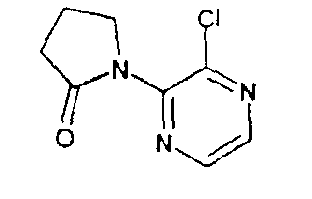
Стадия 1: 3-Хлорпиразина 1-оксид
Смесь хлорпиразина (9,6 г, 83,3 ммоль) и раствора пероксида водорода (30%, 16 мл) в ледяной уксусной кислоте (26 мл) нагревают при 70°C 18 часов. Смесь оставляют охлаждаться до комнатной температуры, выливают в воду (250 мл) и экстрагируют дихлорметаном (3×100 мл). Дихлорметановые экстракты объединяют, промывают насыщенным раствором бикарбоната натрия (2×70 мл), водой (3×100 мл) и насыщенным соляным раствором (100 мл). Органическую фракцию сушат над сульфатом натрия и упаривают в вакууме, получая белое твердое вещество, которое перекристаллизовывают из абсолютного этанола, получая указанное в заголовке соединение (0,45 г). 1H ЯМР (CDCl3) 8,27-8,26 (1H, д), 8,15 (1H, с), 8,03-8,02 (1H, дд).
Стадия 2: 2,3-Дихлорпиразин
3-Хлорпиразина 1-оксид (D46, стадия 1) (2,2 г, 16,9 ммоль) медленно добавляют к оксихлориду фосфора (10 мл) при 60°C. После завершения добавления смесь нагревают с обратным холодильником в течение 60 минут. Смесь оставляют охлаждаться и выливают в твердый ацетат натрия со льдом (5 г). Перемешивают, пока лед не растает, и затем экстрагируют дихлорметаном. Дихлорметановые экстракты объединяют, промывают насыщенным раствором бикарбоната натрия, водой и насыщенным соляным раствором. Органическую фракцию сушат над сульфатом натрия и упаривают в вакууме. Полученный остаток очищают колоночной хроматографией, элюируя смесью этилацетат:гексан (1:20), и получают указанное в заголовке соединение (0,86 г). 1H ЯМР (CDCl3) 8,32 (2H, с).
Стадия 3: 1-(3-Хлор-2-пиразинил)-2-пирролидинон
Гидрид натрия (60% в минеральном масле, 67 мг, 1,62 ммоль) добавляют к раствору пирролидинона (0,12 мл, 1,54 ммоль) в сухом диметилформамиде (5 мл) в атмосфере аргона при 0°C. Смесь оставляют нагреваться до комнатной температуры в течение 1,5 часов. Добавляют раствор 2,3-дихлорпиразина (D46, стадия 2) (250 мг, 1,69 ммоль) в сухом диметилформамиде (2 мл) и смесь перемешивают при комнатной температуре в атмосфере аргона в течение 2 часов. Смесь выливают в воду (30 мл) и экстрагируют этилацетатом (×3). Этилацетатные экстракты объединяют, промывают насыщенным соляным раствором, сушат над сульфатом магния и упаривают в вакууме. Полученный остаток очищают колоночной хроматографией, элюируя смесью этилацетат:пентан (1:1), получая указанное в заголовке соединение (0,10 г); МС (ES+) m/e 198 [M+H]+.
Описание 47
2,5-Дихлорпиразин (D47)
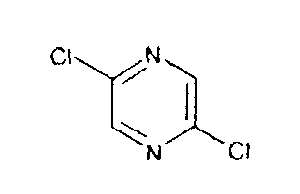
Стадия 1: 5-Хлор-2-пиразинамин
Аминопиразин (10 г, 10,5 ммоль) растворяют в сухом диметилформамиде (60 мл) и обрабатывают N-хлорсукцинимидом (15,36 г, 11,5 ммоль) в атмосфере аргона при 0°C. Смесь перемешивают 30 минут и затем оставляют нагреваться до комнатной температуры. Смесь выливают в воду и экстрагируют диэтиловым эфиром. Диэтиловые слои объединяют и упаривают в вакууме. Полученный остаток очищают колоночной хроматографией, элюируя смесью этилацетат:пентан (1:9), и получают указанное в заголовке соединение (1,40 г); 1H ЯМР (CDCl3) 8,02 (1H, с), 7,76 (1H, с), 4,61 (2H, с).
Стадия 2: 2,5-Дихлорпиразин
5-Хлор-2-пиразинамин (D47, стадия 1) (2,41 г, 18,6 ммоль) растворяют в концентрированной хлористоводородной кислоте (24 мл), охлаждают в бане со смесью лед-ацетон и по каплям обрабатывают раствором нитрита натрия (2,63 г, 38,1 ммоль) в воде (18 мл) в течение 1 часа. Смесь охлаждают в бане со смесью лед-вода и оставляют перемешиваться в течение 1 часа. Смесь оставляют нагреваться до комнатной температуры в течение 1 часа, нейтрализуют добавлением раствора (2M) гидроксида натрия и экстрагируют дихлорметаном. Дихлорметановые слои объединяют, сушат над сульфатом магния и упаривают в вакууме. Полученный остаток очищают колоночной хроматографией, элюируя смесью этилацетат:пентан (1:9), и получают указанное в заголовке соединение (0,33 г); 1H ЯМР (CDCl3) 8,40 (2H, с).
Описание 48
2,5-Дибромпиразин (D48)
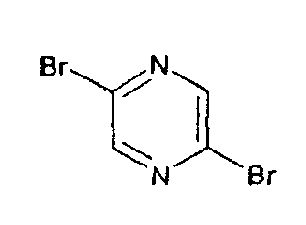
Стадия 1: 5-Бром-2-пиразинамин
Аминопиразин (5,0 г, 52,6 ммоль) растворяют в хлороформе (150 мл) и добавляют пиридин (5,11 мл, 63,2 ммоль). В течение 1 часа добавляют по каплям раствор брома (3,24 мл, 63,2 ммоль) в хлороформе (50 мл). Смесь оставляют перемешиваться в течение 30 минут, разбавляют водой (50 мл) и перемешивают еще 10 минут. Органический слой отделяют, промывают водой (50 мл), сушат над сульфатом магния и упаривают в вакууме. Полученный остаток очищают колоночной хроматографией, элюируя смесью этилацетат:пентан (1:4), и получают указанное в заголовке соединение (0,32 г); МС (ES+) m/e 175 [M+H]+.
Стадия 2: 2,5-Дибромпиразин
5-Бром-2-пиразинамин (D48, стадия 1) (317 мг, 1,82 ммоль) добавляют к охлажденному (в бане со смесью лед-ацетон) раствору бромистоводородной кислоты (водный 48% раствор) (2 мл). После перемешивания в течение 5 минут добавляют бром (0,28 мл, 5,46 ммоль) и затем раствор нитрита натрия (314 мг, 4,55 ммоль) в воде по каплям в течение 15 минут. Смесь перемешивают 30 минут и оставляют нагреваться до комнатной температуры в течение 30 минут. Добавляют раствор гидроксида натрия (2,6 г) в воде (7 мл) и смесь перемешивают 1 час. Смесь экстрагируют дихлорметаном. Дихлорметановые слои объединяют и упаривают в вакууме, получая указанное в заголовке соединение (60 мг). 1H ЯМР(CDCl3) 8,49 (2H, с).
Описание 49
N-Метил-5-(2,3,4,5-тетрагидро-1H-3-бензазепин-7-илокси)-2-пиразинкарбоксамид (D49)
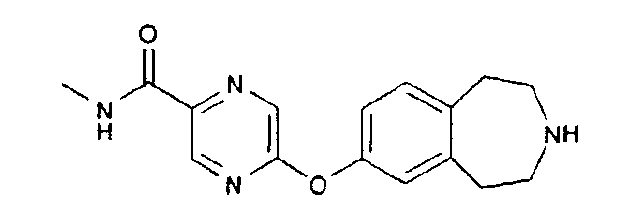
Стадия 1: 1,1-Диметилэтил 7-({5-[(метилокси)карбонил]-2-пиразинил}окси)-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилат
Гидрид натрия (60% дисперсия в минеральном масле) (6,4 г, 0,16 моль) добавляют порциями к раствору трет-бутилового эфира 7-гидрокси-1,2,4,5-тетрагидробензо[d]азепин-3-карбоновой кислоты (PCT Int. Appl. (2002), WO 02/40471) (40 г, 0,15 моль) в сухом диметилформамиде (200 мл), охлажденному до 5°C в течение 15 минут. Через 15 минут смесь оставляют нагреваться до комнатной температуры при перемешивании в течение 60 минут. Смесь охлаждают в бане со смесью лед-вода и порциями добавляют метил 5-хлор-2-пиразинкарбоксилат (31,2 г, 0,18 моль). Смесь оставляют нагреваться до комнатной температуры и перемешивают 18 часов. Смесь выливают в воду (500 мл) со льдом (500 мл) и перемешивают, пока лед не растает. Полученное твердое вещество собирают фильтрацией, промывают водой и растворяют в этилацетате (1500 мл). Этилацетатный слой промывают насыщенным соляным раствором (200 мл), сушат над сульфатом натрия и упаривают в вакууме. Неочищенный продукт очищают колоночной хроматографией, элюируя смесью этилацетат:гексан (1:2), и получают указанное в заголовке соединение (35,07 г).
Стадия 2: 5-[(3-{[(1,1-Диметилэтил)окси]карбонил}-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-2-пиразинкарбоновая кислота
2M раствор гидроксида натрия (110 мл) добавляют к раствору 1,1-диметилэтил 7-({5-[(метилокси)карбонил]-2-пиразинил}окси)-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилата (D49, стадия 1) (29,38 г, 73,6 ммоль) в ацетоне (480 мл) и полученную смесь перемешивают при комнатной температуре 25 минут. Смесь подкисляют 2M хлористоводородной кислотой и затем выливают в воду (2 л). Полученное белое твердое вещество собирают фильтрацией, промывают водой и растворяют в этилацетате (1 л). Данный раствор сушат над сульфатом натрия и упаривают в вакууме, получая указанное в заголовке соединение (27,3 г); МС (ES+) m/e 384 [M-H]+.
Стадия 3: 1,1-Диметилэтил 7-({5-[(метиламино)карбонил]-2-пиразинил}окси)-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилат
1,1'-Карбонилдиимидазол (16,6 г, 102 ммоль) добавляют к раствору 5-[(3-{[(1,1-диметилэтил)окси]карбонил}-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-2-пиразинкарбоновой кислоты (D49, стадия 2) (37,5 г, 97 ммоль) в сухом дихлорметане (400 мл) и полученную смесь перемешивают при комнатной температуре 18 часов. Добавляют метиламин (2M раствор в тетрагидрофуране) (100 мл) и смесь перемешивают 2 часа. Растворитель удаляют в вакууме и остаток очищают колоночной хроматографией, элюируя смесью этилацетат:хлороформ (1:1), и получают указанное в заголовке соединение (25,8 г); МС (ES+) m/e 399 [M+H]+.
Стадия 4: N-Метил-5-(2,3,4,5-тетрагидро-1H-3-бензазепин-7-илокси)-2-пиразинкарбоксамид
Раствор 1,1-диметилэтил 7-({5-[(метиламино)карбонил]-2-пиразинил}окси)-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилата (D49, стадия 3) (44,26 г, 0,11 моль) в дихлорметане (800 мл) добавляют по каплям к перемешиваемому раствору 4M хлористого водорода в диоксане (270 мл, 1,1 моль). Полученную смесь перемешивают при комнатной температуре 60 минут. Добавляют дополнительное количество 4M хлористого водорода в диоксане (30 мл, 0,12 моль) и смесь перемешивают 60 минут. Полученное белое твердое вещество собирают фильтрацией и промывают дихлорметаном. Твердое вещество растворяют в воде (2 л) и подщелачивают добавлением насыщенного раствора карбоната натрия. Водный слой экстрагируют дихлорметаном и экстракты фильтруют через целит. Целит промывают метанолом и объединенные дихлорметановые и метанольные смывы упаривают в вакууме, получая указанное в заголовке соединение (25,1 г); МС (ES+) m/e 299 [M+H]+.
Описания 50-52
Соединения описаний 50-52 (D50-D52) получают по способу описания 5 (D5) из соответствующих арилгалогенидов и аминов, указанных в таблице, и используют их без дополнительной характеристики:
Описание 53
(2E)-1-{6-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-пиридинил}-3-(диметиламино)-2-пропен-1-он (D53)
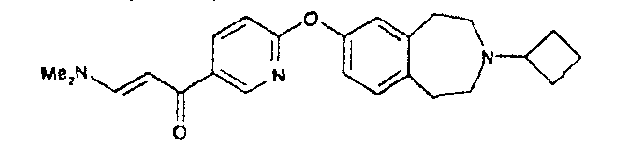
Смесь 1-{6-[(3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-пиридинил}этанона (Е214) (186 мг, 0,55 ммоль), диметилформамиддиметилацетила (0,25 мл) и ксилола (4 мл) нагревают с обратным холодильником 8 часов. Остаток разбавляют толуолом и концентрируют в вакууме, получая соединение (D53); МС (ES+) m/e 392 [M+H]+.
Описание 54
6-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-пиридинкарбогидразид (D54)

Смесь тионилхлорида (2 мл) и 6-[(3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-пиридинкарбоновой кислоты (E196b) (200 мг, 0,59 ммоль) перемешивают при температуре кипения с обратным холодильником 1 час. Реакционную смесь концентрируют в вакууме, получая неочищенный остаток. Остаток растворяют в тетрагидрофуране (5 мл), охлаждают до 0°C и добавляют по каплям гидразин гидрат (1,5 мл) в тетрагидрофуране (1,5 мл). Реакционную смесь оставляют нагреваться до комнатной температуры и перемешивают в течение 1 часа. Затем реакционную смесь разбавляют этилацетатом, промывают насыщенным раствором карбоната натрия, водой и насыщенным соляным раствором и сушат (сульфат магния). Органический слой фильтруют и концентрируют в вакууме, получая указанное в заголовке соединение (D54); МС (ES+) m/e 361 [M+H]+.
Описание 55
цис-4-(4-Морфолинилкарбонил)циклогексанол (D55)
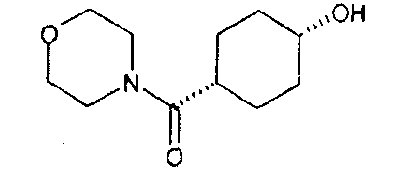
Раствор цис-4-гидроксициклогексанкарбоновой кислоты (720 мг, 0,5 ммоль), гидрохлорида 1-(3-диметиламинопропил)-3-этилкарбодиимида (1,33 г, 6 ммоль) и 1-гидрокси-7-азабензотриазола (816 мг, 6 ммоль) в дихлорметане (6 мл) обрабатывают морфолином (1,3 мл, 15 ммоль). После перемешивания при комнатной температуре в течение 18 часов неочищенную реакционную смесь наносят на ионообменный картридж SCX (Varian bond-elute, 5 г) и промывают сначала метанолом, затем смесью .880 аммиак:метанол (1:9). Объединенные основные фракции концентрируют в вакууме, полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:этанол:дихлорметан (1:9:90), получая указанное в заголовке соединение (D55); МС (ES+) m/e 214 [M+H]+.
Описание 56
2-Хлор-6-[4-(метилсульфонил)фенил]пиразин (D56)
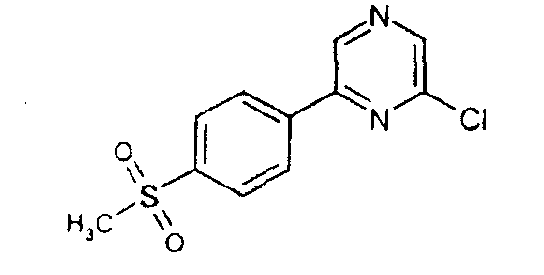
2,6-Дихлорпиразин (2,98 г, 20,0 ммоль),
[4-(метилсульфонил)фенил]борную кислоту (2 г, 10,0 ммоль), тетракис(трифенилфосфин)палладия (1,15 г, 1,0 ммоль), фосфат калия (10,2 г, 48 ммоль) и диметилформамид (90 мл) нагревают при 80°С в течение 16 часов. Растворитель удаляют в вакууме, продукт растворяют в хлороформе и фильтруют через целит. Фильтрат промывают водой, после чего разделяют. Остаток очищают колоночной хроматографией, элюируя смесью этилацетат:гексан (4:6), и получают указанное в заголовке соединение. МС (ES+) m/e 270 [M+H]+.
Пример 1
7-Бензилокси-3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин (Е1)
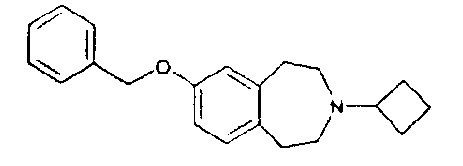
7-Бензилокси-1,2,4,5-тетрагидробензо[d]азепин (D2) (25,3 г, 100 ммоль) растворяют в 2,5% растворе уксусной кислоты в дихлорметане (400 мл) при 0°C и обрабатывают по каплям циклобутаноном (11,2 мл, 150 ммоль). Смесь перемешивают 30 минут и затем порциями добавляют триацетоксиборгидрид натрия (31,8 г, 150 ммоль). Реакционную смесь перемешивают при комнатной температуре 4 часа, подщелачивают насыщенным раствором карбоната натрия и экстрагируют дихлорметаном. Объединенные экстракты промывают водой, насыщенным соляным раствором, сушат над безводным сульфатом натрия и концентрируют в вакууме.
Неочищенный остаток перетирают с гексаном и фильтруют, получая указанный в заголовке продукт (E1).
МС (ES+) m/e 308 [M+H]+.
Пример 2
7-Бензилокси-3-циклопентил-2,3,4,5-тетрагидро-1H-бензо[d]азепин (E2)
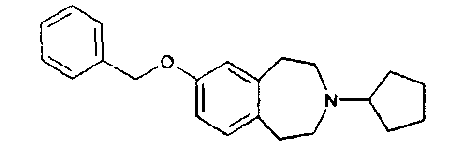
Указанное в заголовке соединение (E2) получают из 7-бензилокси-1,2,4,5-тетрагидробензо[d]азепина (D2) и циклопентанона по способу примера 1; МС (ES+) m/e 322 [M+H]+.
Пример 3
3-Циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ол (E3)
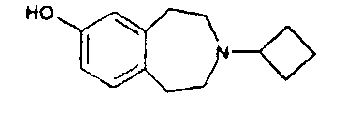
7-Бензилокси-3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин (E1) (9,22 г, 30 ммоль) растворяют в этаноле (150 мл) и тетрагидрофуране (50 мл). Добавляют палладий (1,5 г, 10% на угольной пасте) и реакционную смесь перемешивают при комнатной температуре в атмосфере водорода (1 атмосфера) в течение 5 часов. Реакционную смесь фильтруют через целит и фильтрат концентрируют в вакууме. Неочищенный остаток перетирают с диэтиловым эфиром и фильтруют, получая указанный в заголовке продукт (E3); МС (ES+) m/e 218 [M+H]+.
Пример 4
3-Циклопентил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ол (E4)
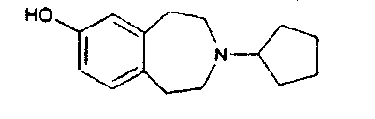
Указанное в заголовке соединение (E4) получают из 7-бензилокси-3-циклопентил-2,3,4,5-тетрагидро-1H-бензо[d]азепина (E2) по способу примера 3 (E3); 1H ЯМР (ДМСО-d6) 9,08 (1H, ушир.с), 6,70 (1H, д), 6,53-6,47 (2H, м), 3,31-2,50 (9H, м) 1,88-1,43 (8H, м).
Пример 5a
Трет-бутиловый эфир 4-(3-циклопентил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илокси)пиперидин-1-
карбоновой кислоты (E5a)
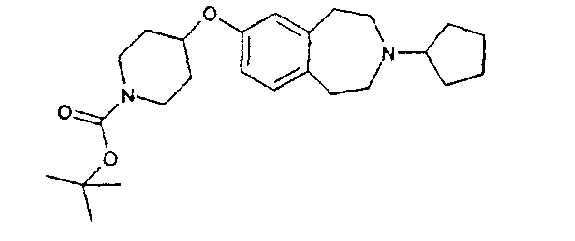
3-Циклопентил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ол (E4) (1,1 г, 4,8 ммоль), трет-бутиловый эфир 4-гидроксипиперидин-1-карбоновой кислоты (1,15 г, 5,7 ммоль), ди-трет-бутилазодикарбоксилат (1,31 г, 5,7 ммоль) и трифенилфосфин (1,5 г, 5,7 ммоль) перемешивают при комнатной температуре в течение 16 часов в тетрагидрофуране (20 мл). Смесь подкисляют уксусной кислотой, наносят на ионообменный картридж SCX (Varian bond-elute, 10 г) и промывают сначала метанолом, затем смесью .880 аммиак:метанол (1:9). Объединенные основные фракции концентрируют в вакууме и полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:метанол:дихлорметан (1:9:90), и получают указанный в заголовке продукт (E5a); МС (ES+) m/e 415[M+H]+.
Пример 5
3-Циклопентил-7-(пиперидин-4-илокси)-2,3,4,5-тетрагидро-1H-бензо[d]азепин (E5)
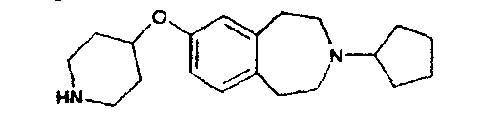
Трет-бутиловый эфир 4-(3-циклопентил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илокси)пиперидин-1-
карбоновой кислоты (E5a) (593 мг, 1,43 ммоль) растворяют в дихлорметане (5 мл) и обрабатывают трифторуксусной кислотой (3 мл). Раствор перемешивают при комнатной температуре 1 час, концентрируют в вакууме и наносят на ионообменный картридж SCX (Varian bond-elute, 5 г) и промывают сначала метанолом, затем смесью .880 аммиак:метанол (1:9). Объединенные основные фракции концентрируют в вакууме и полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:метанол:дихлорметан (1:9:90), получая указанный в заголовке продукт (E5). МС (ES+) m/e 315 [M+H]+.
Примеры 6-12
Соединения примеров 6-12 (E6-12) получают либо из 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3), либо из 3-циклопентил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E4) и соответствующих спиртов, указанных в таблице, по способу примера 5a (E5a) и затем по способу примера 5 (E5).
илокси)-2,3,4,5-тетрагидро-1Н-бензо[d]азепин (Е6)
илметокси)-2,3,4,5-тетрагидро-1Н-бензо[d]азепин (Е7)
илметокси)-2,3,4,5-тетрагидро-1Н-бензо[d]азепин (Е12)
Пример 13
4-{1-[4-(3-Циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илокси)пиперидин-1-ил]метаноил}бензонитрил (Е13)
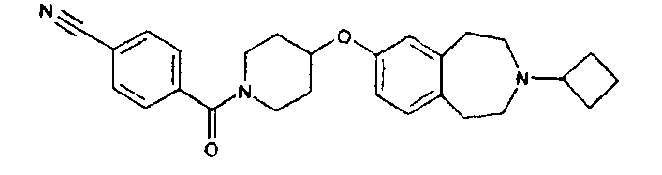
4-Цианобензойную кислоту (147 мг, 1 ммоль), гидрат 1-гидроксибензотриазола (154 мг, 1 ммоль) и N-циклогексилкарбодиимид N'-метилполистирол (1,8 ммоль/г, 555 мг, 1 ммоль) перемешивают при комнатной температуре в дихлорметане (5 мл) в течение 15 минут. Добавляют 3-циклобутил-7-(пиперидин-4-илокси)-2,3,4,5-тетрагидро-1H-бензо[d]азепин (E6) (150 мг, 0,5 ммоль) и перемешивание продолжают еще 16 часов. Реакционную смесь наносят на ионообменный картридж SCX (Varian bond-elute, 5 г) и промывают сначала метанолом, затем смесью .880 аммиак:метанол (1:9). Объединенные основные фракции концентрируют в вакууме и полученный остаток очищают колоночной хроматографией, элюируя дихлорметаном и затем смесью .880 аммиак:этанол:дихлорметан (1:9:90), и получают указанный в заголовке продукт (E13). МС (ES+) m/e 430 [M+H]+.
Примеры 14-42
Соединения примеров 14-42 (E14-E42) получают по способу примера 13 (E13) из соответствующих аминов и кислот, как указано в таблице:
метанон (Е22)
метаноил}-1Н-пиридон (Е32)
карбоновая кислота
карбоновая кислота
илметокси)пиперидин-1-ил]-метаноил}-
бензонитрил (Е36)
метанон (Е37)
бензойная кислота (WO 03/04468A1)
метанон (Е41)
бензойная кислота (WO 03/04468A1)
Пример 43
1-[4-(3-Циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илокси)пиперидин-1-ил]-1-циклопентилметанон (E43)
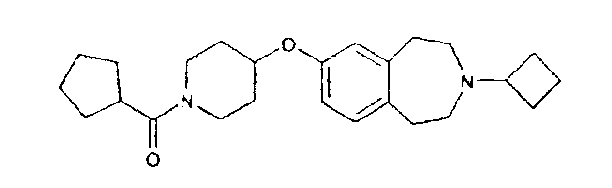
3-Циклобутил-7-(пиперидин-4-илокси)-2,3,4,5-тетрагидро-1H-бензо[d]азепин (E6) (150 мг, 0,5 ммоль) перемешивают в дихлорметане (5 мл) с диэтиламинометилполистиролом (3,2 ммоль/г, 625 мг, 2 ммоль). Добавляют циклопентанкарбонилхлорид (80 мкл, 0,6 ммоль) и смесь перемешивают при комнатной температуре 16 часов. Смолу фильтруют, промывают дихлорметаном и фильтрат концентрируют в вакууме. Остаток очищают колоночной хроматографией, элюируя дихлорметаном, затем смесью .880 аммиак:этанол:дихлорметан (1:9:90), и получают указанный в заголовке продукт (E43); МС (ES+) m/e 397 [M+H]+.
Примеры 44-51
Соединения примеров 44-51 (E44-E51) получают по способу примера 43 (E43) из соответствующих аминов и карбонилхлоридов, указанных в таблице:
азепин-7-илоксиметил)пиперидин-1-ил]-
метаноил}бензонитрил (Е44)
азепин-7-илоксиметил)пирролидин-1-ил]-
метаноил}бензонитрил (Е45)
азепин-7-илокси)пирролидин-1-ил]-метаноил}
бензонитрил (Е46)
азепин-7-илокси)пирролидин-1-ил]-метаноил}
бензонитрил (Е47)
азепин-7-илокси)пирролидин-1-ил]-метаноил}-
бензонитрил (Е48)
азепин-7-илокси)пиперидин-1-ил]-2,2-диметилпропан-1-он (Е49)
азепин-7-илокси)пиперидин-1-ил]-1-циклопропилметанон (Е50)
азепин-7-илокси)пиперидин-1-ил]метанон (Е51)
Пример 52
4-{1-{4-(3-Циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илокси)пиперидин-1-ил]-1-морфолин-4-илметанон (E52)
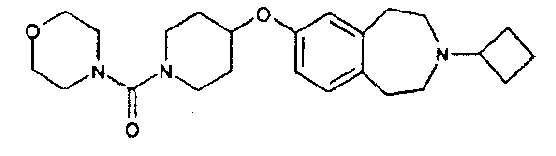
3-Циклобутил-7-(пиперидин-4-илокси)-2,3,4,5-тетрагидро-1H-бензо[d]азепин (E6) (150 мг, 0,5 ммоль) перемешивают в дихлорметане (5 мл) с диэтиламинометилполистиролом (3,2 ммоль/г, 625 мг, 2 ммоль). Добавляют морфолинкарбамоилхлорид (70 мкл, 0,6 ммоль) и смесь перемешивают при комнатной температуре 16 часов. Смолу фильтруют, промывают дихлорметаном и фильтрат концентрируют в вакууме. Остаток очищают колоночной хроматографией, элюируя дихлорметаном, затем смесью .880 аммиак:этанол:дихлорметан (1:9:90), и получают указанный в заголовке продукт (E52). МС (ES+) m/e 414 [M+H]+.
Примеры 53-60
Соединения примеров 53-60 (E53-E60) получают по способу примера 52 (E52) из соответствующих аминов и карбонилхлоридов, указанных в таблице:
(М+Н)+
илметокси)-2,3,4,5-тетрагидро-1Н-бензо[d]азепин (Е7)
азепин (Е8)
азепин (Е9)
азепин (Е10)
карбоновой кислоты (Е57)
илокси)-2,3,4,5-тетрагидро-1Н-бензо[d]азепин (Е6)
пирролидин-1-илметанон (Е58)
азепин (Е6)
азепин (Е6)
азепин (Е11)
Пример 61
Диэтиламид 4-(3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илокси)пиперидин-1-карбоновой кислоты (E61)
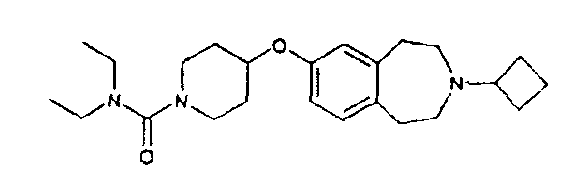
3-Циклобутил-7-(пиперидин-4-илокси)-2,3,4,5-тетрагидро-1H-бензо[d]азепин (E6) (1,5 г, 5 ммоль), растворенный в толуоле (40 мл), медленно добавляют к 20% раствору фосгена в толуоле (12,5 мл, 25 ммоль) при 0°C. Смесь перемешивают при комнатной температуре в течение 3 часов и концентрируют в вакууме, получая неочищенный остаток (1,91 г). Неочищенный продукт (300 мг, 0,75 ммоль) затем добавляют к перемешиваемой взвеси диэтиламина (207 мкл, 2 ммоль) и диэтиламинометилполистирола (3,2 ммоль/г, 1,41 г, 4,5 ммоль) в дихлорметане (10 мл). Реакционную смесь перемешивают при комнатной температуре 16 часов, фильтруют и концентрируют в вакууме. Неочищенный остаток очищают колоночной хроматографией, элюируя дихлорметаном, затем смесью .880 аммиак:этанол:дихлорметан (1:9:90), и получают указанный в заголовке продукт (E61). МС (ES+) m/e 400 [M+H]+.
Примеры 62-65
Соединения примеров 62-65 (E62-E65) получают по способу примера 61 (E61) из 3-циклобутил-7-(пиперидин-4-илокси)-2,3,4,5-тетрагидро-1H-бензо[d]азепина (E6) и соответствующих аминов, указанных в таблице:
Пример 66
Изопропиламид 4-(3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илокси)пиперидин-1-карбоновой кислоты (E66)
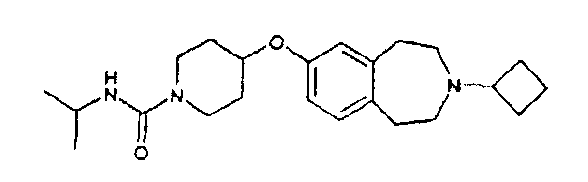
Раствор 3-циклобутил-7-(пиперидин-4-илокси)-2,3,4,5-тетрагидро-1H-бензо[d]азепина (E6) (150 мг, 0,5 ммоль) и изопропилизоцианата (60 мкл, 0,6 ммоль) в дихлорметане (5 мл) перемешивают при комнатной температуре 16 часов. Раствор концентрируют в вакууме и остаток очищают колоночной хроматографией, элюируя дихлорметаном, затем смесью .880 аммиак:этанол:дихлорметан (1:9:90), и получают указанный в заголовке продукт (E66). МС (ES+) m/e 386 [M+H]+.
Пример 67
(4-Фторфенил)амид 4-(3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илокси)пиперидин-1-карбоновой кислоты (E67)
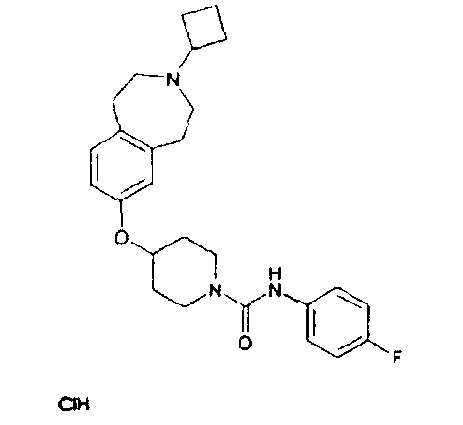
Соединения примера 67 получают из 3-циклобутил-7-(пиперидин-4-илокси)-2,3,4,5-тетрагидро-1H-бензо[d]азепина (E6) и 4-фторфенилизоцианата по способу примера 66 (E66); МС (ES+) m/e 438 [M+H]+.
Пример 68
2-(3-Циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илокси)-N,N-диметилацетамид (Е68)
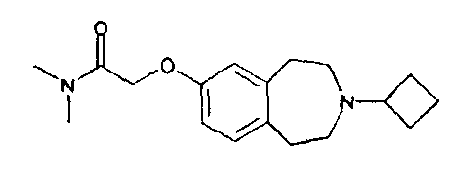
Гидрид натрия (60% дисперсия в минеральном масле, 60 мг, 1,5 ммоль) добавляют к перемешиваемому раствору 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) (200 мг, 0,9 ммоль) в диметилсульфоксиде (10 мл). Через 0,5 часа добавляют 2-хлор-N,N-диметилацетамид (0,3 мл, 2,4 ммоль) и реакционную смесь нагревают при 120°C в течение 6 часов. Реакционную смесь оставляют охлаждаться, затем неочищенную смесь наносят на ионообменный картридж SCX (Varian bond-elute, 10 г) и промывают сначала метанолом, затем смесью .880 аммиак:метанол (1:9). Объединенные основные фракции упаривают в вакууме, получая указанное в заголовке соединение (E68). МС (ES+) m/e 303 [M+H]+.
Примеры 69-71
Соединения примеров 69-71 (E69-E71) получают по способу примера 68 (E68) из 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) и соответствующих хлоридов, указанных в таблице.
илокси)-N-фенилацетамид (Е69)
илокси)-1-пирролидин-1-илэтанон (Е70)
илокси)-1-морфолин-4-илэтанон (Е71)
Пример 72
3-Циклобутил-7-(1-метансульфонилпиперидин-4-илокси)-2,3,4,5-тетрагидро-1H-бензо[d]азепин (E72)
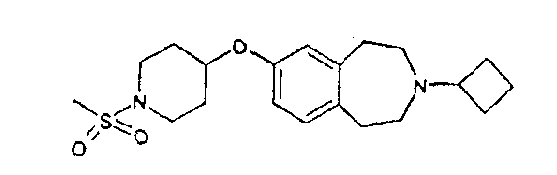
3-Циклобутил-7-(пиперидин-4-илокси)-2,3,4,5-тетрагидро-1H-бензо[d]азепин (E6) (150 мг, 0,5 ммоль) перемешивают в дихлорметане (5 мл) с диэтиламинометилполистиролом (3,2 ммоль/г, 625 мг, 2 ммоль). Добавляют метансульфонилхлорид (43 мкл, 0,55 ммоль) и смесь перемешивают при комнатной температуре 16 часов. Смолу фильтруют, промывают дихлорметаном и фильтрат концентрируют в вакууме. Остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:этанол:дихлорметан (1:9:90), и получают указанный в заголовке продукт (E72); МС (ES+) m/e 379 [M+H]+.
Примеры 73-78
Соединения примеров 73-78 (E73-E78) получают по способу примера 72 (E72) из соответствующих аминов и сульфонилхлоридов, указанных в таблице:
бензонитрил (Е73)
илокси)-2,3,4,5-тетрагидро-1Н-бензо[d]
азепин (Е6)
пиперидин-4-илокси]-2,3,4,5-тетрагидро-1Н-бензо[d]азепин (Е74)
илокси)-2,3,4,5-тетрагидро-1Н-бензо[d]
азепин (Е6)
сульфонил]бензонитрил (Е75)
илметокси)-2,3,4,5-тетрагидро-1Н-бензо[d]
азепин (Е7)
сульфонил]бензонитрил (Е76)
азепин (Е8)
азепин (Е9)
азепин (Е10)
Пример 79
3-Циклобутил-7-(2,4-дифторбензилокси)-2,3,4,5-тетрагидро-1H-бензо[d]азепин (E79)
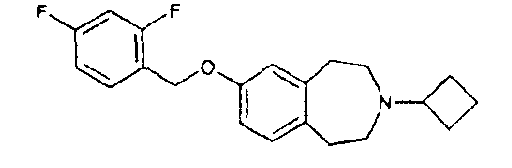
Карбонат калия (778 мг, 5,6 ммоль) добавляют к перемешиваемому раствору 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) (868 мг, 4,0 ммоль), 2,4-дифторбензилбромида (0,25 мл, 2,1 ммоль) и иодида калия (25 мг) в бутаноне (9 мл). Реакционную смесь перемешивают при температуре кипения с обратным холодильником в течение 18 часов, охлаждают, фильтруют и концентрируют в вакууме. Неочищенный остаток растворяют в этилацетате и промывают водой и насыщенным соляным раствором. Органический слой сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:этанол:дихлорметан (0,25:2,25:97,5, затем 1:9:10), и получают указанное в заголовке соединение (E79); МС (ES+) m/e 344 [M+H]+.
Примеры 80-87
Соединения примеров 80-87 (E80-E87) получают из 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) и соответствующих галогенидов, указанных в таблице, по общему способу, описанному в примере 80 (E80):
илоксиметил)бензонитрил (Е80)
илоксиметил)бензонитрил (Е85)
илоксиметил)бензонитрил (Е86)
илоксиметил)-1-метил-1Н-хинолин-2-он (Е87)
Пример 88
Метиловый эфир 4-(3-циклопентил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илоксиметил)бензойной кислоты (E88)
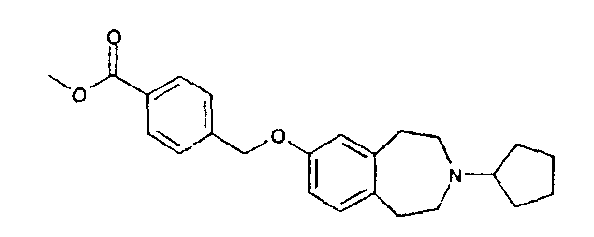
Метиловый эфир 4-(2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илоксиметил]бензойной кислоты (D4) (2,83 г, 9,1 ммоль) и циклопентанон (1,6 мл, 18,2 ммоль) растворяют в дихлорметане (30 мл) и уксусной кислоте (0,5 мл). Добавляют триацетоксиборгидрид натрия (3,85 г, 18,2 ммоль) и раствор перемешивают при комнатной температуре 4 часа. Реакционную смесь промывают насыщенным раствором карбоната натрия, органический слой сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Неочищенную смесь очищают колоночной хроматографией, элюируя смесью .880 аммиак:этанол:дихлорметан (1:9:90), и получают указанное в заголовке соединение (E88); МС (ES+) m/e 380 [M+H]+.
Пример 89
4-(3-Циклопентил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илоксиметил)бензойная кислота (E89)
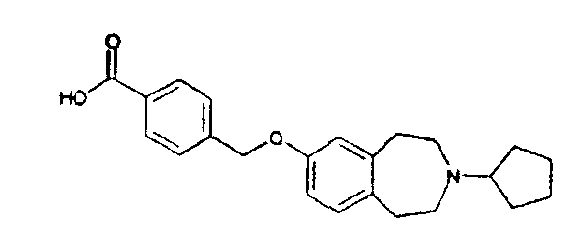
Метиловый эфир 4-(3-циклопентил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илоксиметил)бензойной кислоты (E88) (3,1 г, 8,1 ммоль) растворяют в смеси метанола (90 мл), 2N раствора гидроксида натрия (12 мл) и воды (30 мл). Полученную смесь перемешивают при 60°С в течение 4 часов и затем охлаждают до комнатной температуры. Смесь концентрируют в вакууме, чтобы удалить органические растворители, и затем подкисляют до рН 6 (2N раствором хлористоводородной кислоты). Полученный осадок отфильтровывают, промывают водой и сушат в вакууме, получая указанное в заголовке соединение (E89); МС (ES+) m/e 366 [M+H]+.
Пример 90
1-[4-(3-Циклопентил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илоксиметил)фенил]-1-пирролидинилметанон (E90)
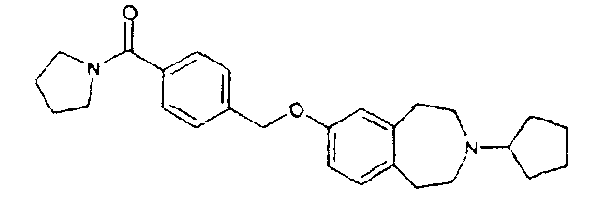
4-(3-Циклопентил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илоксиметил)бензойную кислоту (E89) (0,201 мг, 0,55 ммоль), 1,3-диизопропилкарбодиимид (44 мкл, 0,6 ммоль) и гидрат 1-гидроксибензотриазола (82 мг, 0,6 ммоль) растворяют в смеси дихлорметана (2 мл) и диметилформамида (1 мл). После перемешивания при комнатной температуре в течение 0,5 часа добавляют пирролидин (41 мкл, 0,5 ммоль) и полученную смесь оставляют перемешиваться в течение 16 часов. Неочищенную реакционную смесь наносят на ионообменный картридж SCX (Varian bond-elute, 5 г) и промывают метанолом и затем смесью .880 аммиак:метанол (1:9). Объединенные основные фракции концентрируют в вакууме, полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:этанол:дихлорметан (1:9:90), и получают указанное в заголовке соединение (E90); МС (ES+) m/e 419 [M+H]+.
Примеры 91-93
Соединения примеров 91-93 (E91-E93) получают по способу примера 90 (E90) из 4-(3-циклопентил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илоксиметил)бензойной кислоты (E89) и соответствующих аминов, указанных в таблице:
илоксиметил)фенил]-1-морфолин-4-илметанон (Е91)
илоксиметил)фенил]-1-(4-пиридин-4-ил-пиперазин-1-ил)метанон (Е92)
илоксиметил)фенил]-1-[4-(4-фторфенил)пиперазин-1-ил]метанон (Е93)
Пример 94
Метиловый эфир 3-(3-циклопентил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илоксиметил)бензойной кислоты (E94)
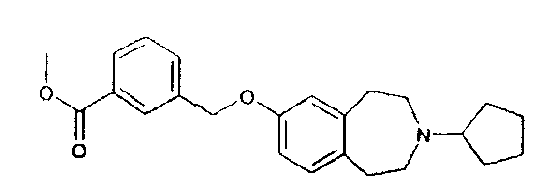
Соединение примера 94 (E94) получают по способу примера 88 (E88) из трет-бутилового эфира 7-гидрокси-1,2,4,5-тетрагидробензо[d]азепин-3-карбоновой кислоты (WO 02/40471) и метилового эфира 3-бромметилбензойной кислоты, используя способы, описанные в описании 3 (D3), описании 4 (D4) и примере 88 (E88); МС (ES+), m/e 380 [M+H]+.
Пример 95
3-(3-Циклопентил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илоксиметил)бензойная кислота (E95)
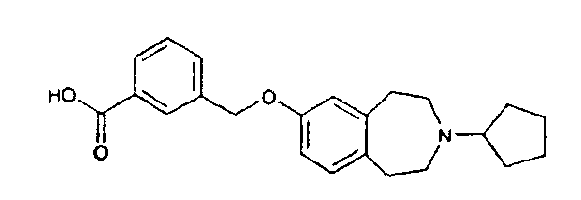
Соединение примера 95 (E95) получают из метилового эфира 3-(3-циклопентил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илоксиметил)бензойной кислоты примера 94 (E94) по способу примера 89 (E89); МС (ES+), m/e 366 [M+H]+.
Пример 96
1-[3-(3-Циклопентил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илоксиметил)фенил]-1-пирролидинилметанон (E96)
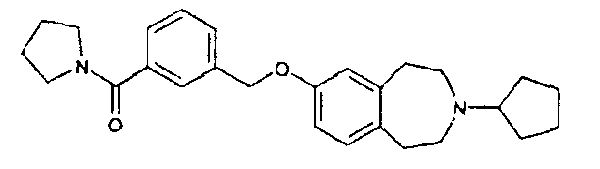
Соединение примера 96 (E96) получают из пирролидина и 3-(3-циклопентил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илоксиметил)бензойной кислоты (E95) по способу примера 90 (E90); МС (ES+), m/e 419 [M+H]+.
Примеры 97-99
Соединения примеров 97-99 (E97-E99) получают из 3-(3-циклопентил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илоксиметил)бензойной кислоты (E95) и соответствующих аминов, указанных в таблице, по способу примера 96 (E96).
илоксиметил)фенил]-1-морфолин-4-илметанон (Е97)
илоксиметил)фенил]-1-(4-пиридин-4-ил-пиперазин-1-ил)метанон (Е98)
илоксиметил)фенил]-1-[4-(4-фторфенил)пиперазин-1-ил)метанон (Е99)
Пример 100
6-(3-Циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илокси)никотинонитрил (E100)
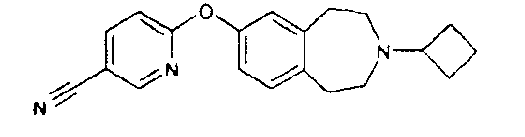
Гидрид натрия (60% дисперсия в минеральном масле, 60 мг, 1,5 ммоль) добавляют к перемешиваемому раствору 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) (200 мг, 0,9 ммоль) в диметилсульфоксиде (10 мл). Через 0,5 часа добавляют 6-хлорникотинилнитрил (250 мг, 1,8 ммоль) и реакционную смесь нагревают при 120°C в течение 6 часов. После охлаждения неочищенную реакционную смесь наносят на ионообменный картридж SCX (Varian bond-elute, 10 г) и промывают сначала метанолом, затем смесью .880 аммиак:метанол (1:9). Объединенные основные фракции упаривают в вакууме, получая указанное в заголовке соединение (E100); МС (ES+) m/e 320 [M+H]+.
Примеры 101-120
Соединения примеров 101-120 (E101-E120) получают по способу примера 100 (E100) из 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) и соответствующих ароматических хлоридов, указанных в таблице:
илокси)пиридин-3-ил]-1-морфолин-4-илметанон (Е102)
илокси)пиридин-3-ил]-1-пирролидин-1-илметанон (Е103)
илокси)никотинамид (Е104)
илокси)-N,N-диметилникотинамид (Е105)
илокси)-N-этил-N-метилникотинамид (Е106)
илокси)-N-циклопентилникотинамид (Е107)
илокси)пиридин-3-ил]-1-пиперидин-1-илметанон (Е108)
илокси)пиридин-4-ил]-1-пиперидин-1-илметанон (Е109)
илокси)пиридин-4-ил]-1-пирролидин-1-илметанон (Е110)
илокси)пиридин-4-ил]-1-морфолин-4-илметанон (Е111)
илокси)пиридин-2-ил]-1-пиперидин-1-илметанон (Е112)
илокси)пиридин-2-ил]-1-(1,1-диоксотиоморфолин-4-ил)метанон (Е113)
илокси)пиридин-2-ил]-1-пирролидин-1-илметанон (Е114)
илокси)пиридин-2-ил]-1-морфолин-4-илметанон (Е115)
илокси)пиридин-3-ил]-1-морфолин-4-илметанон (Е116)
илокси)пиридин-3-ил]-1-пиперидин-1-илметанон (Е117)
Пример 121
6-(3-Циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илокси)-N-метилникотинамид (E121)
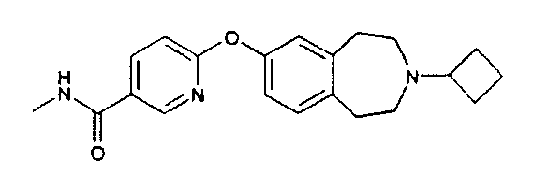
Гидрид натрия (60% дисперсия в минеральном масле, 60 мг, 1,5 ммоль) добавляют к перемешиваемому раствору 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) (200 мг, 0,9 ммоль) в диметилсульфоксиде (10 мл). Через 0,5 часа добавляют 6-хлор-N-метилникотинамид (D10) (400 мг, 2,5 ммоль) и реакционную смесь нагревают при 120°C в течение 6 часов. Реакционную смесь оставляют охлаждаться, затем неочищенную смесь наносят на ионообменный картридж SCX (Varian bond-elute, 10 г) и промывают сначала метанолом, затем смесью .880 аммиак:метанол (1:9). Объединенные основные фракции упаривают в вакууме, получая указанное в заголовке соединение (E121). 1H ЯМР (ДМСО-d6) δ 8,56 (1H, дд, J=2,4, 0,4 Гц), 8,48 (1H, ушир.м), 8,20 (1H, дд, J=8,4, 2,4 Гц), 7,16 (1H, д, J=8,0 Гц), 7,03 (1H, дд, J=8,4, 0,4 Гц), 6,91 (1H, д, J=2,4 Гц), 6,86 (1H, дд, J=8,0, 2,4 Гц), 2,87-2,77 (8H, м), 2,36 (4H, м), 2,00 (2H, м), 1,78 (2H, м), 1,58 (2H, м); МС (ES+) m/e 352 [M+H]+.
Пример 121 (Альтернативный способ 1)
6-(3-Циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илокси)-N-метилникотинамид (E121)
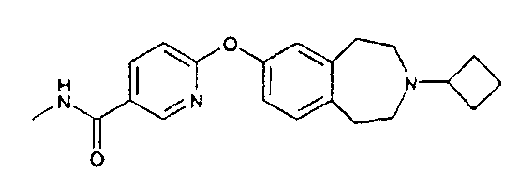
Гидрид натрия (0,331 г, 8,28 ммоль, 60% дисперсия в минеральном масле) добавляют к перемешиваемому раствору 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) (1,5 г, 6,9 ммоль) в диметилсульфоксиде (15 мл). Через 0,5 часа добавляют 6-хлор-N-метилникотинамид (D10) (2,34 г, 13,8 ммоль) и реакционную смесь нагревают при 100°C в течение 18 часов. Реакционную смесь оставляют охлаждаться до комнатной температуры и затем распределяют между этилацетатом и водой. Этилацетатный слой отделяют, а водный слой промывают дополнительным объемом этилацетата. Затем объединенные органические слои промывают водой, насыщенным соляным раствором, сушат (Na2SO4) и фильтруют. Смесь концентрируют в вакууме и полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:этанол:дихлорметан (0,5:4,5:95, затем 1:9:90), и получают указанное в заголовке соединение (E121), которое затем перекристаллизовывают из толуола. 1H ЯМР (ДМСО-d6) δ 8,56 (1H, дд, J=2,4, 0,4 Гц), 8,48 (1H, ушир.м), 8,20 (1H, дд, J=8,4, 2,4 Гц), 7,16 (1H, д, J=8,0 Гц), 7,03 (1H, дд, J=8,4, 0,4 Гц), 6,91 (1H, д, J=2,4 Гц), 6,86 (1H, дд, J=8,0, 2,4 Гц), 2,87-2,77 (8H, м), 2,36 (4H, м), 2,00 (2H, м), 1,78 (2H, м), 1,58 (2H, м); МС (ES+) m/e 352 [M+H]+.
Пример 121 (Альтернативный способ 2)
6-(3-Циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илокси)-N-метилникотинамид (E121)
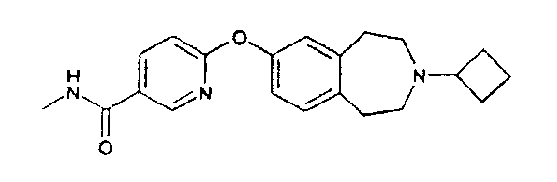
Смесь N-метил-6-(2,3,4,5-тетрагидро-1H-3-бензазепин-7-илокси)-3-пиридинкарбоксамида (D40) (1,04 г, 3,5 ммоль) в дихлорметане (12 мл), содержащем уксусную кислоту (240 мкл) при 0°C обрабатывают по каплям циклобутаноном (400 мкл, 5,3 ммоль) и затем перемешивают при комнатной температуре в течение 1 часа. Затем смесь охлаждают до 0°C, порциями добавляют триацетоксиборгидрид натрия (1,11 г, 5,3 ммоль) и перемешивают при комнатной температуре 16 часов. Раствор осторожно подщелачивают 2N раствором гидроксида натрия, перемешивают 30 минут и затем экстрагируют дихлорметаном. Объединенные экстракты промывают насыщенным соляным раствором, сушат над безводным сульфатом натрия и концентрируют в вакууме. Неочищенное вещество очищают колоночной хроматографией, элюируя сначала дихлорметаном, затем смесью .880 аммиак:метанол:дихлорметан (1:9:90), и получают указанное в заголовке соединение (E121); МС (ES+) m/e 352[M+H]+.
Пример 122
Метиловый эфир 5-(3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илокси)пиразин-2-карбоновой кислоты (E122)
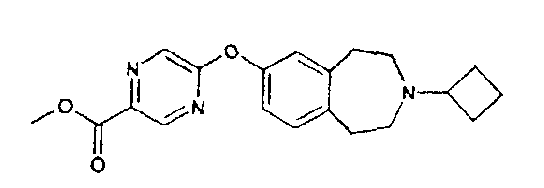
Гидрид натрия (60% дисперсия в минеральном масле, 332 мг, 8,3 ммоль) добавляют к перемешиваемому раствору 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) (1,64 г, 7,5 ммоль) в диметилформамиде (4 мл). Через 0,5 часа добавляют раствор метилового эфира 5-хлорпиразин-2-карбоновой кислоты (1,95 г, 11,3 ммоль) в диметилформамиде (8 мл) и реакционную смесь перемешивают при комнатной температуре 1 час. Реакционную смесь разбавляют дихлорметаном и органический слой промывают водой, насыщенным соляным раствором и сушат над сульфатом магния. Органический слой фильтруют, концентрируют в вакууме и полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:этанол:дихлорметан (1:9:90), и получают указанное в заголовке соединение (E122). МС (ES+) m/e 354 [M+H]+.
Пример 123a
5-(3-Циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илокси)пиразин-2-карбоновая кислота (E123a)
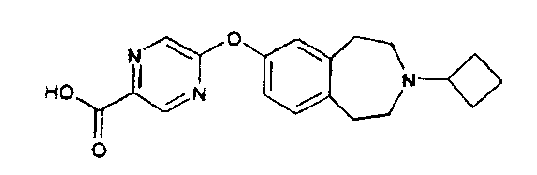
Метиловый эфир 5-(3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илокси)пиразин-2-карбоновой кислоты (E122) (880 мг, 2,5 ммоль) растворяют в смеси этанола (15 мл) и 2N раствора гидроксида натрия (4 мл). Полученную смесь перемешивают при комнатной температуре 0,5 часа и затем концентрируют в вакууме, чтобы удалить органические растворители. Затем реакционную смесь подкисляют до pH 5 (2N раствором хлористоводородной кислоты) и полученные осадки фильтруют, промывают водой и сушат в вакууме, получая указанное в заголовке соединение (E123a); МС (ES+) m/e 340 [M+H]+.
Пример 123
1-[5-(3-Циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илокси)пиразин-2-ил]-1-морфолин-4-илметанон (E123)
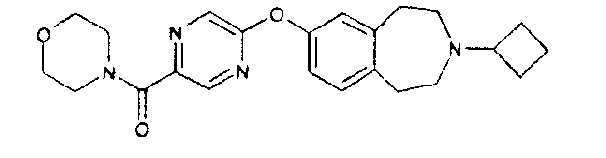
Стадия 1: 5-(3-Циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илокси)пиразин-2-
карбонилхлорид
Тионилхлорид (5 мл) медленно добавляют к 5-(3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илокси)пиразин-2-карбоновой кислоте (E123a) (485 мг). Полученную реакционную смесь перемешивают при комнатной температуре 1 час и затем нагревают с обратным холодильником еще 1 час. Реакционную смесь охлаждают, разбавляют толуолом и концентрируют в вакууме, получая указанное в заголовке соединение, которое используют без дополнительной характеристики.
Стадия 2: 1-[5-(3-Циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илокси)пиразин-2-ил]-1-морфолин-4-илметанон
Морфолин (0,17 мл, 2,0 ммоль) добавляют к перемешиваемому раствору продукта стадии 1 (394 мг, 1 ммоль) и диэтиламинометилполистирола (1,88 г, 3,2 ммоль/г, 6 ммоль) в дихлорметане (10 мл). Полученную смесь оставляют перемешиваться при комнатной температуре в течение 24 часов и фильтруют. Фильтрат концентрируют в вакууме, полученный неочищенный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:этанол:дихлорметан (1:9:90), и получают указанное в заголовке соединение (E123). МС (ES+) m/e 409 [M+H]+.
Примеры 124 и 126-127
Соединения примеров 124 и 126-127 (E124 и E126-E127) получают из продукта примера 123, стадия 1, и соответствующих аминов, указанных в таблице, по способу примера 123, стадия 2:
пиразин-2-карбоновой кислоты (Е124)
Пример 125
Метиламид 5-(3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илокси)пиразин-2-карбоновой кислоты (E125)
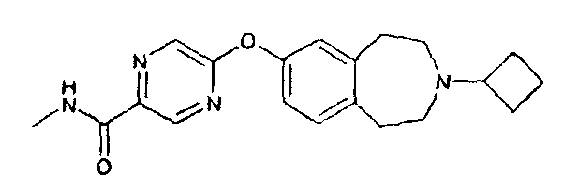
Продукт примера 123, стадия 1 (1,59 ммоль) в сухом дихлорметане (10 мл) обрабатывают метиламином (5 мл, 10 ммоль, 2M раствор в ТГФ) и перемешивают при комнатной температуре 18 часов. Смесь упаривают в вакууме, полученное неочищенное вещество наносят на ионообменный картридж SCX (Varian bond-elute, 10 г) и промывают сначала метанолом, затем смесью .880 аммиак:метанол (1:9). Затем основные фракции упаривают, неочищенный продукт очищают колоночной хроматографией, элюируя смесью .880 аммиак:этанол:дихлорметан (0,2:1,8:98 и затем 0,4:3,6:96), и получают указанное в заголовке соединение (E125). 1H ЯМР (CDCl3) δ 8,91 (1H, д, J=1,3 Гц), 8,26 (1H, д, J=1,3 Гц), 7,61 (1H, ушир.квартет, J=4,8 Гц), 7,15 (1H, м), 6,92 (2H, м), 3,03 (3H, д, J=5,1 Гц), 2,93 (4H, м), 2,79 (1H, м), 2,47 (4H, м), 2,08 (2H, м), 1,91 (2H, м), 1,70-1,62 (2H, м).
Пример 128
3-Циклобутил-7-фенокси-2,3,4,5-тетрагидро-1H-бензо[d]азепин (E128)
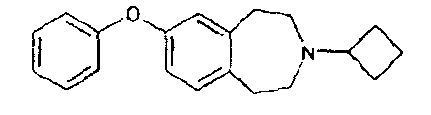
Гидрид натрия (60% дисперсия в минеральном масле, 96 мг, 2,4 ммоль) добавляют к перемешиваемому раствору 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) (435 мг, 2,0 ммоль) и бромида меди (I) (402 мг, 2,8 ммоль) в пиридине (10 мл) при 0°C. После перемешивания в течение 0,5 часа при комнатной температуре добавляют иодбензол (0,45 мл, 4,0 ммоль) и реакционную смесь нагревают с обратным холодильником в течение 24 часов. Реакционную смесь оставляют охлаждаться, фильтруют и затем фильтрат концентрируют в вакууме. Неочищенный остаток растворяют в этилацетате и промывают водой и насыщенным соляным раствором. Органический слой сушат над сульфатом магния, фильтруют, концентрируют в вакууме, полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:этанол:дихлорметан (от 0,25:2,25:97,5 до 1:9:90), и получают указанное в заголовке соединение (E128); МС (ES+) m/e 294 [M+H]+.
Примеры 129-138
Соединения примеров 129-138 (E129-E138) получают из 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) и соответствующих ароматических галогенидов, указанных в таблице, по способу примера 128 (E128):
илокси)фенил]-1-морфолин-4-илметанон (Е129)
илокси)-N-циклопропилметилбензамид (Е130)
илокси)фенил]-1-пирролидин-1-илметанон (Е131)
илокси)бензамид (Е132)
илокси)-N,N-диэтилбензамид (Е133)
илокси)-N-метилбензамид (Е134)
илокси)фенил]-1-морфолин-4-илметанон (Е135)
илокси)-N-циклопропилметилбензамид (Е136)
илокси)-N,N-диэтилбензолсульфонамид (Е138)
Пример 139
7-Бензилокси-3-циклогексил-2,3,4,5-тетрагидро-1H-бензо[d]азепин (E139)
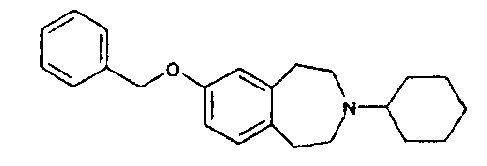
Соединение примера 139 (E139) получают из соединения описания 2 (D2) и циклогексанона по способу примера 1; МС (ES+) m/e 336 [M+H]+.
Пример 140
3-Циклобутил-7-{[2-(1-пиперидинил)-5-пиримидинил]окси}-2,3,4,5-тетрагидро-1H-3-бензазепин (E140)
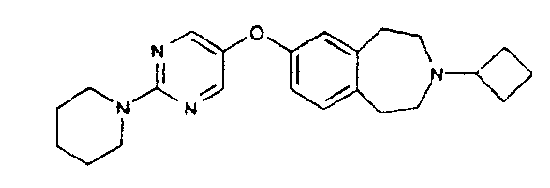
Гидрид натрия (60% дисперсия в минеральном масле, 44 мг, 1,1 ммоль) добавляют к перемешиваемому раствору 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) (200 мг, 0,92 ммоль) и бромида меди (I) (184 мг, 1,3 ммоль) в пиридине (10 мл) при 0°C. После перемешивания в течение 0,5 часа при комнатной температуре добавляют 5-бром-2-(1-пиперидинил)пиримидин (D32) (0,669 г, 2,8 ммоль) и реакционную смесь нагревают с обратным холодильником 2 часа. Реакционную смесь оставляют охлаждаться, фильтруют и фильтрат концентрируют в вакууме. Неочищенный остаток растворяют в этилацетате и промывают водой и насыщенным соляным раствором. Органический слой сушат (сульфат магния), фильтруют и концентрируют в вакууме. Полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:этанол:дихлорметан (от 0,25:2,25:97,5 до 1:9:90), и получают указанное в заголовке соединение (E140). МС (ES+) m/e 379 [M+H]+.
Примеры 141-143
Соединения примеров 141-143 (E141-E143) получают из 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) и соответствующих бромидов, указанных в таблице, по способу примера 140 (E140):
окси]-N-метил-2-пиримидинамин (Е143)
Пример 144
3-Циклобутил-7-{[2-(метилокси)-5-пиримидинил]окси-2,3,4,5-тетрагидро-1H-3-бензазепин (E144)
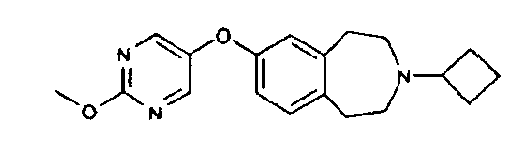
Соединение примера 144 (E144) получают из 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) и 5-бром-2-(метилокси)пиримидина (PCT Int. Appl. PCT (2002), WO 02/62423) по способу примера 140 (E140); МС (ES+) m/e 326 [M+H]+.
Примеры 145-147
Соединения примеров 145-147 (E145-E147) получают из 3-циклобутил-7-(пиперидин-4-илокси)-2,3,4,5-тетрагидро-1H-бензо[d]азепина (E6) и соответствующих кислот, указанных в таблице, по способу примера 13 (E13):
Примеры 148-150
Соединения примеров 148-150 (E148-E150) получают из 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) и соответствующих спиртов, указанных в таблице, по способу примера 5a (E5a) и затем по способу примера 5 (E5).
Примеры 151-153
Соединения примеров 151-153 (E151-E153) получают из соответствующих аминов, указанных в таблице, и морфолинкарбамоилхлорида по способу примера 52:
Примеры 154-156
Соединения примеров 154-156 (E154-E156) получают из соответствующих аминов, указанных в таблице, и 4-цианобензоилхлорида по способу примера 43 (E43):
Примеры 157-159
Соединения примеров 157-159 (E157-E159) получают из соответствующих аминов, указанных в таблице, и тетрагидропиран-4-карбоновой кислоты по способу примера 13 (E13):
Пример 160
6-{4-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-1-пиперидинил}-3-пиридинкарбонитрил (E160)
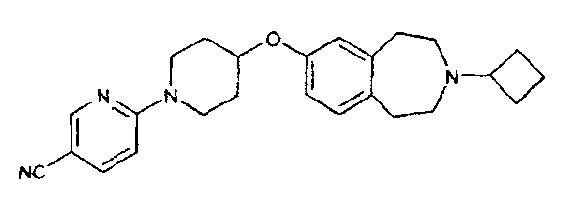
3-Циклобутил-7-(пиперидин-4-илокси)-2,3,4,5-тетрагидро-1H-бензо[d]азепин (E6) (60 мг, 0,2 ммоль), 6-хлорникотинонитрил (31 мг, 0,22 ммоль) и триэтиламин (0,03 мл, 0,22 ммоль) растворяют в ацетонитриле (2 мл) и нагревают при 180°С в микроволновом реакторе в течение 10 минут. Реакционную смесь разбавляют этилацетатом, промывают водой, насыщенным соляным раствором и сушат (сульфат магния). Органический слой фильтруют, концентрируют в вакууме, полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:этанол:дихлорметан (от 0,25:2,25:97,5 до 1:9:90), и получают указанное в заголовке соединение (Е160); МС (ES+) m/e 403 [M+H]+.
Примеры 161-166
Соединения примеров 161-166 (E161-E166) получают из 3-циклобутил-7-(пиперидин-4-илокси)-2,3,4,5-тетрагидро-1H-бензо[d]азепина (E6) и соответствующих хлоридов, указанных в таблице, по способу примера 160 (E160):
окси]-1-пиперидинил}-N-(циклопропилметил)-3-пиридинкарбоксамид (Е161)
Пример 167a
Этил 4-[(3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]бутаноат (E167a)
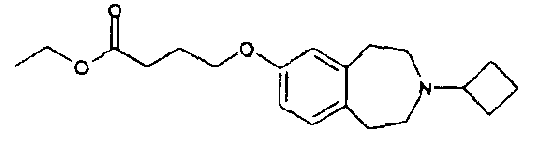
Этил 4-бромбутират (2 мл, 13,8 ммоль) добавляют к перемешиваемому раствору 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) (2,00 г, 9,2 ммоль) и карбоната калия (3,8 г, 27,6 ммоль) в 2-бутаноне (50 мл). После перемешивания при температуре кипения с обратным холодильником в течение 24 часов реакционную смесь охлаждают до комнатной температуры, фильтруют и концентрируют в вакууме. Полученное неочищенное вещество очищают колоночной хроматографией, элюируя смесью метанол:дихлорметан (5:95), и получают указанное в заголовке соединение (E167a). МС (ES+) m/e 332 [M+H]+.
Пример 167b
4-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси] бутановая кислота (E167b)
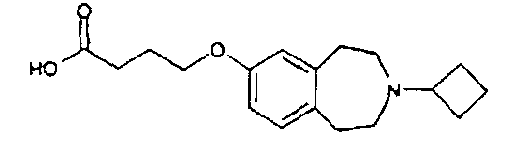
Этил 4-[(3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]бутаноат (E167a) (1,5 г, 4,5 ммоль) разбавляют этанолом (30 мл) и обрабатывают 2N раствором гидроксида натрия (7,9 мл). После перемешивания при температуре кипения с обратным холодильником в течение 24 часов реакционную смесь охлаждают до комнатной температуры, фильтруют и концентрируют в вакууме. Неочищенную смесь наносят на ионообменный картридж SCX (Varian bond-elute) и промывают водой, метанолом и смесью .880 аммиак:метанол (1:9). Объединенные основные фракции упаривают в вакууме, получая указанное в заголовке соединение (E167b) в виде аммониевой соли. МС (ES+) m/e 303 [M+H]+.
Пример 167
3-Циклобутил-7-{[4-оксо-4-(1-пиперидинил)бутил]окси}-2,3,4,5-тетрагидро-1H-3-бензазепин (E167)
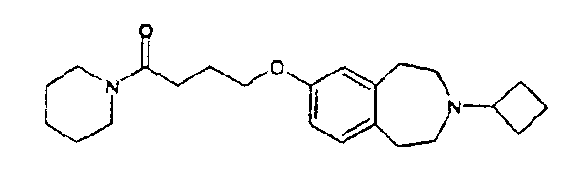
Стадия 1: 3-Циклобутил-7-{[4-(1H-имидазол-1-ил)-4-оксобутил]окси}-2,3,4,5-тетрагидро-1H-3-бензазепин
4-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]бутановую кислоту (E167b) (0,90 г, 2,8 ммоль) растворяют в диметилформамиде (10 мл) и обрабатывают 1,1'-карбонилдиимидазолом (0,59 г, 3,6 ммоль). После перемешивания при комнатной температуре в течение 2,5 часов реакционную смесь концентрируют в вакууме. Неочищенный остаток растворяют в дихлорметане, промывают насыщенным соляным раствором и сушат (сульфатом натрия). Органический слой фильтруют, концентрируют в вакууме и неочищенный остаток используют на следующей стадии без дополнительной очистки.
Стадия 2: 3-Циклобутил-7-{[4-оксо-4-(1-пиперидинил)бутил]окси}-2,3,4,5-тетрагидро-1H-3-бензазепин (E167)
Пиперидин (0,1 мл, 1,1 ммоль) добавляют к перемешиваемому раствору 3-циклобутил-7-{[4-(1H-имидазол-1-ил)-4-оксобутил]окси}-2,3,4,5-тетрагидро-1H-3-бензазепина (E167, стадия 1) (150 мг, 0,42 ммоль) в дихлорметане (5 мл). После перемешивания при комнатной температуре в течение 5 дней реакционную смесь концентрируют в вакууме, полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:этанол:дихлорметан (1:9:90), и получают указанное в заголовке соединение (E167); МС (ES+) m/e 371 [M+H]+.
Примеры 168-170
Соединения примеров 168-170 (E168-E170) получают из соединения примера 167, стадия 1, по способу примера 167, стадия 2, заменяя пиперидин на соответствующий амин, указанный в таблице:
Примеры 171-176
Соединения примеров 171-176 (E171-E176) получают из соединения примера 123, стадия 1, и соответствующих аминов, указанных в таблице, по способу примера 123, стадия 2 (E123):
Пример 177a
5-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-2-пиримидинкарбонитрил (E177a)
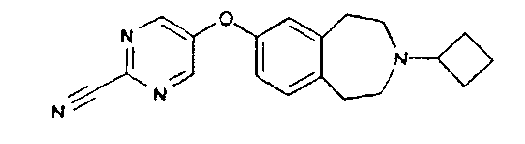
3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ол (E3) (1,81 г, 8,33 ммоль) растворяют в пиридине (40 мл) и добавляют гидрид натрия (60% в минеральном масле, 0,40 г, 10,0 ммоль) при перемешивании в атмосфере аргона при 0°С. Смесь оставляют перемешиваться в течение 5 минут. Добавляют бромид меди (I) (1,68 г, 11,7 ммоль) и смесь оставляют нагреваться до комнатной температуры в течение 30 минут. Добавляют 5-бром-2-пиримидинкарбонитрил (D38) (2,30 г, 12,5 ммоль) в пиридине (8 мл) и смесь нагревают при 100°С в течение 1 часа. Смесь оставляют охлаждаться до комнатной температуры и растворитель удаляют в вакууме. Неочищенный продукт очищают колоночной хроматографией, элюируя смесью .880 аммиак:метанол:дихлорметан (0,2:1,8:98), и получают указанное в заголовке соединение (E177a); МС (ES+) m/e 321 [M+H]+.
Пример 177b
5-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-2-пиримидинкарбоновая кислота (E177b)
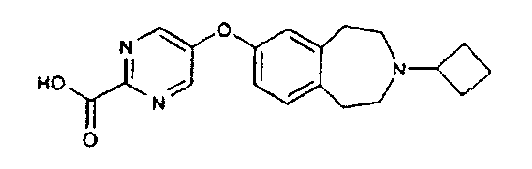
5-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-2-пиримидинкарбонитрил (E177a) (1,22 г, 3,81 ммоль) растворяют в этаноле (20 мл), обрабатывают 10% раствором гидроксида натрия (20 мл) и нагревают с обратным холодильником в течение 90 минут. Смесь охлаждают до комнатной температуры и наносят на ионообменную колонку SCX (Varian bond-elute, 10 г), элюируя водой, метанолом и затем смесью 0,880 аммиак:метанол (1:9). Основные фракции объединяют и концентрируют в вакууме, получая указанное в заголовке соединение (E177b); МС (ES+) m/e 340 [M+H]+.
Пример 177
3-Циклобутил-7-{[2-(4-морфолинилкарбонил)-5-пиримидинил]окси}-2,3,4,5-тетрагидро-1H-3-бензазепин (E177)
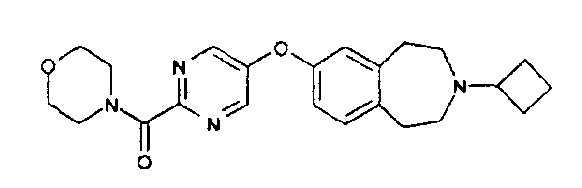
5-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-2-пиримидинкарбоновую кислоту (E177b) (130 мг, 0,37 ммоль) растворяют в диметилформамиде (4 мл), обрабатывают 1,1'-карбонилдиимидазолом (180 мг, 1,11 ммоль) и оставляют перемешиваться в атмосфере аргона при комнатной температуре в течение 5 часов. Смесь обрабатывают морфолином (0,19 мл, 2,22 ммоль) и оставляют перемешиваться при комнатной температуре в течение 18 часов. Реакционную смесь концентрируют в вакууме, полученный остаток очищают колоночной хроматографией, элюируя смесью 0,880 аммиак:метанол:дихлорметан (0,5:1,5:95), и получают указанное в заголовке соединение (E177). МС (ES+) m/e 409 [M+H]+.
Примеры 178-186
Соединения примеров 178-186 (E178-E186) получают из соединения примера 177b (E177b) и соответствующих аминов, указанных в таблице, по способу примера 177 (E177):
Пример 187a
5-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-2-пиридинкарбоновая кислота (E187a)
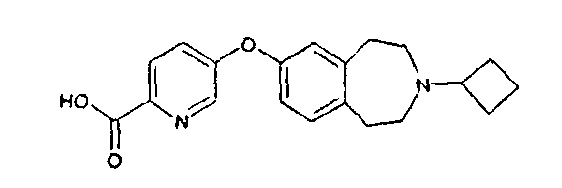
Указанное в заголовке соединение (E187a) получают из 5-[(3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-2-пиридинкарбонитрила (Е206) по способу примера 177b (E177b); МС (ES+) m/e 339 [M+H]+.
Примеры 188-195
Соединения примеров 188-195 (E188-E195) получают из 5-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-2-пиридинкарбоновой кислоты (E187a) и соответствующих аминов, указанных в таблице, по способу примера 177 (E177):
Пример 196a
Метиловый эфир 6-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-пиридинкарбоновой кислоты
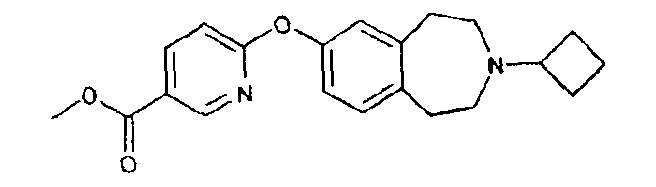
Указанное в заголовке соединение получают из 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) и метил 6-хлор-3-пиридинкарбоксилата по способу, описанному для соединения E122; МС
(ES+) m/e 353 [M+H]+.
Пример 196b
6-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-пиридинкарбоновая кислота (E196b)
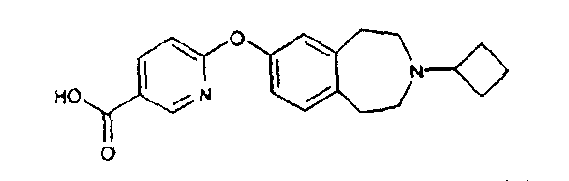
Указанное в заголовке соединение получают из соединения примера 196a (E126a) по способу примера 123a (E123a); МС (ES+) m/e 339 [M+H]+.
Пример 196
6-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-N-циклопропил-3-пиридинкарбоксамид (E196)
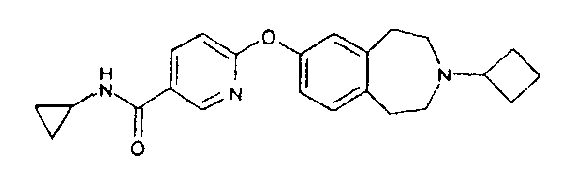
Карбонилдиимидазол (142 мг, 0,88 ммоль) добавляют к перемешиваемому раствору 6-[(3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-пиридинкарбоновой кислоты (E196b) (150 мг, 0,44 ммоль) в дихлорметане (5 мл). После перемешивания при комнатной температуре в течение 3 часов добавляют циклопропиламин (0,15 мл, 2,2 ммоль) и смесь оставляют перемешиваться еще 18 часов. Реакционную смесь наносят на ионообменный картридж SCX (Varian bond-elute, 10 г) и промывают сначала метанолом, затем смесью .880 аммиак:метанол (1:9). Объединенные основные фракции концентрируют в вакууме, получая указанное в заголовке соединение (E196). МС (ES+) m/e 378 [M+H]+.
Примеры 197-202
Соединения примеров 197-202 (E197-E202) получают из 6-[(3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-пиридинкарбоновой кислоты (E196b) и соответствующих аминов, указанных в таблице, по способу примера 196 (E196):
Примеры 203-205
Соединения примеров 203-205 (E203-205) получают из 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) и соответствующих ароматических иодидов, указанных в таблице, по способу примера 128 (E128):
Пример 206
5-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-2-пиридинкарбонитрил (E206)
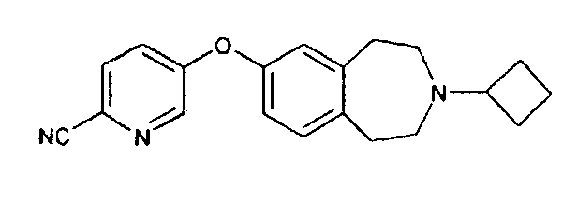
Указанное в заголовке соединение (E206) получают из 3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ола (E3) и 5-иод-2-пиридинкарбонитрил (Biochemical Journal, 1973, 131 (4), 625) по способу, описанному для соединения E177a; МС (ES+) m/e 320 [M+H]+.
Примеры 207-208
Соединения примеров 207-208 (E207-208) получают из 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) и соответствующих ароматических хлоридов, указанных в таблице, по способу примера 100 (E100):
Пример 209
N-{6-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-пиридинил}ацетамид (E209)
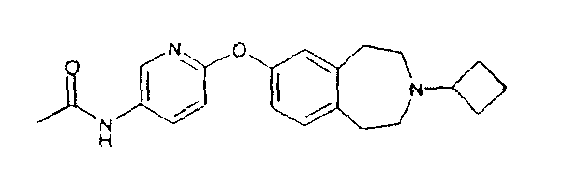
Железные опилки (451 мг, 8,07 ммоль) добавляют к перемешиваемому раствору 3-циклобутил-7-[(5-нитро-2-пиридинил)окси)]-2,3,4,5-тетрагидро-1H-3-бензазепина (E208) (550 мг, 1,62 ммоль) в смеси уксусная кислота: раствор уксусного ангидрида (1:1, 10 мл) и нагревают при 80°C 16 часов. Реакционную смесь охлаждают, выливают на лед и доводят до pH8 бикарбонатом натрия. Продукт экстрагируют в этилацетат, затем органический экстракт промывают насыщенным соляным раствором и сушат над сульфатом натрия. Остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:метанол:дихлорметан (0,5:4,5:95), и получают указанное в заголовке соединение (E209). МС (ES+) m/e 352 [M+H]+.
Пример 210a
3-Циклобутил-7-[(5-нитро-1,3-тиазол-2-ил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепин (E210a)
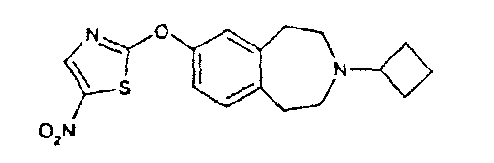
Гидрид натрия (60% дисперсия в минеральном масле, 150 мг, 3,66 ммоль) добавляют к перемешиваемому раствору 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) (530 мг, 2,43 ммоль) в диметилформамиде (10 мл) при 5°C. Через 0,5 часа добавляют раствор 2-бром-5-нитро-1,3-тиазола (1,0 г, 4,78 ммоль) в диметилформамиде (5 мл) и реакционную смесь оставляют нагреваться до комнатной температуры при перемешивании в течение 2 часов. Реакционную смесь разбавляют этилацетатом, органический слой промывают водой, насыщенным соляным раствором, сушат (сульфатом натрия) и концентрируют в вакууме. Очищают колоночной хроматографией, элюируя смесью 0,880 аммиак:метанол:дихлорметан (0,25:2,25:97,5), и получают указанное в заголовке соединение (E210a); МС (ES+) m/e 346 [M+H]+.
Пример 210
N-{2-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-1,3-тиазол-5-ил}ацетамид (E210)
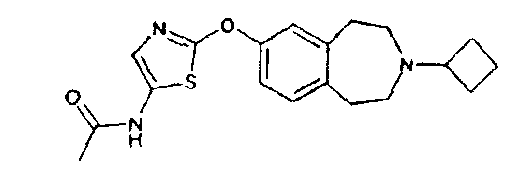
Железный порошок (162 мг, 2,9 ммоль) добавляют к перемешиваемому раствору 3-циклобутил-7-[(5-нитро-1,3-тиазол-2-ил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепина (E210a) (162 мг, 0,47 ммоль) в уксусной кислоте (1 мл) и уксусном ангидриде (1 мл). Реакционную смесь перемешивают при 80°C в течение 16 часов, затем охлаждают и выливают на лед. Раствор подщелачивают до pH 8 (бикарбонатом натрия) и полученную смесь экстрагируют этилацетатом. Органический слой промывают насыщенным соляным раствором и сушат (сульфатом натрия). Концентрирование в вакууме с последующей очисткой полученного остатка колоночной хроматографией (элюируют смесью .880 аммиак:метанол:дихлорметан (0,3:2,7:97) дает указанное в заголовке соединение (E210). МС (ES+) m/e 358 [M+H]+.
Пример 211
3-Циклобутил-7-[(5-нитро-2-тиенил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепин (E211)
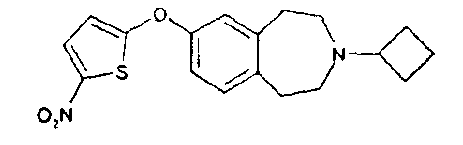
Смесь 2-бром-5-нитротиофена (478 мг, 2,3 ммоль), 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) (500 мг, 2,3 ммоль) и карбоната калия (765 мг, 5,5 ммоль) в диметилформамиде (10 мл) перемешивают при 80°C в течение 16 часов. Реакционную смесь охлаждают, разбавляют этилацетатом и промывают водой, насыщенным соляным раствором и сушат (сульфатом натрия). Концентрирование в вакууме и очистка полученного остатка колоночной хроматографией (элюируют смесью .880 аммиак:метанол:дихлорметан (1:8:300) дает указанное в заголовке соединение (E211); МС (ES+) m/e 345 [M+H]+.
Пример 212
N-{5-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-2-тиенил}ацетамид (E212)
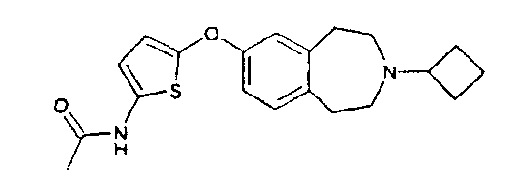
Соединение примера 212 (E212) получают из 3-циклобутил-7-[(5-нитро-2-тиенил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепина (E211) по способу примера 210 (E210); МС (ES+) m/e 357 [M+H]+.
Пример 213a
3-Циклобутил-7-{[6-(метилокси)-3-пиридинил]окси}-2,3,4,5-тетрагидро-1H-3-бензазепин (E213a)
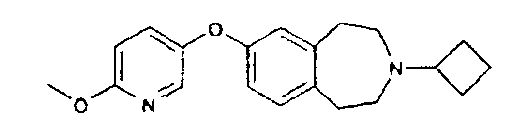
Указанное в заголовке соединение получают из 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) и 5-бром-2-метоксипиридина по способу примера 128 (E128); МС (ES+) m/e 325 [M+H]+.
Пример 213
5-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-2(1H)-пиридинон (E213)
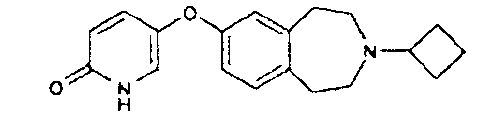
3-Циклобутил-7-{[6-(метилокси)-3-пиридинил]окси}-2,3,4,5-тетрагидро-1H-3-бензазепин (E213a) (69 мг, 0,21 ммоль) растворяют в насыщенном растворе хлористого водорода в этаноле (5 мл). Реакционную смесь перемешивают с обратным холодильником 18 часов, охлаждают и концентрируют в вакууме. Полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:метанол:дихлорметан (1:9:90), и получают указанное в заголовке соединение (E213). МС (ES+) m/e 311 [M+H]+.
Пример 214
1-{6-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-пиридинил}этанон (E214)
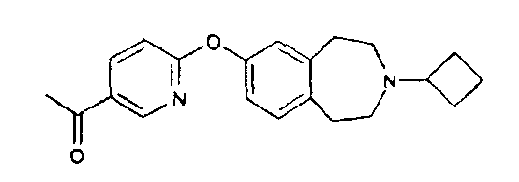
Соединение примера 214 (E214) получают из 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) и 1-(6-хлорпиридин-3-ил)этанона по способу примера 100 (E100); МС (ES+) m/e 337 [M+H]+.
Пример 215
3-Циклобутил-7-{[5-(1H-пиразол-5-ил)-2-пиридинил]окси}-2,3,4,5-тетрагидро-1H-3-бензазепин (E215)
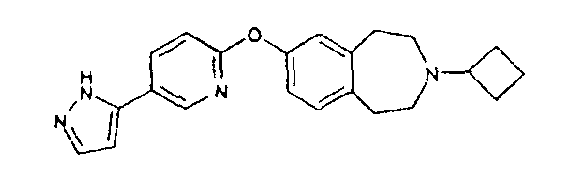
Смесь (2E)-1-{6-[(3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-пиридинил}-3-(диметиламино)-2-пропен-1-она (D53) (195 мг, 0,5 ммоль) и гидрата гидразина (0,4 мл) в метаноле (3 мл) нагревают с обратным холодильником в течение 24 часов. Реакционную смесь охлаждают, наносят на ионообменный картридж SCX (Varian bond-elute, 10 г) и промывают сначала метанолом, затем смесью .880 аммиак/метанол (1:9). Объединенные основные фракции концентрируют в вакууме, полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:метанол:дихлорметан (1:9:90), и получают указанное в заголовке соединение (E215). МС (ES+) m/e 361 [M+H]+.
Пример 216
3-Циклобутил-7-{[5-(5-метил-1,3,4-оксадиазол-2-ил)-2-пиридинил]окси}-2,3,4,5-тетрагидро-1H-3-бензазепин (E216)
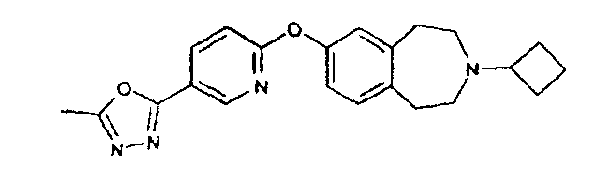
Смесь триэтилортоацетата (3 мл) и 6-[(3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-пиридинкарбогидразида (D54) (185 мг, 0,52 ммоль) нагревают с обратным холодильником в течение 16 часов. Реакционную смесь концентрируют, полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:метанол:дихлорметан (0,1:5:95), и получают указанное в заголовке соединение (E216). МС (ES+) m/e 377 [M+H]+.
Пример 217
1-{6-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-пиридинил}-2-пирролидон (E217)
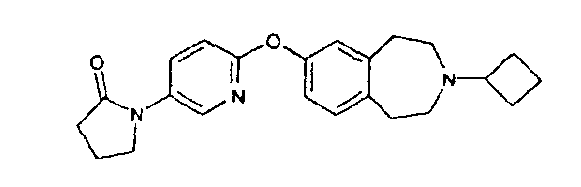
Смесь 3-циклобутил-7-[(5-иод-2-пиридинил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепина (E207) (252 мг, 0,6 ммоль), 2-пирролидинона (153 мг, 1,8 ммоль), карбоната калия (83 мг, 0,6 ммоль) и медного порошка (126 мг, 1,2 ммоль) нагревают в микроволновом реакторе при 150°C в течение 1 минуты. Реакционную смесь разбавляют 2-пирролидиноном (1 г, 12 ммоль) и нагревают еще 20 минут при 200°C. Реакционную смесь охлаждают, наносят на ионообменный картридж SCX (Varian bond-elute, 10 г) и промывают сначала метанолом, затем смесью .880 аммиак/метанол. Объединенные основные фракции концентрируют в вакууме, полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:метанол:дихлорметан (1:9:90), и получают указанное в заголовке соединение (E217). МС (ES+) m/e 378 [M+H]+.
Пример 218
1-{6-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-пиридинил}-2-пиперидинон (E218)
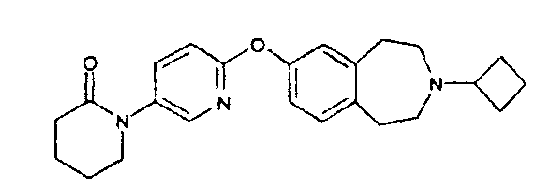
Соединение примера 218 (E218) получают из 3-циклобутил-7-[(5-иод-2-пиридинил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепина (E207) и 2-пиперидинона по способу примера 217 (E217); МС (ES+) m/e 392 [M+H]+.
Пример 219
1-{6-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-пиридинил}-2-азетидинон (E219)
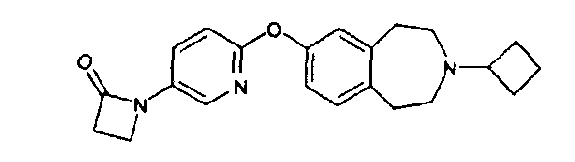
Карбонат цезия (678 мг, 1,04 ммоль) добавляют к раствору 2-азетидинона (308 мг, 4,3 ммоль) в диоксане (1 мл). Смесь нагревают в микроволновом реакторе при 150°C в течение 1 минуты, затем добавляют смесь 3-циклобутил-7-[(5-иод-2-пиридинил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепина (E207) (294 мг, 0,7 ммоль), транс-1,2-диаминоциклогексана (0,02 мл) и иодида меди (I) (126 мг, 1,2 ммоль) и полученную смесь нагревают в микроволновом реакторе при 180°С в течение 1 часа. Реакционную смесь охлаждают, наносят на картридж SCX (Varian bond-elute, 10 г) и промывают сначала метанолом, затем смесью .880 аммиак/метанол (1:9). Объединенные основные фракции концентрируют в вакууме, полученный остаток очищают колоночной хроматографией (0,5:2,5:97,5), получая указанное в заголовке соединение (E219). МС (ES+) m/e 364 [M+H]+.
Пример 220
3-{6-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-пиридинил}-1,3-оксазолидин-2-он (E220)
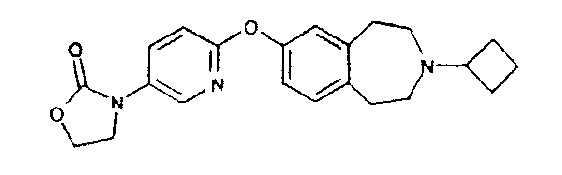
Соединение примера 220 (E220) получают из 3-циклобутил-7-[(5-иод-2-пиридинил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепина (E207) и 1,3-оксазолидин-2-она по способу примера 219 (E219); МС (ES+) m/e 380 [M+H]+.
Пример 221
3-Циклобутил-7-{[5-(1H-пиразол-1-ил)-2-пиридинил]окси}-2,3,4,5-тетрагидро-1H-3-бензазепин (E221)
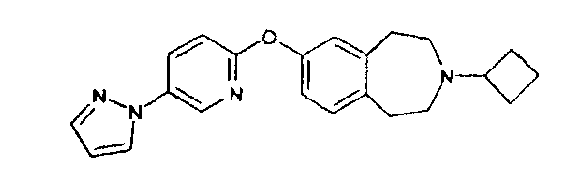
Смесь 3-циклобутил-7-[(5-иод-2-пиридинил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепина (E207) (294 мг, 0,7 ммоль), пиразола (58 мг, 0,84 ммоль), карбоната цезия (479 мг, 1,5 ммоль), иодида меди (I) (7 мг, 0,04 ммоль) и 1,10 фенантролина (13 мг, 0,07 ммоль) в диоксане (2 мл) нагревают в микроволновом реакторе при 180°C в течение 20 минут. Реакционную смесь разбавляют этилацетатом и промывают насыщенным раствором хлорида аммония, водой, насыщенным соляным раствором и сушат (сульфатом магния). Органический слой фильтруют, концентрируют в вакууме, полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:метанол:дихлорметан (0,5:4,5:95), и получают указанное в заголовке соединение (E221); МС (ES+) m/e 361 [M+H]+.
Пример 222
3-Циклобутил-7-{[5-(3,5-диметил-4-изоксазолил)-2-пиридинил]окси}-2,3,4,5-тетрагидро-1H-3-бензазепин (E222)
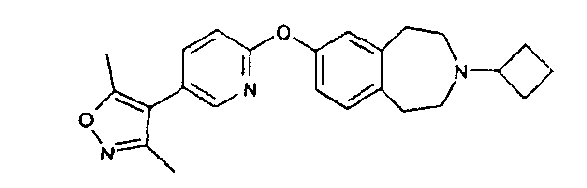
Смесь 3-циклобутил-7-[(5-иод-2-пиридинил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепина (E207) (252 мг, 0,6 ммоль), 3,5 диметил-4-изоксазолилборной кислоты (168 мг, 1,2 ммоль) и тетракис(трифенилфосфин)палладия (0) в 2M растворе карбоната натрия (5 мл) и диметиловом эфире этиленгликоля (10 мл) перемешивают с обратным холодильником в течение 14 часов. Реакционную смесь разбавляют этилацетатом, промывают насыщенным раствором бикарбоната натрия, водой, насыщенным соляным раствором и сушат (сульфатом натрия). Органический слой фильтруют, концентрируют в вакууме, полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:метанол:дихлорметан (0,5:4,5:95), и получают указанное в заголовке соединение (E222); МС (ES+) m/e 390 [M+H]+.
Пример 223
6-[(3-Циклопентил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-N-метил-3-пиридинкарбоксамид (E223)
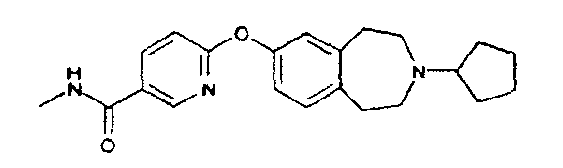
N-Метил-6-(2,3,4,5-тетрагидро-1H-3-бензазепин-7-илокси)-3-пиридинкарбоксамид (D40) (150 мг, 0,5 ммоль) растворяют в 2,5% растворе уксусной кислоты в метаноле (5 мл) и обрабатывают по каплям циклопентаноном (0,09 мл, 1 ммоль). Смесь перемешивают 30 минут и затем добавляют цианоборгидрид (полистирилметил)триметиламмония (2,04 ммоль/г, 490 мг, 0,1 ммоль). Реакционную смесь перемешивают при комнатной температуре 14 часов, наносят на картридж SCX (Varian bond-elute, 10 г) и промывают сначала метанолом, затем смесью .880 аммиак/метанол. Объединенные основные фракции концентрируют в вакууме, полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:метанол:дихлорметан (0,25:2,25:97,5), и получают указанное в заголовке соединение (E223). МС (ES+) m/e 366 [M+H]+.
Пример 224
N-Метил-6-{[3-(2-метилциклопентил)-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил]окси}-3-пиридинкарбоксамид (E224)
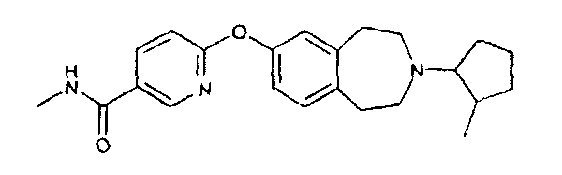
Соединение примера 224 (E224) получают из N-метил-6-(2,3,4,5-тетрагидро-1H-3-бензазепин-7-илокси)-3-пиридинкарбоксамида (D40) и 2-метилциклопентанона по способу примера 223; МС (ES+) m/e 380 [M+H]+.
Пример 225
6-[(3-Циклобутил-8-иод-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-N-метил-3-пиридинкарбоксамид (E225)
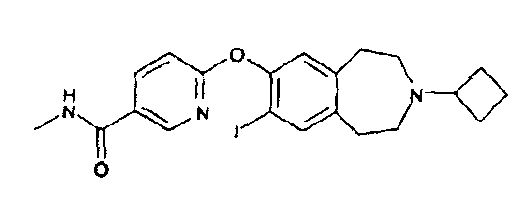
N-Метил-6-(8-иод-2,3,4,5-тетрагидро-1H-3-бензазепин-7-илокси)-3-пиридинкарбоксамид (D43) (423 мг, 1,0 ммоль) растворяют в 2,5% растворе уксусной кислоты в метаноле (5 мл) и обрабатывают по каплям циклобутаноном (0,11 мл, 1,5 ммоль). Смесь перемешивают 30 минут и затем добавляют цианоборгидрид (полистирилметил)триметиламмония (2,0 ммоль/г, 1 г, 2 ммоль). Реакционную смесь перемешивают при комнатной температуре 18 часов, наносят на ионообменный картридж SCX (Varian bond-elute, 10 г) и промывают сначала метанолом, затем смесью .880 аммиак:метанол (1:9). Объединенные основные фракции концентрируют в вакууме, полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:метанол:дихлорметан (0,5:2,25:97,5), и получают указанное в заголовке соединение (E225). МС (ES+) m/e 478 [M+H]+.
Пример 226
3-Циклобутил-7-иод-8-[(фенилметил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепин (E226)
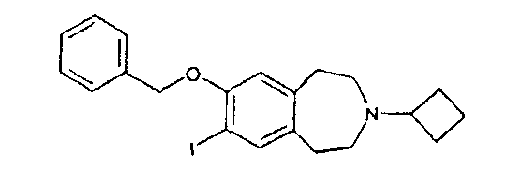
Соединение примера 226 (E226) получают из 7-иод-8-[(фенилметил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепина (D45) и циклобутанона по способу примера 225 (E225); МС (ES+) m/e 434 [M+H]+.
Пример 227
3-Циклобутил-7-{[6-метил-4-(метилокси)-2-хинолинил]окси}-2,3,4,5-тетрагидро-1H-3-бензазепин (E227)
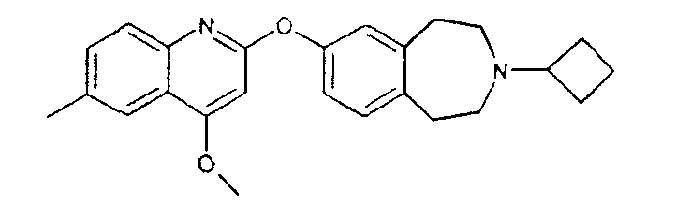
Смесь 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) (58 мг, 0,267 ммоль), 2-хлор-6-метил-4-(метилокси)хинолина (WO 99/55677) (56 мг, 0,027 ммоль) и карбоната цезия (260 мг, 0,801 ммоль) в сухом ДМФ (3 мл) нагревают при 150°C в течение 2×30 минут (300W) в микроволновом реакторе. Охлажденную реакционную смесь распределяют между этилацетатом (3×20 мл) и водой (30 мл). Объединенные органические слои промывают насыщенным соляным раствором (2×30 мл), сушат (Na2SO4), фильтруют и концентрируют в вакууме. Полученный остаток очищают колоночной хроматографией на силикагеле, элюируя смесью .880 аммиак:метанол:дихлорметан (0,5:4,5:95), и получают указанное в заголовке соединение (E227); МС (ES+) m/e 389 [M+H]+.
Примеры 228-230
Соединения примеров 228-230 (E228-E230) получают из 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) и соответствующих ароматических галогенидов, указанных в таблице, по способу примера 227:
ацетамид (S. Carboni, Gazz. Chim. Ital., 1966, 96(11), 1456-1469)
Пример 231
Диметил 6-[(3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-2,3-пиридиндикарбоксилат (E231)
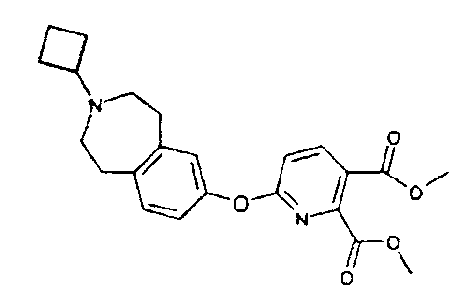
Смесь 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) (1,5 г), диметил 6-хлор-2,3-пиридиндикарбоксилата (1,58 г; Kenji Niiyama et al. Bioorg. Med. Chem. Lett. 12, 21, 2002, 3041-3054) и карбоната цезия (4,4 г) в сухом ДМФ (30 мл) нагревают при 80°C в течение 3 ч. Охлажденную смесь распределяют между водой (20 мл) и этилацетатом (3×100 мл), объединенные органические экстракты промывают насыщенным соляным раствором (2×100 мл) и сушат (Na2SO4). Растворитель упаривают, получая масло, которое очищают колоночной хроматографией, элюируя смесью .880 аммиак:метанол:дихлорметан (0,5:4,5:95), и получают указанное в заголовке соединение (E231); МС (ES+) m/e 411 [M+H]+.
Пример 232
Динатрия 6-[(3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-2,3-пиридиндикарбоксилат (E232)
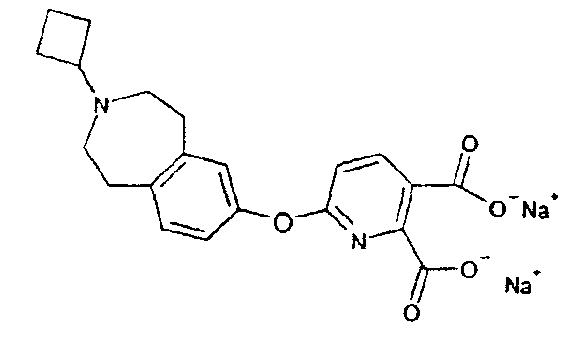
Раствор гидроксида натрия (0,66 г) в воде (3 мл) добавляют к раствору диметил 6-[(3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-2,3-пиридиндикарбоксилата (E231) (1,69 г, 4,12 ммоль) в этаноле (20 мл) при комнатной температуре. Смесь энергично перемешивают при комнатной температуре в течение 4 ч и полученный осадок отфильтровывают, получая указанное в заголовке соединение в виде бесцветного твердого вещества (E232); МС (ES+) m/e 383 [M+H]+.
Пример 233
2-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-5H-пирроло[3,4b]пиридин-5,7(6Н)-дион (E233)
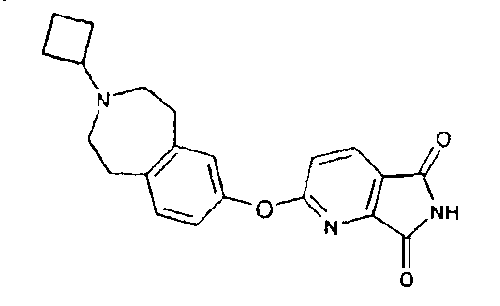
Суспензию динатрия 6-[(3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-2,3-пиридиндикарбоксилата (E232) (0,2 г, 0,52 ммоль) в уксусном ангидриде (2 мл) перемешивают и нагревают при 120°C в течение 20 мин. Охлажденную смесь концентрируют в вакууме, к остатку добавляют ацетамид (0,1 г) и смесь нагревают при 160°C в течение 0,5 ч. Затем охлажденную смесь очищают колоночной хроматографией, элюируя смесью .880 аммиак:метанол:дихлорметан (0,5:4,5:95). Полученное бледно-желтое твердое вещество перетирают с эфиром (5 мл) и фильтруют, получая указанное в заголовке соединение (E233); МС (ES+) m/e 364[M+H]+.
Пример 234
2-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-7-гидрокси-6,7-дигидро-5H-пирроло[3,4-b]пиридин-5-он (E234)
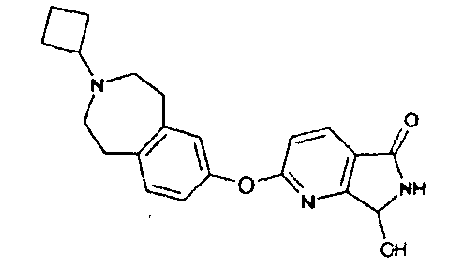
Перхлорат магния (0,89 г) добавляют к раствору 2-[(3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-5H-пирроло[3,4-b]пиридин-5,7(6H)-диона (E233) (0,72 г, 1,98 ммоль) в смеси хлороформ:метанол (1:1; 20 мл) при 0°C в атмосфере аргона. Добавляют боргидрид натрия (113 мг) и смесь перемешивают в течение 0,5 ч. рН смеси доводят до 2 с помощью HCl (2M), перемешивают еще 0,5 ч, затем доводят до pH 11 гидроксидом натрия (2N). Затем смесь экстрагируют дихлорметаном, объединенные органические экстракты сушат (Na2SO4) и упаривают. Остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:метанол:дихлорметан (1:9:90), и получают указанное в заголовке соединение (E234); МС (ES+) m/e 366 [M+H]+.
Пример 235
2-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-6,7-дигидро-5H-пирроло[3,4-b]пиридин-5-он (E235)
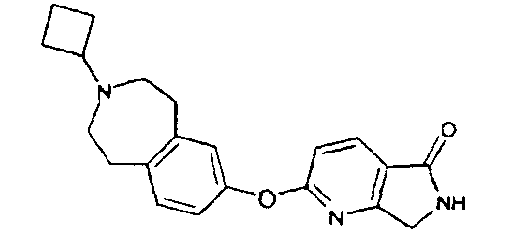
Смесь 2-[(3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-7-гидрокси-6,7-дигидро-5H-пирроло[3,4-b]пиридин-5-она (E234) (90 мг, 0,25 ммоль) и триэтилсилана (0,1 мл) в трифторуксусной кислоте (0,1 мл) энергично перемешивают при комнатной температуре в течение 1 ч. Смесь концентрируют в вакууме и остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:метанол:дихлорметан (1:9:90); МС (ES+) m/e 350 [M+H]+.
Пример 236
6-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-пиридинамин (E236)
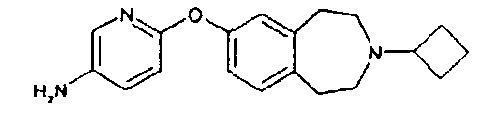
3-Циклобутил-7-[(5-нитро-2-пиридинил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепин (E208) (100 мг, 0,29 ммоль) растворяют в этаноле (10 мл). Добавляют палладий (20 мг, 10% на угольной пасте) и реакционную смесь перемешивают при комнатной температуре в атмосфере водорода (1 атмосфера) в течение 12 часов. Реакционную смесь фильтруют через целит и фильтрат концентрируют в вакууме, получая указанное в заголовке соединение (E236); МС (ES+) m/e 310 [M+H]+.
Пример 237
Морфолин-4-карбоновой кислоты [6-(3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илокси)пиридин-3-ил]амид (E237)
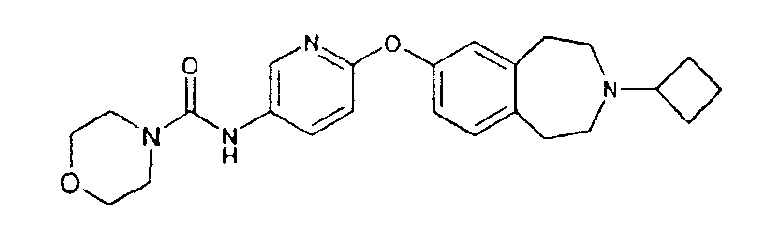
Морфолин-4-карбонилхлорид (0,15 мл, 1,38 ммоль) добавляют к перемешиваемому раствору 6-[(3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-пиридинамина (E236) (77 мг, 0,25 ммоль) и триэтиламина (0,04 мл, 0,30 ммоль) в дихлорметане (5 мл) при 0°C. Реакционную смесь нагревают до комнатной температуры и оставляют перемешиваться в течение 24 часов. Реакционную смесь наносят на ионообменный картридж SCX (Varian bond-elute, 5 г) и промывают сначала метанолом, затем смесью .880 аммиак:метанол (1:9). Объединенные основные фракции концентрируют в вакууме и полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:метанол:дихлорметан (0,5:4,5:95), и получают указанное в заголовке соединение; МС (ES+) m/e 423 [M+H]+.
Примеры 238-240
Соединения примеров 238-240 получают из 6-[(3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-пиридинамина (E236) и соответствующих карбонилхлоридов или хлорангидридов, указанных в таблице, по способу примера 237 (E237):
хлорангидрид
илокси)пиридин-3-ил]амид (E238)
илокси)пиридин-3-ил]амид (E239)
илокси)пиридин-3-ил]изобутирамид (E240)
Пример 241
Тетрагидропиран-4-карбоновой кислоты [6-(3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илокси)пиридин-3-ил]амид (E241)
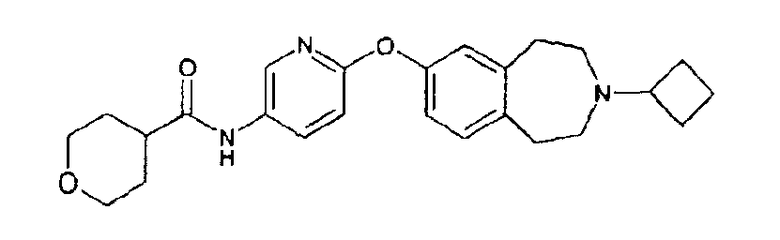
Тетрагидропиран-4-карбоновую кислоту (252 мг, 1,94 ммоль), 1-гидроксибензотриазолгидрат (262 мг, 1,94 ммоль) и N-циклогексилкарбодиимид N'-метилполистирол (1,7 ммоль/г, 2,3 г, 3,88 ммоль) перемешивают при комнатной температуре в дихлорметане (10 мл) в течение 15 минут. Добавляют 6-[(3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-пиридинамин (E236) (300 мг, 0,97 ммоль) и перемешивание продолжают в течение 16 часов. Реакционную смесь наносят на ионообменный картридж SCX (Varian bond-elute, 5 г) и промывают сначала метанолом, затем смесью .880 аммиак/метанол. Объединенные основные фракции концентрируют в вакууме, полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:метанол:дихлорметан (0,5:4,5:95), и получают указанный в заголовке продукт (E241); МС (ES+) m/e 422 [M+H]+.
Пример 242
3-Циклобутил-7-[5-(4,6-диметоксипиримидин-2-ил)пиридин-2-илокси]-2,3,4,5-тетрагидро-1H-бензо[d]азепин (E242)
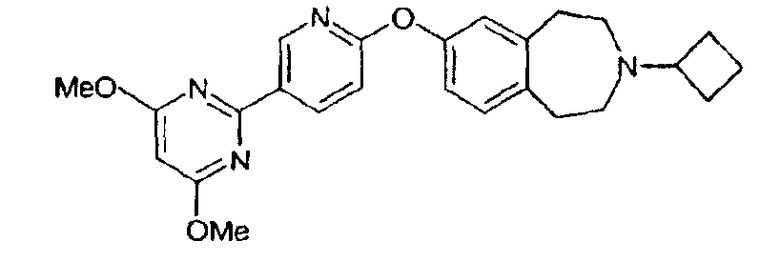
3-Циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ол (E3) (125 мг, 0,58 ммоль), 2-(6-хлорпиридин-3-ил)-4,6-диметоксипиримидин (145 мг, 0,58 ммоль), карбонат кальция (720 мг, 2,2 ммоль) и диметилформамид (4 мл) нагревают в микроволновом реакторе при 180°С в течение 900 секунд при 300 Вт. Смесь разбавляют этилацетатом, промывают водой, затем насыщенным соляным раствором и сушат над сульфатом натрия. Остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:метанол:дихлорметан (0,2:1,8:98), и получают указанный в заголовке продукт. МС (ES+)m/e 433 [M+H]+.
Примеры 243-249
Соединения примеров 243-249 (E243-E249) получают из 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) и арилхлоридов, указанных в таблице, по способу примера 242 (E242).
илокси)пиразин-2-ил]фенил}ацетамид (E244)
илокси)-4-этоксиникотинонитрил (Е248)
илокси)-2-метилникотинонитрил (Е249)
Пример 250
1-{6-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-пиридинил}-5-метил-2-пирролидинон (E250)
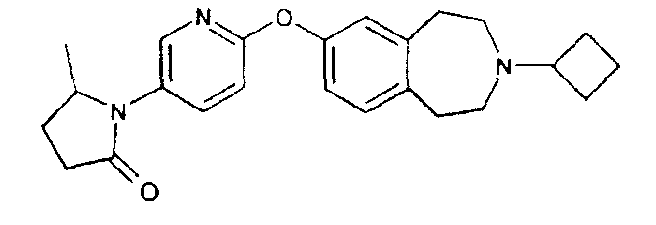
3-Циклобутил-7-[(5-иод-2-пиридинил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепин (E207) (294 мг, 0,7 ммоль), 1,10 фенантролин (38 мг, 0,2 ммоль) и 5-метил-2-пирролидон (139 мг, 1,4 ммоль) растворяют в диоксане (2 мл). Добавляют иодид меди (I) (39 мг, 0,2 ммоль) и карбонат цезия (479 мг, 1,5 ммоль) и смесь нагревают в микроволновом реакторе при 175°C в течение 15 минут. Смесь охлаждают и фильтруют через целит, промывая дихлорметаном. Фильтрат концентрируют в вакууме и неочищенное вещество очищают колоночной хроматографией, элюируя дихлорметаном и затем смесью .880 аммиак:метанол:дихлорметан (1:9:90), и получают указанное в заголовке соединение (137 мг); МС (ES+) m/e 392 [M+H]+.
Пример 251
1-{6-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-пиридинил}-3-метил-2-имидазолидин (E251)
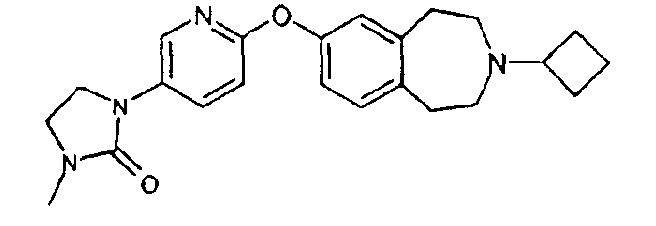
3-Циклобутил-7-[(5-иод-2-пиридинил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепин (E207) (294 мг, 0,7 ммоль), 1-метил-2-имидазолидинон (90 мг, 0,9 ммоль), карбонат цезия (364 мг, 1,1 ммоль) и ксантфос (12 мг, 0,02 ммоль) суспендируют в толуоле (10 мл). Добавляют трис(дибензилиденацетон)дипалладия (0) (6 мг, 0,007 ммоль) и смесь нагревают с обратным холодильником в течение ночи. Затем реакционную смесь сразу наносят на ионообменный картридж SCX (Varian, 5 г) и промывают метанолом и затем смесью .880 аммиак:метанол (1:9). Основные фракции упаривают и неочищенное вещество очищают автоматизированной хроматографией на обращенной фазе, получая указанный в заголовке продукт (104 мг); МС (ES+) m/e 393 [M+H]+.
Пример 252
(4R)-1-{6-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-пиридинил}-4-гидрокси-2-пирролидинон (E252)
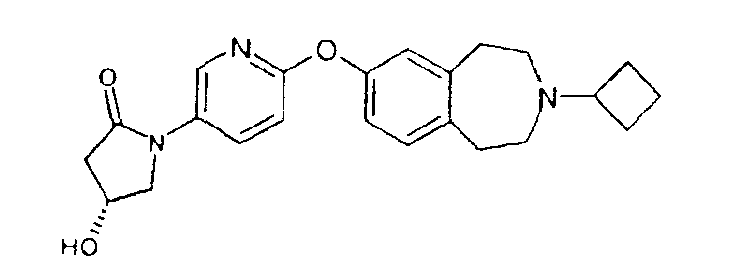
Соединение примера 252 (E252) получают из 3-циклобутил-7-[(5-иод-2-пиридинил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепина (E207) и (4R)-4-{[(1,1-диметилэтил)(диметил)силил]окси}-2-пирролидинона (Tetrahedron, 2000, 56 (39), 7705-7713) по способу, описанному для E251; МС (ES+) m/e 394 [M+H]+.
Пример 253
N-Метил-6-{[3-(3-метилциклопентил)-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил]окси}-3-пиридинкарбоксамид (E253)
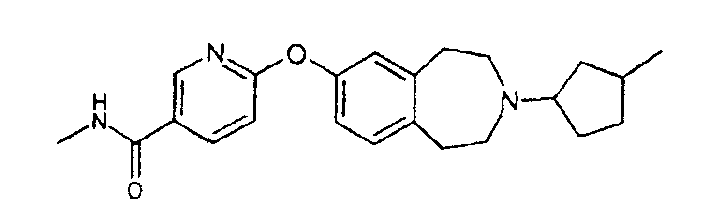
Соединение примера 253 (E253) получают из N-метил-6-(2,3,4,5-тетрагидро-1H-3-бензазепин-7-илокси)-3-пиридинкарбоксамида (D40) и 3-метилциклопентанона по способу примера 223; МС (ES+) m/e 380 [M+H]+.
Пример 254
5-[(3-Циклопентил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-N-метил-2-пиразинкарбоксамид (E254)
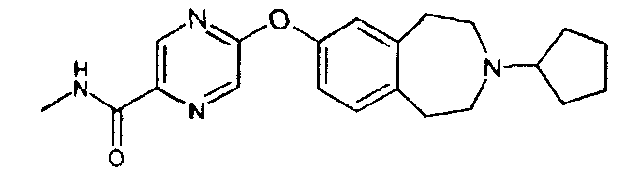
Соединение примера 254 (E254) получают из N-метил-5-(2,3,4,5-тетрагидро-1H-3-бензазепин-7-илокси)-2-пиразинкарбоксамида (D49) и циклопентанона по способу примера 223; МС (ES+) m/e 367 [M+H]+.
Пример 255
N-Метил-5-{[3-(3-метилциклопентил)-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил]окси}-2-пиразинкарбоксамид (E255)
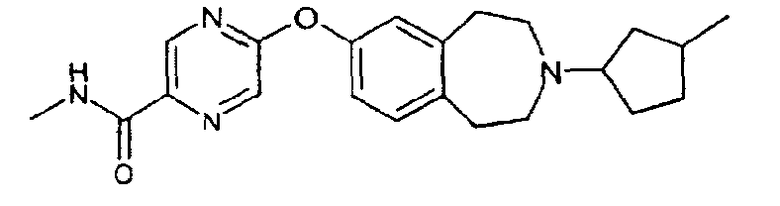
Соединение примера 255 (E255) получают из N-метил-5-(2,3,4,5-тетрагидро-1H-3-бензазепин-7-илокси)-2-пиразинкарбоксамида (D49) и 3-метилциклопентанона по способу примера 223; МС (ES+) m/e 381 [M+H]+.
Пример 256
1-{3-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-2-пиразинил}-2-пирролидинон (E256)
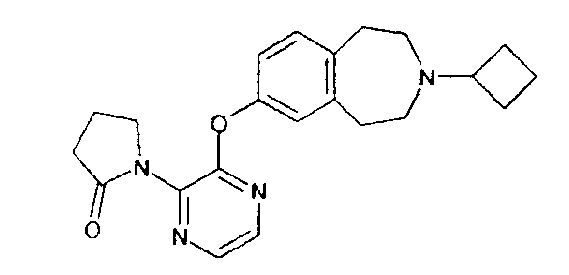
3-Циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ол (E3) (103 мг, 0,47 ммоль) растворяют в сухом диметилформамиде (3 мл), охлаждают до 0°C и обрабатывают гидридом натрия (60% в минеральном масле, 20 мг, 0,49 ммоль). Смесь оставляют нагреваться до комнатной температуры в течение 40 минут. Добавляют раствор 1-(3-хлор-2-пиразинил)-2-пирролидинона (D46) (103 мг, 0,52 ммоль) в сухом диметилформамиде (1 мл), смесь перемешивают при комнатной температуре 2 часа и нагревают при 80°C в течение 2,5 часов. Смесь оставляют охлаждаться до комнатной температуры, наносят на колонку SCX и промывают метанолом и затем смесью .880 аммиак/метанол (1:9). Основные фракции объединяют, концентрируют в вакууме, полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:метанол:дихлорметан (0,2:1,8:98), и получают указанное в заголовке соединение (86 мг); МС (ES+) m/e 379 [M+H]+.
Пример 257
7-[(5-Хлор-2-пиразинил)окси]-3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин (E257)
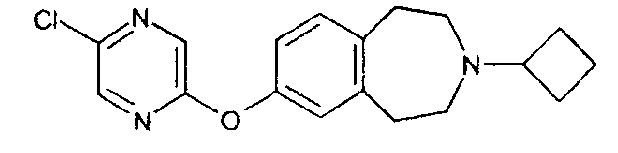
3-Циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ол (E3) (184 мг, 0,85 ммоль) растворяют в сухом диметилформамиде (3 мл), охлаждают до 0°C и обрабатывают гидридом натрия (60% в минеральном масле, 36 мг, 0,89 ммоль). Смесь оставляют нагреваться до комнатной температуры в течение 30 минут. Добавляют раствор 2,5-дихлорпиразина (D47) (139 мг, 0,94 ммоль) в сухом диметилформамиде (1 мл) и смесь перемешивают при комнатной температуре в течение 5 часов. Смесь наносят на колонку SCX и промывают метанолом и затем смесью .880 аммиак/метанол (1:9). Основные фракции объединяют и концентрируют в вакууме, получая указанное в заголовке соединение (268 мг); МС (ES+) m/e 330 [M+H]+.
Пример 258
1-{5-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-2-пиразинил}-2-пирролидинон (E258)
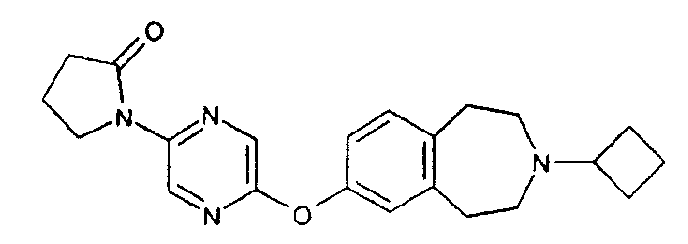
Смесь 7-[(5-Хлор-2-пиразинил)окси]-3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепина (E257) (132 мг, 0,40 ммоль), пирролидинона (0,06 мл, 0,80 ммоль), карбоната калия (200 мг, 1,45 ммоль), иодида меди (I) (23 мг, 0,12 ммоль) и N,N'-диметилэтилендиамина (0,01 мл, 0,12 ммоль) в сухом диоксан (3 мл) нагревают в микроволновом реакторе при 175°C в течение 30 минут. Смесь разбавляют метанолом, наносят на колонку SCX и промывают метанолом и затем смесью .880 аммиак/метанол (1:9). Основные фракции объединяют, концентрируют в вакууме, полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:метанол:дихлорметан (0,2:1,8:98), и получают указанное в заголовке соединение (64 мг); МС (ES+) m/e 379 [M+H]+.
Пример 259
7-[(5-Бром-2-пиразинил)окси]-3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин (E259)
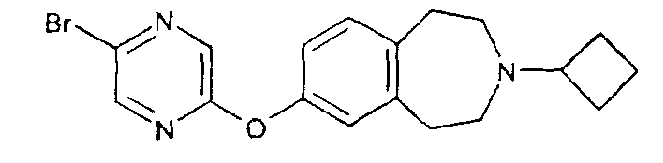
Указанное в заголовке соединение получают из 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) и 2,5-дибромпиразина (D48) по способу примера 257 (E257); МС (ES+) m/e 375 [M+H]+.
Пример 260
3-{5-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-2-пиразинил}-1,3-оксазолидин-2-он (E260)
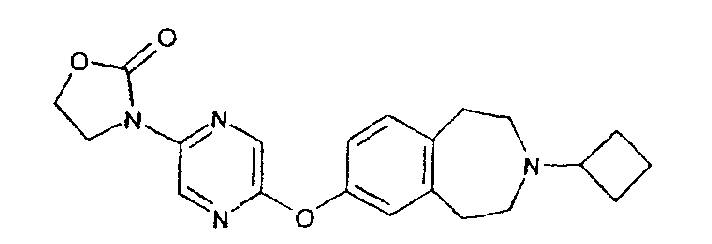
Указанное в заголовке соединение получают из 7-[(5-бром-2-пиразинил)окси]-3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепина (E259) и оксазолидинона по способу примера 258 (E258); МС (ES+) m/e 381 [M+H]+.
Пример 261
3-Циклобутил-7-[5-(1,1-диоксо-2-изотиазолидин-2-ил)пиридин-2-илокси]-2,3,4,5-тетрагидро-1H-3-бензазепин (E261)
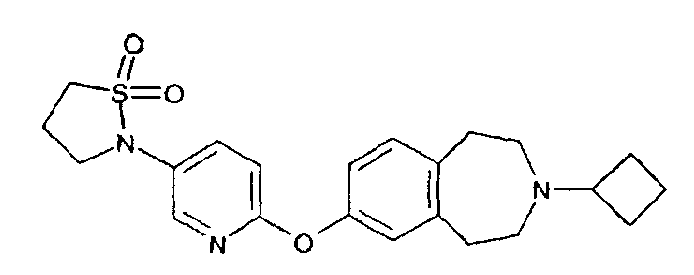
Смесь 3-циклобутил-7-[(5-иод-2-пиридинил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепина (E207) (200 мг, 0,48 ммоль), изотиазолидина 1,1-диоксида (116 мг, 0,96 ммоль), (Evans, Brian J.; Takahashi Doi, Joyce; Musker, W. Kenneth; J. Org. Chem.; 55; 9; 1990; 2580-2586), карбоната калия (238 мг, 1,73 ммоль), иодида меди (I) (27 мг, 0,14 ммоль) и N,N-диметилэтилендиамина (0,02 мл, 0,14 ммоль) в сухом диоксане (3 мл) нагревают в микроволновом реакторе при 140°C в течение 20 минут. Смесь разбавляют метанолом и наносят на колонку SCX, элюируя метанолом и затем смесью .880 аммиак/метанол (1:9). Основные фракции объединяют и концентрируют в вакууме. Полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:метанол:дихлорметан (0,5:4,5:95), и получают указанное в заголовке соединение (145 мг); МС (ES+) m/e 414 [M+H]+.
Пример 262
1-{6-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-пиридинил}-2-имидазолидинон (E262)
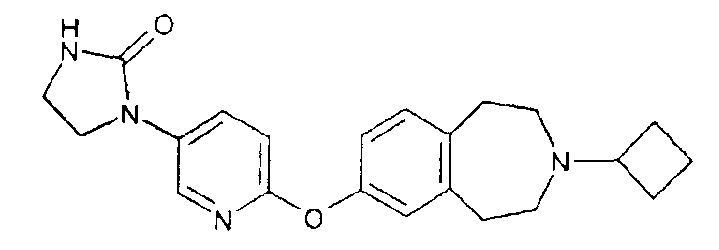
Указанное в заголовке соединение получают из 3-циклобутил-7-[(5-иод-2-пиридинил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепина (E207) и 2-имидазолидинона по способу примера 261; МС (ES+) m/e 379 [M+H]+.
Пример 263
5-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-2-пиразинкарбоксамид (E263)

5-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-2-пиразинкарбоновую кислоту (E123a) (168 мг, 0,47 ммоль) растворяют в сухом диметилформамиде (5 мл), обрабатывают 1,1'-карбонилдиимидазолом (230 мг, 1,42 ммоль) и полученную смесь перемешивают при комнатной температуре в течение 1,5 часов. Смесь обрабатывают .880 аммиаком (0,14 мл, 2,84 ммоль) и перемешивают в течение 4 часов. Реакционную смесь концентрируют в вакууме, полученный остаток очищают колоночной хроматографией, элюируя смесью (0,5:4,5:95), и получают указанное в заголовке соединение; МС (ES+) m/e 339 [M+H]+.
Пример 264
4-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-N-метил-3-(метилокси)бензамид (E264)
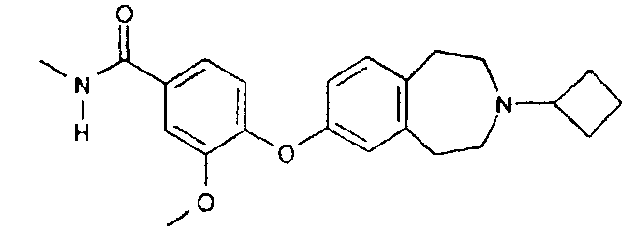
Стадия 1: 1,1-Диметилэтил 7-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилат
Смесь 1,1-диметилэтил 7-{[(трифторметил)сульфонил]окси}-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилата (2,0 г, 5,06 ммоль) (Bioorg. Med. Chem. Lett.; 10; 22; 2000; 2553-2556), бис(пинаколато)дибора (1,41 г, 5,57 ммоль), комплекс 1,1'-бис(дифенилфосфино)ферроцендихлорпалладия (II) (0,22 г, 0,30 ммоль), 1,1'-бис(дифенилфосфино)ферроцена (0,17 г, 0,30 ммоль) и ацетата калия (1,49 г, 15,2 ммоль) в сухом диоксане нагревают при 80°C в течение 3 часов. Смесь оставляют охлаждаться до комнатной температуры, разбавляют этилацетатом и промывают водой и насыщенным соляным раствором. Органическую фракцию сушат над сульфатом магния и упаривают в вакууме. Полученный остаток очищают колоночной хроматографией, элюируя смесью этилацетат:пентан (1:9), и получают указанное в заголовке соединение (1,60 г); МС (ES+) m/e 274 [(M+H)-CO2 tBu]+.
Стадия 2: (3-{[(1,1-Диметилэтил)окси]карбонил}-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)борная кислота
1,1-Диметилэтил 7-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилат (E264, стадия 1) (1,60 г, 4,29 ммоль) растворяют в ацетоне (25 мл), обрабатывают периодатом натрия (2,75 г, 12,9 ммоль), ацетатом аммония (0,73 г, 9,44 ммоль) и водой (25 мл) и полученную смесь перемешивают 18 часов при комнатной температуре. Ацетон удаляют упариванием в вакууме и оставшийся водный слой экстрагируют этилацетатом и дихлорметаном. Органические слои объединяют, сушат над сульфатом магния и упаривают в вакууме, получая указанное в заголовке соединение (1,06 г); МС (ES+) m/e 192 [(M+H)-CO2 tBu]+.
Стадия 3: 1,1-Диметилэтил 7-({2-(метилокси)-4-[(метилокси)карбонил]фенил}окси)-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилат
(3-{[(1,1-Диметилэтил)окси]карбонил}-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)борную кислоту (E264, стадия 2) (500 мг, 1,72 ммоль) растворяют в сухом дихлорметане (15 мл) и последовательно обрабатывают метилванилатом (313 мг, 1,72 ммоль), молекулярными ситами (4Е, 1,0 г), ацетатом меди (467 мг, 2,58 ммоль) и триэтиламином (1,20 мл, 8,60 ммоль) и полученную смесь перемешивают при комнатной температуре 18 часов. Смесь разбавляют дихлорметаном, фильтруют через целит и упаривают в вакууме. Остаток растворяют в этилацетате и промывают насыщенным раствором бикарбоната натрия. Органическую фракцию сушат над сульфатом магния и упаривают в вакууме. Полученный остаток очищают колоночной хроматографией, элюируя смесью (0,1:9,9), и получают указанное в заголовке соединение (240 мг). МС (ES+) m/e 328 [(M+H)-CO2 tBu]+.
Стадия 4: 4-[(3-{[(1,1-Диметилэтил)окси]карбонил}-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-(метилокси)бензойная кислота
1,1-Диметилэтил 7-({2-(метилокси)-4-[(метилокси)карбонил]фенил}окси)-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилат (E264, стадия 3) (240 мг, 0,56 ммоль) растворяют в этаноле (2 мл), обрабатывают 2M раствором гидроксида натрия (1 мл) и полученную смесь перемешивают 1,5 часа. Смесь подкисляют 2M раствором хлористоводородной кислоты и экстрагируют этилацетатом. Этилацетатные слои объединяют, сушат над сульфатом магния и упаривают в вакууме, получая указанное в заголовке соединение (0,15 г); МС (ES+) m/e 314 [(M+H)-CO2 tBu]+.
Стадия 5: 1,1-Диметилэтил 7-{[4-[(метиламино)карбонил]-2-(метилокси)фенил]окси}-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилат
4-[(3-{[(1,1-Диметилэтил)окси]карбонил}-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-(метилокси)бензойную кислоту (E264, стадия 4) (145 мг, 0,35 ммоль) растворяют в сухом диметилформамиде (5 мл), обрабатывают 1,1'-карбонилдиимидазолом (85 мг, 0,53 ммоль) и полученную смесь перемешивают при комнатной температуре 3 часа. Смесь обрабатывают метиламином (0,53 мл, 1,05 ммоль, 2M раствор в ТГФ) и перемешивают 4 часа. Реакционную смесь концентрируют в вакууме и полученный остаток очищают колоночной хроматографией (1:1 этилацетат:пентан), получая указанное в заголовке соединение (0,10 г); МС (ES+) m/e 327 [(M+H)-CO2 tBu]+.
Стадия 6: N-Метил-3-(метилокси)-4-(2,3,4,5-тетрагидро-1H-3-бензазепин-7-илокси)бензамид
1,1-Диметилэтил 7-{[4-[(метиламино)карбонил]-2-(метилокси)фенил]окси}-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилат (E264, стадия 5) (100 мг, 0,23 ммоль) растворяют в сухом дихлорметане (2 мл), обрабатывают трифторуксусной кислотой (1 мл) и полученную смесь перемешивают при комнатной температуре 2 часа. Растворитель удаляют в вакууме, остаток растворяют в метаноле и наносят на колонку SCX, элюируя метанолом и затем смесью .880 аммиак:метанол (1:9). Основные фракции объединяют и концентрируют в вакууме, получая указанное в заголовке соединение (78 мг); МС (ES+) m/e 327 [M+H]+.
Стадия 7: 4-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-N-метил-3-(метилокси)бензамид
N-Метил-3-(метилокси)-4-(2,3,4,5-тетрагидро-1H-3-бензазепин-7-илокси)бензамид (E264, стадия 6) (78 мг, 0,24 ммоль) растворяют в сухом дихлорметане (5 мл), обрабатывают циклобутаноном (0,04 мл, 0,48 ммоль) и уксусной кислотой (1 капля) и полученную смесь перемешивают 15 минут. Добавляют триацетоксиборгидрид натрия (102 мг, 0,48 ммоль) и смесь перемешивают 30 минут. Смесь разбавляют метанолом и наносят на колонку SCX, элюируя метанолом и затем смесью .880 аммиак/метанол (1:9). Основные фракции объединяют и концентрируют в вакууме. Полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:метанол:дихлорметан (0,5:4,5:95), и получают указанное в заголовке соединение (20 мг); МС (ES+) m/e 381 [M+H]+.
Пример 265
2-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]бензонитрил (E265)
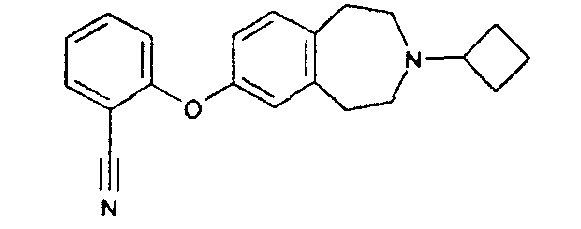
3-Циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ол (E3) (300 мг, 1,38 ммоль) растворяют в пиридине (10 мл), охлаждают на ледяной бане и обрабатывают гидридом натрия (60% в минеральном масле) (66 мг, 1,66 ммоль) в атмосфере аргона. Полученную смесь перемешивают 5 минут, обрабатывают бромидом меди (I) (277 мг, 1,93 ммоль) и оставляют нагреваться до комнатной температуры в течение 30 минут. Добавляют раствор 2-иодбензонитрила (948 мг, 4,14 ммоль) в пиридине (2 мл) и смесь нагревают с обратным холодильником в течение 2,5 часов. Смесь оставляют охлаждаться до комнатной температуры и растворитель удаляют в вакууме. Полученный остаток очищают колоночной хроматографией, элюируя смесью аммиак:метанол:дихлорметан (0,2:1,8:98), и получают указанное в заголовке соединение (180 мг); МС (ES+) m/e 319 [M+H]+.
Пример 266
3-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-N-метил-4-(метилокси)бензамид (E266)
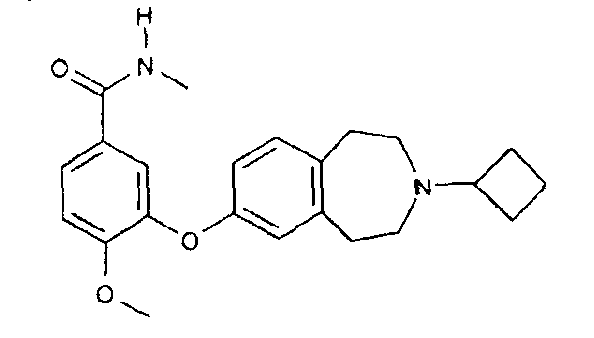
Стадия 1: 1,1-Диметилэтил 7-({2-(метилокси)-5-[(метилокси)карбонил]фенил}окси)-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилат
Указанное в заголовке соединение получают из (3-{[(1,1-диметилэтил)окси]карбонил}-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)борной кислоты (E264, стадия 2) и метил-3-гидрокси-4-метоксибензоата по способу примера 264, стадия 3; МС (ES+) m/e 328 [(M+H)-CO2 tBu]+.
Стадия 2: 3-[(3-{[(1,1-Диметилэтил)окси]карбонил}-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-4-(метилокси)бензойной кислоты
Указанное в заголовке соединение получают из 1,1-диметилэтил 7-({2-(метилокси)-5-[(метилокси)карбонил]фенил}окси)-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилата (E266, стадия 1) по способу примера 264, стадия 4; МС (ES+) m/e 314[(M+H)-CO2 tBu]+.
Стадия 3: 1,1-Диметилэтил 7-{[5-[(метиламино)карбонил]-2-(метилокси)фенил]окси}-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилат
Указанное в заголовке соединение получают из 3-[(3-{[(1,1-диметилэтил)окси]карбонил}-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-4-(метилокси)бензойной кислоты (E266, стадия 2) и метиламина по способу примера 264, стадия 5; МС (ES+) m/e 327 [(M+H)-CO2 tBu]+.
Стадия 4: N-Метил-4-(метилокси)-3-(2,3,4,5-тетрагидро-1H-3-бензазепин-7-илокси)бензамид
Указанное в заголовке соединение получают из 1,1-диметилэтил 7-{[5-[(метиламино)карбонил]-2-(метилокси)фенил]окси}-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилата (E266, стадия 3) по способу примера 264, стадия 6; МС (ES+) m/e 327 [M+H]+.
Стадия 5: 3-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-N-метил-4-(метилокси)бензамид
Указанное в заголовке соединение получают из N-метил-4-(метилокси)-3-(2,3,4,5-тетрагидро-1H-3-бензазепин-7-илокси)бензамида (E266, стадия 4), по способу примера 264, стадия 7; МС (ES+) m/e 381 [M+H]+.
Пример 267
3-Хлор-4-[(3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-N-метилбензамид (E267)
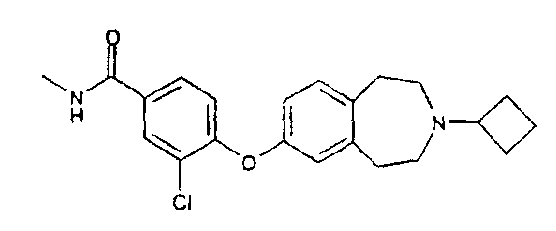
Стадия 1: 1,1-Диметилэтил 7-({2-хлор-4-[(метилокси)карбонил]фенил}окси)-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилат
Указанное в заголовке соединение получают из метил 3-хлор-4-гидроксибензоата (320 мг, 1,72 ммоль) и (3-{[(1,1-диметилэтил)окси]карбонил}-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)борной кислоты (E264, стадия 2) по способу, описанному в примере 264, стадия 3 (211 мг, 29%); ЯМР (CDCl3) δ 1,49 (9H, с), 2,88 (4H, м), 3,56 (4H, м), 3,91 (3H, с), 6,78-6,89 (3H, м), 7,12 (H, м), 7,84 (H, м), 8,14 (H, с).
Стадия 2: 3-Хлор-4-[(3-{[(1,1-диметилэтил)окси]карбонил}-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]бензойная кислота
Указанное в заголовке соединение получают из 1,1-диметилэтилового эфира 7-({2-хлор-4-[(метилокси)карбонил]фенил}окси)-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоновой кислоты (E267, стадия 1) по способу, описанному в примере 264, стадия 4; МС (ES-), m/e 416 и 418 [M-H].
Стадия 3: 1,1-Диметилэтил 7-({2-хлор-4-[(метиламино)карбонил]фенил}окси)-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилат
Указанное в заголовке соединение получают из 3-хлор-4-[(3-{[(1,1-диметилэтил)окси]карбонил}-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]бензойной кислоты (E267, стадия 2) и метиламина по способу, описанному в примере 264, стадия 5 (82 мг, 52%); МС (ES+), m/e 431 и 433 [M+H]+.
Стадия 4: 3-Хлор-N-метил-4-(2,3,4,5-тетрагидро-1H-3-бензазепин-7-илокси)бензамид
Указанное в заголовке соединение получают из 1,1-диметилэтил 7-({2-хлор-4-[(метиламино)карбонил]фенил}окси)-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилата (E267, стадия 3) по способу, описанному в примере 264, стадия 6 (54 мг, 94%); МС (ES+), m/e 331 и 333 [M+H]+.
Стадия 5: 3-Хлор-4-[(3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-N-метилбензамид
Указанное в заголовке соединение получают из 3-хлор-N-метил-4-(2,3,4,5-тетрагидро-1H-3-бензазепин-7-илокси)бензамида (E267, стадия 4) и циклобутанона по способу, описанному в примере 264, стадия 7 (36 мг, 57%); МС (ES+), m/e 385 и 387 [M+H]+.
Пример 268
4-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-N,3-диметилбензамид (E268)
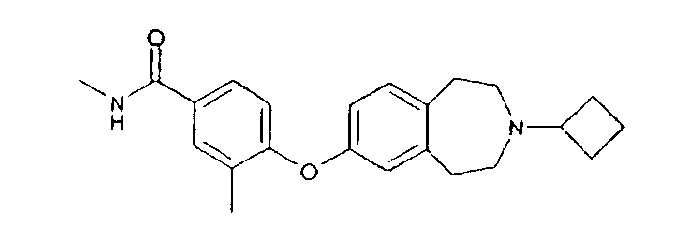
Стадия 1: 1,1-Диметилэтил 7-({2-метил-4-[(метилокси)карбонил]фенил}окси)-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилат
Указанное в заголовке соединение получают из трет-бутилового эфира 7-гидрокси-1,2,4,5-тетрагидробензо[d]азепин-3-карбоновой кислоты (PCT Int. Appl. (2002), WO 02/40471) и метил 4-бром-3-метилбензоата по способу, описанному в примере 128 (211 мг, 29%); ЯМР (CDCl3) δ 1,49 (9H, с), 2,32 (3H, м), 2,86 (4H, м), 3,55 (4H, м), 3,89 (3H, с), 6,71-6,81 (3H, м), 7,08 (H, м), 7,80 (H, м), 7,94 (H, с).
Стадия 2: 4-[(3-{[(1,1-Диметилэтил)окси]карбонил}-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-метилбензойная кислота
Указанное в заголовке соединение получают из 1,1-диметилэтил 7-({2-метил-4-[(метилокси)карбонил]фенил}окси)-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилата (E268, стадия 1) по способу, описанному в примере 264, стадия 4; (247 мг, 94%); МС (ES-), m/e 396 [M-H].
Стадия 3: 1,1-Диметилэтил 7-({2-метил-4-[(метиламино)карбонил]фенил}окси)-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилат
Указанное в заголовке соединение получают из 4-[(3-{[(1,1-диметилэтил)окси]карбонил}-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-метилбензойной кислоты (E268, стадия 2) и метиламина по способу, описанному в примере 264, стадия 5 (136 мг, 53%); МС (ES+), m/e 411 [M+H]+.
Стадия 4: N,3-Диметил-4-(2,3,4,5-тетрагидро-1H-3-бензазепин-7-илокси)бензамид
Указанное в заголовке соединение получают из 1,1-диметилэтил 7-({2-метил-4-[(метиламино)карбонил]фенил}окси)-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилат (E268, стадия 3) по способу, описанному в примере 264, стадия 6 (90 мг, 88%); МС (ES+), m/e 311 [M+H]+.
Стадия 5: 4-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-N,3-диметилбензамид
Указанное в заголовке соединение получают из N,3-диметил-4-(2,3,4,5-тетрагидро-1H-3-бензазепин-7-илокси)бензамида (E268, стадия 4) (90 мг, 0,29 ммоль) и циклобутанона (50 мкл, 0,58 ммоль) по способу, описанному в примере 264, стадия 7 (71 мг, 67%); МС (ES+), m/e 365 [M+H]+.
Пример 269
3-Циклобутил-8-[(фенилметил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепин-7-карбонитрил (E269)
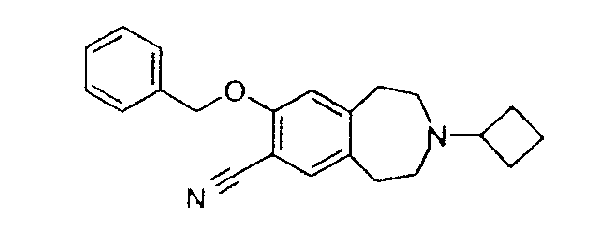
Смесь 3-циклобутил-7-иод-8-[(фенилметил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепина (E226) (250 мг, 0,58 ммоль), тетракис(трифенилфосфин)палладия(0) (33 мг, 0,029 моль), иодида меди (I) (11 мг, 0,058 ммоль) и цианида натрия (56 мг, 1,15 ммоль) в тетрагидрофуране (5 мл) нагревают с обратным холодильником 16 часов. Смесь охлаждают и разбавляют этилацетатом, фильтруют через целит, промывают водой, затем насыщенным соляным раствором и сушат над сульфатом натрия и концентрируют в вакууме. Неочищенную смесь очищают ВЭЖХ на обращенной фазе, получая указанное в заголовке соединение; МС (ES+) m/e 333 [M+H]+.
Пример 270
3-Циклобутил-7-[(2-фторфенил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепин (E270)
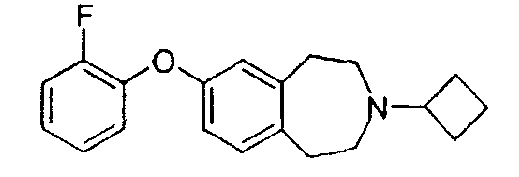
Соединение примера 270 (E270) получают из 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) и 2-фториодбензола по способу примера 128; МС (ES+) m/e 312 [M+H]+.
Пример 271
4-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-фторбензонитрил (E271)
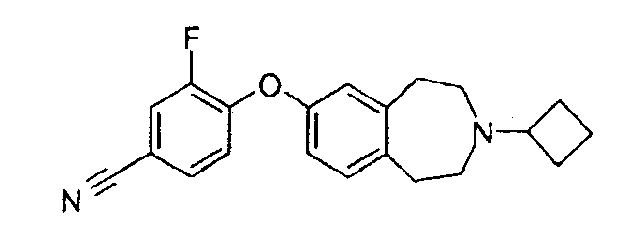
Смесь 3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ола (E3) (100 мг, 0,46 ммоль), 3,4-дифторбензонитрила (70 мг, 0,51 ммоль) и карбоната калия (159 мг, 1,15 ммоль) в диметилсульфоксиде (2 мл) нагревают при 85°C в течение 2 часов. Реакционную смесь охлаждают, наносят на ионообменный картридж SCX (Varian bond-elute, 10 г) и промывают сначала метанолом, затем смесью .880 аммиак/метанол (1:9). Объединенные основные фракции концентрируют в вакууме, получая указанное в заголовке соединение (E271). МС (ES+) m/e 337 [M+H]+.
Пример 272
4-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-фторбензойная кислота (E272)
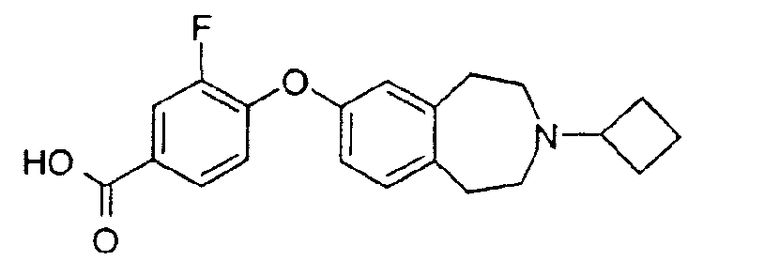
4-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-фторбензонитрил (E271) (150 мг, 0,45 ммоль) растворяют в смеси этанола (1 мл) и воды (1,5 мл), обрабатывают гидроксидом натрия (150 мг, 4,5 ммоль) и нагревают с обратным холодильником в течение 2 часов. Затем реакционную смесь обрабатывают уксусной кислотой (0,39 мл, 6,75 ммоль) и концентрируют в вакууме. Полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:метанол:дихлорметан (2:18:80), и получают указанное в заголовке соединение. МС (ES+) m/e 356 [M+H]+.
Пример 273
4-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-фтор-N-метилбензамид (E273)
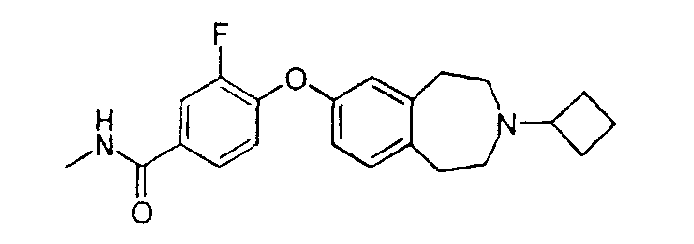
Раствор 4-[(3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-фторбензойной кислоты (E272) (164 мг, 0,36 ммоль) и О-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилурония гексафторфосфата (438 мг, 1,15 ммоль) в диметилформамиде (2 мл) обрабатывают диизопропилэтиламином (0,40 мл, 2,3 ммоль), затем 2M раствором метиламина в тетрагидрофуране (2 мл). Реакционную смесь перемешивают при комнатной температуре 4 часа, наносят на ионообменную колонку SCX (Varian bond-elute, 10 г), промывают сначала метанолом, затем смесью .880 аммиак/метанол, и основные фракции концентрируют в вакууме. Полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:метанол:дихлорметан (0,5:4,5:95), и получают указанное в заголовке соединение. МС (ES+) m/e 369 [M+H]+.
Пример 274
3-Циклобутил-7-[(2-фтор-4-иодфенил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепин (E274)
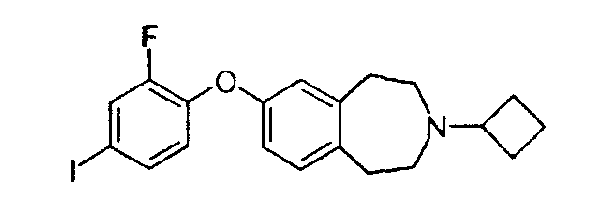
Стадия 1: 1,1-Диметилэтил 7-[(2-фтор-4-нитрофенил)окси]-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилат
3,4-дифторнитробензол (664 мг, 4,18 ммоль) добавляют к смеси трет-бутилового эфира 7-гидрокси-1,2,4,5-тетрагидробензо[d]азепин-3-карбоновой кислоты (WO 02/40471) (1 г, 3,8 ммоль) и карбоната калия (1,3 г, 9,49 ммоль) в диметилформамиде (10 мл) и реакционную смесь нагревают при 130°C в течение 3 часов. Реакционную смесь охлаждают, разбавляют этилацетатом, промывают водой, затем смесью вода:насыщенный соляной раствор (1:1), сушат над сульфатом натрия и концентрируют в вакууме. Полученный остаток очищают колоночной хроматографией, элюируя смесью этилацетат:пентан (1:10), получая указанное в заголовке соединение. МС (ES+) m/e 303 [M-COOtBu]+.
Стадия 2: 1,1-Диметилэтил 7-[(4-амино-2-фторфенил)окси]-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилат
К раствору 1,1-диметилэтил 7-[(2-фтор-4-нитрофенил)окси]-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилата (E274, стадия 1) (1,37 г, 3,40 ммоль) в этаноле (25 мл) добавляют палладий-на-угле (10 масс.% палладия) (300 мг) и реакционную смесь перемешивают при комнатной температуре в атмосфере водорода (1 атмосфера) 3 часа. Реакционную смесь фильтруют через целит и концентрируют в вакууме, получая указанное в заголовке соединение. МС (ES+) m/e 273 [M-M-COOtBu]+.
Стадия 3: 1,1-Диметилэтил 7-[(2-фтор-4-иодфенил)окси]-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилат
К раствору 1,1-диметилэтил 7-[(4-амино-2-фторфенил)окси]-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилата (E274, стадия 2) (0,5 г, 1,34 ммоль) и иодоформа (1 г, 2,69 ммоль) в тетрагидрофуране (10 мл) добавляют по каплям трет-бутилнитрит (0,32 мл, 2,69 моль). Затем реакционную смесь нагревают с обратным холодильником 1 час, охлаждают, концентрируют в вакууме, полученный остаток очищают колоночной хроматографией, элюируя смесью этилацетат:пентан (1:10), и получают указанное в заголовке соединение. МС (ES+) m/e 384 [M-COOtBu]+.
Стадия 4: 7-[(2-Фтор-4-иодфенил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепин
Указанное в заголовке соединение получают из 1,1-диметилэтил 7-[(2-фтор-4-иодфенил)окси]-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилата (E274, стадия 3) по способу описания 2 (D2). МС (ES+) m/e 384 [M+H]+.
Стадия 5: 3-Циклобутил-7-[(2-фтор-4-иодфенил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепин
Указанное в заголовке соединение получают из 7-[(2-фтор-4-иодфенил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепина (E274, стадия 4) по способу примера 1 (E1). МС (ES+) m/e 438 [M+H]+.
Пример 275
1-{4-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-фторфенил}-2-пирролидон (E275)
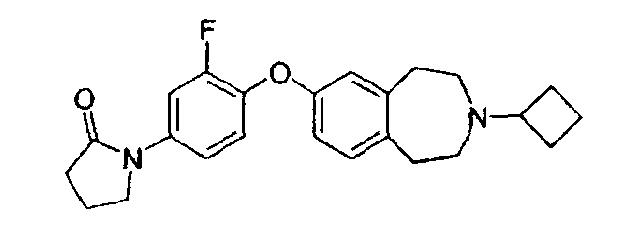
Указанный в заголовке продукт получают из 3-циклобутил-7-[(2-фтор-4-иодфенил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепина (E274) по способу примера 258 (E258). МС (ES+) m/e 395 [M+H]+.
Пример 276
N-{4-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-фторфенил}ацетамид (E276)
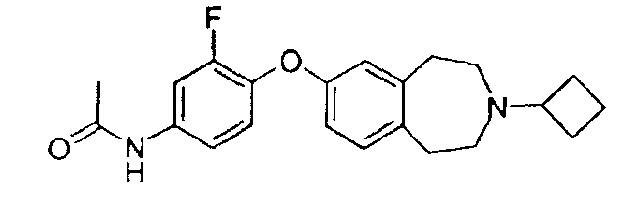
Стадия 1: 1,1-Диметилэтил 7-{[4-(ацетиламино)-2-фторфенил]окси}-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилат
К раствору 1,1-диметилэтил 7-[(4-амино-2-фторфенил)окси]-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилата (E274, стадия 2) (250 мг, 0,67 ммоль) в дихлорметане (10 мл) добавляют триэтиламин (0,19 мл, 1,34 ммоль) и ацетилхлорид (50 мкл, 0,74 мл) и реакционную смесь перемешивают при комнатной температуре 16 часов. Затем реакционную смесь разбавляют дихлорметаном, промывают 3N водным раствором лимонной кислоты, насыщенным раствором бикарбоната натрия, водой и дихлорметаном, сушат над сульфатом натрия и концентрируют в вакууме. Полученный остаток очищают колоночной хроматографией, элюируя смесью этилацетат:пентан (1:1), и получают указанное в заголовке соединение. МС (ES+) m/e 413 [M-H]-.
Стадия 2: N-{4-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-3-фторфенил}ацетамид
Указанное в заголовке соединение получают из 1,1-диметилэтил 7-([4-(ацетиламино)-2-фторфенил]окси}-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилата (E276, стадия 1), используя 2-стадийный способ, описанный в примере 274, стадии 4-5. МС (ES+) m/e 369 [M+H]+.
Пример 277
Соединение примера 277 (E277) получают из 3-циклобутил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ола (E3) и соответствующего ароматического иодида, указанного в таблице, по способу примера 128 (E128):
азепин-7-илокси)фенил]-1-пирролидин-1-илметанон (Е277)
Пример 278
Соединение примера 278 (E278) получают из 5-[(3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-2-пиридинкарбоновой кислоты (E187a) и соответствующего амина, указанного в таблице, по способу примера 177 (E177):
Пример 279
3-Циано-4-[(3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-N-метилбензамид (E279)
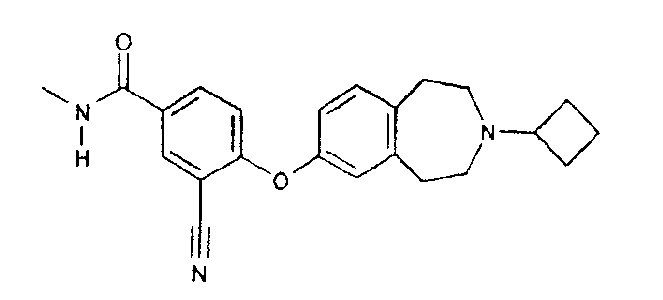
Стадия 1: 3-Циано-4-(метилокси)бензойная кислота
Указанное в заголовке соединение получают из метил 3-циано-4-(метилокси)бензоата по способу примера 264, стадия 4; 1H ЯМР (CDCl3) 8,32 (1H, д), 8,29-8,27 (1H, дд), 7,06-7,04 (1H, д), 4,03 (3H, с).
Стадия 2: 3-Циано-N-метил-4-(метилокси)бензамид
Указанное в заголовке соединение получают из 3-циано-4-(метилокси)бензойной кислоты (E279, стадия 1) по способу примера 264, стадия 5; МС (ES+) m/e 191 [M+H]+.
Стадия 3: 3-Циано-4-гидрокси-N-метилбензамид
3-Циано-N-метил-4-(метилокси)бензамид (E279, стадия 2) (346 мг, 1,82 ммоль) растворяют в сухом дихлорметане (10 мл), охлаждают до 0°C и обрабатывают бромидом бора (1 M раствор в дихлорметане) (9,11 мл, 9,11 ммоль). Смесь перемешивают 30 минут, оставляют нагреваться до комнатной температуры и перемешивают в течение 18 часов. Смесь охлаждают на ледяной бане, обрабатывают добавляемой по каплям водой и затем оставляют нагреваться до комнатной температуры. Смесь выливают в 2M раствор хлористоводородной кислоты (10 мл) и экстрагируют этилацетатом. Этилацетатные слои объединяют, сушат над сульфатом магния и упаривают в вакууме. Полученный остаток очищают колоночной хроматографией, элюируя смесью этилацетат:дихлорметан (1:1), и получают указанное в заголовке соединение (86 мг); МС (ES+) m/e 177 [M+H]+.
Стадия 4: 1,1-Диметилэтил 7-({2-циано-4-[(метиламино)карбонил]фенил}окси)-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилат
Указанное в заголовке соединение получают из 3-циано-4-гидрокси-N-метилбензамида (E279, стадия 3) и (3-{[(1,1-диметилэтил)окси]карбонил}-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)борной кислоты (E264, стадия 2) по способу примера 264, стадия 3; МС (ES+) m/e 322 [(M+H)-CO2 tBu]+.
Стадия 5: 3-Циано-N-метил-4-(2,3,4,5-тетрагидро-1H-3-бензазепин-7-илокси)бензамид
Указанное в заголовке соединение получают из 1,1-диметилэтил 7-({2-циано-4-[(метиламино)карбонил]фенил}окси)-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилата (E279, Стадия 4) по способу примера 264, стадия 6; МС (ES+) m/e 322 [M+H]+.
Стадия 6: 3-Циано-4-[(3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]-N-метилбензамид
Указанное в заголовке соединение получают из 3-циано-N-метил-4-(2,3,4,5-тетрагидро-1H-3-бензазепин-7-илокси)бензамида (E279, стадия 5), по способу примера 264, стадия 7; МС (ES+) m/e 376 [M+H]+.
Пример 280
3-Циклобутил-7-{[6-(4-морфолинилкарбонил)-3-пиридазинил]окси}-2,3,4,5-тетрагидро-1H-3-бензазепин (E280)
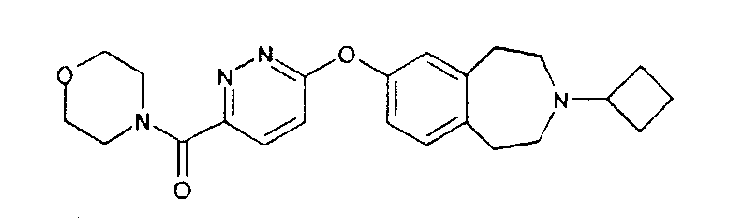
Стадия 1: 4-[(6-Хлор-3-пиридазинил)карбонил]морфолин
Смесь 6-оксо-1,6-дигидро-3-пиридазинкарбоновой кислоты (A.E. Mourad et al. J. Het. Chem. 1992; 29 (6), 1583-1592; 0,5 г) и оксихлорида фосфора (2 мл) нагревают с обратным холодильником 2 ч. Избыток оксихлорида фосфора упаривают и к остатку добавляют ТГФ (5 мл). Затем раствор охлаждают до 0°C, добавляют триэтиламин (1,1 мл) и затем морфолин (1,87 мл). Смесь оставляют нагреваться до комнатной температуры, перемешивают в течение 16 ч, после чего разбавляют этилацетатом (10 мл) и фильтруют. Фильтрат упаривают и очищают хроматографией на силикагеле, элюируя этилацетатом, и получают указанное в заголовке соединение; МС (ES+) m/e 228 [M+H]+.
Стадия 2: 3-Циклобутил-7-{[6-(4-морфолинилкарбонил)-3-пиридазинил]окси}-2,3,4,5-тетрагидро-1H-3-бензазепин
Смесь 3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ола (E3) (84 мг, 0,385 ммоль), 4-[(6-хлор-3-пиридазинил)карбонил]морфолина (E280, стадия 1) (70 мг, 0,308 ммоль) и карбоната калия (85 мг, 0,616 ммоль) в сухом ацетоне (3 мл) нагревают при 140°C в течение 2×15 мин (300 Вт) в микроволновом реакторе. Охлажденную реакционную смесь фильтруют, концентрируют в вакууме и очищают колоночной хроматографией на силикагеле, элюируя смесью .880 аммиак:метанол:дихлорметан (0,5:4,5:190), и получают указанное в заголовке соединение; МС (ES+) m/e 409 [M+H]+.
Примеры 281-282
Соединения примеров 281-282 (E281-282) получают из 3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ола (E3) и 6-оксо-1,6-дигидро-3-пиридазинкарбоновой кислоты, используя соответствующий амин, указанный в таблице, по двухстадийному способу, описанному в примере 280:
Пример 283
3-Циклобутил-7-{[4-(4-морфолинил)-4-оксобутил]окси}-2,3,4,5-тетрагидро-1H-3-бензазепин (E283)
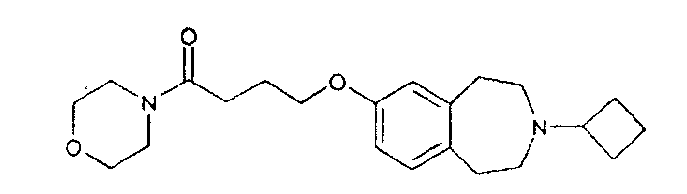
Стадия 1: 4-[(3-Циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]бутановая кислота
Этил 4-[(3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]бутаноат (E167a) (2,2 г, 6,6 ммоль) растворяют в метаноле (40 мл) и обрабатывают 2N раствором гидроксида натрия (10,0 мл). После перемешивания при нагревании с обратным холодильником в течение 1 часа реакционную смесь охлаждают до комнатной температуры и концентрируют в вакууме. Неочищенную смесь наносят на ионообменный картридж SCX (Varian bond-elute) и промывают водой и затем метанолом. Органические фракции упаривают в вакууме, получая указанное в заголовке соединение (E283); МС (ES+) m/e 304 [M+H]+.
Стадия 2: 3-Циклобутил-7-{[4-(4-морфолинил)-4-оксобутил]окси}-2,3,4,5-тетрагидро-1H-3-бензазепин
4-[(3-циклобутил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)окси]бутановую кислоту (E283, стадия 1) (0,15 г, 0,50 ммоль) растворяют в сухом дихлорметане (5 мл) и сухом диметилформамиде (2 мл), обрабатывают гидратом 1-гидроксибензотриазола (0,14 г, 1,0 ммоль), N-циклогексилкарбодиимидом и N'-метилполистиролом HL (0,53 г, 1,0 ммоль, 1,7 ммоль/г) и перемешивают 45 минут. Добавляют морфолин (0,056 мл, 0,65 ммоль) и смесь перемешивают 3 часа при температуре окружающей среды. Неочищенную реакционную смесь наносят на ионообменный картридж SCX (Varian bond-elute) и промывают водой, метанолом и затем смесью .880 аммиак:метанол (1:9). Объединенные основные фракции упаривают в вакууме. Полученный остаток очищают колоночной хроматографией, элюируя смесью .880 аммиак:метанол:дихлорметан (от 0,5:4,5:95 до 1:9:90), и получают указанное в заголовке соединение (E283); МС (ES+) m/e 373 [M+H]+.
Примеры 284-285
Соединения примеров 284-285 (E284-285) получают из 3-циклобутил-7-(пиперидин-4-илокси)-2,3,4,5-тетрагидро-1H-бензо[d]азепина (E6) и соответствующей кислоты, указанной в таблице, по способу примера 13 (E13):
Пример 286
3-Циклобутил-7-[(1-{[(2R,6S)-2,6-диметил-4-морфолинил]карбонил}-4-пиперидинил)окси]-2,3,4,5-тетрагидро-1H-3-бензазепин (Е286)
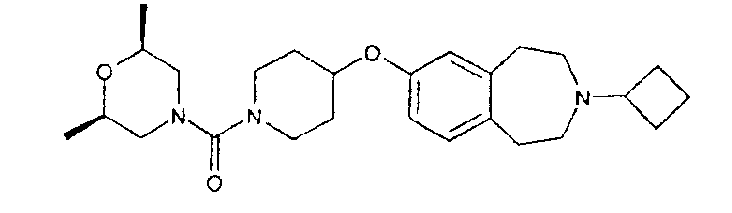
Соединение примера 286 (Е286) получают из 3-циклобутил-7-(пиперидин-4-илокси)-2,3,4,5-тетрагидро-1Н-бензо[d]азепина (Е6) и цис-2,6-диметилморфолина по способу примера 61 (E61). МС (ES+) m/e 442 [M+H]+.
Пример 287
3-Циклобутил-7-{[транс-4-(4-морфолинилкарбонил)циклогексил]окси}-2,3,4,5-тетрагидро-1H-3-бензазепин (Е287)
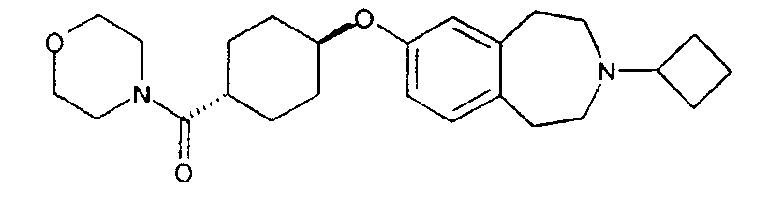
Соединение примера 287 (Е287) получают из 3-циклобутил-7-(пиперидин-4-илокси)-2,3,4,5-тетрагидро-1Н-бензо[d]азепина (Е6) и цис-4-(4-морфолинилкарбонил)циклогексанола (D55) по способу примера 5а (E5a). МС (ES+) m/e 413 [M+H]+.
Все указанные в данном документе публикации, которые включают в себя, не ограничиваясь ими, патенты и патентные заявки, включены в данное описание в качестве ссылки, как если бы в отношении каждой индивидуальной публикации было указано, что она полностью включена в данное описание в качестве ссылки.
Пример 288
3-Циклобутил-7-{[6-(4-морфолинил)-2-пиразинил]окси}-2,3,4,5-тетрагидро-1H-3-бензазепин (Е288)
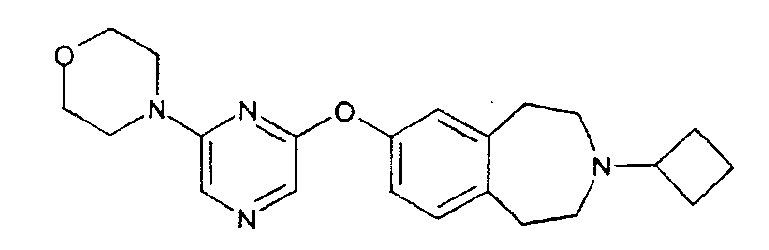
Соединение примера 288 (Е288) получают из 3-циклобутил-2,3,4,5-тетрагидро-1Н-бензо[d]азепин-7-ола (Е3) и 4-(6-хлор-2-пиразинил)морфолина [Zagulyaeva, O.A. J. Org. Chem. USSR, EN, 14; 1978; 377-380] по способу примера 242 (E242); МС (ES+) m/e 381 [M+H]+.
Биологические данные
Мембранный препарат, содержащий рецепторы гистамина Н3, можно получить следующим способом.
(i) Получение клеточной линии, содержащей гистамин H3
ДНК, содержащую ген человеческого гистамина H3 (Huvar, A. et al. (1999) Mol. Pharmacol. 55(6), 1101-1107), клонируют в несущем векторе pCDNA3.1 TOPO (InVitrogen), кДНК выделяют из данного вектора путем рестрикционного расщепления плазмидной ДНК ферментами BamH1 и Not-1 и лигируют в индуцируемый вектор экспрессии pGene (InVitrogen), расщепляемый такими же ферментами. С системой GeneSwitchTM (система, где экспрессия трансгена прекращается в отсутствие индуцирующего фактора и запускается в присутствии индуцирующего фактора) работают по методу, описанному в патентах №№: 5364791; 5874534 и 5935934. Лигированную ДНК переносят в компетентные бактериальные клетки хозяина DH5α E. coli и помещают их на агар с бульоном Луриа (Luria Broth (LB)), содержащим ZeocinTM (антибиотик, который позволяет осуществить селекцию клеток, экспрессирующих ген sh ble, который присутствует в pGene и pSwitch) в концентрации 50 мкг/мл. Колонии, содержащие заново лигированную плазмиду, идентифицируют с помощью рестрикционного анализа. ДНК для трансфекции в клетки млекопитающих получают из 250 мл культуры бактериального хозяина, содержащего плазмиду pGeneH3, и выделяют с помощью набора для получения ДНК (Qiagen Midi-Prep), следуя инструкциям производителя (Qiagen). Клетки CHO K1, заранее трансфицированные регуляторной плазмидой pSwitch (InVitrogen), за 24 часа до использования высевают в концентрации 2×106 клеток на колбу T75 в полной среде, содержащей среду HamsF12 (GIBCOBRL, Life Technologies), дополненную 10% об./об. диализированной фетальной бычьей сывороткой, L-глутамином и гидромицином (100 г/мл). Плазмидную ДНК трансфицируют в клетки, используя липофектамин, в соответствии с инструкциями производителя (InVitrogen). Через 48 часов после трансфекции клетки помещают в полную среду, дополненную 500 мкг/мл ZeocinTM.
Чтобы индуцировать экспрессию рецептора, через 10-14 дней после селекции к культуральной среде добавляют 10 нМ мифепристона (InVitrogen). Через 18 часов после индуцирования клетки отсоединяют от колбы, используя этилендиаминтетрауксусную кислоту (EDTA; 1:5000; InVitrogen), затем их несколько раз промывают забуференным фосфатом физиологическим раствором pH 7,4 и повторно суспендируют в среде для сортинга, содержащей минимальную поддерживающую среду (MEM) без фенолового красного, дополненную солями Эрла и 3% Foetal Clone II (Hyclone). Приблизительно 1×107 клеток анализируют на экспрессию рецептора путем окрашивания кроличьими поликлональными антителами, 4a, против N-концевого домена рецептора гистамина H3, затем их инкубируют на льду в течение 60 минут и дважды промывают средой для сортинга. Антитела, связанные с рецептором, детектируют путем инкубации клеток в течение 60 минут на льду с козлиными антителами против кроличьих антител, конъюгированными с флуоресцентным маркером Alexa 488 (Molecular Probes). После двух дополнительных промываний средой для сортинга клетки фильтруют через 50 мкм FilconTM (BD Biosciences) и затем анализируют на проточном цитометре FACS Vantage SE, оборудованном автоматической приставкой для приготовления клеточных препаратов. В качестве контроля используют неиндуцированные клетки, обработанные подобным образом. Окрашенные клетки помещают в виде отдельных клеток в 96-луночные планшеты, в которые добавлена полная среда, содержащая 500 мкг/мл ZeocinTM, и оставляют расти перед повторным анализом экспрессии рецептора по связыванию антител и лигандов. Клон 3H3 отбирают для получения мембран.
(ii) Получение мембран из культивированных клеток
Все стадии метода проводят при 4°C с использованием предварительно охлажденных реагентов. Клеточный осадок ресуспендируют в 10 объемах буфера A2, содержащего 50 мМ N-2-гидроксиэтилпиперазин-N'-2-этансульфоновую кислоту (HEPES) (pH 7,40), дополненного 10-4 M лейпептина (ацетил-лейцил-лейцил-аргинал; Sigma L2884), 25 мкг/мл бацитрацина (Sigma B0125), 1 мМ этилендиаминтетрауксусной кислоты (EDTA), 1 мМ фенилметилсульфонилфторида (PMSF) и 2×10-6 M пепстатина A (Sigma). Затем клетки гомогенизируют импульсами 2×15 секунд в 1-литровом стеклянном смесителе Waring и центрифугируют 20 минут при 500g. После чего супернатант центрифугируют 30 минут при 48000g. Осадок снова суспендируют в 4 объемах буфера A2 путем интенсивного перемешивания в течение 5 секунд, затем гомогенизируют в гомогенизаторе Dounce (10-15 ударов). В этот момент берут аликвоты препарата, помещают их в полипропиленовые пробирки и хранят при -70°C.
Биологическую активность соединений данного изобретения можно анализировать in vitro следующими методами.
(I) Анализ связывания гистамина H3
Для каждого анализируемого соединения в 96-луночный планшет, лунки которого имеют прозрачное дно и белые стенки, добавляют:
(a) 10 мкл анализируемого соединения (или 10 мкл иодофенпропита (известного антагониста гистамина H3) с конечной концентрацией 10 мМ), разбавленного до нужной концентрации 10% ДМСО;
(b) 10 мкл 125I 4-[3-(4-иодфенилметокси)пропил]-1H-имидазолия (иодпроксифан) (Amersham; 1,85 мБк/мкл или 50 мкКи/мл; удельная активность ~2000 Ки/ммоль) разбавляют до 200 пМ буфером для анализа (50 мМ трис(гидроксиметил)аминометановый буфер (TRIS) pH 7,4, 0,5 мМ этилендиаминтетрауксусная кислота (EDTA)), получая конечную концентрацию 20 пМ; и
(c) 80 мкл смеси шарики/мембраны, полученной следующим образом: шарики для сцинтилляционного проксимального анализа (SPA) типа WGA-PVT суспендируют в буфере для анализа в концентрации 100 мг/мл, затем смешивают с мембранами (полученными по описанному выше способу) и разбавляют в буфере для анализа, получая конечный объем 80 мкл, который содержит 7,5 мкг белка и 0,25 мг шариков на лунку - смесь предварительно смешивают при комнатной температуре в течение 60 минут на роллере. Планшет встряхивают 5 минут и затем оставляют стоять при комнатной температуре 3-4 часа перед прочтением на счетчике Wallac Microbeta с помощью программы, нормализованной в течение 1 минуты для счета по тритию. Данные анализируют, используя 4-параметрическое логистическое уравнение.
(II) Функциональный антагонистический анализ гистамина H3
Для каждого анализируемого соединения в 96-луночный планшет, лунки которого имеют прозрачное дно и белые стенки, добавляют:
(a) 10 мкл анализируемого соединения (или 10 мкл гуанозин-5'-трифосфата (ГТФ) (Sigma) в качестве контроля неспецифического связывания), разбавленного до нужной концентрации буфером для анализа (20 мМ N-2-гидроксиэтилпиперазин-N'-2-этансульфоновая кислота (HEPES) + 100 мМ NaCl +10 мМ MgCl2, pH 7,4 NaOH);
(b) 60 мкл смеси шарики/мембраны/ГДФ, полученной следующим образом: шарики для сцинтилляционного проксимального анализа (SPA) агглютинин зародышей пшеницы-поливинилтолуол (WGA-PVT) суспендируют в буфере для анализа в концентрации 100 мг/мл, затем смешивают с мембранами (полученными по описанному выше способу) и разбавляют буфером для анализа, получая конечный объем 60 мкл, который содержит 10 мкг белка и 0,5 мг шариков на лунку - смесь предварительно смешивают при 4°С в течение 30 минут на роллере и непосредственно перед внесением в планшет добавляют гуанозин 5'-дифосфат (ГДФ) (Sigma; разбавленный аналитическим буфером) с получением конечной концентрации 10 мкМ. Чтобы уравновесить антагонист и рецептор/шарики, планшет инкубируют при комнатной температуре и при встряхивании в течение 30 минут, после чего добавляют:
(c) 10 мкл гистамина (Tocris) с конечной концентрацией 0,3 мкМ; и
(d) 20 мкл соли триэтиламина и гуанозин 5'[γ35-S]тиотрифосфата (Amersham; концентрация радиоактивности = 37 кВк/мкл или 1 мКи/мл; удельная активность 1160 Ки/ммоль), разбавленного буфером для анализа до концентрации 1,9 нМ, с получением конечной концентрации 0,38 нМ.
Затем планшет инкубируют на шейкере при комнатной температуре в течение 30 минут, после чего центрифугируют 5 минут при 1500 об/мин. Через 3-6 часов после завершения центрифугирования планшет прочитывают на счетчике Wallac Microbeta с помощью программы, нормализованной в течение 1 минуты для счета по тритию. Данные анализируют, используя 4-параметрическое логистическое уравнение. Базальную активность, когда в лунки не добавляют гистамин, используют как минимальную.
Результаты
Соединения примеров E1-3, E5-149, E151-230, E233-235, E237-256, E258, E260-270, E273 и E275-288 тестируют с помощью функционального антагонистического анализа гистамина H3 и обнаруживают, что они проявляют антагонизм в следующем интервале: 6,5-10,5 pKb. Более конкретно, соединения примеров 1, 52, 121, 125 и 217 проявляют антагонизм в следующем интервале: 9,0-10,5 pKb. Еще более конкретно, соединение примера 121 проявляет антагонизм > 9,5 pKb.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ ПРОИЗВОДНЫЕ БЕНЗАЗЕПИНА | 2003 |
|
RU2423353C1 |
| ПРОИЗВОДНЫЕ 1,2,4,5-ТЕТРАГИДРОБЕНЗО[D]АЗЕПИНОВ И ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ИХ ОСНОВЕ | 2000 |
|
RU2240317C2 |
| КОНДЕНСИРОВАННЫЕ ПРОИЗВОДНЫЕ АЗЕПИНА И ИХ ИСПОЛЬЗОВАНИЕ В КАЧЕСТВЕ АНТИДИУРЕТИЧЕСКИХ АГЕНТОВ | 2001 |
|
RU2269517C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ АЗОТИСТЫЕ ПРОИЗВОДНЫЕ ПИРРОЛА, ИХ ПОЛУЧЕНИЕ И ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2008 |
|
RU2473543C2 |
| ПРОИЗВОДНЫЕ БЕНЗИМИДАЗОЛА В КАЧЕСТВЕ ИНГИБИТОРОВ ФАКТОРА Ха | 2004 |
|
RU2346944C2 |
| НОВЫЙ ИНГИБИТОР β-ЛАКТАМАЗЫ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2019 |
|
RU2800050C2 |
| НОВЫЙ ИНГИБИТОР бета-ЛАКТАМАЗЫ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2693898C2 |
| АЗАИНДОЛЬНЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ФАКТОРА Xa | 2004 |
|
RU2330853C2 |
| КОНДЕНСИРОВАННЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1991 |
|
RU2095361C1 |
| ПИРРОЛИДИНОВЫЕ И ПИПЕРИДИНОВЫЕ СОЕДИНЕНИЯ | 2020 |
|
RU2803455C1 |
Настоящее изобретение относится к производным бензазепина формулы (I), где R1 представляет собой незамещенный циклобутил, R2 представляет собой 2-пиразинил, замещенный CON(H)(Me), или 2-пиридинил-М-пирролидинил, где указанная пирролидинильная группа замещена группой =O; которое представляет собой: метиламид 5-(3-циклобутил-2,3,4,5-тетрагидро
-1Н-бензо[d]азепин-7-илокси) пиразин-2-карбоновой кислоты
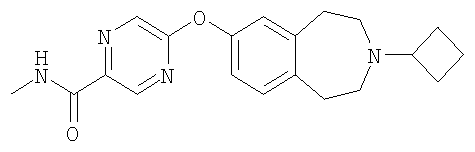
или 1-{6-[(3-циклобутил-2,3,4,5-тетрагидро
-1Н-3-бензазепин-7-ил)окси]-3-пиридинил}-2-пирролидинон
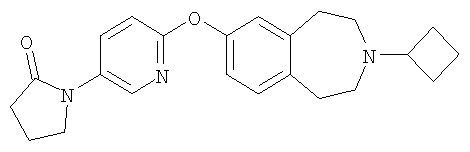
которые обладают сродством к рецептору гистамина НЗ, к способам их получения и к фармацевтическим композициям, содержащим данные соединения.
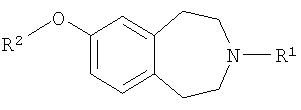
7 н. и 4 з.п.ф-лы.
1. Соединение общей формулы (I)
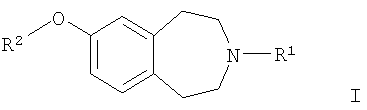
где R1 представляет собой незамещенный циклобутил;
R2 представляет собой 2-пиразинил, замещенный CON(H)(Me), или 2-пиридинил-М-пирролидинил, где указанная пирролидинильная группа замещена группой =O; которое представляет собой:
метиламид 5-(3-циклобутил-2,3,4,5-тетрагидро-1Н-бензо[d]азепин-7-илокси)пиразин-2-карбоновой кислоты
 ; или
; или
1-{6-[(3-циклобутил-2,3,4,5-тетрагидро-1Н-3-бензазепин-7-ил)окси]-3-пиридинил}-2-пирролидинон
 ;
;
или их фармацевтически приемлемую соль.
2. Соединение формулы (I) по п.1, которое представляет собой 1-{6-[(3-циклобутил-2,3,4,5-тетрагидро-1Н-3-бензазепин-7-ил)окси]-3-пиридинил}-2-пирролидинон

или его фармацевтически приемлемую соль.
3. Соединение формулы (I) по п.1, которое представляет собой 1-{6-[(3-циклобутил-2,3,4,5-тетрагидро-1Н-3-бензазепин-7-ил)окси]-3-пиридинил}-2-пирролидинон
 .
.
4. Фармацевтически приемлемая соль по п.2, которая представляет собой кислотно-аддитивную соль, образованную 1-{6-[(3-циклобутил-2,3,4,5-тетрагидро-1Н-3-бензазепин-7-ил)окси]-3-пиридинил}-2-пирролидиноном и кислотой.
5. Фармацевтически приемлемая соль по п.4, где кислота представляет собой малеиновую, хлористоводородную, бромистоводородную, фосфорную, уксусную, фумаровую, салициловую, серную, лимонную, молочную, миндальную, виннокаменную и метансульфоновую кислоту.
6. Фармацевтическая композиция, обладающая сродством к рецептору гистамина Н3, которая содержит терапевтически эффективное количество 1-{6-[(3-циклобутил-2,3,4,5-тетрагидро-1Н-3-бензазепин-7-ил)окси]-3-пиридинил}-2-пирролидинона
 или
или
его фармацевтически приемлемой соли, и фармацевтически приемлемый носитель или наполнитель.
7. 1-{6-[(3-циклобутил-2,3,4,5-тетрагидро-1Н-3-бензазепин-7-ил)окси]-3-пиридинил}-2-пирролидинон или его фармацевтически приемлемая соль, используемая в качестве терапевтического вещества, обладающего сродством к рецептору гистамина Н3.
8. Способ получения соединения формулы (I) по п.1 или его фармацевтически приемлемой соли
 ,
,
где R1 представляет собой незамещенный циклобутил;
R2 представляет собой 2-пиразинил, замещенный CON(H)(Me), 2-пиридинил-N-пирролидинил, где указанная пирролидинильная группа замещена группой =O;
где соединение соответственно является метиламидом 5-(3-циклобутил-2,3,4,5-тетрагидро-1Н-бензо[с1]азепин-7-ил окси)пиразин-2-карбоновой кислоты
 ; или
; или
1-{6-[(3-циклобутил-2,3,4,5-тетрагидро-1Н-3-бензазепин-7-ил)окси]-3-пиридинил}-2-пирролидиноном

или их фармацевтически приемлемой солью, который включает взаимодействие соединения формулы (II)
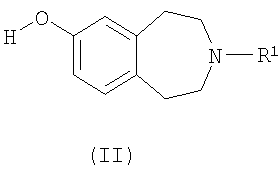
где R1 определен выше,
с соединением формулы R2'-L1, где R2' такой, как определено выше для R2,
а L1 обозначает подходящую уходящую группу, такую как атом галогена или необязательно активированная гидроксильная группа.
9. Способ получения соединения формулы (I) по п.1 или его фармацевтически приемлемой соли

где R1 представляет собой незамещенный циклобутил;
R2 представляет собой 2-пиразинил, замещенный CON(H)(Me), 2-пиридинил-N-пирролидинил, где указанная пирролидинильная группа замещена группой =O;
где соединение соответственно является метиламидом 5-(3-циклобутил-2,3,4,5-тетрагидро-1Н-бензо[d]азепин-7-ил окси)пиразин-2-карбоновой кислоты

или
1-{6-[(3-циклобутил-2,3,4,5-тетрагидро-1Н-3-бензазепин-7-ил)окси]-3-пиридинил}-2-пирролидиноном

или их фармацевтически приемлемой солью, который включает взаимодействие соединения формулы (III)
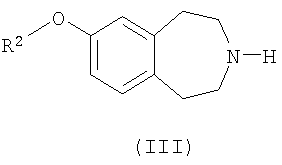
где R2 как определено выше, с соединением формулы R1'-L2, где R1' такой, как определено выше для R1, а L2 обозначает подходящую уходящую группу, такую как атом галогена.
10. Способ получения соединения формулы (I) по п.1 или его фармацевтически приемлемой соли
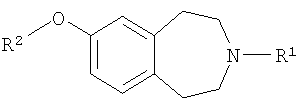 ,
,
где R1 представляет собой незамещенный циклобутил;
R2 представляет собой 2-пиразинил, замещенный CON(H)(Me), 2-пиридинил-N-пирролидинил, где указанная пирролидинильная группа замещена группой =O;
где соединение соответственно является метиламидом 5-(3-циклобутил-2,3,4,5-тетрагидро-1Н-бензо[с1]азепин-7-ил окси)пиразин-2-карбоновой кислоты

или
1-{6-[(3-циклобутил-2,3,4,5-тетрагидро-1Н-3-бензазепин-7-ил)окси]-3-пиридинил}-2-пирролидиноном

или их фармацевтически приемлемой солью, который включает взаимодействие соединения формулы (III)

где R2 такой, как определено выше, с кетоном формулы R1'-O, где R1' такой, как определен для R1.
11. Способ получения соединения формулы (I) по п.1 или его фармацевтически приемлемой соли
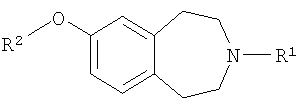 ,
,
где R1 представляет собой незамещенный циклобутил;
R2 представляет собой 2-пиразинил, замещенный CON(H)(Me), 2-пиридинил-N-пирролидинил, где указанная пирролидинильная группа замещена группой =O;
где соединение соответственно является метиламидом 5-(3-циклобутил-2,3,4,5-тетрагидро-1Н-бензо[d]азепин-7-илокси)пиразин-2-карбоновой кислоты

или
1-{6-[(3-циклобутил-2,3,4,5-тетрагидро-1Н-3-бензазепин-7-ил)окси]-3-пиридинил}-2-пирролидиноном

или их фармацевтически приемлемой солью,
который включает удаление защитной группы с защищенного соединения формулы (I).
| АДАПТИВНЫЙ ТРЕХПОЗИЦИОННЫЙ РЕГУЛЯТОР | 2010 |
|
RU2408913C1 |
| УСТРОЙСТВО для КОНТРОЛЯ УГЛОВОЙ СКОРОСТИ ВАЛА | 0 |
|
SU234760A1 |
| Устройство для предупреждения столкновений поездов | 1925 |
|
SU6254A1 |
| 2,3,4,5-ТЕТРАГИДРО-1Н-3-БЕНЗАЗЕПИНЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ЛЕЧЕНИЯ И СПОСОБЫ ПОЛУЧЕНИЯ | 1993 |
|
RU2114839C1 |
| PILLOT С | |||
| et al "CIPROXIFAN, A HISTAMINE H3-RECEPTOR ANTAGONIST/INVERSE AGONIST, POTENTIATES NEUROCHEMICAL AND BEHAVIORAL EFFECTS OFHALOPERIDOL IN THE RAT" J.NEUROSCI., 2002, Aug, 22(16):7272-7280 | |||
| LIGNEAU X | |||
| et al | |||
| "NEUROCHEMICAL AND | |||
Авторы
Даты
2010-05-10—Публикация
2003-12-18—Подача