Изобретение относится к новому химическому соединению класса 19β,28-эпокси-18α-олеанановых 2,3-секотритерпеноидов, конкретно к ацетилгидразону 1-циано-19β,28-эпокси-2,3-секо-18α-олеан-3-аля, который проявляет ингибирующую активность в отношении вируса везикулярного стоматита (ВВС) штамм «Индиана».
Описания заявляемого соединения и его свойств в источниках информации не обнаружено.
Ближайший аналог описываемого соединения по структуре - 1-циано-19β,28-эпокси-2,3-секо-18α-олеан-3-аль [Толмачева И.А., Назаров А.В., Майорова О.А., Гришко В.В. Синтез лупановых и 19β,28-эпокси-18α-олеанановых 2,3-секопроизводных на основе бетулина. // Химия природных соединений. - 2008. - №5. - С.491-494] указанной активности не проявляет.
Несмотря на создание вакцины против вируса везикулярного стоматита, остается актуальным использование противовирусных агентов и поиск новых вирусингибирующих соединений.
Так, известен широко применяемый для профилактики и лечения широкого спектра вирусных инфекций препарат Интерферон человеческий лейкоцитарный, который обладает профилактической активностью в отношении ВВС [Basu M., Maitra R.K., Xiang Y., Meng X., Banerjee A.K., Bose S. Inhibition of vesicular stomatitis vims infection in epithelial cells by alpha interferon-induced soluble secreted proteins. // Journal of General Virology. - 2006. - V.87. - P.2653-2662]. Однако этот препарат не оказывает вирусингибирующего эффекта в условиях первичного инфицирования клеток вирусом ВВС.
Среди анти-ВВС активных соединений описаны полициклические тритерпеноиды, проявляющие in vitro вирусингибирующее действие в условиях первичного ВВС-инфицирования клеток млекопитающих.
Известна тритерпеновая глицирретовая кислота [Патент US №4891221, А61К 35/14 Whole blood antiviral process and composition, опубл. 02.01.1990], подавляющая репродукцию ВВС. Недостатком данного соединения является высокая вирусингибирующая доза (от 0,1 до 0,7 вес.%) и необходимость подкисления среды культивирования клеток до уровня рН 6,5-7,4 для проявления тритерпеноидом анти-ВВС активности.
Известна также динатриевая соль полусинтетического олеананового производного циклоксолона [Dargan D.J., Galt C.B., Subak-Sharpe J.H. Effect of cicloxolone sodium on the replication of vesicular stomatitis virus in BSC-1 cells. // Journal of General Virology. - 1992. - V.73. - P.397-406], характеризующаяся вирулицидной активностью в отношении ВВС и ингибирующим действием в отношении всех стадий репликационного цикла ВВС. Основной недостаток динатриевой соли циклоксолона - высокая (300 µM) вирусингибирующая доза препарата.
Ближайшим аналогом заявляемого соединения по противовирусному действию является бетулиновая кислота [Kaminska Т., Kaczor J., Rzeski W., Wejksza К., Kandefer-Szerszen M., Witek M. A comparison of the antiviral activity of three triterpenoids isolated from Betula alba bark. // Annales Universitatis Mariae Curie-Sklodowska: Sectio C. Biologia. - 2004. - V.LIX. - P.1-7], которая in vitro наряду с ВВС-ингибирующей активностью проявляет вирулицидное действие (ЕС50 26,8 мкг/мл) в отношении ВВС.
В указанной публикации приведены данные по противовирусному (ЕС50 1,0 мкг/мл, TI-20) действию коммерческого реактива 90% бетулиновой кислоты Sigma Aldrich (США). По нашим экспериментальным данным противовирусная активность 95% бетулиновой кислоты значительно ниже. Таким образом, в качестве недостатка бетулиновой кислоты можно отметить ее невысокую вирусингибирующую активность. Кроме того, не обнаружено сведений о профилактических свойствах бетулиновой кислоты в отношении ВВС.
Задачей изобретения является синтез новых тритерпеновых производных, проявляющих профилактическую анти-ВВС активность и ингибирующих репродукцию ВВС в первично инфицированных клетках млекопитающих.
Для решения поставленной задачи синтезирован ацетилгидразон 1-циано-19β,28-эпокси-2,3-секо-18α-олеан-3-аля формулы I.
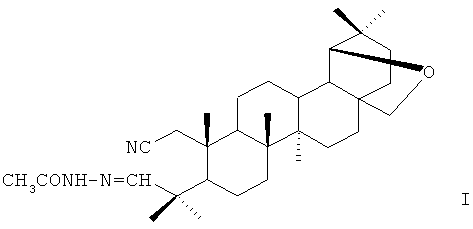
Ацетилгидразон 1-циано-19β,28-эпокси-2,3-секо-18α-олеан-3-аля формулы I проявляет ингибирующую активность в отношении вируса везикулярного стоматита штамм «Индиана».
Синтезированное соединение представляет собой мелкокристаллическое вещество белого цвета, хорошо растворимое в хлороформе, дихлорметане, четыреххлористом углероде, этиловом спирте, бензоле, толуоле, диметилсульфоксиде. Указанное соединение плохо растворимо в гексане и не растворимо в воде.
Синтез соединения формулы I проводили способом, включающим взаимодействие гидразида уксусной кислоты с 1-циано-19β,28-эпокси-2,3-секо-18β-олеан-3-алем в этаноле в присутствии каталитических количеств ледяной уксусной кислоты.
Получение ацетилгидразона 1-циано-19β,28-эпокси-2,3-секо-18α-олеан-3-аля I
К раствору 0,44 ммоль 1-циано-19β,28-эпокси-2,3-секо-18α-олеан-3-аля в 15 мл этанола добавляли 0,44 ммоль гидразида уксусной кислоты и 2 капли ледяной уксусной кислоты. Реакционную смесь оставляли при комнатной температуре в течение 7 часов. Контроль за ходом реакции проводили с помощью метода ТСХ. Растворитель упаривали, остаток очищали с помощью колоночной хроматографии на силикагеле. После очистки выход полученного соединения составил 0,23 г (45%); Rf 0,12 (хлороформ: этилацетат - 10:1); т. пл. 65-67°С (хлороформ: этилацетат - 10:1);
[α]21 D+30,0° (с 0,5; CHCl3).
Найдено, %: С 75,26; Н 9,85; N 8,47. C32H51N3O2.
Вычислено, %: С 75,40; Н 10,08; N 8,24.
Структура соединения формулы I подтверждена методами ИК и ЯМР спектроскопии. ИК спектр регистрировали на спектрофотометре SPECORD М80 (Германия) в пасте с вазелиновым маслом. Спектры 1Н- и 13С-ЯМР записывали для растворов в CDCl3 на спектрометре «Varian Mercury+» (США) при рабочей частоте прибора 300,0 или 75,5 МГц, внутренний стандарт - ГМДС. Температуру плавления измеряли на приборе для определения температуры плавления ПТП (Россия). Величину удельного оптического вращения регистрировали для растворов в CHCl3 на поляриметре 341 модели Perkin-Elmer (США) при длине волны 589 нм. Элементный анализ (С, Н, N) выполняли с помощью элементного анализатора Leco CHNS-9321P (Нидерланды), данные элементного анализа соответствовали расчетным.
Спектральные характеристики соединения формулы I представлены в таблице 1.
Исследование противовирусной активности ацетилгидразона 1-циано-19β,28-эпокси-2,3-секо-18α-олеан-3-аля I
Цитотоксичность соединений оценивали in vitro в отношении перевиваемой линии клеток почки эмбриона свиньи (СПЭВ) по известной методике [Первичное изучение антивирусных свойств синтетических и природных соединений. Методические рекомендации. /Вотяков В.И., Бореко Е.И., Владыко Г.В., Карако Н.И., Галегов Г.А., Леонтьева Н.А. Минск, 1986. - 25 с.]. Соединение I растворяли в 10% этаноле (концентрация маточного раствора - 5 мг/мл) и затем в среде поддержки - до требуемых концентраций (концентрация маточного раствора бетулиновой кислоты в 10% ДМСО составляла 2,667 мг/мл). Через 48 часов инкубации подсчитывали долю жизнеспособных клеток и определяли токсичную концентрацию (ЦД50), вызывающую гибель 50% клеток СПЭВ. Оценивали также максимальную из исследованных доз вещества (МПК), не вызывающую морфологических изменений ткани. Установлено, что показатели ЦД50 и МПК соединения I составляют 31,25 и 1,95 мкг/мл соответственно. По показателю ЦД50 соединение I более чем в 16 раз уступает интерферону. В то же время по уровню цитотоксического действия соединение I в 6 раз менее токсично по сравнению с бетулиновой кислотой (таблица 2).
Противовирусные свойства соединения I исследовали in vitro с использованием методик, соответствующих двум моделям инфицирования клеток млекопитающих.
Согласно методике 1 [Отраслевой стандартный образец активности лейкоцитарного интерферона альфа типа. Инструкция по применению. - М.: ФГУН ГНИИСК им. Л.А.Тарасовича, 2008], демонстрирующей защиту клеточной системы от поражения вирусом, клетки СПЭВ до внесения ВВС предварительно инкубировали с исследуемыми соединениями в течение 24 часов. В условиях данной модели (таблица 2) среднеэффективная концентрация (ИД50) соединения I, на 50% подавляющая развитие ВВС, составляет 0,0001589 мкг/мл, что значительно превышает аналогичные показатели интерферона (ИД50 0,689 мкг/мл) и бетулиновой кислоты (ИД50 62,55 мкг/мл) (таблица 2). При этом химиотерапевтический индекс (ХТИ) соединения I, рассчитываемый как отношение ЦД50 к ИД50, составил 196665. Отношение МПК к ИД50 для соединения I достигает 12272, что превышает аналогичные показатели интерферона и бетулиновой кислоты в 52 и 306800 раз соответственно.
Исследование противовирусной активности соединений в условиях методики 2 [Первичное изучение антивирусных свойств синтетических и природных соединений. Методические рекомендации. / Вотяков В.И., Бореко Е.И., Владыко Г.В., Карако Н.И., Галегов Г.А., Леонтьева Н.А. Минск, 1986. - 25 с.], демонстрирующей подавление размножения вируса в первично инфицированных клетках, свидетельствует (таблица 3), что соединение I, несмотря на более низкую (по сравнению с первой моделью) вирусингибирующую активность (ИД50 0,21 мкг/мл), имеет высокий показатель ХТИ 149, который в 2129 раз превышает такой бетулиновой кислоты. Интерферон в условиях данной модели противовирусной активности не проявил.
Результаты исследования противовирусной активности соединения формулы I в сравнении с аналогами представлены в таблицах 2 и 3.
Заявляемое соединение формулы I обладает высокой профилактической активностью ИД50 0,0001589 мкг/мл и эффективно ингибирует репродукцию вируса везикулярного стоматита штамм «Индиана» в первично инфицированных клетках ИД50 0,21 мкг/мл. При этом уровень противовирусной активности и величина ХТИ соединения I значительно превосходят аналогичные показатели известных анти-ВВС активных аналогов интерферона и бетулиновой кислоты.

| название | год | авторы | номер документа |
|---|---|---|---|
| ТРИТЕРПЕНОИДЫ С ФРАГМЕНТОМ ЕН-НИТРИЛА В А-ПЕНТАЦИКЛЕ | 2012 |
|
RU2496785C1 |
| 2,3-СЕКО-ПРОИЗВОДНЫЕ БЕТУЛОНОВОЙ КИСЛОТЫ | 2009 |
|
RU2410390C1 |
| А-СЕКОТРИТЕРПЕНОИДЫ С ФРАГМЕНТОМ МЕТИЛКЕТОНА | 2013 |
|
RU2537840C1 |
| ЛУПАНОВЫЕ А-СЕКОТРИТЕРПЕНОИДЫ, ПРОЯВЛЯЮЩИЕ ПРОТИВОВИРУСНУЮ АКТИВНОСТЬ | 2011 |
|
RU2470003C1 |
| ЦИТОТОКСИЧЕСКАЯ И ПРОТИВОВИРУСНАЯ АКТИВНОСТЬ 3-АЦИЛОКСИМЕТИЛ-3-ОКСО-1-ЦИАНО-2,3-СЕКО-2-НОР-ТРИТЕРПЕНОИДОВ | 2018 |
|
RU2686100C1 |
| ЦИТОТОКСИЧЕСКАЯ И ПРОТИВОВИРУСНАЯ АКТИВНОСТЬ 3-АЦИЛОКСИМЕТИЛ-3-ОКСО-1-ЦИАНО-2,3-СЕКО-2-НОР-ТРИТЕРПЕНОИДОВ | 2018 |
|
RU2682669C1 |
| 3-ГИДРОКСИМИНОПРОИЗВОДНЫЕ 2,3-СЕКОЛУПАНОВОГО ТИПА, ПРОЯВЛЯЮЩИЕ ИНГИБИРУЮЩУЮ АКТИВНОСТЬ В ОТНОШЕНИИ ВИРУСА ГРИППА А И ВИЧ-1 | 2011 |
|
RU2475476C1 |
| СПОСОБ ПОЛУЧЕНИЯ А-СЕКОТРИТЕРПЕНОВЫХ С-3(28) МОНО-И ДИАМИДОВ И ИХ СЕКОИНТЕРМЕДИАТОВ | 2013 |
|
RU2525546C1 |
| ТРИТЕРПЕНОВЫЕ АМИДЫ ЛУПАНОВОГО ТИПА С ФРАГМЕНТОМ 2-АМИНОБУТАН-1-ОЛА, ПРОЯВЛЯЮЩИЕ ВИРУСИНГИБИРУЮЩУЮ И ВИРУЛИЦИДНУЮ АКТИВНОСТЬ | 2017 |
|
RU2664804C1 |
| ВОДОРАСТВОРИМОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОВИРУСНОЙ И ИММУНОМОДУЛИРУЮЩЕЙ АКТИВНОСТЬЮ, НА ОСНОВЕ СОЕДИНЕНИЯ ИОННОГО СЕРЕБРА С МЕТИЛЕНОВЫМ СИНИМ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2008 |
|
RU2390343C1 |
Ацетилгидразон 1-циано-19β,28-эпокси-2,3-секо-18α-олеан-3-аля формулы I:
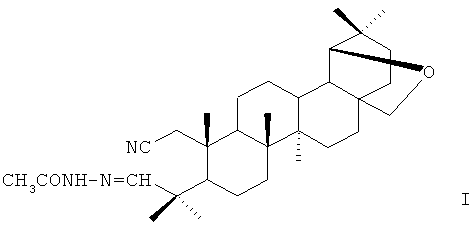
обладает высокой профилактической активностью ИД50 0,0001589 мкг/мл и эффективно ингибирует репродукцию вируса везикулярного стоматита штамм «Индиана» в первично инфицированных клетках ИД50 0,21 мкг/мл. 1 з.п.ф-лы, 3 табл.
1. Ацетилгидразон 1-циано-19β,28-эпокси-2,3-секо-18α-олеан-3-аля формулы I

2. Ацетилгидразон 1-циано-19β,28-эпокси-2,3-секо-18α-олеан-3-аля формулы I по п.1, проявляющий ингибирующую активность в отношении вируса везикулярного стоматита штамм «Индиана».
| KAMINSKA Т | |||
| et al // Annales Univers.M | |||
| Curie-Sklodowska, 2004, v LIX, p 1-7 | |||
| US 4891221 A, 02.01.1990 | |||
| Устройство для записи речевых сигналов | 1977 |
|
SU687465A1 |
| ТОЛМАЧЁВА И.А., НАЗАРОВ А.В | |||
| И и др.// Хим | |||
| прир | |||
| соед | |||
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| Бензиновая зажигалка | 1923 |
|
SU491A1 |
Авторы
Даты
2011-09-20—Публикация
2010-04-08—Подача