Область, к которой относится изобретение
Настоящее изобретение относится к антителам или к их фрагментам, обладающим высокой аффинностью к человеческим α-синуклеиновым протофибриллам и низкой способностью к связыванию с α-синуклеиновыми мономерами, где указанные антитела или их фрагменты имеют последовательности специфических гипервариабельных областей (CDR). Настоящее изобретение также относится к композициям, содержащим такое антитело или его фрагмент, и к способам детектирования α-синуклеиновых протофибрилл с использованием указанного антитела или его фрагмента. В других своих вариантах, настоящее изобретение относится к способам предупреждения, замедления развития или лечения нейродегенеративного расстройства, ассоциированного с α-синуклеиновой патологией, путем введения указанного антитела или его фрагмента, и к применению такого антитела или его фрагмента в целях получения фармацевтической композиции для лечения нейродегенеративного расстройства, ассоциированного с α-синуклеиновой патологией. Настоящее изобретение также относится к применению указанного антитела или его фрагмента для диагностики или мониторинга развития нейродегенеративного расстройства, ассоциированного с α-синуклеиновой патологией, и к способам снижения или ингибирования агрегации α-синуклена путем введения указанного антитела или его фрагмента.
Предшествующий уровень техники
Болезнь Парикинсона (БП) и деменция, ассоциированная с образованием телец Леви (ДТЛ), представляют собой два наиболее распространенных нейродегенеративных расстройства, ассоциированных с α-синуклеиновой патологией головного мозга. БП представляет собой наиболее распространенное нарушение двигательных функций и характеризуется ригидностью, гиперкинезией, тремором и постуральной нестабильностью. Известно, что болезнью Паркинсона страдает приблизительно от четырех до шести миллионов человек во всем мире. Из всех случаев заболеваний деменцией, ДТЛ составляет 5-15%. Помимо забывчивости и других симптомов деменции, котрые часто являются неустойчивыми, пациенты с ДТЛ обычно страдают рецидивирующими припадками и зрительными галлюцинациями.
Аккумуляция α-синуклеина внутри нейронов приводит к образованию либо телец Леви, круглых и крупных включений эозинофильного гуалина длиной 10-20 мкм, либо нейритов Леви, удлиненных нитеподобных дистрофических аксонов и дендритов. В головном мозге пациентов с БП, отложение телец Леви и нейритов Леви ограничено, главным образом, нейронами, соединяющими полосатое тело с черным веществом. Эти клетки играют очень важную роль в осуществлении двигательных и постуральных функций, что объясняет природу симптомов БП. В головном мозге пациентов с ДТЛ, обширные отложения телец Леви и нейритов Леви наблюдаются в среднем мозге и в области коры головного мозга.
Альфа-синуклеин представляет собой белок, который присутствует, главным образом, внутри нейронов. В нейронах, α-синуклеин локализован преимущественно в пресинаптических нейронах, а поэтому было высказано предположение, что он играет определенную роль в регуляции синаптической активности. Были идентифицированы три основные изоформы α-синуклеина, из которых самая длинная и самая распространенная форма содержит 140 аминокислот. Эта форма рассмотрена в настоящем описании, и свойства антител, направленных против альфа-синуклеина (α-синуклеина) и описанных в настоящем изобретении, относятся именно к этой изоформе α-синуклеина.
Тельца Леви, помимо α-синуклеина, состоят из различных молекул широкого ряда, одна из которых представляет собой 4-гидрокси-2-ноненал (HNE), α,β-ненасыщенный гидроксиалкенал (Qin et al., 2007). Было показано in vitro, что HNE может модифицировать α-синуклеин и тем самым облегчать олигомеризацию α-синуклеина. В частности, было показано, что HNE усиливает и стабилизирует образование протофибрилл, то есть, более крупных растворимых олигомерных форм α-синуклеина (Qin et al., 2007; заявка WO 2009/133521, вводимые в настоящее описание посредством ссылки).
Окислительный стресс приводит к развитию ряда нейродегенеративных расстройств, характеризующихся патологической аккумуляцией α-синуклеина с неправильной укладкой. Различные реакционноспособные молекулы кислорода могут индуцировать перокисление липидов, таких как клеточные мембраны или липопротеины, а также могут приводить к образованию в высокой степени реакционноспособных альдегидов из полиненасыщенных жирных кислот (Yoritaka et al., 1996).
Патологии головного мозга, характерные для болезни Альцгеймера (БА), то есть наличие амилоидных бляшек и нейрофибриллярных клубков, наблюдается приблизительно в 50% случаев заболевания ДТЛ. Однако, неясно, являются ли такие параллельные патологии двумя различными заболеваниями, либо они представляют лишь вариант каждого из соответствующих расстройств. Иногда, случаи заболевания с одновременным наличием этих патологий описаны в литературе как вариант БА с образованием телец Леви (Hansen et al., 1990).
В недавно проведенных исследованиях была выявлена роль α-синуклеина в развитии болезни Альцгеймера и синдрома Дауна, поскольку было продемонстрировано, что при таких расстройствах белок α-синуклеин аккумулируется в области конечностей (Crews et al., 2009).
HNE взаимодействует с боковыми цепями цистеина, гистидина и лизина, и модифицирует такие боковые цепи, что приводит к значительному изменению структуры и физических свойств этих боковых цепей. Следовательно, HNE может взаимодействовать либо с атомом углерода в положении C-3, либо с альдегидной группой, либо с их комбинациями. Поэтому HNE может ковалентно модифицировать как межмолекулярные, так и внутримолекулярные белки.
Генетика болезни Паркинсона и деменции, ассоциированной с образованием телец Леви
Редко встречающиеся доминантно наследуемые формы БП и ДТЛ могут быть вызваны точковыми мутациями или дупликациями гена α-синуклеина. Сообщалось, что патогенные мутации A30P и A53T (Kruger et al., 1998) (Polymeropoulos et al., 1998) и дупликация этого гена (Chartier-Harlin et al. 2004) приводят к развитию наследственной БП, и кроме того сообщалось, что другая мутация α-синуклеина, E46K (Zarranz et al, 2004), а также утроение гена α-синуклеина (Singleton et al., 2003) приводят к развитию БП или ДТЛ.
Патогенные изменения в результате мутаций гена α-синуклеина понятны лишь частично. Однако, данные in vitro показали, что мутации A30P и A53T приводят к увеличению уровня агрегации (Conway et al., 2000). В процессе агрегации участвуют молекулы α-синуклеина широкого ряда, различающиеся по своему составу (мономеры, димеры, олигомеры, включая протофибриллы), и все эти молекулы обладают различными токсическими свойствами. Пока неясно, какие именно виды молекул оказывают токсическое действие на головной мозг. Однако, недавно проведенные исследования позволяют предположить, что особенно высокой степенью нейротоксичности обладают олигомерные формы α-синуклеина. Дополнительное свидетельство о роли олигомеров было получено после обнаружения того факта, что некоторые мутации α-синуклеина (A30P и A53T), являющиеся причиной наследственной болезни Паркинсона, приводят к увеличению степени олигомеризации.
До сих пор абсолютно неизвестно, каким образом инициируется каскад реакций агрегации α-синуклеина. Возможно, что изменение конформации мономерного α-синуклеина инициирует образование димеров и тримеров, что приводит к образованию более высокомолекулярных растворимых олигомеров, включая протофибриллы, после чего эти молекулы промежуточного размера осаждаются в виде нерастворимых фибрилл в тельцах Леви. Также известно, что олигомеры α-синуклеина, сразу после их образования, могут связываться с новыми мономерами и/или с более мелкими мультимерами α-синуклеина, и тем самым ускоряют процесс образования фибрилл. Вероятно, что такие эффекты рассеяния могут также происходить во внеклеточном пространстве, и недавно проведенные исследования позволяют предположить, что α-синуклеиновая патология может передаваться от нейрона к нейрону в пораженном головном мозге.
Помимо нейропатологических изменений при α-синуклеинопатии, уровни белка α-синуклеина повышаются, в основном, в пораженных участках головного мозга (Klucken et al., 2006).
Патология при α-синуклеинопатии является, в основном, внутриклеточной, что создает определенную проблему при разработке способа иммунной терапии. Однако, очевидно, что фракция активно индуцируемых или пассивно вводимых антител может также связываться с антигенами их мишени внутри нейронов. Кроме того, идентификация α-синуклеина в плазме и в цереброспинальной жидкости (El-Agnaf et al, 2006) показала, что указанный белок не присутствует исключительно в нейронах. Снижение уровня такого внеклеточного α-синуклеина может приводить к сдвигу равновесия между внутриклеточными и внеклеточными пулами белков, а также к снижению уровня внутриклеточного α-синуклеина. Имеются данные, которые позволяют предположить, что α-синуклеин в растворе может проникать через липидные бислои в клеточных мембранах, а поэтому он может быть либо интернализирован в клетку, либо выведен из этой клетки. Недавно проведенные исследования продемонстрировали, что α-синуклеин обладает токсическим действием во внеклеточном пространстве, что служит правдоподобным объяснением механизма распространения α-синуклеиновой патологии по всему головному мозгу по мере прогрессирования заболевания. Исследования показали, что патология телец Леви передается привитым нейронам у подвергнутых трансплантации пациентов с БП (Li et al. 2008). Кроме того, α-синуклеин передается соседним нейронам посредством эндоцитоза, и передача агрегатов α-синуклеина от клетки в клетку ассоциируется с гибелью нейронов и с прогрессированием патологии при БП и других α-синуклеинопатиях (Desplats et al. 2009).
Диагностика БП и ДТЛ
В настоящее время существует необходимость в разработке усовершенствованных средств диагностики и способов идентификации риска развития нейродегенеративного заболевания, ассоциированного с α-синуклеиновой патологией. На сегодняшний день, не существует какого-либо биохимического метода, который мог бы облегчить врачу-клиницисту диагностику клинических симптомов у пациента на ранних стадиях развития заболевания, еще до серьезного поражения головного мозга.
По мере появления все новых и совершенных методов терапии, особую важность приобретает разработка точных диагностических анализов. В настоящее время, для пациентов с БП применяется только симптоматическое лечение (путем компенсации потери активного допамина в головном мозге). Для пациентов с ДТЛ выбор методов терапии является еще более ограниченным. Тем не менее, врачи-клиницисты часто ищут возможности достижения благоприятных эффектов у пациентов с ДТЛ с применением стандартных методов лечения БА, то есть, с использованием ингибиторов холинэстеразы. В любом случае, ни одна из существующих стратегий лечения α-синуклеинопатий не может быть использована для подавления процессов, лежащих в основе описанного заболевания. Кроме того, существует также необходимость в мониторинге прогрессирования заболевания и эффекта его лечения. Обзор различных методов, предотвращающих прогрессирование болезни Паркинсона, можно найти у George et al., 2009.
Принимая во внимание вышеуказанное участие α-синуклеина в нескольких нейродегенеративных расстройствах, следует отметить, что необходимо разработать новые способы лечения, которые могли бы предотвращать или снижать действие токсических молекул α-синуклеина, а также получить биомаркеры, подходящие для мониторинга эффектов новых способов лечения и обладающие высокой прогностической специфичностью.
Описание сущности изобретения
Настоящее изобретение относится к улучшенным антителам и к их фрагментам, обладающим высокой аффинностью по отношению к человеческим α-синуклеиновым протофибриллам и низкой способностью к связыванию с α-синуклеиновыми мономерами. Настоящее изобретение также относится к композициям, содержащим такое антитело или его фрагмент, и к способам детектирования α-синуклеиновых протофибрилл с использованием такого антитела или его фрагмента. В других своих вариантах, настоящее изобретение относится к способам предупреждения, замедления развития или лечения нейродегенеративного расстройства, ассоциированного с α-синуклеиновой патологией, где указанный способ включает введение такого антитела или его фрагмента, и к применению такого антитела или его фрагмента в целях получения фармацевтической композиции для лечения нейродегенеративного расстройства, ассоциированного с α-синуклеиновой патологией. Настоящее изобретение также относится к применению такого антитела или его фрагмента для диагностики или мониторинга развития нейродегенеративного расстройства, ассоциированного с α-синуклеиновой патологией, и к способам снижения или ингибирования агрегации α-синуклена путем введения указанного антитела или его фрагмента.
В одном из вариантов изобретения, антитело или его фрагмент обладают высокой аффинностью по отношению к человеческим α-синуклеиновым протофибриллам и низкой способностью к связыванию с α-синуклеиновыми мономерами, и имеют три последовательности CDR вариабельной области тяжелой цепи (VH) (VH-CDR-1, VH-CDR-2 и VH-CDR-3) и три последовательности CDR вариабельной области легкой цепи (VL) (VL-CDR-1, VL-CDR-2 и VL-CDR-3), где шесть последовательностей CDR антитела или его фрагмента выбраны из нижеследующих соответствующих групп:
VH-CDR-1 SEQ ID NO: 22, 23, 24, 25, 26 или 27
VH-CDR-2 SEQ ID NO: 28, 29, 30, 31, 32, 33 или 34
VH-CDR-3 SEQ ID NO: 35, 36, 37, 38, 39 или 40
VL-CDR-1 SEQ ID NO: 41, 42, 43, 44, 45 или 46
VL-CDR-2 SEQ ID NO: 47, 48 или 49
VL-CDR-3 SEQ ID NO: 50, 51, 52, 53, 54 или 55.
В другом варианте изобретения, антитело или его фрагмент обладают высокой аффинностью по отношению к человеческим α-синуклеиновым протофибриллам и низкой способностью к связыванию с α-синуклеиновыми мономерами, и имеют три последовательности CDR вариабельной области тяжелой цепи (VH) (VH-CDR-1, VH-CDR-2, и VH-CDR-3) и три последовательности CDR вариабельной области легкой цепи (VL) (VL-CDR-1, VL-CDR-2 и VL-CDR-3), где шесть последовательностей CDR антитела или его фрагмента выбраны из нижеследующих соответствующих групп; причем, указанные последовательности более, чем на 70, 80, 90, 95 или 98% аналогичны любой из указанных последовательностей соответствующих групп:
VH-CDR-1 SEQ ID NO: 22, 23, 24, 25, 26 или 27
VH-CDR-2 SEQ ID NO: 28, 29, 30, 31, 32, 33 или 34
VH-CDR-3 SEQ ID NO: 35, 36, 37, 38, 39 или 40
VL-CDR-1 SEQ ID NO: 41, 42, 43, 44, 45 или 46
VL-CDR-2 SEQ ID NO: 47, 48 или 49
VL-CDR-3 SEQ ID NO: 50, 51, 52, 53, 54 или 55,
и где указанное антитело или его фрагмент связывается с эпитопом в области аминокислотной последовательности 113-140, например, 113-131, а в частности, с эпитопами 125-131, 121-124, 121-127, 121-131, 113-123 или 136-140 иммобилизованного линейного α-синуклеина в системе-модели, содержащей 15-мерные пептиды альфа-синуклеина с перекрыванием в 11 аминокислот.
Антитела, фрагменты, композиции и способы согласно изобретению облегчают диагностику, мониторинг, предупреждение, замедление развития и/или лечение нейродегенеративных расстройств, ассоциированных с α-синуклеиновой патологией, у индивидуумов, стадающих указанными расстройствами, и/или у индивидуумов с риском развития указанных расстройств.
Другие аспекты, варианты и преимущества различных вариантов настоящего изобретения будут более очевидными из нижеследующего подробного описания.
Краткое описание графического материала
Подробное описание изобретения будет более понятным из описания графического материала, где:
На фиг. 1 проиллюстрирована эффективность моноклональных антител, специфичных к протофибриллам, как было определено с помощью конкурентного ELISA-анализа. Этот анализ осуществляли с помощью HNE-стабилизированных α-синуклеиновых протофибрилл, описанных в примере 4.
На фиг. 2A и 2B проиллюстрирована эффективность специфичного к протофибриллам антитела mAb49/G, проанализированная с помощью конкурентного ELISA-анализа, описанного в примере 4. На фиг. 2A показано, что специфичное к протофибриллам моноклональное антитело mAb49/G связывается с высокой аффинностью с человеческими α-синуклеиновыми протофибриллами, стабилизированными HNE или ONE. На фиг. 2B показано, что моноклональное антитело также связывается с высокой аффинностью с HNE-стабилизированными протофибриллами мутированных человеческих форм α-синуклеина, A30P и A53T.
На фиг. 3A-3C проиллюстрирована эффективность специфичных к протофибриллам антител, которая был проанализирована с помощью конкурентного ELISA-анализа, описанного в примере 4. Специфичные к протофибриллам моноклональные антитела связываются с высокой аффинностью с человеческими α-синуклеиновыми протофибриллами дикого типа, стабилизированными либо HNE (PF-HNE), либо ONE (PF-ONE). Моноклональные антитела также связываются с высокой аффинностью с HNE-стабилизированными протофибриллами мутированных человеческих форм α-синуклеина, A30P (A30P-HNE) и A53T (A30P-HNE).
На фиг. 4A и 4B проиллюстрирована количественная оценка α-синуклеиновых протофибрилл, проводимая с помощью «сэндвич»- ELISA-анализа, описанного в примере 5. На фиг. 4A представлен график для специфичного к протофибриллам антитела mAb49/G, используемого в качестве антитела для захвата и детектирующего антитела. На фиг. 4B представлена стандартная кривая, построенная по данным, полученным для HNE-стабилизированных α-синуклеиновых протофибрилл. Эффективность анализа позволяет достигать предела квантификации LOQ=9 пМ.
На фиг. 5A и 5B представлены результаты анализов экстрактов головного мозга, взятых у пациента, страдающего ДТЛ, и контрольных экстрактов человеческого головного мозга, где указанные результаты были получены с помощью «сэндвич»-ELISA-анализа, специфичного в α-синуклеиновым протофибриллам и описанного в примере 6.
На фиг. 6 проиллюстрирован анализ экстрактов головного мозга, взятых у контрольных мышей (ntg, нетрансгенных) и у 5-месячных мышей, полученных от трансгенной (tg) мыши Khale с моделью БП, как описано в примере 7. Ткань головного мозга экстрагировали трис-забуференным физиологическим раствором (TBS) и TBS в присутствии тритона. Анализ проводили с помощью «сэндвич»-ELISA-анализа α-синуклеиновых протофибрилл как описано в примере 5. Специфичное к протофибриллам антитело mAb49/G использовали в качестве антитела для захвата и детектирующего антитела. На этом графике, по оси y отложена оптическая плотность OD450.
На фиг. 7A-7F проиллюстрирован иммуногистохимический (ИГХ) анализ тканей, описанный в примере 8. На фиг. 7A показано, что антитело 38E2/7 связывается с тельцами Леви и с нейритами в черном веществе пациентов с БП и с α-α-синуклеином, используемым в качестве позитивного контроля. На фиг. 7B показано, что антитело 38E2/7 связывается с тельцами Леви и с нейритами в коре головного мозга и в черном веществе пациентов с ДТЛ и с α-α-синуклеином, используемым в качестве позитивного контроля. На фиг. 7С показано, что различные антитела связываются с тельцами Леви и с нейритами в коре головного мозга и в черном веществе пациентов с ДТЛ и с негативным контролем. На фиг. 7D показано, что различные антитела связываются с тельцами Леви и с нейритами в черном веществе пациентов с БП и с негативным контролем. На фиг.7E показано, что антитело 38E2/7 не связывается в черном веществе нормальных индивидуумов и с α-α-синуклеином, используемым в качестве позитивного контроля. На фиг. 7F проиллюстрировано сравнение связывания антитела 38E2/7 и антитела α-Αβ, используемого в качестве позитивного контроля, в коре головного мозга у пациента с болезнью Альцгеймера.
На фиг. 8A и 8B проиллюстрирована иммунопреципитация экстрактов человеческого головного мозга под действием селективного к протофибриллам моноклонального антитела 38E2/7 в соответствии с протоколом получения экстрактов головного мозга, описанным в примере 9.
На фиг. 9A и 9B представлены результаты флуоресценции, полученные на микроскопе Axiovert200, снабженном ФИТЦ-эпитопфлуоресцентным фильтром, как описано в примере 10. На фиг. 9A показаны обработанные клетки, а на фиг. 9B представлены данные, вычисленные как относительный % снижения интенсивности флуоресценции по сравнению с интенсивностью флуоресценции, полученной с использованием не обработанных антителом клеток, сверхэкспрессирующих альфа-синуклеин, которая принималась за 100%.
Представленный графический материал будет более полно проиллюстрирован представленными ниже примерами.
Подробное описание изобретения
В первом своем варианте, настоящее изобретение относится к антителам и к их фрагментам с улучшенными свойствами, обладающим высокой аффинностью по отношению к человеческим α-синуклеиновым протофибриллам и низкой способностью к связыванию с α-синуклеиновыми мономерами. В конкретном варианте изобретения, такими антителами являются антитела класса IgG или их мутанты. В настоящем описании, термин «высокая аффинность по отношению к человеческим α-синуклеиновым протофибриллам» означает, что антитела или их фрагменты имеют константы диссоциации Kd менее чем 10-7 М для человеческих α-синуклеиновых протофибрилл. Как известно специалистам, протофибриллами являются растворимые олигомеры α-синуклеина. Типичные протофибриллы имеют молекулярную массу в пределах от примерно 1000 до примерно 5000 кДа, как было определено с помощью эксклюзионной хроматографии на глобулярных белках, используемых в качестве эталона, однако, настоящее изобретение не ограничивается этими типичными протофибриллами. Кроме того, в настоящем описании, термин «низкий уровень связывания α-синуклеиновых мономеров» означает, что связывание антитела или его фрагмента согласно изобретению с α-синуклеиновыми мономерами по меньшей мере в 100 раз ниже уровня связывания с α-синуклеиновыми протофибриллами. В конкретном варианте изобретения, такую аффинность связывания измеряют с помощью конкурентного ELISA-анализа, например, описанного в примере 4.
Настоящее изобретение также относится к способам получения таких антител и их фрагментов и к их применению для предупреждения, замедления развития симптомов, лечения, мониторинга и/или диагностики нейродегенеративных расстройств, ассоциированных с α-синуклеиновой патологией, включая, но не ограничиваясь ими, болезнь Паркинсона (БП), деменцию, ассоциированную с образованием телец Леви (ДТЛ), вариант болезни Альцгеймера, ассоциированной с образованием телец Леви, атрофию многих органов, психоз, шизофрению и болезнь Крейцфельда-Якоба. При α-синуклеинопатиях, агрегированный α-синуклеин, такой как тельца Леви и нейриты Леви аккумулируются в головном мозге, а в некоторых случаях, также и в других органах.
Примерами антител согласно изобретению являются антитела, которые были получены классическими гибридомными методами. Антитела могут быть поликлональными или моноклональными. В конкретном варианте изобретения, антитела являются моноклональными. Хотя в настоящем описании рассматривается много антител и их фрагментов, однако, для удобства, термин «антитело», используемый в настоящем описании, включает их фрагменты, которые, как подразумевается, являются активными фрагментами, то есть, фрагментами, обладающими такими же свойствами, которые были указаны в определении антитела согласно изобретению, а именно, высокой аффинностью по отношению к α-синуклеиновым олигомерам/протофибриллам и низкой способностью к связыванию с α-синуклеиновыми мономерами. Антитела и их фрагменты обладают высокой эффективностью в отношении клиренса патогенных форм α-синуклеина.
Заявленные антитела связываются с агрегированными формами, в частности, с протофибриллами, содержащими α-синуклеин, который является немодифицированным или конъюгированным, например, конъюгированным с 4-гидрокси-2-ноненалом (HNE) или 4-оксо-2-ноненалом (ONE), или с другими α,β-ненасыщенными гидроксиалкеналами или с полиненасыщенными жирными кислотами, которые стабилизируют эпитоп патогенных протофибрилл/олигомер-ного α-синуклеина. Указанный эпитоп или указанные эпитопы присутствуют на конформационно измененном или модифицированном α-синуклеине, то есть, на α-синуклеиновых протофибриллах и олигомерах, которые присутствуют в человеческом головном мозге пациентов с α-синуклеинопатиями, такими как, но не ограничивающимися ими, болезнь Паркинсона, ДТЛ и т.п. Заявленные антитела также связываются с патогенными протофибриллами/олигомерными структурами, образованными α-синуклеиновыми мутантами, например, A30P и A53T (Kruger et al., 1998) (Polymeropoulos et ai, 1997), которые, как было описано, приводят к развитию наследственной БП. Другими примерами таких мишеней для антител согласно изобретению являются протофибриллы, образованные мутантным α-синуклеином E46K, вызывающим БП или ДТЛ.
В одном из своих конкретных вариантов, настоящее изобретение относится к моноклональным антителам, используемым для дифференциации, диагностики, идентификации риска развития и/или для лечения расстройств, ассоциированных с α-синуклеиновой патологией, включая, но не ограничиваясь ими, например, болезнь Паркинсона, деменцию, ассоциированную с образованием телец Леви, вариант болезни Альцгеймера, ассоциированной с образованием телец Леви, болезнь Альцгеймера, синдром Дауна, атрофию многих органов, психоз, шизофрению, болезнь Крейцфельда-Якоба и другие нейродегенеративные расстройства.
Антитела и их фрагменты согласно изобретению содержат определенные аминокислотные последовательности областей CDR1-3 в вариабельной области легкой цепи (VL) и тяжелой цепи (VH) антител, обладающих высокой аффинностью по отношению к растворимым α-синуклеиновым протофибриллам, содержащим «эпитоп, специфичный для заболеваний БП и/или ДТЛ». В конкретных вариантех изобретения, области CDR объединяют с модифицированной Fc-областью в целях модуляции эффекторных функций, таких как, но не ограничивающихся ими, связывание с Fc-рецептором, связывание с фактором комплемента C1q, время полужизни, активация комплемента и воспалительные процессы. Константная область антитела имеет множество важных функций, таких как способность связываться с Fc-рецепторами и с фактором комплемента C1q. Во избежание воспалительных реакций, последняя функция может быть инактивирована.
Применение заявленных антител и их фрагментов, обладающих высокой аффинностью по отношению к α-синуклеиновым протофибриллам и низкой способностью к связыванию с α-синуклеиновыми мономерами, по сравнению с другими известными способами иммунотерапии, имеет нижеследующие явные преимущества:
1) Заявленные антитела и их фрагменты направлены на α-синуклеиновые протофибриллы, вызывающие заболевание, и инактивируют их, или по меньшей мере снижают уровень таких протофибрилл, например, посредством ингибирования олигомеризации (см. пример 10) или в соответствии с другими механизмамами.
2) Высокая аффинность по отношению к α-синуклеиновым протофибриллам, которой обладают заявленные антитела и их фрагменты, позволяют снижать клиническую дозу, необходимую для эффективного лечения.
3) Применение заявленных антител и их фрагментов, по сравнению со стратегией активной иммунизации, такой как вакцинация, позволяет разработать способ точного введения дозы пожилым пациентам.
4) Благодаря низкому уровню связывания с α-синуклеиновыми мономерами в периферических органах/в крови большее число антител/фрагментов становится доступным для связывания и элиминации α-синуклеиновых олигомерных форм в головном мозге.
5) Благодаря низкому уровню связывания или отсутствию связывания с фактором комплемента C1q, антитела и их фрагменты снижают риск возникновения воспалительных побочных эффектов, например, менингоэнцефалита.
В одном из своих аспектов, настоящее изобретение основано на обнаружении аминокислотных последовательностей CDR-областей антитела, которые играют важную роль в связывании с человеческими α-синуклеиновыми протофибриллами дикого типа и с мутантными α-синуклеиновыми протофибриллами. Антитела согласно изобретению, имеющие сайты связывания (CDR-области), характеризуются высокой аффинностью по отношению к человеческим α-синуклеиновым олигомерам/протофибриллам дикого типа и могут быть использованы в терапии или диагностике.
Молекула базовой структуры иммуноглобулина (IgG) содержит две идентичных легких цепи и две идентичных тяжелых цепи, связанные вместе дисульфидными мостиками. Легкая цепь, которая представляет собой либо лямбда-, либо каппа-цепь, имеет вариабельную область (VL) и константную область (CL), состоящие приблизительно из 110 аминокислотных остатков каждая. Тяжелая цепь имеет вариабельную область (VH), состоящую приблизительно из 110 аминокислотных остатков, но более крупную константную область (CH), состоящую из 300-400 аминокислотных остатков, содержащую области или домены CHγ1, CHγ2 и СНγ3.
Константная область (Fc) активирует систему комплемента и связывается с Fc-рецепторами на макрофагах, микроглиальных клетках и нейтрофилах, что приводит к поглощению и инактивации инфекционных микроорганизмов или чужеродных антигенов/не-аутоантигенов. Эта функция имеет важное значение, поскольку она является частью терапевтического механизма действия антитела, то есть, фагоцитоза микроглиальных клеток, опосредуемого Fc-рецептором, и клиренса α-синуклеиновых протофибрилл. Клиренс α-синуклеиновых олигомерных промежуточных соединений по пути деградации лизосом описан в литературе (Lee et al, 2004). Этот процесс включает зависимый или не зависимый от рецептора эндоцитоз комплексов антитело/протофибриллы, с последующим слиянием лизосом, где происходит деградация α-синуклеиновых протофибрилл (Masliah et al., 2005). Рецепторами, которые, предположительно, регулируют этот процесс, являются рецептор Thy 1.1 и белок, родственный рецептору липопротеина (LPR).
Вероятно также действуют и другие механизмы клиренса антитела против α-синуклеина. Клиренс растворимых α-синуклеиновых протофибрилл представляет собой основной механизм, применяемый для лечения согласно изобретению. α-Синуклеиновые протофибриллы рассматриваются как протофибриллы, которые являются в высокой степени нейротоксичными, и которые инициируют и запускают процесс развития заболевания. Клиренс α-синуклеиновых протофибрилл в головном мозге имеет важное клиническое значение. Помимо клиренса α-синуклеиновых протофибрилл может быть снижен уровень и других α-синуклеиновых агрегированных форм, включая α-синуклеиновые фибриллы, посредством удаления форм-предшественников α-синуклеиновых фибрилл, таких как α-синуклеиновые протофибриллы, димеры, тримеры, тетрамеры и более крупные олигомерные формы. Другие α-синуклеиновые формы, включая протофибриллы и фибриллы, находятся в равновесии друг с другом. Лечение с применением высокоаффинного антитела, связывающегося с протофибриллами, и клиренса α-синуклеиновых протофибрилл под действием указанного антитела также имеет преимущество с точки зрения опосредуемого снижения уровня других агрегированных или олигомерных α-синуклеиновых форм. Другой механизм действия антител заключается в блокировании или ингибировании α-синуклеиновой токсичности посредством их связывания с токсичными молекулами α-синуклеина и предупреждения взаимодействия этих молекул с нейронами.
Соответствующие вариабельные области тяжелой и легкой цепей содержат три гипервариабельные области, называемые гипервариабельными областями или CDR (комплементарность-определяющими областями). CDR-области представляют собой короткие фрагменты, состоящие примерно из 7-23, например, 13-23 аминокислот и локализованные в областях VL и VH. Шесть областей CDR на одной «ветви» антитела образуют «карман», который связывается с антигеном. В литературе имеется несколько определений последовательностей CDR. SEQ ID NO: 1-21 представляют собой заявленные последовательности CDR, определенные с использованием первой системы идентификации, и идентифицированные таким образом последовательности CDR в VL- и VH-областях моноклональных антител, специфичных к человеческим α-синуклеиновым протофибриллам дикого типа и к их мутантам, указаны в таблице 1 (см. пример 2), где эти области подчеркнуты. SEQ ID NO: 22-55 представляют собой заявленные последовательности CDR, определенные с использованием известной системы Кэбата, и идентифицированные таким образом последовательности CDR в VL- и VH-областях моноклональных антител, специфичных к человеческим α-синуклеиновым протофибриллам дикого типа и к их мутантам, указаны в таблице 2 (см. пример 2), где эти области подчеркнуты. В настоящем описании используется идентификация заявленных последовательностей CDR в соответствии с системой Кэбата (SEQ ID NO: 22-55).
Таким образом, в одном из вариантов изобретения, антитело согласно изобретению характеризуется присутствием шести последовательностей CDR (VH-CDR-1, VH-CDR-2, VH-CDR-3, VL-CDR-1, VL-CDR-2 и VL-CDR-3), каждая из которых выбрана из нижеследующих соответствующих групп последовательностей CDR в любой комбинации.
Одно из антител, которое было первоначально выбрано по определенным представляющим интерес свойствам, впоследствии было исключено как не удовлетворяющее критериям определения антитела согласно изобретению. Важным критерием такого исключения является сравнительно короткая последовательность CDR-3 VH этого антитела, состоящая из пяти аминокислот. Поэтому был сделан вывод, что последовательность CDR-3 VH должна иметь более чем 5 аминокислот. В конкретных вариантах изобретения, последовательность CDR-3 VH имеет 9, 10, 11 или 12 аминокислот.
В конкретных вариантах изобретения, антитела и фрагменты согласно изобретению имеют шесть последовательностей CDR, выбранных из нижеследующих комбинаций:
SEQ ID NO: 22, 28, 35, 41, 47 и 50,
SEQ ID NO: 23, 29, 36, 42, 47 и 50,
SEQ ID NO: 24, 30, 37, 43, 48 и 51,
SEQ ID NO: 25, 31, 38, 44, 47 и 52,
SEQ ID NO: 26, 32, 39, 45, 47 и 53,
SEQ ID NO: 23, 33, 37, 43, 48 и 54, и
SEQ ID NO: 27, 34, 40, 46, 49 и 55.
В других конкретных вариантах изобретения, антитела, обладающие желательной специфичностью к α-синуклеиновым протофибриллам и удовлетворяющие другим важным указанным здесь критериям, имеют шесть последовательностей CDR антитела или его фрагмента, выбранных из нижеследующих соответствующих групп:
или выбранных из нижеследующих соответствующих групп:
или выбранных из нижеследующих соответствующих групп:
или выбранных из нижеследующих соответствующих групп:
Как указывалось ранее, антитела и их фрагменты согласно изобретению, связывающиеся с α-синуклеиновыми протофибриллами, характеризуются высокой аффинностью по отношению к мишени. Высокая аффинность, выражаемая как константа диссоциации Kd, составляет менее чем 10-7 М. В других вариантах изобретения, константа диссоциации Kd для человеческих α-синуклеиновых протофибрилл составляет менее чем 10-8 М, менее чем 10-9 М, менее чем 10-10 М или даже менее чем 10-11 М. Эти антитела и их фрагменты имеют преимущество, заключающееся в том, что они могут быть введены в более низких дозах, чем антитела с аффинностью примерно 10-6 М или выше. Такое свойство имеет особую клиническую ценность, поскольку высокоаффинные антитела, которые могут быть введены путем инъекции, могут быть введены подкожно, так как в этом случае для достижения эффективности требуется лишь небольшое количество антитела. Способы введения не ограничиваются подкожными или внутривенными инъекциями. Кроме того, более низкие дозы, необходимые для достижения нужной эффективности, позволяют снизить затраты на получение антител.
Помимо высокой аффинности антител по отношению к α-синуклеиновым протофибриллам, такие антитела и их фрагменты имеют низкий уровень связывания с α-синуклеиновыми мономерами и, необязательно, низкий уровень связывания с α-синуклеиновыми фибриллами. Как указывалось выше, термин «низкий уровень связывания с α-синуклеиновыми мономерами» означает, что связывание антитела или его фрагмента согласно изобретению с α-синуклеиновыми мономерами по меньшей мере в 100 раз ниже уровня связывания с α-синуклеиновыми протофибриллами. В более конкретных вариантах изобретения, уровень связывания антитела или его фрагмента согласно изобретению с α-синуклеиновыми протофибриллами более чем в 500 раз или даже более чем в 1000 раз превышает уровень связывания с α-синуклеиновыми мономерами.
В другом варианте изобретения, антитела и их фрагменты обладают низким уровнем связывания с α-синуклеиновыми фибриллами. В более конкретных вариантах изобретения, уровень связывания антитела или его фрагмента согласно изобретению с α-синуклеиновыми протофибриллами более чем в 100 раз, более чем в 500 раз или даже более чем в 1000 раз превышает уровень связывания, чем связывание с α-синуклеиновыми фибриллами.
В другом варианте изобретения, антитела и их фрагменты обладают низким уровнем связывания с бета-амилоидными (Αβ) протофибриллами (например, с Kd>10-5 М) и с бета-амилоидными мономерами (например, с Kd>10-5 М).
В другом варианте изобретения, антитела и их фрагменты обладают низким уровнем связывания с β-синуклеиновым мономером, γ-синуклеиновым мономером, IAPP (амилоидным полипептидом островков Лангерганса) и/или с полипептидом, ассоциированным с болезнью Медина, например, уровень связывания указанных антител и их фрагментов с одним или несколькими из этих пептидов/белков по меньшей мере в 100 раз ниже уровня связывания с человеческими α-синуклеиновыми протофибриллами.
В соответствии с другим вариантом изобретения, антитело или его фрагмент согласно изобретению могут быть идентифицированы по их связыванию в системе-модели с линейным эпитопом, присутствующим в аминокислотной последовательности α-синуклеина в области аминокислот (а.к.) 113-140, например, в областях аминокислот 113-131, 125-131, 121-124, 121-127, 121-131, 113-123 и 136-140, представленных в качестве примеров специфических эпитопов. В этой системе-модели используются 15-мерные пептиды α-синуклеина с перекрыванием последовательностей в 11 аминокислот (см. ниже пример 3).
В соответствии с другим своим вариантом, настоящее изобретение относится к антителу или к его фрагменту, обладающим высокой аффинностью по отношению к человеческим α-синуклеиновым протофибриллам и низкой способностью к связыванию с α-синуклеиновыми мономерами и содержащим комбинацию одной последовательности CDR, выбранной из группы, состоящей из шести последовательностей CDR SEQ ID NO: 22-27, 28-34, 35-40, 41-46, 47-49 и 50-52, и последовательностей, имеющих сходство более чем на 70, 80, 90, 95 или 98% с любой из указанных последовательностей в каждой соответствующей группе. Антитело или его фрагмент связываются с эпитопом в области аминокислот (а.к.) 113-140, например, в области а.к. 113-131, а в частности, с а.к. эпитопов 125-131, 121-124, 121-127, 121-131, 113-123 или 136-140 иммобилизованного линейного α-синуклеина в системе-модели, содержащей 15-мерные пептиды α-синуклеина с перекрыванием последовательностей в 11 аминокислот.
В соответствии с другим конкретным вариантом изобретения, высокоаффинные антитела, связывающиеся с α-синуклеиновыми протофибриллами, могут снижать или ингибировать агрегацию α-синуклеина и тем самым снижать уровни растворимых олигомерных α-синуклеиновых форм в головном мозге.
В соответствии с другим конкретным вариантом изобретения, высокоаффинные антитела, связывающиеся с α-синуклеиновыми протофибриллами, могут связываться с α-синуклеиновыми олигомерами/протофибриллами, расположенными за пределами ЦНС, и тем самым сдвигать равновесие указанных α-синуклеиновых форм в сторону гематоэнцефалического барьера, что может приводить к снижению уровней указанных α-синуклеиновых форм в ЦНС (дренирование).
В соответствии с другим конкретным вариантом изобретения, антитела принадлежат к классу IgG, который является подходящим для применения в терапии, поскольку такие антитела могут проходить через гематоэнцефалический барьер. Высокоаффинные антитела IgG, связывающиеся с α-синуклеиновыми протофибриллами, могут быть сконструированы так, чтобы они снижали уровень связывания фактора комплемента C1q с CH2-доменом IgG1, подавляли активацию комплемента и снижали риск воспаления. Такая модификация может быть осуществлена несколькими различными способами. Один из способов включает получение химерного антитела, в котором домен СНγ2 константной области IgG1 был делетирован и заменен соответствующим доменом от IgG4 или частью домена, сообщающей способность к связыванию с C1q. Хорошо известно, что IgG4 не связывается с C1q, а поэтому не активирует каскад реакций комплемента. Для достижения этой цели, константную область тяжелой цепи (CH) конструируют так, чтобы она была объединена с высокоаффинным доменом Fc-рецептора (СНγ3), присутствующим на IgG1 и с доменом IgG4 (СНγ2), который не связывается с фактором комплемента C1q. Это новое антитело, содержащее химерную константную область тяжелой цепи (IgG1:СНγ1, СНγ2:IgG4, СНγ3:IgG1), имеет ценные свойства, а именно, обладает способностью к эффективному клиренсу α-синуклеиновых протофибрилл посредством фагоцитоза, опосредуемого Fc-рецептором, и к снижению риска развития побочных эффектов, то есть, воспаления, такого как менингоэнцефалит.
Другим способом снижения риска воспаления является модификация олигосахаридной структуры антитела, что позволяет снижать уровень связывания с фактором комплемента C1q и активации комплемента. Было описано тридцать различных биантеннальных структур олигосахаридных комплексов, имеющих замену Asn-297 в человеческом IgG1. Отсутствие CH2-ассоциированных углеводов, очевидно, вызывает конформационные изменения в «шарнирной» области антитела, снижает эффективность взаимодействия с эффекторными молекулами и приводит к потере функции активации комплемента и связывания с C1q.
Модификация высокоаффинного человеческого антитела, связывающегося с α-синуклеиновыми протофибриллами посредством сайт-направленного мутагенеза путем замены Asn-297 любой другой аминокислотой, будет приводить к продуцированию антитела, сохраняющего способность связываться с Fc-рецептором и не связываться с C1q, и тем самым к снижению риска воспаления, в частности, в гематоэнцефалическом барьере. Альтернативой способу модификации путем гликозилирования антитела является экспрессия антитела в клетках, в которых был инактивирован фермент N-ацетилглюкозаминил-трансфераза I. Этот способ позволяет получить антитело с углеводной структурой, модифицированной в положении Asn-297. Такой структурой является, но не ограничивается ею, структура Man5GlcNAc2. Такая углеводная модификация будет снижать уровень связывания с фактором комплемента C1q и подавлять воспаление (Wright et al. 1998). Альтернативно, негликозилированные антитела, связывающиеся с протофибриллами, могут быть получены путем культивирования клеток, экспрессирующих антитела в присутствии туникамицина, который ингибирует гликозилирование. Эти антитела обладают измененной способностью активировать комплемент, а также модифицированной функцией связывания с Fc-рецептором (Leatherbarrow et al. 1985). Скрининг клонов, экспрессирующих антитела с низкой активацией комплемента и с высоким уровнем связывания с Fc-рецептором, позволяет получить связывающиеся с протофибриллами антитела, обеспечивающие высокий уровень Fc-опосредуемого клиренса α-синуклеиновых протофибрилл и имеющие низкую способность связывания с C1q.
В другом варианте изобретения, высокоаффинным человеческим антителом, связывающимся с α-синуклеиновыми протофибриллами, является антитело подкласса IgG, например, IgG1 или IgG4, в котором сайт связывания с фактором комплемента C1q, то есть, Pro331>Ser331 (Xu et al. 1994), был модифицирован так, чтобы он снижал или ингибировал связывание с фактором комплемента C1q. Такие антитела являются особенно подходящими для введения, то есть, для лечения, предупреждения или замедления развития нейродегенеративного расстройства с α-синуклеиновой патологией у индивидуума, страдающего указанным расстройством или имеющего риск развития указанного расстройства, такого как, например, но не ограничивающегося им, индивидуум, страдающий БП, или индивидуум с риском развития БП. Пролиновый остаток в положении 331 в человеческом IgG1 может быть также заменен треонином или глицином или любой другой полярной аминокислотой. Такая модификация может быть достигнута стандартными методами молекулярной биологии, такими как сайт-направленный мутагенез или делеции ДНК.
Другим аспектом настоящего изобретения является применение высокоаффинных человеческих антител, связывающихся с α-синуклеиновыми протофибриллами, в целях точного определения уровней протофибрилл в тканях человека или животного, например, в цереброспинальной жидкости (ЦСЖ), в крови, в моче, в слюне, или в ткани головного мозга, которые могут быть использованы в качестве диагностического инструмента или биомаркера нейродегенеративного расстройства с α-синуклеиновой патологией или для мониторинга такого расстройства. Такие расстройства, как болезнь Паркинсона (БП), деменция, ассоциированная с образованием телец Леви (ДТЛ), вариант болезни Альцгеймера, ассоциированной с образованием телец Леви, атрофия многих органов, психоз, шизофрения и болезнь Крейцфельда-Якоба являются репрезентативными только, если они представляют собой нейродегенеративные расстройства с α-синуклеиновой патологией. Так, например, уровни человеческих α-синуклеиновых протофибрилл в цереброспинальной жидкости (ЦСЖ) или в крови пациента с БП также отличаются от уровней этих протофибрилл у пожилых пациентов соответствующей контрольной группы, не страдающих болезнью Паркинсона или любой другой α-синуклеинопатией. Аналогичным образом, у индивидуума с развивающейся болезнью Паркинсона или любой другой α-синуклеинопатией наблюдаются другие уровни α-синуклеиновых протофибрилл в ЦСЖ или в крови, отличающиеся от уровней этих протофибрилл у контрольных индивидуумов. Следовательно, определение уровней α-синуклеиновых протофибрилл в ЦСЖ или в крови позволит поставить диагноз заболевания на ранней стадии его развития. Это может быть достигнуто с использованием новых высокоаффинных антител согласно изобретению, связывающихся с α-синуклеиновыми протофибриллами, а в конкретном варианте изобретения, это может быть достигнуто в комбинации с «сэндвич»-ELISA-анализом (см. пример 5), где уровень α-синуклеиновых протофибрилл, как было определено, составляет ниже 9 пМ. Влияние других α-синуклеиновых форм, в частности, α-синуклеиновых мономеров, и, необязательно, α-синуклеиновых фибрилл и фрагментов α-синуклеина в данном анализе ничтожно мало.
Примерами подходящих методов анализа α-синуклеиновых протофибрилл в этих тканях, а также в клеточных культурах, проводимого с использованием антитела против α-синуклеиновых протофибрилл, являются иммуноанализы, такие как ELISA, РИА, вестерн-блот-анализ или дот-блот-анализ. Эти методы могут оказаться подходящими для эффективного лечения, на что указывает снижение уровней протофибрилл в клинических испытаниях и/или в диагностическом тесте. Поскольку уровни α-синуклеиновых протофибрилл в ЦСЖ и в крови очень малы, то высокоаффинное антитело согласно изобретению, связывающееся с α-синуклеиновыми протофибриллами, является предпочтительным для проведения диагностического теста, например, на основе ELISA-метода, для определения низких уровней α-синуклеиновых протофибрилл.
С применением таких методов, антитело или его фрагмент согласно изобретению добавляют к биологическому образцу, содержащему или предположительно содержащему α-синуклеиновые протофибриллы, и детектируют присутствие комплекса, образующегося между α-синуклеиновыми протофибриллами и антителом или его фрагментом. Такой комплекс может быть детектирован качественно, то есть, определяют присутствие комплекса, или количественно, то есть, определяют концентрацию комплекса или пороговую концентрация этого комплекса, если это необходимо.
В других своих вариантах, настоящее изобретение относится к применению высокоаффинных и специфичных к протофибриллам антител и их фрагментов в методах визуализации для детектирования, определения локализации и количественной оценки α-синуклеиновых протофибрилл в тканях человека и животного. Антитело или его фрагмент могут быть помечены детектируемой меткой, например, радиоактивным лигандом, таким как, но не ограничивающимся ими, I131, C14, H3 или галлий68, и подвергнуты контактированию с образцом или введены в этот образец в целях детектирования. Такие методы являются подходящими в качестве инструмента для диагностики нейродегенеративных расстройств с α-синуклеиновой патологией, включая, но не ограничиваясь ими, болезнь Паркинсона, деменцию, ассоциированную с образованием телец Леви, и другие нейродегенеративные расстройства, ассоциированные с α-синуклеином. В конкретном варианте изобретения, такие методы могут быть проведены в целях мониторинга развития у индивидуума заболевания, ассоциированного с α-синуклеином, без введения или при введении лекарственных препаратов или при проведении другого возможного курса лечения.
Поэтому в одном из аспектов изобретения, антитела добавляют к биологическому образцу, содержащему или, предположительно, содержащему α-синуклеиновые протофибриллы, а затем измеряют концентрацию комплекса между указанными протофибриллами и указанным антителом в целях детектирования и/или количественной оценки протофибрилл в образце. В конкретных вариантах изобретения, методами детектирования являются иммуноанализ и анализ, проводимый методом лигирования «по соседству». Биологический образец может представлять собой in vitro образец, взятый у индивидуума, а также некоторый объем физиологической жидкости in vivo.
В другом своем аспекте, настоящее изобретение относится к получению молекул антитела, специально для применения в ветеринарии. Описанные диагностические методы также могут быть применены в ветеринарии.
В другом своем аспекте, настоящее изобретение относится к гуманизации указанных антител в целях предотвращения побочных эффектов, то есть, иммунных ответов у человека на антитела, используемые в качестве терапевтического иди диагностического средства. Такие методы гуманизации известны среднему специалисту в данной области.
Фармацевтические композиции согласно изобретению содержат антитело или его фрагмент, описанные в настоящей заявке, и фармацевтически приемлемый носитель. В конкретном варианте изобретения, относящемся к применению в терапии, указанными композициями являются физиологически приемлемые препараты, содержащие терапевтически активное количество антитела или его фрагмента согласно изобретению в физиологическом буфере, таком как, например, но не ограничивающимся им, PBS, подходящий для введения человеку и/или животным. Антитело или его фрагмент могут быть лиофилизованы для повышения стабильности. Лиофилизованнный препарат может содержать любые подходящие стандартные наполнители, включая стабилизаторы, лиозащитные средства, буферы и т.п., такие как, но не ограничивающиеся ими, маннит, используемый для защиты и/или стабилизации продукта во время и/или после лиофилизации и/или последующего хранения.
Препарат антитела может содержать, но необязательно, антибактериальное средство или другой консервант или другую добавку, которые не оказывают негативного влияния на функцию или эффективность антитела или его фрагмента, связывающихся с протофибриллами.
ПРИМЕРЫ
Нижеследующие примеры приводятся лишь в целях иллюстрации, и не должны рассматриваться как ограничение объема настоящего изобретения.
Пример 1
Антитела против α-синуклеиновых протофибриллов
Иммунизация/Поликлональные антитела
В схеме иммунизации были использованы мыши Balb/C. В качестве антигена были использованы HNE-стабилизированные α-синуклеиновые протофибриллы. Они были получены как описано ранее (в заявке WO 2009/133521, которая вводится в настоящее описание посредством ссылки), за исключением того, что в данном случае отношение между HNE и α-синуклеином составляло 60:1. Для иммунизации, мышам инъецировали (например, 3-6 раз) HNE-стабилизированные α-синуклеиновые протофибриллы и адъювант. Мышам инъецировали одну ударную дозу, содержащую HNE-модифицированные α-синуклеиновые протофибриллы, после чего мышей умерщвляли. Кровь иммунизованных мышей анализировали на реактивность с α-синуклеиновыми протофибриллами и с α-синуклеиновыми мономерами. Специфичность ответа с вырабатыванием поликлональных антител анализировали с помощью прямого ELISA-анализа. В типичном эксперименте, плоскодонный 96-луночный полистироловый микротитрационный планшет с высоким уровнем связывания покрывали мономерным α-синуклеином (немодифицированным или модифицированным HNE или другими альдегидами), протофибриллами/олигомерным α-синуклеином (немодифицированным или модифицированным HNE или другими альдегидами), или фибриллярным α-синуклеином, в конечной концентрации 400 нг/лунку. Лунки блокировали 2% BSA, промывали 0,05% твином-20/PBS, и в лунки, в качестве «первых» антител, добавляли супернатанты клеточной среды (неразведенные или разведенные 1:1 забуференным фосфатом физиологическим раствором), полученные от исследуемых поликлональных антител. В качестве «второго» антитела было использовано козье антитело против мышиных IgG/IgM, конъюгированное с щелочной фосфатазой (Pierce Biotechnology, Rockford, IL, USA) при разведении 1/1000. Иммунореактивность визуализировали с использованием п-нитрофенилфосфата (Sigma-Aldrich, MO, USA).
Антитела, которые специфически распознают α-синуклеиновые протофибриллы/олигомеры, были детектированы в сыворотке. Кроме того, могут быть обнаружены антитела, которые распознают α-синуклеиновые мономеры. В качестве негативного контроля использовали неиммунизованных мышей.
Гибридомы/моноклональные антитела
Мышиные B-клеточные гибридомы использовали для продуцирования моноклональных антител, связывающихся с α-синуклеиновыми протофибриллами. Клетки селезенки выделяли, измельчали в стерильном забуференном фосфатом физиологическом растворе (PBS) и центрифугировали при 1200×g в течение 10 минут для сбора обогащенного клетками осадка. Затем клетки промывали PBS и центрифугировали при 1200×g в течение 10 минут. Клеточный осадок ресуспендировали в минимальной поддерживающей среде Дульбекко (DMEM, Invitrogen, La Jolla, CA, USA), в которую добавляли 1% антибиотиков. Клетки селезенки смешивали в отношении 1:1 с клетками Sp2/0 (мышиной миеломной клеточной линией) в DMEM. Для облегчения слияния клеток, к клеточной смеси добавляли 1 мл полиэтиленгиликоля (Sigma-Aldrich, St. Louis, MO, USA) и реакцию прекращали добавлением DMEM. Клетки собирали, и осадок ресуспендировали в DMEM, в которую было добавлено 10% (об/об) фетальной бычьей сыворотки (Cambrex, Charles City, IA, USA), и которая также содержала 1% (об/об) пирувата натрия (Cambrex, Charles City, IA, USA), 1% (об/об) антибиотиков (Sigma-Aldrich, St. Louis, MO, USA), 1% (об/об) L-глютамина (Cambrex, Charles City, IA, USA), 5% (об/об) кондиционированной среды BM (Roche Diagnostics Scandinavia, Bromma, Sweden) и 2% (об/об) среды HAT, используемой в качестве добавки (Sigma-Aldrich, St. Louis, MO, USA). Клетки высевали на 96-луночные планшеты для культивирования клеток и оставляли на 2 недели для выращивания.
Супернатанты гибридомной клеточной культуры анализировали с помощью прямого ELISA-анализа. В типичном эксперименте, плоскодонный 96-луночный полистироловый микротитрационный планшет с высоким уровнем связывания покрывали мономерным α-синуклеином (немодифицированным или модифицированным HNE или другими альдегидами), олигомерным/протофибриллярным α-синуклеином (немодифицированным или модифицированным HNE или другими альдегидами) или фибриллярным α-синуклеином. Лунки блокировали 1% BSA, промывали PBS-твином- (0,05%), и супернатанты клеточной среды (неразведенные или разведенные 1:2 или 1:5 PBS-твином-20 (0,05%)), взятой от исследуемой гибридомы, добавляли в лунки в качестве «первых» антител. Козье антитело против мышиных Ig, конъюгированное с пероксидазой хрена (ПХ) (Southern Biotechnology, prod. No.1010-05), использовали в качестве «второго» антитела при разведении 1/5000. Иммунореактивность визуализировали с использованием водного субстрата TMB K-Blue (Neogen Corp. prod. No. 331177).
Пример 2
Аминокислотные последовательности вариабельных областей тяжелой цепи (VH) и легкой цепи (VL/V каппа) моноклональных антител, специфичных к α-синуклеиновым протофибриллам
Аминокислотные последовательности вариабельных областей тяжелой цепи (VH) и легкой цепи (VL), включая области CDR антител, определяли с помощью ОТ-ПЦР матричной мРНК с последующим секвенированием ДНК. Аминокислотные последовательности вариабельной области тяжелой цепи (VH) и вариабельной области легкой цепи (VL) выбранных антител представлены в таблице 1. Положения областей CDR 1-3 подчеркнуты. Аминокислотные последовательности областей CDR образуют структурную основу для связывания человеческих α-синуклеиновых протофибрилл дикого типа и мутантных α-синуклеиновых протофибрилл, составляющих «патогенный эпитоп» α-синуклеиновых протофибрилл.
Аминокислотные последовательности областей CDR 1-3 соответствующих цепей VL и VH антител согласно изобретению, специфичных к протофибриллам, представлены в таблице 1. В таблице 2 представлены последовательности CDR серии дополнительных антител согласно изобретению.
Комбинированные аминокислотные последовательности областей CDR1-3 цепей VH и VL образуют молекулярный «карман», который связывается с человеческими α-синуклеиновыми протофибриллами дикого типа с выокой аффинностью и специфичностью. Этот «карман» образует молекулярную основу «эпитопа БП/ДТЛ». Изменения длины аминокислотных последовательностей CDR наблюдались в обеих цепях VH и VL и соответствовали связыванию с человеческими α-синуклеиновыми протофибриллами. Более короткая область CDR образовывала более затрудненную трехмерную структуру связывающего кармана антитела, а более длинная область CDR была более гибкой.
Последовательности CDR, представленные в таблицах 1 и 2, являются вариантами настоящего изобретения, поскольку они представляют собой, но не ограничиваются ими, аминокислотные последовательности, присутствующие в «мышиных каркасных» областях цепей VH и VL, то есть, за пределами областей CDR, а также человеческие каркасные области VL и VH антител, специфичных к протофибриллам.
Другие аминокислотные замены в областях CDR, отличающиеся от замен, представленных в таблицах 1 и 2, соответствуют в высокой степени аффинному и специфичному связыванию с человеческими α-синуклеиновыми протофибриллами. Если в конкретном положении области CDR присутствует полярная аминокислота, то такая конкретная аминокислота может быть заменена другой полярной аминокислотой, которая обладает такой же или более высокой аффинностью и специфичностью связывания с α-синуклеиновыми протофибриллами. Аналогичным образом, если в определенном положении присутствует неполярная аминокислота или отрицательно или положительно заряженная аминокислота, то такая конкретная аминокислота может быть заменена аналогичной аминокислотой, выбранной из группы аминокислот с той же самой полярностью.
Поскольку конкретная аминокислота или конкретные аминокислоты могут быть заменены в любом положении областей CDR функциональными эквивалентами, которые, в основном, сообщают антителу, обладающему аффинностью к α-синуклеиновым протофибриллам, такую же функцию и структуру, то такие конструкции входят в объем настоящего изобретения. В соответствии с этим, в объем настоящего изобретения входят антитела и их фрагменты, которые более чем на 70, 80, 90, 95 или 98% аналогичны одной из ранее указанных последовательностей CDR VH и VL соответствующих групп, и которые сохраняют способность связываться с эпитопом, описанным в настоящей заявке.


Пример 3
Картирование эпитопа для моноклональных антител, специфичных к α-синуклеиновым протофибриллам
Картирование эпитопов для антител осуществляли путем иммуноблоттинга на мембране PepSpots. Синтетические пептиды, охватывающие всю последовательность (аминокислоты 1-140) человеческого α-синуклеина, специально синтезировали с применением пептидной технологии JPT (на средства Sigma Aldrich, UK) и иммобилизовали на мембране PepSpots. Было сконструировано 33 синтезированных 15-мерных пептида с перекрыванием последовательностей в 11 аминокислот. Эти пептиды были ковалентно связаны с целлюлозной мембраной Whatman 50 (Whatman, England) у С-конца и обычно имели ацетилированный N-конец, что обусловлено более высокой стабильностью к разложению. Незаряженный ацетилированный N-конец лучше представляет область нативного антигена, чем заряженная NH3+-группа. Результаты представлены в таблице 3.
Человеческий α-синуклеин (SEQ ID NO: 80)

Альтернативно, картирование эпитопов для антител может быть осуществлено методом иммуноблотинга на мембране PepSpots (Sigma Aldrich) следующим образом: Синтетические пептиды, охватывающие С-концевую последовательность человеческого α-синуклеина в положениях аминокислот от 100 до 140, специально синтезировали и иммобилизовали на мембране PepSpots (Sigma Aldrich). Было сконструировано 30 синтетических 10-мерных пептида с перекрыванием последовательностей в 9 аминокислот. Результаты представлены в таблице 4.
В соответствии с этим, длина и точные положения эпитопа зависят от способа их определения.
Пример 4
Характеризация высокоаффинных моноклональных антител, связывающихся с человеческими α-синуклеиновыми протофибриллами, с помощью конкурентного ELISA
В этом примере описано четыре антитела (mAb49/G, mAb38E2/7, mAb38F11/2_8 и mAb48B 11/8). Эти антитела обнаруживали высокую аффинность связывания с α-синуклеиновыми протофибриллами и низкую перекрестную реактивность (низкий уровень перекрестного связывания) с α-синуклеиновыми мономерами, как было определено с помощью конкурентного ELISA-анализа, описанного ниже. Вкратце, тестируемое антитело против α-синуклеина оставляли в растворе для взаимодействия с α-синуклеиновыми мономерами или протофибриллами, а затем смесь добавляли в микротитрационный планшет, предварительно покрытый α-синуклеиновыми протофибриллами. Если антитело связывается с антигеном в стадии предварительного инкубирования, то лишь немногие антитела будут связываться с иммобилизованным антигеном на микротитрационном планшете. Антитело, связанное с иммобилизованным антигеном, детектировали с использованием «второго» антитела, конъюгированного с щелочной фосфатазой (ЩФ). Конъюгат инкубировали с субстратом ЩФ (pNPP), в результате чего появлялась желтая окраска, которая может быть детектирована в микротитрационном планшет-ридере на 405 нм. В результате было определено, что низкая величина OD соответствует высокой аффинности антитела к антигену в растворе.
В частности, микротитрационный ELISA-планшет с высоким уровнем связывания покрывали α-синуклеиновыми протофибриллами в концентрации 1 мкг/мл при плотности 100 мкм/лунку, разведенными в 1 × PBS, а затем герметично заклеивали клеевым герметиком и инкубировали в течение ночи при +4°C. Затем раствор для покрытия отбрасывали, и остаточную способность планшета к связыванию блокировали добавлением 200 мкл/лунку PBS-твина 20 (0,05%). Герметично закрытый планшет инкубировали в течение 60 минут при комнатной температуре (К.T.) путем встряхивания при 900 об/мин.
Кроме того, пептидный раствор получали в 1 × PBS-твине 20 (0,05%) путем разведения α-синуклеиновых мономеров или протофибрилл до концентрации 140 нМ. 10-стадийное 3× разведение серий α-синуклеиновых мономеров и протофибрилл осуществляли в объеме 50 мкл в круглодонном микротитрационном планшете с низким уровнем связывания белка. К этому раствору добавляли 50 мкл тестируемого антитела, разведенного в PBS-твине 20 (0,05%) до концентрации 100 нг/мл и оставляли на 60 минут для взаимодействия при комнатной температуре со встряхиванием при 900 об/мин. Затем эти предварительно инкубированные образцы добавляли в промытый (3 раза) сенсибилизированный планшет с высоким уровнем связывания и оставляли на 15 минут при комнатной температуре для инкубирования без встряхивания. Затем ELISA-планшет промывали для удаления несвязанных антител. Связанные антитела детектировали с использованием 100 мкл ЩФ-конъюгированного антитела против мышиных IgG (Mabtech, Sweden 3310-4), разведенного 1/1000 в PBS-твине 20 (0,05%), и инкубировали в течение 60 минут при комнатной температуре со встряхиванием при 900 об/мин.
И наконец, ELISA-планшет промывали для удаления несвязанных антител, и в каждую лунку добавляли 100 мкл субстрата ЩФ. Во время инкубирования планшет хранили в темноте при комнатной температуре, в результате чего появлялась желтая окраска. Величины оптической плотности измеряли в непрерывном режиме на длине волны 405 нм через каждые 15-120 минут. Данные измерений использовали для определения IC50 только в том случае, если наблюдалась линейная зависимость времени от оптической плотности.
Величины IC50 вычисляли как концентрацию мономеров или протофибрилл, необходимую для гашения половины сигнала в ELISA-анализе. Концентрацию α-синуклеиновых мономеров или протофибрилл, используемых в этом методе, определяли с помощью УФ-ЭХ с использованием коммерчески доступного стандартного α-синуклеина в качестве эталона (cat. S-1001-1, rPeptide, USA, 0,5 мг, как было определено с использованием BCA). На фиг. 1 указана оптическая плотность на 450 нм для четырех специфичных к протофибриллам моноклональных антител, как было определено с помощью описанного конкурентного ELISA-анализа. Этот анализ осуществляли с использованием HNE-стабилизированных α-синуклеиновых протофибрилл.
Другие ELISA-эксперименты показали, что антитела-кандидаты обнаруживают одинаковую аффинность по отношению к человеческим α-синуклеиновым протофибриллам, стабилизированным HNE или ONE. Эти антитела также связывались с α-синуклеиновыми протофибриллами/агрегатами, состоящими из α-синуклеиновых мутантов A30P или A53T, стабилизированных HNE, как было продемонстрировано с помощью конкурентного ELISA-анализа.
В частности, на фиг. 2A и 2B показаны результаты специфичного к протофибриллам антитела mAb49/G, проанализированного с помощью конкурентного ELISA-анализа. Специфичное к протофибриллам моноклональное антитело mAb49/G связывается с высокой аффинностью с человеческими α-синуклеиновыми протофибриллами, стабилизированными HNE или ONE (фиг. 2A). Моноклональное антитело также связывается с высокой аффинностью с HNE-стабилизированными протофибриллами человеческих мутантных форм α-синуклеина, A30P и A53T (фиг. 2B). Агрегация α-синуклеиновых мономеров с ONE приводит к образованию двух различных популяций комплексов, как было определено с помощью эксклюзионной хроматографии. Эти два отличающихся пика были отдельно элюированы и помечены как большой пик, FP-ONE_large, и небольшой пик, FP-ONE_small.
Кроме того, на фиг. 3A-3C показаны результаты для дополнительных специфичных к протофибриллам антител 38E2/7, 38F11/2_8 и 48B11/8, проанализированных с помощью конкурентного ELISA. Специфичные к протофибриллам моноклональные антитела связываются с высокой аффинностью с человеческими α-синуклеиновыми протофибриллами дикого типа, стабилизированными HNE (PF-HNE) или ONE (PF-ONE). Моноклональные антитела также связываются с высокой аффинностью с HNE-стабилизированными протофибриллами человеческих мутантных форм альфа-синуклеина, A30P (A30P-HNE) и A53T (A30P-HNE).
Пример 5
Проведение «сэндвич»-ELISA-анализа, специфичного для α-синуклеиновых протофибрилл
Для определения уровней α-синуклеиновых протофибрилл в биологических образцах был разработан «сэндвич»-ELISA-анализ, проводимый с использованием mAb49/G в качестве антитела для захвата и детектирующего антитела. Этот анализ позволяет измерять α-синуклеиновые протофибриллы с пределом квантификации LOQ=9 пМ (см. фиг. 4B). Из-за неопределенности размера α-синуклеиновых протофибрилл, используемых для постронения стандартной кривой, концентрацию в пМ брали исходя из молекулярной массы одного α-синуклеинового мономера (14000 г/моль). Поскольку молекулярная масса протофибрилл, как показала эксклюзионная хроматография, составляла по меньшей мере 1000000 г/моль, то предел детектирования, вычисленный как молярная концентрация α-синуклеиновых протофибрилл, может составлять минимум 0,13 пМ.
α-Синуклеиновые протофибриллы, стабилизированные HNE, и мономерный α-синуклеин были использованы для подтверждения конформационной специфичности ELISA-анализа.
Для продуцирования сигнала в ELISA-анализе, проводимом с использованием двух идентичных антител, требовался по меньшей мере димер белка. Однако, большой избыток мономерного α-синуклеина, который обычно присутствует в биологических образцах, может негативно влиять на проведение анализа α-синуклеиновых протофибрилл в результате занятия сайтов связывания пленки из антител для захвата, и тем самым, ингибировать связывание протофибрилл. Эта проблема была исследована путем добавления возрастающего избытка α-синуклеинового мономера к фиксированной концентрации α-синуклеиновых протофибрилл (500 пМ, выраженных как мономерные звенья) и их ELISA-анализа с использованием mAb49/G. Как и ожидалось, 30000-кратный молярный избыток α-синуклеинового мономера (15 мкΜ) по сравнению с α-синуклеиновыми протофибриллами (500 пМ), не оказывал негативного воздействия на результаты измерений mAb49/G в «сэндвич»-ELISA-анализе, поскольку α-синуклеиновый мономер плохо связывается с антителом для захвата.
На фиг. 4A схематически проиллюстрирован ELISA-анализ на связывание, проводимый в формате «сэндвич»-ELISA» для количественной оценки α-синуклеиновых протофибрилл. На фиг. 4B представлена стандартная кривая, построенная по данным, полученным для HNE-стабилизированных α-синуклеиновых протофибрилл. Предел квантификации, достигаемый в режиме этого анализа, составляет LOQ=9 пМ.
Пример 6
Анализ экстрактов человеческого головного мозга пациента, страдающего заболеванием, и контрольного индивидуума, проводимый в формате «сэндвич»-ELISA, специфичного для α-синуклеиновых протофибрилл
Экстракцию головного мозга проводили с использованием различных детергентов в соответствии с протоколом, включающим получение трех различных экстрактов: TBS-экстракта (фиг. 5A, белый столбец), содержащего внеклеточные и цитозольные молекулы α-синуклеина; тритонового экстракта (фиг. 5A, заштрихованный полосами столбец), содержащего мембраносвязанные молекулы α-синуклеина; и ДСН-экстракта (Fig. 5B, черный столбец), содержащего растворимые в ДСН молекулы α-синуклеина. Экстракты головного мозга анализировали у пациента с диагностированной α-синуклеинопатической деменцией, ассоциированной с образованием телец Леви (ДТЛ). Затем анализировали ткань головного мозга, выделенную из коры головного мозга и черного вещества. В качестве контроля также анализировали ткань головного мозга, взятую из коры головного мозга индивидуума, у которого иммуногистохимический анализ не выявил патологию, ассоциированную с образованием телец Леви. «Сэндвич»-ELISA проводили с использованием антитела mAb49/G, специфичного к α-синуклеиновым протофибриллам, в качестве антитела для захвата и детектирующего антитела. На фиг. 5A и 5B представлены результаты анализов экстрактов человеческого головного мозга пациентов, страдающих заболеванием, и контрольных пациентов, проводимых с помощью «сэндвич»-ELISA-анализа, специфичного для α-синуклеиновых протофибрилл. Этот анализ позволяет проводить количественную оценку протофибрилл на уровне >9 пМ (предел квантификации; LOQ=9 пМ).
Пример 7
Измерение уровня α-синуклеиновых протофибрилл в экстракте головного мозга, взятого у трансгенных мышей с моделью БП
Было высказано предположение о присутствии α-синуклеиновых протофибрилл в клетке и у мышей с моделью соответствующего заболевания, хотя до настоящего времени не существовало метода проведения прямого анализа α-синуклеиновых протофибрилл в биологических образцах. Поэтому «сэндвич»-ELISA с использованием mAb49/G впервые дал возможность измерить уровни α-синуклеиновых протофибрилл в биологических образцах и у мышей с моделями α-синуклеинопатии, характеризующейся аккумуляцией агрегированного α-синуклеина.
Образцы экстракта головного мозга, взятые у трансгенных мышей, у которых сверхэкспрессируется человеческий мутантный α-синуклеин A53T, сравнивали с образцами, взятыми у мышей дикого типа. Головной мозг этих мышей гомогенизировали в TBS или TBS+твин и, перед проведением анализа, центрифугировали для выделения растворимой фракции α-синуклеина. Результаты измерений уровней α-синуклеиновых протофибрилл в растворимых в TBS фракциях гомогенатов головного мозга нетрансгенных мышей сравнивали с результатами уровней α-синуклеиновых протофибрилл у трансгенных мышей (модель Kahle) (фиг. 6). Для гарантии того, что весь α-синуклеин, оцениваемый в этом анализе, будет присутствовать в растворимой форме, перед проведением анализа, все образцы центрифугировали в течение 5 минут при 16000 × g. Уровни α-синуклеиновых протофибрилл измеряли в головном мозге 5-месячных трансгенных крыс с α-синуклеиновой патологией.
На фиг. 6 представлены результаты анализа экстрактов головного мозга, взятых у контрольных мышей (ntg, нетрансгенных) и у 5-месячных мышей, полученных от трансгенной (tg) мыши Khale с моделью БП, где на оси «y» отложена оптическая плотность OD450.
Пример 8
Иммуногистохимический (ИГХ) анализ ткани человеческого головного мозга
Для проведения иммуногистохимического (ИГХ) анализа использовали кору головного мозга и черное вещество, взятые у пациентов с БП и ДТЛ, как описано выше (Oinas et al. 2010). В качестве контроля использовали кору головного мозга и черное вещество, взятые у здоровых индивидуумов того же возраста. Антителом против α-синуклеина, используемым в качестве позитивного контроля, является мышиное mAb против α-синуклеина (BD 610787).
Связывание с Αβ-бляшками оценивали следующим образом: два предметных стекла с образцами двух соседних областей коры головного мозга пациента с БА обрабатывали для представления антигенов и инкубировали либо с анти-Αβ mAb (mAb158, BioArctic), используемым в качестве позитивного контроля, либо с каждым одним антителом из антител-кандидатов. Связанное антитело детектировали с помощью «второго» видоспецифического антитела, конъюгированного с пероксидазой хрена (ПХ). Затем конъюгат инкубировали с ПХ-субстратом DAB, образующим окрашенный осадок, который детектировали под оптическим микроскопом. Область, в которой Αβ-бляшки детектировали благодаря получению окрашенного осадка в анализе с позитивным контролем, анализировали в соответствующей области предметных стекол, обработанных антителом-кандидатом. Отсутствие окрашенного осадка оценивали визуально и интерпретировали как отсутствие связывания антител-кандидатов с Αβ-бляшками.
На фиг. 7A показано, что антитело 38E2/7 связывается с тельцами Леви и с нейритами в черном веществе пациентов с БП и с α-α-синуклеином, используемым в качестве позитивного контроля. На фиг. 7B показано, что антитело 38E2/7 связывается с тельцами Леви и с нейритами в коре головного мозга и в черном веществе пациентов с ДТЛ и с α-α-синуклеином, используемым в качестве позитивного контроля. На фиг. 7С показано, что различные антитела связываются с тельцами Леви и с нейритами в коре головного мозга и в черном веществе пациентов с ДТЛ и с негативным контролем. На фиг. 7D показано, что различные антитела связываются с тельцами Леви и с нейритами в черном веществе пациентов с БП и с негативным контролем. На фиг.7E показано, что антитело 38E2/7 не связывается в черном веществе нормальных индивидуумов и с α-α-синуклеином, используемым в качестве позитивного контроля. На фиг. 7F проиллюстрировано сравнение связывания антитела 38E2/7 и антитела против α-Αβ, используемого в качестве позитивного контроля, в коре головного мозга у пациента с болезнью Альцгеймера.
Пример 9
Анализ экстрактов человеческого головного мозга посредством иммунопреципитации (ИП) и вестерн-блот-анализа
Иммунопреципитацию экстрактов человеческого головного мозга, проводимую с использованием моноклонального антитела 38E2/7, связывающегося с протофибриллами, осуществляли с помощью вестерн-блот-анализа. Экстракцию головного мозга проводили с использованием различных детергентов в соответствии с протоколом, включающим получение четырех различных экстрактов: TBS-экстракта, содержащего внеклеточные и цитозольные молекулы α-синуклеина; тритонового экстракта, содержащего мембраносвязанные молекулы α-синуклеина; ДСН-экстракта, содержащего растворимые в ДСН молекулы α-синуклеина, и FA-экстракта, содержащего нерастворимый α-синуклеин. Эти экстракты подвергали иммунопреципитации на магнитных сферах, с которыми связывались антитело 38E2/7 или контрольное антитело 15P. Антитело 15P может связываться с α-синуклеиновыми протофибриллами и в равной степени с мономерами, в результате чего можно предположить, что оно будет снижать уровень присутствующих молекул всех видов. На фиг. 8A проиллюстрирован ДСН-экстракт черного вещества, взятого у пациента с ДТЛ, а на фиг. 8B проиллюстрирован тритоновый экстракт черного вещества, взятого у пациента с ДТЛ. Как показано на фиг. 8A и 8B, mAb 38E2/7 захватывает только α-синуклеиновые протофибриллы черного вещества пациента с ДТЛ, как в тритоновом экстракте, так и в ДСН-экстракте, тогда как mAb15 захватывает α-синуклеиновые мономеры во всех экстрактах.
Пример 10
Анализ на ингибирование олигомеризации α-синуклеина
В этом примере показано, что антитело mAb49/G ингибирует олигомеризацию α-синуклеиновых мономеров в методе in vitro, в котором нейронные клетки трансфецировали 2 векторами, каждый из которых содержит одну копию α-синуклеина (аминокислоты 1-140), присоединенного к N-концевому или C-концевому фрагменту GFP. Окраску, которую дает белок, флуоресцирующий в зеленом диапазоне спектра и которая может быть детектирована под флуоресцентным микроскопом, давали только те клетки, в которых α-синуклеин подвергался олигомеризации и образовывал фрагменты с GFP. Присутствие антитела, которое может ингибировать и/или предотвращать олигомеризацию, может быть оценено путем сравнения интенсивности флуоресценции этих культур с интенсивностью флуоресценции контрольных культур, в которые не было добавлено антитело.
В частности, клетки нейроглиомы H4 трансфецировали эквимолярными отношениями ДНК-конструкций, содержащих либо α-синуклеин (аминокислоты 1-140), связанный с N-концевым фрагментом белка, флуоресцирующего в зеленом диапазоне спектра (GFP) (аминокислоты 1-155), либо α-синуклеин (аминокислоты 1-140), связанный с С-концевым фрагментом GFP (аминокислоты 156-238), с использованием трансфецирующего реагента FuGENE 6 (Roche Diagnostics, Basel, Switzerland). Одновременно с этим, контрольное моноклональное антитело против α-синуклеина (mAb5C2, Santa Cruz Bio) и антитело mAb49/G экзогенно добавляли к клеткам в конечной концентрации 1 мкг/мл. Клетки инкубировали в течение 24 часов при 37°C в 5% СО2. Через 24 часа, клетки переносили в условия при 30°C для полного восстановления GFP-флуорофора и инкубировали еще 24 часа. Флуоресценцию измеряли на микроскопе Axiovert200, снабженном фильтром для ФИТЦ-эпифлуоресценции. Все данные вычисляли как относительный % интенсивности флуоресценции по отношению к интенсивности флуоресценции не обработанных антителом клеток, сверхэкспрессирующих α-синуклеин, которую принимали за 100%.
Как показано на фиг. 9A, обработка антителом mAb49/G давала значимое (*p<0,05) снижение (42%-ое снижение интенсивности флуоресценции по сравнению с интенсивностью флуоресценции необработанных клеток) степени олигомеризации α-синуклеина. На фиг. 9B представлены графики результатов, выраженных как процент интенсивности флуоресценции по отношению к интенсивности флуоресценции необработанных клеток, сверхэкспрессирующих α-синуклеин, которую принимали за 100%.
Конкретно описанные здесь примеры и варианты приводятся лишь в целях иллюстрации и не должны рассматриваться как ограничение объема изобретения, определенного в формуле изобретения. Дополнительные варианты, примеры и преимущества настоящего изобретения будут очевидны для среднего специалиста в данной области исходя из настоящего описания и входят в объем заявленного изобретения.
Библиография
Chartier-Harlin, MC, et al. 2004. Alpha-synuclein locus duplication as a cause of familial Parkinson's disease. Lancet 1, 364,1167-1169.
Conway, K., et al., 2000. Acceleration of oligomerization, not fibrillization, is a shared property of both a-synuclein mutations linked to early-onset Parkinson's disease: Implications for pathogenesis and therapy. Proc Natl Acad Sci USA 97, 571-576.
Crews, L., et al., 2009. Role of synucleins in Alzheimer's disease. Neurotox Res. 16, 306-317.
Desplats, P., et al., 2009. Inclusion formation and neuronal cell death through neuron-to-neuron transmission of alpha-synuclein. Proc Natl Acad Sci USA. 4, 106, 13010-13015. Erratum in: Proc Natl Acad Sci USA. 2009, 106, 17606. Comment in: Proc Natl Acad Sci USA. 2009, 106, 12571-12572.
El-Agnaf, O. M., et al., 2006. Detection of oligomeric forms of α-synuclein protein in human plasma as a potential biomarker for Parkinson's disease. Faseb J 20, 419-425.
George, J. L., et al. 2009. Targeting the progression of Parkinson's disease. Curr Neuropharmacol. 7, 9-36.
Hansen, L, et al., 1990. The Lewy body variant of Alzheimer's disease. A clinical and pathologic entity. Neurology 40, 1-8.
Klucken, J., et al., 2006. Clinical and biochemical correlates of insoluble α-synuclein in dementia with Lewy bodies. Acta Neuropathol (Berl) 111, 101-108.
Kruger, R., et al., 1998. Ala30Pro mutation in the gene encoding α-synuclein in Parkinson's disease. Nat Genet 18, 106-108.
Leatherbarrow, R.J., et al. 1985. Effector functions of a monoclonal aglycosylated mouse IgG2a: binding and activation of complement component C1 and interaction with human monocyte Fc receptor. Mol Immunol 22, 407-415.
Lee, H-J., et al. 2004. Clearance of a-synuclein oligomeric intermediates via the lysosomal degradation pathway. Journal of Neuroscience 24, 1888-1896.
Li, J.Y., et al Li et al. 2008. Lewy bodies in grafted neurons in subjects with Parkinson's disease suggest host-to-graft disease propagation Nature Med., 14, 501-503.
Masliah, E., et al. 2005. Effects of alpha-synuclein immunization in a mouse model of Parkinson's disease. Neuron. 46, 857-868.
Oinas, M., et al. 2010. alpha-Synuclein pathology in the spinal cord autonomic nuclei associates with alpha-synuclein pathology in the brain: a population-based Vantaa 85+ study. Acta Neuropathol. 119, 715-722.
Polymeropoulos, M.H., et al., 1997. Mutation in the oc-Synuclein Gene Identified inFamilies with Parkinson's Disease. Science 276, 2045-2047.
Qin, Z., et al., 2007. Effect of 4-hydroxy-2-nonenal modification on α-synuclein aggregation. J Biol Chem 282, 5862-5870.
Singleton, AB., et al., 2003. alpha-Synuclein locus triplication causes Parkinson's disease. Science 302:841.
Wrigth, A., 1998. Effect of C2-associated carbohydrate structure on Ig effector function: studies with chimeric mouse-human IgGl antibodies in glycosylation mutants of Chinese hamster ovary cells. J Immunol 160, 3393-3402.
Xu, Y., et al. 1994. Residue at position 331 in the IgG1 and IgG4 CH2 domains contributes to their differential ability to bind and activate complement. J Biol Chem. 269, 3469-3474.
Yoritaka, A., et al., 1996. Immunohistochemical detection of 4-hydroxynonenal protein adducts in Parkinson disease. Proc Natl Acad Sci USA 93, 2696-2701.
Zarranz, J., et al., 2004. The new mutation, E46K, of α-synuclein causes Parkinson and Lewy body dementia. Ann Neurol. 55, 164-173.
| название | год | авторы | номер документа |
|---|---|---|---|
| УЛУЧШЕННЫЕ СЕЛЕКТИВНЫЕ В ОТНОШЕНИИ ПРОТОФИБРИЛЛ АНТИТЕЛА И ИХ ПРИМЕНЕНИЕ | 2007 |
|
RU2429244C2 |
| Антитела, связывающиеся с протофибриллами α-синуклеина | 2021 |
|
RU2810587C1 |
| СРЕДСТВА, ПУТИ ПРИМЕНЕНИЯ И СПОСОБЫ ЛЕЧЕНИЯ СИНУКЛЕОПАТИИ | 2016 |
|
RU2765303C2 |
| УЛУЧШЕННЫЕ АНТИТЕЛА, СВЯЗЫВАЮЩИЕ Аβ-ПРОТОФИБРИЛЛЫ | 2015 |
|
RU2700104C2 |
| Моноклональные антитела к альфа-синуклеину для предотвращения агрегации тау-белка | 2017 |
|
RU2760334C2 |
| АНТИТЕЛА К АЛЬФА-СИНУКЛЕИНУ И ВАРИАНТЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2812765C2 |
| АНТИТЕЛА | 2018 |
|
RU2798399C2 |
| АНТИТЕЛА ПРОТИВ АЛЬФА-СИНУКЛЕИНА | 2018 |
|
RU2787039C2 |
| ГУМАНИЗИРОВАННЫЕ АНТИТЕЛА К β-АМИЛОИДНОМУ ПЕПТИДУ | 2008 |
|
RU2475500C2 |
| ГУМАНИЗИРОВАННЫЕ АНТИ-ТАУ-АНТИТЕЛА | 2015 |
|
RU2743152C2 |

























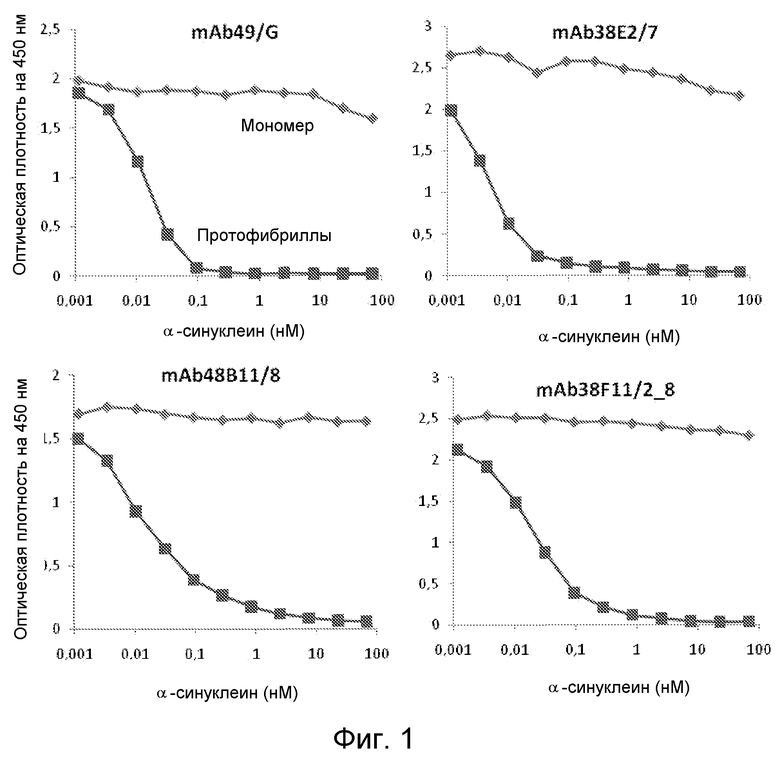
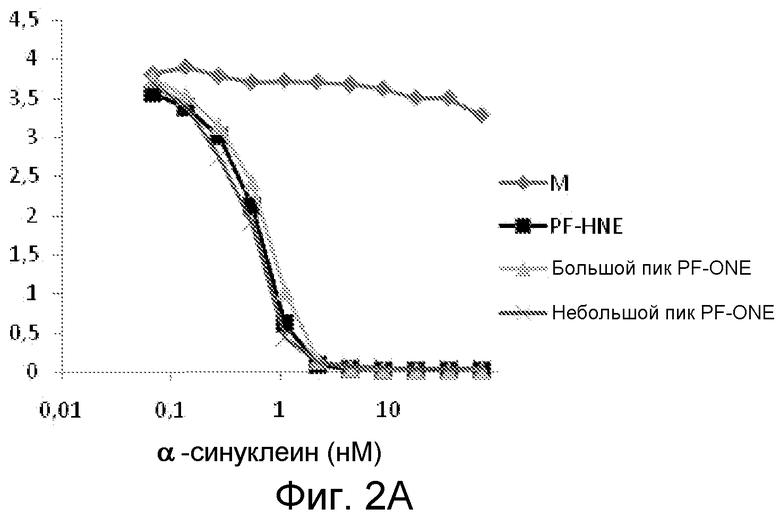
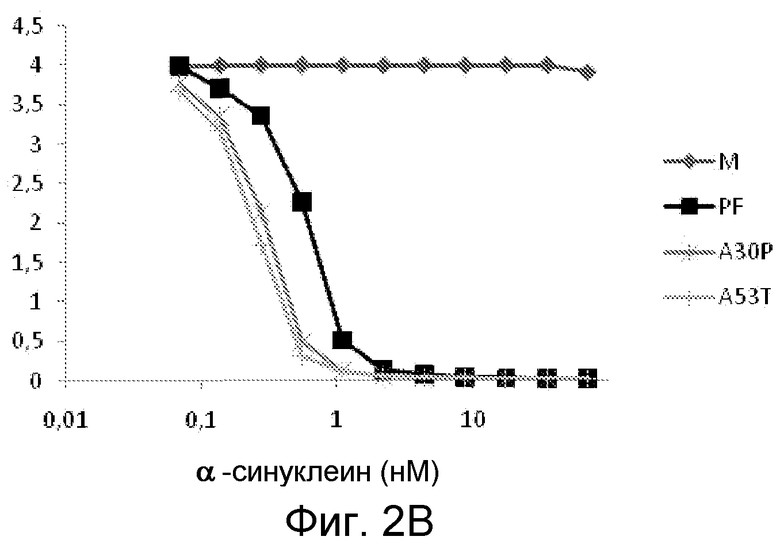
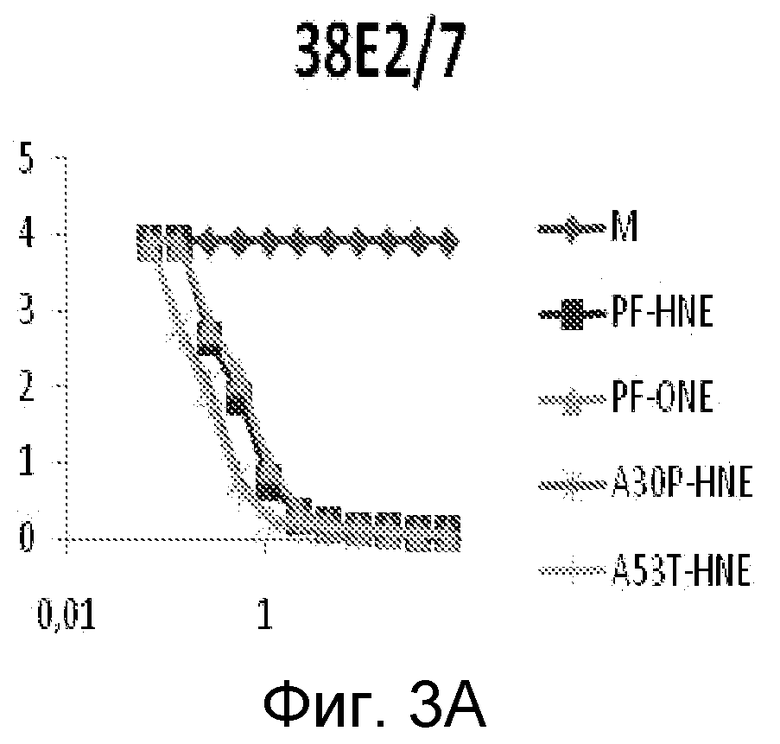
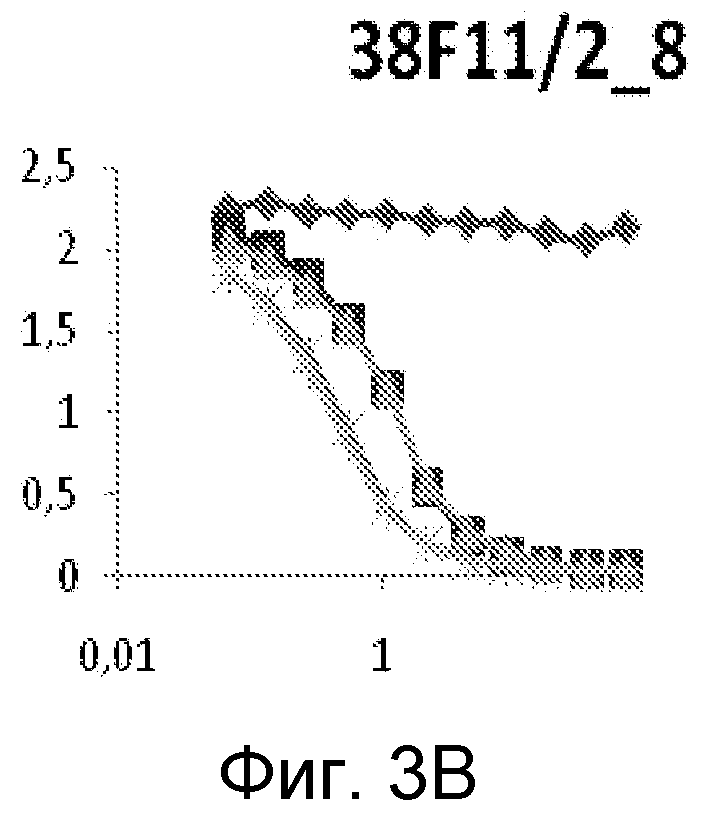
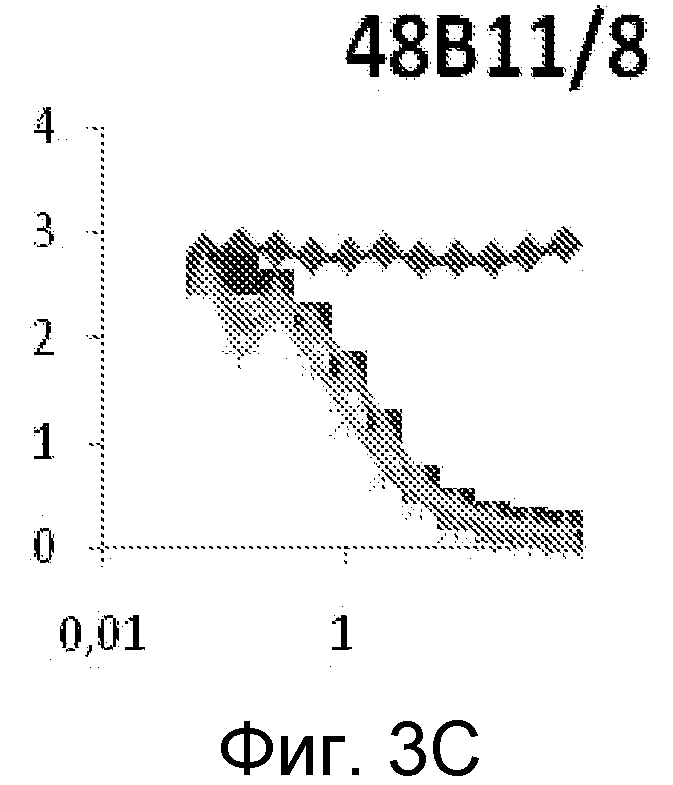
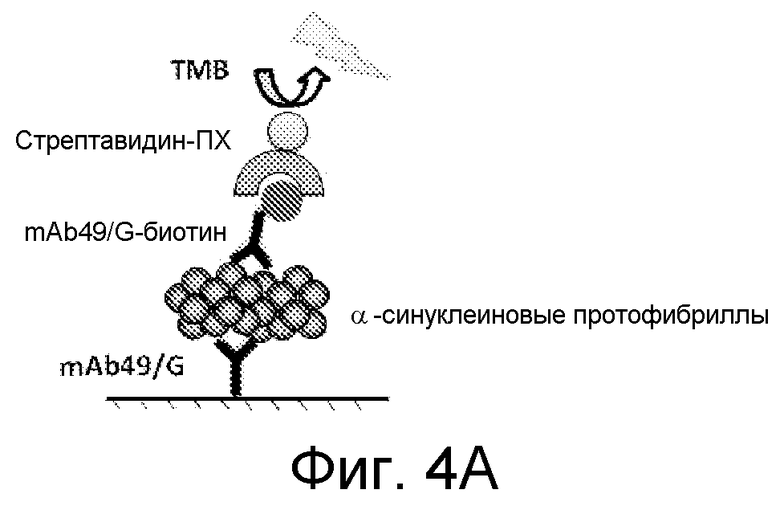

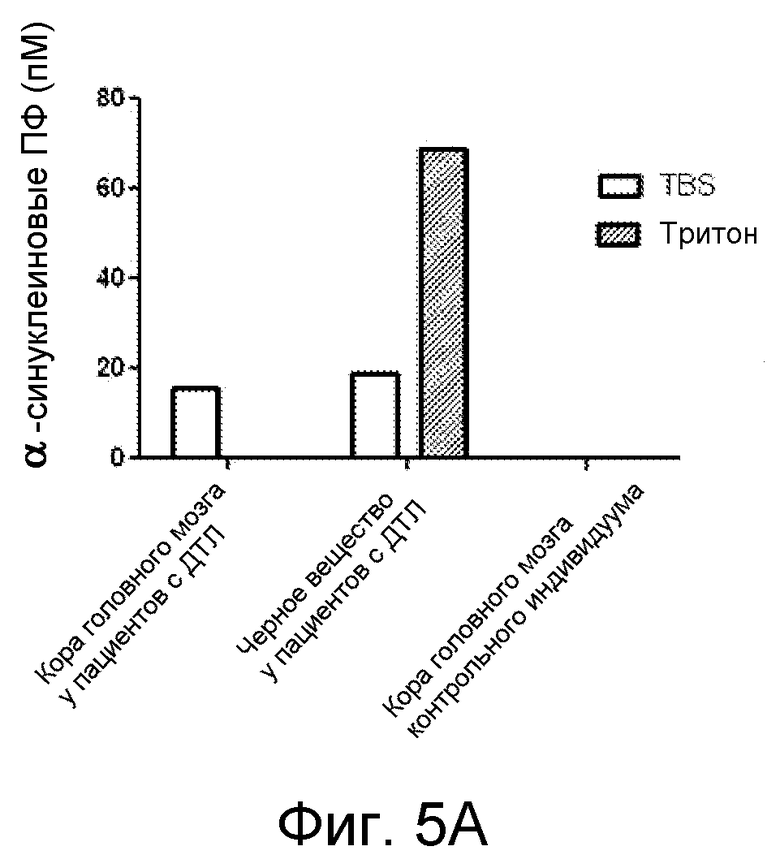
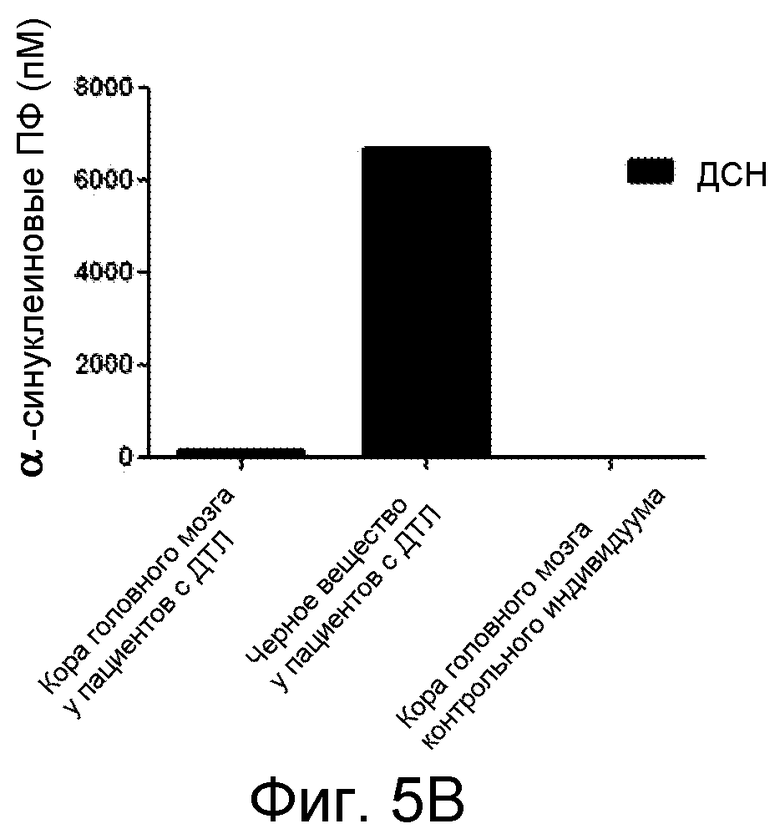
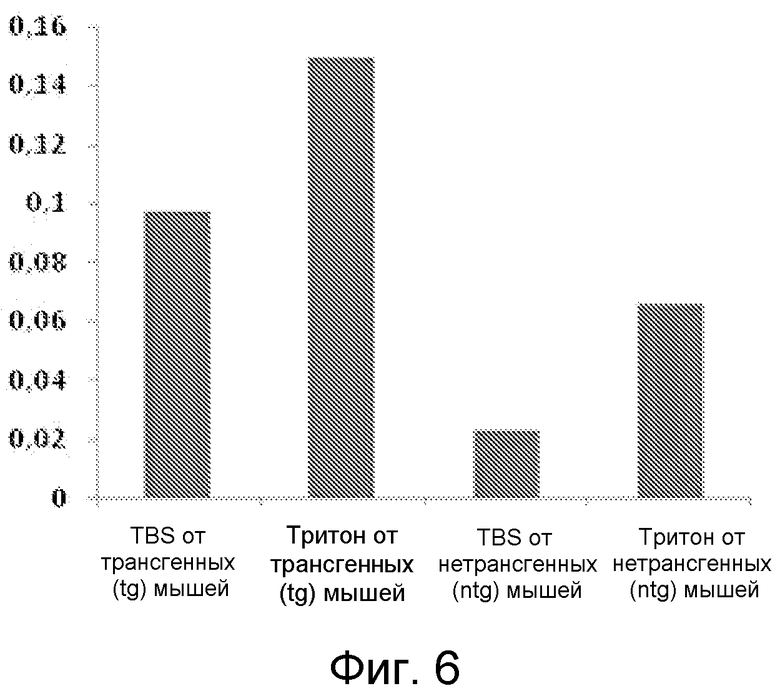
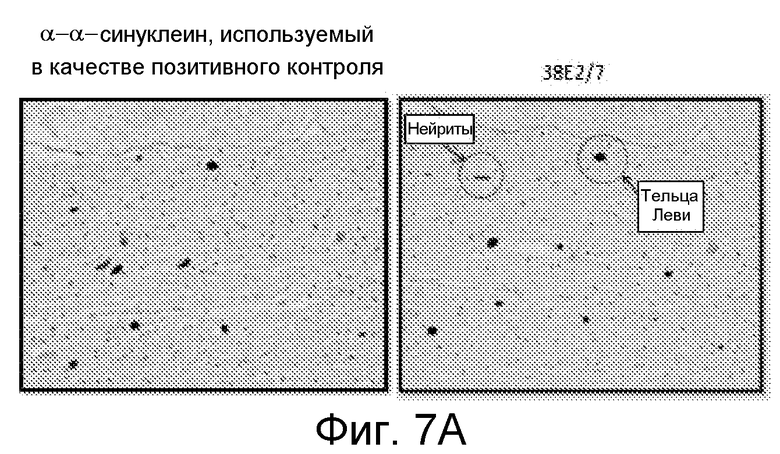
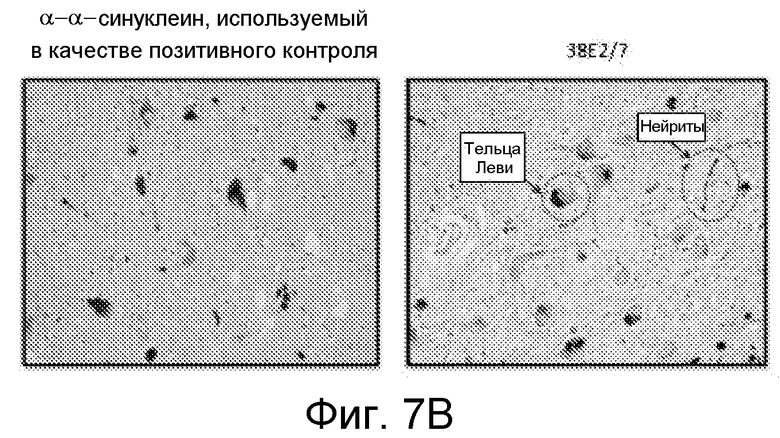



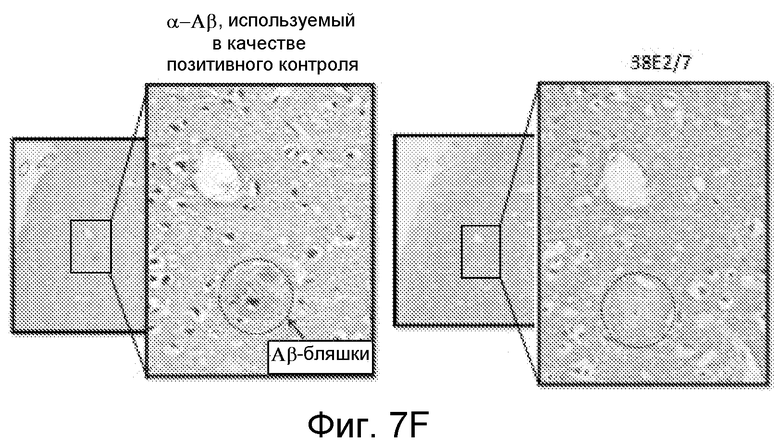



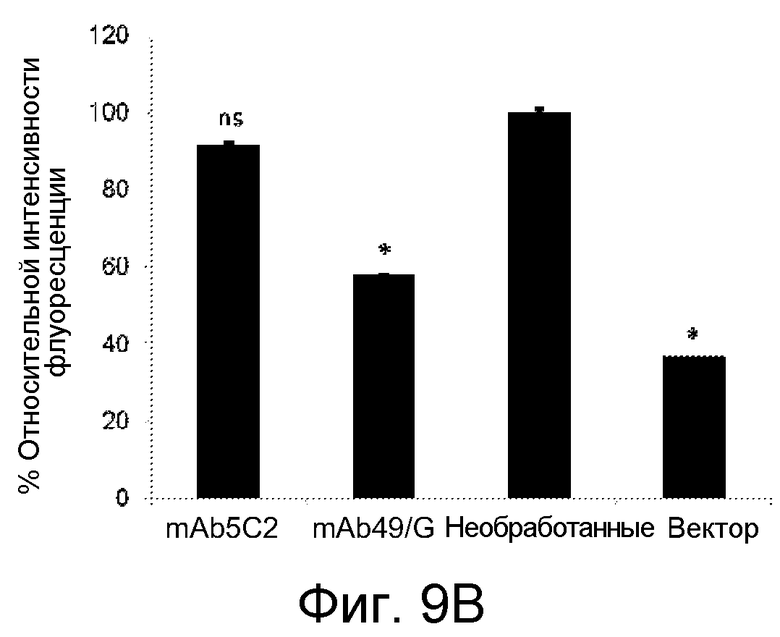
Изобретение относится к биохимии. Описаны антитела и их фрагменты, обладающие высокой аффинностью по отношению к человеческим α-синуклеиновым протофибриллам и низкой способностью к связыванию с α-синуклеиновыми мономерами. Раскрыты композиции, содержащие описанное антитело или его фрагмент, и способы детектирования α-синуклеиновых протофибрилл с использованием описанного антитела или его фрагмента. В других своих вариантах настоящее изобретение относится к способам предупреждения, замедления развития или лечения нейродегенеративного расстройства, ассоциированного с α-синуклеиновой патологией, где указанные способы включают введение описанного антитела или его фрагмента. Также относится к применению такого антитела или его фрагмента в целях получения фармацевтической композиции для лечения нейродегенеративного расстройства, ассоциированного с α-синуклеиновой патологией. Изобретение используется для диагностики или мониторинга развития нейродегенеративного расстройства, ассоциированного с α-синуклеиновой патологией, и в способах снижения или ингибирования агрегации α-синуклеина путем введения указанного антитела или его фрагмента. 7 н. и 24 з.п. ф-лы, 9 ил., 4 табл., 10 пр.
1. Антитело или его фрагмент, каждый из которых обладает высокой аффинностью по отношению к α-синуклеиновым протофибриллам человека и низкой способностью к связыванию с α-синуклеиновыми мономерами, причем указанное антитело или его фрагмент имеет комбинацию из трех последовательностей CDR вариабельной области тяжелой цепи (VH) и трех последовательностей CDR вариабельной области легкой цепи (VL), выбранных из следующих комбинаций:
SEQ ID NO: 22, 28, 35, 41, 47 и 50,
SEQ ID NO: 23, 29, 36, 42, 47 и 50,
SEQ ID NO: 24, 30, 37, 43, 48 и 51,
SEQ ID NO: 25, 31, 38, 44, 47 и 52,
SEQ ID NO: 26, 32, 39, 45, 47 и 53,
SEQ ID NO: 23, 33, 37, 43, 48 и 54 и
SEQ ID NO: 27, 34, 40, 46, 49 и 55.
2. Антитело или его фрагмент по п.1, где антитело или его фрагмент имеет комбинацию последовательностей CDR из SEQ ID NO: 22, 28, 35, 41, 47 и 50.
3. Антитело или его фрагмент по п.1, где антитело или его фрагмент имеет комбинацию последовательностей CDR из SEQ ID NO: 23, 29, 36, 42, 47 и 50.
4. Антитело или его фрагмент по п.1, где антитело или его фрагмент имеет комбинацию последовательностей CDR из SEQ ID NO: 24, 30, 37, 43, 48 и 51.
5. Антитело или его фрагмент по п.1, где антитело или его фрагмент имеет комбинацию последовательностей CDR из SEQ ID NO: 25, 31, 38, 44, 47 и 52.
6. Антитело или его фрагмент по п.1, где антитело или его фрагмент имеет комбинацию последовательностей CDR из SEQ ID NO: 26, 32, 39, 45, 47 и 53.
7. Антитело или его фрагмент по п.1, где антитело или его фрагмент имеет комбинацию последовательностей CDR из SEQ ID NO: 23, 33, 37, 43, 48 и 54.
8. Антитело или его фрагмент по п.1, где антитело или его фрагмент имеет комбинацию последовательностей CDR из SEQ ID NO: 27, 34, 40, 46, 49 и 55.
9. Антитело или его фрагмент по любому из пп.1-8, где антитело представляет собой моноклональное антитело.
10. Антитело или его фрагмент по любому из пп.1-8, где антитело или его фрагмент имеет низкую аффинность связывания с мономерами β-синуклеина.
11. Антитело или его фрагмент по любому из пп.1-8, где антитело или его фрагмент имеет низкую аффинность связывания с фибриллами α-синуклеина.
12. Фармацевтическая композиция для профилактики, замедления развития или лечения нейродегенеративного расстройства, связанного с α-синуклеиновой патологией у индивидуума, содержащая эффективное количество антитела или его фрагмента по любому из пп.1-9, и фармацевтически приемлемый носитель.
13. Фармацевтическая композиция по п.12, где антитело представляет собой моноклональное антитело.
14. Способ детектирования α-синуклеиновых протофибрилл, включающий стадии
- добавления антитела или его фрагмента по любому из пп.1-9 к биологическому образцу, содержащему или предположительно содержащему α-синуклеиновые протофибриллы, и
- детектирования присутствия комплекса между α-синуклеиновыми протофибриллами и указанным антителом или его фрагментом.
15. Способ по п.14, где антитело представляет собой моноклональное антитело.
16. Способ профилактики, замедления развития или лечения нейродегенеративного расстройства, связанного с α-синуклеиновой патологией у индивидуума, где указанный способ включает введение антитела или его фрагмента по любому из пп.1-9 или композиции по п.12 указанному индивидууму.
17. Способ по п.16, где антитело представляет собой моноклональное антитело.
18. Способ по п.16, где нейродегенеративным заболеванием являются болезнь Паркинсона (БП), деменция, связанная с образованием телец Леви (ДТЛ), вариант болезни Альцгеймера, связанный с образованием телец Леви, болезнь Альцгеймера или атрофия многих органов.
19. Способ по п.16, где нейродегенеративным заболеванием является болезнь Паркинсона (БП).
20. Способ по п.16 для лечения нейродегенеративного заболевания.
21. Способ по п.16 для замедления развития нейродегенеративного заболевания.
22. Способ по п.16 для профилактики развития нейродегенеративного заболевания.
23. Способ по п.16, где указанным нейродегенеративным расстройством являются болезнь Паркинсона (БП), деменция, связанная с образованием телец Леви (ДТЛ), вариант болезни Альцгеймера, связанный с образованием телец Леви, болезнь Альцгеймера, синдром Дауна, атрофия многих органов, психоз, шизофрения или болезнь Крейцфельда-Якоба.
24. Применение антитела или его фрагмента по любому из пп.1-9 для получения фармацевтической композиции для лечения нейродегенеративных расстройств, ассоциированных с α-синуклеиновой патологией.
25. Применение по п.24, где антитело представляет собой моноклональное антитело.
26. Применение по п.24, где указанным нейродегенеративным расстройством являются болезнь Паркинсона (БП), деменция, связанная с образованием телец Леви (ДТЛ), вариант болезни Альцгеймера, связанный с образованием телец Леви, болезнь Альцгеймера, синдром Дауна, атрофия многих органов, психоз, шизофрения или болезнь Крейцфельда-Якоба.
27. Применение антитела или его фрагмента по любому из пп.1-9 или композиции по п.12 для диагностики или мониторинга развития нейродегенеративного расстройства, связанного с α-синуклеиновой патологией.
28. Применение по п.27, где антитело представляет собой моноклональное антитело.
29. Применение по п.27 для диагностики или мониторинга развития болезни Паркинсона (БП), деменции, связанной с образованием телец Леви (ДТЛ), варианта болезни Альцгеймера, связанной с образованием телец Леви, синдрома Дауна, атрофии многих органов, психоза, шизофрении или болезни Крейцфельда-Якоба.
30. Способ снижения или ингибирования агрегации α-синуклеина путем введения антитела или его фрагмента по любому из пп.1-9 или композиции по п.12 в образец, содержащий растворимые молекулы α-синуклеина.
31. Способ по п.30, где антитело представляет собой моноклональное антитело.
| WO2009133521 A2, 05.11.2009 | |||
| Водотрубный паровозный котел | 1927 |
|
SU10055A1 |
Авторы
Даты
2015-07-10—Публикация
2011-02-25—Подача