Настоящее изобретение относится к тозилатной соли соединения формулы (1), как описано здесь, фармацевтической композиции, содержащей данную соль, и способам лечения расстройств или состояний, которые можно лечить путем антагонизации гистаминовых рецепторов 3 типа (Н3-рецепторов) с применением тозилатной соли.
Гистамин является хорошо известным медиатором в реакциях гиперчувствительности (например аллергиях, сенной лихорадке и астме), которые обычно лечат антагонистами гистамина или «антигистаминными лекарственными средствами». Также было установлено, что гистаминовые рецепторы существуют в по меньшей мере двух различных типах, называемых Н1- и Н2-рецепторы.
Полагают, что третий гистаминовый рецептор (Н3-рецептор) играет роль в нейропередаче в центральной нервной системе, где, как предполагают, Н3-рецептор расположен пресинаптически на гистаминергических нервных окончаниях (Nature, 302, S32-S37 (1983)). Существование Н3-рецептора было подтверждено разработкой селективных агонистов и антагонистов Н3-рецептора (Nature, 327, 117-123 (1987)), и впоследствии было показано, что он регулирует высвобождение нейромедиаторов как в центральной нервной системе, так и в периферических органах, в частности легких, сердечно-сосудистой системе и желудочно-кишечном тракте.
Несколько заболеваний или состояний можно лечить лигандами гистаминовых рецепторов 3 типа, где Н3-лиганд может представлять собой антагонист, агонист или частичный агонист, см.:



Такие заболевания или состояния включают сердечно-сосудистые расстройства, такие как острый инфаркт миокарда; расстройства процессов памяти, деменцию, когнитивные расстройства, такие как болезнь Альцгеймера и синдром дефицита внимания с гиперактивностью; неврологические расстройства, такие как болезнь Паркинсона, шизофрения, депрессия, эпилепсия и эпилептические припадки или судороги; рак, такой как рак кожи, медуллярный рак щитовидной железы и меланома; респираторные расстройства, такие как астма; расстройства сна, такие как нарколепсия; вестибулярные расстройства, такие как болезнь Меньера; желудочно-кишечные расстройства, воспаление, мигрень, болезнь движения, ожирение, боль и септический шок.
Антагонисты Н3-рецепторов были также описаны ранее, например, в WO 03/050099, WO 02/0769252, WO 02/12224 и публикации патента США №2005/0171181 А1. Гистаминовый Н3-рецептор (H3R) регулирует высвобождение гистамина и других нейромедиаторов, включая серотонин и ацетилхолин. H3R относительно специфичен для нейронов и ингибирует высвобождение определенных моноаминов, таких как гистамин. Селективный антагонизм в отношении H3R-рецепторов повышает уровни гистамина в головном мозге и ингибирует такие активности, как потребление пищи, минимизируя в то же время неспецифические периферические эффекты. Антагонисты этого рецептора увеличивают синтез и высвобождение церебрального гистамина и других моноаминов. В соответствии с этим механизмом они вызывают длительное бодрствование, улучшение когнитивной функции, уменьшение потребления пищи и нормализацию вестибулярных рефлексов. Соответственно, хотя и без какого-либо ограничения этим объяснением, рецептор представляет собой важную мишень для новых лекарственных средств от болезни Альцгеймера, расстройств настроения и расстройств внимания, включая синдром дефицита внимания с гиперактивностью (ADHD), когнитивные расстройства, ожирение, головокружение, шизофрению, эпилепсию, расстройства сна, нарколепсию и болезнь движения, и различные формы тревоги.
В настоящее время большинство антагонистов гистаминовых Н3-рецепторов напоминают гистамин в том, что они имеют имидазольное кольцо, которое может быть замещено, как описано, например, в WO 96/38142. Некоторая активность в отношении гистаминовых Н3-рецепторов, но с незначительным эффектом, была продемонстрирована для неимидазольных нейроактивных соединений, таких как бета-гистамины (Arrang, Eur. J.Pharm. 1985, 111:72-84). В ЕР 978512 и ЕР 0982300А2 раскрыты неимидазольные алкиламины в качестве антагонистов гистаминовых Н3-рецепторов. В WO 02/12224 (Ortho McNeil Pharmaceuticals) описаны неимидазольные бициклические производные в качестве лигандов гистаминовых Н3-рецепторов. Другие антагонисты рецепторов описаны в WO 02/32893 и WO 02/06233.
Соединения, представляющие собой антагонисты гистаминовых рецепторов 3 типа, включая транс-N-этил-3-фтор-3-[3-фтор-4-(пирролидин-1-илметил)фенил]-циклобутанкарбоксамид и его гидрохлоридную соль, и другие родственные соединения, упомянуты в U.S. с серийным номером 11/549175, поданной 13 октября 2006 г. В вышеупомянутой заявке того же заявителя, что и настоящая заявка, полностью включенной сюда посредством ссылки, в общем изложены фармацевтически приемлемые соли присоединения кислот для упомянутых в ней соединений.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к тозилатной соли соединения формулы (1):

ее сольватам (например гидратам), ее полиморфным модификациям и ее фармацевтическим композициям. Соединение формулы (1) может быть названо здесь транс-N-этил-3-фтор-3-[3-фтор-4-(пирролидин-1-илметил)-фенил]-циклобутанкарбоксамидом, который может также быть назван этиламидом (транс)-3-фтор-3-[3-фтор-4-(пирролидин-1-илметил)фенил]циклобутанкарбоновой кислоты.
Соединение формулы (1) является антагонистом гистаминовых рецепторов 3 типа (Н3-рецепторов) и полезно в лечении некоторых расстройств, заболеваний и состояний центральной нервной системы. Данное соединение особенно полезно в лечении расстройства или состояния, выбранного из группы, состоящей из депрессии, расстройств настроения, шизофрении, тревожных расстройств, когнитивных расстройств, болезни Альцгеймера, синдрома дефицита внимания (ADD), синдрома дефицита внимания с гиперактивностью (ADHD), психотических расстройств, расстройств сна, ожирения, головокружения, эпилепсии, болезни движения, респираторных заболеваний, аллергии, индуцированных аллергией реакций дыхательных путей, аллергического ринита, заложенности носа, аллергической гиперемии, гиперемии, гипотензии, сердечно-сосудистого заболевания, заболеваний желудочно-кишечного тракта (ЖКТ), гипер- и гипокинезии и секреции кислоты в желудочно-кишечном тракте.
Настоящее изобретение относится к тозилатной соли транс-N-этил-3-фтор-3-[3-фтор-4-(пирролидин-1-илметил)фенил]-циклобутанкарбоксамида.
В одном воплощении тозилатная соль по изобретению является безводной или почти безводной и может представлять собой полиморфную модификацию.
Тозилатная соль по настоящему изобретению демонстрирует свойства, включая стабильность в твердом состоянии и совместимость с определенными эксципиентами для изготовления лекарственных средств, которые делают ее лучше известных ранее солей транс-N-этил-3-фтор-3-[3-фтор-4-(пирролидин-1-илметил)фенил]-циклобутанкарбоксамида.
Соединение (то есть соединение формулы (1)) по изобретению может существовать в ряде твердых состояний, варьирующих от полностью аморфных до полностью кристаллических. Термин «аморфный» относится к состоянию, при котором в веществе отсутствует дальний порядок на молекулярном уровне, и, в зависимости от температуры, оно может демонстрировать физические свойства твердого тела или жидкости. Обычно такие вещества не дают характерных картин дифракции рентгеновских лучей, и, несмотря на то, что они демонстрируют свойства твердого тела, их более формально описывают как жидкость. При нагревании происходит смена свойств твердого тела на свойства жидкости, что характеризуется изменением структуры, обычно второго порядка («стеклование»). Термин «кристаллический» относится к твердой фазе, в которой вещество имеет регулярно упорядоченную внутреннюю структуру на молекулярном уровне и дает характерную картину дифракции рентгеновских лучей с определенными пиками. Такие вещества при достаточном нагревании также будут демонстрировать свойства жидкости, но смена твердого тела на жидкость характеризуется фазовым переходом, обычно первого порядка («точка плавления»).
Соединение (то есть соединение формулы (1)) по изобретению может также существовать в несольватированных и сольватированных формах. Термин «сольват» использован здесь для описания молекулярного комплекса, содержащего соединение по изобретению и одну или более чем одну молекулу фармацевтически приемлемого растворителя, например, этанола. Термин «гидрат» используют, когда указанный растворитель представляет собой воду.
В принятой в настоящее время системе классификации органических гидратов определены гидраты с выделенным сайтом, канальные гидраты или гидраты, координируемые ионом металла; см. Polymorphism in Pharmaceutical Solids by К.R.Morris (Ed. H.G.Brittain, Marcel Dekker, 1995). В гидратах с выделенным сайтом молекулы воды разделены от непосредственного контакта друг с другом органическими молекулами. В канальных гидратах молекулы воды расположены в каналах кристаллической решетки, где они расположены рядом с другими молекулами воды. В гидратах, координируемых ионом металла, молекулы воды связаны с ионом металла.
Когда растворитель или вода прочно связаны, комплекс будет иметь строго определенную стехиометрию независимо от влажности. Тем не менее, когда растворитель или вода связаны слабо, как в канальных сольватах и гигроскопичных соединениях, содержание воды/растворителя будет зависеть от влажности и условий высушивания. В таких случаях отсутствие стехиометрии будет нормой.
Также в объем изобретения включены многокомпонентные комплексы (отличные от солей и сольватов), где лекарственное средство и по меньшей мере один другой компонент представлены в стехиометрических или нестехиометрических количествах. Комплексы такого типа включают клатраты (соединения включения лекарственное средство-хозяин) и сокристаллы. Последние обычно определяют как кристаллические комплексы из нейтральных молекулярных составляющих, связанных друг с другом нековалентными взаимодействиями, но они также могут представлять собой комплекс нейтральной молекулы с солью. Сокристаллы могут быть получены кристаллизацией из расплава, перекристаллизацией из растворителей или физическим измельчением компонентов друг с другом; см. Chem. Commun., 17. 1889-1896, O.Almarsson and M. J. Zaworotko (2004). Общий обзор многокомпонентных комплексов см. в J. Pharm. Sci., 64 (8), 1269-1288, Haleblian (August 1975).
Соединение по изобретению (то есть соединение формулы (1)), под воздействием подходящих условий, может также существовать в мезоморфном состоянии (мезофазе или жидком кристалле). Мезоморфное состояние является промежуточным между истинным кристаллическим состоянием и истинным жидким состоянием (либо расплавом, либо раствором). Мезоморфизм, появляющийся в результате изменения температуры, описывают как «термотропный», а являющийся результатом добавления второго компонента, такого как вода или другой растворитель, описывают как «лиотропный». Соединения, способные образовывать лиотропные мезофазы, описывают как «амфифильные», и они состоят из молекул, имеющих ионную (как например -COO-, Na+, -COO-К+ или -SO3 -Na+) или неионную (как например -N-N+(СН3)3) полярную головную группу. Дополнительную информацию см. в Crystals and the Polarizing Microscope, N.H.Hartshorne and A.Stuart, 4th Edition (Edward Arnold, 1970).
В дальнейшем все ссылки на соединение формулы (1) включают ссылки на его соли, сольваты, многокомпонентные комплексы и жидкие кристаллы, и на сольваты, многокомпонентные комплексы и жидкие кристаллы его солей.
Тозилатная соль по изобретению также характеризуется основными пиками картины дифракции рентгеновских лучей, выраженными в единицах 2θ, как измерено с использованием медного излучения (с указанием пределов погрешности), как представлено в Таблице 1 и на Фиг.1, и как обсуждено здесь.
Гигроскопичность оценивали с применением методики динамической сорбции пара, при которой точно взвешенный образец подвергают прогрессивному изменению давления водяного пара при одновременной записи изменения массы. Эксперимент проводят изотермически при 25°С.
Другое воплощение изобретения относится к фармацевтической композиции, содержащей тозилатную соль соединения формулы (1) и фармацевтически приемлемый носитель или эксципиент, в частности, к композиции для применения в лечении депрессии, расстройств настроения, шизофрении, тревожных расстройств, когнитивных расстройств, болезни Альцгеймера, синдрома дефицита внимания (ADD), синдрома дефицита внимания с гиперактивностью (ADHD), психотических расстройств, расстройств сна, ожирения, головокружения, эпилепсии, болезни движения, респираторных заболеваний, аллергии, индуцированных аллергией реакций дыхательных путей, аллергического ринита, заложенности носа, аллергической гиперемии, гиперемии, гипотензии, сердечно-сосудистого заболевания, заболеваний ЖКТ, гипер- и гипокинезии и секреции кислоты в желудочно-кишечном тракте.
Настоящее изобретение также относится к способу лечения депрессии, расстройств настроения, шизофрении, тревожных расстройств, когнитивных расстройств, болезни Альцгеймера, синдрома дефицита внимания (ADD), синдрома дефицита внимания с гиперактивностью (ADHD), психотических расстройств, расстройств сна, ожирения, головокружения, эпилепсии, болезни движения, респираторных заболеваний, аллергии, индуцированных аллергией реакций дыхательных путей, аллергического ринита, заложенности носа, аллергической гиперемии, гиперемии, гипотензии, сердечно-сосудистого заболевания, заболеваний желудочного кишечного тракта, гипер- и гипокинезии и секреции кислоты в желудочно-кишечном тракте, включающему введение соли соединения формулы (1) млекопитающему, нуждающемуся в таком лечении.
Изобретение также относится к способу получения тозилатной соли соединения формулы (1), включающему стадии:
(1) приведения в контакт соединения формулы (1), растворенного в подходящем растворителе, с пара-толуолсульфоновой кислотой (обычно называемой "тозиевой" кислотой (tosic acid)); и
(2) сбора образованных кристаллов.
Настоящее изобретение также относится к тозилатной соли транс-N-этил-3-фтор-3-[3-фтор-4-(пирролидин-1-илметил)фенил]-циклобутанкарбоксамида (1), полученной способом по изобретению.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На Фиг.1 представлена наблюдаемая картина дифракции рентгеновских лучей на порошке тозилатной соли транс-N-этил-3-фтор-3-[3-фтор-4-(пирролидин-1-ил-метил)фенил]-циклобутанкарбоксамида (по оси Y представлены линейные единицы счета в секунду; на оси Х представлены градусы 2-тета) с условиями проведения 2Th/Th закрытый тип, вначале при градусах 3000, при окончании при градусах 40000, с шагом 0,040 градуса. Время шага 1 с, при комнатной температуре (25°С).
На Фиг.2 представлена запись дифференциальной сканирующей калоримертрии (с нанесением на график теплового потока (Вт/г) и температуры, экзотермического подъема (exo up)) для 1,5220 мг образца тозилатной соли транс-N-этил-3-фтор-3-[3-фтор-4-(пирролидин-1-илметил)фенил]-циклобутанкарбоксамида, проведенной от 30°С до 300°С при 5,00°С/мин, с двумя основными событиями, первым при 161,27°С, 100,4 Дж/г. Производная теплового потока показана на нижней записи.
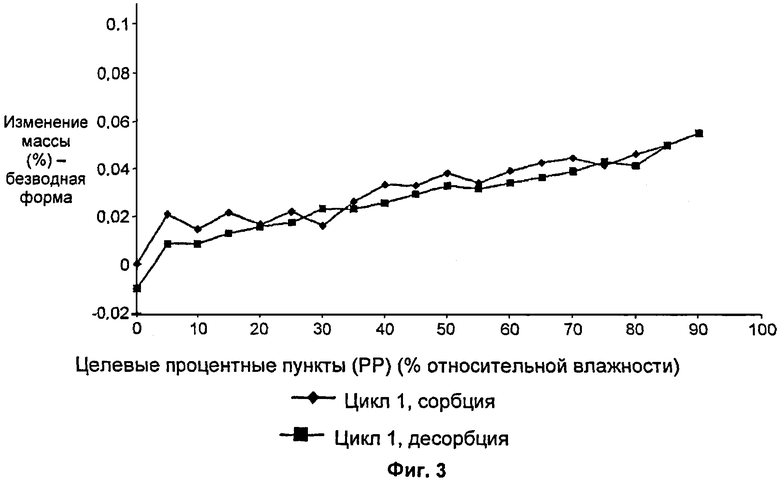
На Фиг.3 представлена изотерма сорбции влаги тозилатной соли транс-N-этил-3-фтор-3-[3-фтор-4-(пирролидин-1-илметил)фенил]-циклобутанкарбоксамида, с абсорбцией в виде кривой (♦) и десорбцией в виде кривой (■), с нанесением процентного изменения массы как функции относительной влажности с применением способа движущегося непрерывного потока (образец 8,1 мг, 25°С).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Соединение формулы (1) является антагонистом гистаминового рецептора 3 типа (Н3-рецептора) и полезно в лечении ряда заболеваний, расстройств и состояний центральной нервной системы (ЦНС). Свободное основание соединения и его гидрохлоридная соль могут быть получены способами, изложенными в U.S. с серийным номером 11/549175, поданной 13 октября 2006 г. (см. также "Histamine-3 Receptor Antagonists", WO 2007/049123, полное описание которой полностью включено сюда посредством ссылки). Тозилатная соль может быть получена во множестве различных условий. В одном воплощении способа свободное основание соединения формулы (1) предпочтительно растворяют в подходящем растворителе до полного растворения, после чего к полученному таким образом раствору добавляют пара-толуолсульфоновую кислоту для образования тозилатной соли присоединения по изобретению. Подходящие растворители включают этилацетат, метилацетат, изопропилацетат, метанол, этанол, н-пропанол, изопропанол, трет-бутанол, диэтиловый эфир, диизопропиловый эфир и метил-трет-бутиловый эфир; предпочтительно этилацетат или метанол. В другом воплощении способа приведение в контакт соединения формулы (1) в фазе раствора осуществляют или с раствором пара-толуолсульфоновой кислоты, или с твердой формой пара-толуолсульфоновой кислоты.
Предпочтительно стадию приведения в контакт проводят в течение периода от 1 до 24 часов, более предпочтительно от 10 до 20 часов, и она включает перемешивание или смешивание получаемой смеси. Предпочтительным воплощением способа является такое воплощение, в котором стадию (1) способа проводят при температуре между температурой окружающей среды и температурой дефлегмации растворителя; более предпочтительно между температурой окружающей среды и приблизительно 80°С; наиболее предпочтительно способ осуществляют при температуре 25°С-60°С. Предпочтительным подходящим растворителем является этилацетат или метанол. Предпочтительно реакционную смесь оставляют охлаждаться до температуры окружающей среды после завершения добавления пара-толуолсульфоновой кислоты и позволяют перемешиваться в течение оставшейся части реакционного периода. В предпочтительном воплощении см. протокол Примера 1.
Тозилатная соль соединения формулы (1) лишь незначительно гигроскопична и имеет высокую растворимость в воде. Эти характеристики, в комбинации с ее относительной инертностью в отношении обычных эксципиентов, используемых в фармацевтической композиции, делают ее в высшей степени подходящей для применения в фармацевтических композициях.
Физические свойства
1(а) Кристалличность
Образец приготавливали в силиконовом масле и наблюдали в поперечно поляризованном свете. Образец был кристаллическим, и он содержит частицы нерегулярной формы в виде призм с выраженными свойствами двойного лучепреломления с некоторыми агрегатами. Аморфное вещество в образце обнаружено не было.
1(б) Картины дифракции рентгеновских лучей на порошке
Для тозилатной соли по изобретению получали картину дифракции рентгеновских лучей на порошке с использованием дифрактометра Bruker D5000 (Madison, Wisconsin), оборудованного источником медного излучения, фиксированными щелями (дивергентной 1,0 мм, антирассеивающей 1,0 мм и принимающей 0,6 мм) и полупроводниковым детектором Solex. Данные получали в тета-два (2θ) тета-гониометрической конфигурации от плоской пластины держателя образца при длине волны медного излучения Kα1=1,54056 и Kα2=1,54439 (относительная интенсивность 0,5) от градусов два-тета 3,0 до 40,0 с использованием длины шага 0,040 градуса и времени шага одна секунда. Напряжение и сила тока рентгеновской трубки были установлены на 40 кВ и 30 мА соответственно.
Данные получали и анализировали с использованием программного обеспечения Bruker DIFFRAC Plus. Образцы приготавливали, помещая их в кварцевый держатель (Следует отметить, что дифрактометр Bruker D5000 в процессе работы сходен с моделью Siemans D5000). Результаты суммированы в Таблице 1, в которой представлены значения два-тета и относительные интенсивности для всех отражений (линий) с относительной интенсивностью, большей или равной 7%, с использованием ширины отражения 0,30 и порогового значения 4,0.
Настоящее изобретение включает тозилатную соль соединения формулы (1), где основные пики картины дифракции рентгеновских лучей, выраженные в показателях 29, как измерено с использованием медного (Kα1=1,54056, Kα2=1,54439) излучения, включают любую комбинацию пиков Таблицы 1 и как представлено на Фиг.1. Например, настоящее изобретение включает тозилатную соль соединения формулы (1), где основные пики картины дифракции рентгеновских лучей, выраженные в показателях 29 (±0,2) включают, например, 8,959; 13,816; 15,515; 17,991, 18,523; 19,406; 19,741; 20,250; 21,054; 21,995; 22,590; 24,409; 25,327; 26,328 и 28,050, или любое их подмножество или отдельный пик, например, 8,959; 13,816; 15,515 и 17,991, совместно или по отдельности. Было определено, что исследованное вещество было полностью кристаллическим.
2. Термический анализ
При дифференциальной сканирующей калориметрии было выявлено единственное эндотермическое событие с начальной температурой приблизительно 161°С (ΔН=100,4 Дж/г) с последующим экзотермическим событием с началом приблизительно 175°С (см. Фиг.2). Это согласуется с плавлением и разложением вещества, наблюдаемым при высокотемпературной микроскопии плавления (hot stage fusion microscopy).
Высокотемпературную микроскопию плавления проводили без силиконового масла и частицы наблюдали под поперечно поляризованным светом при нагревании до 225°С с применением Linkam Variable Temperature Stage. Плавление призматических частиц происходило при приблизительно 165°С, и плавление завершалось при 168°С. Других событий выявлено не было, и при охлаждении предметного стекла до комнатной температуры кристаллизации не наблюдали.
3. Гигроскопичность
В течение начального цикла сушки (25°С, 1% относительная влажность (RH)) наблюдали потерю массы менее 0,1%, что соответствует безводной негигроскопичной форме. Приблизительно 0,06% увеличение массы было выявлено при DVS-анализе, когда образец подвергали воздействию относительной влажности от 5% до 90% при 25°С. Фаза десорбции была похожа на фазу сорбции при снижении относительной влажности до 5% (см. Фиг.3). В дополнение, картина дифракции рентгеновских лучей на порошке для образца после исследования гигроскопичности совпадала с картиной дифракции образца до этого исследования.
4. Растворимость в воде
В отношении растворимости в воде были получены следующие данные. Тозилатная соль по изобретению имеет растворимость более чем 10 мг/мл в 0,1 М забуференном фосфатом физиологическом растворе (конечный рН 6,5); растворимость более чем 11 мг/мл в 0,1 М забуференном фосфатом физиологическом растворе с весовым процентом таурохолата натрия/солей фосфатидилхолина 0,5 при конечном рН 6,5; и 23,6 мг/мл в незабуференной воде (конечный рН 3,8). Эти величины отражают растворимость кристаллического соединения, определенную посредством обращенно-фазовой высокоэффективной жидкостной хроматографии (RP-HPLC-анализа) после воздействия на смесь лекарственного средства и среды программой термоциклирования (40°С в течение 8 часов, 15°С в течение 5 часов и 25°С в течение 12 часов).
Тозилатная соль по настоящему изобретению может быть представлена, например, в форме твердых "пробок" (plug), порошков или пленок такими способами, как осаждение, кристаллизация, лиофильная сушка, распылительная сушка или сушка выпариванием. С этой целью могут быть использованы микроволновая или радиочастотная сушка.
Тозилатная соль может быть введена сама по себе или в комбинации с одним или более другими соединениями по изобретению или в комбинации с одним или более другими лекарственными средствами (или как любая их комбинация). В большинстве случаев их будут вводить в форме композиции совместно с одним или более фармацевтически приемлемыми эксципиентами. Термин «эксципиент» использован здесь для описания любого ингредиента, отличного от соединения (соединений) по изобретению. Выбор эксципиента будет в значительной степени зависеть от таких факторов, как конкретный способ введения, воздействие эксципиента на растворимость и стабильность и тип лекарственной формы.
Фармацевтические композиции, подходящие для доставки соединений по настоящему изобретению, и способы их изготовления будут ясны специалистам в данной области техники. Такие композиции и способы их изготовления могут быть обнаружены, например, в Remington's Pharmaceutical Sciences. 19th Edition (Mack Publishing Company, 1995).
Соль по изобретению может быть введена перорально. Пероральное введение может включать прием внутрь таким образом, что соединение попадает в желудочно-кишечный тракт, и/или трансбуккальное, лингвальное или сублингвальное введение, посредством которого соединение проникает в кровоток непосредственно из полости рта.
Композиции, подходящие для перорального введения, включают твердые, полутвердые и жидкие системы, такие как таблетки, мягкие или твердые капсулы, содержащие мульти- или наночастицы, жидкости или порошки; пастилки (включая наполненные жидкостью); жевательные таблетки; гели; быстродиспергируемые лекарственные формы; пленки; овули; спреи; и буккальные/мукоадгезивные пластыри.
Жидкие композиции включают суспензии, растворы, сиропы и эликсиры. Такие композиции могут быть использованы в качестве наполнителей в мягких или твердых капсулах (изготовленных, например, из желатина или гидроксипропилметилцеллюлозы), и они обычно содержат носитель, например воду, этанол, полиэтиленгликоль, пропиленгликоль, метилцеллюлозу или подходящее масло и один или более чем один эмульгатор и/или суспендирующий агент. Жидкие композиции могут также быть изготовлены растворением твердого вещества, например, из саше.
Соль по изобретению может также быть использована в быстрорастворимых, быстрораспадающихся лекарственных формах, таких как формы, описанные в Expert Opinion in Therapeutic Patents, 11 (6), 981-986, Liang and Chen (2001).
Для таблетированных лекарственных форм в зависимости от дозы лекарственное средство может составлять от 1 мас.% до 80 мас.% лекарственной формы, более типично от 5 мас.% до 60 мас.% лекарственной формы. В дополнение к лекарственному средству таблетки в большинстве случаев содержат разрыхлитель. Примеры разрыхлителей включают крахмалгликолят натрия, натрий-карбоксиметилцеллюлозу, кальций-карбоксиметилцеллюлозу, натрий-кроскармелозу, кросповидон, поливинилпирролидон, метилцеллюлозу, микрокристаллическую целлюлозу. гидроксипропилцеллюлозу, замещенную низшими алкилами, крахмал, прежелатинизированный крахмал и альгинат натрия. В большинстве случаев разрыхлитель будет составлять от 1 мас.% до 25 мас.%, предпочтительно от 5 мас.% до 20 мас.% лекарственной формы.
Для придания таблетированной композиции когезионных свойств в большинстве случаев используют связывающие агенты. Подходящие связывающие агенты включают микрокристаллическую целлюлозу, желатин, сахара, полиэтиленгликоль, природные и синтетические смолы, поливинилпирролидон, прежелатинизированный крахмал, гидроксипропилцеллюлозу и гидроксипропилметилцеллюлозу. Таблетки могут также содержать разбавители, такие как лактоза (моногидрат, моногидрат, высушенный распылительной сушкой, безводная форма и тому подобное), маннит, ксилит, декстроза, сахароза, сорбит, микрокристаллическая целлюлоза, крахмал и дигидрат гидрофосфата кальция.
Таблетки могут также, возможно, содержать поверхностно-активные вещества, такие как лаурилсульфат натрия и полисорбат 80, и скользящие вещества, такие как диоксид кремния и тальк. В случае присутствия поверхностно-активные вещества могут составлять от 0,2 мас.% до 5 мас.% таблетки, и скользящие вещества могут составлять от 0,2 мас.% до 1 мас.% таблетки.
Таблетки также в большинстве случаев содержат смазывающие вещества, такие как стеарат магния, стеарат кальция, стеарат цинка, стеарилфу марат натрия и смеси стеарата магния с лаурилсульфатом натрия. В большинстве случаев смазывающие вещества составляют от 0,25 мас.% до 10 мас.%, предпочтительно от 0,5 мас.% до 3 мас.% таблетки.
Другие возможные ингредиенты включают антиоксиданты, красители, корригенты, консерванты и вещества, исправляющие вкус лекарственного средства.
Типичные таблетки содержат до приблизительно 80% лекарственного средства, от приблизительно 10 мас.% до приблизительно 90 мас.% связывающего агента, от приблизительно 0 мас.% до приблизительно 85 мас.% разбавителя, от приблизительно 2 мас.% до приблизительно 10 мас.% разрыхлителя и от приблизительно 0,25 мас.% до приблизительно 10 мас.% смазывающего вещества.
Таблетки могут быть изготовлены из таблеточных смесей прямым прессованием или с использованием валика. Перед таблетированием таблеточные смеси или части смесей могут альтернативно быть подвергнуты влажному гранулированию, сухому гранулированию или гранулированию плавлением, затвердеванию из расплава или экструзии. Конечная композиция может содержать один или более чем один слой и может иметь покрытие или не иметь покрытия; она может даже быть инкапсулирована.
Изготовление таблеток обсуждено в Pharmaceutical Dosage Forms: Tablets. Vol.1, H.Lieberman and L.Lachman (Marcel Dekker, New York, 1980).
Годные к употреблению пероральные пленки для применения у людей или животных обычно представляют собой мягкие растворимые в воде или набухающие в воде тонкие пленчатые лекарственные формы, способные быстро растворяться или являющиеся мукоадгезивными, и обычно содержащие соединение формулы (1), пленкообразующий полимер, связывающий агент, растворитель, увлажнитель, пластификатор, стабилизатор или эмульгатор, агент, модифицирующий вязкость, и растворитель. Некоторые компоненты композиции могут выполнять более чем одну функцию.
Соединение формулы (1) может быть растворимым в воде или нерастворимым в воде. Водорастворимое соединение обычно содержит от 1 мас.% до 80 мас.%, более типично от 20 мас.% до 50 мас.% растворенных веществ. Менее растворимые соединения могут составлять большую часть композиции, обычно до 88 мас.% растворенных веществ. Альтернативно соединение формулы (1) может быть представлено в форме гранул из множества частиц.
Пленкообразующий полимер может быть выбран из природных полисахаридов, белков или синтетических гидроколлоидов, и обычно представлен в количестве от 0,01 до 99 мас.%, более типично в количестве от 30 до 80 мас.%.
Другие возможные ингредиенты включают антиоксиданты, красители, корригенты и усилители вкуса и запаха, консерванты, агенты, стимулирующие слюноотделение, охлаждающие агенты, сорастворители (включая масла), смягчающие средства, наполнители, пеногасители, поверхносто-активные вещества и вещества, исправляющие вкус лекарственного средства.
Пленки по изобретению обычно изготавливают сушкой выпариванием тонких водных пленок, нанесенных на легкоотслаивающуюся подложку или бумагу. Это может быть выполнено в сушильном шкафу или камере, обычно в комбинированной сушилке для нанесения покрытий, или лиофильной сушкой, или вакуумной сушкой.
Твердые композиции для перорального введения могут быть изготовлены для немедленного и/или модифицированного высвобождения. Композиции с модифицированным высвобождением включают замедленное, длительное, импульсное, регулируемое, направленное и программируемое высвобождение.
Подходящие композиции с модифицированным высвобождением для целей изобретения описаны в патенте США №6106864. Подробности о других подходящих технологиях высвобождения, таких как высокоэнергетические дисперсии, и осмотические частицы, и частицы с покрытием представлены в Pharmaceutical Technology On-line. 25(2), 1-14, Verma et al (2001). Применение жевательной резинки для достижения регулируемого высвобождения описано в WO 00/35298.
Тозилатная соль по изобретению может также быть введена непосредственно в кровоток, в мышцу или во внутренний орган. Подходящие способы парентерального введения включают внутривенный, внутриартериальный, внутрибрюшинный, интратекальный, внутрижелудочковый, интрауретральный, внутригрудинный, интракраниальный, внутримышечный, внутрисуставной и подкожный. Подходящие устройства для парентерального введения включают игольные (включая микроигольные) инъекторы, безыгольные инъекторы и методики инфузии.
Композиции для парентерального применения обычно представляют собой водные растворы, которые могут содержать эксципиенты, такие как соли, углеводы и буферные агенты (предпочтительно до рН от 3 до 9), но, для некоторых применений, они могут быть более подходяще изготовлены в виде стерильного неводного раствора или в виде высушенной формы для применения в сочетании с подходящим носителем, таким как стерильная апирогенная вода.
Изготовление композиций для парентерального применения в стерильных условиях, например, лиофилизацией, может легко быть осуществлено с применением стандартных фармацевтических методик, хорошо известных специалистам в данной области техники.
Растворимость тозилатной соли, используемой в изготовлении растворов для парентерального применения, может быть увеличена применением подходящих методик изготовления, таких как включение агентов, увеличивающих растворимость.
Композиции для парентерального введения могут быть изготовлены для немедленного и/или модифицированного высвобождения. Композиции с модифицированным высвобождением включают замедленное, длительное, импульсное, регулируемое, направленное и программируемое высвобождение. Таким образом, соединения по изобретению могут быть приготовлены в виде суспензии или в виде твердой, полутвердой лекарственной формы или тиксотропной жидкости для введения в виде имплантируемого депо, обеспечивающего модифицированное высвобождение активного соединения. Примеры таких композиций включают покрытые лекарственным средством стенты и полутвердые лекарственные формы или суспензии, содержащие нагруженные лекарственным средством микросферы сополимера D- и L-изомеров молочной и гликолевой кислот (PGLA).
Тозилатная соль по изобретению может также быть введена местно, (внутри)кожно или чрескожно на кожу или слизистую оболочку. Типичные композиции для этой цели включают гели, гидрогели, лосьоны, растворы, кремы, мази, присыпки, перевязочный материал, пены, пленки, трансдермальные пластыри, прокладки, имплантаты, губки, волокна, повязки и микроэмульсии. Также могут быть использованы липосомы. Типичные носители включают спирт, воду, минеральное масло, вазелиновое масло, медицинский вазелин, глицерин, полиэтиленгликоль и пропиленгликоль. Могут быть включены вещества, усиливающие проникновение; см., например, J.Pharm. Sci., 88 (10), 955-958, Finnin and Morgan (October 1999).
Другие способы местного введения включают доставку посредством электропорации, ионтофореза, фонофореза, сонофореза и микроигольной или безыгольной (например, Powderject™, Bioject™ и тому подобное) инъекции.
Композиции для местного введения могут быть изготовлены для немедленного и/или модифицированного высвобождения. Композиции с модифицированным высвобождением включают замедленное, длительное, импульсное, регулируемое, направленное и программируемое высвобождение.
Тозилатная соль по изобретению может также быть введена интраназально или ингаляцией, обычно в форме сухого порошка (либо сама по себе, либо в виде смеси, например, в сухой смеси с лактозой, или в виде смешанной компонентной частицы, например, смешанная с фосфолипидами, такими как фосфатидилхолин) из ингалятора сухого порошка, в виде аэрозольного спрея из герметизированного контейнера, насоса, спрея, аэрозольного ингалятора (предпочтительно аэрозольного ингалятора с использованием электрогидродинамики для образования мелкодисперсного аэрозоля), или небулайзера, с применением или без применения подходящего пропеллента, такого как 1,1,1,2-тетрафторэтан или 1,1,1,2,3,3,3-гептафторпропан, или в виде капель в нос. Для интраназального применения порошок может содержать биоадгезивный агент, например, хитозан или циклодекстрин.
Герметизированный контейнер, насос, спрей, аэрозольный ингалятор или небулайзер содержит раствор или суспензию соединения (соединений) по изобретению, содержащую, например, этанол, водный этанол или подходящий альтернативный агент для диспергирования, солюбилизации или продления высвобождения активного соединения, пропеллент (пропелленты) в качестве растворителя и, возможно, поверхностно-активное вещество, такое как сорбитантриолеат, олеиновая кислота или олигомолочная кислота.
Перед применением в сухом порошке или суспензионной композиции лекарственное средство микронизируют до размера, подходящего для доставки ингаляцией (обычно менее 5 мкм). Это может быть осуществлено любым подходящим способом измельчения, таким как измельчение в спиральной струе, измельчение в струе псевдоожиженного слоя, обработка сверхкритической жидкостью с образованием наночастиц, гомогенизация под высоким давлением или распылительная сушка.
Капсулы (изготовленные, например, из желатина или гидроксипропилметилцеллюлозы), блистеры и картриджи для использования в ингаляторе или инсуффляторе могут быть изготовлены таким образом, чтобы содержать порошковую смесь соединения по изобретению, подходящего порошкового основания,- такого как лактоза или крахмал, и вещество, модифицирующее свойства, такое как L-лейцин, маннит или стеарат магния. Лактоза может быть безводной или в форме моногидрата, последний предпочтительнее. Другие подходящие эксципиенты включают декстран, глюкозу, мальтозу, сорбит, ксилит, фруктозу, сахарозу и трегалозу.
Подходящая композиция в виде раствора для использования в аэрозольном ингаляторе с применением электрогидродинамики для образования мелкодисперсного аэрозоля может содержать от 1 мкг до 20 мг соединения по изобретению на срабатывание, и объем срабатывания может варьировать от 1 мкл до 100 мкл. Типичная композиция может содержать соединение формулы (1), пропиленгликоль, стерильную воду, этанол и хлорид натрия. Альтернативные растворители, которые могут быть использованы вместо пропиленгликоля, включают глицерин и полиэтиленгликоль.
Подходящие корригенты, такие как ментол и левоментол, или подсластители, такие как сахарин или сахарин-натрий, могут быть добавлены к тем композициям по изобретению, которые предназначены для ингаляционного/интраназального введения.
Композиции для ингаляционного/интраназального введения могут быть изготовлены для немедленного и/или модифицированного высвобождения, с использованием, например, PGLA. Композиции с модифицированным высвобождением включают замедленное, длительное, импульсное, регулируемое, направленное и программируемое высвобождение.
В случае ингаляторов сухого порошка и аэрозолей единицу дозы определяют посредством клапана, доставляющего дозированное количество. Единицы в соответствии с изобретением обычно объединены для введения дозированного количества или «пшика», содержащего от 1 мкг до 20 мг соединения формулы (1). Общая суточная доза будет обычно составлять от 1 мг до 200 мг, которые могут быть введены в одной дозе, или, более обычно, как отдельные дозы в течение всего дня.
Тозилатная соль по изобретению может быть введена ректально или вагинально, например, в форме суппозитория, пессария или клизмы. Масло какао является обычной основой суппозиториев, но по необходимости могут быть использованы различные альтернативы.
Композиции для ректального/вагинального введения могут быть изготовлены для немедленного и/или модифицированного высвобождения. Композиции с модифицированным высвобождением включают замедленное, длительное, импульсное, регулируемое, направленное и программируемое высвобождение.
Тозилатная соль по изобретению может также быть введена непосредственно в глаз или ухо, обычно в виде капель микронизированной суспензии или раствора в изотоническом стерильном физиологическом растворе с откорректированным рН. Другие композиции, подходящие для глазного или ушного введения включают мази, гели, биодеградируемые (например, губки с абсорбируемыми гелями, коллаген) и небиодеградируемые (например, силикон) имплантаты, облатки, линзы и системы на основе частиц или везикул, таких как ниосомы или липосомы. Полимер, такой как поперечно сшитая полиакриловая кислота, поливиниловый спирт, гиалуроновая кислота, целлюлозный полимер, например гидроксипропилметилцеллюлоза, гидроксиэтилцеллюлоза или метилцеллюлоза, или гетерополисахаридный полимер, например гелановая камедь, могут быть включены совместно с консервантом, таким как хлорид бензалкония. Такие композиции могут также быть доставлены ионтофорезом.
Композиции для глазного/ушного введения могут быть изготовлены для немедленного и/или модифицированного высвобождения. Композиции с модифицированным высвобождением включают замедленное, длительное, импульсное, регулируемое, направленное или программируемое высвобождение.
Тозилатную соль по изобретению можно объединять с растворимыми макромолекулярными веществами, такими как циклодекстрин и его подходящие производные или полиэтиленгликольсодержащие полимеры, с целью улучшения их растворимости, скорости растворения, коррекции вкуса, биодоступности и/или стабильности для применения в любом из вышеупомянутых способов введения.
Например, было обнаружено, что комплексы циклодекстрин-лекарственное средство, в целом, применимы для большинства лекарственных форм и путей введения. Могут быть использованы как комплексы включения, так и комплексы без включения. В качестве альтернативы прямому комплексообразованию с лекарственным средством циклодекстрин может быть использован в качестве вспомогательной добавки, то есть в качестве носителя, разбавителя или солюбилизатора. Для этих целей чаще всего используют альфа-, бета- и гамма-циклодекстрины, примеры которых могут быть обнаружены в международных заявках на патент № WO 91/11172, WO 94/02518 и WO 98/55148.
Поскольку может быть желательным вводить комбинацию активных соединений, например, с целью лечения конкретного заболевания или состояния, в объем настоящего изобретения входит то, что две или более чем две фармацевтические композиции, по меньшей мере одна из которых содержит соединение по изобретению, могут быть подходяще объединены в форме набора, подходящего для совместного введения этих композиций.
Таким образом, набор по изобретению включает две или более чем две отдельные фармацевтические композиции, по меньшей мере одна из которых содержит тозилатную соль по изобретению, и средство для раздельного хранения указанных композиций, такое как контейнер, разделенная бутылка или разделенный пакет из фольги. Примером такого набора является общая блистерная упаковка, используемая для упаковки таблеток, капсул и тому подобного.
Набор по изобретению является особенно подходящим для введения различных лекарственных форм, например, пероральных и парентеральных, для введения отдельных композиций с различными интервалами дозирования, или для титрования отдельных композиций в отношении друг друга. Для способствования приверженности лечению набор обычно содержит инструкцию по введению и может быть снабжен так называемой мнемонической помощью.
Тозилатная соль по изобретению может быть введена посредством либо перорального, чрескожного (например, посредством применения пластыря), интраназального, сублингвального, ректального, парентерального, либо местного способов введения. Трансдермальное и пероральное введение являются предпочтительными. Наиболее желательно, активную соль вводят в дозе от приблизительно 0,001 мг/кг вплоть до приблизительно 50 мг/кг в сутки, предпочтительно от приблизительно 0,01 мг/кг до приблизительно 50 мг/кг в сутки, в разовой или раздельных дозах, хотя обязательно будут возникать изменения в зависимости от массы тела и состояния субъекта, проходящего лечение, и конкретного выбранного пути введения. Тем не менее, наиболее желательно используют уровень дозы от приблизительно 0,01 мг/кг до приблизительно 10 мг/кг массы тела в сутки. Тем не менее, могут возникать изменения в зависимости от массы тела и состояния людей, проходящих лечение, и их индивидуальных ответов на указанное лекарственное средство, а также от выбранного типа фармацевтической композиции и периода времени, и интервала, в течение которого осуществляют такое введение. В некоторых случаях уровни доз, меньшие чем нижний предел указанного выше интервала, могут быть более чем адекватны, в то время как в других случаях еще большие дозы могут быть использованы, не вызывая вредных побочных эффектов, при условии, что такие большие дозы сначала разделяют на несколько небольших доз для введения в течение всего дня. Величины доз, изложенные в этом описании и в прилагаемой формуле изобретения, могут быть использованы, например, для среднего субъекта-человека с массой тела от приблизительно 60 кг до приблизительно 70 кг. Опытный практикующий врач сможет легко определить любое изменение величины дозы, которое может быть необходимо для субъекта, масса тела которого выходит за пределы диапазона от приблизительно 60 кг до приблизительно 70 кг, такого как дети и пожилые люди, исходя из истории болезни субъекта. Фармацевтические комбинации могут быть введены по схеме до 6 раз в сутки, предпочтительно от 1 до 3 раз в сутки, как например 2 раза в сутки или один раз в сутки.
Во избежание сомнений, здесь ссылки на «лечение» включают ссылки на радикальное, паллиативное и профилактическое лечение.
Следующий пример иллюстрирует способ и соединение по настоящему изобретению. Тем не менее, следует понимать, что изобретение не ограничено этим конкретным примером.
Пример 1
Пример 1 - Тозилатная соль транс-N-этил-3-фтор-3-[3-фтор-4-(пирролидин-1-илметил)фенил]-циклобутанкарбоксамида
Раствор п-толуолсульфоновой кислоты (2,50 г, 13,14 ммоль) в этилацетате (70 мл) добавляли в течение 20 минут к перемешиваемому раствору транс-N-этил-3-фтор-3-[3-фтор-4-(пирролидин-1-илметил)фенил]-циклобутанкарбоксамида (4,18 г, 12,97 ммоль) в этилацетате (35 мл). Полученную смесь перемешивали в течение дополнительного часа. Белый осадок отфильтровывали, промывали EtOAc и сушили на воздухе с получением 6,32 г тозилатной соли. Это вещество растворяли в метаноле и фильтровали для удаления твердых частиц и повторно концентрировали. Полученное твердое вещество растворяли в ~12-14 мл метанола при умеренном нагревании. Этилацетат (75 мл) добавляли в течение 20 минут и затем смесь перемешивали в течение одного часа при комнатной температуре. Твердое вещество отфильтровывали, промывали этилацетатом и сушили на воздухе с получением 5,59 г тозилатной соли этиламида (транс)-3-фтор-3-[3-фтор-4-(пирролидин-1-илметил)фенил]-циклобутанкарбоновой кислоты в виде белого кристаллического порошка.
1H ЯМР (CDCl3) δ 7,71 (d, J=8,3 Гц, 2Н), 7,65 (t, J=7,9 Гц, 1Н), 7,28-7,22 (m, 2Н), 7,15 (d, J=7,9 Гц, 2Н), 6,52 (br s, 1Н), 4,28 (d, J=5,4 Гц, 2Н), 3,68-3,37 (m, 2Н), 3,33-3,18 (m, ЗН), 2,97-2,88 (m, 2Н), 2,84-2,57 (m, 4H), 2,32 (s, 3Н), 2,27-1,96 (m, 4H), 1,07 (t, J=7,3 Гц, 3Н).
13С ЯМР (CDCl3) δ 173,8, 161,3 (d, JC-F=248,7 Гц), 147,4 (dd, JC-F=24,1, 7,5 Гц), 142,4, 140,4, 133,5, 129,1, 126,0, 121,7 (d, JC-F=6,0 Гц), 116,4 (d, JC-F=14,3 Гц), 112,6 (dd, JC-F=23,3, 9,0 Гц), 96,7 (d, JC-F=197,6 Гц), 53,4, 50,4, 39,0, 38,7, 34,7, 32,6, 23,0, 21,52, 14,9.
Элементный анализ, рассчитанный для C18H24F2N2O·C7H8O3S: С 60,71, Н 6,52, N 5,66, F 7,68, S 6,48. Обнаружено: С 60,55 (60,52, 60,57), Н 6,40 (6,35, 6,44), N 5,58 (5,56, 5,59), F 7,67 (7,78, 7,55), S 6,68; с молекулярной массой 494,61 г/моль, что соответствует безводной монотозилатной соли.
| название | год | авторы | номер документа |
|---|---|---|---|
| ТОЗИЛАТНАЯ СОЛЬ ТРАНС-N-ИЗОБУТИЛ-3-ФТОР-3-[3-ФТОР-4-(ПИРРОЛИДИН-1-ИЛМЕТИЛ)ФЕНИЛ]ЦИКЛОБУТАНКАРБОКСАМИДА | 2008 |
|
RU2451016C2 |
| ЗАМЕЩЕННЫЕ N-ФЕНИЛПИРРОЛИДИНИЛМЕТИЛПИРРОЛИДИНАМИДЫ И ИХ ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ В КАЧЕСТВЕ МОДУЛЯТОРОВ РЕЦЕПТОРА Н3 ГИСТАМИНА | 2008 |
|
RU2477721C2 |
| НОВАЯ СОЛЕВАЯ ФОРМА АГОНИСТА ДОФАМИНА | 2006 |
|
RU2393153C2 |
| ТЕРАПЕВТИЧЕСКИЕ АГЕНТЫ 713 | 2010 |
|
RU2526055C2 |
| ПОЛИМОРФНЫЕ И АМОРФНАЯ ФОРМЫ ФОСФАТНОЙ СОЛИ 8-ФТОР-2-{4-[(МЕТИЛАМИНО)МЕТИЛ]ФЕНИЛ}-1,3,4,5-ТЕТРАГИДРО-6Н-АЗЕПИНО[5.4.3-CD]ИНДОЛ-6-ОНА | 2005 |
|
RU2355691C2 |
| НАПАДИЗИЛАТНАЯ СОЛЬ АНТАГОНИСТА МУСКАРИНОВОГО М3-РЕЦЕПТОРА | 2008 |
|
RU2459810C2 |
| ТОЗИЛАТНАЯ СОЛЬ ПРОИЗВОДНОГО 5-ПИРАЗОЛИЛ-2-ПИРИДОНА, ПОЛЕЗНАЯ В ЛЕЧЕНИИ COPD | 2010 |
|
RU2526038C2 |
| СОЛЬ СУКЦИНАТ 2-((4-(1-МЕТИЛ-4-(ПИРИДИН-4-ИЛ)-1Н-ПИРАЗОЛ-3-ИЛ)ФЕНОКСИ)МЕТИЛ)ХИНОЛИНА | 2007 |
|
RU2430918C2 |
| 3-ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ПИРИДИНА В КАЧЕСТВЕ АНТАГОНИСТОВ ГИСТАМИНОВЫХ Н3 РЕЦЕПТОРОВ | 2005 |
|
RU2389721C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ КОГНИТИВНЫХ РАССТРОЙСТВ | 2005 |
|
RU2420318C2 |


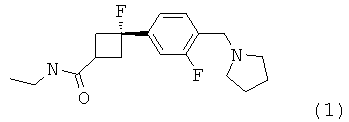
Изобретение относится к тозилатной соли транс-N-этил-3-фтор-3-[3-фтор-4-(пирролидин-1-илметил)-фенил]-циклобутанкарбоксамида формулы (1)
 .
.
Изобретение также относится к фармацевтической композиции, а также к способу лечения. Технический результат - получение новой биологически активной соли соединения, обладающей активностью на гистаминовых рецепторах 3 типа (Н3-рецепторах). 3 н. и 8 з.п. ф-лы, 1 табл., 3 ил.
1. Тозилатная соль транс-N-этил-3-фтор-3-[3-фтор-4-(пирролидин-1-илметил)-фенил]-циклобутанкарбоксамида формулы (1)
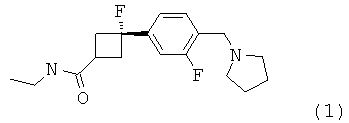
2. Тозилатная соль по п.1, имеющая картину дифракции рентгеновских лучей, характеризующуюся по существу пиком картины дифракции рентгеновских лучей, как измерено с использованием медного (Kα1=1,54056, Кα2=1,54439) излучения, при 2Ө 8,959±0,2.
3. Тозилатная соль по п.1, имеющая картину дифракции рентгеновских лучей, характеризующуюся по существу пиком картины дифракции рентгеновских лучей, как измерено с использованием медного (Kα1=1,54056, Кα2=1,54439) излучения, при 2Ө 17,991±0,2.
4. Тозилатная соль по п.1, имеющая картину дифракции рентгеновских лучей, характеризующуюся по существу пиком картины дифракции рентгеновских лучей, как измерено с использованием медного (Kα1=1,54056, Kα2=1,54439) излучения, при 2Ө 21,054±0,2.
5. Тозилатная соль по п.1, имеющая картину дифракции рентгеновских лучей, характеризующуюся по существу пиком картины дифракции рентгеновских лучей, как измерено с использованием медного (Kα1=1,54056, Kα2=1,54439) излучения, при 2Ө 22,590±0,2.
6. Тозилатная соль по п.1, имеющая картину дифракции рентгеновских лучей, характеризующуюся по существу пиком картины дифракции рентгеновских лучей, как измерено с использованием медного (Kα1=1,54056, Kα2=1,54439) излучения, при 2Ө 28,050±0,2.
7. Тозилатная соль по п.1, имеющая картину дифракции рентгеновских лучей, характеризующуюся по существу пиком картины дифракции рентгеновских лучей, как измерено с использованием медного (Kα1=1,54056, Кα2=1,54439) излучения, при 2Ө 15,515 (±0,2).
8. Тозилатная соль по п.1, имеющая картину дифракции рентгеновских лучей, характеризующуюся по существу пиками картины дифракции рентгеновских лучей, как измерено с использованием медного (Kα1=1,54056, Кα2=1,54439) излучения, при 2Ө (±0,2): 8,959, 15,515, 17,991, 21,054, 22,590 и 28,050.
9. Тозилатная соль по п.1, где соль является безводной.
10. Фармацевтическая композиция, обладающая активностью на гистаминовых рецепторах 3 типа (Н3-рецепторах), содержащая тозилатную соль по любому из пп.1-9 и фармацевтически приемлемый носитель.
11. Способ лечения депрессии, расстройств настроения, шизофрении, тревожных расстройств, когнитивных расстройств, болезни Альцгеймера, синдрома дефицита внимания (ADD), синдрома дефицита внимания с гиперактивностью (ADHD), психотических расстройств, расстройств сна, ожирения, головокружения, эпилепсии, болезни движения, респираторных заболеваний, аллергии, индуцированных аллергией реакций дыхательных путей, аллергического ринита, заложенности носа, аллергической гиперемии, гиперемии, гипотензии, сердечно-сосудистого заболевания, заболеваний желудочного кишечного тракта (ЖКТ), гипер- и гипокинезии и секреции кислоты в желудочно-кишечном тракте у млекопитающего, включающий введение субъекту, нуждающемуся в лечении, терапевтически эффективного количества тозилатной соли по п.1.
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| RU 2005134006 A, 10.04.2006. | |||
Авторы
Даты
2011-09-27—Публикация
2008-01-10—Подача