Область техники
Настоящее изобретение, в основном, относится к лечению рака и, в частности, к применению противораковых средств на основе полимеров при таком лечении рака.
Предпосылки изобретения
Рак представляет собой класс заболеваний, характеризующихся неконтролируемым делением клеток и способностью этих клеток распространяться или путем направленного роста внутрь примыкающей ткани посредством инвазии, или путем имплантации в отдаленные участки тела при помощи метастазов.
На сегодняшний день рак является основной причиной смерти у человека, и число пораженных болезнью индивидуумов возрастает с каждым годом. Хотя различные способы лечения рака, например химиотерапия, эндокринная терапия, лучевая терапия и хирургическое вмешательство, были чрезвычайно улучшены за последние десять лет, они далеки от совершенства с точки зрения результата для различных типов злокачественных опухолей. Кроме того, некоторые из известных способов лечения рака обладают недостатками в виде высокой стоимости лечения, побочных эффектов и страдания пациентов и относительной неэффективности. По этим причинам проводится обширное исследование для обнаружения альтернативных или дополнительных форм лечения рака.
Документ [1] раскрывает применение неферментируемых осмотических слабительных средств в качестве активных веществ для получения лекарственного препарата для лечения колоректального рака и/или рака прямой кишки. Примером такого слабительного средства является PLURONIC® F68, доступный от BASF Corporation. Эти соединения обладают слабительными и гелеобразующими свойствами. Соединения притягивают и удерживают воду внутри толстой кишки благодаря своим физико-химическим свойствам и способны увеличивать выведение фекалий без тканей. Предполагают, что слабительные, неферментируемые, осмотические и водоудерживающие свойства соединений оказывают защитное действие в отношении двух конкретных типов рака, колоректального рака и рака прямой кишки.
В документе [2] обсуждается способность циркулирующих опухолевых клеток развиваться в метастазы, где эта способность основана на свойственном физико-химическом прилипании к эндотелию и образовании микроскопления. Описано, что вещества, препятствующие процессу коагуляции, могли бы быть использованы для предотвращения опухолевых метастазов. Предлагаемые вещества включают гепарин, варфарин натрия и PLURONIC® F68. Эти вещества можно использовать в сочетании с хирургическим вмешательством для предотвращения метастазов, образующихся после оперативной манипуляции с опухолью.
Краткое описание изобретения
Настоящим изобретением преодолеваются эти и другие недостатки предшествующих мер.
Основной задачей настоящего изобретения является создание лекарственного средства на основе полимеров, которое может быть использовано для лечения или предупреждения рака.
Другой задачей настоящего изобретения является создание лекарственного средства на основе полимеров, которое уменьшает скорость пролиферации раковых клеток.
Эти и другие задачи соответствуют изобретению, что определено пунктами прилагаемой формулы изобретения.
Кратко, настоящее изобретение относится к применению неожиданного противоракового эффекта амфифильных блок-сополимеров. Эти сополимеры представляют собой эффективные химиотерапевтические средства против разнообразных видов рака и обладают эффектом уменьшения скорости пролиферации раковых клеток.
Амфифильные блок-сополимеры по настоящему изобретению предпочтительно содержат одну гидрофобную полимерную цепь, соединенную с, по меньшей мере, двумя гидрофильными боковыми цепями. Гидрофобная полимерная цепь предпочтительно является основной цепью, у которой первый конец соединен с, по меньшей мере, одной, предпочтительно одной или двумя гидрофильными боковыми цепями, и у которой второй конец соединен с, по меньшей мере, одной, предпочтительно одной или двумя гидрофильными боковыми цепями. Предпочтительные амфифильные блок-сополимеры представляют собой сополимеры, имеющие структуру (I)
HO-(CH2CH2O)n-(CH2CHCH3O)m-(CH2CH2O)P-H (I)
Таким образом, сополимеры с основной полимерной цепью пропиленоксида, фланкированного боковыми цепями этиленоксида, являются предпочтительными. Кроме того, n предпочтительно равно p. Такие сополимеры доступны под торговым названием PLURONIC® от BASF Corporation.
Предпочтительно такие сополимеры PLURONIC® по изобретению представляют собой сополимеры, которые имеют среднее содержание этиленоксида, по меньшей мере, 40% масс./масс. и предпочтительно среднее содержание этиленоксида меньше 80% масс./масс. Среднее содержание пропиленоксида в амфифильном блок-сополимере составляет, предпочтительно, по меньшей мере, 2000 г/моль, более предпочтительно, по меньшей мере, 3000 г/моль, такое как примерно 4000±500 г/моль. Примером предпочтительного сополимера является PLURONIC® F127, имеющий среднюю молекулярную массу 12600 г/моль, среднее содержание этиленоксида 73,2±1,7% и температуру плавления 56°C.
Авторами изобретения, на удивление, обнаружено, что эти сополимеры оказывают противораковое действие с точки зрения ослабления или ингибирования пролиферации или скорости роста раковых клеток и уменьшения синтеза ДНК раковых клеток. Этот удивительный эффект, по меньшей мере, частично может быть обусловлен действием сополимеров в связывании с клеточными мембранами и блокировании связывания различных факторов роста со своими соответствующими рецепторами на мембране.
Фармацевтическая композиция по изобретению предпочтительно содержит один амфифильный блок-сополимер по изобретению или смесь из, по меньшей мере, двух таких сополимеров в качестве единственных химиотерапевтических средств.
Краткое описание чертежей
Изобретение вместе с дальнейшими задачами и их преимуществами может быть наилучшим образом осмыслено со ссылкой на следующее описание, взятое вместе с сопровождающими чертежами, на которых:
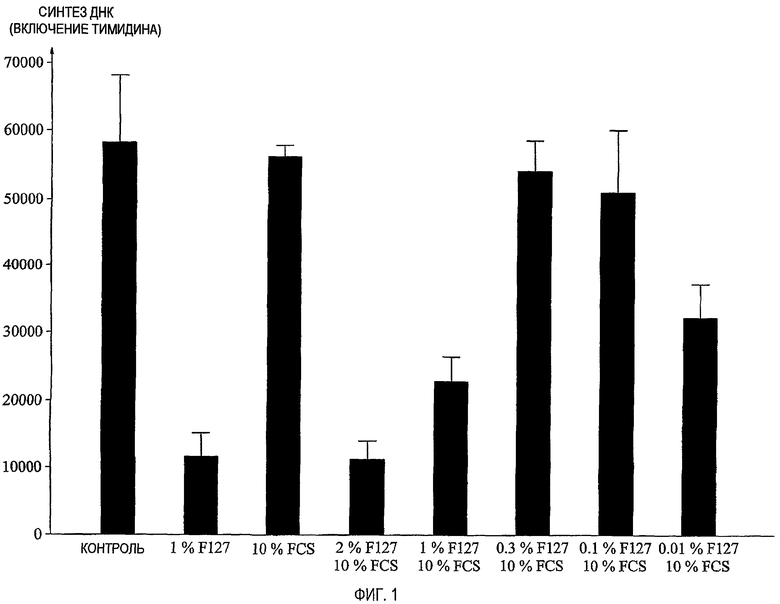
фиг.1 представляет собой диаграмму, демонстрирующую действия PLURONIC® F127 на скорость роста клеток линии MCF-7 рака молочной железы человека;
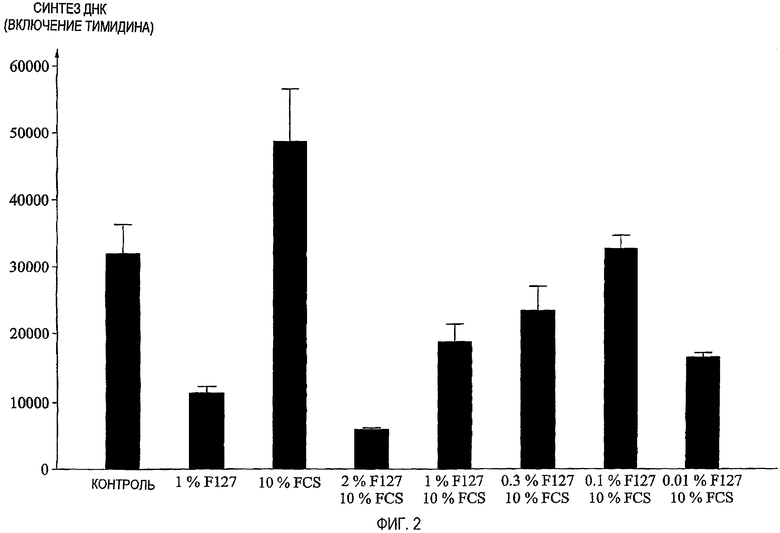
фиг.2 представляет собой диаграмму, демонстрирующую действия PLURONIC® F127 на скорость роста клеток линии SK-BR-3 рака молочной железы человека;
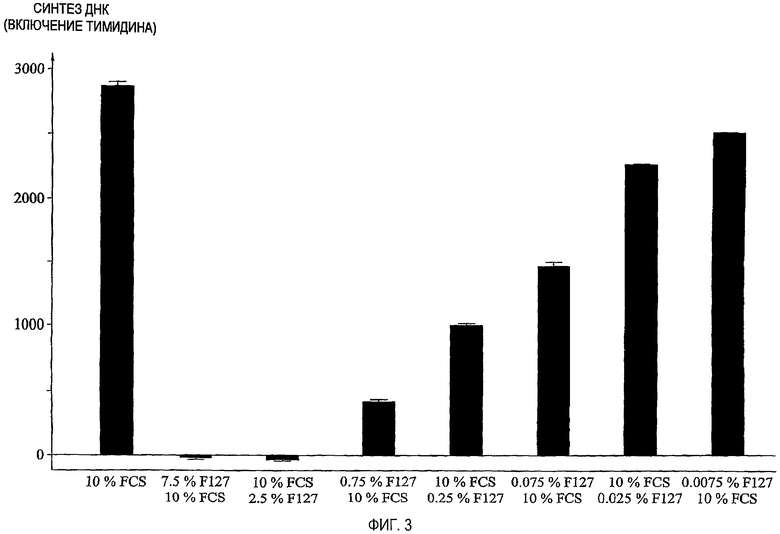
фиг.3 представляет собой диаграмму, демонстрирующую действия PLURONIC® F127 на скорость роста FCS-стимулированных клеток васкулярной гладкой мышцы человека;
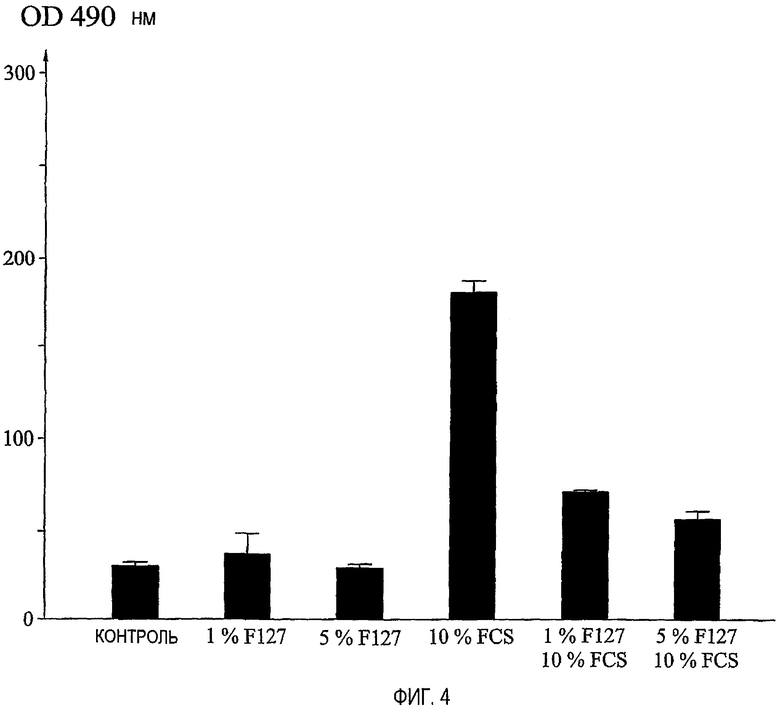
фиг.4 представляет собой диаграмму, демонстрирующую действия PLURONIC® F127 на скорость роста нестимулированных и FCS-стимулированных клеток аортальной гладкой мышцы крысы;
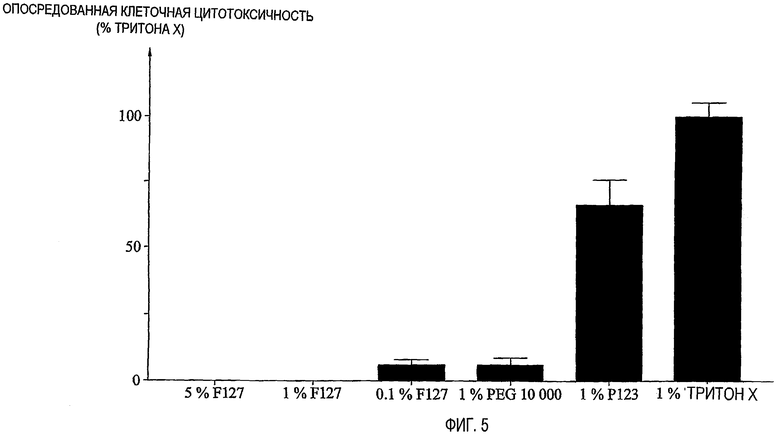
фиг.5 представляет собой диаграмму, иллюстрирующую сравнение опосредованной клеточной цитотоксичности PLURONIC® F127 и Triton X-100;
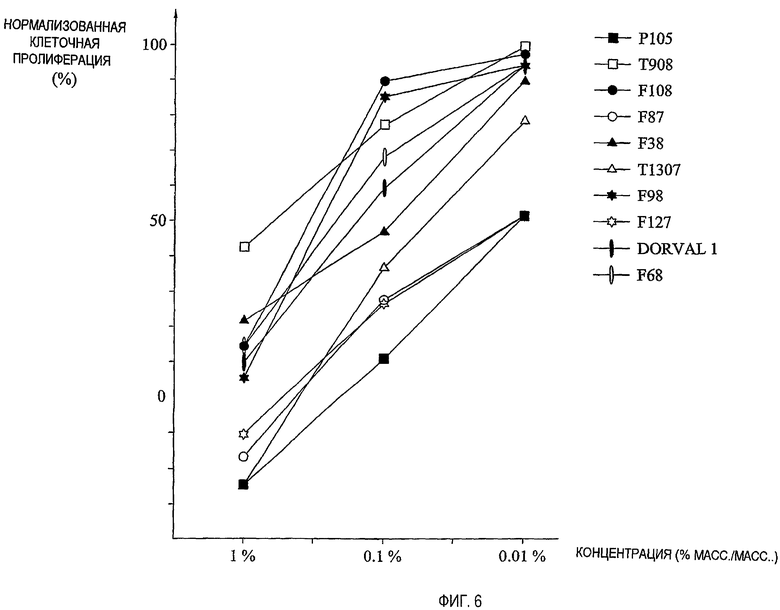
фиг.6 представляет собой график, иллюстрирующий относительный эффект ингибирования клеточного роста различными амфифильными блок-сополимерами на FCS-стимулированных васкулярных гладкомышечных клетках человека;
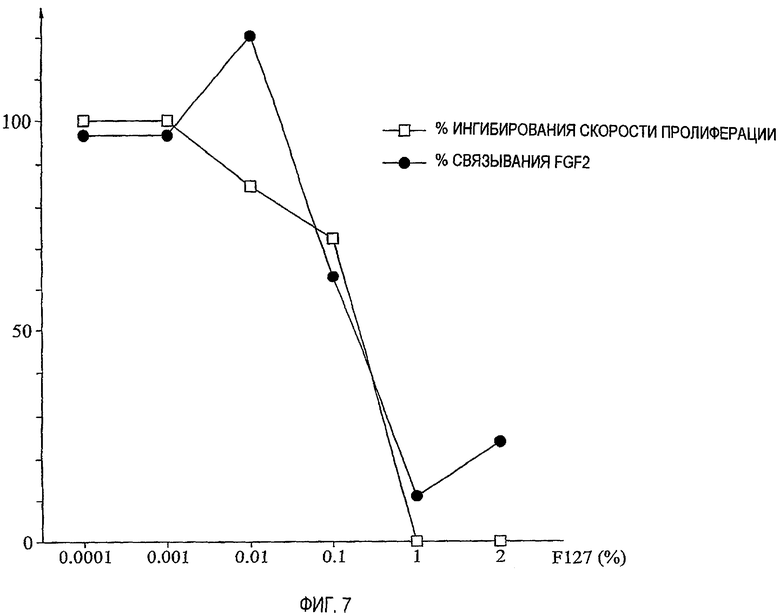
фиг.7 представляет собой график, иллюстрирующий сопоставление ингибирования PLURONIC® F127 скорости роста на стимулированных клетках аортальной мышцы крысы и действия PLURONIC® F127 в блокировании связывания фактора роста фибробластов с рецепторами на гладкомышечных клетках;
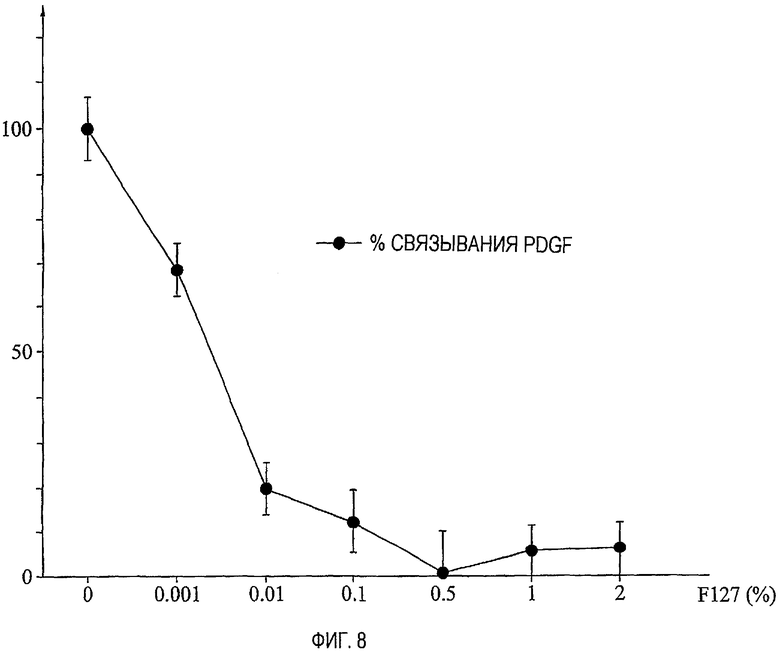
фиг.8 представляет собой график, иллюстрирующий действие PLURONIC® F127 на блокирование связывания тромбоцитарного фактора роста с рецепторами на клетках аортальной гладкой мышцы крысы;
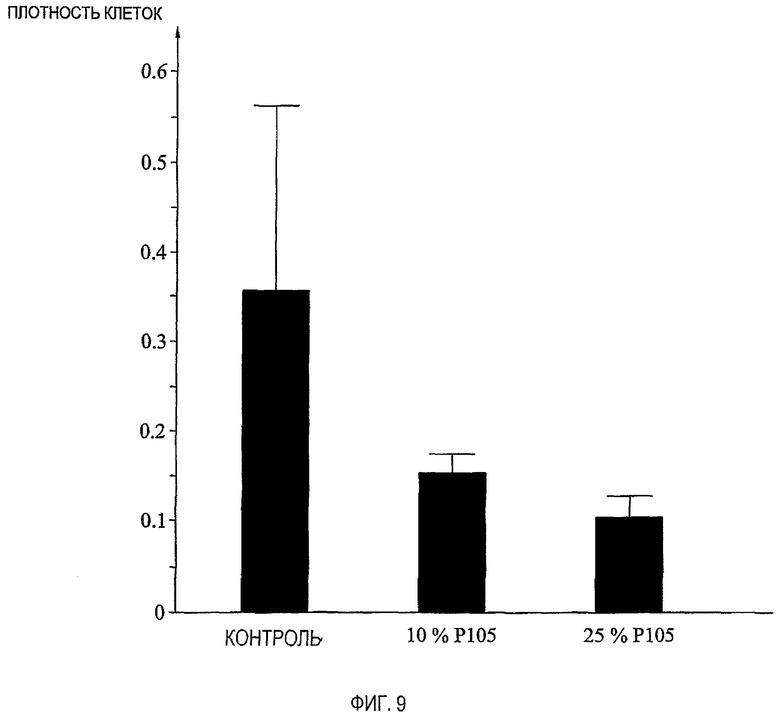
фиг.9 представляет собой диаграмму, демонстрирующую плотность клеток в имплантированном мыши полом волокне с раковыми клетками U937/gtb с обработкой PLURONIC® P105 или без нее;
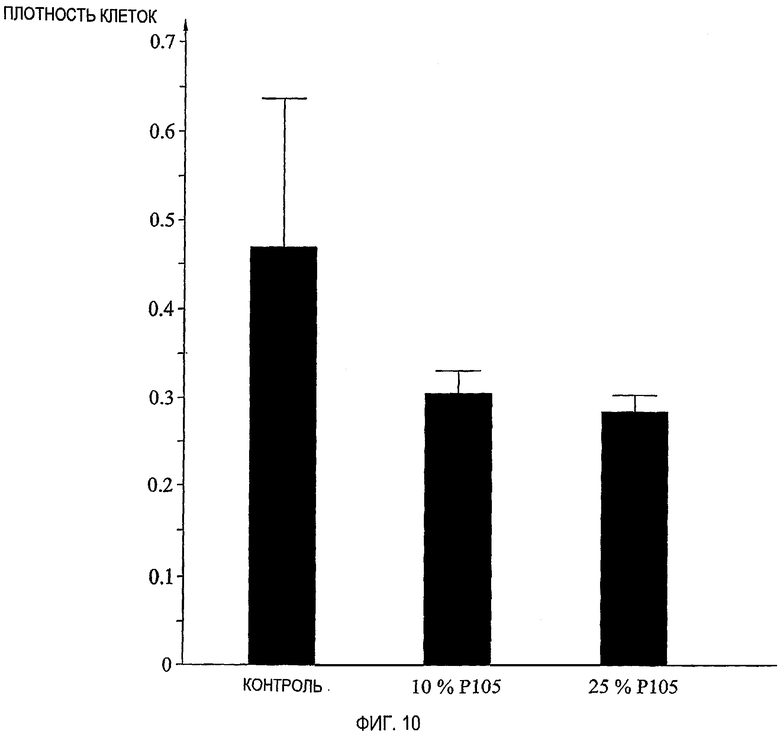
фиг.10 представляет собой диаграмму, демонстрирующую плотность клеток в имплантированном мыши полом волокне с раковыми клетками Н69 с обработкой PLURONIC® P105 или без нее;
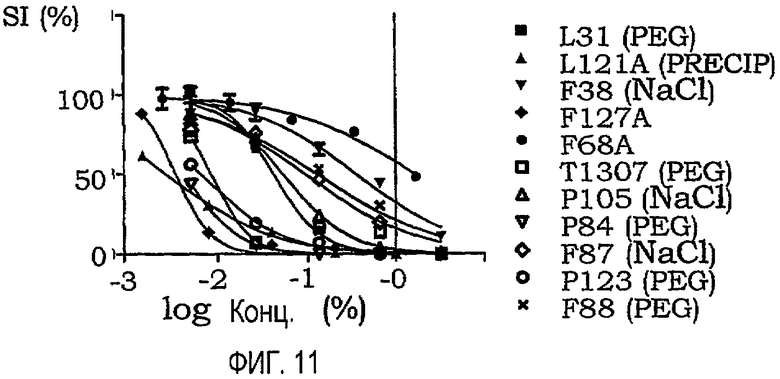
фиг.11 представляет собой график, иллюстрирующий индекс выживаемости раковых клеток U937/gtb, подвергнутых воздействию различных амфифильных блок-сополимеров;
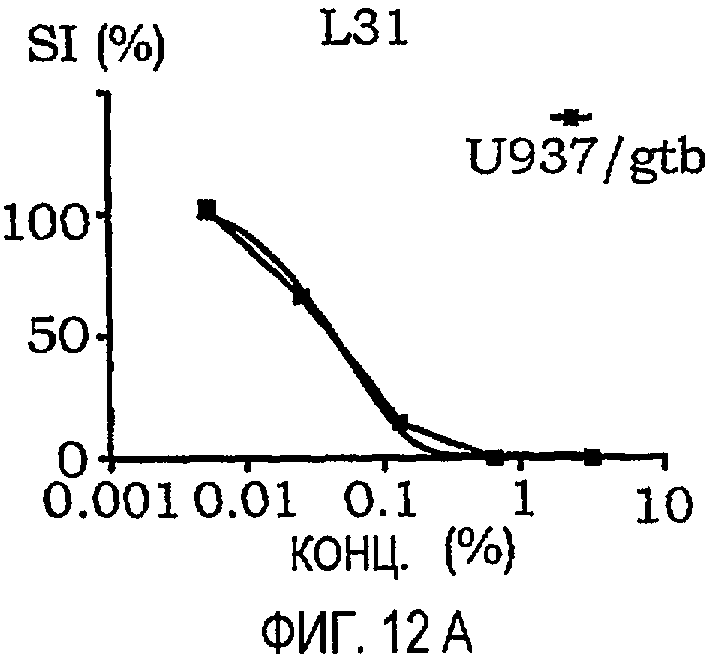
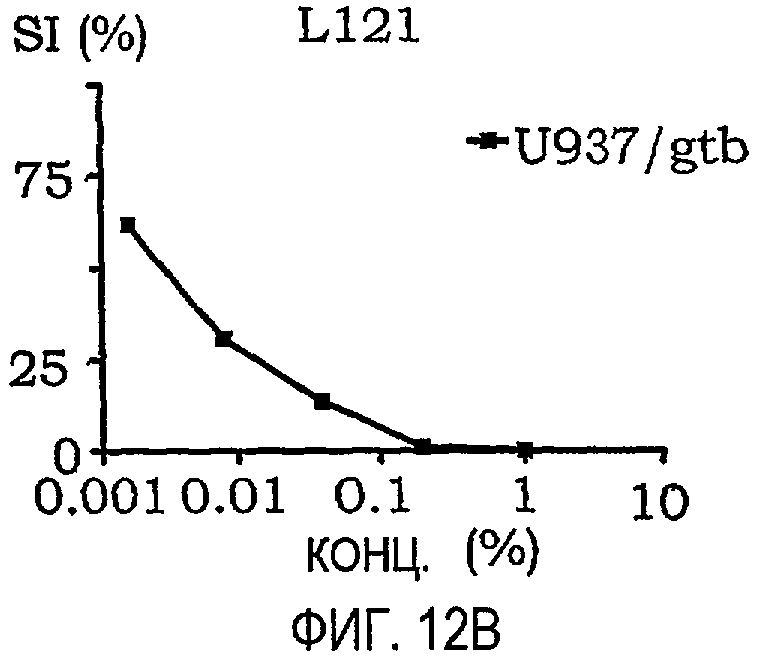
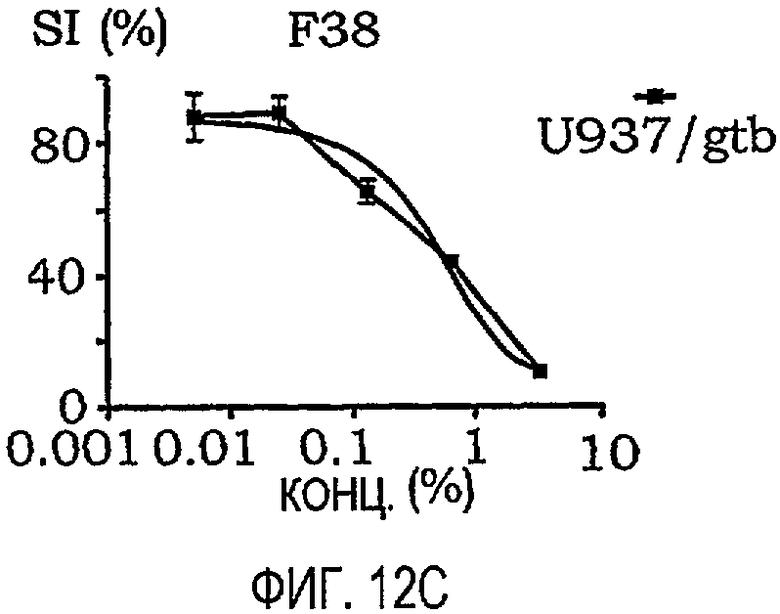
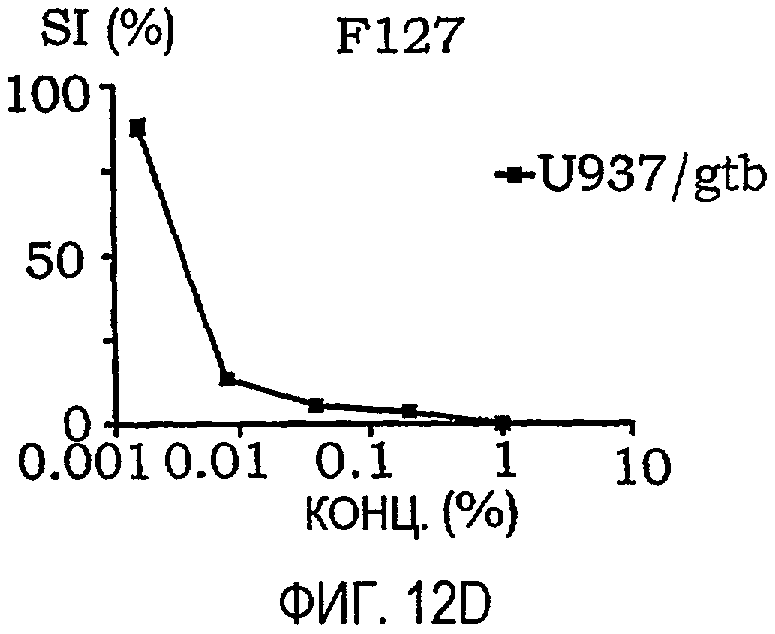
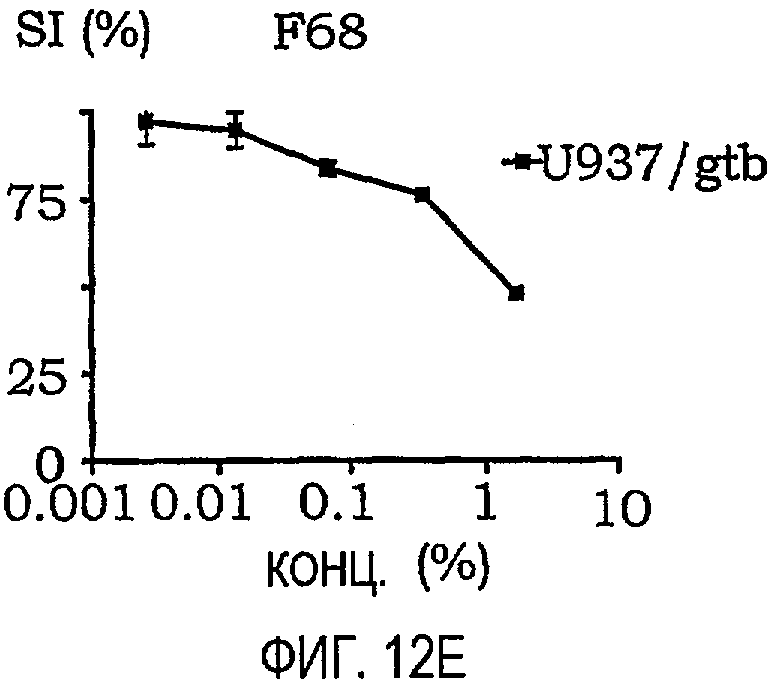
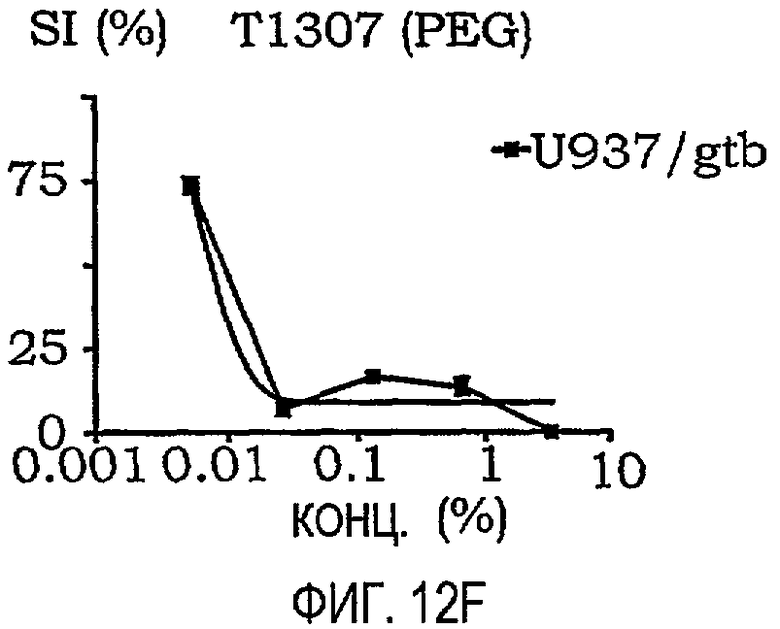
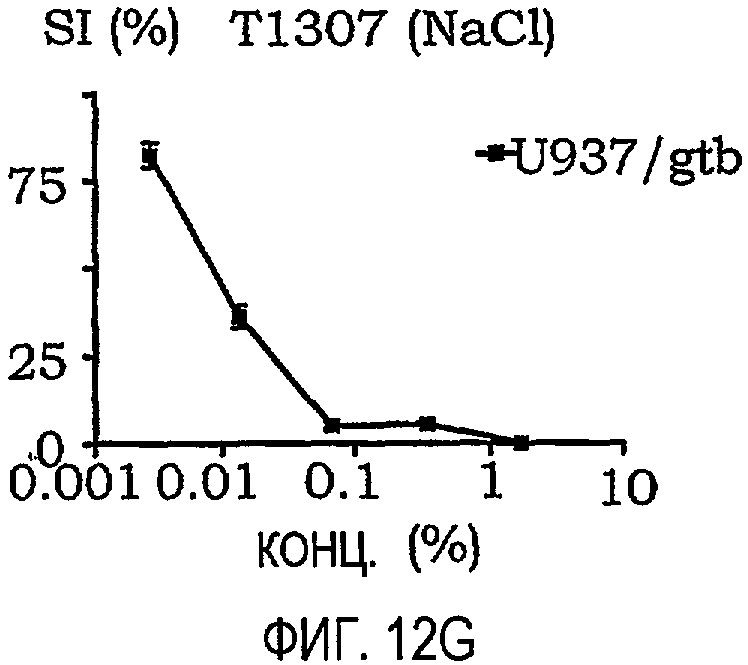
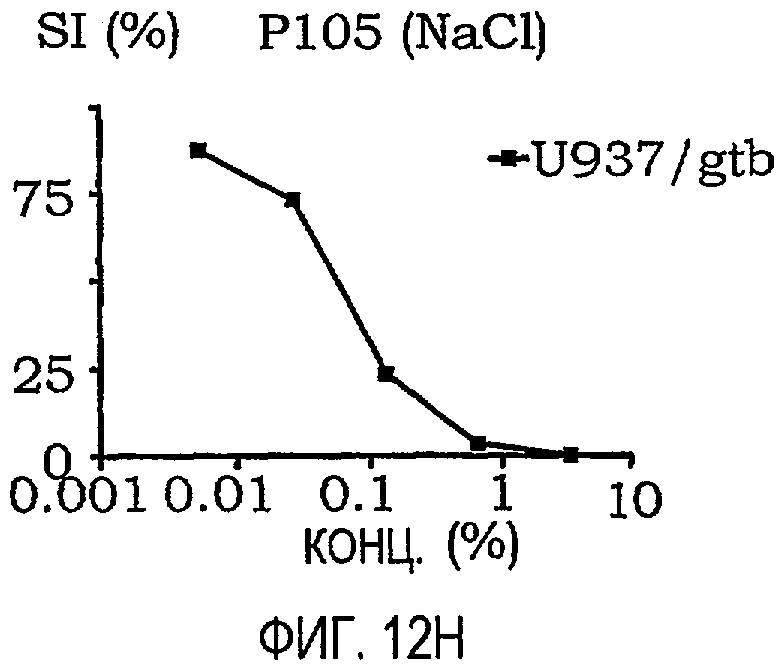
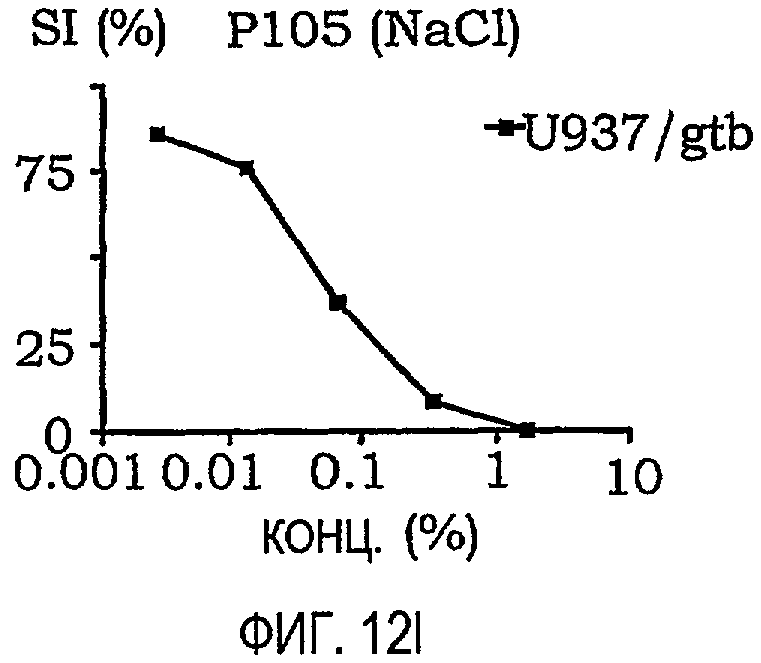
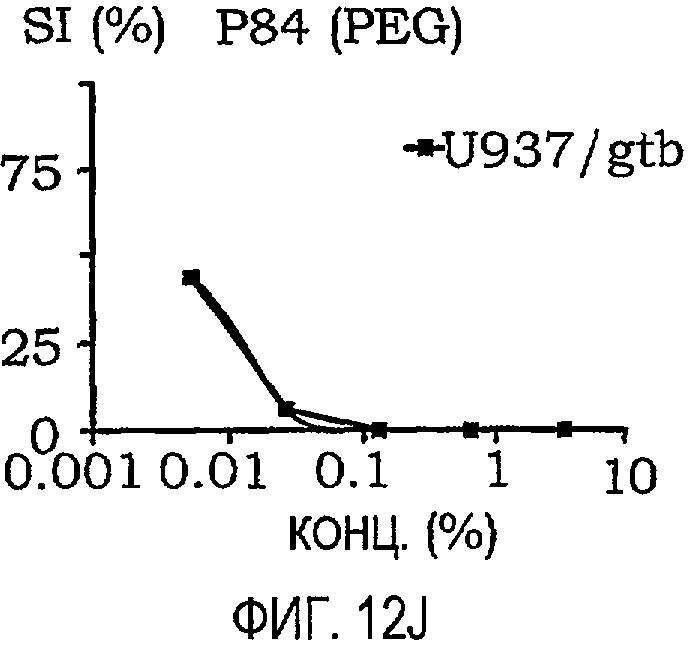
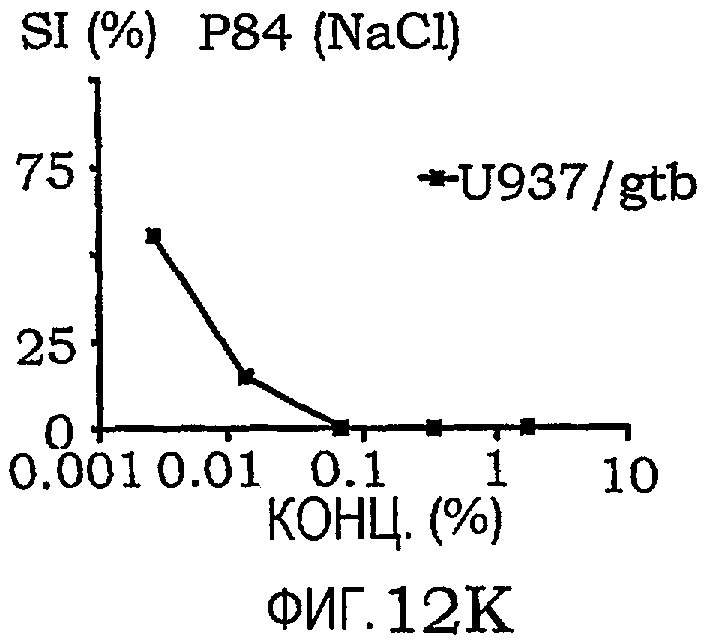
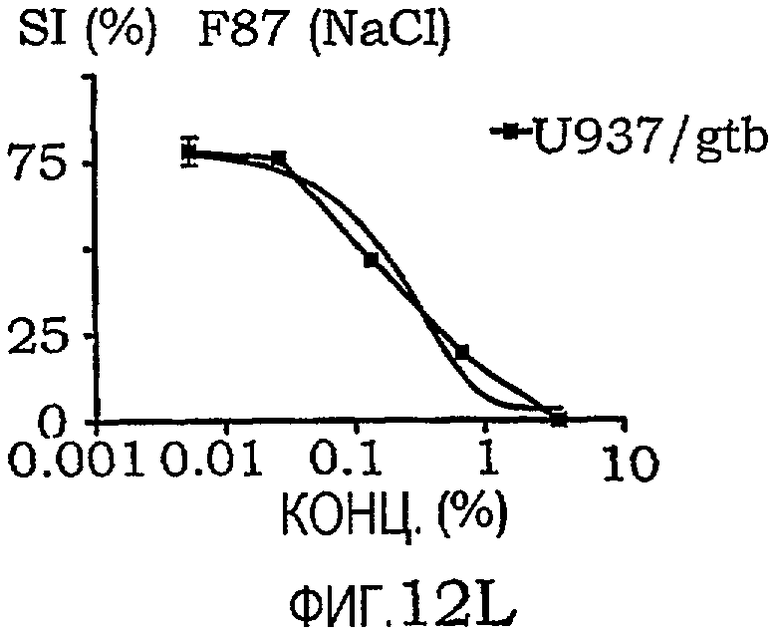
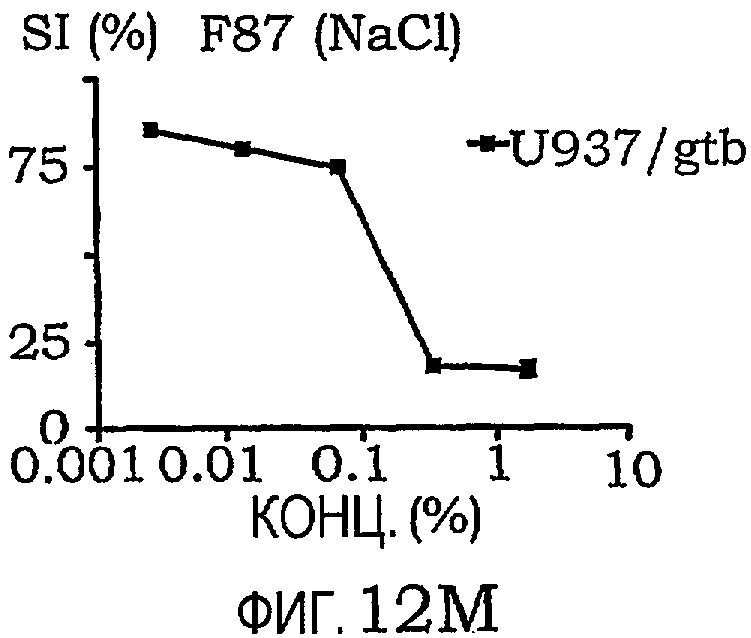
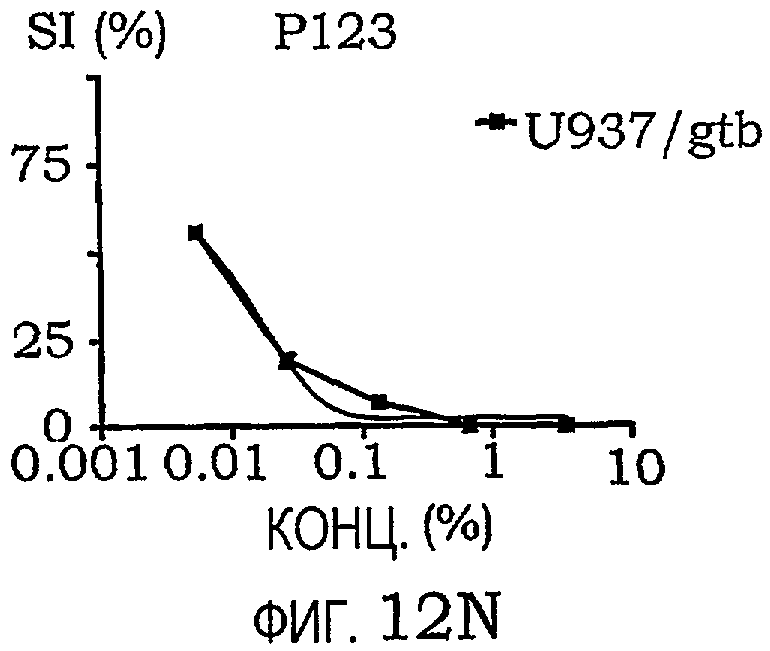
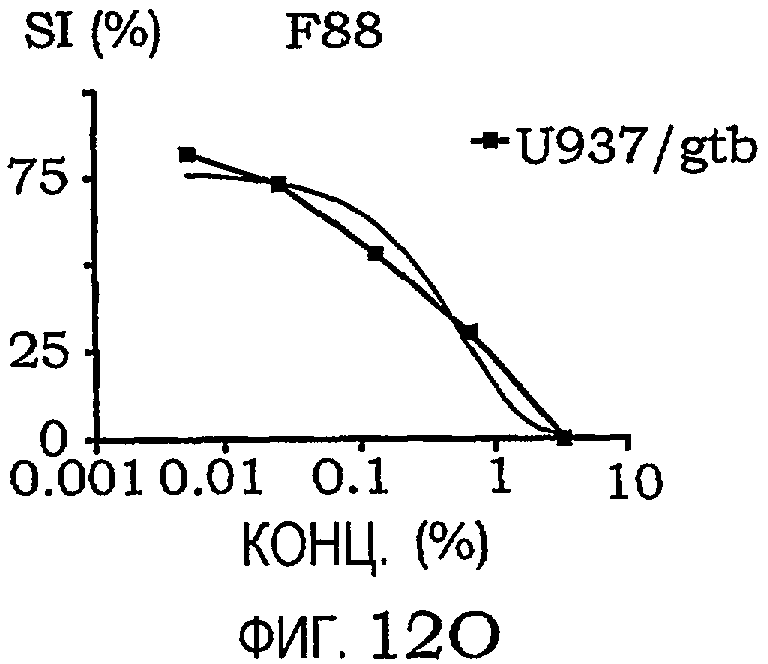
фиг.12A-12O представляют собой графики, иллюстрирующие индекс выживаемости раковых клеток U937/gtb, подвергнутых воздействию различных амфифильных блок-сополимеров; и
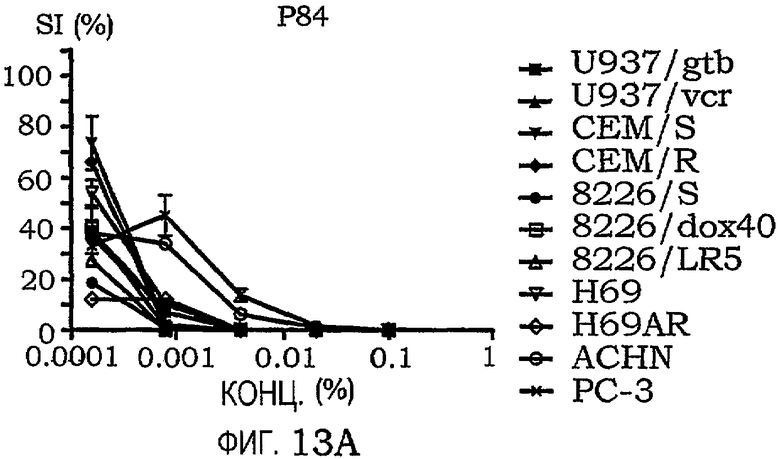
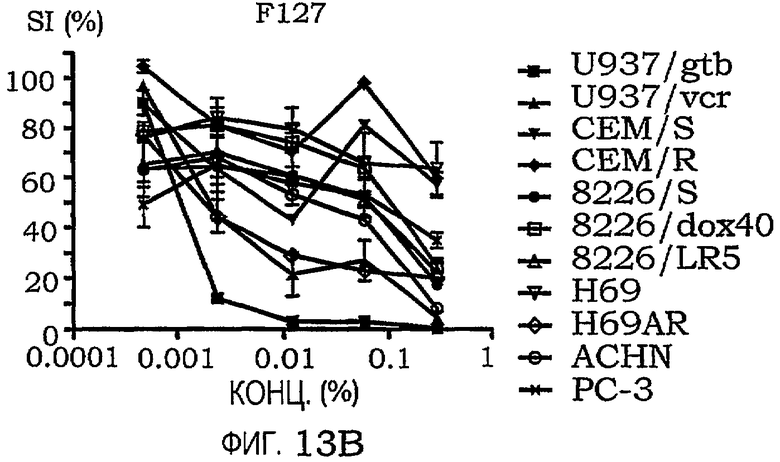
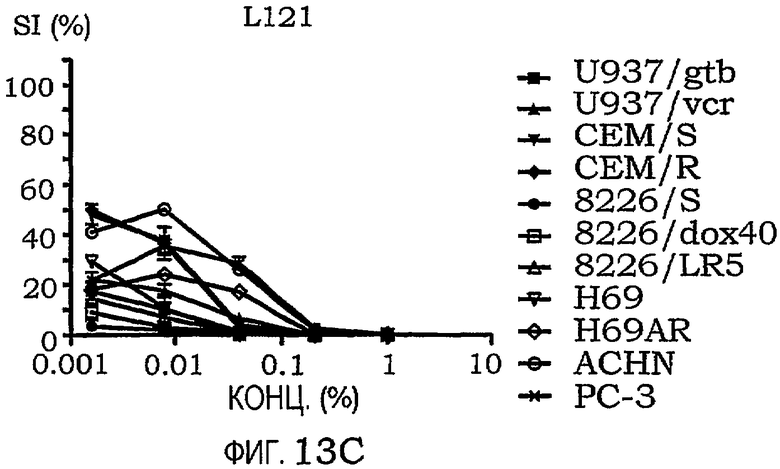
фиг.13A-13С представляют собой графики, иллюстрирующие индекс выживаемости различных линий раковых клеток, подвергнутых воздействию PLURONIC® P84, F127 или L121.
Подробное описание изобретения
Настоящее изобретение, в основном, относится к лечению рака и, в частности, к применению амфифильных блок-сополимеров для ингибирования и уменьшения скорости роста и пролиферации раковых клеток.
Активные противораковые соединения по настоящему изобретению представляют собой амфифильные блок-сополимеры гидрофобных и гидрофильных мономеров. Блок-сополимеры, таким образом, содержат, по меньшей мере, одну растворимую в воде (гидрофильную) часть и, по меньшей мере, одну менее растворимую в воде или даже нерастворимую в воде (гидрофобную) часть. У предпочтительных в настоящее время блок-сополимеров основная гидрофобная цепь окружена, по меньшей мере, двумя гидрофильными боковыми цепями. Более предпочтительно, у основной гидрофобной цепи первый конец цепи соединен с, по меньшей мере, одной, предпочтительно одной или двумя гидрофильными боковыми цепями, и второй конец цепи соединен с, по меньшей мере одной, предпочтительно одной или двумя гидрофильными боковыми цепями. Приведенные ниже формулы (II) и (III) схематически иллюстрируют такие предпочтительные амфифильные блок-сополимеры
X-Y-Z (II)
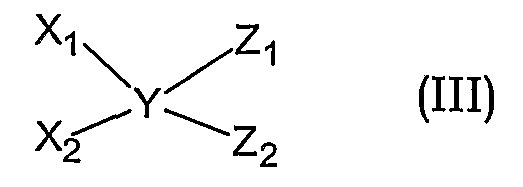
где X, X1, X2 и Z, Z1, Z2 представляют соответствующие гидрофильные боковые цепи и Y представляет гидрофобную основную цепь. В предпочтительном варианте осуществления X=Z, и X1=X2, Z1=Z2, и более предпочтительно X1=X2=Z1=Z2.
В предпочтительном варианте осуществления амфифильные блок-сополимеры по настоящему изобретению представляют собой блок-сополимеры этиленоксида и пропиленоксида. Несколько различных таких сополимеров сегодня доступны от различных производителей, включая полимеры PLURONIC® и TETRONIC® от BASF Corporation.
Кратко, PLURONIC® представляет собой сополимер этиленоксида (EO) и пропиленоксида (PO) общей структуры (III):
(EO)n-(PO)m-(EO)p (IV)
или более подробной структуры (I):
HO-(CH2CH2O)n-(CH2CHCH3O)m-(CH2CH2O)P-H (I)
В предпочтительном варианте осуществления n=p.
В приведенной ниже таблице I перечислено несколько полимеров PLURONIC®, доступных от BASF, которые могут быть использованы в соответствии с настоящим изобретением.
Сополимеры PLURONIC®
** Вязкость по Брукфилду при 60°C
*** Вязкость по Брукфилду при 77°C
Как известно в данной области, буквенное обозначение названия продукта PLURONIC® указывает физическую форму продукта при 25°C, где “L” представляет жидкую, “P” представляет пастообразную и “F” представляет твердую форму. Первая цифра или две первые цифры в трехзначном наименовании продукта, умноженные на 300, указывают приблизительную молекулярную массу гидрофобной основной полипропиленоксидной цепи. Последняя цифра, умноженная на 10, указывает приблизительное содержание этиленоксида (в %) в полимере. Это процентное содержание этиленоксида можно вычислить по формуле (1)
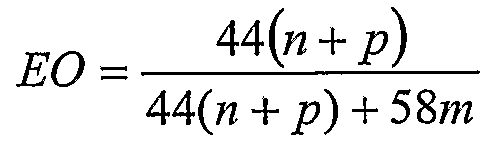 (1)
(1)
где m, n и p определены в структуре (I).
Если гидрофобная или липидная растворимая часть (PO) слишком сильно уменьшена, т.е. m представляет собой небольшое целое число, эффект ингибирования роста заметно уменьшается. Как следствие, предпочтительными сополимерами PLURONIC® по настоящему изобретению поэтому являются сополимеры, которые имеют гидрофобную часть, которая составляет, по меньшей мере, примерно 2000 г/моль, т.е. те полимеры PLURONIC® из таблицы I, которые имеют три цифры в названии продукта или где первая цифра в названии продукта больше шести.
Кроме того, сополимеры PLURONIC® с высоким гидрофильным содержанием, т.е. с приблизительным содержанием этиленоксида примерно 80% или более, обладают, что было также показано, наименее эффективным противораковым действием из исследованных сополимеров. Эти сополимеры имеют последнюю цифру 8 в названии продукта в таблице I.
Если содержание этиленоксида в блок-сополимере является слишком низким по отношению к содержанию пропиленоксида, то сополимер слаборастворим или даже нерастворим в воде. Такие блок-сополимеры могут быть менее полезны для клинического применения, поскольку в этом случае необходимо использовать растворитель не на основе воды.
Более того, если каждое значение m, n и p в структуре (I) является слишком маленьким, таким как L31, L42, L43, L44, L61, L62 и L63, т.е. близкородственным гидрофобным блок-сополимером, то полимер становится токсичным как для раковых, так и для нераковых клеток. Как следствие, для таких сополимеров необходимо использовать низкие фармацевтические концентрации.
На данный момент предпочтительные примеры сополимеров PLURONIC® включают F127, P84, P105, P123, F87 и L121 и, в частности, F127.
Были проведены эксперименты, в которых удаляли одну из гидрофильных боковых цепей сополимера PLURONIC®. В этом случае ингибиторный эффект заметно уменьшается или даже отсутствует. Как следствие, предпочтительные амфифильные сополимеры по настоящему изобретению содержат, по меньшей мере, две гидрофильные (полиэтиленоксидные) цепи, соединенные с гидрофобной (полипропиленоксидной) цепью.
Другие родственные сополимеры, которые можно использовать в соответствии с изобретением, представляют собой полимеры TETRONIC®, также доступные от BASF Corporation. Эти сополимеры можно представить следующей структурой (V):
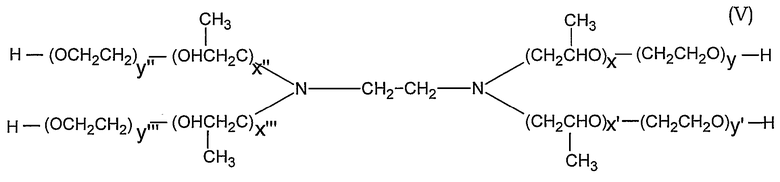
В приведенной ниже таблице II перечислены некоторые свойства доступных полимеров TETRONIC®.
Сополимеры TETRONIC®
** Вязкость по Брукфилду при 60°C
*** Вязкость по Брукфилду при 77°C
Из этих сополимеров TETRONIC® наиболее предпочтительным на данный момент является амфифильный сополимер TETRONIC® 1307 по настоящему изобретению. Сополимер 1307 обладает эффективным противораковым действием, несмотря на то, что является растворимым в воде и относительно нетоксичным для непролиферирующих клеток.
Другие амфипатические (амфифильные) блок-сополимеры также можно использовать в соответствии с изобретением. Например, сополимер, имеющий основную полистирольную цепь, соединенную с соответствующей боковой цепью полиэтиленоксида, обладает эффектом ингибирования роста. Таким образом, настоящее изобретение также охватывает другой амфифильный блок-сополимер помимо тех, которые содержат полиэтиленоксидную цепь и несколько полиэтиленоксидных боковых цепей.
BASF Corporation также располагает другими родственными амфифильными блок-сополимерами, которые родственны сополимерам PLURONIC® и TETRONIC®. PLURONIC® R представляет собой сополимер, у которого этиленоксид и пропиленоксид меняются местами по сравнению с PLURONIC®. Другими словами, полимер имеет следующую общую структуру:
HO-(CH2CHCH3O)k-(CH2CH2O)q-(CH2CHCH3O)r-H (VI)
В таблице III перечислены доступные такие сополимеры.
Сополимеры PLURONIC® R
Соответственно сополимеры, у которых этиленоксид и пропиленоксид в TETRONIC® меняются местами, обозначены как полимеры TETRONIC® R. В таблице IV перечислены такие полимеры, доступные от BASF Corporation.
Сополимеры TETRONIC® R
Следует отметить, что когда в данном документе констатируют молекулярную массу сополимеров, то подразумевают среднюю теоретическую молекулярную массу. Как хорошо известно специалисту в данной области, в данной группе конкретных сополимеров не все полимерные молекулы имеют идентичную длину полимера и молекулярную массу. Таким образом, данная молекулярная масса является средним значением и представляет собой распределение вокруг этого среднего значения. Такие же рассуждения о распределении вокруг среднего значения применимы к гидрофильности сополимера, что выражается, например, средним содержанием этиленоксида в полимере.
Сополимеры по изобретению являются эффективными ингибиторами роста злокачественных опухолей in vitro даже при очень низких дозах. Более того, эффект ингибирования роста более выражен на быстрорастущих раковых клетках по сравнению с медленно растущими раковыми клетками. Кроме того, по меньшей мере, некоторые из амфифильных блок-полимеров по настоящему изобретению не обладают какими-либо функциями, влияющими на пролиферацию нераковых клеток, несмотря на стимулирование их путем добавления различных факторов роста.
Сополимеры можно использовать для уменьшения и нормализации скорости роста различных типов линий раковых клеток. Более того, представляется, что сополимеры уменьшают высокую пролиферацию до нормальной скорости роста, но не более. Как следствие, нераковые клетки не будут подвергаться воздействию, поскольку они пролиферируют уже с низко нормальной скоростью роста.
После того как скорость роста раковых клеток уменьшилась, иммунную систему пациента (человека) можно более эффективно регулировать и бороться с раковыми клетками для уничтожения злокачественной опухоли.
Сополимеры по настоящему изобретению могут также оказывать эффект по предотвращению или, по меньшей мере, уменьшению скорости, с которой мутация возникает в раковых клетках. Установление этого факта является чрезвычайно важным, поскольку это уменьшает риск образования раковых клеток, которые благодаря мутациям являются более склонными к тому, чтобы избежать или противодействовать врожденным механизмам защиты от рака у субъекта.
В соответствии с изобретением амфифильные блок-сополимеры могут быть представлены в виде фармацевтически приемлемых композиций с использованием способов получения, известных специалистам в данной области. Эти композиции могут быть введены стандартными способами. Как правило, сополимеры могут быть введены внутривенно, внутрибрюшинно, подкожно, буккально, ректально, через кожу, через нос, перорально, трахеально, бронхиально, местно, любыми другими парентеральными способами введения или путем ингаляции, в форме фармацевтического препарата, содержащего активный ингредиент в фармацевтически приемлемой лекарственной форме.
На данный момент предпочтительным способом введения является внутривенное введение, при котором фармацевтическая лекарственная композиция содержит амфифильный сополимер по изобретению в растворе выбранного растворителя.
В конкретном осуществлении введения раствор, содержащий сополимер, инъецируют однократно или, предпочтительно, несколько раз субъекту, нуждающемуся в лечении рака. Можно также использовать непрерывную или полунепрерывную подачу лекарственного средства с помощью, например, медицинского насоса или другого оборудования для введения. Возможны также способы введения посредством так называемого медленного высвобождения и в объеме настоящего изобретения.
В другом конкретном осуществлении можно использовать локальное введение в опухоль или в связи с опухолью для обеспечения относительно высокой локальной концентрации активного ингредиента. Такое локальное введение может сопровождаться одним или несколькими системными введениями.
Как правило, композиции получают равномерным и непосредственным объединением активного ингредиента с предпочтительно жидкими носителями, или иногда мелкоизмельченными твердыми носителями, или и с теми, и с другими, а затем, в случае необходимости, формовкой продукта.
Композиции, подходящие для парентерального введения, включают водные и неводные стерильные растворы для инъекций, которые могут содержать антиоксиданты, буферы, бактериостаты и растворы, которые придают композиции изотоничность с кровью предполагаемого реципиента, и водные и неводные стерильные суспензии, которые могут включать суспендирующие средства и загустители. Композиции могут быть представлены в упаковках с единичной дозой или несколькими дозами, например в герметически закрытых ампулах и флаконах, и могут храниться в высушенном сублимацией (лиофилизированном) виде, требующем лишь добавления стерильного жидкого носителя, например воды для инъекций, непосредственно перед использованием.
В частности, для нерастворимых в воде сополимеров по настоящему изобретению при инъекции фармацевтических препаратов помимо водных сред можно использовать другие среды. Примером такой среды является полиэтиленгликоль (PEG). Другие примеры включают эмульсии типа «масло в воде» или «вода в масле». Минеральное масло или другое маслянистое вещество, такое как Drakeol 6VR или Drakeol 5 (Penreco, Butler, PA), можно использовать в качестве масляной фазы эмульсии. Водной фазой может быть физиологический забуференный фосфатом солевой раствор или другой физиологический солевой раствор. Соотношение масла и воды предпочтительно составляет приблизительно от 80:20 до 1:100.
Композиции, подходящие для перорального введения, могут быть представлены в виде капсул, крахмальных капсул или таблеток, каждая из которых содержит заданное количество активного ингредиента, в виде порошка или гранул; в виде раствора, или суспензии, или эмульсии в водной жидкости или неводной жидкости. Композиции, подходящие для местного введения в кожу, могут быть представлены в виде мазей, кремов, гелей и паст, содержащих ингредиент для введения в фармацевтически приемлемом носителе. Композиции для ректального введения могут быть представлены в виде суппозитория с подходящей основой, содержащей, например, масло какао или салицилат. Композиции, подходящие для вагинального введения, могут быть представлены в виде пессариев, тампонов, кремов, гелей, паст, пен или распыляемых композиций, содержащих в дополнение к активному ингредиенту подходящие носители, известные в данной области.
Примерами стандартных дозированных композиций являются композиции, содержащие ежедневную дозу или единицу, ежедневную субдозу, как изложено в данном описании выше, или их соответствующую фракцию, вводимого ингредиента.
Максимально допустимая дозировка, которая может быть использована в соответствии с настоящим изобретением, зависит, наряду с прочим, от токсичности конкретного амфифильного блок-сополимера, его противоракового действия, т.е. эффекта ингибирования скорости роста, и способа введения. Максимально допустимую концентрацию амфифильного сополимера можно оценить на основании исследования токсичности, описанного в разделе примеров настоящего документа. Результат такого исследования токсичности на мышах или каком-либо другом животном можно затем скоррелировать для оценки максимально допустимой концентрации для других животных, включая людей, с использованием методик, хорошо известных в данной области. Например, можно использовать таблицу факторов дозовой конверсии Freireich et al. [17]. Согласно этой таблице факторов конверсии фактор конверсии от мыши к человеку, как предполагают, составляет 1/12, подразумевая, что если максимальная концентрация полимера в X% является допустимой для мышей, то соответствующая расчетная максимальная концентрация для человека составляет X/12%.
Например, исследования токсичности у мыши показали, что максимальную концентрацию полимера примерно 30% масс./масс. можно безопасно инъецировать мыши без каких-либо побочных эффектов. Тогда это должно соответствовать предельной концентрации примерно 2,5% масс./масс. для введения людям. Некоторые из перечисленных выше амфифильных сополимеров по настоящему изобретению, включая PLURONIC®, подвергали испытаниям на клиническом этапе и экстенсивной проверке на токсичность.
Концентрации, используемые для введения полимеров, могут быть определены вне изобретения специалистом в данной области на основе описанных выше методик. Ожидается, что концентрация полимера до 30% масс./масс., такая как до 25, 20, 25 или 10% масс./масс. или до 7,5% масс./масс., предпочтительно от 0,001 до 5% масс./масс., более предпочтительно, по меньшей мере, 0,01% масс./масс., такая как, по меньшей мере, 0,1% масс./масс., может быть подходящей концентрацией.
Подходящими концентрациями могут быть концентрации, которые обеспечивают среднюю концентрацию в крови ниже 5% масс./масс., вероятно, менее чем 2,5% масс./масс. и особенно менее чем 1% масс./масс. Диапазон предпочтительных концентраций составляет от 0,0001% масс./масс. до 1% масс./масс. полимера, например более чем 0,01% масс./масс. или более чем 0,1% масс./масс.
Настоящее изобретение можно использовать применительно к субъектам-животным, предпочтительно субъектам-млекопитающим и более предпочтительно субъектам-людям.
Активные сополимеры по настоящему изобретению могут быть полезными для уменьшения скорости роста опухолей различных раковых линий и типов. Настоящее изобретение применимо при нескольких различных типах злокачественных опухолей, включая, но не ограничиваясь ими, саркому и карциному человека, например фибросаркому, миксосаркому, липосаркому, хондросаркому, остеобластическую саркому, хордому, ангиосаркому, эндотелиальную саркому, лимфангиосаркому, лимфангиоэндотелиальную саркому, синовиому, мезотелиому, опухоль Эвинга, лейомиосаркому, рабдомиосаркому; рак поджелудочной железы, рак молочной железы, рак яичника, рак предстательной железы, плоскоклеточную карциному, базально-клеточную карциному, аденокарциному, карциному потовых желез, карциному сальных желез, папиллярную карциному, папиллярную аденокарциному, цистаденокарциному, медуллярную карциному, бронхогенную карциному, гепатому, карциному желчных протоков, хориокарциному, семиному, эмбриональную карциному, опухоль Вилмса, рак шейки матки, тестикулярную опухоль, карциному легкого, мелкоклеточную карциному легкого, карциному мочевого пузыря, эпителиальную карциному, глиому, астроцитому, медуллобластому, краниофарингиому, эпендимому, гемангиобластому, олигодендроглиому, меланому, нейробластому и ретинобластому, лейкемию, например, острый лимфоцитарный лейкоз (ALL) и острую миелоцитарную лейкемию (миелобластный, промиелоцитарный, миеломоноцитарный, моноцитарный эритролейкоз), хроническую лейкемию (хронический миелоцитарный лейкоз, хронический гранулоцитарный лейкоз и хронический лимфоцитарный лейкоз), истинную полицитемию, лимфому (болезнь Ходжкина и неходжкинскую лимфому), множественную миелому, макроглобулинемию Вальденстрема и болезнь тяжелых цепей.
Фармацевтическая композиция по настоящему изобретению может включать один из амфифильных блок-сополимеров по изобретению. В альтернативном варианте осуществления композиция содержит смесь, по меньшей мере, двух амфифильных блок-сополимеров по изобретению.
Кроме того, для борьбы со злокачественной опухолью у пациента настоящее изобретение можно использовать в качестве дополнения к другим традиционным способам лечения рака, например облучению, химиотерапии, лечению гормонами и т.д.
Полимеры по изобретению можно успешно использовать в связи с другими химиотерапевтическими лекарственными средствами. В этом случае, по меньшей мере, одно такое химиотерапевтическое лекарственное средство можно вводить одновременно или раздельно по времени с введением, по меньшей мере, одного амфифильного сополимера по настоящему изобретению.
Примеры подходящих химиотерапевтических средств, которые могут быть использованы в связи с сополимерами по изобретению, включают:
- алкилирующие средства, такие как цисплатин, карбоплатин, оксаплатин, мехлоэтамин, циклофосфамид, хлорамбуцил:
- антиметаболиты, такие как метотрексат, азатиоприн, меркаптопурин, тиогуанин, флударабин, пентостатин, кладрибин, 5-фторурацил, флоксуридин, арабинозид цитостина;
- антрациклины, такие как даунорубицин, доксорубицин, эпирубицин, идарубицин, митоксантрон;
- алкалоиды барвинка, такие как винкристин, винбластин, винорелбин, виндезин;
- подофиллотоксин, такой как этопозид, тенипозид;
- таксаны, такие как паклитаксел, доцетаксел; и
- ингибиторы топоизомеразы, такие как иринотекан, топотекан, амсакрин, этопозид, этопозида фосфат, тенипозид.
В данном описании приводится возможное теоретическое объяснение эффекта ингибирования роста амфифильными сополимерами по изобретению. Настоящее изобретение, однако, вообще не связано с этой теорией. Сополимеры являются предпочтительно растворимыми в воде, так что они после введения или in vitro могут достичь и вступить во взаимодействие с раковыми клетками. Гидрофобная часть сополимеров может затем внедряться в клеточную мембрану и связываться в ней. Гидрофильные части препятствуют полному проникновению сополимера в мембрану. Это означает, что сополимеры, как правило, должны быть заякорены в клеточной поверхности. После закрепления в мембране сополимеры могут оказывать свое действие ингибирования клеточного роста различными путями.
Амфифильные сополимеры могут связываться с факторами роста, тем самым, инактивируя их или, по меньшей мере, препятствуя их связыванию с рецепторами роста и активации рецепторов роста в мембранах раковых клеток. Это было обнаружено в экспериментах с одним из амфифильных блок-сополимеров по изобретению, который способен блокировать связывание фактора роста фибробластов 2 (FGF2, также обозначенного как главный FGF) и фактора роста тромбоцитов (PDGF) с соответствующими рецепторами на клеточных мембранах.
Кроме того, амфифильные сополимеры могут блокировать рецепторы роста в мембране и препятствовать образованию этими рецепторами пар между собой, которое часто необходимо для передачи сигнала внутрь клетки.
В дополнение или альтернативно, амфифильные сополимеры могут связываться с рецепторами роста, тем самым, инактивируя их или, по меньшей мере, частично блокируя их, и посредством этого препятствуют факторам роста связываться с рецепторами и активировать их.
Некоторые из амфифильных блок-сополимеров по настоящему изобретению ранее использовали в связи с веществами, препятствующими неоплазии. Например, известно [18], что комбинация выбранного полимера PLURONIC® и полиэтиленоксида может быть использована для уменьшения токсичности веществ, препятствующих неоплазии, и для усиления противораковой активности путем i) повышения стабильности вещества в кровотоке, ii) обеспечения большей растворимости вещества или iii) усовершенствования транспорта вещества через клеточные мембраны. Известно также [19], что блок-сополимеры PLURONIC® воздействуют на некоторые определенные механизмы устойчивости к лекарственным средствам, включая ингибирование транспортеров выведения лекарственных средств, прекращение разрушения лекарственных средств в кислотосодержащих везикулах и ингибирование глутион/глутатион S-трансферазной системы детоксикации. Все эти механизмы устойчивости к лекарственным средствам являются энергозависимыми, и, вследствие этого, расходование ATP, вызванное блок-сополимерами PLURONIC®, в раковых клетках с множественной устойчивостью к лекарственным средствам рассматривается в качестве причины возникновения чувствительности к химиотерапевтическим препаратам, проявившейся в результате совместного введения антрациклиновых антибиотиков и сополимеров PLURONIC®.
Тем не менее, до сих пор нет понимания того, что амфифильные блок-сополимеры, такие как сополимеры PLURONIC®, обладают противораковым действием per se в виде ингибирования скорости пролиферации и роста раковых клеток. Поэтому нет осознания того, что эффективное противораковое лекарственное средство может содержать амфифильный блок-сополимер по настоящему изобретению без каких-либо химиотерапевтических веществ-прототипов и, тем не менее, эффективное для предупреждения или лечения рака.
Первый аспект изобретения относится к фармацевтической композиции, содержащей амфифильный блок-сополимер по настоящему изобретению в качестве средства, препятствующего клеточной пролиферации или клеточному росту. Этот аспект также относится к применению амфифильного блок-сополимера по изобретению для получения лекарственного средства, препятствующего клеточной пролиферации или клеточному росту. Изобретение также охватывает способ регулирования in vitro, а именно уменьшения или даже ингибирования скорости пролиферации или скорости роста клетки, предпочтительно раковой клетки. Этот способ включает контактирование клетки, предпочтительно раковой клетки, с амфифильным блок-сополимером. Амфифильный блок-сополимер предпочтительно добавляют в культуральную среду, используемую для клетки. Дополнительный вариант осуществления относится к способу регулирования in vivo, а именно уменьшения скорости пролиферации или скорости роста клетки, предпочтительно раковой клетки. Способ включает введение фармацевтической композиции по первому аспекту изобретения субъекту, где этот субъект является субъектом-животным, предпочтительно субъектом-млекопитающим и более предпочтительно субъектом-человеком.
Второй аспект изобретения относится к фармацевтической композиции, содержащей амфифильный блок-сополимер по настоящему изобретению в качестве химиотерапевтического средства для лечения или предупреждения рака при условии, что амфифильный блок-сополимер не является PLURONIC® F68 (средняя молекулярная масса 8400 г/моль, среднее содержание этиленоксида 81,8±1,9%, температура плавления 52°C и средняя вязкость по Брукфилду 1000 сП при 77°C, и усредненная химическая структура HO-(CH2CH2O)80-(CH(CH3)CH2O)27-(CH2CH2O)80-H). Другой вариант осуществления относится к применению амфифильного блок-сополимера в качестве химиотерапевтического вещества (активного противоракового вещества) для получения лекарственного средства для лечения или предупреждения рака при условии, что блок-сополимер не является PLURONIC® F68. Этот аспект также относится к способу лечения или предупреждения рака у субъекта, предпочтительно субъекта-млекопитающего и более предпочтительно субъекта-человека. Способ включает введение субъекту фармацевтической композиции по второму аспекту.
Третий аспект изобретения относится к фармацевтической композиции, содержащей амфифильный блок-сополимер по настоящему изобретению для уменьшения или ингибирования скорости роста раковых клеток у субъекта, предпочтительно субъекта-млекопитающего и более предпочтительно субъекта-человека, страдающего раком. Вариант осуществления этого аспекта относится к применению амфифильного блок-сополимера по изобретению для получения лекарственного средства для ингибирования или уменьшения скорости роста раковых клеток у субъекта, страдающего раком. Этот аспект также относится к способу уменьшения скорости роста раковых клеток у субъекта, страдающего раком, где способ включает введение субъекту фармацевтической композиции по третьему аспекту.
Четвертый аспект изобретения относится к фармацевтической композиции, содержащей амфифильный блок-сополимер, представленный формулой (IV)
HO-(CH2CH2O)n-(CH(CH3)CH2O)m-(CH2CH2O)P-H (IV)
где m, n и p являются, каждый, целыми числами, предпочтительно множественными целыми числами, для лечения или предупреждения рака у субъекта, предпочтительно субъекта-млекопитающего и более предпочтительно субъекта-человека, при условии, что рак не представляет собой колоректальный рак или рак прямой кишки. Вариант осуществления предписывает применение амфифильного блок-сополимера, представленного формулой (IV), в качестве химиотерапевтического вещества для получения лекарственного средства для лечения или предупреждения рака у субъекта при условии, что указанный рак не представляет собой колоректальный рак или рак прямой кишки. Этот аспект также относится к способу лечения или предупреждения рака, отличного от колоректального рака и рака прямой кишки у субъекта, путем введения субъекту фармацевтической композиции по четвертому аспекту.
Пятый аспект изобретения относится к способу, включающему in vitro-способ блокирования связывания фактора роста с рецептором фактора роста на клеточной мембране клетки. Способ включает контактирование клетки с амфифильным блок-сополимером по настоящему изобретению.
ПРИМЕРЫ
В экспериментах используют различные амфифильные блок-сополимеры. Полимеры PLURONIC® и TETRONIC® были получены от BASF Corporation. Амфифильный блок-сополимер, обозначенный DORVAL 1, представляет собой вариант полимера PLURONIC®, у которого основная пропиленоксидная цепь заменена на соответствующую полистирольную цепь. Этот блок-сополимер был заказан у Polymer Source Inc., Canada. Сополимер имеет следующую схематичную структуру: (EO)x-(St)y-(EO)x, где x≈70 и y≈27, Mn: PEO(3100)-PSt(2800)-PEO(3100) и Mw/Mn=1,11.
Ингибирование скорости роста раковых клеток молочной железы
Действие PLURONIC® F127 тестировали по клеточному росту линии клеток рака молочной железы человека, культивируемых in vitro. Скорость роста определяли по включению 3H-тимидина. Были проверены энергично растущая клеточная линия рака молочной железы, MCF-7, и более медленно растущая клеточная линия рака молочной железы, SK-BR-3.
Кратко, примерно 3×104 клеток засевали в 24-луночные планшеты для микротитрования в 1,0 мл культуральной среды RPMI (Roswell Park Memorial Institute), дополненной 10% FCS (фетальная сыворотка теленка), инсулином (1 мг/100 мл) и 1% антибиотика, и инкубировали (увлажненный воздух, 5% CO2, 37°C) в течение ночи. После инкубирования в течение ночи среду удаляли вакуумным отсосом с использованием стерильных пипеток Пастера и заменяли на 1,0 мл RPMI с 0,1% FCS на лунку. После инкубирования в течение ночи к клеткам (n=3) добавляли RPMI с различными концентрациями (0,01, 0,1, 0,3, 1 и 2% по массе) модулирующего скорость роста PLURONIC ® F127 и/или 10% FCS. Во все лунки, за исключением контрольных лунок и лунок с 1% F127, также добавляли FCS. Лунки инкубировали примерно 15 часов.
Добавляли 1 мкКи/мл 3H-тимидина (Amersham-Pharmacia Biotech) на лунку и инкубировали в течение 4 часов. В конце отмеченного периода среду удаляли и клетки дважды промывали PBS и фиксировали в охлажденной (4°C) 10% TCA (трихлоруксусной кислоте) в течение 10 минут. TCA затем удаляли и монослои промывали 95% этанолом и сушили на воздухе при комнатной температуре в течение 20 минут.
После этого добавляли 1,0 мл 0,2M NaOH на лунку и инкубировали, по меньшей мере, один час при комнатной температуре для растворения клеток. 1,0 мл содержимого каждой лунки разводили 4 мл сцинтилляционного раствора Highsafe II в сцинтилляционных флаконах на 5 мл. Радиоактивность измеряли при помощи бета-счетчика.
Как можно видеть на фиг.1 и 2, PLURONIC® F127 заметно замедлял рост обеих линий клеток рака молочной железы. Эффект был наиболее отчетливым на быстро растущей злокачественной опухоли (MCF-7), где 1% PLURONIC® F127 уменьшал клеточную пролиферацию приблизительно на 80%. Эффект был также ярко выраженным для SK-BR-3, где рост был уменьшен приблизительно на 60%.
Добавление стимулятора роста FCS увеличивало пролиферацию в SK-BR-3, но не в MCF-7, возможно, из-за того, что MCF-7 сам по себе пролиферирует с максимальной скоростью. В SK-BR-3 действие PLURONIC® F127 возрастало в FCS-стимулированных клетках по сравнению с нестимулированными клетками.
PLURONIC® F127 был эффективен в качестве ингибитора пролиферации даже при наименьшей из тестируемых концентраций (0,01% масс./масс.).
Ингибирование синтеза ДНК у стимулированных гладкомышечных клеток
Описанные выше эксперименты по скорости роста также проводили in vitro на васкулярных гладкомышечных клетках человека, крысы и кролика. Эксперименты подтвердили, что PLURONIC® F127 ингибирует синтез ДНК дозозависимым образом, что определяли по включению тимидина в рост-стимулированные (присутствие 10% FCS) васкулярные гладкомышечные клетки человека, крысы и кролика. Однако PLURONIC® F127 не влиял на скорость роста нестимулированных мышечных клеток.
Кратко, для крупных сосудов, извлеченный сосуд рассекали и эндотелий соскребали скальпелем. Сосуд поворачивали и затем соскребали адвентициальную оболочку. Для более мелких сосудов эндотелий удаляли промыванием просвета сосуда 0,1% Triton X-100 в течение 10 секунд, после чего промывали культуральной средой DMEM (модифицированная Дульбекко среда Игла).
Сосуд разбивали на меньшие кусочки, примерно 1×1 мм. Кусочки сосуда переносили во флакон для клеточной культуры с DMEM, дополненной 10% FCS и 1% антибиотика, для инкубирования в течение 10 дней. Для клеток человека среду DMEM дополняли 10% сыворотки человека (NHS).
При пассировании клеток истощенную культуральную среду отсасывали пипеткой и удаляли. Клетки промывали дважды добавлением PBS (10 мл/75 см2-флакон) во флаконы, стараясь в то же время не нарушить клеточный монослой. Монослой промывали путем осторожного покачивания вперед и назад. PBS удаляли и отбрасывали. Трипсин (3,5 мл/75 см2-флакон) добавляли во флаконы и осторожно покачивали флаконы, чтобы гарантировать покрытие всех монослоев раствором трипсина.
Флаконы инкубировали примерно 3-5 минут до тех пор, пока клетки не начнут отделяться. Для «нейтрализации» трипсина добавляли по 3,5 мл 10% FCS на флакон и растворы набирали в пипетку и выпускали обратно до тех пор, пока клетки не были диспергированы в суспензию отдельных клеток.
Раствор центрифугировали при 300g в течение 5 минут и супернатант удаляли и отбрасывали. Клеточный осадок растворяли в DMEM и переносили в два культуральных флакона.
Эксперименты по скорости клеточного роста (синтезу ДНК) затем проводили таким же образом, как и для описанных выше двух линий рака молочной железы.
На фиг.3 показана скорость роста в результате модуляции PLURONIC® F127 на васкулярных гладкомышечных клетках человека. Обнаружено, что PLURONIC® F127 оказывает дозозависимое ингибирующее действие на скорость пролиферации FCS-стимулированных мышечных клеток. Сопоставимые результаты были также получены для васкулярных гладкомышечных клеток крысы и кролика.
В сравнительном исследовании изучали эффект ингибирования синтеза ДНК у FCS-стимулированных (10%) гладкомышечных клеток F127 и другими полимерами PLURONIC®. Представленные ниже в таблице V результаты нормализованы для синтеза ДНК (как определено с использованием описанного выше способа на основе тимидина) у контрольных клеток, выращенных в среде, дополненной 10% FCS. Тестируемые клетки выращивали в среде, дополненной 10% FCS и сополимером в концентрации 10, 1 или 0,1 мг/мл. В этих тестах синтез ДНК у контрольных клеток принимают за 100% и исследуемые вещества выражают в виде процентного отношения к синтезу ДНК контрольных клеток.
Ингибирование синтеза ДНК
Эти эксперименты подтверждают, что полимеры PLURONIC® можно использовать для ингибирования синтеза ДНК. Эксперименты также показывают, что PLURONIC® F68, как оказалось, не обладает каким-либо таким ингибирующим действием. При наивысшей тестируемой концентрации (10 мг/мл) L31 обладает тенденцией к убийству клеток.
Ингибирование клеточного роста стимулированных гладкомышечных клеток
Для подтверждения того, что ингибирование синтеза ДНК происходило из-за уменьшения числа клеток, т.е. ингибирования скорости пролиферации, для определения числа клеток после лечения PLURONIC® F127 использовали колориметрический способ.
Васкулярные гладкомышечные клетки из аорты крысы получали с использованием описанной выше методики. 5000 клеток аорты крысы в 200 мкл DMEM, дополненной 10% FCS, засевали в лунку в CellTiter 96™ AQueous plate (Promega). Клетки оставляли инкубироваться в течение примерно 1 дня. Среду отбирали пипеткой, отбрасывали и заменяли на 200 мкл DMEM с 10% FCS на лунку.
Через 2 дня клеточную среду DMEM (отрицательный контроль), среду DMEM с 10% FCS (положительный контроль), среду DMEM с 1 или 5% PLURONIC® F127 или среду DMEM с 10% FCS и 1 или 5% PLURONIC® F127 добавляли к различным лункам (n=3) и инкубировали согласно протоколу производителя CellTiter 96™ Non-Radioactive Cell Proliferation/Cytoxicty Assay. Лунки затем три раза промывали PBS согласно протоколу производителя, а затем добавляли 20 мкл раствора MTS на лунку. Планшет инкубировали в течение 1-4 часов и измеряли оптическую плотность при 490 нм.
Результаты представлены на фиг.4. Из диаграммы видно, что колориметрический способ подтверждает ингибирование скорости клеточной пролиферации PLURONIC® F127, наблюдаемой с использованием описанного выше способа синтеза ДНК. PLURONIC® F127 ингибирует эффект стимуляции роста FCS, однако не оказывает какого-либо влияния на нестимулированные клетки.
Опосредованная клеточная цитотоксичность
Для того, чтобы определить, является ли эффект ингибирования скорости клеточной пролиферации PLURONIC® F127 следствием какого-либо токсического действия сополимера на клетки, было проведено испытание на опосредованную клеточную цитотоксичность, где цитотоксичность PLURONIC® F127 сравнивали с 1% Triton X-100, PEG 10000 и другим полимером PLURONIC® P123.
Описанную выше методику с использованием CellTiter 96™ Non-Radioactive Cell Proliferation/Cytoxicty Assay от Promega осуществляли, используя различные концентрации PLURONIC® F127, 1% Triton X-100, 1% PEG 10000 и 1% PLURONIC® P123. На фиг.5 показано цитотоксическое действие различных концентраций PLURONIC® F127, выраженных в процентном отношении к цитотоксичности Triton X-100. PLURONIC® F127 не проявляет никакой клеточной токсичности даже при наивысшей тестируемой концентрации 5%. Однако другой тестируемый полимер PLURONIC® P123 по сравнению с этим проявляет значительно более высокую цитотоксичность.
Сравнительное исследование амфифильных блок-сополимеров
Эффект ингибирования скорости роста других амфифильных блок-сополимеров, помимо PLURONIC® F127, включая PLURONIC® F38, F68, F87, F98, P105, F108, и TETRONIC® T908, T1307 от BASF corporation и DORVAL 1 от Polymer Source Inc., проверяли на стимулированных (10% FCS) васкулярных гладкомышечных клетках человека.
Эксперименты проводили таким же способом, как описанные выше и проиллюстрированные на фиг.3 эксперименты по синтезу ДНК на основе тимидина, с тем отличием, что тестировали три концентрации 1, 0,1 и 0,01% масс./масс. на блок-сополимер.
Результаты ингибирования скорости роста представлены на фиг.6, где скорости роста нормализованы относительно наивысшей определенной скорости роста клеток (T908 и 0,01% масс./масс.).
На чертеже можно видеть, что сополимер, имеющий наибольшее гидрофильное содержание (примерно 80%), т.е. F38, F68, F108 и T908, показал наименьший эффект ингибирования скорости роста на FCS-стимулированных гладкомышечных клетках. Сополимер F87 обладал эффектом, подобным эффекту F127, в то время как P105 достигал наибольшего ингибирующего эффекта при данных экспериментальных условиях.
Эксперименты по связыванию
Проверочные эксперименты проводили для определения того, может ли эффект ингибирования скорости роста PLURONIC® F127 быть опосредован посредством блокирования связывания различных факторов роста с соответствующими рецепторами на гладкомышечных клетках аорты крысы.
Клетки аорты крысы, полученные, как уже было описано, добавляли к культуральной среде (+ 10% FCs) в лунки 24-луночного планшета для микротитрования в концентрации примерно 5000 клеток на лунку. Планшет инкубировали в течение ночи для того, чтобы дать возможность клеткам образовать слой на дне лунок. Культуральную среду затем заменяли культуральной средой, дополненной 0,1% FCS, и оставляли для инкубирования в течение двух дней.
Культуральную среду затем удаляли и лунки дважды промывали PBS. 150 мкл раствора NaCl с различными концентрациями PLURONIC® F127 (2, 1, 0,1, 0,01, 0,001 и 0,0001% масс./масс.) добавляли вместе с 1 мкл 125I-FGF2 (радиоактивно меченый фактор роста фибробластов 2) или 1 мкл 125I-PDGF (фактор роста тромбоцитов), разведенных буферным раствором (0,237M NaCl, 0,0054M KCl, 0,00044M KH2PO4, 0,00126M CaCl2, 0,00018M MgSO4, 0,020M HEPES и 0,3% BSA) и инкубировали 30 минут при 37°C. Затем лунки пять раз промывали PBS (забуференный фосфатом физиологический раствор; 0,2 г KCl, 0,2 г KH2PO4, 1,35 г Na2HPO4 и 8,0 г NaCl на 1000 мл дистиллированной H2O). Затем добавляли 1 мл 0,2M NaOH на лунку и планшеты помещали в холодильник на ночь. Количество связавшихся радиоактивно меченых факторов роста затем определяли посредством традиционного γ-измерения.
Был сделан вывод о том, что PLURONIC® блокирует связывание двух факторов роста со своими соответствующими рецепторами на клетке дозозависимым образом. Кроме того, как продемонстрировано на фиг.7, имеет место весьма высокая корреляция между концентрациями F127, необходимыми для эффектов ингибирования роста и ингибирования связывания FGF2. На фиг.8 демонстрируется соответствующий эффект блокирования связывания полимера F127 на радиоактивно меченом PDGF. Как следствие, блокирование связывания этого фактора роста с рецепторами на клеточной мембране может быть, по меньшей мере, одним из механизмов ингибирования скорости роста амфифильными блок-сополимерами по настоящему изобретению.
Исследование токсичности на мышах
Эксперименты проводили, чтобы исследовать, вызывает ли PLURONIC® P105 токсическую реакцию после внутривенного введения мыши.
Для эксперимента использовали десять мышей-альбиносов NMRI, весящих при поступлении примерно по 25 г. Животные были получены от Scanbur BK и кондиционированы за неделю до начала исследования. Животные были обеспечены пищей и водой ad libitum.
Активное вещество PLURONIC® P105 было представлено в двух объемах растворов с 10 и 50% по массе соответственно сополимера в NaCl (9 мг/л) для 10% раствора и в NaCl (9 мг/л) и PEG для 50% раствора.
Животных разделяли на пять групп и обрабатывали внутривенным введением в хвостовую вену, один раз ежедневно в течение 5 дней. Вводимый объем составлял 150 мкл для всех групп. Инъекции проводили в течение 10 секунд.
Группа 1: 50% PLURONIC® P105 (n=2)
Группа 2: 40% PLURONIC® P105 (n=2)
Группа 3: 30% PLURONIC® P105 (n=2)
Группа 4: 20% PLURONIC® P105 (n=2)
Группа 5: 10% PLURONIC® P105 (n=2)
Массы тел регистрировали перед первым введением и на 6 день. У животных наблюдали за клиническими симптомами токсичности (качество шерсти, слюнотечение, слезотечение, диарея, дыхание, расстройства движения, вялость, дрожь, судороги и кома) в течение 0-30 минут и через 1, 2, 3, 4, 8, 24, 48 и 72 часа после введения исследуемого вещества.
Диагностическое исследование проводили на 2 мышах, обработанных 10% PLURONIC® P105, и 2 мышах, обработанных 50% PLURONIC® P105. Было обнаружено, что животные, обработанные наименьшей концентрацией P105, хорошо переносили повторную обработку, а животные, обработанные 50% P105, показали отечные и гемолитические хвосты уже после второй инъекции. Кроме того, эти двое животных демонстрировали уменьшение двигательной активности и были впоследствии подвергнуты эвтаназии на третий день после начала обработки. В этот момент было принято решение обработать 6 мышей 50% композицией, разведенной физиологическим раствором до 40%, 30% и 20%.
Животные, обработанные 40% P105, демонстрировали небольшое гемолитическое изменение цвета хвостов на 2 день, которое сохранялось в течение периода обработки. Была отмечена некоторая отечность. Эти животные также демонстрировали уменьшение прироста массы, см. таблицу VI.
Было обнаружено, что животные, инъецированные 20% и 30% разведениями, хорошо переносят обработку.
Прирост массы мышей
Тест с имплантацией пористого волокна
Тесты проводили, чтобы исследовать, ингибирует ли PLURONIC® P105 рост опухолевых клеток в модели с пористым волокном на мышах.
В эксперименте использовали восемнадцать самцов мышей-альбиносов NMRI, с массой в среднем примерно 25 г. Животных получали от Scanbur BK и их кондиционировали за неделю до начала исследования. Животные были обеспечены пищей и водой ad libitum.
Наполнение волокон осуществляли в Uppsala University Hospital, Department of Clinical Pharmacology. Волокна заполняли следующими опухолевыми клетками: желтые волокна - U936/gtb и синие волокна - H69.
После бритья и дезинфекции на спине животных, с анестезией изофлураном, делали небольшой кожный разрез. Три волокна, два желтых и одно синее, случайным образом имплантировали подкожно и кожный разрез устраняли с использованием скобок.
Животных разделяли на три группы и обрабатывали, как указано далее, внутривенным введением в хвостовую вену, один раз ежедневно в течение 5 дней, начиная непосредственно после имплантации:
Группа 1: 10% PLURONIC® P105, разведенный NaCl (n=6)
Группа 2: 25% PLURONIC® P105, разведенный PEG и NaCl (n=6)
Группа 3: носитель (n=6)
Массы тел регистрировали перед первым введением и перед эвтаназией. Животных ежедневно проверяли на наличие признаков изменения в потреблении пищи, активности и т.д. как признаков изменения общего состояния здоровья. Через шесть дней после имплантаций волокон животных анестезировали изофлураном и из глазничного сплетения получали приблизительно 250 мкл крови для гематологии. После этого животных подвергали эвтаназии путем цервикальной дислокации и волокна эксплантировали и помещали в среду для культивирования клеток (37°C) перед определением плотности и жизнеспособности клеток.
Статистическую оценку проводили с использованием Graph Pad Prism version 4 (Graph Pad Software Inc., San Diego, U.S.) на компьютере HP Compac dx 2000 с Windows XP. Однонаправленный дисперсионный анализ (ANOVA) с тестом множественного сравнения Тьюки использовали для проверки статистических различий в гематологических параметрах между обработанными группами. Парный t-тест использовали для проверки статистических различий в массах до и после обработки.
Никаких выраженных признаков изменения в состоянии здоровья какого-либо животного обнаружено не было. Не было статистически значимых различий внутри групп в отношении масс до и после обработки.
Статистически значимые различия между группами были обнаружены в гематологических параметрах RBs (p=0,0127, группа 1 в сравнении с группой 3 и группа 2 в сравнении с группой 3), HGB (p=0,021, группа 1 в сравнении с группой 3 и группа 2 в сравнении с группой 3) и PLT (p=0,0006, группа 1 в сравнении с группой 3 и группа 2 в сравнении с группой 3), см. таблицу VII.
Гематологические параметры
Плотность клеток в волокнах была значительно уменьшена (p<0,05) в U937/gtb, содержащих волокна, обработанные высокой дозой PLURONIC® P105, в сравнении с контролем. Подобную тенденцию наблюдали также для клеток, имплантированных животным, обработанным низкой дозой P105, см. фиг.9. Тенденцию к снижению значения средней плотности клеток также отмечали для линии клеток H69 у животных, обработанных сополимером, см. фиг.10.
In vitro-оценивание цитотоксической активности сополимеров
Настоящее исследование имеет целью изучение цитотоксической активности различных сополимеров PLURONIC® и TETRONIC®. В качестве модельных систем используют хорошо охарактеризованную панель из 10 выбранных линий опухолевых клеток человека и одну дополнительную линию раковых клеток предстательной железы. Три соединения, выбранных после скрининга на чувствительной лимфомной линии клеток U937/gtb, исследуют на всех линиях клеток.
Модельная система, используемая в этом исследовании, представляет собой панель линий клеток из десяти опухолевых линий клеток человека [3]. Эта модель создана National Cancer Institute (NCI) в США, где панель линий клеток приблизительно с 60 различными линиями клеток (представляющих большинство форм рака человека) повсеместно используют для определения профиля активности нового соединения [4]. Панель линий клеток может успешно классифицировать вещества как относящиеся к специфической механистической группе (например, антиметаболиты, алкилирующие вещества, ингибиторы топоизомеразы II) с использованием корреляционного анализа [5]. Ранее было обнаружено, что более ограниченное число (10) линий опухолевых клеток человека, представляющих определенные виды цитотоксической лекарственной устойчивости, можно успешно использовать для первичной оценки и предварительной механистической классификации противораковых веществ [6].
Опухолевые клетки могут приобретать устойчивость к цитотоксическим лекарственным средствам, и примерами известных механизмов устойчивости являются P-гликопротеин (Pgp) и белок, ассоциированный с множественной устойчивостью (MRP), увеличенная активность клеточных систем детоксикации, изменение функционирования ядерных ферментов-мишеней, подобных топоизомеразе II (topo II), а также изменение связывания/функционирования тубулина и внутриклеточное перераспределение лекарственного средства. Используемая панель линий клеток содержит линии клеток, экспрессирующих некоторые из этих фенотипов [3].
Помпы вывода лекарственных средств, например Pgp и MRP, демонстрируют низкую специфичность к субстратам и, таким образом, способствуют уменьшению чувствительности к веществам различных классов, например алкалоидам барвинка, антрациклинам, таксанам, эпиподофиллотоксинам и другим лекарственным средствам [7].
Первичные культуры опухолевых клеток человека представляют собой альтернативную модельную систему, которая получила относительно мало внимания в контексте скрининга и разработки новых лекарственных средств. Однако было обнаружено, что in vitro-анализы, проведенные на первичных культурах различных опухолей, хорошо коррелируют с клинической, специфической для типа опухоли активностью [8].
Комбинирование различных цитотоксических лекарственных средств и создание лекарственных препаратов, включающих соединения, которые увеличивают усвоение лекарственного средства или лекарственный эффект, представляет собой развивающуюся область в химиотерапии рака. Были предложены многочисленные способы проведения и интерпретации доклинических исследований лекарственных взаимодействий. При наличии данных по определенным концентрациям для отдельных веществ и их комбинаций широко используется «мультипликативная концепция» (аддитивная модель). В данном описании аддитивное взаимодействие определяют как комбинирование двух лекарственных средств, которое приводит к доле выживших, равной сумме долей выживших от отдельных веществ, что должно означать независимое действие лекарственных средств [9]. Если эффект комбинирования превосходит аддитивный эффект, то взаимодействие является синергичным.
Для оценки образцов активности лекарственных средств использовали панель клеточных линий клеток человека из четырех чувствительных первичных линий клеток, пяти устойчивых к лекарственным средствам подлиний, представляющих различные механизмы устойчивости, и одной линии клеток с первичной устойчивостью. Включенными линиями клеток были линия клеток миеломы RPMI 8226/S и ее подлинии 8226/Dox40 и 8226/LR-5 (любезно предоставленные W.S. Dalton, Dept of Medicine, Arizona Cancer Center, University of Arizona, Tucson, AZ), линии клеток лимфомы U-937/gtb и U-937-Vcr (любезно предоставленные K. Nilsson, Dept of Pathology, University of Uppsala, Sweden), SCLC-линия клеток NCI-H69 и ее подлиния H69AR (American Type Culture Collection; ATCC, Rockville, MD), линия клеток почечной аденокарциномы ACHN (ATCC) и лейкемическая линия клеток CCRF-CEM и ее подлиния CEM/VM-1 (любезно предоставленные W.T. Beck, Dept of Pharmacology, College of Medicine, University of Tennessee, Memphis, TN).
8226/Dox40 выбрана по устойчивости к доксорубицину и демонстрирует классический MDR-фенотип со сверхэкспрессией P-гликопротеина 170 (Pgp)[10]. 8226/ LR-5 выбрана по устойчивости к мелфалану, связанной, как полагают, с увеличенными уровнями GSH [11]. U-937-Vcr выбрана по устойчивости к винкристину, связанной, как полагают, с тубулином [12]. H69AR, выбранная по устойчивости к доксорубицину, экспрессирует MDR-фенотип, опосредованный, как полагают, MRP [13]. CEM/VM-1, выбранная по устойчивости к тенипозиду, экспрессирует нетипичный MDR, который, как полагают, ассоциирован с топоизомеразой II (topo II) [14]. Точный механизм устойчивости первичной устойчивой линии клеток ACHN неизвестен и может быть многофакторным [15].
Клеточные линии выращивали в описанной выше полной культуральной среде при 37°C в увлажненной атмосфере, содержащей 5% CO2. 8226/Dox40 обрабатывали один раз в месяц доксорубицином в концентрации 0,24 мкг/мл, а 8226/LR-5 при каждой замене среды - мелфаланом в концентрации 1,53 мкг/мл. U-937-Vcr непрерывно культивировали в присутствии 10 нг/мл винкристина, а H69AR поддерживали попеременно в среде без лекарственного средства и среде, содержащей 0,46 мкг/мл доксорубицина. Линию клеток CEM/VM-1 культивировали в среде, не содержащей лекарственного средства, без какой-либо потери устойчивости в течение периода 6-8 месяцев. Устойчивые образцы клеточных линий были подтверждены обычным способом в контрольных экспериментах.
Клетки рака предстательной железы человека PC-3 получали из American Type Culture Collection (Rockville, MD). Их выращивали в модифицированной Дульбекко среде Игла, дополненной 10% фетальной бычьей сыворотки, пенициллином G и стрептомицином.
Линии опухолевых клеток человека
Везде для клеточных линий использовали полную среду, состоящую из забуференной карбонатом культуральной среды RPMI-1640 (HyClone, Cramlington, UK), дополненной 10% инактивированной FCS, 2 мМ глутамина, 50 мкг/мл стрептомицина и 60 мкг/мл пенициллина. FDA (Sigma, St Louis, MO) растворяли в ДМСО и хранили в замороженном виде (-20°C) в виде маточного раствора в защищенном от света месте.
Тестируемые соединения растворяли согласно приведенной ниже таблице IX.
Тестируемые вещества
Основную часть первичного скрининга проводили на первой группе веществ (F127 и F68), растворенных только в хлориде натрия и этаноле. В нескольких экспериментах сравнивали активность сополимеров, растворенных в NaCl и этаноле и растворенных в PEG и этаноле, и значительной разницы в эффективности не обнаружили. Для простоты концентрацию тестируемого вещества во всех полученных пробирках принимали за 50% масс./масс. Для получения из них прозрачных растворов последующие разведения готовили на забуференном фосфатом физиологическом растворе (PBS; Sigma Aldrich).
Опухолевые клетки засевали в 96-луночные планшеты с подготовленными лекарственными средствами до плотности клеток примерно 20000 клеток/лунку.
Использовали флуорометрический анализ цитотоксичности микрокультур (FMCA), основанный на измерении флуоресценции, генерируемой в результате гидролиза FDA до флуоресцеина клетками с интактными плазматическими мембранами, и как подробно описано ранее [16]. Планшеты инкубировали при 37°C в увлажненной атмосфере, содержащей 5% CO2, в течение 72 часов. В конце периода инкубирования планшеты центрифугировали (1000 об/мин, 5 минут) и среду удаляли отсасыванием. После одной промывки в PBS добавляли 100 мкл/лунку FDA, растворенного в физиологическом буфере (10 мкг/мл). Планшеты инкубировали в течение 45 минут и генерируемую флуоресценцию от каждой лунки измеряли при помощи 96-луночного сканирующего флуориметра (Fluoroscan II, Labsystems Oy, Helsinki, Finland). Флуоресценция пропорциональна числу интактных клеток в лунке.
Критерии качества для успешного анализа включали флуоресцентный сигнал в контрольных лунках более чем в пять раз больше среднего нулевого значения, средний коэффициент вариации (CV) в контрольных лунках менее чем 30% и более чем 70% опухолевых клеток в препарате клеток перед инкубированием. Эксперименты проводили дважды, везде используя средние значения.
Клеточная выживаемость представлена в виде индекса выживаемости (SI), определяемого как флуоресценция в экспериментальных лунках в процентах от флуоресценции в контрольных лунках, с вычетом значений в нулевых лунках. Все эксперименты с клеточными линиями проводили, по меньшей мере, два раза, и все данные были включены в анализ.
Данные экспериментов с панелью клеточных линий сравнивали с базой данных, содержащей данные о более чем 150 различных соединений, включая наиболее широко используемые цитотоксические вещества. С этой целью для каждого лекарственного средства и линии клеток рассчитывали IC50, определенную при помощи простой логарифмической регрессии как концентрация лекарственного средства, вызывающая индекс выживаемости 50%. Серию из десяти значений IC50 для каждого лекарственного средства коррелировали при помощи коэффициента корреляции Пирсона с соответствующей серией данных для всех других лекарственных средств в базе данных. Из этих значений IC50 с использованием Delta был также показан образец активности, определенный как отклонение log IC50 одной линии клеток от среднего log IC50 панели клеточных линий. Эти вычисления проводили согласно Dhar et al. [3], модифицируя методики, используемые в National Cancer Institute (www.dtp.nci.nih.gov).
Данные концентрация-эффект для обеих панелей клеточных линий приводили в соответствие с сигмоидальным уравнением доза-ответ с переменным угловым коэффициентом, используя нелинейную регрессию, при помощи программного обеспечения GraphPad Prism (GraphPad Software, San Diego, CA). 0 и 100% выживаемость клеток принимали за максимальный эффект и базовый уровень соответственно и EC50 (концентрация, приводящая к 50% эффекту) прогнозировали путем подбора аппроксимирующей кривой. Факторы устойчивости рассчитывали в виде соотношения между EC50 для устойчивой и исходной линии клеток в парах клеточных линий [3].
Соединения сохраняли свою цитотоксическую активность после 4 недель хранения в планшетах для микротитрования при -70°C. Кривые концентрация-эффект при использовании планшетов, хранившихся 4 недели, и при использовании только что приготовленных планшетов (данные не приведены) были сходными.
Кривые концентрация-эффект для всех тестируемых соединений на U937gtb представлены на фиг.11. Соответствующие тестируемые сополимеры отдельно показаны на фиг.12A-12O. Значения IC50 представлены ниже в таблице X. При сравнении образцов, растворенных в NaCl/EtOH и PEG/NaCl/EtOH, были получены сходные результаты (данные не приведены).
Значения IC50 для сополимеров
В очередной раз результаты подтверждают, что сополимер PLURONIC® со средним гидрофильным содержанием примерно 80% обладает гораздо меньшим противораковым действием. EC50 для всех клеточных линий представлены в таблице XI для трех наиболее эффективных сополимеров, выбранных из таблицы XI. Фиг.13A-13C являются наглядным представлением результатов.
EC50-активность в панели клеточных линий
Вещества тестировали при минимальной концентрации 0,0016% масс./масс. EC50-значения ниже этой концентрации представляют собой определение из анализа линейной регрессии, позволяющего экстраполировать кривую. Когда аппроксимация кривой была неадекватной и большинство клеток погибало при минимальной концентрации, использовали EC50 <<0,0016.
Специалист в данной области должен осознавать, что в настоящем изобретении можно сделать различные модификации и изменения без выхода из его объема, который определен прилагаемой формулой изобретения.
ССЫЛКИ
[1] US 2001/0051659 Al
[2] Silk et al, Cancer 1972, 29, 171-172
[3] Dhar et al., Br J Cancer 1996, 74, 888-896
[4] Alley et al., Cancer Res 1988, 48, 589-601
[5] Paull et al., J Natl Cancer Inst 1989, 81, 1088-1092
[6] Dhar et al., Eur J Pharmacol 1998, 346, 315-322
[7] Fisher et al., Eur J Cancer 1996, 32A, 1082-1088
[8] Fridborg et al., Eur J Cancer 1999, 35, 424-432
[9] Valeriote et al., Cancer Chemother Rep 1975, 59, 895-900
[10] Dalton et al., Cancer Res 1986, 46, 5125-5130
[11] Bellamy et al., Cancer Res 1991, 51, 995-1002
[12] Botling et al., Int J Cancer 1994, 58, 269-274
[13] Cole et al., Science 1992, 258, 1650-1654
[14] Danks et al., Biochemistry 1988, 27, 8861-8869
[15] Nygren et al., Biosci Rep 1990, 10, 231-237
[16] Larsson et al., Int J Cancer 1992, 50, 177-185
[17] Freireich et al., Cancer Chemother Rep 1966, 50, 219-244
[18] WO 98/07434
[19] Kabanov et al., Advanced Drug Delivery Reviews 2002, 54, 759-779
Изобретение относится к фармацевтической области и касается применения амфифильных блок-сополимеров для лечения и предупреждения рака, в частности, путем уменьшения скорости роста и пролиферации раковых клеток. Кроме того, амфифильные блок-сополимеры могут быть использованы для блокирования связывания факторов роста тромбоцитов и фибробластов со своими соответствующими рецепторами на мембране. Предпочтительные блок-сополимеры содержат основную гидрофобную цепь, предпочтительно полипропиленоксидную цепь, к которой присоединены, по меньшей мере, две гидрофильные боковые цепи, предпочтительно полиэтиленоксидные цепи, причем среднее содержание указанного этиленоксида составляет менее чем 80% указанного амфифильного блок-сополимера и молекулярная масса основной гидрофобной полимерной цепи составляет по меньшей мере 2000 г/моль. Изобретение обеспечивает новое химиотерапевтическое средство на основе полимеров против разнообразных видов рака, обладающее эффектом уменьшения скорости пролиферации раковых клеток. 8 н. и 10 з.п. ф-лы, 13 ил., 11 табл.
1. Применение амфифильного блок-сополимера, имеющего основную гидрофобную полимерную цепь, у которой первый конец соединен с, по меньшей мере, одной гидрофильной этиленоксидной боковой полимерной цепью и второй конец соединен с, по меньшей мере, одной гидрофильной этиленоксидной боковой полимерной цепью, в качестве химиотерапевтического средства при получении лекарственного препарата для лечения или предупреждения рака, при условии, что указанный рак не является колоректальным раком или раком прямой кишки, где среднее содержание указанного этиленоксида составляет менее чем 80% указанного амфифильного блок-сополимера и молекулярная масса основной гидрофобной полимерной цепи составляет по меньшей мере 2000 г/моль и указанный лекарственный препарат содержит указанный амфифильный блок-сополимер или смесь, по меньшей мере, двух амфифильных блок-сополимеров в качестве единственного химиотерапевтического средства.
2. Применение амфифильного блок-сополимера, имеющего основную гидрофобную полимерную цепь, у которой первый конец соединен с, по меньшей мере, одной гидрофильной этиленоксидной боковой полимерной цепью и второй конец соединен с, по меньшей мере, одной гидрофильной этиленоксидной боковой полимерной цепью, при получении лекарственного препарата для уменьшения скорости роста раковых клеток у субъекта, страдающего раком, при условии, что указанный рак не является колоректальным раком или раком прямой кишки, где среднее содержание указанного этиленоксида составляет менее чем 80% указанного амфифильного блок-сополимера и молекулярная масса основной гидрофобной полимерной цепи составляет по меньшей мере 2000 г/моль и указанный лекарственный препарат содержит указанный амфифильный блок-сополимер или смесь, по меньшей мере, двух амфифильных блок-сополимеров в качестве единственного средства, уменьшающего скорость роста.
3. Применение амфифильного блок-сополимера, имеющего основную гидрофобную полимерную цепь, у которой первый конец соединен с, по меньшей мере, одной гидрофильной этиленоксидной боковой полимерной цепью и второй конец соединен с, по меньшей мере, одной гидрофильной этиленоксидной боковой полимерной цепью, для получения лекарственного препарата против клеточной пролиферации, при условии, что указанная клетка не является клеткой колоректального рака или рака прямой кишки, где среднее содержание указанного этиленоксида составляет менее чем 80% указанного амфифильного блок-сополимера и молекулярная масса основной гидрофобной полимерной цепи составляет по меньшей мере 2000 г/моль и указанный лекарственный препарат содержит указанный амфифильный блок-сополимер или смесь, по меньшей мере, двух амфифильных блок-сополимеров в качестве единственного средства против клеточной пролиферации.
4. Применение по любому из пп.1-3, где указанный амфифильный блок-сополимер представлен формулой (I):
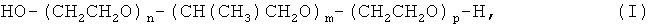
где m, n и р являются, каждый, целыми числами.
5. Применение по п.4, где m, n и р выбраны так, что
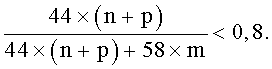
6. Применение по п.4, где n равно р.
7. Применение по любому из пп.1-3, где среднее содержание этиленоксида в указанном амфифильном блок-сополимере составляет, по меньшей мере, 40% мас./мас., но ниже 80% мас./мас.
8. Применение по п.4, где среднее содержание пропиленоксида в указанном амфифильном блок-сополимере составляет, по меньшей мере, 2000 г/моль.
9. Применение по п.8, где указанное среднее содержание пропиленоксида составляет, по меньшей мере, 3000 г/моль.
10. Применение по п.9, где указанное среднее содержание пропиленоксида находится в диапазоне от 3500 до 4500 г/моль, предпочтительно около 4000 г/моль.
11. Применение по любому из пп.1-3, где указанный амфифильный блок-сополимер имеет среднюю молекулярную массу 12600 г/моль, среднее содержание этиленоксида 73,2±1,7% и температуру плавления 56°С.
12. Применение по п.11, где указанный рак выбран из группы, состоящей из рака почки, рака легкого, миеломы, лимфомы и рака предстательной железы.
13. Способ ингибирования скорости пролиферации клетки in vitro, при условии, что указанная клетка не является клеткой колоректального рака или рака прямой кишки, включающий контактирование указанной клетки с амфифильным блок-сополимером, имеющим основную гидрофобную полимерную цепь, у которой первый конец соединен с, по меньшей мере, одной гидрофильной этиленоксидной боковой полимерной цепью и второй конец соединен с, по меньшей мере, одной гидрофильной этиленоксидной боковой полимерной цепью, где среднее содержание указанного этиленоксида составляет менее чем 80% указанного амфифильного блок-сополимера и молекулярная масса основной гидрофобной полимерной цепи составляет по меньшей мере 2000 г/моль.
14. Способ по п.13, где указанная клетка представляет собой раковую клетку, но не является клеткой колоректального рака или рака прямой кишки.
15. Способ блокирования связывания фактора роста фибробластов (FGF) с рецептором фактора роста фибробластов или фактора роста тромбоцитов (PDGF) с рецептором (PDGF) на клеточной мембране клетки, включающий контактирование указанной клетки с амфифильным блок-сополимером, имеющим основную гидрофобную полимерную цепь, у которой первый конец соединен с, по меньшей мере, одной гидрофильной этиленоксидной боковой полимерной цепью и второй конец соединен с, по меньшей мере, одной гидрофильной этиленоксидной боковой полимерной цепью, где среднее содержание указанного этиленоксида составляет менее чем 80% указанного амфифильного блок-сополимера и молекулярная масса основной гидрофобной полимерной цепи составляет по меньшей мере 2000 г/моль.
16. Способ лечения или предупреждения рака у субъекта, при условии, что указанный рак не является колоректальным раком или раком прямой кишки, включающий введение указанному субъекту лекарственного препарата, содержащего амфифильный блок-сополимер, имеющий основную гидрофобную полимерную цепь, у которой первый конец соединен с, по меньшей мере, одной гидрофильной этиленоксидной боковой полимерной цепью и второй конец соединен с, по меньшей мере, одной гидрофильной этиленоксидной боковой полимерной цепью, в качестве химиотерапевтического средства, где среднее содержание указанного этиленоксида составляет менее чем 80% указанного амфифильного блок-сополимера и молекулярная масса основной гидрофобной полимерной цепи составляет по меньшей мере 2000 г/моль и указанный лекарственный препарат содержит указанный амфифильный блок-сополимер или смесь, по меньшей мере, двух амфифильных блок-сополимеров в качестве единственного химиотерапевтического средства.
17. Способ уменьшения скорости роста раковых клеток у субъекта, страдающего раком, при условии, что указанный рак не является колоректальным раком или раком прямой кишки, включающий введение указанному субъекту лекарственного препарата, содержащего амфифильный блок-сополимер, имеющий основную гидрофобную полимерную цепь, у которой первый конец соединен с, по меньшей мере, одной гидрофильной этиленоксидной боковой полимерной цепью и второй конец соединен с, по меньшей мере, одной гидрофильной этиленоксидной боковой полимерной цепью, где среднее содержание указанного этиленоксида составляет менее чем 80% указанного амфифильного блок-сополимера и молекулярная масса основной гидрофобной полимерной цепи составляет по меньшей мере 2000 г/моль и указанный лекарственный препарат содержит указанный амфифильный блок-сополимер или смесь, по меньшей мере, двух амфифильных блок-сополимеров в качестве единственного средства, уменьшающего скорость роста.
18. Способ ингибирования клеточной пролиферации у субъекта, при условии, что указанная клетка не является клеткой колоректального рака или рака прямой кишки, включающий введение указанному субъекту лекарственного препарата против клеточной пролиферации, содержащего амфифильный блок-сополимер, имеющий основную гидрофобную полимерную цепь, у которой первый конец соединен с, по меньшей мере, одной гидрофильной этиленоксидной боковой полимерной цепью и второй конец соединен с, по меньшей мере, одной гидрофильной этиленоксидной боковой полимерной цепью, где среднее содержание указанного этиленоксида составляет менее чем 80% указанного амфифильного блок-сополимера и молекулярная масса основной гидрофобной полимерной цепи составляет по меньшей мере 2000 г/моль и указанный лекарственный препарат содержит указанный амфифильный блок-сополимер или смесь, по меньшей мере, двух амфифильных блок-сополимеров в качестве единственного средства против клеточной пролиферации.
| US 6359014 B1, 19.03.2002 | |||
| US 5234683 A, 10.08.1993 | |||
| КОМПОЗИЦИИ, ВКЛЮЧАЮЩИЕ БИОЛОГИЧЕСКИЙ АГЕНТ | 1996 |
|
RU2166934C2 |
| N.S.MELIK-NUBAROV et al | |||
| Способ пропитывания дерева | 1921 |
|
SU446A1 |
| A.V.KABANOV et al | |||
| Pluronic® block copolymers for overcoming drug resistance in cancer // Advanced Drug | |||
Авторы
Даты
2011-10-27—Публикация
2007-04-23—Подача