Данное изобретение относится к карбонатным пролекарствам фениколов, имеющим улучшенную растворимость и уменьшенную вязкость в подходящих растворителях - носителях.
Уровень техники
Хлорамфеникол, тиамфеникол и флорфеникол представляют собой антибиотики широкого спектра действия, в общем известные как "фениколы." Флорфеникол представляет собой антибиотик широкого спектра действия с активностью против многих грамотрицательных и грамположительных бактерий. Флорфеникол полезен для предупреждения и лечения бактериальных инфекций, обусловленных чувствительными болезнетворными микроорганизмами, у млекопитающих, птиц, пресмыкающихся, рыб и ракообразных. Одним из его основных применений является лечение пневмонии и сопутствующих респираторных инфекций крупного рогатого скота (часто в общем именуемых как Бычье респираторное заболевание или BRD), вызванных Mannhemia haemolytica, Pasteurella multocida и(или) Histophilus somni. Он также предписывается для лечения инфекционного пододерматита крупного рогатого скота, вызванного Fusobacterium necrophorum и/или Prevotella melaninogenicus, свиного респираторного заболевания, вызванного Pasteurella multocida, Actinobacillus pleuropneumoniae, Streptococcus suis, Salmonella cholerasuis и/или Mycoplasma spp., колибактериоза цыплят, вызванного Escherichia coli, кишечного сепсиса у зубатковых, вызванного Edwardsiella ictaluri, и фурункулеза лососевых рыб, вызванного Aeromonas salmonicida. Другой род бактерий, который уже показал чувствительность к флорфениколу, включает в себя Enterobacter, Klebsiella, Staphylococcus, Enterococcus, Bordetella, Proteus и Shigella. В частности, резистентные к хлорамфениколу штаммы микроорганизмов, такие как К. pneumoniae, E. cloacae, S. typhus и Е. Coli, чувствительны к флорфениколу.
Как показано ниже, флорфеникол является структурным аналогом тиамфеникола, который, в свою очередь, является производным хлорамфеникола, в котором ароматическая нитрогруппа, которую уже связали с вызываемой хлорамфениколом, независимо от дозы, необратимой апластической анемией у людей, замещается метилсульфонильной группой.
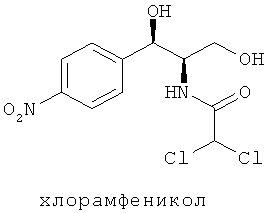
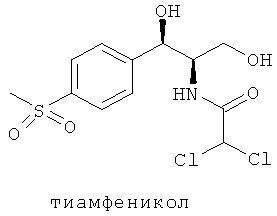
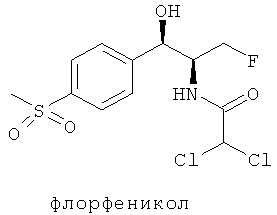
Флорфеникол имеет атом фтора вместо первичной гидроксильной группы хлорамфеникола и тиамфеникола. Это делает флорфеникол менее чувствительным к дезактивации бактериями, содержащими кодируемый плазмидой фермент хлорамфеникол ацетил-трансферазу (CAT), который ацетилирует первичную гидроксильную группу хлорамфеникола и тиамфеникола. Ацетилирование предотвращает связывание этих антибиотиков с рибосомальными субъединицами чувствительных бактерий. Связывание этого класса антибиотиков с рибосомальными субъединицами является основным (но не единственным) механизмом действия хлорамфеникола и тиамфеникола при ингибировании пептидил-трансферазы бактерий, которая ответственна за перенос аминокислот к растущим пептидным цепям и последующему образованию белка.
Флорфеникол чаще всего вводят субъекту, который может получить пользу от его преимуществ, либо перорально, либо подкожно, либо парентерально, причем последним преимущественно является внутримышечное или внутривенное введение. Принимая во внимание необходимость экономичного лечения однократной дозой в ветеринарной практике, остается необходимость в новых композициях с высокими концентрациями флорфеникола.
Кроме того, также существует необходимость в форме флорфеникола. которая способна поддерживать эффективные уровни антибиотика в плазме в течение продолжительных периодов времени, для того чтобы достичь большей экономии при введении лекарства, например, более быстро проводить лечение однократными дозами, в частности в ветеринарной практике.
При попытке усилить эффект однократной инъекции флорфеникола в данной области техники рассмотрели сложноэфирные производные флорфеникола в качестве пролекарств. Например, Murthy и другие, в опубликованной заявке на патент США US No. 2005/0014828, описали этерифицированные флорфениколы, такие как ацетат флорфеникола, пропионат флорфеникола, бутират флорфеникола, пентаноат флорфеникола, гексаноат флорфеникола, гептаноат флорфеникола, октаноат флорфеникола, нонаноат флорфеникола, деканоат флорфеникола, ундеканоат флорфеникола, додеканоат флорфеникола и фталат флорфеникола и тому подобное.
Флорфениколы с улучшенной растворимостью в воде и активность пролекарства в форме сложных эфиров фосфата флорфеникола также описаны совладельцами в опубликованной заявке на патент США US No. 2005/0182031.
Тем не менее, остается давно существующая необходимость в данной области техники в дополнительных фениколах с улучшенной растворимостью в подходящих носителях, что может обеспечить экономичное лечение однократной дозой.
Упоминание в настоящем документе любой ссылки должно быть истолковано как допущение, что такая ссылка доступна в качестве "известного уровня техники" для заявки, рассматриваемой в данный момент.
Краткое изложение сущности изобретения
Соответственно, для того чтобы принять меры по поводу вышеописанных потребностей, изобретение предоставляет карбонатные производные фениколов. имеющие полезные свойства пролекарств. В одном варианте осуществления изобретения предоставляются карбонаты фениколов, соответствующие формуле (I):
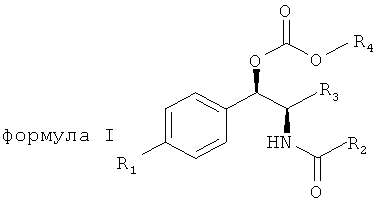 ,
,
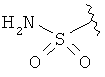
где R1 выбирается из группы, состоящей
из:
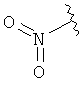 ,
, 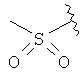 ,
, 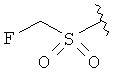 ,
, 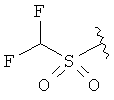 ,
, 
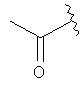 ,
, 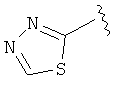 ,
, 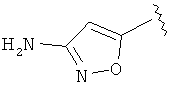 и
и 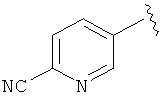
R2 выбирается из группы, состоящей из дихлорметила, дифторметила, хлорфторметила, хлорметила и метила,
R3 выбирается из группы, состоящей из гидроксиметила, фторметила, дифторметила, трифторметила и CH2O-С(O)O-R5,
R4 и R5 независимо выбираются из группы, состоящей из замещенного или незамещенного, C1-10 неразветвленного, разветвленного или циклоалкила, замещенного или незамещенного C1-10 алкоксиалкила, C1-10 арила, C1-10 арилалкила, замещенного или незамещенного, C1-10 неразветвленного, разветвленного или циклоалкенила. Предпочтительно R3 представляет собой CH2F. В конкретном варианте осуществления изобретения R1 представляет собой CH3SO2, R2 представляет собой CHCl2 и R3 представляет собой CH2F. Более того, если R1 представляет собой NO2, R3 не представляет собой CH2O-C(O)O-R5.
В другом варианте осуществления изобретения R4 и R5 независимо замещены составляющей, выбранной из группы, состоящей из метила, метокси, карбокси, карбоалкокси и ацилокси.
В еще одном варианте осуществления изобретения R4 и R5 независимо выбираются из группы, состоящей из метила, этила, пропила, изопропила, н-бутила, трет-бутила, изобутила, пентила, изопентила, н-гексила, н-гептила, н-октила, н-нонила, н-децила, н-додецила, н-октадецила, 2-метилбутила, 1-этилпропила, 3-метилпроп-2-енила, 2-метоксиэтила, 2-этоксиэтила, 2-пропоксиэтила, 2-бутоксиэтила, 1-метил-2-метоксиэтила, циклопропилметила, цикпопентилметила, циклогексилметила, циклопропила, циклобутила, циклопентила, циклогексила, 3,7-диметилокт-6-енила, бензила, 2-метилбензила, 3-метилбензила, 4-метилбензила, 2-метоксибензила, 3-метоксибензила, 4-метоксибензила, метил-2-фурила, 2-(метоксиэтокси)-этила, 2-(этоксиэтокси)-этила, 2-[2-(метоксиэтокси)-этокси]-этила, 2-[2-(этоксиэтокси)-этокси]-этила, 2-(гидроксиэтокси)-этила, 2-[2-(гидроксиэтокси)-этокси]-этила, 2-ацетоксиэтила, 2-(ацетоксиэтокси)-этила, 3-ацетоксипропила, 2-карбоксиэтила, 3-карбоксипропила, 4-карбоксибутила, 2-метоксикарбонилэтила, 3-метоксикарбонилпропила, 4-метоксикарбонилбутила, 2-метоксикарбонилбензила, 3-метоксикарбонилбензила, 4-метоксикарбонилбензила, 1-этоксикарбонилэтила, 1-метоксикарбонилэтила, фенила, 4-метилфенила, 4-метоксифенила, 4-карбоксифенила, 2-карбоксифенила, 4-метоксикарбонилфенила, 2-метоксикарбонилфенила и 4-ацетиламинофенила.
В следующем варианте осуществления изобретения R1 выбирается из группы, состоящей из
 ,
,  и
и  ,
,
R2 представляет собой дихлорметил или дифторметил и R3 выбирается из группы, состоящей из гидроксиметила, фторметила и CH2O-C(O)O-R5, и, возможно, но не обязательно, R4 выбирается из группы, состоящей из метила, этила, пропила, изопропила, н-бутила, трет-бутила, изобутила, пентила, изопентила, н-гексила, н-гептила, н-октила, н-нонила, н-децила, н-додецила, н-октадецила, 2-метилбутила, 1-этилпропила, 3-метилпроп-2-енила, 2-метоксиэтила, 2-этоксиэтила, 2-пропоксиэтила, 2-бутоксиэтила, 1-метил-2-метоксиэтила, циклопропилметила, циклопентилметила, циклогексилметила, циклопропила, циклобутила, циклопентила, циклогексила, 3,7-диметилокт-6-енила, бензила, 2-метилбензила, 3-метилбензила, 4-метилбензила, 2-метоксибензила, 3-метоксибензила, 4-метоксибензила, метил-2-фурила, 2-(метоксиэтокси)-этила, 2-(этоксиэтокси)-этила, 2-[2-(метоксиэтокси)-этокси]-этила, 2-(2-(этоксиэтокси)-этокси]-этила, 2-(гидроксиэтокси)-этила, 2-[2-(гидрокси-этокси)-этокси]-этила, 2-ацетоксиэтила, 2-(ацетоксиэтокси)-этила, 3-ацетоксипропила, 2-карбоксиэтила, 3-карбоксипропила, 4-карбоксибутила, 2-метоксикарбонилэтила, 3-метоксикарбонилпропила, 4-метоксикарбонилбутила, 2-метоксикарбонилбензила, 3-метоксикарбонилбензила, 4-метоксикарбонилбензила, 1-этоксикарбонилэтила, 1-метоксикарбонилэтила, фенила, 4-метилфенила, 4-метоксифенила, 4-карбоксифенила, 2-карбоксифенила, 4-метоксикарбонилфенила, 2-метоксикарбонилфенила и 4-ацетиламинофенила.
В следующем варианте осуществления изобретения R1 представляет собой CH3SO2 или NO2, R2 представляет собой CHCl2, R3 представляет собой ОН и R4 представляет собой этил, или, в качестве альтернативы, R1 представляет собой CH3SO2 или NO2, R2 представляет собой CHCl2, R3 представляет собой
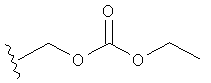 ,
,
и R4 представляет собой этил.
Предпочтительно карбонат феникола по изобретению выбирается из следующей группы соединений:
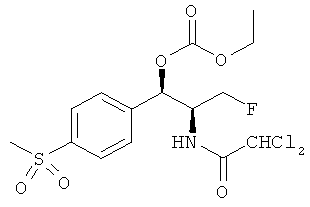 ,
, 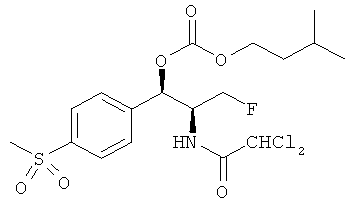 ,
, 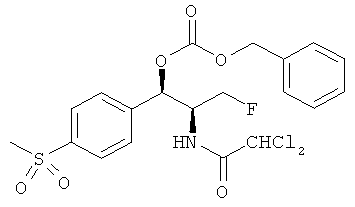 ,
,
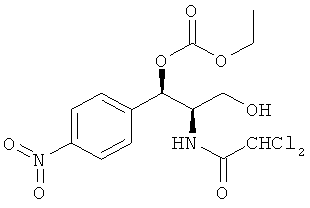 ,
, 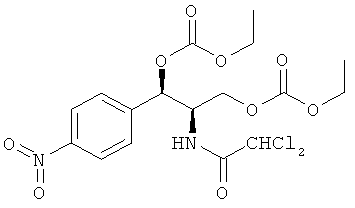 и
и 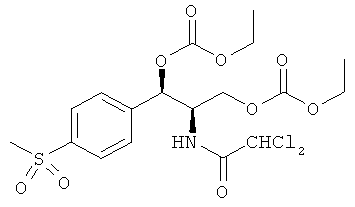
Изобретение, в частности, также включает соединения, представленные в настоящем документе в качестве примеров, включая карбонаты фениколов, перечисленные в Таблице 2, приведенной ниже.
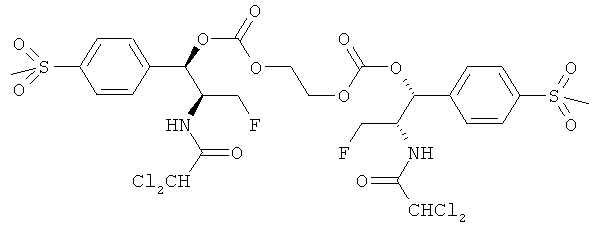
Более того, также предполагается, что соединения по изобретению включают в себя бис(карбонаты фениколов). Например, такие бис(карбонаты фениколов) включают в себя соединения, содержащие структуру формулы II, приведенную ниже.
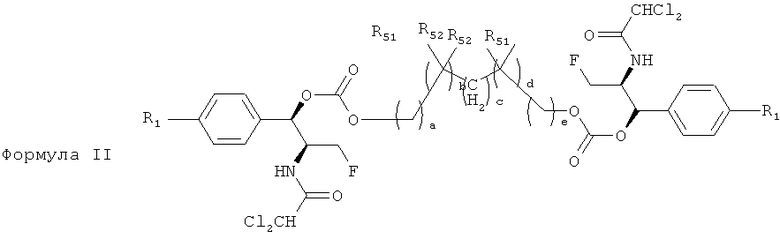
где R1 выбирается из группы, состоящей из
 ,
,  ,
,  ,
,  ,
, 
 ,
,  ,
,  и
и 
где а, с и е представляют собой целые числа, которые независимо изменяются в пределах значений от 0 вплоть до 4, b и d представляют собой целые числа, которые независимо изменяются в пределах значений от 0 вплоть до 2, при условии, что сумма целых а, b, с, d и е колеблется в пределах значений от 2 до 8, и
R51 и R52 независимо выбираются из группы, состоящей из водорода (Н), метила, гидроксила, метокси и ацетокси. Предпочтительно сумма целых а, b, с, d и е колеблется в пределах значений от 2 до 4.
Более предпочтительно изобретение включает в себя соединение формулы II, где R1 представляет собой

и R3 представляет собой CH2F.
Даже более предпочтительно изобретение содержит соединение формулы II, имеющее структуру, выбранную из группы, состоящей из:
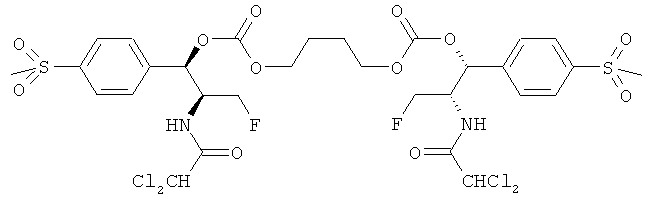 ,
,
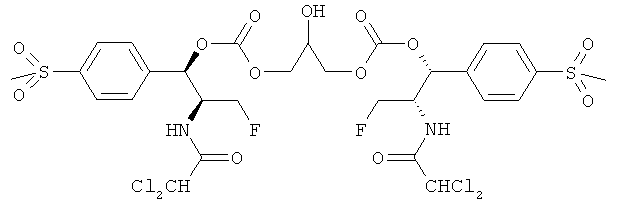 ,
,
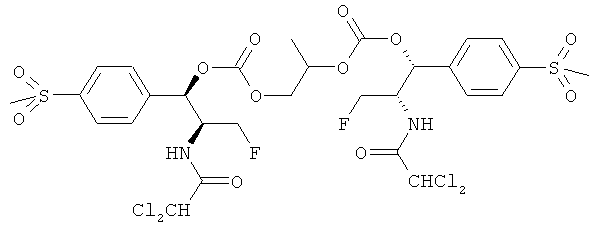 и
и
В следующем варианте осуществления изобретения изобретение также включает фармацевтическую композицию, содержащую эффективное количество карбоната феникола, соответствующего формуле I или формуле II, или его сольвата, вместе с фармацевтически приемлемым инертным наполнителем или растворителем. Предпочтительно карбонат феникола содержится в количестве от около 80 процентов до около 5 процентов, по весу композиции.
Предпочтительно фармацевтически приемлемый растворитель содержит, по меньшей мере, один фармацевтически приемлемый спирт, например, такой как, бензиловый спирт. Как правило, содержание спирта в фармацевтической композиции находится в пределах от около 5% до около 98%, по весу композиции. Предпочтительно содержание спирта находится в пределах от около 10% до около 90% по весу композиции. Более предпочтительно содержание спирта находится в пределах от около 20% до около 45%, по весу композиции. Концентрация бензилового спирта до 45%, по весу, особенно благоприятна.
Изобретение, более того, включает в себя фармацевтическую композицию, содержащую эффективное количество карбоната феникола формулы I, в которой R1 представляет собой CH3SO2, R2 представляет собой CHCl2 и R3 представляет собой CH2F, вместе с фармацевтически приемлемыми инертными наполнителями или растворителями.
Изобретение, более того, включает в себя фармацевтическую композицию, содержащую эффективное количество карбоната феникола формулы I или формулы II, вместе с фармацевтически приемлемыми инертными наполнителями или растворителями, и содержащую соответствующий феникол, который идентичен фениколу, высвобождаемому in vivo из карбоната феникола формулы I или формулы II соответственно.
Также предполагается, что фармацевтические композиции по изобретению более того, содержат, по меньшей мере, один дополнительный терапевтический агент, который может вводиться животному, при необходимости этого, до, после или одновременно с карбонатом феникола по изобретению.
Дополнительным фармацевтическим агентом является, например, флорфеникол и/или любой другой тип агента, подходящий для введения животному, при необходимости этого. Такие дополнительные агенты включают в себя, например, эндектоциды, такие как авермектин. Авермектин, просто в качестве примера, выбирается из группы: Ивермектин, Дорамектин, Абамектин, Селамектин, Эмамектин, Эприномектин, Моксидектин, Милбемицин и их комбинаций. Предпочтительно авермектин присутствует в количестве, колеблющемся от около 0.03% в/о до около 20% в/о. Дополнительный агент может, более того, также включать флукицид, возможно, но не обязательно, объединенный с эндектоцидом или с другим агентом, как более подробно описано ниже.
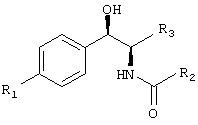
В еще одном варианте осуществления изобретения изобретение включает в себя фармацевтическую композицию, содержащую карбонат феникола формулы 1 в комбинации с фениколом формулы III
 ,
,
где карбонат феникола формулы I и феникол формулы III присутствуют в соотношении, колеблющемся в пределах от 50:1 до 1:50, по весу, и где R1 представляет собой CH3SO2, R2 представляет собой CHCl2 и R3 представляет собой ОН или F. R1, R2 и R3 в Формуле III определяются так же, как приведено ранее для Формулы I. Аналогичная композиция, содержащая соединение формулы II и соединение формулы III, также предполагается, применяя те же или аналогичные соотношения. Фармацевтические композиции данного изобретения могут вводиться животным или рыбам в профилактически эффективных количествах и/или для метафилактики, в качестве необходимости и/или в установленном порядке.
Соответствующие методы введения профилактически эффективных количеств фармацевтических композиций данного изобретения и/или методы метафилактики, в качестве необходимости и/или в установленном порядке, также предоставляются данным изобретением. Данное изобретение также предоставляет методы лечения или предупреждения заболеваний или нарушений у животных, нуждающихся в этом. Такие методы могут включать в себя введение профилактически эффективного количества карбоната феникола формулы I и/или формулы II, включая любое из соединений примеров 1-30, как описано ниже. Эффективное количество находится в пределах, например, от около 1 до около 150 мг на кг веса животного, которое будут лечить. В общих чертах, животным, которое подлежит лечению, является любое животное, которому будет полезно введение соединений по изобретению. Как правило, животное, которое подлежит лечению, относится к классу млекопитающих, птиц, рыб, пресмыкающихся или беспозвоночных, включая любое из животных, более подробно перечисленных ниже.
Изобретение, более того, предоставляет процессы синтеза соединения формулы I, содержащие реакцию феникола с соответствующим хлорформиатом, в подходящем растворителе. Подходящий растворитель может включать, например, хлорированные растворители, сложноэфирные растворители, простые полиэфирные растворители, ацетали формальдегида, простые циклические эфиры, кетоны, растворители, представляющие собой смешанные (простые и сложные) эфиры, и диэтиленгликоли, и предпочтительно включает в себя тетрагидрофуран.
Процесс синтеза предпочтительно проводят в присутствии катализатора, например, 4-диметиламинопиридина (ДМАП), 4-метилпиридина, пиридина и комбинаций из них. Процесс синтеза предпочтительно проводят в присутствии кислотного акцептора, например, триэтиламина, пиридина, карбоната натрия, бикарбоната натрия, карбоната калия и комбинации из них.
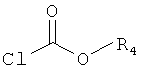
Предпочтительно проводят процесс синтеза, в котором хлорформиат представляет собой
 ,
,
где R4 представляет собой группу, определенную ранее для Формулы I.
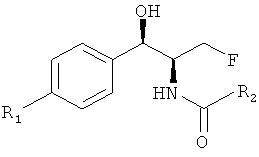
Предпочтительно проводят процесс синтеза, в котором феникол имеет структуру:
или
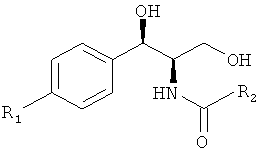 ,
,
и хлорформиат, в ходе реакции, присутствует в мольном избытке по отношению к фениколу. R1 и R2 ранее определены для формулы I.
Процесс синтеза соединения формулы II включает в себя реакцию феникола с соответствующим бисхлорформиатом, в подходящем растворителе, где феникол присутствует в мольном избытке, по отношению к хлорформиату.
Предпочтительно в процессе приготовления соединения формулы II феникол представляет собой соединение, приведенное ниже,
 ,
,
и бисхлорформиат предпочтительно представляет собой
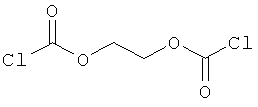
R1 и R2 представляют собой группы, определенные ранее для формулы I и/или для формулы II.
Краткое описание чертежей
На Фиг.1А показана Схема 1 реакции синтеза пролекарств, представляющих собой бензильные карбонаты флорфеникола и аналогов флорфеникола, с использованием хлорформиатов.
На Фиг.1В показана Схема 2 реакции синтеза сложных эфиров пролекарств, представляющих собой бензильные карбонаты, из дигидроксифениколов (типа хлорамфеникола).
На Фиг.2А показана Схема 3 (феникол дигидрокси типа, Способ А) реакции синтеза сложных эфиров пролекарств, представляющих собой бензильные карбонаты, из дигидроксифениколов, с использованием менее чем одного мольного эквивалента реагента хлорформиата.
На Фиг.2В показана Схема 4 (феникол дигидрокси типа, Способ В) реакции синтеза пролекарств, представляющих собой бензильные монокарбонаты дигидроксифениколов (типа хлорамфеникола), с использованием метода защитных групп.
На Фиг.3А показана Схема 5 (феникол дигидрокси типа, Способ С) реакции синтеза пролекарств, представляющих собой бензильные монокарбонаты дигидроксифениколов (типа хлорамфеникола), с использованием метода селективного гидролиза.
На Фиг.3В показана Схема 6 реакции синтеза пролекарств, представляющих собой бензильные карбонаты флорфеникола и аналогов флорфеникола, с использованием X-(O)C-O-R4 реагентов, отличных от хлорформиатов. Группа "X" приводится в Таблице 1, ниже.
На Фиг.4 показан синтез карбоната феникола, соединения D, путем реакции исходного спирта А с триэтиламином, с получением хлорформиата В, с которым реагирует феникол С, с получением соединения D.
На Фиг.5 показан синтез бис(карбоната феникола), соединения F, путем реакции бисхлорформиата Е с субстратом С, с получением карбоната феникола - соединения F.
На Фиг.6 показан синтез карбоната феникола, соединения Н, путем реакции этилхлорформиата В с субстратом G и триэтиламином (не показан), с получением бензильного бис-карбоната феникола - соединения Н, бензильного карбоната 1 и первичного карбоната.
На Фиг.7а показана Схема 7а реакции синтеза бис-карбоната, где R4 отличен от R5.
На Фиг.7b показана Схема 7b реакции альтернативного синтеза бис-карбоната, где R4 отличен от R5.
Подробное описание изобретения
Соответственно, данное изобретение предоставляет карбонатную форму феникола, например, пролекарство флорфеникола. Такие карбонаты фениколов являются, в целом, плохо растворимыми в воде, но очень хорошо растворимы в других подходящих, не вызывающих раздражение органических растворителях, пригодных для введения путем инъекции, и такие карбонаты фениколов могут применяться для лечения и/или предупреждения бактериальных инфекций. Соединения, согласно данному изобретению, легко превращаются in vivo в свободные, активные антибиотические агенты.
Для более полного понимания настоящего изобретения приводятся следующие определения.
Предполагается, что использование сингулярных терминов для удобства описания, никоим образом, не является ограничением. Таким образом, например, упоминание "микроб" включает в себя упоминание одного или более таких микробов. Предполагается, что использование множественных терминов также не является ограничением, если иного не указано. Например, фраза, такая как "карбонатное производное феникола", относится к любому карбонатному производному феникола, установленному здесь, включая одно такое соединение само по себе, или комбинацию двух или более таких соединений, если иного не указано.
Использованный здесь термин "приблизительно" употребляется взаимозаменяемо с термином "около" и, как правило, означает, что значение находится в пределах двадцати процентов от указанного значения, если иного не оговорено.
Использованный здесь термин "пролекарство" означает соединение, которое является предшественником лекарственного вещества и которое, при введении субъекту, подвергается химическому превращению посредством метаболических или химических процессов, с получением активного лекарственного вещества, например, карбонат антибиотика феникола представляет собой пролекарство, которое высвобождает in vivo антибиотик феникол.
Использованный здесь термин "бензильный" относится к заместителю или присоединению заместителя, когда заместитель находится при или присоединение заместителя происходит при алифатическом насыщенном атоме углерода, непосредственно связанном с фенилом или замещенном фенильным кольцом. Термин бензильный карбонат означает карбонатный заместитель O-(O)C-OR, присоединенный в такое бензильное положение.
Использованный здесь термин "фармацевтическая композиция" относится к композиции соединения по изобретению, включая его сольваты (например, пролекарство флорфеникола), с фармацевтически приемлемым инертным наполнителем и/или носителем. Соединение по изобретению присутствует в носителе в количестве от около 1 до около 80 процентов, по весу. В конкретном варианте осуществления изобретения носителем является растворитель соединения по изобретению, который не вызывает раздражение живых тканей и который подходит для инъекций, как, например, некоторые органические растворители. Органические растворители значительно различаются по их вязкости, и в качестве компонентов композиции феникола и пролекарств фениколов они вносят вклад в вязкость конечной композиции. Поэтому органические растворители с более низкой вязкостью являются предпочтительными компонентами высококонцентрированных композиций фениколов и пролекарств фениколов. Например, спирты, такие как этиловый спирт, изопропиловый спирт, бензиловый спирт, глицеринформаль (например, равновесная смесь 1,3-диоксан-5-ола и 1,3-диоксан-4-ил метанола), низкомолекулярные простые моноэфиры этиленгликоля, представляют собой примеры растворителей с низкой вязкостью, подходящих для композиций, вводимых путем инъекций. Другие растворители с относительно низкой вязкостью, такие как сложные эфиры (бензилацетат, этиленгликоль - бис-ацетат, пропиленгликоль - бис-ацетат), простые эфиры (низкомолекулярные простые бис-эфиры этиленгликоля или пропиленгликоля) или амиды (2-метилпирролидинон, 2-пирролидинон) могут также применяться в качестве компонентов смеси растворителей, понижающих общую вязкость растворов пролекарств, представляющих собой карбонаты фениколов. Однако такие растворители или комбинации, содержащие такие растворители, обычно не обеспечивают достаточную растворимость исходных лекарственных веществ фениколов. Желаемые высокие концентрации фениколов в растворителях с низкой вязкостью или смесях растворителей, содержащих высокую долю растворителей с низкой вязкостью, могут все же быть достигнуты посредством применения пролекарств, представляющих собой бензильные карбонаты фениколов. Предпочтительным растворителем является бензиловый спирт, в комбинации с возможными, но не обязательными инертными наполнителями. Более предпочтительным является носитель, содержащий смесь растворителей триацетин/бензиловый спирт в соотношении 2:1 (об./об.).
Термин "инертный наполнитель" относится к инертному веществу, добавляемому к фармакологической композиции, чтобы облегчить введение активного ингредиента. Примеры инертных наполнителей, без ограничения, включают в себя, например, различные сахара и типы крахмала, производные целлюлозы, желатин, растительные масла и полиэтиленгликоли, и известные в данной области техники стабилизаторы, красители и тому подобное, при необходимости.
Термин "терапевтически эффективное количество", использованный здесь, относится к количеству пролекарства данного изобретения, которое будет достаточно быстро подвергаться гидролизу и в степенях, достаточных, чтобы обеспечить концентрацию активного феникола, при которой он может облегчить в некоторой степени один или несколько симптомов бактериальной инфекции у субъекта. В конкретном варианте осуществления изобретения терапевтически эффективное количество относится к тому количеству соединения, обладающего признаками изобретения, которое, при введении субъекту, доставляет активный антибиотик субъекту, например, феникол, с концентрацией в плазме, достаточной чтобы: (1) уменьшить и предпочтительно ликвидировать популяцию бактериальных клеток в организме субъекта; (2) ингибировать (то есть замедлить или предпочтительно остановить) пролиферацию бактериальных клеток; (3) ингибировать (то есть замедлить или предпочтительно остановить) распространение бактериальной инфекции; и/или (4) ослабить (предпочтительно устранить) один или более симптомов, связанных с инфекцией.
Термин "профилактически эффективное количество" относится к количеству пролекарства данного изобретения, которое, при введении животному или рыбе, приводит к концентрации соответствующего активного антибиотика в плазме, достаточной, чтобы значительно уменьшить вероятность и/или степень инфекции, обусловленной бактериями, которые чувствительны к этому активному антибиотику. Профилактически эффективное количество соединения данного изобретения, обладающего признаками изобретения, может также применяться после проведения предшествующего курса антибиотика, чтобы поддерживать пониженный уровень (или устранение) популяции бактериальных клеток в организме животного или рыбы.
"Метафилактика" - это своевременное массовое медикаментозное лечение целой группы животных с целью исключения или сведения к минимуму ожидаемых вспышек болезни, например, при высоком риске инфекции у одного или нескольких животных. В конкретном варианте осуществления изобретения большому риску подвержены телята с небольшим весом, перевозимые на большие расстояния совместно с другим крупным рогатым скотом, для которого неизвестны истории здоровья.
Использованный здесь термин "Минимальные ингибирующие концентрации" применяется взаимозаменяемо с "МИК". "МИК50" представляет собой концентрацию соединения (например, пролекарства данного изобретения), при которой ингибируется рост 50% изолята. Подобным образом, МИК90 представляет собой концентрацию соединения, при которой ингибируется рост 90% изолята.
Использованный здесь, в контексте синтеза соединения, обладающего признаками изобретении, термин "подходящий" растворитель относится к растворителю, в котором реагенты могут растворяться и который не будет участвовать в реакции неблагоприятным образом, либо путем его собственной реакции с одним или более компонентами реакционной смеси, либо препятствуя взаимодействию компонентов друг с другом. Для любой данной реакции выбор подходящего растворителя находится в пределах компетентности специалистов в данной области техники и может быть выполнен без чрезмерного экспериментирования.
Синтез соединений по изобретению
Следующие схемы реакций демонстрируют, как получают соединения по изобретению.
Схема 1.
Синтез пролекарств, представляющих собой бензильные карбонаты флорфеникола и аналогов флорфеникола, с использованием хлорформиатов.
В одном варианте осуществления изобретения, на Фиг.1А, показан удобный способ приготовления пролекарств, представляющих собой бензильные карбонаты, подходящий для фениколов, имеющих только одну бензильную гидроксигруппу (например, флорфеникол и его аналоги). Как показано, феникол, соединение (1), реагирует с соответствующем хлорформиатом, с получением бензильного карбоната (2), в подходящем растворителе, с катализатором или без него. R1, R2 и R4 всех соединений, представленных на схемах, представляют собой группы, определенные выше для соединения Формулы I. Подходящие растворители включают в себя, например, хлорированные растворители, такие как дихлорметан и 1,2-дихлороэтан; сложноэфирные растворители, такие как этилацетат, изопропилацетат, изоамилацетат, диацетат этиленгликоля, диацетат пропиленгликоля, глицеринтриацетат, простые моноэфирные растворители, такие как простой диэтиловый эфир, простой диизопропиловый эфир, простой метилтретбутиловый эфир; простые полиэфирные растворители, такие как простые эфиры этиленгликоля: диметиловый эфир этиленгликоля, простые эфиры диэтиленгликоля: простой диметиловый эфир диэтиленгликоля, простой диэтиловый эфир диэтиленгликоля; ацетали формальдегида, такие как диметоксиметан, диэтоксиметан, дибутоксиметан; простые циклические эфиры, такие как тетрнагидрофуран, 1,3-диоксолан, 1,4-диоксан; кетоны, такие как ацетон, метилэтилкетон, метилизобутилкетон; растворители, представляющие собой смешанные (простые и сложные) эфиры, как представлено простыми моноэфирами этилен- и диэтиленгликоля, такими как 2-метоксиэтилацетат, 2-этоксиэтилацетат, 2-(метоксиэтокси)этилацетат, 2-(этоксиэтокси)этилацетат.
Примеры, приведенные ниже, показывают применение тетрагидрофурана в качестве растворителя. Реакция превращения феникола в пролекарство, представляющее собой бензильный карбонат, возможно, но не обязательно, проводится при мольном (вплоть до троекратного) избытке реагента хлорформиата по отношению к фениколу, в присутствии катализатора или комбинации катализаторов и кислотного акцептора, в течение длительного реакционного времени и при повышенной температуре. Предпочтительные катализаторы включают в себя, например, 4-диметиламинопиридин, 4-метилпиридин и пиридин. Предпочтительные кислотные акцепторы включают в себя, например, триэтиламин, пиридин, карбонат натрия, бикарбонат натрия и карбонат калия. Реакцию предпочтительно проводят в течение периода времени, колеблющегося от около 0.5 до около 10 часов, и при температуре, колеблющейся от около 0°С до около 50°С.
Типично реакцию проводят путем добавления 1.5-2.0 эквивалентов хлорформиата в растворе тетрагидрофурана к раствору тетрагидрофурана, содержащему феникол, 1.0 эквивалент триэтиламина и 0.5 эквивалента 4-N,N-диметиламинопиридина, при 0°С и позволяя реакции пройти до конца. Непрореагировавший феникол (если остается после реакции) может быть полностью удален стандартными способами, известными в данной области техники, или возможно, но не обязательно, его оставляют в конечном очищенном веществе пролекарства, представляющего собой бензильный карбонат, для того чтобы обеспечить первоначальные повышенные уровни флорфеникола, сразу после введения.
Реагент хлорформиат получают, например, с помощью реакции соответствующего спирта с фосгеном или с эквивалентом фосгена (например, дифосгеном, трифосгеном). Преимущественно полученный неочищенный раствор хлорформиата может применяться на стадии образования карбоната без очищения. Альтернативно продажный хлорформиат может применяться на стадии образования карбоната, если доступен. Коммерческие источники хлорформиата включают, например, Aldrich и Lancaster.
Схема 2.
Синтез пролекарств фениколов типа хлорамфеникола (дигидроксифениколов), представляющих собой бис-карбонаты, образованные замещением бензильной и первичной гидроксильных групп.
В следующем варианте осуществления изобретения, как показано на Фиг.1В, сложные эфиры пролекарств, представляющих собой бензильные карбонаты, например, соединение (4), могут также быть получены из фениколов, например, соединение (3), несущих две гидроксильные группы (например, хлорамфеникол, тиамфеникол, цетофеникол), путем либо селективного превращения бензильной гидроксигруппы в соответствующую карбонатную составляющую пролекарства, либо путем превращения как бензильной, так и терминальной первичной гидроксигруппы в составляющие пролекарства, с образованием пролекарств, представляющих собой бис-карбонаты, образованные замещением бензильной и первичной гидроксильных групп.
Фениколы, несущие две гидроксигруппы (типа хлорамфеникола) могут быть превращены в пролекарства, представляющие собой бис-карбонаты, образованные замещением бензильной и первичной гидроксильных групп, путем обработки соответствующего феникола двумя или более эквивалентами соответствующего хлорформиата, применяя условия, подобные условиям, описанным выше для фениколов типа флорфеникола. В таких условиях превращение обеих функциональных гидроксигрупп может быть достигнуто одновременно, с получением пролекарств, представляющих собой бис-карбонаты, образованные замещением бензильной и первичной гидроксильных групп (Схема 2).
Схема 3.
Синтез пролекарств фениколов типа хлорамфеникола (дигидроксифениколов), представляющих собой бензильные монокарбонаты - Способ А
Как показано на Фиг.2А, пролекарства фениколов типа хлорамфеникола (дигидрокси, R1=NO2), представляющие собой бензильные моно-карбонаты, могут быть получены, применяя менее чем один мольный эквивалент реагента хлорформиата и выделяя желаемое пролекарство, представляющее собой бензильный карбонат, из смеси конечных моно- и бис-карбонатов, с помощью кристаллизации, применяя растворители, показанные в Таблице 5, или, например, с помощью хроматографии на силикагеле (Схема 3).
Схема 4.
Синтез пролекарств фениколов типа хлорамфеникола (дигидроксифениколов), представляющих собой бензильные монокарбонаты - Способ В
Как показано на Фиг.2В, пролекарства фениколов типа хлорамфеникола (дигидрокси, Ri=NO2), представляющие собой бензильные моно-карбонаты, могут быть получены с использованием метода защитных групп, селективно защищая функциональную первичную гидроксигруппу, за чем следует реакция с хлорформиатом, селективно вводящая карбонатную составляющую пролекарства в бензильное положение (Схема 4).
Защитной группой, применяемой для защиты первичной гидроксигруппы, может быть сложноэфирная группа, такая как формиат, ацетат, бензоат, пивалоат, карбонатная группа, такая как трет-бутоксикарбонат, силильная защитная группа, такая как триметилсилил, трет-бутилдиметилсилил. Удаление защитной группы, после введения желаемой карбонатной составляющей пролекарства в бензильное положение молекулы феникола, может выполняться химически, применяя условия, подходящие для удаления конкретной группы (Protective Groups in Organic Synthesis; Theodora W.Greene, Peter G.M.Wuts; 3rd Edition, June 1999, John Wiley & Sons Inc) или с помощью селективного ферментативного гидролиза, позволяющего удалить защитную группу без воздействия на бензильную карбонатную составляющую пролекарства (Схема 4).
Схема 5.
Синтез пролекарств фениколов типа хлорамфеникола (дигидроксифениколов), представляющих собой бензильные монокарбонаты - Способ С
Как показано на Фиг.3А, приготовление пролекарств фениколов типа хлорамфеникола (дигидрокси, R1=NO2), представляющих собой бензильные моно-карбонаты, может быть выполнено путем получения сначала пролекарства, представляющего собой бензильный/первичный бис-карбонат, за чем следует селективный гидролиз функциональной карбонатной группы, замещающей первичную гидроксигруппу, осуществляемый химически или ферментативно (Схема 5).
Схема 6.
Синтез пролекарств, представляющих собой бензильные карбонаты флорфеникола и аналогов флорфеникола, использующий Х-(O)С-O-R4 реагенты, отличные от хлорформиатов.
Как показано на Фиг.3B, реагенты, отличные от хлорформиатов, также могут применяться для приготовления пролекарств, представляющих собой бензильные карбонаты фениколов. Реагенты, в которых уходящие группы отличны от хлорид-анионов, могут применяться для того, чтобы вводить карбонатную составляющую аналогичным образом, как в реакции с хлорформиатом, в присутствии катализатора или без добавления катализатора. Многочисленные примеры таких реагентов, которые могут применяться для таких превращений, встречаются в литературе, и некоторые приводятся ниже.
В соответствии с Фиг.3В, Схема 6, группа Х может представлять собой любую из групп, приведенных в Таблице 1, как изложено ниже. Для каждой такой группы приводятся репрезентативные источники, каждый из которых включен в настоящий документ в виде ссылки.
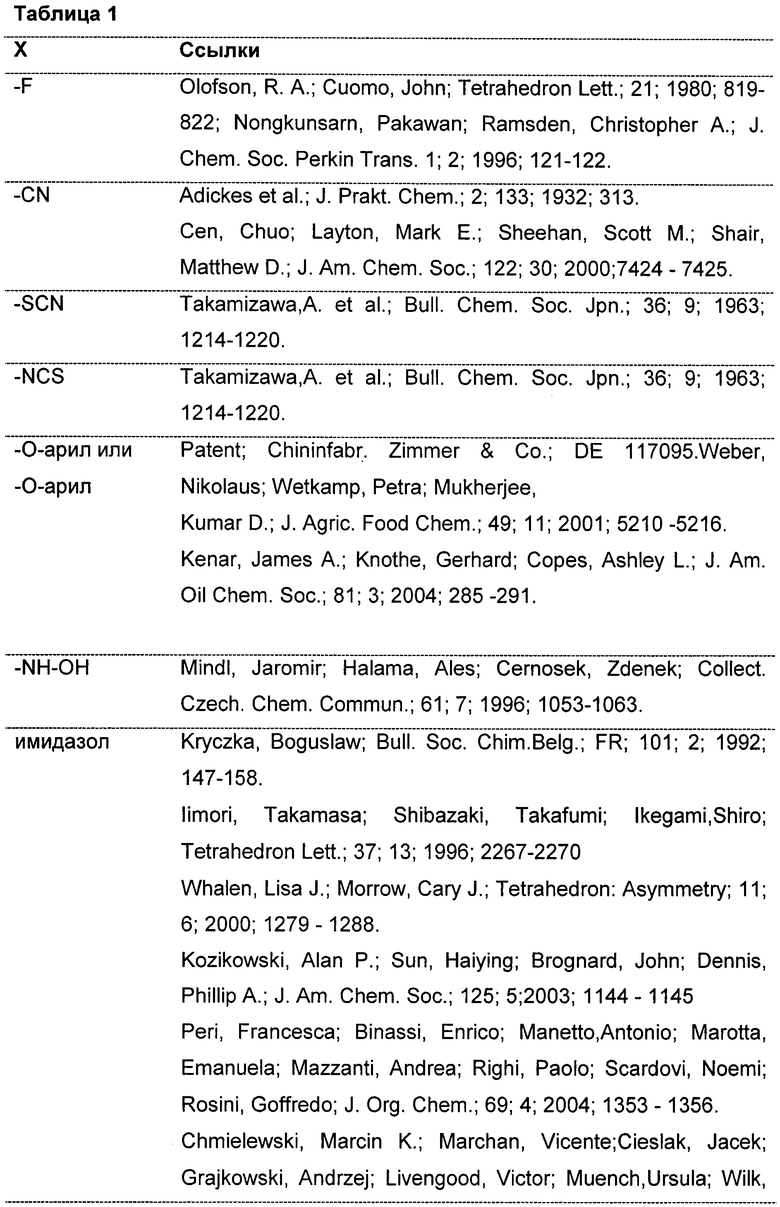
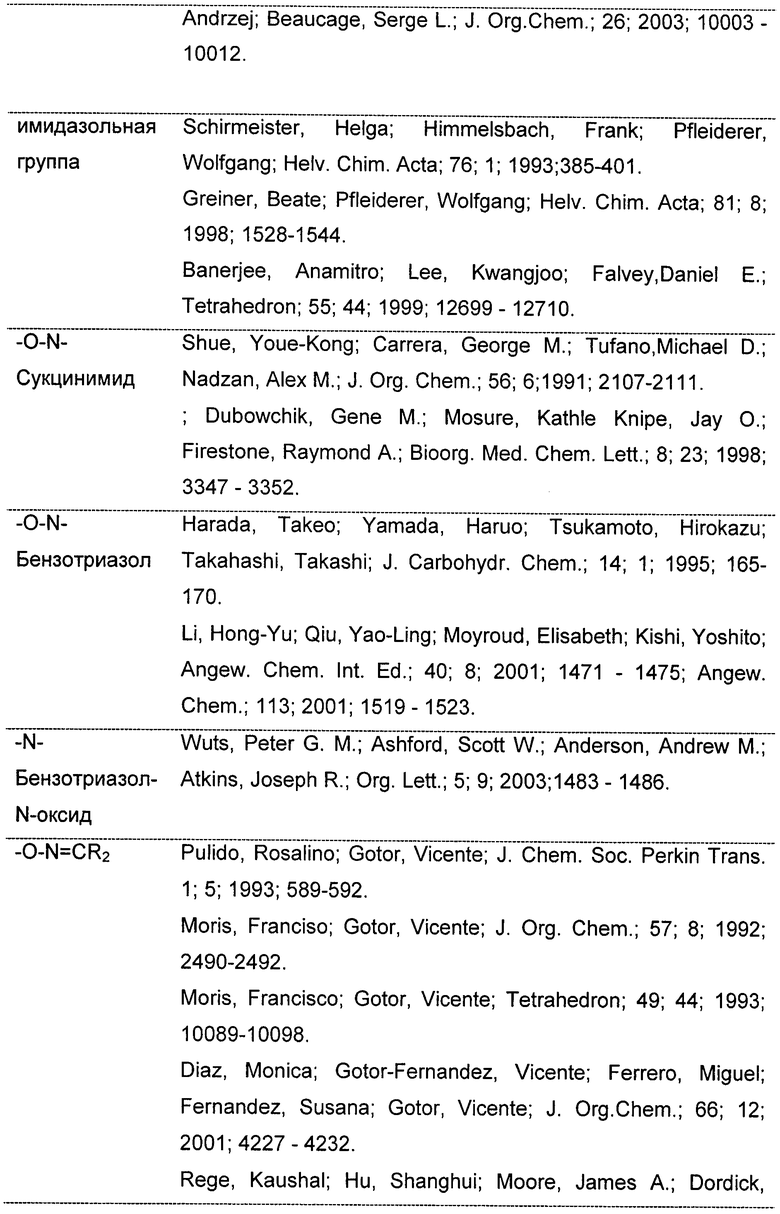

Схемы 7а и 7b.
Синтез пролекарств фениколов типа хлорамфеникола (дигидроксифениколов), представляющих собой бис-карбонаты, образованные замещением бензильной и первичной гидроксильных групп различными карбонатными заместителями.
Как показано на Фиг.7А, получение пролекарств фениколов типа хлорамфеникола (дигидроксифениколов), представляющих собой бис-карбонаты, образованные замещением бензильной и первичной гидроксильных групп различными карбонатными заместителями, может быть осуществлено, как показано на схеме 7а, применяя монокарбонаты (соединение 6), полученные с помощью способов А-С, описанных выше, и подвергая их второй реакции с хлорформиатом Cl-(O)C-O-R5 (R4≠R5) или с реагентом типа X-(O)C-O-R5 (R4≠R5), описанным выше для Схемы 6.
В качестве альтернативы, желаемая функциональная карбонатная группа пролекарства может быть введена сначала в положение первичной функциональной гидроксигруппы, с получением промежуточного продукта, представляющего собой карбонат феникола, образованный замещением первичной гидроксигруппы (соединение 5), который затем вводят в реакцию с хлорформиатом Cl-(O)C-O-R4 (R4≠R5) или в реакцию с реагентом типа X-(O)C-O-R4 (R4≠R5), описанным выше для схемы 6, с получением желаемого пролекарства, представляющего собой бис-карбонат, образованный замещением первичной и бензильной гидроксильных групп (приведено на Фиг.7В, Схема приготовления 7b). В этой конкретной схеме синтеза можно удобно воспользоваться преимуществом ожидаемой, более высокой реакционной способности первичной функциональной гидроксигруппы.
Способы применения соединений по изобретению
Данное изобретение также предоставляет методы введения профилактически эффективных количеств для предупреждения, то есть профилактики, и/или для метафилактики, в качестве необходимости и/или в установленном порядке, и/или для лечения инфекций, например, бактериальных инфекций, которые могут быть предупреждены и/или вылечены и т.д., с помощью антибиотического агента или агентов, высвобождаемых in vivo соединениями по изобретению. Животное, которое будут таким образом защищать или лечить, предпочтительно, но не исключительно, относится к классу позвоночных и более предпочтительно к классу млекопитающих, птиц или рыб. Любое из соединений по изобретению, или подходящая комбинация таких соединений может вводиться животному - субъекту. Подходящие животные-субъекты включают в себя диких животных, домашний скот (например, выращиваемый для получения мяса, молока, масла, яиц, меха, шкуры, перьев и/или шерсти), вьючных животных, подопытных животных, домашних животных, так же как и животных, выращиваемых для или в зоопарках, диких местах обитания и/или цирках.
В конкретном варианте осуществления изобретения животным является млекопитающее. Млекопитающие, которых будут лечить, включают в себя приматов, например, обезьян, высших приматов и возможно, но не обязательно, людей. Другие субъекты, относящиеся к млекопитающим, включают в себя животных из семейства бычьих (например, крупный рогатый скот или молочные коровы), животных из семейства свиньих (например, кабаны или свиньи), животных из семейства овечьих (например, козы или овцы), животных из семейства лошадиных (например, лошади), животных из семейства собачьих (например, собаки), животных из семейства кошачьих (например, домашние кошки), верблюдов, оленей, антилоп, кроликов, подопытных кроликов и грызунов (например, белки, крысы, мыши, песчанки и хомяки), животных из семейства китообразных (киты, дельфины, морские свиньи), ластоногих животных (тюлени, моржи). Класс птиц включают в себя семейство Пластинчатоклювые (Anatidae) (например, лебеди, утки и гуси), семейство Голубиные (Columbidae) (например, горлицы и голуби), семейство Фазановые (Phasianidae) (например, серая куропатка, шотландская куропатка и индюки), семейство Thesienidae (например, домашние цыплята), Семейство Попугаи (Psittacines) (например, длиннохвостые попугаи, попугаи ара и попугаи), охотничье-промысловых птиц, и бескилевых птиц (например, страусы). Птицы, которые подлежат лечению или защите с помощью соединений по изобретению могут относиться к промышленному или непромышленному птицеводству. Они включают в себя, например, представителей семейства Пластинчатоклювые (Anatidae), таких как лебеди, гуси и утки, семейства Голубиные (Columbidae), например, горлицы и голуби, такие как домашние голуби, семейства Фазановые (Phasianidae), например, серая куропатка, шотландская куропатка и индюки, семейства Thesienidae, например, домашние цыплята, семейства Попугаи (Psittacines), например, длиннохвостые попугаи, попугаи ара и попугаи, например, выращиваемых для рынка домашних животных или коллекционирования, среди прочего.
В целях данного изобретения, термин "рыба", как следует понимать, включает в себя, без ограничения, надотряд (Teleosti), то есть Костистые рыбы. Как отряд лососеобразные (Salmoniformes) (который включает в себя семейство Лососевые (Salmonidae)), так и отряд Окунеобразные (Perciformes), (который включает в себя семейство Центрарховые (Centrarchidae)) входят в состав надотряда Костистые рыбы (Teleosti). Примеры рыб - реципиентов включают в себя семейство Лососевые (Salmonidae), семейство Серрановые (Serranidae), семейство Спаровые (Sparidae), семейство Цихловые (Cichlidae), семейство Центрарховые (Centrarchidae), Простипома (Parapristipoma trilineatum) и Плекостомус (Plecostomus spp), помимо прочего.
Более того, примеры потенциальных рыб - реципиентов включают в себя семейство Лососевые (Salmonidae), семейство Серрановые (Serranidae), семейство Спаровые (Spandae), семейство Цихловые (Cichlidae), семейство Центрарховые (Centrarchidae), Простипому (Parapristipoma trilineatum) и Плекостомус (Plecostomus spp). Дополнительные примеры рыб, которые подлежат лечению с помощью соединения, обладающего признаками изобретения, приведены в таблице ниже только с целью иллюстрации.
Семейство лососевые




Следующие примеры рыб, которых можно лечить, включают в себя, но без ограничения, зубатку, морского окуня, тунца, палтуса, арктического гольца, осетра, калкана, камбалу, палтуса, карпа, тилапию, полосатого окуня, угря, морского леща, желтохвостика, сериолу, каменного окуня и молочную рыбу.
Предполагается, что другие животные, которые также получают пользу от методов по изобретению включают в себя животных из отряда сумчатые (как, например, кенгуру), класса пресмыкающиеся (Рептилии) (таких как черепахи, выращиваемые на ферме), класса ракообразные (таких как омары, крабы, мелкие ракообразные и креветки), отряда моллюсков (такие как осьминоги и ракообразные) и другие экономически важные виды животных, для которых методы по изобретению безопасны и эффективны при лечении и/или предупреждении инфекции.
В другом варианте осуществления изобретения субъектом является домашнее животное. В целях данного изобретения термин "домашнее" животное, как следует понимать, включает в себя домашних кошек (животных из семейства Кошачьих), собак (семейство Собачьих), род кроликов, лошадей (семейство Лошадиных), подопытных кроликов, грызунов (например, белок, крыс, мышей, песчанок и хомяков), приматов (например, обезьян) и представителей семейства птичьих, такие как голуби, горлицы, попугаи, длиннохвостые попугаи, попугаи ара, канарейки и тому подобное.
Фармацевтические композиции
Соединение данного изобретения, или физиологически приемлемый сольват соединения, может вводиться животному как таковое, при необходимости этого, или может вводиться в фармацевтической композиции, в которой вышеупомянутые вещества смешиваются с подходящим инертным наполнителем (инертными наполнителями). Технологии приготовления и введения лекарственных средств могут быть обнаружены в Remington's Pharmacological Sciences, Mack Publishing Co., Easton, PA, последнее издание. Композиции и технологии, обсуждаемые в Remington, прежде всего, относятся к применению на людях; однако они легко могут быть модифицированы для применения на пациентах, не относящихся к людям, с помощью методов, хорошо известных специалистам в области ветеринарии.
Если соединения, описанные здесь, вводятся в качестве компонента корма для животных или растворяются или суспендируются в питьевой воде, предусматриваются композиции, в которых активный агент (агенты) диспергирован в инертном носителе или разбавителе. Инертным носителем является носитель, который не реагирует с соединением по изобретению и который может вводиться безопасно для животных. Предпочтительно носителем для введения с кормом является носитель, который является или может быть ингредиентом рациона животного.
Подходящие композиции включают в себя предварительно смешиваемые с кормом композиции или добавки, в которых активный ингредиент присутствует в относительно больших количествах и которые подходят для непосредственного кормления животных или для добавления в корм, либо сразу, либо после стадии разбавления или смешивания. Типичные носители или разбавители, подходящие для таких композиций, включают в себя, например, сухую гранулированную барду, кукурузную муку, муку из цитрусовой пульпы, остатки ферментации, измельченные раковины устриц, помолотую пшеницу, фильтрат мелассы, гранулят кукурузы, перемолотые бобы, пригодные для кормления, соевую крупу, дробленый известняк и тому подобное. Соединение по изобретению диспергируется в носителе методами, такими как растирание, перемешивание, размалывание, галтование и тому подобное. Композиции, содержащие от около 0.05 до около 5.0% или от около 0.005 до около 2.0%, по весу, соединений по изобретению, особенно подходят в качестве композиций, предварительно смешиваемых с кормом. Кормовые добавки, которыми непосредственно кормят животное, включают в себя от около 0.0002 до 0.3%, по весу, соединения по изобретению.
Такие добавки добавляются в корм животного в количестве, необходимом для получения концентрации активного соединения в конечном корме, желательной для уничтожения или контроля чувствительных микроорганизмов. Хотя желаемая концентрация соединения, обладающего признаками изобретения, будет изменяться в зависимости от факторов, упомянутых ранее, так же как и от конкретной применяемой производной, соединение обычно добавляют в корм в концентрациях от около 0.0001 до 0.02% или от около 0.00001 до около 0.002%, для того чтобы достичь желаемого противомикробного результата.
Пути введения
Использованный здесь термин "вводить" или "введение" относится к доставке соединения или сольвата соединения данного изобретения или фармацевтической композиции, содержащей соединение данного изобретения, в организм с целью лечения или предупреждения микробных инфекций.
Подходящие пути введения могут включать в себя, без ограничения, пероральное, ректальное, местное, трансмукозальное, внутримышечное, подкожное, интрамедуллярное, интратекальное, внутрижелудочковое. внутривенное введение, введение в стекловидное тело, внутрибрюшинное, интраназальное, ушное или внутриглазное введение. Предпочтительными путями введения являются пероральный и парентеральный.
Альтернативно можно вводить соединение локально, а не системным образом, например, приготавливая его в виде целебной мази или композиции, наносимой локально, которая наносится прямо на инфицированную поверхность, или вводя соединение путем инъекции прямо в инфицированную ткань. В любом случае может применяться композиция продолжительного высвобождения.
Таким образом, введение соединений изобретения или их фармацевтически приемлемых сольватов, в чистом виде или в подходящей фармацевтической композиции, может осуществляться с помощью любого из приемлемых способов введения или агентов, служащих в подобных целях. Пути введения могут быть любыми, известными средним специалистам в данной области техники. Соединения по изобретению вводятся тем, кто нуждается в этом, в любой форме, принятой в данной области техники, т.е. есть твердой, полутвердой форме, форме лиофилизованного порошка или жидкой лекарственной форме, таких как, например, таблетки, суппозитории, пилюли, мягкие эластичные или твердые желатиновые капсулы, порошки, растворы, суспензии или аэрозоли или тому подобное, в единичной дозировочной форме или мультидозных формах, подходящих для простого введения точных доз. Композиции будут включать в себя обычные фармацевтические носители или инертные наполнители и соединение по изобретению, в качестве активного агента, и, кроме того, могут включать другие лекарственные средства, фармацетические агенты, носители, адъюванты и т.д.
Состав/Способы приготовления композиций
Фармацевтические композиции данного изобретения могут производиться с помощью процессов, хорошо известных в данной области техники, например, применяя ряд хорошо известных процессов, таких как смешивание, растворение, грануляция, изготовление драже, растирание в порошок, эмульгация, инкапсуляция, включение или лиофилизация. Композиции могут быть приготовлены в сочетании с одним или более физиологически приемлемыми носителями, включающими инертные наполнители и вспомогательные вещества, которые способствуют преобразованию активных соединений в препараты, которые могут применяться в фармацевтических целях. Надлежащая композиция зависит от выбранного пути введения.
Для инъекций, включая, без ограничения, внутривенную, внутримышечную и подкожную инъекцию, соединения изобретения могут быть приготовлены в виде растворов в полярных растворителях, включающих, без ограничения, пропиленгликоль, спирты, такие как бензиловый спирт или этанол, полиэтиленгликоль, и N-метил-2-пирролидон, 2-пирролидон, другие пирролидоны, N,N-диметилацетамид, N,N-диметилформамид, диметилсульфоксид, ацетон, триацетин, глицеролформаль, возможно воду, в концентрациях до 10%, так же как и комбинации любых из вышеописанных инертных наполнителей или другие вещества, известные средним специалистам в данной области техники. Для трансмукозального введения, пенетранты, подходящие для барьеров, которые будут преодолеваться, используются в рецептуре. Такие пенетранты, в целом, известны в данной области техники.
Дозировка
Терапевтически эффективное количество относится к количеству соединения, эффективному для предупреждения и/или минимизации микробной инфекции, и/или лечения, облегчения и/или уменьшения симптомов, обусловленных микробной инфекцией. Определение терапевтически эффективного количества находится в пределах компетенции специалистов в данной области техники, особенно принимая во внимание изложенное здесь.
Для любого соединения, применяемого в методах изобретения, терапевтически эффективное количество может быть первоначально оценено исходя из известных свойств антибиотического агента, который высвобождается пролекарствами, представляющими собой соединения, обладающие признаками изобретения. Затем можно разработать дозировку для применения на животных моделях, такую, чтобы достигнуть циркулирующей концентрации, интервал которой находится в пределах от и выше значения минимальной ингибирующей концентрации ("МИК"), уже известной в данной области техники. Такая информация может затем быть использована для более точного определения дозировок, полезных для пациентов.
Токсичность и терапевтическая эффективность соединений, описанных здесь, может быть определена с помощью стандартных фармацевтических процедур с культурами клеток или экспериментальными животными. Например, минимальная ингибирующая концентрация ("МИК") и летальная доза для 50% группы лечения ("LD50"), для конкретного соединения, могут быть определены с помощью методов, хорошо известных в данной области техники. Например, МИК определяется в соответствии с нормативами, установленными Институтом клинических и лабораторных стандартов (CLSI)
Полученные данные могут применяться для определения интервала доз полезных для пациентов. Доза, конечно, может изменяться в зависимости от лекарственной формы и пути введения препарата. Точная рецептура, путь введения и дозировка препарата могут выбираться исходя из индивидуального клинического состояния пациента (смотрите, например, Fingl et al., 1975, "The Pharmacological Basis of Therapeutics", глава 1, стр.1). В общих чертах, соединения по изобретению вводятся животному, нуждающемуся в таком лечении, в дозах, эффективных для достижения и/или поддержания концентраций высвобожденного антибиотика в плазме и тканях тела на уровнях, эффективных в целях лечения или уничтожения чувствительных инфекционных микроорганизмов, или для предупреждения новых инфекций в течение периода времени, достаточного для достижения желаемой цели. Квалифицированный специалист в данной области техники оценит, что следующие предполагаемые интервалы доз регулируются на основании клинического отклика, а также принимая во внимание относительное количество антибиотика феникола, высвобождаемое из каждого соответствующего пролекарства, также как и мольное отношение феникола к пролекарству, представляющему собой (моно или бис) карбонат. Например, при подкожном введении соединения по изобретению, как правило, вводятся в дозе, колеблющейся от около 1 мг до около 150 мг/кг веса тела. Частота введения может также находиться в пределах от одной дозы в день до многократных доз в день. При пероральном введении доза предпочтительно будет вводиться один раз в день.
Интервал и величина дозировки устанавливаются индивидуально для обеспечения уровней соединения в плазме, достаточных для поддержания концентрации выше или равной МИК, или любого другого желаемого уровня. Такие уровни в плазме часто упоминаются как минимальные эффективные концентрации (МЭК). МЭК будет варьироваться для каждого соединения, но ее можно предположить исходя из данных in vitro, например, концентрации, необходимой для ингибирования более чем 80% микробной популяции. МЭК может быть определена, применяя анализы, описанные здесь. Дозировки, необходимые для достижения МЭК, будут зависеть от индивидуальных характеристик соединения и/или животного и/или пути введения. Анализы HPLC (жидкостная хроматография высокого давления) или биоисследования могут проводиться для определения концентраций соединения и/или его соответствующего активного продукта в плазме.
Интервалы дозировок могут быть определены, применяя значение МЭК. Соединения следует вводить в соответствии с режимом, который поддерживает уровни в плазме выше МЭК в течение 10-90% времени.
В случаях местного введения или избирательного поглощения эффективная локальная концентрация лекарственного вещества может быть не связана с концентрацией в плазме, и другие процедуры, известные в данной области техники, могут применяться для определения надлежащего интервала и величины дозировки.
Композиции могут вводиться один раз в день или делиться на несколько приемов. Часто только одной дозы будет достаточно для лечения инфекции. В некоторых случаях для лечения животного будут необходимы одна доза и следующая за ней через 48 часов вторая доза. Точная доза зависит от стадии и серьезности инфекции, чувствительности инфекционного микроорганизма к композиции и индивидуальных характеристик вида животного, подлежащего лечению, что будет оценено по достоинству средним специалистом в данной области техники.
Вводимое количество композиции будет, конечно, зависеть от пациента, подлежащего лечению, патогенных микроорганизмов или бактерий, вызывающих инфекцию, серьезности инфекции, метода введения, то есть перорального, внутривенного, местного и т.д., и предписания врача, ветеринара и т.д.
Соединение по изобретению будет, как правило, вводиться в интервале доз от 1 мг до 150 мг/кг веса тела крупного рогатого скота, при использовании подкожного пути введения. Предпочтительно доза колеблется в пределах от около 20 мг до около 70 мг/кг веса тела. Более предпочтительно доза составляет около 60 мг/кг. Однако, когда соединение по изобретению вводится внутримышечно (маршрут IM), доза предпочтительно вводится дважды, причем вторая доза вводится через около 24 - около 48 часов после введения первой дозы.
Для свиней соединение по изобретению будет, как правило, вводиться в интервале доз от около 10 мг до около 150 мг/кг веса тела. Предпочтительно доза находится в интервале от 20 мг до 70 мг/кг веса тела. Как правило, первая внутримышечная инъекция будет сопровождаться второй инъекцией через около 24 до около 48 часов.
Для домашней птицы соединение по изобретению будет, как правило, вводиться в интервале доз от около 10 мг до 150 мг/кг веса тела. При пероральном введении пролекарство будут вводить в питьевой воде ежедневно, столько, сколько указано клинически, например, в течение от около трех до около семи дней.
Введение водным животным
Данное изобретение также предоставляет методы уничтожения, уменьшения или предупреждения бактериальных инфекций у рыб и, возможно, у водных беспозвоночных животных. Такие методы включают в себя введение эффективного количества соединения, обладающего признаками изобретения, водному животному, нуждающемуся в этом. Введение эффективного количества соединения, обладающего признаками изобретения, как правило, осуществляют либо при кормлении животного, либо, погружая животное или популяцию животных в раствор, который содержит эффективное количество активного соединения в растворе. Кроме того, необходимо понимать, что соединение по изобретению можно вводить путем внесения лекарственного вещества в водоем или другое водное пространство, содержащее животное, и позволяя животному всасывать соединение через его жабры или же позволяя дозе соединения, обладающего признаками изобретения, впитываться. Для индивидуального лечения специфических животных, например конкретной рыбы, например, в ветеринарной или аквариумной практике, прямая инъекция или инъекция препаратов с механизмом осмотического высвобождения, содержащих соединение по изобретению, само по себе или в комбинации с другими агентами представляют собой возможный метод введения соединения по изобретению.
Доза соединений по изобретению, которая эффективна для уменьшения, уничтожения или предупреждения бактериальной инфекции у рыб или других водных видов животных, может определяться в плановом порядке ветеринаром, применяя параметры и методы, рассмотренные ранее для других типов животных, хотя она может изменяться в зависимости от вида рыб, подлежащих лечению, конкретных микроорганизмов, связанных с инфекцией, и степени инфекции. Указания для аквакультур: соединения по изобретению будут, как правило, вводиться в дозах от около 1 мг/кг до около 70 мг/кг, предпочтительно от 10 мг/кг до 30 мг/кг. Подходящие пути введения включают: внутривенное, подкожное, внутримышечное введение и/или введение путем обрызгивания или погружения водных видов, при необходимости, и/или путем добавления соединения непосредственно в воду, в удерживающем объеме.
При пероральном введении соединения по изобретению предпочтительно вводятся в дозах, определенных выше, от около 10 до около 15 дней.
Несмотря на то, что активный ингредиент может вводиться отдельно от корма, предполагается, в предпочтительном аспекте, что активный ингредиент будет включен в корм для рыб. Корм для рыб, содержащий лекарственное вещество, может быть приготовлен путем включения количества соединения данного изобретения в коммерчески доступный корм для рыб, подходящего для достижения желаемых уровней дозировок. Количество соединения данного изобретения, включенное в корм для рыб, будет зависеть от интенсивности кормления рыб. При интенсивности кормления рыб около 0.2%-4% от биомассы в день корм предпочтительно содержит лекарственное вещество в количестве от около 50 до 10,000 мг на кг корма и более предпочтительно от около 100 до 2,000 мг на кг корма.
Хотя соединения данного изобретения могут быть включены в кормовую смесь до момента таблетирования, содержащий лекарственное средство корм, предпочтительно формируют, покрывая таблетки корма соединением данного изобретения.
Любые виды рыб, включая разновидности, обитающие в пресной и соленой воде, также как и беспозвоночные водные виды животных, перечисленные здесь выше, могут быть обработаны соединениями данного изобретения для лечения или предупреждения бактериальных инфекций.
Комбинации с другими средствами и способы лечения
Также предполагается введение пролекарств, представляющих собой соединения по изобретению в комбинации, одновременно или последовательно (например, в той же самой композиции или в отдельных композициях) с другими полезными, известными в данной области техники, лекарственными средствами. Такие лекарственные средства включают в себя, например, другие микробиоциды, такие как антибиотики, противогрибковые средства, противовирусные средства, средства для уничтожения паразитов и тому подобное, также, как например, биологически активные добавки, кормовые добавки и тому подобное. Например, предполагается введение любого стандартного, известного в данной области техники феникола (не пролекарства) в комбинации с соединениями по изобретению. Такие фениколы включают в себя флорфеникол, также известный как D-(трео)-1-(4-метилсульфонилфенил)-2-дихлорацетамидо-3-фтор-1-пропанол. Другим предпочтительным антибиотиком является D-(трео)-1-(4-метилсульфонилфенил)-2-дифторацетамидо-3-фтор-1-пропанол. Другим полезным антибиотиком является тиамфеникол. Процессы производства этих антибиотиков и промежуточные продукты, полезные в таких процессах, описываются в патентах США US No. 4311857; 4582918; 4973750; 4876352; 5227494; 4743700; 5567844; 5105009; 5382673; 5352832 и 5663361, включенных в настоящий документ путем ссылки. Другие аналоги флорфеникола и/или пролекарства уже были раскрыты, и такие аналоги также могут применяться в композициях и методах данного изобретения [смотрите, например, опубликованную заявку на патент США US No. 2004/0082553 и опубликованную заявку на патент США US No. 2005/0182031, обе из которых включены в данный документ во всей полноте путем ссылки]. Когда антибиотиком является флорфеникол, концентрация флорфеникола типично составляет от около 10% до около 50% в/о, предпочтительные концентрации находятся в пределах от около 20% до около 40% в/о, причем даже более предпочтительная концентрация составляет, по меньшей мере, 30% в/о.
Другим полезным антибиотиком для применения в комбинации с соединениями по изобретению является тилмикозин. Тилмикозин представляет собой макролидный антибиотик с химическим названием 20-дигидро-20-деокси-20-(цис-3,5-диметилпиперидин-1-ил)-десмикозин, который, как сообщают, раскрывается в патенте US No. 4820695, включенном в настоящий документ путем ссылки. В патенте US No. 4820695 также раскрывается инъецируемая водная композиция, содержащая 50% (по объему) пропиленгликоля, 4% (по объему) бензилового спирта и 50-500 мг/кг активного ингредиента. Тилмикозин может присутствовать в виде основания или в виде фосфата. Как уже было обнаружено, тилмикозин полезен для лечения респираторных инфекций, особенно инфекций крупного рогатого скота, вызванных Pasteurella haemolytica, при введения путем инъекции в течение 4 дней лечения. Соответственно, тилмикозин может применяться для лечения, например, пневмонии у новорожденных телят и бычьего респираторного заболевания. Когда тилмикозин присутствует, он присутствует в количестве от 1% до около 50%, предпочтительно от 10% до около 50% и в конкретном варианте осуществления изобретения в количестве 30%.
Другим полезным антибиотиком для применения в комбинации с соединениями по изобретению является тулатромицин. Тулатромицин может быть получен в соответствии с процедурами, изложенными в опубликованном патенте США US No. 2003/0064939 А1, который включен в настоящий документ во всей полноте путем ссылки. Тулатромицин может присутствовать в инъецируемых лекарственных формах, при уровнях концентраций, находящихся в пределах от около 5.0% до около 70% по весу. Тулатромицин наиболее желательно вводить в дозировках от около 0.2 мг на кг веса тела в день (мг/кг/день) до около 200 мг/кг/день, в виде однократной дозы или дробных доз (то есть от 1 до 4 доз в день) и более предпочтительно вводить 1.25, 2.5 или 5 мг/кг один раз или дважды в неделю, хотя вариации будут непременно происходить в зависимости от вида, веса и состояния субъекта, подлежащего лечению. Тулатромицин может присутствовать в инъецируемых лекарственных формах при уровнях концентраций, находящихся в пределах от около 5.0% до около 70% по весу.
Другими полезными антибиотиками для применения в комбинации с соединениями по изобретению являются антибиотики семейства флуороквинолоны, такие как, например, энрофлоксацин, данофлоксацин, дифлоксацин, орбифлоксацин и марбофлоксацин. В случае энрофлоксацина он может вводиться в концентрации около 100 мг/мл. Данофлоксацин может присутствовать в концентрации около 180 мг/мл.
Другие полезные макролидные антибиотики для применения в комбинации с соединениями по изобретению включают в себя соединения из класса кетолиды или, более конкретно, азалиды. Такие соединения описываются, например, в патентах US No. 6514945, 6472371, 6270768, 6437151 и 6271255 и в патентах US No. 6239112, 5958888 и US No. 6339063 и 6054434, каждый из которых включен в настоящий документ во всей полноте путем ссылки.
Другие полезные антибиотики для применения в комбинации с соединениями по изобретению включают в себя тетрациклины, в частности хлортетрациклин и окситетрациклин.
Другие антибиотики могут включать бета-лактамы, такие как один из пенициллинов, например, пенициллин G, пенициллин К, ампициллин, амоксициллин, или комбинацию амоксицилина с клавулановой кислотой или другие бета-лактамные ингибиторы. Дополнительные, заслуживающие особого внимания, бета-лактамы включают в себя цефалоспорины, такие как, например цефтиофур, цефкином и т.д. Концентрация цефалоспорина в композиции данного изобретения варьируется, по выбору, от около 1 мг/кг до 500 мг/кг.
Кроме того, данное изобретение дополнительно включает в себя композицию для лечения микробной и паразитической инфекции у животных, которая содержит один или более из вышеописанных антибиотиков, подмешанных и/или находящихся в комбинации с одним или более из соединений по изобретению, и произвольный носитель и/или инертный наполнитель.
Для всех методов и соединений по изобретению, описанных здесь, также предполагается, что установленные соединения охотно применяются в комбинации с одним или более хорошо известными средствами уничтожения или контроля различных типов паразитов, включая, например, все экто- и эндопаразиты, описанные здесь. Таким образом, хотя соединения и методы по изобретению предпочтительны по сравнению с ранее известными средствами и методами применения ранее известных средств в определенных необязательных вариантах осуществления изобретения, предполагается их применение в комбинации, одновременно или последовательно (например, в одной и той же композиции или в отдельных композициях) с другими известными в данной области техники средствами или комбинациями таких известных в данной области средств, применяемых для уничтожения или контроля различных типов вредителей.
Эти дополнительные агенты для применения в комбинации с соединениями по изобретению включают в себя, например, известные в данной области техники противоглистные средства, такие как, например авермектины (например, ивермектин, моксидектин, милбемицин), бензимидазолы (например, албендазол, триклабендазол), салициланилиды (например, клозантел, оксиклозанид), замещенные фенолы (например, нитроксинил), пиримидины (например, пирантел), имидазотиазолы (например, левамизол) и празиквантел.
Дополнительные, известные в данной области техники средства уничтожения или контроля вредителей, для применения в комбинации с соединениями по изобретению, включают в себя органофосфатные пестициды. Этот класс пестицидов имеет очень широкий спектр действия, например, в качестве инсектицидов и в определенных случаях имеет противоглистную активность. Органофосфатные пестициды включают в себя, например, дикротофос, тербуфос, диметоат, диазинон, дисульфотон, трихлорфон, азинфосметил, хлорпирифос, малатион, оксидеметонметил, метамидофос, ацефат, этил паратион, метил паратион, мевинфос, форат, карбофентион, фозалон с указанием только некоторых из таких соединений. Также предполагается включение комбинаций методов и соединений по изобретению с карбоматными пестицидами, включая, например, карбарил, карбофуран, алдикарб, молинат, метомил и т.д., так же как комбинаций с пестицидами типа органохлорина. Кроме того, предполагается включать комбинации с биологическими пестицидами, включая, например, репелленты, пиретрины (так же как их синтетические разновидности, например, аллетрин, ресметрин, перметрин, тралометрин) и никотин, который часто применяется в качестве акарицида. Другие предполагаемые комбинации представляют собой комбинации со смешанными пестицидами, включающими в себя: бактерии Bacillus thuringiensis, хлоробензилат, формамидины (например, амтитаз), соединения меди, например, гидроксид меди, оксихлорид и сульфат меди, цифлутрин, циперметрин, дикофол, эндосульфан, эсфенвалерат, фенвалерат, ламбда-цихалотрин, метоксихлор и серу.
Кроме того, для всех методов и новых соединений, описанных здесь, более того, предполагается, что указанные соединения могут легко применяться в комбинации с синергистами, такими как пиперонилбутоксид (РВО) и трифенилфосфат (ТРР); и/или с регуляторами роста насекомых (IGR) и аналогами ювенильного гормона (JHA), такими как дифлубензурон, циромазин, метопрен и т.д., обеспечивая, таким образом, как начальный, так и непрерывный контроль паразитов (на всех стадиях развития насекомого, включая стадию яйцеклеток) у субъекта - животного, так же как и в окружающей среде субъекта - животного.
Комбинации с циклодиенами, рианией, КТ-199 и/или с предшествующими хорошо известными в данной области техники противоглистными средствами, такими как авермектины (например, ивермектин, моксидектин, милбемицин), бензимидазолы (например, албендазол, триклабендазол), салициланилиды (например, клозантел, оксиклозанид), замещенные фенолы (например, нитроксинил), пиримидины (например, пирантел), имидазотиазолы (например, левамизол), празиквантел и некоторые органофосфаты, такие как нафталофос и пираклофос, так же, как предполагается, будут использоваться в таких комбинациях.
В частности, дополнительными противопаразитарными средствами, применяемыми в объеме данного изобретения, являются предпочтительно соединения класса авермектины. Как указано выше, соединения семейства авермектины представляют собой ряд очень сильных противопаразитарных средств, как известно, полезных против широкого спектра эндопаразитов и эктопаразитов у животных.
Предпочтительным соединением для применения в комбинации с соединениями по изобретению, в объеме данного изобретения, является ивермектин. Ивермектин представляет собой полусинтетическую производную авермектина, его, как правило, получают в виде смеси, по меньшей мере, 80% 22,23-дигидроавермектина В1а и менее чем 20% 22,23-дигидроавермектина B1b. Ивермектин раскрывается в патенте США US No. 4199569, включенном в настоящий документ путем ссылки. Ивермектин применяется с середины 80-х годов, в качестве противопаразитарного средства для лечения различных паразитов у животных и паразитических заболеваний.
Абамектин представляет собой авермектин, который раскрывается, как авермектин В1а/B1b в патенте US No. 4310519, который включен в настоящий документ в полном объеме путем ссылки. Абамектин включает в себя, по меньшей мере, 80% авермектина В1а и не более чем 20% авермектина B1b.
Другим предпочтительным авермектином является дорамектин, также известный как 25-циклогексилавермектин B1. Структура и получение дорамектина раскрываются в патенте US No. 5089480, который включен в настоящий документ в полном объеме путем ссылки.
Другим предпочтительным авермектином является моксидектин. Моксидектин, также известный как LL-F28249 альфа, известен из патента US No. 4916154, который включен в настоящий документ в полном объеме путем ссылки.
Другим предпочтительным авермектином является селамектин. Селамектин представляет собой 25-циклогексил-25-де(1-метилпропил)-5-деокси-22,23-дигидро-5-(гидроксиимино)-авермектин B1 моносахарид.
Милбемицин, или В41, представляет собой вещество, которое выделяют из ферментационного бульона штамма Streptomyces, продуцирующего милбемицин. Микроорганизм, условия ферментации и процедуры выделения более полно описываются в патенте US No. 3950360 и патенте US No. 3984564.
Эмамектин (4"-деокси-4"-эпи-метиламиноавермектин B1), который может быть приготовлен, как описано в патенте US No. 5288710 или 5399717, представляет собой смесь двух гомологов, 4"-деокси-4"-эпи-метиламиноавермектина В1а и 4"-деокси-4"-эпи-метиламиноавермектина B1b. Предпочтительно применяется соль эмамектина. Неограничивающие примеры солей эмамектина, которые могут применяться в данном изобретении, включают в себя соли, описанные в патенте US No. 5288710, например, соли бензойной кислоты, замещенной бензойной кислоты, бензолсульфоновой кислоты, лимонной кислоты, фосфорной кислоты, винной кислоты, малеиновой кислоты и тому подобного. Наиболее предпочтительно солью эмамектина, применяемой в данном изобретении, является бензоат эмамектина.
Эприномектин имеет химическое название 4"-эпи-ацетиламино-4"-деоксиавермектин B1. Эприномектин был специально разработан для применения на всех классах крупного рогатого скота и любых возрастных группах. Он стал первым авермектином, который показал широкий спектр действия как против эндо-, так и эктопаразитов, оставляя минимальные остатки в мясе и молоке. Он имеет дополнительное преимущество, будучи весьма эффективным при местной доставке.
Композиции данного изобретения возможно, но не обязательно, содержат комбинации одного или более следующих противопаразитарных соединений.
Противопаразитарные соединения имидазо[1,2-b]пиридазин, как описано в опубликованной заявке на патент US No. 2005/0182059, включенной в настоящий документ путем ссылки. Противопаразитарные соединения 1-(4-моно и ди-галометилсульфонилфенил)-2-ациламино-3-фторпропанол, как описано в опубликованной заявке на патент US No. 2005/0182139, включенной в настоящий документ путем ссылки. Противопаразитарные производные соединения простой эфир оксима трифторметансульфонанилида, как описано в опубликованной заявке на патент US No. 2006/0063841, включенной в настоящий документ путем ссылки. Противопаразитарное соединение фенил-3-(1Н-пиррол-2-ил)акрилонитрил, как описано в опубликованной заявке на патент US No. 2006/0128779, включенной в настоящий документ путем ссылки. Противопаразитарные производные соединения N-[(фенилокси)фенил]-1,1,1-трифторметансульфонамид и N-[(фенилсульфанил)фенил]-1,1,1-трифторметансульфонамид, как описано в заявке на патент US No. 11/448421, зарегистрированной 7 июня 2006 г., включенной в настоящий документ путем ссылки. Противопаразитарное соединение N-фенил-1,1,1-трифторметансульфонамид гидразон, как описано во временной заявке на патент US No. 60/790893, зарегистрированной 10 апреля 2006 г., включенной в настоящий документ путем ссылки.
Композиции данного изобретения могут также применяться в комбинации с флукицидом. Подходящий флукицид включает в себя, например, триклабендазол, фенбендазол, албендазол, клорсулон и оксибендазол. Будет оценено по достоинству, что приведенные выше комбинации могут, более того, включать комбинации антибиотиков, противопаразитарных средств и соединений с активностью против двуустки.
В дополнение к вышеописанным комбинациям также предполагается предоставление комбинаций методов и соединений по изобретению, как описано здесь, с другими лекарственными средствами для лечения животных, такими как микроэлементы, противовоспалительные средства, противоинфекционные средства, гормоны, дерматологические препараты, включая антисептики и дезинфицирующие средства, и иммунобиологические средства, такие как вакцины и антисыворотки для предупреждения заболевания.
Например, такие противоинфекционные средства включают в себя один или более антибиотиков, которые возможно, но не обязательно, вводятся совместно в процессе лечения, применяющего соединения или методы по изобретению, например, в объединенной композиции и/или в раздельных лекарственных формах. Известные в данной области техники антибиотики, подходящие для этой цели, включают, например, антибиотики, перечисленные здесь выше.
Более того, также предполагается, что методы и соединения по изобретению будут применяться преимущественно в комбинации, одновременно или последовательно с известными в данной области техники лекарственными средствами для лечения животных, такими как микроэлементы, витамины, противовоспалительные средства, противоинфекционные средства и тому подобное, в одной и той же или различных композициях.
Подходящие противовоспалительные средства включают в себя, например, как стероидные, так и нестероидные противовоспалительные средства. Нестероидные противовоспалительные средства, включая смеси их рацематов или индивидуальные энантиомеры, где применимо, могут включать ибупрофен, флурбипрофен, кетопрофен, аклофенак, диклофенак, алоксиприн, апроксен, аспирин, дифлунизал, фенопрофен, индометацин, мефенамовую кислоту, напроксен, фенилбутазон, пироксикам, салициламид, салициловую кислоту, сулиндак, дезоксисулиндак, теноксикам, трамодол, кеторалак, флуфенизал, салсалат, триэтаноламина салицилат, аминопирин, антипирин, оксифенбутазон, апазон, синтазон, флуфенамовую кислоту, клониксерил, клониксин, меклофенамовую кислоту, флюниксин, колхицин, демеколцин, аллопуринол, оксипуринол, бензидамин гидрохлорид, димефадан, индоксол, интразол, мимбан гидрохлорид, паранилин гидрохлорид, тетридамин, бензиндопирин гидрохлорид, флупрофен, ибуфенак, напроксол, фенбуфен, цинхофен, дифлумидон натрия, фенамол, флутиазин, метазамид, летимид гидрохлорид, нексеридин гидрохлорид, октазамид, молиназол, неоцинчофен, нимазол, проксазол цитрат, тезикам, тезимид, толметин и трифлумидат.
В конкретном варианте осуществления изобретения соединение данного изобретения применяется в комбинации с флуниксином [смотрите, например, патент US No. 6790867 В2, который включен в настоящий документ в полном объеме путем ссылки.] В родственном варианте осуществления изобретения данное изобретение предоставляет фармацевтические композиции, содержащие соединение данного изобретения и флуниксин.
Стероидные противовоспалительные средства включают, например, глюкокортикоидные средства, такие как дексаметазон, кортизон, гидрокортизон, преднизон, беклометазон, бетаметазон, флюнизолид, метилпреднизон, параметазон, преднизолон, триамцинолом, алклометазон, амцинонид, клобетазол, флудрокортизон, дифлурозон диацетат, флуоцинолон ацетонид, флюорометолон, флурандренолид, халцинонид, медризон, мометазон и их фармацевтически приемлемые соли и смеси из них.
Упаковка
Композиции могут при желании, быть представлены в упаковке или дозаторе, как например, набор, одобренный FDA, который может содержать одну или более единиц лекарственных форм, содержащих активный ингредиент. Упаковка может, например, включать металлическую или пластиковую фольгу, как, например, блистерная упаковка. Упаковка или дозатор могут сопровождаться инструкциями по применению. Упаковка или дозатор могут также сопровождаться информацией, связанной с контейнером, в форме, ранее установленной правительственным агентством, регулирующим производство, применение и продажу фармацевтических препаратов, информация которого отражает одобрение агентством формы композиций или их применение на людях или животных. Такая информация, например, может предоставляться в виде маркировки, принятой Управлением по контролю за пищевыми продуктами и лекарственными средствами США (FDA) для лекарств, продаваемых по рецепту, или вкладыша в одобренный продукт. Композиции, содержащие соединение изобретения, основанные на совместимом фармацевтическом носителе, могут также быть приготовлены, помещены в подходящую емкость и маркированы для лечения указанного состояния. В необязательном варианте осуществления изобретения упаковка включает стеклянные или пластиковые ампулы или другие емкости, содержащие несколько доз.
Примеры
Следующие примеры приводятся с целью иллюстрации определенных вариантов осуществления данного изобретения, но не с целью ограничения, также они не должны быть истолкованы как ограничение объема изобретения каким-либо образом.
Примеры 1-25
Приготовление пролекарств, представляющих собой карбонаты флорфеникола
Синтез пролекарств, представляющих собой карбонаты флорфеникола и его аналогов.
В соответствии с Фиг.4 раствор исходного спирта А (0.68 М, 1.78 мольных эквивалентов) и триэтиламина (0.68 М, 1.78 мольных эквивалентов) в безводном тетрагидрофуране добавляли капля по капле в раствор трифосгена (0.48 М, 0.64 мольных эквивалентов) в безводном тетрагидрофуране, при 0°С, в атмосфере азота. Полученную смесь перемешивали при 0°С в течение 30 минут и затем быстро отфильтровали через бумажный фильтр для удаления соли аммония. Отфильтрованный раствор хлорформиата, раствор В, использовали для следующей реакции карбонизации без дальнейшего очищения.
Свежеприготовленный раствор хлорформиата В или раствор коммерчески доступного хлорформиата в безводном тетрагидрофуране В (0.34 М, 1.78 мольных эквивалентов) перенесли в капельную воронку и 2/3 раствора добавили капля по капле в безводный раствор тетрагидрофурана, содержащий соответствующий феникол С (0.64 М, 1 мольный эквивалент), 4-N,N-диметиламинопиридин (0.5 мольных эквивалентов) и триэтиламин (1.5 мольных эквивалента), при 0°С, в атмосфере азота. Смесь перемешивали при 0°С в течение 30 минут и ход реакции контролировали с помощью тонкослойной хроматографии. Дополнительный раствор хлорформиата добавляли, если реакция не прошла до конца, на что указывала тонкослойная хроматография, и реакцию проводили до исчезновения исходного вещества. Полученный раствор быстро отфильтровывали через бумажный фильтр для удаления соли аммония. Фильтрат концентрировали и добавляли этилацетат для растворения неочищенного продукта. Полученный раствор последовательно промывали 1 М HCl(водный), насыщенным раствором NaHCO3(водный) и насыщенным раствором NaCl(водный), за чем следовала быстрая фильтрация через слой силикагеля и Na2SO4. Фильтрат концентрировали и полученный неочищенный продукт очищали с помощью флэш-хроматографии на силикагелевой колонке или перекристаллизации (применяя растворители, перечисленные в Таблице 5) с выделением чистого карбоната - пролекарства D. Следующие соединения, под номером примера, получили с помощью вышеописанного метода:
Пример 1
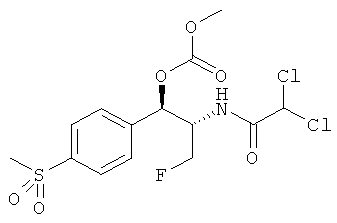
(1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропилметил карбонат.
Неочищенный продукт перекристаллизовывали из смеси растворителей метанол/вода с выделением приведенного в заглавии продукта в виде белого твердого вещества, выход которого составил 93%; Н1-ЯМР (ДМСО-d6), δ=32 чнм (синглет, 3Н), 3.70 чнм (синглет, 3Н), 4.3-4.7 чнм (мультиплет, 3Н), 5.9 чнм (дублет, 1Н), 6.4 чнм (синглет, 1Н), 7.6 чнм (дублет, 2Н), 7.9 чнм (дублет, 2Н), 9.05 чнм (дублет, 1Н); масс-спектр 438.0 (М+Na).
Пример 2
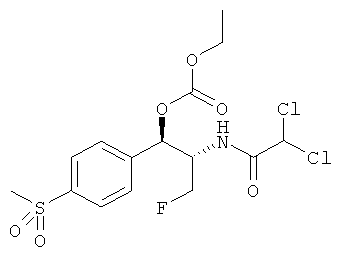
(1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропилэтил карбонат.
Раствор флорфеникола (250 г, 0.7 моль), 4-диметиламинопиридина (42 г, 0.35 моль), триэтиламина (130 мл, 0.91 моль) в 1.2 л тетрагидрофурана перемешивали при 0-5°С, в то время как очищенный этилхлорформиат (80 мл, 0.83 моль) добавляли капля по капле через воронку для введения. Реакция прошла, что установили с помощью осаждения соли -триэтиламин гидрохлорида. Смесь перемешивали при комнатной температуре в течение 30 минут и соль удаляли из смеси с помощью фильтрации. Фильтрат концентрировали, добавляли 600 мл этилацетата и раствор промывали с помощью 1 М HCl (2×200 мл), а затем с помощью насыщенного раствора NaCl (200 мл) и отфильтровывали через слой Na2SO4/силикагель. Фильтрат концентрировали, и неочищенное масло кристаллизовали из 450 мл изопропанола, с выделением чистого продукта, приведенного в заглавии (286 г). Точка плавления 110-112°С; Н1-ЯМР (ДМСО-d6), δ=1.2 чнм (триплет, 3 Н), 3.2 чнм (синглет, 3Н), 4.1 чнм (квадруплет, 2Н), 4.3-4.7 чнм (мультиплет, 3Н), 5.9 чнм (дублет, 1Н), 6.4 чнм (синглет, 1Н), 7.6 чнм (дублет, 2Н), 7.9 чнм (дублет, 2Н), 9.2 чнм (дублет, 1Н); масс-спектр 452.0 (М+Na).
Пример 3
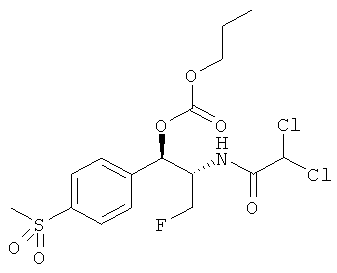
(1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропилпропил карбонат.
Неочищенный продукт кристаллизовали из изопропанола с выделением приведенного в заглавии продукта в виде твердого белого вещества, выход которого составил 91%. Н1-ЯМР (ДМСО-d6), δ=0.85 чнм (триплет, 3Н), 1.58 чнм (hex, 2Н), 3.2 чнм (синглет, 3Н), 4.1 чнм (триплет, 2Н), 4.3-4.7 чнм (мультиплет, 3Н), 5.9 чнм (дублет, 1Н), 6.4 чнм (синглет, 1Н), 7.6 чнм (дублет, 2Н), 7.9 чнм (дублет, 2Н), 9.2 чнм (дублет, 1Н); масс-спектр 466.0 (М+Na).
Пример 4
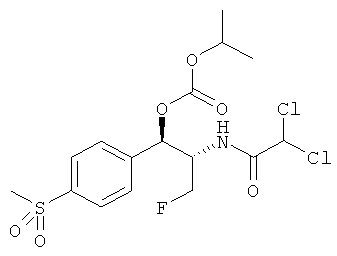
(1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропилизопропил карбонат.
Неочищенный продукт кристаллизовали из изопропанола, с выделением приведенного в заглавии продукта в виде твердого белого вещества, выход которого составил 92%. H1-ЯМР (ДМСО-d6), δ=1.2 чнм (два дублета, 6Н), 3.2 чнм (синглет, 3Н), 4.3-4.7 чнм (мультиплет, 3Н), 4.75 чнм (секстет, 1Н), 5.9 чнм (дублет, 1Н), 6.4 чнм (синглет, 1Н), 7.6 чнм (дублет, 2Н), 7.9 чнм (дублет, 2Н), 9.0 чнм (дублет, 1Н); масс-спектр 466.0 (М+Na).
Пример 5
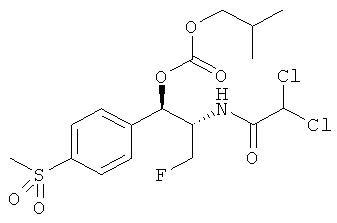
(1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропилизобутил карбонат.
Неочищенный продукт кристаллизовали из смеси растворителей изопропанол/этанол, с выделением приведенного в заглавии продукта в виде твердого белого вещества, выход которого составил 92%. Н1-ЯМР (ДМСО-d6), δ=0.85 чнм (дублет, 6Н), 1.85 чнм (секстет, 1 Н), 3.2 чнм (синглет, 3Н), 4.3-4.7 чнм (мультиплет, 3Н), 5.9 чнм (дублет, 1Н), 6.45 чнм (синглет, 1Н), 7.6 чнм (дублет, 2Н), 7.9 чнм (дублет, 2Н), 9.05 чнм (дублет, 1Н); масс-спектр 480.0 (М+Na).
Пример 6
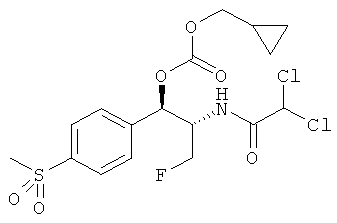
Циклопропилметил (1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропил карбонат.
Неочищенный продукт очищали с помощью колоночной гель-хроматографии, за чем следовала кристаллизация из смеси растворителей этилацетат/гексан, с выделением приведенного в заглавии продукта в виде твердого белого вещества, выход которого составил 72%. Н1-ЯМР (ДМСО-d6), δ=0.25 чнм (дублет дублетов, 2Н), 0.55 чнм (дублет дублетов, 2Н), 1.05 (мультиплет, 1Н), 3.2 чнм (синглет, 3Н), 3.9 чнм (дублет, 2Н), 4.3-4.7 чнм (мультиплет, 3Н), 5.9 чнм (дублет, 1Н), 6.45 чнм (синглет, 1Н), 7.6 чнм (дублет, 2Н), 7.9 чнм (дублет, 2Н), 9.05 чнм (дублет, 1 Н); масс-спектр 477.9 (М+Na).
Пример 7
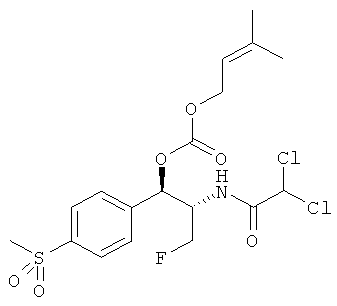
(1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропил 3-метилбут-2-енил карбонат.
Неочищенный продукт очищали с помощью колоночной гель-хроматографии, с выделением приведенного в заглавии продукта в виде белой пены, выход которого составил 80%. H1-ЯМР (ДМСО-d6), δ=1.65 чнм (синглет, 3Н), 1.70 чнм (синглет, 3Н), 3.2 чнм (синглет, 3Н), 4.25-4.7 чнм (мультиплет, 5Н), 5.25 чнм (триплет, 1Н), 59 чнм (дублет, 1Н), 6.45 чнм (синглет, 1Н), 7.6 чнм (дублет, 2Н), 7.9 чнм (дублет, 2Н), 9.05 чнм (дублет, 1Н); масс-спектр 491.8 (М+Na).
Пример 8
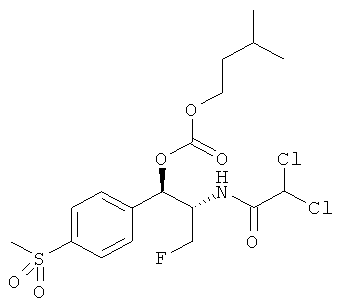
(1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропилизопентил карбонат.
Неочищенный продукт перекристаллизовали из смеси растворителей этилацетат/гексан, с выделением приведенного в заглавии продукта в виде твердого белого вещества, выход которого составил 85%. Н1-ЯМР (ДМСО-d6), δ=0.85 чнм (дублет, 6Н), 1.45 чнм (мультиплет, 2Н), 1.60 чнм (секстет, 1 Н), 3.2 чнм (синглет, 3Н), 4.10 чнм (мультиплет, 2Н), 4.3-4.7 чнм (мультиплет, 3Н), 5.9 чнм (дублет, 1Н), 6.45 чнм (синглет, 1Н), 7.6 чнм (дублет, 2Н), 7.9 чнм (дублет, 2Н), 9.05 чнм (дублет, 1Н); масс-спектр 494.1 (М+Na).
Пример 9
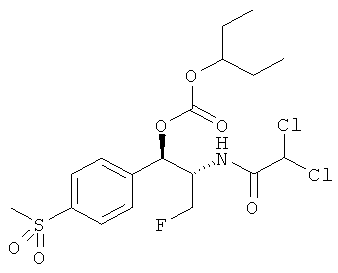
(1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропилпентан-3-ил карбонат.
Неочищенный продукт очищали с помощью колоночной гель-хроматографии, с выделением приведенного в заглавии продукта в виде твердого белого вещества, выход которого составил 73%. Н1-ЯМР (ДМСО-d6), δ=0.8 чнм (дублет триплетов, 6Н), 1.5 чнм (мультиплет, 4Н), 3.2 чнм (синглет, 3Н), 4.3-4.7 чнм (мультиплет, 4Н), 5.95 чнм (дублет, 1Н), 6.45 чнм (синглет, 1Н), 7.6 чнм (дублет, 2Н), 7.9 чнм (дублет, 2Н), 9.05 чнм (дублет, 1Н); масс-спектр 493.9 (М+Na).
Пример 10
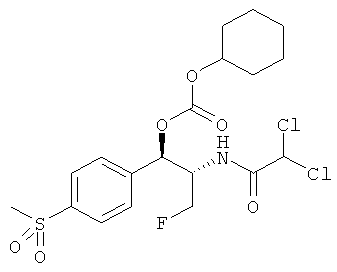
Циклогексил (1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропил карбонат.
Неочищенный продукт очищали с помощью колоночной гель-хроматографии, с выделением приведенного в заглавии продукта в виде твердого белого вещества, выход которого составил 75%. Н1-ЯМР (ДМСО-d6), δ=1.1-1.9 чнм (мультиплет, 10Н), 3.2 чнм (синглет, 3Н), 4.3-4.65 чнм (мультиплет, 4Н), 5.95 чнм (дублет, 1Н), 6.45 чнм (синглет, 1Н), 7.6 чнм (дублет, 2Н), 7.9 чнм (дублет, 2Н), 9.05 чнм (дублет, 1Н); масс-спектр 505.0 (М+Na).
Пример 11
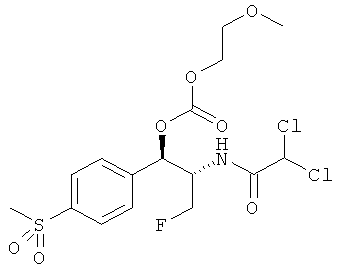
(1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропил 2-метоксиэтил карбонат.
Неочищенный продукт очищали с помощью колоночной гель-хроматографии, с выделением приведенного в заглавии продукта в виде полутвердого белого вещества, выход которого составил 78%. Н1-ЯМР (ДМСО-d6), δ=3.15 чнм (синглет, 3Н), 3.25 чнм (синглет, 3Н), 3.5 чнм (мультиплет, 2Н), 4.2 чнм (мультиплет, 2Н), 4.3-4.7 чнм (мультиплет, 3Н), 5.95 чнм (дублет, 1Н), 6.45 чнм (синглет, 1Н), 7.6 чнм (дублет, 2Н), 7.9 чнм (дублет, 2Н), 9.05 чнм (дублет, 1Н); масс-спектр 481.9 (М+Na).
Пример 12
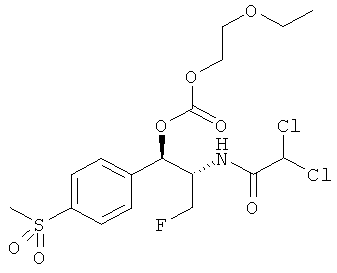
(1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропил 2-этоксиэтил карбонат.
Неочищенный продукт очищали с помощью колоночной гель -хроматографии, с выделением приведенного в заглавии продукта в виде полутвердого белого вещества, выход которого составил 33%. H1-ЯМР (ДМСО-d6), δ=1.05 чнм (триплет, 3Н), 3.15 чнм (синглет, 3Н), 3.4 чнм (квадруплет, 2Н), 3.55 чнм (мультиплет, 2Н), 4.2 чнм (мультиплет, 2Н), 4.3-4.7 чнм (мультиплет, 3Н), 5.95 чнм (дублет, 1Н), 6.45 чнм (синглет, 1Н), 7.6 чнм (дублет, 2Н), 7.9 чнм (дублет, 2Н), 9.05 чнм (дублет, 1Н); масс-спектр 496.0 (М+Na).
Пример 13
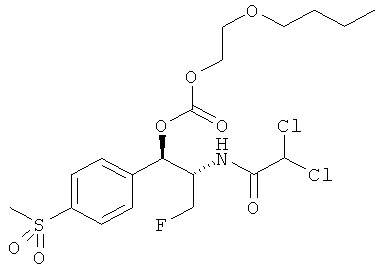
(1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропил 2-бутоксиэтил карбонат.
Неочищенный продукт очищали с помощью колоночной гель-хроматографии, с выделением приведенного в заглавии продукта в виде полутвердого белого вещества, выход которого составил 93%. Н1-ЯМР (ДМСО-d6), δ=0.85 чнм (триплет, 3Н), 1.25 чнм (мультиплет, 2Н), 1.45 чнм (мультиплет, 2Н), 3.15 чнм (синглет, 3Н), 3.35 чнм (триплет, 2Н), 3.55 чнм (мультиплет, 2Н), 4.2 чнм (мультиплет, 2Н), 4.3-4.7 чнм (мультиплет, 3Н), 5.95 чнм (дублет, 1Н), 6.45 чнм (синглет, 1Н), 7.6 чнм (дублет, 2Н), 7.9 чнм (дублет, 2Н), 9.05 чнм (дублет, 1Н); масс-спектр 524.0 (М+Na).
Пример 14
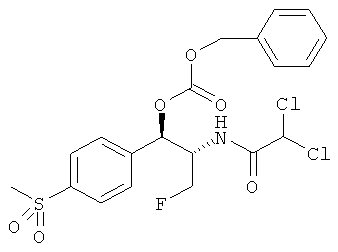
Бензил (1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропил карбонат.
Неочищенный продукт кристаллизовали из смеси растворителей изопропанол/этанол, с выделением приведенного в заглавии продукта в виде твердого белого вещества, выход которого составил 88%. Н1-ЯМР (ДМСО-d6), δ=3.2 чнм (синглет, 3Н), 4.3-4.7 чнм (мультиплет, 3Н), 5.15 чнм (синглет, 2Н), 5.9 чнм (дублет, 1Н), 6.4 чнм (синглет, 1Н), 7.38 чнм (синглет, 5Н), 7.6 чнм (дублет, 2Н), 7.9 чнм (дублет, 2Н), 9.05 чнм (дублет, 1Н); масс-спектр 514.0 (М+Na).
Пример 15
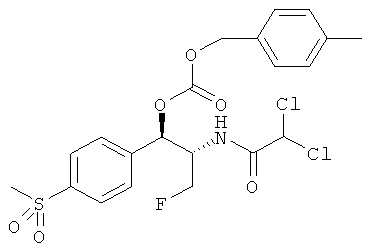
(1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропил 4-метилбензил карбонат.
Неочищенный продукт очищали с помощью колоночной гель-хроматографии, с выделением приведенного в заглавии продукта в виде белой пены, выход которого составил 73%. Н1-ЯМР (ДМСО-d6), δ=2.3 чнм (синглет, 3Н), 3.2 чнм (синглет, 3Н), 4.3-4.7 чнм (мультиплет, 3Н), 5.07 чнм (синглет, 2Н), 5.9 чнм (дублет, 1Н), 6.4 чнм (синглет, 1Н), 7.15 чнм (дублет, 2Н), 7.25 чнм (дублет, 2Н), 7.6 чнм (дублет, 2Н), 7.9 чнм (дублет, 2Н), 9.05 чнм (дублет, 1Н); масс-спектр 528.0 (М+Na).
Пример 16
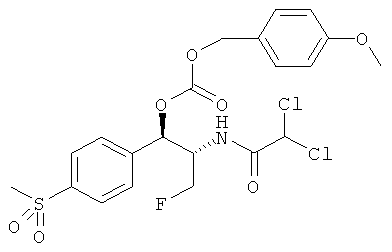
(1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропил 4-метоксибензил карбонат.
Неочищенный продукт очищали с помощью колоночной гель-хроматографии, с выделением приведенного в заглавии продукта в виде полутвердого белого вещества, выход которого составил 41%. Н1-ЯМР (ДМСО-d6), δ=3.2 чнм (синглет, 3Н), 3.75 чнм (синглет, 3Н), 4.3-4.7 чнм (мультиплет, 3Н), 5.05 чнм (синглет, 2Н), 5.9 чнм (дублет, 1Н), 6.4 чнм (сингпет, 1 Н), 6.9 чнм (дублет, 2Н), 7.25 чнм (дублет, 2Н), 7.6 чнм (дублет, 2Н), 7.9 чнм (дублет, 2Н), 9.05 чнм (дублет, 1Н); масс-спектр 543.9 (М+Na).
Пример 17
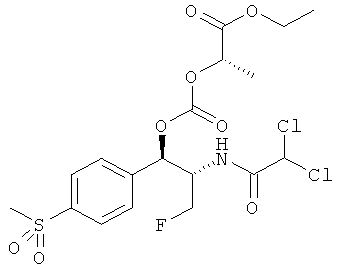
(S)-этил 2-(1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропокси)карбонилокси)пропаноат.
Неочищенный продукт очищали с помощью колоночной гель-хроматографии, с выделением приведенного в заглавии продукта в виде полутвердого белого вещества, выход которого составил 71%. Н1-ЯМР (ДМСО-d6), δ=1.15 чнм (триплет, 3Н), 1.4 чнм (дублет, 3Н), 3.2 чнм (синглет, 3Н), 4.15 чнм (квадруплет, 2Н), 4.3-4.7 чнм (мультиплет, 3Н), 4.95 чнм (квадруплет, 1Н), 5.98 чнм (дублет, 1Н), 6.42 чнм (синглет, 1Н), 7.6 чнм (дублет, 2Н), 7.9 чнм (дублет, 2Н), 9.05 чнм (дублет, 1Н); масс-спектр 523.9 (М+Na).
Пример 18
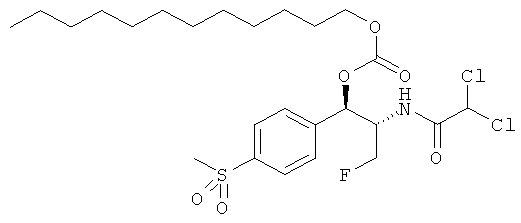
(1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропил додецил карбонат.
Неочищенный продукт очищали с помощью колоночной гель-хроматографии, с выделением приведенного в заглавии продукта в виде полутвердого белого вещества, выход которого составил 35%. Н1-ЯМР (CDCl3), δ=0.9 чнм (триплет, 3Н), 1.2-1.4 чнм (мультиплет, 18Н), 1.65-1.75 (мультиплет, 2Н), 3.1 чнм (синглет, 3Н), 4.1-4.6 чнм (мультиплет, 5Н), 5.95 чнм (синглет, 1Н), 6.05 чнм (дублет, 1Н), 6.95 чнм (дублет, 1Н), 7.6 чнм (дублет, 2Н), 7.95 чнм (дублет, 2Н).
Пример 19
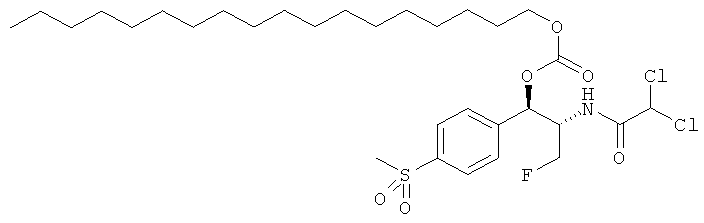
(1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропилоктадецил карбонат.
Неочищенный продукт очищали с помощью колоночной гель-хроматографии, с выделением приведенного в заглавии продукта в виде твердого белого вещества, выход которого составил 42%. Н1-ЯМР (CDCl3), δ=0.9 чнм (триплет, 3Н), 1.2-1.4 чнм (мультиплет, 30Н), 1.65-1.75 (мультиплет, 2Н), 3.05 чнм (синглет, 3Н), 4.1-4.6 чнм (мультиплет, 5Н), 5.9 чнм (синглет, 1Н), 6 02 чнм (дублет, 1Н), 6.98 чнм (дублет, 1Н), 7.6 чнм (дублет, 2Н), 7.95 чнм (дублет, 2Н).
Пример 20
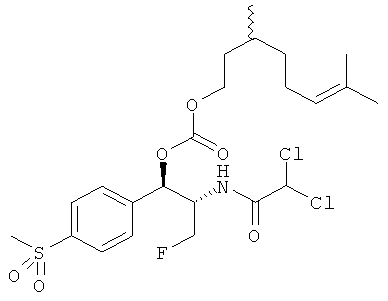
(1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропил-(3R,S)-3,7-диметилокт-6-енил карбонат.
Неочищенный продукт очищали с помощью колоночной гель-хроматографии, с выделением приведенного в заглавии продукта в виде твердого белого вещества, выход которого составил 30%. Приведенная структура показывает, что это смесь изомеров. Н1-ЯМР (CDCl3), δ=0.9 чнм (дублет, 3Н), 1.1-2.0 чнм (мультиплет, 13Н), 3.05 чнм (синглет, 3Н), 4.1-4.6 чнм (мультиплет, 5Н), 5.05 чнм (триплет, 1Н), 5.9 чнм (синглет, 1Н), 6.0 чнм (дублет, 1Н), 7.0 чнм (дублет, 1Н), 7.6 чнм (дублет, 2Н), 7.95 чнм (дублет, 2Н).
Пример 21
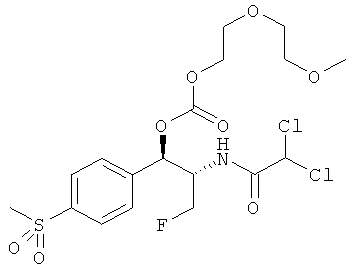
(1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропил 2-(2-метоксиэтокси)этил карбонат.
Неочищенный продукт очищали с помощью колоночной гель-хроматографии, с выделением приведенного в заглавии продукта в виде твердого белого вещества. H1-ЯМР (CDCl3), δ=3.05 чнм (синглет, 3Н), 3.38 чнм (синглет, 3Н), 3.55-3.65 чнм (мультиплет, 6Н), 4.25-4.6 чнм (мультиплет, 5Н), 5.9 чнм (синглет, 1Н), 6.0 чнм (дублет, 1Н), 7.05 чнм (дублет, 1 Н), 7.6 чнм (дублет, 2Н), 7.95 чнм (дублет, 2Н).
Пример 22
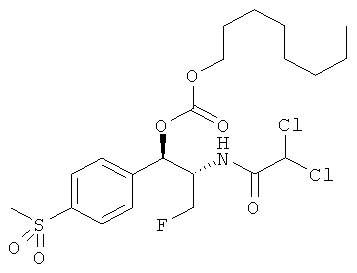
(1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропилоктил карбонат.
Неочищенный продукт очищали с помощью колоночной гель-хроматографии, чтобы выделить желаемый продукт, с получением приведенного в заглавии продукта в виде твердого белого вещества, выход которого составил 44%. Н1-ЯМР (CDCl3), δ=0.9 чнм (триплет, 3Н), 1.2-1.4 чнм (мультиплет, 12Н), 1.65-1.75 (мультиплет, 2Н), 3.05 чнм (синглет, 3Н), 4.1-4.6 чнм (мультиплет, 5Н), 5.9 чнм (синглет, 1Н), 6.0 чнм (дублет, 1Н), 6.9 чнм (дублет, 1Н), 7.6 чнм (дублет, 2Н), 7.95 чнм (дублет, 2Н).
Пример 23
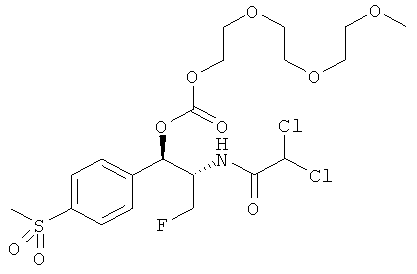
(1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропил 2-(2-(2-метоксиэтокси)этокси)этил карбонат.
Неочищенный продукт очищали с помощью колоночной гель-хроматографии, с выделением приведенного в заглавии продукта в виде полутвердого белого вещества, выход которого составил 31%. Н1-ЯМР (CDCl3), δ=3.05 чнм (синглет, 3Н), 3.38 чнм (синглет, 3Н), 3.55-3.7 чнм (мультиплет, 10Н), 4.2-4.6 чнм (мультиплет, 5Н), 5.95 чнм (мультиплет, 2Н), 7.25 чнм (дублет, 1Н), 7.6 чнм (дублет, 2Н), 7.95 чнм (дублет, 2Н).
Пример 24
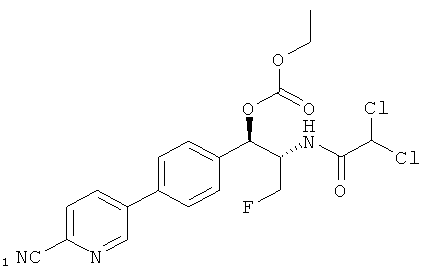
(1R,2S)-1-(4-(6-цианопиридин-3-ил)фенил)-2-(2,2-дихлорацетамидо)-3-фторпропилэтил карбонат.
Неочищенный продукт очищали с помощью колоночной гель-хроматографии, с выделением приведенного в заглавии продукта в виде белой пены, выход которого составил 97%. Н1-ЯМР (ДМСО-d6), δ=1.19 чнм (триплет, 3Н), 4.1 чнм (квадруплет, 2Н), 4.25-4.6 чнм (мультиплет, 3Н), 5.05 чнм (синглет, 2Н), 5.9 чнм (дублет, 1Н), 6.2 чнм (триплет, 1Н), 7.5 чнм (дублет, 2Н), 7.85 чнм (дублет, 2Н), 8.1 чнм (дублет, 1Н), 8.35 чнм (дублет, 1Н), 9.1 чнм (синглет, 1Н), 9.3 чнм (дублет, 1Н).
Пример 25
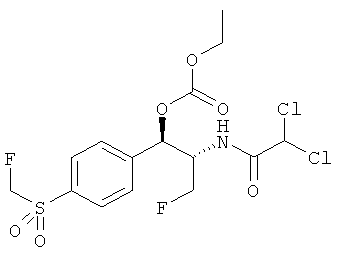
(1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-фторметилсульфонил)фенил)пропил этил карбонат.
Неочищенный продукт очищали с помощью колоночной гель-хроматографии, с получением приведенного в заглавии продукта в виде белой пены, с количественным выходом. Н1-ЯМР (ДМСО-d6), δ=1.2 чнм (триплет, 3Н), 4.1 чнм (квадруплет, 2Н), 4.3-4.7 чнм (мультиплет, 3Н), 5.7 чнм (дублет, 2Н), 5.95 чнм (дублет, 1Н), 6.4 чнм (синглет, 1Н), 7.85 чнм (дублет, 2Н), 7.95 чнм (дублет, 2Н), 9.05 чнм (дублет, 1Н).
Пример 26
Синтез пролекарств флорфеникола и его аналогов путем реакции с бисхлорформиатами диолов
Согласно Фиг.5 раствор бисхлорформиата в безводном тетрагидрофуране Е (1 мольный эквивалент, 0.34 М) помещали в капельную воронку и добавляли капля по капле в безводный раствор тетрагидрофурана, содержащий субстрат С (2.2 мольных эквивалента, 0.64 М), 4-N,N-диметиламинопиридин (0.5 мольных эквивалента), и триэтиламин (2.2 мольных эквивалента), при 0°С, в атмосфере азота. Смесь перемешивали при 0°С в течение 30 минут и затем при комнатной температуре всю ночь. Полученный раствор быстро отфильтровали через бумажный фильтр, чтобы удалить соль аммония. Фильтрат концентрировали и добавляли этилацетат, чтобы растворить неочищенный продукт. Полученный раствор последовательно промывали 1 М раствором HCl(водный), насыщенным раствором NaHCO3(водный) и насыщенным раствором NaCl(водный), за чем последовала быстрая фильтрация через слой силикагеля и Na2SO4. Фильтрат концентрировали и полученный неочищенный продукт очищали с помощью флэш-хроматографии на силикагелевой колонке с выделением чистого пролекарства F, представляющего собой карбонат.
Следующее соединение получали с помощью приведенного выше метода:
Пример 26
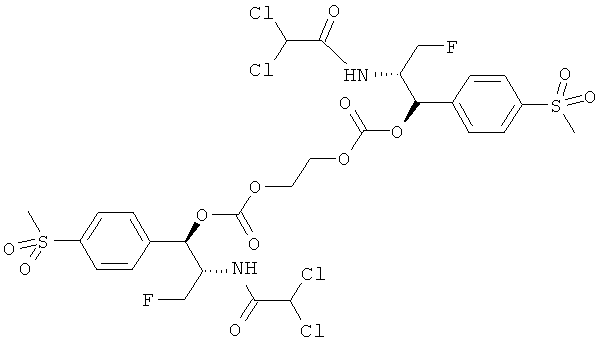
Бис((1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропил)этан-1,2-диил дикарбонат.
Неочищенный продукт очищали с помощью колоночной гель-хроматографии, с выделением приведенного в заглавии продукта в виде полутвердого белого вещества, выход которого составил 62%. H1-ЯМР (ДМСО-d6), δ=3.2 чнм (синглет, 6Н), 4.3-4.7 чнм (мультиплет, 10Н), 5.95 чнм (дублет, 2Н), 6.42 чнм (синглет, 2Н), 7.6 чнм (дублет, 4Н), 7.9 чнм (дублет, 4Н), 9.05 чнм (дублет, 2Н); масс-спектр 852.9 (М+Na).
Примеры 27-30
Синтез пролекарств, представляющих собой бензильные карбонаты фениколов типа хлорамфеникола (Н и I)
Следующие методы применяли со ссылкой на Фиг.6.
Метод I
Раствор этилхлорформиата В в безводном тетрагидрофуране (2.2 мольных эквивалента, 0.34 М) помещали в капельную воронку и прибавляли капля по капле в безводный раствор тетрагидрофурана, содержащий субстрат G (1 мольный эквивалент, 0.64 М), 4-N,N-диметиламинопиридин (0.5 мольных эквивалента) и триэтиламин (2.4 мольных эквивалента) при 0°С в атмосфере азота. Смесь перемешивали при 0°С в течение 30 минут и затем при комнатной температуре всю ночь. Полученный раствор быстро отфильтровали через бумажный фильтр, чтобы удалить соль аммония. Фильтрат концентрировали и добавляли этилацетат, чтобы растворить неочищенный продукт. Полученный раствор последовательно промывали 1 М раствором HCl(водный), насыщенным раствором NaHCO3(водный) и насыщенным раствором NaCl(водный), за чем последовала быстрая фильтрация через слой силикагеля и Na2SO4. Фильтрат концентрировали и полученный продукт высушивали при пониженном давлении с выделением чистого пролекарства Н, представляющего собой карбонат.
Метод II
Раствор этилхлорформиата В в безводном тетрагидрофуране (1 мольный эквивалент, 0.34 М), помещали в капельную воронку и прибавляли капля по капле в безводный раствор тетрагидрофурана, содержащий субстрат G (1 мольный эквивалент, 0.64 М), 4-N,N-диметиламинопиридин (0.5 мольных эквивалента), и триэтиламин (2.4 мольных эквивалента) при 0°С в атмосфере азота. Смесь перемешивали при 0°С в течение 30 минут и затем при комнатной температуре всю ночь. Полученный раствор быстро отфильтровали через бумажный фильтр, чтобы удалить соль аммония. Фильтрат концентрировали и добавляли этилацетат, чтобы растворить неочищенный продукт. Полученный раствор последовательно промывали 1 М раствором НCl(водный), насыщенным раствором NaHCO3(водный) и насыщенным раствором NaCl(водный), за чем последовала быстрая фильтрация через слой силикагеля и Na2SO4. Фильтрат концентрировали и полученный неочищенный продукт очищали с помощью флэш-хроматографии на силикагелевой колонке, с выделением чистых пролекарств Н и I, представляющих собой карбонаты.
Соединения следующих примеров получали с помощью приведенного выше метода:
Пример 27
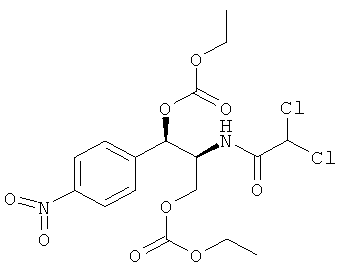
(1R,2S)-2-(2,2-дихлорацетамидо)-1-(4-нитрофенил)пропан-1,3-диил диэтил дикарбонат.
Продукт получали с помощью метода I, приведенного ранее, с выделением названного в заглавии продукта в виде белой пены, выход которого составил 88%. Этот продукт также получали с помощью метода II, с выделением названного в заглавии продукта в виде белой пены, выход которого составил 25%. H1-ЯМР (ДМСО-d6), δ=1.2 чнм (мультиплет, 6Н), 4.05-4.25 чнм (мультиплет, 6Н), 4.5 чнм (мультиплет, 1Н), 5.95 чнм (дублет, 1Н), 6.4 чнм (синглет, 1Н), 7.6 чнм (дублет, 2Н), 8.2 чнм (дублет, 2Н), 8.95 чнм (дублет, 1Н).
Пример 28
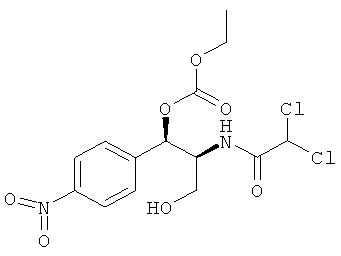
(1R,2R)-2-(2,2-дихлорацетамидо)-3-гидрокси-1-(4-нитрофенил)пропилэтил карбонат.
Продукт получали с помощью метода II, приведенного ранее, с выделением названного в заглавии продукта в виде белой пены, выход которого составил 19%. Н1-ЯМР (ДМСО-d6), δ=1.2 чнм (триплет, 3Н), 3.35 чнм (мультиплет, 1Н), 3.45 чнм (мультиплет, 1Н), 4.0-4.2 чнм (мультиплет, 3Н), 5.19 чнм (триплет, 1Н), 5.9 чнм (дублет, 1Н), 6.4 чнм (синглет, 1Н), 7.6 чнм (дублет, 2Н), 8 2 чнм (дублет, 2Н), 8.75 чнм (дублет, 1Н).
Пример 29
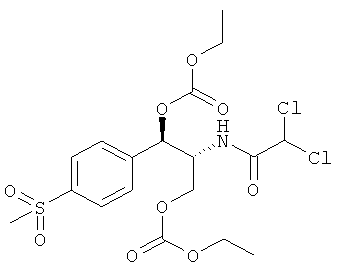
(1R,2R)-2-(2,2-дихлорацетамидо)-1-(4-(метилсульфонил)фенил)пропан-1,3-диил диэтил дикарбонат.
Неочищенный продукт получали с помощью метода II, приведенного ранее, с выделением названного в заглавии продукта в виде белой пены, выход которого составил 19%. Н1-ЯМР (ДМСО-d6), δ=1.2 чнм (мультиплет, 6Н), 3.19 чнм (синглет, 3Н), 4.05-4.25 чнм (мультиплет, 6Н), 4.45 чнм (мультиплет, 1Н), 5.9 чнм (дублет, 1Н), 6.4 чнм (синглет, 1Н), 7.6 чнм (дублет, 2Н), 7.9 чнм (дублет, 2Н), 8.95 чнм (дублет, 1Н).
Пример 30
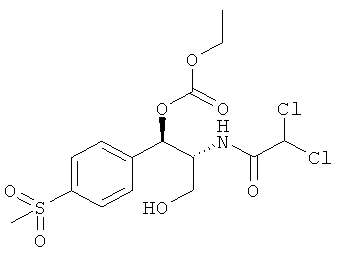
(1R,2R)-2-(2,2-дихлорацетамидо)-3-гидрокси-1-(4-(метилсульфонил)фенил)пропилэтил карбонат.
Неочищенный продукт получали с помощью метода II, приведенного ранее, с выделением названного в заглавии продукта в виде белой пены, выход которого составил 20%. H1-ЯМР (ДМСО-d6), δ=1.2 чнм (триплет, 3Н), 3.2 чнм (синглет, 3Н), 3.35 чнм (мультиплет, 1Н), 3.45 чнм (мультиплет, 1Н), 4.0-4.2 чнм (мультиплет, 3Н), 5.19 чнм (триплет, 1Н), 5.85 чнм (дублет, 1Н), 6.42 чнм (синглет.1Н), 7.58 чнм (дублет, 2Н), 7.9 чнм (дублет, 2Н), 8.75 чнм (дублет, 1Н).
Примеры 31-35
Оценка полезности пролекарств, представляющих собой бензильные карбонаты флорфеникола
Пример 31
Вязкость композиций
В Таблице 4 приведены оценки инъецируемости дозируемых растворов выбранных пролекарств, представляющих собой бензильные карбонаты флорфеникола, при концентрациях, эквивалентных 300 мг/мл флорфеникола (30% вес/об.).
2:1
2:1
2:1.5
бензиловый спирт - 2:1
полиэтиленгликоль 300
Обсуждение
Высокие концентрации феникола или лекарственного препарата феникола, входящие в состав пролекарства феникола, часто необходимы для удобного введения необходимого количества или желаемого количества антибиотика. Из-за ограниченной растворимости фениколов во многих органических растворителях или смесях растворителей, пригодных для инъецируемых композиций, выбор растворителей для приготовления высококонцентрированных растворов флорфеникола ограничен. В результате высококонцентрированные растворы лекарственных препаратов фениколов в органических растворителях или смесях растворителей могут стать весьма вязкими и затруднить введение с помощью шприца. Поэтому способность пролекарств, представляющих собой бензильные карбонаты фениколов, растворяться в широком ряду органических растворителей или смесях растворителей, пригодных для инъецируемых композиций, дала возможность приготовить высококонцентрированные растворы для инъекций, с низкой вязкостью. Таблица 4 показывает сравнение инъецируемости концентрированных растворов пролекарств, представляющих собой бензильные карбонаты флорфеникола, в примерах смесей органических растворителей, которые, в целом, пригодны для введения доз препарата путем внутривенных или внутримышечных инъекций. Были приготовлены испытательные растворы бензильных карбонатов флорфеникола, содержащие концентрации флорфеникола (мг/мл), эквивалентные концентрации, присутствующей вкомпозиции Nuflor®. Инъецируемость растворов оценили посредством метода "капающего шприца", в котором время капанья (с) одинаковых объемов таких растворов, в условиях свободного гравитационного течения из вертикально расположенного шприца, измеряли при 15°С. После удаления плунжера из одноразового полиэтиленового шприца на 5 мл (5 мл Luer, Norm-Ject Zentrish / Henke Saas Wolf GMBH) и установки на шприц одноразовой иглы (B-D®16G1 Precision Glide/BentonDickinson & CO) испытательные растворы заливали сверху в шприц, и время, необходимое для истечения двух миллилитров раствора (от отметки 3 мл до отметки 1 мл), регистрировали в трех экземплярах. Инъецируемости по отношению к Nuflor® вычисляли путем деления времени капанья испытательных растворов (записи 1-12) на время капанья, измеренное для образца продажного препарата Nuflor® (запись 13). Как ясно из результатов Таблицы 4. испытательные растворы, содержащие бензиловый спирт в качестве уменьшающего вязкость агента, имели относительные инъецируемости <1.00 и, вследствие этого, были лучше, чем Nuflor® (раствор флорфеникола в смеси растворителей пропиленгликоль/ полиэтиленгликоль 300 / 2-метилпирролидинон с концентрацией флорфеникола 30% вес/объем). Благодаря более хорошей инъецируемости эти растворы представляют собой более благоприятные композиции для доставки флорфеникола путем инъекции. Раствор бензильного карбоната флорфеникола Примера 2 в смеси растворителей триацетин/2-пирролидинон - 1/1, не содержащий бензиловый спирт в качестве уменьшающего вязкость агента, был единственным раствором с более плохой инъецируемостью, чем у препарата Nuflor® (запись 5). Раствор бензильного карбоната флорфеникола Примера 2, содержащий более высокие концентрации флорфеникола, чем в препарате Nuflor® (запись 2; 35% в/о против 30% в/о), также показал более высокую инъецируемость. Интересно, что растворы, содержащие концентрации флорфеникола, равные 30% в/о, в смеси свободного флорфеникола и пролекарства, представляющего собой бензильный карбонат флорфеникола (записи 11-12), также показали более высокие значения инъецируемости, чем композиция Nuflor®.
Пример 32
Сравнения точек плавления и растворимостей в воде
Модификации физико-химических свойств, достигаемые с помощью пролекарств, представляющих собой карбонаты фениколов, или пролекарств, представляющих собой бензильные карбонаты фениколов (аналогов фениколов), важны для возможности получения композиций для введения животным, основанных на желаемых органических растворителях. Высокие растворимости пролекарств, представляющих собой бензильные карбонаты фениколов, по сравнению с исходными фениколами, в определенных органических растворителях или смесях органических растворителей, частично обуславливаются более низкими точками плавления таких пролекарств, представляющих собой карбонаты, по сравнению с исходными лекарственными средствами. Эти более низкие точки плавления отражают пониженную энергию кристаллической решетки пролекарств, представляющих собой карбонаты, которая ответственна за повышенную растворимость. Сравнение точки плавления флорфеникола и точками плавления доступных кристаллических форм различных примеров пролекарств флорфеникола показано в Таблице 5.
Для некоторых терапевтических применений флорфеникол вводится в концентрированном органическом растворе подкожно, где, как известно, он образует локализованное депо лекарственного вещества, что приводит к желаемому продолжительному выделению лекарственного вещества в круг кровообращения. В таких случаях растворимость флорфеникола в водной среде представляет собой один из важных факторов, определяющих скорость продолжительного высвобождения. Другим важным фактором, оказывающим воздействие на продолжительное высвобождение флорфеникола из области подкожного депо, является концентрация дозируемого раствора и смесь растворителей композиции. Помимо широкого ряда растворителей, которые могут быть использованы для приемлемых композиций пролекарств, представляющих собой бензильные карбонаты флорфеникола, эти пролекарства также допускают широкий интервал растворимостей в воде. Растворимости в воде, которые измерили для ряда пролекарств, представляющих собой бензильные карбонаты флорфеникола, показаны в Таблице 5. Растворимости, достигаемые этими пролекарствами, находятся в интервале от слегка до значительно более низких, чем растворимость флорфеникола. Уменьшенные растворимости в воде таких пролекарств могут быть полезны для контроля скорости растворения пролекарства в области подкожного депо и могут позволить достигнуть оптимальное продолжительное высвобождение исходного лекарственного вещества.
Пример 33
Сравнение растворимостей в органических растворителях (смеси растворителей триацетин/бензиловый спирт 2:1)
Таблица 6 показывает растворимости эквивалентов флорфеникола, которые были достигнуты с помощью выбранных пролекарств, представляющих собой бензильные карбонаты флорфеникола, в смеси растворителей триацетин/бензиловый спирт 2:1 (об./об.), в которой бензиловый спирт применяется в качестве компонента с низкой вязкостью.
Желаемые концентрации, равные или большие чем 30% (вес/объем), достигли с помощью пролекарств, представляющих собой бензильные карбонаты флорфеникола. Исходное лекарственное вещество флорфеникол было нерастворимо в смеси растворителей триацетин/бензиловый спирт 2:1 (об./об.), даже в таких низких концентрациях, как 10% (вес/объем). Интересно, что флорфеникол стал более растворимым в смеси растворителей триацетин/бензиловый спирт 2:1 (об./об.), когда пролекарство, представляющее собой бензильный карбонат флорфеникола, также присутствовало. Комбинация пролекарства Примера 14, с концентрацией 275 мг/мл, и флорфеникола, с концентрацией 100 мг/мл, была растворима в смеси растворителей триацетин/бензиловый спирт 2:1 (об./об.) и обеспечила стабильный раствор с содержанием флорфеникола 30% (вес/объем) (Таблица 4, приведенная ранее, позиция 12).
мый
мый
мый
мый
мый
мый
мый
Пример 34
IN VITRO ферментативное высвобождение исходного лекарственного вещества флорфеникола из пролекарств, представляющих собой бензильные карбонаты
Способность пролекарств, производных молекулы исходного лекарственного вещества, эффективно действовать in vivo в качестве источника свободного исходного лекарственного вещества означает полезность конкретного пролекарства для лечения. Способность пролекарства высвобождать исходное лекарственное вещество in vivo, в присутствии эндогенных ферментов, может быть определена путем измерения системных уровней исходного лекарственного вещества после введения пролекарства животному. Эта высвобождаемость может также быть оценена in vitro, измеряя высвобождение исходного лекарственного вещества после смешения со всей кровью, плазмой или сывороткой животного. Выбранные пролекарства флорфеникола, представляющие собой бензильные карбонаты, протестировали на высвобождение флорфеникола после смешения in vitro с бычьей сывороткой. Протестированные соединения показали благоприятные профили высвобождения исходного лекарственного вещества, как показано в Таблице 7, приведенной ниже. Соединения Примеров 8 и 14 показали самые высокие скорости высвобождения флорфеникола в сыворотку. Как оказывается, среди протестированных соединений присутствует общая тенденция, что более липофильные карбонаты флорфеникола показывают более высокие скорости расщепления и высвобождения. Было обнаружено интересное исключение, представленное Примером 26 (бис-(карбонат флорфеникола)).
50 микролитров стокового раствора пролекарства, представляющего собой карбонат (10 мг/мл в ДМСО), добавили к 5 мл бычьей сыворотки донора и перемешали. Аликвоты по 400 микролитров конечного раствора перенесли в пластмассовые центрифужные пробирки на 1.5 мл. Каждую пластмассовую пробирку поместили в водяную баню при 37°С для инкубации. Образцы вынимали из бани в момент времени 0, 1, 2, 4, 8 и 24 часа и быстро перемешивали в течение 30 секунд после добавления 400 микролитров ацетонитрила для прекращения реакции. Осадок удаляли с помощью центрифугирования на приборе Eppendorf 5415G при 14000 об./мин в течение 5 минут. Чистый раствор супернатанта отобрали для анализа HPLC (жидкостная хроматография высокого разрешения). Площадь пика флорфеникола использовали для вычисления превращения пролекарств.
Условия HPLC изложены ниже:
Градиент представлен ниже:
Результаты исследования стабильности выбранных пролекарств в бычьей сыворотке, представленные в Таблице 7, подтвердили, что бензильные карбонаты флорфеникола высвобождают исходное лекарственное вещество при обработке in vitro ферментами сыворотки. Эти результаты доказывают, что бензильные карбонаты флорфеникола представляют собой субстраты для гидролитических ферментов, присутствующих в бычьей сыворотке.
Пример 35
IN VIVO высвобождение исходного лекарственного вещества флорфеникола из пролекарств, представляющих собой бензильные карбонаты
Фармакокинетический профиль активного антибиотика in vivo, после ведения пролекарства, определили, как изложено ниже:
1. In vivo высвобождение активного антибиотика, подтвержденное для двух различных видов животных.
Пролекарство, представляющее собой соединение Примера 18, ввели внутривенным путем ("IV") двум субъектам: крысе и крупному рогатому скоту, за чем последовало определение концентраций флорфеникола в плазме, собранной по истечении времени.
Данные Таблицы 8, приведенной ниже, показывают уровни флорфеникола в плазме, которые возникли после внутривенного введения пролекарства, представляющего собой соединение Примера 18, как крысе, так и крупному рогатому скоту.
2. Активные антибиотики высвобождаются из пролекарства независимо от пути введения пролекарства.
Данные Таблицы 9, приведенной ниже, показывают уровни флорфеникола в плазме, которые возникают после введения пролекарства, представляющего собой соединение Примера 2, двумя различными путями, то есть внутривенно и подкожно.
3. Доза - зависимое увеличение высвобождения активной составляющей.
Данные таблицы 10, приведенной ниже, подтверждают доза - зависимое увеличение уровней активного антибиотика (флорфеникола) в плазме после введения возрастающих доз пролекрства, представляющего собой соединение Примера 2.
4. Время высвобождения активной составляющей:
а. Данные Таблиц 11 и 12, приведенных ниже, подтверждают, что активный антибиотик (флорфеникол) высвобождается за менее чем полчаса с момента ведения пролекарства, представляющего собой соединение Примера 2, независимо от вида животного.
Значение ± стандартное отклонение*
b. Данные Таблиц 13 и 14, приведенных ниже, подтверждают, что активные антибиотики быстро высвобождаются из пролекарства, представляющего собой соединение Примера 2, при введении внутривенным и подкожным путем крупному рогатому скоту.
5. Действие композиции
Преимущества композиции пролекарства, представляющего собой карбонат феникола, основанной на смеси растворителей триацетин/бензиловый спирт.
Кинетику высвобождения соединения примера 2, при введении в композиции, основанной на смеси растворителей триацетин/бензиловый спирт (соотношение 2:1 вес/об), сравнили с кинетикой высвобождения соединения Примера 2, при введении в композиции, основанной на системе растворителей триацетин/2-пирролидинон (соотношение 2:1 вес/об.). Исследование провели на крупном рогатом скоте (n=3).
Среднее значение AUC после подкожного введения соединения Примера 2, в размере дозы 20 мг/кг, в системе растворителей триацетин/2-пирролидинон, составило 42.6 ч·мг/л.
Среднее значение AUC после подкожного введения соединения Примера 2, в размере дозы 40 мг/кг, в системе растворителей триацетин/бензиловый спирт, составило 152.1 ч·мг/л.
Так как в двух исследованиях применялась различная доза, вычислили приведенные к дозе значения, которые составили 2.13 ч/л (42.6/20) и 3.8 ч/л (152.1/40) для систем растворителей триацетин/2-пирролидинон и триацетин/бензиловый спирт соответственно.
6. Биодоступность флорфеникола в организме крупного рогатого скота после подкожного введения пролекарства Примера 2, представляющего собой бензильный карбонат
Вычисление фармакокинетических данных для соединения Примера 2
Полное усредненное значение AUC для активной составляющей(флорфеникола) = 152.11 ч·мг/л
Полное усредненное значение AUC для соединения Примера 2= 38.04, что в свою очередь равно 30.43 ч·мг/л для эквивалента флорфеникола.
83.5% МС-9148 превратилось в флорфеникол, однократно абсорбировавшись из области подкожного депо.
Исследования эффективности с помощью соединения Примера 2
Терапевтическую эффективность однократной дозы Nuflor® (компания Schering-Plough Animal Health) сравнили с терапевтической эффективностью однократной дозы пролекарства, представляющего собой соединение Примера 2, после подкожного введения крупному рогатому скоту, страдающему от возникшего естественным образом бычьего респираторного заболевания (BRD). Результаты изложены ниже.
кий раствор
В заключение, эффективность, наблюдаемая для флорфеникола, который высвободился из пролекарства, представляющего собой соединение Примера 2, сопоставима с эффективностью для торговой марки флорфеникола (Nuflor®).
Заключение
Таким образом, будет оценено по достоинству, что данное изобретение предоставляет новые пролекарства антибиотиков фениколов и способы их применения при лечении или предупреждении бактериальных инфекций у животных или людей.
Хотя определенные варианты осуществления изобретения и примеры использовались для описания данного изобретения, будет очевидно специалистам в данной области техники, что изменения в показанных вариантах осуществления изобретения и примерах могут быть сделаны без выхода за пределы объема изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ИНДОЛОНА В ВИДЕ РАЦЕМАТА ИЛИ ОПТИЧЕСКИ АКТИВНОГО ИЗОМЕРА ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ АДДИТИВНЫЕ СОЛИ КИСЛОТЫ И КЕТОПРОИЗВОДНЫЕ ИНДОЛОНА | 1991 |
|
RU2068414C1 |
| ПРОИЗВОДНЫЕ АЗЕТИДИНОНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1992 |
|
RU2047602C1 |
| СОЕДИНЕНИЕ ЦЕФЕМА И ЕГО ФАРМАЦЕВТИЧЕСКИ ИЛИ ВЕТЕРИНАРНО ПРИЕМЛЕМЫЕ СОЛИ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 1990 |
|
RU2074186C1 |
| ПРОИЗВОДНЫЕ КАРБАПЕНЕМА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1993 |
|
RU2097383C1 |
| ФЕНИКОЛОВЫЕ ПРОТИВОБАКТЕРИАЛЬНЫЕ СРЕДСТВА | 2013 |
|
RU2593204C2 |
| ГЕКСАГИДРОНАФТАЛИНОВЫЕ СЛОЖНОЭФИРНЫЕ СОЕДИНЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1993 |
|
RU2104997C1 |
| АЗАСТЕРОИДНЫЕ СОЕДИНЕНИЯ | 1991 |
|
RU2070204C1 |
| 3-АЦИЛ-2-ОКСОИНДОЛ-1-КАРБОКСАМИДЫ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 1991 |
|
RU2036905C1 |
| ПРОИЗВОДНЫЕ 3-(ПИПЕРИДИНИЛ-1)-ХРОМАН-4,7-ДИОЛА И 1-(4-ГИДРОКСИФЕНИЛ)-2-(ПИПЕРИДИНИЛ-1)-АЛКАНОЛА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ СВЯЗЫВАНИЯ NMDA РЕЦЕПТОРА | 1995 |
|
RU2139857C1 |
| КРЕМНИЙСОДЕРЖАЩИЕ СОЕДИНЕНИЯ ИЛИ ИХ СОЛИ, ОБЛАДАЮЩИЕ ФУНГИЦИДНОЙ АКТИВНОСТЬЮ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1992 |
|
RU2069213C1 |
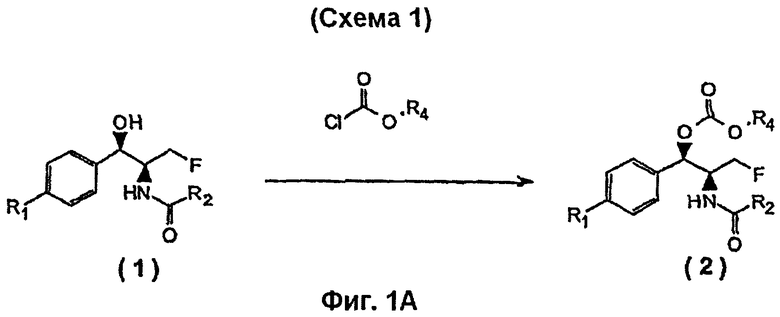
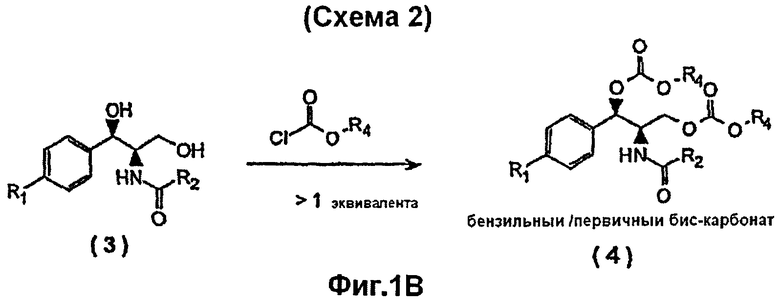
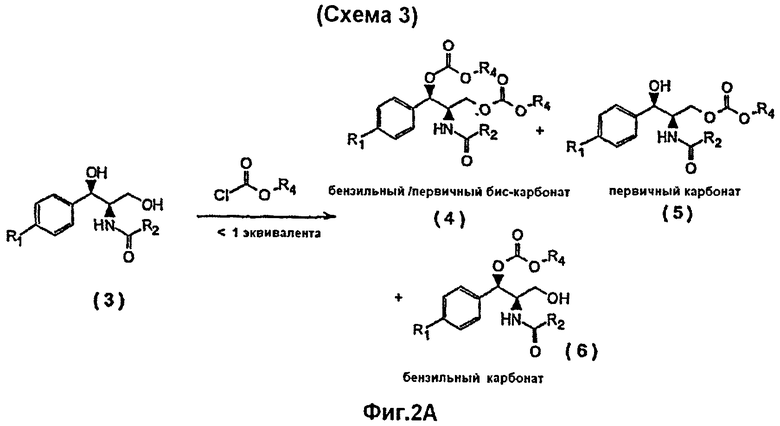
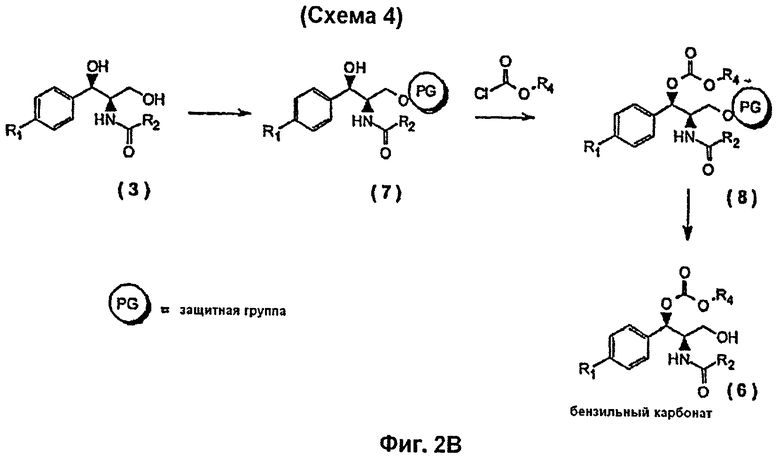
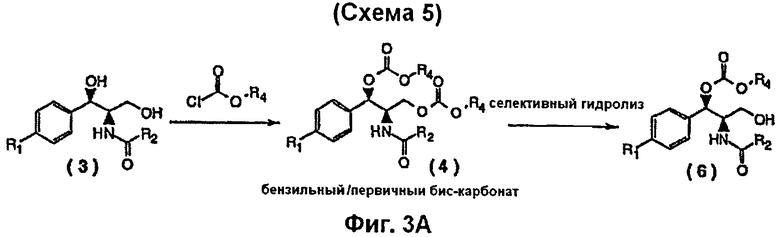
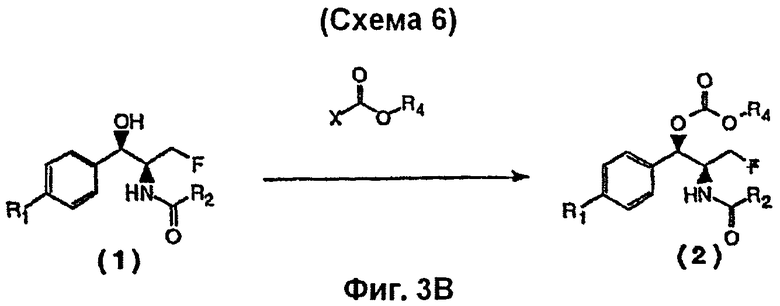
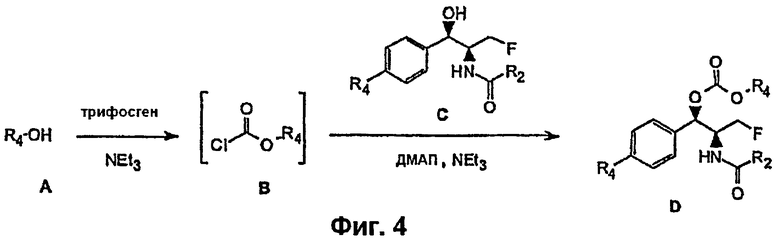
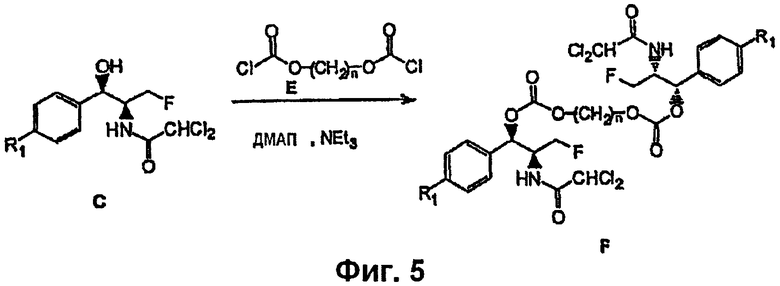
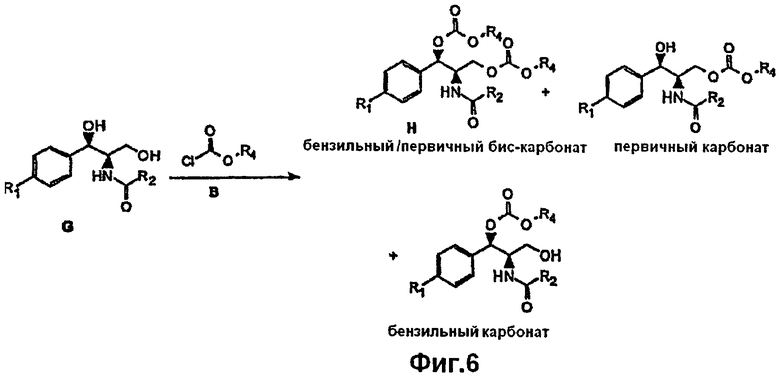
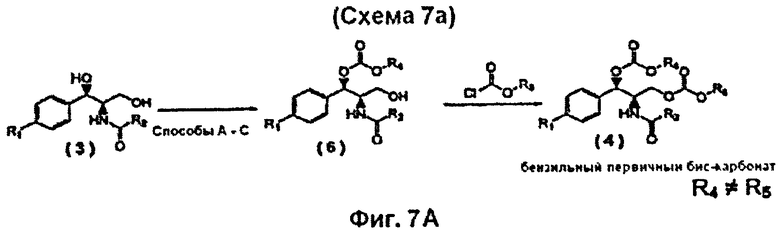
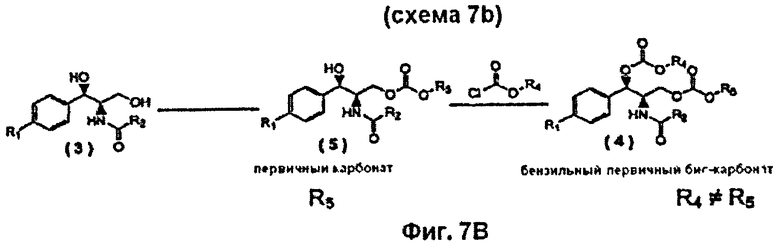
Изобретение относится к карбонатным производным фениколов, представляющим собой соединения Формулы 1

где R1 выбирается из группы, состоящей из 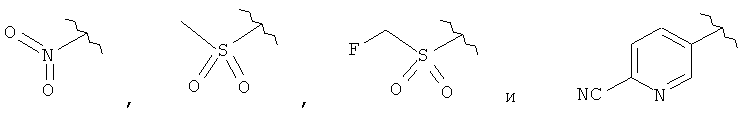
R2 выбирают из группы, состоящей из дихлорметила, дифторметила, хлорфторметила, хлорметила и метила, R3 выбирают из группы, состоящей из гидроксиметила, фторметила, дифторметила, трифторметила и CH2O-C(O)O-R5, R4 и R5 независимо выбирают из группы, состоящей из неразветвленного или разветвленного, замещенного С1-10-алкилом или С1-10-карбоалкокси или незамещенного C1-10-алкила, С1-10-циклоалкила, C1-10 алкоксиалкила, фенила, фенилалкила, неразветвленного или разветвленного, замещенного С1-10-алкилом или незамещенного С1-10-алкенила или С1-10-циклоалкенила, или его сольват. 10 з.п. ф-лы, 15 табл., 7 ил.
1. Карбонат феникола формулы I или его сольват
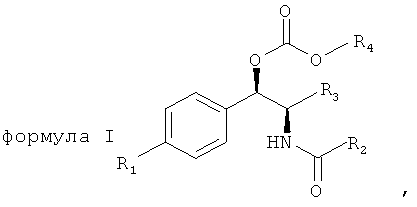
где R1 выбирается из группы, состоящей из
 ,
,  ,
,  и
и  ,
,
R2 выбирают из группы, состоящей из дихлорметила, дифторметила, хлорфторметила, хлорметила и метила,
R3 выбирают из группы, состоящей из гидроксиметила, фторметила, дифторметила, трифторметила и CH2O-C(O)O-R5,
R4 и R5 независимо выбирают из группы, состоящей из неразветвленного или разветвленного, замещенного С1-10-алкилом или С1-10-карбоалкокси или незамещенного С1-10-алкила, C1-10-циклоалкила, С1-10алкоксиалкила, фенила, фенилалкила, неразветвленного или разветвленного, замещенного C1-10-алкилом или незамещенного С1-10-алкенила или C1-10-циклоалкенила.
2. Карбонат феникола по п.1, в котором, если R1 представляет собой NO2, R3 не представляет собой CH2O-C(O)O-R5.
3. Карбонат феникола по п.1, в котором R4 и R5 независимо выбираются из группы, состоящей из метила, этила, пропила, изопропила, изобутила, изопентила, н-додецила, н-октадецила, 1-этилпропила, 3-метилбут-2-енила, 2-метоксиэтила, 2-этоксиэтила, 2-бутоксиэтила, циклопропилметила, циклогексила, 3,7-диметилокт-6-енила, бензила, 4-метилбензила, 4-метоксибензила, 2-(метоксиэтокси)-этила, 2-[2-(метоксиэтокси)-этокси]-этила, 1-этоксикарбонилэтила.
4. Карбонат феникола по п.3, в котором R1 выбирается из группы, состоящей из
 ,
,  и
и  ,
,
R2 представляет собой дихлорметил или дифторметил, и R3 выбирается из группы, состоящей из гидроксиметила, фторметила и CH2O-С(O)O-R5.
5. Карбонат феникола по п.1, в котором R1 представляет собой CH3SO2, R2 представляет собой CHCl2, и R3 представляет собой CH2F.
6. Карбонат флорфеникола по п.5, в котором R4 выбирается из группы, состоящей из метила, этила, пропила, изопропила, изобутила, изопентила, н-додецила, н-октадецила, 1-этилпропила, 3-метилбут-2-енила, 2-метоксиэтила, 2-этоксиэтила, 2-бутоксиэтила, циклопропилметила, циклогексила, 3,7-диметилокт-6-енила, бензила, 4-метилбензила, 4-метоксибензила, 2-(метоксиэтокси)-этила, 2-[2-(метоксиэтокси)-этокси]-этила, 1-этоксикарбонилэтила.
7. Карбонат феникола по п.1, в котором R3 представляет собой CH2F.
8. Карбонат феникола по п.1, в котором R1 представляет собой CH3SO2 или NO2, R2 представляет собой CHCl2, R3 представляет собой СН2ОН, и R4 представляет собой этил.
9. Карбонат феникола по п.1, в котором R1 представляет собой CH3SO2 или NO2, R2 представляет собой CHCl2, R3 представляет собой
 , и R4 представляет собой этил.
, и R4 представляет собой этил.
10. Карбонат феникола по п.1, который выбирается из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
,  и
и 
11. Карбонат феникола по п.1, который выбирается из группы, состоящей из (1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропилметил карбоната, (1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропилэтил карбоната, (1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропилпропил карбоната, (1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропилизопропил карбоната, (1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропилизобутил карбоната, циклопропилметил (1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропил карбоната, (1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропил-3-метилбут-2-енил карбоната, (1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропилизопентил карбонат, (1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропилпентан-3-ил карбоната, циклогексил (1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропил карбоната, (1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропил-2-метоксиэтил карбоната, (1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропил-2-этоксиэтил карбоната, (1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропил-2-бутоксиэтил карбоната, бензил (1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропил карбоната, (1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропил-4-метилбензил карбоната, (1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропил-4-метоксибензил карбоната, (S)-этил-2-(1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропокси)карбонилокси)пропаноата, (1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропилдодецил карбоната, (1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропилоктадецил карбоната, (1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропил-(3R,S)-3,7-диметилокт-6-енил карбоната, (1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропил 2-(2-метоксиэтокси)этил карбоната, (1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропилоктил карбоната, (1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропил-2-(2-(2-метоксиэтокси)этокси)этил карбоната, (1R,2S)-1-(4-(6-цианопиридин-3-ил)фенил)-2-(2,2-дихлорацетамидо)-3-фторпропилэтил карбоната, (1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-фторметилсульфонил)фенил)пропилэтил карбоната, бис((1R,2S)-2-(2,2-дихлорацетамидо)-3-фтор-1-(4-(метилсульфонил)фенил)пропил) этан-1,2-диил дикарбоната.
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| СПОСОБ АСИММЕТРИЧНОГО ПОЛУЧЕНИЯ ФЛОРФЕНИКОЛА, СПОСОБ РЕГИОИЗБИРАТЕЛЬНОГО ОТКРЫТИЯ ХИРАЛЬНОГО ЭПОКСИДА И СПОСОБ ПОЛУЧЕНИЯ ЕГО R, S-ИЗОМЕРА | 1993 |
|
RU2126383C1 |
Авторы
Даты
2011-10-27—Публикация
2006-12-20—Подача