1. Область применения изобретения
[0001] Настоящее изобретение относится к способу зарядки литиевой вторичной батареи, которая использует аморфный электродно-активный материал.
2. Описание известного уровня техники
[0002] Поскольку персональные компьютеры, цифровые видеокамеры, мобильные телефоны и другие подобные устройства становятся все меньше, литиевые вторичные батареи стали широко использоваться как источники питания в областях связи и связанных с информацией устройствах из-за их высокой плотности энергии. Кроме того, в автомобильной промышленности также есть тенденции для быстрого развития электрических транспортных средств из-за экологических и ресурсных вопросов, и литиевые вторичные батареи рассматриваются для использования в качестве источников питания для питания этих электрических транспортных средств.
[0003] В настоящее время аморфный электродно-активный материал известен как использующийся в качестве электродно-активного материала в литиевых вторичных батареях. Например, в патентной заявке Японии, публикация №2005-135866 (JP-A-2005-135866), рассматривается электродно-активный материал, который является в основном аморфным металлическим комплексом, представленным общим выражением М2-ZxВ2xО3. Ограничительная часть пункта 1 формулы заявленного изобретения основана на раскрытии в JP 2005-135866. Также в патентной заявке Японии, публикация №8-78002 (JP-A-8-78002), описывается положительный электродно-активный материал, который состоит из оксидов переходных металлов из семейства 7А или оксидов переходных металлов из семейства 8А или из обоих, в которых часть этого оксида переходного металла имеет аморфную структуру. Кроме того, в патентной заявке Японии, публикация №10-74515 (JP-A-10-74515), рассматривается положительный электродно-активный материал, в котором переходной металл из семейства 7А или переходной металл из семейства 8А или обоих является Me и в котором часть или все со структурой LiMeO2 состоит из аморфного оксида металла.
[0004] Аморфный электродно-активный материал выгоден в том, что состав может быть установлен свободно по сравнению с кристаллическим электродно-активным материалом. Кроме того, хотя аморфный электродно-активный материал представляется как многообещающий электродно-активный материал с высокой емкостью, его реальная емкость в настоящее время еще низка, поэтому есть потребность в аморфном электродно-активном материале с высокой емкостью. Кстати, в патентной заявке Японии, публикация №10-134813 (JP-A-10-134813), и в патентной заявке Японии, публикация №9-22695 (JP-A-9-22695), в обеих описывается материал, подобный электродно-активному и который, хотя не аморфен, состоит в основном из железного комплекса FeBU3 или подобного ему.
В JP 2002-270171 раскрыт положительный электродно-активный материал для литиевой вторичной батареи с безводным электролитом, образованной из сложного оксида лития-железа. Сложный оксид лития-железа имеет аморфную структуру, а состав перед начальной зарядкой выражается следующей формулой (1): LixFeOy(1). В формуле 0,65≤x≤1,00 и 1,83≤y≤2,05.
Сущность изобретения
[0005] Изобретение раскрывает аморфный электродно-активный материал с улучшенными характеристиками зарядки и разрядки.
[0006] Изобретатели выявили корреляционную связь между окислительным потенциалом Fe и средней электроотрицательностью М в амoрфном электродно-активном материале, представленном общим выражением LixFeMyOz (где М - один или два или более типов стеклообразующего элемента). Более конкретно, изобретатели выявили, что окислительный потенциал Fe падает, когда средняя электроотрицательность М снижается, и что не только двухвалентный-трехвалентный редокс (т.е. окисление-восстановление) Fe, но также трехвалентное-четырехвалентное окисление-восстановление Fe можно применить на практике. Обычно упомянутый окислительный потенциал от трехвалентного Fe до четырехвалентного Fe выше, чем потенциал разложения раствора электролита (далее также называется "потенциал разложения электролита"), поэтому, если потенциал увеличивается, первым начинает разлагаться раствор электролита, таким образом не позволяя практическое использование трехвалентного-четырехвалентного окисления-восстановления. Однако изобретатели обнаружили, что путем контроля средней электроотрицательности М упомянутый окислительный потенциал от трехвалентного Fe до четырехвалентного Fe может быть снижен, и в результате может активно использоваться трехвалентное-четырехвалентное окисление-восстановление Fe.
[0007] Аспект изобретения относится к способу зарядки литиевой вторичной батареи, которая содержит слой положительного электрода, включающий положительный электродно-активный материал; слой отрицательного электрода, включающий отрицательный электродно-активный материал; сепаратор, размещенный между слоем положительного электрода и слоем отрицательного электрода; и раствор электролита, имеющий потенциал Ve разложения электролита и введенный, по меньшей мере, в сепаратор, при этом положительный электродно-активный материал является аморфным и представлен общим выражением LixFeMyOz, где x и y являются значениями, которые независимо удовлетворяют 1<x≤2,5 и 0<y≤3 соответственно, и z=(x+(валентность Fe)+(валентность М)×y)/2, чтобы удовлетворить стехиометрии, М представляет собой один или два или более типов стеклообразующего элемента, а средняя электроотрицательность М меньше чем (Ve+6,74)/5,41, причем способ отличается тем, что вторичную батарею заряжают до 4,5 В.
[0008] В соответствии с этим первым аспектом упомянутый окислительный потенциал от трехвалентного Fe до четырехвалентного Fe может быть уменьшен так, чтобы он был меньше, чем потенциал разложения электролита, путем установки средней электроотрицательности М с учетом потенциала Ve разложения электролита. В результате может быть использовано трехвалентное-четырехвалентное окисление-восстановление, таким образом позволяя получить электродно-активный материал с высокой емкостью.
[0009] Также средняя электроотрицательность М может быть равна или меньше чем 2,07. Это позволяет получить более практичный электродно-активный материал.
[0010] Далее, М может быть бором (В). Соответственно, электроотрицательность может сохраняться в рамках соответствующего диапазона, так что может быть получен электродно-активный материал с высокой емкостью.
[0011] Второй аспект настоящего изобретения относится к способу изготовления электродно-активного материала, снабженного раствором электролита, имеющего потенциал Ve разложения электролита. Этот способ изготовления включает смешивание в расплавленном состоянии состава из сырьевых материалов, которые образуют общее выражение LixFeMyOz, и быстрое затвердевание из расплавленного состояния упомянутого состава из сырьевых материалов, который был смешан расплавленным. В упомянутом выражении x и y являются значениями, которые независимо удовлетворяют 1<x≤2,5 и 0<y≤3 соответственно, и z=(x+(валентность Fe)+(валентность М)× y)/2, чтобы удовлетворить стехиометрии, М представляет собой один или два или более типов стеклообразующего элемента, а средняя электроотрицательность М меньше чем (Ve+6,74)/5,41.
[0012] В соответствии со вторым аспектом упомянутый окислительный потенциал от трехвалентного Fe до четырехвалентного Fe может быть уменьшен так, что он будет меньше, чем потенциал разложения электролита, путем установки средней электроотрицательности М с учетом потенциала Ve разложения электролита. В результате может использоваться трехвалентное-четырехвалентное окисление, таким образом позволяя получить электродно-активный материал с высокой емкостью.
Краткое описание чертежей
[0013] Вышеизложенные и дальнейшие признаки и преимущества настоящего изобретения будут очевидны из следующего описания на примерах воплощения со ссылкой на сопутствующие чертежи, в которых одинаковые позиции используются для представления одинаковых элементов и в которых:
Фиг.1А и 1В - графики, показывающие связь между окислительным потенциалом Fe и средней электроотрицательностью М в аморфном электродно-активном материале, представленном общим выражением LixFeMyOz;
Фиг.2 - график, показывающий характеристики зарядки и разрядки испытуемых ячеек в соответствии с примером; и
Фиг.3 - график, показывающий связь между окислительным потенциалом Fe и средней электроотрицательностью М в аморфном электродно-активном материале в соответствии с примером.
Подробное описание изобретения
[0014] Далее будут подробно описаны аморфный электродно-активный материал и литиевая вторичная батарея в соответствии с настоящим изобретением.
[0015] Сначала будет описан аморфный электродно-активный материал в соответствии с первым примером осуществления настоящего изобретения. Упомянутый электродно-активный материал в соответствии с этим примером воплощения настоящего изобретения является электродно-активным материалом, который используется совместно с раствором электролита, имеющим потенциал Ve разложения электролита. Упомянутый электродно-активный материал аморфный и может быть представлен общим выражением LixFeMyOz, где x и y являются значениями, которые независимо удовлетворяют 1<x≤2,5 и 0<y≤3 соответственно, и z=(х+(валентность Fe)+(валентность М)×y)/2, чтобы удовлетворить стехиометрии. Также М представляет один или два или более типов стеклообразующего элемента, а средняя электроотрицательность М меньше чем (Ve+6,74)/5,41.
[0016] В соответствии с примером осуществления настоящего изобретения окислительный потенциал от трехвалентного ло четырехвалентного Fe может быть уменьшен так, что он будет меньше, чем потенциал разложения электролита, путем установки средней электроотрицательности М с учетом потенциала Ve разложения электролита. В результате может использоваться трехвалентное-четырехвалентное окисление-восстановление, что позволяет получить электродно-активный материал с высокой емкостью. Кроме того, упомянутый электродно-активный материал в соответствии с примером осуществления настоящего изобретения аморфен, это выгодно тем, что он позволяет свободно устанавливать состав электродно-активного материала. Кстати, упомянутый электродно-активный материал в соответствии с примером осуществления настоящего изобретения обычно используется как положительный электродно-активный материал. Также упомянутый электродно-активный материал в соответствии с примером осуществления настоящего изобретения может быть назван аморфным электродно-активным материалом и представлен общим выражением LixFeMyOz.
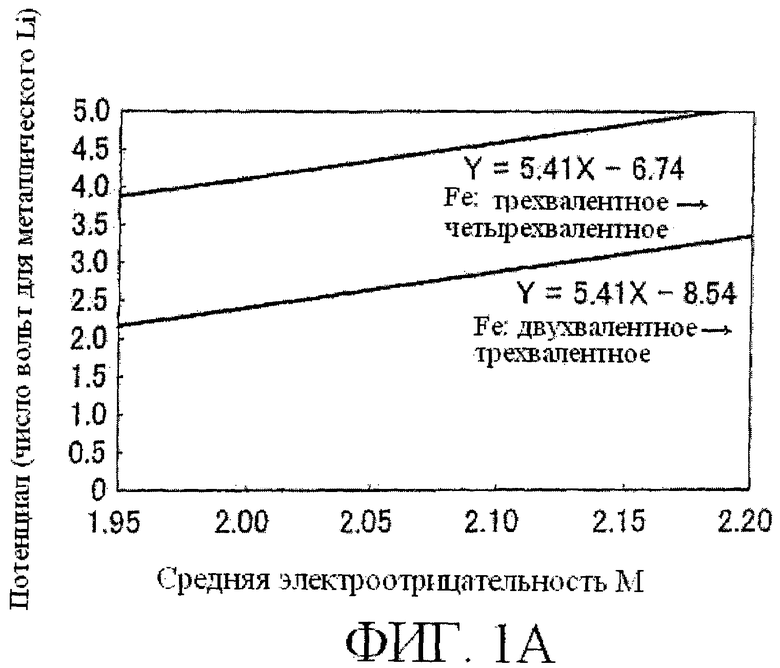
[0017] Фиг.1А и 1В - графики, показывающие связь между окислительным потенциалом Fe и средней электроотрицательностью М в аморфном электродно-активном материале, представленном общим выражением LixFeMyOz. Как показано на Фиг.1А, для аморфного электродно-активного материала, представленного общим выражением LixFeMyOz, когда ось x представляет среднюю электроотрицательность М и ось y представляет упомянутый потенциал (В для металлического лития), соотношение Y=5,41X-6,74 выполняется для окислительного потенциала от трехвалентного Fe до четырехвалентного Fe, и соотношение Y=5,41X-8,54 выполняется для окислительного потенциала от двухвалентного до трехвалентного Fe.
[0018] В известном уровне техники упомянутый окислительный потенциал от трехвалентного до четырехвалентного Fe выше, чем потенциал разложения раствора электролита, используемого так, чтобы раствор электролита сначала разложить, когда потенциал увеличивается. В результате трехвалентное-четырехвалентное окисление-восстановление не могло быть использовано. Однако в этом примере осуществления настоящего изобретения, как показано на Фиг.1В, когда потенциал разложения электролита равен Ve (число вольт для металлического Li), средняя электроотрицательность М устанавливается так, чтобы соответствовать этому значению Ve. Более конкретно, средняя электроотрицательность М устанавливается меньше чем (Ve+6,74)/5,41. В результате упомянутый окислительный потенциал от трехвалентного до четырехвалентного Fe становится меньше, чем потенциал разложения используемого раствора электролита, так что может использоваться трехвалентное-четырехвалентное окисление-восстановление, таким образом позволяя получить электродно-активный материал с высокой емкостью. Таким образом, средняя электроотрицательность М в этом примере осуществления настоящего изобретения определяется как меньшая чем (Ve+6,74)/5,41. Далее, упомянутый электродно-активный материал в соответствии с примером осуществления настоящего изобретения будет описан с делением на следующие пункты: i) структура упомянутого электродно-активного материала, ii) раствор электролита, используемый с упомянутым электродно-активным материалом, и iii) способ изготовления упомянутого электродно-активного материала.
[0019] Электродно-активный материал в соответствии с примером осуществления настоящего изобретения является аморфным и представлен общим выражением LixFeMyOz, где x и y являются значениями, которые независимо удовлетворяют 1<x≤2,5 и 0<y≤3 соответственно, и z=(x+(валентность Fe)+(валентность М)×y)/2, чтобы удовлетворить стехиометрии, М представляет собой один или два или более типов стеклообразующего элемента, а средняя электроотрицательность М меньше чем (Ve+6,74)/5,41.
[0020] В этом общем выражении значение x обычно 1<x≤2,5, предпочтительно 1,5≤х≤2,5 и более предпочтительно 1,75≤х≤2,5. Если значение x равно или меньше чем 1, то теоретически Fe не может иметь валентность 4. И наоборот, если значение x слишком большое, то аморфный электродно-активный материал не может быть получен.
[0021] В вышеизложенном общем выражении значение y обычно 0<y≤3, предпочтительно 1,5≤y≤3 и более предпочтительно 1,5≤y≤2,5. Если значение y слишком мало, то аморфный электродно-активный материал не может быть получен. С другой стороны, если значение y слишком велико, то емкость становится меньше так, что на практике электродно-активный материал не может быть получен.
[0022] В вышеизложенном общем выражении значение z изменяется в зависимости от значения x, валентности Fe, электроотрицательности М и значения y, но оно обычно представляется z=(х+(валентность Fe)+(валентность М)×y)/2, чтобы удовлетворить стехиометрии. То есть в этом примере осуществления настоящего изобретения значение z определяется, чтобы удовлетворить электронейтральности. Кстати, в примере осуществления настоящего изобретения валентность Fe изменяется от 2 до 4 с зарядкой и разрядкой, но когда электродно-активный материал в соответствии с этим примером осуществления настоящего изобретения синтезируется с использованием способа быстрого охлаждения расплава, который будет описан позже, например, валентность Fe обычно равна 2 или 3.
[0023] В вышеизложенном общем выражении М представляет собой один или два или более типов стеклообразующего элемента. Элемент М не особенно ограничивается, пока он является стеклообразующим элементом. Более конкретно, элемент М может быть, например, бором (В), фосфором (Р), кремнием (Si) или оловом (Sn). Из этих элементов бор (В) является предпочтительным, пока электроотрицательность находится в пределах соответствующего диапазона, который позволяет повысить емкость упомянутого электродно-активного материала.
[0024] В вышеизложенном общем выражении средняя электроотрицательность М меньше чем (Ve+6,74)/5,41. Кстати, упомянутый потенциал Ve разложения электролита будет описан позже по отношению к раствору электролита, который используется вместе с упомянутым электродно-активным материалом. Термин «электроотрицательность» в этом примере осуществления настоящего изобретения относится к электроотрицательности по Полингу. Более конкретно, для бора (В) она состаляет 2,04, для фосфора (Р) - 2,19, для кремния (Si) - 1,90 и для олова (Sn) - 1,96. Также термин «средняя электроотрицательность» в этом примере осуществления настоящего изобретения относится к взвешенной средней электроотрицательности каждого элемента, который составляет или образует М. Например, когда М образуется из бора (В) и фосфора (Р), так что М=В1.5Р0.5, средняя электроотрицательность ((2,04×1,5)+(2,19×0,5))/(1,5+0,5)=2,08.
[0025] Здесь, когда средняя электроотрицательность М равна (Ve+6,74)/5,41, упомянутый окислительный потенциал от трехвалентного до четырехвалентного Fe становится равным потенциалу разложения раствора электролита, так что раствор электролита заканчивает разлагаться одновременно с окислением Fe. Поэтому средняя электроотрицательность М просто должна быть меньше чем (Ve+6,74)/5,41, предпочтительно равна или меньше чем ((Ve+6,74)/5,41)-0,05 и более предпочтительно равна или меньше чем ((Ve+6,74)/5,41)-0,1, пока она позволяет электродно-высокоактивному материалу быть безопаснее.
[0026] Хотя диапазон средней электроотрицательности М отличается в зависимости от потенциала разложения раствора электролита и подобного, она предпочтительно равна или меньше чем 2,17 и более предпочтительно равна или меньше чем 2,07.
[0027] Одна характеристика электродно-активного материала в соответствии с примером осуществления настоящего изобретения состоит в том, что он аморфен. Этот электродно-активный материал является предпочтительно аморфным в той мере, что выполняются одно или два или более следующих условий: (1) средний размер кристаллов равен или меньше чем примерно 1000 ангстрем (предпочтительно равен или меньше чем примерно 100 ангстрем и более предпочтительно равен или меньше чем 50 ангстрем); (2) удельный вес упомянутого электродно-активного материала больше или равен или больше примерно 3% (и более предпочтительно равен или больше чем примерно 5%) по сравнению с конкретным удельным весом (теоретическое значение), когда электродно-активный материал является полностью кристаллическим; и (3) нет максимального значения нагрузки, которая поддерживает упомянутый электродно-активный материал кристаллическим, что может наблюдаться на дифракционной рентгеновской картине. Упомянутый электродно-активный материал, рассмотренный здесь, является предпочтительно электродно-активным материалом, который удовлетворяет одному или двум или более из условий от (1) до (3). Или электродно-активный материал является предпочтительно электродно-активным материалом, который удовлетворяет, по меньшей мере, условию (3). Дифракционная рентгеновская картина может быть получена, например, с использованием дифрактометра рентгеновских лучей (номер модели: Rigaku RINT 2100 HLR/PC) или подобного устройства фирмы Rigaku Corporation. Эффект от применения этого примера осуществления настоящего изобретения имеет тенденцию к увеличению с электродно-активным материалом, который более аморфен (т.е. менее кристалличен).
[0028] Далее будет описан раствор электролита, который используется вместе с упомянутым электродно-активным материалом. Упомянутый электродно-активный материал в соответствии с примером осуществления настоящего изобретения используется вместе с раствором электролита, имеющим потенциал Ve разложения электролита. Единицей измерения упомянутого потенциала Ve разложения электролита является (число вольт для металлического Li), но для удобства может просто быть названа как В.
[0029] Упомянутый потенциал Ve разложения электролита отличается в зависимости от состава используемого раствора электролита и, хотя не ограничивается практически, предпочтительно находится в пределах диапазона от 4,00 В до 5,00 В и более предпочтительно в пределах диапазона, например, от 4,00 В до 4,50 В. Кстати, самый высокий потенциал разложения какого-либо практического раствора электролита, используемый в настоящее время, равен примерно 4,50 В. Однако в этом примере осуществления настоящего изобретения проявляются достаточные эффекты от примера осуществления настоящего изобретения, даже если используется раствор электролита, имеющий потенциал разложения, который превышает 4,50 В. Потенциал разложения может определяться значением, указанным в химической брошюре или подобной брошюре, или результатами измерений, когда с упомянутым раствором электролита проводится фактический эксперимент разложения.
[0030] Раствор электролита обычно содержит соль-носитель и растворитель. Упомянутая соль-носитель может быть какой-либо из различных литиевых солей, таких как, например, LiPF6, LiBF4, LiN(CF3SO2)2, LiCF3SO3, LiC4F9SO3, LiC(CF3SO2)3 и LiClO4. Растворитель может быть каким-либо из различных типов апротонных растворителей, таких как карбонатного типа, типа сложных эфиров, типа простых эфиров, типа нитрилов, сульфонов или лактонов, или, например, соль, расплавленная при окружающей температуре. Конкретные примеры включают пропиленкарбонат; этиленкарбонат; диэтилкарбонат; диметилкарбонат; этилметилкарбонат; 1,2-диметоксиэтан; 1,2-диэтоксиэтан; ацетонитрил; пропионитрил; тетрагидрофуран; 2-метилтетрагидрофуран; диоксан; 1,3-диоксолан; нитрометан; N,N-диметилформамид; диметилсульфоксид; сульфолан; γ-бутиролактон и 1-этил-3-метилимидазолия тетрафторборат (EMI-BF4). В этом примере осуществления настоящего изобретения может использоваться только один тип или смесь из двух или более типов этих растворителей.
[0031] Далее будет описан способ производства упомянутого электродно-активного материала в соответствии со вторым примером осуществления настоящего изобретения. Способ производства упомянутого электродно-активного материала в соответствии с этим примером осуществления настоящего изобретения не особенно ограничен, пока он является способом, посредством которого может быть получен упомянутый, описанный выше, электродно-активный материал. Одним примером является способ быстрого охлаждения расплава. Одним конкретным примером упомянутого способа быстрого охлаждения расплава является способ перемешивания расплава состава из сырьевых материалов, который включает сырьевые материалы, образующие общее выражение LixFeMyOz, и быстрого затвердевания этого состава из сырьевых материалов из расплавленного состояния. Упомянутый состав из сырьевых материалов обычно содержит Li-сырьевой материал, Fe-сырьевой материал и М-сырьевой материал.
[0032] Упомянутый Li-сырьевой материал не особенно практически ограничен, пока он содержит элемент Li. Например, Li-сырьевой материал может быть Li2O, LiOH или Li2CO3 или подобным. Li2O является предпочтительным. В этом примере осуществления настоящего изобретения может быть использован один или два или более типов Li-сырьевого материала. Упомянутый Fe-сырьевой материал не особенно ограничен, пока он содержит элемент Fe. Например, Fe-сырьевой материал может быть FeO или Fe2O3, FeO является более предпочтительным. В этом примере осуществления настоящего изобретения может быть использован один или два или более типов Fe-сырьевого материала.
[0033] Упомянутый М-сырьевой материал не особенно ограничен, пока он включает стеклообразующий элемент, описанный выше. Примеры М-сырьевого материала включают гидроксид и оксид, имеющие стеклообразующий элемент, описанный выше. Более конкретно, когда стеклообразующим элементом является бор (В), может быть использован В2O3 или подобное. Когда стеклообразующим элементом является фосфор (Р), может быть использован Р2O5 или подобное. Когда указанный стеклообразующий элемент является кремнием (Si), может быть использован SiO2 или подобное. Когда указанный стеклообразующий элемент является оловом (Sn), может быть использован SnO2 или подобное. В этом примере осуществления настоящего изобретения может быть использован один или два или более типов М. В этом примере осуществления настоящего изобретения тип и количество М, которое используется, устанавливаются так, что средняя электроотрицательность М меньше, чем упомянутое значение, описанное выше.
[0034] В этом примере осуществления настоящего изобретения аморфный электродно-активный материал может быть получен путем регулирования состава из сырьевых материалов для соответствия соотношения целевого элемента, расплавления этого состава из сырьевых материалов при примерно 1200°С, например, и затем быстрого охлаждения его с использованием однороликового аппарата быстрого охлаждения, снабженного медным (Cu) роликом.
[0035] Далее будет описана литиевая вторичная батарея в соответствии с третьим примером осуществления настоящего изобретения. Упомянутая литиевая вторичная батарея в соответствии с примером осуществления настоящего изобретения включает слой положительного электрода, который включает вышеизложенный электродно-активный материал как положительный электродно-активный материал; слой отрицательного электрода, который включает отрицательный электродно-активный материал; сепаратор, расположенный между слоем положительного электрода и слоем отрицательного электрода; и раствор электролита, имеющий потенциал Ve разложения электролита, которым пропитан, по меньшей мере, сепаратор.
[0036] В соответствии с этим примером осуществления настоящего изобретения литиевая вторичная батарея с высокой емкостью может быть получена путем комбинирования вышеописанного электродно-активного материала с вышеописанным раствором электролита. То есть, как показано на Фиг.1В, описанной выше, трехвалентное-четырехвалентное окисление-восстановление Fe может использоваться путем установки значения средней электроотрицательности М в аморфном электродно-активном материале, представленном общим выражением LixFeMyOz, в соответствии с упомянутым потенциалом Ve разложения электролита. Возможность использовать это трехвалентное-четырехвалентное окисление-восстановление Fe позволяет получить литиевую вторичную батарею с высокой емкостью.
[0037] Упомянутый электродно-активный материал и раствор электролита, используемый в этом примере осуществления настоящего изобретения, являются теми же, что и упомянутый электродно-активный материал и раствор электролита в первом примере осуществления настоящего изобретения, поэтому их описания будут пропущены здесь. Также упомянутая структура литиевой вторичной батареи в соответствии с этим примером осуществления настоящего изобретения не особенно ограничена и может быть установлена по мере необходимости, пока она, по меньшей мере, имеет вышеописанный электродно-активный материал и вышеописанный раствор электролита.
[0038] Слой положительного электрода обычно включает проводящее вещество и связующее в дополнение к положительному электродно-активному материалу. Проводящее вещество может быть, например, сажей или ацетиленовой сажей. Связующим может быть, например, поливинилиденфторид (PVDF) или политетрафторэтилен (PTFE). Также упомянутая литиевая вторичная батарея в соответствии с этим примером осуществления настоящего изобретения может также иметь положительный электродный коллектор, который отбирает энергию от слоя положительного электрода. Материалом этого положительного электродного коллектора может быть, например, нержавеющая сталь, никель, алюминий, железо или титан.
[0039] Слой отрицательного электрода обычно включает отрицательный электродно-активный материал, проводящее вещество и связующее. Упомянутый отрицательный электродно-активный материал не особенно ограничен, пока он может хранить и высвобождать литиевые ионы. Примеры включают литий, литиевый сплав, оксид металла, сульфид металла, нитрид металла и углеродный материал, такой как графит. Применение лития является предпочтительным. Проводящее вещество и связующее могут быть теми же, что и используемые со слоем положительного электрода, описанного выше. Также литиевая вторичная батарея в соответствии с этим примером осуществления настоящего изобретения может иметь отрицательный электродный коллектор, который отбирает энергию от слоя отрицательного электрода. Материалом отрицательного электродного коллектора может быть, например, медь, нержавеющая сталь или никель.
[0040] Упомянутый сепаратор не особенно ограничен, пока он действует, чтобы отделять слой положительного электрода от слоя отрицательного электрода и удерживать раствор электролита. Возможные примеры включают пористую мембрану, такую как полиэтилен или полипропилен, и нетканый материал, например смолистый нетканый материал или стекловолокнистый нетканый материал. Также литиевая вторичная батарея, получаемая в примере осуществления настоящего изобретения, может быть любой из различных форм, например в виде монеты, ламинированной (пакетированной) или цилиндрической.
[0041] Настоящее изобретение не ограничивается вышеизложенными примерами осуществления. Вышеизложенные примеры осуществления иллюстрируют только примеры. Другие примеры, имеющие, по существу, ту же структуру, как и упомянутые технические предложения, описанные в объеме формулы изобретения для патента на изобретение и отражающие ту же работу и эффекты, также включаются в технический объем настоящего изобретения.
[0042] Далее настоящее изобретение будет описано еще более подробно со следующими примерами. Были приготовлены LiOH как Li-сырьевой материал, FeO как Fe-сырьевой материал Р2O5 как Р-сырьевой материал и В2O3 как В-сырьевой материал. С использованием этих сырьевых материалов затем были получены компоненты от А до С сырьевых материалов путем смешивания составляющих компонентов вместе так, что соотношение молярности было тем же, что показано в Таблице 1 ниже.
[0044] Далее упомянутые компоненты сырьевых материалов были расплавлены в течение 1 минуты при 1200°С в среде аргона и затем быстро охлаждены с помощью однороликового аппарата быстрого охлаждения, снабженного медным (Cu) роликом, для получения электродно-активных материалов от А до С. Кристалличность каждого из полученных электродно-активных материалов от А до С была затем оценена с использованием дифракционной рентгеновской картины при следующих условиях измерений: используемый аппарат: Rigaku, RAD-X; рентгеновские лучи: CuКα, 40 кВ, 40 мА; диапазон сканирования: 2 θ ≈ от 10° до 80°. В результате для любого из упомянутых электродно-активных материалов от А до С на дифракционной рентгеновской картине не могло наблюдаться максимальное значение напряжения, которое поддерживает кристалличность, поэтому аморфность всех упомянутых электродно-активных материалов от А до С была подтверждена.
[0045] Далее с использованием упомянутых электродно-активных материалов от А до С были изготовлены испытуемые ячейки и оценивались характеристики зарядки и разрядки каждой ячейки. Сначала 0,4 грамма электродно-активного материала А было взвешено и добавлено в циркониевый резервуар мельницы. Затем было осуществлено перемешивание в шаровой мельнице в течение 3 часов при 300 оборотах в минуту. Далее было добавлено 0,1429 граммов ацетиленовой сажи и осуществлено перемешивание в шаровой мельнице в течение еще 3 часов при 300 оборотах в минуту. Затем в полученный порошок было добавлено 0,053 грамма PTFE, и эта смесь затем была нанесена на сетку из нержавеющей стали для получения положительного электрода.
[0046] Далее были приготовлены металлический литий как противоположный электрод и полиэтиленовый сепаратор (Ube Industries, Ltd.). Также был приготовлен раствор электролита путем растворения 1 моль/литр LiPF6 как соли-носителя в смешанном растворителе, имеющего объемное соотношение 3:7 этиленкарбоната (ethylene carbonate - ЕС) и диэтилкарбоната (diethyl carbonate - DEC). С использованием этих материалов была получена испытуемая ячейка А, которая является ячейкой в виде монеты типа 2032. Затем тем же образом были получены испытуемые ячейки В и С, за тем исключением, что вместо электродно-активного материала А были использованы, соответственно, электродно-активные материалы В и С.
[0047] Далее осуществили зарядку и разрядку с использованием упомянутых испытуемых ячеек от А до С, полученных как описано выше, при следующих условиях: зарядка: 4,5 В, СС157 мкА, состояние покоя: 5 минут, разрядка: 1,5 В, СС157 мкА, состояние покоя: 5 минут.
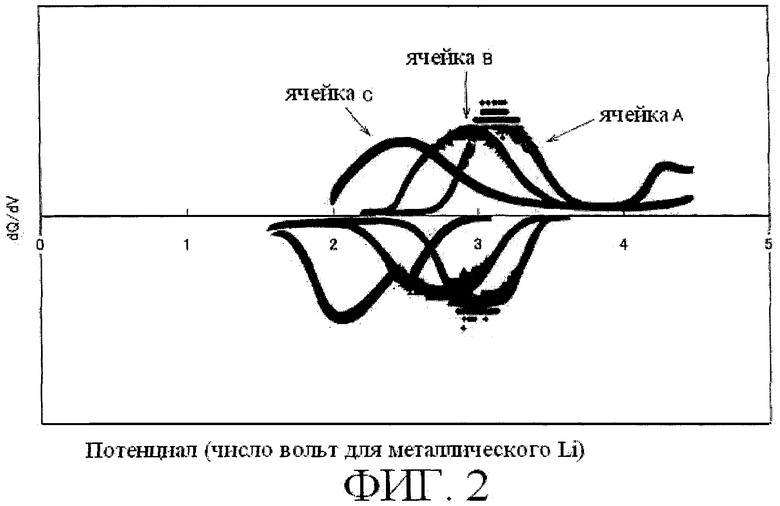
[0048] Фиг.2 представляет собой график, на котором полученные кривые зарядки и разрядки были преобразованы в дифференциальную емкость. Как очевидно следует из Фиг.2, двухвалентное-трехвалентное окисление-восстановление Fe было подтверждено в испытуемых ячейках А и В, хотя трехвалентное-четырехвалентное окисление-восстановление Fe не было подтверждено. С другой стороны, в испытуемой ячейке С окислительный потенциал трехвалентного-четырехвалентного Fe наблюдался около 4,3 В, а также окислительный потенциал двухвалентного-трехвалентного Fe наблюдался около 2,5 В.
[0049] Результаты Фиг.2 сведены в показанной ниже Таблице 2.
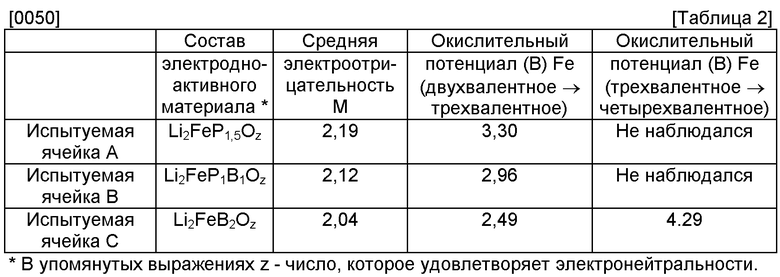
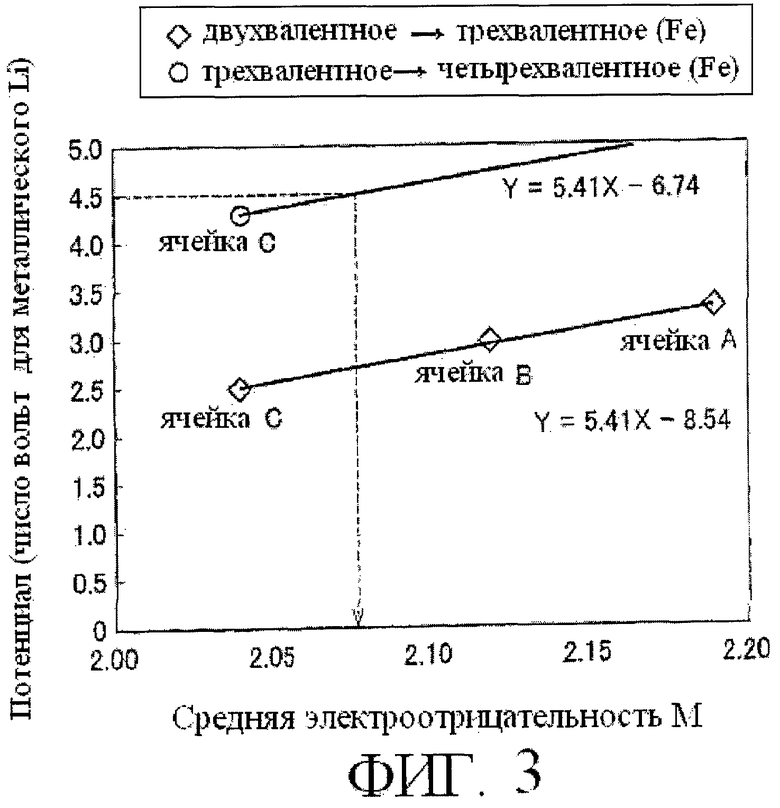
[0051] Фиг.3 является графиком, на котором ось x представляет среднюю электроотрицательность М, а ось y представляет упомянутый окислительный потенциал. Как очевидно следует из Фиг.3, было подтверждено, что, когда средняя электроотрицательность М снижается, окислительный потенциал от двухвалентного до трехвалентного Fe также снижается. Кстати, на Фиг.3 прямая линия окислительного потенциала от двухвалентного до трехвалентного Fe и прямая линия окислительного потенциала от трехвалентного до четырехвалентного Fe параллельны. Это так, поскольку окислительно-восстановительный потенциал определяется соотношением между присущим потенциалом, который имеет изменение валентности Fe, и электроотрицательностью, которую имеет элемент (Li, М, О) возле Fe. Кроме того, принимая во внимание, что напряжение разложения раствора электролита, используемое в этом примере, составляет 4,50 В, средняя электроотрицательность М может быть равна или меньше чем 2,07, чтобы реализовать трехвалентное-четырехвалентное окисление-восстановление Fe. Средняя электроотрицательность М в обеих испытуемых ячейках А и В выше чем примерно 2,07, поэтому фактически в испытуемых ячейках А и В не было возможности использовать трехвалентное-четырехвалентное окисление-восстановление. Средняя электроотрицательность М в испытуемой ячейке С, однако, ниже чем примерно 2,07, поэтому в испытуемой ячейке С не было возможности использовать трехвалентное-четырехвалентное окисление-восстановление.
Изобретение относится к способу зарядки литиевой вторичной батареи, которая использует аморфный электродно-активный материал. Согласно изобретению литиевая вторичная батарея содержит слой положительного электрода, который включает положительный электродно-активный материал; слой отрицательного электрода, который включает отрицательный электродно-активный материал; сепаратор, расположенный между слоем положительного электрода и слоем отрицательного электрода; и раствор электролита, имеющий потенциал Ve разложения электролита, которым пропитан, по меньшей мере, сепаратор; в котором положительный электродно-активный материал является аморфным и положительный электродно-активный материал представлен общим выражением LixFeMyOz, при этом в указанном выражении х и у являются значениями, которые независимо удовлетворяют 1<х≤2,5 и 0<y≤3 соответственно, и z=(x+(валентность Fe)+(валентность М)×y)/2, чтобы удовлетворить стехиометрии, М представляет собой один или два или более типов стеклообразующего элемента. Средняя электроотрицательность М меньше чем (Ve+6,74)/5,41. Батарея заряжается до 4,5 В. Техническим результатом является улучшение характеристик зарядки и разрядки. 2 з.п. ф-лы, 4 ил., 2 табл.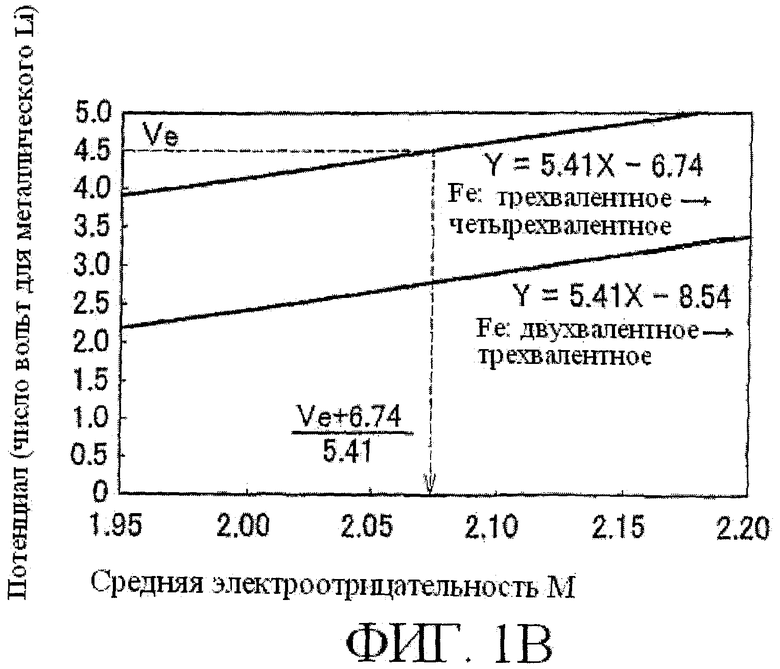
1. Способ зарядки литиевой вторичной батареи, литиевая вторичная батарея содержит:
слой положительного электрода, который включает положительный электродно-активный материал;
слой отрицательного электрода, который включает отрицательный электродно-активный материал;
сепаратор, расположенный между слоем положительного электрода и слоем отрицательного электрода; и
раствор электролита, имеющий потенциал Ve разложения электролита, которым пропитан, по меньшей мере, сепаратор;
в котором положительный электродно-активный материал является аморфным и положительный электродно-активный материал представлен общим выражением LixFeMyOz, при этом в указанном выражении x и y являются значениями, которые независимо удовлетворяют 1<x≤2,5 и 0<y≤3 соответственно, и z=(x+(валентность Fe)+(валентность М)×y)/2, чтобы удовлетворить стехиометрии, М представляет собой один, или два, или более типов стеклообразующего элемента, а средняя электроотрицательность М меньше, чем (Ve+6,74)/5,41, способ характеризуется тем, что вторичная батарея заряжается до 4,5 В.
2. Способ по п.1, в котором средняя электроотрицательность М равна или меньше чем 2,07.
3. Способ по п.1 или 2, в котором М является бором.
| Топчак-трактор для канатной вспашки | 1923 |
|
SU2002A1 |
| Способ измерения расхода горючего двигателем внутреннего сгорания | 1980 |
|
SU1681739A3 |
| Установка для сульфитирования продуктов газообразным сернистым ангидридом | 1974 |
|
SU503901A1 |
| RU 2005118109 A, 20.01.2006. | |||
Авторы
Даты
2011-11-10—Публикация
2008-03-28—Подача