СВЯЗАННЫЕ ЗАЯВКИ
По этой заявке испрашивается приоритет согласно предварительной заявке США 60/790340, поданной 7 апреля 2006 г., содержание которой включено в полном объеме посредством ссылки.
УРОВЕНЬ ТЕХНИКИ
Запор, распространенное и неприятное состояние, наблюдается у приблизительно 20% населения на западе. Наиболее часто это состояние может вызвать рацион с низким содержанием клетчатки, недостаток физической активности, недостаточное потребление воды или несвоевременное посещение туалета. Стресс и путешествия также могут приводить к возникновению запора. Другие причины включают кишечные заболевания (например, воспалительное заболевание кишечника и синдром раздраженной кишки), кистозный фиброз, беременность, проблемы с психикой или прием лекарственных средств.
Сбалансированная диета, регулярные упражнения и уменьшение стресса могут помочь в предотвращении запора. Кроме того, существует ряд слабительных средств с подтвержденной клинически эффективностью для избавления от запора. Тем не менее при проведении новых терапий было доказано, что такие средства неудовлетворительны. Таким образом, существует потребность в альтернативном средстве для лечения запора.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к композиции и к способу лечения запора.
В одном аспекте, это изобретение относится к фармацевтической композиции, как в твердой (сухой), так и в солюбилизирированной форме, содержащей фармацевтически приемлемый энтеросолюбильный носитель и антрацендионовое соединение формулы (I):
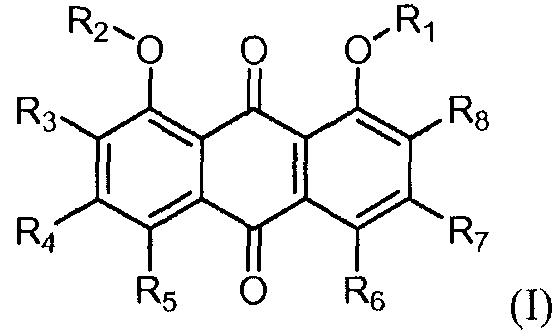 ,
,
где каждый из R1 и R2, независимо, представляет собой Н, C1-C6 алкил или C(O)Ra; каждый R3, R5, R6 и R8, независимо, представляет собой Н, C1-C6 алкил или ORb; и каждый R4 и R7, независимо, представляет собой Н, ORc, COORc, OC(O)ORd, SRd, NHRd или C1-C6 алкил, необязательно замещенный C3-C20 циклоалкилом, C1-C20 гетероциклоалкилом, арилом, гетероарилом, ORс, COORd, OC(O)ORd, SRd или NHRd; где каждый из Ra и Rc представляет собой C1-C10 алкил; и каждый из Rb и Rd, независимо, представляет собой Н или C1-C10 алкил.
Соединения, описанные выше, включают их фармацевтически приемлемые соли и их комплексы с металлами. Соли могут быть образованы, например, между отрицательно заряженным кислородом соединения и положительно заряженным неорганическим или органическим ионом. Комплексы с металлами могут быть образованы, например, когда атомы кислорода соединения образуют координационную связь с одним или более ионов металла.
В соответствии с формулой (I) ряд антрацендионовых соединений, описанных выше, включает таковые, где каждый из R4 и R7, независимо, представляет собой Н, C1-C6 алкил (например, CH3) или ORc (например, OCH3). В этих соединениях каждый из R1, R2, R3, R5, R6 и R8 может представлять собой H. Типичные антрацендионовые соединения включают хризофанол и фисцион:
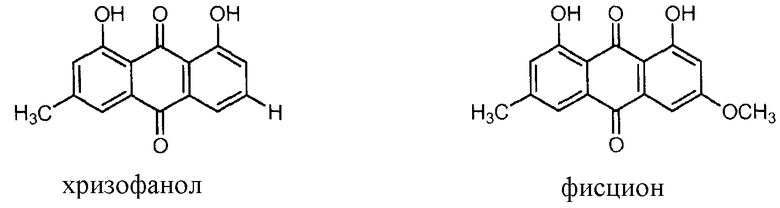 .
.
Термин "алкил" относится к насыщенной или ненасыщенной, линейной или разветвленной углеводородной группе, такой как -CH3, -CH2-CH═CH2 или разветвленному -C3H7. Термин "циклоалкил" относится к насыщенной или ненасыщенной, неароматической, циклической углеводородной группе, такой как циклогексил или циклогексен-3-ил. Термин "гетероциклоалкил" относится к насыщенной или ненасыщенной, неароматической, циклической группе, имеющей по меньшей мере один гетероатом в кольце (например, N, O или S), такой как 4-тетрагидропиранил или 4-пиранил. Термин "арил" относится к углеводородной группе, имеющей одно или более ароматических колец. Примеры арильных групп включают фенил, фенилен, нафтил, нафтилен, пиренил, антрил и фенантрил. Термин "гетероарил" относится к группе, имеющей одно или более ароматических колец, которые содержат по меньшей мере один гетероатом (например, N, O или S). Примеры гетероарильных групп включают фурил, фурилен, флуоренил, пирролил, тиенил, оксазолил, имидазолил, тиазолил, пиридил, пиримидинил, хиназолинил, хинолил, изохинолил и индолил.
Если не указано иначе, упомянутые здесь алкил, циклоалкил, гетероциклоалкил, арил и гетероарил включают как замещенные, так и незамещенные группы. Возможные заместители в циклоалкиле, гетероциклоалкиле, ариле и гетероариле без ограничения включают C1-C10 алкил, C2-C10 алкенил, C2-C10 алкинил, C3-C8 циклоалкил, C5-C8 циклоалкенил, C3-C20 циклоалкил, C1-C20 гетероциклоалкил, C1-C10 алкокси, арил, арилокси, гетероарил, гетероарилокси, амино, C1-C10 алкиламино, C1-C20 диалкиламино, ариламино, диариламино, гидроксил, галоген, тио, C1-C10 алкилтио, арилтио, C1-C10 алкилсульфонил, арилсульфонил, ациламино, аминоацил, аминотиоацил, амидино, гуанидин, уреидо, циано, нитро, ацил, тиоацил, ацилокси, карбоксил и эфир карбоновой кислоты. С другой стороны, возможные заместители в алкиле включают все вышеупомянутые заместители, за исключением C1-C10 алкила, C2-C10 алкенила и C2-C10 алкинила. Циклоалкил, гетероциклоалкил, арил и гетероарил также могут быть объединены друг с другом.
Антрацендионовые соединения, описанные выше, могут применяться для лечения запора, то есть для улучшения перистальтики кишечника при поддержании нормальной кишечной функции. Усиление перистальтики кишечника сокращает продолжительность прохождения пищей кишечного тракта. В результате кишечный тракт адсорбирует меньше пищи, которая часто включает углеводы, жиры, холестерин, липопротеины низкой плотности или триглицериды. Соответственно, антрацендионовые соединения позволяют уменьшить поглощение в теле индивидуума этих нутриентов и, таким образом, (i) снизить уровни холестерина или триглицеридов или (ii) уменьшить или поддержать вес тела. Таким образом, это изобретение также относится к способу использования этих композиций для улучшения перистальтики кишечника и обеспечения нормальной функции кишечника, снижения уровней холестерина, липопротеинов низкой плотности или триглицеридов и уменьшения или поддержания веса тела.
В другом аспекте это изобретение относится к способу лечения воспалительного заболевания кишечника или синдрома раздраженной кишки вышеупомянутыми антрацендионовыми соединениями.
Также в объем этого изобретения включены (1) применение антрацендионовых соединений, описанных выше, для лечения запора, воспалительного заболевания кишечника или синдрома раздраженной кишки, улучшения перистальтики кишечника и поддержания нормальной функции кишечника, снижения уровней холестерина, липопротеинов низкой плотности или триглицеридов, или уменьшения или поддержания веса тела; и (2) применение антрацендионовых соединений для производства лекарственного средства или диетической добавки для указанных выше случаев.
Подробное описание одного или более вариантов выполнения изобретения раскрываются ниже в описании. Другие признаки, объекты и результаты изобретения будут ясны из описания и формулы изобретения.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Это изобретение основано, по меньшей мере частично, на неожиданном установлении того, что два антрацендионовых соединения, хризофанол и фисцион, обнаружены в китайском растении Rheum palmatum Linne, каждое из которых эффективно при лечении запора. Они не вызывают побочных эффектов, часто наблюдаемых при приеме растительных экстрактов из Rheum palmatum Linne, например спазмов, вздутия, газообразования и диареи. Кроме того, каждое соединение обладает очень низкой адсорбцией в кишечнике и поэтому оказывает минимальные побочные эффекты по всему телу.
Соответственно, в объем настоящего изобретения включена композиция, которая содержит энтеросолюбильный носитель и одно или больше антрацендионовых соединений, описанных в разделе «раскрытие изобретения» выше. Энтеросолюбильный носитель выбирается таким образом, чтобы минимизировать быстрое высвобождение лекарственного средства при пероральном введении, до тех пор, пока лекарственное средство не достигнет кишечника. См., например, патенты США 5188836 и 6306434.
Композиция может представлять собой фармацевтическую композицию, которая содержит фармацевтически приемлемый носитель или диетическую композицию, которая содержит приемлемый пищевой носитель. Предпочтительно, антрацендионовое соединение добавляют в композицию в чистом виде или по существу чистом виде. Антрацендионовые соединения для применения в этом изобретении могут быть химически синтезированы или выделены из растений. Например, фисцион и хризофанол могут быть выделены из растений, указанных ниже в таблицах А и B соответственно.
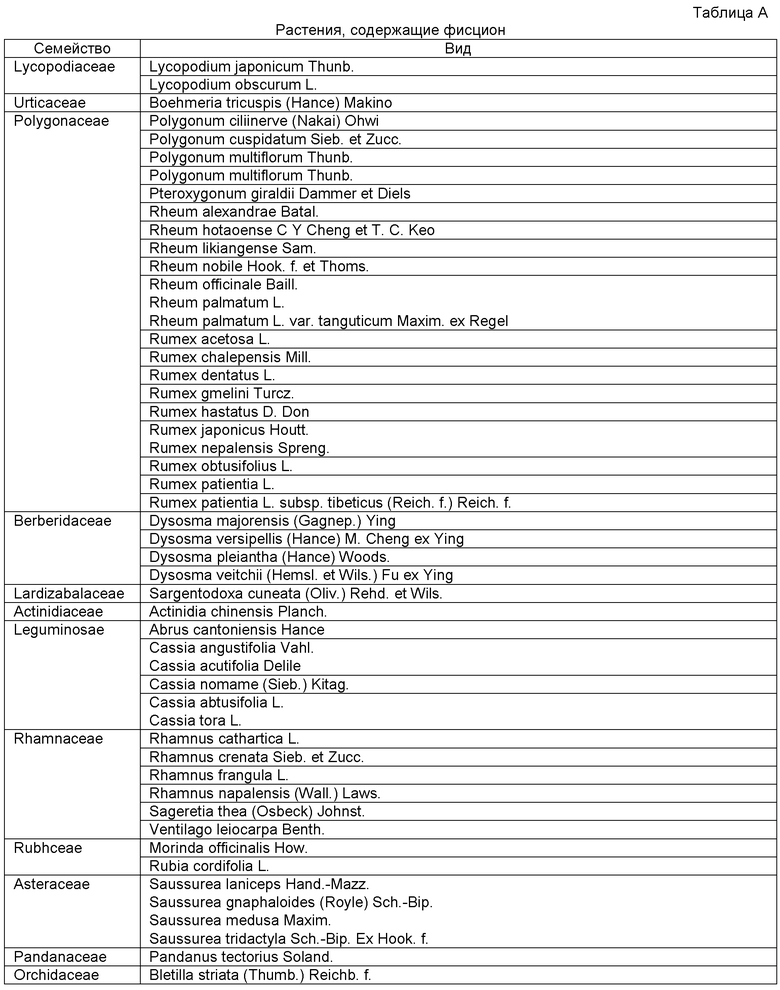
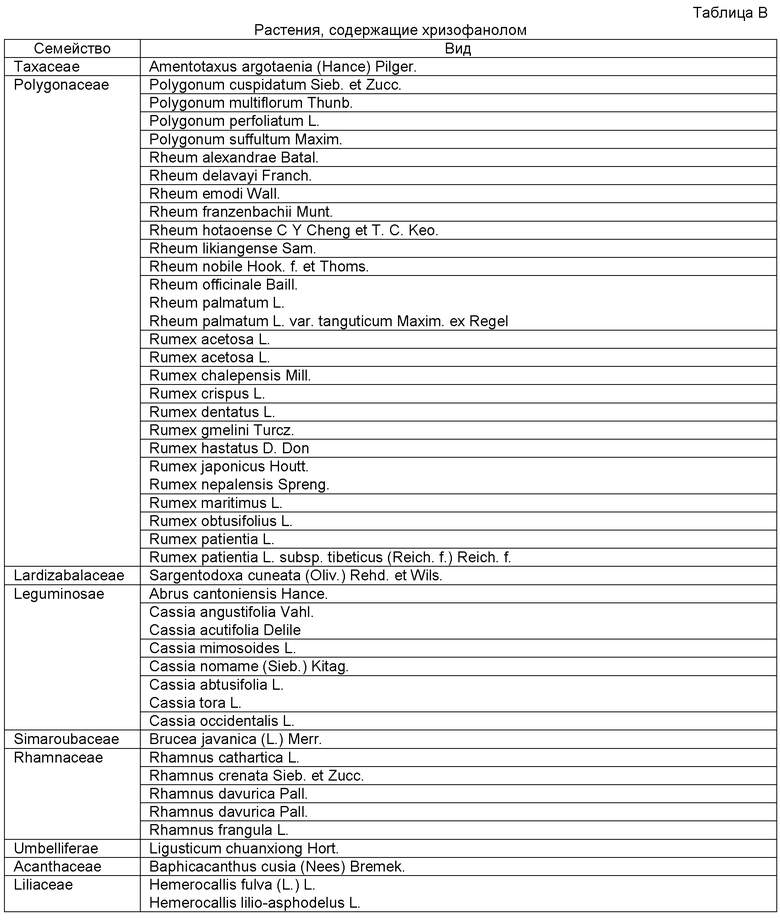
Примеры композиции по настоящему изобретению без ограничения включают пищевые продукты, пищевые добавки, нутрицевтические добавки и фармацевтические препараты. Композиция может быть представлена в виде таблеток, суспензий, имплантов, растворов, эмульсий, капсул, порошков, сиропов, жидких композиций, мазей, лосьонов, кремов, паст, гелей или т.п.
Диетическая композиция по настоящему изобретению как в сухой, так и в солюбилизированной форме содержит одно или более антрацендионовых соединений и пищевой носитель. Могут быть добавлены дополнительные нутриенты, такие как минералы или аминокислоты. Диетическая композиция также может представлять собой питьевой или пищевой продукт. Примеры питьевых продуктов без ограничения включают напитки на основе чая, сок, кофе и молоко. Примеры пищевого продукта включают желе, печенье, продукты из хлебных злаков, конфеты, батончики, экстракты растений, молочные продукты (например, мороженое и йогурт), соевые продукты (например, тофу) и рисовые продукты.
Фармацевтическая композиция для перорального введения может представлять собой любую дозированную форму для перорального приема, включая капсулы, таблетки, эмульсии и водные суспензии, дисперсии и растворы. В случае таблеток, обычно используемые носители включают лактозу и кукурузный крахмал. Также обычно добавляют смазывающие компоненты, такие как стеарат магния. Для перорального введения в виде капсулы используемые разбавители включают лактозу и сухой кукурузный крахмал. При пероральном введении водных суспензий или эмульсий активный ингредиент может быть суспендирован или растворен в масляной фазе, объединенной с эмульгирующими или суспендирующими компонентами. При желании могут быть добавлены некоторые подслащивающие, вкусовые или окрашивающие добавки.
Композиция по настоящему изобретению включает носитель. В зависимости от вида композиции носитель может быть соответствующим диетическим носителем или фармацевтически приемлемым носителем. Примеры фармацевтически приемлемого носителя без ограничения включают биологически совместимые носители, адъювантны, добавки и разбавители для придания композиции соответствующей дозированной формы.
"Фармацевтически приемлемый носитель" относится к такому носителю что, после введения или применения на индивидууме, он не вызывает нежелательных физиологических эффектов. Носитель в фармацевтической композиции должен быть "приемлем" также в том смысле, что он совместим с активным ингредиентом и, предпочтительно, стабилизирует его. Один или более солюбилизирующих компонентов могут использоваться в качестве фармацевтических носителей для доставки активного антрацендионового соединения. Примеры других носителей включают коллоидный оксид кремния, стеарат магния, целлюлозу, лаурилсульфат натрия и D&C Yellow # 10.
Вышеописанная композиция, в любой из форм описанных выше, может применяться для лечения запора. Действительно, как показано в примерах ниже, композиция увеличила выработку кала и содержание воды в кале у индивидуума, не вызывая побочные эффекты, такие как диарея. Также она была эффективна в сокращении или поддержании веса тела индивидуума.
Термин "лечение" относится к введению эффективного количества антрацендионового соединения индивидууму, имеющему заболевание, например запор, воспалительное заболевание кишечника или синдром раздраженной кишки, или имеющему симптомы такого заболевания, или имеющему предрасположение к такому заболеванию, с целью вылечить, излечить, облегчить, уменьшить, изменить, вылечивать, улучшить, оздоровить или воздействовать на заболевание, симптомы заболевания или предрасположение к заболеванию. Термин "введение" охватывает пероральную доставку композиции по изобретению индивидууму в любом соответствующем виде, например пищевом продукте, напитке, таблетке, капсуле, суспензии и растворе. "Эффективное количество" относится к дозе композиции, которая является достаточной для обеспечения физического эффекта (например, увеличение выработки кала и снижение веса тела) или терапевтического эффекта (например, снижение уровней холестерина). Для определения оптимальных путей введения и доз могут быть выполнены как in vivo, так и in vitro исследования. Увеличение выработки кала означает увеличение массы влажного кала, производимого индивидуумом, на 15% или больше, спустя день после получения индивидуумом активной композиции, как определено в методике, описанной в примере 3 ниже, или в любой аналогичной методике.
Композиция по настоящему изобретению может быть использована отдельно или в комбинации с другими биологически активными ингредиентами. Она может быть введена индивидууму в одной дозе или в нескольких дозах в течение периода времени, в общем случае перорально. Различные схемы введения очевидны для специалистов в данной области. Диапазоны доз для введения композиции должны находиться в таких пределах, чтобы обеспечить требуемый эффект. Доза не должна вызывать какие-либо неблагоприятные побочные эффекты, такие как нежелательные перекрестные реакции и т.п. В общем случае доза зависит от возраста, веса, пола, состояния и степени состояния индивидуума и поставленной цели. Доза может быть определена специалистом в данной области без проведения чрезмерного количества экспериментов. Доза может быть скорректирована при возникновении противопоказаний, толерантности или подобных состояний. Специалисты в данной области легко могут оценить такие факторы и, основываясь на такой информации, могут определить конкретную эффективную концентрацию композиции по настоящему изобретению для применения по соответствующему назначению.
Конкретные примеры, приведенные ниже, следует рассматривать как иллюстративные, а не ограничивающие раскрытие изобретения. Специалист в данной области без проведения дополнительных экспериментов, основываясь на описании, может использовать настоящее изобретение в наиболее полной степени. При указании ссылок на документы, их содержание включается полностью.
Пример 1
Алоэ-эмодин, реин, эмодин, хризофанол и фисцион выделяли из экстракта STD-05 из Rheum palmatum Linne. Для получения STD05 3,2 кг Rheum palmatum дважды экстрагировали 12 л этилацетата в течение 18 часов. Полученный раствор фильтровали через фильтр 200 меш. Фильтрат концентрировали под вакуумом, растворяли в 2 л 95% этанола и осаждали в 6 л воды. Затем преципитат растворяли в 95% этаноле и снова осаждали водой, получая преципитат "Fr-I". Супернатант фракционировали на колонке Dianon HP-20 и элюировали 30% этанолом, а затем 95% этанолом и этилацетатом. Элюаты, фракционированные 95% этанолом (Fr-D) и этилацетатом (Fr-E), объединяли с Fr-I, получая STD05. Двадцать граммов STD05 растворяли в этилацетате и смешивали с небольшим количеством силикагеля. Затем удаляли этилацетат под вакуумом, получая смесь. Смесь очищали элюированием на колонке с силикагелем от 0% до 5% этилацетата в гексане. Полученные таким образом фракции анализировали ВЭЖХ. ВЭЖХ были идентифицированы пять соединений. Фракции каждого соединения объединяли соответственно. Растворитель из каждого объединенного раствора удаляли под вакуумом, получая пять твердых продуктов. Твердые продукты перекристаллизовывали из ацетона, получая 220 мг алоэ-эмодина, 290 мг реина, 1270 мг эмодина, 2220 мг хризофанола и 790 мг фисциона. Результаты показаны в таблице 1 ниже.
Выделение соединений
Гексан:Этилацетат
Каждое из выделенных соединений кристаллизовывали и исследовали под микроскопом.
Пример 2
Исследовали слабительное действие экстрактов Rheum palmatum Linne. Неочищенный экстракт Rheum palmatum Linne и STD05 получали от SunTen Phytotech Co., Ltd. (Jhonghe City, Taiwan). Коммерческие доступные слабительные - Through® (Chung Mei Pharmaceutical Co., Ltd.; активный ингредиент: Сеннозиды 20 мг, Сеннозиды A+B 12 мг, Партия 009А 051) и Dulcolax ® (Boehringer Ingelheim, Taiwan, Ltd.; активный ингредиент: Бисакодил; Партия 4804942) были закуплены в аптеке.
Сорок два здоровых самцов крыс S.D. (8 недель; National Laboratory Animal Center, Taiwan) делили на семь групп (по шесть в каждой) и использовали для исследования слабительной активности экстрактов из Rheum palmatum Linne. Одна группа крыс не получала экстракты и лекарственные средства и ее использовали в качестве отрицательного контроля. Крысы во второй и третьей группе получали Сеннозиды (3,55 мг/кг) и Бисакодил (1,75 мг/кг) соответственно, и их использовали в качестве положительного контроля. Крысы в других четырех группах получали неочищенный экстракт из Rheum palmatum Linne (500 мг/кг), отфильтрованный неочищенный экстракт STD03 (180 мг/кг) и STD05 (STD05-1: 12 мг/кг и STD05-2: 24 мг/кг) соответственно. Все вещества вводили перорально каждый день в течение трех недель.
Эксперименты выполняли в условиях контроля температуры, влажности и освещения. Каждой крысе был доступен ad libitum стандартный корм для крыс и вода, в помещении с 12-часовым циклом освещения/темноты. Крыс разделяли на семь групп в соответствии с массой.
В первой части эксперимента исследовали влияние вышеупомянутых экстрактов на выработку фекалий. В течение трехнедельного периода крысу, у которой наблюдали признаки гибели, подвергали эвтаназии, проводили вскрытие и исследовали на предмет болезни или повреждений. При любых осложнениях или болезни проводили анализ H&E окрашиванием для определения причины смерти и переоценки доз для будущих экспериментов.
В этот период проводили взвешивание крыс и регистрировали массу тела. Три раза за этот период исследовали фекалии каждой крысы на предмет любых необычных признаков. Более конкретно, фекалии взвешивали на 11, 15, 18 и 21 день. Во время наблюдения каждую крысу помещали в метаболическую клетку. Фекалии собирали каждые двадцать четыре часа. Подсчитывали количество собранных пеллет фекалий и оценивали форму и цвет пеллет. После взвешивания влажных фекалий их высушивали в печи при 100°C в течение двадцати четырех часов. Содержание воды в кале рассчитывали по следующей формуле:
Процент содержания воды = [(влажный вес - сухой вес)/влажный вес] × 100%. (I)
Полученные результаты представлены таблице 2 ниже.
Действие экстрактов Rheum palmatum Linne на выработку фекалий
После вышеуказанных исследований фекалий проводили исследование перистальтики кишечника. Перед экспериментом крысы не получали пищи по меньшей мере шестнадцать часов. Затем крысы получали вышеуказанные лекарственные средства или экстракты. Через 3 часа каждая крыса получала 3 мл/кг раствора 0,5% метилцеллюлозы - 0,5% красителя Evans blue. Каждую крысу умерщвляли через 30 минут и вскрывали брюшную полость. Весь тонкий кишечник извлекали и тщательно выпрямляли. Длину тонкой кишки измеряли как расстояние между пилорусом и слепой кишкой. Также измеряли расстояние, пройденное по кишечному тракту красителем Evans blue. Во время проведения исследования любые необычные наблюдения регистрировали и фотографировали. Функция перистальтики кишечника рассчитывали по следующей формуле:
Перистальтика кишечника = (длина, окрашенная Evans blue/длина тонкой кишки) × 100%. (II)
Полученные результаты представлены в Таблице 3 ниже.
Действие экстрактов Rheum palmatum Linne на перистальтику кишечника
Данные по перистальтике кишечника выражали как среднее значение ± SD (стандартное отклонение). Данные анализировали однофакторным ANOVA (дисперсионный анализ). Для сравнения в пределах группы использовали апостериорное сравнение. В обоих исследованиях по выработке фекалий и перистальтике кишечника, при p<0,05 были показаны значительные различия. При исследовании по выработке фекалий данные для каждой группы и в каждый момент времени представлены в виде влажного веса или количества пеллет у шести крыс в группе.
Пример 3
Исследовали слабительную активность вышеуказанных STD05 и соединений. Для этого исследования здоровых самцов крыс S.D. (BioLASCO Taiwan Co. Ltd.) делили на три группы (а именно, Группы 1-3).
В группе I, 6 крыс, как отрицательный контроль, не получали никакого лечения; 6 крыс, как положительный контроль, получали 3,35 мг/кг/день сеннозидов (Through®, Chung Mei Pharmaceutical Co., Ltd; активный ингредиент: сеннозиды 20 мг, как сеннозид A+B 12 мг, партия. 012F 006); 6 крыс получали STD05 (8 мг/кг/день); 6 крыс получали фракцию экстракта, содержащую алоэ-эмодин, реин и эмодин ("ARE", 8 мг/кг/день); 6 крыс получали алоэ-эмодин (4 мг/кг/день); и 6 крыс получали реин (4 мг/кг/день).
В группе II, 6 крыс, как отрицательный контроль, не получали никого лечения; 6 крыс, как положительный контроль, получали 3,35 мг/кг/день сеннозидов; 6 крыс получали STD05 (24 мг/кг/день); 6 крыс получали фракцию экстракта, содержащую ARE (24 мг/кг/день); 6 крыс получали хризофанол (4 мг/кг/день); и 6 крыс получали эмодин (4 мг/кг/день).
В группе III, 6 крыс, как отрицательный контроль, не получали никакого лечения; 6 крыс получали фисцион (4 мг/кг/день); и 6 крыс получали смесь хризофанола и фисциона (8 мг/кг/день, "CP").
Эксперименты выполняли в условиях контроля температуры, влажности и освещения. Каждой крысе была доступна ad libitum стандартный корм для крыс и вода, в помещении с 12-часовым циклом освещения/темноты. Для статистического сравнения крыс разделили на шесть групп в соответствии с массой.
В первой части эксперимента изучали влияние исследуемых веществ на выработку фекалий. В течение 10-дневного периода крыс взвешивали каждый день и регистрировали массу тела. В течение 10-дневного периода фекалии крыс также исследовали три раза, как описано выше, на предмет наличия каких-либо необычных наблюдений. Во время 10-дневного периода крысу, у которой наблюдали признаки гибели, подвергали эвтаназии, проводили вскрытие и исследовали на предмет болезни или повреждений. При любых осложнениях или болезни проводили анализ H&E окрашиванием для определения причины смерти и переоценки доз для будущих экспериментов. Данные, демонстрирующие влияние соединений, смесей или экстрактов на массу тела крыс, показаны в таблице 4.
Действие соединений и экстрактов из Rheum palmatum Linne
Как показано в таблице 4, STD05 и соединения эффективны для поддержания веса тела. Неожиданно было установлено, что соединения в чистом виде также эффективны.
Во время эксперимента фекалии крыс изучали в 1, 5 и 10 дни, как описано выше. Было установлено, что STD05 стимулировал выработку кала. В 10-дневный период от крыс, получающих STD05, было получено больше кала (влажный вес) по сравнению с крысами в группе контроля примерно до 32%. Кроме того, количество пеллет у крыс, получавших STD05, было больше чем у крыс контроля примерно до 20%. Кроме того, при STD05 увеличилось содержание воды в кале примерно до 18%. Те же самые эксперименты проводили на крысах, получающих фисцион, алоэ-эмодин, хризофанол, реин, эмодин, CP и ARE. Результаты показаны в таблице 5 ниже.
Как показано в таблице 5, в течение 10-дневного периода все соединения, кроме ARE, стимулировали выработку кала в следующем порядке фисцион>CP>алоэ-эмодин>хризофанол>реин>эмодин (от наиболее сильного к наименее сильному). Например, фисцион, CP, алоэ-эмодин, хризофанол, реин и эмодин усилили количество кала (влажный вес) в День 1 на 93%, 57%, 27%, 19%, 31% и 30% соответственно; в День 5 на 57%, 39%, 9%, 16%, 9% и 12% соответственно; и в День 10 на 32%, 18%, 20%, 14%, 1% и 4% соответственно. Средние значения составляют 61%, 38%, 19%, 16%, 7% и 5% соответственно.
После исследования кала проводили исследование перистальтики кишечника, как описано выше. Во время проведения исследования зарегистрировали и фотографировали любые необычные наблюдения. Для сравнения в пределах группы использовали апостериорное сравнение, при p<0,05 со значительными различиями. Было показано, что у крыс, получающих STD05 (содержащий фисцион и хризофанол) и сеннозиды, наблюдали большую перистальтику кишечника (69,3% и 67,9%), чем у крыс контроля (61,1%).
Пример 4
Для STD05 проводили тест при увеличении стимуляции электрическим током тканей подвздошной кишки морских свинок при тестовых концентрациях от 10 нм до 10 мкМ MDS Pharma Services. Исследование проводили по методике, описанной в Moritoki, et al., "Effects of methylxanthines and imidazole on the contraction of guinea pig ileum induced by transmural simulation" Eur. J. Pharmacol. 35, 185-198.
Результаты показывают, что STD05 увеличил нейрогенное сокращение мышц на 36% при концентрациях 0,03 и 0,3 мкМ и вызвал уменьшение базального сокращения мышц после введения на 24% при концентрации 10 мкМ.
Пример 5
STD05 исследовали на возможную гипохолестеринемическую активность у хомячков, получавших высокохолестериновую диету. STD05 30 и 100 мг/кг вводили перорально один раз в день каждый день в течение 14 дней. Кровь отбирали у хомячка, не получавшего еду с предыдущего вечера, в 1 день (перед введением), в 8 день (7 после введения) и в 15 день (14 после введения) для измерения в сыворотке содержания общего холестерина, липопротеинов высокой плотности, липопротеинов низкой плотности и триглицеридов. Значения после введения на 8 день и 15 день выражали как процент от соответствующих значений перед введением (день), чтобы оценить липид-понижающее действие исследуемой композиции. Уменьшение на 20% или больше общего холестерина или липопротеинов низкой плотности или увеличение на 20% или больше липопротеинов высокой плотности, а также уменьшение на 40% или больше триглицеридов по сравнению с группой носителя считали значительным. Для статистического сравнения между группой носителя и обрабатываемой группой использовали однофакторный ANOVA (дисперсионный анализ) с последующим тестом Даннета.
Результаты показывают, что STD05 в концентрации 100 мг/кг показал значительное снижение липопротеинов с низкой плотностью. Действие стало выраженным после введения в течение двух недель.
ДРУГИЕ ВАРИАНТЫ ВЫПОЛНЕНИЯ ИЗОБРЕТЕНИЯ
Все признаки, раскрытые в этом описании, могут быть объединены в любой комбинации. Каждый признак, раскрытый в этом описании, может быть заменен альтернативным признаком, служащим для той же самой, эквивалентной или подобной цели. Таким образом, если не указано иначе, каждый раскрытый признак является только примером ряда эквивалентных или подобных признаков.
Из вышеизложенного описания специалист в данной области легко может установить основные характеристики настоящего изобретения и, не отступая от сущности и объема, может выполнить различные изменения и модификации изобретения для возможности использования для различных целей и условий. Таким образом, другие варианты выполнения изобретения также включены в объем нижеследующей формулы изобретения.
Настоящее изобретение относится к фармацевтике и медицине и касается композиции для лечения воспалительного заболевания кишечника или синдрома раздраженной толстой кишки, включающей эффективное количество соединения формулы (I). Изобретение обеспечивает повышенную эффективность лечения. 11 з.п. ф-лы, 7 табл., 5 пр.

1. Композиция для лечения воспалительного заболевания кишечника или синдрома раздраженной кишки у индивидуума, включающая эффективное количество очищенного соединения формулы (I):
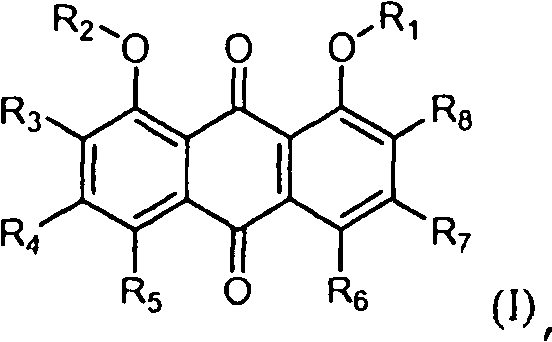
где каждый из R1-R6 и R8 независимо представляет собой Н или C1-C6 алкил; и
R7 представляет собой Н или О(C1-С10)алкил.
2. Композиция по п.1 для лечения воспалительного заболевания кишечника.
3. Композиция по п.1 для лечения синдрома раздраженной кишки.
4. Композиция по п.1, где каждый из R1, R2, R3, R5, R6 и R8 представляет собой Н.
5. Композиция по п.4, где R4 представляет собой C1-C6 алкил.
6. Композиция по п.5, где соединение представляет собой хризофанол.
7. Композиция по п.4, где R7 представляет собой O(C1-С10)алкил.
8. Композиция по п.7, где соединение представляет собой фисцион.
9. Композиция по п.1, представляющая собой фармацевтическую композицию.
10. Композиция по п.9, дополнительно включающая фармацевтически приемлемый носитель.
11. Композиция по п.10, где фармацевтически приемлемый носитель представляет собой энтеросолюбильный носитель.
12. Композиция по п.1, представляющая собой диетическую композицию.
| ФИТОЧАЙ ДЛЯ ОЧИЩЕНИЯ ОРГАНИЗМА И СНИЖЕНИЯ ВЕСА | 2001 |
|
RU2215424C2 |
| МИКСТУРА СЛАБИТЕЛЬНАЯ СУХАЯ, СЛАБИТЕЛЬНОЕ СРЕДСТВО, ПРЕПАРАТИВНАЯ ФОРМА МИКСТУРЫ СЛАБИТЕЛЬНОЙ СУХОЙ И СПОСОБ ПРИГОТОВЛЕНИЯ МИКСТУРЫ СЛАБИТЕЛЬНОЙ | 2000 |
|
RU2264223C2 |
| ПРЕПАРАТ, ОБЛАДАЮЩИЙ ИММУНОМОДУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 2002 |
|
RU2200023C1 |
| ПРЕПАРАТ, ОБЛАДАЮЩИЙ ИММУНОМОДУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 2004 |
|
RU2244555C1 |
| ЧАЙ "НЕПОЛНИТА-ФИТО" ИЗ ЛЕКАРСТВЕННЫХ РАСТЕНИЙ ДЛЯ СНИЖЕНИЯ ИЗБЫТОЧНОГО ВЕСА | 2003 |
|
RU2259839C2 |
| Топчак-трактор для канатной вспашки | 1923 |
|
SU2002A1 |
| US 6187313 B1, 13.02.2001. | |||
Авторы
Даты
2012-02-27—Публикация
2007-04-09—Подача