Предлагаемое изобретение относится к области органического синтеза, а именно к способу получения холестерил циклопропа[1,9](С60-Ih)[5,6]фуллерен-3'-карбоксилата формулы (I):
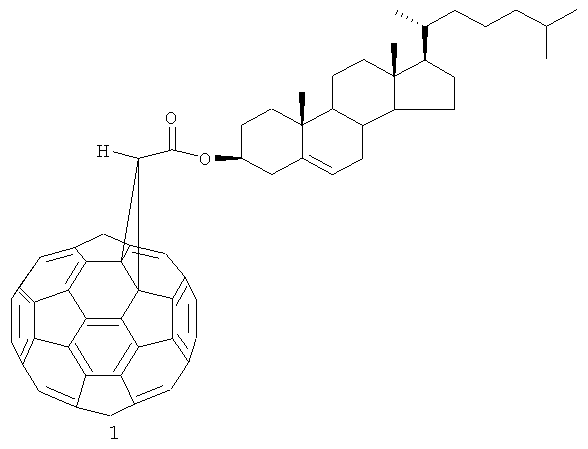
Карбоксипроизводные метанофуллеренов могут найти применение в качестве высокоактивных исходных веществ в синтезе лекарственных препаратов нового поколения для лечения опасных заболеваний человека (Л.Н.Сидоров, М.А.Юровская, А.Я.Борщевский, И.В.Трушков, И.Н.Иоффе. Фуллерены: Учебное пособие, М.: Издательство «Экзамен», 2005, 688 с. [1], Л.Б.Пиотровский, О.И.Киселев. Фуллерены в биологии, СПб.: ООО «Издательство "Росток"», 2006, 336 с. [2]).
Известен способ (F.Wudl, A.Hirsch, K.C.Khemani, T.Suzuki, P.M.Allemand, A.Koch, H.Eckert, G.Srdanov, H.M.Webb. Fullerenes: Synthesis, Properties, and Chemistry of Large Carbon Clusters, Eds. G.S.Hammond and V.J.Kuck, ACS Symposium Series 468, Washington, 1992, 161 [3]) получения производного фуллерена (4), содержащего стероидный фрагмент с выходом 12% фотохимической реакцией в бензоле С60-фуллерена (2) с соответствующим еноном (3).
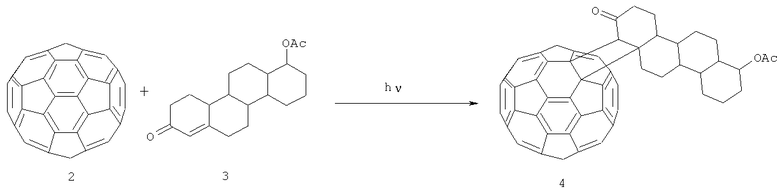
Предложенным методом невозможно получить холестерил циклопропа[1,9](С60-Ih)[5,6]фуллерен-3'-карбоксилат формулы (1).
Известен способ (Y.Nakamura, K.Inamura, R.Oomuro, R.Laurenco, T.T.Tidwell, J.Nishimura. Org. Biomol. Chem., 2005, 3, 3032 [4]) получения холестан циклопропа[1,9](С60-Ih)[5,6]фуллерен-3'-пропилкарбоксилата (8) в пять стадий реакцией С60-фуллерена (2) с тозилгидразоном (5) с последующей изомеризацией полученного гомофуллерена (6) в метанофуллерен (7) и его дальнейшей функционализацией по сложноэфирной группе.
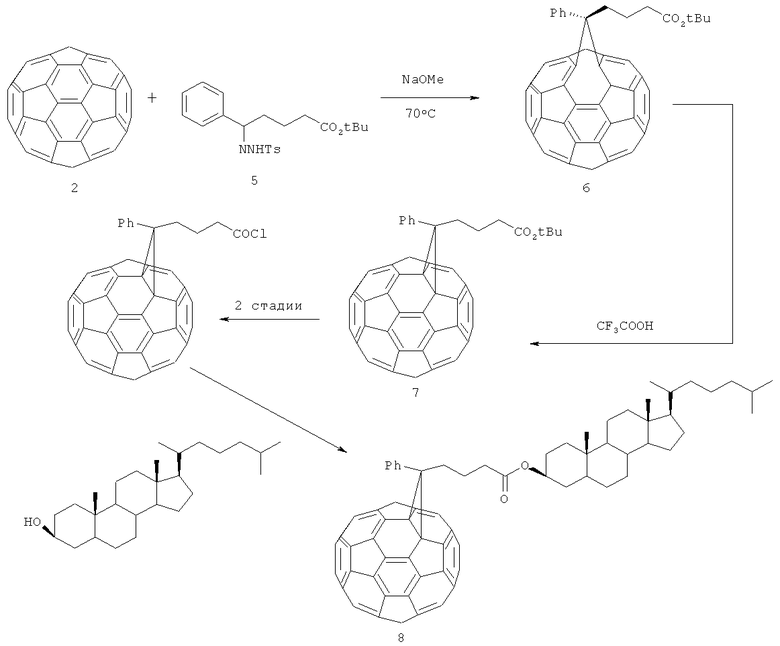
Недостатками способа являются многостадийность и низкий выход образования целевого циклоаддукта. Предложенным методом невозможно получить холестерил циклопропа[1,9](С60-Ih)[5,6]фуллерен-3'-карбоксилат формулы (1).
Предлагается новый эффективный способ получения холестерил циклопропа[1,9](С60-Ih)[5,6]фуллерен-3'-карбоксилата (1).
Сущность способа заключается во взаимодействии фуллерена (С60) (2) с холестерил диазоацетатом (9) в о-дихлорбензоле (о-ДХБ) в присутствии трехкомпонентной каталитической системы {Pd(acac)2:2PPh3:4Et3Al}, взятыми в мольном соотношении С60:диазосоединение:Pd(acac)2:PPh3:Et3Al=1:(3-7):(0.1-0.3):(0.2-0.6):(0.4-1.2), предпочтительно 1:5:0.2:0.4:0.8, при температуре 80°С в течение 0.5-1.5 ч. Получают холестерил циклопропа[1,9](С60-Ih)[5,6]фуллерен-3'-карбоксилат с выходом 44-68%. Реакция протекает по схеме:
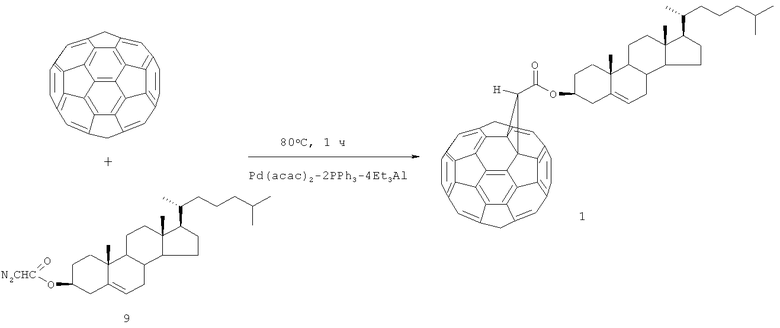
Проведение указанной реакции в присутствии палладиевого катализатора [Pd] больше 20 мол.% по отношению к фуллерену С60 не приводит к существенному увеличению выхода целевого продукта (1). Применение палладиевого катализатора [Pd] в количестве меньше 20 мол.% по отношению к фуллерену С60 снижает выход целевого продукта, что связано с уменьшением реакционных центров. Реакцию следует проводить при температуре 80°С. Проведение реакции при более высокой температуре (например, 110°С) связано с увеличением энергозатрат, при меньшей температуре (например, 40°С) снижается скорость реакции.
Существенные отличия предлагаемого способа.
Предлагаемый способ базируется на использовании палладиевого комплекса в каталитических количествах и холестерил диазоацетата в качестве исходного соединения. В известном способе применяется тозилгидразон карбоксикетона, что не позволяет в одну препаративную стадию получать целевой продукт.
Способ поясняется примерами.
К раствору 0.002 ммолей Pd(acac)2 в 0.5 мл о-ДХБ в токе сухого аргона при температуре -5°С и перемешивании добавляют 0.004 ммолей PPh3, 0.008 ммолей Et3Al и 0.01 ммолей С60-фуллерена в 1 мл о-ДХБ. Реакционную массу нагревают до 80°С и по каплям добавляют 0.05 ммолей холестерил диазоацетата в 0.5 мл о-ДХБ. Через 1 ч реакционную массу охлаждают и пропускают через колонку с небольшим слоем силикагеля. Получают холестерил циклопропа[1,9](С60-Ih)[5,6]фуллерен-3'-карбоксилат с выходом 58% (по данным ВЭЖХ).
Спектральные характеристики (1)
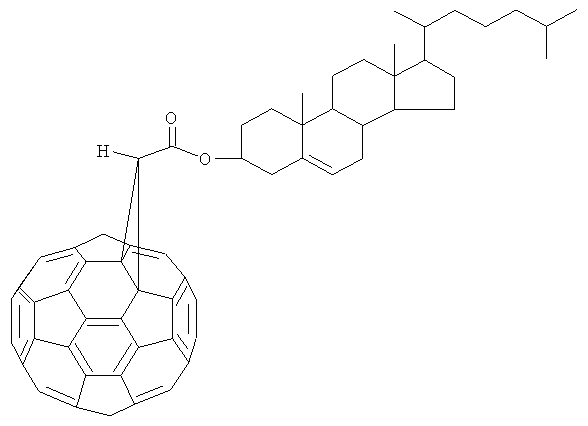
Спектр ЯМР 1H (δ, м.д., J/Гц): 0.74 (с, 3Н, Me), 0.90 (д, 3Н, Me, J=6.8), 0.91 (д, 3Н, Me, J=6.8), 0.99-2.05 (м, 27Н, 6СН, 9СН2, Me), 1.14 (с, 3Н, Me), 2.06-2.11 (м, 2Н, СН2), 2.60 (д, 2Н, СН2, J=8.0), 4.74 (с, Н, СН), 4.96 (м, 1Н, СН), 5.49 (м, 1Н, СН). Спектр ЯМР 13С (δ, м.д.): 12.17, 19.03, 19.60, 21.43, 22.87, 23.12, 24.24, 24.77, 28.42, 28.73, 30.16, 32.06, 32.39, 36.10, 36.55, 36.81, 37.36, 38.48, 39.65, 39.83, 40.11, 42.49, 50.25, 56.42, 56.95, 70.87 (sp3), 76.40, 123.66, 139.09, 140.70, 140.95, 141.24, 142.07, 142.50, 142.81, 143.03, 143.37, 143.78, 144.02, 144.65, 144.68, 145.13, 145.22, 145.29, 145.83, 148.58, 164.79. Масс-спектр (MALDI-TOF), m/z: найдено 1147.542; вычислено для С89Н46О2, 1147.316.
Другие примеры, подтверждающие способ, приведены в табл.1
Реакции проводили при температуре 80°С в о-дихлорбензоле.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ 1'-[2-(МЕТИЛСУЛЬФАНИЛ)ЭТИЛ]-1'-ЭТИЛФОРМИЛ-(C-I)[5,6]ФУЛЛЕРО[2',3':1,9]ЦИКЛОПРОПАНА И 1'a-[2-(МЕТИЛСУЛЬФАНИЛ)ЭТИЛ]-1'a-ЭТИЛФОРМИЛ-1'a-КАРБА-1'(2')a-ГОМО(C-I)[5,6]ФУЛЛЕРЕНА | 2008 |
|
RU2440337C2 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ 1'-(3-1Н-ИНДОЛМЕТИЛ)-1'-ЭТИЛФОРМИЛ-( C-I)[5,6]ФУЛЛЕРО[2',3':1,9]ЦИКЛОПРОПАНА И 1'a-(3-1Н-ИНДОЛМЕТИЛ)-1'a-ЭТИЛФОРМИЛ-1'a-КАРБА-1'(2')a-ГОМО(C-I)[5,6]ФУЛЛЕРЕНА | 2008 |
|
RU2440340C2 |
| СПОСОБ ПОЛУЧЕНИЯ 3'-МЕТИЛ-3'-ФУРИЛ- ИЛИ 3'-МЕТИЛ-3'-ТИЕНИЛ-3'Н-ЦИКЛОПРОПА[1,9](С-I)[5,6]ФУЛЛЕРЕНОВ | 2011 |
|
RU2478629C2 |
| СПОСОБ СЕЛЕКТИВНОГО ПОЛУЧЕНИЯ 1'-АЛКИЛ-1'-N-ЦИКЛОГЕКСИЛКАРБОКСААМИДИЛЦИКЛОПРОПА[2',3':1,9](C-I)[5,6]ФУЛЛЕРЕНОВ | 2013 |
|
RU2540080C2 |
| СПОСОБ ПОЛУЧЕНИЯ N-АЛКИЛ- И N-АРИЛКАРБОКСАМИДИЛ-1aH,2'H-[1,2]ПИРАЗОЛИНО[3',4':1,9](C-I)-[5,6]ФУЛЛЕРЕНОВ | 2012 |
|
RU2517170C2 |
| СПОСОБ СЕЛЕКТИВНОГО ПОЛУЧЕНИЯ 1'-[2-МЕТИЛСУЛЬФАНИЛ)-ЭТИЛ]-1'-ЭТИЛФОРМИЛЦИКЛОПРОПА[2',3':1,9](C-I)[5,6]ФУЛЛЕРЕНА | 2010 |
|
RU2447062C2 |
| СПОСОБ ПОЛУЧЕНИЯ (C-I)[5,6]ФУЛЛЕРО[2',3':1,9]ЦИКЛОПРОПАН-1'-ИЛ(ЦИКЛОАЛКИЛ)МЕТАНОНОВ | 2009 |
|
RU2434839C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1'а-МЕТИЛ-1'а-ЭТИЛФОРМИЛ-1'А-КАРБА-1'(2')а-ГОМО(C-I)[5,6]ФУЛЛЕРЕНА | 2008 |
|
RU2434843C2 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ 1'-ЭТИЛФОРМИЛ-(C-I)[5,6]ФУЛЛЕРО[2',3':1,9]ЦИКЛОПРОПАНА И 1'a-ЭТИЛФОРМИЛ-1'a-КАРБА-1'(2')a-ГОМО(C-I)[5,6]ФУЛЛЕРЕНА | 2008 |
|
RU2383527C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИКЛОАЛКИЛИДЕНГОМО(C-C)[5,6]ФУЛЛЕРЕНА | 2009 |
|
RU2417980C2 |
Изобретение относится к области органической химии и может быть использовано при получении комплексообразователей, сорбентов, биологически активных соединений, а также новых материалов с заданными свойствами. С60-фуллерен взаимодействует с холестерил диазоацетатом в о-дихлорбензоле в присутствии трехкомпонентной каталитической системы {Рd(асас)2:2РРh3:4Еt3Аl} при температуре 80°С в течение 0,5-1,5 ч. Мольное соотношение С60:Диазосоединение:Рd(асас)2:РРh3:Еt3Аl=1:(3-7):(0,1-0,3):(0,2-0,6):(0,4-1,2), предпочтительно 1:5:0,2:0,4:0,8. Получают холестерил циклопропа[1,9](С60-Ih)[5,6]фуллерен-3'-карбоксилат формулы (1) с выходом 44-68%.
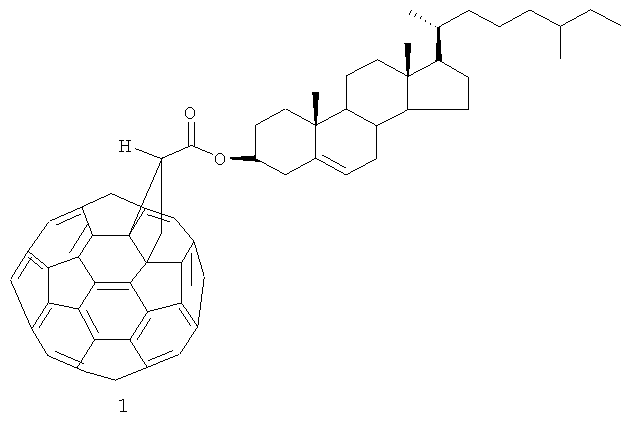 .
.
Способ получения холестерил циклопропа[1,9](С60-Ih)[5,6]фуллерен-3'-карбоксилата формулы (I)
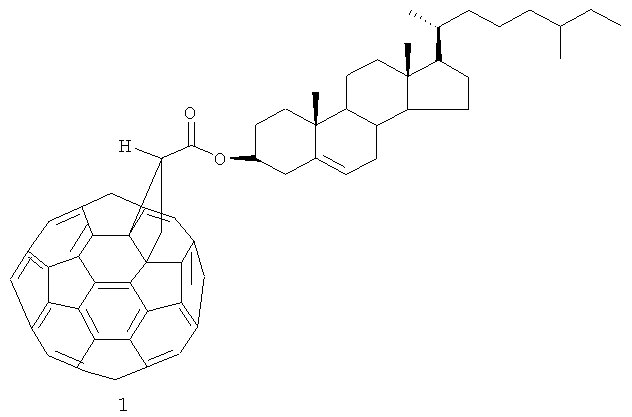
характеризующийся тем, что С60-фуллерен взаимодействует с холестерил диазоацетатом в о-дихлорбензоле в присутствии трехкомпонентной каталитической системы {Pd(асас)2:2PPh3:4Et3Al}, взятыми в мольном соотношении С60:диазосоединение:Pd(асас)2:PPh3:Et3Al=1:(3-7):(0,1-0,3):(0,2-0,6):(0,4-1,2), предпочтительно 1:5:0,2:0,4:0,8, при температуре 80°С в течение 0,5-1,5 ч.
| YOSUKE NAKAMURA et al | |||
| Способ получения молочной кислоты | 1922 |
|
SU60A1 |
| Biomol | |||
| Chem., 2003, v.3, p.p.3032-3038 | |||
| RU 2008144404 A, 20.05.2010 | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
| MOROZOV V.I | |||
| et al, The magnetic exchange in the neutral and anionic | |||
Авторы
Даты
2012-04-10—Публикация
2010-06-02—Подача