Изобретение относится к области медицины и биотехнологии, а именно к способам терапевтического ангиогенеза, направленным на усиление роста новых сосудов в ишемизированных тканях с целью лечения таких заболеваний, как критическая ишемия нижних конечностей (КИНК) и ишемическая болезнь сердца (ИБС), а также препаратам для его осуществления.
ИБС и КИНК, наряду с ишемическими нарушениями мозгового кровообращения, в настоящее время относят к основным причинам инвалидизации населения. В России ИБС страдает около 10 миллионов человек трудоспособного возраста, и более чем у трети из них имеется стабильная стенокардия. В 2000 г. заболеваемость ИБС в России составила 425,5 случая на 100 тыс. населения (В.И.Маколкин, Ф.Н.Зябрев. Почему надо снижать частоту сердечных сокращений при лечении стабильной стенокардии. Кардиология 2006. Т.46. С.88-91); при этом на долю ИБС в РФ приходится 48% всех сердечно-сосудистых заболеваний. По данным иностранных авторов на долю больных с рефракторной стенокардией приходится около 15% от всех больных ИБС.
Согласно материалам Европейской согласительной комиссии (European working group on chronic critical leg ischemia "Second European Consensus Document on chronic critical leg ischemia." Eur. J. Vasc. Surg. 1992. V.6 (Suppl. A). P.1-32) из миллиона больных сахарным диабетом КИНК ежегодно диагностируется у 500-1000 пациентов. По статистическим данным окклюзионно-стенотические поражения артерий нижних конечностей возникают у 18-22,5% пациентов с сахарным диабетом, причем данное заболевание характеризуется быстрым прогрессированием и ранним развитием ишемических и гнойно-некротических осложнений. В целом же около 90% ампутаций проводится именно по поводу ишемии нижних конечностей.
Лечение КИНК включает целый ряд мер медикаментозного характера, изменение образа жизни, коррекцию сопутствующей патологии, однако наиболее выраженный эффект часто дают хирургические методы восстановления нарушенного кровотока - шунтирование, ангиопластика, атерэктомия и т.д. При этом всегда существует определенная когорта больных с множественными критическими стенозами сосудов нижних конечностей, для которых описанные выше лечебные мероприятия являются неэффективными. То же относится и к лицам, которым уже было выполнено хирургическое вмешательство, в результате чего все последующие операции по восстановлению перфузии становятся крайне затруднительными или невозможными. В связи со сказанным возникает необходимость разработки альтернативных методов лечения КИНК, одним из которых является терапевтический ангиогенез - направление регенеративной медицины, активно развивающееся в последнее время.
Ангиогенез является естественной реакцией организма на ишемию, призванной восстановить кровоснабжение ткани за счет образования новых сосудов. При этом в очаге ишемии активируется синтез ангиогенных факторов роста (АФР), а эндотелиальные клетки-предшественники мобилизуются из костного мозга и мигрируют в очаги неоваскуляризации. Стимуляция ангиогенеза с помощью генной терапии получает все большее распространение как потенциальный метод лечения КИНК и других ишемических заболеваний. Для индукции ангиогенеза в ишемизированной скелетной мускулатуре было предложено использовать плазмидные конструкции, несущие кДНК генов b-FGF, VEGF165, HGF и других факторов роста. Безопасность таких конструкций была показана во многих исследованиях. Однако эффективность известных методов терапевтического ангиогенеза оказалась не слишком высокой (Yla-Herttuala S., Rissanen T.T., Vajanto I. Vascular endothelial growth factors: biology and current status of clinical application in cardiovascular medicine. JMCC 2007. V.49. P.1015-26; Rissanen T.T., Yla-Herttuala S. Current status of cardiovascular gene therapy. Mol. Ther. 2007. V.15. P.1233-47).
Это во многом обусловлено тем, что ангиогенез - это многоэтапный процесс, и каждый этап находится под контролем различных цитокинов и факторов роста, поэтому применение только одного ангиогенного фактора (как в виде рекомбинантого белка, так и виде генетической конструкции) не позволяет добиться значительных результатов.
Известно использование в терапевтическом ангиогенезе комплексного введения нескольких плазмид, кодирующих разные АФР, в комбинации друг с другом.
Так, известно использование в экспериментальных исследованиях на животных сочетания гена фактора роста эндотелия сосудов человека (VEGF) с генами эндотелиальной NO-синтазы или простациклин-синтазы либо в комбинации с геном фермента, подавляющим активность эндогенного ингибитора эндотелиальной NO-синтазы (Hiraoka K., Koike H., Yamamoto S. et al. Enhanced therapeutic angiogenesis by cotransfection of prostacyclin syntase gene or optimization of intramuscular injection of naked plasmid DNA. Circulation 2003. V.108. P.2689-96; Jacobi J., Sydow K., von Degenfeld G. et al. Overex-pression of dimethylarginine dimethylaminohydrolase reduces tissue asymmetric dimethylarginine levels and enhances angiogenesis. Circulation 2005. V.111. P.1431-8).
Наиболее близким по технической сущности к заявляемому способу является применение в терапевтическом ангиогенезе гена VEGF в комбинации с геном фактора стабилизации сосудов ангиопоэтина-1 (Shyu K.-G., Chang H., Isner J.M. Synergistic effect of angiopoietin-1 and vascular endothelial growth factor on neoangiogenesis in hypercholesterolemic rabbit model with acute hind limb ischemia. Life Sciences 2003. V.73. P.563-79). При этом образовывалась сосудистая сеть, остававшаяся стабильной даже через год после отмены этих факторов.
Вместе с тем сочетание VEGF с другими АФР, такими как FGF-2 или PDGF-BB, оказалось неэффективным, что свидетельствовало о том, что простое механическое смешение генов различных АФР не позволяет добиться надежных результатов (Cao R., Brakenhielm Е., Pawliuk R. et al. Angiogenic synergism, vascular stability and improvement of hind-limb ischemia by a combination of PDGF-BB and FGF. Nat. Med. 2003. V.9. P.604-13).
Задачей, решаемой авторами настоящего изобретения, являлась разработка более эффективного средства за счет создания комбинации плазмидных конструкций, несущих гены АФР, и способа лечения, которые обеспечивали бы наиболее эффективный ангиогенез в ишемизированной ткани.
Технический результат был достигнут при использовании средства, содержащего смесь плазмидных конструкций pC4W-hVEGFopt с оптимизированным геном hVEGFopt фактора роста эндотелия сосудов человека (VEGF) и pC4W-hHGFopt с оптимизированным геном hHGFopt фактора роста гепатоцитов человека (HGF) в массовом соотношении от 1:3 до 3:1. Лучшие результаты достигались при их массовом соотношении 1:1.
Способ терапевтического ангиогенеза заключался во введении внутримышечно физиологического раствора, содержащего смесь плазмидных конструкций pC4W-hVEGFopt и pC4W-hHGFopt в концентрации суммарно 2 мг/мл.
Все плазмидные конструкции получали на основе экспрессионного плазмидного вектора pC4W для синтеза белков в клетках млекопитающих, являющегося предметом ранее выданного патента РФ 2364627. В качестве генов, кодирующих VEGF и HGF, использовали оптимизированные нуклеотидные последовательности, являющиеся предметом ранее поданных заявок RU 2008125416 и RU 2008125409 на патенты РФ «Ген HGFopt фактора роста гепатоцитов» и «Ген VEGFopt фактора роста эндотелия сосудов человека», по которым приняты решения о выдаче патентов.
Комплексное средство получали смешением концентратов ингредиентов в заданных соотношениях и разведением в растворе стерильного 0,9%-ного NaCl до нужной концентрации.
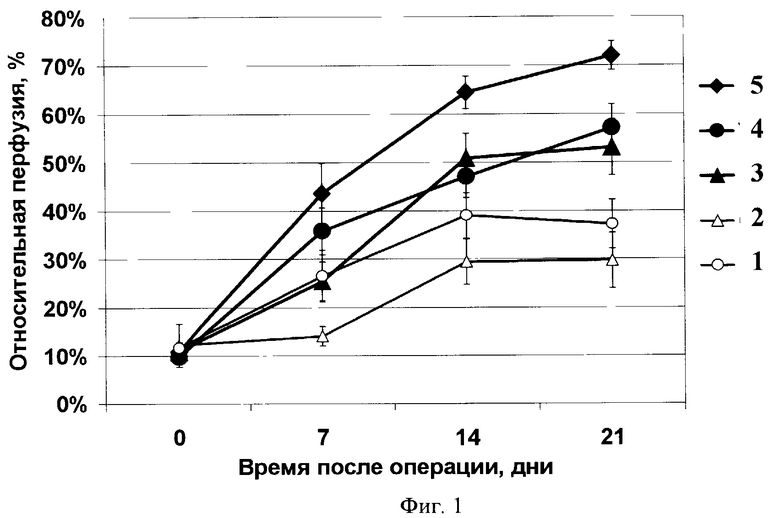
На фиг.1 показаны кривые зависимости относительной перфузии ишемизированной конечности мыши от времени, прошедшего после операции, в случае введения: 1) контрольной плазмидной конструкции pC4W-β-GAL, кодирующей β-галактозидазу; 2) контрольного раствора 0,9% NaCl; 3) отдельной плазмидной конструкции pC4W-hHGFopt, кодирующей HGF; 4) отдельной плазмидной конструкции pC4W-hVEGFopt, кодирующей VEGF; и 5) смеси плазмидных конструкций pC4W-hVEGFopt и pC4W-hHGFopt в соотношении 1:1.
Методология проведения экспериментов и полученные результаты иллюстрируются следующими примерами.
Пример 1. Испытания заявляемого препарата проводили в ходе исследований на мышах с ишемизированной задней конечностью. Ишемизацию тканей нижней конечности мыши проводили по модифицированной методике Takeshita с соавторами (Takeshita S. Isshiki Т., Ochiai M., Eto K., Mori H., Tanaka E., Umetani K., Sato Т. Endothelium-dependent relaxation of collateral microvessels after intramuscular gene transfer of vascular endothelial growth factor in a rat model of hindlimb ischemia. Circulation 1998. V.98. P.1261-3). В исследованиях использовали самцов мышей линии С57Вl весом 30 граммов. Операцию проводили в асептических условиях под анестезией (2,5%-ный авертин, интраперитонеально). Производили продольный разрез кожи левого бедра мыши от области паховой связки до коленной области. Бедренную артерию выделяли целиком от начала бифуркации брюшной аорты до разделения на a. poplitae и a. saphenous и ее ветви, включая a. epigastrica inferior, a. femoralis profunda, a. circumflexus lateralis, перевязывали и отсекали. После контроля гемостаза разрез зашивали шелковой нитью с атравматической иглой.
Растворы плазмид в стерильном 0,9%-ном NaCl вводили в объеме 100 мкл в переднюю большеберцовую мышцу (m. tibialis anterior) с помощью инсулинового шприца однократной многоточечной (4 точки на мышь) болюсной инъекцией. Суммарная концентрация вводимой плазмидной ДНК составляла 1 мг/мл, если вводили только одну плазмиду, и 2 мг/мл при введении смеси двух плазмид. Для предотвращения вытекания раствора введение проводили медленно в течение 3 секунд под наблюдением.
Для повышения эффективности трансфекции проводили чрескожную низковольтовую электропорацию с пластинчатыми электродами, для чего использовали генератор импульсов "Harvard apparatus BCM830" и прилагаемые к нему электроды. На кожу заранее обработанной и выбритой области голени мыши накладывались электроды, смазанные электропроводящим гелем «Униагель» таким образом, чтобы мышца с введенной плазмидой оказалась зажатой пластинками электродов. Затем подавали 3 импульса длительностью 20 мс, с частотой 1 Гц и напряжением 32-35 В (80 В на 1 см расстояния между пластинками электрода). Затем полярность электродов меняли и подавали еще 3 импульса с такими же характеристиками.
Пример 2. Анализ восстановления кровотока в ишемизированной конечности мыши.
Эффекты плазмид, несущих гены разных АФР, на стимуляцию ангиогенеза по примеру 1 оценивали по восстановлению кровотока в подошвенной области лапы мышей. Для оценки кровотока по методике Т. Couffinhal использовали лазерный доплеровский флоуметр (Laser Doppler Imaging System, Moor, Великобритания). В данном приборе используется инфракрасный лазер 2,5 мВт, генерирующий луч света, способный проникать на глубину до 1 мм. Метод измерения кровотока основан на том, что клетки крови, проходящие по сосуду, вызывают сдвиг частоты испускаемого света, который и фиксируется прибором.
Кровоток измеряли непосредственно до и после операции, а также на 7-й, 14-й и 21-й дни. Анестезию проводили газовой смесью 1,5%-ного изофлюрана/O2 и поддерживали на этой анестезии в течение всего процесса измерения. Во избежание влияния перепадов температуры животных помещали на матрас с поверхностной температурой 37°С и до начала сканирования выдерживали минимум 10 мин при этих условиях. Обрабатывали только данные, отвечающие следующему критерию: «разница в результатах трех последовательных измерений, проведенных с интервалом в 2 мин, не превышает 5%». Для снижения возможного разброса результатов измерений при переходе от одного животного к другому, а также для исключения влияния внешних факторов (свет, глубина наркоза и т.д.) кровоток в ишемизированной конечности выражали в процентном отношении к кровотоку в интактной конечности. В течение периода наблюдения животные получали стандартные лабораторные корма с достаточным количеством питьевой воды.
Полученные результаты приведены на фиг.1. Все результаты представлены в виде числа наблюдений или выборочного среднего ±СОС (стандартная ошибка среднего). Статистическую значимость различий оценивали с помощью критерия χ2 для частотных показателей или Т-критерия Стьюдента после соответствующей проверки на нормальность распределения. Статистически значимыми считались различия, значение р для которых было <0,05.
Из приведенных экспериментальных данных следует, что ангиогенная активность смеси плазмидных конструкций pC4W-hVEGFopt и pC4W-hHGFopt статистически значимо превосходит ангиогенную активность как отдельной плазмидной конструкции pC4W-hHGFopt (на 7-й, 14-й и 21-й дни, р<0,05), так и отдельной плазмидной конструкции pC4W-hVEGFopt (на 14-й и 21-й дни, р<0,05).
Статистически значимое превосходство смеси pC4W-hVEGFopt и pC4W-hHGFopt по сравнению с контрольным раствором 0,9%-ного NaCl показано на 7-й, 14-й и 21-й дни (р<0,001), а по сравнению с контрольной плазмидной конструкцией pC4W-β-GAL - на 14-й и 21-й дни (р<0,01).
| название | год | авторы | номер документа |
|---|---|---|---|
| ГЕННО-ИНЖЕНЕРНАЯ КОНСТРУКЦИЯ ДЛЯ СТИМУЛЯЦИИ АНГИОГЕНЕЗА | 2019 |
|
RU2737487C1 |
| СПОСОБ СТИМУЛЯЦИИ АНГИОГЕНЕЗА В ИШЕМИНИЗИРОВАННЫХ ТКАНЯХ И КОМБИНИРОВАННОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ОСУЩЕСТВЛЕНИЯ СПОСОБА | 2015 |
|
RU2628706C2 |
| ГЕННОТЕРАПЕВТИЧЕСКИЙ СПОСОБ ЛЕЧЕНИЯ СИНДРОМА ДИАБЕТИЧЕСКОЙ СТОПЫ | 2015 |
|
RU2599507C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ИШЕМИЧЕСКИХ ПОРАЖЕНИЙ ТКАНЕЙ И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2012 |
|
RU2522778C2 |
| Оптимизированная нуклеотидная последовательность и фармацевтическая композиция на ее основе с пролонгированной экспрессией трансгена vegf | 2015 |
|
RU2612497C2 |
| Способ стимулирования ангиогенеза, лечения нейродегенеративных заболеваний и регенерации скелетной мышцы с помощью плазмидных конструкций с генами ангиогенных и нейротрофических факторов | 2020 |
|
RU2805082C2 |
| СПОСОБ ОЦЕНКИ АНГИОГЕННОГО ПОТЕНЦИАЛА ПРОГЕНИТОРНЫХ КЛЕТОК У БОЛЬНЫХ СЕРДЕЧНО-СОСУДИСТЫМИ ЗАБОЛЕВАНИЯМИ | 2011 |
|
RU2548801C2 |
| СПОСОБ СТИМУЛЯЦИИ РЕГЕНЕРАТИВНЫХ ПРОЦЕССОВ В ИШЕМИЗИРОВАННЫХ ТКАНЯХ | 2011 |
|
RU2497529C2 |
| КОДОН-ОПТИМИЗИРОВАННЫЕ ПОСЛЕДОВАТЕЛЬНОСТИ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ВОССТАНОВЛЕНИЯ КРОВЕНОСНЫХ СОСУДОВ | 2014 |
|
RU2557385C1 |
| Способ комбинированной хирургической стимуляции неоангиогенеза хронической ишемии нижних конечностей | 2018 |
|
RU2703395C1 |
Группа изобретений относится к области медицины и биотехнологии и может быть использована для усиления роста новых сосудов в ишемизированных тканях. Средство по изобретению содержит плазмидную конструкцию pC4W-hVEGFopt, несущую оптимизированный ген hVEGFopt фактора роста эндотелия сосудов, и дополнительно плазмидную конструкцию pC4W-hHGFopt, несущую оптимизированный ген hHGFopt фактора роста гепатоцитов. Способ по изобретению заключается во внутримышечном введении в ишемизованную конечность смеси плазмидных конструкций pC4W-hVEGFopt и pC4W-hHGFopt в растворе 0,9%-ного NaCl. Использование изобретений позволяет достичь эффективного ангиогенеза в ишемизированной ткани. 2 н. и 3 з.п. ф-лы, 1 ил., 2 пр.
1. Средство для осуществления терапевтического ангиогенеза на основе плазмидных конструкций, несущих гены ангиогенных факторов роста, отличающееся тем, что оно содержит плазмидную конструкцию, pC4W-hVEGFopt, несущую оптимизированный ген hVEGFopt фактора роста эндотелия сосудов, и дополнительно плазмидную конструкцию pC4W-hHGFopt, несущую оптимизированный ген hHGFopt фактора роста гепатоцитов.
2. Средство по п.1, отличающееся тем, что оно содержит комбинацию плазмидных конструкций, несущих гены hVEGFopt и hHGFopt, в массовом соотношении от 1:3 до 3:1.
3. Средство по п.2, отличающееся тем, что оно содержит комбинацию плазмидных конструкций, несущих гены hVEGFopt и hHGFopt, в массовом соотношении 1:1.
4. Способ терапевтического ангиогенеза, заключающийся во внутримышечном введении в ишемизованную конечность смеси плазмидных конструкций, кодирующих, соответственно, hVEGFopt и hHGFopt, в растворе 0,9%-ного NaCl, отличающийся тем, что в качестве плазмидных конструкций используют конструкции pC4W-hVEGFopt и pC4W-hHGFopt.
5. Способ по п.4, отличающийся тем, что смесь плазмидных конструкций вводят в суммарной концентрации 2 мг/мл.
| ГИБРИДНЫЕ МАТРИЧНЫЕ ИМПЛАНТАТЫ И ЭКСПЛАНТАТЫ | 1996 |
|
RU2201765C2 |
| ГЕННО-ИНЖЕНЕРНАЯ КОНСТРУКЦИЯ VEGF-ИБМЕД (VEGF-IBMED) | 2005 |
|
RU2297848C2 |
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
| Способ изготовления фанеры-переклейки | 1921 |
|
SU1993A1 |
| DIAO Y et al | |||
| Construction and activity of recombinant adeno-associated virus expressing vasostatin // Sheng Wu Gong Cheng Xue Bao | |||
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
Авторы
Даты
2012-05-10—Публикация
2009-10-30—Подача