Настоящее изобретение относится к новым гибридным антибиотикам, которые получают из производных оксазолидинона, связанных с хинолоном или нафтиридиноном через спейсер, фармацевтическим антибактериальным композициям, содержащим их, и применению этих соединений для получения лекарственного средства для лечения инфекций (например, бактериальных инфекций). Эти гибридные соединения, применяемые в качестве антимикробных агентов, эффективны против различных болезнетворных организмов у человека и животных, включая, среди прочих, грамположительные аэробные бактерии, грамотрицательные бактерии, анаэробные организмы и кислотоустойчивые организмы.
Интенсивное применение антибиотиков оказывает селективное развивающее давление на микроорганизмы, способствуя продуцированию генетически сформированных механизмов резистентности. Современное медицинское и социоэкономическое поведение обостряет проблему развития резистентности, создавая условия замедленного роста патогенных микроорганизмов, например, в искусственных суставах и в условиях долговременной поддержки резервов хозяина, например, у иммунологически «скомпрометированных» пациентов.
В больничных условиях увеличение целого ряда штаммов Staphylococcus aureus, Streptococcus pneumonia, Enterococcus spp. и Pseudomonas aeruginosa, главных источников инфекций, делает их резистентными и вызывает трудности, вплоть до невозможности лечения вообще:
- S.aureus является резистентным к β-лактаму, хинолону и теперь даже к ванкомицину;
- S.pneumoniae является резистентным к пенициллину, хинолону и даже к новым макролидам;
- Enteroccocci являются резистентными к хинолону и ванкомицину, а β-лактамы не оказывают никакого эффективного действия на эти штаммы.
К тому же, новые недавно появившиеся организмы типа Acinetobacter spp. или С.difficile, которые отбирают при проведении терапии с использованием современных антибиотиков, становятся реальной проблемой в госпитальной терапии.
Кроме того, микроорганизмы, которые вызывают персистентные инфекции, все более и более признаются в качестве агентов, являющихся причиной или кофакторами различных хронических болезней, подобных пептической язве или болезням сердца.
В гибридных молекулах две или более молекулы, которые существуют раздельно в их естественном состоянии, объединяют вместе для образования единого объекта (то есть молекулы), имеющего требуемую функциональность всех составляющих его молекул.
Молекулы, в которых связаны два антибиотика, обладающие двумя различными моделями действия, представлены в литературе (например, Journal of Antimicrobial Chemotherapy, (1994), 33, 197-200). Многие из них, однако, являются такими, где две части антибиотиков действуют после биологической активации (например, отщепления сложно-эфирной группировки, расщепления β-лактама). Сведения о химической и биохимической стабильности гибридных молекул, которые связаны с двумя различными мишенями, реже встречаются в литературе. Например, гибриды оксазолидинон-хинолон описаны в качестве антимикробных агентов, эффективных против устойчивых болезнетворных организмов, в публикациях: WO 03/032962, WO 03/031443 и WO 2004/096221, WO 2005/023801 и WO 2005/058888). Кроме того, синтетическая и биологическая оценка этих гибридов (Bioorg. & Med. Chem., (2003), 11, 2313-2319) и влияние центрального спейсера на антибактериальную активность во взамоотношении структура-активность в серии оксазолидинон-хинолон также исследована (Bioorg. Med. Chem. Lett. (2003), 13, 4229-4233). Все эти производные содержат 4-аминометилоксазолидиноновый остаток как часть оксазолидинонового фармакофора.
Недавно неожиданно было установлено, что гибридные производные формулы I по определению, приведенному далее, являются особенно эффективными в качестве антимикробных агентов против ряда бактерий с мультилекарственной резистенцией.
Так, настоящее изобретение относится к соединениям формулы I
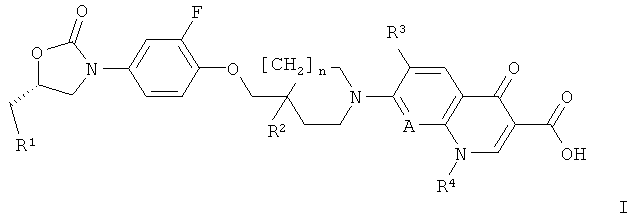
где R1 представляет собой ОН, ОРО3Н2 или OCOR5;
R2 представляет собой Н, ОН или ОРО3Н2;
А представляет собой N или CR6;
R3 представляет собой Н или фтор;
R4 представляет собой Н, C1-3алкил или циклоалкил;
R5 представляет собой остаток природной аминокислоты, энантиомера природной аминокислоты или диметиламиноглицина;
R6 представляет собой Н, алкоксигруппу или галоген; и
n=0 или 1;
и к солям (в частности, фармацевтически приемлемым солям) соединений формулы I.
Соединения формулы (I) могут содержать один или более стерео- или асимметрических центров, таких как один или более асимметрических атомов углерода. Соединения формулы (I) могут, таким образом, присутствовать в виде смеси стереоизомеров или, предпочтительно, в виде чистых стереоизомеров. Смеси стереоизомеров могут быть разделены с использованием методов, известных специалистам в области техники.
В следующих параграфах представлены определения различных химических фрагментов для соединений согласно изобретению. Названные определения предназначены для единообразного применения во всем описании и в формуле изобретения, если не указано иначе и если определения не подлежат более широкому или, наоборот, более узкому толкованию.
Если не указано иначе, термин "алкил", используемый самостоятельно или в комбинации, относится к насыщенной линейной или разветвленной алкильной группе, содержащей от 1 до 6 атомов углерода, и предпочтительно, от 1 до 3 атомов углерода. Типичные примеры алкильных группп включают, но не лимитируют, метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, н-пентил, неопентил, изопентил, н-гексил и изогексил. Термин "C1-халкил" (х обозначает целое число) относится к насыщенной линейной или разветвленной алкильной группе, содержащей от 1 до х атомов углерода.
Термин "алкоксигруппа" относится к насыщенной линейной или разветвленной алкоксигруппе, содержащей от 1 до 6 атомов углерода, предпочтительно от 1 до 3 атомов углерода. Типичные примеры алкоксигрупп включают, но не лимитируют, метоксигруппу, этоксигруппу, пропоксигруппу, изопропоксигруппу, н-бутоксигруппу, изобутоксигруппу, втор-бутоксигруппу, трет-бутоксигруппу или н-гексилоксигруппу. Термин "C1-халкоксигруппа" (х обозначает целое число) относится к линейной или разветвленной алкоксигруппе, содержащей от 1 до х атомов углерода.
Термин "галоген" относится к фтору, хлору, брому или йоду, предпочтительно к фтору или хлору.
Термин "циклоалкил", используемый самостоятельно или в комбинации, относится к насыщенному циклическому фрагменту, содержащему от 3 до 6 атомов углерода, предпочтительно от 3 до 5 атомов углерода. Типичные примеры циклоалкильных групп включают, не лимитируя, циклопропил и циклопентил.
Когда указано, что R5 представляет собой остаток аминокислоты, это означает, что R5-COOH представляет собой аминокислоту.
Термин "фармацевтически приемлемые соли" относится к нетоксичным, неорганическим или органическим кислотно- и/или основно-аддитивным солям. Сведения о таких солях могут быть найдны в публикации: "Salt selection for basic drugs". Int. J. Pharm. (1986), 33, 201-217.
Когда речь идет не о температурах, термин "приблизительно", расположенный перед численной величиной "X" относится в обычном применении к интервалу, составляющему от Х минус 10% Х к Х плюс 10% X, и предпочтительно, к интервалу, составляющему от Х минус 5% Х к Х плюс 5% X. В особом случае, касающемся температур, термин "приблизительно" (или, альтернативно, термин "около"), расположенный перед температурой "Y", относится в обычном применении к температурному интервалу, составляющему от Y минус 10°С до Y плюс 10°С, и предпочтительно, к интервалу, составляющему от Y минус 5°С до Y плюс 5°С; кроме того, комнатная температура в данном описании подразумевает температуру около 25°С.
В частности, изобретение относится к соединениям формулы I, которые также являются соединениями формулы ICE

где R1 представляет собой ОН, ОРО3Н2 или OCOR5;
R2 представляет собой Н, ОН или ОРО3Н2;
А представляет собой N или CR6;
R3 представляет собой фтор;
R4 представляет собой Н, C1-3алкил или циклоалкил;
R5 представляет собой остаток природной аминокислоты (в частности, остаток аланина);
R6 представляет собой Н или алкоксигруппу; и
n=0 или 1;
и к солям (в частности, фармацевтически приемлемым солям) соединений формулы ICE.
Согласно первому основному варианту осуществления настоящего изобретения, соединения формулы I являются соединениями, где n=0. Такие соединения отнесены далее к "соединениям формулы I5".
Согласно одному особому варианту первого основного варианта изобретения, соединения формулы I5 являются такими соединениями, которые имеют следующую стереохимическую формулу:
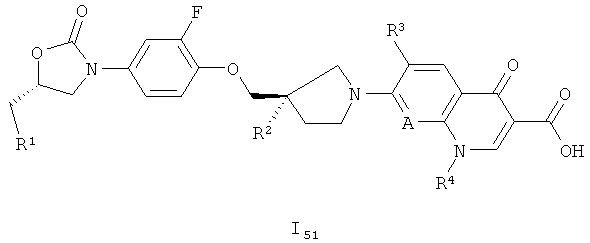
Согласно другому варианту первого основного варианта осуществления изобретения, соединения формулы I5 являются такими соединениями, которые имеют следующую стереохимическую формулу:
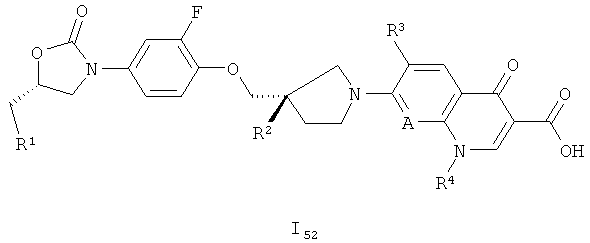
Согласно второму варианту основного варианта осуществления изобретения, соединения формулы I являются такими соединениями, где n=1. Такие соединения отнесены далее к "соединениям формулы I6".
Согласно следующему основному варианту осуществления настоящего изобретения, соединениями формулы I являются такие соединения, которые также являются соединениями формулы ID
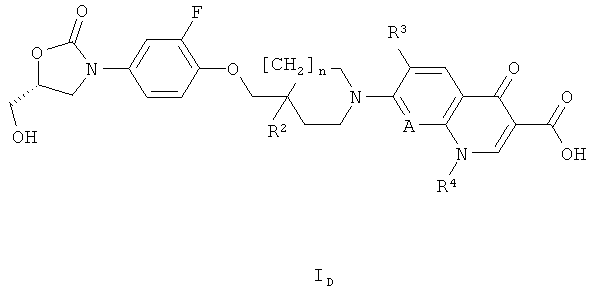
где R2 представляет собой Н или ОН;
А представляет собой N или CR6;
R3 представляет собой фтор;
R4 представляет собой Н, C1-3алкил или циклоалкил;
R6 представляет собой Н или алкоксигруппу; и
n=0 или 1.
Согласно еще одному другому основному варианту осуществления настоящего изобретения, соединениями формулы I являются такие соединения, которые также являются соединениями формулы IPDG
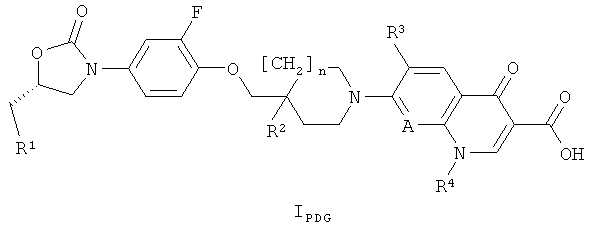
где R1 представляет собой ОН и R2 представляет собой ОРО3Н2, или R1 представляет собой ОРО3Н2 или OCOR5 и R2 представляет собой Н, ОН или ОРО3Н2;
А представляет собой N или CR6;
R3 представляет собой фтор;
R4 представляет собой Н, C1-3алкил или циклоалкил;
R5 представляет собой остаток природной аминокислоты (в частности, остаток аланина);
R6 представляет собой Н или алкоксигруппу; и
n=0 или 1.
Согласно особому варианту осуществления настоящего изобретения, соединениями формулы I являются такие соединения, где А представляет собой N.
Согласно другому особому варианту осуществления настоящего изобретения, соединениями формулы I являются такие соединения, где А представляет собой CR6. В таком случае R6 предпочтительно представляет собой Н или алкоксигруппу (и, в частности, Н или метоксигруппу).
Согласно важному варианту осуществления настоящего изобретения, соединениями формулы I являются такие соединения, где R1 обозначает ОН.
Согласно другому важному варианту осуществления настоящего изобретения, соединениями формулы I являются такие соединения, где R1 обозначает ОРО3Н2 или OCOR5.
Согласно еще одному другому важному варианту осуществления настоящего изобретения, соединениями формулы I являются такие соединения, где R2 обозначает Н.
Согласно еще одному другому важному варианту осуществления настоящего изобретения, соединениями формулы I являются такие соединения, где R2 обозначает ОН.
Согласно следующему важному варианту осуществления настоящего изобретения, соединениями формулы I являются такие соединения, где R2 обозначает ОРО3Н2.
Предпочтительно, аминокислотный остаток R5 является таким, что R5-СООН представляет собой натуральную аминокислоту (предпочтительно, аланин).
Предпочтительными соединениями формулы I являются такие соединения, в которых присутствует, по крайней мере, одна из следующих характеристик:
- А представляет собой CR6;
- R1 представляет собой ОН или ОРО3Н2;
- R2 представляет собой Н или ОН;
- R3 представляет собой фтор;
- R4 представляет собой C1-3алкил или циклоалкил.
Более предпочтительными соединениями формулы I являются такие соединения, в которых присутствует, по крайней мере, одна из следующих характеристик:
- n=0;
- А представляет собой CR6, R6 при этом представляет собой Н или алкоксигруппу (и предпочтительно, Н или метоксигруппу);
- R1 представляет собой ОН;
- R2 представляет собой Н или ОН;
- R3 представляет собой фтор;
- R4 представляет собой циклоалкил.
Еще более предпочтительными соединениями формулы I являются такие соединения, в которых присутствует, по крайней мере, одна из следующих характеристик:
- n=0;
- А представляет собой CR6, R6 при этом представляет собой Н или метоксигруппу;
- R1 представляет собой ОН;
- R2 представляет собой Н или ОН (и предпочтительно, ОН);
- R3 представляет собой фтор;
- R4 представляет собой С3-5циклоалкил (и в частности, циклопропил).
Следующие соединения формулы I являются особенно предпочтительными:
1-циклопропил-6-фтор-7-{4-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-4-гидроксипиперидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-7-{4-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]пиперидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-7-{4-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-4-гидроксипиперидин-1-ил}-4-оксо-1,4-дигидро-[1,8]нафтиридин-3-карбоновая кислота;
7-(4-{4-[(R)-5-((S)-2-аминопропионилоксиметил)-2-оксооксазолидин-3-ил]-2-фторфеноксиметил}-4-гидроксипиперидин-1-ил)-1-циклопропил-6-фтор-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-7-{4-[2-фтор-4-((R)-2-оксо-5-фосфоноксиметилоксазолидин-3-ил)феноксиметил]-4-гидроксипиперидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-7-{(R)-3-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-3-гидроксипирролидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-7-{(S)-3-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-3-гидроксипирролидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-7-{(R)-3-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-3-гидроксипирролидин-1-ил}-8-метокси-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-7-{(S)-3-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-3-гидроксипирролидин-1-ил}-8-метокси-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-7-{(R)-3-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]пирролидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-7-{(S)-3-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]пирролидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-7-{(R)-3-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]пирролидин-1-ил}-8-метокси-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-7-{(S)-3-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]пирролидин-1-ил}-8-метокси-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-7-{4-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-4-фосфонооксипиперидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
1-этил-6-фтор-7-{4-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]пиперидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
7-(4-{4-[(R)-5-((S)-2-аминопропионилоксиметил)-2-оксооксазолидин-3-ил]-2-фторфеноксиметил}пиперидин-1-ил)-1-циклопропил-6-фтор-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
6-фтор-7-{4-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-4-гидроксипиперидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
6-фтор-7-{4-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-4-гидроксипиперидин-1-ил}-4-оксо-1,4-дигидро-[1,8]нафтиридин-3-карбоновая кислота;
а также их соли (и в частности, их фармацевтически приемлемые соли).
Гибридные производные формулы I пригодны для применения в качестве лекарственных средств, особенно в качестве антимикробных агентов, как в медицине, так и в ветеринарии при лечении таких животных, как свиньи, жвачные, лошади, собаки, кошки и домашняя птица.
Гибридные производные формулы I согласно настоящему изобретению также применяются для получения лекарственного средства для лечения инфекций (особенно бактериальных инфекций или протозойных инфекций) и заболеваний, связанных с инфекциями (особенно заболеваний, связанных с бактериальными инфекциями или протозойными инфекциями).
Соединения согласно настоящему изобретению особенно активны против бактериальных и подобных бактериям организмов и поэтому являются особенно подходящими для человека, а также животных при профилактике и химиотерапии локальных и системных инфекций, вызываемых этими патогенными организмами, а также заболеваний, связанных с бактериальными инфекциями, включая пневмонию, воспаление среднего уха, синусит, бронхит, тонзиллит и мастоидит, связанные с инфекцией, вызываемой Streptococcus pneumoniae, Haemophilus influenzas, Moraxella catarrhalis, Staphylococcus aureus, Enterococcus faecalis, E.faecium, E.casseliflavus, S.epidermidis, S.haemolyticus или Peptostreptococcus spp.; фарингит, ревматическую лихорадку и гломерулонефрит, связанные с инфекцией, вызываемой Streptococcus pyogenes, группами С и G streptococci, Corynebacterium diphtheriae или Actinobacillus haemolyticum; инфекции верхних дыхательных путей, связанные с инфекцией, вызываемой Mycoplasma pneumoniae, Legionella pneumophila, Streptococcus pneumoniae, Haemophilus influenzae или Chlamydia pneumoniae; инфекции крови и тканей, включая эндокардит и остеомиелит, вызываемые S.aureus, S.haemolyticus, E.faecalis, E.faecium, E.durans, включая наследственную резистентность к известным антибактериальным средствам таким, как, не лимитируя, β-лактамы, ванкомицин, аминогликозиды, хинолоны, хлорамфеникол, тетрациклины и макролиды; неосложненные инфекции кожи и мягких тканей и абсцессы и послеродовой сепсис, связанные с инфекцией, вызываемой Staphylococcus aureus, некоагулируемыми staphylococci (то есть S.epidermidis, S.haemolyticus и тому подобные). Streptococcus pyogenes, Streptococcus agalactiae, Streptococcal групп C-F (мельчайшая колония streptococci), viridans streptococci, Corynebacterium minutissimum, Clostridium spp. или Bartonella henselae; неосложненные острые инфекции мочевого тракта, связанные с инфекцией, вызываемой Staphylococcus aureus, некоагулируемыми видами стафилоккоков или Enterococcus spp.; уретрит и цервицит; болезни, передаваемые половым путем, связанные с инфекцией, вызываемой Chlamydia trachomatis, Haemophilus ducreyi, Treponema pallidum, Ureaplasma urealyticum или Neiserria gonorrhoeae; токсикозы, связанные с инфекцией, вызываемой S.aureus (пищевое отравление и токсический шок), или группами А, В и С streptococci; язвы, связанные с инфекцией, вызываемой Helicobacter pylori; системный лихорадочный синдром, связанный с инфекцией, вызываемой Borrelia recurrentis; болезнь Лайма, связанная с инфекцией, вызываемой Borrelia burgdorferi; конъюктивит, кератит и дакриоцистит, связанные с инфекцией, вызываемой Chlamydia trachomatis, Neisseria gonorrhoeae, S.aureus, S.pneumoniae, S.pyogenes, H.Influenzae или Listeria spp.; диссеминированный Mycobacterium avium комплекс (MAC), связанный с инфекцией, вызываемой Mycobacterium avium или Mycobacterium intracellulare; инфекции, вызываемые Mycobacterium tuberculosis, M.leprae, M.paratuberculosis, M.Kansasii или М.chelonei; гастроэнтерит, связанный с инфекцией, вызываемой Campylobacter jejuni; кишечные протозойные инфекции, связанные с инфекцией, вызываемой Cryptosporidium spp.; стоматологическая инфекция, связанная с инфекцией, вызываемой viridans streptococci, стойкий кашель, связанный с инфекцией, вызываемой Bordetella pertussis; газовая гангрена, связанная с инфекцией, вызываемой Clostridium perfringens или Bacteroides spp.; и атеросклероз или сердечно-сосудистая болезнь, связанные с инфекцией, вызываемой Helicobacter pylori или Chlamydia pneumoniae.
Соединения формулы I согласно настоящему изобретению применяются, кроме того, для получения лекарственного средства для лечения инфекций, вызываемых такими бактериями, как Е.coli, Klebsiella pneumoniae и другими энтеробактериями, Acinetobacter spp., Stenothrophomonas maltophilia, Neisseria meningitidis, Bacillus cereus, Bacillus anthracis, Corynebacterium spp., Propionibacterium acnes и бактероидами spp. В добавление, соединения формулы I согласно настоящему изобретению применяются, кроме того, для получения лекарственного средства для лечения инфекций, вызываемых Clostridium difficile.
Соединения формулы I согласно настоящему изобретению применяются, кроме того, для лечения протозойных инфекций, вызываемых Plasmodium malaria, Plasmodium falciparum, Tokcoplasma gondii, Pneumocystis carinii, Trypanosoma brucei и Leishmania spp.
Представленный перечень патогенных микроорганизмов должен рассматриваться только в качестве примеров и никоим образом в качестве лимитирующего перечня.
Так же, как у человека, бактериальные инфекции могут подлежать лечению и у других видов животных, например, у таких, как свиньи, жвачные, лошади, собаки, кошки и домашняя птица.
Поэтому соединения формулы I или их фармацевтически приемлемые соли могут быть использованы для получения лекарственного средства, и являются подходящими для профилактики или лечения бактериальных инфекций (особенно инфекций, вызываемых патогенными микроорганизмами, упомянутыми в перечне выше).
Соединения формулы I и их фармацевтически приемлемые соли могут быть использованы в качестве лекарственных средств, например в форме фармацевтических композиций для энтерального и парентерального введения.
Изготовление фармацевтических композициий осуществляется методом, известным любому специалисту в области техники (см., например, Mark Gibson, Editor, Pharmaceutical Preformulation and Formulation, IHS Health Group, Englewood, CO, USA, 2001; Remington, The Science and Practice of Pharmacy, 20th Edition, Philadelphia College of Pharmacy and Science), путем введения описанных соединений формулы I или их фармацевтически приемлемых солей, необязательно в комбинации с другими фармацевтически приемлемыми субстанциями, в лекарственную форму вместе с подходящим, нетоксичными, инертными, терапевтически совместимыми твердыми или жидкими носителями и, если необходимо, обычными фармацевтическими наполнителями.
Другой аспект по изобретению относится к способу лечения инфекции, заключающему во введении пациенту фармацевтически активного количества соединения формулы I или его фармацевтически приемлемой соли.
Более того, соединения формулы I могут быть применены для целей очистки, например для очистки хирургических инструментов от патогенных микробов и бактерий или асептической очистки помещения или поверхности. Для этих целей соединения формулы I могут применяться в виде раствора или спрея.
Любая ссылка на соединение формулы I, I51, I52, I6, ID или IPDG подразумевает ссылку на соль (в частности, фармацевтически приемлемую соль) соединения формулы I, I51, I52, I6, ID или IPDG, соответственно, как уместную и целесообразную. Кроме того, любые ссылки на соединения формулы I (или на сами соединения, их соли, композиции, содержащие соединения или их соли, применение соединений или их солей и тому подобное), конечно, с изменениями, применимы к соединениям формулы ICE, соединениям формулы I5, соединениям формулы I51, соединениям формулы I52, соединениям формулы I6, соединениям формулы ID и соединениям формулы IPDG.
Согласно изобретению, соединения формулы I (или формулы ICE) могут быть получены с помощью методов, описанных ниже.
Получение соединений формулы I
Аббревиатуры:
В описании и примерах используются следующие аббревиатуры:
АсОН - уксусная кислота, AD-mix α - 1,4-бис-(дигидрохинин)фталазин, K3Fe(CN)6, К2СО3 и K2OsO4·2H2O, AD-mix β - 1,4-бис-(дигидрохинин)фталазин, K3Fe(CN)6, К2СО3 и K2OsO4·2H2O, Alloc - аллилоксикарбонил, BnBr -бензилбромид, Бок - трет-бутоксикарбонил, t-BuOK-трет-бутилат калия, Кбз - бензилоксикарбонил, ДБУ - 1,8-диазабицикло[5.4.0]ундец-7-ен, ДХМ - дихлорметан, ДИАД - диизопропилазодикарбоксилат, ДИПЭА - N,N-диизопропилэтиламин, ДМА - диметилацетамид, ДМАП - 4-диметиламинопиридин, ДМФ - N,N-диметилформамид, ДМСО - диметилсульфоксид, ЭА - этилацетат, ЭДК - гидрохлорид 1-(диметиламинопропил)-3-этилкарбодиимида, ЭСИ - ионизационное электрораспыление, эфир или Et2O - диэтиловый эфир, УХ - ускоренная хроматография, ч - час, гексан - н-гексан, MeCN - ацетонитрил, м-ХПБК - м-хлорпербензойная кислота, МеОН - метанол, МС - масс-спектроскопия, NaOMe - метилат натрия, N-МП - N-метилпирролидинон, Pd/C или Pd(OH)2/C -палладий или дигидроксипалладий на угле, PPh3 - трифенилфосфин, КТ - комнатная температура, SiO2 - силикагель, ТБДМССl - трет-бутилдиметилсилилхлорид, ТЭА - триэтиламин, ТФК - трифторуксусная кислота, ТГФ - тетрагидрофуран, TMCCl - триметилсилилхлорид.
Общие пути синтеза:
Новые соединения формулы I могут быть получены в соответствии с настоящим изобретением посредством:
а) реакции соединения формулы II
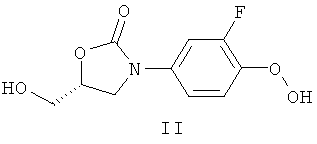
с соединением формулы III
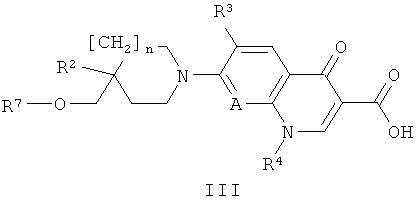
где n, A, R3 и R4 имеют значения, обозначенные в формуле I, и R7 обозначает
C1-3алкилсульфонил (например, метилсульфонил), трифторметилсульфонил или арилсульфонил (например, фенил- или п-толилсульфонил) и R2 обозначает ОН или Н, или R2 и R7 вместе образуют связь (то есть R2 и OR7 образуют, вместе с атомами углерода, содержащими их, эпоксидное кольцо), предпочтительно, в температурном интервале от 10°С до 100°С (более предпочтительно, приблизительно от 40°С до 80°С), в присутствии неорганического основания такого, как К2СО3, или органического основания такого, как ТЭА, в органическом растворителе (например, ДМФ);
или посредством
б) реакции соединения формулы IV

где n обозначено в формуле I и R2 обозначает Н или ОН,
с соединением формулы V

где A, R3 и R4 имеют значения, обозначенные в формуле I, Y обозначает галоген и R8 обозначает водород, BF2 или В(ОС(=O)(С1-4алкил)2, C1-5алкил (например, метил, этил, н-пропил, изопропил или трет-бутип), аллил, арилС1-5алкил (например, бензил, п-нитробензил или п-метоксибензил), три-(C1-5алкил)силил (например, триметилсилил или трет-бутилдиметилсилил) или диарилС1-5алкилсилил (например, трет-бутилдифенилсилил), предпочтительно в температурном интервале от 10°С до 100°С, более предпочтительно, приблизительно между 40°С и 80°С, в присутствии органического основания такого, как ТЭА или ДИПЭА, в органическом растворителе, например, N-МП;
или посредством
в) превращения соединения формулы I, где R1 обозначает ОН, в соединение формулы I, где R1 обозначает ОРО3Н2 или OCOR5, при этом R5 является остатком натуральной аминокислоты, энантиомером натуральной аминокислоты или диметиламиноглицина;
или посредством
г) превращения соединения формулы IPG
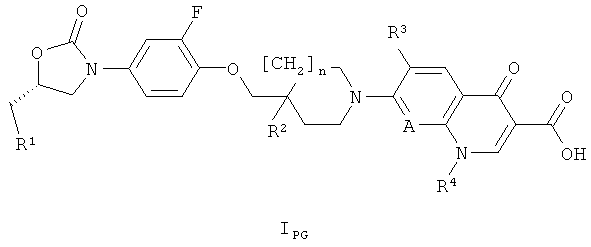
где R1 обозначает OPG1 (PG1 при этом обозначает защитную группу для гидроксильной функциональной группы), R2 обозначает ОН, и n, R3, R4 и А имеют те же значения, которые указаны в формуле I, в соединение формулы I, где R2 обозначает ОРО3Н2, и последующего удаления защитной группы PG1, примерами подходящих защитных группу PG1 являются алкилсилильные или диарилалкилсилильные группы такие, как триметилсилил, трет-бутилдиметилсилил или трет-бутилдифенилсилил (методы введения и удаления этих защитных групп суммированы в публикации: Protecting Groups, Kocienski, P.J., Thieme (1994));
или посредством
д) превращения соединения формулы VI
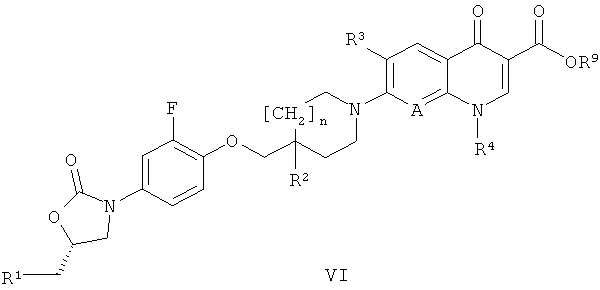
где R9 обозначает С1-5алкил (например, метил, этил, н-пропил, изопропил или трет-бутил), арил-С1-5алкил (например, бензил, п-нитробензил или п-метоксибензил), аллил, три(С1-5алкил)силил (например, триметилсилил или трет-бутилдиметилсилил) или диарилС1-5алкилсилил (например, трет-бутилдифенилсилил), и n, А, R1, R2, R3 и R4 имеют значения, приведенные в формуле I, в соответствующее соединение формулы I путем гидролиза, омыления или гидрогенолиза (например, как указано в публикации Protecting Groups, Kocienski, P.J., Thieme (1994)).
Рассматривая приведенный выше процесс, следует остановиться на нескольких замечаниях:
- относительно варианта а), соединение формулы III может быть также заменено его сложным эфиром, то есть соединением формулы IIIE
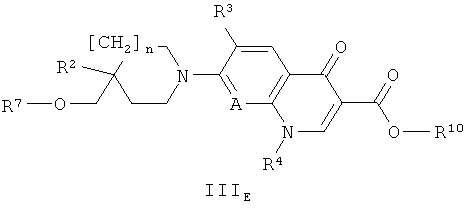
где n, A, R2, R3, R4 и R7 имеют значения, приведенные для формулы III, и R10 представляет собой алкил, аллил или арилалкил, в этом случае стадия удаления защитной сложно-эфирной группы должна следовать за реакцией соединения формулы IIIE с соединением формулы II (общие методы удаления защитной сложно-эфирной группы см. в публикации: Protecting Groups, Kocienski, P.J., Thieme (1994));
- относительно варианта а), соединение формулы II может быть также замещено силильной эфирной группой, то есть соединение формулы IIPG
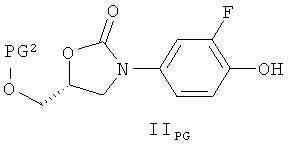
где PG2 представляет собой силильную защитную группу для гидроксильной функциональной группы такую, как три-С1-5алкилсилил (например, триметилсилил или трет-бутилдиметилсилил) или диарилС1-5алкилсилил (например, трет-бутилдифенилсилил), в этом случае стадия удаления защитной группы должна следовать за реакцией соединения формулы III или IIIE с соединением формулы IIPG (общие методы осуществления таких реакций можно найти в публикации: Protecting Groups, Kocienski, P.J., Thieme (1994)), при этом следует иметь в виду, что когда R2 обозначает Н, конденсация между соединением формулы IIPG и соединением формулы III или IIIE осуществляется в условиях проведения реакции Митсунобу, как описано в публикации: Synthesis (1981), 1, 1-28, и особенно в присутствии ДИАД и PPh3;
- относительно варианта б), соединение формулы IV может быть также замещено соединением формулы IVp
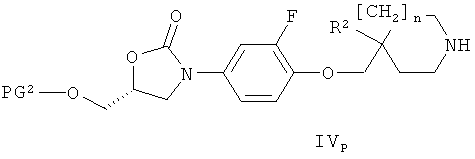
где n и R2 имеют значения, приведенные для формулы IV, и PG2 представляет собой защитную группу для гидроксильной функциональной группы (например, алкилсилилильную или диарилалкилсилильную группу такую, как триметилсилильная, трет-бутилдиметилсилильная или трет-бутилдифенилсилильная), в этом случае соответствующая стадия удаления защитной группы должна следовать за реакцией соединения формулы IVP с соединением формулы V (общие методы осуществления таких реакций можно найти в публикации: Protecting Groups, Kocienski, P.J., Thieme (1994));
- относительно варианта б), когда R8 не является H, требуется дополнительная стадия удаления сложно-эфирной группы (общие методы осуществления таких реакций можно найти в публикации: Protecting Groups, Kocienski, P.J., Thieme (1994)), за исключением случаев, когда R обозначает BF2 или В(ОС(=O)С1-4алкил)2 и где гидролиз осуществляется уже на стадии кислотной обработки;
- относительно варианта в), соединение формулы I, где R1 обозначает ОН, может быть замещено соединением формулы VI, где R1 обозначает ОН, и R2 обозначает Н или ОН, в этом случае требуется дополнительная стадия удаления сложно-эфирной группы (общие методы осуществления таких реакций можно найти в публикации: Protecting Groups, Kocienski, P.J., Thieme (1994));
- относительно вариантов в) и г):
соединения формулы I, где R1 или R2 обозначают ОРО3Н2, могут быть получены путем удаления защитных групп у соединений, где R1 или R2 обозначает OPO(OR)2 и R обозначает аллил или бензил (данные относительно природы R, о различных методах удаления защитных групп можно найти в публикации: Protecting Groups, Kocienski, P., J., Thieme (1994), примером методов удаления защитных групп может служить каталитическое гидрирование над соответствующим катализатором таким, как палладий, или гидролиз бромистоводородной кислотой в растворителе таком, как АсОН, когда R обозначает бензил);
соединения формулы I, где R1 обозначает OCOR5, могут быть получены, например, реакцией соединений формулы I, где R1 обозначает ОН, или соединений формулы VI, где R1 обозначает ОН и R2 обозначает Н или ОН, с диметиламиноглицином или N-защищенной аминокислотой с последующим удалением защитной группы с аминогруппы в стандартных условиях, известных специалисту в области техники (дополнительная стадия удаления сложно-эфирной защитной группы требуется в случае реакции с соединением формулы VI).
Соединения формулы I, получаемые согласно вышеприведенным общим методам синтеза, могут быть затем, при необходимости, превращены в их соли, а именно в их фармацевтически приемлемые соли.
Кроме того, в случае, когда соединения формулы I получают в виде смеси энантиомеров, последние могут быть разделены с помощью методов, известных специалисту в области техники (например, путем получения и разделения диастереомерных солей или путем хроматографии на хиральной стационарной фазе). В случае, когда соединения формулы I получают в виде смеси диастереоизомеров, они могут быть выделены с помощью соответствующей комбинации хроматографии на силикагеле, ВЭЖХ и кристаллизации.
Получение различных синтетических промежуточных соединений:
Получение соединений формулы II
Соединения формулы II могут быть получены посредством гидрирования соединения формулы VII
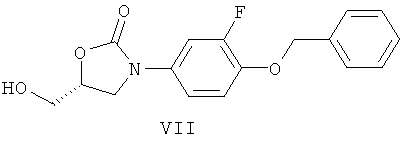
над соответствующим катализатором таком, как палладий или платина на угле, в растворителе таком, как ТГФ, МеОН или AcOEt, в температурном интервале от 0°С до 40°С, или посредством гидролиза в присутствии раствора HBr в воде или АсОН, при температуре от 0°С до 80°С и в растворителе таком, как АсОН.
Получение соединения формулы III
Соединения формулы III могут быть получены в соответствии с нижеприведенной схемой 1.
Схема 1

На схеме 1 R8 обозначает Н, алкил, аллил или арилалкил, при этом другие символы обозначены ранее.
Соединения формулы IIIS, где R2 обозначает Н или ОН, R7 обозначает SO2R11, R11 при этом обозначает алкил, трифторметил или арил типа фенила или п-толила, получают (схема 1) из соединений формулы IIIA, где R7 обозначает Н, посредством реакции с соответствующими сульфонилхлоридами в присутствии органического основания такого, как ТЭА, в растворителе таком, как ДХМ или ТГФ, в температурном интервале от -10°С до 50°С. Соединения формулы IIIA получают посредством реакции соединений формулы V с пиперидинами формулы VIII в присутствии органического основания такого, как ТЭА или ДИПЭА, в температурном интервале от 40°С до 100°С, в растворителе таком, как ТГФ, ДМФ или N-МП. В случае, когда R8 обозначает бензил, карбоновую кислоту формулы IIIS освобождают от защитной группы, используя стандартные методы, описанные в публикации: Protecting Groups, Kocienski, P.J., Thieme (1994) (например, с помощью гидрирования над Pd/C).
Соединения формулы III, где R2 и R7 вместе образуют связь, то есть соединения формулы IIIO
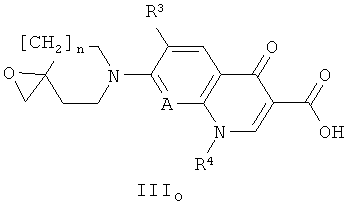
могут быть получены посредством внутримолекулярной циклизации соединения формулы IIIS, где R2 обозначает ОН, в присутствии органического основания (например, ТЭА) или неорганического основания (например, К2СО3 или щелочной метилат такой, как NaOMe, или щелочной гидрид такой, как NaH).
Получение соединений формулы IV
Соединения формулы IV могут быть получены, как представлено на нижеприведенной схеме 2.
Схема 2

Соединения формулы IV могут быть получены посредством удаления защитной группы с соединения формулы X, где PG3 представляет собой азотную защитную группу такую, как алкоксикарбонил (например, Бок), бензилоксикарбонил (например, Кбз), аллилоксикарбонил или бензил. Общие методы осуществления последовательного введения/удаления защиты у вторичной азотной группы описаны в публикации: Protecting Groups, Kocienski, P.J., Thieme (1994).
Соединения формулы X, где R2 обозначает ОН, получают посредством реакции соединения формулы II с соединением формулы IX, где либо R2 обозначает ОН и R7 обозначает SO2R11, при этом R11 обозначает алкил, трифторметил или арил типа фенила или п-толила, либо R2 и R7 вместе образуют связь (эпоксид). Названный эпоксид может быть получен из соединений формулы IX, где R2 обозначает ОН и R7 обозначает SO2R11, путем обработки или органическим основанием таким, как ТЭА, пиридин или ДБУ, или неорганическим основанием таким, как K2CO3, в растворителе таком, как ТГФ или ДХМ, в температурном интервале от -10°С до 40°С. Соединения формулы X, где R2 обозначает Н, получают посредством реакции соединения формулы II с соединением формулы IX, где R7 обозначает SO2R11. Соединения формулы IX являются коммерчески доступными (например, соединения формулы IX, где PG3 обозначает Бок, n=0 и R2 и R7 образуют эпоксид, или где PG обозначает Бок, n=1 и R2=R7=ОН) или их получают, как описано далее. Альтернативно, соединения формулы Х могут быть получены посредством реакции соединения формулы II с соединениями формулы IX, где R7 обозначает Н, в условиях проведения реакции Митсуноби.
Получение соединений формулы V
Соединения формулы V, где R8 обозначает Н и Y галоген, коммерчески доступны (например, соединения, где R3 обозначает F, R4 обозначает циклопропил и А обозначает СН, CF или СОМе, или R3 обозначает F, R4 обозначает Et и А обозначает СН или CF, или R3 обозначает F, R4 обозначает циклопропил и А обозначает N). Соединения формулы V, где R обозначает BF2 или В(ОС(=O)(С1-4алкил)2, получают из соединений формулы V, где R8 обозначает Н, согласно публикации WO 88/07998.
Получение соединений формулы VI
Соединения формулы VI могут быть получены посредством конденсации соединений формулы IV или, альтернативно, соединений формулы IVP по определению, данному ранее, с соединениями формулы V по определению, данному ранее, исключая, что R8 представляет собой С1-5алкил (например, метил, этил, н-пропил, изопропил или трет-бутил), арил-С1-5алкил (например, бензил, п-нитробензил или п-метоксибензил), аллил, триС1-5алкилсилил (например, триметилсилил или трет-бутилдиметилсилил) или диарил-C1-5алкилсилил (например, трет-бутилдифенилсилил), в тех же условиях, которые описаны для реакции соединений формулы IV с соединениями формулы V. В случае, когда используются соединения формулы IVP, стадия удаления защитной группы может быть проведена после реакции конденсации.
Получение соединений формулы VII
Соединение формулы VII может быть получено согласно публикации WO 2004/096221.
Получение соединений формулы VIII
Соединения формулы VIII либо коммерчески доступны (R2 обозначает Н), либо могут быть получены путем снятия защитной группы у соединений формулы IX (R2 обозначает ОН и R7 обозначает Н), например, посредством обработки Бок-защищенных соединений с помощью ТФК или гидрированием соответствующего Кбз-защищенных соединений над Pd/C.
Получение соединений формулы IX
Соединения формулы IX могут быть получены из метилиденовых производных формулы XI, как представлено на нижеприведенной схеме 3.
Схема 3
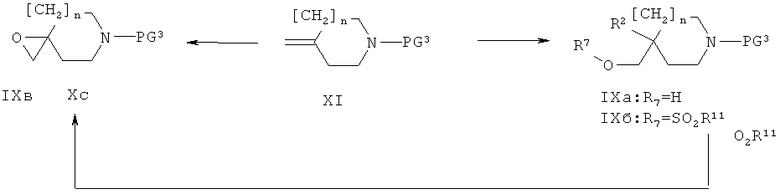
Соединения формулы IXб, то есть соединения формулы IX, где R2 обозначает Н или ОН и R7 обозначает SO2R11, получают из соответствующих соединений формулы IХа, где R7 обозначает Н, с использованием тех же методов, которые использовались при превращении соединений формулы IIIA в соединения формулы IIIS. Соединения формулы IХа либо коммерчески доступны (R2 обозначает Н), либо могут быть получены из известных метилиденовых производных формулы XI (например, соединения, где n=0 и PG3 обозначает бензил, Бок или бензилоксикарбонил (см. ЕР 241206 и ЕР 550025); или соединения, где n=1 и PG3 обозначает бензил, Бок, которые являются коммерчески доступными). Они могут быть также получены посредством каталитического цис-дигидроксилирования с использованием тетроксида осмия в качестве катализатора или путем его асимметрической версии (Sharpless дигидроксилирование с использованием AD-mix α или β), как описано в публикации J. Am. Chem. Soc. (1988), 110, 1968, где R2 обозначает ОН. Соединения формулы IХв, то-есть соединения формулы IX, где R2 и R7 вместе образуют связь (эпоксид), получают либо путем внутримолекулярной циклизации соединений формулы IХб с неорганическим основанием таким, как К2СО3 или NaH, или с органическим основанием таким, как ТЭА или ДБУ, или посредством эпоксидирования метилиденовой двойной связи перкислотой такой, как м-ХПБК. Альтернативно, соединения формулы IХв могут быть также получены посредством реакции соответствующих оксопроизводных (коммерчески доступны соединения, где n=0 или 1 и PG3 обозначает бензилоксикарбонил или Бок) с йодидом триметилсульфоксония или йодидом триметилсульфония в присутствии щелочи такой, как КОН, в полярном растворителе таком, как MeCN, в температурном интервале от 20 до 100°С (как описано в публикациях: J. Am. Chem. Soc. (1965), 87, 1353-1364 и Tetrahedron Lett. (1987), 28, 1877-1878).
Соединения следующих примеров иллюстрируют получение фармакологически активных соединений по изобретению, не лимитируя его объема.
Примеры
Все температуры приведены в °С. Все аналитические и препаративные ВЭЖХ исследования на нехиральных фазах проводились с использованием RP-С18 колонок. Аналитические ВЭЖХ исследования проводились на двух различных приборах с временными циклами около 2,5 мин и около 3,5 мин, соответственно. Если не указано иначе, значения, приведенные для МС, соответствуют главному пику ((М+H)+ с разбросом +/- 0,5 единиц). В ЯМР-спектрах константы взаимодействия J приведены в Гц.
Стандартные методики обработки:
После растворения в соответствующем органическом растворителе (см. описание соответствующего примера) органическую фазу отделяют и последовательно промывают водой и рассолом. В случае реакции, проводимой в водорастворимом растворителе (например, МеОН, ТГФ или ДМФ), объединенные водные слои промывают тем же растворителем, который использовался при обработке реакционной смеси. Объединенные органические фазы высушивают над MgSO4 и фильтруют. Фильтрат выпаривают при пониженном давлении.
Стандартная хроматографическая методика:
Сырой продукт растворяют в минимальном количестве элюента (см. описание соответствующего примера) и хроматографируют на SiO2. Соответствующие фракции объединяют и выпаривают при пониженном давлении.
Пример 1: 1-циклопропил-6-фтор-7-{4-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-4-гидроксипиперидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота:
1.i (R)-3-(3-Фтор-4-гидроксифенил)-5-гидроксиметилоксазолидин-2-он:
Раствор (R)-3-(4-бензилокси-3-фторфенил)-5-гидроксиметилоксазолидин-2-она (6,34 г, получен согласно WO 2004/096221) в смеси ТГФ/МеОН (в соотношении 1:1; 200 мл) гидрируют над 10%-ным Pd/C (1 г) в течение ночи. Катализатор отфильтровывают, фильтрат выпаривают при пониженном давлении и остаток перемешивают с ЭА. Кристаллы отделяют фильтрованием, получая 3,16 г (70% выход) бесцветного твердого вещества.
1Н ЯМР (ДМСОd6; δ м.д.): 3,5 (m, 1H), 3,64 (m, 1H), 3,74 (dd, J=8,8, 6,4, 1 H), 3,99 (t, J=8,8, 1H), 4,64 (m, 1H), 5,16 (t, J=5,6, 1H), 6,93 (dd, J=9,7, 8,8, 1 H), 7,08 (ddd, J=8,8, 2,6, 1,2, 1H), 7,45 (dd, J=13,5, 2,6, 1H), 9,66 (s, 1H).
МС (ЭСИ): 228,1.
1.ii. Бензиловый эфир 4-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-4-гидроксипиперидин-1-карбоновой кислоты:
Раствор промежуточного соединения (1.i) (1,27 г) и 1-окса-6-аза-спиро[2.5]октан-6-карбоновой кислоты (1,60 г; получен согласно US 4244961) растворяют в ДМФ (15 мл) и обрабатывают Na2CO3 (1,16 г). Смесь затем нагревают при температуре 100°С в течение ночи. Остаток, полученный после обработки (ДХМ), перемешивают с ЭА, твердое вещество отделяют фильтрованием и последовательно промывают ЭА и гексаном, получая 2,52 г (94,5% выход) бежевого твердого вещества.
1Н ЯМР (ДМСОd6; δ м.д.): 1,57 (m, 4Н), 3,14 (m, 2H), 3,54 (m, 1H), 3,64 (m, 1H), 3,79 (m, 5H), 4,03 (t, J=9,1, 1H), 4,66 (m, 1H), 4,78 (s, 1H), 5,05 (s, 2 H), 5,16 (t, J=5,6, 1H), 7,18 (m, 2H), 7,32 (m, 5H), 7,55 (d, J=12, 1H).
MC (ЭСИ): 475,0.
1.iii. (R)-3-[3-Фтор-4-(4-гидроксипиперидин-4-илметокси)фенил]-5-гидроксиметилоксазолидин-2-он:
Суспензию промежуточного соединения (1.ii) (2,5 г) в смеси ЭА/МеОН (соотношение 1:1; 100 мл) гидрируют над Pd/C в течение 48 ч. Затем суспензию нагревают при температуре 40°С, после чего катализатор отфильтровывают. Фильтрат выпаривают при пониженном давлении, получая 1,61 г (89% выход) желтого порошка.
1Н ЯМР (ДМСОd6; δ м.д.): 1,4-1,63 (m, 4H), 2,67 (m, 2H), 2,83 (m, 2H), 3,53 (dd, J=4,0 и 12,0, 1Н); 3,66 (dd, J=3,3 и 12,0, 1Н), 3,71 (s, 2H); 3,80 (m, 1 H), 4,05 (t, J=9,0, 1H), 4,48 (s, 1H), 4,68 (m, 1H), 5,20 (s, 1H), 7,20 (m, 2H), 7,57 (d, 1H).
МС (ЭСИ): 341,5.
1.iv. 1-Циклопропил-6-фтор-7-{4-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-4-гидроксипиперидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота:
Раствор промежуточного соединения (1.iii) (200 мг), комплекса 7-хлор-1-циклопропил-6-фтор-1,4-дигидро-4-оксо-3-хинолинкарбоновой кислоты с бордиацетатом (241 мг; получен согласно WO 88/07998) и ДИПЭА (100 мкл) в N-МП (2 мл) перемешивают при температуре 85°С в течение 5 ч. Реакционную смесь затем выпаривают при пониженном давлении, а остаток переносят в 5-молярный раствор HCl в МеОН (3 мл) и перемешивают. Образовавшееся твердое вещество отделяют фильтрованием и промывают МеОН, получая 230 мг (67% выход) желтого твердого вещества.
1Н ЯМР (ДМСОd6; δ м.д.): 1,66-1,35 (m, 4Н), 1,75 (d, J=12,8, 2H), 1,95 (m, 2H), 3,33 (t расширенный, J=11,0, 2H), 3,57 (m, 3H), 3,67 (dd, J=12,3, 3,3, 1 H), 3,83 (m, 2H), 3,92 (s, 2H), 4,06 (t, J=9,0, 1H), 4,69 (m, 1H), 7,24 (m, 2H), 7,60 (m, 2H), 7,90 (d, J=13,3, 1H), 8,66 (s, 1H).
MC (ЭСИ): 585,9.
Пример 2: 1-Циклопропил-6-фтор-7-{4-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]пиперидин-1-ил)-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота:
2.i. (R)-3-(4-Бензилокси-3-фторфенил)-5-(трет-бутилдиметил-силанилоксиметил)оксазолидин-2-он:
Раствор ТБДМССl (3,77 г) в ДХМ (5 мл) по каплям прибавляют при температуре 0°С к раствору (R)-3-(4-бензилокси-3-фторфенил)-5-гидроксиметилоксазолидин-2-она (6,35 г; полученного согласно WO 2004/096221) и имидазола (2,04 г) в ДМФ (15 мл). После перемешивания при КТ в течение 16 ч реакционную смесь концентрируют в вакууме. Остаток затем переносят в ДХМ и последовательно промывают 1-нормальным раствором HCl, насыщенным водным раствором NaHCO3 и рассолом, высушивают над MgSO4, фильтруют и концентрируют, получая 8,41 г (97% выход) бесцветного твердого вещества.
1Н ЯМР (ДМСОd6; δ м.д.): 0,04 (6Н, s); 0,79 (9Н, s); 3,69-3,78 (2Н, m), 3,86 (1H, dd, J=3 и J=12); 4,07 (1H, t, J=9); 4,69-4,77 (1H, m); 5,15 (2Н, s); 7,15-7,21 (1H, m); 7,25 (1H, t, J=9); 7,30-7,36 (1H, m); 7,37-7,50 (4H, m); 7,57 (1H, dd, J=3 и J=14).
2.ii. (R)-5-(трет-Бутилдиметилсиланилоксиметил)-3-(3-фтор-4-гидроксифенил)оксазолидин-2-он:
Раствор промежуточного соединения (2.i) (7,22 г) в смеси ТГФ/МеОН (соотношение 1:1; 150 мл) гидрируют над 10%-ным Pd/C (150 мг) в течение 3 ч. Катализатор отфильтровывают и фильтрат концентрируют в вакууме, получая 5,51 г (96% выход) бесцветного твердого вещества.
1H ЯМР (ДМСОd6; δ м.д.): 0,04 (6Н, s); 0,80 (9Н, s); 3,69-3,78 (2Н, m), 3,86 (1H, dd, J=3 и J=12); 4,07 (1H, t, J=9); 4,68-4,75 (1H, m); 6,94 (1H, t, J=9); 7,04-7,10 (1H, m); 7,45 (1H, dd, J=3 и J=14); 9,65 (1H, s).
МС (ЭСИ): 342,2.
2.iii. трет-Бутиловый эфир 4-{4-[(R)-5-(трет-бутилдиметилсиланилоксиметил)-2-оксооксазолидин-3-ил]-2-фторфеноксиметил}пиперидин-1-карбоновой кислоты:
К суспензии трет-бутилового эфира 4-гидроксиметилпиперидин-1-карбоновой кислоты (200 мг; коммерчески доступна), промежуточного соединения (2.ii) (317 мг) и PPh3 (365 мг) в ТГФ (5 мл) по каплям в течение 90 мин прибавляют ДИАД (0,294 мл). После перемешивания в течение ночи при КТ реакционную смесь обрабатывают смесью толуол/гексан (в соотношении 1:2) и хроматографируют (гексан/ЭА в соотношении 2:1), получая 351 мг (70% выход) грязно-белого твердого вещества.
МС (ЭСИ): 539,2.
2.iv. (R)-3-[3-Фтор-4-(пиперидин-4-илметокси)фенил]-5-гидроксиметилоксазолидин-2-он:
Раствор промежуточного соединения (2.iii) (351 мг) в МеОН (2 мл) обрабатывают 5-молярным раствором HCl в МеОН (1 мл) и перемешивают при КТ в течение 3 ч. Образовавшееся твердое вещество отделяют фильтрованием и промывают МеОН (5 мл), получая 180 мг (85% выход) бесцветного твердого вещества.
1H ЯМР (ДМСОd6; δ м.д.): 1,48 (2Н, m); 1,89 (2Н, m); 2,05 (1Н, m); 2,88 (2Н, t, J=10); 3,10 (2Н, m); 3,55 (1Н, m); 3,63 (1Н, m); 3,78 (1Н, dd, J=6,4 и J=8,8); 3,91 (2Н, d, J=6,2); 4,02 (1Н, t, J=8,8); 4,66 (1Н,т); 5,19 (1Н, t, J=5,6); 7,20 (2Н, m); 7,56 (1Н, dd, J=2,35 и J=14).
МС (ЭСИ): 325,5.
2.v. 1-Циклопропил-6-фтор-7-{4-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]пиперидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота:
Названное в заголовке соединение получают в виде бесцветного порошка с 12%-ным выходом, исходя из промежуточного соединения (2.iv) (177 мг) и 7-хлор-1-циклопропил-6-фтор-1,4-дигидро-4-оксо-3-хинолинкарбоновая кислота/бордиацетат комплекса (205 мг), использую метод примера 1, стадия 1.iv.
1Н ЯМР (ДМСОd6; δ м.д.): 1,13-1,33 (m, 4Н), 1,45-1,6 (m, 2H), 1,94 (d1, J=12,0, 2H), 2,04 (m, 1H), 2,98 (t, J=12,0, 2H), 3,50-3,69 (m, 2H), 3,73-3,89 (m, 4H), 3,98 (d, J=6,2, 2H), 4,02 (t, J=9,3, 1H), 4,66 (m, 1H), 5,18 (t, J=5,6, 1H), 7,21 (m, 2H), 7,56 (m, 2H), 7,88 (d, J=13,5, 1H), 8,64 (s, 1H).
МС (ЭСИ): 570,2.
Пример 3: 1-Циклопропил-6-фтор-7-{4-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-4-гидроксипиперидин-1-ил}-4-оксо-1,4-дигидро-[1,8]нафтиридин-3-карбоновая кислота:
Раствор 7-хлор-1-циклопропил-6-фтор-1,4-дигидро-4-оксо-1,8-нафтиридин-3-карбоновой кислоты (166 мг; коммерческая) и промежуточного соединения (1.iii) (200 мг) в N-МП (5 мл) обрабатывают ТЭА (0,32 мл) и TMCCl и нагревают при температуре 85°С в течение 5 ч. Реакционную смесь затем выпаривают при пониженном давлении и остаток переносят в 5-молярный раствор HCl в МеОН (3 мл), после чего перемешивают в течение 30 мин. Раствор выпаривают при пониженном давлении, а остаток переносят в ЭА, Образовавшееся твердое вещество отделяют фильтрованием и промывают этилацетатом, получая 271 мг (78% выход) желтого твердого вещества.
1Н ЯМР (AMCOd6; δ м.д.): 0,89-1,27 (4Н, m); 1,78 (2Н, d, J=12,8); 1,90-2,04 (2Н, m); 3,53-3,88 (6Н, m); 3,88 (2Н, s), 4,06 (1Н, t, J=9,0), 4,42 (2Н, d расширенный, J=13,2), 4,44 (1Н, m); 7,11 (2Н, m); 7,55 (1Н, d, J=14,5); 8,05 (1H, d, J=13,5); 8,60 (1H, s).
МС (ЭСИ): 586,8.
Пример 4: Гидрохлорид 7-(4-{4-[(R)-5-((S)-2-аминопропионилоксиметил)-2-оксооксазолидин-3-ил]-2-фторфеноксиметил}-4-гидроксипиперидин-1-ил)-1-циклопропил-6-фтор-4-оксо-1,4-дигидрохинолин-3-карбоновой кислоты:
4.i. Бензиловый эфир 1-циклопропил-6-фтор-7-{4-[2-фтор-4-((R)-5-гидрокиметил-2-оксооксазолидин-3-ил)феноксиметил]-4-гидроксипиперидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновой кислоты:
Суспензию промежуточного соединения (1.iv) (300 мг) и К2СО3 (77,8 мг) в ДМФ (10 мл) обрабатывают BnBr (82 мкл) и перемешивают при температуре 80°С в течение 2 дней. Растворители удаляют затем при пониженном давлении. Остаток обрабатывают (ДХМ) и очищают с помощью хроматографии (ДХМ/МеОН в соотношении 95:5), получая 219 мг (63% выход) белого порошка.
1Н ЯМР (ДМСОd6; δ м.д.): 1,0-1,25 (4Н, m); 1,71 (2Н, dd, J=0,6 и J=12,9); 1,92 (2Н, m); 3,25 (2Н, m); 3,50 (3H, m); 3,65 (2Н, m); 3,78 (1H, dd, J=6,4 и J=8,8); 3,89 (2Н, s); 4,03 (1Н, t, J=9,1); 4,65 (1Н, m); 4,82 (1Н, s); 5,17 (1Н, t, J=5,6); 5,25 (2Н, s); 7,21 (2Н, m); 7,35-7,60 (7H, m); 7,74 (1Н, d, J=13,5); 8,45 (1Н, s).
МС (ЭСИ): 676,2.
4.ii. Бензиловый эфир 7-(4-{4-[(R)-5-((S)-2-трет-бутоксикарбониламинопропионилоксиметил)-2-оксооксазолидин-3-ил]-2-фторфеноксиметил}-4-гидроксипиперидин-1-ил)-1-циклопропил-6-фтор-4-оксо-1,4-дигидрохинолин-3-карбоновой кислоты:
Раствор промежуточного соединения (4.i) (219 мг) в ДМФ (3 мл) обрабатывают Бок-L-Ala-OH (79,7 мг), ЭДК (81 мг) и ДМАП (20 мг). Реакционную смесь перемешивают при КТ в течение 2 ч. Затем ДМФ выпаривают при пониженном давлении и остаток очищают с помощью хроматографии (ДХМ/МеОН в соотношении 95:5). Соответствующие фракции выпаривают при пониженном давлении и перемешивают в эфире. Твердое вещество отделяют фильтрованием, получая 280 мг (100% выход) белой пены.
1Н ЯМР (ДМСОd6; δ м.д.): 1,06-1,11 (2Н, m); 1,17-1,27 (5Н, m); 1,34 (9Н, s); 1,67-1,76 (2Н, d, J=12); 1,86-1,99 (2Н, m); 3,18-3,25 (2Н, m); 3,40-3,50 (2Н, m); 3,60-3,72 (1Н, m); 3,77-3,85 (1Н, m,); 3,89 (2Н, s); 3,96-4,04 (1H, t, J=7,3); 4,10 (1H, t, J=9); 4,2-43 (1H, dd, J=4,7 и J=13,2); 4,38-4,44 (1Н, d, J=11,7); 4,83-4,95 (1Н, m); 5,26 (2Н, s); 7,20-7,55 (9Н, m); 7,75 (1H, d, J=12,6); 8,46 (1Н, s).
МС (ЭСИ): 847,5.
4.iii. 7-(4-{4-[(R)-5-((S)-2-трет-Бутоксикарбониламинопропионилоксиметил)-2-оксооксазолидин-3-ил]-2-фторфеноксиметил}-4-гидроксипиперидин-1-ил)-1-циклопропил-6-фтор-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота:
Раствор промежуточного соединения (4.ii) (285,3 мг) в смеси диоксан/МеОН (в соотношении 1:1; 10 мл) гидрируют над 10%-ным Pd/C (10 мг) в течение 4 ч. Катализатор затем удаляют с помощью фильтрования и промывают МеОН (2 мл). Фильтрат выпаривают при пониженном давлении, получая 215 мг (84,4% выход) желтой пены.
МС (ЭСИ): 757,3.
4.iv. Гидрохлорид 7-(4-{4-[(R)-5-((S)-2-аминопропионилоксиметил)-2-оксооксазолидин-3-ил]-2-фторфеноксиметил}-4-гидроксипиперидин-1-ил)-1-циклопропил-6-фтор-4-оксо-1,4-дигидрохинолин-3-карбоновой кислоты:
Раствор промежуточного соединения (4.iii) (193 мг) в диоксане (1 мл) обрабатывают 0,15 мл HCl (5-молярный в диоксане). Реакционную смесь перемешивают при КТ в течение 14 ч. Растворитель затем выпаривают при пониженном давлении. Остаток переносят в диоксан (10 мл) и образовавшееся твердое вещество отделяют с помощью фильтрования, получая 153 мг (86,7% выход) желтого порошка.
1Н ЯМР (ДМСОd6; δ м.д.): 1,15-1,33 (4Н, m); 1,35 (3Н, d, J=6,4); 1,73 (2Н, d, J=13); l,93(2H, m); 3,31 (2Н, t, J=11); 3,84 (4Н, m); 4,13 (2Н, m); 4,35 (1Н, dd, J=5 и J=12); 4,55 (2Н, dd, J=2 и J=12); 4,95 (1Н, m); 7,23 (2Н, m); 7,56 (2Н, m); 7,88 (1Н, d, J=13,2); 8,51 (2Н, sl); 8,64 (1Н, s).
МС (ЭСИ): 657,3.
Пример 5: 1-Циклопропил-6-фтор-7-{4-[2-фтор-4-((R)-2-оксо-5-фосфоноксиметилоксазолидин-3-ил)феноксиметил]-4-гидроксипиперидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота:
5.i. 7-(4-{4-[(R)-5-(бис-Бензилоксифосфорилоксиметил)-2-оксооксазолидин-3-ил]-2-фторфеноксиметил}-4-гидроксипиперидин-1-ил)-1-циклопропил-6-фтор-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота:
Суспензию промежуточного соединения (1.iv) (300 мг) и 4,5-дицианоимидазол (109 мг) в ДХМ (3 мл) обрабатывают при температуре 0°С дибензил-N,N-диизопропилфосфорамидатом (0,303 мл). Реакцию перемешивают при КТ в течение 1 ч, а затем прибавляют 70%-ный раствор трет-бутилгидропероксида в воде (0,147 мл), после чего раствор перемешивают в течение 1 ч при КТ. Растворитель затем выпаривают при пониженном давлении, остаток обрабатывают (ДХМ) и очищают с помощью хроматографии (ДХМ/МеОН в соотношении 95:5), получая 214 мг (49,45% выход) грязно-белой пены.
МС (ЭСИ): 846,3.
5.ii. 1-Циклопропил-6-фтор-7-{4-[2-фтор-4-((R)-2-оксо-5-фосфоноксиметилоксазолидин-3-ил)феноксиметил]-4-гидроксипиперидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота:
Раствор промежуточного соединения (5.i) (214 мг) в АсОН (1,5 мл) обрабатывают HBr (1,5 мл; 33%-ный раствор в АсОН). Реакционную смесь перемешивают при КТ в течение 2 ч, после чего переносят в воду (20 мл). Смолу перемешивают в течение 1 ч и декантируют. Маслянистый продукт переносят в этилацетат (20 мл) и дополнительно перемешивают в течение 2 ч. Твердое вещество отделяют фильтрованием, перемешивают в ДХМ (10 мл) и снова отделяют с помощью фильтрования, получая 110 мг (65% выход) желтого порошка.
1Н ЯМР (ДМСОd6; δ м.д.): 1,18-1,30 (4Н, m); 1,73 (1H, d, J=13); 1,95 (2H, m); 2,40 (2Н, d, J=13); 3,26 (2H, m); 3,58 (2Н, m); 3,76-3,87 (2Н, m); 3,90 (1H, s); 3,95-4,15 (3Н, m); 4,47 (1Н, s); 4,86 (1Н, m); 7,21 (2Н, m); 7,57 (2Н, m); 7,89 (1Н, dd, J=5,9 и J=13,2); 8,65 (1Н, s).
МС (ЭСИ): 666,2.
Пример 6: 1-Циклопропил-6-фтор-7-{(RS)-3-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-3-гидроксипирролидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота:
6.i. Бензиловый эфир диаллилкарбаминовой кислоты:
Бензоилхлорид (15,5 мл) по каплям прибавляют в течение 30 мин к раствору диаллиламина (12,3 мл) и ТЭА (21 мл) в ДХМ (100 мл) при температуре 0°С. Реакционную смесь перемешивают затем при КТ в течение 16 ч. Остаток, полученный после обработки (ДХМ), очищают с помощью хроматографии (гексан/ЭА в соотношении 95:5), получая 20,71 г (88% выход) бесцветной жидкости.
1Н ЯМР (ДМСОd6; δ м.д.): 3,83 (4Н, dt, J=1 и J=6); 5,05-5,18 (6H, m); 5,70-5,86 (2Н, m); 7,27-7,48 (5H, m).
6.ii. Бензиловый эфир 2,5-дигидропиррол-1-карбоновой кислоты:
Бензилиден-бис(трициклогексилфосфин)дихлоррутений (5 г) прибавляют к раствору промежуточного соединения (6.i) (17,56 г) в ДХМ (1,5 л) при КТ в атмосфере азота. Реакционную смесь перемешивают затем при температуре 40°С в течение 2 ч, после чего концентрируют в вакууме. Остаток очищают с помощью хроматографии (гексан/ЭА в соотношении 90:10), получая 14,08 г (91% выход) желтой жидкости.
1Н ЯМР (ДМСOd6; δ м.д.): 4,05-4,16 (4Н, m); 5,08 (2Н, s); 5,81-5,92 (2Н, m); 7,27-7,41 (5H, m).
6.iii. Бензиловый эфир (RS)-3-гидроксипирролидин-1-карбоновой кислоты:
1-Молярный раствор боргидрида в ТГФ (9 мл) прибавляют к раствору промежуточного соединения (6.ii) (1,81 г) в ТГФ (25 мл) при температуре 0°С в атмосфере азота. Реакционную смесь перемешивают при КТ в течение 16 ч и охлаждают до температуры 0°С. 20%-ный раствор NaOH (1,8 мл) осторожно добавляют по каплям, затем добавляют 35%-ный водный раствор перекиси водорода (1,2 мл). Смесь перемешивают при 0°С в течение 30 мин, а затем при КТ в течение 2 ч. После этого добавляют EtaO и 40%-ный водный раствор бисульфита натрия и реакционную смесь энергично перемешивают в течение 15 мин. Остаток, полученный после обработки (Et2O), очищают с помощью хроматографии (гексан/ЭА в соотношении от 5:5 до 3:7), получая 1,01 г (51% выход) бесцветного масла.
1Н ЯМР (ДМСОd6; δ м.д.): 1,67-1,82 (1Н, m); 1,82-1,96 (1Н, m); 3,16-3,25 (1Н, m); 3,28-3,44 (3Н, m); 4,20-4,29 (1Н, расширенный); 4,92 (1Н, d, J=3); 5,06 (2H, s); 7,27-7,41 (5H, m).
6.iv. Бензиловый эфир 3-оксопирролидин-1-карбоновой кислоты:
Раствор промежуточного соединения (6.iii) (1,10 г) в ДХМ (8 мл) охлаждают до температуры 0°С и прибавляют по каплям ДИПЭА (2,5 мл), а затем раствор комплекса триоксид серы/пиридин (1,79 г) в ДМСО (6,5 мл). Реакционную смесь перемешивают при 0°С в течение 1 ч и гасят водой (6 мл). Водный слой экстрагируют смесью Et2O/гексан (в соотношении 1:1, трижды по 5 мл) и объединенные органические слои концентрируют в вакууме. Остаток, полученный после обработки (Et2O/гексан в соотношении 1:1), очищают с помощью хроматографии (гексан/ЭА в соотношении 5:5), получая 1,05 г (96% выход) желтоватого масла.
1Н ЯМР (ДМСОв6; δ м.д.): 2,48-2,61 (2H, m); 3,61-3,80 (4Н, m); 5,09 (2H, s); 7,27-7,41 (5H, m).
6.v. Бензиловый эфир 3-метиленпирролидин-1-карбоновой кислоты:
t-BuOK (617 мг) прибавляют одной порцией к суспензии бромида метилтрифенилфосфония (1,98 г) в ТГФ (10 мл) при КТ в атмосфере азота. Желтую суспензию перемешивают при КТ в течение 1 ч, а затем охлаждают до температуры -10°С, после чего прибавляют по каплям раствор промежуточного соединения (6.iv) (1,05 г) в ТГФ (2 мл) в течение 10 мин и реакционную смесь оставляют самопроизвольно нагреваться при КТ в течение 2 ч. Реакцию затем гасят добавлением насыщенного водного раствора NH4Cl (1 мл) и разбавляют этилацетатом. Остаток, полученный после обработки (ЭА), очищают с помощью хроматографии (гексан/ЭА в соотношении 90:10), получая 633 мг (64% выход) желтоватой жидкости.
1Н ЯМР (ДМСОd6; δ м.д.): 2,48-2,61 (2Н, m); 3.36-3,53 (2Н, m); 3,84-4,01 (2Н, m); 4,97-5,03 (2Н, m); 5,08 (2Н, s); 7,27-7,41 (5Н, m).
6.vi. Бензиловый эфир 1-окса-5-аза-спиро[2,4]гептан-5-карбоновой кислоты:
Раствор промежуточного соединения (6.v) (7,21 г) в ДХМ (400 мл) обрабатывают м-ХПБК (20,1 г) и NaHCO3 (22,3 г) при КТ. Реакцию перемешивают при КТ в течение 2 ч, разбавляют ДХМ (200 мл) и переносят в раствор Na2SO3 (45 г) в воде (400 мл). Затем смесь перемешивают в течение 10 мин, после чего отделяют органический слой. Остаток, полученный после обработки (ДХМ), очищают с помощью хроматографии (гексан/ЭА в соотношении 6:4), получая 4,37 г (56% выход) желтого масла.
1Н ЯМР (ДМСОd6; δ м.д.): 1,70-1,83 (1Н, m); 2,22-2,37 (1Н, m); 2,90-2,94 (1Н, m); 2,95-2,99 (1Н, m); 3,15 (1Н, t, J=11); 3,39-3,77 (3Н, m); 5,09 (2Н, s); 7,27-7,41 (5Н, m).
6.vii. Бензиловый эфир (RS)-3-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-3-гидроксипирролидин-1-карбоновой кислоты:
К2СО3 (274 мг) прибавляют к суспензии промежуточного соединения (1.i) (300 мг) и промежуточного соединения (6.vi) (338 мг) в ДМФ (3 мл). Реакционную смесь перемешивают при температуре 80°С в течение 3 ч, после чего растворитель удаляют в вакууме. Остаток, полученный после обработки (ДХМ), очищают с помощью хроматографии (ДХМ/МеОН в соотношении 95:5), получая 531 мг (87% выход) бежевой пены.
1Н ЯМР (ДМСОd6; δ м.д.): 1,80-1,92 (1Н, m); 1,96-2,08 (1Н, m); 3,32-3,59 (5Н, m); 3,66 (1Н, ddd, J=3, J=6 и J=13); 3,80 (1Н, dd, J=6 и J=9); 3,97-4,09 (3Н, m); 4,64-4,72 (1Н, m); 5,07 (2Н, s); 5,19 (1Н, t, J=6); 5,23 (1Н, s); 7,18-7,23 (2Н, m); 7,27-7,38 (5Н, m); 7,57 (1Н, dd, J=2 и J=14).
МС (ЭСИ): 460,9.
6.viii. (R)-3-[3-Фтор-4-((RS)-3-гидроксипирролидин-3-илметокси)фенил]-5-гидроксиметилоксазолидин-2-он:
Раствор промежуточного соединения (6.vii) (259 мг) в смеси ТГФ/МеОН (в соотношении 1:1; 20 мл) гидрируют над 10%-ным Pd/C (60 мг) в течение 20 ч при КТ. Реакционную смесь затем концентрируют в вакууме, переносят в смесь ДХМ/МеОН в соотношении 90:10 (20 мл) и перемешивают при КТ в течение 30 мин. Катализатор отфильтровывают и фильтрат концентрируют в вакууме, получая 184 мг (100% выход) оранжевой пены.
МС (ЭСИ): 327,3.
6.ix. 1-Циклопропил-6-фтор-7-{(RS)-3-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-3-гидроксипирролидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота:
Раствор промежуточного соединения (6.viii) (226 мг) и комплекса 7-хлор-1-циклопропил-6-фтор-1,4-дигидро-4-оксо-3-хинолинкарбоновой кислоты с бордиацетатом (270 мг; получен согласно WO 88/07998) в N-МП (5 мл) обрабатывают ДИПЭА (120 мкл) и перемешивают при температуре 60°С в течение 2 ч. Реакционную смесь затем концентрируют в вакууме и остаток переносят в 5-молярный раствор HCl в МеОН (2 мл). После этого раствор перемешивают при КТ в течение 1 ч, концентрируют в вакууме и остаток очищают с помощью хроматографии (ДХМ/МеОН/АсОН в соотношении от 95:4:1 до 90:9:1). Пенистый остаток переносят в МеОН (2 мл), перемешивают в течение 1 ч и фильтруют. Кристаллы отделяют и высушивают в вакууме, получая 23 мг (6% выход) бежевого твердого вещества.
1Н ЯМР (ДМСОd6; δ м.д.): 1,10-1,34 (4Н, m); 1.98-2,10 (1Н, m); 2.14-2,26 (1Н, m); 3,48-3,70 (3Н, m); 3,71-3,89 (5Н, m); 4,05 (1Н, t, J=9); 4,09-4,18 (2H, m); 4,66-4,74 (1Н, m); 5,19 (1Н, t, J=6); 5,40 (1Н, s); 7,09 (1Н, d, J=8); 7,18-7,31 (2H, m); 7,59 (1Н, dd, J=2 и J=14); 7,82 (1Н, d, J=14); 8,59 (1Н, s); 15,52 (1Н, s).
МС (ЭСИ): 572,3.
Пример 7: 1-Циклопропил-6-фтор-7-{(RS)-3-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-3-гидроксипирролидин-1-ил}-8-метокси-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота:
Это соединение получают в виде желтого твердого вещества с 52%-ным выходом, исходя из промежуточного соединения (6.viii) (85 мг), комплекса 1-циклопропил-6,7-дифтор-1,4-дигидро-8-метокси-4-оксо-3-хинолинкарбоновой кислоты с бордиацетатом (100 мг; получают согласно Sakurai et al., Bioorg. Med. Chem. Lett. (1998), 8, 2185-2190) и ДИПЭА (43 мкл) и применяя методику примера 6, стадия 6.ix. Пенистый остаток перемешивают в ЭА (5 мл) и высушивают.
МС (ЭСИ): 602,2.
Пример 8: 1-Циклопропил-6-фтор-7-{(RS)-3-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]пирролидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота:
8.i. Бензиловый эфир (RS)-3-гидроксиметилпирролидин-1-карбоновой кислоты:
Это соединение получают в виде бесцветного масла с 68%-ным выходом, исходя из промежуточного соединения (6.v) (630 мг) и 1-молярного раствора борана в ТГФ (9 мл), и применяя методику примера 6, стадия 6.iii.
1Н ЯМР (ДМСОd6; δ м.д.): 1,51-1,71 (1Н, m); 1,79-1,97 (1Н, m); 2,19-2,35 (1Н, m); 3,00-3,15 (1Н, m); 3,19-3,50 (5Н, m); 4,65 (1Н, t, J=5); 5,05 (2H, s); 7,27-7,40 (5Н, m).
МС (ЭСИ): 235,9.
8.ii. Бензиловый эфир (RS)-3-{4-[(R)-5-(трет-бутилдиметилсиланилоксиметил)-2-оксооксазолидин-3-ил]-2-фторфеноксиметил}пирролидин-1-карбоновой кислоты:
Суспензию промежуточного соединения (8.i) (456 мг), промежуточного соединения (2.ii) (630 мг) и РРh3 (726 мг) в ТГФ (8 мл) обрабатывают ДИАД (0,55 мл), добавляя его по каплям в течение 2 ч при КТ. Реакционную смесь далее перемешивают при КТ в течение 2 ч, а затем концентрируют в вакууме. После этого остаток очищают с помощью хроматографии (гексан/ЭА в соотношении от 7:3 до 6:4), получая 966 мг (94% выход) желтого масла.
1Н ЯМР (ДМСОd6; δ м.д.): 0,04 (6Н, s); 0,79 (9Н, s); 1,65-1,82 (1Н, m); 1,93-2,08 (1Н, m); 2,56-2,74 (1Н, m); 3,14-3,25 (1Н, m); 3,30-3,59 (3Н, m); 3,69-3,78 (1Н, m); 3,74 (1Н, dd, J=3 и J=12); 3,87 (1Н, dd, J=3 и J=12); 3,95-4,12 (3Н, m); 4,70-4,83 (1Н, m); 5,05-5,08 (2H, m); 7,16-7,21 (2H, m); 7,27-7,38 (5Н, m); 7,56 (1Н, dd, J=2 и J=14).
МС (ЭСИ): 559,3.
S.iii. Бензиловый эфир (RS)-3-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил1пирролидин-1-карбоновой кислоты:
Раствор промежуточного соединения (8.ii) (200 мг) в диоксане (1 мл) обрабатывают 6-молярным раствором HCl в диоксане (0,30 мл) при КТ. Реакционную смесь перемешивают при КТ в течение 2 ч, а затем концентрируют без досушивания. Остаток разбавляют ДХМ, промывают насыщенным водным раствором NaHCO3 и обрабатывают (ДХМ). Сырой продукт затем очищают с помощью ускоренной хроматографии (ДХМ/МеОН в соотношении от 98:2 до 96:4), получая 258 мг (81% выход) желтоватого масла.
1Н ЯМР (ДМСОd6; δ м.д.): 1,66-1,82 (1Н, m); 1,96-2,10 (1Н, m); 2,58-2,74 (1Н, m); 3,14-3,26 (1Н, m); 3,28-3,38 (1Н, m); 3,39-3,61 (3Н, m); 3,66 (1Н, ddd, J=4, J=6 и J=13); 3,80 (1Н, dd, J=б и J=9); 3,94-4,08 (3Н, m); 4,62-4,71 (1Н, m); 5,05 (2Н, s); 5,19 (1Н, t, J=6); 7,18-7,21 (2H, m); 7,27-7.38 (5Н, m); 7,57 (1Н, dd, J=2 и J=14).
МС (ЭСИ): 445,2.
8.iv. (R)-3-[3-Фтор-4-((RS)-1-пирролидин-3-илметокси)фенил]-5-гидроксиметилоксазолидин-2-он:
Это соединение получают с 100%-ным выходом в виде розоватого твердого вещества гидрированием промежуточного соединения (8.in) (230 мг) над 10%-ным Pd/C (72 мг) с применением методики примера 6, стадия 6.viii.
МС (ЭСИ): 311,3.
8.v. 1-Циклопропил-6-фтор-7-{(RS)-3-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]пирролидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота:
Это соединение получают с 17%-ным выходом в виде желтого твердого вещества, исходя из промежуточного соединения (8.iv) (67 мг), комплекса 7-хлор-1-циклопропил-6-фтор-1,4-дигидро-4-оксо-хинолинкарбоновой кислоты с бордиацетатом (80 мг; получен согласно WO 88/07998) и ДИПЭА (36 мкл) и применяя методику примера 6, стадия 6.ix. Сырой продукт очищают с помощью хроматографии (ДХМ/МеОН/АсОН в соотношении от 98:1:1 до 94:5:1) пенистый остаток перемешивают в МеОН (1 мл).
1Н ЯМР (ДМСОd6; δ м.д.): 1,10-1,34 (4Н, m); 1,85-2,01 (1Н, m); 2,14-2,28 (1Н, m); 2,75-2,90 (1Н, m); 3,48-3,60 (2H, m); 3,60-3,88 (6Н, m); 4,05 (1Н, t, J=9); 4,09-4,18 (2Н, m); 4,63-4,72 (1H, m); 5,19 (1H, t, J=6); 7,09 (1H, d, J=8); 7,18-7,29 (2Н, m); 7,58 (1H, dd, J=3 и J=14); 7,80 (1H, d, J=14); 8,58 (1H, s); 14,48 (1H, s).
MC (ЭСИ): 556,3.
Пример 9: 1-Циклопропил-6-фтор-7-{(RS)-3-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]пирролидин-1-ил}-8-метокси-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота:
Это соединение получают в виде желтого твердого вещества с 12%-ным выходом, исходя из промежуточного соединения (8.iv) (65 мг), комплекса 1-циклопропил-6,7-дифтор-1,4-дигидро-8-метокси-4-оксо-3-хинолинкарбоновой кислоты с диацетатом бора (80 мг; получен согласно Sakurai et al., Bioorg. Med. Chem. Lett. (1998), 8, 2185-2190) и ДИПЭА (27 мкл), применяя методику примера 6, стадия 6.ix. Сырой продукт очищают с помощью хроматографии (ДХМ/МеОН/АсОН в соотношении от 98:1:1 до 94:5:1) и перемешивая пенистый остаток в смеси ЭА/Et2O (в соотношении 2:1; 1,5 мл).
1Н ЯМР (ДMCOd6; δ м.д.): 0,90-1,18 (4Н, m); 1,76-1,93 (1H, m); 2,10-2,24 (1H, m); 2,70-2,81 (1H, m); 3,57 (3Н, s); 3,56-3,83 (7H, m); 3,99-4,20 (4Н, m); 4,62-4,73 (1H, m); 5,19 (1H, t, J=6); 7,18-7,29 (2Н, m); 7,58 (1H, dd, J=3 и J=14); 7,68 (1H, d, J=14); 8,64 (1H, s); 15,13 (1H, s).
MC (ЭСИ): 586,3.
Пример 10: 1-Циклопропил-6-фтор-7-{4-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-4-фосфоноксипиперидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота:
10.i. Бензиловый эфир 7-(4-{4-[5-(трет-бутилдиметилсиланилоксиметил)-2-оксооксазолидин-3-ил]-2-фторфеноксиметил}-4-гидроксипиперидин-1-ил)-1-циклопропил-6-фтор-4-оксо-1,4-дигидрохинолин-3-карбоновой кислоты:
Имидазол (67 мг) и ТБДМССl (162 мг) добавляют к раствору промежуточного соединения (4.i) (600 мг) в ДМФ (6 мл). Раствор перемешивают при КТ в течение 6 ч. Растворитель затем выпаривают при пониженном давлении, а остаток обрабатывают (ДХМ) и очищают с помощью хроматографии (ДХМ/МеОН; в соотношении 95:5), получая 544 мг (75,6% выход) желтого твердого вещества.
1Н ЯМР (ДМСОd6; δ м.д.): 0,03 (6Н, s); 0,78 (9Н, s); 1,10 (2Н, m); 1,22 (2H, m); 1.70 (2H, m); 1,92 (2H, m); 3,2 (2H, m); 3,45 (2H, m); 3.70 (3Н, m); 3,83-3,88 (1H, dd, J=2,6 и J=12); 3,89 (2H, s); 4,07 (1H, t, J=9); 4,73 (1H, m); 4,82 (1H, s); 5,26 (2H, s); 7,20 (2H, m); 7,28-7,58 (7H, m); 7,75 (1H, d, J=13,5); 8,46 (1H, s).
MC (ЭСИ): 790,5.
10.ii. Бензиновый эфир 7-(4-(бис-бензилоксифосфорилокси)-4-{4-[(R)-5-(треуи-бутилдиметилсиланилоксиметил)-2-оксооксазолидин-3-ил]-2-фторфеноксиметил}пиперидин-1-ил)-1-циклопропил-6-фтор-4-оксо-1,4-дигидрохинолин-3-карбоновой кислоты:
Суспензию промежуточного соединения (10.i) (523 мг) в ДХМ (4 мл) последовательно обрабатывают 4,5-цианоимидазолом (140 мг) и дибензил-N,N-диизопропилфосфорамидатом (392 мкл). После обработки в течение 1 ч при КТ реакционную смесь обрабатывают 190 мкл трет-бутилгидропероксида (70%-ный водный раствор), затем перемешивают при КТ в течение 1 ч. Растворитель выпаривают при пониженном давлении, после чего остаток обрабатывают (ДХМ) и очищают с помощью хроматографии (ДХМ/МеОН; в соотношении 97,5:2,5). Образовавшееся твердое вещество (369 мг) перемешивают с эфиром (5 мл), получая 287 мг (41% выход) желтого твердого вещества.
1H ЯМР (ДМСОd6; δ м.д.): 0,02 (6Н, s); 0,77 (9Н. m); 1,07 (2H, m); 1.19 (2H, dd, J=1,2 и J=6,4), 2,07 (2H, t расширенный, J=9); 2,29 (2H, d, J=13,5); 3,18 (2H, t, J=11); 3.49 (2H, m); 3,61 (1H, m); 3.73 (2H, m); 3,85 (1H, dd, J=2,6 и J=12); 4,07 (1H, t, J=9,1); 4,38 (2H, s); 4,73 (1H, m); 5,02 (4Н, d, J=7,6); 5.26 (2H, s); 7,17 (2H, m); 7,42 (17Н, m); 7,77 (1H, d, J=13,2); 8,46 (1H, s).
МС(ЭСИ): 1050,3.
10.iii. Бензиловый эфир 7-{4-[4-((R)-5-ацетоксиметил-2-оксооксазолидин-3-ил)-2-фторфеноксиметил]-4-фосфонооксипиперидин-1-ил}-1-циклопропил-6-фтор-4-оксо-1,4-дигидрохинолин-3-карбоновой кислоты:
Суспензию промежуточного соединения (10.ii) (200 мг) в АсОН (1,5 мл) обрабатывают HBr (1 мл; 33%-ный раствор в АсОН), затем перемешивают при КТ в течение 2 ч, после чего реакционную смесь переносят в холодную воду (10 мл). После обработки (ДХМ) остаток перемешивают с эфиром (30 мл). Образовавшееся желтое твердое вещество отделяют с помощью фильтрования (144,5 мг; 95% выход).
МС (ЭСИ): 798,1.
10.iv. 1-Циклопропид-6-фтор-7-{4-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-4-фосфонооксипиперидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота:
Раствор промежуточного соединения (10.iii) (144,5 мг) в смеси диоксан/МеОН/вода (3 мл; в соотношении 1:1:1) обрабатывают ацетатом натрия (29 мг) и гидрируют над Pd/C (10%-ный, 10 мг) в течение 10 ч при КТ. Катализатор отфильтровывают и промывают водой (5 мл). Фильтрат выпаривают при пониженном давлении, переносят в воду (1 мл) и обрабатывают 1-нормальным раствором HCl (400 мкл) до тех пор, пока не выпадет осадок. Твердое вещество отделяют фильтрованием, снова растворяют в МеОН (10 мл) и обрабатывают К2СО3 (56,25 мг). После перемешивания смеси при КТ в течение 30 мин растворитель выпаривают при пониженном давлении, а остаток растворяют в воде (4 мл) и обрабатывают 1-нормальным раствором HCl (814 мкл) до тех пор, пока не выпадет осадок. Твердое вещество отделяют фильтрованием, промывают водой и высушивают при пониженном давлении, получая 105 мг (82% выход) желтого твердого вещества.
1Н ЯМР (ДМСОd6; δ м.д.): 1,13-1,30 (4Н, m); 1,95-2,11 (2Н, t расширенный, J=10); 2,24 (2Н, d, J=12,5); 3,59 (3Н, t, J=10); 3,5-3,69 (3Н, m); 3,74-3,87 (2Н, m); 4,02 (1Н, t, J=9); 4,31 (2Н, m); 4,66 (1Н, m); 5,17 (1Н, m); 7,19 (2Н, m); 7,56 (2Н, m); 7,87 (1Н, d, J=13,2); 8,63 (1Н, s).
МС (ЭСИ): 666,2.
Пример 11: 1-Этил-6-фтор-7-{4-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил1пиперидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота:
Это соединение получают аналогично получению примера 1, стадия 1.iv, исходя из промежуточного соединения (2.iv) (250 мг) и комплекса 7-хлор-1-этил-6-фтор-1,4-дигидро-4-оксо-3-хинолинкарбоновой кислоты с бором (280 мг; получен согласно WO 87/03595). Остаток, полученный после выпаривания растворителя при пониженном давлении, растворяют в воде (100 мл) и смеси ДХМ/МеОН (500 мл; в соотношении 9:1). Органическую фазу затем высушивают над MgSO4 и фильтруют. Фильтрат выпаривают и перемешивают в смеси ДХМ/МеОН (10 мл; в соотношении 9:1). Желтое твердое вещество выделяют с помощью фильтрования (171 мг; 44% выход).
1Н ЯМР (ДМСОd6; δ м.д.): 1,45 (3Н, t, J=7); 1,57 (2Н, dq, J=4,7 и J=9); 1.95 (2Н, d, J=12,5); 2,01-2,09 (1H, m); 3,00 (2Н, m); 3,62, (3Н, dq, J=4 и J=13,2), 3,73-3,78 (1H, m); 3,80 (1H, dd, J=6,5 и J=9); 3,99-4,07 (3Н, m); 4,49 (2Н, q, J=7), 4,65 (1H, m); 7,16 (3Н, m); 7,47-7,54 (1H, m); 7,88 (1H, d, J=13,8); 8,83 (1H, s),
МС (ЭСИ): 558,2.
Пример 12: Гидрохлорид 7-(4-{4-[(R)-5-((S)-2-аминопропионилоксиметил)-2-оксооксазолидин-3-ил]-2-фторфеноксиметил}пиперидин-1-ил)-1-циклопропил-6-фтор-4-оксо-1,4-дигидрохинолин-3-карбоновой кислоты:
12.i. Бензиловый эфир 1-циклопропил-6-фтор-7-{4-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил1пиперидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновой кислоты:
Раствор соединения примера 2 (600 мг) в ДМФ (10 мл) обрабатывают К2СО3 (155 мг) и BnBr (160 мкл) и перемешивают при температуре 80°С в течение 24 ч. Растворитель выпаривают при пониженном давлении, а остаток обрабатывают (ДХМ). Затем остаток смешивают с эфиром (100 мл) и образовавшиеся кристаллы отделяют фильтрованием, получая 612 мг (90,6% выход) грязно-белого твердого вещества.
1Н ЯМР (ДМСОd6; δ м.д.): 1,08-1,27 (4Н, m); 1,45-1,60 (2H, m); 1,88-2,05 (3Н, m); 2,89 (2Н, t, J=10,8); 3,50-3,57 (1H, m); 3,62-3,71 (4H, m); 3,78 (1H, dd, J=6,2 и J=8,8); 3,98 (2Н, d, J=6,2); 4,03 (1H, t, J=8,8); 4,62-4,71 (1H, m); 5,17 (1H, t, J=5,9); 5,25 (2Н, s); 7,19-7,22 (2Н, m); 7,31-7,41 (3Н, m); 7,43-7,49 (3Н, m); 7,53-7,55 (1H, dd, J=2,0 и J=13,8); 7,75(1H, d, J=13,8); 8,46 (1H, s).
МС (ЭСИ): 660,3.
12.ii. Бензиловый эфир 7-(4-{4-[(R)-5-((S)-2-трет-бутоксикарбониламинопропионилоксиметил)-2-оксооксазолидин-3-ил]-2-фторфеноксиметил}пиперидин-1-ил)-1-циклопропил-6-фтор-4-оксо-1,4-дигидрохинолин-3-карбоновой кислоты:
Это соединение (307 мг; 81% выход) получают в виде бесцветного твердого вещества аналогично получению соединения примера 4, стадия 4.ii, исходя из промежуточного соединения (12.i) (300 мг), Бок-L-Ala-OH (111 мг), ЭДК (113 мг) и ДМАП (27 мг).
1Н ЯМР (ДМСОd6; δ м.д.): 1,05-1,11 (2Н, m);, 1,17-1,26 (5Н, m); 1,32 (9H, s); 1,52 (2H, m); 1,96 (3H, m); 2,90 (2H, t, J=11); 3,59-3,72 (3H, m); 3,81 (1H, dd, J=6,7 и J=9,7); 3,94-4,00 (3H, m); 4,12 (1H, t, J=9); 4,25 (1H, dd, J=4,7 и J=11); 4,40 (1H, dd, J=2,6 и J=12,3); 4,85-4,95 (1H, m); 5.26 (2Н, s); 7,18-7,23 (2Н, m); 7,26-7,46 (7H, m); 7,75 (1H, d, J=13,5); 8,45 (1H, s).
МС (ЭСИ): 831,3.
12.iii. 7-(4-{4-[(R)-5-((S)-2-трет-Бутоксикарбониламинопропионилоксиметил)-2-оксооксазолидин-3-ил]-2-фторфеноксиметил}пиперидин-1-ил)-1-циклопропил-6-фтор-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота:
Это соединение (252 мг; 100% выход) получают в виде желтого твердого вещества аналогично получению соединения примера 4, стадия 4.iii, гидрированием промежуточного соединения (12. ii) (279 мг) над Pd/C (10%-ный, 10 мг).
1H ЯМР (ДМСОd6; δ м.д.): 1,12-1,22 (5Н, m); 1,26-1,36 (11Н, m); 1,47-1,59 (2Н, m); 1,92 (2Н, d, J=12); 1,98-2,10 (1H, m); 2,99 (2Н, t, J=12); 3,79 (4H, m); 3,97 (3H, d, J=7,6); 4,10 (1H, t, J=9); 4,26 (1H, dd, J=5,3 и J=12,6); 4,36-4,43 (1H, m); 4,84-4,96 (1H, m); 7,17-7,32 (3H, m); 7,52 (1H, d, J=12,9); 7,54 (1H, d, J=8,2); 7,88 (1H, d, J=13,5); 8,64 (1H, s).
МС (ЭСИ): 741,3.
12.iv. Гидрохлорид 7-(4-{4-[(R)-5-((S)-2-аминопропионилоксиметил)-2-оксооксазолидин-3-ил]-2-фторфеноксиметил}пиперидин-1-ил)-1-циклопропил-6-фтор-4-оксо-1,4-дигидрохинолин-3-карбоновой кислоты:
Это соединение (84 мг; 97% выход) получают в виде желтого твердого вещества аналогично получению соединения примера 4, стадия 4.iv, исходя из промежуточного соединения (12.iii) (100 мг) и 5-молярного раствора HCl в диоксане (0,5 мл).
1H ЯМР (ДМСОd6; δ м.д.): 1,13-1,32 (4H, m); 1,36 (3H, d, J=7,3); 1,46-1,61 (2Н, m); 1,92(2H, d расширенный, J=12); 1,98-2,10 (1H, m); 2,99 (2Н, t, J=12); 3,74-3,91 (5Н, m); 3,98 (2Н. d, J=6,4); 4,10-4,18 (1H, m); 4,35 (1H, dd, J=5,3 и J=12,3); 4,55 (1Н, dd, J=2,6 и J=12,3); 4,96 (1H, m); 7,19-7,24 (2H, m); 7,52-7,58 (2H, m); 7,88 (1H, d, J=13,5); 8,47 (3H, m); 8,64 (1H, s).
МС (ЭСИ): 641,2.
Пример 13: 6-Фтор-7-{4-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-4-гидроксипиперидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота:
Раствор промежуточного соединения (1.iv) (150 мг) в ДМА (10 мл) гидрируют над 20%-ным Pd(OH)2/C (100 мг) в течение 5 дней при температуре 80°С. Реакционную смесь затем концентрируют в вакууме, переносят в смесь ДХМ/МеОН в соотношении 90:10 (50 мл) и перемешивают при КТ в течение 30 мин. Катализатор отфильтровывают и фильтрат концентрируют в вакууме. Остаток переносят в МеОН (0,2 мл) и прибавляют этилацетат (2 мл). Суспензию перемешивают при КТ в течение 30 мин и фильтруют. Кристаллы отделяют и высушивают в вакууме, получая 48 мг (34% выход) желтого твердого вещества.
1H ЯМР (ДМСОd6; δ м.д.): 1,64-1,77 (2H, m); 1,82-1,98 (2H, m); 3,14-3,30 (2H, m); 3,38-3,59 (3H, m); 3,59-3,71 (1H, m); 3,78 (1H, dd, J=6 и J=9); 3,89 (2H, s); 4,03 (1H, t, J=9); 4,62-4,73 (1H, m); 4,84 (1H, s); 5,17 (1H, t, J=6); 7,16-7,23 (2H, m); 7,28 (1H, d, J=8); 7,51-7,60 (1H, m); 7,81 (1H, d, J=13); 8,79 (1H, s); 13,09 (1H, расширенный); 15,44 (1H, s),
МС (ЭСИ): 546,2.
Пример 14: 6-Фтор-7-{4-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-4-гидроксипиперидин-1-ил}-4-оксо-1,4-дигидро-[1,8]нафтиридин-3-карбоновая кислота:
Раствор промежуточного соединения (3.i) (110 мг) в ДМА (10 мл) гидрируют над 10%-ным Pd/C (35 мг) в течение 16 ч при температуре 80°С. Реакционную смесь концентрируют в вакууме, переносят в смесь ДХМ/МеОН в соотношении 90:10 (25 мл) и перемешивают при КТ в течение 30 мин. Катализатор отфильтровывают и фильтрат концентрируют в вакууме. Остаток переносят в этилацетат (2 мл), перемешивают при КТ в течение 16 ч и фильтруют. Кристаллы отделяют и высушивают в вакууме, получая 35 мг (34% выход) желтого твердого вещества.
1Н ЯМР (ДMCOd6; δ м.д.): 1,62-1,92 (4Н, m); 3,41-3,60 (3H, m); 3,60-3,69 (1H, m); 3,78 (1H, dd, J=6 и J=9); 3,86 (2H, s); 4,02 (1H, t, J=8); 4,22-4,37 (2H, m); 4,60-4,72 (1H, m); 4,95 (1H, расширенный); 5,18 (1H, расширенный); 7,13-7,23 (2Н, m); 7,50-7,59 (1H, m); 8,01 (1H, d, J=14); 8,79 (1H, расширенный); 13,26 (1H, расширенный); 15,34 (1H, расширенный).
МС (ЭСИ): 547,3.
Биологические анализы
In vitro анализ
Экспериментальные методы:
Эти анализы осуществляются в соответствие с описанием, приведенным в: "Methods for dilution Antimicrobial Susceptibility Tests for Bacteria that Grow Aerobically, 4th ed.; Approved standard: NCCLS Document M7-A4; National Committee for Clinical Laboratory Standards: Villanova, PA, USA, 1997". Минимальные концентрации ингибирования (MICs; мг/л) определялись в катион-регулируемой питательной среде Mueller-Hinton Broth (BBL) с использованием метода микроразбавления согласно указаниям NCCLS (National Committee for Clinical Laboratory Standards. Methods for Dilution Antimicrobial Susceptibility). Величина рН тестируемой среды составляла 7,2-7,3.
В особом случае, где соединение, подлежащее тестированию, является соединением формулы IPDG, в которой, по крайней мере, один из R1 и R2 представляет собой группу ОРО3Н2, тестирование проводили в присутствии человеческой щелочной фосфатазы (концентрация: 1 ед./мл).
В особом случае, где соединение, подлежащее тестированию, является соединением формулы IPDG, в которой R1 представляет собой группу OCOR5, тестирование проводили в присутствии 50% человеческой сыворотки. Однако это не является необходимым для соединений примеров 4 и 12, которые уже проявляют значительную активность в отсутствие человеческой сыворотки.
Результаты:
Соединения всех вышеприведенных примеров протестированы относительно воздействия на грамположительные и грамотрицательные бактерии. Типичный антибактериальный спектр приведен в таблице ниже (MIC в мг/л).
Кроме того, следующие результаты были получены для соединений, соответствующих формуле ID, воздействующих на S.aureus A798 (MIC в мг/л):
Дополнительно, соединение примера 11 имеет MIC 8 мг/л против Е. faecalis 29212 бактерии.
Более того, в физиологической среде (включая фосфатазы и эстеразы) соединения формулы IPDG быстро превращаются в соответствующие соединения формулы ID. Действительно:
- соединения примеров 5 и 10 в присутствии человеческой щелочной фосфатазы имеют значения MIC соответственно 0,25 и 0,5 мг/л против S.aureus A798, тогда как те же соединения имеют значения MIC соответственно >16 мг/л и 16 мг/л против S.aureus A798, когда фосфатаза отсутствует; и
- соединения примеров 4 и 12, даже в отсутствие человеческой сыворотки, каждое имеет MIC 0,5 мг/л против S.aureus A798.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ 5-ГИДРОКСИМЕТИЛОКСАЗОЛИДИН-2-ОНА ДЛЯ ЛЕЧЕНИЯ БАКТЕРИАЛЬНЫХ КИШЕЧНЫХ ЗАБОЛЕВАНИЙ | 2009 |
|
RU2527769C2 |
| ПРОИЗВОДНЫЕ 5-АМИНОЦИКЛИЛМЕТИЛОКСАЗОЛИДИН-2-ОНА | 2008 |
|
RU2492169C2 |
| ОКСАЗОЛИДИНИЛОВЫЕ АНТИБИОТИКИ | 2009 |
|
RU2516701C2 |
| ТРИЦИКЛИЧЕСКИЕ ОКСАЗОЛИДИНОНОВЫЕ АНТИБИОТИЧЕСКИЕ СОЕДИНЕНИЯ | 2009 |
|
RU2530884C2 |
| АНТИБИОТИЧЕСКИЕ ПРОИЗВОДНЫЕ 2-ОКСО-ОКСАЗОЛИДИН-3, 5-ДИИЛА | 2012 |
|
RU2616609C2 |
| ИНГИБИТОРЫ ТИРОЗИНКИНАЗЫ БРУТОНА | 2010 |
|
RU2542585C2 |
| ПРИМЕНЕНИЕ ОКСАЗОЛИДИНОН-ХИНОЛИНОВЫХ ГИБРИДНЫХ АНТИБИОТИКОВ ДЛЯ ЛЕЧЕНИЯ СИБИРСКОЙ ЯЗВЫ И ДРУГИХ ИНФЕКЦИЙ | 2004 |
|
RU2351335C2 |
| СПИРОСОЕДИНЕНИЕ ИЛИ ЕГО СОЛИ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ, ОБЛАДАЮЩАЯ ПРОТИВОМИКРОБНОЙ АКТИВНОСТЬЮ | 1989 |
|
RU2094432C1 |
| ПРОИЗВОДНЫЕ 2-ГИДРОКСИЭТИЛ-1Н-ХИНОЛИН-2-ОНА И ИХ АЗАИЗОСТЕРИЧЕСКИЕ АНАЛОГИ С АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТЬЮ | 2010 |
|
RU2540862C2 |
| КОНДЕНСИРОВАННЫЕ ПРОИЗВОДНЫЕ ИМИДАЗОЛА И ПИРАЗОЛА В КАЧЕСТВЕ МОДУЛЯТОРОВ АКТИВНОСТИ TNF | 2014 |
|
RU2687093C1 |
Изобретение относится к соединениям общей формулы I, где R1 представляет собой ОН, ОРО3Н2 или OCOR5; R2 представляет собой Н, ОН или ОРО3Н2; А представляет собой N или CR6; R3 представляет собой фтор; R4 представляет собой Н, С1-3алкил или С3-6циклоалкил; R5 представляет собой остаток аланина; R6 представляет собой Н, C1-6алкоксигруппу или галоген; и n=0 или 1; и к фармацевтически приемлемым солям соединений формулы I. Также изобретение относится к фармацевтической композиции, обладающей антибактериальной активностью, и к применению соединений формулы I для получения лекарственного средства, предназначенного для профилактики или лечения бактериальных инфекций. Технический результат - соединения формулы I, обладающие антибактериальной активностью. 3 н. и 11 з.п. ф-лы, 2 табл., 14 пр.
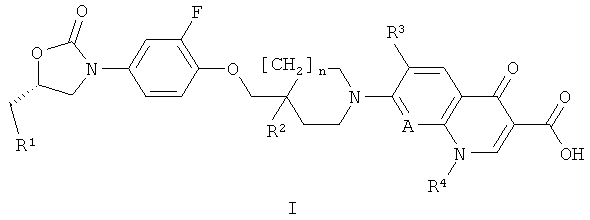
1. Соединение формулы I
 ,
,
где R1 представляет собой ОН, ОРО3Н2 или OCOR5;
R2 представляет собой Н, ОН или ОРО3Н2;
А представляет собой N или CR6;
R3 представляет собой фтор;
R4 представляет собой Н, C1-3алкил или С3-6циклоалкил;
R5 представляет собой остаток аланина;
R6 представляет собой Н, С1-6алкоксигруппу или галоген; и
n=0 или 1;
или фармацевтически приемлемая соль такого соединения.
2. Соединение формулы I по п.1, которое представляет собой соединение формулы ID
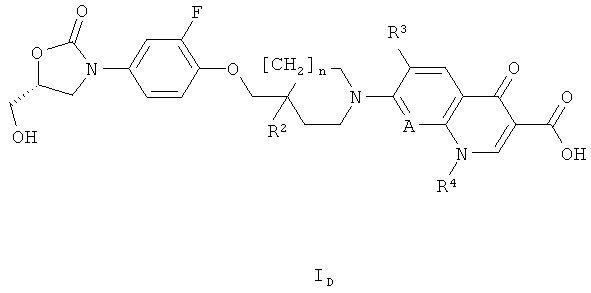 ,
,
где R2 представляет собой Н или ОН;
А представляет собой N или CR6;
R3 представляет собой фтор;
R4 представляет собой Н, С1-3алкил или С3-6циклоалкил;
R6 представляет собой Н или С1.6алкоксигруппу; и
n=0 или 1;
или фармацевтически приемлемая соль такого соединения.
3. Соединение формулы I по одному из пп.1 или 2, где R2 представляет собой ОН;
или фармацевтически приемлемая соль такого соединения.
4. Соединение формулы I по п.1 или 2, где n=0;
или фармацевтически приемлемая соль такого соединения.
5. Соединение формулы I по п.1 или 2, где n=1;
или фармацевтически приемлемая соль такого соединения.
6. Соединение формулы I по п.1 или 2, где А обозначает CR6, R6 представляет собой Н или С1-6алкоксигруппу;
или фармацевтически приемлемая соль такого соединения.
7. Соединение формулы I по п.6, где А обозначает CR6, R6 представляет собой Н или метокси;
или фармацевтически приемлемая соль такого соединения.
8. Соединение формулы I по п.1, где R4 обозначает циклоалкил; или фармацевтически приемлемая соль такого соединения.
9. Соединение по п.1, которое выбирают из следующих соединений:
1-циклопропил-6-фтор-7-{4-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-4-гидроксипиперидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-7-{4-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]пиперидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-7-{4-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-4-гидроксипиперидин-1-ил}-4-оксо-1,4-дигидро-[1,8]нафтиридин-3-карбоновая кислота;
7-(4-{4-[(R)-5-((S)-2-аминопропионилоксиметил)-2-оксооксазолидин-3-ил]-2-фторфеноксиметил}-4-гидроксипиперидин-1-ил)-1-циклопропил-6-фтор-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-7-{4-[2-фтор-4-((R)-2-оксо-5-фосфоноксиметилоксазолидин-3-ил)феноксиметил]-4-гидроксипиперидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-7-{(R)-3-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-3-гидроксипирролидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-7-{(S)-3-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-3-гидроксипирролидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-7-{(S)-3-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-3-гидроксипирролидин-1-ил}-8-метокси-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-7-{(S)-3-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-3-гидроксипирролидин-1-ил}-8-метокси-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-7-{(R-3-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]пирролидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-7-{(S)-3-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]пирролидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-7-{(R)-3-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]пирролидин-1-ил}-8-метокси-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-7-{(S)-3-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]пирролидин-1-ил}-8-метокси-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-7-{4-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-4-фосфонооксипиперидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
1-этил-6-фтор-7-{4-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]пиперидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
7-(4-{4-[(R)-5-((S)-2-аминопропионилоксиметил)-2-оксооксазолидин-3-ил]-2-фторфеноксиметил}пиперидин-1-ил)-1-циклопропил-6-фтор-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
6-фтор-7-{4-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-4-гидроксипиперидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
6-фтор-7-{4-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-4-гидроксипиперидин-1-ил}-4-оксо-1,4-дигидро-[1,8]нафтиридин-3-карбоновая кислота;
или фармацевтически приемлемая соль такого соединения.
10. Соединение по п.9, которое представляет собой 1-циклопропил-6-фтор-7-{4-[2-фтор-4-((R)-5-гидроксиметил-2-оксооксазолидин-3-ил)феноксиметил]-4-гидроксипиперидин-1-ил}-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота;
или фармацевтически приемлемая соль такого соединения.
11. Соединение формулы I по п.1 или его фармацевтически приемлемая соль в качестве лекарственного средства, обладающего антибактериальной активностью.
12. Фармацевтическая композиция, обладающая антибактериальной активностью, содержащая в качестве активного компонента соединение формулы I по п.1 или его фармацевтически приемлемую соль, и, по крайней мере, один терапевтически инертный наполнитель.
13. Применение соединения формулы I по п.1 или его фармацевтически приемлемой соли для получения лекарственного средства, предназначенного для профилактики или лечения бактериальных инфекций.
14. Соединение формулы I по п.1 или его фармацевтически приемлемая соль для профилактики или лечения бактериальных инфекций.
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Способ получения производных 3-( @ -алкилсульфонилфенил)оксазолидинона или их фармацевтически приемлемых кислотно-аддитивных солей | 1982 |
|
SU1156597A3 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| АВТОМАТИЧЕСКАЯ ТЕЛЕФОННАЯ СТАНЦИЯ | 1927 |
|
SU7157A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
Авторы
Даты
2012-06-20—Публикация
2007-11-09—Подача