Область техники, к которой относится изобретение
Настоящее изобретение представляет собой способ получения неочищенной ароматической дикарбоновой кислоты, которая предпочтительна для применения в гидрогенизационной очистке при получении ароматической дикарбоновой кислоты высокой очистки посредством гидрогенизационной очистки после получения неочищенной ароматической дикарбоновой кислоты посредством жидкофазного окисления диалкилированного ароматического углеводорода с использованием газа, содержащего кислород.
Конкретно, способ получения ароматической дикарбоновой кислоты жидкофазным окислением относится к составу катализатора жидкофазного окисления и условиям реакции, способствующим получению неочищенной ароматической дикарбоновой кислоты с высокой эффективностью при жидкофазном окислении, выявляющем производительность катализатора гидрирования при осуществлении гидрогенизационной очистки в виде водного раствора неочищенной ароматической дикарбоновой кислоты, полученной более экономичным способом.
Предпосылки создания изобретения
Способ получения ароматической дикарбоновой кислоты из диалкилированного ароматического углеводорода, применяемого в качестве исходного материала, такого, как пара-ксилол или мета-ксилол, путем осуществления жидкофазного окисления кислородсодержащим газом в присутствии катализатора, включающего кобальт (Со), марганец (Mn) и бром (Br) в растворителе - уксусной кислоте - используется в промышленности в крупных масштабах и находит практическое применение.
Поскольку ароматическая дикарбоновая кислота, полученная указанным способом, включает промежуточные продукты окисления, например 4-карбоксибензальдегид (4-КБА) и 3-карбоксибензальдегид (3-КБА), а также окрашенные продукты, например дифенилы и флуореноны, ароматическую дикарбоновую кислоту растворяют в воде, проводят реакцию гидрирования на катализаторе на основе благородного металла, нанесенного на углеродный носитель, с целью удаления или снижения содержания примесей, при этом получают очищенную ароматическую дикарбоновую кислоту, предназначенную для использования в качестве исходного вещества для получения ароматических полиэфиров.
Этот способ предназначен для превращения промежуточного продукта и окрашенного материала, который не подходит для получения ароматических полиэфиров, предназначенных, например, для получения волокон, в легко растворимый в воде материал посредством реакции гидрирования с последующим удалением гидрированных примесей растворением их в водном растворителе с кристаллизацией и выделением ароматической дикарбоновой кислоты.
С другой стороны, было проведено изучение условий реакции и состава катализатора в жидкофазной реакции окисления кислородсодержащим газом в растворителе - уксусной кислоте, чтобы получить высокочистую ароматическую дикарбоновую кислоту, способную к прямой полимеризации с гликолями без проведения дополнительной стадии очистки в реакции гидрирования.
Как показано в патенте 1 (JP-B № Sho 45-36732), патентном документе 2 (JP-B № Sho 53-30700) и патентном документе 3 (JP-B № Sho 56-21015), они представляют собой разработанные до настоящего времени способы улучшения температуры реакции и состава катализатора для реакции окисления и получения высокочистой ароматической дикарбоновой кислоты при меньшем содержании в ней ароматического альдегида монокарбоновой кислоты, например 4-КБА, и окрашенных материалов в виде примесей; чистота получаемой кислоты достаточна для проведения прямой полимеризации после проведения единственной стадии реакции, а именно окисления.
В соответствии с этим, со времени патентного документа 4 (JP-B № Sho 34-2666) на «катализатор, включающий тяжелый металл и бром», не было подано заявок на способ получения неочищенных ароматических дикарбоновых кислот, подходящих для гидрогенизационной очистки, по части улучшений состава катализатора окисления в составе каталитической композиции, предназначенной для получения неочищенной ароматической дикарбоновой кислоты (ароматической дикарбоновой кислоты, не обладающей высокой чистотой) по реакции окисления диалкилароматического углеводорода в качестве исходного материала, поскольку удаление примесей сильно зависит от стадии гидрогенизационной очистки, проводимой на следующей после окисления стадии.
Патентный документ 1: JP-B № Sho 45-36732
Патентный документ 2: JP-B № Sho 53-30700
Патентный документ 3: JP-B № Sho 56-21015
Патентный документ 4: JP-B № Sho 34-2666
Патентный документ 5: JP-B № Sho 53-24057
Патентный документ 6: JP-A № Hei 11-228492
Подробное описание изобретения
Проблема, которая решается данным изобретением
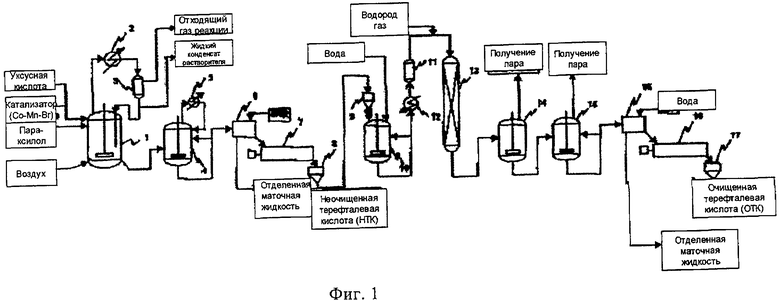
Процесс получения очищенной ароматической дикарбоновой кислоты, который в настоящее время применяют в промышленности, представлен на фиг.1 процессом получения очищенной терефталевой кислоты, который подразделяется на две стадии: стадия получения неочищенной терефталевой кислоты (НТК) и стадия очистки для получения очищенной терефталевой кислоты (ОТК).
То есть в процессе получения неочищенной терефталевой кислоты (НТК) пара-ксилол в качестве исходного вещества, уксусную кислоту в качестве растворителя и катализатор (Со, Mn, Br) подают в реактор окисления 1, в котором происходит перемешивание при высокой температуре (от 180 до 210°С) и при высоком давлении (от 10 до 20 кг/см2 (отн.)), а также подают воздух в нижнюю часть реактора 1 для непрерывного проведения реакции окисления. Отходящий газ с пониженным содержанием кислорода вследствие осуществления реакции окисления выходит из верхней части реактора 1 совместно с парами растворителя. Отходящий газ, содержащий пары продукта, пропускают через охладитель-конденсатор 2, в котором способные к конденсации составляющие конденсируют и отделяют с получением жидкого конденсата и отходящего газа реакции в сепараторе газа и жидкости 3. Большую часть жидкого конденсата возвращают в реактор 1, но часть экстрагируют с целью регулирования концентрации воды в растворителе, находящемся в реакторе.
Продукт реакции удаляют из нижней части реактора, регулируя уровень жидкости, а также предварительно определенный реакционный объем, в дополнительный реактор окисления (не показан на фиг.1, этот дополнительный реактор, как и основной реактор, снабжен мешалкой, конденсатором-охладителем, сепаратором газа и жидкости) и в него подают кислородсодержащий газ, например воздух, для завершения реакции окисления. Полученный после завершения реакции окисления продукт реакции переносят в кристаллизатор 4 при более низком давлении и охлаждают выпариванием под давлением; полученную терефталевую кислоту осаждают и получают суспензию с растворителем. Полученную суспензию отделяют и промывают в сепараторе твердого вещества и жидкости 6, например в фильтровальном устройстве, и выделяют кристаллы терефталевой кислоты. Затем их сушат в сушилке с получением неочищенной терефталевой кислоты (НТК).
Затем на стадии получения очищенной терефталевой кислоты (ОТК) указанную высушенную неочищенную терефталевую кислоту (НТК) и воду количественно загружают в сосуд для приготовления суспензии 10, с целью приготовления водной суспензии предварительно заданной концентрации (от 20 до 33 мас.%). Суспензию также количественно переносят в нагреватель 12 и сосуд для растворения 11 при высоком давлении (от 60 до 80 кг/см2 (отн.)) и терефталевую кислоту растворяют при нагревании в водном растворе, а затем направляют в реактор гидрогенизационной очистки 13. В реакторе гидрогенизационной очистки 13 при высокой температуре (от 260 до 290°С) и высоком давлении (от 60 до 80 кг/см2 (отн.)) загружают активированный углеродный катализатор, содержащий благородный металл, например палладий, водный раствор терефталевой кислоты, содержащий примеси, одновременно подают водород и пропускают его через слой катализатора, таким образом проводят реакцию гидрирования примесей.
Водный раствор терефталевой кислоты, подвергнутый обработке в реакции гидрирования, как описано выше, охлаждают с использованием равновесного испарения при ступенчатом понижении давления в нескольких кристаллизаторах, объединенных в серию (от 3 до 6 стадий) (набор кристаллизаторов на фиг.1 не показан) с целью осаждения кристаллов терефталевой кислоты. Очищенную суспензию, в которой кристаллизовалась терефталевая кислота, отделяют и промывают в сепараторе твердого вещества и жидкости, например в центрифуге, с целью выделения кристаллов терефталевой кислоты. Затем очищенную терефталевую кислоту сушат с использованием сушилки и получают на этой стадии в виде продукта (ОТК).
В соответствии с этим, поскольку процесс очистки на стадии гидрогенизационной очистки работает эффективно, предъявляется меньше требований к стадии получения неочищенной ароматической дикарбоновой кислоты, предшествующей стадии гидрогенизационной очистки, и отсутствуют предложения по стадии реакции окисления, подходящей для гидрогенизационной очистки, включая обе стадии - реакцию окисления и гидрогенизационную очистку.
Конкретно, что касается катализатора реакции жидкофазного окисления в процессе получения неочищенной ароматической дикарбоновой кислоты, отсутствуют предложения по улучшению состава катализатора, включающего Со, Mn и Br, со времени опубликования патентного документа 4, описанного выше и описывающего «осуществление жидкофазного окисления молекулярным кислородом в присутствии тяжелого металла и брома».
Кроме того, в патентах, содержащих признак регулирования отношения составляющих частей катализатора в количественном интервале, например отношения Mn/Со или отношения Br/Со к концентрации Со в растворителе для проведения реакции окисления, введенных в настоящее описание в качестве ссылки (патентные документы с 1 по 3, описанные выше), описано, что терефталевую кислоту высокой чистоты можно получить при снижении количества примесей (4-КБА в качестве промежуточного продукта) до примерно 500 част./млн. или менее.
Однако, хотя улучшения могут обеспечить высокую чистоту ароматических дикарбоновых кислот в качестве исходного материала для получения ароматических полиэфиров без использования стадии гидрогенизационной очистки в качестве последующей стадии, потери при окислении растворителя (уксусной кислоты), происходящие при окислении совместно с реакциями глубокого окисления, могут составлять примерно 0,2 в качестве основной единицы уксусной кислоты (массовое отношение израсходованной при окислении уксусной кислоты в расчете на массу полученной терефталевой кислоты), как показано в примере из патентного документа 3, описанного выше, и поэтому этот метод не является превосходным с экономической точки зрения способом.
Далее, также и в других патентах, описанных выше (патентные документы 1 и 2, описанные выше), хотя количество израсходованной при окислении уксусной кислоты конкретно не указано, поскольку данный способ включает получение терефталевой кислоты, содержащей такое же количество 4-КБА, как и в описанной выше патентной публикации, считают, что и в этом случае на окисление расходуется примерно такое же количество уксусной кислоты.
С другой стороны, на стадии гидрогенизационной очистки примеси, например, промежуточные продукты реакции, содержащиеся в неочищенной ароматической дикарбоновой кислоте, гидрируются с получением хорошо растворимых в воде продуктов.
Например, стадию гидрогенизационной очистки проводят на основании того, что промежуточный продукт реакции, альдегид ароматической монокарбоновой кислоты, например 4-КБА, превращается в метилированную ароматическую монокарбоновую кислоту, например пара-толуиловую кислоту, а окрашенные примеси, например флуоренон, подвергаются гидрокрекингу и их содержание в очищенных кристаллах ароматической дикарбоновой кислоты сильно снижается по ходу ее кристаллизации и выделения.
Среди перечисленных реакций в гидрогенизационной очистке от альдегида ароматической монокарбоновой кислоты (4-КБА) реакция гидрирования альдегида ароматической монокарбоновой кислоты (4-КБА, молекулярная масса 150) в метилированную ароматическую монокарбоновую кислоту (пара-толуиловая кислота, молекулярная масса 136) протекает практически количественно (91 мас.% в расчете на молекулярную массу), и, поскольку метилированная ароматическая монокарбоновая кислота (пара-толуиловая кислота) содержится после реакции гидрирования практически в том же количестве (примерно 90 мас.%), что и альдегид ароматической монокарбоновой кислоты (4-КБА) в неочищенной ароматической дикарбоновой кислоте, эту реакцию проводят в качестве способа получения очищенной терефталевой кислоты, в кристаллах которой содержание пара-толуиловой кислоты не превышает 150 част./млн, с использованием улучшенного способа кристаллизации из водного раствора гидрированной терефталевой кислоты, как показано в патентном документе 4 (JP-B № Sho 53-24057) и патентном документе 5 (JP-A № Hei 11-228492). Поскольку другие примеси легко удалить при перекристаллизации после реакции благодаря протеканию гидрокрекинга и т.д., улучшение способа кристаллизации проводили, рассматривая его как критическую стадию в снижении содержания метилированной ароматической монокарбоновой кислоты (пара-толуиловой кислоты) при очистке.
Улучшенный способ представляет собой способ восстановления альдегида ароматической монокарбоновой кислоты (4-КБА), содержащегося в неочищенной ароматической дикарбоновой кислоте, по реакции гидрирования до метилированной ароматической монокарбоновой кислоты (пара-толуиловой кислоты), и затем осуществления успешной кристаллизации в системе многостадийного испарения с понижением давления (испарительное охлаждение со сбросом давления) так, что метилированная ароматическая монокарбоновая кислота (пара-толуиловая кислота) не захватывается выделенными кристаллами.
В соответствии с этим в патенте JP-B № Sho 53-24057 описано, что достаточно получить кристаллизованную терефталевую кислоту с количеством примесей, не превышающим 150 част./млн, посредством проведения многостадийного испарения с понижением давления с количеством стадий от 5 до 8 из терефталевой кислоты, содержащей от 2000 до 6000 част./млн пара-толуиловой кислоты, в расчете на терефталевую кислоту. Затем, в приведенном примере, терефталевую кислоту с содержанием 2500 част./млн пара-толуиловой кислоты, растворяют в воде, и осуществляют многостадийное испарение с понижением давления с получением кристаллизованной терефталевой кислоты, содержание примесей в которой составляет 150 част./млн или менее.
Далее, в примере, приведенном в JP-A 11-228492, терефталевую кислоту, содержащую 3000 част./млн пара-толуиловой кислоты, растворяют в воде с получением кристаллизованной терефталевой кислоты с содержанием 150 част./млн или менее пара-толуиловой кислоты.
В соответствии с этим содержание альдегида ароматической монокарбоновой кислоты (4-КБА) в ароматической дикарбоновой кислоте (НТК), полученной окислением в виде ароматической дикарбоновой кислоты (НТК), подходящей для гидрогенизационной очистки, значительно превосходит количество метилированной ароматической монокарбоновой кислоты (пара-толуиловой кислоты), содержащейся в очищенной ароматической дикарбоновой кислоте. Однако при этом не требуется ароматическая дикарбоновая кислота (НТК) такой высокой чистоты, чтобы содержание альдегида ароматической дикарбоновой кислоты (4-КБА) составляло 500 част./млн или менее, как предложено в патентных документах с 1 по 3, описанных выше, а можно проводить такую реакцию окисления, как получение неочищенной ароматической дикарбоновой кислоты (НТК), содержащей примерно 3000 част./млн альдегида ароматической монокарбоновой кислоты (4-КБА).
Для осуществления этой цели полагают, что должен существовать отдельный способ мягкого окисления в жидкой фазе диалкилароматического углеводорода, подходящий в качестве предварительной стадии перед стадией гидрогенизационной очистки, отличающийся от предложений, описанных выше (в патентных документах с 1 по 3).
Для неочищенной ароматической дикарбоновой кислоты (НТК), предназначенной для применения в гидрогенизационной очистке, полагают, что содержание альдегида ароматической монокарбоновой кислоты (4-КБА), который является примесью, предпочтительно составляет от 2000 до 3500 част./млн, а предметом настоящего изобретения являются составляющие части катализатора (Со, Mn и Br) и реакционные условия, необходимые для проведения реакции мягкого окисления, в котором образуется неочищенная ароматическая дикарбоновая кислота (НТК), содержащая от 2000 до 3500 част./млн альдегида ароматической монокарбоновой кислоты (4-КБА).
Способы решения проблемы
Авторы настоящего изобретения провели полные исследования температуры реакции и катализатора окисления (Со, Mn, Br), предназначенного для реакции мягкого окисления с получением неочищенной ароматической дикарбоновой кислоты, содержащей от 2000 до 3500 част./млн. альдегида ароматической монокарбоновой кислоты. Конкретно, они обнаружили, что снижение температуры реакции и снижение содержания брома (Br), что является наиболее чувствительным инструментом регулирования реакционной способности в реакции окисления, оказывает воздействие на катализатор гидрогенизационной очистки на последующей стадии, и изучили изменение состава катализатора окисления и реакционной температуры в качестве способа получения неочищенной ароматической дикарбоновой кислоты, предназначенной для гидрогенизационной очистки.
В результате авторы настоящего изобретения обнаружили, что количество растворителя, уксусной кислоты (основного звена уксусной кислоты), потерянного при окислении, происходящем наряду с образованием ароматической дикарбоновой кислоты при реакции окисления, находится в компенсационной корреляции с количеством альдегида ароматической монокарбоновой кислоты (4-КБА), содержащегося в получающейся ароматической дикарбоновой кислоте, и воздействие на количество окисленной уксусной кислоты (основного звена уксусной кислоты) становится ниже при снижении температуры реакции, при одинаковом содержании альдегида ароматической монокарбоновой кислоты (4-КБА) в полученной ароматической дикарбоновой кислоте; и количество окисленной уксусной кислоты не снижается, даже если температуру снижают до 185°С или ниже. Затем было подтверждено, что количество окисленной уксусной кислоты (основное звено уксусной кислоты) составляет от 37 до 45 кг в расчете на тонну полученной дикарбоновой кислоты, что значительно ниже по сравнению с примером, приведенным в патенте (ссылка на патентный документ 3) (0,2 составляет примерно 200 кг/т).
В соответствии с этим для получения ароматической дикарбоновой кислоты, содержащей от 2000 до 3500 част./млн альдегида ароматической монокарбоновой кислоты (4-КБА), предназначенной для гидрогенизационной очистки, как было найдено, реакционная температура должна составлять предпочтительно от 197 до 185°С.
Однако, хотя считают необходимым увеличение количества катализатора (Со, Mn, Br), необходимого для получения ароматической дикарбоновой кислоты с одинаковым содержанием альдегида ароматической монокарбоновой кислоты (4-КБА) с целью снижения температуры реакции, если отношение содержания Br в катализаторе окисления снижают в соответствии с требованиями, например, с целью достижения более низкой активности в реакции и подавления коррозии оборудования, было найдено, что это приводит к засорению слоя катализатора гидрирования в последующей стадии, что заставляет прерывать работу установки и оказывает воздействие на активность водорода на стадии гидрогенизационной очистки (сравнительный пример 1). В то же время было найдено, что это происходит вследствие содержания золы в образующейся ароматической дикарбоновой кислоте; содержание Mn в золе чрезвычайно велико, что происходит вследствие снижения отношения количества брома к количеству марганца (Br/Mn). Далее, было найдено, что отношение Br/Mn, способное ограничить содержание золы, зависит от температуры реакции, то есть оно обратно пропорционально температуре реакции в приведенном ниже уравнении (2). В соответствии с этим было найдено, что необходимо увеличивать содержание брома и снижать содержание марганца, а также снижать температуру реакции.
Полагают, что причиной является снижение воздействия Со, Mn в качестве катализаторов и Br в качестве промотора и регенерирующего агента в реакции жидкофазного автоокисления, поэтому автоматическая регенерация марганца с образованием оксида марганца протекать не может. Далее, в то время как обычно полагают, что активность катализатора водородной очистки снижается при агрегации и потере активного металла и налипании на него примесей, поскольку осаждение оксида марганца вызывает снижение гидрирующей активности до загрязнения слоя катализатора, образования золы следует избегать, чтобы сохранить продолжительность активной жизни катализатора.
Далее, регулирование количества катализатора (Со, Mn, Br), которое требуется наряду со снижением температуры реакции, увеличивается с увеличением массового отношения Br/(Co+Mn); было также найдено, что когда массовое отношение Br/(Co+Mn) повышается до величины 1,7 или более при температуре реакции, составляющей 185°С, это не оказывает воздействия на содержание альдегида ароматической монокарбоновой кислоты (4-КБА) в ароматической дикарбоновой кислоте (НТК). Затем было найдено, что при температуре реакции, превышающей 185°С, достаточное количество брома определяется массовым соотношением Br/(Co+Mn), составляющим 1,7.
Соответственно, предпочтительно, чтобы предельное количество брома регулировалось так, чтобы минимальное отношение Br/Mn, рассчитанное в соответствии с уравнением (2), коррелировало с каждой температурой реакции, а максимальное количество определялось соотношением Br/(Co+Mn) в составе катализатора, составляющим 1,7.
Основываясь на новых открытиях, описанных выше, для получения неочищенной ароматической дикарбоновой кислоты, предназначенной для гидрогенизационной очистки, с содержанием альдегида ароматической монокарбоновой кислоты, составляющим от 2000 до 3500 част./млн., можно получить наиболее экономичную неочищенную ароматическую дикарбоновую кислоту и обеспечить способ получения неочищенной ароматической дикарбоновой кислоты, способный обеспечить работоспособность катализатора гидрогенизационной очистки в течение длительного времени посредством получения каталитической композиции для катализатора окисления, которая содержит (1) каталитически активный металл (Co+Mn) в количестве 2650 част./млн. или менее и в количестве, равном или превышающем содержание, представленное уравнением зависимости:
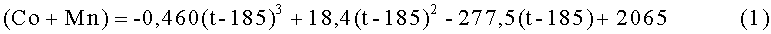
(в котором (Co+Mn) представляет собой содержание (Co+Mn) в част./млн, t представляет собой температуру реакции (°С) (интервал температуры от 185 до 200°С)),
(2) массовое отношение Mn/Со регулируется в пределах от 0,2 до 1,5, предпочтительно от 0,2 до 1,
(3) содержание брома составляет 1,7 или менее в массовом отношении Br/(Co+Mn) и по меньшей мере в количестве, равном или выше представленного уравнением зависимости (2)
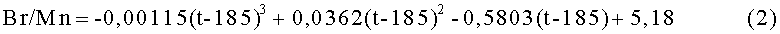
в котором Br/Mn представляет собой массовое отношение Br/Mn (масса/масса), t представляет собой температуру реакции (°С),
а реакцию окисления проводят при температуре реакции жидкофазного окисления, составляющей от 185 до 197°С, предпочтительно от 185 до 195°С.
Эффект данного изобретения
Настоящее изобретение может обеспечить составляющие части катализатора (Со, Mn и Br) и реакционные условия, необходимые для проведения реакции мягкого окисления, способной производить неочищенную ароматическую дикарбоновую кислоту (НТК), содержащую альдегид ароматической монокарбоновой кислоты (4-КБА) в количестве от 2000 до 3500 част./млн, который представляет собой типичные примеси, содержащиеся в неочищенной ароматической дикарбоновой кислоте (НТК), наиболее подходящей для проведения гидрогенизационной очистки.
Наилучший способ практического осуществления настоящего изобретения
В настоящем изобретении ароматическую дикарбоновую кислоту, содержащую от 2000 до 3500 част./млн альдегида ароматической монокарбоновой кислоты, предназначенную для гидрогенизационной очистки, получают окислением диалкилированного ароматического углеводорода в качестве исходного материала в жидкой фазе кислородсодержащим газом в растворителе, уксусной кислоте, в присутствии катализатора, включающего Со, Mn и Br.
В качестве исходного диалкилированного ароматического углеводорода применяют пара-ксилол или мета-ксилол, а в качестве растворителя в реакции применяют уксусную кислоту. В катализаторе окисления, приготовленном в уксусной кислоте в качестве растворителя, количество содержащихся (Co+Mn) составляет максимально 2650 част./млн, содержание составляет 2065 част./млн при 185°С, и регулируется внутри интервалов количества, рассчитанных по уравнению (1), то есть содержание снижается с повышением температуры реакции.
Количество катализатора (Co+Mn), составляющее 2650 част./млн, дает возможность получить ароматическую дикарбоновую кислоту, содержащую примерно 2000 част./млн альдегида ароматической монокарбоновой кислоты при соотношении Br/(Co+Mn)=1,7 (мас./мас.) при температуре реакции 185°С, то есть содержание катализатора оказывает меньшее воздействие на содержание брома с повышением соотношения Br/(Co+Mn) выше величины 1,7. Далее, при данном содержании катализатора отсутствует необходимость повышения его активности в реакции путем увеличения содержания Co+Mn (поскольку отсутствует необходимость снижения содержания альдегида монокарбоновой кислоты до ниже 2000 част./млн).
Кроме того, количество Co+Mn, рассчитанное по уравнению (1), представляет собой такое содержание катализатора, при котором по реакции окисления образуется ароматическая дикарбоновая кислота, содержащая максимально примерно 3500 част./млн альдегида ароматической монокарбоновой кислоты, и количество Co+Mn представляет собой минимальное количество катализатора, которое требуется при регулировании (повышении) количества по сравнению со значением, рассчитанным на основании уравнения (1) при каждой температуре реакции при условии снижения содержания альдегида ароматической монокарбоновой кислоты или количества брома. Соответственно, предпочтительно, чтобы количество Co+Mn в уксусной кислоте, используемой в качестве растворителя, регулировалось внутри интервала значений между двумя указанными содержаниями Co+Mn.
Далее, в реакции окисления, например, в заявках, приведенных в патентных документах с 1 по 3, описанных выше, отношение Mn/Со (массовое отношение) регулируется внутри интервала от 0,2 до 1,5, предпочтительно от 0,2 до 1, в соответствии с влиянием марганца в качестве сокатализатора на кобальтовый катализатор. Предпочтительно, чтобы соотношение Mn/Со (массовое отношение) снижалось с понижением температуры реакции, в связи с ограничениями по температуре реакции и отношению Br/Mn (массовое отношение), и отношение Mn/Со предпочтительно регулируют так, чтобы оно составляло 0,49 или менее, в связи с ограничениями по отношению Br/Mn при температуре реакции, составляющей 185°С.
Затем, поскольку количество Br необходимо повышать по мере снижения температуры реакции, повышение его содержания выше величины Br/(Co+Mn)=1,7 при температуре реакции 185°С меньше воздействует на содержание альдегида ароматической монокарбоновой кислоты (4-КБА) в качестве продукта реакции. Достаточное регулирование количества достигается повышением температуры и регулированием соотношения Br/(Co+Mn) на уровне 1,7 или менее. Соответственно, катализатор готовят так, чтобы его состав находился в регулируемом интервале, составляющем, по меньшей мере, то количество, которое рассчитывается по уравнению (2) или более в отношении содержания марганца, чтобы ограничить образование золы в конечной ароматической дикарбоновой кислоте при максимальном содержании брома, которое регулируется отношением Br/(Co+Mn)=1,7.
То есть количество брома в катализаторе по меньшей мере соответствует рассчитанному по уравнению (2) или более, чтобы избежать образования золы и ее попадания в ароматическую дикарбоновую кислоту, предназначенную для гидрогенизационной очистки, и количество брома при температуре реакции 185°С было таким, чтобы отношение (Br/Mn) составляло 5,18. Это количество соответствует контрольному соотношению Mn/Со, составляющему 0,49 и дающему возможность получить катализатор с соотношением Br/(Co+Mn)=1,7.
Уксусную кислоту в качестве растворителя, приготовленную, как описано выше, подают в количестве, которое от 2,5 до 4 раз превышает количество (по массе) диалкилированного ароматического углеводорода, который подают в качестве исходного материала в реактор окисления, и подают в реактор кислородсодержащий газ, например воздух, с целью проведения реакции окисления. Отходящий газ, обедненный кислородом, израсходованным на реакцию окисления, и содержащий пары растворителя отводят из верхней части реактора, пары растворителя конденсируют в конденсаторе-охладителе 2, затем жидкий конденсат разделяют с использованием сепаратора газ/жидкость 3 и возвращают в реактор. Концентрацию кислорода в отходящих газах реакции, отделенных от жидких конденсатов, измеряют, и затем газы выпускают из реакционной системы при регулируемом давлении. Температуру в реакторе, то есть температуру реакции, регулируют в интервале от 185 до 197°С, предпочтительно от 185 до 195°С, посредством регулирования генерации пара с помощью регулировки давления (от 11 до 18 кг/см2 (отн.)).
Далее, подаваемое в реактор количество кислородсодержащего газа регулируют так, чтобы концентрация кислорода в отходящих из реакции газах составляла от 2,5 до 4 об.%.
Кроме того, часть рециркулирующего жидкого конденсата удаляют с целью регулирования содержания воды в растворителе на протяжении реакции, так чтобы оно составляло от примерно 8 до 15 мас.%, предпочтительно от 10 до 13 мас.%. С целью регулирования количества воды в реактор подают растворитель, уксусную кислоту (не содержащую катализатора), в количестве, соответствующем удаленному количеству жидкого конденсата, так чтобы поддержать постоянной концентрацию катализатора окисления в используемом в реакции растворителе.
Продукт реакции, полученный по завершении реакции мягкого окисления, нужно удалить из нижней части реактора при регулировании уровня жидкости или при поддержании постоянным реакционного объема. Реакционный объем соответствует времени пребывания в реакторе подаваемой реакционной смеси, его предпочтительно регулируют так, чтобы оно составляло от 0,7 до 1,5 часов, более предпочтительно от 1 до 1,3 часов.
В реакции окисления, которую проводят описанным выше способом, растворитель, то есть уксусная кислота, расходуется по реакции разложения на газообразный диоксид углерода (включая монооксид углерода) и воду, протекающей параллельно реакции окисления исходного диалкилированного ароматического углеводорода. Реакция совместного окисления уксусной кислоты, протекающая в данном случае, определяет потери на окисление уксусной кислоты; в промышленности эти потери рассчитывают и учитывают как потери на окисление уксусной кислоты в расчете на получаемую ароматическую дикарбоновую кислоту (основная единица уксусной кислоты, кг/т).
Полагают, что количество окисленной кислоты зависит от жесткости условий реакции окисления и находится в компромиссном соотношении с содержанием альдегида ароматической монокарбоновой кислоты, остающимся в полученной ароматической дикарбоновой кислоте, то есть равна этой величине, умноженной на некоторый коэффициент. Соответственно, содержание альдегида монокарбоновой кислоты (4-КБА) (от 2000 до 3500 част./млн) в соответствии со способом по настоящему изобретению, отличается от содержания альдегида ароматической монокарбоновой кислоты (4-КБА) (500 част./млн или менее) в соответствии с патентным документом 3, описанным выше, так что количество окисленной уксусной кислоты значительно отличается для процесса окисления в соответствии с настоящим изобретением, предназначенного для получения ароматической дикарбоновой кислоты. Условия протекания реакции окисления, которые являются предметом настоящего изобретения, отличаются от условий, предложенных в патентном документе 3, описанном выше. Далее, количество окисленной уксусной кислоты в описанном в настоящем описании способе значительно снижается, что повышает экономичность способа получения ароматической дикарбоновой кислоты в соответствии с настоящим изобретением.
Однако, даже если в реакции окисления образуется одинаковое количество альдегида ароматической монокарбоновой кислоты (4-КБА), количество окисленной уксусной кислоты (основная единица уксусной кислоты) снижается при проведении реакции окисления при более низких температурах, и, кроме того, степень снижения по мере снижения температуры уменьшается по мере приближения к температуре 180°С. Затем при температуре реакции, составляющей 180°С, количество окисленной уксусной кислоты (основная единица уксусной кислоты) практически совпадает с количеством, окисленным при температуре 185°С.
Соответственно, если реакцию окисления в процессе по настоящему изобретению проводят при температуре 185°С или выше, или при температуре 197°С или ниже, количество окисленной уксусной кислоты (основная единица уксусной кислоты) практически составляет 45 кг/т или ниже, при этом получается ароматическая дикарбоновая кислота с содержанием альдегида ароматической монокарбоновой кислоты (4-КБА) в интервале от 2500 до 3500 част./млн. Чтобы получить очищенную ароматическую дикарбоновую кислоту еще более сильно улучшенного качества, предпочтительно проводить реакцию окисления в интервале температур от 185 до 195°С.
Далее, окисление растворителя, то есть уксусной кислоты, сопровождается реакцией совместного окисления уксусной кислоты и исходного реагирующего вещества в реакторе. Содержание альдегида ароматической монокарбоновой кислоты (4-КБА) измеряют и, насколько позволяет это содержание, время пребывания реагентов в реакторе делают насколько возможно более коротким, то есть от 0,7 до 1,5 ч. С целью получения ароматической дикарбоновой кислоты, содержащей альдегид ароматической монокарбоновой кислоты (4-КБА) в количестве от 2000 до 3500 част./млн, и стабилизации окисленного количества уксусной кислоты, предпочтительно проводить реакцию окисления при временах пребывания в реакторе, составляющих от 1 до 1,3 часов.
Реакционную смесь, содержащую продукт, образованную так, как описано выше, удаляют из реактора в дополнительный реактор окисления, в него подают кислородсодержащий газ и в нем завершается реакция исходного вещества и промежуточного продукта реакции, оставшегося в реакционной смеси. Затем смесь, содержащую продукт реакции, переносят в кристаллизатор 4 и в нем охлаждают, а полученную ароматическую дикарбоновую кислоту кристаллизуют, затем в виде суспензии пропускают через стадии разделения твердого и жидкого компонентов, удаляют уксусную кислоту промыванием и сушат с получением порошкообразной неочищенной ароматической дикарбоновой кислоты, содержащей от 2000 до 3500 част./млн альдегида ароматической монокарбоновой кислоты.
Затем неочищенную ароматическую дикарбоновую кислоту, полученную так, как описано выше, подают на стадию очистки; после превращения неочищенной ароматической дикарбоновой кислоты в водный раствор, как описано выше, ее подают на гидрогенизационную очистку с использованием палладиевого катализатора, нанесенного на активированный уголь, при высокой температуре и высоком давлении, с целью поддержания активности в гидрировании в течение длительного времени (от 1 до 3 лет). Затем ее кристаллизуют в многостадийном охлаждении с понижением давления, подвергают разделению на твердые и жидкие компоненты, промывают водой и сушат с получением кристаллического порошка очищенной ароматической дикарбоновой кислоты, в которой содержание метилового производного ароматической монокарбоновой кислоты составляет 150 част./млн или менее, то есть такая очищенная ароматическая дикарбоновая кислота обладает свойствами, позволяющими применять ее в качестве исходного вещества для получения ароматических полиэфиров.
Примеры
Способ в соответствии с настоящим изобретением далее будет описан подробно для конкретных предпочтительных вариантов со ссылкой на примеры, сравнительные примеры и базовые примеры.
Примеры с 1 по 4 и сравнительные примеры с 1 по 2
Схема получения неочищенной терефталевой кислоты (НТК) показана на фиг.1, реакцию окисления с целью получения неочищенной терефталевой кислоты проводили с использованием в качестве исходного материала пара-ксилола.
В качестве оборудования для проведения реакции применяли реактор окисления для работы с высоким давлением (внутренний объем составлял примерно 48 м3), оборудованный роторным смесителем; в реактор подавали пара-ксилол в качестве исходного реагента, реакционный растворитель, содержащий катализатор и воздух под давлением; уксусную кислоту подавали отдельно с целью регулирования содержания воды в реакционном растворителе.
Затем смешанный с парами отходящий газ реакции, который образовывался в результате реакции окисления, удаляли из верхней части реактора окисления, пропускали через конденсатор - охладитель 2, где способные к конденсации составляющие смешанного отходящего газа конденсировались и охлаждались, с целью отделения жидкого конденсата, который возвращали в реактор окисления.
Часть жидкого конденсата, предназначенного для возвращения в реактор, удаляли через отвод в циркуляционном контуре и таким образом регулировали содержание воды в растворителе на протяжении реакции.
Далее, отходящий газ реакции, отделенный от жидкого конденсата, вводили в абсорбер газа (не показан) при высоком давлении и разгружали посредством промывной обработки уксусной кислотой и водой.
С другой стороны, прореагировавшую и образовавшуюся конечную суспензию переносили в дополнительный реактор окисления (не показан) и после проведения дополнительной реакции окисления ее обрабатывали в кристаллизаторе 4 и сепараторе твердых и жидких продуктов 6 (отделение твердого вещества от жидкости и промывание осадка) с получением влажного отжатого осадка конечной терефталевой кислоты. Затем, после сушки в сушилке 7, получали неочищенную терефталевую кислоту (НТК).
Реакцию окисления проводили при подаче уксусной кислоты, содержащей катализатор, в количестве, которое в три раза больше по массе в расчете на 100 частей в час исходного пара-ксилола, подаче сжатого воздуха, регулировании давления отходящего газа на выходе из реактора так, чтобы достичь соответствующих температур реакции, и продувании воздуха в таком количестве, чтобы концентрация газообразного кислорода в отходящем газе составляла примерно 3,5 об.% и обеспечивала проведение реакции окисления. Затем продукт реакции переносили в дополнительный реактор окисления, контроль уровня жидкости осуществляли с применением рентгеновских лучей, так что время пребывания в реакторе составляло примерно 70 мин. Концентрацию воды в реакционной смеси в процессе реакции регулировали так, чтобы она составляла примерно 11,5 мас.% (вода в маточной жидкости реакции).
Для этого примера температура реакции, содержание катализатора (Со, Mn, Br) в подаваемом растворителе, то есть уксусной кислоте, и содержание 4-КБА в неочищенной терефталевой кислоте приведены в таблицах с 1 по 6. В то же время измеряли также содержание газообразных диоксида углерода (СО2) и моноксида углерода (СО) в отходящем газе, определяли количество окисленной уксусной кислоты (основная единица уксусной кислоты) и рассчитывали отношение количества окисленной уксусной кислоты к количеству полученной терефталевой кислоты на поданный пара-ксилол (кг/т ТК), эти данные также приведены совместно в таблицах с 1 по 6.
Сравнительный пример 2. Температура реакции 180°С
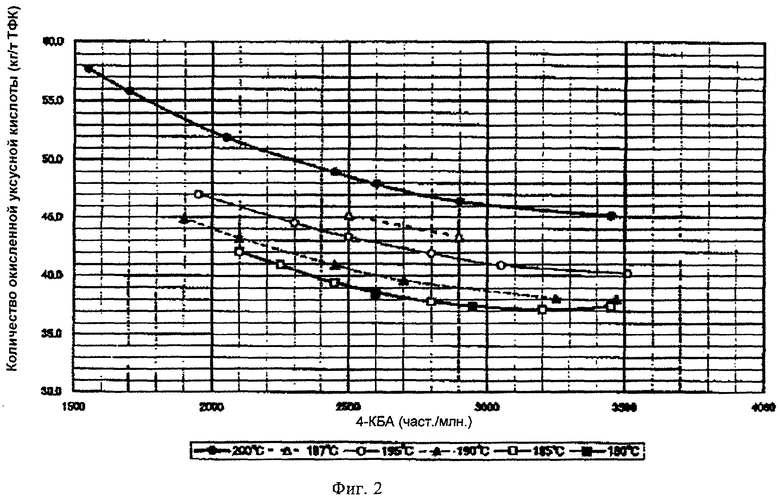
Соотношения между содержанием 4-КБА в образовавшейся терефталевой кислоте и окисленным количеством уксусной кислоты приведены на фиг.2.
Было найдено, что количество окисленной уксусной кислоты находится в компенсационном соотношении с содержанием 4-КБА, и количество окисленной уксусной кислоты при более низкой температуре реакции снижали с целью получения терефталевой кислоты с тем же содержанием 4-КБА в этой реакции окисления, и, кроме того, количество окисленной уксусной кислоты не снижалось даже при снижении температуры до величин ниже 185°С.
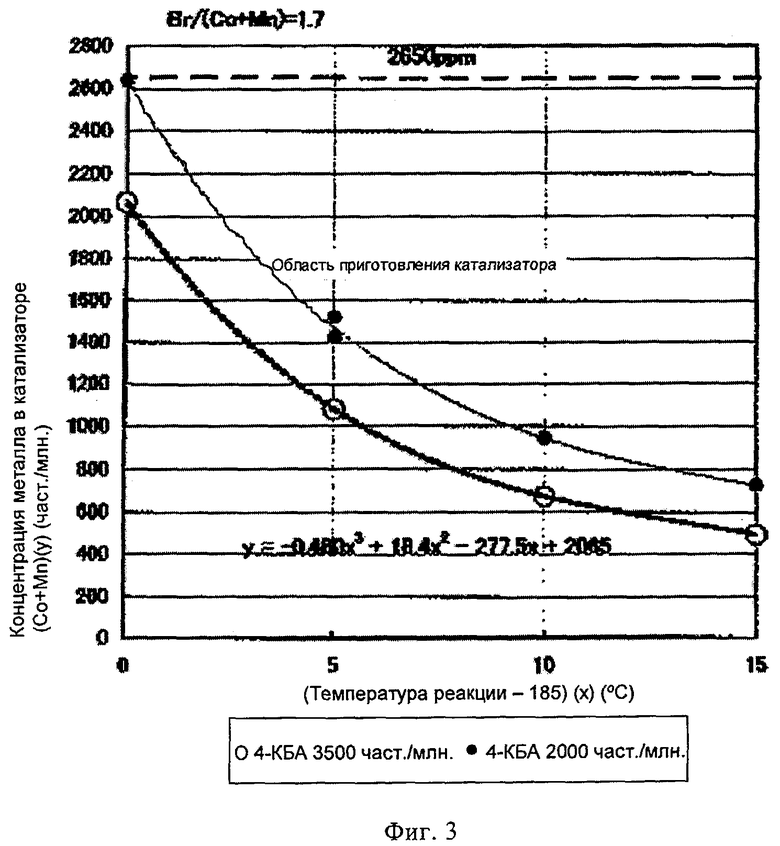
Далее, что касается соотношения между содержанием металлов в катализаторе (Co+Mn) и температурой реакции, необходимо снижать количество Co+Mn при снижении температуры; содержание Co+Mn, необходимое для получения терефталевой кислоты, содержащей примерно 3500 част./млн (от 3450 до 3510 част./млн) и примерно 2000 част./млн. (от 1900 до 2100 част./млн) при каждой температуре реакции в зависимости от температуры реакции (от 185 до 200°С) приведено на фиг.3 (в виде ◦ и •).
В данной реакции для получения НТК, предназначенной для гидрогенизационной очистки, содержание Co+Mn в растворителе делают таким, чтобы оно попало в область составов на фиг.3, заключенную между двумя линиями содержаний 4-КБА, составляющими 3500 и 2000 част./млн. при каждой температуре реакции.
Затем, поскольку реакцию проводят при соотношении Br/(Co+Mn)=1,7, если ее осуществляют в интервале более высоких температур (190, 195°С), НТК для применения в гидрогенизационной очистке можно получить, повышая содержание Co+Mn и снижая соотношение Br/(Co+Mn). Для этого кривая, обозначенная символами ◦ на фиг.3, определяет контрольное количество катализатора с минимальным содержанием Co+Mn при каждой температуре.
Далее, кривая, представленная символами ◦ на фиг.3, описывается приведенной ниже формулой
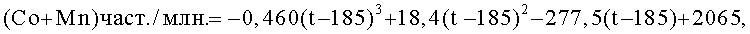
в которой t представляет собой температуру реакции (°С), а температурный интервал составляет от 185 до 200°С.
Поскольку снижение содержания брома при температуре реакции 185°С вызывает образование золы и поскольку трудно снизить содержание брома ниже количества, определяемого соотношением Br/(Co+Mn)=1,7, контрольное количество катализатора (количество Co+Mn, равное 2650 част./млн) при 185°С в условиях реакции с целью получения терефталевой кислоты, содержащей 2000 част./млн. 4-КБА (кривая, обозначенная символом • на фиг.3) представляет собой максимальное содержание катализатора в данной реакции.
В соответствии с этим количество каталитически активного металла (Co+Mn) в растворителе для реакции окисления, предназначенной для получения НТК (содержание 4-КБА от 2000 до 3500 част./млн), для гидрогенизационной очистки при приготовлении катализатора задают таким, как и количество Co+Mn, рассчитанное по уравнению, описанному выше, или более, и содержание катализатора поддерживают таким, чтобы содержание в нем Co+Mn находилось на контрольном уровне в 2650 част./млн или менее (внутри интервала, заданного жирной пунктирной линией, показанной на фиг.3).
Базовый пример 1
В соответствии со схемой получения очищенной терефталевой кислоты, представленной на фиг.1, получение неочищенной терефталевой кислоты (НТК) и получение очищенной терефталевой кислоты (ОТК) гидрогенизационной очисткой проводят с использованием в качестве исходного материала пара-ксилола.
Условия реакции окисления при производстве НТК идентичны тем, которые приведены в примерах 1, 2, 3 и 4, в которых реакционный растворитель подавали в количестве, трехкратно превышающем по массе количество исходного пара-ксилола, воздух подавали так, чтобы концентрация кислорода (О2) в отходящем газе составляла примерно 3,5 об.%, и реакцию проводили в непрерывном режиме при температуре 193°С. Удаление образовавшегося продукта реакции и жидких конденсатов, последующую обработку удаленных продуктов и т.д. проводили так же, как и в перечисленных примерах.
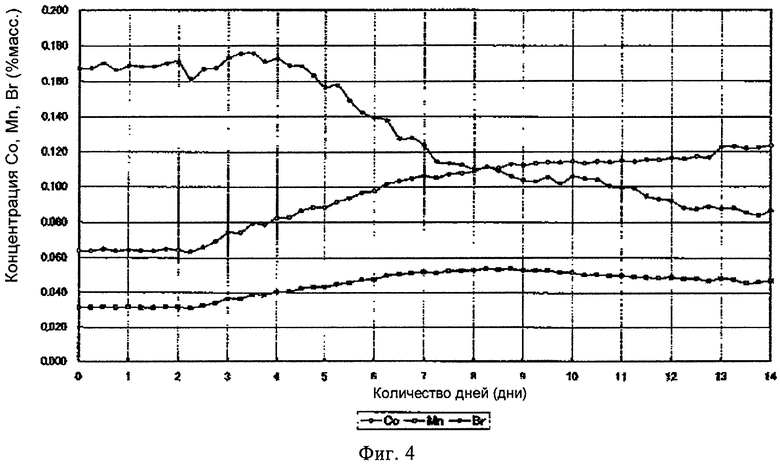
Чтобы приготовить подаваемую в реакцию каталитическую композицию, содержащую Со, Mn и Br в растворителе для реакции, раствор каталитически активных металлов (Со, Mn), бромоводородную кислоту и уксусную кислоту подавали в качестве исходного материала с использованием отделенной от продукта реакции маточной жидкости. Поскольку растворитель для реакции готовили так, чтобы воздержаться от добавления избыточного количества брома в полученную при отделении от продукта маточную жидкость, а только возместить то количество, которое расходуется в реакции, а в основном добавляли каталитически активные металлы (Со, Mn) и измеряли содержание 4-КБА, и на основании измерений добавляли Со и Mn в таких количествах, чтобы содержание 4-КБА в получающейся НТК составляло примерно 2500 част./млн. Содержание кобальта, марганца и брома измеряли в соответствующем процессе, как показано на фиг.4 (увеличение содержания кобальта и марганца и снижение содержания брома).
НТК, которую получали этим способом, содержала от 1800 до 3300 част./млн. 4-КБА.
Затем, с целью гидрогенизационной очистки полученной таким образом НТК в соответствии со схемой на фиг.1, ее смешивали с водой с получением водной суспензии, содержащей примерно 27 мас.% НТК, и растворяли при нагревании (285°С), а затем подавали в реактор гидрогенизационной очистки, содержащий твердый катализатор (0,5% Pd катализатор, нанесенный на активированный уголь), и проводили гидрогенизационную очистку НТК.
В реакторе гидрогенизационной очистки давление поддерживали на уровне 70 кг/см2 (отн.) по мере подачи газообразного водорода, в реактор подавали НТК в количестве, которое в три раза превосходило (мас./мас. в час) количество катализатора гидроочистки, в виде водного раствора в ту часть реактора, которая расположена выше слоя катализатора гидрогенизационной очистки. Затем реакционную смесь подавали в кристаллизатор 14 и осуществляли в пять стадий испарительное охлаждение, происходящее под влиянием ступенчатого сброса давления в кристаллизаторе 14, в результате осаждались кристаллы очищенной терефталевой кислоты (ОТК).
Полученную суспензию кристаллов ОТК подавали в сепаратор твердого вещества и жидкости 15 с целью выделения кристаллов ОТК, которые сушили с получением продукта - очищенной терефталевой кислоты.
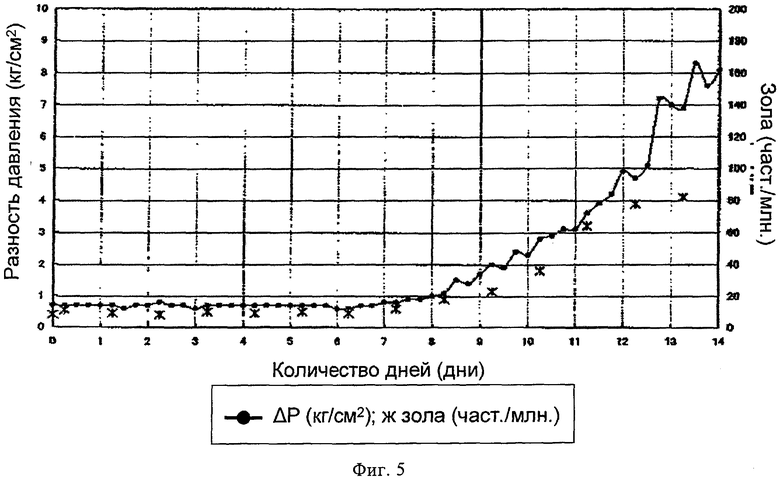
По мере проведения процесса разница давлений до и после слоя катализатора гидрогенизационной очистки (дифференциальное давление) повышалось только за половину месяца (14 дней), давление со стороны подачи водного раствора повышалось до 75 кг/см2 (отн.) или выше, и увеличивались колебания давления так, что подача водного раствора прерывалась и гидрогенизационную очистку останавливали. После промывания реактора гидрогенизационной очистки 13 водой, когда температура и давление снижались до величин, позволяющих открыть реактор, наблюдали, что на слой катализатора налипло мелкое черное смолистое вещество, особенно в нижней части слоя. Результаты измерения разницы давлений на выходе/входе в слой твердого катализатора (дифференциальное давление ΔР) представлены на фиг.5. Также на фиг.5 приведены измеренные величины содержания золы в подаваемой на очистку НТК.
На основании приведенных результатов предполагают, что резкое увеличение дифференциального давления ΔР в слое катализатора зависит от содержания золы в подаваемой в реакцию НТК.
На основании содержания золы, измеренного так, как описано выше (после 1, 25 и 13, 25 дней работы), результаты для падения содержания металлов представлены в приведенной ниже таблицу 7.
Результаты показывают, что содержание золы определяется составляющими частями катализатора; при увеличении содержания золы количество марганца в ее составе увеличивается необычно быстро (после 13, 25 дней работы соотношение Mn/Со составляет 8,3), в то время как в составе катализатора получения НТК соотношение ингредиентов совсем другое (Mn/Со=0,49), то есть в основном зола образована осаждающимся марганцем. Было высказано предположение, что причиной является снижение концентрации брома в составе катализатора получения НТК.
Базовые примеры с 2 по 4, примеры с 5 по 14 и сравнительные примеры с 3 по 11
Применяли прибор для проведения реакции окисления, содержащий реактор высокого давления (внутренний объем 20 л), оснащенный мешалкой, нагревателем и обратным холодильником, а также отверстием для введения исходного материала, отверстием для подачи кислородсодержащего газа, а также отверстием для удаления продукта реакции; 8 кг растворителя для реакционной смеси, уксусной кислоты, в которой растворяли ацетат кобальта, ацетат марганца и бромоводородную кислоту, загружали в реактор, продували газообразным азотом, а затем повышали температуру до 200°С и давление до 19 кг/см2 (отн.) при перемешивании.
Через отверстие для подачи исходного материала непрерывно подавали 2 кг/ч пара-ксилола, через отверстие для подачи кислородсодержащего газа подавали непрерывно воздух, подаваемое количество и давление воздуха регулировали так, чтобы концентрация кислорода в отходящем газе из верхнего отверстия для отхода газа в обратном холодильнике составляла примерно 4 об.%, температуру устанавливали на заданных уровнях (200, 195, 185°С) и проводили реакцию в течение 1 часа.
Далее, при поддержании соответствующих температур реакции, описанных выше, и продолжении подачи пара-ксилола и воздуха, начинали подавать реакционный растворитель (растворитель, в котором был приготовлен катализатор) со скоростью 7,5 кг/ч через отверстие для введения исходного материала, а продукт реакции удаляли через отверстие для удаления продукта реакции в приемник для продукта при регулировании уровня жидкости таким образом, чтобы внутренний объем жидкости составлял 9 л. Одновременно рециркулирующую жидкость удаляли со скоростью 1,5 кг/ч из бокового отвода с целью повторного использования жидкого конденсата, чтобы реакция протекала в непрерывном режиме. Следовательно, среднее время выдержки исходной реакционной смеси регулировали так, чтобы оно составляло примерно 1,1 часа.
Далее запускали непрерывную реакцию; через три часа подачу пара-ксилола, реакционного растворителя и удаление продуктов, а также рециркуляцию жидких конденсатов останавливали, подачу воздуха поддерживали в течение еще одной минуты и затем прекращали.
После окончания реакции и охлаждения реакционного продукта, оставшегося в реакторе, до примерно 70°С, его удаляли из реактора и фильтровали, затем промывали 6 кг уксусной кислоты и сушили в сушилке с получением конечного продукта - терефталевой кислоты (примерно 3 кг).
Содержание катализатора (Со, Mn, Br), приготовленного в растворителе, и отношения составляющих катализатор компонентов (отношения Mn/Со и Br/Mn) при каждой температуре реакции представлены в таблицах с 8 по 11. Содержание катализатора (Со, Mn, Br) в реакционном растворителе примерно в 1,25 раз выше содержания, приведенного в таблицах с 8 по 11 (поскольку рециркулирующую жидкость удаляли со скоростью 1,5 кг/ч).
Измеряли содержание 4-КБА в терефталевой кислоте и содержание золы, полученное при соответствующих условиях реакции, эти значения приведены в таблицах с 8 по 11.
С целью регулирования содержания катализатора в реакционном растворителе приведены примеры, в которых содержание 4-КБА в полученной терефталевой кислоте составляло от 2300 до 2800 част./млн.
Как можно видеть из приведенных результатов, при каждой температуре содержание золы резко увеличивается, когда отношение Br/Mn в катализаторе снижается. Было найдено, что отношение Br/Mn, которое является предельным (базовый пример 4, пример 8, пример 10, пример 14), по существу присутствует при каждой температуре реакции.
Соответственно, можно сказать, что отношение Mn/Co в составе каталитически активного металла (Mn, Со) также предпочтительно имеет тенденцию к понижению (Mn/Со=1,5→0,2) по мере снижения температуры реакции, что связано с ограничением отношения Br/Mn.
Далее, было также найдено, что они практически соответствуют величине для отношения Br/Mn=2,5→2,2 на 7 день→8 день, причем содержание золы в терефталевой кислоте увеличивалось в базовом примере 1 (температура реакции 193°С), как и величина отношения Br/Mn в качестве предела в примерах (пример 8: предельное отношение Br/Mn=1,82 при 195°С; пример 10: предельное отношение Br/Mn=3,04 при 190°С).
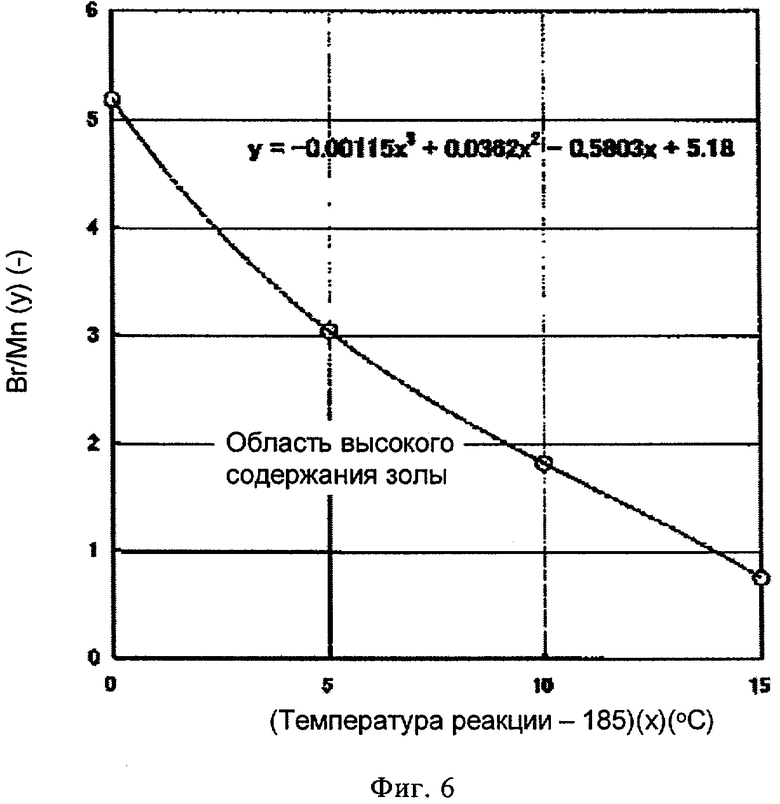
Далее, на график наносили предельное отношение Br/Mn при каждой температуре реакции, как показано на фиг.6; существует корреляция между температурой реакции и предельным отношением Br/Mn, которая описывается следующим уравнением:
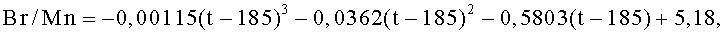
в котором t представляет собой температуру реакции, °С (интервал температур от 185 до 200°С).
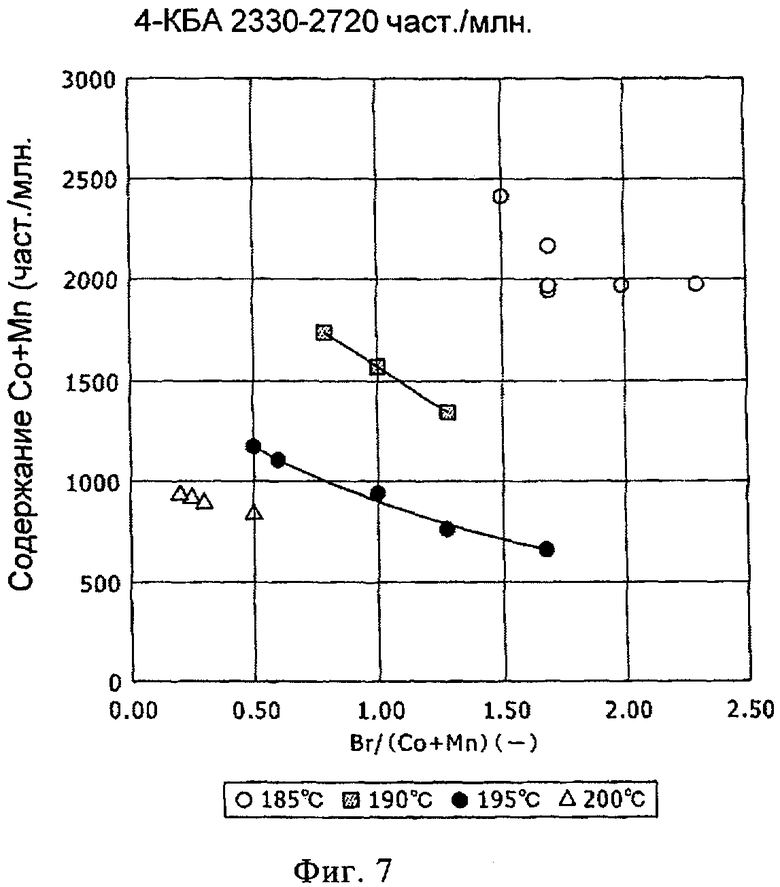
Кроме того, в примерах (включая базовые и сравнительные примеры) содержание брома (отношение Br/(Co+Mn)) в зависимости от количества каталитически активного металла (Co+Mn) представлено в виде кривой на фиг.7. Из фиг.7 можно видеть, что зависимость между количеством каталитически активного металла (Co+Mn) и отношением Br/(Co+Mn) различается для каждой из температур реакции, также соответствующим образом отличается влияние увеличения количества брома. При температуре реакции 185°С, при которой требуется самое большое количество брома, влияние увеличения количества брома в виде соотношения Br/(Co+Mn) кажется большим, но это влияние не проявляется, даже если отношение Br/(Co+Mn) повышается до примерно 1,7 или более. Соответственно, в реакции окисления при 185°С полагают, что отношение Br/(Co+Mn), равное 1,7, является максимальным получаемым количеством (содержание брома при Br/(Co+Mn)=1,7 или менее является достаточным при температуре реакции 185°С или выше).
Соответственно, при каждой реакционной температуре в данной реакции предпочтительно применять такое количество брома, которое бы было достаточным для того, чтобы отношение Br/Mn было не меньше величины, рассчитанной по уравнению, описанному выше, и приготовление нужно вести при таком количестве брома, чтобы отношение Br/(Co+Mn) составляло 1,7 или менее.
Пример 15
В соответствии со схемой получения чистой терефталевой кислоты, приведенной на фиг.1, получение неочищенной терефталевой кислоты и очищенной терефталевой кислоты проводили в непрерывном режиме с использованием в качестве исходного материала пара-ксилола способом, описанным в базовом примере 1.
После подачи реакционного растворителя, раствора металлсодержащего катализатора (Со, Mn) и бромоводородной кислоты так, чтобы обеспечить содержание катализатора, представленное в табл.12, проводили реакцию окисления при температуре 193±1°С.
В результате, для терефталевой кислоты, полученной на стадии получения неочищенной терефталевой кислоты, содержание 4-КБА составило примерно 2500 част./млн., а окисленное количество уксусной кислоты (основная единица уксусной кислоты) составило примерно 42 кг/т. Далее, очищенная терефталевая кислота, полученная на стадии получения очищенной терефталевой кислоты, содержала пара-толуиловую кислоту в количестве 120 част./млн. или менее, и давление в слое катализатора гидрогенизационной очистки 13 оставалось на уровне примерно 70 кг/см2 (отн.), работа установки без сбоев продолжалась в течение примерно 1 года без признаков появления перепадов давления, разница давлений (дифференциальное давление) составляло 1 кг/см2 или менее.
Краткое описание чертежей
На фиг.1 показана схема стадий получения неочищенной терефталевой кислоты с применением пара-ксилола в качестве исходного материала и стадий получения очищенной терефталевой кислоты растворением неочищенной терефталевой кислоты в воде с последующей гидрогенизационной очисткой.
На фиг.2 показано количество растворителя, уксусной кислоты, потерянное в результате реакции жидкофазного окисления (базовая единица уксусной кислоты) в 4-КБА (4-карбоксибензальдегид), содержащейся в терефталевой кислоте, полученной при жидкофазном окислении исходного пара-ксилола воздухом в присутствии катализатора с использованием уксусной кислоты в качестве растворителя (окисленное количество уксусной кислоты (базовая единица уксусной кислоты) представляет собой количество уксусной кислоты, потерянное при окислении, по отношению к количеству полученной терефталевой кислоты (кг/т терефталевой кислоты)).
На фиг.3 показаны количества Co+Mn в катализаторе для приготовления терефталевой кислоты при содержании 4-КБА (4-карбоксибензальдегида), составляющем 2000 и 3500 част./млн при каждой из температур реакции при жидкофазном окислении исходного материала, пара-ксилола, воздухом в присутствии катализатора с использованием в качестве растворителя уксусной кислоты (символом ◦ обозначена кривая, соответствующая содержанию 4-КБА 3500 част./млн; символом • обозначена кривая, соответствующая содержанию 4-КБА 2000 част./млн); температура реакции показана индексом (x) и приведена в виде величины (температура реакции - 185). Формула, определяющая соотношение между температурой реакции (температура реакции -185) (x) при получении терефталевой кислоты с содержанием 4-КБА 3500 част./млн и концентрацией металла в полученном катализаторе (количество Со+ количество Mn) (y), приведена на чертеже. Каждый катализатор приготовлен при соотношении Br/(Co+Mn)=1,7.
На фиг.4 показано изменение концентрации компонентов катализатора окисления (Со, Mn, Br) в подаваемом растворителе, приготовленном при непрерывном получении терефталевой кислоты при жидкофазном окислении пара-ксилола воздухом (с интервалом в 6 ч) (содержание 4-КБА в терефталевой кислоте в ходе протекания реакции составляло от 1800 до 3300 част./млн).
На фиг.5 показана разность давлений (дифференциальное давление), возникающих в слое катализатора гидрирования при осуществлении гидрогенизационной очистки после непрерывного получения терефталевой кислоты в жидкой фазе окислением пара-ксилола воздухом (аналогично фиг.4) с последующим осуществлением гидрогенизационной очистки после приготовления водного раствора терефталевой кислоты. На чертеже также показано содержание золы в терефталевой кислоте, подаваемой в реактор гидрогенизационной очистки.
На фиг.6 показано отношение Br/Mn (обозначено символом ○) в примерах по приготовлению катализатора (Со, Mn, Br) получения терефталевой кислоты с содержанием 4-КБА, составляющим примерно 2500 част./млн (в пределах от 2300 до 2800 част./млн.), при каждой из температур при жидкофазном окислении воздухом пара-ксилола в качестве исходного материала, причем выбраны примеры до резкого увеличения содержания золы (базовый пример 4, пример 8, пример 10, пример 14) (в результате соотношение Br/Mn (y) коррелирует с температурой реакции (температура реакции -185) (x), уравнение корреляции показано на чертеже. Соответственно, область соотношений Br/Mn под кривой на чертеже при каждой из реакционных температур можно определить как область высокого содержания золы.
На фиг.7 показано отношение Br/(Co+Mn) и количество Co+Mn для полученной каталитической композиции (Со, Mn, Br) при получении терефталевой кислоты с содержанием 4-КБА, составляющим примерно 2500 част./млн (от 2330 до 2720 част./млн), жидкофазным окислением воздухом пара-ксилола в качестве исходного материала в зависимости от температуры.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ НЕПРЕРЫВНОГО ПОЛУЧЕНИЯ АРОМАТИЧЕСКОЙ ДИКАРБОНОВОЙ КИСЛОТЫ | 2006 |
|
RU2314284C2 |
| СПОСОБ КРИСТАЛЛИЗАЦИИ ДЛЯ ПОЛУЧЕНИЯ ОЧИЩЕННЫХ АРОМАТИЧЕСКИХ ДИКАРБОНОВЫХ КИСЛОТ | 2002 |
|
RU2288216C2 |
| СПОСОБ ПОЛУЧЕНИЯ ОЧИЩЕННОЙ ТЕРЕФТАЛЕВОЙ КИСЛОТЫ | 2002 |
|
RU2292332C2 |
| СПОСОБ ПОЛУЧЕНИЯ И ОЧИСТКИ ИЗОФТАЛЕВОЙ КИСЛОТЫ | 2010 |
|
RU2458042C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИЗОФТАЛЕВОЙ КИСЛОТЫ С ВЫСОКОЙ СТЕПЕНЬЮ ЧИСТОТЫ | 2004 |
|
RU2266277C2 |
| ПОЛУЧЕНИЕ АРОМАТИЧЕСКОЙ ДИКАРБОНОВОЙ КИСЛОТЫ | 2015 |
|
RU2671210C2 |
| СПОСОБ РЕГЕНЕРАЦИИ КАТАЛИЗАТОРА ОКИСЛЕНИЯ АЛКИЛАРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ | 1998 |
|
RU2155098C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИЗОМЕРОВ ФТАЛЕВЫХ КИСЛОТ С ВЫСОКОЙ СТЕПЕНЬЮ ЧИСТОТЫ | 1993 |
|
RU2047595C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТЕРЕФТАЛЕВОЙ КИСЛОТЫ | 2012 |
|
RU2573564C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОЧИСТОЙ ИЗОФТАЛЕВОЙ КИСЛОТЫ | 1997 |
|
RU2137753C1 |
Изобретение относится к усовершенствованному способу получения неочищенной терефталевой кислоты для применения на стадии гидрогенизационной очистки посредством проведения жидкофазного окисления кислородсодержащим газом в реакторе окисления, снабженном мешалкой, с использованием в качестве исходного материала пара-ксилола в растворителе - уксусной кислоте, в присутствии металлсодержащего катализатора, включающего кобальт (Co), марганец (Mn) и бром (Br) в качестве промотора окисления, где температуру реакции окисления регулируют так, что она находится в интервале от 185 до 197°С, среднее время пребывания в реакторе исходной смеси для жидкофазного окисления составляет от 0,7 до 1,5 часов, содержание воды в реакционном растворителе регулируют так, чтобы оно составляло от 8 до 15 мас.%, а состав катализатора в растворе регулируют в интервале содержания, определенного в зависимости от температуры реакции так, что он включает: (1) каталитически активный металл (Co+Mn) в количестве от 2650 част./млн. или менее и в количестве, равном или более величины, определяемой следующим отношением: (Co+Mn)=-0,460(t-185)3+18,4(t-185)2-277,5(t-185)+2065, в котором (Co+Mn) представляет собой содержание (Co+Mn) в част./млн., t представляет собой температуру реакции (°С) (интервал температур от 185 до 200°С), (2) массовое отношение Mn/Co регулируют в интервале от 0,2 до 1,5, предпочтительно от 0,2 до 1; (3) содержание Br составляет 1,7 или менее, если его представляют величиной Br/(Co+Mn) в виде массового отношения и в количестве, равном или более величины, представленной уравнением: Br/Mn=-0,00115(t-185)3+0,0362(t-185)2-0,5803(t-185)+5,18, в котором Br/Mn представляет собой массовое отношение Br/Mn (мас./мас.), a t представляет собой температуру реакции (°С) (интервал температур от 185 до 200°С), и получение неочищенной терефталевой кислоты осуществляют с содержанием 4-карбоксибензальдегида в количестве от 2000 до 3500 част./млн. в качестве промежуточного продукта реакции жидкофазного окисления. В способе предложены экономичное получение неочищенной терефталевой кислоты для применения в гидрогенизационной очистке и использование регулируемого количества катализатора окисления, не оказывающего нежелательного воздействия на продолжительность работы катализатора гидрогенизационной очистки, а также условия проведения соответствующей реакции. Получение терефталевой кислоты при жидкофазном окислении соответствующего диалкилированного ароматического углеводорода с применением растворителя, уксусной кислоты, осуществляли путем снижения окисленного количества уксусной кислоты, потерянной при окислении, ограничения образования золы в полученной терефталевой кислоте и обеспечения регулирования состава катализатора окисления в зависимости от температуры реакции. 12 табл., 7 ил., 15 пр.
Способ получения неочищенной терефталевой кислоты для применения на стадии гидрогенизационной очистки посредством проведения жидкофазного окисления кислородсодержащим газом в реакторе окисления, снабженном мешалкой, с использованием в качестве исходного материала пара-ксилола в растворителе - уксусной кислоте, в присутствии металлсодержащего катализатора, включающего кобальт (Co), марганец (Mn) и бром (Br) в качестве промотора окисления, отличающийся тем, что температуру реакции окисления регулируют так, что она находится в интервале от 185 до 197°С, среднее время пребывания в реакторе исходной смеси для жидкофазного окисления составляет от 0,7 до 1,5 ч, содержание воды в реакционном растворителе регулируют так, чтобы оно составляло от 8 до 15 мас.%, а состав катализатора в растворе регулируют в интервале содержания, определенного в зависимости от температуры реакции так, что он включает:
(1) каталитически активный металл (Co+Mn) в количестве от 2650 част./млн или менее и в количестве, равном или более величине, определяемой следующим отношением:
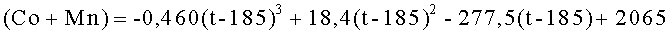 ,
,
в котором (Co+Mn) представляет собой содержание (Co+Mn) в част./млн,
t представляет собой температуру реакции (°С) (интервал температур от 185 до 200°С),
(2) массовое отношение Mn/Co регулируют в интервале от 0,2 до 1,5, предпочтительно от 0,2 до 1;
(3) содержание Br составляет 1,7 или менее, если его представляют величиной Br/(Co+Mn) в виде массового отношения, и в количестве, равном или более величины, представленной уравнением:
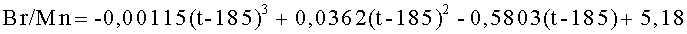 ,
,
в котором Br/Mn представляет собой массовое отношение Br/Mn (мас./мас.), a t представляет собой температуру реакции (°С) (интервал температур от 185 до 200°С), и получение неочищенной терефталевой кислоты осуществляют с содержанием 4-карбоксибензальдегида в количестве от 2000 до 3500 част./млн в качестве промежуточного продукта реакции жидкофазного окисления.
| WO 2006028873 А2, 16.03.2006 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ запрессовки не выдержавших гидравлической пробы отливок | 1923 |
|
SU51A1 |
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| Перекатываемый затвор для водоемов | 1922 |
|
SU2001A1 |
| Видоизменение прибора для получения стереоскопических впечатлений от двух изображений различного масштаба | 1919 |
|
SU54A1 |
| Способ смешанной растительной и животной проклейки бумаги | 1922 |
|
SU49A1 |
| Способ очистки терефталевой кислоты | 1980 |
|
SU929627A1 |
| WO 2006102336 А2, 28.09.2006. | |||
Авторы
Даты
2012-08-10—Публикация
2007-02-28—Подача