Область техники
Настоящее изобретение относится к способу получения мезенхимных клеток для формирования зуба, к способу получения зуба и мезенхимным клеткам для формирования зуба.
Предшествующий уровень техники
Зуб представляет собой орган, имеющий эмаль во внешнем поверхностном слое и дентин во внутреннем слое, которые являются твердыми тканями, одонтобласты во внутреннем слое дентина, продуцирующие дентин и пульпу зуба в центральной его части, они могут быть уничтожены в результате кариеса зубов, парадонтита и тому подобное.
Зубы являются функциональными единицами, которые формируются путем индукции во время процесса развития зародыша, они построены из многих типов клеток, которые, как полагают, являются такими же как органы или системы внутренних органов. Поэтому зубы не могут создаваться системой стволовых клеток, такими как гематопоэтическая стволовая клетка или мезенхимная стволовая клетка во взрослом организме. В результате зубы не могут регенерировать исключительно трансплантацией стволовых клеток (терапия трансплантации стволовых клеток), которая в регенеративной медицине в настоящее время находится в процессе разработки.
Поэтому недавно были проведены исследования, направленные на регенерацию зуба путем трансплантации реконструированного зубного зачатка, полученного реконструкцией зубного зачатка из изолированных клеток зубного зачатка.
Например, в J. Dent. Res., 2002, Vol.81(10), pp.695-700 описывается, что ткань, подобная зубной ткани, регенерирует путем трансплантации клеток, таких как эпителиальные клетки, выделенные из зубного зачатка, и мезенхимные клетки фолликул, с биодеградирующим носителем в брюшную полость крысы.
Способ регенерирования зубного зачатка описан, например, в опубликованной заявке на патент Японии (JP-A) №2004-331557, в которой клетки зубного зачатка, выделенные из живого организма, выращиваются в присутствии биологически активных веществ, таких как фибробластные факторы роста и тому подобное. В JP-A №2004-357567 предполагается, что по меньшей мере один тип клеток, выбранный из клеток зубного зачатка и клеток, которые могут быть дифференцированы в эти клетки зубного зачатка, оба из них выделяют из живого организма, выращивают вместе с фибринсодержащим носителем, и там же описывается, что путем применения фибринсодержащего носителя, имеющего желаемую форму для зубного зачатка, формируется "зуб", имеющий желемую форму.
В заявках на патент США (номер публикации) 2002/0119180 и 2004/0219489 описывается способ формирования зуба, включающий засев смеси клеток зубного зачатка из нижней челюсти шестимесячной свиньи, содержащей образующие дентин мезенхимные клетки, имеющие происхождение из пульпы зуба, и эпителиальные клетки, способствующие образованию эмали, в матрице, которая представляет собой биодеградирующий полимер, содержащий сополимер полигликолевой кислоты и полиуксусной кислоты, и трансплантации его в тело животного. Здесь описывается, что при применении матрицы, имеющей желаемую форму для зубного зачатка, формируется "зуб", имеющий желаемую форму.
Кроме того, в WO 2005/014070 описывается способ регенерации зуба для лечения пациента с остеопорозом или костным повреждением. По этому способу кость образуется посевом мезенхимных клеток в ячеистом носителе из полигликолевой кислоты с последующим ламинированием носителя эпителиальными клетками и коллагеном или обертыванием носителя лентой из эпителиальных клеток. Дополнительно, в WO 2005/014070 для воспроизведения формы кости применяют носитель.
В WO 2006/129672 описывается способ выращивания зуба, включающий получение клеточных масс из эпителиальных клеток и мезенхимных клеток из зубного зачатка соответственно; контакт этих клеточных масс друг с другом в коллагеновом геле; выращивание этих клеточных масс в условиях контакта с целью получить зуб, имеющий размещение клеток, специфичное для зуба.
Однако, для того чтобы регенерировать зуб или зубной зачаток согласно вышеописанным способам, клетки зубного зачатка или клетки, способные в них дифференцироваться, получают из живого организма. При таком приеме, когда применяют клетки, отобранные из живого организма, количество получаемых клеток иногда является недостаточным. Кроме того, иногда ограничен источник снабжения клеток.
Для того чтобы воссоздать функцию ткани, необходимо, чтобы разнообразные типы клеток, составляющие ткань, расположились (организация клеток) в необходимых позициях относительно друг друга и имели анизотропию как в ткани.
Описание изобретения
Настоящее изобретение было сделано с учетом вышеописанных обстоятельств и предлагает способ получения зуба и получения мезенхимной клетки для формирования зуба.
В первом аспекте настоящее изобретение предлагает способ получения мезенхимных клеток для формирования зуба, способ, включающий выращивание стволовых тотипотентных клеток в присутствии индуктора дифференцировки для создания клеточной популяции после обработки индуктором дифференцировки, при этом клеточная популяция содержит CD44-позитивные и CD29-позитивные клетки или CD44-позитивные и CD106-позитивные клетки, и отбор из клеточной популяции после обработки для индукции дифференцировки CD44-позитивных и CD29-позитивных клеток или CD44-позитивных и CD106-позитивных клеток в качестве мезенхимных клеток для формирования зуба.
Во втором аспекте настоящего изобретения предлагается способ получения зуба, включающий позиционирование в поддерживающем носителе первой клеточной массы, по существу состоящей только из одного типа клеток, выбранного из мезенхимных клеток и эпителиальных клеток, и второй клеточной массы, по существу состоящей только из другого типа клеток, выбранного из мезенхимных клеток и эпителиальных клеток, причем первую и вторую клеточные массы не смешивают друг с другом, но приводят друг с другом в тесный контакт, и выращивание первой и второй клеточной массы в указанном поддерживающем носителе, где мезенхимные клетки включают в себя вышеописанные мезенхимные клетки для формирования зуба.
В третьем аспекте настоящего изобретения предлагаются мезенхимные клетки для формирования зуба, которые индуцированы из стволовых тотипотентных клеток и являются CD44-позитивными и CD29-позитивными или CD44-позитивными и CD106-позитивными.
По настоящему изобретению предлагается способ получения мезенхимных клеток, с помощью которого желаемые зубы могут быть эффективно получены в большом количестве, и способ получения зуба, где зубы, сохраняющие организацию клеток, характерную для эмали и дентина, могут быть эффективно получены в большом количестве.
Краткое описание графических материалов
Фиг.1 представляет собой схематическое концептуальное изображение, показывающее образование зубного зачатка.
Фиг.2А показывает состояние двойного окрашивания CD44 и CD29 клеток ЕС (клеток эмбриональной карциномы) по Примеру 1 настоящего изобретения.
Фиг.2В показывает состояние двойного окрашивания CD44 и CD29 на 6 сутки после обработки ДМСО по Примеру 1 настоящего изобретения.
Фиг.2С показывает состояние двойного окрашивания CD44 и CD29 выбранных CD44-позитивных и CD29-позитивных клеток по Примеру 1 настоящего изобретения.
Фиг.3А представляет собой схематическое концептуальное изображение, показывающее процедуру по Примерам настоящего изобретения для реконструкции зубного зачатка с применением мезенхимных клеток и эпителиальных клеток, имеющих происхождение из зубного зачатка, и показывающее состояние гелевой упаковки до организации клеток.
Фиг.3В представляет собой схематическое концептуальное изображение, показывающее процедуру по Примерам настоящего изображения для реконструкции зубного зачатка с применением мезенхимных клеток и эпителиальных клеток, имеющих происхождение из зубного зачатка, и показывающее состояние позиционирования первой клеточной массы в гелевой упаковке.
Фиг.3С представляет собой схематическое концептуальное изображение, показывающее процедуру по Примерам настоящего изобретения для реконструкции зубного зачатка с применением мезенхимных клеток и эпителиальных клеток, имеющих происхождение из зубного зачатка, и показывающее позиционирование второй клеточной массы в гелевой упаковке.
Фиг.3D представляет собой схематическое концептуальное изображение, показывающее процедуру по Примерам настоящего изобретения для реконструкции зубного зачатка с применением мезенхимных клеток и эпителиальных клеток, имеющих происхождение из зубного зачатка, и показывающее затвердевшее состояние гелевой упаковки, в которой позиционируется первая клеточная масса и вторая клеточная масса.
Фиг.4А представляет собой окрашенное НЕ (гематоксилин+эозин) изображение зубного зачатка по Примеру 4 настоящего изобретения, полученного из эпителиальной ткани зубного зачатка и из мезенхимной ткани зубного зачатка (увеличение: × 100).
Фиг.4В представляет собой окрашенное НЕ изображение зубного зачатка по Примеру 4 настоящего изобретения, полученного из эпителиальной ткани зубного зачатка и клеток DMSO-EC (увеличение: × 100).
Фиг.4С представляет собой окрашенное НЕ изображение зубного зачатка по Примеру 4 настоящего изобретения, полученного из эпителиальной ткани зубного зачатка и клонированных клеток DMSO-EC (увеличение: × 100).
Фиг.5А показывает состояние двойного окрашивания CD44 и CD29 клеток ЕС по Примеру 5 настоящего изобретения.
Фиг.5В показывает состояние двойного окрашивания клеток CD44 и CD29 на 7 сутки после обработки RA по Примеру 5 настоящего изобретения.
Фиг.5С показывает состояние двойного окрашивания клеток CD44 и CD29 выбранных CD44-позитивных и CD29-позитивных клеток по Примеру 5 настоящего изобретения.
Фиг.6 представляет собой окрашенное НЕ изображение зубного зачатка, полученного из CD44-позитивных и CD106-позитивных клеток, полученных обработкой RA по Примеру 5 настоящего изобретения, и эпителиальной ткани зубного зачатка (увеличение: × 200, полоса соответствует 50 мкм).
Фиг.7А показывает состояние двойного окрашивания CD44 и CD106 из клеток ЕС по Примеру 6 настоящего изобретения.
Фиг.7В показывает состояние двойного окрашивания CD44 и CD106 из клеток на 7 сутки после обработки RA по Примеру 6 настоящего изобретения.
Фиг.7C показывает состояние двойного окрашивания CD44 и CD106 из отобранных CD44-позитивных и CD106-позитивных клеток по Примеру 6 настоящего изобретению.
Лучший вариант осуществления изобретения
Способ получения мезенхимных клеток
Способ получения мезенхимных клеток по настоящему изобретению является способом получения мезенхимных клеток для формирования зуба, при этом способ включает выращивание стволовых тотипотентных клеток в присутствии индуктора дифференцировки с целью получения популяции клеток после обработки индуктором дифференцировки, при этом популяция клеток содержит CD44-позитивные и CD29-позитивные клетки или CD44-позитивные и CD106-позитивные клетки, и отбор из популяции клеток после обработки индуктором дифференцировки CD44-позитивных и CD29-позитивных клеток или CD44-позитивных и CD106-позитивных клеток в качестве мезенхимных клеток для формирования зуба.
В настоящем изобретении было обнаружено, что CD44-позитивные и CD29-позитивные клетки или CD44-позитивные и CD106-позитивные клетки, полученные индукцией дифференцировки стволовых тотипотентных клеток, могут применяться в качестве мезенхимных клеток для формирования зуба. Согласно этому мезенхимные клетки, необходимые для формирования зуба, могут быть получены из источников иных, чем зуб или зубной зачаток, полученных из живого организма, и они не требуются для получения мезенхимных клеток необходимых для формирования зуба. В результате необходимое количество мезенхимных клеток можно легко получить, в некоторых случаях в больших количествах, обходя такие обстоятельства, как незначительное количество клеток, непосредственно собранных из зубного зачатка или возможные ограничения источника поступления.
В настоящем изобретении термин "зуб" означает ткань, имеющую сплошной слой дентина внутри и слой эмали снаружи, конкретно ткань, имеющую анизотропию вследствие наличия коронки и корня. Анизотропия зуба может быть идентифицирована расположением коронки и корня. Коронка и корень могут визуально различаться по их форме, гистологическому окрашиванию и тому подобное. Коронка является частью, имеющей структуру из слоев эмали и дентина, а в корне слой эмали отсутствует.
Дентин и эмаль могут быть легко морфологически идентифицированы специалистами в данной области техники путем гистологического окрашивания или тому подобное. Эмаль может быть также идентифицирована наличием энамелобласта, что можно удостоверить наличием/отсутствием амелогенина. С другой стороны, дентин можно идентифицировать наличием одонтобласта, что можно удостоверить наличием/отсутствием сиалопротеина. Подтверждение наличия амелогенина или сиалопротеина можно выполнить способами, хорошо известными специалистам в данной области техники, и примеры способа включают гибридизацию in situ и окрашивание антителом или тому подобное.
Мезенхимные клетки по настоящему изобретению первоначально можно применить для формирования зубного зачатка с целью формирования зуба.
В настоящем изобретении термины "зубной зачаток" и "зародыш зуба" применяют, чтобы сослаться на разницу, основанную на различии в стадиях, описанную ниже. В этом случае "зубной зачаток" означает эмбрион на ранней стадии развития зуба, которому еще предстоит стать зубом в будущем, то, что по традиционной классификации стадий развития зуба находится на стадии зачатка зуба или стадии колокола, и особенно подразумевает такую ткань, в которой еще не наблюдается накопление эмали и дентина, характерных для твердых тканей зуба. С другой стороны, «зародыш зуба» означает ткань на переходной стадии от "зубного зачатка", применяемого в настоящем изобретении, когда начинается накопление дентина и эмали, характерных для твердой ткани зуба и стадия обособления от десен для выполнения типичных функций зуба.
В процессе онтогенеза развитие зуба из зубного зачатка на стадии зачатка в свою очередь проходит каждую из стадий, шапочкообразная почка, ранняя стадия колокола и поздняя стадия колокола, как показано на Фиг.1. Здесь на стадии зачатка эпителиальные клетки инвагинируются таким образом, что они «обертываются» вокруг мезенхимных клеток, а достигнув ранней стадии колокола и поздней стадии колокола, порция эпителиальных клеток становится внешней эмалью, а порция мезенхимных клеток внутри начинает формировать дентин. Поэтому зуб формируется из зубного зачатка путем межклеточного взаимодействия между эпителиальными клетками и мезенхимными клетками.
В настоящем изобретении термин "мезенхимная клетка" означает клетку, происходящую из мезенхимной ткани, а "эпителиальная клетка" означает клетку, происходящую из эпителиальной ткани.
Дополнительно в настоящем изобретении "периодонтальная ткань" означает альвеолярный отросток и периодонтальную мембрану, формирующуюся в основном во внешнем слое зуба. Альвеолярный отросток и периодонтальную мембрану специалисты в данной области техники могут морфологически легко различить путем гистологического окрашивания или тому подобное.
Теперь будут описаны мезенхимные клетки по настоящему изобретению для формирования зуба.
Предпочтительно применяются стволовые тотипотентные клетки, применяемые для получения мезенхимных клеток по настоящему изобретению для формирования зуба, имеющие отношение к клеткам, обладающим потенциалом для мультидифференцировки, которые могут дифференцироваться в два или более типа клеток, и к клеткам, выбранным из группы, состоящей из клеток эмбриональной карциномы, эмбриональных стволовых клеток и эмбриональных клеток зародышевого пути. Среди них наиболее предпочтительными с точки зрения доступности являются клетки эмбриональной карциномы (далее именуемые "клетками ЕС"). Клетками ЕС, применимыми по настоящему изобретению, могут служить клетки, полученные из любой ткани, такой как нерв, семенник или яичник. Примеры такой клетки ЕС включают NCR-G3 клетку и NTERA-2 клетку, полученные у человека, и линии клеток, полученные у мыши, такие как с-1300 клетка, F9 клетка, LT-2 клетка, ОТТ6050 клетка, РСС4 клетка, Р19 клетка, МЕТТ-1 клетка или STT-3 клетка. Эти клетки можно соответствующим образом отобрать, в зависимости от намечаемого применения из клеток, полученных у различных животных, например приматов (например, человека и обезьяны) и копытных (например, свиньи, коровы и лошади), являющихся млекопитающими, и грызунов (например, мыши, крысы и кролика), являющихся мелкими млекопитающими. Примерами клеточной линии эмбриональной карциномы, полученной у мыши, являются вышеупомянутые линии клеток и полученные из них клоны.
Средой для выращивания стволовых тотипотентных клеток могут служить традиционно применяемые культуральные среды. Примеры сред, которые могут применяться для выращивания, включают среды, обычно применяемые для выращивания клеток животных, такая как среда Игла, модифицированная Дульбекко (DMEM). К этой среде для способствования росту клеток можно добавлять сыворотку или, в качестве альтернативы сыворотке, клеточный фактор роста, такой как FGF (фактор роста фибробластов), EGF (эпидермальный фактор роста) или PDGF (тромбоцитарный фактор роста), или известный компонент сыворотки, такой как трансферрин. В случаях, если добавляется сыворотка, ее концентрация может соответственно изменяться в зависимости от условий выращивания, обычно она составляет 10%. Для культуры клеток могут применяться обычные условия культуральной среды, такие как для культур в инкубаторе при 37°С и при 5% CO2. Можно также добавлять антибиотик(и), такой как стрептомицин.
В настоящем изобретении обработка для индукции дифференцировки стволовых тотипотентных клеток выполняется выращиванием в присутствии индуктора дифференцировки. При этой обработке для индукции дифференцировки клеточная популяция, содержащая CD44-позитивные и CD29-позитивные клетки или CD44-позитивные и CD106-позитивные клетки, образуется из стволовых тотипотентных клеток. Достаточно, чтобы клеточная популяция, полученная при обработке для индукции дифференцировки, содержала вышеописанные CD44-позитивные и CD29-позитивные клетки или CD44-позитивные и CD106-позитивные клетки, и она может содержать оба этих типа клеток.
Примеры пригодного для применения вышеупомянутого индуктора дифференцировки включают любой фактор, индуцирующий дифференцировку CD44-позитивной клетки из стволовых тотипотентных клеток в клетке, экспрессирующей CD44. Примеры такого фактора, индуцирующего CD44-позитивную клетку, включают факторы, индуцирующие клетки нервного гребешка, факторы, ответственные за развитие клеток нервного гребешка, и факторы, являющиеся промоторами роста клеток нервного гребешка. Фактор, являющийся индуктором клеток нервного гребня, является фактором, способным индуцировать превращение стволовой тотипотентной клетки в клетку нервного гребня или клетку из него происходящую (например, клетку гладкой мышцы или клетку сердечной мышцы), и примеры фактора включают диметилсульфоксид (DMSO), дексаметазон (Dex), циклоаденозинмонофосфат (сАМР), гексаметилен-бис-ацетамид, 5′-азацитидин, трансформирующий фактор роста бета (TGF(3) и ноггин. Примеры факторов, ответственных за развитие клеток нервного гребня, включают ретиноевую кислоту (RA), факторы BMP-4, BMP-7, Shh, Wnt, фактор роста фибробластов 2 (FGF2), эндотелин-1, эндотелин-3, активинβА, тромбоцитарный фактор роста (PDGF) и фактор роста эндотелия сосудов (VEGF). Примеры факторов, запускающих рост клеток нервного гребня, включают FGF2, FGF8, FGF10, BMP-2, SCF и активный витамин D3. Фактор, индуцирующий клетки нервного гребня, фактор, ответственный за развитие клеток нервного гребня, и фактор, запускающий рост клеток нервного гребня, могут быть точно не отличимы один от другого и каждый из них можно применять поодиночке или два или более, в комбинации. Среди прочих в настоящем изобретении предпочитаются DMSO и RA, которые могут применяться поодиночке или в комбинации, способные эффективно производить далее упомянутую интересующую клеточную популяцию.
Эти индукторы дифференцировки можно добавлять к среде клеток, способных к дифференцировке, в такой концентрации, при которой возможна индукция дифференцировки. Отсюда концентрация, при которой возможна индукция пролиферации, различна в зависимости от природы индуктора и типа применяемых стволовых тотипотентных клеток.
В случае DMSO его концентрация может быть главным образом от 0,5 об.% до 10 об.% и с точек зрения выживаемости клеток при обработке и выхода интересующих клеток, получаемых в культуре, предпочтительно от 2,5 об.% до 5 об.%, более предпочтительно от 4 об.% до 5 об.%, относительно объема среды. Дифференцировка тотипотентных стволовых клеток может быть индуцирована в достаточной степени, как только концентрация станет не меньше чем 2,5 об.%, и выход интересующих клеток не уменьшается чрезмерно если концентрация не превышает 5 об.%.
В случае RA ее концентрация может быть главным образом от 0,1 мкМ по объему до 10 мкМ по объему и с точек зрения выживаемости клеток при обработке и выхода интересующих клеток, получаемых в культуре, предпочтительно от 0,5 мкМ по объему до 5 мкМ по объему, более предпочтительно от 0,5 мкМ по объему до 2 мкМ по объему, относительно объема среды. Дифференцировка стволовых тотипотентных клеток может быть индуцирована в достаточной степени, как только концентрация станет не меньше чем 0,1 мкМ по объему, и выход интересующих клеток не уменьшается чрезмерно, если концентрация не превышает 10 мкМ по объему.
Обработка для индукции дифференцировки стволовых тотипотентных клеток проводится культурированием стволовых клеток, способных к дифференцировке, в присутствии вышеописанного индуктора(ов) дифференцировки. Хотя время обработки для индукции дифференцировки варьируют в зависимости от концентрации индуктора(ов) дифференцировки и активности роста клеток, в основном оно может составлять от 2 часов до 3 суток и, с точек зрения выживаемости клеток и выхода клеток интереса, получаемых в культуре, предпочтительно от 6 часов до 24 часов. В значительной степени дифференцированные клетки могут эффективно получаться при времени не меньше чем 6 часов и выход интересующих клеток не уменьшается чрезмерно, если время не превышает 24 часа.
Имеется определенное соотношение между временем обработки стволовых тотипотентных клеток, индукцией дифференциации и концентрацией индуктора(ов) дифференцировки, позволяющей эффективное осуществление индукции дифференцировки стволовых тотипотентных клеток. То есть период времени выращивания в присутствии индуктора(ов) дифференцировки (время обработки) варьируют в зависимости от концентрации индуктора(ов) дифференцировки и типа индуктора(ов) дифференцировки, но в случае специфичного индуктора дифференцировки, когда количество дней выращивания фиксировано, обычно для концентрации имеется предпочтительный диапазон. Дополнительно в случаях, если количество суток выращивания уменьшается, диапазон оптимальных концентраций сдвигается в сторону более высоких концентраций, в то время как в тех случаях, когда количество суток выращивания увеличивается, диапазон оптимальных концентраций сдвигается в сторону более низких концентраций. Принимая во внимание эти факторы, эффект индукции дифференцировки может проявляться в широких диапазонах концентраций путем подбора количества дней выращивания, и специалисты в данной области техники смогут легко определить оптимальный диапазон концентраций, в которых может проявляться индуцирующий эффект.
В клеточной популяции, полученной после обработки для индукции дифференцировки путем вышеописанной обработки для индукции дифференцировки, существует клеточная популяция, содержащая CD44-позитивные и CD29-позитивные клетки или CD44-позитивные и CD106-позитивные клетки. Также в клеточной популяции могут содержаться оба типа клеток. После обработки для индукции дифференцировки клеточная популяция подвергается селекционной обработке, при которой в качестве мезенхимных клеток для формирования зуба отбираются CD44-позитивные и CD29-позитивные клетки или CD44-позитивные и CD106-позитивные клетки.
Для селекции клеток может применяться любой способ, при условии, что им можно отбирать мезенхимные клетки по настоящему изобретению, как выше описано. Примеры таких способов селекции включают способы селекции, основанные на моделях генной экспрессии, поверхностных клеточных антигенах и морфологии, и один или более из этих способов можно применять для селекции стволовых тотипотентных клеток. Способ селекции с точки зрения эффективности предпочтительно является способом, применяющим сортировку клеток на основе экспрессии на поверхности клеток, и для того чтобы гарантированно отобрать мезенхимные клетки, предпочтительно применять комбинацию многих способов, особенно комбинацию профиля генной экспрессии и поверхностно-клеточного антигена.
Мезенхимные клетки для формирования зуба, отбираемые по настоящему изобретению, являются CD44-позитивными и вдобавок обладают свойствами CD29-позитивных или CD106-позитивных клеток. Про CD44 известно, что он представляет собой мембранный белок, который экспрессируется на поверхности клетки как гиалуронановый рецептор. С другой стороны, про CD29 известно, что он является мембранным белком, который экспрессируется на клеточной поверхности как молекула интегрина β1 и про который сообщалось, что он является слабо позитивным у клеток ЕС и экспрессируется в мезенхимных клетках на уровне мРНК. Про CD106 известно, что он является молекулой VCAM-1, про которую известно, что она является адгезионной молекулой, часто применяемой в качестве маркера для эпителиальных клеток. Клетки, демонстрирующие такие свойства, можно применять в качестве мезенхимных клеток для формирования зуба, как описано ниже.
Мезенхимные клетки по настоящему изобретению для формирования зуба могут являться популяцией, являющейся CD44-позитивной и также позитивной по меньшей мере по одному из антигенов CD29 и CD106, а также могут являться популяцией, содержащей тройные позитивные клетки, то есть позитивные по всем из антигенов CD44, CD29 и CD106.
Мезенхимные клетки по настоящему изобретению для формирования зуба также можно отбирать на основании свойств клеток иных, чем выше описанные свойства антигенов CD44, CD29 и CD106.
Примеры других свойств клеток включают другие профили поверхностно-активных антигенов и профили генной экспрессии. Примеры профилей клеточной экспрессии антигенов включают CD14-негативные, CD34-негативные и CD45-негативные профили и их можно применять поодиночке или в комбинации. Примеры генной экспрессии включают, но не ограничены ими, экспрессию генов Slug, Wnt5a, Lhx8, BMP4, Рах3, Рах9, Msx1 и отсутствие экспрессии генов Oct3/4, nanog, Sox9 и Sox5 и их можно применять поодиночке или в комбинации.
Мезенхимные клетки для формирования зуба по настоящему изобретению в добавление к вышеописанным CD44, CD29 и CD106, предпочтительно, экспрессируют по меньшей мере один ген, выбранный из группы генов Slug, Рах3, Msx1 и Рах9, более предпочтительно экспрессируют, как Slug ген, так и Рах3 ген, еще более предпочтительно экспрессируют все четыре гена благодаря их высокому потенциалу в образовании зуба.
Для подтверждения этих антигенов поверхности клеток и профилей генной экспрессии и основанной на них селекции применяют различные антитела, узнающие антигены поверхности, последовательности нуклеиновых кислот, с помощью которых можно подтвердить экспрессию и тому подобное. Все эти антитела и последовательности нуклеиновых кислот известны и их можно легко получить. Подтверждение и селекция на основании этих антигенов поверхности и профилях генной экспрессии могут проводиться с применением способов, общепринятых в таких приложениях, как иммуноокрашивание различными антителами, проточная цитометрия, сортировка клеток или РВ-ПЦР (полимеразная цепная реакция в реальном времени).
В способе получения клетки по настоящему изобретению клонирование с целью получения единичной мезенхимной клетки может применяться в сочетании с вышеприведенным способом селекции. Примерами способа клонирования являются способы, обычно применяемые для этой цели, такие как способ серийных разведений, сортировка клеток и клонзапирающие кольца. Хотя клонирование может проводиться или до, или после селекции вышеописанным способом селекции, предпочтительно, чтобы повысить эффективность получения мезенхимной клетки(ок), проводить его после селекции.
Для эффективного получения желаемого количества клеток на стадии селекции перед стадией селекции можно провести стадию пролиферации. На этой стадии пролиферации выращивание клеточной популяции после индукции дифференцировки проводят, применяя среду для нормальной культуры, не содержащую индуктора дифференцировки. По этому способу интересующим клеткам, дифференцировка которых была индуцирована, позволяют пролиферировать до установленного числа клеток. В результате селекцию можно легко проводить, имея достаточное количество клеток.
Хотя временной период для такой стадии пролиферации может быть легко установлен на основании данных о количестве клеток и их состоянии после обработки индукцией дифференцировки, с точки зрения эффективной концентрации клеток интереса, временной период может в основном составлять от 3 до 30 суток, предпочтительно от 5 до 10 суток. В результате интересующие мезенхимные клетки для формирования зуба, содержащиеся в клеточной популяции, подвергаются селекции и после стадии селекции мезенхимные клетки по настоящему изобретению могут быть эффективно получены в большом количестве.
Мезенхимные клетки, полученные по способу настоящего изобретения, применяют для формирования зуба. Формирование зуба может проводиться любым способом, при условии, что в способе используются мезенхимные клетки по настоящему изобретению, и эти клетки наиболее предпочтительно применять в нижеследующем способе по настоящему изобретению для получения зуба.
Далее будет описываться способ получения зуба по настоящему изобретению.
Способ получения зуба
Предпочтительный способ получения зуба с применением мезенхимных клеток по настоящему изобретению включает в себя позиционирование в поддерживающем носителе первой клеточной массы, по существу состоящей только из одного типа клеток, выбранного из мезенхимных клеток и эпителиальных клеток, и второй клеточной массы, по существу состоящей только из другого типа клеток, выбранного из мезенхимных клеток и эпителиальных клеток, причем первую и вторую клеточные массы не смешивают друг с другом, но приводят друг с другом в тесный контакт (стадия позиционирования), и выращивание первой второй клеточной массы в указанном поддерживающем носителе (стадия выращивания); где мезенхимные клетки включают в себя вышеописанные мезенхимные клетки для формирования зуба.
В способе получения по настоящему изобретению, поскольку мезенхимные клетки и эпителиальные клетки выращивают в виде клеточных масс в поддерживающем носителе при условии, что массы не смешиваются друг с другом, но находятся в тесном контакте, межклеточное взаимодействие может легко осуществляться ввиду тесного контакта так, чтобы зуб имел расположение клеток, характерное для зуба, то есть дентин внутри и эмаль снаружи. Отсюда клеточная масса, состоящая в основном из мезенхимных клеток, содержит мезенхимные клетки по настоящему изобретению для формирования зуба таким образом, чтобы зубы, имеющие характерное расположение клеток, можно было получать в большом количестве.
На стадии позиционирования первая клеточная масса и вторая клеточная масса приводятся в контакт друг с другом и позиционируются в поддерживающем носителе.
Поэтому и первая клеточная масса, и вторая клеточная масса по существу состоит только из мезенхимных клеток или только эпителиальных клеток. Клеточная масса по существу состоит только из мезенхимных клеток, включающих вышеупомянутые мезенхимные клетки для формирования зуба. Клеточная масса, содержащая мезенхимные клетки для формирования зуба, может быть приготовлена на стадии получения согласно вышеупомянутому способу получения, а, с другой стороны, клеточная масса, по существу состоящая только из эпителиальных клеток, может быть получена независимо от клеточной массы, по существу состоящей из мезенхимных клеток (первая стадия получения клеток и вторая стадия получения клеток).
Термин "клеточная масса" означает состояние, где клетки являются плотно упакованными, и клетки могут находиться в состоянии ткани или в состоянии клеточной массы (клеточного агрегата), полученного из единичных клеток. Термин "по существу состоит" означает, что количество материи, состоящей из клеток иных, чем интересующие клетки, является настолько малым, насколько возможно. Поэтому клеточная масса, состоящая из эпителиальных клеток, может являться частью ткани или массы из единичных клеток. Как эпителиальные клетки, так и мезенхимные клетки могут также образовывать клеточные массы, составленные из единичных клеток.
Каждая из клеточных масс, первая клеточная масса и вторая клеточная масса могут составляться из эпителиальных клеток или мезенхимных клеток. Количества клеток, составляющих эти клеточные массы, варьирует в зависимости от вида животного и от типа, твердости и размера поддерживающего носителя и могут обычно составлять от 101 до 108 клеток и предпочтительно от 103 до 108 клеток на клеточную массу.
Так как клеточная популяция, по существу состоящая из мезенхимных клеток, содержит мезенхимные клетки для формирования зуба, она все же может содержать иные мезенхимные клетки.
Примерами мезенхимных клеток иных, чем вышеописанные мезенхимные клетки, могут являться мезенхимные клетки, имеющие происхождение из зубного зачатка и других источников. Примеры мезенхимных клеток, имеющих происхождение из источников иных, чем зубной зачаток, включают клетки, имеющие происхождение из других мезенхимных тканей в организме, таких как, предпочтительно, клетки костного мозга, не содержащие клетки крови, и мезенхимные стволовые клетки, более предпочтительно, мезенхимные клетки полости рта, клетки костного мозга внутри нижней челюсти, мезенхимные клетки, имеющие происхождение из клеток краниального нервного гребня, предшественников мезензимных клеток, которые могут генерировать мезенхимные клетки и их стволовые клетки.
Эпителиальные клетки, применяемые по настоящему изобретению, предпочтительно получают из зубного зачатка таким образом, чтобы они могли воспроизвести взаимное расположение клеток в живом организме и эффективно сформировать зуб, имеющий характерную структуру и анизотропию, и, предпочтительно, на стадии между зародыш зуба и шапкообразной почкой, имея в виду незрелость и гомогенность стадии дифференцировки клеток.
Эпителиальными клетками также могут являться те, которые образованы не из зубного зачатка, и их примеры включают клетки, имеющие происхождение из других эпителиальных тканей живого организма. Предпочтительные примеры эпителиальных клеток включают клетки эпителия кожи, слизистых оболочек и десен полости рта и более предпочтительные примеры клеток эпителия включают незрелые клетки предшественников эпителия, способные производить дифференцированные, например кератинизированные (ороговевшие) или паракератинизированные эпителиальные клетки кожи, слизистой оболочки и тому подобное. Примерами таких незрелых предшественников клеток эпителия являются неороговевшие клетки эпителия и их стволовые клетки.
В случаях выделения клеток для получения клеточной массы из тканей, зубной зачаток и другие ткани могут быть получены из нижней челюсти и тому подобное различных животных, например приматов, таких как человек и обезьяна, и копытных, таких как свинья, корова и лошадь, являющихся млекопитающими, и грызунов, таких как мышь, крыса и кролик, являющихся мелкими млекопитающими. Для сбора зубных зачатков и тканей могут применяться условия, обычно применяемые для сбора ткани без модификации, и зубной зачаток и ткань могут быть собраны в стерильных условиях и их можно хранить в надлежащем консервирующем растворе. Примерами зубного зачатка человека являются зубной зачаток третьего моляра, который является так называемым зубом мудрости, а также зубной зачаток плода, и, с точки зрения использования аутогенных тканей, предпочтителен зубной зачаток зуба мудрости.
В случаях, когда вышеупомянутые клетки получают из ткани, например, зубного зачатка, зубной зародыш, отделенный от окружающей ткани, сначала разделяют на мезенхимную ткань зубного зачатка и эпителиальную ткань зубного зачатка на основе их форм. Так как ткань зубного зачатка можно структурно идентифицировать под микроскопом, ее можно легко изолировать расчленением или разрезанием с применением анатомических ножниц, пинцетов и тому подобное. Выделение мезенхимной ткани зубного зачатка и эпителиальной ткани зубного зачатка из зубного зачатка может быть легко выполнено на основе их форм расчленением или разрезанием с применением игл для инъекции, вольфрамовых игл, пинцетов и тому подобное.
Предпочтительно для простого выделения клеток зубного зачатка из окружающей ткани и/или выделения эпителиальной ткани и мезенхимной ткани из ткани зубного зачатка применяют фермент. Примеры фермента, применяемого в таких целях, включают диспазу, коллагеназу и трипсин.
Клетки, составляющие клеточные массы, могут быть получены переводом из состояния собранной ткани в состояние единичных клеток. На стадии получения для упрощения диспергирования до единичных клеток может применяться фермент. Примеры такого фермента включают диспазу, коллагеназу и трипсин. В этом случае для выделения эпителиальных клеток из ткани эпителия, предпочтительно, применять обработку трипсином и обработку ДНКазой после обработки коллагеназой. С другой стороны, для выделения мезенхимных клеток из мезенхимной ткани предпочтительно применять одновременную обработку коллагеназой и трипсином и затем применять обработку ДНКазой. В этом случае обработку ДНКазой применяют, чтобы предотвратить уменьшение количества извлекаемых клеток из-за агрегации клеток, обусловленной ДНК, высвобождаемой в раствор, при повреждении части клеток обработкой ферментом и лизисе клеточной мембраны.
Клетки, составляющие клеточные массы, могут подвергаться предварительному выращиванию до стадии позиционирования для получения достаточного количества клеток каждого типа. Для выращивания клеток могут без модификации применяться условия, обычные для выращивания клеток животных, такие как температура.
В качестве культуральной среды может применяться среда, обычно применяемая для выращивания клеток животных, такая как среда Игла, модифицированная Дульбекко (DMEM), и может добавляться сыворотка для стимулирования клеточной пролиферации или, в качестве альтернативы сыворотке, фактор роста клеток, такой как FGF, EGF или PDGF, или известный компонент сыворотки, такой как трансферрин. В случаях, когда добавляется сыворотка, ее концентрация может изменяться в соответствии с условиями выращивания и обычно может составлять 10 об.%. Для выращивания клеток могут применяться нормальные условия, такие как для культур в инкубаторе при 37°С и при 5% CO2. Может быть добавлен антибиотик, такой как стрептомицин.
В случаях, когда применяется предварительное выращивание мезенхимных клеток, процедура может совпадать с вышеупомянутым выращиванием для пролиферации мезенхимных клеток для формирования зуба или может проводиться после стадии селекции или совпадать с обоими стадиями.
С целью сохранения свойств клеток предварительное выращивание мезенхимных клеток и вышеупомянутое выращивание для простой пролиферации мезенхимных клеток для формирования зуба проводится в среде, не содержащей вышеупомянутый индуктор дифференцировки.
В отношении организации клеточных масс на стадии позиционирования, первая и вторая клеточная массы позиционируются в поддерживающем носителе, способном поддерживать клетки в контакте. В этом случае клеточные массы не смешиваются друг с другом. Так, поскольку клеточные массы позиционируются без смешивания друг с другом, между клеточными массами формируется пограничная поверхность. Такой способ позиционирования называют "компартментализацией", как принято в описании настоящего изобретения.
Поддерживающий носитель, применяемый здесь, может являться носителем, в котором возможно выращивание клеток, и предпочтительно смесью с вышеописанной средой. Примерами такого поддерживающего носителя являются коллаген, гель агарозы, карбоксиметилцеллюлоза, желатин, агар, гидрогель, Cellmatrix (торговое название), Mebiol Gel (торговое название), Matrigel (торговое название), эластин, фибрин, ламинин, смесь экстрацеллюларного матрикса, полигликолевая кислота (PGA), полиуксусная кислота (PLA) и сополимер молочной кислоты и гликолевой кислоты (PLGA). Эти поддерживающие носители могут обладать твердостью, достаточной для практического поддержания клеток в местоположении, где они позиционированы в поддерживающем носителе, и примеры поддерживающего носителя включают носители в форме геля, волокна и твердого тела. Среди них с учетом того, что гели, такие как смеси внеклеточного матрикса имеют тенденцию обеспечивать необходимую твердость и удерживающую способность, более предпочтительными являются коллаген, гель агарозы, карбоксиметилцеллюлоза, желатин, агар, гирогель, Cellmatrix, Mebiol Gel, Matrigel, смесь внеклеточного матрикса, эластин, фибрин и ламинин. В этом случае твердость, при которой клетки могут практически поддерживаться в своих местоположениях, может являться твердостью, которая необходима для трехмерного выращивания, то есть твердостью, при которых сохраняется положение клеток и при этом не ингибируется гипертрофия клеток благодаря их пролиферации, и такую твердость можно легко определить.
Кроме того, в этом случае поддерживающий носитель может иметь консистенцию, достаточную для обеспечения роста первой и второй клеточной массы внутри нее, и консистенция может быть надлежащим образом установлена в зависимости от размера интересующей ткани и тому подобное,
Дополнительно поддерживающий носитель может иметь удерживающую способность, посредством которой клетки в состоянии поддерживать состояние контакта, не рассеиваясь. Под выражением "состояние контакта" здесь понимают предпочтительно плотно упакованное (высокой плотности) состояние, которое обеспечивает межклеточное взаимодействие внутри данной клеточной массы и между клеточными массами, и при этом такое состояние высокой плотности в агрегате клеток позволяет выращивание клеток при степени удерживания, например такой, при которой может поддерживаться состояние более сильного контакта, чем состояние простого касания. Например, в случае коллагена приемлемая твердость обеспечивается применением конечной концентрации от 2 до 3 мг/мл, которая представляет собой концентрацию, обуславливающую прочность геля от 120 г до 250 г по способу JIS-K6503-1996 (измеряемая как нагрузка, необходимая для опускания на 4 мм, применяя поршень с диаметром 12,7 мм). Прочность геля не ограничивается, и в качестве поддерживающих носителей по настоящему изобретению могут предпочтительно применяться и другие поддерживающие носители, если они имеют ту же прочность геля, полученную на основании того же способа оценки. Кроме того, поддерживающий носитель, имеющий ту же твердость, соответствующую желаемой прочности геля, может быть получен смешиванием более одного вида поддерживающего носителя.
Состояние высокой плотности подразумевает плотность, почти эквивалентную плотности построения ткани, например, для клеточных масс 5×107-1×109 клеток/мл к моменту позиционирования клеток, предпочтительно 1×108-1×109 клеток/мл, чтобы обеспечить межклеточное взаимодействие без нарушения активности клеток, наиболее предпочтительно 2×108-8×108 клеток/мл. Для получения клеточной массы, имеющей такую клеточную плотность, предпочтительно концентрировать и осаждать клетки центрифугированием, поскольку оно, как считается, обеспечивает достижение высокой плотности без нарушения клеточной активности. Такое центрифугирование может проводиться при скорости вращения эквивалентной силе центрифугирования от 300 до 1200×g, которая не влияет отрицательно на выживаемость клеток и предпочтительно 500-1000×g, в течение от 3 до 10 минут. Центрифугирование при менее 300×g возможно приведет к недостаточному осаждению клеток и клеточная плотность может оказаться низкой, в то время как центрифугирование при более 1200×g может вызвать повреждение клеток, и поэтому оба этих варианта не являются предпочтительными.
В случаях, когда высокая клеточная плотность достигается центрифугированием, обычно центрифугирование проводят после получения суспензии единичных клеток в контейнере, таком как пробирка для центрифугирования и надосадочную жидкость удаляют с наиболее возможной степенью полноты, оставляя клетки в осадке. Для полного удаления надосадочной жидкости предпочтительно силиконизировать контейнер, такой как пробирка.
В случаях, когда осадки получают центрифугированием, они могут непосредственно позиционироваться в поддерживающем носителе. При этом объем компонентов иных, чем интересующие клетки (например, объем среды для выращивания, буферного раствора, поддерживающего носителя или тому подобное), предпочтительно не должен превышать объем клеток, и наиболее предпочтительно, чтобы не содержались компоненты иные, чем интересующие клетки интереса. В такой клеточной массе высокой плотности клетки находятся в тесном контакте друг с другом, и межклеточное взаимодействие может эффективно осуществляться. В частности, если клеточная масса, содержащая только чрезвычайно малые количества компонентов иных, чем клетки интереса, позиционируется внутри поддерживающего носителя, клетки дополнительно агрегируются по причине затвердевания поддерживающего носителя и тому подобное, что обеспечивает состояние, при котором клетки наиболее плотно упакованы.
В случаях, когда клетки применяют в состоянии ткани, является предпочтительным удалять компоненты иные, чем интересующие клетки, такие как соединительная ткань и тому подобное, применяя ферментативную обработку или тому подобное. Если имеется много компонентов иных, чем интересующие клетки, например, в случаях, если иных компонентов не меньше, чем клеток, межклеточное взаимодействие не может осуществляться в достаточной степени, что не является предпочтительным.
Чем теснее контакт между первой клеточной массой и второй клеточной массой, тем лучше, и особенно предпочтительно, если вторая клеточная масса позиционируется таким образом, что сдавливает первую клеточную массу. Кроме того, обертывание вокруг первой клеточной массы и второй клеточной массы твердым веществом, не ингибирующим среду для выращивания или не препятствующим проникновению кислорода, также эффективно в создании более тесного контакта между клеточными массами. Также, предпочтительно добавлять клеточную суспензию высокой плотности к раствору, имеющую различную вязкость, чтобы позиционировать там клеточную суспензию, с последующим затвердеванием раствора как он есть, так как с помощью этого можно легко достигнуть поддержания контакта клетки. Также, если первая клеточная масса представляет собой массу из единичных мезенхимных клеток зубного зачатка, а вторая клеточная масса представляет собой эпителиальную ткань зубного зачатка, предпочтительно позиционировать узлы эмали эпителиальной ткани зубного зачатка в контакте с первой клеточной массой, однако, настоящее изобретение не ограничено только этим.
В случае, если поддерживающий носитель находится в форме геля, раствора или тому подобное, за стадией позиционирования может следовать стадия затвердевания, во время которой поддерживающий носитель затвердевает. После стадии затвердевания, клетки, позиционируемые внутри поддерживающего носителя, могут фиксироваться внутри поддерживающего носителя. Для затвердевания поддерживающего носителя могут применяться без модификации условия, обычно применяемые для затвердевания твердого носителя. Например, в случае, если в качестве поддерживающего носителя применяют соединение, способное затвердевать, такое как коллаген, затвердевание может достигаться при общеизвестных условиях, например, путем выдерживания при температуре выращивания в течение от нескольких минут до нескольких десятков минут. Посредством этого связи между клетками внутри поддерживающего носителя фиксируются и становятся жесткими.
На стадии выращивания при способе получения по настоящему изобретению первую клеточную массу и вторую клеточную массу выращивают внутри поддерживающего носителя. На этой стадии выращивания для реконструкции ткани, а именно зуба, межклеточное взаимодействие эффективно осуществляется в первой клеточной массе и второй клеточной массе, которые находятся в тесном контакте друг с другом.
Стадию выращивания можно выполнять таким образом, что состояние контакта между первой и второй клеточными массами сохраняется поддерживающим носителем, и выращивание проводится в поддерживающем носителе, который просто содержит первую и вторую клеточные массы или другие клетки животных.
Время выращивания варьирует в зависимости от количества клеток, позиционируемых в поддерживающем носителе и состояний клеточных масс, а также от условий, в которых проходит выращивание и может составлять в основном 1-300 суток, предпочтительно 1-120 суток, чтобы сформировать зуб, имеющий эмаль снаружи и дентин внутри, и предпочтительно 1-60 суток с точки зрения быстрого получения зуба. Дополнительно с целью формирования зуба, имеющего периодонтальную ткань, время может составлять в основном 1-300 суток, предпочтительно 1-60 суток.
В случае, если выращивание производится только с поддерживающим носителем, выращивание можно проводить в условиях традиционно применяемых для выращивания клеток животных. Отсюда, в целом, условия выращивания клеток животных могут применяться без модификации, и вышеупомянутые условия могут применяться без модификации. Дополнительно к культуре может быть добавлена сыворотка, полученная из млекопитающих, и различные клеточные факторы, про которые известно, что они эффективны для роста и дифференцировки таких клеток. Примеры таких клеточных факторов включают FGF и BMP.
Кроме того, предпочтительно применять культуру органа с учетом газового обмена и запаса питательных веществ для тканей и клеточных масс. В культуре органа в основном выращивание проводят на пористой мембране, плавающей на культуральной среде роста клеток животных, и путем размещения поддерживающего носителя на мембране. Применяемая здесь пористая мембрана содержит много пор с диаметром от 0,3 до 5 мкм, и конкретные примеры мембраны включают Cell Culture Insert (торговое название) и Isopore Filter (торговое название).
Предпочтительно проведение выращивания в присутствии других клеток животных, так как зуб, имеющий специфическое расположение клеток, на ранней стадии может формироваться под влиянием действия различных цитокинов и тому подобное из клеток животных. Такое выращивание в присутствии других клеток животных может проводиться путем выращивания ех vivo с применением выделенных клеток или выращенных клеток.
Кроме того, поддерживающий носитель, содержащий первую и вторую клеточные массы, можно трансплантировать в живой организм с целью выращивания in vivo. Такое выращивание in vivo является особенно предпочтительным, поскольку зуб и/или периодонтальная ткань могут формироваться на ранней стадии. В этом случае первая и вторая клеточные массы трансплантируются в живой организм вместе с поддерживающим носителем.
Предпочтительными примерами животных, применимых для этого, являются млекопитающие, такие как человек, свинья и мышь, и особенно предпочтительно применять животное того же вида, что ткань зубного зачатка. В случаях, если трансплантируется ткань зубного зачатка человека, предпочтительно использовать человека или иммунодефицитное млекопитающее иное, чем человек. Для оптимального, насколько это возможно, развития органа или ткани для клеток животных, предпочтительными примерами мест живого организма, пригодных для такого выращивания in vivo, являются субренальная капсула, мезентерий (сальник), подкожные места и полость рта.
При трансплантации время выращивания варьирует в зависимости от размера эксплантата на время трансплантации и размера выращиваемого зуба обычно может составлять от 3 до 400 суток. Например, время трансплантации в субренальную капсулу предпочтительно составляет от 7 до 60 суток с учетом регенерации зуба и размера зуба, развивающегося в месте трансплантации, хотя оно изменяется и в зависимости от размера трансплантируемого эксплантата и размера регенерируемого зуба.
Выращивание ех vivo (предварительное выращивание) может проводиться до трансплантации в живой организм. Предварительное выращивание предпочтительно, так как связи между клетками и связь между первой и второй клеточными массами необходимо сделать сильной, чтобы усилить межклеточное взаимодействие. В результате может сократиться общее время выращивания.
Период предварительного выращивания может быть или коротким, или длительным. Чем длительнее период времени, например 3 суток или более, предпочтительно 7 суток или более, тем предпочтительнее, так как за это время из зубного зачатка может образоваться зародыш зуба и таким образом может сократиться период времени до образования зуба после трансплантации. Например, в случае трансплантационной культуры органа под субренальной капсулой для эффективной регенерации зуба время предварительного выращивания предпочтительно составляет 1-7 суток.
Зуб, полученный способом по настоящему изобретению, имеет расположение клеток (структуру), характерную для зуба: с дентином внутри и эмалью снаружи и предпочтительно имеет анизотропию, то есть имеет верхушку (коронку) и корень зуба. Функции зуба могут осуществляться при наличии по меньшей мере такого расположения клеток и предпочтительно, в дополнение к расположению клеток, при наличии анизотропии. Поэтому полученный зуб может широко применяться в качестве альтернативы зуба. В частности, если применяются мезенхимные клетки и эпителиальные клетки, полученные из аутогенного зубного зачатка, можно избежать проблем, связанных с отторжением. В целом, также возможно избежать проблем, вызванных отторжением в случаях, когда клетки получены из зубного зачатка другого индивида с совместимым антигеном трансплантации.
Зуб, полученный способом по настоящему изобретению, может находиться в составе набора зубов, имеющих расположение клеток, характерных для зуба.
Поскольку такой набор зубов составлен из многих зубов, имеющих расположение клеток, характерное для зуба, каждый зуб может быть отделен из набора зубов и применяться в качестве эксплантата единичного зуба, как описано ниже. В результате зубы можно эффективно получать как эксплантаты.
Для получения набора зубов, составленных из многих зубов, предпочтительно чтобы как первая, так и вторая клеточная масса были составлены из единичных клеток для облегчения реиндукции зубных зачатков для развития большого количества зубов.
Стадия выращивания может проводиться в культуре органа, либо культуре субренальной капсулы, как описано выше, и если созданный зуб применяется в качестве эксплантата, предпочтительно осуществляют культуру органа, которая не имеет контакта с другими клетками, и процедура в целом может быть осуществлена in vitro.
Кроме того, по способу получения по настоящему изобретению время выращивания может быть продлено до формирования периодонтальной ткани. В соответствии с этим, возможно формирование в дополнение к зубу как таковому периодонтальной ткани, такой как альвеолярный отросток и периодонтальная мембрана, которые поддерживают и стабилизируют зубы на челюсти. В результате после трансплантации может быть получен пригодный для использования зуб.
Для создания периодонтальной ткани после вышеописанной стадии выращивания с целью получения только периодонтальной ткани может выполняться стадия выделения периодонтальной ткани, полученной из вышеописанной культуры. Выделение периодонтальной ткани может проводиться любым способом, при котором периодонтальная ткань, образующаяся на стадии выращивания, может быть отделена от зуба, и примеры такого способа включает разделение пинцетом или тому подобное и частичное переваривание ферментами.
Зуб и периодонтальная ткань, полученная по настоящему изобретению, могут применяться в качестве эксплантата и также, предпочтительно, могут применяться в исследованиях с целью выяснения процесса развития зуба, поэтому они в будущем могут служить эффективным инструментом для исследования тканей, связанных с зубом.
В случаях, когда полученный зуб или периодонтальная ткань применяются в качестве эксплантата, стадия выращивания по способу предпочтительно осуществляется как культура органа, в которой отсутствует контакт с другими клетками животных, и вся процедура может быть проведена in vitro.
В настоящее изобретение также включается способ трансплантации зуба. Способ трансплантации включает в себя стадию получения вышеописанного набора зубов; стадию отделения зуба из комплекса зубов и стадию трансплантации отделенного зуба с выравниванием зуба так, чтобы он имел ту же анизотропию, как и другие зубы в месте трансплантации.
Этим способом много зубов, имеющих конкретные расположение клеток и анизотропию, можно получать одновременно, и трансплантацию зуба можно выполнять эффективно.
Зуб по настоящему изобретению также может применяться в терапии и лечении различных симптомов, сопровождающих потерю или повреждение зубов, и примеры симптомов включают кариес зубов, краевой периодонтит (альвеолярную пиорею), потерю зубов из-за периодонтита, поломка или авульсия зуба из-за несчастных случаев и тому подобное.
Другими словами, терапевтический способ по настоящему изобретению включает трансплантацию зуба и/или периодонтальной ткани, полученных способом по настоящему изобретению, в место потери и/или повреждения зуба. Посредством этого вышеописанные симптомы в месте потери и/или повреждения зуба могут быть излечены или ослаблены.
Другой терапевтический способ по настоящему изобретению включает проведение только стадии выращивания по настоящему изобретению или выполнение стадии позиционирования и стадии выращивания в месте потери и/или повреждения зуба. В этом случае окружающая ткань в месте потери и/или повреждения зуба сама по себе может применяться в качестве поддерживающего носителя в дополнение к вышеупомянутым поддерживающим носителям. Так, благодаря цитокинам или тому подобное, из окружающих тканей живого организма, терапия или тому подобное в месте потери и/или повреждения может проводиться быстрее.
Примеры
Здесь будут приведены примеры по настоящему изобретению, однако настоящее изобретение ими не ограничивается. Если специально не оговорено, проценты (%) в примерах приводятся по массе (мас.%).
Пример 1
(1) Способ выращивания клеток ЕС (эмбриональной карциномы)
В качестве клеток ЕС применяли клетки АТ805 (клон, выведенный из ОТТ6050, клеток ЕС штамма 129; полученные из Cell Bank, RIKEN Bioresource Center). Выращивание клеток АТ805 осуществляли в среде Игла, модифицированной Дульбекко (DMEM; производства SIGMA или Kohjin Bio Co. Ltd.), дополненной 10 об.% фетальной телячьей сывороткой (FCS: производства JRH, JBS или Hyclone) и 55 мкМ 2-меркаптоэтанола (производства GIBCO). Клетки ЕС обычно высевали в концентрации 5-8×105 клеток в 100 мм чашку и полную замену среды и пересев культуры повторяли через день. В пересеянной культуре клетки однократно промывали буфером HCMF (рН 7,4; 10 мМ Hepes (N-2-гидроксиэтилпиперазин-N'-2-этансульфоновая кислота), 136,9 мМ NaCl, 0,34 мМ Na2HPO3, 13,9 мМ глюкозы, 5,37 мМ KCI) и затем туда же добавляли 5 мл раствора фермента, в котором содержится трипсин-ЕОТА*2Na (динатриевая соль этилендиаминтетрауксусной кислоты) (производства GIBCO), разбавленная до конечной концентрации 0,025%, с последующей обработкой ферментом при 37°С в течение 1 мин. Затем для диспергирования клеток добавляли равное количество DMEM, дополненной 10% FCS, и затем клетки осаждали и собирали центрифугированием. Собранные клетки ресуспендировали и наносили в новую чашку для пересева культуры.
(2) Индукция дифференцировки клеток ЕС и сбор клеток
Клетки ЕС, собранные обработкой трипсином, суспендировали в DMEM, дополненной 10 об.% FCS и диметилсульфоксидом (DMSO: производства SIGMA) при конечной концентрации 0,5-5 об.%, и высевали в концентрации 1,0×106 клеток в 100 мм чашку. Выращивание проводили под 5% CO2 при 37°С, и после 14 часов клетки однократно промывали буфером HCMF с последующим замещением среды DMEM, дополненной 10 об.% FCS.
Клетки ЕС, обработанные DMSO, непрерывно выращивали в течение 6 суток (19 суток в случае 5 об.% DMSO), замещая половину количества среды каждые трое суток DMEM, дополненной 10 об.% FCS, и проводили соответствующее наблюдение. Если выращивали клеточную популяцию, содержащую недифференцированные клетки, ее однократно промывали буфером HCMF и затем суспендировали добавлением PBS(-)(EDTA/BSA-PBS) без Ca2+/Mg2+ (где PBS - фосфатно-солевой буфер, EDTA - этилендиаминтетрауксусная кислота, BSA - бычий сывороточный альбумин), дополненную 3 мМ EDTA и 0,5% BSA, с последующим сбором клеток центрифугированием. Клетки ресуспендировали в EDTA/BSA-PBS и затем подвергали двойному окрашиванию меченым FITC (флуоресцеин изотиоцианат) антителом к CD44 (CD44-FITC: производится BD Pharmingen) и меченым РЕ (фикоэритрином) антителом к CD29 (CD29-PE: производится BD Pharmingen). CD44-позитивную и CD29-позитивную клеточную фракцию изолировали с помощью устройства для сортировки клеток, Epics ALTRA (производства Beckman Coulter), получая фракцию клеток ЕС, где дифференцировку индуцировали обработкой DMSO, а недифференцированные клетки удаляли (см. Фиг.2). Эти клетки обозначили как клетки DMSO-EC.
Доля клеток DMSO-EC после обработки различными концентрациями DMSO показаны в Таблице 1. Как показано в Таблице 1, было обнаружено, что количество CD44-позитивных и CD29-позитивных клеток увеличилось при увеличении концентрации DMSO, при которой проводилась обработка. Относительно клеток ЕС, обработанных 5 об.% DMSO, было обнаружено, что хотя большинство клеток погибли немедленно после обработки и потребовалось больше времени выращивания культуры после обработки, чем при обработке другими концентрациями, доля CD44-выращенных позитивных и CD29-позитивных клеток была высокой.
Далее эксперименты проводили с клетками, полученными с применением 5 об.% DMSO.
Клонирование клеток DMSO-EC
Клонирование клеток DMSO-EC проводили выделением колоний с применением клонирующих колец или способом серийных разведений.
При сборе клеток с использованием клонзапирающих колец клетки DMSO-EC высевали в чашку для выращивания клеток в низкой концентрации (около 100 клеток) и, когда количество клеток в колонии, образованной путем роста клеток, становилось не менее 10, на один из концов клонзапирающего кольца наносили простерилизованную силиконовую смазку, и его укрепляли на нижней поверхности чашки после удаления среды таким образом, чтобы клонзапирающее кольцо содержало в себе колонию. После этого внутри клонзапирающего кольца проводили обработку трипсином и собирали клетки. Выращенные клетки последовательно пролиферировали с образованием клона.
При получении клона способом серийных разведении клетки DMSO-EC, полученные вышеописанным способом, однократно промывали буфером HCMF и после этого клетки собирали обработкой трипсином. Подсчитывали количество собранных клеток и затем наносили на планшет с 96 лунками таким образом, чтобы получить 1 клетка/200 мкл/лунка (условное обозначение). Было подтверждено, что через 3-5 суток клетки образовали единичные колонии. После этого их выращивание продолжали, заменяя половинное количество среды каждые 5 суток. Выращенные клетки последовательно пролиферировали с образованием клона.
Таким образом, были получены клон 1 (DMSO-EC клон 1: Клон №1) и клон 2 (DMSO-EC клон 2: Клон №2), полученные из клеток DMSO-EC.
Пример 2
Свойства клеток DMSO-EC
(1) Микросъемка на фазово-контрастном микроскопе
Морфология полученных, как выше описано клонов 1 и 2, и морфология клеток ЕС, клеток DMSO-EC и клеток ATDC5 (полученных из Cell Bank, RIKEN Bioresource Center), являющихся клетками-предшественницами хряща, полученными из клеток ЕС, в каждом случае изучалась с применением фазово-контрастного микроскопа.
В результате авторы наблюдали, что клетки ЕС в колонии имели малый размер и высокую плотность, и активировалась интерференционная полоса колонии, поэтому они сделали вывод, что эти клетки имели морфологию стволовых тотипотентных клеток. С другой стороны, по отношению к клеткам DMSO-EC, клонам 1 и 2 клеток DMSO-EC и клеткам ATDC5 поверхность каждой клетки, составляющей колонию была большой, и клетки образовали монослой, характерный для адгезионных клеток, тем самым показывая морфологию, явно отличную от характерной морфологии клеток ЕС. Морфология адгезионных клеток подобна морфологии мезенхимных клеток, а не клеток ЕС.
(2) Экспрессия различных генов
Экспрессию различных генов в клетках ЕС, клетках DMSO-EC, клонов 1 и 2 клеток DMSO-EC и клеток ATDC5 анализировали с применением ПЦР в реальном времени (РВ-ПЦР) и изучали экспрессию маркерных генов.
Экстракцию общей РНК из клеток ЕС, клеток DMSO-EC, клонов 1 и 2 клеток DMSO-EC и клеток ATDC5 проводили, применяя реагент TRIzol (производства Invitrogen). Среду для выращивания клеток для анализа удаляли и прямо в 100 мм чашку для выращивания по каплям добавляли 2 мл реагент TRIzol. После надлежащего смешивания клеток с помощью скребка для снятия клеток (производства Falcon) полученную смесь собирали в пробирку Эппендорфа и гомогенизировали гомогенизатором Polytron (производства Polytron). Дальнейшие операции перед стадией экстракции РНК проводили согласно инструкции фирмы-изготовителя, вложенной в набор. Общую РНК, экстрагированную из клеток/тканей, растворяли в воде, обработанной DEPC (диэтилпирокарбонат), и ее концентрацию рассчитывали, применяя спектрофотометр, после этого хранили при -30°С.
Применяя общую РНК, экстрагированную из клеток как матрицу, для анализа при помощи ПЦР в реальном времени (RT-ПЦР) синтезировали кДНК. Синтез кДНК проводили, применяя ReverTra Асе (TOYOBO), работу проводили по инструкции фирмы-изготовителя, приложенной к набору.
ПЦР и анализ проводили, применяя ABI PRISM 7000 (производства Applied Biosystems). SYBR Premix Ex Taq (производства TAKARA) применяли в качестве полимеразы и в качестве эндогенного контроля применяли β-актин. На 96-луночный планшет для РВ-ПЦР с целью получения системы реакции добавляли 13 мкл SYBR Premix Ex Taq (производства TAKARA), 2 мкл 20-кратно разбавленного раствора кДНК, 5 мкл каждого из праймеров в концентрации 1 мкМ и 5 мкл стерилизованной воды на образец до конечного объема 25 мкл, и проводили ПЦР согласно общепринятому способу. Кроме того, для каждого гена строили калибровочную кривую, выполняя контрольные реакции для активирования индивидуального количественного анализа. Последовательности праймеров, применяемых для анализа приведены в Таблице 2 и Таблице 3.
Уровень генной экспрессии в каждой группе клеток приводили к уровню экспрессии β-актина и проводили сравнения по уровням относительной экспрессии, принимая, что уровень экспрессии β-актина является постоянным. Результаты показаны в Таблице 4.
Как показано в Таблице 4, экспрессия Oct3/4 и Nanog, являющихся маркерными генами для недифференцированных стволовых клеток, наблюдалась только в клетках ЕС, но не наблюдалась в клетках ЕС, обработанных DMSO, их клонах и клетках ATDC5. Экспрессию Slug, Рах3 и Wnt1, являющихся маркерными генами клеток нервного гребня, не наблюдали в клетках ЕС; экспрессию Slug наблюдали во всех клеточных группах, кроме клеток ЕС, и экспрессию Рах3 и Wnt1 наблюдали во всех группах клеток DMSO-ЕС, кроме клеток ЕС и ATDC5, хотя была разница в уровнях их экспрессии.
Таким образом, авторы полагают, что клетки DMSO-EC и их клоны появились путем индукции дифференцировки недифференцированных стволовых клеток в клетки нервного гребня, и по характеру генной экспрессии было обнаружено, что они являются Ос13/4-негативными, Nanog-негативными, Slug-позитивными, Рах3-позитивными и Wnt1-позитивными клетками.
С другой стороны, что касается групп маркеров мезенхимных клеток зуба, то любой ген, кроме Msx1 и ВМР-7, не экспрессируется в клетках ЕС, хотя гены Msx1, Pax9, Wnt5a и Lhx8 специфично и высокоактивно экспрессировались в клетках DMSO-EC и их клонах. В клетках DMSO-EC и их клонах, а также (при некоторых различиях в уровнях экспрессии) в клетках ATDC5 наблюдали экспрессию ВМР4, Runx2 и Dlx1.
Экспрессия Sox9 и Sox5, являющихся маркерными генами, специфичными для клеток хряща, была высокой только в клетках ATDC5, и поэтому авторы посчитали, что клетки DMSO-EC и их клоны являются клетками, недифференцированными в клетки хряща.
Таким образом, стало очевидным, что клетки ЕС дифференцируются индукцией, обусловленной DMSO, в клетки, подобные клеткам нервного гребня, или в клетки, подобные мезенхимным клеткам.
Пример 3
Исследование потенциала для формирования зуба клеток, дифференцировка которых индуцировалась из клеток ЕС
Потенциал дифференцировки в одонтобласты и потенциалы формирования дентина клетками DMSO-EC и их клонами, полученными по настоящему изобретению, оценивали следующим образом.
(1) Получение эпителиальной ткани зубного зачатка
Из эмбриона мыши C57BL/6 (приобретенных у SLC) при возрасте эмбриона 14,5 суток под микроскопом традиционным способом выделяли ткань зубного зачатка нижнего резца. Изолированную ткань зубного зачатка нижнего резца промывали PBS(-) и при комнатной температуре в течение 12,5 минут обрабатывали раствором фермента, дополненным 1,2 Ед/мл (конечная концентрация) диспазы II (Roche, Mannheim, Германия), и затем 3 раза промывали DMEM (Sigma, St. Louis, МО), дополненной 10% FCS (JRH Biosciences, Lenexa, KS). После этого добавляли раствор ДНКазы I (Takara, Siga, Japan) с таким расчетом, чтобы при диспергировании ткани зубного зачатка достигалась ее концентрация 70 Ед/мл, и эпителиальную ткань зубного зачатка хирургически удаляли с помощью иглы для инъекций 25G (0,5 мм) (Terumo, Tokyo, Japan).
(2) Получение реконструированного зубного зачатка
Получение реконструированного зубного зачатка проводили, применяя эпителиальную ткань зубного зачатка, полученную, как описано выше, в качестве мезенхимных клеток применяли одну из исследуемых клеточных групп, а именно клетки ЕС, клетки DMSO-EC или клоны 1 или 2 DMSO-EC. Каждую из исследуемых клеточных групп, применяемых для реконструкции зубного зачатка, собирали с чашки обработкой трипсином. Исследуемые клетки, суспендированные в DMEM (Sigma), дополненной 10% FCS (JRH), помещали в 1,5 мл микропробирку (Eppendorf, Hamburg, Германия), обработанную силиконовой смазкой, и собирали клетки в виде осадка после центрифугирования (580×g). После тщательного удаления надосадочной жидкости культуры центрифугирование повторяли и оставшуюся внутри осадков среду для выращивания полностью удаляли, применяя наконечник микропипетки GELoader Tip 0,5-20 мкл (производства Eppendorf), наблюдая под стереомикроскопом, с целью подготовить каждую клеточную группу, намеченную к получению реконструированного зубного зачатка, для исследования.
В чашку Петри, обработанную силиконовой смазкой, с целью приготовления коллагеновой гелевой капли, по каплям добавляли 30 мкл 2,4 мг/мл Cellmatrix типа I-A (производства Nitta Gelatin Inc.). К этому раствору добавляли 0,2 мкл - 10,3 мкл вышеописанных клеток, предназначенных для исследования, применяя наконечник микропипетки 0,1-10 мкл (производства Eppendorf), с целью получения агрегата клеток в виде клеточной массы высокой плотности (плотность клеток: 2 × 10е клеток/мл). После этого, применяя наконечник пипетки 10 мкл, на ту же каплю геля наносили эпителиальную ткань зубного зачатка или мезенхимную ткань зубного зачатка, и, применяя вольфрамовую иглу, поверхность эпителиальной ткани зубного зачатка, первоначально соприкасавшуюся с мезенхимной тканью, приводили в тесный контакт с исследуемым агрегатом клеток. После этого при затвердевании капли геля связи между тканью зубного зачатка и исследуемыми клетками стали прочнее, что необходимо для приготовления реконструированного зубного зачатка высокой плотности.
Далее описание излагается со ссылкой Фиг.3.
Агрегат клеток 12, предварительно позиционированный в капле геля 10 (см. Фиг.3А) с помощью наконечника пипетки 16, образует сферу в капле геля 10 (см. Фиг.3 В). Затем путем надавливания на агрегат клеток 14 сферический агрегат клеток 12 часто раздавливается и обертывает агрегат клеток 14 (см. Фиг.3С). После этого при затвердевании капли геля 10 связи между клетками становятся сильнее (см. Фиг.3D).
(3) Культура органа у реконструированного зубного зачатка
Реконструированный зубной зачаток высокой плотности, полученный в геле, оставляли в инкубаторе CD2 в течение 10 минут для затвердевания Cellmatrix тип I-A (Nitta Gelatin). Сосуд для выращивания готовили следующим образом: DMEM (производства Sigma), дополненную 10 об.% FCS (производства JRH), 0,1 мг/мл L-аскорбиновой кислоты (производства Sigma) и 2 мМ L-глютаминовой кислоты (производства GIBCO), приводили в контакт с мембранами для выращивания культур клеток (мембрана из полиэтилентерефталата с размером пор 0,4 мкм; производства BD). Реконструированный зубной зачаток переносили вместе с окружающим гелем, являющимся поддерживающим носителем, на указанные мембраны в сосуде для выращивания, чтобы осуществить выращивание культуры органа.
Обычно, если развитие зуба прослеживали на культуре органа, выращивание проводили 14 суток. Если проводили выращивание культуры органа, реконструированный зубной зачаток изолировали через 10-30 суток после трансплантации и фиксировали 4% параформальдегидфосфатным буфером в течение 6 часов с последующим декальцинированием в нейтральной среде в течение 24 часов, применяя раствор 4,5% EDTA (рН 7,4). После этого проводили заливку парафином согласно общепринятым способом для приготовления срезов 10 мкм. Для гистологического анализа общепринятым способом проводили окрашивание гематоксилин+эозин (окрашивание НЕ).
Исследование в культуре органа
В случае реконструированного зубного зачатка высокой плоскости, из эпителиальной ткани зубного зачатка нижнего резца в возрасте 14,5 суток этот реконструированный зубной зачаток увеличился в размере ввиду ненормального роста клеток ЕС, и также, судя по окрашиванию НЕ, не наблюдались одонтобласты и дентин, имеющий происхождение из мезенхимных клеток зуба.
В отличие от этого, в клетках DMSO-EC и клонах 1 и 2 DMSO-EC индуцировалось взаимодействие с эпителиальной тканью и по данным фазово-контрастной микрографии наблюдалась индукция ткани тем же образом, как и в культуре органа зубного зачатка. Кроме того, в любых культурах клеток DMSO-EC и клонах 1 и 2 DMSO-EC, данные по изображениям, окрашенным НЕ, подтвердили, что вероятно образуется реконструированный зубной зачаток, имеющий эмаль снаружи и дентин внутри, таким образом показывая возможность образования тканевой структуры, характерной для зуба.
По этим данным стало очевидным, что благодаря взаимодействию с эпителиальными клетками зубного зачатка, клетки DMSO-EC и клоны 1 и 2 DMSO-EC дифференцируются в одонтобласты, составляющие мезенхимную ткань зуба и в состоянии создавать дентин, специфичный для зуба. Кроме того, стало очевидным, что зуб со специфичной тканевой структурой, имеющий эмаль снаружи и дентин внутри, клетки внутренней пульпы зуба, а также коронку и корень также может получать способом реконструкции зубного зачатка высокой плотности в культуре органа.
Пример 4
Способ трансплантации в субренальную капсулу
Затем из клеток DMSO-EC, клеток клонов 1 и 2 DMSO-EC и эпителиальных клеток зачатка нижнего резца эмбриона в возрасте 14,5 суток были получены реконструированные зубные зачатки и полученные реконструированные зубные зачатки трансплантировали в субренальную капсулу мышей C57BL6 (полученных из CLEA Japan, Inc.) с целью исследования их потенциала для формирования зуба.
Реконструированные зубные зачатки, полученные как в Примере 3, для анализа подвергали органному выращиванию в течение 48-96 часов и затем трансплантировали в субренальную капсулу восьминедельных мышей NOD-SCID (полученных из Charles River) вместе с окружающим гелем, чтобы способствовать эктопическому развитию зубов.
При трансплантации в субренальную капсулу реконструированный зубной зачаток на 10-30 сутки после трансплантации изолировали вместе с окружающей ренальной тканью. Изолированную ткань фиксировали в 4% параформальдегидфосфатном буфере в течение 6 часов и в течение 24 часов проводили декальцинирование в нейтральных условиях в растворе 4,5% EDTA (рН 7,4). После этого для приготовления 10 мкм срезов традиционным способом проводили парафиновую заливку. Для гистологического анализа традиционным способом проводили окрашивание НЕ.
(1) Исследование путем трансплантации в субренальную капсулу
При трансплантации в субренальную капсулу, когда трансплантировали эпителиальные клетки зубного зачатка резца эмбриона в возрасте 14,5 суток, зуб с характерной структурой с дентином внутри и эмалью снаружи мог образоваться через 16 суток после трансплантации в субренальную капсулу (см. Фиг.4). В случае зубных зачатков, реконструированных посредством эпителиальной ткани зубного зачатка и мезенхимных клеток зубного зачатка, имеющих происхождение из зубного зачатка резца эмбриона в возрасте 14,5 суток (см. Фиг.4А), эпителиальной ткани зубного зачатка и клеток DMSO-EC (см. Фиг.4В) и эпителиальной ткани зубного зачатка и клона DMSO-EC (клон №1; см. Фиг.4С); на 14 день после трансплантации в субренальную капсулу можно было легко идентифицировать амелобласты и эмаль снаружи, дентин и одонтобласты внутри, так же как в случае, когда в субренальную капсулу трансплантировали нормальный зубной зачаток как он есть. Образовавшийся зуб имел коронку и корень, показывая ту же структуру, как и нормально развившийся зуб.
Частота образования зуба составила 0% для клеток ЕС и ATDC, и в то же время 51,3±8,8% для клеток DMSO-EC, 23,3%±16,7% для клона 1 DMSO-EC и 33,3%±47,1% для клона 2 DMSO-EC.
Из этих результатов стало ясно, что клетки DMSO-EC и клоны 1 и 2 DMSO-EC могут дифференцироваться в одонтобласты, которые образуют ткань, имеющую происхождение из мезенхимы зуба, и могут создавать дентин, являющийся твердой тканью зуба. Кроме того, стало ясно, что зуб, имеющий специфическую тканевую структуру, может быть создан способом реконструкции зубного зачатка высокой плотности при трансплантации в субренальную капсулу клеток DMSO-EC или клонов 1 или 2 DMSO-EC.
(2) Гибридизация in situ
Эпителиальную ткань зубного зачатка, образовавшуюся из зубного зачатка резца эмбриона в возрасте 14,5 суток, и клетки DMSO-EC трансплантировали в субренальную капсулу и через 14 суток брали ткань, в которой проводили гибридизацию для анализа экспрессии мРНК амелогенина, входящего в состав эмали, и экспрессии мРНК сиалофосфопротеина (DSPP) дентина, входящего в состав дентина, а также экспрессию мРНК периостина, являющегося геном, специфичным для периодонтальной мембраны.
Реконструированный зубной зачаток на день 14 после трансплантации в субренальную капсулу изолировали и фиксировали 4% параформальдегидфосфатным буфером в течение 6 часов, после чего последовало декальцинирование 4,5% раствором EDTA в нейтральных условиях (рН 7,4) в течение 24 часов. После этого полученный препарат после вымачивания в 12,5% растворе сахарозы и 25% растворе сахарозы заливали «ОСТ compound» (композиция из водорастворимых гликолей и смол для заливки тканей при низкой температуре, производства SAKURA Finetechnica). 10 мкм срезы последовательно получали в криостате (производства Leica).
Вышеописанные срезы обрабатывали PBS(-), содержащим протеазу К (Nacalai tesque, Kyoto, Japan) в конечной концентрации 2 мкг/мл, в течение 10 минут и фиксировали в течение 10 минут в PBS(-), содержащем параформальдегид (Nacalai tesque). После обработки полученных препаратов диэтилпирокарбонатом (DEPC), обработанным водой, дополненной 1,325% триэтаноламина, 0,0175N HCl (Wako) и 0,25% уксусным ангидридом (все значения показаны как конечные концентрации) в течение 10 минут, полученные препараты 3 раза промывали PBS(-) в течение 5 минут. После обработки препаратов водным DEPC, дополненным 1,5% (об./об.) триэтаноламином (Nacalai tesque), 0,33N HCl (Wako) и 0,25% (об./об.) уксусным ангидридом (Nacalai tesque) в течение 10 минут, их дважды промывали буфером 2×SSC (хлорид натрия+цитрат натрия). Пробу на периостин (№ доступа в GenBank - NM_015784), являющийся геном, специфичным для периодонтальной мембраны, готовили мечением DIG (дигоксигенином) фрагмента комплементарной ДНК, полученной обработкой ПЦР с применением прямого праймера (-7; ggctgaagatggttcctctc: SEQ ID NO:35) и обратного праймера (573; gtacattgaaggaataacca: SEQ ID NO:36).
Гибридизацию in situ проводили традиционным способом и затем проводили окрашивание анти-DIG фрагментом Fab щелочной фосфатазы (АР) (Roche) и окрашивание NBT/BCIP Stock Solution (раствор нитротетразолиевого синего/ 5-бром-4-хлор-3-индолилфосфата, Roche), с последующим анализом на Axio ImagerA.1 (Zeiss) и AxioCam MRc5 (Zeiss).
По результатам, в окрашенных НЕ изображениях наблюдалась экспрессия мРНК амелогенина в амелобластах и экспрессия матричной РНК DSPP в одонтобластах соответственно. Кроме того, наблюдалась экспрессия мРНК периостина. Таким образом, явно и однозначно обнаружена экспрессия мРНК соответствующих молекул в клетках, вовлеченных в формирование твердых тканей. Кроме того, авторы предположили образование периодонтальной ткани благодаря обнаружению экспрессии периостина, экспрессирующегося в периодонтальной ткани.
Пример 5
Индукция ретиноевой кислотой (RA)
(1) Способ индукции дифференцировки клеток ЕС для получения CD44-положительных и CD29-положительных клеток
Клетки АТ805, собранные обработкой трипсином по Примеру 1, наносили на 100 мм кювету в концентрации 1,0 × 106 клеток на кювету, и на следующий день среду заменяли DMEM, дополненную FCS 10 об.%, а также для стимулирования клеток добавляли ретиноевую кислоту (производства SIGMA) при конечной концентрации от 0 до 10,0 мкМ. Через 72 часа выращивания клетки дважды промывали буфером HCMF и заменяли весь объем среды на DMEM, дополненную только 10 об.% FCS.
(2) Получение CD44-положительных и CD29-положительных клеток после обработки RA
Выращивание продолжали в течение 7 суток, через каждые 3 дня заменяя половину количества среды DMEM, дополненной FCS 10 об.%, и провели соответствующее исследование. Клеточную популяцию, выращенную после обработки RA, содержащую недифференцированные клетки, однократно промывали HCMF и туда же добавляли 3 мМ EDTA-0,5% BSA-PBS(-) с последующей инкубацией при 37°С. После сбора клеток их подвергали двойному окрашиванию CD44 FITC (BD Pharmingen) и CD29 (BD Pharmingen) РЕ для идентификации и разделения CD44-позитивных и CD29-позитивных клеток, применяя Epics ALTRA(Beckman Coulter), и таким образом исключив недифференцированные клетки, получали клеточную популяцию, состоящую только из дифференцированных клеток. Эти клетки обозначили как клетки RA-ЕС. Результаты показаны на Фиг.5.
Кроме того, в Таблице 5 показаны пропорции клеток RA-EC после обработки различными концентрациями RA. Как показано в Таблице 5, было обнаружено, что доли CD44-положительных и CD29-положительных клеток изменяются в зависимости от концентрации RA, при которой проводили обработку.
Экспрессию генов в CD44-положительных и CD29-положительных клетках после обработки RA подтверждали по Примеру 2(2), и эти клетки оказались Oct3/4-негативными, Nanog-негативными, Slug-позитивными, Рах3-позитивными и Wnt1-позитивными, как в случае клеток DMSO-EC.
(3) Исследование потенциала CD44-позитивных и CD29-позитивных клеток в формировании зуба после обработки RA
Для исследования применяли CD44-позитивные и CD29-позитивные клетки (концентрация RA: 2 мкМ), полученные как описано выше, реконструкцию зубного зачатка и выращивание культуры органа проводили по Примеру 3. Через 14 суток выращивания культуры органа клетки дифференцировались в одонтобласты, соответствующие мезенхимным клеткам зуба, благодаря взаимодействию с эпителиальными клетками зубного зачатка. Кроме того, по способу реконструкции зубного зачатка высокой плотности сформировался зуб с тканевой структурой, специфичной для зуба, имеющий эмаль снаружи и дентин внутри и клетки внутренней пульпы зуба (см. Фиг.6).
Кроме того, после того как была подтверждена экспрессия амелогенина, DSPP и периостина в CD44-позитивных и CD29-позитивных клетках после обработки RA по Примеру 4(2), как и в случае клеток DMSO-EC обнаружили соответствующие им мРНК. Таким образом, авторы предположили образование периодонтальной ткани, содержащей твердую ткань, а также периодонтальной мембраны.
Пример 6
(1) Способ индукции дифференцировки клеток ЕС для получения CD44-позитивных и CD106-позитивных клеток
Клетки АТ805, обработанные трипсином по Примеру 1, наносили на 100 мм кювету в концентрации 1,0×106 клеток на кювету и, на следующий день, среду заменяли DMEM, дополненной FCS 10 об.%, к которой для стимулирования клеток также добавляли RA (производства SIGMA) в конечной концентрации 2 мкМ. После выращивания в течение 72 часов клетки дважды промывали буфером HCMF, и среду полностью заменили DMEM, дополненной только 10 об.% FCS. На следующий день клетки дважды промывали буфером HCMF и удаляли мертвые клетки, затем продолжали выращивание в DMEM, дополненной только 10 об.% FCS. После этого выращивание проводили в течение 7 суток, через день заменяя среду.
(2) Получение CD44-позитивных и CD106-позитивных клеток
Клеточную популяцию, полученную обработкой вышеописанным способом, содержащую недифференцированные клетки, однократно промывали HCMF и к ней добавляли 3 мМ EDTA-0,5% BSA-PBS(-), с последующей инкубацией их при 37°С. После отбора клеток их подвергали двойному окрашиванию CD44 FITC (BD Pharmingen) и антителом к CD106 (CD106(BD Pharmingen)PE) для разделения и получения CD44-позитивной и CD106-позитивной фракции, применяя Epics ALTRA(Beckman Coulter) и тем самым после удаления недифференцированных клеток, получали популяцию, состоящую только из дифференцированных клеток. Результаты показаны на Фиг.7.
(3) Исследование потенциала CD44-позитивных и CD106-позитивных клеток после обработки RA в формировании зуба
Для исследования, применяя CD44-позитивные и CD106-позитивные клетки, полученные как описано выше, проводили реконструкцию зубного зачатка и выращивание культуры органа проводили по Примеру 3. Через 14 суток выращивания культуры органа клетки дифференцировались в одонтобласты, соответствующие мезенхимным тканям зуба, благодаря взаимодействию с эпителиальными клетками зубного зачатка. Далее, с применением способа реконструкции зубного зачатка высокой плотности получали зуб, обладающий тканевой структурой, характерной для зуба, имеющий эмаль снаружи и дентин внутри и клетки внутренней пульпы зуба.
Экспрессию генов подтверждали у этих CD44-позитивных и CD106-позитивных клеток DMSO-EC по Примеру 2(2). В результате, как и в случаях CD44-позитивных и CD29-позитивных клеток DMSO-EC, они оказались Oct3/4-негативными, Nanog-негативными, Slug-позитивными, Рах3-позитивными и Wnt1-позитивными.
Кроме того, подтвердив экспрессию амелогенина, DSPP и периостина по Примеру 4(2), наблюдали экспрессию соответствующих мРНК, как и в случае DMSO-EC. Таким образом, авторы предположили образование периодонтальной ткани, состоящей из твердой ткани и периодонтальной мембраны.
Пример 7
Как и по Примеру 6(2) и (3), путем двойного окрашивания клеток DMSO-EC, применяя CD44 FITC и CD106 РЕ, показали существование CD44-позитивных и CD106-позитивных клеток. Экспрессию генов в этих CD44-позитивных и CD106-позитивных клеток доказали по Примеру 2, и данные клетки, как и CD44-позитивных и CD29-позитивных DMSO-EC клетки, оказались Ост3/4-негативными, Nanog-негативными, Slug-позитивными, Рах3-позитивными и Wnt1-позитивными.
Применяя полученную таким образом клеточную популяцию CD44-позитивных и CD106-позитивных клеток для исследования, реконструкцию зубного зачатка, выращивание культуры органа и экспрессию мРНК выполняли по Примеру 3 и Примеру 4(2). В результате по причине взаимодействия эпителиальных клеток зубного зачатка сформировался зуб, имеющий специфичную тканевую структуру зуба. Кроме того, как и в Примере 4(2), наблюдали экспрессию амелогенина, DSPP и периостина. Таким образом, авторы предположили возможность образования периодонтальной ткани, состоящей из твердой ткани и периодонтальной мембраны.
Таким образом, дифференцировка CD44-позитивных и CD29-позитивных клеток или CD44-позитивных и CD106-позитивных клеток может индуцироваться из стволовых тотипотентных клеток и путем выращивания этих клеток совместно с эпителиальными клетками в условиях компартентализации может быть реконструирован зубной зачаток, что приводит к получению зуба со специфичной структурой, имеющий эмаль и дентин.
Таким образом, по настоящему изобретению мезенхимные клетки для формирования зуба могут быть получены из тотипотентных стволовых клеток и эффективно можно получить большое количество зубов.
Описание заявки на патент Японии №2007-011805 включено в настоящую заявку путем ссылки в полном объеме. Все литературные источники, заявки на патенты или технические стандарты вводятся в настоящую заявку в виде ссылки в той же степени, как в случаях, где каждый литературный источник, заявка на патент или технический стандарт описан конкретно и индивидуально в виде ссылки.
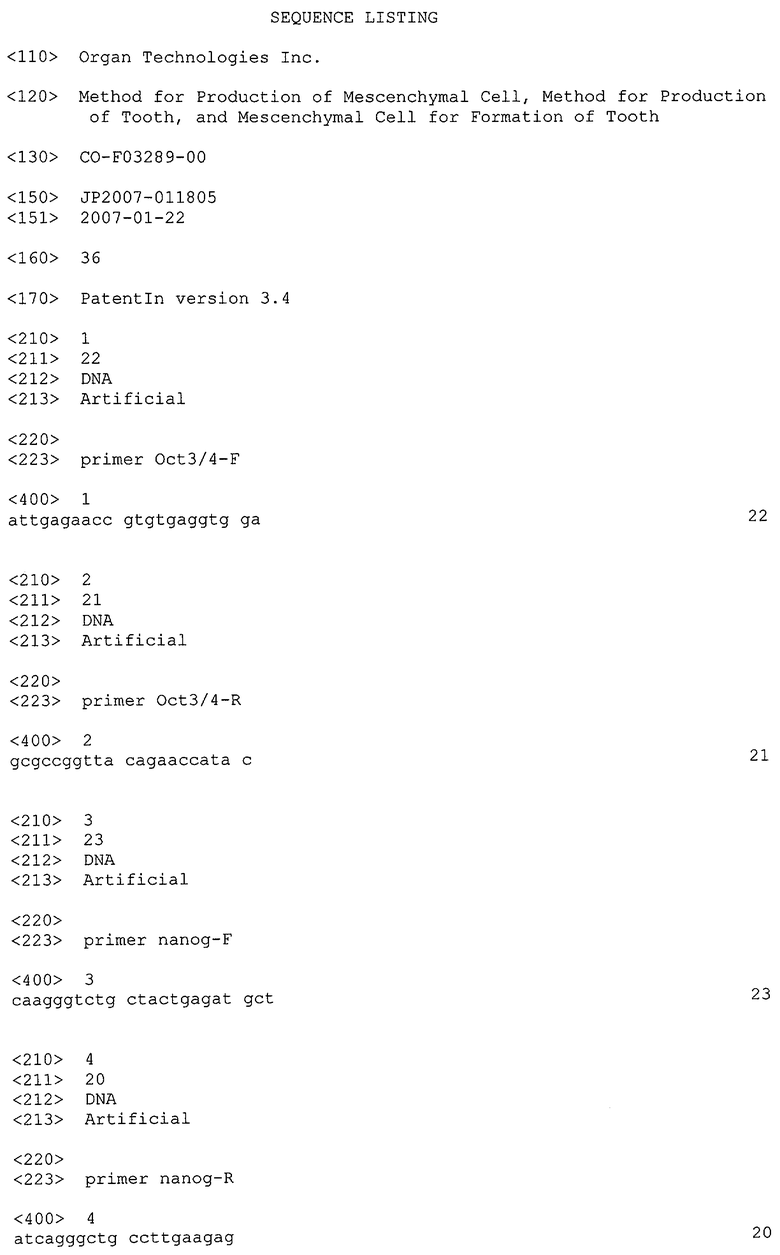






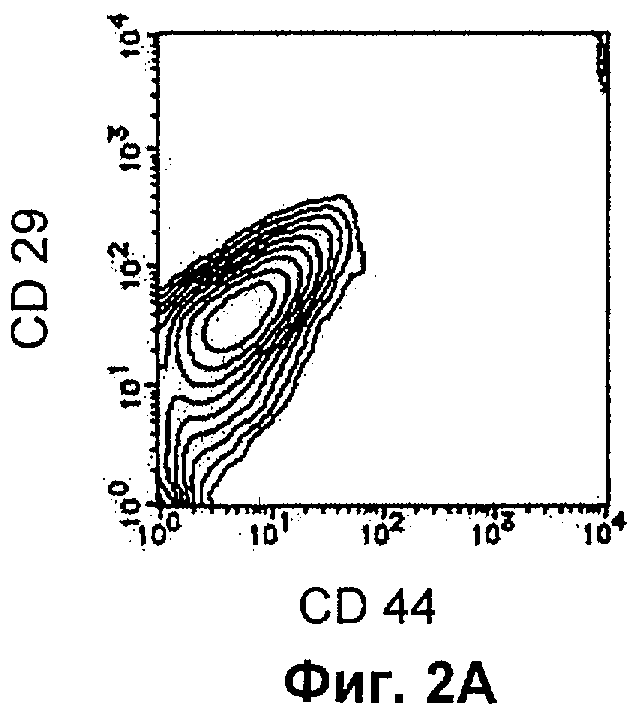
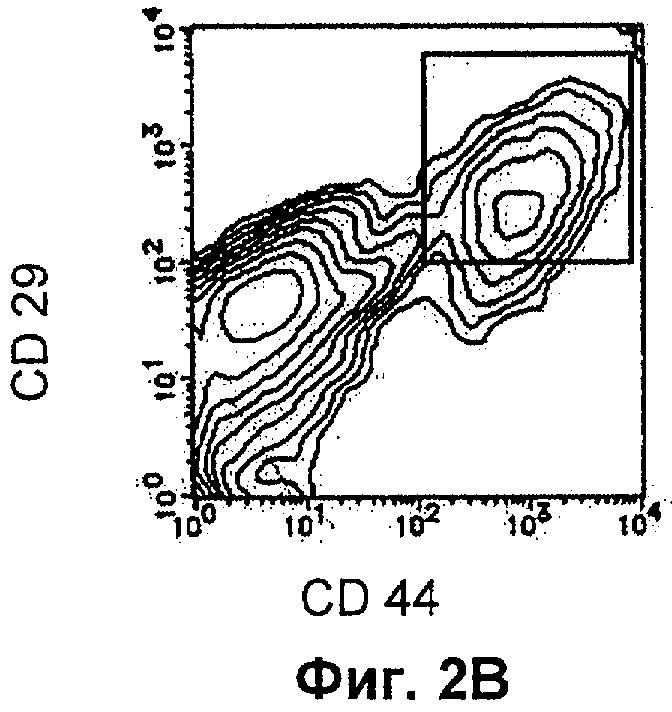
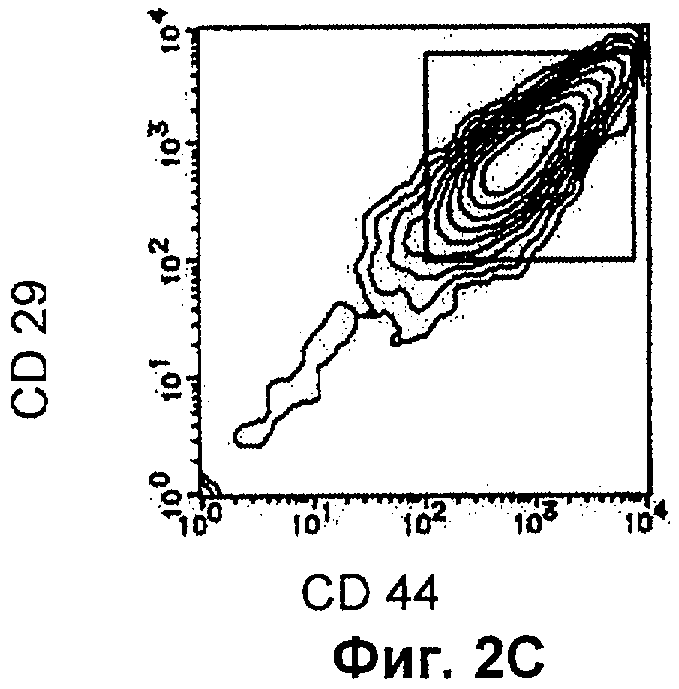
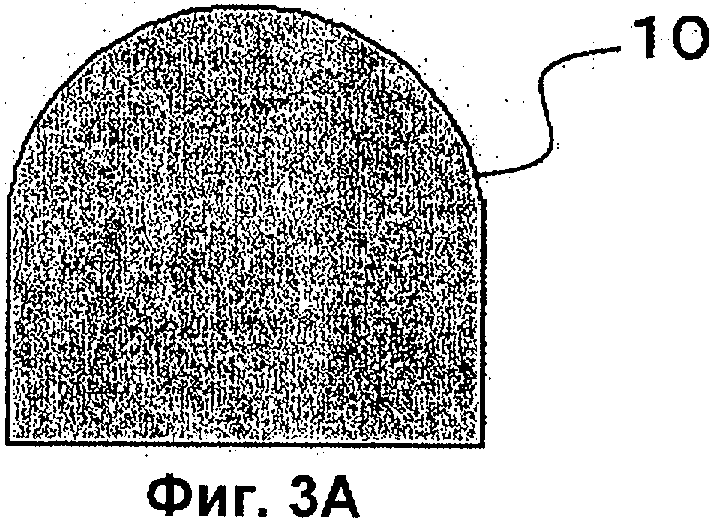
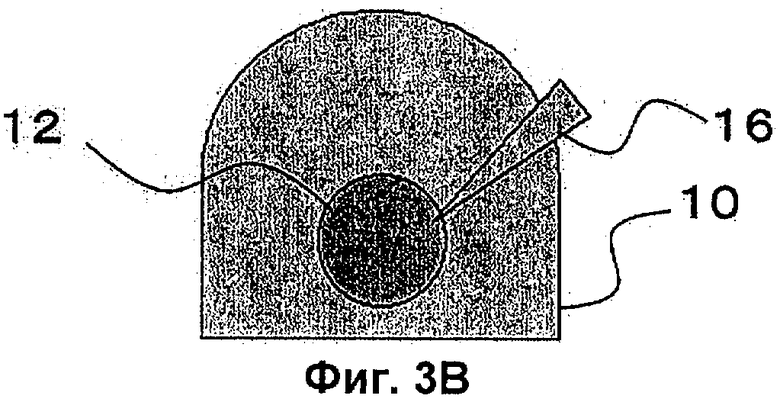

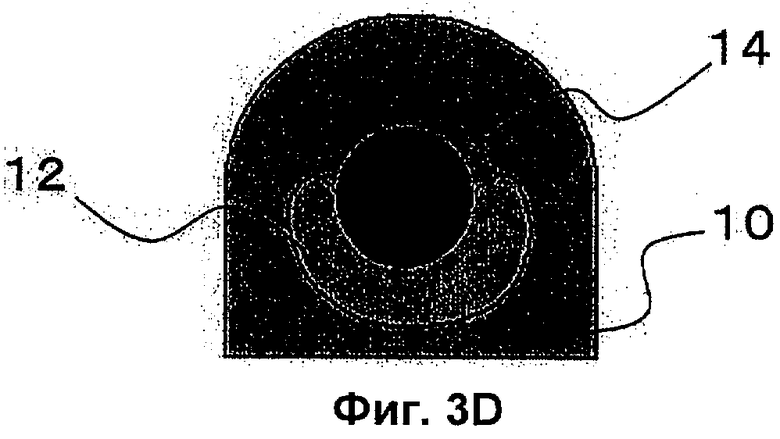
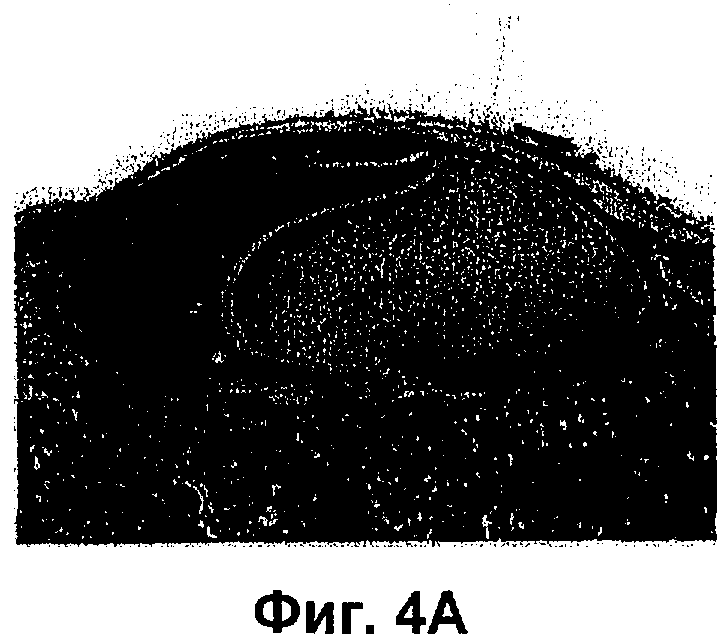
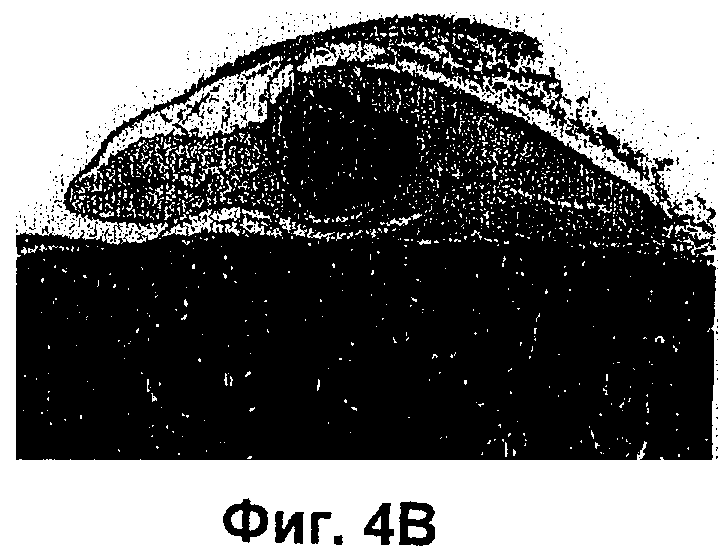


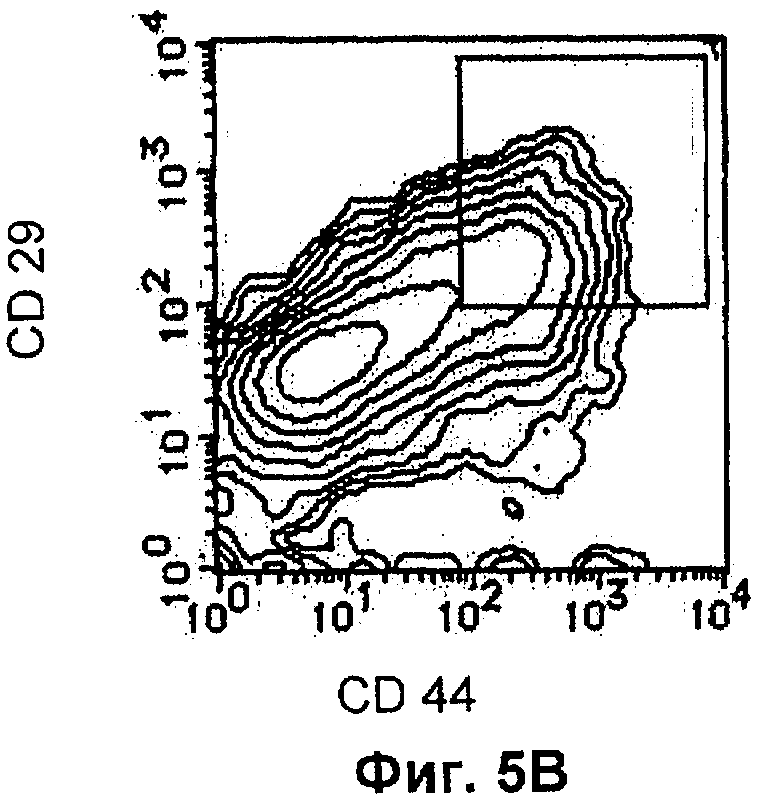
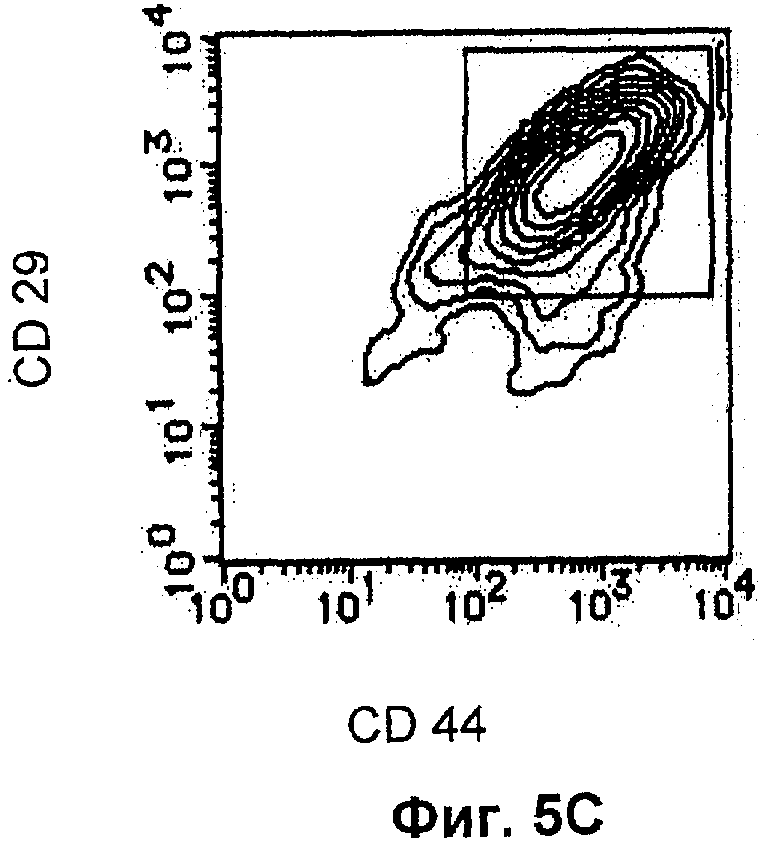



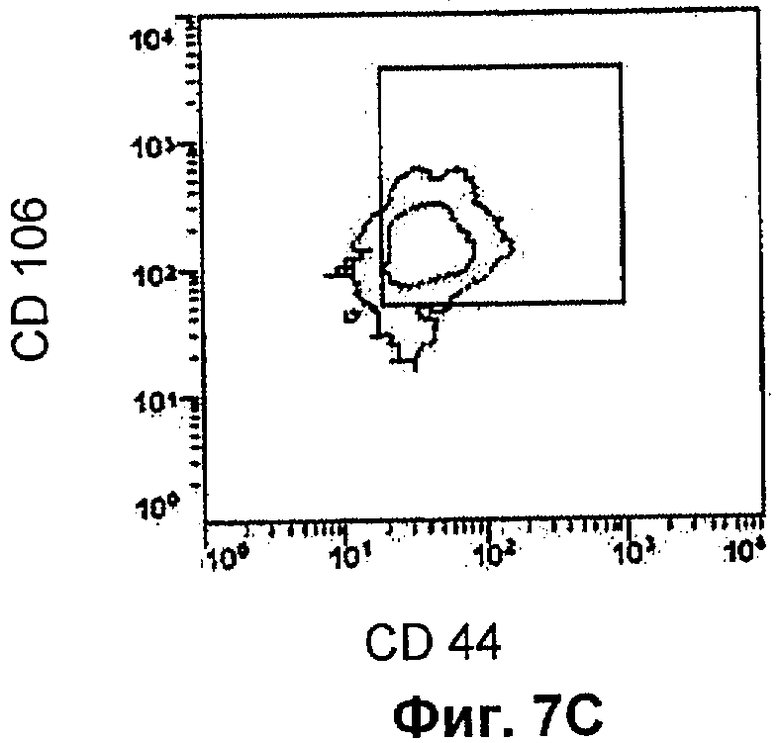
Изобретение относится к области биотехнологии, а именно к способу получения мезенхимных клеток для формирования зуба, способу создания зуба и мезенхимным клеткам для формирования зуба. Способ получения мезенхимных клеток включает выращивание клеток эмбриональной карциномы в присутствии индуктора дифференцировки, выбранного из группы, состоящей из факторов, индуцирующих клетки нервного гребешка, факторов, ответственных за развитие клеток нервного гребешка, и факторов, являющихся промоторами роста клеток нервного гребешка, для создания клеточной популяции, которая содержит СD44-позитивные и CD29-позитивные клетки и/или СD44-позитивные и СD106-позитивные клетки после обработки индуктором дифференцировки. Отбирают из клеточной популяции после обработки индуктором дифференцировки CD44-позитивные и СD29-позитивные клетки и/или СD44-позитивные и CD106-позитивные клетки в качестве мезенхимных клеток для формирования зуба. В результате получают мезенхимные клетки для формирования зуба, которые индуцированы из клеток эмбриональной карциномы и являются СD44-позитивными и СD29-позитивными или СD44-позитивными и CD106-позитивными клетками. Указанные клетки используют в способе создания зуба. Предложенное изобретение позволяет получить мезенхимные клетки для формирования зуба, которые используются при регенерации зуба. 3 н. и 6 з.п. ф-лы, 18 ил., 5 табл., 7 пр.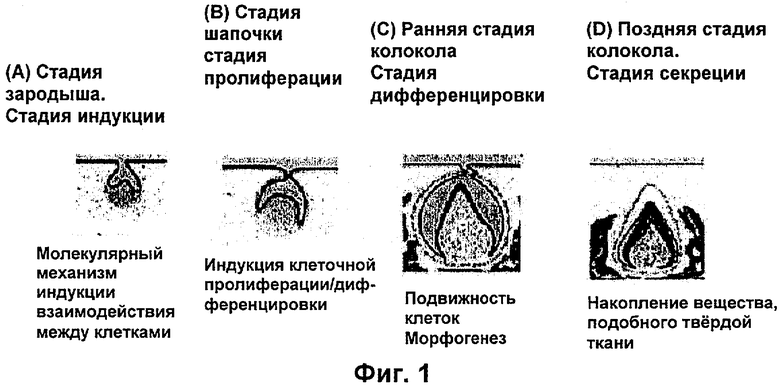
1. Способ получения мезенхимных клеток для формирования зуба, включающий:
выращивание клеток эмбриональной карциномы в присутствии индуктора дифференцировки, выбранного из группы, состоящей из факторов, индуцирующих клетки нервного гребешка, факторов, ответственных за развитие клеток нервного гребешка, и факторов, являющихся промоторами роста клеток нервного гребешка, для создания клеточной популяции, которая содержит СD44-позитивные и СD29-позитивные клетки и/или CD44-позитивные и СD106-позитивные клетки после обработки индуктором дифференцировки, и
отбор из клеточной популяции после обработки для индукции дифференцировки СD44-позитивных и СD29-позитивных клеток и/или CD44-позитивных и СD106-позитивных клеток в качестве мезенхимных клеток для формирования зуба.
2. Способ по п.1, где указанные мезенхимные клетки для формирования зуба дополнительно экспрессируют по меньшей мере один ген, который выбран из группы, состоящей из гена Slug, гена Рах3, гена Msx1 и гена Рах9.
3. Способ по п.1, где указанные мезенхимные клетки для формирования зуба дополнительно экспрессируют как ген Slug, так и ген Рах3.
4. Способ по п.1, где указанный индуктор дифференцировки представляет собой по меньшей мере одно вещество из диметилсульфоксида или ретиноевой кислоты.
5. Способ создания зуба, включающий:
позиционирование в поддерживающем носителе первой клеточной массы, по существу состоящей только из одного типа клеток, выбранного из мезенхимных клеток и эпителиальных клеток, и второй клеточной массы, по существу состоящей только из другого типа клеток, выбранного из мезенхимных клеток и эпителиальных клеток, причем первую и вторую клеточные массы не смешивают друг с другом, но приводят друг с другом в тесный контакт, и
выращивание первой и второй клеточной массы в указанном поддерживающем носителе;
где мезенхимные клетки представляют собой указанные мезенхимные клетки для формирования зуба, полученные по п.1, и
где указанные эпителиальные клетки имеют происхождение из зубного зачатка.
6. Способ по п.5, где указанное выращивание продолжают до образования периодонтальной ткани.
7. Мезенхимные клетки для формирования зуба, полученные способом по п.1, которые индуцированы из клеток эмбриональной карциномы и являются СD44-позитивными и СD29-позитивными или СD44-позитивными и CD106-позитивными клетками.
8. Мезенхимные клетки для формирования зуба по п.7, дополнительно экспрессирующие по меньшей мере один ген из группы, состоящей из гена Slug, гена Рах3, гена Msx1 и гена Рах9.
9. Мезенхимные клетки для формирования зуба по п.7, дополнительно экспрессирующие как ген Slug, так и ген Рах3.
| OHAZAMA A ET AL: "Stem-cell-based tissue engineering of murine teeth" JOURNAL OF DENTAL RESEARCH, INTERNATIONAL ASSOCIATION FOR DENTAL RESEARCH, v.83, no.7, 2004, pp.518-522 | |||
| WO 2005111197 A1, 24.11.2005 | |||
| JP 2004201612 A, 22.07.2004 | |||
| БИОТРАНСПЛАНТАТ, СПОСОБ ЕГО ПОЛУЧЕНИЯ (ВАРИАНТЫ) И СПОСОБ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ПАРОДОНТА | 2004 |
|
RU2265445C1 |
Авторы
Даты
2012-10-27—Публикация
2008-01-18—Подача