Изобретение относится к биотехнологии и медицине, а именно к клинической лабораторной диагностике, и может быть применено при гинекологической и эндокринной патологии, такой как преждевременная недостаточность яичников (ПНЯ), аутоиммунный полигландулярный синдром (АПС), болезнь Аддисона, хроническая надпочечниковая недостаточность, а также при неудачах в программах вспомогательных репродуктивных технологий (ВРТ) и осложнениях беременности. Учитывая, что данные заболевания могут длительно протекать субклинически, важно своевременно выявлять группы риска развития клинических форм болезни. ПНЯ диагностируется у 1% женщин репродуктивного возраста до 40 лет, при этом аутоиммунная форма выявляется в 4%-30% всех случаев ПНЯ в зависимости от выборки пациентов и метода определения аутоантител [1].
ПНЯ может возникать изолированно или в сочетании с другими аутоиммунными состояниями, включая болезнь Аддисона. Как правило, ПНЯ диагностируется до клинических проявлений поражения надпочечников, при этом аутоиммунитет к антигенам надпочечников развивается у 2-3% женщин с ПНЯ [2]. В связи с этим важно проводить обследование надпочечников у пациентов с ПНЯ, особенно при планировании беременности и подготовке к программе ВРТ.
Развитию ПНЯ часто предшествует аутоиммунный оофорит, который ассоциируется с аутоантителами к стероидогенным ферментам семейства цитохрома Р450, таким как 21-гидроксилаза (21OH), фермент, расщепляющий боковую цепь холестерина или 20,22-десмолаза (P450scc), 17α-гидроксилаза (17αОН) и β-гидроксистероиддегидрогеназа (β-HSD) [3]. Несмотря на то, что 21OH экспрессируется в коре надпочечников, антитела к 21OH выявляются как при болезни Аддисона, так и при идиопатической ПНЯ. В связи с этим Европейское общество репродукции человека и эмбриологии рекомендует проводить скрининг на антитела к 21-гидроксилазе у женщин с ПНЯ неизвестной этиологии или при подозрении на нарушение функции иммунной системы [4].
Для выявления антител к 21OH, P450scc и 17αН описано применение метода иммунопреципитации с использованием изотопных меток (35S-метионин или йод-125 (125I)) или люминесцентной метки (люциферазы) [5]. Недавно для определения антител к 21OH предложен иммуноферментный анализ (ИФА) с использованием биотинилированного антигена и конъюгата стрептавидин-пероксидаза [6]. Важное значение для клинической и лабораторной практики имеет разработка модификаций ИФА для определения аутоантител к ферментам стероидогенеза семейства цитохрома Р450 и оценка их диагностического значения при ПНЯ, включая антитела к 21OH, P450scc и ароматазе (ARO), которая, как известно, трансформирует андрогены в эстрогены и широко представлена во многих тканях организма: гонадах, эндометрии, мозге, жировой ткани, кровеносных сосудах, коже, костях и других.
Известен способ определения антител к 21OH с помощью иммуноферментного анализа [6], заключающийся в том, что на поверхность лунок полистирольного микропланшета (Nunc, Denmark) иммобилизуют препарат очищенной рекомбинантной 21-гидроксилазы человека, экспрессированной в Saccharomyces cerevisiae, в количестве 52.5 нг на лунку. Исследуемые образцы вносят в лунки с наслоенной 21OH по 50 мкл в повторностях, а затем добавляют по 50 мкл усилителя реакции (RSR Ltd., Великобритания), планшет встряхивают в течение 1 минуты с частотой 500 об/мин и инкубируют при 4°С в течение 16-18 часов без встряхивания. Затем содержимое лунок аспирируют, лунки промывают трижды промывным раствором (RSR Ltd.) с последующим добавлением в лунки 100 мкл раствора 21OH, конъюгированной с биотином (5 нг/лунку), проводят инкубацию при комнатной температуре (20-25°С) на встряхивателе при 500 об/мин в течение 1 часа, после инкубации раствор из лунок аспирируют, лунки планшета промывают трижды, затем добавляют конъюгат стрептавидин-пероксидаза (RSR Ltd.) по 100 мкл на лунку и инкубируют в течение 20 минут.После этапа промывания в лунки добавляют по 100 мкл субстратного раствора, содержащего 3,3',5,5'-тетраметилбензидин (RSR Ltd.), при комнатной температуре проводят ферментативную реакцию в течение 20 минут, затем реакцию останавливают добавлением 50 мкл 0,5 моль/л H2SO4 и измеряют абсорбцию (оптическую плотность (ОП)) реакционной смеси с использованием планшетного анализатора для ИФА при 450 нм. Результаты анализа выражают в условных единицах RSR или путем расчета индекса позитивности (ИП) по формуле: ИП=ОП тестируемого образца/ ОП эталонного препарата х 100
Технической задачей изобретения является создание способа лабораторной диагностики преждевременной недостаточности яичников по определению аутоантител к стероидогенным ферментам цитохрома Р450 человека, а именно к 21OH (CYP21A2), P450scc (CYP11A1) и ARO (CYP19A1) в сыворотке (плазме) крови человека методом иммуноферментного анализа.
Эта задача решается описываемым способом определения данных аутоантител, заключающимся в иммобилизации рекомбинантных ферментов цитохрома Р450 человека (CYP21A2, CYP11A1, CYP19A1) на поверхность полистирольного микропланшета из водного солевого буферного раствора (рН 7,2±0,2) в концентрации 1-5 мкг/мл, удалении раствора и промывании лунок водным буферным раствором, содержащим 0,05-0,1% твина-20, обработке поверхности водным солевым буферным раствором, содержащим 10-20 мг/мл инертного белка (бычьего сывороточного альбумина (БСА), желатина), инкубации сывороток крови, разведенных в водном буферном растворе, содержащем 5-10 мг/мл инертного белка (БСА, желатин) и 0,05-0,1% детергента твина-20, в соотношении 1:50-1:100 по объему, удалении раствора и промывании поверхности лунок до и после инкубации водным буферным раствором, содержащим 0,05-0,1% твина-20, детекции искомых антител с использованием конъюгатов мышиных моноклональных антител к иммуноглобулинам человека классов М, G с ферментом.
Практически способ осуществляется следующим образом: препараты рекомбинантных ферментов семейства цитохрома Р450 человека CYP21A2, CYP11A1, CYP19A1, экспрессированных в Е. coli (Cloud-Clone Corp., США), в водном солевом буферном растворе (фосфатно-солевом, трисовом) с рН 7,2±0,2 в концентрации 1-5 мкг/мл иммобилизуют на поверхность лунок полистирольного микропланшета с высокой адсорбционной емкостью при 20±2°С в течение 18±2 часов, после удаления жидкости поверхность лунок промывают водным буферным раствором, содержащим 0,05-0,1%) по объему твина-20 по 250-300 мкл на лунку 3-4 раза. Поверхность лунок обрабатывают водным буферным раствором, содержащим 10-20 мг/мл инертного белка (БСА, желатина) при 20±2°С в течение 60-90 минут, затем промывают водным буферным раствором, содержащим 0,05-0,1% по объему твина-20. Образцы сыворотки, плазмы крови, разведенные в соотношении 1:50-1:100 по объему в водном буферном растворе, содержащем 5-10 мг/мл инертного белка и 0,05-0,1%) по объему твина-20, инкубируют при 20±2°С на орбитальном шейкере при 100-300 об/мин в течение 30-90 минут, после удаления жидкости поверхность твердой фазы промывают водным буферным раствором, содержащим 0,05-0,1% по объему твина-20, и инкубируют с конъюгатами мышиных моноклональных антител против иммуноглобулинов человека класса М, G с пероксидазой хрена в рабочем разведении в соотношении 1:500-1:5000 по объему в водном буферном растворе, содержащем 5-10 мг/мл инертного белка и 0,05%-0,1% по объему твина-20, при 20±2°С на орбитальном шейкере при 100-300 об/мин в течение 30-90 минут. После удаления жидкости и промывания лунок водным буферным раствором, содержащим 0,05% твина-20, планшет инкубируют с субстратно-хромогенным раствором, содержащим 3,3',5,5'-тетраметилбензидин и перекись водорода, при 20±2°С в течение 15±5 минут, ферментативную реакцию останавливают добавлением равного объема 0,5М H2SO4, результат анализа оценивают инструментально путем измерения оптической плотности (ОП) реакционного раствора в лунках на фотометре при длине волны 450 нм.
Отличительной особенностью предлагаемого способа является то, что в качестве антигена используют препараты рекомбинантных ферментов семейства цитохрома Р450 человека CYP21A2, CYP11 Al, CYP19A1, экспрессированных в Е. coli; адсорбцию антигена на поверхность полистирола с высокой адсорбционной емкостью проводят в концентрации 100-500 нг/лунку из водного солевого буферного раствора (рН 7,2±0,2) при 20±2°С в течение 18±2 часов, после удаления жидкости лунки промывают водным буферным раствором, содержащим 0,05-0,1% по объему твина-20; лунки планшета обрабатывают водным буферным раствором (рН 7,2±0,2), содержащим 10-20 мг/мл инертного белка (БСА, желатина), при 20±2°С в течение 60-90 минут; образцы сыворотки, плазмы крови разводят в водном буферном растворе, содержащем 5-10 мг/мл инертного белка и 0,05-0,1%) по объему твина-20, в соотношении 1:50-1:100 по объему, и инкубируют в лунках при 20±2°С на орбитальном шейкере при 100-300 об/мин в течение 30-90 минут, лунки до и после инкубации промывают водным буферным раствором, содержащим 0,05-0,1%) по объему твина-20; проводят инкубацию с мышиными моноклональными антителами к иммуноглобулинам человека класса М, G, меченными ферментом, в водном буферном растворе, содержащем 5-10 мг/мл инертного белка и 0,05%-0,1% по объему твина-20, при 20±2°С на орбитальном шейкере при 100-300 об/мин в течение 30-90 минут.
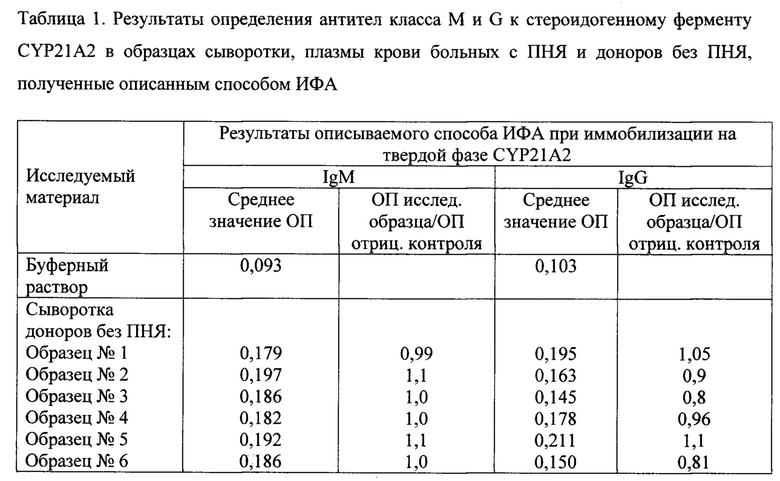
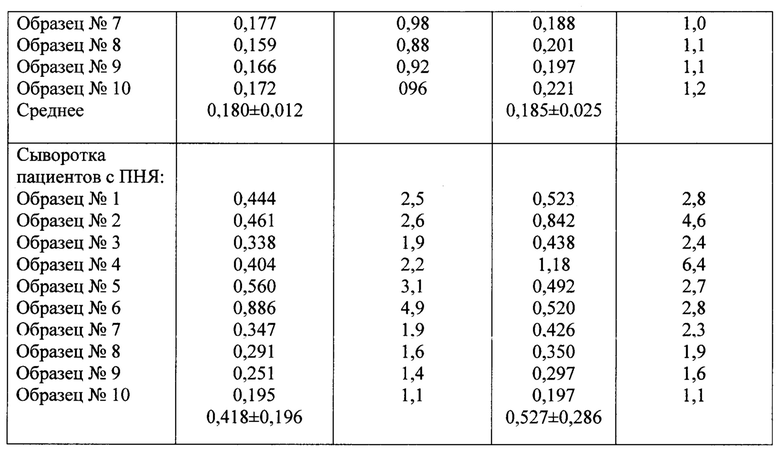
Пример 1. Для подтверждения возможности получения технического результата с помощью заявленного способа на полистирольную поверхность лунок микропланшета иммобилизуют рекомбинантный фермент человека CYP21A2 и определяют антитела к CYP21A2 классов М и G в образцах сыворотки (плазмы) крови пациенток репродуктивного возраста с ПНЯ, диагностированной по клинико-лабораторным данным, включающим данные гормонального, ультразвукового исследования (УЗИ) и лапароскопической визуализации, и в образцах сыворотки (плазмы) крови пациенток без ПНЯ с нормальным овариальным резервом. Критерии исключения из исследования: ятрогенная форма ПНЯ, сопутствующие пролиферативные гинекологические заболевания, инфекционно-воспалительные заболевания в стадии обострения, онкологические, тяжелые соматические и системные аутоиммунные заболевания.
Препарат рекомбинантного фермента семейства цитохрома Р450 человека CYP21A2 (Cloud-Clone Corp., США) с молекулярной массой 35,8 кДа (аминокислотная последовательность Aspl06~Gln389) в 0,1 М фосфатно-солевом буферном растворе (ФСБР) с рН 7,2±0,2 в концентрации 2,5 мкг/мл вносят по 100 мкл в лунки полистирольного микропланшета с высокой адсорбционной емкостью (Nunc™ MaxiSorp, Thermo Fisher Scientific Inc., США) и инкубируют при 20±2°С в течение 18±2 часов, жидкость из лунок удаляют, поверхность лунок промывают ФСБР, содержащим 0,05% по объему твина-20, по 300 мкл в лунку 3 раза. В лунки планшета вносят по 200 мкл ФСБР, содержащего 10 мг/мл БСА, и инкубируют при 20±2°С в течение 90 минут, после удаления жидкости лунки промывают ФСБР, содержащим 0,05% по объему твина-20, 3 раза. Образцы сыворотки, плазмы крови, предварительно разведенные в соотношении 1:100 по объему в ФСБР, содержащем 5 мг/мл БСА и 0,05% по объему твина-20, вносят в лунки по 100 мкл и инкубируют при 20±2°С на орбитальном шейкере при 200 об/мин в течение 60 минут, затем после удаления жидкости поверхность твердой фазы промывают ФСБР, содержащим 0,05% по объему твина-20, 3 раза. В лунки вносят по 100 мкл конъюгатов мышиных моноклональных антител к IgM и IgG человека с пероксидазой хрена, разведенных в ФСБР, содержащем 5 мг/мл БСА и 0,05% по объему твина-20, в соотношении 1:2500 и 1:3000 по объему, и инкубируют при 20±2°С на орбитальном шейкере при 200 об/мин в течение 60 минут. После удаления раствора и промывания лунок ФСБР, содержащим 0,05% по объему твина-20, в лунки вносят по 100 мкл субстратно-хромогенного раствора, содержащего 3,3',5,5'-тетраметилбензидин и перекись водорода, инкубируют при 20±2°С в темноте в течение 15±5 минут, ферментативную реакцию останавливают добавлением 100 мкл 0,5М H2SO4. Результат анализа оценивают инструментально путем измерения ОП раствора в лунках микропланшета на фотометре при длине волны 450 нм.
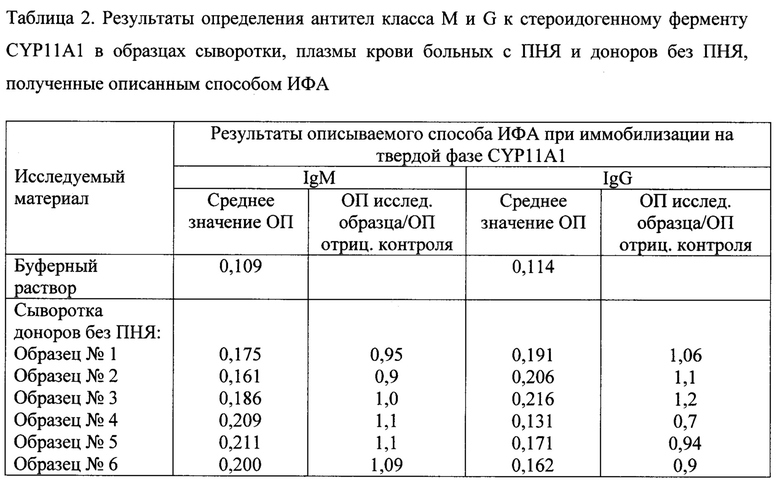
Пример 2. Анализ проводят аналогично способу, описанному в примере 1, за исключением того, что в качестве антигена для иммобилизации на твердую фазу используют препарат рекомбинантного фермента семейства цитохрома Р450 человека CYP11A1 (Cloud-Clone Corp., США) с молекулярной массой 18 кДа и аминокислотной последовательностью Val392~Gln521.

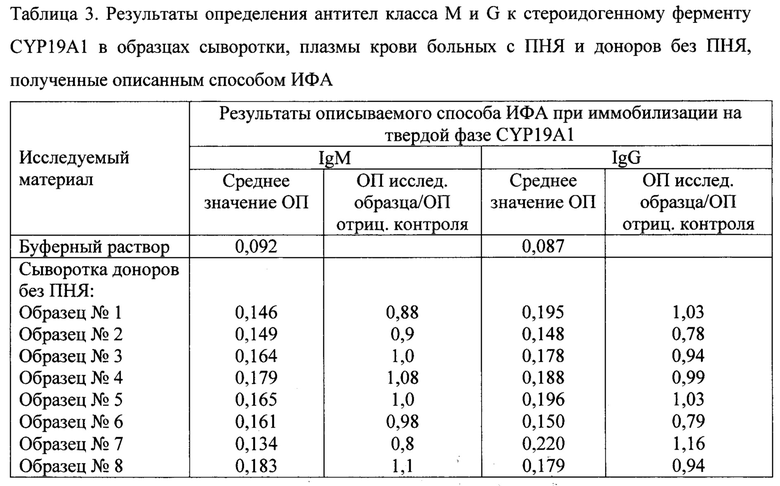
Пример 3. Анализ проводят аналогично способу, описанному в примере 1, за исключением того, что в качестве антигена для иммобилизации на твердую фазу используют препарат рекомбинантной ароматазы человека (CYP19A1) (Cloud-Clone Corp., США) с молекулярной массой 22,3 кДа и аминокислотной последовательностью Leul96~Val373.

Пример 4. Анализ проводят аналогично способу, описанному в примере 1, за исключением того, что в качестве антигена на поверхность твердой фазы иммобилизуют инертный белок БСА в концентрации 5 мг/мл.
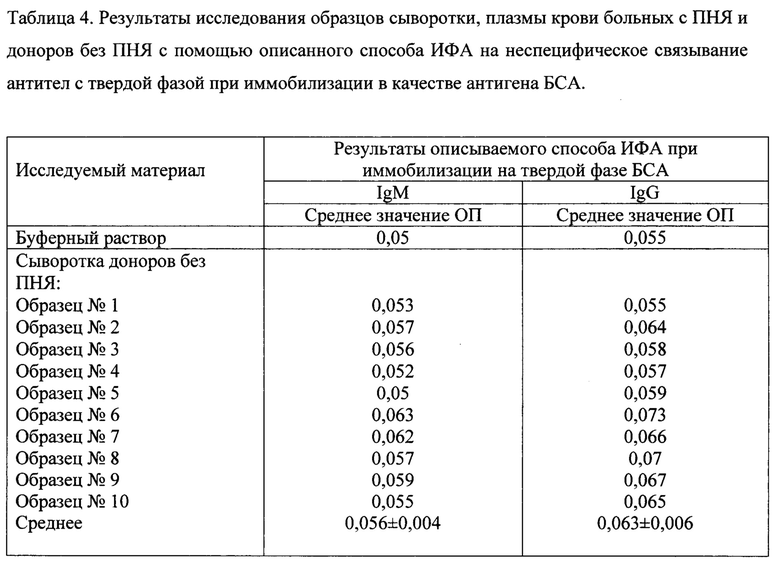

Пример 5. Анализ проводят аналогично способу, описанному в примере 1, в качестве антигенов на поверхность лунок полистирольных микропланшетов иммобилизуют CYP21A2, CYP11A1 и CYP19A1. Исследуют сыворотки больных с ПИЯ (n=21) и сыворотки пациентов без ПНЯ (n=20), диагностированных по клинико-лабораторным данным, включающим данные гормонального, ультразвукового исследования и лапароскопической визуализации, с исключением из исследования пациентов с ятрогенной формой ПНЯ, сопутствующими пролиферативными гинекологическими заболеваниями, инфекционно-воспалительными заболеваниями в стадии обострения, онкологическими, тяжелыми соматическими и системными аутоиммунными заболеваниями. Оценивают диагностическое значение данных антител с помощью ROC-анализа, а также диагностическую точность - с помощью анализа логистической регрессии.
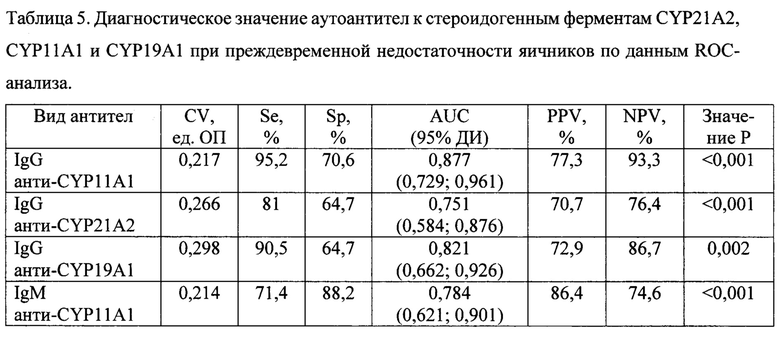
Примечание: CV - значение критерия, Se - чувствительность, Sp - специфичность, AUC -площадь под ROC-кривой, PPV - положительная прогностическая значимость, NPV -отрицательная прогностическая значимость.
Использование данного способа подтверждается конкретными клиническими примерами:
Пример 1.
Пациентка К. 34 лет поступила в гинекологическое отделение для проведения хирургического лечения с диагнозом первичного бесплодия и преждевременной недостаточности яичников: аменореей в течение 2 лет, снижением овариального резерва (фоликулостимулирующий гормон (ФСГ) до 44 мМЕ/мл, антимюллеров гормон (АМГ) 0,01 нг/мл, ультразвуковые признаки (У3-признаки) ПНЯ (снижение количества антральных фолликулов (КАФ), уменьшение объема яичников)).
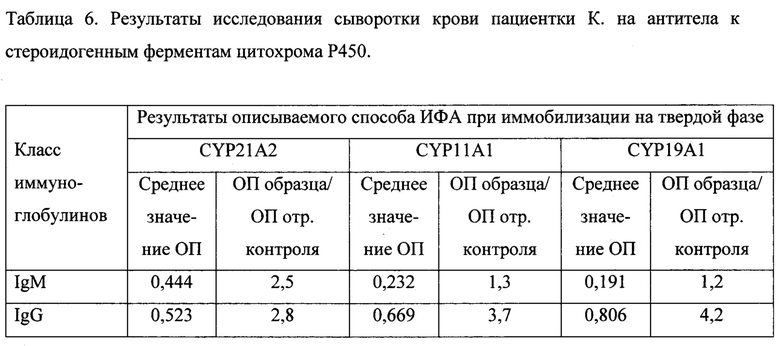
Пример 2.
Пациентка В. 38 лет поступила в гинекологическое отделение для проведения хирургического лечения с диагнозом первичного бесплодия, неэффективными попытками ЭКО в анамнезе и преждевременной недостаточности яичников: аменореей в течение 10 лет, снижением овариального резерва (ФСГ до 49,6 мМЕ/мл, АМГ 0,01 нг/мл, У3-признаки ПНЯ).

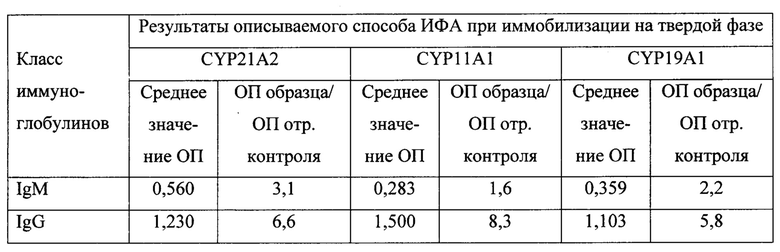
Пример 3.
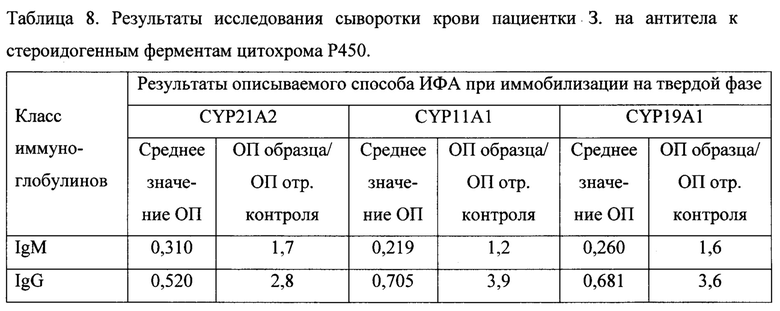
Пациентка 3. 30 лет поступила в гинекологическое отделение для проведения хирургического лечения с диагнозом первичного бесплодия и преждевременной недостаточности яичников, аменореей в течение 10 лет, снижением овариального резерва (ФСГ до 20,7 мМЕ/мл, АМГ 0,01 нг/мл, У3-признаки ПНЯ).
Пример 4
Пациентка Б., 41 год поступила в гинекологическое отделение для проведения хирургического лечения с диагнозом вторичного бесплодия и преждевременной недостаточности яичников, аменореей в течение 6 месяцев, снижением овариального резерва (ФСГ до 47,9 мМЕ/мл, АМГ 0,01 нг/мл, У3-признаки ПНЯ).

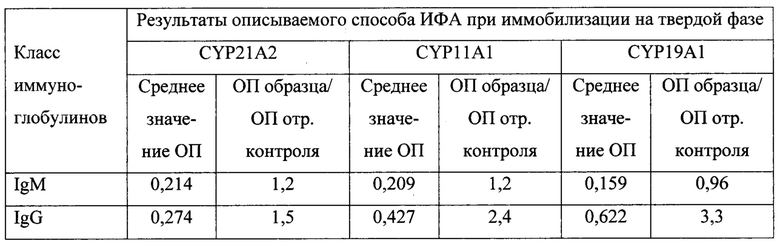
Описанная методика непрямого твердофазного ИФА с использованием в качестве антигенов для иммобилизации рекомбинантных ферментов CYP21A2, CYP11A1 и CYP19A1 эффективно выявляет аутоантител а к этим стероид огенным ферментам разных классов в сыворотке (плазме) крови человека. По данным таблиц 1-3, описанный способ показывает высокие значения ОП у пациентов с ПНЯ и низкие значения ОП у пациентов в группе сравнения без ПНЯ при исследовании сыворотки крови в разведении в соотношении 1:100 по объему, низкие значения ОП в лунках с буферным раствором вместо сыворотки (плазмы) крови, а также высокие значения индекса позитивности как соотношения ОП исследуемых образцов к ОП отрицательного контроля, достигающие 6,4 при определении антител (М, G) к CYP21A2, 7,8 при определении антител к CYP11A1, 5,7 при определении антител к CYP19A1, и, таким образом, обеспечивает высокую чувствительность и специфичность определения данных антител в сыворотке (плазме) крови. При этом пациенты с ПНЯ имеют разные комбинации и разный профиль аутоантител к стероидогенным ферментам.
Данные, приведенные в таблице 4, демонстрируют при исследовании положительных сывороток больных с ПНЯ низкий уровень неспецифического связывания антител с инертным белком (БСА), который используется для блокирования свободных центров связывания на полистироле при приготовлении твердой фазы, что подтверждает высокую специфичность и точность определения антител (М, G) к данным стероидогенным ферментам.
В таблице 5 представлены данные ROC-анализа, демонстрирующие высокое диагностическое значение IgG-антител к CYP11 Al, CYP19A1 и CYP21A2 и IgM-антител к CYP11A1 при ПНЯ: высокие показатели чувствительности (71,5%-95,2%), специфичности (64,7%-88,2%) и значения AUC (0,751-0,877), а также положительной и отрицательной прогностической значимости (>70%). При этом наиболее высокие показатели были получены при определении IgG-антител к CYP11A1: чувствительность 95,2%, специфичность 70,6%, значение AUC 0,877. По данным анализа логистической регрессии, процент корректно классифицированных случаев заболевания на основании определения данных антител варьировал от 68,4% до 78,9%>и достигал максимального значения при определении IgG-антител к CYP11A1. По данным анализа логистической регрессии при определении комбинации аутоантител для диагностики ПНЯ, включающей IgG-антитела к CYP11 Al, CYP19A1 и CYP21A2 и IgM-антитела к CYP11A1, значение AUC повышалось и достигало 0,955 (0,834; 0,996) (Р<0,0001), а процент корректно классифицированных случаев заболевания составлял 84,2%.
Пациентки с выраженной клинической картиной ПНЯ показали характерный профиль аутоантител к стероидогенным ферментам цитохрома Р450 человека (таблицы 6-9) с более значительным повышением уровня IgG-антител к CYP11A1 и CYP19A1, особенно у больных с длительным течением заболевания, и повышением в меньшей степени уровня IgG-антител к CYP21A2 и IgM-антител разной специфичности.
Таким образом, описанный способ является простым в исполнении и эффективно выявляет аутоантитела к стероидогенным ферментам цитохрома Р450 человека CYP11A1, CYP19A1 и CYP21A2 в сыворотке (плазме) крови человека. Установлено, что данные антитела имеют высокое диагностическое значение при ПНЯ, являются эффективными биомаркерами заболевания и их определение повышает качество диагностики ПНЯ.
Данное изобретение может быть использовано в биотехнологии и медицине для создания диагностических тест-систем для определения антител к стероидогенным ферментам цитохрома Р450 человека CYP11A1, CYP19A1 и CYP21A2, применение которых для диагностики и уточнения этиопатогенеза при эндокринной и акушерско-гинекологической патологии будет способствовать своевременному проведению этиотропной терапии заболевания, повышению эффективности программ ВРТ и улучшению исходов беременности у данных пациенток.
Список литературы
1. Kirshenbaum М., Orvieto R. Premature ovarian insufficiency (POI) and autoimmunity-an update appraisal. Journal of Assisted Reproduction and Genetics/ 2019; 36:2207-2215. https://doi.org/10.1007/sl 0815-019-01572-0
2. Vogt E.C., Bratland E., Berland S., Berentsen R., Lund A., Björnsdottir S., Husebye E., ∅ksnes M. Improving diagnostic precision in primary ovarian insufficiency using comprehensive genetic and autoantibody testing. Human Reproduction, 2023, 00(0), 1-13. DOI: 10.1093/humrep/dead233.
3. Chen J., Wu S., Wang M., Zhang H., Cui M. A review of autoimmunity and immune profiles in patients with primary ovarian insufficiency. Medicine. 2022; 101:51 (e32500). http://dx.doi.org/10.1097/MD.0000000000032500
4. Webber L, Davies M, Anderson R, Bartlett J, Braat D, Cartwright B, Cifkova R, de Muinck Keizer-Schrama S, Hogervorst E, Janse F et al. ESHRE guideline: management of women with premature ovarian insufficiency. Hum. Reprod. 2016; 31:926-937.
5. Falorni A, Bini V, Betterle C, Brozzetti A, Castano L, Fichna M, Kämpe O, Mellgren G, Peterson P, Chen S, Ronnelid J, Seissler J, Tiberti C, Uibo R, Yu L, Lernmark Å, Husebye E. Determination of 21-hydroxylase autoantibodies: inter-laboratory concordance in the Euradrenal International Serum Exchange Program. Clin. Chem. Lab. Med. 2015; 53(11):1761-70.
6. Del Pilar Larosa, Chen S., Steinmaus N., Macrae H., Guo L., Masiero S., Garelli S., Costa M.D., Bossowski A., Furmaniak J., Betterle C, Smith B.R. A new ELISA for autoantibodies to steroid 21-hydroxylase. Clin. Chem. Lab. Med. 2018; 56(6):933-938. doi: 10.1515/cclm-2017-0456.
Изобретение относится к области биотехнологии, в частности к способу лабораторной диагностики преждевременной недостаточности яичников. Указанный способ основан на определении аутоантител к стероидогенным ферментам цитохрома Р450 в сыворотке и плазме крови методом иммуноферментного анализа. Изобретение обеспечивает способ лабораторной диагностики преждевременной недостаточности яичников по определению аутоантител к стероидогенным ферментам цитохрома Р450 человека, а именно к CYP21A2, CYP11A1 и CYP19A1, в сыворотке крови человека методом иммуноферментного анализа. 9 табл., 4 пр.
Способ лабораторной диагностики преждевременной недостаточности яичников по определению аутоантител к стероидогенным ферментам цитохрома Р450 в сыворотке и плазме крови методом иммуноферментного анализа, включающий адсорбцию стероидогенных ферментов на поверхность полистирола, обработку поверхности водным раствором инертного белка, инкубацию с разведенной сывороткой, плазмой крови, инкубацию с антителами к иммуноглобулинам человека, меченными ферментом, инкубацию с субстратно-хромогенным раствором, отличающийся тем, что на поверхность лунок полистирольного микропланшета с высокой адсорбционной емкостью адсорбируют рекомбинантные ферменты цитохрома Р450 человека CYP11A1 с аминокислотной последовательностью Va1392~Gln521, CYP19A1 с аминокислотной последовательностью Leu196~Va1373, CYP21A2 с аминокислотной последовательностью Asp106~Gln389 в водном фосфатно-солевом или трисовом буферном растворе с рН 7,2±0,2 в концентрации 1-5 мкг/мл при 20±2°С в течение 18±2 часов, поверхность лунок промывают указанным буферным раствором, содержащим 0,05-0,1% по объему твина-20, и обрабатывают водным буферным раствором, содержащим инертный белок БСА или желатин в концентрации 10-20 мг/мл, при 20±2°С в течение 60-90 минут; инкубируют с образцами сыворотки, плазмы крови, разведенными в буферном растворе, содержащем инертный белок в концентрации 5-10 мг/мл и 0,05-0,1% по объему твина-20, в соотношении 1:50-1:100 по объему, при 20±2°С на орбитальном шейкере при 100-300 об/мин в течение 30-90 минут; поверхность до и после инкубации промывают буферным раствором, содержащим 0,05-0,1% по объему твина-20; инкубируют с мышиными моноклональными антителами к иммуноглобулинам человека класса М, G, меченными пероксидазой хрена, при 20±2°С на орбитальном шейкере при 100-300 об/мин в течение 30-90 минут; используют субстратно-хромогенный раствор, содержащий 3,3',5,5'-тетраметилбензидин и перекись водорода, и стоп-реагент, измеряют оптическую плотность раствора при длине волны 450 нм.
| US 6458550B1, 01.10.2002 | |||
| IPEK EVRUKE et al | |||
| Скоропечатный станок для печатания со стеклянных пластинок | 1922 |
|
SU35A1 |
| Exp | |||
| Obst | |||
| Gyn., 01.02.2023, vol | |||
| Устройство для выпрямления многофазного тока | 1923 |
|
SU50A1 |
| НУРАЛИЕВА Н.Ф | |||
| и др | |||
| Выбрасывающий ячеистый аппарат для рядовых сеялок | 1922 |
|
SU21A1 |
Авторы
Даты
2024-10-31—Публикация
2023-12-15—Подача