Изобретение относится к кремнийорганической химии, а именно к способам получения α,ω-бис(метилдифенилсилил)олигодиорганосилоксанов общего вида:
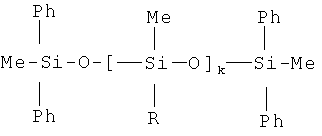
где k=1, 2; для k=1 R=Me (1a), R=Ph (1b); для k=2 R=Ph (1в),
которые находят свое применение в качестве рабочих жидкостей паромасляных вакуумных насосов для создания умеренного и сверхглубокого вакуума; в качестве рабочих тел капельных холодильников-излучателей бескаркасных систем отвода низкопотенциального тепла космических ядерных энергетических установок.
К качеству силиконовых вакуумных жидкостей, применяющихся в космических объектах, предъявляются повышенные требования, для обеспечения которых необходимо использовать безводный метилдифенилсиланолят натрия при их получении.
Известен способ получения α,ω-бис (метилдифенилсилил)диметил-, метилфенил- или дифенил- трисилоксана реакцией силанолята натрия (MePh2SiONa) с дихлорсиланами (MeRSiCl2, где R=Me, Ph) (Патент US 3523131, МПК C07F 7/08, 1970), в котором для обезвоживания полученного метилдифенилсиланолята натрия проводят азеотропную отгонку воды. В результате азеотропной перегонки удаляют спирт, влагу и частично толуол, а критерием окончания отгонки является постоянство температуры в парах, которая соответствует температуре кипения толуола.
Способ имеет существенный недостаток, заключающийся в том, что азеотропная перегонка не обеспечивает полного обезвоживания метилдифенилсиланолят натрия.
Наиболее близким по технической сущности и достигаемому эффекту к предложенному способу и принятое за прототип является технологическое решение (J.F.Hyde et all. // J. Amer. Chem. Soc., 1953, Vol.75, №22, P.5615), согласно которому полное обезвоживание осуществляют в результате многократной азеотропной осушки метилдифенилсиланолята натрия с толуолом.
Данный способ является крайне нетехнологичным и имеет много недостатков:
- использование легковоспламеняющихся и токсичных растворителей требует решения вопросов технологической и экологической безопасности;
- необходимость многократно регенерировать растворитель приводит к дополнительным трудо- и энергозатратам и значительно увеличивает время синтеза;
- необходимость утилизации отходов.
Задача предлагаемого изобретения заключается в создании простого безопасного способа обезвоживания метилдифенилсиланолята натрия, использующегося в процессе получения α,ω-бис(метилдифенилсилил)олигодиорганосилоксанов, сокращение энергетических, трудовых и временных затрат и улучшение экологической обстановки.
Указанная задача достигается тем, что предложен способ получения α,ω-бис(метилдифенилсилил)олигодиорганосилоксанов конденсацией диорганодихлорсилана и метилдифенилсиланолята натрия, включающий стадию осушки метилдифенилсиланолята натрия, отличающийся тем, что осушку проводят диметилдихлорсиланом, взятым в количестве от 0,1 до 1% мол. от количества силанолята натрия.
Процесс осуществляют следующим образом: в реакционную колбу помещают расчетное количество едкого натра, суспендированного в толуоле, добавляют определенное количество метанола и при энергичном перемешивании осторожно прикапывают метилдифенилсилан или диметилтетрафенилдисилоксан, не допуская сильного вспенивания за счет выделяющегося водорода. По окончании выделения водорода отгоняют спирт и частично толуол при атмосферном давлении до постоянной температуры в парах 110°С. Полученный продукт охлаждают, добавляют технологически необходимое количество свежего толуола и диметилдихлорсилан (ДМДХС) в качестве осушителя, выдерживают при энергичном перемешивании, после чего прикапывают расчетное количество диорганодихлорсилана с диметильными, метилфенильными или дифенильными звеньями. Смесь выдерживают при повышенной температуре до завершения реакции, после чего охлаждают, добавляют 20%-ную соляную кислоту до слабокислой реакции среды, отделяют органический слой и отгоняют растворитель и последующей вакуумной ректификацией выделяют целевой продукт.
Применение высокоактивного ДМДХС оказывает не только исчерпывающее дегидратирующее действие на стадии получения силанолята натрия, но также нейтрализующее, диспергирующее и промотирующее действие на последующий процесс его гетерофункциональной конденсации до целевых олигометилфенилсилоксанов.
Предлагаемый способ иллюстрируется следующими примерами.
Пример 1.
В реакционную колбу, снабженную мешалкой, термометром, капельной воронкой загружают 80 г (2 моль) едкого натра, 600 мл сухого толуола, добавляют 80 мл метанола, затем при энергичном перемешивании к смеси прикапывают 410 г (1 моль) симметричного диметилтетрафенилдисилоксана, после чего реакционную смесь выдерживают при нагревании в течение 4 часов, отгоняют растворители при атмосферном давлении до достижения температуры в парах 110°С, при этом отгоняют весь спирт и около половины загруженного толуола. Образовавшийся силанолят натрия охлаждают, добавляют к нему 400 мл толуола и 2 г (0,77% мол. от количества силанолята натрия) ДМДХС и проводят полное обезвоживание раствора силанолята натрия при энергичном перемешивании в течение 30 мин. Затем прикапывают раствор 127 г (1 моль) ДМДХС в 125 мл толуола. Смесь выдерживают при 70°С, охлаждают, добавляют 20%-ную соляную кислоту до слабокислой реакции среды, отделяют органический слой и отгоняют растворитель сначала при атмосферном давлении, затем при остаточном давлении 10 мм рт.ст. Последующей вакуумной ректификацией остатка выделяют 411 г (выход 85%) трисилоксана (Ia). Содержание основного вещества - 99%. Кинематическая вязкость продукта при 20°С составляла значение 45 сСт. Спектр ЯМР 1H, δ, м.д. (CDCl3): 7,26-7,56 м (20Н, 4С6Н5), 0,58 с (6Н, 2СН3), 0,097 с (6Н, 2СН3). Упругость пара при 20°С составляла 1,5×10-9 мм рт.ст.
Пример 2.
Метилдифенилсиланолят натрия получают по способу и в количестве, указанном в примере 1. После отгонки спирта и половины загруженного толуола массу охлаждают, добавляют 400 мл толуола и 2 г (0,77% мол. от количества образовавшегося силанолята натрия) ДМДХС и при энергичном перемешивании проводят полное обезвоживание раствора силанолята натрия в течение 30 мин. Затем к массе прикапывают смесь 62,5 г (0,5 моль) ДМДХС, 95,5 г (0,5 моль) МФДХС и 150 мл толуола. Смесь выдерживают 5 часов при 70°С, охлаждают, добавляют 20%-ную соляную кислоту до слабокислой реакции среды, отделяют органический слой и отгоняют растворитель. Последующей вакуумной ректификацией остатка выделяют 463 г (выход около 90%) смеси 47% мас. трисилоксана (Ia) и 53% мас. трисилоксана (Iб) по спектру ЯМР. Кинематическая вязкость продукта при 20°С составляла значение 85 сСт. Спектр ЯМР 1Н, δ, м.д. (CDCl3): 7,26-7,56 м (20Н, 4С6Н5), 0,584 с (6Н, 2СН3 - Ia), 0,552 с (6Н, 2СН3 - Iб), 0,314 с (3Н, СН3 - Iб), 0,097 с (6Н, 2СН3 - Ia). Упругость пара при 20°С составляла 7,5×10-10 мм рт.ст.
Пример 3.
В реакционную колбу, снабженную мешалкой, термометром, капельной воронкой, загружают 40 г (1 моль) едкого натра, 300 мл сухого толуола, добавляют 20 мл метанола и к смеси осторожно прикапывают при энергичном перемешивании 198 г (1 моль) свежеперегнанного метилдифенилсилана, не допуская сильного вспенивания за счет выделяющегося водорода. По окончании выделения водорода растворители отгоняют при атмосферном давлении до достижения температуры в парах 110°С, при этом отгоняется весь спирт и около половины загруженного толуола. Массу охлаждают, добавляют 200 мл толуола и 1,29 г (1% мол. от количества образовавшегося силанолята натрия) ДМДХС и при энергичном перемешивании проводят полное обезвоживание раствора силанолята натрия в течение 30 мин. Затем к реакционной массе прикапывают смесь 93,5 г (0,489 моль) МФДХС и 100 мл толуола. Смесь выдерживают 5 часов при 70°С, охлаждают, добавляют 20%-ную соляную кислоту до слабокислой реакции среды, отделяют органический слой и отгоняют растворитель. Последующей вакуумной ректификацией остатка выделяют 215 г (выход около 77%) трисилоксана (Iб), содержащего по спектру ЯМР в качестве сопутствующего вещества только 1,5% мас. трисилоксана (Ia). Кинематическая вязкость продукта при 20°С составляла значение 200 сСт. Упругость пара при 20°С составляла 2,5×10-10 мм рт.ст. Спектр ЯМР 1Н, δ, м.д. (CDCl3): 7,26-7,56 м (20Н, 4С6Н5), 0,584 с (6Н, 2СН3 - Ia), 0,552 с (6Н, 2СН3 - Iб), 0,314 с (3Н, СН3 - Iб), 0,097 с (6Н, 2СН3 - Ia).
Пример 4.
Синтез проводят аналогично указанному в примере 3, но ДМДХС и МФДХС добавляют в количестве 12,9 г (0,1 моль) и 115 г (0,6 моль) соответственно. Вакуумной ректификацией выделяют 277 г (выход около 88%) смеси трисилоксанов (Ia-в) в массовом соотношении 1:3,4:2,1 по данным спектров ЯМР. Кинематическая вязкость продукта при 20°С составляла значение 198 сСт. Упругость пара при 20°С составляла 1,5×10-10 мм рт.ст. Спектр ЯМР 1Н, δ, м.д. (CDCl3): 7,26-7,56 м (20Н, 4С6Н5), 0,584 с (6Н, 2СН3 - Ia), 0,552 с (6Н, 2СН3 - Iб), 0,538 д (6Н, 2СН3 - Iв), 0,314 с (3Н, СН3 - Iб), 0,273 с (3Н, СН3 - Iв), 0,229 с (3Н, СН3 - Iв), 0,097 с (6Н, 2СН3 - Ia). Дополнительной вакуумной ректификацией могут быть выделены индивидуально чистые силоксаны (Ia) и (Iв).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ МЕТАКРИЛОКСИМЕТИЛАЛКОКСИСИЛАНОВ | 2016 |
|
RU2612252C1 |
| Способ получения органоциклосилоксанов | 1976 |
|
SU556158A1 |
| СПОСОБ ПОЛУЧЕНИЯ ФТОРОРГАНОСИЛОКСАНОВЫХ СОПОЛИМЕРОВ | 2011 |
|
RU2455319C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-АЛКОКСИКАРБОНИЛМЕТИЛПИРРОЛИДОНОВ-2 | 1992 |
|
RU2032668C1 |
| БИС[2-(ТОЗИЛАМИНО)БЕНЗИЛИДЕН-N-АЛКИЛ(АРИЛ, ГЕТАРИЛ)АМИНАТЫ]ЦИНКА, ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЮМИНОФОРОВ | 2006 |
|
RU2295527C1 |
| БИС-[2-(ЗАМЕЩЁННЫЕ БЕНЗИЛИДЕН)-3',4'-ДИМЕТОКСИФЕНИЛЭТИЛИМИНАТЫ]ЦИНКА(II), ОБЛАДАЮЩИЕ ЛЮМИНЕСЦЕНТНОЙ АКТИВНОСТЬЮ | 2015 |
|
RU2602263C1 |
| Фосфорилсодержащие четвертичные соли аммония с высшими алкильными заместителями, обладающие бактерицидной и фунгицидной активностью | 2021 |
|
RU2770537C1 |
| СПОСОБЫ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 4А,5,9,10,11,12-ГЕКСАГИДРО-6Н-БЕНЗОФУРО(3А,3,2-EF)(2)БЕНЗАЗЕПИНА И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ | 1995 |
|
RU2146258C1 |
| ПРОИЗВОДНЫЕ ГУАНИДИНАЛКИЛ-1,1-БИС-ФОСФОНОВОЙ КИСЛОТЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ЛЕКАРСТВЕННОЕ СРЕДСТВО И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1992 |
|
RU2124519C1 |
| СПОСОБ ПОЛУЧЕНИЯ (R) - (Z) - 7 (2-АМИНО-2-КАРБОКСИЭТИЛ) ТИО-2- (2,2-ДИМЕТИЛЦИКЛОПРОПИЛКАРБОНИЛ)АМИНО-2-ГЕПТЕНОВОЙ КИСЛОТЫ | 1993 |
|
RU2046792C1 |
Изобретение относится к способам получения олигодиорганосилоксанов, используемых в качестве рабочих жидкостей паромасляных вакуумных насосов для создания умеренного и сверхглубокого вакуума; в качестве рабочих тел капельных холодильников-излучателей бескаркасных систем отвода низкопотенциального тепла космических ядерных энергетических установок. Предложен способ получения α,ω-бис(метилдифенилсилил)олигодиорганосилоксанов формулы (I), где k=1, 2; для k=1 R-Me (1a), R=Ph (1b); для k=2 R-Ph (1в), конденсацией диорганодихлорсилана и метилдифенилсиланолята натрия, включающий стадию осушки метилдифенилсиланолята натрия, которую проводят диметилдихлорсиланом, взятым в количестве от 0,1 до 1% мол. от количества силанолята натрия. Технический результат - предложенный способ экологичен и приводит к снижению энергетических, трудовых и временных затрат. 4 пр.
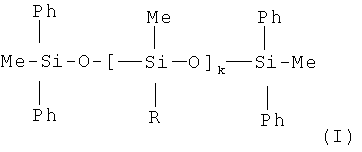
Способ получения α,ω-бис(метилдифенилсилил)олигодиорганосилоксанов конденсацией диорганодихлорсилана и метилдифенилсиланолята натрия, включающий стадию осушки метилдифенилсиланолята натрия, отличающийся тем, что осушку проводят диметилдихлорсиланом, взятым в количестве от 0,1 до 1 мол.% от количества силанолята натрия.
| J.Franklin Hyde et al | |||
| Sodium and Potassium Salts of Triorganosilanols | |||
| Journal of the American Chemical Society, 1953, vol.75, No.22, pp.5615-5618 | |||
| US 3523131 A, 04.08.1970 | |||
| Способ получения жидких полиметилфенилсилоксанов | 1961 |
|
SU141156A1 |
| Способ изготовления высокопрочной проволоки | 1978 |
|
SU799852A1 |
Авторы
Даты
2013-01-10—Публикация
2011-11-25—Подача