ПЕРЕКРЕСТНЫЕ ССЫЛКИ НА СВЯЗАННЫЕ ЗАЯВКИ
[0001] По этой заявке испрашиваются приоритеты по временным заявкам на патенты №61/054,785, поданной 20 мая 2008, №61/102,913, поданной 6 октября 2008, и №61/179,674, поданной 19 мая 2009, содержание которых включается здесь ссылкой.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
[0002] Это изобретение относится к способу индуцирования гибели клеток за счет индуцирования температурного шокового ответа в клетке в сочетании с ингибированием адаптивного температурного шокового ответа.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
[0003] Рак является главной проблемой здравоохранения. Он составляет приблизительно одну четверть всех смертельных случаев в Соединенных Штатах и является главной причиной смерти среди мужчин и женщин в возрасте до 85 лет. Пожизненная вероятность развития рака составляет 46% для мужчин и 38% для женщин. Многие способы лечения рака сопровождаются побочными эффектами, включающими тошноту, рвоту, потерю волос, лихорадку и риск инфекции. Химиотерапия и лучевая терапия обе приводят к высоким скоростям воспаления слизистой оболочки полости рта и слизистой оболочки желудочно-кишечного тракта (гастроинтестинальной) у лечившихся пациентов, и эти эффекты могут являться ограничивающими дозу токсичности некоторых способов лечения.
[0004] Опухолевые клетки приобретают высокий уровень адаптивного температурного шокового ответа. Температурный шоковый ответ - адаптивный механизм, используемый всеми живыми клеточными организмами, чтобы остаться в живых в условиях так называемого протеотоксического стресса - состояния, заканчивающегося накоплением неправильно упакованных белков, которые имеют тенденцию к агрегации, приводящей к гибели клеток из-за общей денатурации белка, вызванной такой агрегацией. Клетки могут активизировать этот защитный механизм, вызывая синтез дополнительных белковых шаперонов, известных как белки теплового шока (HSP).
[0005] Жизнеспособность опухолевых клеток может зависеть от температурного шокового ответа, поскольку они имеют более высокий уровень неправильной упаковки белка. Однако эффективность температурных способов лечения рака ограничена индукцией адаптивного температурного шокового ответа, который может значительно уменьшить чувствительность опухолевой клетки к лечению и ограничить использование термотерапии и других модулирующих тепловой шок способов терапии. Соответственно, существует потребность в улучшенных способах индуцирования гибели клеток.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
[0006] Представленный здесь способ индуцирования гибели клеток может включать ингибирование и индуцирование адаптивного температурного шокового ответа в клетке. Температурный шоковый ответ может быть вызван применением агента индуцирования температурного шока к клетке. Агент индуцирования температурного шока может быть гелданамицином, ингибитором протеасом, арсенитом или этанолом. Температурный шоковый ответ может быть также вызван увеличением внутренней температуры клетки, которое может быть осуществлено с помощью нагревающих средств. Температура может быть повышена до по крайней мере 39-60°С, и может быть увеличена инфракрасным излучением. Излучение может иметь длину волны 5-15 мкм. Температура также может быть увеличена источником тепла, выбранным из группы, состоящей из электролюминесцентного устройства, лазерного диода, лазера, излучающего с поверхности вертикальной полости, светоизлучающего диода и резистивной лампы накаливания. Ингибитор адаптивного температурного шокового ответа может быть аминоакридином, таким как акрихин, или 9-аминоакридин, или карбазол.
[0007] Клетка может быть раковой клеткой, а рак может быть из группы, состоящей из: метастатического рака молочной железы, рака мочевого пузыря, рака легкого, рака желудка, базально-клеточной карциномы, злокачественной меланомы, глазной опухоли, опухоли головы и шеи. Совместно с индуцированном температурного шокового ответа в клетке может быть использована вторая терапия. Вторая терапия может включать противоопухолевый агент.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0008] Фигура 1 показывает, что акрихин (QC) и 9АА предотвращает индукцию белка HSP70 в клетках, обработанных ингибиторами протеасом.
[0009] Фигура 2 показывает, что QC и 9АА ингибируют транскрипцию гена HSP70 в ответ на ингибиторы протеасом.
[0010] Фигура 3 показывает, что DMAG 17 - индуцированный синтез HSP70 чувствителен к QC и 9АА.
[0011] Фигура 4 показывает, что QC и 9АА подавляют транскрипцию HSP70A1/B' гена, индуцированную DMAG 17 и MG132.
[0012] Фигура 5 показывает токсический эффект DMAG 17, объединенного с QC, в HeLa клетках.
[0013] Фигура 6 показывает токсический эффект температурной шоковой терапии (43°С, 30 минут), объединенной с QC.
[0014] Фигура 7 показывает, что температурная чувствительность опухолевых, но не нормальных клеток, увеличивается после терапии с использованием QC и CZ (соединение CBL0137).
[0015] Фигура 8 показывает, что siPHK-опосредованный нокаут компонента FACT ядерного комплекса, SSPT1 и FACT киназы CKII, увеличивает чувствительность клетки к тепловому шоку.
[0016] Фигура 9 показывает, что акрихин и 9АА предотвращают hsp70 синтез в клетках, обработанных ингибиторами протеасом. Фиг.9А показывает результаты иммуноблоттинга с использованием анти-hsp70 антитела белковых экстрактов из HeLa клеток, обработанных в течение 5 часов ингибитором протеасом MG 132 (MG) (5 мкМ) в комбинации с противомалярийными препаратами эмитином (ЕМ) (1 мкМ), хлорохином (CQ) (20 мкМ), хинином (Q) (20 µМ) или акрихином (QC) (20 µМ). Линия 1 содержит экстракт из необработанных HeLa клеток. Выраженность пирина исследована как контроль на белковую нагрузку (Lx). Фиг.9 В показывает белковые экстракты из HeLa клеток, которые обработаны в течение 5 часов MG132 (5 µМ) одним или в комбинации с 20 µМ QC или 9АА как исследовано иммуноблоттингом с использованием антитела, специфичного для hsp70. Отрицательные контроли включали необработанные HeLa клетки (линия 1) и клетки, обработанные с использованием QC или 9АА в отсутствие MG132 (линии 6 и 7). Пирин исследован как контроль на белковую нагрузку (Lx). Фиг.9С показывает, что эметин, но не QC или 9АА, ингибирует общий синтез белка. 835-маркированные белки из HeLa клеток, оставленные необработанными (линия 1) или обработанные в течение 4 часов QC (20 µМ), 9АА (20 µМ), или эметином (ЕМ) (1 µМ) анализировали с использованием электрофореза и авторадиографии. Фиг.9D показывает, что аминоакридины не оказывают влияния на ингибирование протеасом MG132, как показано результатами in vitro пробы на активность протеасом, использующей экстракты HeLa клеток, обработанных в течение 4 часов указанными комбинациями MG132 (5 µМ), QC (20 µМ) и 9АА (20 µМ). Активность протеасом показана по отношению к активности необработанных клеток (установлена при 100%). Фиг.9Е показывает, что QC ингибирует активацию hsp70A1 транскрипции ингибиторами протеасом в HeLa клетках. 10 µг общего количества РНК из необработанных HeLa клеток (линия 1) или обработанных в течение 5 часов 0,1 µM Бортезомида (BZ) или 5 µМ MG132 (MG) одним или в комбинации с 20 µМ QC анализированы Северным блоттингом с hsp70A1 (верхняя панель) и GAPDH (нижняя панель) пробами. GAPDH использовался для контроля специфичности QC ингибирующей активности и на РНК нагрузку. Фиг.9F показывает, что аминоакридины не предотвращают индукцию экспрессии гена металлотионеина с использованием ZnCl2. HeLa клетки оставлены необработанными (линия 1) или обработаны в течение 5 часов 200 µМ ZnCl2(Zn) одним или в комбинации с 20 µМ QC или 9АА. 10 µг общего количества РНК анализировали Северным блоттингом пробами металлотионеина МТ1 (МТ), hsp70A1 и GAPDH.
[0017] Фигура 10 показывает, что HSR индукция MG132, 17-DMAG или температурным шоком, чувствительна к аминоакридинам. Фиг.10А показывает результаты иммуноблоттинга с анти-hsp70 антителом белковых экстрактов (10 µг) от HeLa клеток, обработанных в течение 5 часов 5 µМ MG132 (MG) или 1 µМ 17-DMAG(GM) только одним или в комбинации с 20 µМ QC или 9АА. Линия 1 содержит экстракт из необработанных HeLa клеток. K18 экспрессия оценена как контроль на белковую нагрузку (L.c). Фиг.10В показывает, что QC и 9АА подавляют транскрипцию hsp70Al гена, вызванную 17-DMAG или MG132. Северная гибридизация РНК из необработанных HeLa клеток (линия 1), обработанных в течение 5 часов 1 µМ 17-DMAG (GM) или 5 µМ MG132 (MG) одним и в комбинации с 20 µМ QC или 9АА. GAPDH и РНК анализировалась для контроля на специфичность ингибитора и РНК нагрузку. Фиг.10С показывает, что QC и 9АА не изменяют и РНК накопление генов, которое не индуцируется 17-DMAG, как показано Северной гибридизацией РНК из HeLa клеток, которые обработаны в течение 5 часов 1 µМ 17-DMAG(GM) одним или в комбинации с 20 µМ QC или 9АА. GAPDH, p65Re1A и GRP94 являются генами, экспрессия которых не вызывается 17-DMAG. Hsp70A1 был включен как позитивный контроль для 17-DMAG индуцибельного гена. Фиг.10D показывает, что QC подавляет HSF1-зависимую экспрессию EGFP репортерного гена, вызванную протеотоксическим стрессом. HeLa клетки, несущие HSF1-EGFP репортерную конструкцию, оставили необработанными, или обработали 0,1 µМ Бортезомида (BZ), 1 µМ 17-DMAG (GM) или 43°С в течение 1 часа температурного шока (HS) одного или в комбинации с 20 µМ QC. EGFP экспрессия оценена через 8 часов флуоресцентной микроскопией.
[0018] Фигура 11 показывает, что аминоакридины действуют на снижение HSF1 активации и транслокации к ядрам. Фиг.11А показывает, что обработка HeLa клеток MG132, 17-MAG или температурным шоком вызывает ДНК HSF1 связывающую активность. Электрофоретический анализ изменения подвижности (EMSA) выполнен с цитоплазматическими экстрактами из HeLa клеток, оставленных необработанными, обработанными 5 µМ MG132 (MG) или 1 µМ 17-DMAG (GM) в течение 4 часов, или подвергнутыми воздействию температурного шока (43°С) в течение 1 часа. Образование комплекса между HSF1 и 32 P-меченной олигонуклеотидной пробой, содержащей HSF1 связывающий сайт, ингибировано 50-кратным превышением того же самого немаркированного олигонуклеотида (линия 3), но не подобным избытком немаркированного олигонуклеотида, содержащего NFkB связывающий сайт (линия 4). Специфичность детектированного комплекса далее подтверждена его суперсдвигом в присутствии анти-HSF1 антитела (линия 7). Фиг.11В показывает, что QC не оказывает влияние на связывающую активность ядер ДНК HSF1, вызванную протеотоксическим стрессом. EMSA выполнен как в разделе А меченной HSF1-специфической олигонуклеотидной пробой, и ядерные экстракты из HeLa клеток оставили необработанным (линия 1), или обработали в течение 4 часов 5 µМ MG132 (MG) или 1 µМ 17-DMAG(GM) одного или в комбинации с 20 µ QC. Фиг.11С показывает, что бафиломицин увеличивает ядерную концентрацию QC. HeLa клетки обработаны 5 µМ QC одного или в комбинации с 0,5 µМ бафиломицина в течение 1 часа. Внутриклеточная локализация QC анализировалась УФ микроскопией с синим светофильтром. Фиг.11D показывает, что бафиломицин увеличивает HSR ингибирующую активность QC. HeLa клетки оставили необработанными (линия 1) или обработали в течение 5 часов указанными комбинациями 5 µМ MG132 (MG), 0,5 µМ бафиломицина (Baf) и переменным количеством QC. Полученные экстракты клеточного белка анализировались Вестерн-блоттингом с анти-hsp70 антителом. Пирин исследован как контроль на белковую нагрузку (L.c).
[0019] Фигура 12 показывает, что QC увеличивает цитотоксичность индукторов протеотоксического стресса. Фиг.12А показывает токсичность комбинаций лекарств, как оценено с использованием анализа на жизнеспособность клеток. HeLa клетки обработаны в течение 4 часов указанными комбинациями 17-DMAG (1 µМ) и QC (10 или 20 µМ). Жизнеспособность клеток оценена через 72 часа окрашиванием метиленовым синим. Показанные данные являются средним числом трех экспериментов. Фиг.12В показывает токсичность бортезомид/QC обработки, как оценено с использованием пробы на жизнеспособность клеток, как на фиг.12А. HeLa клетки обработаны в течение 4 часов 0,1 µM бортезомида (BZ) одним или в комбинации с 10 µМ. QC. Показанные данные являются средним числом 2 экспериментов. Фиг.12С показывает иммуноблоттинг-анализ апоптоза в HeLa клетках, обработанных комбинациями бортезомида (BZ) (0,1 µМ), 17-DMAG (GM) (1 µМ) и QC (10 µM). Показаны PARP и K1 8 белки во всю длину - так же, как апоптоз-специфичные протеолитические фрагменты (PARP/apopt и K18/apopt). Фиг.12D показывает, что siPHK-опосредованный нокаут Hsp70 делает чувствительными клетки к бортезомиду и 17-DMAG, как показано иммуноблоттингом белков из hsp70 siPHK (siPHK) - выраженных HeLa клеток, обработанных указанными концентрациями 0,1 µМ бортезомида (BZ), 20 µМ QC и 1 µМ 17-DMAG (GM). Белковые экстракты получены из клеток, на которые переносилась hsp70 siPHK в течение 24 часов, и обработаны бортезомидом и DMAG накануне вечером. Экспрессия hsp70 и апоптоз-специфичный распад K18 оценены соответствующими антителами. HeLa клетки контроля были необработанными лекарственными препаратами (линия 1), или обработаны накануне вечером количеством препаратов, указанных выше (линии 5-9). Фиг.12Е показывает, что ингибитор ZVAD-FMK каспаз защищает клетки от апоптоза, вызванного комбинациями протеотоксического стресса и аминоакридинов, как показано иммуноблотинг-анализом уровней hsp70 белка и апоптоз-специфичным распадом K18 в HeLa клетках, обработанных накануне вечером указанными комбинациями 1 µM 17-DMAG (GM), 0,1 µМ бортезомида (BZ), 20 µМ QC и 20 µМ ZVAD-FMK (ZVAD). Обработка клеток анти-Fas антителом (Fas, линия 9) и комбинацией анти-Fas антитела и ZVAD-FMK (линия 10) обеспечила положительные контроли для индукции апоптоза и защитного эффекта ZVAD-FMK, соответственно.
[0020] Фигура 13 показывает эффект 17-DMAG и акрихина на рост клеток опухоли in vitro и in vivo. Фиг.13А показывает, что QC подавляет hsp70 синтез в ответ на протеотоксический стресс в МСА205 и В-16клетках. РНК от клеток контроля и клеток, обработанных в течение 5 часов 1 µМ 17-DMAG (GM) в присутствии или отсутствии 20 µМ QC, анализирована Северной гибридизацией с GAPDH и hsp70A1 пробами. Фиг.13В показывает результаты проб на жизнеспособность клеток МСА205 и В-16клеток, которые обработаны в течение 4 часов 1 µМ 17-DMAG (GM) в комбинации с 20 µM QC. Клетки собраны, разбавлены 1:50 и анализированы на жизнеспособность клеток окрашиванием метиленовым синим через 72 часа. Показанные данные являются средними из двух экспериментов. Фиг.13С показывает, что внутриопухолевая инъекция QC блокирует 17-DMAG-индуцированную hsp70 экспрессию. C57BL/6 мышам, несущим МСА205опухоли, сделали единственную внутриопухолевую инъекцию PBS (контроль), 25 µг, 17-DMAG (GM) или 1,25 мг QC+25 µг 17-DMAG. Пять часов спустя мыши забиты. РНК, полученная из опухолей, анализировалась Северной гибридизацией с hsp70A1 специфичной пробой. Гибридизация с GAPDH-пробой использовалась в качестве контроля на РНК нагрузку (L.c). Показанные данные представляют собой данные от единственной опухоли для каждой обработки. Это представительные данные двух экспериментов. Фиг.13D и Е показывают результаты инъекции C57BL/6 мышей МСА205 (D) или В-16 (Е) клетками. Показан средний объем опухоли в пределах каждой группы.
[0021] Фигура 14 показывает антиопухолевые эффекты в модели мыши комбинированных неэффективных доз акрихина и местной гипертермии.
[0022] Фигура 15 показывает эффекты CRBZ на экспрессию hsp70 гена в ответ на PS, как показано Северной гибридизацией РНК из контрольных HeLa клеток, клеток, обработанных в течении 5 часов MG132 и комбинациями MG132 с 10 µМ 9АА или 1 µМ CRBZ (Crbz) 159, 188, и 198 с пробой на hsp70A1/B гены. GAPDH - контроль на нагрузку.
[0023] Фигура 16 показывает, что CRBZ 198 влияет на HSF1-специфичную экспрессию GFP репортера. HeLa клетки, инфицированные лентивирусом, выражающим репортерный ген, обработаны 0,1 µМ Бортезомида (Brtz) одним и в комбинации с 1 µМ CRBZ 188 (неактивный), или CRBZ 198 (активный). Экспрессия GFP анализирована микроскопически через 10 часов после обработки.
[0024] Фигура 17 показывает эффекты температурного шока (HS) и AA/CRBZ на HSF1-специфичную GFP экспрессию. HeLa клетки, инфицированные лентивирусом, выражающим HSF1 специфичные GFP, обработаны HS при 43°С в течение 30 минут, или HS в комбинации с 20 µМ АА, или 1 µМ CRBZ 198 или CRBZ 159. u/t - необработанные HeLa клетки. GFP экспрессия показана на 12 час при восстановлении при 37°С.
ПОДРОБНОЕ ОПИСАНИЕ
[0025] Изобретатели сделали удивительное открытие, состоящее в том, что индуцирование температурного шокового ответа в комбинации с ингибированием адаптивного шокового температурного ответа может вызвать гибель клеток. Вне связи с теорией, ингибиторы адаптивного шокового температурного ответа могут предотвращать способность клеток переносить индукцию шокового температурного ответа за счет подавления HSF-I, главного медиатора индуцибельной вызванной температурным шоком транскрипции. Температурные шоковые белки являются белками шаперонами, которые предотвращают фатальные в других обстоятельствах последствия разрушительных стимулов за счет разъединения, повторного свертывания и ренатурирования неправильно упакованных белков. Защитный эффект температурных шоковых белков может также состоять в их способности подавлять некоторые формы гибели клеток, включая апоптоз. В отсутствие температурных шоковых белков, клетки менее способны отвечать на химические, экологические и физиологические стрессы. В частности опухолевые клетки могут быть более чувствительными к ингибированию температурного шокового ответа, так как они обычно выражают более высокие уровни температурных шоковых белков и могут зависеть от этих повышенных уровней как механизма подавления эффектов накопленных мутаций, которые в других обстоятельствах закончились бы экспрессией вредных белков. Соответственно, комбинация ингибирования адаптивного температурного шокового ответа и индуцирования температурного шокового ответа обеспечивает простой и гибкий подход к стимулированию гибели клеток.
1. Определения.
[0026] Терминология, используемая здесь, - это терминология, которая единственно имеет целью описание частных воплощений и не является ограничивающей. Как используются в описании и приложенных пунктах формулы, формы единственного числа "a", «an» и «the» включают множественные ссылки, если контекст ясно не диктует иначе.
[0027] При перечислении числовых диапазонов, каждое число в интервале между рассматривается с той же степенью точности. Например, для диапазона 6-9, 7 и 8 рассматриваются в дополнение к 6 и 9, а для диапазона 6,0-7,0, числа 6,0, 6,1, 6,2, 6,3, 6,4, 6,5, 6,6, 6,7, 6,8, 6,9 и 7,0 явно рассматриваются.
a. акрил
[0028] Термин "акрил", как здесь используется, один или в комбинации может относиться к группе, представленной СН2=С (Q) С (О) О-, где Q - алифатическая или ароматическая группа.
b. ацил
[0029] Термин "ациламино" может означать R(=O)N-, где R является алкилом или арилом.
c. давать, назначать, вводить
[0030] Как здесь используются, термины "давать, назначать, вводить", когда применяются для описания дозировки состава, могут означать единственную дозу или множественные дозы соединения.
d. алифатический
[0031] Термин "алифатический", как здесь используется, может относиться к неразветвленной, разветвленной или циклической углеводородной группе, которая может быть замещенной или незамещенной, и которая может быть насыщенной или ненасыщенной, но которая не является ароматической. Термин алифатический может далее включать алифатические группы, которые включают кислород, азот, серу или атомы фосфора, заменяющие один или более углеродов остова углеводородной молекулы.
e. алкокси
[0032] Термин "алкокси", как здесь используется один или в комбинации, может относиться к алкил, алкенил или алкинилгруппе, связанной посредством единственной предельной эфирной связи. Примеры алкоксигрупп могут включать метокси, этокси, n-пропокси, изо-пропокси, n-бутокси, 2-бутокси, терт-бутокси, n-пентокси, 2-пентокси, 3-пентокси, изопентокси, неопентокси, n-гексокси, 2-гексокси, 3-гексокси, 3-метилпентокси, флюорометокси, дифлюорометокси, трифлюорометокси, хлорометокси, дихлорометокси и трихлорометокси. Алкокси может также означать - OR, где R - алкил.
f. алкоксиалкил
[0033] Термин "алкоксиалкил" означает алкилгруппу, в которой водород замещен алкокси группой.
g. алкенил
[0034] Термин "алкенил", как здесь используется один или в комбинации, может относиться к разветвленной или неразветвленной алифатической группе, содержащей по крайней мере одну углерод-углерод двойную связь, которая может встречаться в любой устойчивой точке вдоль цепи. Представительные примеры алкенилгрупп могут включать этенил, Е и Z пентенил, деценил и т.п.
h. алкил
[0035] Термин "алкил", как «здесь используется один или в комбинации, может относиться к цепочечным или разветвленным углеводородным группам, содержащим указанное число углеродных атомов, как правило, метил, этил и прямую цепь, и разветвленные группы пропила и бутила. Термин "циклоалкил" определяется как циклическая углеводородная группа, содержащая указанное число атомов углерода, например, циклопропил, циклобутил, циклогексил и циклопентил.
i. алкилтио
[0036] Термин "алкилтио" может означать - SR, где R является алкилом.
j. алкинил
[0037] Термин "алкинил", как здесь используется один или в комбинации, может относиться к разветвленной или неразветвленной алифатической группе, содержащей по крайней мере одну углерод-углерод тройную связь, которая может встречаться в любой устойчивой точке вдоль цепи. Представительные примеры алкинилгрупп могут включать этинил, пропинил, пропаргил, бутинил, гексинил, децинил и т.п.
k. амино
[0038] Термин "амино", как здесь используется один или в комбинации, может относиться к группе, содержащей атом азота остова молекулы. Представительные примеры аминогрупп включают, но не ограничены, алкиламино, диалкиламино, ариламино, диариламино, алкилариламино, алкилкарбониламино, арилкарбониламино, карбамоил, уреидо и т.п. Амино может также означать -NH2, а термин "алкиламино" может означать-NR2, где по крайней мере один R является алкилом, а второй R - алкилом или водородом.
1. ароматический
[0039] Термин "ароматический", как здесь используется, может относиться к ненасыщенной циклической углеводородной группе, имеющей 4n+2 нелокализованные p (pi) электроны, которая может быть замещенной или незамещенной. Термин ароматический может далее включать ароматические группы, которые включают атом азота, заменяющий один или более углеродов углеводородного остова молекулы. Примеры ароматических групп могут включать фенил, нафтил, тиэнил, фуранил, пиридинил, (из)оксазоил и т.п.
м. алкилсульфинил
[0040] Термин "алкилсульфинил" означает R-SO2-, где R - алкил.
n. алкилсульфонил
[0041] Термин "алкилсульфонил" означает R-SO2-, где R - алкил.
o. морфолино компонент
[0042] Термин "морфолино компонент" означает 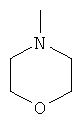
p. тетрагидрофурил компонент
[0043] Термин "тетрагидрофурил компонент» означает 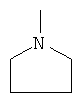
q. пиперидинил компонент
[0044] Термин "пиперидинил компонент" означает 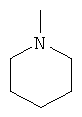 , произвольно замещенный -ОН или -СН2ОН группой.
, произвольно замещенный -ОН или -СН2ОН группой.
r. арил
[0045] Термин "арил", как здесь используется один или в комбинации, может относиться к замещенной или незамещенной ароматической группе, которая может быть необязательно сплавлена с другими ароматическими или неароматическими циклическими группами. Представительные примеры арилзамещенных групп могут включать фенил, бензил, нафтил, бензилидин, ксилил, стирол, стирил, фенетил, фенилен, бензенетриил и т.п.
s. арилокси
[0046] Термин "арилокси", как здесь используется один или в комбинации, может относиться к арилгруппе, связанной посредством единственной предельной эфирной связи.
t. разветвленный
[0047] Термин "разветвленный", как здесь используется, может относиться к группе, содержащей от 1 до 24 атомов остова, где цепь остова группы содержит одно или более зависимых ответвлений от главной цепи. Разветвленная группа может содержать от 1 до 12 атомов остова. Примеры разветвленных групп могут включать изобутил, t-бутил, изопропил, СН2СН2СН(СН3)СН2СН3, СН2СН(СН2СН3)СН2СН3, СН2СН2С(СН3)2СН3, СН2СН2С(СН3)3 и т.п.
u. рак
[0048] Как используется здесь, термин "рак" может означать любое состояние, характеризующееся резистентностью к апоптотическим стимулам.
v. терапия рака
[0049] Как используется здесь, термин "лечение рака" может означать любую терапию рака, известную в уровне техники, включая химиотерапию и радиационную терапию.
w. карбонил
[0050] Термин "карбонил" или "карбокси", как здесь используется один или в комбинации, может относиться к группе, которая содержит углерод-кислород двойную связь. Представительные примеры групп, которые содержат карбонил, включают, но не ограничены этим, альдегиды (то есть формилы), кетоны (то есть ацилы), карбоксиловые кислоты (то есть карбоксилы), амиды (то есть амидо), имиды (то есть имидо), сложные эфиры, ангидриды и т.п.
x. комбинация
[0051] Как используется здесь, термин "комбинация с" или "совместно назначенный", когда используется для описания назначения аминоакридина и дополнительной терапии, может означать, что аминоакридин может быть применен до, вместе с, или после дополнительной терапии или их комбинации.
y. циано
Термин "циано", "цианат" или "цианид", как здесь используется один или в комбинации, может относиться к углерод-азот двойной связи. Представительные примеры цианогрупп включают, но не ограничены этим, изоцианат, изотиоцианат и т.п. Термин "циано" означает-CN.
Z. цикличный
[0052] Термин "цикличный" или "цикло", как здесь используется один или в комбинации, может относиться к группе, имеющей одно или более закрытые кольца, ненасыщенные или насыщенные, обладающие кольцами от 3 до 12 атомов остова, или от 3 до 7 атомов остова.
aa. эффективное количество
[0053] Термин "эффективное количество," когда используется в отношении соединения, продукта или композиции, как здесь предусмотрено, может означать достаточное количество соединения, продукта или композиции для обеспечения желаемого результата. Точное требуемое количество может изменяться в зависимости от конкретного соединения, продукта или используемой композиции, способа его введения и т.п. Таким образом, не всегда возможно определить точное "эффективное количество." Однако адекватное эффективное количество может быть определено специалистом области, информированным настоящим описанием, использующим только обычное экспериментирование.
bb. галоалкил
[0054] Термин "галоалкил" означает алкил группу, замещенную одним или более, например, 1-3 галозаместителями, а также фторо, хлоро, бромо, иодо или их комбинацией. Точно так же "галоциклоалкил" определяется как циклоалкил группа, имеющая один или более гало заместителей.
[0055] Термин "арил", один или в комбинации, означает моноциклическую или полициклическую ароматическую группу, предпочтительно моноциклическую или бициклическую ароматическую группу, например, фенил или нафтил. Если иначе не указано, "арил" группа может быть незамещенной или замещенной, например, одим или более, и в частности от одного до трех, гало, алкил, гидроксиалкил, алкокси, алкоксиалкил, галоалкил, нитро, амино, алкиламино, ациламино, алкилтио, алкилсульфинил и алкилсульфонилом. Типичные арилгруппы включают фенил, нафтил, тетрагидронафтил, 2 хлорофенил, 3-хлорофенил, 4-хлорофенил, 2-метилфенил, 4-метоксифенил, 3 трифлюорометилфенил, 4-нитрофенил и т.п.
ee. галоген
[0056] Термин "галоген", "галид" или "гало", как здесь используется один или в комбинации, может относиться к фтору "F", хлору "Cl", брому "Br", йоду "I" и астату "At". Представительные примеры гало групп могут включать хлорацетамидо, бромацетамидо, идоацетамидо и т.п.
dd. гетеро
[0057] Термин "гетеро", как здесь используется в комбинации, может относиться к группе, которая включает один или более атомов любого элемента, кроме углерода или водорода. Представительные примеры гетеро групп могут включать те группы, которые содержат гетероатомы, включая азот, кислород, серу и фосфор.
ee. гетероарил
[0058] Термин "гетероарил" означает моноциклическую или бициклическую кольцевую систему, содержащую одно или два ароматических кольца и содержащую по крайней мере один атом азота, кислорода или серы в ароматическом кольце, и которая может быть незамещенной или замещенной, например, одним или более, и в частности одним - тремя заместителями такими, как гало, алкил, гидрокси, гидроксиалкил, алкокси, алкоксиалкил, галоалкил, нитро, амино, алкиламино, ациламино, алкилтио, алкилсульфинил и алкилсульфонил. Примеры гетероарил групп включают, но не ограничены этим, тиэнил, фурил, пиридил, оксазолил, хинолил, изохинолил, индолил, триазолил, изотиазолил, изоксазолил, имидизолил, бензотиазолил, пиразинил, пиримдинил, тиазонил и тиадиазолил.
[0059] Термин "алкилен" означает алкил группу, имеющую заместитель. Например, термин "С1-3 алкиленарил" относится к алкил группе, содержащей один - три атома углерода и замещенной арил группой.
ff. гетероцикл
[0060] Термин "гетероцикл", как здесь используется, может относиться к циклической группе, содержащей гетероатом. Представительные примеры гетероциклов включают, но не ограничены этим, пиридин, пиперадин, пиримидин, пиридазин, пирразин, пиррол, пирролидинон, пирролидин, морфолин, тиоморфолин, индол, изоиндол, имидазол, триазол, тетразол, фуран, бензофуран, дибензофуран, тиофен, тиазол, бензотиазол, бензоксазол, бензотиофен, хинолин, изохинолин, азопин, нафтопиран, фуранобензопиранон и т.п.
gg. гетероциклоалкил
[0061] Термин "гетероциклоалкил" означает моноциклические, бициклические и трициклические циклоалкил группы, содержащие один или более гетероатомов, выбранных из группы, состоящей из кислорода, азота и серы в кольцевой структуре. "Гетероциклоалкил" группа также может содержать оксо группу (=0), присоединенную к кольцу. Неограничивающие примеры гетероциклоалкил групп включают, но не ограничены этим, 1,3-диоксолан, 2-пиразолин, пиразолидин, пирролидин, пирразин, пирролин, 2Н-пиран, 4Н-пиран, морфолин, тиофолин, пиперидин, 1,4-дитиан и 1,4-диоксан.
hh. гидрокси
[0062] Термин "гидрокси" означает - ОН.
ii. гидроксиалкил
[0063] Термин "гидроксиалкил" означает алкил группу, в которой водород замещен гидрокси группой.
jj. низший
[0064] Термин "низший", как здесь используется, может относиться к группе с 1-6 атомами остова.
kk. нитро
[0065] Термин "нитро" означает -NO2.
ll. необязательный
[0066] Термин "необязательный" или "необязательно", как здесь используется, может означать, что впоследствии описанный случай или обстоятельство могут или, возможно, не встречаются, и что описание включает случаи, где упомянутый случай или обстоятельство встречаются, и случаи, где они не встречается. Например, фраза "необязательно замещенный алкил", может означать, что алкилгруппа может или не может быть замещена и что описание включает как незамещенный алкил, так и алкил, где имеет место замена.
мм. пептид
[0067] "Пептид" или "полипептид" - это связанная последовательность аминокислот, которые могут быть натуральными, синтетическими, или модификациями, или комбинациями натуральных и синтетических.
nn. фосфатсодержащая группа
[0068] Термин " фосфатсодержащая группа", как здесь используется, может относиться к группе, содержащей по крайней мере один фосфорный атом в оксидированном состоянии. Представительные примеры включают, но не ограничены этим, фосфоник кислоты, фосфиник кислоты, фосфат сложные эфиры, фосфинидены, фосфино, фосфинилы, фосфинилидены, фосфо, фосфоно, фосфоранилы, фосфоранилидены, фосфоросо и т.п.
oo. насыщенный
[0069] Термин "насыщенный", как здесь используется, может относиться к группе, где все доступные валентные связи атомов остова присоединены к другим атомам. Представительные примеры насыщенных групп могут включать бутил, циклогексил, пиперидин и подобные.
pp. замещенный
[0070] Термин "замещенный", как здесь используется, может относиться к группе, имеющей один или более водородов или других атомов, перемещенных из углерода или подходящего гетероатома и замещенных другой группой. Замещенные группы можно заменить одним - пятью, или одним - тремя заместителями. Атом с двумя заместителями обозначается "ди", тогда как атом с более чем двумя заместителями обозначается "поли-". Представительные примеры таких заместителей могут включать алифатические группы, ароматические группы, алкил, алкенил, алкинил, арил, алкокси, гало, арилокси, карбонил, акрил, циано, амино, нитро, фосфатсодержащие группы, содержащие серу группы, гидроксил, алкилкарбонилокси, арилкарбонилокси, алкоксикарбонилокси, арилоксикарбонилокси, алкилкарбонил, арилкарбонил, алкоксикарбонил, аминокарбонил, алкиламинокарбонил, диалкиламинокарбонил, алкилтиокарбонил, ациламино, амидино, имино, алкилтио, арилтио, тиокарбоксилат, алкилсульфинил, трифлюорометил, азидо, гетероциклил, алкиларил, гетероарил, семикарбазидо, тиосемикарбазидо, малимидо, оксимино, имидат, циклоалкил, циклоалкилкарбонил, диалкиламино, арилциклоалкил, арилкарбонил, арилалкилкарбонил, арилциклоалкилкарбонил, арилфосфинил, арилалкилфосфинил, арилциклоалкилфосфинил, арилфосфонил, арилалкилфосфонил, арилциклоалкилфосфонил, арилсульфонил, арилалкилсульфонил, арилциклоалкилсульфонил, их комбинации, и заместители.
qq. содержащая серу группа
[0071] Термин "содержащая серу группа", как здесь используется, может относиться к группе, содержащей атом серы. Представительные примеры включают, но не ограничены этим, сульфидрилы, сульфоны, сульфины, сульфинилы, сульфо, сульфонилы, тио, тиоксо и подобное.
rr. лечить
[0072] Как здесь используется, термин "лечить" или "лечение", когда относится к защите млекопитающего от состояния, может означать предотвращать, подавлять, сдерживать или устранять состояние. Предотвращение состояния включает лечение млекопитающего до начала состояния. Подавление состояния включает лечение млекопитающего после возбуждения состояния, но перед его клиническим появлением. Сдерживание состояния включает лечение млекопитающего после клинического появления состояния, таким образом, что состояние уменьшается или поддерживается. Устранение состояние включает лечение млекопитающего после клинического появления состояния, таким образом, что млекопитающее больше не страдает от состояния.
ss. трифлюорометокси
[0073] термин "трифлюорометокси" означает-OCF3.
tt. трифлюорометил
[0074] термин "трифлюорометил" означает- CF3.
uu. опухолевая клетка
[0075] Как здесь используется, термин "опухолевая клетка" может означать любую клетку, характеризующуюся устойчивостью к апоптотическим стимулам.
vv. неразветвленный
[0076] Термин "неразветвленный", как здесь используется, может относиться к группе, содержащей от 1 до 24 атомов остова, где цепь остова группы простирается по прямой линии. Неразветвленная группа может содержать от 1 до 12 атомов остова.
ww. ненасыщенный
[0077] Термин "ненасыщенный", как здесь используется, может относиться к группе, где по крайней мере одна доступная валентная связь двух смежных атомов остова не присоединена к другим атомам. Представительные примеры ненасыщенных групп могут включать-СН2СН2СН=СН2, фенил, пиррол и т.п.
xx. незамещенный
[0078] Термин "незамещенный", как здесь используется, может относиться к группе, у которой нет других групп, присоединенных к ней или замещающих ее.
2. Способ индуцирования гибели клеток
[0079] Здесь представлен способ индуцирования гибели клеток. Гибель клеток может быть вызвана ингибированием адаптивного шокового температурного ответа в комбинации со стимулированием температурного шокового ответа в клетке. Температурный шоковый ответ может быть вызван введением агента индуцирования температурного шокового ответа в клетку, или увеличением внутренней температуры клетки нагревающим средством.
a. Ингибирование адаптивного температурного шокового ответа
[0080] Ингибитор адаптивного температурного шокового ответа может быть агентом, способным к действию как ДНК-интеркалирующий, негенотоксический агент, который может подавлять HSF-I - опосредованную транскрипцию. Ингибитором адаптивного температурного шокового ответа может быть аминоакридин, карбазол или их производные.
(1) Аминоакридин
[0081] Аминоакридин может иметь следующую формулу:
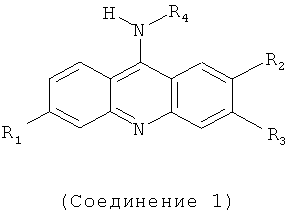 ,
,
где
R1 - это Н или галоген;
R2 - это Н или необязательно замещенный алкокси;
R3 - это Н или необязательно замещенный алкокси; и
R4 - это Н или необязательно замещенный алифатический, арил или гетероцикл.
[0082] Аминоакридином может быть 9-аминоакридин или Мепакрин, который иначе известен как Акрихин. Аминоакридином может также быть, как описано в международной патентной публикации № WO/06/12419, содержание которой включается здесь ссылкой.
(2) Производная карбазола
[0083] Ингибитором адаптивного температурного шокового ответа может быть карбазол или его производная. Ингибитором адаптивного температурного шокового ответа может быть карбазол или его производная. Карбазолом или его производной могут быть, как описано в американской предварительной заявке №61/102,913, поданной 6 октября 2008, содержание которой включено здесь ссылкой.
[0084] Карбазол или его производная могут иметь формулу (I):
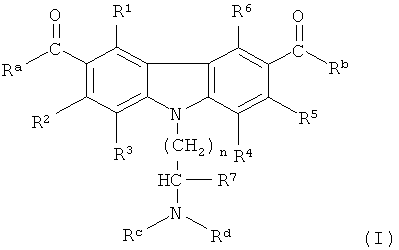
где Ra выбирается из группы, содержащей водород, C1-6-алкил, C1-6галоалкил, циклоалкил, гетероциклоалкил, арил, гетероарил, ORe, N(Re)2, и SRe, или Ra и R1 или NRe и R1 вместе с атомами углерода, к которым они присоединяются, формирующие пяти- или шестичленное алифатическое карбоциклическое или гетероциклическое кольцо;
Rb выбирается из группы, содержащей водород, C1-6-алкил, C1-6галоалкил, циклоалкил, гетероциклоалкил, арил, гетероарил, OR, N(Re)2 и SRe, или Rb и R6 или NRe и R6 вместе с атомами углерода, к которым они присоединены, формирующие пяти- или шестичленное алифатическое карбоциклическое кольцо или пяти- или шестичленное алифатическое карбоциклическое или гетероциклическое кольцо;
Rc выбирается из группы, состоящей из водорода, C1-6-алкил, C1-6гидроксиалкил, циклоалкил, гетероциклоалкил, арил, гетероарил, и С(=O)Re, или Rc и Rd, взятых вместе, чтобы сформировать пяти-, шести- или семичленное алифатическое кольцо, необязательно содержащее атом кислорода;
Rd выбирается из группы, содержащей водород, C1-6-алкил, циклоалкил, гетероциклоалкил, арил, гетероарил и С(=O)Re, или Rd и R7 вместе с атомами, к которым они присоединяются, формирующие пяти- или шестичленное алифатическое кольцо;
Re независимо, выбирается из группы, содержащей водород, C1-6алкил, циклоалкил, гетероциклоалкил, арил и гетероарил, или две Re группы, взятые вместе с азотом, к которому они присоединены для формирования пяти- или шестичленного алифатического кольца;
R1, R2, R3, R4, R5 и R6, независимо, выбираются из группы, содержащей водород, C1-6алкил, циклоалкил, гетероциклоалкил, арил, гетероарил, гало, OR6, С(=O)Re, С(=O)OReORe, ОС(=O)Re, С(=O)N(Re)2, С(=O)NReSO2Re, N(Re)2, NReC(=O)Re, NReC(=O)N(Re)2, CN, NO2, CF3, OCF3, SRe, SORe, SO2R6, SO2N(Re)2 и OSO2CF3;
R7 выбирается из группы, содержащей водород, С1-6алкил, циклоалкил, гетероциклоалкил, арил и гетероарил; а
n - это 0, 1, 2, 3, 4 или 5, или фармацевтически приемлемая соль или ее гидрат.
[0085] Карбазол или его производная может иметь общую структурную формулу (Ia):
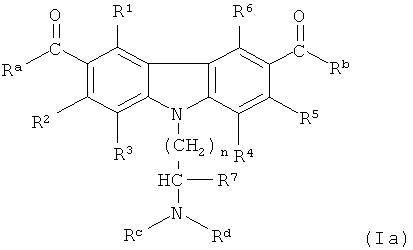
где Ra - это C1-3алкил, С1-4галоалкил, С3-5циклоалкил, N(Re)2 или OR6, или Ra и R1 вместе с атомами углерода, к которым они присоединяются, формирующие пяти- или шестичленное алифатическое карбоциклическое кольцо;
Rb - это C1-4алкил, C1-4галоалкил, С3-5циклоалкил, N(Re)2 или ORe, или Rb и R6 вместе с атомами углерода, к которым они присоединяются, формирующие пяти- или шестичленное алифатическое карбоциклическое кольцо или пяти- или шестичленное алифатическое кольцо, содержащее один атом азота;
Rc - это С1-6алкил, С3-5циклоалкил, или C1-3гидроксиалкил;
Rd - это водород, C1-4алкил или С3-5циклоалкил, или Rd и R7 вместе с атомами, к которым они присоединяются, формирущие пяти или шестичленное алифатическое кольцо, содержащее один атом азота или Rc и Rd взятые вместе для формирования шести- или семичленного алифатического кольца, необязательно содержащего атом кислорода;
Re, независимо, является водородом или С1-3алкилом;
R1 - это водород или С1-3алкил;
R2 - это водород, гидрокси или C1-3алкокси;
R3 и R4, независимо, являются водородом или C1-3алкилом;
R5 - это водород, гидрокси, C1-3алкокси или гало;
R6 - это водород, C1-3алкил, C1-3алкокси или гало;
R7 - это водород или C1-3алкил; и
n - 0, 1, 2, 3, 4, или 5,
или фармацевтически приемлемая соль или ее гидрат.
[0086] Карбазол или его производная может иметь общую структурную формулу (Ib):
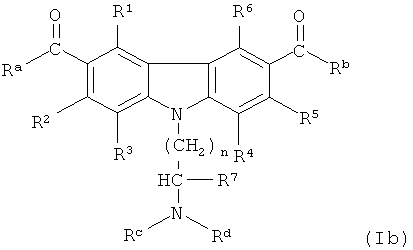
где Ra - метил, этил, n-пропил, циклопропил, NH(СН3), или ОСН3, или Ra и R1 вместе с атомами углерода, к которым они присоединяются, формирующие пятичленное алифатическое карбоциклическое кольцо;
Rb - это метил, этил, n-пропил, циклопропил, NH(СН3), или ОСН3, или Rb и R6 вместе с атомами углерода, к которым они присоединяются, формирующие пятичленное алифатическое карбоциклическое кольцо или пятичленное алифатическое кольцо, содержащее один атом азота;
Rc - это метил, этил, n-пропил, изопропил, циклобутил или 2-гидроксиэтил;
Rd - это водород, метил, этил или циклобутил, или Rd и R7 вместе с атомами, к которым они присоединяются, формирующие пятичленное алифатическое кольцо, содержащее один атом азота, или Rc и Rd, взятые вместе, для формирования морфолино компонента, тетрагидрофурил компонента, пиперидинил компонента, или 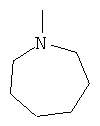 компонента,
компонента, 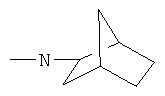 компонента;
компонента;
R1 - это водород;
R2 - это водород, гидрокси или метокси;
R3 и R4 являются водородом;
R5 - это водород, гидрокси, метокси или фтор;
R6 - это водород, метил, метокси или фтор;
R7 - это водород; а
n - 1 или 2,
или фармацевтически приемлемая соль или ее гидрат.
[0087] Карбазол или его производная может иметь структурную формулу (II):
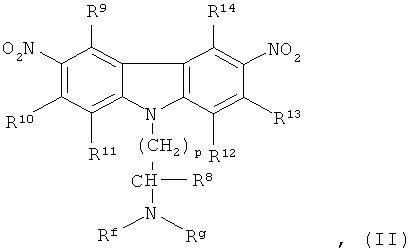
где Rf выбирается из группы, содержащей водород, C1-6алкил, циклоалкил, гетероциклоалкил, арил, гетероарил и С(=O)Rh, или Rf и Rg, взятые вместе, для формирования пяти, шести или семичленного алифатического кольца, необязательно содержащего атом кислорода;
Rg выбирается из группы, содержащей водород, C1-6алкил, циклоалкил, гетероциклоалкил, арил, гетероарил и С(=O)Rh, или Rg и Rh вместе с атомами, к которым они присоединяются, формирующие пяти-, шести- или семичленное алифатическое кольцо;
Rh независимо выбирается из группы, содержащей водород, С1-6алкил, циклоалкил, гетероциклоалкил, арил и гетероарил, или две Rh группы, взятые вместе с азотом, к которому они присоединены для формирования пяти- или шестичленного алифатического кольца;
R9, R10, R11, R12, R13 и R14 независимо выбираются из группы, содержащей водород, C1-6алкил, циклоалкил, гетероциклоалкил, арил, гетероарил, гало, ORh, С(=O)Rh, С(=O)ORh, ОС(=O)Rh, С(=O)N(Rh)2, С(=O)NRh SO2Rh, N(Rh)2, NRhC(=O)Rh, NRhC(=O)N(Rh)2, CN, NO2, CF3, OCF3, SRh, SORh, SO2Rh, SO2N(Rh)2 и OSO2CF3;
R8 выбирается из группы, содержащей водород, C1-6алкил, циклоалкил, гетероциклоалкил, арил и гетероарил; и
p - это 0, 1, 2, 3, 4 или 5,
при условии, что когда p - это 2, один из Rf и Rg отличается от этила, или фармацевтически приемлемой соли, или ее гидрата.
[0088] Карбазол или его производная может иметь общую структурную формулу (IIa):
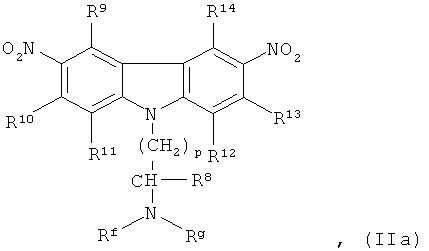
где Rf - это C1-6алкил;
Rg - это водород или C1-4алкил, или Rg и R8 вместе с атомами, к которым они присоединяются, формирующие пяти- или шестичленное алифатическое кольцо, содержащее один атом азота;
R9 - это водород или С1-3алкил;
R10 - это водород, гидрокси или C1-3алкокси;
R11 и R12 - независимо являются водородом или C1-3алкилом;
R13 - это водород, гидрокси, С1-3алкокси или гало;
R14 - это водород, C1-3 алкил или C1-3алкокси;
R8 - это водород или С1-3 алкил; и
p - это 0, 1, 2, 3, 4 или 5,
при условии, что, когда p - это 2, один из Rf и Rg отличается от этила, или его фармацевтически приемлемой соли, или гидрата.
[0089] Карбазол или его производная может иметь структурную формулу (IIb):
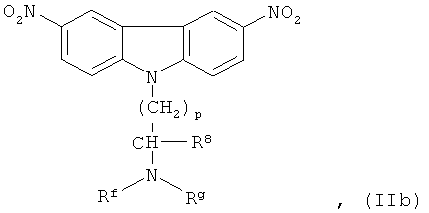
где Rf является метилом или этилом;
Rg - это водород или метил, или Rg и R8 вместе с атомами, к которым они присоединяются, формирующие пятичленное алифатическое кольцо, содержащее один атом азота;
R8 - это водород; и
p - это 1 или 2,
или фармацевтически приемлемая соль, или ее гидрат.
[0090] Карбазол или его производная может иметь формулу, выбранную из группы, состоящей из:
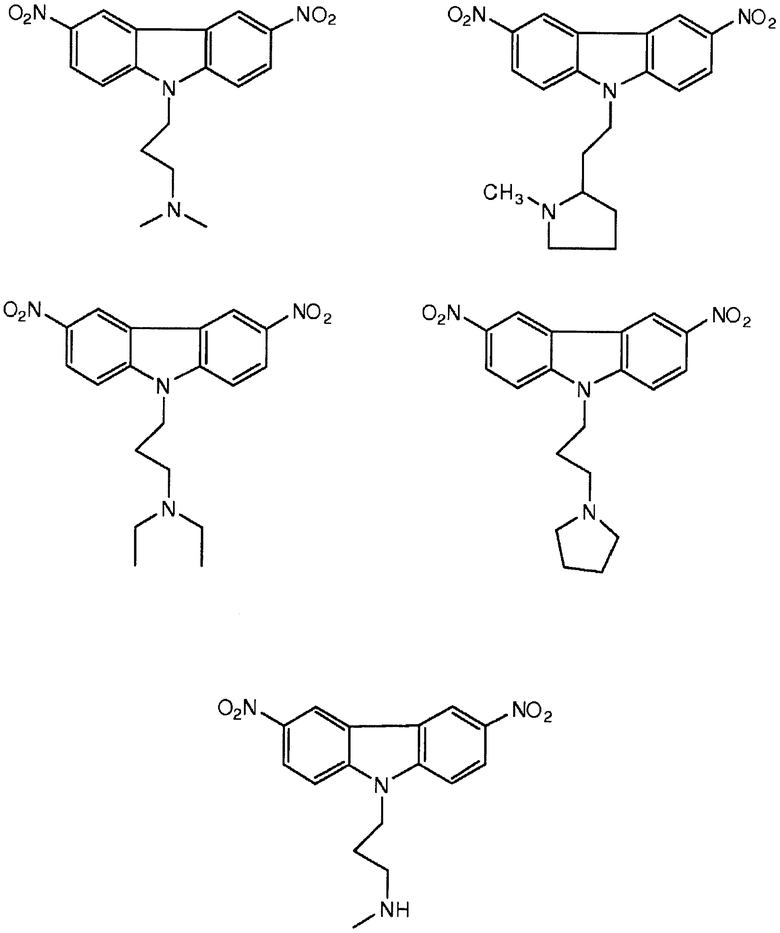
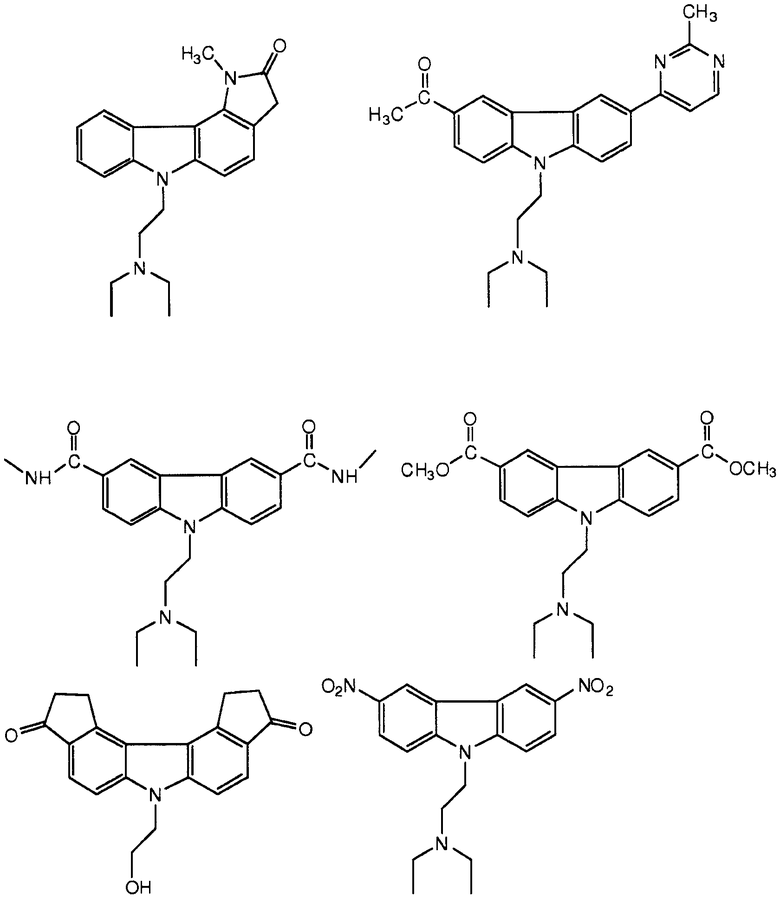
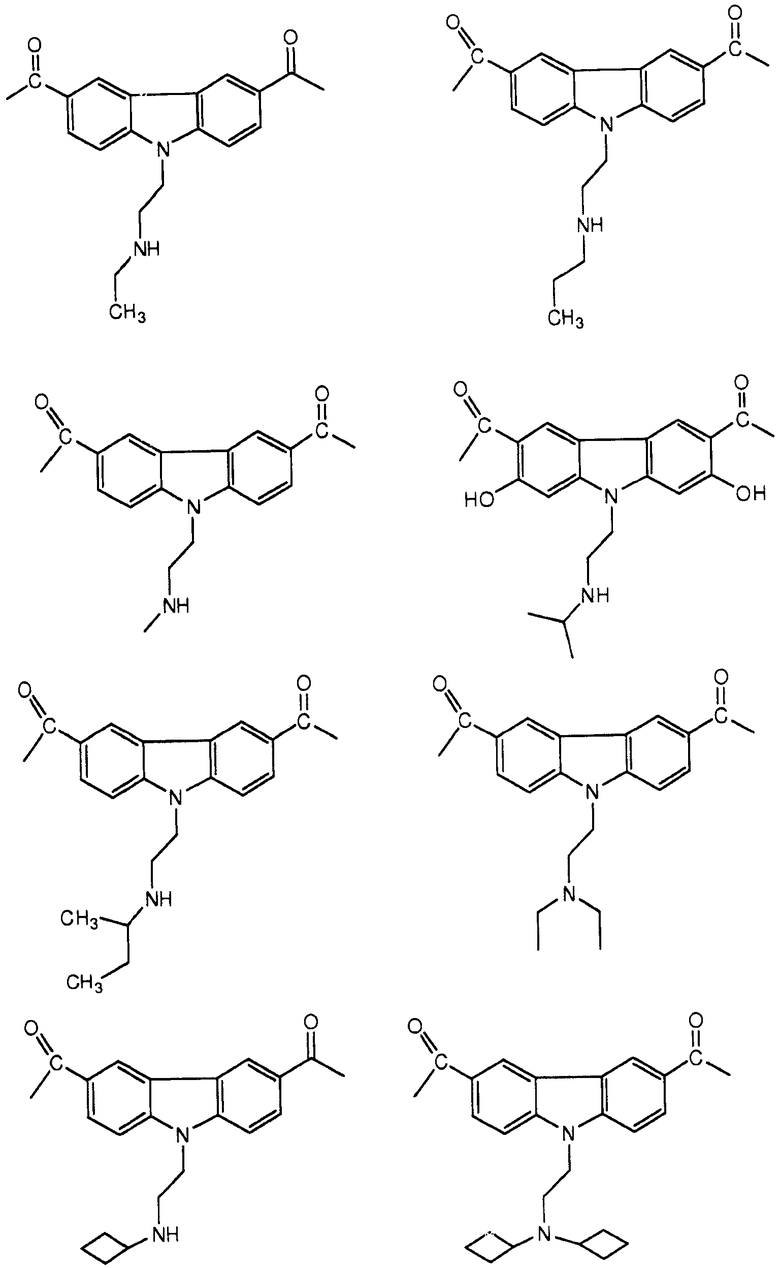
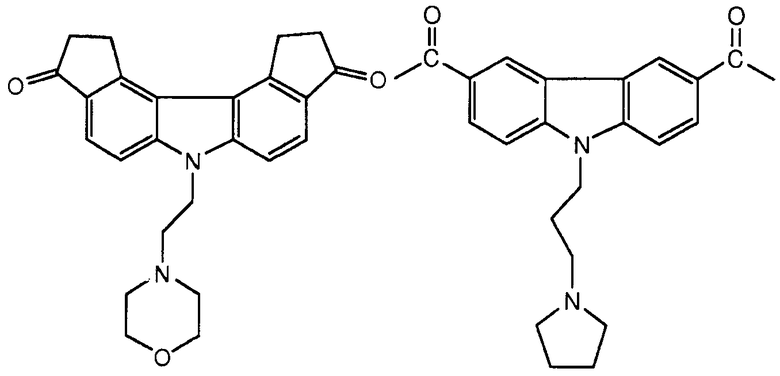
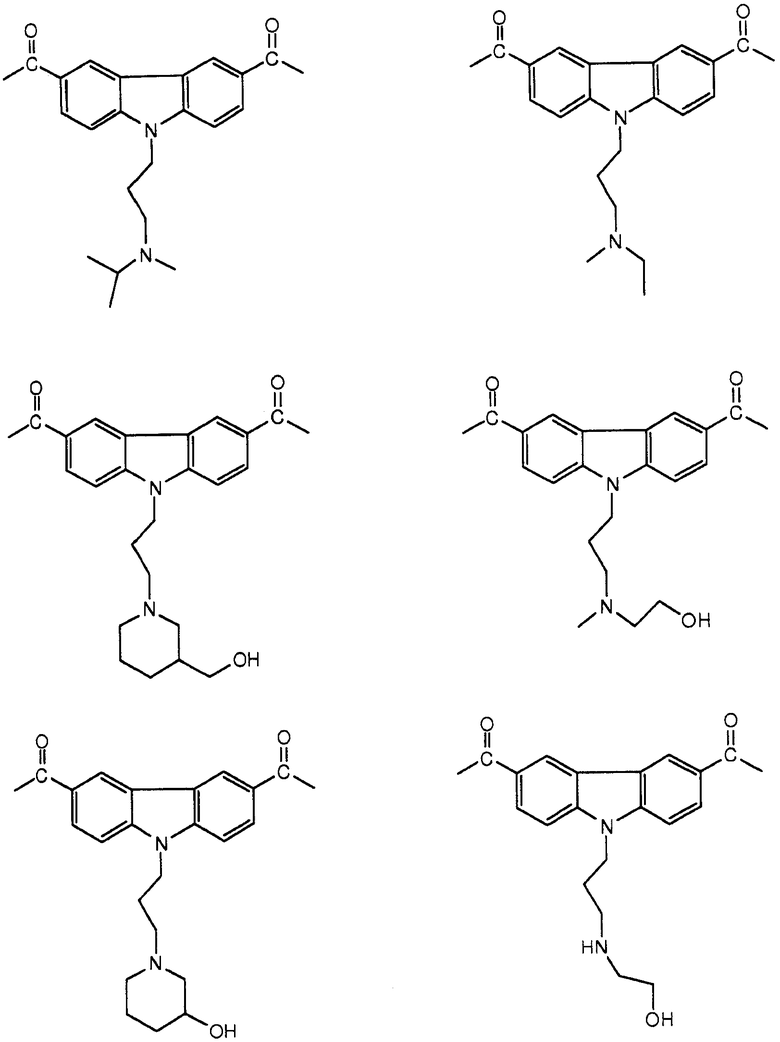
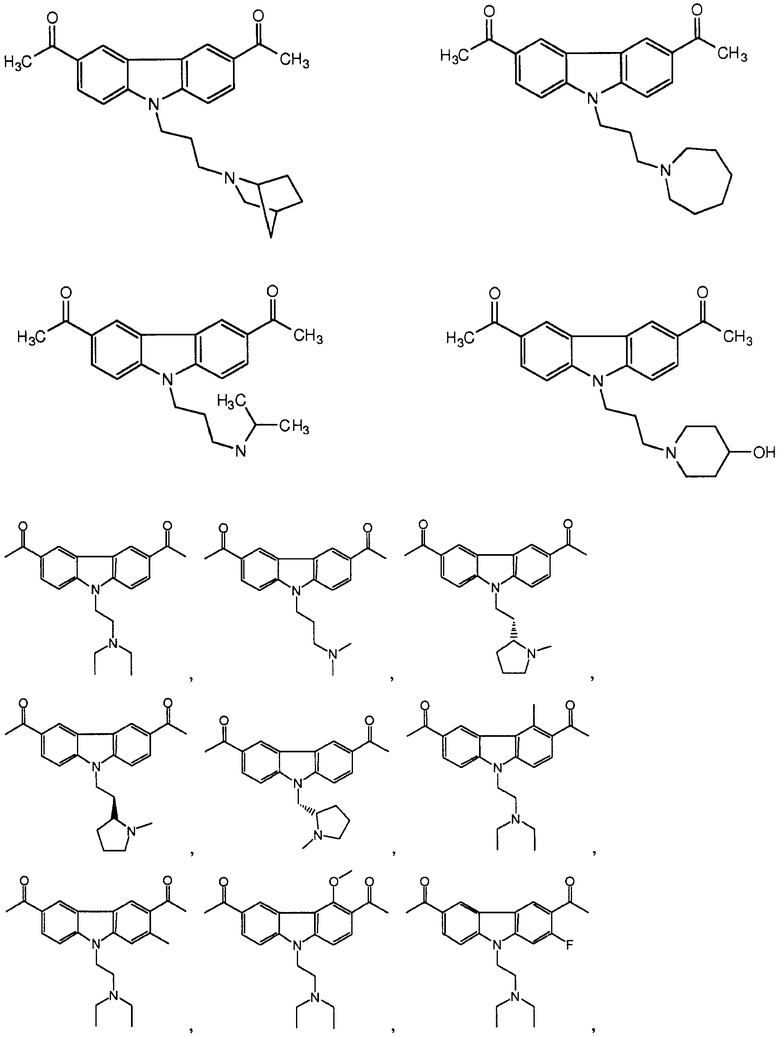
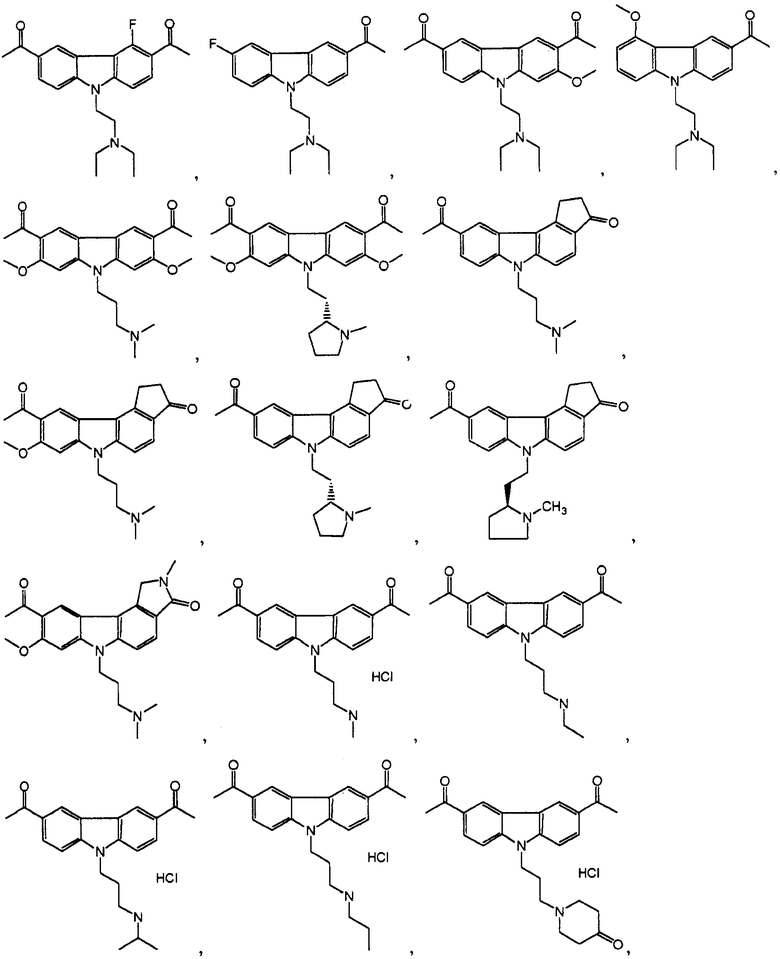
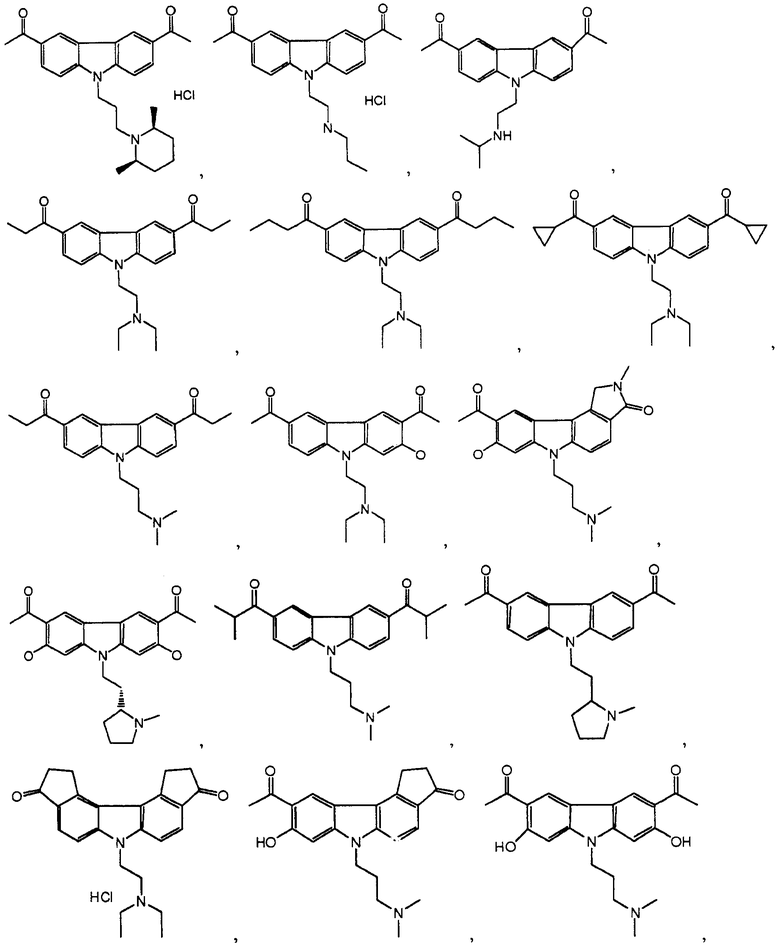
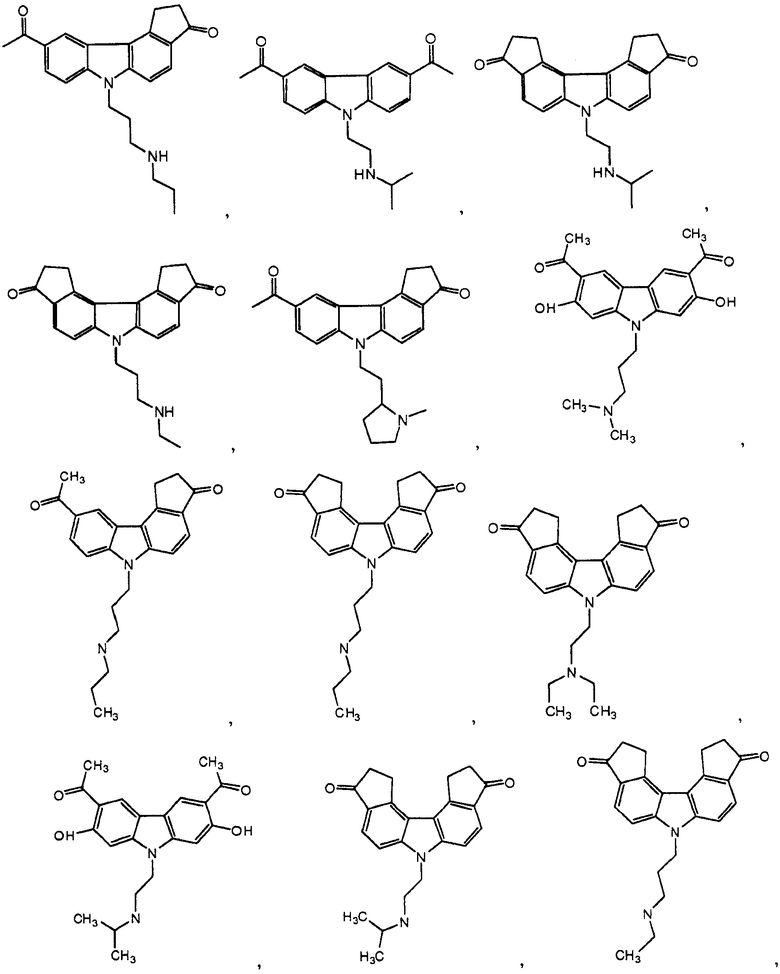
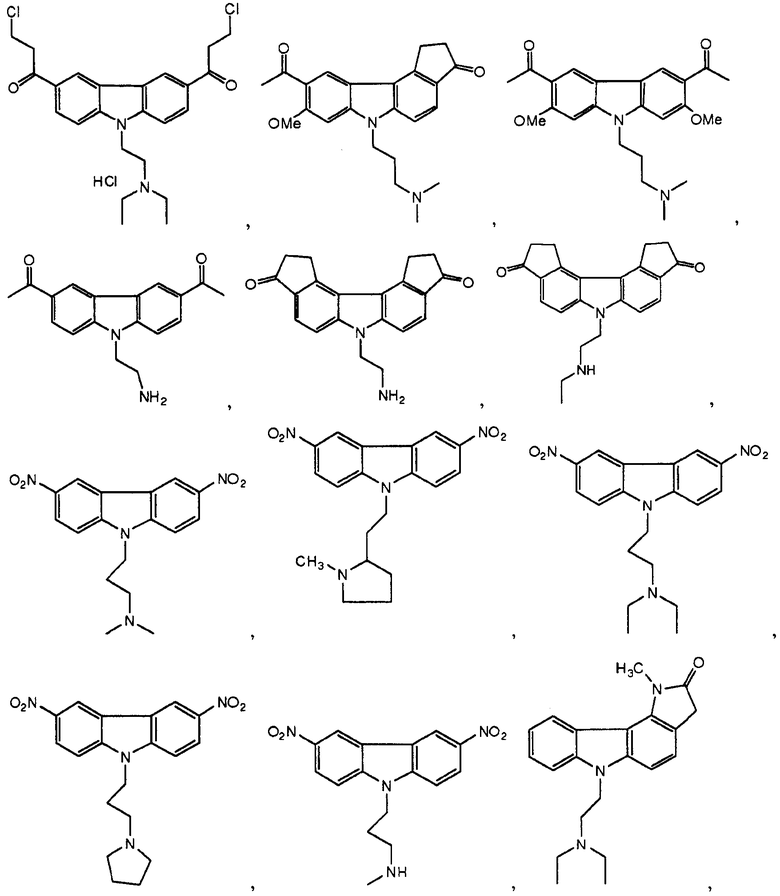
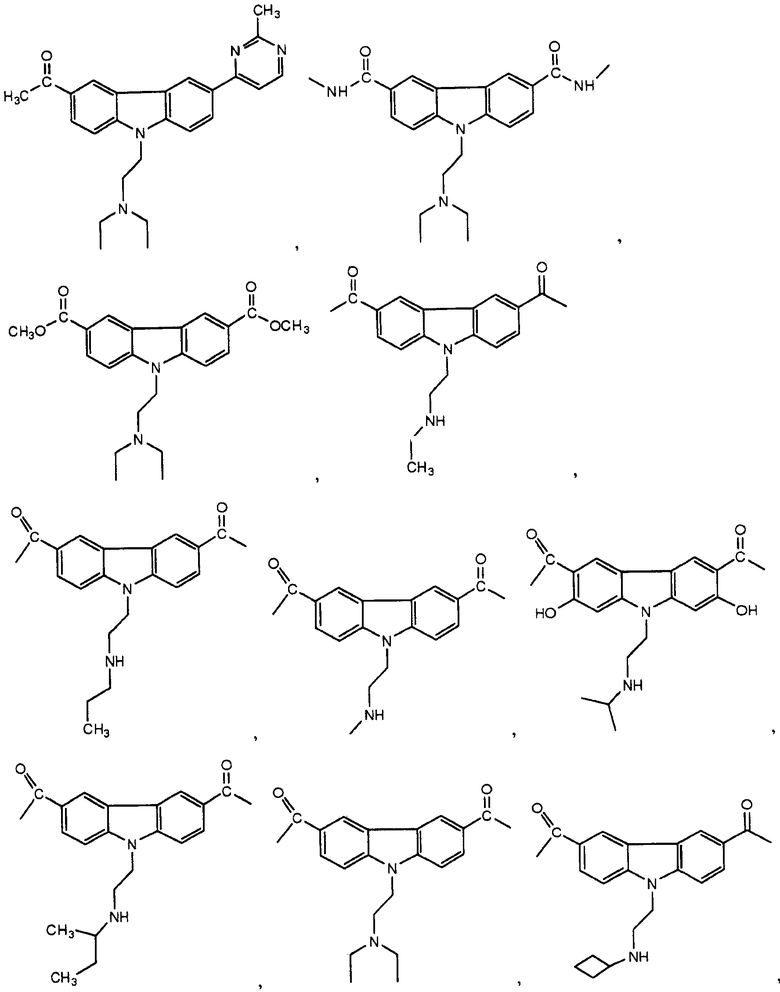
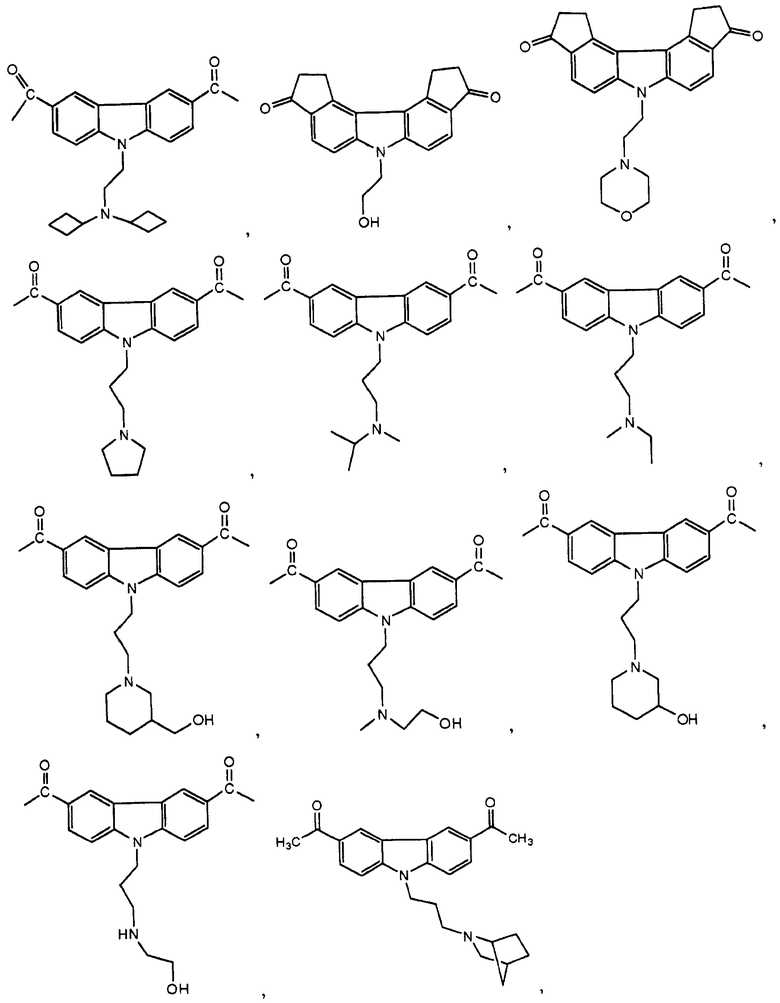
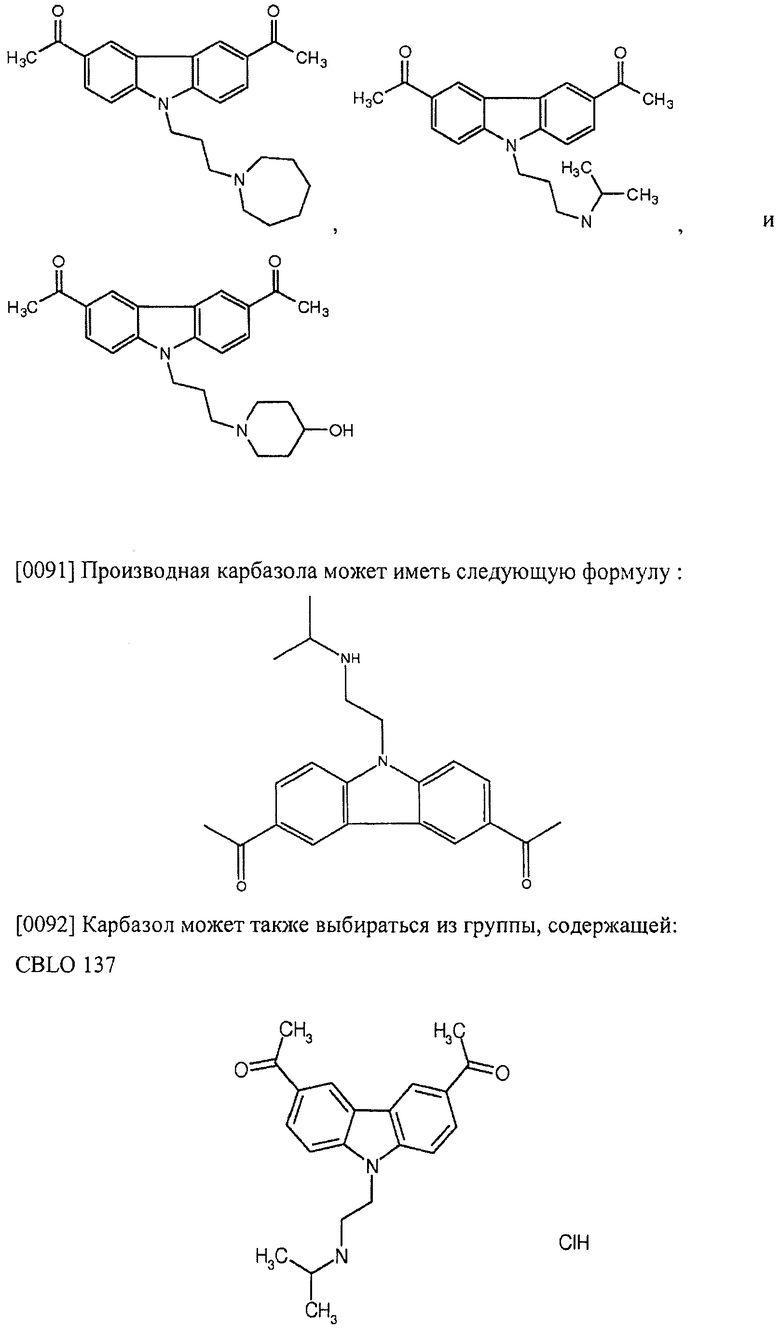
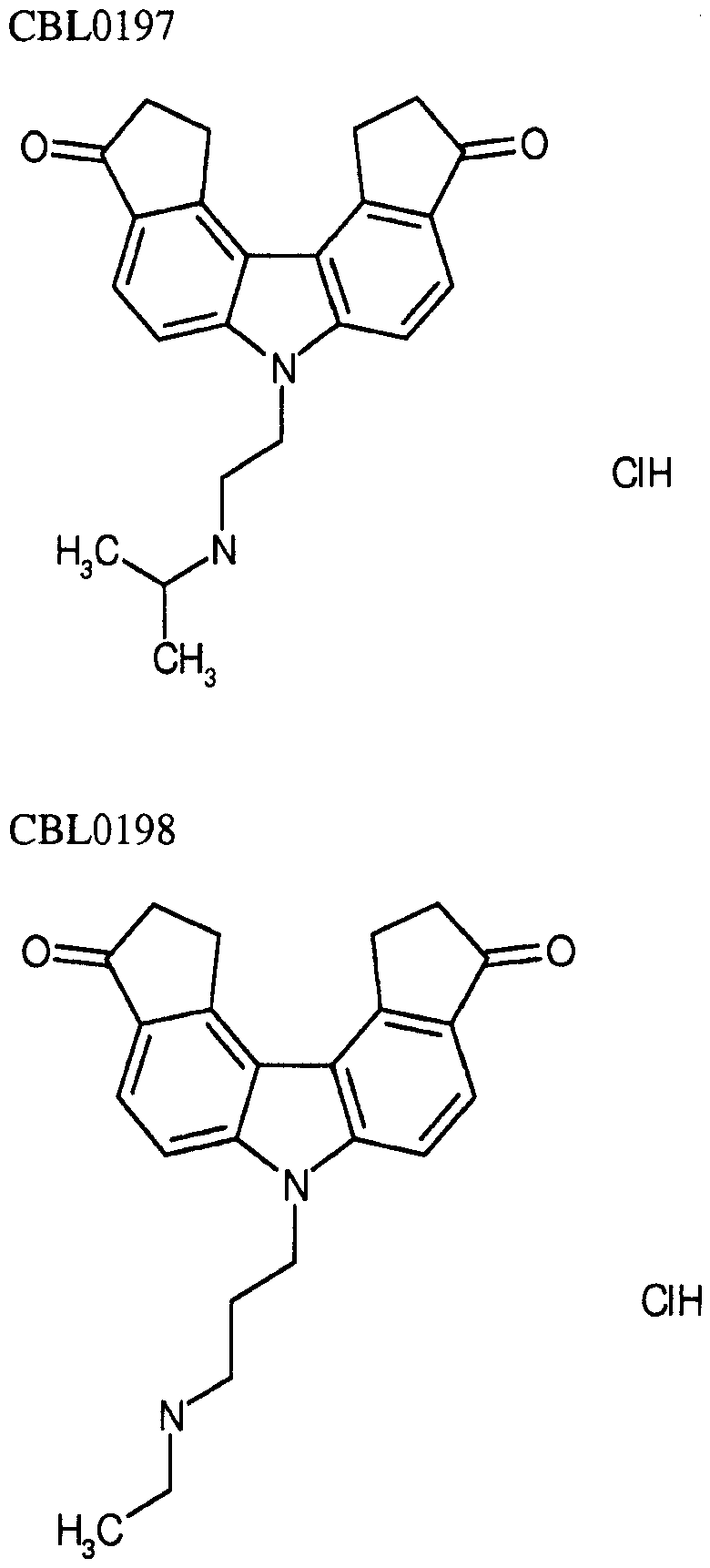
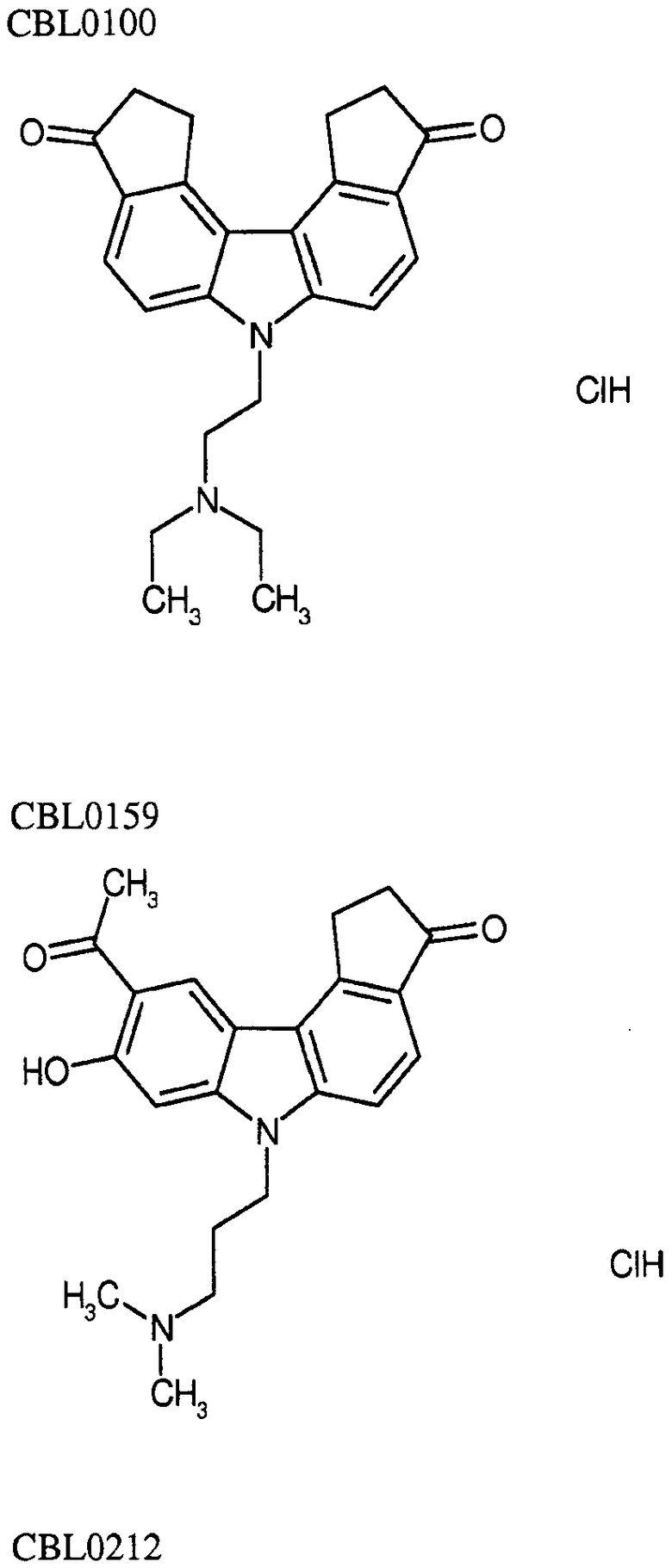
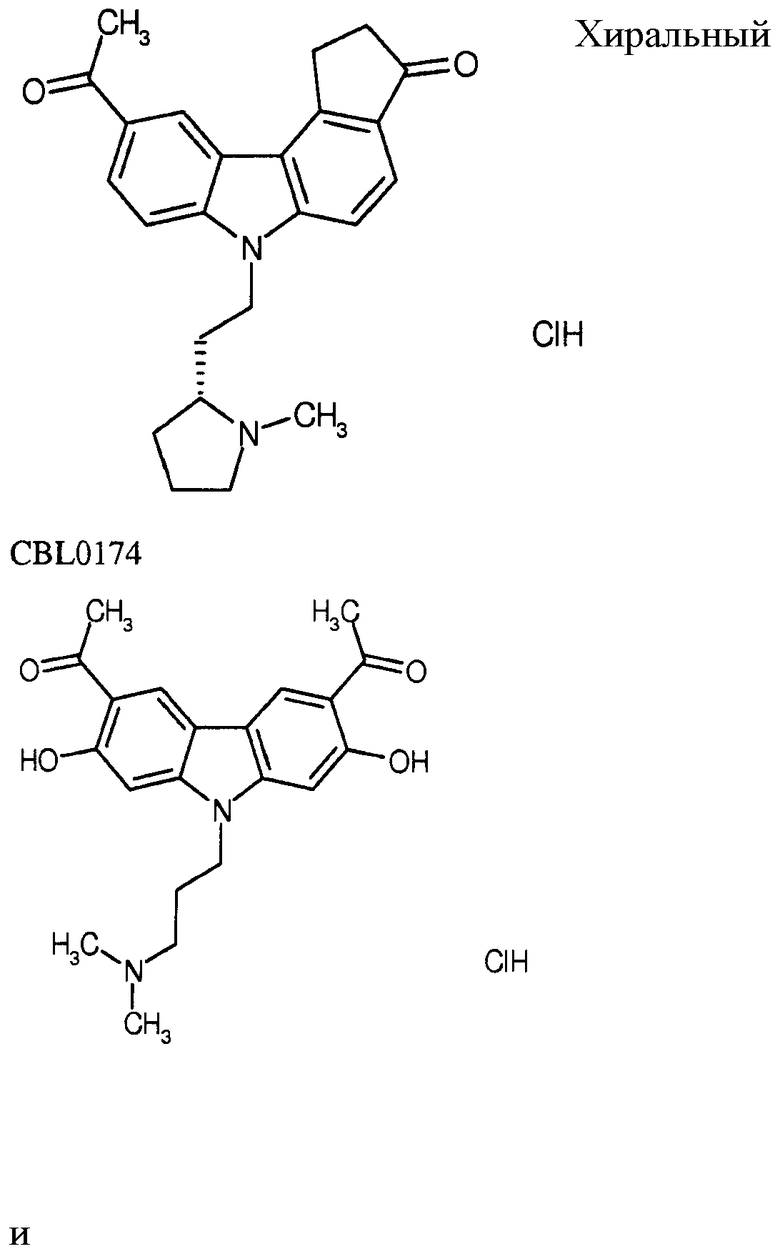
(3) Ингибитор транскрипции или трансляции
[0093] Ингибитор адаптивного температурного шокового ответа может также быть ингибитором транскрипции или трансляции. Например, ингибитор может быть актиномицином D или циклогексимидом.
b. Агент или условие, индуцирующие температурный шоковый ответ
(1) Агент, индуцирующий температурный шоковый ответ
[0094] Температурный шоковый ответ может быть вызван в клетке агентом, вызывающим температурный шоковый ответ. Агент может быть ингибитором синтеза белка, таким как пуромицин или азетидин. Агент может также быть HSP90 ингибитором, таким как гелданамицин (DMAG17), радицикол или 17-AAG. Агент может также быть ингибитором протеасом, таким как MG132, бортезомид или лактацистин. Агент может также быть сывороточным протеасомным ингибитором, таким как DCIC, TPCK или TLCK. Агент может быть медиатором воспаления, таким как циклопентенон, простагландин, арахидонат или фосфолипаза А2. Агент может также быть тритерпеноидом, таким как целастрол. Агент может быть со-индуктором, таким как нестероидный противовоспалительный препарат, такой как салицилат натрия, или индометацин, или производная гидроксиламина, такая как бимокломол или аримокломол. Агент может также быть флавоноидом, таким как кверцетин или бензилиден лактамовым соединением, таким как KNK437. Агент может также быть соединением арсенита или этанолом.
(2) Нагревающие средства
[0095] Температурный шоковый ответ может также быть вызван в клетке нагревающим средством. Нагревающие средства могут быть фотоэлектрическими, механическими или химическими. Нагревающие средства могут подавать клетке высокую температуру неинвазивным образом, например через кожу. Нагревающие средства могут также включать провод, полость, приемник, зонд или катетер, как описано в опубликованной заявке US 20070288075. Нагревающие средства могут включать оптические волокна, нить или имплантированное устройство. Нагревающие средства могут быть выполнены, как описано в патенте US 5814008, содержание которого включается здесь ссылкой.
[0096] Нагревающие средства могут также включать датчик для измерения температуры клетки или ткани на месте обработки, и могут вырабатывать сигнал, указывающий температуру. Температура может измеряться термопарой, резистивным датчиком температуры или термистором. Датчик может быть тепловым игольчатым датчиком или температурным зондом. Температурой нагревающих средств можно управлять в ответ на сигнал. Температурой можно управлять за счет изменения величины мощности, подаваемой для питания источника тепла, чтобы поддерживать температуру на заданном уровне, или чтобы предотвратить превышение температуры обрабатываемой клетки или ткани заданного уровня.
(а) Фотоэлектрические
[0097] Нагревающие средства могут быть выполнены в виде источника светового излучения, такого как множество полупроводниковых приборов светового излучения. Например источник света может быть светодиодом, электролюминесцентным устройством, лазером, лазерным диодом, лазером, излучающим с поверхности вертикальной плоскости, или лампой накаливания. Свет может иметь определенную длину волны, которая может быть видимой, ближней инфракрасной или инфракрасной длиной волны. Например, длина волны может быть от 750 нм до 1 мм. Длина волны может также быть 750, 760, 770, 780, 790, 800, 810, 820, 830, 840, 850, 860, 870, 880, 890, 900, 910, 920, 930, 940, 950, 960, 970, 980, 990 или 1000 нм. Длина волны может также быть 1; 1,1; 1,2; 1,3; 1,4; 1,5; 1,6; 1,7; 1,8; 1,9; 2; 2,1; 2,2; 2,3; 2,4; 2,5; 2,6; 2,7; 2,8; 2,9; 3; 3,1; 3,2; 3,3; 3,4; 3,5; 3,6; 3,7; 3,8; 3,9; 4; 4,1; 4,2; 4,3; 4,4; 4,5; 4,6; 4,7; 4,8; 4,9; 5; 5,1; 5,2; 5,3; 5,4; 5,5; 5,6; 5,7; 5,8; 5,9; 6; 6,1; 6,2; 6,3; 6,4; 6,5; 6,6; 6,7; 6,8; 6,9; 7; 7,1; 7,2; 7,3; 7,4; 7,5; 7,6; 7,7; 7,8; 7,9; 8; 8,1; 8,2; 8,3; 8,4; 8,5; 8,6; 8,7; 8,8; 8,9; 9; 9,1; 9,2; 9,3; 9,4; 9,5; 9,6; 9,7; 9,8; 9,9; 10; 10,1; 10,2; 10,3; 10,4; 10,5; 10,6; 10,7; 10,8; 10,9; 11; 11,1; 11,2; 11,3; 11.4; 11,5; 11,6; 11,7; 11,8; 11,9; 12; 12,1; 12,2; 12,3; 12,4; 12,5; 12,6; 12,7; 12,8; 12,9; 13; 13,1; 13,2; 13,3; 13,4; 13,5; 13,6; 13,7; 13,8; 13,9; 14; 14,1; 14,2; 14,3; 14,4; 14,5; 14,6; 14,7; 14,8; 14,9 или 15 µм. Длина волны может также быть 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99 или 100 µм. Длина волны может также быть 10, 20, 30, 40, 50, 60, 70, 80, 90, 100, 110, 120, 130, 140, 150, 160, 170, 180, 190, 200, 210, 220, 230, 240, 250, 260, 270, 280, 290, 300, 310, 320, 330, 340, 350, 360, 370, 380, 390, 400, 410, 420, 430, 440, 450, 460, 470, 480, 490, 500, 510, 520, 530, 540, 550, 560, 570, 580, 590, 600, 610, 620, 630, 640, 650, 660, 670, 680, 690, 700, 710, 720, 730, 740, 750, 760, 770, 780, 790, 800, 810, 820, 830, 840, 850, 860, 870, 880, 890, 900, 910, 920, 930, 940, 950, 960, 970, 980, 990 или 1000 µм.
[0098] Источник света может быть интенсивным лазером, и может включать использование двухфотонного способа. Лазер может включать хорошо коллимированный пучок. Источник света может также быть источником некогерентного света низкой мощности. Свет может также излучаться при меньшем количестве частиц на квадратный метр (то есть при более низком уровне флюенса) по сравнению с лазером высокой интенсивности. Например, флюенс может быть 30-25000 джоулей. Интенсивность света может составлять меньше чем 500 мВт/см2.
[0099] Нагревающие средства могут также излучать микроволны или радиочастотную энергию, как описано в патентах US 6904323 и US 5549638, содержание которых включается здесь ссылкой. Нагревающие средства могут включать антенну, такую как в антенной решетке. Нагревающие средства могут также включать ультразвуковой преобразователь.
(b) Механические
[0100] Нагревающие средства могут включать резистивный элемент. Резистивный элемент может быть резистивной лампой накаливания. Нагревающие средства могут также включать нагретую жидкость или газ, который может содержаться внутри баллона, как описано в патентной заявке US 2007/0288075, содержание которой включается здесь ссылкой.
(c) Химические
[0101] Нагревающие средства могут включать химикат, способный к увеличению внутренней температуры клетки. Например, химикат может включать частицу оксигидроксида декстрана железа или комплекс железа. Химикат может также быть галлием, индием, технецием, стронцием, йодом или другим соединением, совместимым с живой тканью. Химикат может увеличить внутреннюю температуру клетки, увеличивая уровень метаболизма или окисление химиката в клетке путем повышения уровней оксигенации крови, как описано в патенте US 4569836, содержание которого включается здесь ссылкой.
(d) Температура
[0102] Внутренняя температура клетки может быть поднята до по крайней мере 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99 или 100°С. Внутренняя температура клетки может также быть поднята до значений между 1-38°С, 39-45°С, 45-60°С, 60-85°С или 85-100°С. Температура может быть достаточной для ослабления или уничтожения обработанной аминоакридином клетки, но слишком низкой для ослабления или уничтожения нормальной клетки, которая может быть необработанной. Температура может также быть достаточной, чтобы вызвать температурный шок. Внутренняя температура клетки может повышаться в течение по крайней мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59 или 60 минут, или 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71 или 72 часов.
c. Назначение
[0103] Соединения, химикаты и агенты, описанные здесь, могут доставляться клетке путем абсорбции и диффузии в сосудистую систему пациента. Назначение пациенту может быть пероральным, парентеральным, трансдермальным или посредством свечи. Доставка к клетке может осуществляться иглой, присоединенной к шприцу, или катетером, соединенным с системой внутривенного вливания, или местно.
3. Лечение Пациента
[0104] Способ, представленный здесь, может использоваться для лечения заболевания или состояния нуждающегося в нем пациента. Ингибитор адаптивного температурного шокового ответа может быть назначен пациенту, а температурный шоковый ответ может быть вызван в пациенте или локально, или в целом. Например, способный вызвать температурный шоковый ответ агент может быть доставлен клетке, такой как инфицированная клетка, или в опухоль. Агент, вызывающий температурный шоковый ответ, может также быть в целом введен пациенту. Внутренняя температура клетки может быть увеличена локальным применением нагревающего средства к клетке. Температура тела пациента может также быть увеличена в целом, как в физиологически допустимой гипертермии.
а. Рак
[0105] Рак или предраковое состояние могут лечиться способом, раскрытым здесь. Рак может быть опухолью, которая может быть подкожной или кожной. У опухоли может быть маленький или большой объем. Опухоль может быть опухолью мозга, такой как глиальная опухоль, глиобластома, астроцитома, анапластическая астроцитома, астроцитома-олигодендроглиома, гипофизарная аденома. Рак может быть легочным или плевральным мезотелиальным раком, таким как рак легких, карцинома легкого, немелкоклеточный рак легкого, рак трахеобронхиального дерева, рак легких ранней стадии, эндобронхиальная метастатическая опухоль, периферический рак легких или злокачественная плевральная мезотелиома.
[0106] Рак может также быть гастроэнтерологическим раком, который имеет предраковое или злокачественное поражение, расположенное в пределах пищевода, желчного протока желудка или колоректума. Опухоль может быть опухолью головы и шеи, пищевода, раком пищевода ранней стадии, болезнью пищевода Баррета, воротной холангиокарциномой, твердым поражением печени или поджелудочной железы, колоректальными метастазами печени или раком поджелудочной железы.
[0107] Рак может также быть урологическим заболеванием, таким как рецидивная папиллярная опухоль, рак мочевого пузыря, поверхностный рак мочевого пузыря, рак простаты или доброкачественная предстательная гиперплазия. Рак может также быть гинекологическим раком, таким как карцинома или дисплазия шейки матки, рак шейки матки или цервикальная интраэпителиальная неоплазия.
[0108] Рак может быть раком кожи, который может быть плоскоклеточным раком (SCC), базально-клеточным раком (ВСС), злокачественной меланомой, ВИЧ связанной саркомой Капоши, Средиземноморско-связанной саркомой Капоши, базальной фолликулярной гамартомой, болезнью Бовена, кожной Т-клеточной лимфомой или гиперплазией сальных желез. Рак может также быть кожным предраковым или злокачественным поражением. Рак может также быть раком молочной железы, таким как метастатический рак молочной железы, раком толстой кишки, внутриматочным раком, глазной опухолью или раком головы и шеи, таким как раком в полости рта, глотке, губной карциномой, раком носовой впадины или гортани.
(1) Комбинационное лечение
[0109] Способ лечения рака или предракового состояния, соединение или композиция, раскрытые здесь, могут быть объединены или назначаться совместно с противоопухолевой терапией. Противоопухолевая терапия может быть противоопухолевым агентом, радиационной терапией, хирургией или PDT.
(а) Противоопухолевая терапия
[0110] Противоопухолевая терапия может быть радиационной терапией, такой как рентгеновская, радиочастотная или микроволновая энергия, ультразвук, радиоизотопная терапия, ионизирующая радиация, внешняя лучевая или телетерапия, брахитерапия или лучевая терапия изолированным источником, или лучевая терапия неизолированным источником. Противоопухолевое лечение может также быть хирургическим, таким как уменьшение объема опухоли, криотерапией или хирургическим иссечением.
(2) Фотодинамическая терапия
[0111] PDT может включать облучение обработанной аминоакридином клетки, на которую также можно воздействовать фотосенсибилизирующим агентом, видимым светом. Свет может иметь особую длину волны, и может активировать фотосенсибилизирующий агент. Активированный фотосенсибилизирующий агент может генерировать синглетный кислород или радикал, который может ослабить или уничтожить клетку. PDT может быть такой, как описано в патентах US 899723 и US 6693093, содержание которых включается здесь ссылкой.
b. Терапия доброкачественного симптома
[0112] Доброкачественный симптом в нуждающемся пациенте может лечиться с использованием способа. Симптом может быть кожное заболевание, такое как псориаз, вирусные бородавки или удаление волос. Симптом также может быть глазное состояние, такое как возрастная дегенерация желтого пятна, субфовеальная хориоидальная васкуляризация, патологическая миопия, глазной гистоплазмозный синдром или хориоидальное неоваскулярное заболевание. Симптом может также быть сердечно-сосудистое заболевание, такое как атеросклеротическая бляшка, гиперплазия интимы, атеросклероз или уязвимая бляшка, или рестеноз.
с. Лечение инфекции
[0113] Инфекция в нуждающемся пациенте может лечиться с использованием способа. Инфекция может быть вирусной инфекцией, такой как вирус герпеса, грипп, вирус иммунодефицита человека или гепатит А, В, или С. Инфекция также может быть бактериальной инфекцией, такой как хламидийная, туберкулезная или микоплазма.
[0114] Инфекция может также быть вызванной эукаратическими паразитами, такими как грибы, лямблии, токсоплазмоз или трипаносома. Грибы могут быть дрожжевыми. Трипаносома может вызывать малярию и может быть плазмодием, или лейшманией.
d. Лечение связанного с воспалением заболевания
[0115] Связанное с воспалением заболевание или состояние могут также лечиться с использованием способа. Воспаление может быть хроническим, аутоиммунным заболеванием, аллергией, астмой, септическим шоком, заболеванием трансплантат против хозяина, хирургической раной, ожогом или ишемическим состоянием.
4. Способ скрининга
[0116] Здесь также представлен способ скрининга соединения, способного модулировать адаптивный температурный шоковый ответ в клетке, когда соединение объединено с индуцированном температурного шокового ответа. Способ может включать индуцирование температурного шокового ответа в популяции клеток и контакт популяции с тестовым соединением. Число клеток, которые погибают в популяции по сравнению с контролем, может быть показателем соединения, которое модулирует адаптивный температурный шоковый ответ.
[0117] Клетки в популяции могут также включать репортер, индуцирующий температурный шоковый ответ. Способ может далее включать измерение уровня репортера. Уровень репортера по сравнению с контролем может быть показателем соединения, которое модулирует адаптивный температурный шоковый ответ. Репортер может включать транскрипт HSP70 гена, такой как HSP70A1 или HSP70'B. Репортер может также включать Н8Р70белок. Репортер может также включать вектор, включающий промоутер, вызывающий температурный шоковый ответ, операбельно связанный с репортерным геном. Репортерный ген может кодировать детектируемый маркер, который может быть люцеферазой, зеленым флуоресцентным белком, желтым флуоресцентным белком, красным флуоресцентным белком или хлорамфениколь ацетилтрансферазой.
5. Композиция
[0118] Данное изобретение касается композиции, которая может включать ингибитор адаптивного температурного шокового ответа. Композиция может также включать агент, вызывающий температурный шоковый ответ. Композиция может также включать терапевтический агент, который может быть противоопухолевым агентом или фотосенсибилизирующим агентом. Композиция может использоваться в терапии, вызывая температурный шоковый ответ в обработанной композицией клетке, который может ослабить или уничтожить клетку.
a. противоопухолевый агент
[0119] Противоопухолевым агентом может быть любой фармакологический агент или соединение, которое вызывает апоптоз. Фармакологический агент или соединение могут быть, например, маленькой органической молекулой, пептидом, полипептидом, нуклеиновой кислотой или антителом.
[0120] Противоопухолевый агент может быть цитотоксическим агентом или цитостатическим агентом или их комбинацией. Цитотоксические агенты препятствуют тому, чтобы раковые клетки множились путем: (1) вмешательства в способность клетки копировать ДНК и (2) вызова гибели клеток и/или апоптоза в раковых клетках. Цитостатические агенты действуют через коррекцию, вмешательство или ингибирование процессов трансдукции клеточного сигнала, который регулирует пролиферацию клеток и иногда на низких постоянных уровнях.
[0121] Цитотоксическим агентом может быть: алкилирующий агент (включающий азотный мустард, производные этиленимина, алкил сульфонаты, nitrosoureas или триазен): урациловый мустард, хлорметин, циклофосфамид (Цитоксан®), изофосфамид, мелфалан, хлорамбуцил, пипоброман, триэтилен-меламин, триэтилентиофосфорамин, бусульфан, кармистин, ломустин, стрептозоцин, дакарбазин или темозоломид, антиметаболит (включающий антагонист фолиевой кислоты, аналог пиримидина, аналог пурина и ингибитор аденозин деаминазы): метотрексат, 5-фтороурацил, флоксиридин, цитарабин, 6-меркаптопурин, 6-тиогунин, флударабин фосфат, пентостатин и гемцитабин; натуральный продукт или его производную (например, алкалоид барвинка, антиопухолевый антибиотик, энзим, лимфокин или эпиподофиллотоксин): винбластин, винкристин, виндезин, бломицин, дактиномицин, даунорубицин, доксорубицин, эпирубицин и дарубицин, ара-с, паклитаксел (Таксол®), митрамицин, dеoксико-формицин, митромицин-с, 1-аспарагиназу, интерферон (предпочтительно IFN-a), этопозид или тенипозид. Цитотоксическим агентом может также быть навелбен, СРТ-11, анастразол, летразол, капецитабин, релоксафин, циклофосфамид, ифозамид или дролоксафин.
[0122] Цитотоксическим агентом может также быть действующий на микротубулы агент, который может влиять на клеточный митоз. Действующим на микротубулы агентом может быть: аллоколхицин (СНБ 406042), галихондрин В (СНБ 609395), колхицин (СНБ 757), производная колхицина (например, СНБ 33410), доластатин 10 (СНБ 376128), мейтанзин (СНБ 153858), ризоксин (СНБ 332598), паклитаксел (Таксол®, СНБ 125973), производная Таксола® (например, СНБ 608832), тиокохицин (СНБ 361792), тритил цистеин (СНБ 83265), винбластин сульфат (СНБ 49842), винкристин сульфат (СНБ 67574), естественный или синтетический эпотилон, такой как эпотилон А, эпотилон В или дискодермолид (см. Service, (1996) Science, 274:2009), эстрамустин, нокодазол, МАР4, и т.п. Действующим на микротубулы агентом может также быть описанный в Bulinski (1997) J. Cell Sci. 110:3055 3064; Panda (1997) Proc. Natl. Acad. Sci. USA 94:10560-10564; Muhlradt (1997) Cancer Res. 57:3344-3346; Nicolaou (1997) Nature 387:268-272; Vasquez (1997) Mol. Biol. Cell. 8:973-985; и Panda (1996) J. Biol. Chem. 271:29807-29812.
[0123] Цитотоксическим агентом может также быть: эпидофиллотоксин; противоопухолевый фермент; ингибитор топоизомеразы; прокарбазин; митоксантрон; платиновый координирующий комплекс, такой как цисплатин или карбоплатин; биологический модификатор ответа; ингибитор роста; антигормональное терапевтическое средство; лейковорин; тегафур; или гематопоэтический фактор роста.
[0124] Цитостатическим агентом может быть гормон или стероид (включая синтетический аналог): 17.альфа.-этинилстрадиол, диэтилстилбэстрол, тестостерон, преднизон, флюоксиместерон, дромостанолон пропионат, тестолактон, мегастролацетат, метилпреднизолон, метилтестостерон, преднизолон, триамцинолон, хлоротрианизен, гидроксипрогестерон, аминоглютетимид, эстрамустин, медроксипрогестеронацетат, леупролид, флютамид, торемифен или золадекс.
[0125] Цитостатиком может также быть антиангиогеник, такой как ингибитор матриксной металлопротеиназы или другой ингибитор VEGF, такой как анти-VEGF антитело или маленькая молекула, такая как ZD6474 и SU6668. Цитостатическим агентом может также быть анти-Her2 антитело от Genentech, EGFR ингибитор, такой как EKB-569 (необратимо действующий ингибитор) или Imclone антитело С225, которое может быть иммуноспецифическим для EGFR, или src ингибитор.
[0126] Цитостатическим агентом может также быть Casodex® (бикалутамид, Astra Zeneca), который может представлять андрогензависимый карциномный непролиферативный; антиэстроген Тамоксифен®, который может ингибировать пролиферацию или рост эстрогензависимого рака молочной железы; или ингибитор трансдукции клеточного пролиферативного сигнала, такого как ингибитор эпидермального фактора роста, Her-2 ингибитор, ингибитор MEK-I киназы, ингибитор МАРК киназы, ингибитор PI3-киназы, ингибитор Src киназы или PDGF ингибитор. Противоопухолевым может также быть соединение, указанное в Таблице 1 американской предварительной заявки №61/102,913, поданной 6 октября 2008, содержание которой включается здесь ссылкой.
b. Фотосенсибилизирующие агенты
[0127] Фотосенсибилизирующим агентом может быть соединение, которое поглощается клеткой, и которое, когда подвергнуто воздействию света, активируется и вызывает выработку вещества, которое ослабляет или уничтожает клетку. Веществом может быть синглетный кислород или радикал. Фотосенсибилизирующий агент может поглощать свет с длиной волны от 500 нм до 1,1 µм. Фотосенсибилизирующими агентами может быть один из раскрытых в патентах US 693093 или US 7018395, содержание которых включается здесь ссылкой.
[0128] Например, фотосенсибилизирующим агентом может быть зеленый порфирин; полипирролитическое макроциклическое светочувствительное соединение, которое является гидрофобным; ангелицин; липофусцин; реакционный центр фотосистемы II; D1-D2-cyt b-559 реакционный центр фотосистемы II; халкогенпирилловый краситель; хлор; хлорофилл; кумарин; цианин; ДНК-связанное соединение, такое как аденозин, цитозин, 2'-деоксигуанозин-5'-монофосфат, дезоксирибонуклеиновая кислота, гуанин, 4-тиоуридин; 2'-тимидин 5'-монофосфат, тимидилил (3'-5')-2'-деоксиаденозин, тимидлил (3'-5')-2'-дезоксигуанозин, тимин или урацил; лекарственное средство, такое как адриамицин; афлохалон, амодиахин дигидрохлорид, хлорохин дифосфат, хлорпромазин гидрохлорид, дауномицин, дауномицинон, 5-иминодауномицин, доксициклин, фуросемид, гилвокарцин М, галвокарцин V, гидроксихлорохин сульфат, лумидоксициклин, мефлохин гидрохлорид, мехитазин, мембромин (меркурохром), примахин дифосфат, хинин сульфат или тетрациклина гидрохлорид; флавин или относящееся соединение, такое как аллоксазин, флавин мононуклеотид, 3-гидроксифлавон, лимихром, лимифлавин, 6-метилаллоксазин, 7-метилаллоксазин, 8-метилаллоксазин, 9-метилаллоксазин, 1-метил лимихром, метил-2-метоксибензоат, 5-нитросалициклическая кислота, профлавин или рибофлавин; фуллерен; металлопорфирин; металлофталоцианины; производная метиленового синего; нафталимид; нафталоцианин; натарульное соединение, такое как бис(4-гидрокси-3-метоксифенил)-1,6-эптадиен-3,5-дион, 4-(4-гидрокси-3-метоксифенил)-3-бутен-2-один, N-формилкинуренин, кинуреновая кислота, кинуренин, 3-гидроксикинуренин, DL-3-гидроксикинуренин, сангунарин, берберин, капмин или 5; 7; 9 (1 1); 22-эргостатетраен-3β-ол; производная нильского синего; NSAID (нестероидный противовоспалительный препарат); апериленхинон; фенол; феофорбид; феофитин; димер фотосенсибилизатора или конъюгата; фталоцианин; порфицин; порфирин; псорален; пурпурин; хинон; ретиноид; родамин; тиофен; вердинс; витамин или ксантеновый краситель (Redmond and Gamlin, Photochem. Photobiol, 70(4):391-475 (1999)).
c. Составы
[0129] Состав может далее включать один или более фармацевтически приемлемый дополнительный компонент (ы), такой как квасцы, стабилизаторы, антимикробные средства, буферный агент, красящие агенты, ароматические агенты, вспомогательные вещества и т.п.
[0130] Состав может быть в форме таблеток или лепешек, сформулированных обычным способом. Например, таблетки и капсулы для перорального приема могут содержать обычные наполнители, включая, но без ограничения, связывающие агенты, наполнители, смазки, дезинтеграторы и смачивающие агенты. Связывающие агенты включают, но без ограничений, сироп, акацию, желатин, сорбитол, трагакант, растительный крахмал и поливинилпирролидон. Наполнители включают, но без ограничения, лактозу, сахар, микрокристаллическую целлюлозу, кукурузный крахмал, фосфат кальция и сорбитол. Смазки включают, но без ограничения, стеарат магния, стеариновую кислоту, тальк, гликоль полиэтилен гликоль и кварц. Дезинтеграторы включают, но без ограничения, картофельный крахмал и гликолят натриевого крахмала. Смачивающие агенты включают, но без ограничения, лаурил сульфат натрия). Таблетки могут быть покрыты в соответствии с известными в области техники способами.
[0131] Композиция может также быть жидким составом, включающим, но без ограничения, водные или масляные суспензии, растворы, эмульсии, сиропы и эликсиры. Композиция может также быть составлена как сухой продукт для соединения с водой или другой подходящей средой перед использованием. Такие жидкие препараты могут содержать добавки, включая, но без ограничения, суспендирующие агенты, эмульгирующие средства, эмульсификаторы, неводные среды и консерванты. Суспендирующий агент включает, но без ограничения, сироп сорбитола, метил целлюлозу, сироп глюкозы/сахарный сироп, желатин, гидроксиэтилцеллюлозу, карбоксиметил целлюлозу, гель стеарата алюминия и гидрогенизированные пищевые жиры. Эмульгирующие агенты включают, но без ограничения, лецитин, сорбитан моноолеат и акацию. Неводные среды включают, но без ограничения, пищевые масла, миндальное масло, фракционированное кокосовое масло, масляные сложные эфиры, пропилен гликоль и этиловый спирт. Консерванты включают, но без ограничения, метил или пропил p-гидроксибензоат и сорбиновую кислоту.
[0132] Композиция может также быть составлена в виде свечей, которые могут содержать основу свечи, включая, но без ограничения, масло какао или глицерины. Композиция может также быть сформулирована для ингаляции в форме, включающей, но без ограничения, раствор, суспензию или эмульсию, которая может вводиться как сухой порошок или в форме аэрозоля, используя пропеллент, такой как дихлордифторметан или трихлорфторметан. Композиция может также быть сформулирована как трансдермальный препарат, включающий водные или неводные среды, включая, но без ограничения, сливки, мази, лосьоны, пасты, лекарственные пластыри, кусочки пластыря или мембрану.
[0133] Композиция может также быть сформулирована для парентерального введения, включая, но без ограничения, инъекции или непрерывное вливание. Препараты для инъекции могут быть в форме суспензий, растворов или эмульсий в масляных или водных средах, и могут содержать агенты препарата, включая, но без ограничения, суспендирующие, стабилизирующие и диспергирующие агенты. Композиция может также быть представлена в форме порошка для соединения с подходящей средой, включая, но без ограничения, стерильную, апирогенную воду.
[0134] Композиция может также быть сформулирована как депо-препарат, который может быть применен путем имплантации или внутримышечной инъекции. Композиция может быть сформулирована с подходящими полимерными или гидрофобными материалами (как эмульсия в приемлемом масле, например), ионообменными смолами, или как недостаточно растворимыми производными (как недостаточно растворимой солью, например).
[0135] Композиция может также быть сформулирована как липосомный препарат. Липосомный препарат может включать липосомы, которые проникают через целевые клетки или stratum corneum и сплавляются с клеточной мембраной, приводя к доставке содержимого липосомы в клетку. Например, могут использоваться липосомы, такие как описано в патентах US 5077211, 4621023 или US 4508703, которые включаются здесь ссылкой. Композиция, предназначенная для кожных заболеваний, может быть применена до, во время или после воздействия на кожу млекопитающего УФ или агентов, вызывающих окислительные нарушения. Другие подходящие препараты могут использовать ниосомы. Ниосомы - липидные среды, подобные липосомам, с мембранами, состоящими в значительной степени из неионогенных липидов, некоторые формы которых эффективны для транспортировки соединений через stratum corneum.
d. Дозировка
[0136] Терапевтически эффективное количество агента, требующегося для использования в терапии, меняется в зависимости от природы состояния, которое подвергается лечению, отрезка времени, в течение которого требуется активность, и возраста и состояния пациента, и в конечном счете определяется лечащим врачом. Желаемая доза может быть удобно назначена в единственной дозе, или как многократные дозы, применяемые через адекватные интервалы, например как один, два, три, четыре или больше поддоз в день. Многократные дозы часто желательны или требуются.
[0137] При введении в комбинации с другой терапией композиция может назначаться в относительно более низких дозировках. Кроме того, использование целевых агентов может позволить необходимой дозировке быть относительно низкой. Определенные композиции могут применяться в относительно высоких дозировках из-за факторов, включающих, но без ограничения, низкую токсичность, высокую очистку, низкий процент расщепления третичного амина. В результате дозировка композиции может быть приблизительно от 1 нг/кг до приблизительно 200 мг/кг, от приблизительно 1 µг/кг до приблизительно 100 мг/кг, или от приблизительно 1 мг/кг до приблизительно 50 мг/кг. Дозировка композиции может быть в любой дозировке, включающей, но без ограничения, приблизительно 1 µг/кг - 1 мг/кг, или 1 мг/кг - 100 мг/кг.
[0138] Данное изобретение обладает многократными аспектами, иллюстрированными следующими неограничивающими примерами.
Пример 1
Ингибирование адаптивного температурного шокового ответа, объединенное со стимулированием температурного шокового ответа, может вызвать гибель клеток
[0139] Этот пример демонстрирует, что эффективность температурной шокоцелевой терапии может быть в значительной степени облегчена агентами, которые блокируют индукцию адаптивного температурного шокового ответа, таким образом препятствуя мобилизации опухолевыми клетками естественного устойчивого механизма через механизм задействования индуцибельных шаперонов. Адаптивный температурный шоковый ответ может быть выборочно заблокирован путем подавления HSF-I, главного медиатора индуцибельной, вызванной температурным шоком транскрипции. Агенты ингибирования адаптивного температурного шокового ответа могли использоваться в комбинации с соединениями или состояниями, индуцирующими температурный шок, которые должны привести к их увеличенной цитотоксичности. Эта цитотоксичность, как предполагается, будет более явной в опухоли, чем в нормальных клетках из-за более высокой степени зависимости опухолевой клетки от шаперонов.
[0140] Этот пример также демонстрирует, что противомалярийный препарат акрихин (QC), связанное с ним соединение 9-аминоакридин (9АА) и другие химикаты, принадлежащие семье карбазолов (CZ), действуют как ДНК-интеркалирующие негенотоксичные агенты, которые оказывают влияние на функцию определенных классов генных промоутеров, которые являются индуцибельными, путем активации проводящих путей трансдукции сигнала. Тестирование температурного шокового ответа клеток в присутствии этих соединений продемонстрировало, что эти соединения могут подавлять HSF-I - опосредованную транскрипцию в зависимости от дозы независимо от того, обработка или агент используется, чтобы вызывать температурный шоковый ответ.
[0141] Акрихин и 9АА добавлен к опухолевым клеткам в культуре для исследования влияния этих соединений на hsp70 активацию в ответ на обработку, вызывающую температурный шок. Температурный шоковый ответ вызван при использовании известного ингибитора протеасом MG132 и Бортезомида, Н8Р90ингибитора DMAG17 (Гелданамицин) и термообработки (42-45°С, 10-60 минут). Чтобы контролировать температурный шоковый ответ, индуцибельная изоформа Hsp70 детектировалась Вестен иммуноблоттингом, использующим антитело, которое распознает индуцибельную форму HSP70 белка, и Северной гибридизацией, использующей пробу, которая специфично распознает иДНК индуцибельные HSP70A1 и HSP70B' гены, но не распознает иРНК, которая кодирует конституцивно выраженный HSC70 белок. QC и 9АА предотвращали индукцию HSP70 белка (Фиг.1А). Акрихин и 9АА не оказывали влияние на способность MG 132 или Бортезомида ингибировать активность протеасом (Фиг.1В), указывая, что эффекты QC и 9АА не связаны с инактивацией индуцирующих температурный шок обработок. Кроме того, индуцибельные HSP70 транскрипты накапливались в клетках, обработанных вышеупомянутыми вызывающими температурный шоковый ответ средствами, но транскрипция блокировалась в присутствии акрихина и 9АА (Фиг.2). В дополнение к аминоакридинам подобный эффект наблюдался при обработке клеток эмитином, который является общим ингибитором трансляции (Фиг.2). Это подтверждает, что наблюдаемый эффект QC и 9АА имеет место благодаря отсутствию температурной шоковой белковой индукции.
[0142] Фигура 1 показывает, что QC и 9АА предотвращали индукцию HSP70 белка в клетках, обработанных ингибиторами протеасом. Белковые экстракты из HeLa клеток, обработанные 5 µМ ингибитора MG 132 протеасом в течение 8 часов одним или в комбинации с QC, или 9АА исследованы, используя антитело к индуцибельной форме HSP70 и к Пирину (контроль на гелевую нагрузку) (Фиг.1А). Результаты in vitro анализа активности протеасом из экстрактов клеток, обработанных MG132 одним или в комбинации с акрихином и 9АА показывают, что QC и 9АА не оказывают влияние на ингибирование протеасом, оказываемое MG132 (Фиг.1В).
[0143] Фигура 2 показывает что QC и 9АА ингибировали транскрипцию HSP70 гена в ответ на ингибиторы протеасом. 10 µг общего количества РНК из HeLa клеток обработаны в течение 5 часов 0,1 µМ Бортезомида (Brtz), или 5 мМ MG 132 (MG) одним или в комбинации с 20 мМ QC (Quin), 20 µМ 9АА, или 1 µМ эмитина (ЕМ). Результаты анализировали Северным блоттингом с HSP70A1/B'-специфической гибридизационной пробой. GAPDH был контролем на РНК нагрузку. Hsp70 (x) указывает на индукцию HSP70 транскрипции.
[0144] Фигура 3 показывает, что DMAG 17 - индуцированный HSP70 синтез был чувствителен к QC и 9АА. Иммуноблоттинг с анти HSP70 антителами Юцг экстрактов белка из HeLa клеток, обработанных в течение 5 часов 5 µМ MG132 (MG) или DMAG 17 одним или в комбинации с акрихином (Quin) или 9АА. Относительная индукция HSP70 экспрессии (индикатор) показана (результаты денситометрии).
[0145] Фигура 4 демонстрирует, что QC и 9АА подавляли транскрипцию индукции HSP70A1/B' гена при использовании DMAG 17 и MG 132, как показано Северной гибридизацией 10 µг общего количества РНК из HeLa клеток, обработанных 1 µМ DMAG 17, в течение 5 часов одним или в комбинации с 9АА. GAPDH использовался в качестве контроля на РНК нагрузку. Hsp70 (x) указывает относительную индукцию HSP70 транскрипции.
[0146] Фигура 5 демонстрирует токсический эффект сочетания лекарств в HeLa клетках, как показано результатами пробы формирования колонии HeLa клеток, обработанных в течение 6 часов протеотоксическим лекарственным препаратом DMAG 17 (1 µМ) в комбинации с переменными концентрациями акрихина (10 или 20 µм). Клетки собраны, разбавлены 1:50 и анализированы на формирование колонии. Величины колоний оценены окрашиванием бромфенола синего после 7 дней роста и фиксации 10%-ным формальдегидом. Данные являются средним числом трех экспериментов. Агенты, вызывающие температурный шок, и QC показывают синергическую цитотоксичность.
[0147] Фигура 6 показывает результаты эксперимента, подобного показанному на фигуре 5, но вместо DMAG17 использовалась температурная шоковая обработка (43°С, 30 минут). Синергическая цитотоксичность наблюдалась, когда QC был объединен с высокой температурой.
[0148] Фигура 7 показывает, что температурная чувствительность опухолевых клеток, но не нормальных клеток, увеличивалась после обработки с использованием QC и CZ (соединение CBLO 137). RCC45 (клетки почечно-клеточной карциномы) и NKE-hTEPT (нормальные почечные эпителиальные клетки, иммортализованные трансдукцией теломеразы) обработаны различными концентрациями QC или соединения CBLO 137 и затем немедленно помещены на водяную баню при 45°С (суспендированы в питательной среде). Время инкубации в водяной бане показано различными оттенками. После нагревания клетки размещены в 96 луночной пластине и инкубированы в течение 24 часов в присутствии лекарственного средства и затем еще 48 часов в несодержащей лекарств питательной среде. Жизнеспособность клеток оценена окрашиванием клеточным титром синим (Alamar Blue, Promega).
[0149] Фигура 8 показывает, что siPHK-опосредованный нокаут компонента FACT ядерного комплекса, SSPT1 и FACT киназы CKII увеличил чувствительность клетки к температурному шоку. НТ1080 клетки трансформированы с siPHK группами, разработанными против белковой казеиновой киназы (CKII), SSPT1 и GAPDH (контроль) (Dharmacon) согласно протоколу изготовителя. 24 часа спустя все клетки разделены в 6-ти луночные пластины. Еще после 24 часов клетки в пластинах помещены для нагрева до 45°С в течение 10, 15 и 20 минут на водяной бане. Жизнеспособность клеток оценена через 48 часов после нагрева пробой Клеточным Титром Синим (Promega).
[0150] Эти результаты указывают, что комбинированная обработка опухолевых клеток нетоксичными или незначительно токсичными вызывающими температурный шоковый ответ агентами в присутствии нетоксичных или малотоксичных концентраций соединений, ингибирующих HSF-I - опосредованную транскрипцию, приводит к синергической цитотоксичности, которая более распространена для опухоли, чем для нормальных клеток. Молекулярный механизм ингибирования HSF-I - опосредованной транскрипции путем использования QC, 9AA и CZ соединений связана с их способностью к ингибированию активности ядерного хроматин реконструирующего комплекса FACT, который, по-видимому, важен для JSF-I и NF-kB-управляемой транскрипции (Фиг.8).
Пример 2
Аминоакридины предотвращают активацию hsp70 в ответ на ингибирование протеасом
[0151] Этот пример показывает, что аминоакридины предотвращают hsp70 активацию в ответ на ингибирование протеасом. Повышенная регуляция индуцибельной формы hsp70 - признак HSR после протеотоксического стресса, такого как создаваемый ингибированием протеасом. Влияние нескольких противомалярийных препаратов на синтез hsp70, активизированного маломолекулярным ингибитором MG 132, тестировано в культивированных HeLa клетках. Эмитин и акрихин (QC) подавили hsp70 синтез в ответ на MG132 (Фиг.9А). 9-аминоакридин (9АА), который близок по структуре к QC, имел подобный подавляющий эффект на MG132-вызванную hsp70 экспрессию (Фиг.9В).
[0152] Эмитин - ингибитор общей трансляции; поэтому его способность подавлять индуцибельный hsp70 синтез - вероятно отражение этого свойства. Однако QC и 9АА не имели никакого влияния на общий синтез белка (как показано введением 35S-метионина и 35S-цистеина) при концентрациях, которые были достаточны для полного подавления hsp70 индукции (Фиг.9С). Это указывает, что эти соединения на основе аминоакридина подавляют индуцибельный hsp70 синтез через другой, более специфичный механизм. Ни QC, ни 9АА не оказали влияние на способность MG132 ингибировать активность протеасом (Фиг.9D). Поэтому препараты не блокировали hsp70 индукцию просто путем взаимодействия с созданием протеотоксического стресса через ингибирование протеасом.
[0153] Ингибирующее влияние QC на hsp70 индукцию обнаружено при mРНК уровне, как показано Северной гибридизацией РНК из HeLa клеток, обработанных MG132 или другим протеасомальным ингибитором, бортезомидом с или без QC (Фиг.9Е). Гибридизационная проба, используемая в этом эксперименте, была специфичной для индуцибельной hsp70A1 mРНК и не обнаруживала mРНК, кодирующую конституционный hsc70 белок. Результаты показали, что QC подавлял накопление hsp70 mРНК при условии ингибирования протеасом. Этот эффект имел место благодаря подавлению транскрипции, а не стимуляции hsp70 mРНК деградации, поскольку добавление QC после индукции HSR не имело никакого влияния на hsp70 mРНК численность. Ингибирующий эффект QC и 9АА на экспрессию индуцибельного гена не был универсален. Например, ZnCl2-вызванная активация транскрипции металлотионеинового гена не вызывалась этими соединениями при условиях, при которых они аннулировали индукцию hsp70 mРНК (Фиг.9F). Кроме того, QC и 9АА оба вызывали сильную индукцию транскрипции р53 целевых генов.
Пример 3
Акрихин блокирует индукцию температурного шокового ответа за счет hsp90 ингибирования или гипертермии
[0154] Этот пример демонстрирует, что акрихин блокирует температурный шоковый ответ, вызванный hsp90 торможением или гипертермией. Функциональная инактивация hsp90 гелданамицином или его производной 17-DMAG вызывает протеотоксический стресс и активизирует HSR, включающий синтез hsp70. Как показано на фиг.9, для протеотоксического стресса, вызванного ингибиторами протеасом, QC и 9АА также подавляют hsp70 индукцию в ответ на hsp90 ингибирование, и это имеет место на транскрипциональном уровне (Фиг.10А и В). Хотя QC и 9АА эффективно подавляли 17-DMAG - активизированную транскрипцию hsp70A1 гена, они не имели никакого влияния на несколько других уровнях (не - 17-DMAG вызванных) mРНК, включая уровни для GAPDH, p65RelA и GRP94 (Фиг.10С).
[0155] QC также эффективен при блокировании HSR, индуцированного гипертермией, как показано на фиг.10D. В этом эксперименте непосредственно оценена активность HSF1 транскрипционного фактора, который, как известно, является существенным для индукции hsp70 экспрессии во время HSR. Клетки HSF1 репортера получены путем заражения HeLa клеток конструкцией лентивирусного репортера, содержащей EGFP сДНК под контролем HSF1 - зависимого промоутера. После обработки бортезомидом, 17-DMAG или гипертермией, HSF1-зависимый EGFP синтез вызван, как обнаружено флуоресцентной микроскопией. Комбинированная обработка клеток репортера с использованием QC в дополнение к любому из трех различных индукторов протеотоксического стресса блокировала EGFP накопление. Результаты этого примера демонстрируют, что противомалярийное лекарственное средство QC является сильным ингибитором HSR.
Пример 4
Акрихин оказывает влияние на снижение HSF1 функции ядерной транслокации и ДНК связывание
[0156] Этот пример демонстрирует, что акрихин оказывает влияние на снижение функции HSF1 ядерной транслокации и связывание ДНК. Активация HSFl-опосредованной транскрипции требует освобождение HSF1 из его комплекса с hsp90 в цитоплазме. Это сопровождается формированием HSF1 гомодимеров и гомотримеров, которые перемещаются в ядро и связываются с HSF1 специфичными сайтами распознавания внутри промоутеров индуцибельных к высокотемпературному шоку генов. Влияние QC и 9АА на этот процесс изучено для того, чтобы определить точку, в которой эти соединения действуют для ингибирования HSF1 функции. Чтобы оценить внутриклеточную локализацию и ДНК связывающую способность HSF1 комплексов, выполнены электрофоретические пробы на подвижность (EMSA), используя белковые экстракты, очищенные от цитоплазмы или ядер клеток, подвергнутых протеотоксическому стрессу, одни или в комбинации с QC или 9АА. Результаты этих экспериментов показаны на фигуре 11. Обработка HeLa клеток с использованием MG132, высокотемпературного шока или 17-DMAG привело к активации специфичной HSF1 ДНК связывающей активности в обоих цитоплазматических (фиг.11A) и ядерных экстрактах (фиг.11В). QC и 9АА не взаимодействовали с или не модифицировали силу этих воздействий при любой тестированной концентрации (вплоть до 100 мМ) (не показанные данные и фиг.11В). Эти результаты показывают, что ингибирование HSF1 зависимой транскрипции с использованием QC и 9АА встречается в точке ниже его эндоплазматической активации, ядерной транслокации и ДНК связывания.
[0157] Установление факта, что QC и 9АА оказывают влияние на HSF1, снижая его ядерную транслокацию, предполагает, что сами соединения локализованы, по крайней мере частично, в ядрах. Это поддерживается результатами, полученными с использованием экспериментальной модуляции их внутриклеточного распределения. Бафиломицин, лизосомоцелевой антибиотик, может значительно изменить внутриклеточное распределение лизосомтропных соединений, включая акрихин и хлорохин, путем ингибирования лизосомальной Н +-ATPase. Обработка HeLa клеток бафиломицином привела к выключению во внутриклеточную локализацию QC от преобладающе лизосомального к преобладающе ядерному (фиг.11С), как оценено флуоресцентной микроскопией (и QC и 9АА являются натуральными флуоресцентными соединениями). Влияние обработки бафиломицином на чувствительность hsp70 индукции к QC тестировано. Бафиломицин увеличил эффективность QC как HSR ингибитора в MG132-обработанных HeLa клетках, как показано на фиг.11D. В присутствии антибиотика, 5-мМ QC ингибировали hsp70 синтез также эффективно как 20-мМ QC в отсутствие антибиотика. Эти результаты указывают, что подавляющая активность QC против HSF1-опосредованной транскрипции зависит от его ядерной концентрации.
Пример 5
Комбинация акрихина с протеотоксическим стрессом вызывает апоптоз
[0158] Этот пример демонстрирует, что объединение акрихина с протеотоксическим стрессом вызывает апоптоз. Температурный шоковый ответ (HSR) является адаптивной реакцией про-жизнеспособного ответа, который может защитить клетки от множества токсических состояний. Быстрое накопление индуцибельных форм шаперонов, таких как hsp70 и hsp27, как показано, предотвратило гибель клеток при температурных шоковых состояниях или состоянии обработки ингибиторами протеасом или hsp90]. Поэтому способность QC и 9АА предотвращать индукцию белков, закодированных HSF1-зависимыми генами, может в значительной степени увеличить цитотоксичность протеотоксических стрессов. HeLa клетки обработаны 17-DMAG или бортезомидом одним или в комбинации с QC, и влияние на жизнеспособность клеток и индукцию апоптоза анализировалось. Как показано на фигурах 4А и 4В, QC в значительной степени увеличивал токсичность 17-DMAG и бортезомида, соответственно. Комбинированная обработка концентрациями QC, которые вызывали менее чем 50%-ое сокращение жизнеспособности клеток, и фактически нетоксичными концентрациями 17-DMAG или бортезомида, привело к впечатляющему сокращению числа растущих клеток.
[0159] Исследовано, играла ли роль индукция апоптоза при воздействии медикаментозной обработки на число жизнеспособных клеток. Апоптоз контролировался появлением каспаз-специфических продуктов распада кератина 18 и PARP. Последовательно с результатами анализа жизнеспособности клеток, комбинированная обработка QC и или бортезомидом или 17-DMAG сильно активизировала каспаз-опосредованный белковый распад, который едва поддавался обнаружению, когда препараты использовались одни (Фиг.12С и D). Каспаз ингибитор ZVAD-FMK блокировал этот эффект полностью, указывая, что протеолитические события распада были каспаз-специфичными (фиг.12Е).
[0160] Для исследования факта, играет ли торможение hsp70 индукции критическую роль в QC-опосредованной сенсибилизации клеток к бортезомиду и 17-DMAG, сравнивалось влияние QC с его влиянием из альтернативного способа hsp70 супрессии. HeLa клетки запажались siPHK, специфично предназначенной против индуцибельной формы hsp70. Зараженные клетки были неспособны синтезировать индуцибельный hsp70 после обработки ингибиторами протеасом или hsp90 (фиг.12D). Неспособность синтезировать hsp70 при условии протеотоксического стресса активизировала апоптотический ответ, подобный тому, который вызван комплексной обработкой QC и индуцирующими протеотоксический стресс агентами (фиг.12D). Сходство биологических влияний siPHK-опосредованного нокаута hsp70 и QC обработки относительно чувствительности клетки к бортезомиду и 17-DMAG предполагает, что объединенная токсичность QC и индукторов протеотоксического стресса устанавливается супрессией HSR с применением QC.
Пример 6
Антиопухолевый эффект комбинации акрихина с hsp90 ингибитором
[0161] Этот пример демонстрирует, что объединение акрихина с hsp90 ингибитором имеет антиопухолевые эффекты. Обнаружение того, что комбинация QC с вызывающими протеотоксический стресс препаратами имеет сильный токсический эффект на HeLa клетки in vitro, предполагает, что у таких комбинаций может быть значительный потенциал в качестве противоопухолевой терапии. Чтобы исследовать эту возможность, влияние QC/17-DMAG комбинационной обработки на рост опухоли in vivo тестировано с использованием двух изогенных моделей опухоли мыши: МСА205 фибросаркомы и В-16 меланомы. 17-DMAG использовался, так как это - индуктор протеотоксического стресса, который показал ограниченную антиопухолевую эффективность как монотерапия. Влияние 17-DMAG и QC на индукцию HSR (фиг.13А) и жизнеспособность клетки (фиг.13В) в МСА205 и В-16 клетках in vitro тестировалось. Обе клеточных линии ответили на препараты подобным HeLa клеткам образом, указывая, что эти модели могут законно использоваться для тестирования антиопухолевой активности QC/17-DMAG комбинации. Чтобы подтвердить, что препараты имеют подобный эффект на HSR индукцию в опухолях in vivo, МСА205 клетки внедрены в C57BL/6 мышей, и полученные в результате опухоли обработаны единственной внутриопухолевой инъекцией PBS (контроль), 25 мг 17-DMAG одного, или 1,25 мг QC с 25 µг 17-DMAG. Пять часов спустя, мыши забиты, и РНК, полученная из изолированных опухолей, анализировалась на hsp70 индукцию. Как показано на фиг.13С, 17-DMAG обработка вызвала hsp70 синтез в опухолях, выращенных in vivo, a QC предотвратил эту индукцию. Чтобы оценить влияние сочетания лекарств на рост опухоли in vivo, мыши, несущие МСА205 (фиг.13D) или В-16 (фиг.13Е) опухоли, обработаны внутриопухолевой инъекцией QC и 17-DMAG по отдельности или в комбинации. Размер опухолей измерялся регулярно (каждые 2 дня) после инъекции лекарственного средства. В обеих экспериментальных моделях, QC и 17-DMAG, введенный как единственный агент, имел незначительное антиопухолевое воздействие (задержка роста опухоли), тогда как в комбинации они полностью предотвратили рост опухоли. Размеры опухоли измерены спустя 24 дня после имплантации. Опухоли с единственной инъекцией лекарственного средства начали перерастать опухоли с комбинаторными инъекциями лекарственного средства с 16-ого дня для В-16 клеток и с 18-го дня для МСА205 клеток (Фиг.13А и В). Объединенная QC/17-DMAG обработка не только предотвратила рост опухоли, но и фактически привела к регрессу опухоли, для опухолей, уменьшенных от ~50 мм3 в размере до невыявляемых. Эти результаты указывают, что объединение QC с индукторами протеотоксического стресса приводит к апоптозу.
Пример 7
Способы
1. Клеточная культура, лентивирусные векторы, siPHK трансфекция и препараты
[0162] HeLa клетки культивировали в питательной модифицированной среде орла Dulbecco (Invitrogen/Gibco BRL, Carsbad, CA) с добавлением 10%-ной эмбриональной сыворотки теленка. Клетки мышиной меланомы В 16 и фибросаркомы МСА205 выращены в полной питательной RPMI-1640 среде, с добавлением 2 мМ L-глютамина, 100 µг/мл стрептомицина, 100 U/мл пенициллина, 50 µг/мл Гентамицина (Life Technologies, Grand-Island, NY). HSF1-специфичная EGFP экспрессия создана введением 6 копий HSF1 регулятивных элементов (HSE) 5' CAGAACGTTCTAG 3' (последовательность №1) выше минимального CMV промоутера в PTR-mCMV-EGFP лентивирусный вектор. Клетки заражены лентивирусом с MOI 10 в присутствии 4 µг/мл полибрена накануне вечером. Эффективность инфекции детектирована EGFP экспрессией в ответ на 43°С в течение 60 минут температурного шока. Между 70 и 90% клетки заражены вирусом и выражали GFP в ответ на температурный шок.
[0163] HeLa клетки заражены hsp70 siPHK (Santa Cruz Biotechnology, Santa Cruz, CA) в течение 24 часов, чтобы ингибировать hsp70 экспрессию во время дополнительной обработки препаратами. Клетки контроля были инфицированы не-hsp-70-специфичной siPHK-A (Santa Cruz Biotechnology, Santa Cruz, CA). Клетки обработаны, как описано в тексте, ингибитором протеасом MG132 (Calbiochem, San Diego, CA) и бортезомидом (LC Laboratories, Woburn, MA), hsp90 ингибитором 17-DMAG (LC Laboratories, Woburn, MA), акрихином, эмитином, хинином, хлорохином и 9АА (все от Sigma, St. Louis, МО). Воздействие гипертермией/температурным шоком выполнено путем инкубации при 43°С в течение одного часа.
2. Вестерн иммуноблотинг
[0164] Общее количество экстрактов белка из HeLa клеток получено в RIPA буфере (150 мМ NaCl, 1%-SDS, 10 мМ Трис (рН фактор 8,0), 1% натрия деоксилата, 1% NP-40), содержащем коктейль протеазного ингибитора (Sigma, St. Louis, МО). Белковые экстракты сепарированы электрофорезом в 4-20% градиентные полиакриламидные гели с использованием SDS (Invitrogen/Novex, Carlsbad, CA) и затем переданы на нейлоновые PVDF мембраны (Amersham, Piscataway, NJ). Мембраны предварительно инкубированы накануне вечером в 5%-ном растворе молока, и затем введены на 1 час в 1%-ный раствор молока с первичными антителами при 1:1000 разбавлении. Следующие первичные антитела использовались: индуцибельная форма кроличьей анти-hsp70A1 (Assay Designs/StressGen, Victiria, ВС, Canada) и крысиной анти-HSF1 (Assay Designs/StressGen, Victiria, ВС, Canada). Контроли на белковую нагрузку были крысиным антипириновым антителом (Institut агк Biochemie der Ludwig-MAximillians-Universitat Munchen, Germany) и кроличьим антикератин 18 антителом (Burnham research Institute, CA). Апоптоз анализирован детектированием каспазы-специфичного распада K1 8 (Burnham research Institute, CA) и PARP (антитело от Santa Cruz Biotechnology, Santa Cruz, CA). HRP-конъюгированные вторичные антикроличьи, антикрысиные и антимышиные антитела куплены у Santa Cruz Biotechnology. Детектирующий реактив (ECL) поставлен от Perkin Elmer (Shelton, CT).
3. Северный блоттинг и гибридизация
[0165] Общее количество РНК (10 µг) от HeLa, В-16 или МСА205 клеток анализировали Северной гибридизацией с пробами, специфичными для hsp70A1, MT1, p65Re1A, GRP94 и GAPDH генов. PCR фрагмент получен из hsp70A1 cДНК(Invitrogen, Carlsbad, CA) с праймерами, специфичными для hsp70A1 кодирующей последовательности (AIs: 5' ССА ССА ТСС ССА ССА AGC АГА С3' (последовательность №:2); Ala: 5' CAT GAA ССА TCC TCT ССА ССТ 3') (последовательность №3). Все другие гибридизационные пробы созданы ограниченным перевариванием эндонуклеазы от сДНК клонов (ORIGENE).
[0166] In vivo маркирование 35S-белка. HeLa клетки обработали препаратами и их комбинациями согласно протоколам экспериментов. Нормальная питательная среда изменена на питательную среду, не содержащую метеонин/цистеин, с добавлением 35S - метионина и 35S-цистеина (50 мСi/мл) (New England Nuclear/Perkin Elmer, Shelton, CT), и клетки инкубированы в течение дополнительных 60 минут в присутствии препаратов. Цитоплазматические белковые экстракты приготовлены согласно Digman протоколу. Маркированные белки анализировали электрофорезом в 10% полиакрилимидном геле и ауторадиографией.
4. In vitro проба на активность протеасом
[0167] Чтобы определить эффективность ингибиторов протеасом MG 132 и Бортезомида одних и в комбинации с QC и 9АА, мы обработали HeLa клетки указанными препаратами в течение 4 часов, очистили Цитоплазматические белковые экстракты и анализировали активность протеасом, используя флюорисцирующий протеасомальынй субстрат 1 (Calbiochem, San Diego, CA).
5. Проба на электрофоретическое изменение подвижности (EMSA)
[0168] HSF1 ДНК связывающая активность детектировалась с использованием EMSA. Кратко, цитоплазматические и ядерные белковые экстракты очищены, используя Digman протокол, от контроля HeLa клеток, и HeLa клетки обработаны MG132 или 17-DMAG одними или в комбинации с QC или 9АА. 10 µг белковых экстрактов анализировали 32Р-маркированным двухцепочечным олигонуклеотидом (5' TCG-AGC-TAG-AAG-CTT-CTA-GAA-GCT-TCT-AGC 3') (последовательность №:4), специфичным для HSF1 связывания. Для конкурентного анализа 50-кратное превышение немаркированных олигонуклеотидов добавлено к белковым экстрактам вместе с 32P-меченными двухцепочечными олигонуклеотидами. Белковые экстракты предварительно инкубированы с HSF1-специфичными антителами (Assay Designs/StressGen, Victoria, BC,Canada) в течение 15 минут при комнатной температуре перед добавлением 32P-меченного двухцепочечного олигонуклеотида для выполнения анализа суперсдвига.
6. Проба на жизнеспособность клеток
[0169] Чтобы определить цитотоксичность препаратов и сочетаний лекарств использовалась проба на жизнеспособность клеток. Клетки выращены до 75-80% конфлюэнтно и затем обработаны в течение 4 часов различными комбинациями 1 мМ 17-DMAG, 0,1 мМ бортезомида и 10 мМ или 20 мМ QC. Клетки собраны трипсинизацией, и 1:50 разбавление высеяно в 6-луночную пластину. Жизнеспособность клеток определена 72 часами позже окрашиванием метиленовым синим после фиксации клеток 10%-ым формальдегидом. Метиленовый синий извлечен посредством 0,1М HCl, и его поглощательная способность измерена при 560 нм.
7. In vivo анализ роста опухоли в мышах
[0170] МСА205 и В-16 клетки извлечены из пластмассовых Чашек Петри с использованием 0,5% Трипсина- EDTA, вымыты и повторно суспендированы в стерильных PBS. Клетки введены интрадермально в обритую брюшную область C57BL/6 мышей (3×105 клеток в единственной инъекции/мышь). Опухоли измерены в двух измерениях, и объем опухоли вычислен согласно формуле: мм3 = длина опухоли × (ширина опухоли)2. На восьмой день после имплантации опухоли как правило составляли ~50 мм3 в размере. Онкологические мыши разделены на четыре группы из пяти животных каждая и начали получать внутриопухолевые инъекции лекарственного средства на 9 день. Контрольная группа получила PBS в 9, 10, 11 и 12 дни. Мышам в группе 2 введены 1,25 мг QC в PBS в 9 и 10 дни. Мыши в группе 3 получили 25 µг 17-DMAG в PBS в 9, 10, 11 и 12 дни. Мышам в группе 4 введены 1,25 мг QC+25 µг 17-DMAG в 9 и 10 дни, и 25 µг 17-DMAG в 11 и 12 дни. Только две инъекции QC сделаны, потому что это лекарственное средство является устойчивым в клетках. Оно может обнаруживаться в клетках целых 72 часа после обработки и изменения питательной среды. Опухоли измерялись каждые 2 дня после инъекций препаратов в течение 24 дней. Животные с объемом опухолей 500 мм3 и больше подвергнуты эвтаназии.
Пример 8
Комбинация неэффективных доз акрихина и местной гипертермии обеспечивает антиопухолевый эффект в модели мыши
[0171] Этот пример показывает, что объединенные неэффективные дозы акрихина и местная гипертермия имеют антиопухолевые эффекты в модели мыши. S.c. опухоли, сформированные С26 мышиным раком толстой кишки, выращены у изогенных Balb/c мышей. Когда опухоли достигли 50-150 мм3, мышей лечили пероральным приемом акрихина (500 мг/кг), или местной гипертермии (1 час - 41,5°С), или комбинацией обоих (акрихин дан за 2 часа до гипертермии). Пять дней спустя опухоли измерены, и эти результаты показаны на фиг.14 с вычислением статистического значения наблюдаемых различий. Комбинационная обработка показала ясное преимущество с точки зрения антиопухолевого эффекта по сравнению с каждой обработкой, проведенной отдельно.
Пример 9
CRBZ предотвращает экспрессию hsp70 в ответ на протеотоксический стресс (PS)
[0172] Этот пример показывает, что карбазол может предотвратить hsp70 экспрессию в ответ на протеотоксический стресс (PS). Хотя аминоакридины (АА) эффективно подавляют экспрессию hsp70 в ответ на различные индукторы PS, специфическая активность этих соединений невысока. Они являются активными в микромолярных концентрациях. Чтобы найти химикаты с лучшими возможностями, чем АА, соединения со структурой, подобной АА, анализировали. Чтобы проверить способность карбазолов (CRBZ) оказывать влияние на hsp70 экспрессию в ответ на PS, клетки обработали MG132 и переменным количеством нескольких CRBZ и анализировали экспрессию hsp70 Северным блоттингом. CRBZ номера 159 и 198 были активными в этих пробах. Выбранные соединения 159 и 198 были активными при концентрациях, начинающихся с 1 µМ (фиг.15). CRBZ 198 эффективно ингибировал HSF1-специфичную экспрессию GFP в клетках, обработанных Бортезомидом (фиг.16), а CRBZ 159 и 198 были активными в ингибировании экспрессии GFP репортера в ответ на гипертермию (фиг.17). Таким образом, CRBZ может увеличить токсичность PS с лучшими терапевтическими показателями, чем АА.
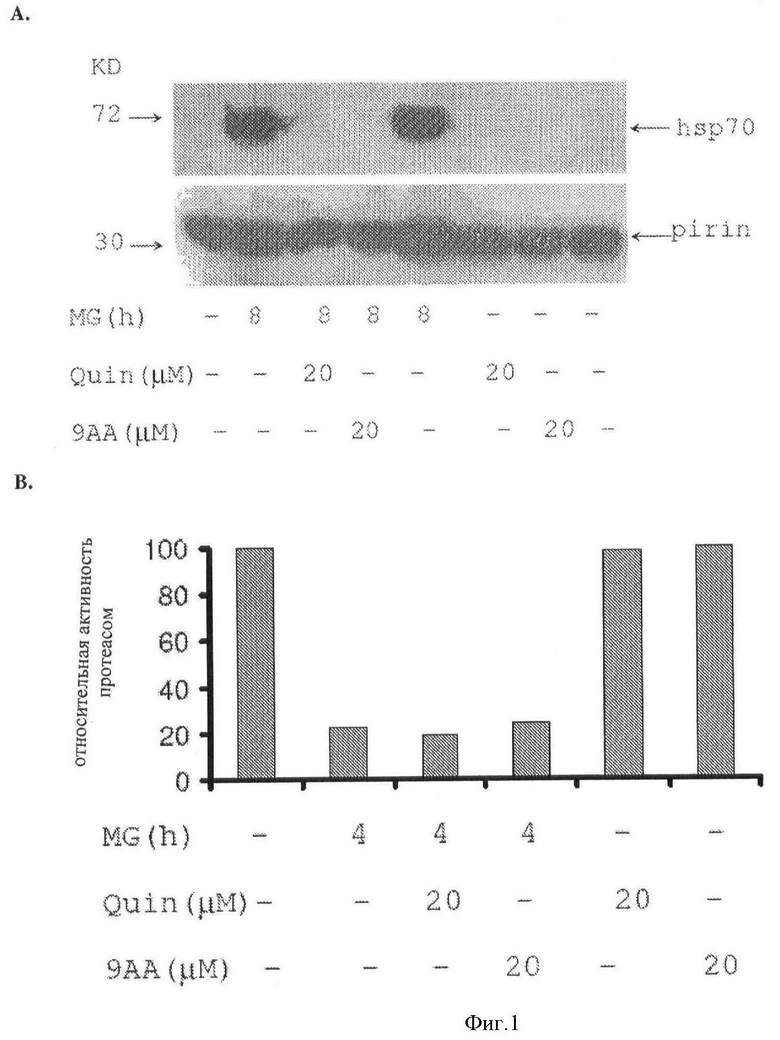
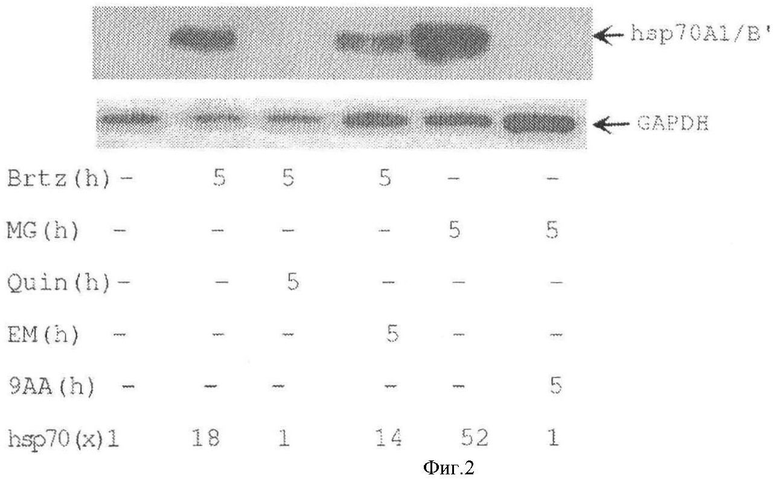
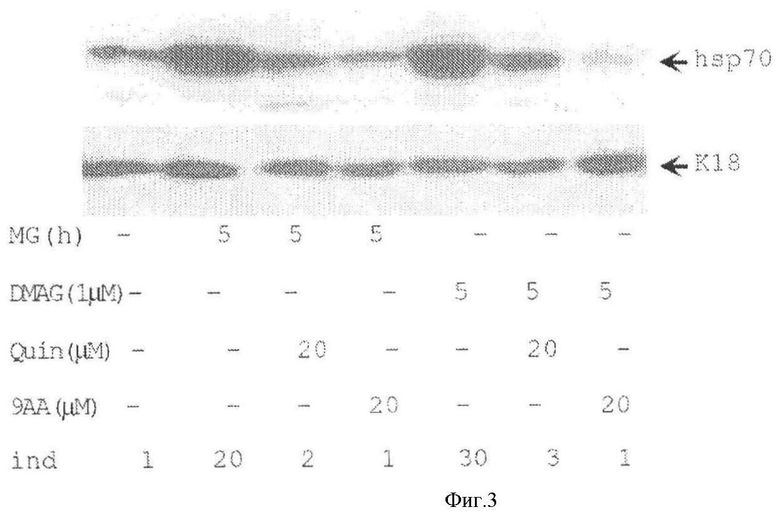
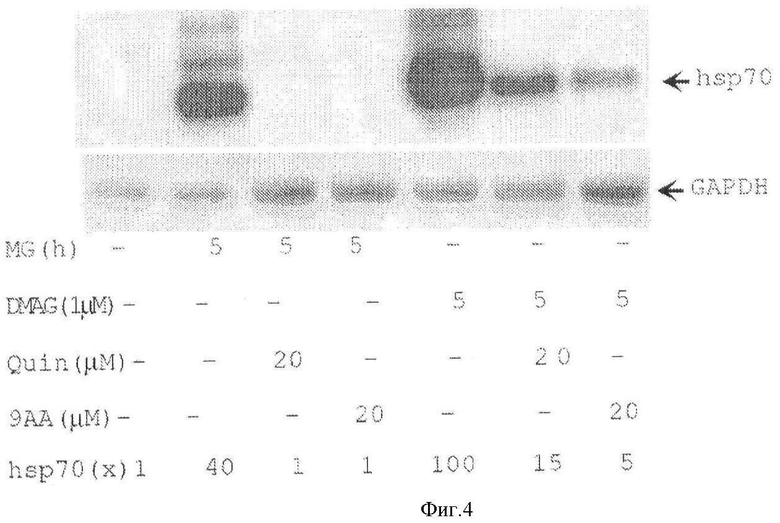
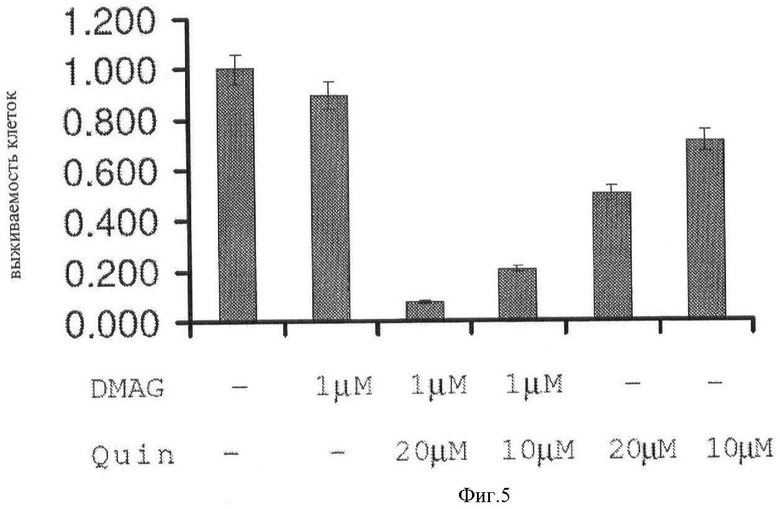
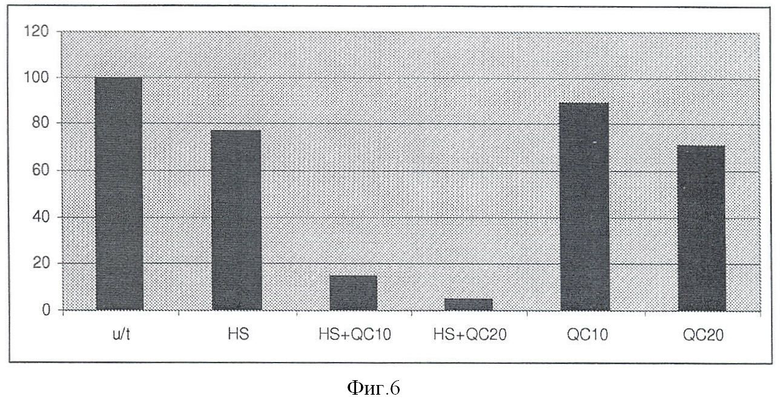
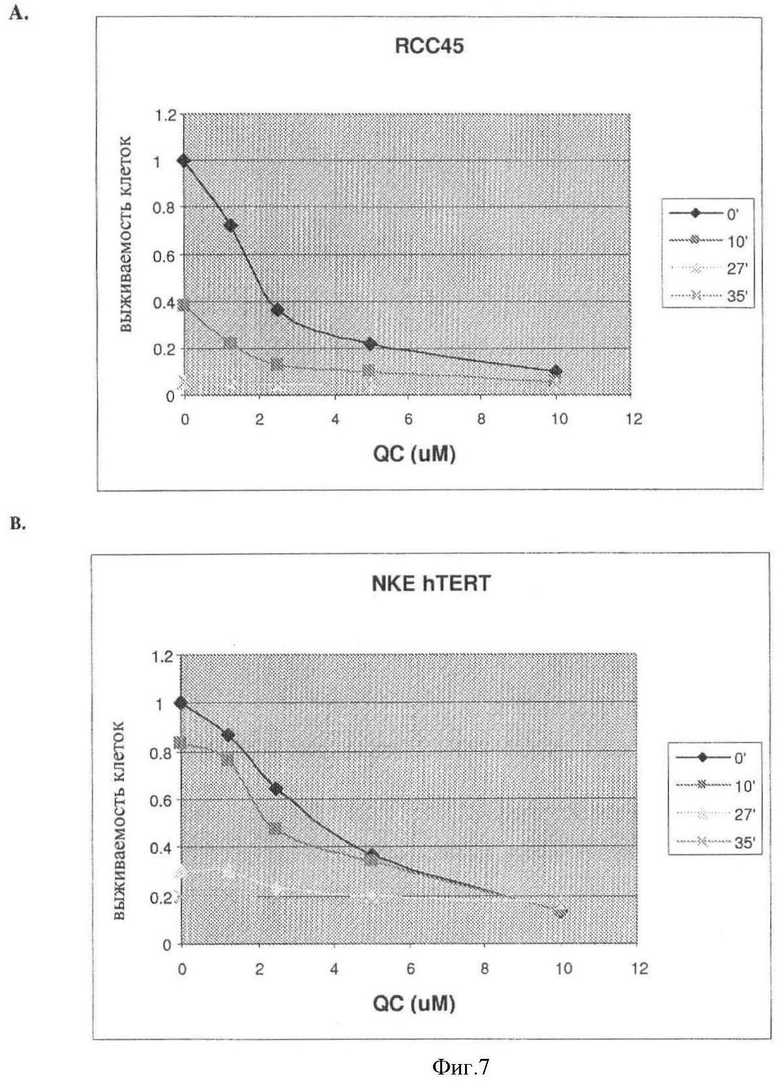
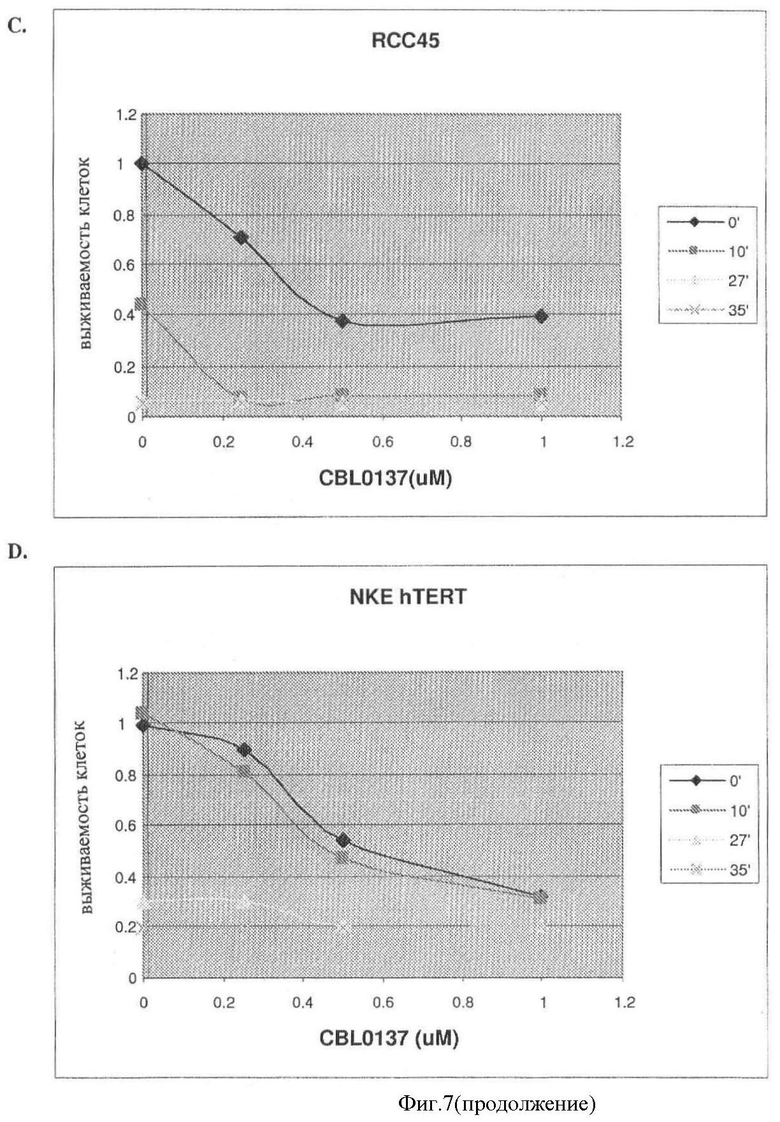
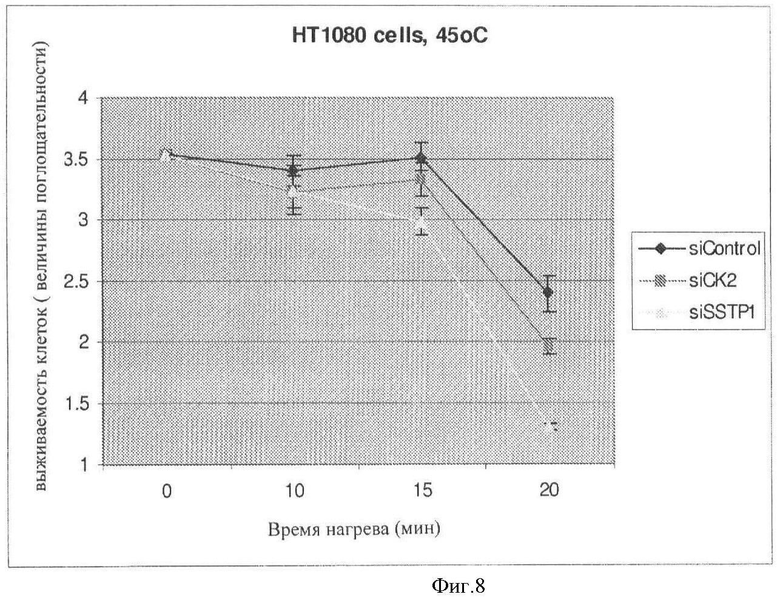
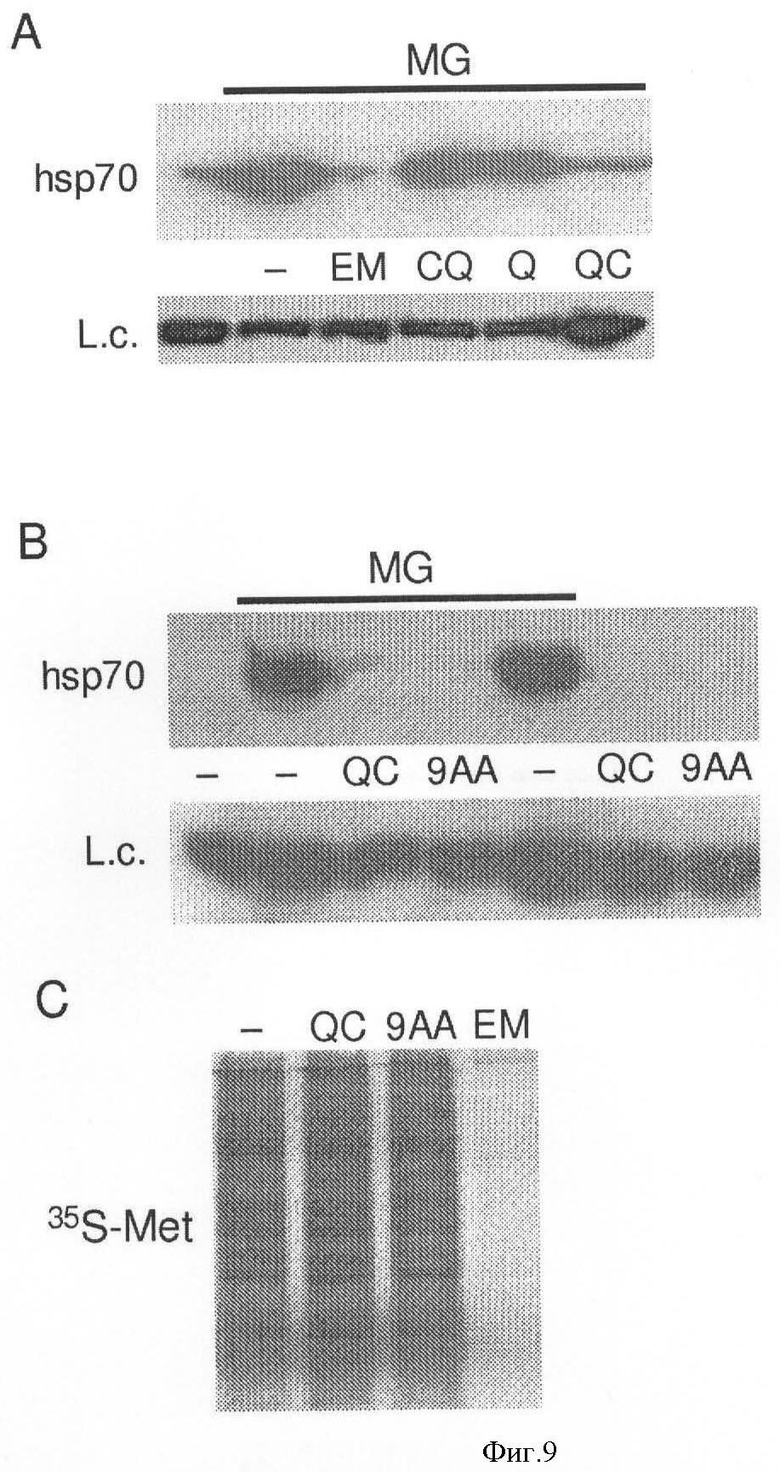
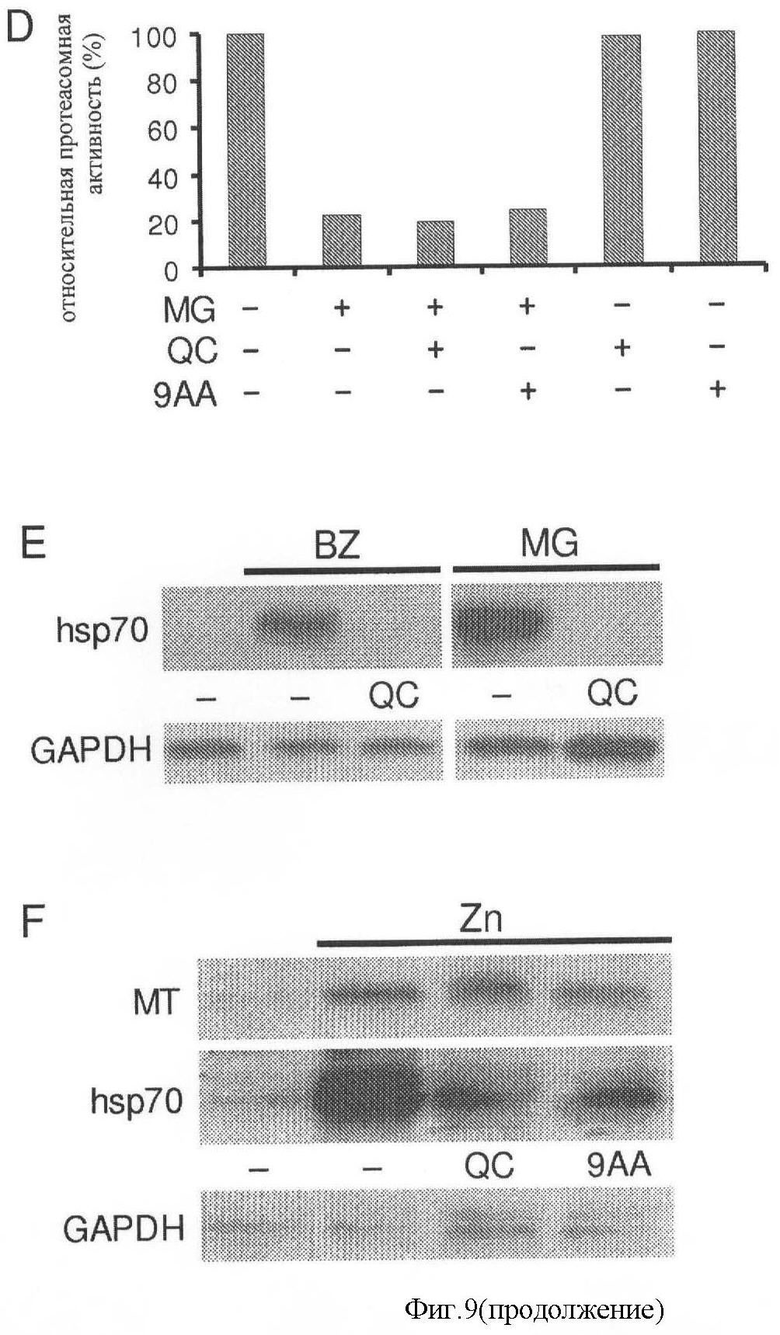
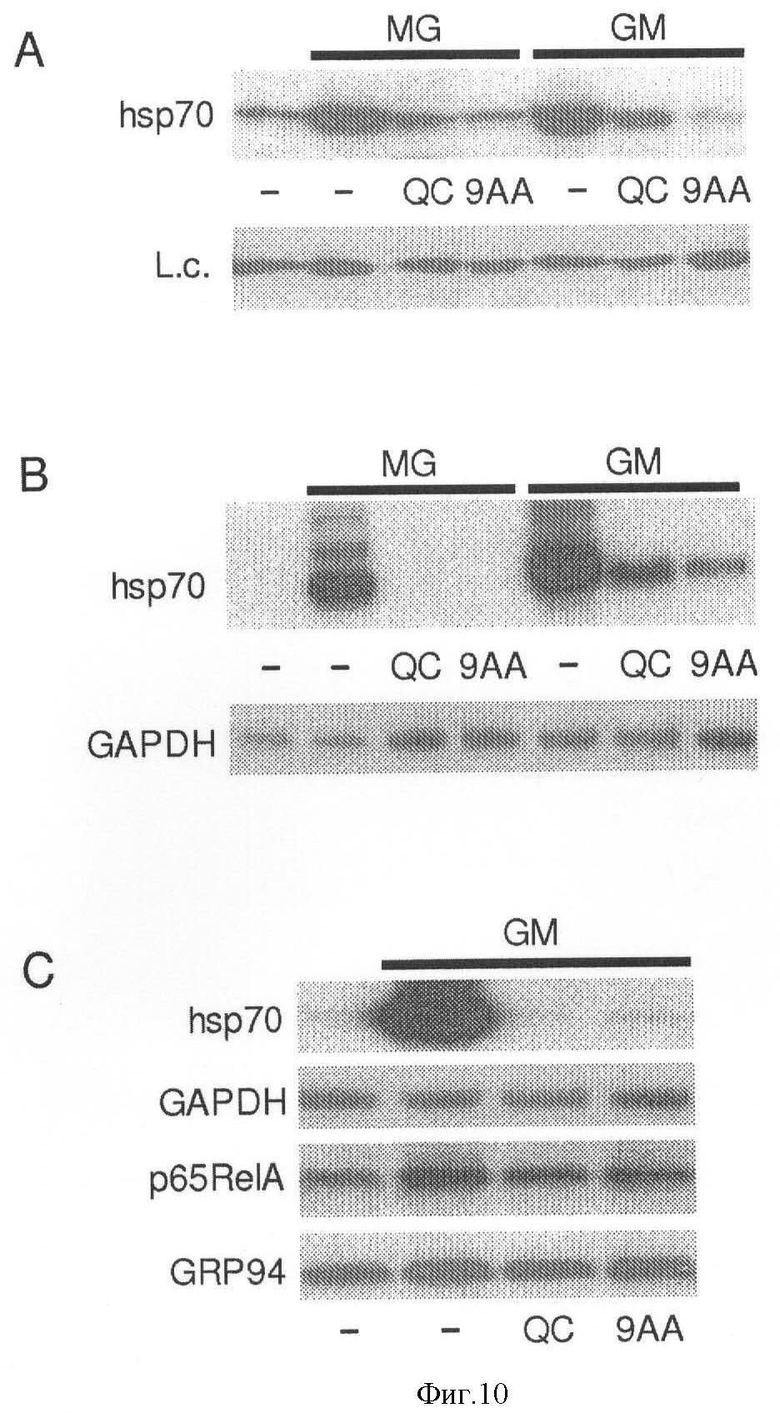
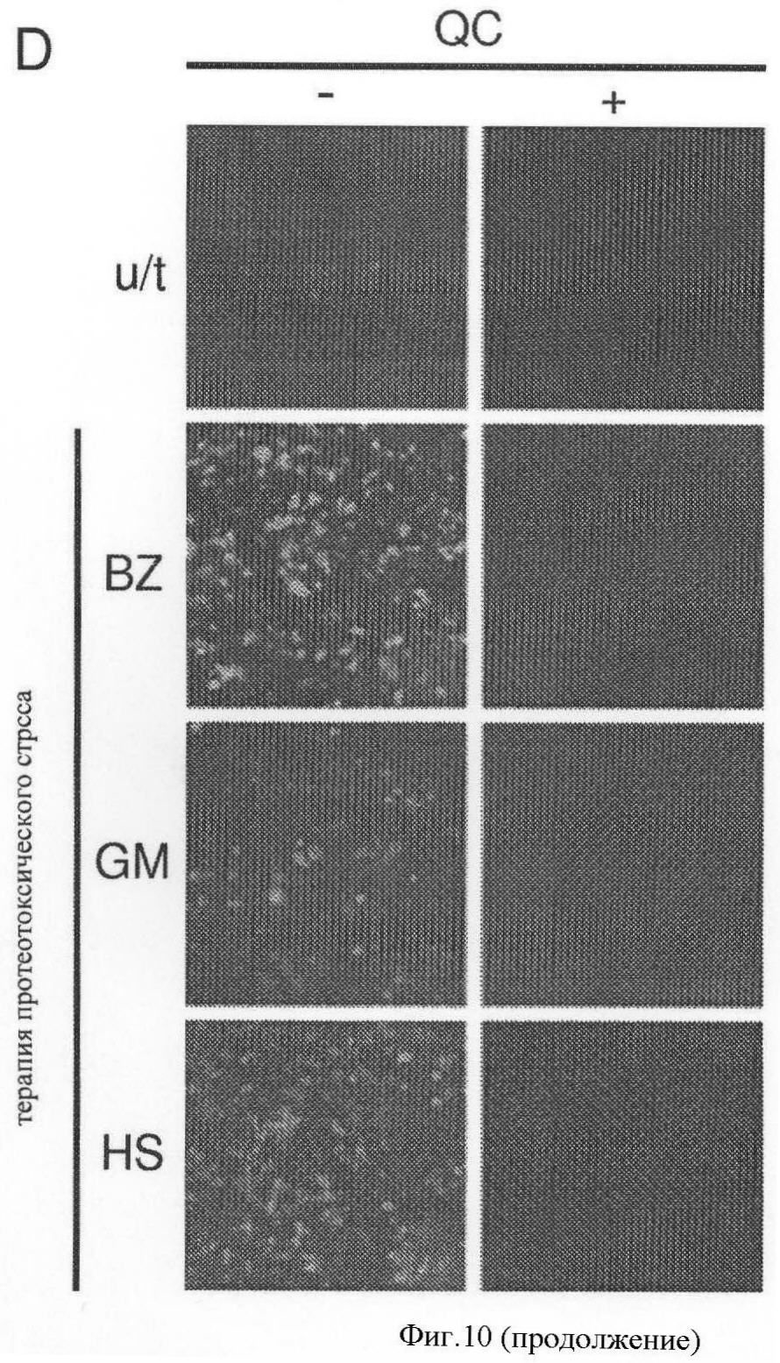
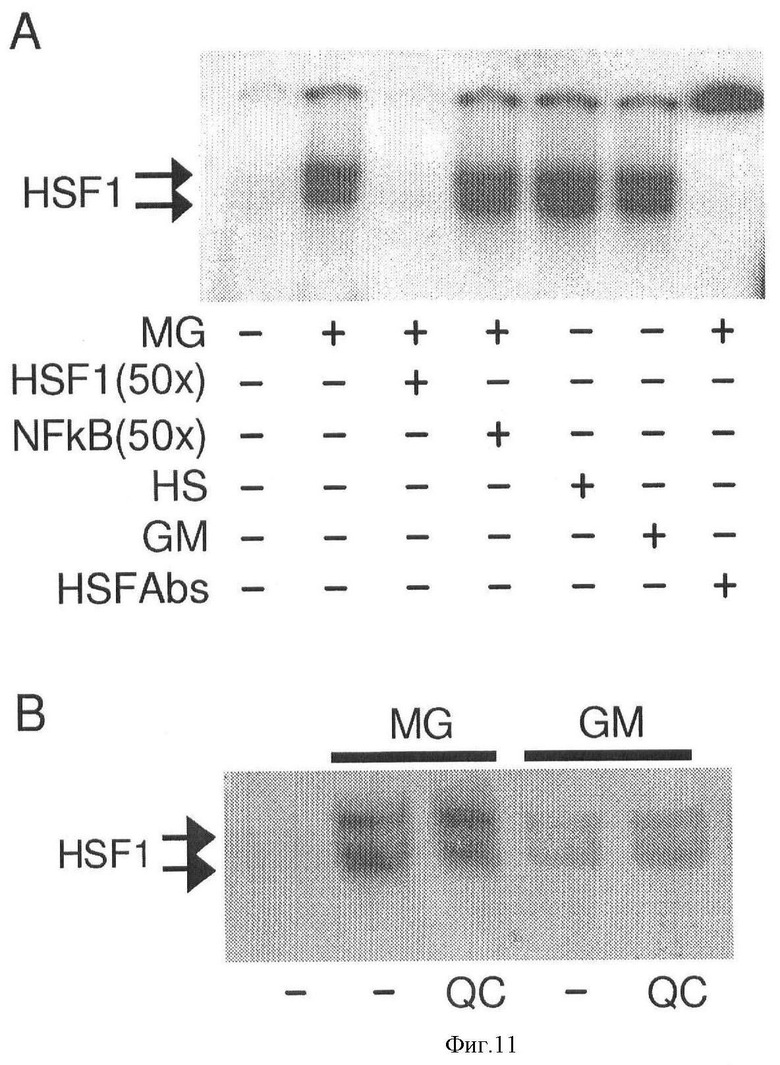
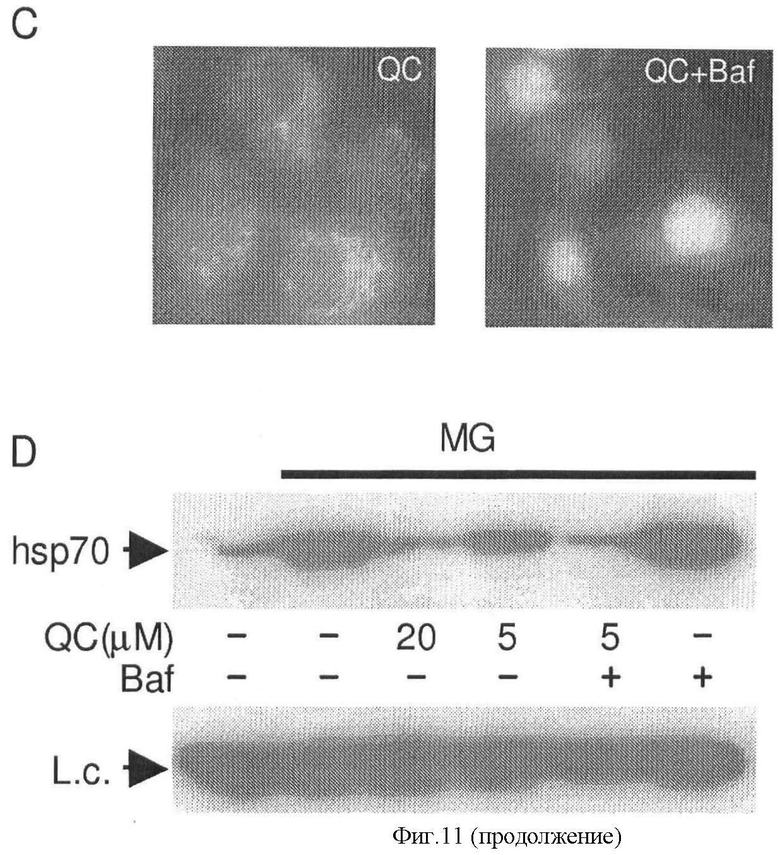
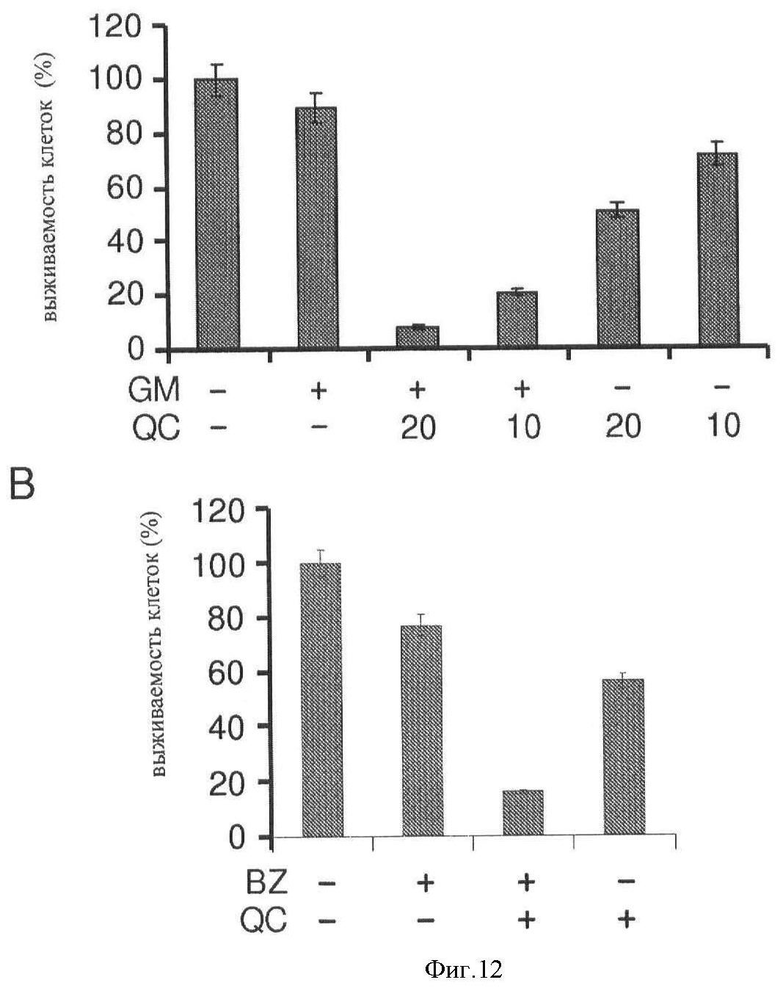
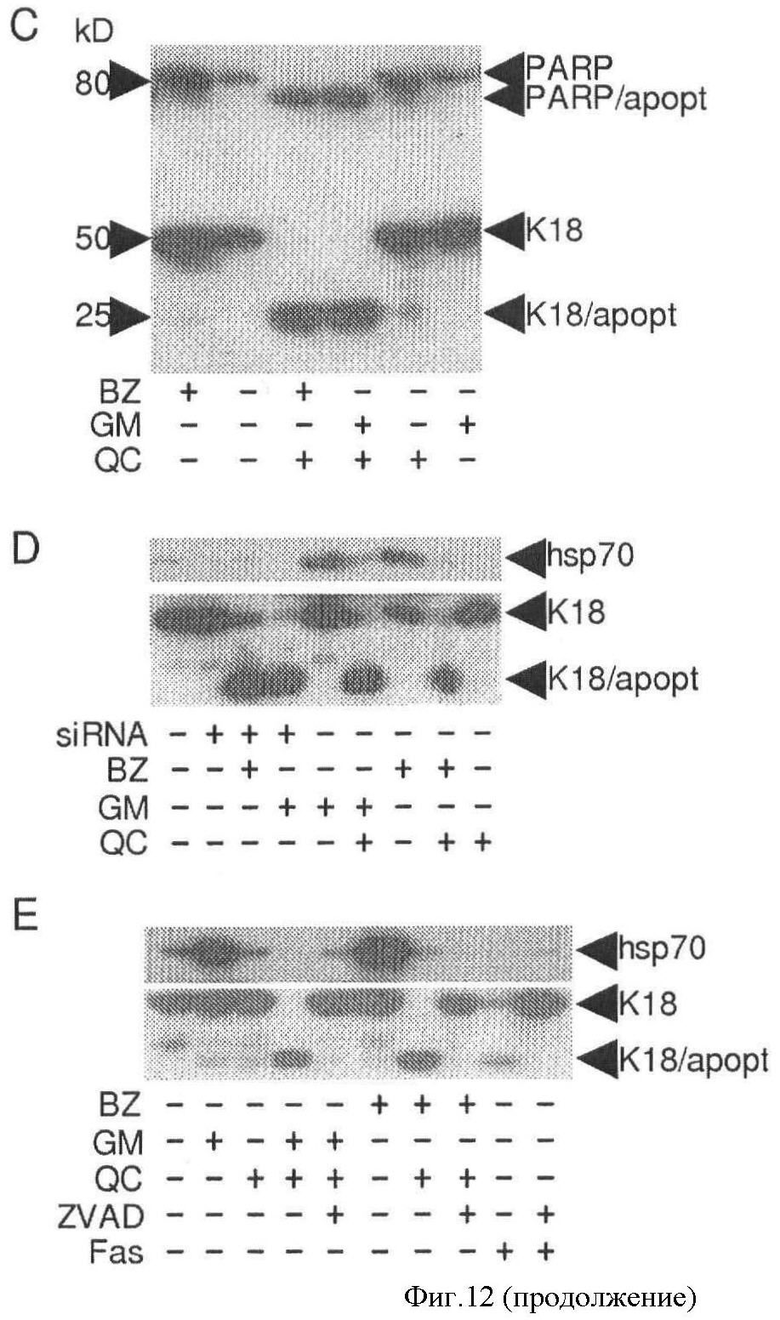

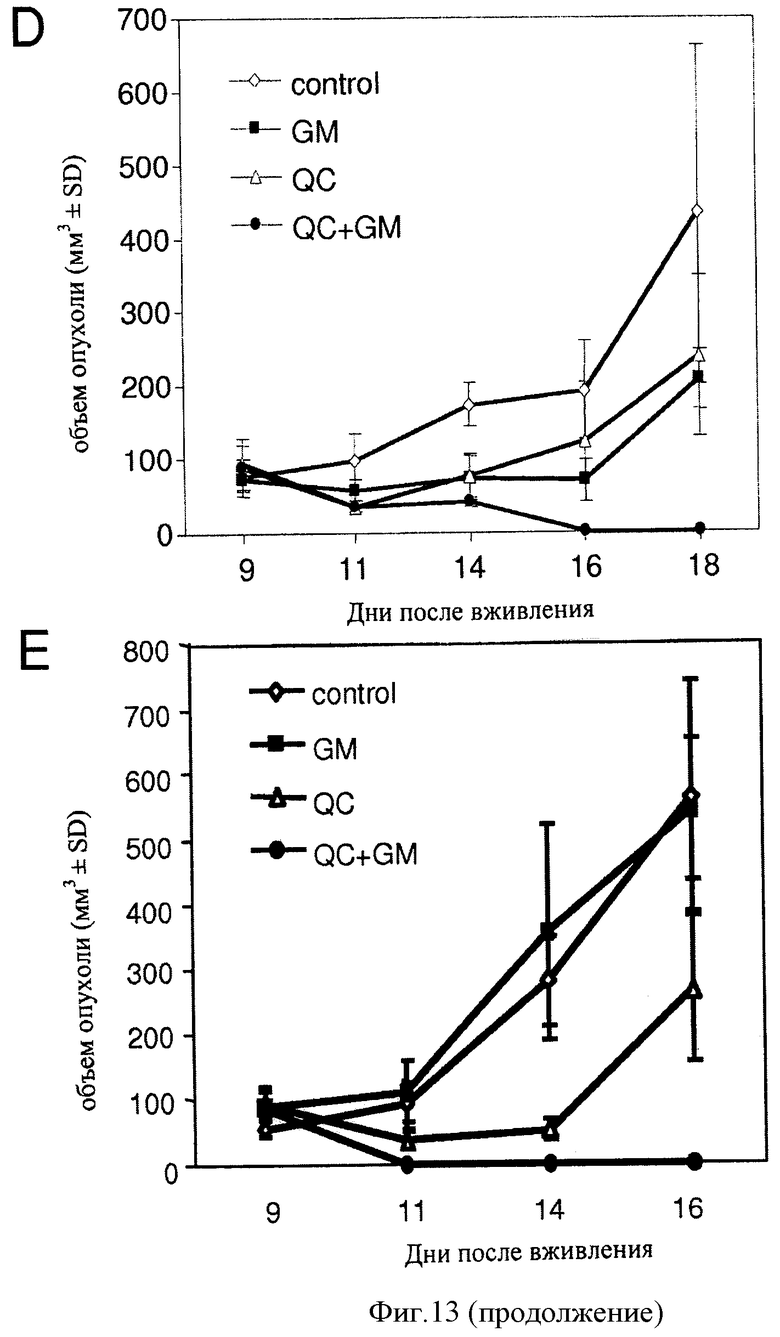
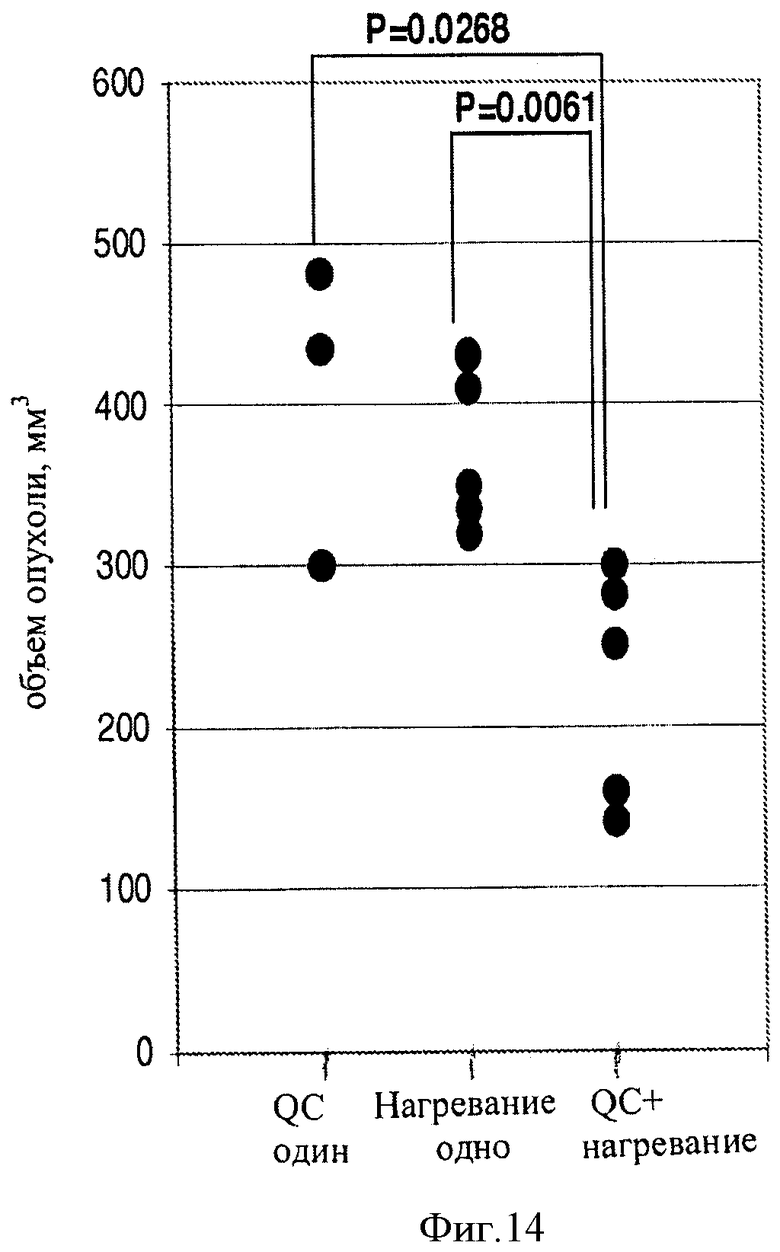
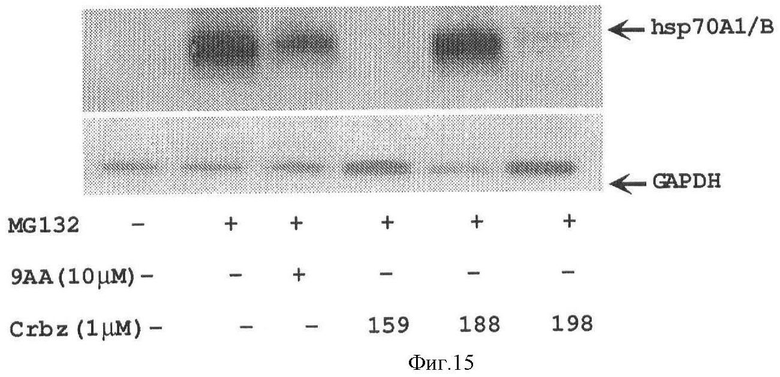
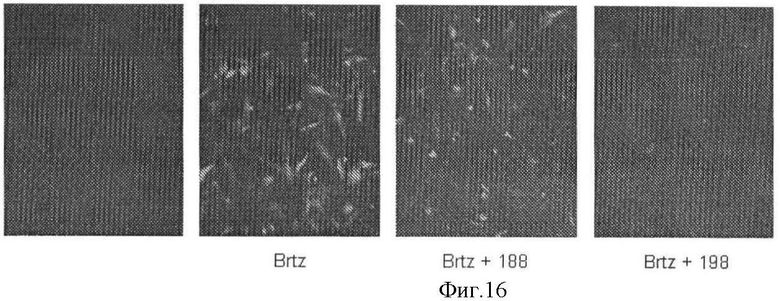

Изобретение относится к области молекулярной биологии и клеточных технологий. Заявлен способ индуцирования гибели клеток за счет индуцирования температурного шокового ответа в клетке в комбинации с ингибированием адаптивного температурного шокового ответа. Изобретение может быть использовано в медицине для предотвращения рака, лечения внутриклеточных паразитарных инфекций и связанных с воспалением состояний. 8 з.п. ф-лы, 17 ил., 9 пр.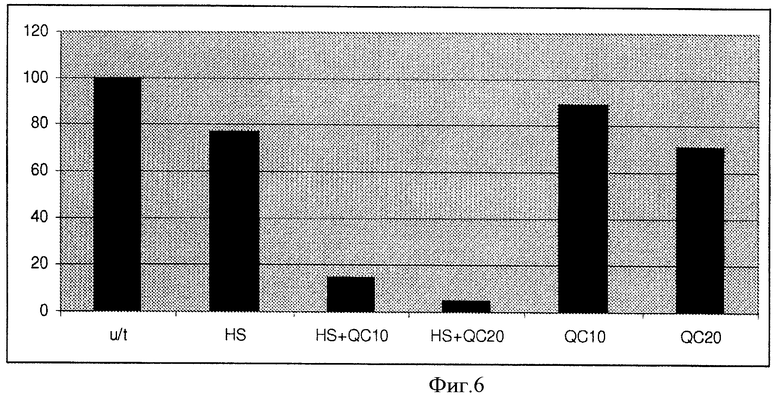
1. Способ индуцирования гибели клетки, включающий:
(a) ингибирование адаптивного температурного шокового ответа в клетке, для чего клетки обрабатывают аминоакридином или карбазолом,
(b) индуцирование температурного шокового ответа в клетке, для чего клетки обрабатывают гелданамицином, ингибитором протеасом, арсенитом, этанолом или инфракрасным излучением.
2. Способ по п.1, в котором ингибитор протеасом - это бортезомид.
3. Способ по п.1, в котором температурный шоковый ответ вызывается увеличением внутренней температуры клетки.
4. Способ по п.1, в котором карбазол выбирается из группы, содержащей CBL0137, CBL0197, CBL0198, CBL0100, CBL0159, CBL0212, СВL0174 и СВL0175.
5. Способ по п.1, в котором аминоакридин выбирается из группы, состоящей из акрихина и 9-аминоакридина.
6. Способ по п.1, в котором клетка является раковой клеткой.
7. Способ по п.6, в котором температуру в клетке увеличивают до 39-60°С.
8. Способ по п.6, в котором температуру увеличивают инфракрасным излучением.
9. Способ по п.6, в котором температуру увеличивают источником тепла, выбранным из группы, содержащей: электролюминесцентное устройство, лазерный диод, лазер, излучающий с поверхности вертикальной полости, светодиод и резистивную лампу накаливания.
| US 20020058679 A1, 16.05.2002 | |||
| US 20060252740 A1, 09.11.2006 | |||
| US 20070297980 A1, 27.12.2007. |
Авторы
Даты
2013-02-10—Публикация
2009-05-20—Подача