Изобретение относится к технологии получения основных углекислых солей цинка, которые могут быть использованы в качестве сырья и промежуточных продуктов в фармацевтике, микроэлектронике, химической, шинной, лакокрасочной и нефтеперерабатывающей промышленности.
Известен способ получения гидроксокарбонатов никеля путем растворения указанного металла в аммиачно-карбонатном растворе при повышенной температуре и последующего осаждения целевого продукта за счет отгонки аммиака, причем растворение никеля ведут в присутствии взятых по отдельности или в сочетании друг с другом азотной кислоты, нитратов аммония и никеля при содержании нитрат-иона 2-50% по отношению к массе растворенного металла [Описание изобретения к а.с. СССР №1518307 от 16.10.1987, МПК4 C01G 53/06, опубл. 30.10.1989]. Поскольку никель относится к d-металлам четвертого периода периодической системы химических элементов Д.И.Менделеева, что и цинк, настоящий способ с успехом можно распространить и на цинк.
К недостаткам настоящего способа следует отнести переменный состав готового продукта, невысокую производительность процесса, его периодичность и низкую эффективность каждой операции, наличие большого количества стоков из-за необходимости отмывки полученных осадков от нитрат-ионов. Кроме этого, технологический процесс включает стадии, протекающие при повышенной температуре, что приводит к аппаратурному усложнению способа и дополнительным энергозатратам.
Наиболее близким к предлагаемому способу по технической сущности является способ получения основных углекислых солей, в частности цинка и его оксидов, который включает растворение (как одну из стадий процесса химического превращения) металлсодержащего соединения цинка в аммиачно-карбонатном растворе (как частном случае водного раствора диоксида углерода и аммиака) с последующим образованием целевого продукта, его фильтрацию, сушку, конденсацию и возврат газообразных продуктов на стадию растворения, причем в качестве металлсодержащего соединения используют неактивный (а точнее - крупнодисперсный) оксид цинка [Описание изобретения к патенту РФ №2043301 от 25.06.1991, МПК6 C01G 3/00, C01G 3/02, C01G 9/00, C01G 9/02, C01G 51/04, C01G 51/06, C01G 53/04, C01G 53/06, опубл. 10. 90.1995]. В результате повышается производительность непрерывного технологического потока за счет интенсификации стадий процесса, обеспечивается возможность получения активных оксидов. Кроме этого, за счет улавливания газовых выбросов, регенерации жидких стоков и повторного их использования в технологическом процессе получают безотходную экологически чистую технологию.
Тем не менее, настоящий способ имеет существенные недостатки. При увеличении температуры протекания процесса моногидрат аммиака разлагается и, соответственно, изменяется концентрация карбонатно-аммиачного раствора, что приводит к непостоянству состава конечного продукта (т.н. плавающий, нестехиометрический состав). В литературе [см. статью Н.С. Николаева, В.В. Иванов, А.А. Шубин. Синтез высокодисперсных форм оксида цинка: химическое осаждение и термолиз. Journal of Siberian Federal University. Chemistry. 2010. серия 3, №2 с.160-170] отмечают существование несколько форм основного карбоната цинка, такие как Zn5(CO3)2(OH)6 (минерал гидроцинкит), Zn3CO3(OH)4, гидраты Zn3CO3(OH)4·2H2O, Zn4CO3(OH)6·2H2O. Поэтому готовый продукт представляет собой сложную смесь этих веществ.
Кроме этого, способ реализуется при температурах и давлениях, повышенных по сравнению с температурой окружающей среды и нормальным атмосферным давлением, что приводит к аппаратурному усложнению техпроцесса и дополнительным энергозатратам. На стадии отмывки готового продукта от примесных катионов и анионов требуются большое количество воды и ее последующая дорогостоящая очистка.
Также известно [см. статью Н.С. Николаева, В.В. Иванов, А.А. Шубин. Синтез высокодисперсных форм оксида цинка: химическое осаждение и термолиз. Journal of Siberian Federal University. Chemistry. 2010. серия 3, №2 с.160 и 170], что размер частиц основного карбоната цинка влияет на размер частиц оксидов, получающихся в процессе термического разложения. Процесс упаривания в настоящем способе приводит к формированию крупнокристаллических частиц карбоната и гидроксокарбоната цинка, и в результате их термолиза получаются, как показали результаты рентгенофазового анализа, крупнодисперсные частицы.
Задача, решаемая настоящим изобретением и достигаемый технический результат заключаются в получении аморфных осадков гидроксокарбоната цинка Zn5(CO3)2·(OH)6 (гексагидроксодикарбонат пентацинка) стехиометрического состава с размером частиц, не превышающим 50 нм, а также в упрощении технологического процесса, снижении энергозатрат на его осуществление и снижении экологической нагрузки на окружающую природную среду.
Для решения поставленной задачи и достижения заявленного технического результата в способе получения основных углекислых солей цинка, включающем химическое превращение металлсодержащего соединения цинка в водном растворе диоксида углерода и аммиака с последующим образованием целевого продукта, его фильтрацию, сушку, конденсацию и возврат газообразных продуктов на стадию химического превращения, причем в качестве металлсодержащего соединения используют крупнодисперсный оксид цинка, химическое превращение оксида цинка в основный карбонат цинка проводят в аммиачно-карбонатном водном растворе в гетерогенных условиях при мольном отношении диоксид углерода:аммиак равном 1:(5-9), температуре 15-50°C и атмосферном давлении.
Таким образом, способ получения основных углекислых солей цинка (Zn) включает химическое превращение (растворение) металлсодержащего соединения цинка в водном растворе диоксида углерода (CO2) и аммиака (NH3) (в аммиачно-карбонатном растворе) с последующим образованием целевого продукта, его фильтрацию, сушку, конденсацию и возврат таких газообразных веществ, как аммиак и в незначительных количествах диоксид углерода на стадию химического превращения (растворения), причем в качестве металлсодержащего соединения используют крупнодисперсный (неактивный) оксид цинка (ZnO), химическое превращение оксида цинка в основный карбонат цинка проводят в аммиачно-карбонатном водном растворе в гетерогенных условиях при мольном отношении CO2:NH3 равном 1:(5-9), температуре 15-50°C и атмосферном давлении.
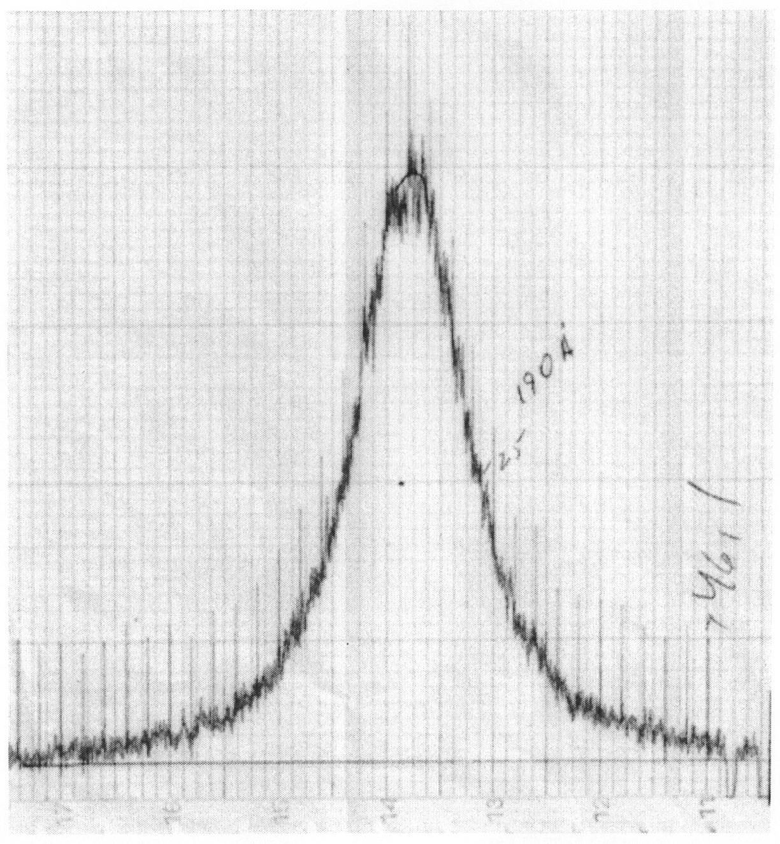
Результаты рентгенофазового анализа исходных и синтезированных соединений и продуктов их термолиза, иллюстрирующие изобретение, сведены в Таблицах 1 и 2 и представлены на дифрактограмме (см. чертеж).
Размер частиц кристаллитов ZnO определялся по уширению формы рентгеновского дифракционного профиля (см. дифрактограмму порошка ZnO). Исходя из экспериментально определенной величины истинного физического уширения линии β (полуширина дифракционных отражений от анализируемого вещества, град), можно определить средний размер кристаллитов D (нм), используя уравнение Селякова-Шеррера:
D=Kλ/βcosθHKL,
где К - коэффициент, равный 0,94 для рентгенографического анализа;
λ - длина волны рентгеновского излучения (нм);
cosθHKL - косинус угла рассеяния (безразмерная величина).
Таким образом, продуктом термолиза Zn5(CO3)2(OH)6, полученного растворением оксида цинка в водном растворе диоксида углерода и аммиака при мольном отношении CO2:NH3 равном 1:(5-9), является оксид цинка со средним размером частиц равным 10-50 нм.
Проанализируем существенные признаки изобретения.
Химическое превращение оксида цинка в основный карбонат цинка проводят в аммиачно-карбонатном водном растворе в гетерогенных условиях. В отличие от ближайшего аналога, где получают гомогенный насыщенный раствор аммиакатов цинка и его последующее выпаривание с выделением основных карбонатов цинка переменного состава, в настоящем техническом решении исходный твердый крупнокристаллический оксид цинка переводят в твердый основный карбонат цинка без получения насыщенного раствора аммиакатов цинка. Это существенно упрощает технологию за счет исключения стадий выпаривания и отмывки осадка. Кроме этого, снижается экологическая нагрузка на окружающую природную среду. Сохраняется постоянство стехиометрического состава соединения Zn5(CO3)2(OH)6 в мелкокристаллической форме с преобладанием аморфной фазы, что после его термического разложения (термолиза) позволяет получить конечный продукт с размером частиц оксида цинка 10-50 нм. Столь малые частицы обладают уникальными функциональными возможностями и используются в производстве компонентов полупроводниковых приборов, электроконтактных материалов, УФ-фильтров, солнечных батарей, сенсоров, катализаторов, сорбентов и т.д., в отличие от свойств крупнодисперсных частиц известного способа [см. патент РФ №2043301], которые не обладают такими свойствами.
Гетерогенное химическое превращение оксида цинка в основный карбонат цинка проводят в водном растворе диоксида углерода и аммиака при мольном отношении CO2:NH3 равном 1:(5-9).
При уменьшении мольного отношения CO2:NH3 растворение оксида цинка в аммиачно-карбонатном водном растворе менее 1:5, например, 1:4,5 или ниже приводит к исчезновению в осадках аморфной фазы и укрупнению частиц в кристаллической фазе, а при увеличении мольного соотношения CO2:NH3 более 1:9, например, 1:9,5 или выше значительно увеличивается время процесса превращения оксида цинка в основный карбонат цинка.
Результаты опытов по исследованию различных мольных соотношений CO3 и NH3 сведены в Таблицу 3.
Химическое превращение оксида цинка ведут при температуре 15-50°C. Температура растворения ниже 15°C, например 10°C и ниже, приводит к значительному снижению скорости процесса получения основного карбоната цинка, а повышение температуры свыше 50°C, например 55°C или выше, приводит к интенсивному разложению водного раствора моногидрата аммиака и улетучиванию газообразного аммиака, что изменяет состав карбонатно-аммиачного раствора и, как следствие, состава конечного продукта (нестехиометрический состав основных карбонатов цинка).
Химическое превращение оксида цинка ведут при атмосферном давлении. Настоящее давление обеспечивает устойчивое и безопасное протекание процесса, что также снижает энергозатраты и упрощает его реализацию на практике.
Реализацию изобретения рассмотрим на следующих примерах.
Пример 1 (сравнительный). Получение гидроксокарбоната цинка Zn5(CO3)2(OH)6 с использованием гомогенного процесса.
Процесс ведут при атмосферном давлении и температуре 25°C. В реакционную колбу на 200 мл помещается навеска оксида цинка массой 1 г и навеска гидрокарбоната аммония массой 1,18 г. Затем вносится 100 мл 0,24 М водного раствора аммиака. Включается магнитная мешалка. Перемешивание осуществляется в течении 2-х часов и раствор становится гомогенным (pH 10,57). Далее полученный раствор упаривают до 50 мл, а в реакционной колбе выпадает осадок основного карбоната цинка, который отделяют фильтрованием и сушат при 60°C в течение шести часов.
Как показали результаты рентгенофазового анализа, полученный осадок представляет собой смесь крупнокристаллических ZnCO3 и Zn5(CO3)2(OH)6, после термолиза которых получается ZnO с размером частиц более 1 мкм. Размер определялся по уширению формы рентгеновского дифракционного профиля на дифрактометре ДРОН-2 (Cu K2 - излучение, λ=1,54Å, графитовый монохроматор на отраженном луче) со скоростью сканирования 2 град/мин.
Гомогенный способ, предлагаемый в прототипе, не позволяет получить основный карбонат цинка заданного состава Zn5(CO3)2(OH)6, а также частицы оксида цинка с размером 10-50 нм.
Пример 2. Получение Zn5(CO3)2(OH)6 в гетерогенных условиях процесса превращения с мольным соотношением CO2 и NH3 - 1:1.
Процесс ведут при атмосферном давлении и комнатной температуре. Навески оксида цинка массой 2 г и гидрокарбоната аммония 0,8 г помещают в химический стакан емкостью 500 мл и добавляют 200 миллилитров дистиллированной воды (мольное соотношение CO2:NH3 - 1:1). Перемешивание реакционной смеси проводят таким образом, чтобы твердые ZnO и образованный в ходе реакции основной карбонат цинка находились во взвешенном состоянии. Время опыта составляет 24 часа. Полученный осадок фильтруют и сушат при 60°C в течение шести часов.
Результаты рентгенофазового анализа показывают, что осадок представляет собой кристаллический Zn5(CO3)2(OH)6 с большим размером частиц (см. Табл.2) от 10 до 100 мкм. Размер частиц определялся с помощью оптического микроскопа NU-2E.
Примеры 3 и 4. Получение Zn5(CO3)2(OH)6 в гетерогенных условиях процесса превращения с рекомендуемым мольным соотношением CO2 и NH3.
Процесс ведут при атмосферном давлении и комнатной температуре 20°C. Навеску оксида цинка массой 0,5 г помещают в химический стакан емкостью 200 мл и добавляют 75 миллилитров дистиллированной воды. Перемешивание реакционной смеси проводят таким образом, чтобы твердые оксид цинка и основной карбонат цинка находились во взвешенной состоянии. Далее в реакционную смесь в зависимости от варианта опыта добавляют:
- по первому варианту - 75 миллилитров бинарного водного раствора гидрокарбоната аммония (NH4HCO3) и водного раствора аммиака (NH3·H2O) с концентрациями 3,3÷10-2 М и 13,2÷10-2 М, соответственно, мольное соотношение CO2:NH3 - 1:5, время опыта составляет 24 часа;
- по второму варианту - 75 миллилитров бинарного водного раствора гидрокарбоната аммония и водного раствора аммиака с концентрациями 3,3÷10-2 М и 2,64÷10-1 М, соответственно, мольное соотношение CO2:NH3 - 1:9, время опыта составляет 48 часов.
Полученные осадки фильтруют и сушат при 60°C в течение шести часов.
Результаты рентгенофазового анализа показывают, что осадки представляют кристаллические структуры Zn5(CO3)2(OH)6 с малым размером частиц от 20 до 50 нм и значительным содержанием аморфной фазы (см. Табл.3). Размер определялся по уширению формы рентгеновского дифракционного профиля на дифрактометре ДРОН-2 (Cu K2 - излучение, λ=1,54Å, графитовый монохроматор на отраженном луче) со скоростью сканирования 2 град/мин.
Существует возможность использовать другие мольные соотношения CO2 и NH3 в пределах между 1:5 и 1:9. Полученные кристаллические структуры и их размеры также будут удовлетворять заявленным требованиям.
Пример 5. Получение Zn5(CO3)2(OH)6 в гетерогенных условиях процесса превращения в опытно-промышленных условиях.
В реактор объемом 20 литров с якорной мешалкой помещали 1 кг оксида цинка (ГОСТ 10262-73, квалификация «Ч») и 0,4 кг гидрокарбоната аммония, затем добавляли 16 л водного раствора аммиака с концентрацией 1,84 М (мольное соотношение CO2:NH3 - 1:7). Синтез проводили при температуре 20°C в течение 48 часов. Полученный осадок, после отделения от маточного раствора, сушили при 50°C в течение 24 часов. Результаты рентгенофазового анализа показывают, что осадок представляет кристаллы Zn5(CO3)2(OH)6 с малым размером частиц и значительным содержанием аморфной фазы. После его термического разложения получаются кристаллиты оксида цинка с усредненным размером 20 нм.
При реализации настоящей технологии в промышленных масштабах, например, с получением основных углекислых солей цинка в количестве до 50 кг упомянутые условия протекания способа пропорционально увеличиваются.
В результате реализации изобретения существенно упростился способ получения основных углекислых солей цинка из карбонатно-аммиачных растворов и были получены аморфные осадки гидроксокарбоната цинка стехиометрического состава и размером частиц, не превышающим 50 нм. Снизились энергозатраты на технологический процесс. Уменьшилась экологическая нагрузка на окружающую природную среду.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ УЛЬТРАДИСПЕРСНОГО ОКСИДА ЦИНКА | 2014 |
|
RU2580731C2 |
| СПОСОБ ПОЛУЧЕНИЯ ОКСИДА ЦИНКА | 2011 |
|
RU2456240C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОСНОВНЫХ УГЛЕКИСЛЫХ СОЛЕЙ МЕДИ, ЦИНКА, НИКЕЛЯ И КОБАЛЬТА И ИХ ОКСИДОВ | 1991 |
|
RU2043301C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА ДЛЯ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ ПРОЦЕССОВ | 2000 |
|
RU2172210C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА ДЛЯ НИЗКОТЕМПЕРАТУРНОЙ КОНВЕРСИИ ОКСИДА УГЛЕРОДА ВОДЯНЫМ ПАРОМ | 2006 |
|
RU2306176C1 |
| Способ приготовления медно-аммиачно-карбонатного раствора | 2017 |
|
RU2679267C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ МЕДЬЦИНКАЛЮМИНИЕВОГО КАТАЛИЗАТОРА (ВАРИАНТЫ) | 2004 |
|
RU2282496C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА ДЛЯ КОНВЕРСИИ ОКСИДА УГЛЕРОДА | 2004 |
|
RU2281162C2 |
| Ниобий-замещенный молибдат натрия-циркония и способ его получения | 2023 |
|
RU2814778C1 |
| МАЛАХИТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2003 |
|
RU2225360C1 |
Изобретение может быть использовано в химической промышленности. Способ получения основных углекислых солей цинка включает химическое превращение крупнодисперсного оксида цинка в водном растворе диоксида углерода и аммиака, последующее образование целевого продукта, его фильтрацию, сушку, конденсацию и возврат газообразных продуктов на стадию химического превращения. Химическое превращение оксида цинка в основный карбонат цинка проводят в аммиачно-карбонатном водном растворе в гетерогенных условиях при мольном отношении диоксид углерода:аммиак, равном 1:(5-9), температуре 15-50°C и атмосферном давлении. Изобретение позволяет получить аморфные осадки гексагидроксодикарбоната пентацинка Zn5(CO3)2(OH)6 стехиометрического состава с размером частиц, не превышающим 50 нм, упростить процесс, снизить энергозатраты и экологическую нагрузку на окружающую среду. 1 ил., 3 табл., 5 пр.
Способ получения основных углекислых солей цинка, включающий химическое превращение металлсодержащего соединения цинка в водном растворе диоксида углерода и аммиака с последующим образованием целевого продукта, его фильтрацию, сушку, конденсацию и возврат газообразных продуктов на стадию химического превращения, причем в качестве металлсодержащего соединения используют крупнодисперсный оксид цинка, отличающийся тем, что химическое превращение оксида цинка в основный карбонат цинка проводят в аммиачно-карбонатном водном растворе в гетерогенных условиях при мольном отношении диоксид углерода: аммиак, равном 1:(5-9), температуре 15-50°C и атмосферном давлении.
| СПОСОБ ПОЛУЧЕНИЯ ОСНОВНЫХ УГЛЕКИСЛЫХ СОЛЕЙ МЕДИ, ЦИНКА, НИКЕЛЯ И КОБАЛЬТА И ИХ ОКСИДОВ | 1991 |
|
RU2043301C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАРБОНАТА ЦИНКА ОСНОВНОГО ИЗ ВОДНЫХ РАСТВОРОВ ХЛОРСОДЕРЖАЩИХ ЦИНКОВЫХ ОТХОДОВ | 2004 |
|
RU2258672C1 |
| Способ получения основного карбоната цинка | 1985 |
|
SU1333639A1 |
| 0 |
|
SU178800A1 | |
| US 6555075 B2, 29.04.2003 | |||
| CN 102092767 A, 15.06.2011. | |||
Авторы
Даты
2013-08-20—Публикация
2012-03-15—Подача