Изобретение относится к биотехнологии и может быть использовано в производстве иммунопероксидазных конъюгатов для индикации возбудителей инфекционных заболеваний в иммуноферментном анализе (ИФА).
Ферменты - специфические белковые вещества, обладающие способностью ускорять химические реакции, имеющие слабожесткую структуру и подверженные отрицательному влиянию температурных, буферных изменений, концентрации водородных ионов и т.д. Срок их годности ограничен и составляет от 6 месяцев (для жидких препаратов, при температуре хранения минус 4°С) до 1 года (для лиофилизированных, при температуре хранения 4-6°С).
Известен способ получения иммуноферментного конъюгата, включающий активирование фермента и иммобилизацию с иммуноглобулинами [1].
Известен способ получения иммуноферментного конъюгата, включающий лиофилизацию иммунопероксидазного конъюгата в растворе бычьего сывороточного альбумина (БСА) и хранение при температуре 4°С [2].
Недостатком способов является ограниченный срок хранения - до 1 года.
Цель изобретения - увеличение срока годности иммунопероксидазного конъюгата с сохранением его физико-химических и иммунологических показателей путем подбора параметров иммобилизации фермента с матрицей.
Технический результат изобретения достигается тем, что в качестве матрицы используются липосомы (обладающие регулируемым составом, размером, поверхностными свойствами, отсутствием токсичности, не инактивирующие фермент, позволяющие функционировать с высокой активностью и т.д.), иммобилизованные с активированной пероксидазой хрена, связанные с иммуноглобулинами, очищенные от несвязавшихся компонентов.
Необходимо разработать и подобрать метод иммобилизации и определить влияние последнего на фермент. Известно, что фермент способен выполнять роль специфического катализатора при соблюдении в основном двух условий. Во-первых, фермент должен находиться в абсолютно правильной конформации. Во-вторых, он должен иметь возможность изменять свою конформацию в процессе катализа.
В качестве матрицы необходимо выбрать такую, которая бы не препятствовала проникновению к нему субстрата и «не приковывала» фермент, лишая его подвижности, необходимой для выполнения присущей ему функции.
Принимая во внимание вышеперечисленные факторы и учитывая свойства липосом, следует отметить, что наиболее подходящей матрицей для фермента-пероксидазы хрена и поставленной задачи - получение иммобилизованного иммунопероксидазного конъюгата - являются липосомы.
Природа препарата иммобилизованного фермента зависит от характера содержащей фермент фазы. Есть способ прикрепления фермента с использованием электростатических или других нековалентных механизмов связывания. С другой стороны, фермент не обязательно должен быть прикреплен к носителю, а может удерживаться внутри него. При этом носитель образует вокруг фермента сетеподобную матрицу, ячейки которой настолько малы, что молекула фермента не может освободиться из сети, но в то же время достаточно велики для проникновения низкомолекулярных субстратов [3]. Один из вариантов этого метода лежит в основе использования двойного фосфолипидного слоя в качестве ферментной фазы. В этом случае фермент может находиться в водном растворе, окруженном фосфолипидным барьером, либо быть растворенным в гидрофобной части двойного слоя.
Технология получения липосомально-иммунопероксидазного конъюгата состояла из нескольких этапов: получение липосом; включение фермента; иммобилизация с иммуноглобулинами; очистка от несвязавшихся компонентов, лиофилизация и контроль. Липосомы получены с помощью хлороформо-этанольной смеси, при этом скорость диффузии катионов через мембраны увеличивается. В качестве сырья использовали гомогенезированный мозг свиньи. После экстракции проводили отделение липидов, добавляя 20% от объема экстракта 0,9% раствора натрия хлорида. После инкубации в течение 2-3 ч липиды отделяли. Значение количества липидов колебалось от 30 до 50 мг/мл. Состав липидов определяли с помощью тонкослойной хроматографии на пластинах «Силуфол» [4].
Липиды, полученные вышеописанным способом, состояли из фосфатидилхолина, фосфатидилсерина, фосфотидилинозита и холестерина. Далее проводили выпаривание экстракта липидов на роторном испарителе для образования пленки липидов на стенках колбы. Данный этап очень важен в связи с тем, что пленка липидов должна быть достаточно тонкая, иначе происходит нежелательное включение значительного количества сухого фосфолипида в систему концентрических бислоев, так как замкнутые мембраны будут эффективно предотвращать дальнейший доступ воды и соли. Далее смывали высушенные липиды хлороформом (из расчета на 50 мг липидов 3,5 мл хлороформа), перемешивали колбу до полного растворения осадка, вносили 1,5 мл 0,9% раствора натрия хлорида и хлороформ удаляли в роторном испарителе. Определение размера липосом проводили на электронном микроскопе и рассчитывали по формуле. Размер полученных липосом составил 100-200 нм.
При получении липосомально-иммунопероксидазного конъюгата первоначально проведены исследования в плане включения фермента в липосомы. Наиболее приемлемым оказался метод включения предварительно активированной пероксидазы хрена: (5±0,1) мг пероксидазы хрена растворили в 1 мл 0,3 М раствора натрия углекислого кислого, добавили 0,025 мл 0,32% раствора формалина. Смесь перемешали на мешалке в течение (30±5) мин при температуре (22±4)°С и добавили 1 мл 0,04 М раствора перйодата натрия, продолжая перемешивать в течение (30±5) мин при температуре (22±4)°С. Далее вносили 1,0 мл 0,16 М раствора этиленгликоля (для снижения поверхностного натяжения), осторожно перемешивая в течение (60±5) мин при температуре (22±4)°С. В конце процедуры препарат активированной пероксидазы должен быть прозрачным, без запаха, зеленовато-коричневой окраски. Активированную пероксидазу переносили в диализный мешок и диализовали против 1 л 0,01 М карбонатно-бикарбонатного буфера (КББ), pH 9,5, в течение (19±1) ч на мешалке при температуре 2-8°С в холодильной камере. Таким образом, в результате активирования фермента перйодатным окислением, образовывались альдегидные группы.
Дальнейший этап получения комплекса липосомально-иммунопероксидазного конъюгата заключался в следующем. К 5 мг окисленной перйодатным методом пероксидазы добавляли 1 мл суспензии липосом в 0,01 М КББ pH 9,5. Суспензию подвергали ультразвуковой обработке (44 кГц) в течение 1 мин, далее инкубировали 1 ч. К липосомам, иммобилизованным пероксидазой хрена, добавляли туляремийные иммуноглобулины (Ig G) в количестве от 2,5 до 10 мг на 3 мл 0,01 М КББ pH 9,5. Иммобилизацию иммуноглобулинов с активированной пероксидазой хрена проводили при температуре (22±4)°С, помешивая на шуттеле в течение 2 ч, стабилизировали 5 мг боргидрида в холодильнике при температуре (4-6)°С. Вероятно, при этом пероксидаза включалась в мембрану липосом, а альдегидные группы углеводной части фермента взаимодействовали с аминогруппами иммуноглобулинов.
Для очистки конъюгата от несвязавшегося фермента использовали гель-хроматографию. Конъюгат наносили на колонку 100×12 мм с сефадексом G-100, уравновешенную 0,1 М раствором ФСБ pH 7,2. В результате происходило фракционирование исходной смеси молекул на зоны в зависимости от их размеров. Поэтому в первом пике выходил липосомально-иммунопероксидазный конъюгат, далее несвязавшиеся иммуноглобулины и фермент. Элюцию проводили тем же буферным раствором, фракции собирали по 2,0 мл и исследовали в иммуноферментном анализе (ИФА).
В результате установлено, что обязательным условием получения качественного препарата является активирование фермента при оптимальном времени иммобилизации 2 ч и концентрации белка иммуноглобулинов 5 мг/мл.
Для увеличения срока годности препарат разливали в ампулы, предварительно добавив к нему 1% БСА, замораживали и лиофилизировали в течение (18±2) ч до конечной температуры 25°С. В готовом препарате контролировали физико-химические (растворимость, цветность, прозрачность, потерю в массе при высушивании) и иммунологические (активность, специфичность, чувствительность) свойства после лиофилизации и в процессе хранения в течение 6 лет (срок наблюдения). Чувствительность и специфичность конъюгата определяли в ИФА с гомологичными и гетерологичными штаммами по методике Dark M.F., Adams A.N. [5].
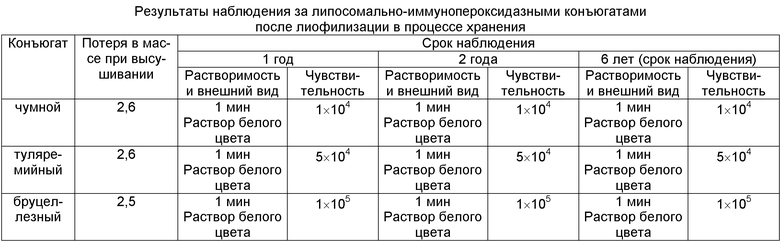
В таблице представлены результаты анализов физико-химических свойств и чувствительности препаратов. Разработанные препараты удовлетворяют требованиям нормативных документов, предъявляемым к диагностическим препаратам, а их стабильность превосходит традиционные иммуноферментные конъюгаты в 6 раз (срок наблюдения).
Таким образом, в результате проведенных исследований разработана технология изготовления иммобилизованного ферментного препарата, значительно увеличивающая его стабильность. Это связано с тем, что иммобилизация эффективно препятствует вредному воздействию внешней среды на ферментный препарат, он становится заключенным в матрицу (липосомы), т.е. защищенным, при отсутствии физических и каталитических ограничений, при этом матрица не препятствует проникновению к нему субстрата за счет эффективного метода получения липосом, включения фермента и иммобилизации антител, подбора температурных, временных параметров, проведения щадящей очистки от несвязавшихся компонентов.
Возможность практического применения заявляемого способа иллюстрируется примерами его конкретного выполнения с использованием совокупности заявляемых признаков.
Пример 1. Получение чумного липосомально-иммунопероксидазного конъюгата и его контроль в ИФА
Предварительно проводили активирование пероксидазы хрена: (5±0,1) мг пероксидазы хрена растворяли в 1 мл 0,3 М раствора натрия углекислого кислого, добавляли 0,025 мл 0,32% раствора формалина. Смесь перемешивали на мешалке в течение (30±5) мин при температуре (22±4)°С и добавляли 1 мл 0,04 М раствора перйодата натрия, продолжая перемешивать в течение (30±5) мин при температуре (22±4)°С. Далее вносили 1,0 мл 0,16 М раствора этиленгликоля, осторожно перемешивая в течение (60±5) мин при температуре (22±4)°С. Активированную пероксидазу переносили в диализный мешок и диализовали против 1 л 0,01 М раствора КББ pH 9,5 в течение (19±1) ч на мешалке при температуре 2-8°С в холодильной камере.
Получение комплекса липосомалыю-иммунопероксидазного конъюгата проводили следующим образом: к 5 мг окисленной перйодатным методом пероксидазы добавляли 1 мл суспензии липосом в 0,01 М растворе КББ pH 9,5. Суспензию подвергали ультразвуковой обработке в течение 1 мин, далее инкубировали 1 ч. К липосомам, иммобилизованным пероксидазой хрена, добавляли чумные иммуноглобулины (Ig G) в количестве 5 мг на 3 мл 0,01 М КББ pH 9,5. Иммобилизацию иммуноглобулинов с активированной пероксидазой хрена проводили при температуре (22±4)°С, помешивая на шуттеле в течение 2 ч, стабилизировали 5 мг боргидрида натрия в холодильнике при температуре (4-6)°С в течение 2 ч. Для очистки конъюгата от несвязавшегося фермента использовали гель-хроматографию. Конъюгат наносили на колонку с сефадексом G-100, уравновешенную 0,1 М раствором ФСБ pH 7,2. В результате происходило фракционирование исходной смеси молекул на зоны в зависимости от их размеров. В первом пике выходил конъюгат, далее несвязавшиеся иммуноглобулины и фермент. Элюцию проводили тем же буферным раствором. Активность проверяли в ИФА. Препарат разливали в ампулы, предварительно добавив к готовому препарату 1% БСА, замораживали и лиофилизировали в течение (18±2) ч до конечной температуры 25°С. В готовом препарате контролировали физико-химические и иммунологические свойства после лиофилизации и в процессе хранения. Чувствительность конъюгата в ИФА с гомологичными штаммами составила 1×104 м.к./мл, при отсутствии перекрестных реакций с гетерологичными штаммами. Срок годности препарата - 6 лет (срок наблюдения).
Пример 2. Получение туляремийного липосомально-иммунопероксидазного конъюгата и его контроль в ИФА
Получали аналогично примеру 1, только вместо чумных использовали туляремийные иммуноглобулины. Чувствительность конъюгата в ИФА с гомологичными штаммами составила 5×104 м.к./мл, при отсутствии перекрестных реакций с гетерологичными штаммами. Срок годности препарата - 6 лет (срок наблюдения).
Пример 3. Получение бруцеллезного липосомально-иммунопероксидазного конъюгата и его контроль в ИФА
Получали аналогично примеру 1, только вместо чумных использовали бруцеллезные иммуноглобулины. Чувствительность конъюгата в ИФА с гомологичными штаммами составила 1×105 м.к./мл, при отсутствии перекрестных реакций с гетерологичными штаммами. Срок годности препарата - 6 лет (срок наблюдения).
Источники информации
1. Nakane, P.K. Peroxidase-labelled antibody - a new method of conjugation / P.K.Nakane, A.Kawaoi // J. Histochem. Cytochem. - 1974. - Vol.22. - P.506-508.
2. Патент РФ №2276362, опубл. 10.05.2006, «Способ выявления вируса крымской геморрагической лихорадки (КГЛ) в биологическом и полевом материале», авторы Василенко Н.Ф., Ефременко В.И., Тюменцева И.С. и др. Бюл. №13.
3. Тривен М. Иммобилизованные ферменты. - М.: Мир, 1983. - С.23.
4. Кейтс М. Техника липидологии. М.: Мир, 1975. - С.68-82.
5. Clark M.F., Adams A.N. Characteristics of the microplate method of enzyme-linked immunosorbent assay for the detection of plant virus // J. Gen. Virol. - 1977. - V.36, №3. - P.475-480.
| название | год | авторы | номер документа |
|---|---|---|---|
| ДИАГНОСТИЧЕСКАЯ ТЕСТ-СИСТЕМА ДЛЯ ВЫЯВЛЕНИЯ ВИРУСА ГРИППА ПТИЦ А/Н5N1 | 2006 |
|
RU2339694C2 |
| СПОСОБ ВЫЯВЛЕНИЯ ВИРУСА КРЫМСКОЙ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ (КГЛ) В БИОЛОГИЧЕСКОМ И ПОЛЕВОМ МАТЕРИАЛЕ | 2004 |
|
RU2276362C1 |
| СПОСОБ КОНСЕРВАЦИИ ИММУНОПЕРОКСИДАЗНОГО КОНЪЮГАТА | 2014 |
|
RU2549971C1 |
| ДИАГНОСТИЧЕСКАЯ ТЕСТ-СИСТЕМА ДЛЯ ВЫЯВЛЕНИЯ ВИРУСА ГЕПАТИТА А | 1992 |
|
RU2065164C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОМАГНОИММУНОСОРБЕНТА ДЛЯ ОБНАРУЖЕНИЯ БАКТЕРИАЛЬНЫХ АНТИГЕНОВ (ВАРИАНТЫ) | 2003 |
|
RU2271540C2 |
| СПОСОБ ПРОВЕДЕНИЯ ИММУНОФЕРМЕНТНОГО АНАЛИЗА (ИФА) | 2005 |
|
RU2290641C1 |
| Способ получения моноклонального пероксидазного конъюгата для идентификации типичных и атипичных штаммов Vibrio cholerae O1, включая и R-варианты в дот-ИФА | 2022 |
|
RU2800470C1 |
| КОНЬЮГАТ ДЛЯ ИММУНОФЕРМЕНТНОГО АНАЛИЗА И СПОСОБ ИММУНОФЕРМЕНТНОГО АНАЛИЗА | 1992 |
|
RU2014610C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛАТЕКСНЫХ АНТИГЕННЫХ ДИАГНОСТИКУМОВ ДЛЯ ВЫЯВЛЕНИЯ АНТИТЕЛ ПРОТИВ ВОЗБУДИТЕЛЕЙ БРУЦЕЛЛЕЗА, ТУЛЯРЕМИИ | 2021 |
|
RU2777803C1 |
| КОМПЛЕКСНАЯ ТЕСТ-СИСТЕМА ИММУНОФЕРМЕНТНОГО АНАЛИЗА (ИФА) ДЛЯ ОПРЕДЕЛЕНИЯ УРОВНЯ АНТИТЕЛ К ВИРУСНЫМ РЕСПИРАТОРНЫМ ЗАБОЛЕВАНИЯМ КРУПНОГО РОГАТОГО СКОТА | 2008 |
|
RU2371726C1 |
Изобретение относится к области биохимии. Используют липосомы в качестве матрицы для активированного фермента - пероксидазы хрена. К 5 мг окисленной перйодатным методом пероксидазы хрена добавляют 1 мл суспензии липосом в 0,01 М растворе карбонатно-бикарбонатного буфера при рН 9,5. Подвергают ультразвуковой обработке в течение 1 мин. Инкубируют 1 ч. Иммобилизуют с иммуноглобулинами в концентрации 5 мг в течение 2 ч при температуре 22±4°С. Стабилизируют 5 мг боргидрида натрия с последующей гель-хроматографической очисткой. Изобретение позволяет получить липосомально-иммунопероксидазный конъюгат для индикации возбудителей инфекционных заболеваний в иммуноферментном анализе и увеличить срок годности препарата до 6 лет. 1 табл., 3 пр.
Способ получения липосомально-иммунопероксидазного конъюгата для индикации возбудителей инфекционных заболеваний в иммуноферментном анализе, характеризующийся тем, что в качестве матрицы для активированного фермента - пероксидазы хрена - используют липосомы, при этом к 5 мг окисленной перйодатным методом пероксидазы хрена добавляют 1 мл суспензии липосом в 0,01 М растворе карбонатно-бикарбонатного буфера при рН 9,5, подвергают ультразвуковой обработке в течение 1 мин, инкубируют 1 ч, иммобилизуют с иммуноглобулинами в концентрации 5 мг в течение 2 ч при температуре 22±4°С, стабилизируют 5 мг боргидрида натрия с последующей гель-хроматографической очисткой.
| СПОСОБ ВЫЯВЛЕНИЯ ВИРУСА КРЫМСКОЙ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ (КГЛ) В БИОЛОГИЧЕСКОМ И ПОЛЕВОМ МАТЕРИАЛЕ | 2004 |
|
RU2276362C1 |
| ДИАГНОСТИЧЕСКАЯ ТЕСТ-СИСТЕМА ДЛЯ ВЫЯВЛЕНИЯ ВИРУСА ГРИППА ПТИЦ А/Н5N1 | 2006 |
|
RU2339694C2 |
| Жарникова И.В | |||
| Разработка и применение иммобилизованных систем для экспресс-диагностики различных заболеваний//ВЕСТНИК РОССИЙСКОЙ ВОЕННО-МЕДИЦИНСКОЙ АКАДЕМИИ | |||
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| ЭПИТОПЫ, ОБРАЗОВАННЫЕ НЕКОВАЛЕНТНЫМ СВЯЗЫВАНИЕМ КОНЪЮГАТОВ | 2000 |
|
RU2259194C2 |
Авторы
Даты
2013-12-10—Публикация
2012-10-15—Подача