Изобретение относится к медицине, а именно к фармакологии и клинической фармакологии и предназначено для внедрения в практику фармаколога и клинического фармаколога с целью прогнозирования возможной принадлежности изучаемых лекарственных препаратов к субстратам эффлюксиого белка-транспортера гликопротеипа-Р (Pgp). а также использования финастерида в качестве положительного контроля повышенной активности Pgp при поиске веществ аналогичного действия.
Pgp - это АТФ-зависимый эффлюксный транспортер с широкой субстратной специфичностью, контролирующий фармакокинетику различных соединений в физиологических и патологических условиях, препятствующий проникновению и ускоряющий выведение липофильных веществ через цитоплазматическис мембраны различных клеток [1].
Известен способ моделирования состояния индукции функциональной активности Pgp в клинике на добровольцах с целью исследования возможного участия белка-транспортера в фармакокинетике раиитидина путем введения рифамиицина в дозе 600 мг один раз в день в течение 7 дней [2]. Рифамиицин в дозе 300 мг дважды в день в течение 7 дней был предложен в качестве модели повышенной активности Pgp па добровольцах с целью его использования в качестве положительного контроля при поиске потенциальных индукторов транспортера [3].
Известен способ моделирования индукции функциональной активности Pgp на пациентах больных шизофренией, введением препаратов зверобоя продырявленного с целью исследования на этом фоне фармакокинетики атипичного нейролептика клозапина [4].
Известен способ моделирования состояния индукции Pgp в эксперименте у крыс с целью создания положительного контроля повышенной функциональной активности белка-транспортера путем двухнедельного пероралыюго введения животным экстракта зверобоя продырявленного в дозе 15 мг/кг в день [5].
Однако рифамиицин как индуктор, применяемый в клинической практике, характеризуется значительной токсичностью [6], а именно нежелательным действием на печень, почки, желудочно-кишечный тракт, систему кроветворения, развитием аллергических реакций. Исследования на добровольцах сопряжены с этическими проблемами, требуют получения разрешения в этическом комитете, госпитализации добровольцев в отделение реанимации для круглосуточного контроля за состоянием и почасового забора крови многократно в течение суток. Препараты растительного происхождения характеризуются сложностью дозирования, связанной с проблемой их стандартизации. Крысы как объект исследования (тест-система) не пригодны для оценки функциональной активности Pgp одним из современных, информативных и распространенных методов - путем анализа фармакокинстики маркерных субстратов белка-транспортера.
Известен способ моделирования состояния индукции функциональной активности Pgp па культуре клеток LS-180 с целью анализа возможного влияния активности Pgp па развитие болезни Альцгеймера путем введения рифампицина, дексаметазона, верапамила, гинерфорипа, β-эстрадиола и нентилентетразола [7].
Однако работа с культурой клеток сопряжена со значительными техническими и методическими сложностями, требует дорогостоящего лабораторного оборудования, поэтому методика не доступна большинству лабораторий.
Не было обнаружено информации о применении финастерида с целью моделирования состояния индукции активности Pgp у кроликов.
Финастерид-4-азо-3-оксостероид, ингибитор 5α-редуктазы II типа, фермента, локализованного на ядерной мембране клеток и трансформирующего тестостерон в дигидротестостерон - ключевой апдроген, ответственный за развитие доброкачественной гиперплазии предстательной железы и андрогенной аллопеции. Финастерид распределяется но всему организму, однако в связи со специфичностью действия вещества на 5α-редуктазу, которая в высоких концентрациях содержится лишь в ткани предстательной железы, коже головы и половых органов, побочные эффекты со стороны других систем организма у мужчин проявляются редко [8], а у женщин практически не будут выражены в связи с низкой активностью фермента в женском организме.
Целью изобретения являлось создание такой модели индукции функциональной активности Pgp, которая не создавала бы этических проблем, не сопровождалась проявлением побочных эффектов вводимого вещества при исследовании на добровольцах, а при изучении на животных была бы методически обоснована и не требовала дорогостоящего лабораторного спецоборудования, материалов и комплектующих для проведения исследований на культурах клеток.
Поставленная задача достигается тем, что в качестве индуктора Pgp выбран ингибитор 5α-редуктазы - финастерид, безопасный и экономически доступный препарат, который вводится перорально один раз в день 14-дневным курсом в дозе 0,225 мг/кг массы в форме суспензии в оливковом масле, а в качестве адекватной и удобной тест-системы используются кролики.
Описание способа
Для решения поставленной задачи нами выполнен эксперимент на 6 половозрелых кроликах-самцах породы Шиншилла, средней массой 3500-4300 г. Финастерид вводился животным в течение 14 дней внутрижелудочно в дозе 0,225 мг/кг массы тела в форме суспензии в оливковом масле. Функциональную активность Pgp определяли путем анализа динамики плазменной концентрации фексофенадина, маркерного субстрата белка-транспортера. Фексофенадин был выбран в качестве примера субстратов Pgp в связи с тем, что его фармакокииетика зависит исключительно от функционароваиия Pgp.
Фексофенадин (Препарат Телфаст 180 мг; производитель: Aventis Pharma, Италия) вводился однократно внутрижелудочно через зонд в дозе 67.5 мг/кг массы тела животного до и после 14 дневного введения финастерида [9]. Пробы крови отбирали в объеме 5-7 мл из краевой вены уха кролика в гепаринизированные побирки через 1, 2, 3, 4, 5, 6, 8, 12 и 24 часа после однократного внутрижелудочного введения фексофенадина, центрифугировали 10 минут при 3000 об/мин, плазму хранили при -28°C до анализа [10].
Содержание фексофенадина в плазме крови определяли методом ВЭЖХ па хроматографе «Стайер» (Россия) с ультрафиолетовым детектором и обращено-фазовой колонке «Весктап Coulter» 4,6*250 мм, зернением 5 мкм. Экстракцию и хроматографирование маркерного субстрата осуществляли по методу Раменской Г.В. с соавт. в собственной модификации. Анализ выполняли при длине волны 220 им и скорости подвижной фазы 1 мл/мин.
Элюирование выполняли подвижной фазой следующего состава (на 200 мл): 133,7 мл бидистиллированной воды, содержащей 2,33 мл ледяной уксусной кислоты и 0,936 мл триэтиламипа, доведенной триэтиламином до pH=4,3 и 64 мл ацетонитрила. Время удерживания пика фексофенадина составило 12,31 мин.
В качестве экстрагентов для жидкостной экстракции фексофенадина использовали дихлорметан, этилацетат и диэтиловый эфир. Коэффициент экстракции фексофенадина из плазмы крови составил 64%.
Полученные данные представлены в виде среднего арифметического значения и стандартной ошибки среднего результата в случае нормального распределения признака или в виде медианы, верхнего и нижнего квартиля - если распределение данных отличалось от нормального (таблица №1).
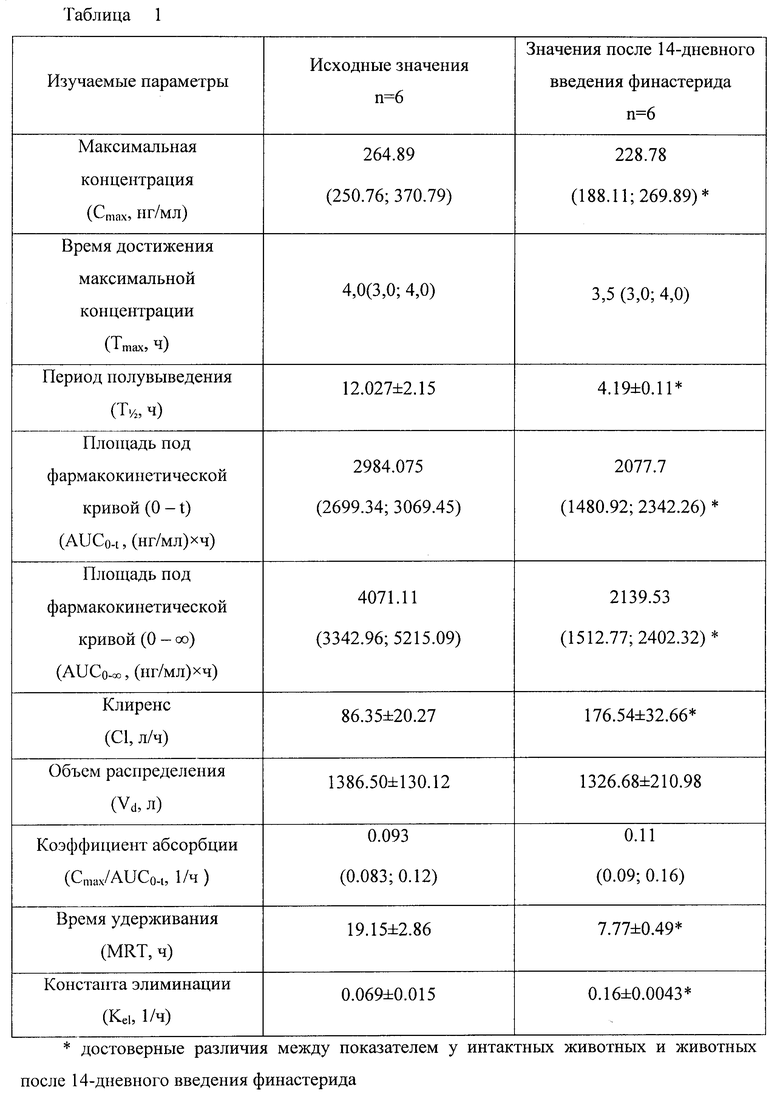
Фармакокииетические параметры рассчитывали с помощью программы Kinetica 5.0.
Достоверное снижение медиан значений Cmax на 13,63% (р□0,05), AUC0-t на 30,37% (р□0.05). AUC0-∞, на 47.45% (р□0,05), средних значений T½ на 65,16% (р□0,05), MRT на 59.43% (р□0,05) и повышению средних значений Kel на 131,88% (p□0,05) и Cl на 104,45% (р□0,05)1 маркерного субстрата Pgp - фексофенадина при назначении финастерида в дозе 0,225 мг/кг массы курсом 14 дней по сравнению с исходными значениями свидетельствует об ускоренном выведении маркерного субстрата, что может служить доказательством индуцирующего влияния финастерида па функциональную активность Pgp.
Использование предлагаемого способа моделирования состояния индукции функциональной активности Pgp на кроликах позволяет применять финастерид в качестве положительного контроля повышенной функциональной активности белка-транспортера при поиске веществ аналогичного действия, а также для прогнозирования потенциальных субстратов Pgp среди лекарственных веществ на этапе доклинических исследований.
Источники информации:
1. The structure and functions of P-glycoprotein / Y. Li [et al.] // Curr. Med. Chcm. - 2010. - V.17. - №8. - P.786-800.
2. Machavaram K.K. Effect of ketoconazole and rifampicin on the pharmacokinetics of ranitidine in healthy human volunteers: a possible role of P-glycoprotein / K.K. Machavaram, J. Gundu, M.R. Yamsani // Drug Metabol. Drug Interact. - 2006. - V.22. - №1. - P.47-65.
3. Gauging the clinical significance of P-glycoprotein-mediated herb-drug interactions: comparative effects of St. John's wort, Echinacea, clarithromycin, and rifampin on digoxin pharmacokinetics / B.J. Gurley [et al] // Mol. Nutr. Food Res. - 2008. - V.52. - №7. - P.772 779.
3. Hughes J. Inhibition of P-glycoprotein-mediated efflux of digoxin and its metabolites by macrolide antibiotics / J.Hughes, A.Crowe // J.Pharmacol. Sci. - 2010. - V.113. - №4. - P.315-234.
4. Van Strater A.C. Interaction of St John's wort (Hypericum perforatum) with clozapine / A.C.Van Strater, J.P.Bogers // Int. Clin. Psychopharmacol. - 2012. - V.27. - №2. - P.121-124.
5. Apocynum venetum extract does not induce CYP3A and P-glycoprotein in rats / Kobayashi M. [et al.] // Biol. Pharm. Bull. - 2004. - V.27. - 10. - P.1649-1652.
6. Adverse reactions to antituberculosis drugs in in-hospital patients: Severity and risk factors / A.S.Vilarica [et al.] // Rev. Port. Pneumol. - 2010. - V.16. - №3. - P.431-451.
7. Up-rcgulation of P-glycoprotein reduces intracellular accumulation of beta amyloid: investigation of P-glycoprotein as a novel therapeutic target for Alzheimer's disease / A.M. Abuznait [et al.] // J. Pharm. Pharmacol. - 2011. - V.63. - №8. - P.11111-1118.
8. Steiner Clinical Pharmacokinetics and Pharmacodynamics of Finasteride / Steiner, F.Joseph // Clinical Pharmacokinetics. - 1996. - V.30. - №1. - P.16-27.
9. Скуридипа E.A. Особенности фармакокииетики фексофенадина при совместном применения с верапамилом и негрустином: автореф. дис. на соискание ученой степени кандидата фармацевтических наук: 15.00.02 / Е.Л. Скуридипа; ГОУ ВПО ММА им. И.М. Сеченова. - Москва, 2007. - 24 с.
10. Колхир С.В. Клиническое значение изучения активности транспортера лекарственных средств гликопротеина-Р для оптимизации фармакотерапии: диссертация на соискание ученой степени кандидата медицинских наук: 14.00.25 / С.В.Колхир; ГОУ ВПО ММА им. И.М. Сеченова. - Москва, 2007. - 21 с.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ МОДЕЛИРОВАНИЯ СОСТОЯНИЯ ИНГИБИРОВАНИЯ ФУНКЦИОНАЛЬНОЙ АКТИВНОСТИ ГЛИКОПРОТЕИНА-Р ЛИНЕСТРЕНОЛОМ В ЭКСПЕРИМЕНТЕ | 2014 |
|
RU2553362C1 |
| СРЕДСТВО ДЛЯ СНИЖЕНИЯ ФУНКЦИОНАЛЬНОЙ АКТИВНОСТИ И ЭКСПРЕССИИ ГЛИКОПРОТЕИНА-Р | 2017 |
|
RU2649134C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ФУНКЦИОНАЛЬНОЙ АКТИВНОСТИ ГЛИКОПРОТЕИНА-Р | 2015 |
|
RU2587780C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ СОСТОЯНИЯ ИНГИБИРОВАНИЯ ФУНКЦИОНАЛЬНОЙ АКТИВНОСТИ ГЛИКОПРОТЕИНА-Р ИНГИБИТОРОМ ДИПЕПТИДИЛПЕПТИДАЗЫ 4 | 2015 |
|
RU2602688C1 |
| СПОСОБ ОЦЕНКИ ФУНКЦИОНАЛЬНОЙ АКТИВНОСТИ ГЛИКОПРОТЕИНА-P В ГЕМАТОЭНЦЕФАЛИЧЕСКОМ БАРЬЕРЕ | 2018 |
|
RU2677286C1 |
| ГИДРОЛИЗАТ ПОЛИСАХАРИДНОГО КОМПЛЕКСА ЦВЕТКОВ ПИЖМЫ ОБЫКНОВЕННОЙ КАК ИНГИБИТОР БЕЛКА-ТРАНСПОРТЕРА ГЛИКОПРОТЕИНА-Р | 2019 |
|
RU2699042C1 |
| СПОСОБ ИНГИБИРОВАНИЯ ГЛИКОПРОТЕИНА-Р В ЭКСПЕРИМЕНТЕ IN VITRO | 2021 |
|
RU2779177C1 |
| СПОСОБ ИНГИБИРОВАНИЯ АВСВ1-БЕЛКА В ЭКСПЕРИМЕНТЕ IN VITRO | 2023 |
|
RU2811993C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ИНДИВИДУАЛЬНОЙ ЧУВСТВИТЕЛЬНОСТИ К ХИМИОТЕРАПИИ СОЛИДНЫХ ОПУХОЛЕЙ ЧЕЛОВЕКА | 2005 |
|
RU2315997C2 |
| Противоопухолевая композиция доксорубицина с ингибитором АТФ-зависимых обратных транспортеров клеток | 2018 |
|
RU2680834C1 |
Изобретение относится к экспериментальной медицине и фармакологии и предназначено для изучения принадлежности изучаемых лекарственных препаратов к субстратам эффлюксного белка-транспортера Pgp (гликопротеина-Р). Для этого моделируют в эксперименте состояние индукции функциональной активности этого белка. В качестве препарата-индуктора используют финастерид. Препарат вводят кроликам внутрижелудочно в форме суспензии в оливковом масле в суточной дозе 0,225 мг/кг массы тела животного в течение 14 дней. Способ обеспечивает создание модели, являясь безопасным, не требующим дорогостоящего лабораторного спецоборудования и материалов. 1 табл.
Способ моделирования состояния индукции функциональной активности гликопротеина-Р финастеридом в эксперименте, включающий введение препарата-индуктора, отличающийся тем, что в качестве такого препарата используют финастерид, который при проведении эксперимента вводят кроликам внутрижелудочно в форме суспензии в оливковом масле в суточной дозе 0,225 мг/кг массы тела животного в течение 14 дней.
| MACHAVARAM КК, Effect of ketoconazole and rifampicin on the pharmacokinetics of ranitidine in healthy human volunteers: a possible role of P-glycoprotein | |||
| Drug Metabol Drug Interact | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| СИСТЕМА-НОСИТЕЛЬ НА ПРОТЕИНОВОЙ ОСНОВЕ ДЛЯ ПРЕОДОЛЕНИЯ РЕЗИСТЕНТНОСТИ ОПУХОЛЕВЫХ КЛЕТОК | 2006 |
|
RU2404916C2 |
| СПОСОБ ПОВЫШЕНИЯ БИОЛОГИЧЕСКОЙ ДОСТУПНОСТИ ФЕКСОФЕНАДИНА И ЕГО ПРОИЗВОДНЫХ | 1998 |
|
RU2197967C2 |
| СПОСОБ ВОССТАНОВЛЕНИЯ ГИПОТАЛАМО-ГИПОФИЗАРНОЙ РЕГУЛЯЦИИ У МУЖЧИН ПОЖИЛОГО ВОЗРАСТА | 2000 |
|
RU2181289C2 |
| US 20120015395 A1, 19.01.2012 | |||
| CN 102288750 A, 21.12.2011 | |||
| US | |||
Авторы
Даты
2014-01-10—Публикация
2012-05-28—Подача