ПЕРЕКРЕСТНАЯ ССЫЛКА
Данная заявка испрашивает приоритет предварительной заявки на патент США №61/088217, поданной 12 августа 2008, полное описание которой включено в данную заявку посредством данной ссылки.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится в общем к некоторым замещенным бензамидам и к их применению в качестве антагонистов, например, в качестве антагонистов рецепторов сфингозин-1-фосфата. Изобретение более конкретно относится к применению этих соединений и фармацевтических композиций для лечения заболеваний, связанных с модулированием рецепторов сфингозин-1-фосфата.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Сфингозин представляет собой соединение, имеющее химическую структуру, представленную общей формулой, описанной ниже, в которой Y1 представляет собой атом водорода. Известно, что различные сфинголипиды, содержащие сфингозин как составную часть, широко распространены в живом организме, в том числе на поверхности клеточных мембран клеток в нервной системе.
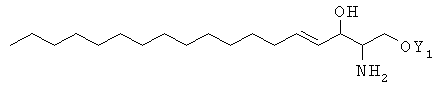
Сфинголипид является одним из липидов, играющих важную роль в живом организме. Заболевание, называемое липидозом, вызвано накоплением определенного сфинголипида в организме. Сфинголипиды, присутствующие на клеточных мембранах, функционируют как регуляторы клеточного роста; участвуют в развитии и дифференциации клеток; функционируют в нервах; вовлечены в инфекционный процесс и злокачественность клеток, и т.д. Многие из физиологических ролей сфинголипидов еще предстоит установить. Недавно было установлено, что церамид, производное сфингозина, может играть важную роль в механизме клеточного преобразования сигнала, а также сообщалось об исследованиях его эффекта в отношении апоптоза и клеточного цикла.
Сфингозин-1-фосфат является важным клеточным метаболитом, производным церамида, который синтезируется de novo или как часть сфингомиелинового цикла (в клетках животных). Он также обнаружен у насекомых, дрожжей и растений.
Фермент церамидаза действует на церамиды, приводя к высвобождению сфингозина, который фосфорилируется сфингозинкиназой, ферментом, повсеместно присутствующим в цитозоле и эндоплазматическом ретикулуме, с образованием сфингозин-1-фосфата. Под действием сфингозинфосфатаз также может идти обратная реакция, причем указанные ферменты действуют в комплексе на регуляцию концентрации метаболита в клетках, и эта концентрация всегда является низкой. В плазме эта концентрация может достигать от 0,2 до 0,9 мкМ, и метаболит находится в ассоциации с липопротеинами, в частности, ЛПВП. Следует также отметить, что образование сфингозин-1-фосфата является существенной стадией в катаболизме сфингоидных оснований.
Подобно его предшественникам, сфингозин-1-фосфат является эффективной молекулой-мессенджером, которая, возможно, одинаковым образом действует как на внутриклеточном, так и на межклеточном уровне, но имеет функции, сильно отличающиеся от функций церамидов и сфингозина. Баланс между этими различными метаболитами сфинголипидов может быть важен для здоровья. Например, в клетке сфингозин-1-фосфат стимулирует клеточное деление (митоз) и в то же время ингибирует клеточную гибель (апоптоз). На внутриклеточном уровне он также функционирует, регулируя мобилизацию кальция и клеточный рост в ответ на ряд внеклеточных стимулов. Ныне является общепринятым мнение, что баланс между уровнями сфингозин-1-фосфата и церамида и/или сфингозина в клетках является критическим для их жизнеспособности. Как и в случае лизофосфолипидов, в частности, лизофосфатидной кислоты, с которой сфингозин-1-фосфат имеет некоторое структурное сходство, многие из внеклеточных эффектов сфингозин-1-фосфата проявляются посредством его взаимодействия с пятью специфичными рецепторами, связанными с G белком, на поверхности клеток. Эти эффекты важны для роста новых кровеносных сосудов, созревания сосудов, развития сердца и иммунитета, а также для направленного движения клеток.
Сфингозин-1-фосфат запасается в относительно высоких концентрациях в тромбоцитах человека, в которых отсутствуют ферменты, ответственные за его катаболизм, и высвобождается в кровоток при активации физиологических стимулов, таких как факторы роста, цитокины, а также агонисты рецепторов и антигены. Он может также играть критическую роль в агрегации тромбоцитов и тромбозе и может вызвать обострение сердечно-сосудистого заболевания. С другой стороны, относительно высокая концентрация этого метаболита в липопротеинах высокой плотности (ЛПВП) может играть благоприятную роль для атерогенеза. Например, недавно были высказаны предположения, что сфингозин-1-фосфат вместе с другими лизолипидами, такими как сфингозилфосфорилхолин и лизосульфатид, отвечает за полезные клинические эффекты ЛПВП за счет того, что он стимулирует продуцирование сосудистым эндотелием эффективной антиатерогенной сигнальной молекулы - оксида азота. Кроме того, подобно лизофосфатидной кислоте, он является маркером некоторых типов рака, и существуют данные, что его роль в клеточном делении или пролиферации может влиять на развитие рака. Именно эти вопросы в настоящее время привлекают большой интерес исследователей в медицине, и потенциал для терапевтического вмешательства в метаболизм сфингозин-1-фосфата активно исследуется.
Грибы и растения содержат сфинголипиды, и основной сфингозин, содержащийся в этих организмах, имеет формулу, описанную ниже. Известно, что эти липиды играют важную роль в росте клеток грибов и растений, но подробные сведения об этой роли еще предстоит выяснить.
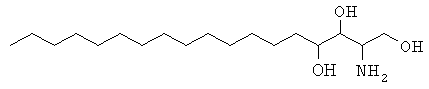
Недавно стало известно, что производные сфинголипидов и родственные им соединения проявляют различную биологическую активность путем ингибирования или стимуляции путей метаболизма. Эти соединения включают ингибиторы протеинкиназы C, индукторы апоптоза, иммуносупрессивные соединения, противогрибковые соединения и тому подобное. Ожидается, что вещества, обладающие такими видами биологической активности, являются полезными соединениями в случае различных заболеваний.
Производные сфингозина получали согласно различным патентам. Например, см. патенты США 4952683; 5110987; 6235912 B1 и 6239297 B1.
Также соединения, которые подобны некоторым производным сфингозина, но о которых не сообщалось, что они являются лигандами рецепторов сфингозина, описаны в различных патентах и опубликованных заявках на патенты. См., например, патенты США 5294722; 5102901; 5403851 и 5580878, публикацию заявки на патент США US 2003/0125371 A2.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
В изобретении предложены некоторые конкретные бензамиды, которые полезны в качестве антагонистов сфингозин-1-фосфата. Как таковые, описанные здесь соединения полезны при лечении широкого ряда расстройств, связанных с модулированием рецепторов сфингозин-1-фосфата.
В одном воплощении изобретения предложены соединения, имеющие структуру
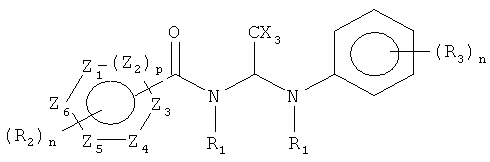
где:
каждый R1 независимо представляет собой -Н или низший алкил;
каждый из R2 и R3 независимо представляет собой -Н, линейный или разветвленный алкил, циклоалкил, гетероциклическую группу, арил, гетероарил, алкенил, алкинил, галогенид, гидрокси, алкокси, алкиламино, алкилкарбоксил, трифторметил, -N(R4)2, -CN, -CO2R4, -CH2OH, -OCF3, -OCHF2 или -NO2; где каждый R2 находится в мета- или пара-положении относительно карбонильной группировки;
каждый R4 независимо представляет собой Н, линейный или разветвленный алкил, циклоалкил, арил, гетероарил, галогеноалкил, гидрокси, алкокси, гидроксиалкил, алкилкарбонил, формил, оксикарбонил, карбоксил, алкилкарбоксилат, алкиламид, амино, алкиламино или аминокарбонил;
каждый из Z1, Z2, Z3, Z4, Z5 и Z6 независимо представляет собой C, N, O или S;
Х представляет собой Н, F, Cl, Br или I;
каждое n независимо равно 1-5; и
p равно 0 или 1;
при условии, что, если каждый из Z1, Z2, Z3, Z4, Z5 и Z6 представляет собой С, p равно 1 и каждый R2 представляет собой -Н, то R3 не является Cl;
или их фармацевтически приемлемые соли.
В другом воплощении предложены фармацевтические композиции, включающие по меньшей мере одно соединение по изобретению в фармацевтически приемлемом носителе для него.
В следующем воплощении изобретения предложены способы лечения расстройств, связанных с модулированием рецепторов сфингозин-1-фосфата. Такие способы можно осуществлять, например, путем введения субъекту, нуждающемуся в этом, фармацевтической композиции, содержащей терапевтически эффективное количество по меньшей мере одного соединения по изобретению.
Еще в одном воплощении изобретения предложены способы лечения расстройств, связанных с модулированием рецепторов сфингозин-1-фосфата, включающих рецепторы S1P1, S1P2 и S1P3. Такие способы можно осуществлять, например, путем введения субъекту, нуждающемуся в этом, терапевтически эффективного количества по меньшей мере одного соединения по изобретению или любой их комбинации, либо его фармацевтически приемлемых солей, гидратов, сольватов, кристаллических форм и индивидуальных изомеров, энантиомеров и диастереомеров.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Должно быть понятно, что как предшествующее общее описание, так и последующее общее описание является только примерным и пояснительным и не ограничивает заявленное изобретение. В данной заявке использование единственного числа включает множественное число, если конкретно не указано иное. Как используется в данной заявке, "или" означает "и/или", если не указано иное. Кроме того, использование термина "включающий", а также других форм, таких как "включает" и "включенный", не является ограничивающим. Используемые в данной заявке заголовки разделов предназначены только для организационных целей, и их не следует истолковывать как ограничивающие описываемую сущность изобретения.
Если не приведены специальные определения, то используемая здесь номенклатура, а также лабораторные методы и методики аналитической химии, органического синтеза и неорганической химии, описанные здесь, известны в данной области техники. Стандартные химические символы используются взаимозаменяемо с полными названиями, представленными такими символами. Так, например, термины "атом водорода" и "Н" понимают как имеющие идентичные значения. Для химического синтеза, химического анализа и приготовления композиций можно использовать стандартные методики.
Термин "алкил", как используется в данной заявке, относится к линейным, разветвленным или циклическим гидрокарбильным группам, имеющим от 1 вплоть до примерно 100 атомов углерода. Числовой диапазон, такой как "1-100" или "C1-С100", там где он встречается в данной заявке, относится к каждому целому числу в данном диапазоне; например, "C1-С100 алкил" означает, что алкильная группа может содержать только 1 атом углерода, 2 атома углерода, 3 атома углерода и т.д. вплоть до 100 атомов углерода включительно, хотя термин "алкил" также включает случаи, когда диапазон количества атомов углерода не указан. "Замещенный алкил" относится к алкильным группировкам, несущим заместители, типично выбранные из алкила, алкенила, алкинила, гидрокси, алкокси, гетероциклической группы, арила, гетероарила, арилокси, галогена, галогеноалкила, циано, нитро, амино, низшего алкиламино, низшего диалкиламино, амидо, азидо, ацила (-С(О)R6), алкоксиметила, меркапто (-S-R6), сульфокси (-S(О)-R6), сульфонила (-S(O)2-R6), сульфонамида (-S(O)2N(R6)2), карбоната (-OC(O)-O-R6), оксиацила (-ОС(О)-R6), карбоксила (-С(О)ОН), сложного эфира (-С(О)OR6), карбамата (-OC(O)-N(R6)2), где R6 представляет собой Н или низший алкил, низший алкенил, низший алкинил, арил, гетероарил, гетероциклическую группу и тому подобное. Термин "низший алкил", как используют в данной заявке, относится к алкильным группировкам, содержащим от 1 до примерно 6 атомов углерода.
Термин "алкенил", как его используют в данной заявке, относится к линейным, разветвленным или циклическим гидрокарбильным группам, имеющим по меньшей мере одну двойную связь углерод-углерод, и в которых количество атомов углерода находится в диапазоне от 2 вплоть до примерно 100, и термин "замещенный алкенил" относится к алкенильным группам, дополнительно несущим один или более чем один заместитель, как описано выше. Термин "низший алкенил", как его используют в данной заявке, относится к алкенильным группировкам, содержащим от 1 до примерно 6 атомов углерода.
Термин "алкинил", как его используют в данной заявке, относится к линейным, разветвленным или циклическим гидрокарбильным группам, имеющим по меньшей мере одну тройную связь углерод-углерод, и в которых количество атомов углерода находится в диапазоне от 2 вплоть до примерно 100, и термин "замещенный алкинил" относится к алкинильным группам, дополнительно несущим один или более чем один заместитель, как описано выше. Термин "низший алкинил", как его используют в данной заявке, относится к алкинильным группировкам, содержащим от 1 до примерно 6 атомов углерода.
Термин "циклоалкил", как его используют в данной заявке, относится к циклическим (то есть содержащим кольцо) алкильным группировкам, в которых количество атомов углерода типично находится в диапазоне от примерно 3 вплоть до примерно 8, и термин "замещенный циклоалкил" относится к циклоалкильным группам, дополнительно несущим один или более чем один заместитель, как описано выше.
Термин "арил", как его используют в данной заявке, относится к ароматическим группам, в которых количество атомов углерода находится в диапазоне от 6 вплоть до 14, и термин "замещенный арил" относится к арильным группам, дополнительно несущим один или более чем один заместитель, как описано выше.
Термин "гетероарил", как его используют в данной заявке, относится к ароматическим группировкам, содержащим один или более чем один гетероатом (например, N, О, S или тому подобное) как часть кольцевой структуры, и где суммарное количество атомов кольцевой структуры (то есть атомов углерода и гетероатомов) составляет от 5 вплоть до 14. "Замещенный гетероарил" относится к гетероарильным группам, дополнительно несущим один или более чем один заместитель, как описано выше.
Термины "гетероциклическая группа" или "гетероцикл", как их используют в данной заявке, относятся к неароматическим циклическим (то есть содержащим кольцо) группам, содержащим один или более чем один гетероатом (например, N, О, S или тому подобное) как часть кольцевой структуры, и в которых количество атомов углерода находится в диапазоне от 3 вплоть до 14, и термины "замещенная гетероциклическая группа" или "замещенный гетероцикл" относятся к гетероциклическим группам или гетероциклам, дополнительно несущим один или более чем один заместитель, как описано выше.
Термины "галоген" или "галогенид", как их используют в данной заявке, относится к фториду, хлориду, бромиду или йодиду. Термины "фтор", "хлор", "бром" и "йод" можно также могут быть использованы при упоминании галогенированных заместителей, например, "трифторметил".
Термин "гидроксиалкил", как его используют в данной заявке, относится к алкил-ОН, такому как гидроксиметил, гидроксиэтил и тому подобное.
Термин "алкилацил" как его используют в данной заявке, относится к алкилкетону, такому как этанон, пропанон и тому подобное.
Термин "фармацевтически приемлемая соль", как его используют в данной заявке, относится к тем солям, которые сохраняют биологическую эффективность и свойства свободных оснований, и которые получают путем взаимодействия с неорганическими кислотами, такими как соляная кислота, бромисто-водородная кислота, серная кислота, азотная кислота, фосфорная кислота, метансульфоновая кислота, этансульфоновая кислота, пара-толуолсульфоновая кислота, салициловая кислота и тому подобное.
Специалистам в данной области техники совершенно очевидно, что некоторые из соединений по изобретению могут содержать один или более чем один асимметрический центр, так что эти соединения могут существовать в энантиомерных, а также в диастереомерных формах. Если специально не указано иное, объем настоящего изобретения включает все энантиомеры, диастереомеры и рацемические смеси. Некоторые из соединений по изобретению могут образовать соли с фармацевтически приемлемыми кислотами или основаниями, и такие фармацевтически приемлемые соли соединений, описанных в данной заявке, также включены в объем изобретения. Согласно изобретению предложены соединения, имеющие структуру:

где:
каждый R1 независимо представляет собой -Н или низший алкил;
каждый из R2 и R3 независимо представляет собой -Н, линейный или разветвленный алкил, циклоалкил, гетероциклическую группу, арил, гетероарил, алкенил, алкинил, галогенид, гидрокси, алкокси, алкиламино, алкилкарбоксил, трифторметил, -N(R4)2, -CN, -CO2R4, -CH2OH, -OCF3, -OCHF2 или -NO2; где каждый R2 находится в мета- или пара-положении относительно карбонильной группировки;
каждый R4 независимо представляет собой Н, линейный или разветвленный алкил, циклоалкил, арил, гетероарил, галогеноалкил, гидрокси, алкокси, гидроксиалкил, алкилкарбонил, формил, оксикарбонил, карбоксил, алкилкарбоксилат, алкиламид, амино, алкиламино или аминокарбонил;
каждый из Z1, Z2, Z3, Z4, Z5 и Z6 независимо представляет собой C, N, О или S;
Х представляет собой Н, F, Cl, Br или I;
каждое n независимо равно 1-5; и
p равно 0 или 1;
при условии, что, когда каждый из Z1, Z2, Z3, Z4, Z5 и Z6 представляет собой С, p равно 1 и каждый R2 представляет собой -Н, то R3 не является Cl;
или их фармацевтически приемлемые соли.
В некоторых воплощениях изобретения Х представляет собой F, Cl или Br.
В некоторых воплощениях каждый R2 независимо представляет собой алкил, галогенид, алкокси или -NO2.
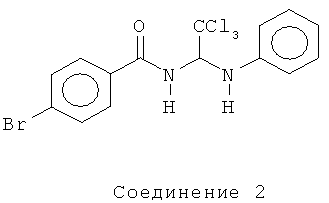
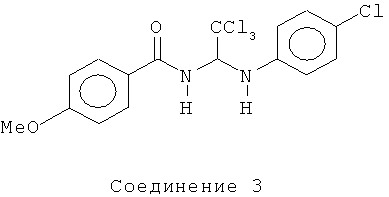
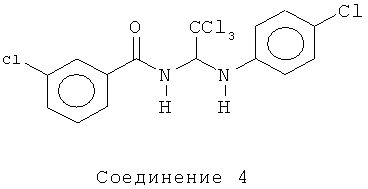
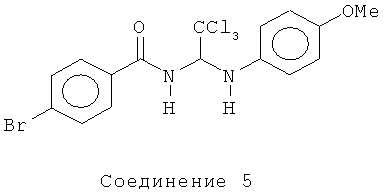
В одном воплощении приведенной выше структуры необязательно исключено одно или все из приведенных ниже соединений:


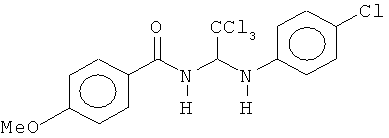
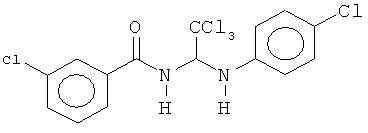
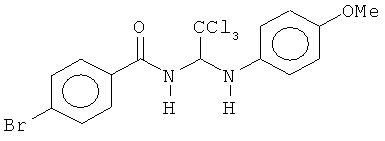
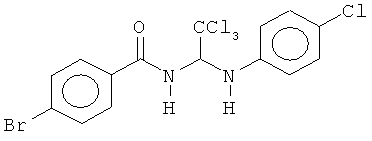
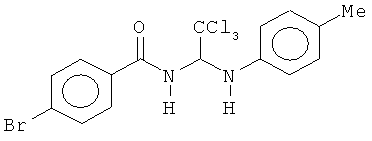
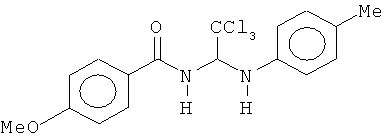

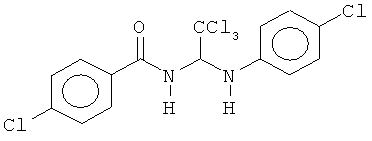
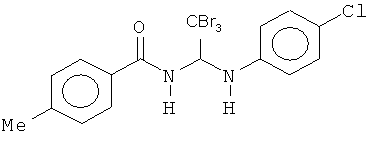
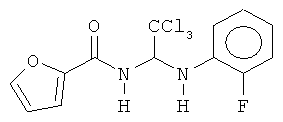
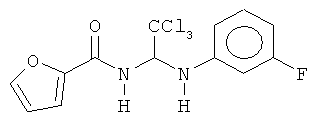
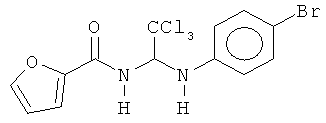
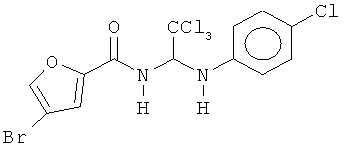
В некоторых воплощениях изобретения предложены соединения, имеющие структуру
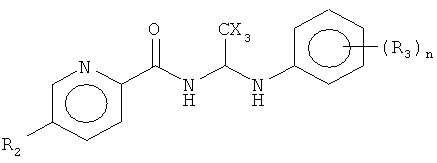
где:
Х представляет собой Cl или Br;
R2 и каждый R3 независимо представляет собой -Н, линейный или разветвленный алкил, циклоалкил, гетероциклическую группу, арил, гетероарил, алкенил, алкинил, галогенид, гидрокси, алкокси, алкиламино, алкилкарбоксил, трифторметил, -N(R4)2, -CN, -CO2R4, -CH2OH, -OCF3, -OCHF2 или -NO2;
каждый R4 независимо представляет собой Н, линейный или разветвленный алкил, циклоалкил, арил, гетероарил, галогеноалкил, гидрокси, алкокси, гидроксиалкил, алкилкарбонил, формил, оксикарбонил, карбоксил, алкилкарбоксилат, алкиламид, амино, алкиламино или аминокарбонил; и
n равно 1-5.
В некоторых воплощениях изобретения предложены соединения, имеющие структуру

где:
Х представляет собой Cl, F или Br;
R2 и каждый R3 независимо представляет собой -Н, линейный или разветвленный алкил, циклоалкил, гетероциклическую группу, арил, гетероарил, алкенил, алкинил, галогенид, гидрокси, алкокси, алкиламино, алкилкарбоксил, трифторметил, -N(R4)2, -CN, -CO2R4, -CH2OH, -OCF3, -OCHF2 или -NO2;
каждый R4 независимо представляет собой Н, линейный или разветвленный алкил, циклоалкил, арил, гетероарил, галогеноалкил, гидрокси, алкокси, гидроксиалкил, алкилкарбонил, формил, оксикарбонил, карбоксил, алкилкарбоксилат, алкиламид, амино, алкиламино или аминокарбонил; и
n равно 1-5,
В других воплощениях предложены соединения, где p равно 1 и каждый из Z1, Z2, Z3, Z4, Z5 и Z6 представляет собой С. Соединения в соответствии с данным воплощением изобретения включают, не ограничиваясь указанным, соединения, имеющие любую из структур:
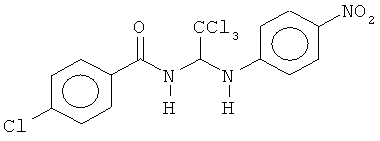
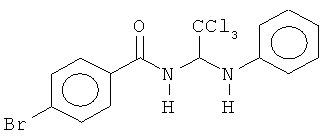

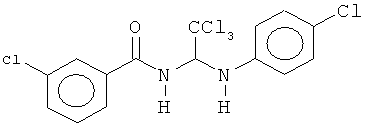






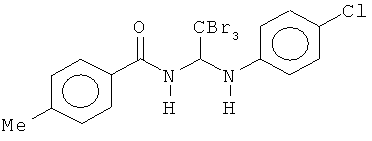
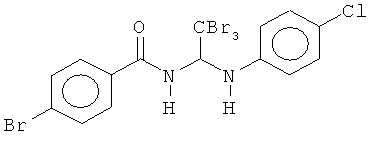
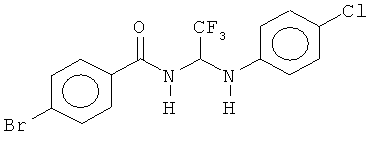
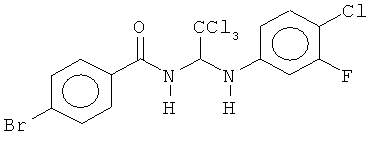
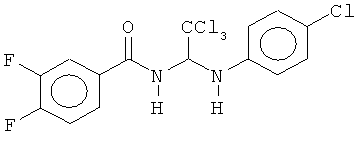
В других воплощениях предложены соединения, где p равно 0, Z1 представляет собой O, и каждый из Z3, Z4, Z5 и Z6 представляет собой C. Соединения в соответствии с данным воплощением изобретения включают, не ограничиваясь указанным, соединения, имеющие любую из структур:

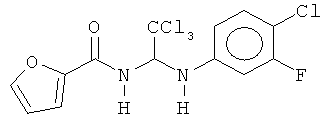
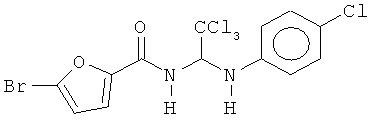
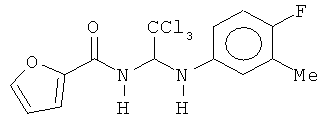
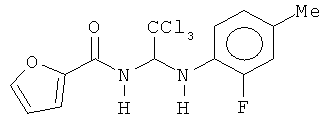
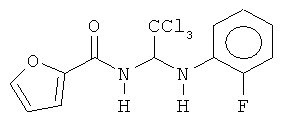
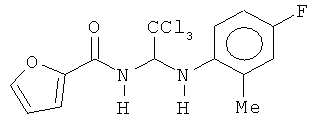
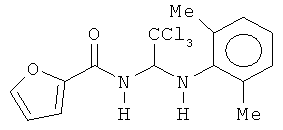
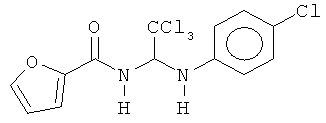
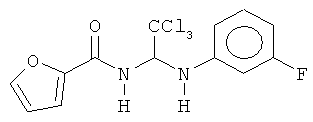
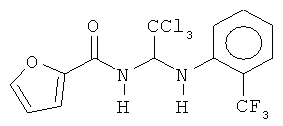
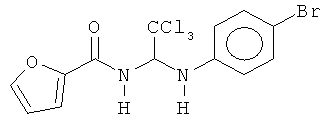
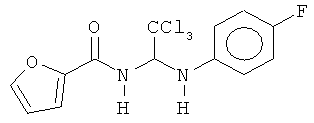

В других воплощениях предложены соединения, где p равно 1 и по меньшей мере один из Z1, Z2, Z3, Z4, Z5 и Z6 представляет собой N. Соединения в соответствии с данным воплощением изобретения включают, не ограничиваясь указанным, соединения, имеющие любую из структур:
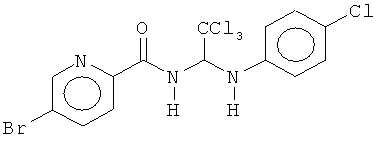
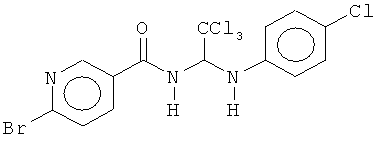
Соединения по изобретению могут быть получены различными путями, хорошо известными специалистам в данной области техники. На приведенной ниже схеме A изображен примерный путь синтеза с получением соединений по изобретению.
Схема A
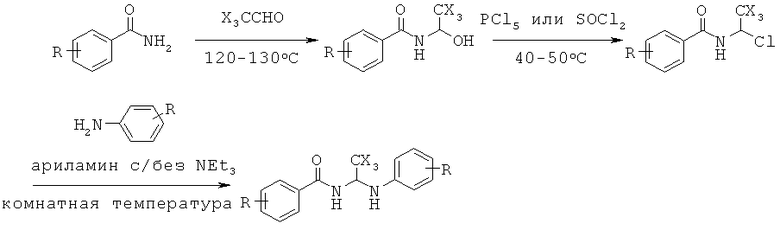
Соединения согалсно изобретению можно синтезировать путем вариаций способов, описанных Guirado, A. et al; Tetrahedron, 58, 2002, 5087 в других источниках, цитируемых в этой публикации. Например (см. схему А), под действием хлораля в присутствии амида происходит плавный переход к спирту. Спирты можно преобразовать в хлориды с подходящим реагентом, таким как PCl5, SOCl2 или тому подобное. Конечной стадией является взаимодействие хлорида с подходящим амином в мягких условиях с последующей соответствующей обработкой и процедурами очистки, известными специалистам в данной области техники.
Соединения по изобретению были протестированы на активность в отношении S1P3 с использованием FLIPR-анализа (FLIPR - Fluorometric Imaging Plate Reader, флуориметрическое считывающее устройство для планшетов). Соединения можно оценить в отношении способности к активации или блокированию активации человеческого рецептора S1P3 в клетках Т24, стабильно экспрессирующих человеческий рецептор S1P3. Клетки высевают в покрытые поли-D-лизином 384-луночные планшеты из расчета десять тысяч клеток/лунка за одни сутки до использования. Средой для роста клеточной линии, экспрессирующей рецептор S1P3, является среда McCoy's 5A с добавлением 10% обработанной углем фетальной бычьей сыворотки (ФБС), 1% антибиотиков и противогрибковых средств и 400 мкг/мл генетицина. В день эксперимента клетки дважды промывают сбалансированным солевым раствором Хэнкса (HBSS) с добавлением 20 мМ N-2-гидроксиэтил-пиперазин-N-2-этансульфоновой кислоты (HEPES) (буфер HBSS/Hepes). Затем на клетки наносят краситель 2 мкМ Fluo-4, разведенный в буфере HBSS/Hepes, с 1,25 мМ пробенецида и инкубируют при 37°C в течение 40 минут. Внеклеточный краситель удаляют путем промывания планшетов с клетками четыре раза, после чего планшеты помещают в FLIPR (Fluorometric Imaging Plate Reader, Molecular Devices). Лиганды разводят в буфере HBSS/Hepes и готовят в 384-луночных микропланшетах. Положительный контроль, сфингозин-1-фосфат (S1P), разводят в буфере HBSS/Hepes с 4 мг/мл бычьего сывороточного альбумина, не содержащего жирных кислот. Устройство FLIPR переносит 12,5 мкл из микропланшета с лигандами в планшет с клетками и снимает измерения флуоресценции в течение 75 секунд, проводя считывание каждую секунду, а затем в течение 2,5 минут, проводя считывание каждые 10 секунд. Лекарства тестируют в пределах диапазона концентраций от 0,61 нМ до 10000 нМ. Данные для ответов Ca2+ получают в произвольных единицах флуоресценции и не переводят в концентрации Ca2+. Значения IC50 определяют с помощью линейного регрессионного анализа, используя алгоритм Levenburg Marquardt. Результаты анализа представлены в приведенной ниже таблице.
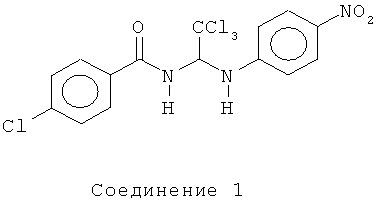



Заболевания, которые можно лечить соединениями, композициями и способами по изобретению, включают, не ограничиваясь указанным, приведенные ниже состояния:
Аллергии и другие воспалительные заболевания: Крапивница, бронхиальная астма и другие воспаления дыхательных путей, включая эмфизему легких и хронические обструктивные болезни легких;
Сердечные функции: брадикардия, застойная сердечная недостаточность, сердечная аритмия, предупреждение и лечение атеросклероза и ишемическое/реперфузионное повреждение;
Противофиброзное действие: глазной, сердечный, печеночный и легочный фиброз, пролиферативная витреоретинопатия, рубцовый пемфигоид, фиброз в роговице, конъюнктиве и теноновом пространстве, индуцированный операцией; и
Боли и воспалительные заболевания: Острая боль, приступ хронической боли, скелетно-мышечные боли, висцеральная боль, боль, обусловленная диабетической невропатией, ревматоидный артрит, хроническая боль в колене и суставе, тендонит, остеоартрит, бурсит, невропатические боли.
Соединения по изобретению можно вводить в фармацевтически эффективных дозировках. Такие дозировки обычно представляют собой минимальную дозу, необходимую для достижения желаемого терапевтического эффекта; при лечении хронической боли это количество должно быть приблизительно таким, какое необходимо для уменьшения дискомфорта, вызванного болью, до переносимых уровней. Обычно такие дозы будут находиться в диапазоне 1-1000 мг/сутки; более предпочтительно в диапазоне от 10 до 500 мг/сутки. Однако действительное количество соединения, которое нужно вводить в любом данном случае, будет определяться врачом с учетом релевантных обстоятельств, таких как тяжесть боли, возраст и масса пациента, общее физическое состояние пациента, причина боли и путь введения.
Соединения полезны при лечении боли у млекопитающего; в частности, у человека. Как острую боль, так и хроническую боль можно лечить путем введения соединений и композиций по изобретению. Под "острой болью" подразумевают немедленную, обычно с высоким порогом, боль, вызванную повреждением, таким как порез, размозжение, ожог, или химической стимуляцией, такую как испытывают под действием капсаицина, острого ингредиента в перцах чили. Под "хронической болью" подразумевают боль, иную, чем острая боль, такую как, не ограничиваясь указанным, невропатическая боль, висцеральная боль (включая боль, вызванную болезнью Крона и синдромом раздраженной кишки (СРК)), и отраженная боль.
Предпочтительно пациент будет вводить соединение перорально в любой приемлемой форме, такой как таблетка, жидкость, капсула, порошок и тому подобное. Однако могут быть желательны или необходимы другие пути, в частности, если пациент страдает тошнотой. Такие другие пути могут включать, без исключения, чрескожный, парентеральный, подкожный, интраназальный, подоболочечный, внутримышечный, внутривенный и ректальный способ доставки. Кроме того, могут быть разработаны составы, характеризующиеся замедленным высвобождением активного соединения за определенный период времени, или точной регуляцией количества лекарственного средства, высвобождающегося за определенный период времени в течение курса лечения.
В другом воплощении изобретения предложены фармацевтические композиции, включающие по меньшей мере одно соединение по изобретению в фармацевтически приемлемом носителе для него. Выражение "фармацевтически приемлемый" означает носитель, разбавитель или эксципиент, который должен быть совместимым с другими ингредиентами препарата и безвредным для его реципиента.
Фармацевтические композиции по настоящему изобретению можно применять в форме твердого вещества, раствора, эмульсии, дисперсии, мицеллы, липосомы и тому подобного, где полученная в результате композиция содержит одно или более чем одно соединение по настоящему изобретению в качестве активного ингредиента в смеси с органическим или неорганическим носителем или эксципиентом, пригодным для энтеральных или парентеральных применений. Соединения по изобретению можно комбинировать, например, с обычными нетоксичными фармацевтически приемлемыми носителями для таблеток, гранул, капсул, суппозиториев, растворов, эмульсий, суспензий и любой другой формы, пригодной для применения. Носители, которые можно использовать, включают глюкозу, лактозу, аравийскую камедь, желатин, маннит, крахмальную пасту, трисиликат магния, тальк, кукурузный крахмал, кератин, коллоидный кремнезем, картофельный крахмал, мочевину, среднецепочечные триглицериды, декстраны и другие носители, пригодные для использования при изготовлении препаратов в твердой, полутвердой или жидкой форме. Кроме того, можно использовать вспомогательные, стабилизирующие, загущающие и красящие агенты и ароматические вещества. Соединения по изобретению включают в фармацевтическую композицию в количестве, достаточном для получения желаемого эффекта при патологическом процессе или болезненном состоянии.
Фармацевтические композиции, содержащие соединения по изобретению, могут быть представлены в форме, пригодной для перорального применения, например, в форме таблеток, пастилок, лепешек, водных или масляных суспензий, диспергируемых порошков или гранул, эмульсий, твердых или мягких капсул, либо сиропов или эликсиров. Композиции, предназначенные для перорального применения, можно готовить в соответствии с любым известным в данной области техники способом изготовления фармацевтических композиций, и такие композиции могут содержать один или более чем один агент, выбранный из группы, состоящей из подсластителя, такого как сахароза, лактоза или сахарин, корригента, такого как перечная мята, винтергреновое или вишневое масло, красители и консерванты, с целью получения фармацевтически элегантных и приятных на вкус препаратов. Таблетки, содержащие соединения по изобретению в смеси с нетоксичными фармацевтически приемлемыми эксципиентами, можно также готовить известными способами. Используемые эксципиенты могут представлять собой, например, (1) инертные разбавители, такие как карбонат кальция, лактоза, фосфат кальция или фосфат натрия; (2) гранулирующие или разрыхляющие агенты, такие как кукурузный крахмал, картофельный крахмал или альгиновая кислота; (3) связующие агенты, такие как трагакантовая камедь, кукурузный крахмал, желатин или аравийская камедь, или (4) смазывающие агенты, такие как стеарат магния, стеариновая кислота или тальк. Таблетки могут быть непокрытыми или покрытыми с помощью известных методик для замедления разрыхления и всасывания в желудочно-кишечном тракте и обеспечивающими благодаря этому пролонгированное действие в течение длительного периода. Например, можно использовать материал, замедляющий высвобождение, такой как глицерилмоностеарат или глицерилдистеарат.
В некоторых случаях препараты для перорального применения могут быть представлены в форме твердых желатиновых капсул, где соединения по изобретению смешаны с инертным твердым разбавителем, например, карбонатом кальция, фосфатом кальция или каолином. Они могут также быть представлены в форме мягких желатиновых капсул, где соединения по изобретению смешаны с водной или масляной средой, например, арахисовым маслом, жидким вазелином или оливковым маслом.
Фармацевтические композиции могут быть представлены в форме стерильной инъекционной суспензии. Эту суспензию можно готовить в соответствии с известными способами с использованием подходящих диспергирующих или увлажняющих агентов и суспендирующих агентов. Стерильный инъекционный препарат может также представлять собой стерильный инъекционный раствор или суспензию в нетоксичном парентерально приемлемом разбавителе или растворителе, например, раствор в 1,3-бутандиоле. В качестве растворяющей или суспендирующей среды как правило используют стерильные нелетучие масла. Для этой цели можно использовать любое легкое нелетучее масло, включая синтетические моно- или диглицериды, жирные кислоты (включая олеиновую кислоту), природные растительные масла, такие как кунжутное масло, кокосовое масло, арахисовое масло, хлопковое масло и т.д., или синтетические жирные носители, такие как этилолеат или тому подобное. При необходимости в композицию могут включать также буферы, консерванты, антиоксиданты и тому подобное.
Соединения по изобретению можно также вводить в форме суппозиториев для ректального введения лекарственного средства. Эти композиции можно готовить путем смешивания соединений по изобретению с подходящим не раздражающим эксципиентом, таким как масло какао, синтетические глицеридные эфиры полиэтиленгликолей, которые являются твердыми при обычных температурах, но становятся жидкими и/или растворяются в полости прямой кишки с высвобождением лекарственного средства.
Поскольку у индивидуальных субъектов может быть широкое разнообразие по тяжести симптомов, и каждое лекарственное средство обладает своими уникальными терапевтическими характеристиками, точный способ введения и применяемая дозировка для каждого субъекта остается на усмотрение практикующего врача.
Соединения и фармацевтические композиции, описанные здесь, полезны в качестве лекарственных средств у млекопитающих, включая людей, для лечения заболеваний или облегчения симптомов, которые отвечают на лечение антагонистами рецепторов сфингозин-1-фосфата. Таким образом, в следующих воплощениях изобретения предложены способы лечения расстройства, связанного с модулированием рецепторов сфингозин-1-фосфата. Такие способы можно осуществлять, например, путем введения субъекту, нуждающемуся в этом, фармацевтической композиции, содержащей терапевтически эффективное количество по меньшей мере одного соединения по изобретению. Как используют в данной заявке, термин "терапевтически эффективное количество" означает количество фармацевтической композиции, которое должно вызывать биологический или клинический ответ субъекта, нуждающегося в этом, который ожидает исследователь, ветеринар, врач или другой клиницист. В некоторых воплощениях субъект, нуждающийся в этом, представляет собой млекопитающее. В некоторых воплощениях млекопитающее представляет собой человека.
Приведенные ниже примеры предназначены только для иллюстрации изобретения, и их не следует истолковывать как ограничивающие изобретение.
ПРИМЕРЫ

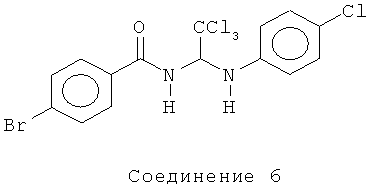
Получение 4-бром-N-(2,2,2-трихлор-1-(4-хлорфениламино)этил) бензамида (Соединение 6). Смесь 4-бромбензамида (2,42 г, 11,7 ммоль) и хлораля (2,2 мл, 22,6 ммоль) нагревали при 120°C в течение 20 мин. Можно добавить ТГФ (~2 мл), чтобы способствовать смешиванию. Смесь охлаждали до комнатной температуры, и эту смесь выпаривали и высушивали в вакууме в течение 18 часов. Промежуточный продукт, 4-бром-N-(2,2,2-трихлор-1-гидроксиэтил)бензамид, был достаточно чистым, чтобы использовать его на последующих стадиях без дальнейшей очистки.
Раствор 4-бром-N-(2,2,2-трихлор-1-гидроксиэтил)бензамида (0,67 г, 1,93 ммоль) в хлороформе (15 мл) обрабатывали PCl5 (0,42 г, 1,91 ммоль). Смесь нагревали до 50°C в течение 30 минут, после чего охлаждали до комнатной температуры и наливали в колотый лед. Органический слой высушивали над MgSO4 и фильтровали. Раствор 4-бром-N-(1,2,2,2-тетрахлорэтил)бензамида охлаждали до комнатной температуры, после чего добавляли 4-хлоранилин (0,52 мл, 4,0 ммоль), и смеси давали перемешиваться в течение 18 часов. Смесь гасили 2 М HCl и экстрагировали эфиром. Органический раствор высушивали над MgSO4, фильтровали и концентрировали на силикагеле. Материал очищали на ЖХСД (жидкостной хроматографии среднего давления) с 7:3 CH2Cl2:гексанами с получением 4-бром-N-(2,2,2-трихлор-1-(4-хлорфениламино)этил)бензамида (Соединение 6) в виде твердого вещества, Этот продукт можно дополнительно очистить подходящей перекристаллизацией, например, в эфире.
1H ЯМР (300 МГц, CDCl3) δ 7.65 (d, J=8.4 Гц, 2Н), 7.59 (d, J=8.7 Гц, 2Н), 7.19 (d, J=9.0 Гц, 2H), 6.77 (d, J=8.7 Гц, 2H), 6.53 (d, J=9.0 Гц, 1Н), 6.33 (d, J=9.3 Гц, 1Н).
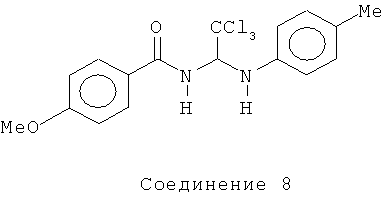
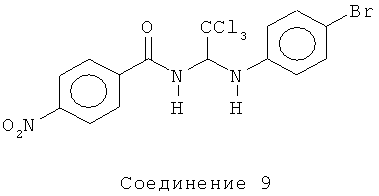
Приведенные ниже соединения были получены в соответствии с общим способом, представленным на схеме А, и как описано выше для Соединения 6.
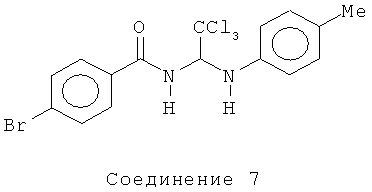
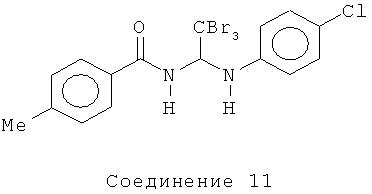
4-бром-N-(2,2,2-трихлор-1-(пара-толуиламино)этил)бензамид (Соединение 7).
1H ЯМР (300 МГц, CDCl3) δ 7.65 (d, J=8.7 Гц, 2Н), 7.58 (d, J=8.7 Гц, 2Н), 7.04 (d, J=8.4 Гц, 2Н), 6.74 (d, J=8.4 Гц, 2Н), 6.52 (d, J=9.3 Гц, 1 Н), 6.35 (d, J=9.0 Гц, 1Н).
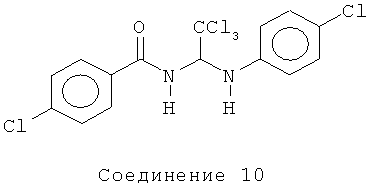
4-хлор-N-(2,2,2-трихлор-1-(4-хлорфениламино)этил)бензамид (Соединение 10).
1H ЯМР (300 МГц, CDCl3) δ 7.72 (d, J=8.7 Гц, 2Н), 7.43 (d, J=8.7 Гц, 2Н), 7.19 (d, J=8.7 Гц, 2Н), 6.77 (d, J=8.7 Гц, 2Н), 6.53 (d, J=9.3 Гц, 1Н), 6.33 (d, J=9.6 Гц, 1Н).
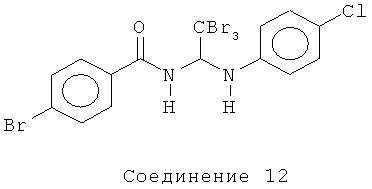
4-бром-N-(2,2,2-трибром-1-(4-хлорфениламино)этил)бензамид (Соединение 12).
1H ЯМР (300 МГц, CDCl3) δ 7.65 (d, J=8.7 Гц, 2Н), 7.58 (d, J=8.7 Гц, 2Н), 7.04 (d, J=8.4 Гц, 2Н), 6.74 (d, J=8.4 Гц, 2Н), 6.52 (d, J=9.3 Гц, 1 Н), 6.35 (d, J=9.0 Гц, 1Н).
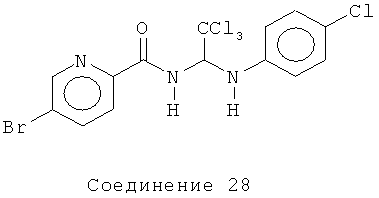
6-бром-N-(2,2,2-трихлор-1-(4-хлорфениламино)этил)никотинамид (Соединение 28).
1H ЯМР (300 МГц, CD3OD) δ выявляется в виде ротамеров 8.75 (d, J=2.4 Гц, 1Н), 8.44 (brs, 1Н) 8.15 (dd, J=8.4, 2.4 Гц, 1Н), 7.42 (d, J=8.1 Гц, 1Н), 7.16 (d, J=8.7 Гц, 2Н), 6.75 (d, J=8.7 Гц, 2Н), 6.34 (d, J=9.6 Гц, 1Н).
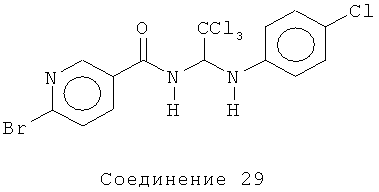
5-бром-N-(2,2,2-трихлор-1-(4-хлорфениламино)этил)пиколинамид (Соединение 29).
1H ЯМР (300 МГц, CDCl3) δ 8.62-8.61 (m, 1H), 8.50 (d, J=9.9 Гц, 1Н), 8.12 (dd, J=8.4, 0.6 Гц, 1H), 8.04-8.00 (m, 1H), 7.18 (d, J=9.0 Гц, 2H), 6.78 (d, J=8.0 Гц, 2H), 6.28 (t, J=9.6 Гц, 1Н), 4.55 (d, J=9.6 Гц, 1Н).
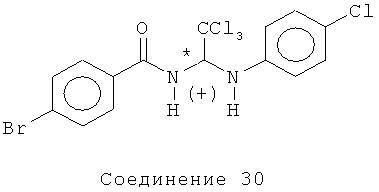
(+)-4-бром-N-(2,2,2-трихлор-1-(4-хлорфениламино)этил)бензамид (Соединение 30). Это соединение было получено в результате хирального разделения на ВЭЖХ (Chiralpak IA, 40% МеОН, 0,1% DEA/CO2 при 100 бар) приведенного выше Соединения 6.
[α]=+96,1° (с 1,08, CHCl3).
1H ЯМР (300 МГц, CDCl3) δ 7.65 (d, J=8.4 Гц, 2H), 7.59 (d, J=8.7 Гц, 2H), 7.19 (d, J=9.0 Гц, 2H), 6.77 (d, J=8.7 Гц, 2H), 6.53 (d, J=9.0 Гц, 1H), 6.33 (d, J=9.3 Гц, 1H).
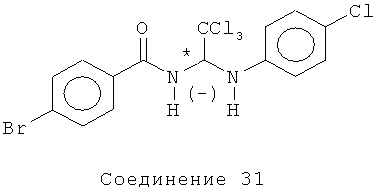
(-)-4-бром-N-(2,2,2-трихлор-1-(4-хлорфениламино)этил)бензамид (Соединение 31). Это соединение было получено в результате хирального разделения на ВЭЖХ (Chiralpak IA, 40% МеОН, 0,1% DEA/CO2 при 100 бар) приведенного выше Соединения 6.
[α]=-99,2° (с 1,12, CHCl3)
1H ЯМР (300 МГц, CDCl3) δ 7.65 (d, J=8.4 Гц, 2H), 7.59 (d, J=8.7 Гц, 2H), 7.19 (d, J=9.0 Гц, 2H), 6.77 (d, J=8.7 Гц, 2H), 6.53 (d, J=9.0 Гц, 1H), 6.33 (d, J=9.3 Гц, 1H).
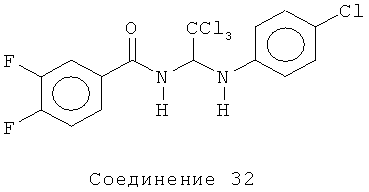
3,4-дифтор-N-(2,2,2-трихлор-1-(4-хлорфениламино)этил)бензамид (Соединение 32).
1H ЯМР (300 МГц, CDCl3) δ 7.68-7.62 (m, 1H), 7.55-7.50 (m, 1H), 7.26-7.17 (m, 3H), 6.76(d, J=8.7 Гц, 2H), 6.53 (d, J=9.3 Гц, 1H), 6.31 (t, J=9.0 Гц, 1H), 4.51 (d, J=8.4 Гц, 1H).
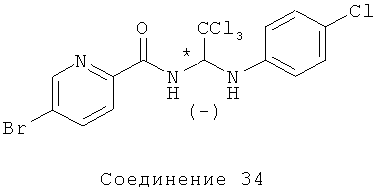
(-)-5-бром-N-(2,2,2-трихлор-1-(4-хлорфениламино)этил)пиколинамид (Соединение 34): Соединение 34 имеет ЯМР, идентичный Соединению 29, но имеет направление оптического вращения (-). Соединение 34 было получено в результате хирального разделения на ВЭЖХ (Chiralpak IA, 30% МеОН, CO2 при 100 бар) приведенного выше Соединения 29, и собран первый пик элюирования (-) энантиомера: [α]=-121° (с 0,69 в CHCl3). 1Н ЯМР (300 МГц, CDCl3) δ 8.62-8.61 (m, 1H), 8.50 (d, J=9.9 Гц, 1H), 8.12 (dd, J=8.4, 0.6 Гц, 1H), 8.04-8.00 (m, 1H), 7.18 (d, J=9.0 Гц, 2Н), 6.78 (d, J=8.0 Гц, 2Н), 6.28 (t, J=9.6 Гц, 1Н), 4.55 (d, J=9.6 Гц, 1Н).
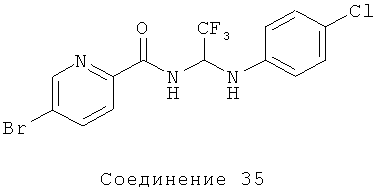
5-бром-N-(1-(4-хлорфениламино)-2,2,2-трифторэтил)пиколинамид (Соединение 35); 1Н ЯМР (300 МГц, CDCl3) δ=8.55 (d, J=2.4 Гц, 1Н), 8.28 (d, J=9.3 Гц, 1Н), 8.09 (d, J=8.1 Гц, 1Н), 7.99 (dd, J=2.4, 8.7 Гц, 1Н), 7.14 (d, J=8.7 Гц, 2Н), 6.71 (d, J=9.0 Гц, 2Н), 6.25-6.12 (m, 1Н), 4.47 (d, J=10.2 Гц, 1Н).
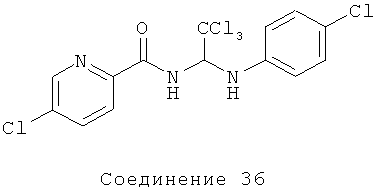
5-хлор-N-(2,2,2-трихлор-1-(4-хлорфениламино)этил)пиколинамид (Соединение 36): 1Н ЯМР (300 МГц, CDCl3) δ=8.51-8.47 (m, 2Н), 8.18 (d, J=9,3 Гц, 1Н), 7.88-7.84 (m, 1Н), 7.17 (d, J=8.7 Гц, 2Н), 6.77 (d, J=8.4 Гц, 2Н), 6.28 (t, J=10.2 Гц, 1 Н), 4.54 (d, J=9.6 Гц, 1Н).
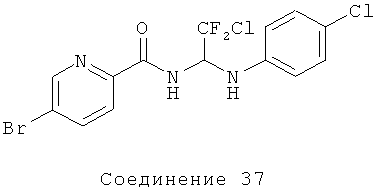
5-бром-N-(2-хлор-1-(4-хлорфениламино)-2,2-дифторэтил)пиколинамид (Соединение 37): 1H ЯМР (300 МГц, CDCl3) δ=8.53 (d, J=2.1 Гц, 1Н), 8.35 (d, J=9,6 Гц, 1Н), 8.08 (d, J=8.7 Гц, 1Н), 7.99-7.95 (m, 1Н), 7.14-7.11 (m, 2Н), 6.73-6.70 (m, 2Н), 6.26-6.16 (9m, 1H), 4.55 (d, J=10.2 Гц, 1Н).
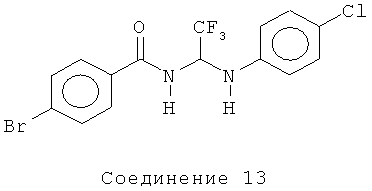
4-бром-N-[1-(4-хлорфениламино)-2,2,2-трифторэтил]-бензамид (Соединение 13) было получено путем использования 2,2,2-трифтор-1-метоксиэтанола вместо хлораля в общем способе, описанном выше, со следующими изменениями методики: Смесь 4-бромбензамида (0,78 г, 3,9 ммоль) и 2,2,2-трифтор-1-метоксиэтанола (0,51 мл, 4,3 ммоль) нагревали при 100°C в течение 18 часов. Смесь выпаривали, и остаток разбавляли хлороформом и концентрировали на силикагеле. Продукт очищали на колонке ЖХСД SiO2 с 1% MeOH:CH2Cl2 с получением промежуточного соединения 4-бром-N-(2,2,2-трифтор-1-гидроксиэтил)бензамида, которое использовали в общем способе, описанном выше, с получением Соединения 13.
1H ЯМР (300 МГц, CDCl3) δ 7.64-7.56 (m, 2Н), 7.18 (d, J=9.0 Гц, 2Н), 6.70 (d, J=8.7 Гц, 2Н), 6.33 (d, J=9.3 Гц, 1 Н), 6.26-6.18 (m, 1Н).
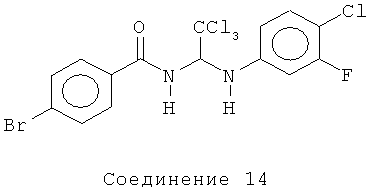
4-бром-N-[2,2,2-трихлор-1-(4-хлор-3-фторфениламино)-этил]-бензамид (Соединение 14)
1H ЯМР (300 МГц, CDCl3) δ 7.65 (d, J=8.7 Гц, 2Н), 7.60 (d, J=9.3 Гц, 2Н), 7.21 (t,J=8.1 Гц, 1H), 6.67 (dd, J=11.1, 3.0 Гц, 1Н), 6.59-6.55 (m, 1Н), 6.30 (d, J=9.0 Гц, 1H), 4.59 (brs, 1Н).
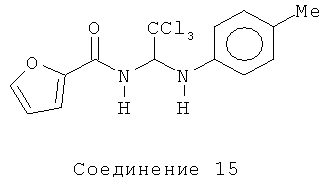
фуран-2-карбоновой кислоты (2,2,2-трихлор-1-пара-толуиламиноэтил)-амид (Соединение 15).
1H ЯМР (300 МГц, CDCl3) δ 7.44 (dd, J=0.9, 1.8 Гц, 1Н), 7.22 (dd, J=0.9, 3.6 Гц, 1 Н), 7.04 (d, J=7.8 Гц, 2Н), 6.85 (d, J=9.3 Гц, 1 Н), 6.74 (d, J=8.4 Гц, 2Н), 6.52 (dd, J=1.8, 3.6 Гц, 1Н), 6.32 (t, J=9.6 Гц, 1Н), 4.43 (d, J=9.3 Гц, 1Н), 2.24 (s, 3H).
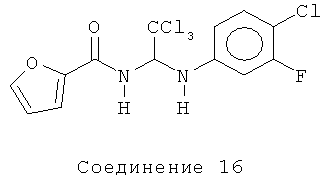
фуран-2-карбоновой кислоты (2,2,2-трихлор-1-(4-хлор-3-фторфениламино)-этил)-амид (Соединение 16).
1H ЯМР (300 МГц, CDCl3) δ 7.46 (dd, J=0.6, 1.8 Гц, 1Н), 7.24 (dd, J=0.6, 3.3 Гц, 1Н), 7.19 (t, J=8.7 Гц, 1Н), 6.90 (d, J=9.3 Гц, 1Н), 6.66 (dd,J=3.0, 11.1 Гц, 1Н), 6.59-6.53 (m, 2Н), 6.26 (d, J=9.3 Гц, 1Н), 4.66 (brs, 1Н).
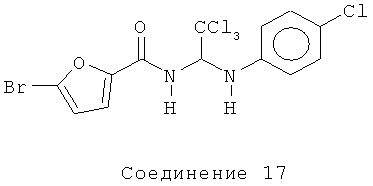
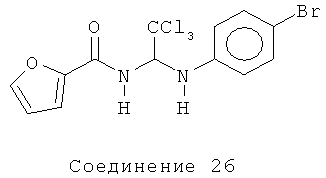
5-бромфуран-2-карбоновой кислоты (2,2,2-трихлор-1-(4-хлорфениламино)-этил)-амид (Соединение 17).
1H ЯМР (300 МГц, CDCl3) δ 7.20-7.17 (m, 3H), 6.76-6.71 (m, 3H), 6.48 (d, J=3.3 Гц, 1Н), 6.27 (d, J=9.3 Гц, 1Н).
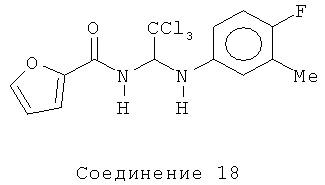
N-{2,2,2-трихлор-1-[(4-фтор-3-метилфенил)амино]этил}-2-фурамид (Соединение 18).
1H ЯМР (500 МГц, CDCl3) δ 7.48 (s, 1Н), 7.24 (d, J=3.5 Гц, 1Н), 6.88 (t, J=8.5 Гц, 1Н), 6.80 (d, J=9.5 Гц, 1Н), 6.66-6.54 (серия m, 3H), 6.25 (t, J=9.5 Гц, 1Н), 4.35 (d, J=9.5 Гц, 1Н), 2.20 (s, 3H).
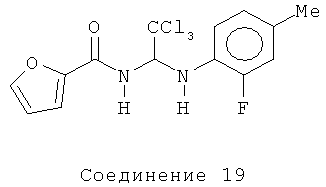
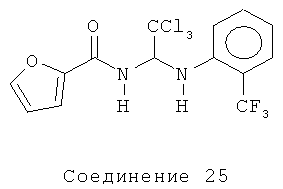
N-{2,2,2-трихлор-1-[(2-фтор-4-метилфенил)амино]этил}-2-фурамид (Соединение 19).
1H ЯМР (500 МГц, CDCl3) δ 7.48 (s, 1Н), 7.24 (d, J=3.5 Гц, 1Н), 6.93-6.84 (серия m, 3H), 6.54 (dd, J=2.0, 1.5 Гц, 1Н), 6.31 (t, J=9.5 Гц, 1Н), 4.66 (dd, J=6.5, 2.5 Гц, 1H), 2.25 (s, 3H).
N-{2,2,2-трихлор-1-[(2-фторфенил)амино]этил}-2-фурамид (Соединение 20).
1H ЯМР (500 МГц, CDCl3) δ 7.48 (dd, J=1.0, 0.5 Гц, 1Н), 7.25 (d, J=3.5 Гц, 1Н), 7.05-7.01 (m, 3H), 6.86 (d, J=10.0 Гц, 1Н), 6.81-6.78 (m, 1Н), 6.55-6.54 (m, 1Н), 6.36 (t, J=9.5 Гц, 1Н), 4.80 (dd, J=2.5, 6.5 Гц, 1Н).
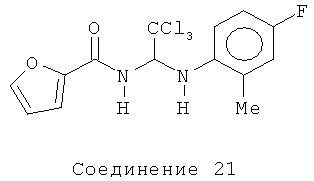
N-{2,2,2-трихлор-1-[(4-фтор-2-метилфенил)амино]этил}-2-фурамид (Соединение 21).
1H ЯМР (500 МГц, CDCl3) δ 7.48 (s, 1Н), 7.25 (dd, J=3.0, 1.0 Гц, 1Н), 6.85-6.81 (m, 2Н), 6.55 (dd, J=2.0, 1.9 Гц, 1Н), 6.28 (d, J=9.0 Гц, 1Н), 4.28 (brs, 1Н), 2.23 (s, 3H).
N-{2,2,2-трихлор-1-[(2,6-диметилфенил)амино]этил}-2-фурамид (Соединение 22).
1H ЯМР (500 МГц, CDCl3) δ 7.47 (d, J=1.0 Гц, 1Н), 7.11 (d, J=7.0 Гц, 1Н), 6.98 (d, J=7.5 Гц, 1Н), 6.86 (t, J=7.5 Гц, 1Н), 6.76 (d, J=9.5 Гц, 1Н), 6.50 (dd, J=1.5,4.0 Гц, 1Н), 6.17 (t, J=10.5 Гц, 1Н), 4.09 (d, J=10.5 Гц, 1Н), 2.41 (s, 6H).
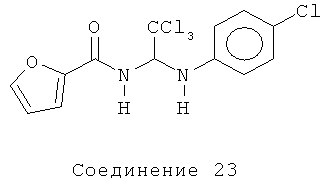
N-{2,2,2-трихлор-1-[(4-хлорфенил)амино]этил}-2-фурамид (Соединение 23).
1H ЯМР (500 МГц, CDCl3) δ 7.40 (t, J=1.0 Гц, 1Н), 7.17 (dd, J=6.5, 0.5 Гц, 1Н), 7.11 (dd, J=4.5, 2.0 Гц, 1Н), 6.22 (t, J=9.0 Гц 1Н), 4.42 (d, J=9.0 Гц, 1Н).
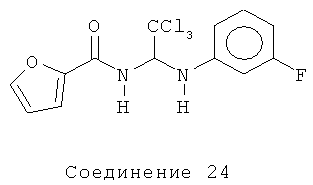
N-{2,2,2-трихлор-1-[(3-фторфенил)амино]этил}-2-фурамид (Соединение 24).
1H ЯМР (500 МГц, CDCl3) δ 7.58-7.56 (m, 3H), 7.45 (s, 1Н), 7.20-7.16 (m, 1Н), 6.84 (d, J=9.5 Гц, 1Н), 6.65-6.51 (серия m, 2H), 6.33 (t, J=9.5 Гц, 1Н), 4.60 (d, J=6.5 Гц, 1Н).
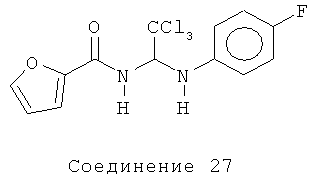
N-{2,2,2-трихлор-1-[(4-фторфенил)амино]этил}-2-фурамид (Соединение 27).
1H ЯМР (300 МГц, CDCl3) δ 7.45 (dd, J=0.6, 1.5 Гц, 1Н), 7.22 (dd, J=0.6, 3.6 Гц, 1Н), 6.95-6.85 (m, 3H), 6.80-6.75 (m, 2H), 6.52 (dd, J=1.8, 3.3 Гц, 1Н), 6.25 (d, J=9.9 Гц, 1H), 4.4 (brs, 1Н).
4-бром-N-(2,2,2-трихлор-1-(4-хлорфениламино)этил)фуран-2-карбоксамид (Соединение 33) было получено в соответствии с описанными способами: см. Ulrich, Н. et al J Org. Chem., 33, 1968, 2887. Раствор 4-бром-N-(2,2,2-трихлор-1-гидроксиэтил)фуран-2-карбоксамида (получение, как для 6 выше) (0,566 г, 1,67 ммоль), 1-хлор-4-изоцианатобензола (0,264 г, 1,68 ммоль) и триэтиламина (2 капли) в бензоле (4 мл) нагревали при 95°C в течение 1,5 ч. Смесь выпаривали при пониженном давлении, остаток сольватировали хлороформом и концентрировали на силикагеле. Хроматографическая очистка на автоматической колонке с 30% дихлорметаном в гексанах дала 4-бром-N-(2,2,2-трихлор-1-(4-хлорфениламино)этил)фуран-2-карбоксамид (Соединение 33) в виде белого твердого вещества; 422 мг (57%).
1H ЯМР (300 МГц, CDCl3) δ 7.46 (d, J=0.9 Гц, 1Н), 7.23 (d, J=0.9 Гц, 1Н), 7.18 (d, J=8.7 Гц, 2H), 6.80 (d, J=9.6 Гц, 1Н), 6.74 (d, J=8.7 Гц, 2H), 6.26 (t, J=9.6 Гц, 1Н), 4.52 (d, J=9.3 Гц, 1Н).
Хотя данное изобретение описано в отношении этих конкретных примеров, понятно, что возможны другие модификации и вариации без отклонения от сущности изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ХИНОЛИН-2-ОНА В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗЫ C-KIT | 2016 |
|
RU2754858C2 |
| ЛИГАНДЫ ДЛЯ АГРЕГИРОВАННЫХ МОЛЕКУЛ ТАУ-БЕЛКА | 2009 |
|
RU2518892C2 |
| АГОНИСТ СФИНГОЗИН-1-ФОСФАТНЫХ РЕЦЕПТОРОВ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ЕГО В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА | 2020 |
|
RU2798605C1 |
| ТИАЗОЛОПИРИМИДИНЫ | 2012 |
|
RU2610840C2 |
| ПРОИЗВОДНЫЕ ФУРО[3,2-В]- И ТИЕНО[3,2-В]ПИРИДИНА В КАЧЕСТВЕ ИНГИБИТОРОВ TBK1 И IKKε | 2013 |
|
RU2622034C2 |
| НОВЫЙ СПОСОБ СИНТЕЗА АГОМЕЛАТИНА | 2014 |
|
RU2683279C1 |
| НОВЫЕ ПРОИЗВОДНЫЕ АЗАБИЦИКЛОГЕКСАНА | 2023 |
|
RU2811800C1 |
| ПРОИЗВОДНЫЕ АМИНА И ИХ ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ ОФТАЛЬМОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ И РАССТРОЙСТВ | 2008 |
|
RU2536040C2 |
| ИНДАЗОЛИЛИЗОКСАЗОЛЬНЫЕ ПРОИЗВОДНЫЕ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, ТАКИХ КАК ЗЛОКАЧЕСТВЕННОЕ НОВООБРАЗОВАНИЕ | 2020 |
|
RU2836662C2 |
| АНТАГОНИСТЫ TLR7/8 И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2833035C2 |
Изобретение относится замещенным бензамидам, которые могут применяться в качестве антагонистов рецепторов сфингозин-1-фосфата. Такие соединения полезны при лечении широкого ряда расстройств, связанных с модулированием рецепторов сфингозин-1-фосфата. 2 н. и 7 з.п. ф-лы, 1 пр.
1. Соединение, имеющее структуру:

где:
каждый R1 независимо представляет собой -H;
каждый R2 независимо представляет собой Cl, Br, I, низший алкокси или -NO2;
каждый R3 независимо представляет собой низший алкил, Cl, Br, I, низший алкокси, трифторметил или -NO2;
где каждый R2 находится в мета- или пара-положении относительно карбонильной группировки,
каждый из Z1, Z2, Z3, Z4, Z5 и Z6 независимо представляет собой C, или один из них представляет собой N;
X представляет собой F, Cl, Br или I;
каждое n независимо равно 1 или 2; и
p равно 1;
или его фармацевтически приемлемые соли.
2. Соединение по п.1, где X представляет собой F, Cl или Br.
3. Соединение по п.2, где каждый R2 представляет собой Cl, Br, I, метокси или -NO2.
4. Соединение по п.1, где p равно 1, и каждый из Z1, Z2, Z3, Z4, Z5 и Z6 представляет собой C.
5. Соединение по п.4, имеющее любую из структур или соединение (-)-5-бром-N-(2,2,2-трихлор-1-(4-хлорфениламино)этил)пиколинамид:
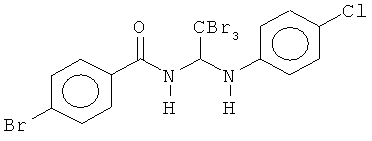
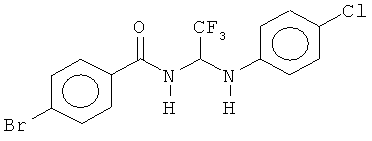
6. Соединение по п.1, где p равно 1, и один из из Z1, Z2, Z3, Z4, Z5 и Z6 представляет собой N.
7. Соединение по п.6, имеющее структуру:

8. Соединение по п.1, имеющее структуру:

где:
X представляет собой Cl, F или Br;
R2 представляет собой Cl, Br или I;
каждый R3 независимо представляет собой Cl, Br или I; и
n равно 1 или 2.
9. Фармацевтическая композиция, обладающая антагонистической активностью в отношении рецепторов сфингозин-1-фосфата, содержащая по меньшей мере одно соединение по п.1 в фармацевтически приемлемом носителе для него.
| US 4659722 A, 21.04.1987 | |||
| DE 1946112 A1, 18.03.1971 | |||
| WO 00/07017 A2, 10.02.2000 | |||
| US 2002082283 A1, 27.06.2002 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| ПРОИЗВОДНЫЕ АМИНОКИСЛОТ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ИХ ПРИМЕНЕНИЕ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2005 |
|
RU2379281C2 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2014-01-27—Публикация
2009-08-12—Подача