Изобретение относится к генетической конструкции, включающей кодон-оптимизированную нуклеотидную последовательность гена дисферлина человека, которая может быть использована в лекарственных средствах.
Известен способ [1] терапии мышечной дистрофии Дюшенна. Авторами были созданы генно-инженерные плазмидные конструкции, содержащие в качестве вставки нуклеотидную последовательность гена дистрофина человека, кодирующего мышечный белок, вовлеченный в развитие патогенеза мышечных дистрофий Дюшенна и Беккера. Полученными конструкциями были генетически модифицированы мышечные волокна пациента с миодистрофией Дюшенна. При этом было показано, что для достижения клинического эффекта требуется большое количество генетически модифицированных мышечных волокон. Таким образом, основным недостатком способа [1] является низкая эффективность генетической модификации мышечных волокон плазмидными векторами, а также низкий уровень экспрессии рекомбинантного белка по сравнению с гентерапевтическими векторами на основе вирусов. Кроме того, вставка нуклеотидной последовательности гена дистрофина позволяет эффективно лечить только миодистрофию Дюшенна, но не другие типы мышечных дистрофий, в том числе связанных с мутациями в гене дисферлина.
Дисферлин (англ. dystrophy-associated fer-1-like, DYSF) - трансмембранный белок, содержащий семь С2 доменов и состоящий из 2080 аминокислот (231 кДа). Мутация в любом из пяти С2 доменах дисферлина (С2А, В, D, Е и G) может привести к формированию аномальной трехмерной структуры белка или к его деградации, что служит причиной развития поясно-конечностной мышечной дистрофии 2В и миопатии Миоши (совместно обозначаемые как дисферлинопатии). Дисферлинопатии относят к нейромышечным заболеваниям человека аутосомно-рецессивного типа наследования, при которых происходит нарушение экспрессии и/или функции белка дисферлина в скелетной поперчно-полосатой мышечной ткани. С2А области дисферлина связывают фосфолипиды Са2+-зависимым способом, что, по-видимому, связано с ролью белка в восстановлении мембран скелетных мышц. Ген DYSF, кодирующий белок дисферлин, охватывает более 150 тысяч пар нуклеотидов (т.п.н.) геномной ДНК и состоит из 55 экзонов. На интронном уровне обнаружено более 300 различных мутаций, большинство из которых представляют собой однонуклеотидные полиморфизмы.
Наиболее близким по существу предлагаемого изобретения (прототипом) является способ [2] для терапии дисферлинопатий. Авторы клонировали кДНК дисферлина в вектор на основе адено-ассоциированного вируса (англ. adeno-associated vector, AAV). Так как кДНК дисферлина превышает размер трансгенной вставки, которую способен нести геном адено-ассоциированного вируса, ученые клонировали кДНК гена dysf в виде 2 частей в два независимых AAV вектора: один рекомбинантный AAV вирус несет 5′ конец кДНК вместе с донорным сайтом сплайсинга интрона, другой рекомбинантный AAV вирус несет акцепторный сайт сплайсинга и следующий за ним 3′ концевую последовательность кДНК. В результате естественной способности AAV вирусов к конкатемеризации происходило объединение двух частей кДНК и экспрессия полноразмерного белка дисферлина.
Внутримышечная инъекция двух рекомбинантных AAV в мышиную модель дисферлинопатии приводила к экспрессии полноразмерного дисферлина, продолжавшейся по крайней мере в течение одного года. Важно, что системная инъекция в хвостовую вену мышей этих двух векторов приводила к системной, хотя и слабой, экспрессии белка. Инъекции приводили к улучшению гистологической картины мышечной ткани, сокращению числа некротических волокон, восстановлению репарации мембраны и глобальному улучшению двигательных функций. В целом эти данные свидетельствуют о перспективности использованной стратегии для лечения дисферлинопатий. Недостатком способа [2] является необходимость одновременного введения двух генетических конструкций, обусловленная ограниченной способностью векторов на основе адено-ассоциированных вирусов нести большие вставки трансгенной ДНК.
Задачей настоящего изобретения является создание эффективной и безопасной генно-инженерной конструкции на основе аденовирусного вектора, экспрессирующей дисферлин человека, а также включение новой генетической конструкции в фармацевтическую композицю. Предлагаемая группа изобретений позволит расширить арсенал лекарственных средст для эффективного лечения дисферлинопатий.
Краткое описание рисунков.
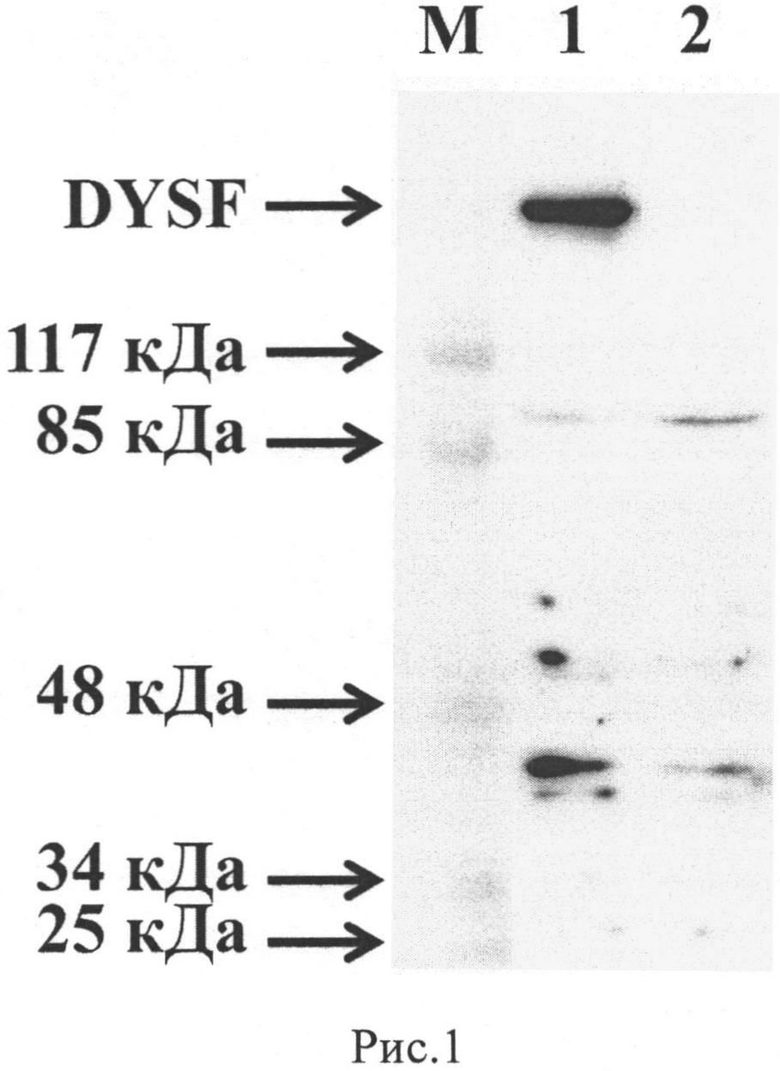
Рис.1. Вестерн-блот анализ экспресии белка DYSF в генетически модифицированных клетках НЕК-293Т. Электрофорез в 8% SDS-PAGE геле по системе Лаэмли. Антитела к дисферлину (Abcam; ab15108) использовались в разведении 1:200. Ожидаемый размер белка DYSF - 231 кДа. Лунка 1 - клетки НЕК293Т, трансфицированные кольцевой плазмидой pAd-Dysf, лунка 2 - нетрансфицированные клетки НЕК-293Т. М - маркер Prestained Protein Molecular Weight Marker (Fermentas International Inc., Канада).
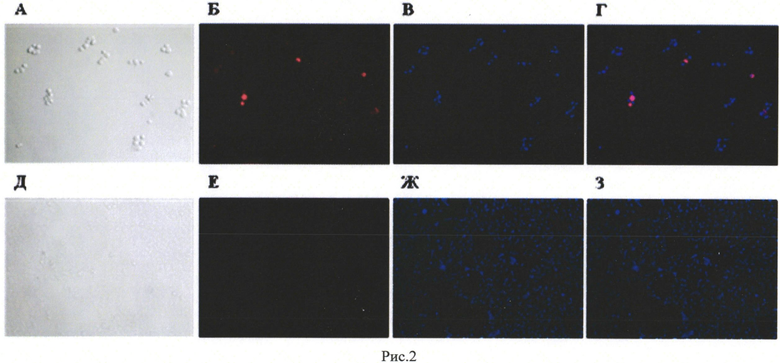
Рис. 2. Иммунофлуоресцентный анализ клеток линии НЕК-293Т, трансдуцированных аденовирусом Ad5-Dysf. 48 часов инкубации после трансдукции. А, Б, В, Г - клетки НЕК-293Т, трансдуцированные аденовирусом Ad5-Dysf. Д, Е, Ж, З - нетрансдуцированный контроль. А, Д - фазово-контрастная микроскопия. Б, Е - окрашивание с помощью первичных антител кролика к дисферлину и вторичных антител осла к иммуноглобулину G кролика, конъюгированных с флуоресцентной меткой Alexa-555. В, Ж - окрашивание флуоресцентным красителем DAPI. Г, З - совмещение синего и красного спектров флуоресценции.
В настоящее время генную терапию на основе аденовирусов (с использованием аденовирусных векторов) считают перспективным методом лечения различных заболеваний человека, в том числе мышечных дистрофий. Аденовирусные векторы способны инфицировать широкий спектр клеток человека, обеспечивая высокий уровень экспрессии трансгена, не интегрируются в геном клетки хозяина (онкологическая безопасность) и могут переносить большие фрагменты рекомбинантной ДНК - до 7,5 т.п.н.
Для решения поставленной задачи предложена генно-инженерная конструкция pAd-Dysf, представляющая собой экспрессионный плазмидный аденовирусный вектор, в который клонирована вставка ДНК (кодон-оптимизированная нуклеотидная последовательность гена дисферлина человека DYSF длиной 6243 п.н.), кодирующая белок дисферлин человека. Генно-инженерная конструкция названа pAd-Dysf.
Необходимость использования генно-инженерной конструкции pAd-Dysf связана с тем, что при дисферлинопатии введение кодон-оптимизированной нуклеотидной последовательности гена дисферлина человека DYSF в составе генетической конструкции способно восстановить нарушенную экспрессию и/или функцию белка дисферлина в скелетной поперечно-полосатой мышечной ткани и вызывать стабильный положительный эффект.
Принцип действия генно-инженерной конструкции pAd-Dysf основан на том, что путем рестрикционного расщепления плазмидной конструкции pAd-Dysf в клетках линии НЕК-293А получают рекомбинантный репликационно дефектный аденовирус серотипа 5, Ad5-Dysf, который впоследствии вводится в мышцу пациента, страдающего дисферлинопатией. За этим следует трансдукция мышечных клеток рекомбинантным аденовирусом и экспрессия гена DYSF. Далее мРНК подвергается процессингу и на ней происходит синтез белка дисферлина.
Основные элементы конструкции pAd-Dysf:
- Кодон-оптимизированная нуклеотидная последовательность гена дисферлина человека (SEQ ID NO:1), 6243 п.н.
- Консенсусная последовательность Козак, находящаяся перед старт-кодоном гена dysf и играющая важную роль для инициации трансляции, 6 п.н.
- Последовательности аденовируса человека Ad5 (включает 5′ левый инвертированный концевой повтор L-ITR и сигнал упаковки), 458 п.н.
- Сайт прямого праймера pAd, 24 п.н.
- Промотор CMV, 588 п.н.
- Сайт праймера промоторного участка Т7, 20 п.н.
- Сайт attB1, 25 п.н.
- Сайт attB1, 25 п.н.
- Эпитоп V5, 42 п.н.
- Сигнал полиаденилирования гена тимидинкиназы, 272 п.н.
- Последовательности аденовируса человека Ad5 (участок Е3 удален, включает 3′ правый инвертированный терминальный повтор R-ITR), 30549 п.н.
- Сайт обратного праймера pAd, 24 п.н.
- Участок начала репликации из плазмиды pUC (ori-pUC), 662 п.н.
- Ген устойчивости к ампициллину (bla), 861 п.н.
- Промотор гена bla, 99 п.н.
- Сайты рестрикции PacI, 2075 п.н.
Для создания конструкции использован экспрессионный вектор pAd/CMV/V5-DEST (Invitrogen, Catalog #V493-20, США), который позволяет получить аденовирус, содержащий необходимый рекомбинантный ген, что обеспечивает его доставку в делящиеся и неделящиеся клетки in vitro или in vivo. Плазмидный вектор содержит промотор цитомегаловируса CMV для эффективной экспрессии трансгена, геном аденовируса, рекомбинационные последовательности, участок начала репликации из pUC плазмиды, гены устойчивости к ампициллину и хлорамфениколу и сайты рестрикции PacI.
Вставка представляет собой кодон-оптимизированную нуклеотидную последовательность гена дисферлина человека. Кодонная оптимизация основана на вырожденности генетического кода, при этом в качестве оптимальных кодонов используют наиболее часто встречающиеся синонимические кодоны вырожденного генетического кода. Чем выше частота встречаемости того или иного кодона, используемого для кодирования аминокислоты в организме, тем с большей скоростью он будет транслироваться рибосомами вследствие высокой внутриклеточной концентрации тРНК, узнающей такой кодон.
Согласно литературным данным кодонная оптимизация активно используется для повышения экспрессии рекомбинантного белка путем увеличения эффективности трансляции кДНК и, тем самым, функциональности интересующего гена [3-5]. Дикий тип нуклеотидной последовательности кодирующей части гена DYSF состоит из 6243 п.н. и содержит тандем редких кодонов, которые могут остановить трансляцию или снизить ее эффективность. Таким образом, кодонная оптимизация позволит увеличить функциональность гена DYSF и экспрессию рекомбинантного белка.
Для оптимизации кодонного состава гена дисферлина DYSF использовали алгоритм OptimumGene, который учитывает различные факторы, влияющие на уровни экспрессии генов, такие как смещение кодонов, GC-состав, содержание CpG-динуклеотидов, вторичную структуру мРНК, тандемные повторы, сайты рестрикции, которые могут помешать клонированию, преждевременные сайты полиаденилирования, дополнительные минорные сайты связывания с рибосомой. В качестве матрицы для кодонной оптимизации была взята нуклеотидная последовательность мРНК гена DYSF (GeneBank #NM_003494). Синтез de novo оптимизированной нуклеотидной последовательности гена dysf был осуществлен компанией GenScript (США).
При оптимизации кодонного состава дикого типа гена DYSF был улучшен индекс адаптации кодонов CAI (англ. Codon Adaptation Index) с 0,83 до 0,88. Для увеличения стабильности мРНК был оптимизирован GC-состав и удалены протяженные участки с высоким сожержанием GC-nap. Кроме того, процесс оптимизации удалил потенциальные цис-действующие сайты.
Таким образом, получена плазмида (pDONR221-Dysf), кодирующая оптимизированную по кодонам последовательность гена DYSF. В результате кодонной оптимизации аминокислотная последовательность дисферлина не изменилась и составила 2080 аминокислотных остатков. pDONR221 (Invitrogen, Catalog #12536-017, США) - вектор-донор (4762 п.н.), предназначен для рекомбинационного клонирования генов в аденовирусный плазмидный вектор pAd/CMV/V5-DEST по технологии Gateway®.
Генетическая конструкция pAd-Dysf получена субклонированием гена DYSF из плазмиды pDONR221-Dysf в аденовирусный плазмидный вектор pAd/CMV/V5-DEST по технологии Gateway® (Invitrogen, США) с помощью реакции LR-рекомбинации. LR-рекомбинация происходит между attL-содержащим вектором-донором и attR-содержащим вектором-реципиентом. После рекомбинации между сайтами attL (L1 и L2)и attR (R1 и R2) образуются сайты для рекомбинации attB (B1 и B2).
Технология Gateway™ основана на сайт-специфической рекомбинационной системе фага λ, которая используется фагом для интеграции в геном Е. coli и перехода между литическим и лизогенным путями.
Полученная таким образом рекомбинантная плазмида, кодирующая аденовирусный геном со вставкой гена DYSF (pAd-DYSF), позволяет получить рекомбинантный аденовирус, содержащий необходимый трансген.
Правильность сборки генетической конструкции проверяли ДНК-секвенированием. Было определено 23 фрагмента, получено полное покрытие открытой рамки считывания гена DYSF. Анализ нуклеотидных последовательностей показал отсутствие мутаций на протяжении всей нуклеотидной последовательности гена дисферлина.
Функциональная активность генетической контрукции подтверждалась анализом экспресси трансгена in vitro. После трансфекции клеток линии НЕК-293Т (АТСС, CRL-11268) полученной генетической конструкцией с использованием трансфекционного агента TurboFect (Fermentas Inc., Канада), анализ экспрессии рекомбинантного белка проводили с помощью иммунофлуоресцентного и вестерн-блот анализов. Иммунофлуоресцентный анализ выявил положительную реакцию с поликлональными антителами кролика к дисферлину. Вестерн-блот анализ белковых лизатов клеток НЕК-293Т показал наличие выраженной специфичной полосы иммунопреципитата, соответствующей ожидаемой молекулярной массе белка дисферлина (231 кДа) (Рис. 1). Таким образом, показана экспрессия белка дисферлина полученной генетической конструкцией pAd-Dysf.
С помощью рестрикции ферментом PacI была получена линейная плазмида pAd-Dysf, которой трансфицировали клетки НЕК-293А (Invitrogen, Catalog #R705-07, США) для сборки и репликации аденовируса. Расщепление вектора способствует взаимодействию левого и правого инвертированных концевых повторов и удалению бактериальных последовательностей (а именно участка начала репликации pUC и гена устойчивости к ампициллину).
Сборка и репликация рекомбинантного аденовируса происходит в клетках линии НЕК-293А - иммортализированная линия первичных человеческих эмбриональных клеток почки, трансформированные фрагментами ДНК аденовируса серотипа 5. Клеточная линия содержит стабильно интегрированную в геном копию гена e1, который экспрессирует белки E1 (Е1а и E1b), необходимые для получения рекомбинантного аденовируса.
После получения неочищенного вирусного лизата путем проведения нескольких циклов замораживания/оттаивания с последующим центрифугированием, для повышения вирусного титра проводили амплификацию аденовируса Ad5-Dysf в клетках НЕК-293А. Через 2 дня после заражения в культуре клеток наблюдался цитопатический эффект, что указывает на то, что клетки продуцируют вирусные частицы.
Рекомбинантный репликационно дефектный аденовирус серотипа 5 Ad5-Dysf, полученный с применением генно-инженерной конструкции pAd-Dysf, содержащей кодон-оптимизированную кДНК, которая кодирует дисферлин человека SEQ ID NO:1, использовали для демонстрации достижения технического результата на модели инфекции культуры клеток НЕК-293Т in vitro. Для этого клетки НЕК-293Т инфицировали полученным рекомбинантным аденовирусом Ad5-Dysf и через 48 часов после вирусной трансдукции проводили анализ экспрессии белка дисферлина с помощью иммунофлуоресцентного анализа (Рис. 2).
Наличие флуоресцентного сигнала в инфицированных клетках НЕК-293Т свидетельствует об экспрессии рекомбинантного белка дисферлина и, следовательно, является подтверждением достижения технического результата.
Полученный аденовирус Ad5-Dysf может быть использован в составе фармацевтической композиции для получения готовой лекарственной формы.
Фармацевтическая композиция для восстановления нарушенной экспрессии и/или функции белка дисферлина в скелетной мышце содержит аденовирус Ad5-Dysf в эффективном количестве и фармацевтически допустимые вспомогательные вещества.
В одном из вариантов фармацевтическая композиция может содержать, в том числе, добавку для трансдукции аутологичных клеток в случае реализации генно-клеточного подхода и трансплантации ген-оптимизированных клеток.
Раствор аденовируса Ad5-Dysf, пригодный для последующего получения фармацевтической композиции и готовой лекарственной формы, может быть получен при помощи стандартных методов выделения и очистки вирусов, известных специалисту в данной области техники.
Готовая лекарственная форма должна быть пригодна для проведения геннотерапии и не должна приводить к существенному изменению свойств основного вещества при продолжительном хранении. Возможная готовая лекарственная форма аденовируса Ad5-Dysf может быть выбрана из группы замороженного раствора, жидкого раствора, лиофилизата, то есть лиофильно высушенного раствора, аморфной пленки, но не ограничивается ими.
Предпочтительными вариантами готовой лекарственной формы являются жидкий раствор или лиофилизат, поскольку они могут храниться при положительной температуре, то есть в стандартных фармацевтических холодильниках, и не требуют значительного времени для подготовки к инъекции.
Наиболее предпочтительным вариантом готовой лекарственной формы является лиофилизат, поскольку отсутствие воды потенциально замедляет химические реакции распада цепей ДНК.
Получение лиофилизата, то есть аморфной или микрокристаллической пористой массы, требует присутствия в лиофилизуемом растворе вспомогательных веществ, выполняющих функции криопротектанта, стабилизатора pH, хелатирующего агента, антиоксиданта, наполнителя и т.д. Минимально возможный набор вспомогательных веществ может включать в себя по меньшей мере один криопротектант, обладающий свойствами наполнителя и стабилизатор pH. Вспомогательное вещество, являющееся криопротектантом и наполнителем, может быть выбрано из группы, включающей моно- и дисахариды, полиолы и полимеры, такие как: сахароза, лактоза, трегалоза, маннитол, сорбитол, глюкоза, раффиноза, поливинилпирролидон или их сочетания. Стабилизатор pH может быть выбран из группы, включающей цитрат натрия, фосфат натрия, Трис-HCl, Трис-ацетат, глицин и другие аминокислоты.
Способ получения лиофилизата может предусматривать добавление к аденовирусу Ad5-Dysf растворов, по меньшей мере, одного криопротектанта, обладающего свойствами наполнителя, и стабилизатора pH с получением изотонического раствора с концентрацией полученного аденовируса от 1×109 до 1×1011 БОЕ/мл (Бляшкообразующих единиц в 1 мл) и pH от 7,0 до 9,0 и последующую лиофилизацию и хранение при температуре от +2°C до +8°C.
Способ применения фармацевтической композиции заключается во введении ее человеку (или животным) таким способом и в таком количестве, которые обеспечат лечебный эффект в зависимости от нозологической формы и медицинских показаний.
Фармацевтическая композиция может вводиться внутримышечно - местно, системно - внутривенно, аэрозольно, в виде генно-клеточной трансплантации или трансфузии после in vitro обработки различных аутологичных клеток, например гемопоэтических и их более дифференцированных производных, мезенхимальных, сосудисто-стромальной фракции, мезангиобластов, миобластов, миосателлитоцитов и др.
Хотя указанные изобретения описаны в деталях, для специалиста в данной области техники очевидно, что могут быть совершены различные изменения и произведены эквивалентные замены, и такие изменения и замены не выходят за рамки настоящего изобретения.
Использованные источники
1. Acsadi, G., et al., Human dystrophin expression in mdx mice after intramuscular injection of DNA constructs. Nature, 1991. 352(6338): p.815-8.
2. Lostal, W., et al., Efficient recovery of dysferlin deficiency by dual adeno-associated vector-mediated gene transfer. Hum Mol Genet, 2010. 19(10): p.1897-907.
3. Deml, L., et al., Multiple effects of codon usage optimization on expression and immunogenicity of DNA candidate vaccines encoding the human immunodeficiency virus type l Gag protein. J Virol, 2001. 75(22): p.10991-1001.
4. Kim, C.H., Y. Oh, and Т.Н. Lee, Codon optimization for high-level expression of human erythropoietin (EPO) in mammalian cells. Gene, 1997. 199(1-2): p.293-301.
5. Takenaka, Y., et al., Transformation of Paramecium caudatum with a novel expression vector harboring codon-optimized GFP gene. Gene, 2002. 284(1-2): p.233-40.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ сохранения статической выносливости у дисферлин-дефицитных мышей в эксперименте | 2023 |
|
RU2829651C1 |
| Способ коррекции миодистрофии с использованием аденоассоциированного вирусного вектора в эксперименте | 2022 |
|
RU2821544C1 |
| Способ повышения физической выносливости в эксперименте на дисферлин-дефицитных мышах | 2023 |
|
RU2833672C1 |
| Способ коррекции миодистрофии с использованием плазмидной ДНК у дисферлин-дефицитных мышей | 2022 |
|
RU2805357C1 |
| СИНТЕТИЧЕСКАЯ МОЛЕКУЛА НУКЛЕИНОВОЙ КИСЛОТЫ (ВАРИАНТЫ), ЭКСПРЕССИОННЫЙ ВЕКТОР ДЛЯ КЛЕТОК МЛЕКОПИТАЮЩЕГО, КЛЕТКА МЛЕКОПИТАЮЩЕГО ХОЗЯИНА И СПОСОБ ЭКСПРЕССИИ ЧЕЛОВЕЧЕСКОГО БЕЛКА АНТИГЕНА ЭПИДЕРМАЛЬНОГО ФАКТОРА РОСТА-2 (HER2/neu) ИЛИ ЕГО УКОРОЧЕННОЙ ФОРМЫ | 2004 |
|
RU2397249C2 |
| СЛИТЫЕ БЕЛКИ КАРЦИНОЭМБРИОНАЛЬНОГО АНТИГЕНА | 2005 |
|
RU2380375C2 |
| КОДОН-ОПТИМИЗИРОВАННЫЕ ПОСЛЕДОВАТЕЛЬНОСТИ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ВОССТАНОВЛЕНИЯ КРОВЕНОСНЫХ СОСУДОВ | 2014 |
|
RU2557385C1 |
| Способ повышения физической работоспособности с использованием аденоассоциированного вирусного вектора в эксперименте на дисферлин-дефицитных мышах | 2023 |
|
RU2828839C1 |
| СЛИТЫЙ БЕЛОК ТЕЛОМЕРАЗНОЙ ОБРАТНОЙ ТРАНСКРИПТАЗЫ, КОДИРУЮЩИЕ ЕГО НУКЛЕОТИДЫ И ИХ ПРИМЕНЕНИЕ | 2007 |
|
RU2473691C2 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДА pAd-SM, КОДИРУЮЩАЯ БЕЛКИ SOX2 И C-MYC ЧЕЛОВЕКА, ЯВЛЯЮЩАЯСЯ ОСНОВОЙ ДЛЯ ПОЛУЧЕНИЯ ВИРУЛЕНТНЫХ АДЕНОВИРУСОВ, ПРЕДНАЗНАЧЕННЫХ ДЛЯ ПОЛУЧЕНИЯ ИНДУЦИРОВАННЫХ ПЛЮРИПОТЕНТНЫХ КЛЕТОК ЧЕЛОВЕКА | 2012 |
|
RU2495127C2 |




Изобретение относится к области биотехнологии и касается кДНК, кодирующей дисферлин человека, генно-инженерной конструкции, в которую клонирована такая кДНК, рекомбинантного аденовируса и фармацевтической композиции. Описанная генно-инженерная конструкция содержит экспрессионный плазмидный аденовирусный вектор pAd/CMV/V5-DEST, в который клонирована по сайтам для рекомбинации attB1 и attB2 кодон-оптимизированная кДНК, имеющая последовательность, представленную в SEQ ID NO: 1 и кодирующая дисферлин человека. Рекомбинатный репликационно дефектный аденовирус серотипа 5 получают с применением такой генно-инженерной конструкции и включают в фармацевтическую композицию в эффективном количестве. Изобретения позволяют восстановить нарушенную экспрессию и/или функцию белка дисферлина в скелетной поперечно-полосатой мышечной ткани и вызывать стабильный положительный эффект. 4 н.п. ф-лы, 2 ил.
1. Кодон-оптимизированная кДНК, представленная в SEQ ID NO: 1, кодирующая дисферлин человека.
2. Генно-инженерная конструкция для получения рекомбинантного репликационно дефектного аденовируса серотипа 5, представляющая собой экспрессионный плазмидный аденовирусный вектор pAd/CMV/V5-DEST, в который клонирована по сайтам для рекомбинации attB1 и attB2 кодон-оптимизированная кДНК, кодирующая дисферлин человека SEQ ID NO: 1.
3. Рекомбинантный репликационно дефектный аденовирус серотипа 5, полученный с применением генно-инженерной конструкции по п.2 для получения фармацевтической композиции.
4. Фармацевтическая композиция для восстановления нарушенной экспрессии и/или функции белка дисферлина в скелетной мышце, содержащая аденовирус по п.3 в эффективном количестве и фармацевтически допустимые вспомогательные вещества.
| US 20100266551 A1, 21.10.2010 | |||
| US 20030110526 A1, 12.06.2003 | |||
| US 20090041764 A1, 12.02.2009 |
Авторы
Даты
2014-08-27—Публикация
2012-12-24—Подача