Изобретение относится к микробиологии и может быть использовано при культивировании сублимированных культур вакцинных и референтных (экспериментальных) штаммов микроорганизмов после длительного хранения или пребывания в неблагоприятных условиях, а также при контроле исходных штаммов в производстве вакцины.
Общепринятые в микробиологии способы культивирования микроорганизмов предусматривают использование элективных питательных сред, содержащих ингибиторы, стабилизаторы, стимуляторы роста, энергообеспечивающие, чаще всего углеродсодержащие вещества, способствующие выделению культур.
Как правило, преследуется цель повышения эффективности выживаемости культур сублимированных штаммов, увеличения выхода бактериальной массы, сокращение времени культивирования.
Известен способ выделения холерных вибрионов, включающий посев и выращивание исследуемого материала из объектов внешней среды на щелочную питательную среду (Хоттингера, Мартена, из сердечной мышцы, рН 7,8-8,0), в которую добавлена сахароза, теллурит калия и фосфомицин [Патент РФ №2039826, C12Q 1/04, C12N 1/00, от 20.07.95, Бюл. №20]. Использование этого способа исключает пересев материала, ускоряет анализ и обеспечивает надежность обнаружения возбудителя холеры в объектах внешней среды.
Известна питательная среда для выращивания холерного вибриона на основе бульона Хоттингера, в которую в качестве стимулятора роста добавляют смесь ганглиозидов из мозгов быка или свиньи [А.с. СССР №1637326, C12N 1/20, C12Q 1/04, 1989]. При использовании этой среды скорость размножения вибрионов увеличивается в 3-3,5 раза. Известна плотная питательная среда для выращивания чумного микроба на основе гидролизата казеина и бульона Хоттингера, которая в качестве стимулятора роста содержит дрожжевой экстракт, в качестве углевода - маннит, а также минеральные соли [А.с. СССР №738998, C12K 1/06, 07.06.81, Бюл. №21].
Использование такой среды обеспечивает получение бактериальной массы с полноценным антигенным составом фракций FI, V и W, необходимых для получения вакцин.
В микробиологической промышленности известно использование ряда эффективных стимуляторов роста микроорганизмов. При использовании в питательной среде ферментативного гидролизата плодов крупного рогатого скота в качестве белковой основы наблюдается значительное повышение выхода биомассы Yersinia pestis EV, Escherichia coli по сравнению с питательной средой на основе бульона Хоттингера культур за счет сбалансированного содержания азота, белка, кальция, магния, железа, фосфора [А.с. СССР №1586180, C12N 1/20, 1989].
Значительно повышается выход биомассы и сокращается время культивирования микроорганизмов бруцеллеза, кишечных инфекций, сибирской язвы и др. при внесении в питательную среду в качестве стимуляторов роста диметилсульфоксида, питуитрина или гифотоцина, последние из которых являются гормональными препаратами [А.с. СССР №1834288, C12N 1/20, 1/38, 1990].
Анализ известных решений и их экспериментальные испытания свидетельствуют о некоторых общих недостатках.
Основным недостатком является то, что не учитывается тот факт, что при хранении культур сублимированных штаммов часть клеток теряет свою жизнеспособность, что снижает их способность к росту, биосинтезу, сохранению специфической морфологической структуры.
Известна среда для регидратации лиофилизированной культуры возбудителя мелиоидоза, содержащая раствор хлорида натрия, агар-агар, гидролизат казеина, желатину и сахарозу [А.с. СССР №1616137, C12N 1/20, 1/04 // (C12N 1/20; C12R 1/38), 1989].
Однако при культивировании штаммов после долгого хранения на такой среде не обеспечивается достаточной степени повышения жизнеспособности клеток.
Известен способ культивирования лиофилизированной культуры возбудителя мелиоидоза, согласно которому культуру высевают на плотную питательную среду на основе мясопептонного бульона и глицерина и обогащенную после ее охлаждения пируватом натрия в количестве 0,3-1,2% от объема среды с последующим инкубированием в желатине в течение 72 часов. Пируват натрия представляет собой соль пировиноградной кислоты. [А.с. СССР №1616138, C12N 1/20 (C12N 1/20, C12R 1/38), 1989].
Недостатком прототипа является недостаточно высокий выход жизнеспособных клеток.
Известно использование этилового спирта в количестве 1,0-1,5% от массы среды в качестве источника углерода в селективной среде для выделения флуоресцирующих псевдомонад, которая также содержит в качестве стимулятора роста и источника азота - диаммоний янтарнокислый и, кроме того, калий фосфорнокислый двузамещенный, сернокислый магний, краситель, агар и воду [А.с. СССР №1299142, C12N 1/20, C12R 1/40, 1985].
Известно использование этилового спирта в количестве 4,0-7,0% от объема среды в качестве стимулятора роста в питательной среде для выращивания белок А продуцирующих бактерий, которая содержит также глюкозу и в качестве питательной основы - ферментативно-кислотные гидролизаты форменных элементов крови сыворотки крупного рогатого скота [А.с. СССР №16303146 C12N 1/20, 1989]. Использование 96° этилового спирта в питательных средах, указанного выше состава, в первом случае обеспечивает углеродный энергетический запас среды при селективном выделении флуоресцирующих псевдомонад, во втором значительное увеличение выхода биомассы белок А продуцирующих бактерий за счет стимуляции их роста по сравнению с выращиванием в бульоне Хоттингера (без спиртовой добавки), однако при культивировании долго хранившихся сублимированных штаммов или исследуемого материала, пребывавшего в неблагоприятных условиях, не обеспечивается контролируемого повышения жизнеспособности клеток.
Наиболее близким к заявляемому способу культивирования сублимированных культур микроорганизмов является описание способов повышения выживаемости микробных клеток в сухих живых вакцинах и пробиотиках (Светлакова Е.В., 2003). Это описание приведено в диссертационных материалах Е.В. Светлаковой, показаны свойства стимулятора роста микроорганизмов (СРМ ТС-1), получаемого на основе «чайного гриба» - Medusomyces Gisevi. В культуральной жидкости «чайного гриба» сохраняются основные компоненты чая (кофеин, танин, витамины Bi, С, Р и др.), а также образуется небольшое количество спирта, углекислого газа, сахара, уксусной кислоты, а также вещества, подавляющие развитие ряда микроорганизмов. Кроме того, в вышеназванной работе показано: «Добавление определенного количества СРМ ТС-1 к основным питательным средам приводит к увеличению накопления общей биологической массы культивируемых микробов на 22-48%, увеличению количества живых микробных клеток на 11-35%, а также обеспечиванию наибольшей выживаемости микробных клеток после лиофильной сушки. При этом не только сохраняются, но и повышаются антигенные и иммуногенные свойства перечисленных микроорганизмов. (Светлакова Е.В. Совершенствование способов повышения выживаемости микробных клеток в сухих живых вакцинах и пробиотиках: диссертация… кандидата биологических наук: 03.00.23. - Ставрополь, 2003. - 164 с.: ил. РГБ ОД, 61-033/1093-3). См. сайт: © 2007-2013 Электронная библиотека диссертаций .
Техническим результатом изобретения является повышение выхода жизнеспособных клеток сублимированных культур вакцинных и референтных штаммов, высеваемых на элективных плотных питательных средах.
Указанный технический результат достигается тем, что способ культивирования сублимированных культур вакцинных и референтных штаммов микроорганизмов: Yersinia pestis EV, Brucella abortus 19 BA, Bacillus anthracis СТИ, Eschericha coli С 600, Vibrio NAG 504, включающий внесение в элективную для каждого вида плотную питательную среду в качестве стимулятора роста и источника углерода 96° этилового спирта в количестве 1,0-2,0% от объема среды для увеличения их выживаемости.
По отношению к прототипу заявляемый способ имеет следующие отличительные признаки.
Введение в питательную среду в качестве стимулятора роста и источника углерода этилового спирта в количестве 1,0-2,0% от объема среды увеличивает выход жизнеспособных клеток на 30-49% по сравнению с культивированием на традиционных элективных питательных средах. Снижение вводимого стимулятора ниже 1,0% не обеспечивает необходимого эффекта, а увеличение более 2,0% приводит к подавлению роста бактерий.
Точные количественные характеристики повышения эффективности роста сублимированных культур вакцинных и референтных штаммов микроорганизмов могут быть получены при последующем посеве материала на элективной плотной питательной среде за счет добавления стимулятора роста - 96% этилового спирта в оптимальной концентрации, определенной опытным путем.
Использование в питательных средах в качестве стимулятора роста и источника углерода этилового спирта в заявляемых количествах - 1,0-2,0% к объему среды - обеспечивает повышение выхода жизнеспособных клеток различных видов микроорганизмов на 30-49% по сравнению с плотными питательными средами на основе агара Хоттингера рН 7,3, рН 7,8, Альбими агара, соответственно, используемых для культивирования возбудителей чумы, сибирской язвы, кишечной палочки, вибрионов бруцелл.
Сравнительные результаты влияния различных количеств этилового спирта на выживаемость некоторых грамотрицательных и грамположительных бактерий приведены в таблице 1. Эти данные получены на основании средних результатов не менее трех раз повторенных опытов.
Возможность практического использования заявляемого способа иллюстрируется примерами его конкретного выполнения.
Пример 1. Плавили агар Хоттингера в объеме 400 мл и в 8 мерных флаконов вносили по 50 мл агара. В каждый из 7 флаконов при температуре 45-47°C дополнительно вносили соответствующие объемы 96° стерильного этилового спирта (0,25, 0,5, 1,0, 1,5, 2,0, 2,5, 3,8 мл). Из каждого флакона готовили по 2 чашки, которые подсушивали. Хранившиеся >10 лет сублимированные культуры чумного вакцинного штамма ресуспендировали в 2 мл физиологического раствора и затем посевные дозы его раститрованной суспензии по 0,5 мл наносили на каждую чашку из разведений 10-6, 10-7, 10-8. Культивировали при 28-30°C. Учет посевов производили через 48±2, 72±3 часов. Подсчитывали среднее число выросших колоний из различных разведений на средах с различным содержанием этилового спирта, определяли увеличение выживаемости клеток чумного вакцинного штамма в процентах по отношению разницы КОЕ/из посевной дозы в опыте и контроле к контролю, данные систематизировали в таблице 1.
Примеры 2 и 3. Не отличаются по методике выполнения от примера 1, за исключением того, что в них испытаны штаммы кишечной палочки и сибиреязвенного вакцинного штамма СТИ, а посевы культивировали при 37°C.
Пример 4. Не отличается по методике выполнения от примера 1, за исключением того, что в нем испытана культура штамма неагглютинирующегося вибриона и использован элективный щелочной агар (рН 7,8), а посевы культивировали при 37°C.
Пример 5. Не отличается по методике выполнения от примера 1, за исключением того, что в нем испытана сублимированная культура бруцеллезного вакцинного штамма и использовали элективную плотную питательную среду Альбими, а посевы культивировали при 37°C.
Таким образом, заявляемый способ практически осуществим и прост в исполнении. Использование предлагаемого способа культивирования сублимированных культур вакцинных и референтных штаммов микроорганизмов в микробиологической практике и экспериментальной работе повысит надежность анализов при культивировании материала после длительного хранения, а также при контроле штаммов и наращивании бактериальной массы в производстве вакцины.
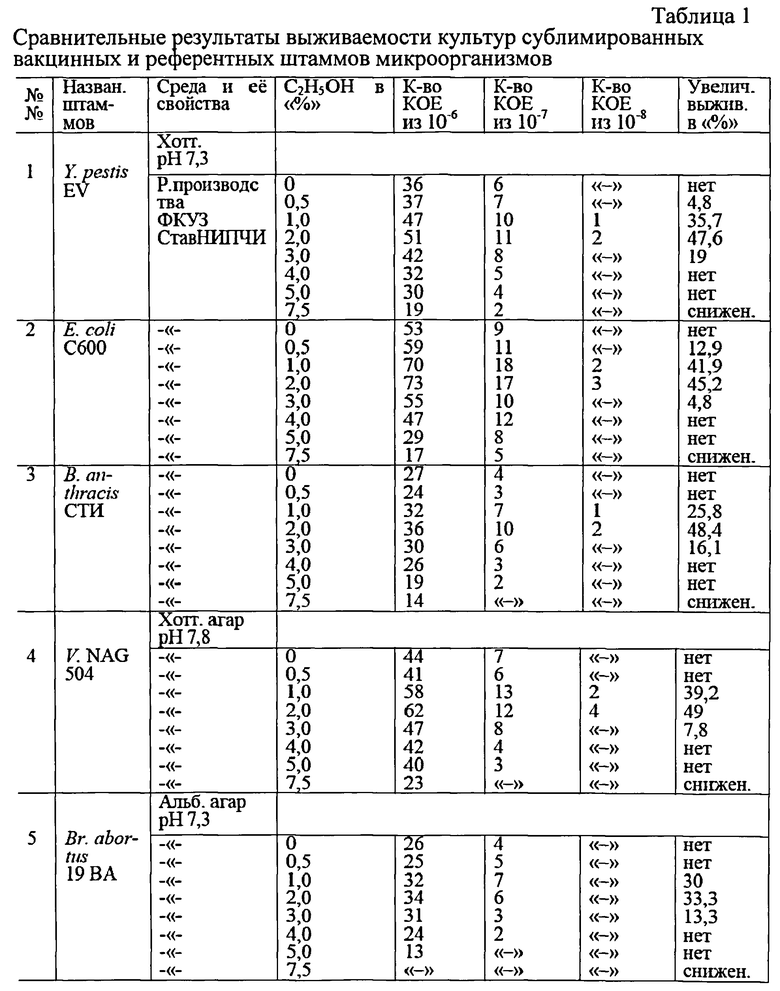
Примечание к таблице 1: выживаемость определяли по отношению разницы КОЕ/из посевной дозы в опыте и контроле к контролю. «-» - нет роста.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КУЛЬТИВИРОВАНИЯ МИКРООРГАНИЗМОВ | 1999 |
|
RU2163265C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПИТАТЕЛЬНОЙ ОСНОВЫ И ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ КУЛЬТИВИРОВАНИЯ МИКРООРГАНИЗМОВ РОДА YERSINIA И VIBRIO | 2007 |
|
RU2360962C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭМБРИОНАЛЬНОГО СТИМУЛЯТОРА РОСТА МИКРООРГАНИЗМОВ | 2004 |
|
RU2283347C2 |
| ПИТАТЕЛЬНАЯ СРЕДА ЖИДКАЯ ДЛЯ ГЛУБИННОГО ВЫРАЩИВАНИЯ ВАКЦИННОГО ШТАММА ЧУМНОГО МИКРОБА Y. PESTIS EV | 2021 |
|
RU2757428C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИМИТАТОРОВ ПАТОГЕННЫХ БИОЛОГИЧЕСКИХ АГЕНТОВ | 2015 |
|
RU2607369C1 |
| ПИТАТЕЛЬНАЯ СРЕДА ЖИДКАЯ ДЛЯ ВЫРАЩИВАНИЯ И СБРОСА БИОМАССЫ ВАКЦИОННОГО ШТАММА ЧУМНОГО МИКРОБА YERSINIA PESTIS EV | 2020 |
|
RU2745504C1 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ КУЛЬТИВИРОВАНИЯ YERSINIA PESTIS EV | 2018 |
|
RU2708029C1 |
| СПОСОБ ВЫДЕЛЕНИЯ ЧУМНОГО МИКРОБА БАКТЕРИОЛОГИЧЕСКИМ МЕТОДОМ ИЗ ИССЛЕДУЕМОГО МАТЕРИАЛА (ВАРИАНТЫ) | 2007 |
|
RU2353654C1 |
| СПОСОБ ПОВЫШЕНИЯ ИММУНОГЕННОСТИ ВАКЦИОННОГО ШТАММА ЧУМНОГО МИКРОБА | 2019 |
|
RU2727258C1 |
| ПИТАТЕЛЬНАЯ СРЕДА ПЛОТНАЯ ДЛЯ КУЛЬТИВИРОВАНИЯ И СБОРА БИОМАССЫ ВАКЦИННОГО ШТАММА ЧУМНОГО МИКРОБА Y.pestis EV | 2018 |
|
RU2702174C1 |
Изобретение относится к микробиологии. Способ культивирования сублимированных штаммов микроорганизмов предусматривает внесение в плотную питательную среду стимулятора роста и источника углерода с последующим посевом клеток микроорганизма, инкубацией посевов и учетом жизнеспособных микробных клеток. В качестве сублимированных штаммов микроорганизмов используют Yersinia pestis EV, Escherichia coli C600, Bacillus anthracis СТИ, Vibrio cholerae NAG 504, Brucella abortus 19BA. В качестве стимулятора роста и источника углерода используют 96% этиловый спирт в количестве 1,0-2,0% от объема среды. При необходимости добавляют генцианвиолет в концентрации 1:100000. Изобретение обеспечивает повышение выхода жизнеспособных клеток штаммов на плотных питательных средах. 1 табл., 5 пр.
Способ культивирования сублимированных штаммов микроорганизмов, включающий внесение в плотную питательную среду стимулятора роста и источника углерода с последующим посевом клеток микроорганизма, инкубацией посевов и учетом жизнеспособных микробных клеток, отличающийся тем, что сублимированными штаммами микроорганизмов являются Yersinia pestis EV, Escherichia coli C600, Bacillus anthracis СТИ, Vibrio cholerae NAG 504, Brucella abortus 19BA, в качестве стимулятора роста и источника углерода используют 96% этиловый спирт в количестве 1,0-2,0% от объема среды, при этом происходит стимуляция роста на плотных питательных средах, при необходимости добавляют генцианвиолет в концентрации 1:100000.
| SU 1616138 A1, 27.04.1999 | |||
| SU 1616137 A1, 20.05.1999 | |||
| FRIED V.A | |||
| AT AL | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| Приспособление для склейки фанер в стыках | 1924 |
|
SU1973A1 |
| CHATTERJEE I | |||
| ET AL | |||
| Very low ethanol concentration | |||
Авторы
Даты
2014-11-10—Публикация
2012-09-20—Подача