Одна из важнейших функций крови состоит в переносе поглощаемого в легких кислорода: органам и тканям, а также в удалении образующегося в них диоксида углерода. Ключевую роль во всех этих процессах играют эритроциты. Эти клетки содержат гемоглобин, способный соединяться с кислородом и высвобождать его в капиллярах тканей. В состав молекулы гемоглобина входят четыре одинаковые гемовые группы. Ключевую роль в активности гемоглобина играет двухвалентный ион железа, расположенный в центре каждого из четырех гемов. Молекула O2 обратимо связывается с гемом. Присоединив кислород, гемоглобин (Hb) превращается в оксигемоглобин (HbO2). Валентность железа при этом не изменяется. Этот процесс называется оксигенацией, а обратный процесс называете дезоксигенацией. Гемоглобин, не связанный с кислородом, называют дезоксигемоглобином.
Гем может подвергаться не только оксигенации, но и истинному окислению. При этом железо становится из двухвалентного трехвалентным. Гемоглобин превращается в метгемоглобин (MetHb). Окисленный гем не способен переносить кислород к тканям. Возникает гипоксия тканей. При уровне MetHb 30-50% наблюдаются тяжелые клинические проявления. В настоящее время в связи с развитием фармакологической и химической промышленности все чаще стали встречаться метгемоглобинемии экзогенного происхождения. Повышенное метгемоглобинообразование в организме человека наблюдается у рабочих при производстве анилина, нитробензола, капрона, свинца и других продуктов химического производства, а так же при употреблении целого ряда лекарственных препаратов (аспирин, нитроглицерин, пирамидон и др.).
В крови человека метгемоглобин содержится в незначительных количествах. Но при некоторых заболеваниях и отравлениях его содержание возрастает. К метгемоглобинобразователям относятся анилин и его производные, аминофенолы и аминофеноны, хлораты, дапсон, некоторые местные анестетики (например, бензокаин), нитриты и нитраты, нафталин, нитробензол и его производные, оксид азота, феназопиридин, примахин и сходные с ним противомалярийные средства и некоторые сульфаниламиды.
Для лечения метгемоглобинемии применяется аскорбиновая кислота. Аскорбиновая кислота способна взаимодействовать с токсикантами в эритроцитах. Однако скорость процесса низка (С.А.Куценко. Основы токсикологии. // Биомедицинский журнал http://Medline.ru. Том 4, стр.119. Март, 2003).
Считается, что лечение аскорбиновой кислотой неэффективно при острой метгемоглобинемии. (Kambiz Soltaninejad, Leiws S. Nelson, Nastaran Khodakarim, Zohreh Dadvar, and Shahin Shadnia Unusual complication of aluminum phosphide poisoning: Development of hemolysis and methemoglobinemia and its successful treatment // Indian J Crit Care Med. 2011 Apr-Jun; 15(2): 117-119). Кроме этого, прием аскорбиновой кислоты в дозах, превышающих физиологические, может укорачивать протромбиновое время, разрушать витамин В12, способствовать образованию оксалатных камней в мочевыводящих путях, оказывать угнетающее влияние на инсулярный аппарат поджелудочной железы, стимулировать образование кортикостероидных гормонов, что при известных условиях может привести к повреждению клубочков почек и развитию артериальной гипертензии. (Е.Г.Казанец Федеральный научно-клинический центр детской гематологии, онкологии, иммунологии, Москва. Метгемоглобинемии // Детская больница. 2009. №1. С.38-42).
Известен метод лечения метгемоглобинемии с помощью внутривенного введения метиленового синего в дозе 1-2 мг/кг. Этот способ базируется на восстановлении окисленного трехвалентного железа до двухвалентного.
Недостатком данного способа является то, что метиленовый синий сам по себе является окисляющим агентом, особенно в больших дозах (как правило, более 4 мг/кг), метиленовый синий может действовать преимущественно в качестве окисляющего агента. У некоторых пациентов после введения метиленового синего происходило первоначальное снижение уровня метгемоглобина, а затем позднее происходил вторичный рост уровня метгемоглобина. При этом метиленовый синий может вызвать развитие гемолитической анемии и метгемоглобинемии. Зарегистрированы клинические осложнения при внутривенном введении метиленового синего пациентам с дефицитом глюкозо-6-фосфатдегидрогеназы, а также маленьким детям. Следовательно, терапия метиленовым синим может иногда быть полностью неэффективной для таких пациентов.
(Greenberg, Michael I. MD, MPH Methylene Blue: Fast-Acting Antidote for Methemoglobinemia // Emergency Medicine News. September 2001 - Volume 23 - Issue 9 - p.26 Toxicology Rounds, doi: 10.1097/01. EEM. 0000292322.94148.37)
Задача изобретения - способ лечения метгемоглобинемии, обладающий меньшими побочными действиями.
Поставленная задача решается способом лечения метгемоглобинемии, заключающемся в том, что внутривенно в кровь вводят перфторан (ПФ) 5-20 мл на 1 кг массы тела.
Способ основан на впервые выявленном нами свойстве ПФ превращать метгемоглобин в оксигемоглобин.
Известно, то «Перфторан» (эмульсия перфтордекалина) (Л.А.Богданова, Е.И.Маевский, Р.Я.Сенина, С.Ю.Пушкин, О.Г.Аксенова, Г.Р.Иваницкий. Краткий обзор клинического применения перфторана // Биомедицинский журнал http://Medline.ru. Февраль, 2001 г. Том 2. СТ.5. Стр.30-36) - кровезаменитель с газотранспортной функцией, обладающий полифункциональным действием. Поэтому его можно вводит пациенту в кровь, не опасаясь токсического действия. ПФ вводится внутривенно из расчета от 1 до 30 мл на 1 кг веса (и более при острых массивных кровопотерях). Возможно повторное введение препарата в той же дозе с интервалом от нескольких часов (при массивной кровопотере) до 3 дней.
Для лечения острой кровопотери вводят ПФ в большей концентрации. (Л.А.Богданова, Е.И.Маевский, Р.Я.Сенина, С.Ю.Пушкин, О.Г.Аксенова, Г.Р.Иваницкий. Краткий обзор клинического применения перфторана// Биомедицинский журнал http://Medline.ru. Февраль, 2001 г. Том 2. СТ.5. Стр.30-36).
Нижеследующие примеры иллюстрирует способ изобретения.
1. Опыты in vitro
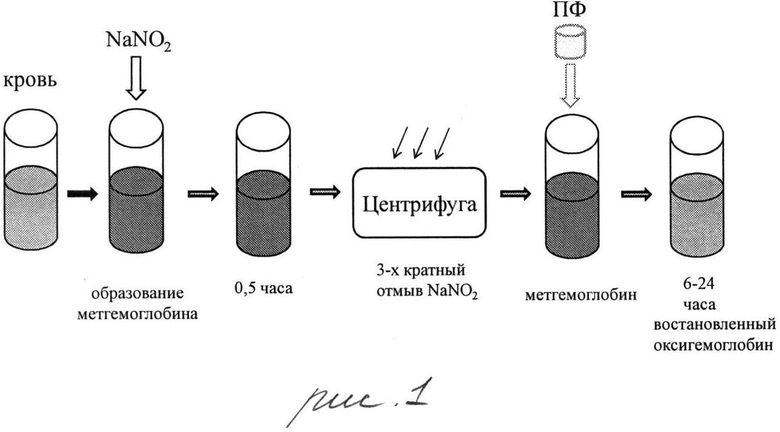
Кровь забирали в микроветты с ЭДТА. Для окисление гемоглобина использовали раствор азотистокислого натрия NaNO2. Для этого приготавливали NaNO2 в дистиллированной воде в концентрации C=0,13 г/мл. В микроветту с кровью (200 мкл) добавляли 10 мкл этого раствора, С=100 мМ (рис.1). Кровь из алой становилась темно-коричневой. Затем кровь 3 раза отмывали от раствора NaNO2 и центрифугировали (2500 об, 5 мин). Каждый раз удаляли 100 мкл физраствора. Затем формировали контрольную суспензию и суспензию с ПФ. Контрольная суспензия: к 100 мкл эритроцитов добавляли 100 мкл физраствора. Суспензия с ПФ - к 100 мкл эритроцитов добавляли 100 мкл ПФ. Обе суспензии по-прежнему оставались коричневой, что качественно свидетельствовало о наличии большого количества MetHb.
На рис.1 представлено превращение оксигемоглобина в метгемоглобин и восстановление метгемоглобина до оксигемоглобина после добавления перфторана.
Через 6-24 час суспензия с ПФ становилась алой, что качественно свидетельствовало о превращении MetHb в HbO2.
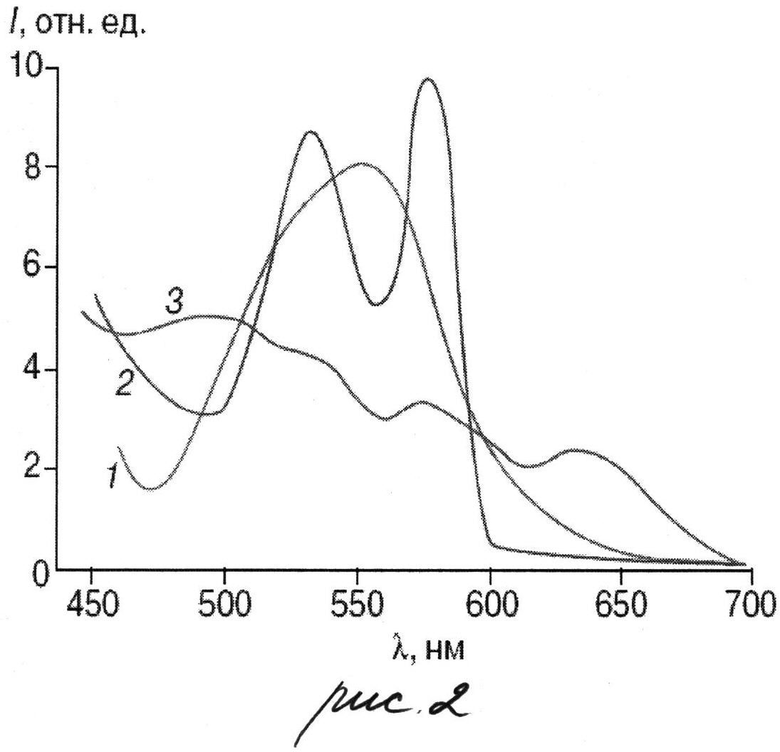
Для количественного определения концентраций производных гемоглобина использовали стандартный спектрофотометрический метод (рис.2). Дезоксигемоглобин имеет максимум в спектре поглощения на длине волны λ=555 нм. Оксигемоглобин - два максимума на λ=542 нм и λ=577 нм (рис.2). Спектр метгемоглобина имеет четыре полосы поглощения, из которых наиболее отчетливая полоса располагается при λ=630 нм.
На рис.2 представлены спектры поглощения: 1 - дезоксигемоглобин; 2 - оксигемоглобин; 3 - метгемоглобин (Блюменфельд Л.А. Гемоглобин // Статьи Соровского Образовательного журнала. 1998.)
На рис.3 представлены фотографии растворов, полученных при добавлении 30 мкл крови в 3 мл дистиллированной воды.
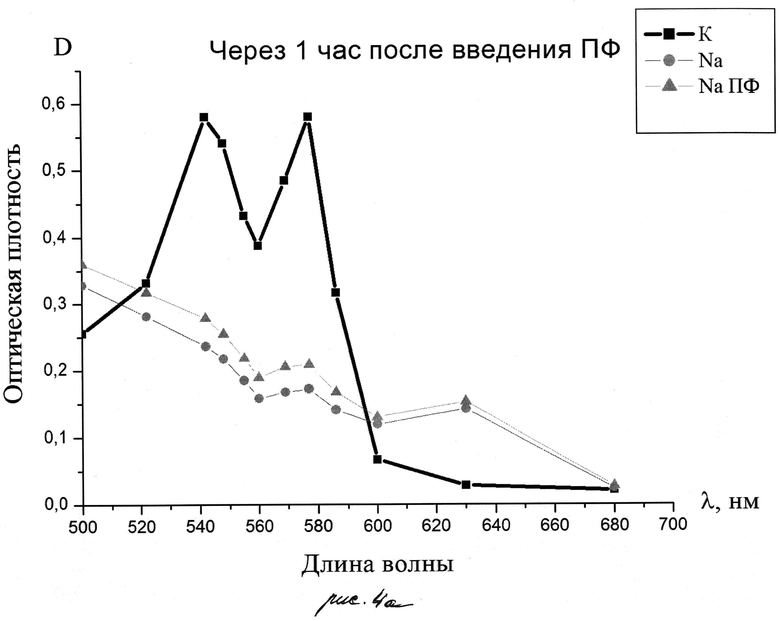
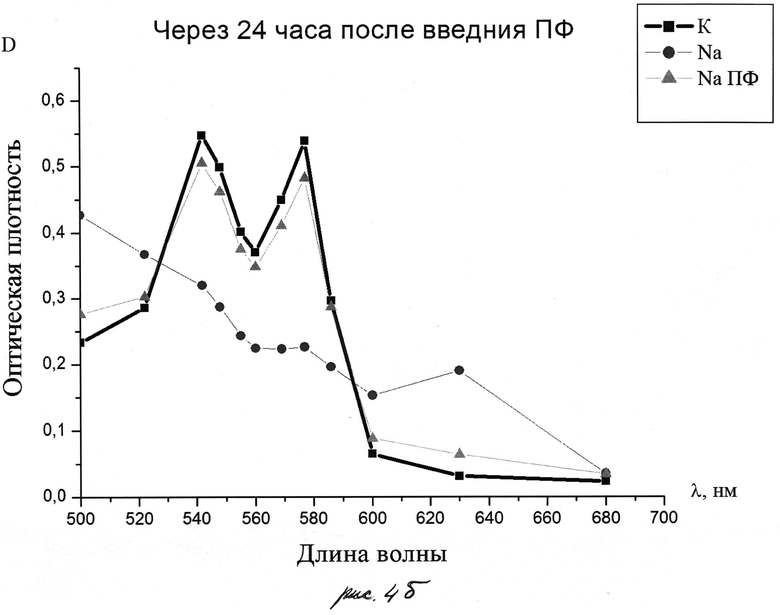
На рис.4. Представлены соответствующие спектры через 1 час после введения ПФ (а), через 24 часа (б)
Для расчета концентраций производных гемоглобина применяли формулы (Стусь Л.Н., Розанова Е.Д. Осцилляция форм гемоглобина в процессе хранения крови. // Биофизика, 1992, 37. С.387-388):
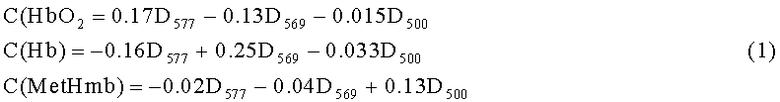
где D577, D569, D500 - значения оптической плотности на длинах волн 577, 569, 500 нм.
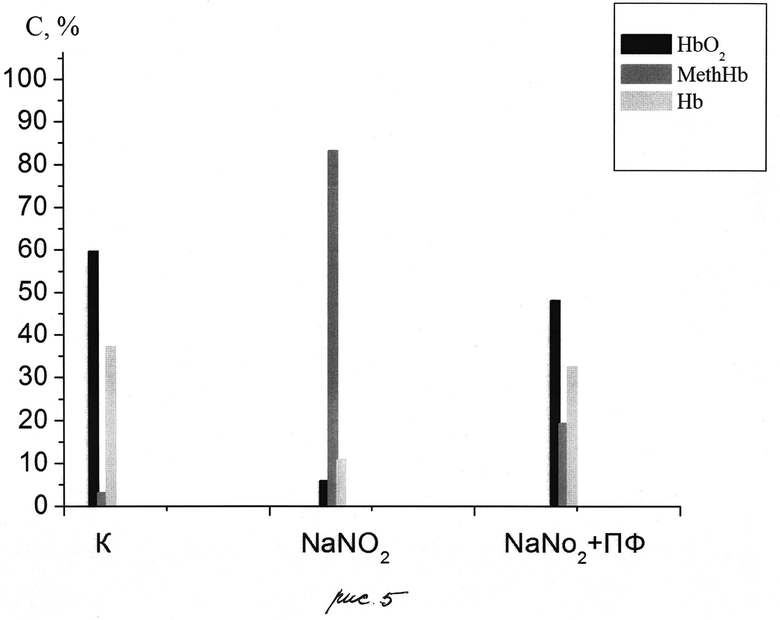
На рис.5 представлены гистограммы концентраций производных гемоглобина в крови в контрольной группе (K), подверженной действию NaNO2, подверженной действию NaNO2 и последующего введения ПФ.
В таблице 1 для сравнения приведены концентрации метгемоглобина и оксигемоглобина в контрольной суспензии, в суспензии после воздействия NaNO2 и после воздействия NaNO2 и последующего введения ПФ.
Таким образом, перфторан эффективно преобразовывает метгемоглобин в оксигемоглобин.
Пример 2. Опыты на лабораторных животных
Эксперименты проводили на нелинейных крысах-самцах массой 470±50 г. У 10 крыс искусственно вызывали метгемоглобинемию путем введения 2%-го раствора солянокислого фенилгидразина из расчета 150 мг на 1 кг веса животного (таблица 2).
В первой группе из 5 животных (нелеченых животных) у четырех крыс произошел летальный исход через 48 часов, у пятой крысы через 48 час уровень MetHb остался тем же, она погибла на 5 сутки.
Во второй группе из 5 животных вводили ПФ в концентрации 20 мл на 1 кг веса. Через 24 часа уровень метгемоглобина снизился до 28-45%. Затем повторили терапию. Для этого снова ввели ПФ в том же количестве. В результате через 48 час от начали лечения ПФ уровень MetHb снизился до 5-17% (таблица 2).
В результате все пять животных испытуемой группы выжили в течение последующих 25 дней наблюдения.
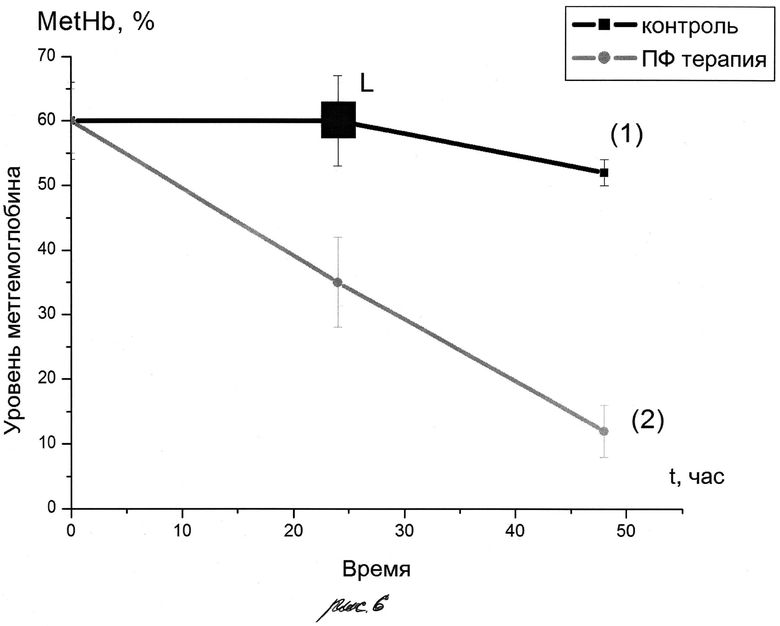
На рис.6 приведены зависимости от времени среднего значения уровня метгемоглобина у крыс в контрольной группе (1) и в группе с терапией ПФ (2). Л - летальный исход у четырех крыс.
Таким образом, приведенные данные свидетельствуют о достижении задачи изобретения лечения метгемоглобинемии.
Следует отметить, при этом ПФ имеет еще другие уже известные полезные свойства, что означает его безопасное применение для трансформации метгемоглобина в оксигемоглобин.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЦИФРОВОЕ УСТРОЙСТВО КОНТРОЛЯ ФИЗИОЛОГИЧЕСКИХ ПОКАЗАТЕЛЕЙ ЗДОРОВЬЯ ПИЛОТА ВОЗДУШНОГО СУДНА | 2021 |
|
RU2766756C1 |
| Способ определения концентраций гемоглобина и его производных в крови | 2017 |
|
RU2663572C1 |
| СПОСОБ ОЦЕНКИ ИНДУЦИРУЮЩЕГО ДЕЙСТВИЯ ОБОСТРЕНИЯ ЦИТОМЕГАЛОВИРУСНОЙ ИНФЕКЦИИ У БЕРЕМЕННОЙ НА ТРЕТЬЕМ ТРИМЕСТРЕ ГЕСТАЦИИ НА СОДЕРЖАНИЕ МЕТГЕМОГЛОБИНА И ОКСИГЕНАЦИЮ ГЕМОГЛОБИНА В ПЕРИФЕРИЧЕСКОЙ КРОВИ НОВОРОЖДЕННОГО | 2013 |
|
RU2536235C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ ГЕМОГЛОБИНА В БИОЛОГИЧЕСКИХ ТКАНЯХ | 2012 |
|
RU2501522C2 |
| ПОЛИФУНКЦИОНАЛЬНЫЙ ПОЛИГЕМОГЛОБИН-ФЕРМЕНТНЫЙ КОМПЛЕКС | 2010 |
|
RU2432172C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИЙ ПРОИЗВОДНЫХ ГЕМОГЛОБИНА В БИОЛОГИЧЕСКИХ ТКАНЯХ | 2013 |
|
RU2517155C1 |
| ДОНОР ОКСИДА АЗОТА, АКТИВИРУЮЩИЙ РАСТВОРИМУЮ ФОРМУ ГУАНИЛАТЦИКЛАЗЫ, ИНГИБИРУЮЩИЙ АГРЕГАЦИЮ ТРОМБОЦИТОВ И ОБЛАДАЮЩИЙ СПАЗМОЛИТИЧЕСКИМ И СОСУДОРАСШИРЯЮЩИМ ДЕЙСТВИЕМ | 2001 |
|
RU2208438C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ ОСНОВНЫХ ПРОИЗВОДНЫХ ГЕМОГЛОБИНА | 1998 |
|
RU2140083C1 |
| КОМПОЗИЦИИ ГЕМОГЛОБИНА | 2010 |
|
RU2589254C2 |
| СПОСОБ РАННЕЙ ДИАГНОСТИКИ МИКРОАНГИОПАТИЙ У БОЛЬНЫХ САХАРНЫМ ДИАБЕТОМ 1-ГО ТИПА | 2005 |
|
RU2316004C2 |

Изобретение относится к медицине и может быть использовано для лечения метгемоглобинемии. Для этого внутривенно вводят перфторан из расчета 5-20 мл на 1 кг массы тела. Изобретение позволяет снизить побочные действия при лечении метгемоглобинемии за счет свойства перфторана превращать метгемоглобин в оксигемоглобин. 6 ил., 2 табл.
Способ лечения метгемоглобинемии, заключающийся в том, что внутривенно вводят перфторан из расчета 5-20 мл на 1 кг массы тела.
| WO 2008007074 A2, 17.01.2008 | |||
| ЭМУЛЬСИЯ ПЕРФТОРОРГАНИЧЕСКИХ СОЕДИНЕНИЙ ДЛЯ МЕДИЦИНСКИХ ЦЕЛЕЙ, СПОСОБ ЕЕ ПРИГОТОВЛЕНИЯ И СПОСОБЫ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЙ С ЕЕ ИСПОЛЬЗОВАНИЕМ | 2000 |
|
RU2206319C2 |
| БОГДАНОВ С.Б., Лечение острой кровопотери с использованием перфторана в условиях ЦРБ, Вестник службы крови России, 2007, N 1, С.26-28.-реферат | |||
| Прибор для нагревания перетягиваемых бандажей подвижного состава | 1917 |
|
SU15A1 |
| SOLTANINEJAD K.et al., Unusual complication of | |||
Авторы
Даты
2014-12-10—Публикация
2013-07-18—Подача