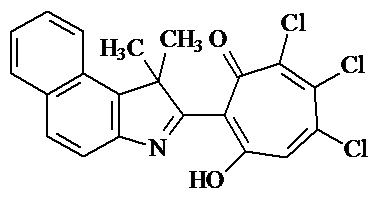
Изобретение относится к новым соединениям в ряду 2-гетарил-1,3-трополонов, в том числе в ряду 2-индолин-2-ил-производных 1,3-трополона, а именно, к неописанному ранее 2-(1,1-диметил-1H-бензо[e]индолин-2-ил)-5,6,7-трихлор-1,3-трополону формулы 1:
 1,
1,
обладающему цитотоксической активностью по отношению к культуре клеток рака кожи А431 и рака легкого Н1299, и может быть использовано при производстве противоопухолевых лекарственных средств.
Онкологические заболевания являются одной из основных причин смерти в мире. Согласно отчету Международного агентства по исследованию рака, в 2020 году во всем мире было зарегистрировано 19,3 миллиона новых случаев рака и почти 10 миллионов смертей от рака, в том числе от рака легких (11,4%), колоректального (10,0%), простаты (7,3%) и рака желудка (5,6%) [1]. В России ежегодно выявляется почти 600 тыс. заболевших раком, умирает от злокачественных новообразований около 300 тыс. онкобольных [2]. Рак является одной из самых значимых медицинских и общественных проблем во многих странах мира, включая Россию. Эта заболеваемость оказывает серьезное воздействие на здоровье населения, экономику и социальное благополучие общества в целом. По распространенности в России лидирующее места среди всех онкологических заболеваний занимают рак молочной железы (12,1%), кожы (кроме меланомы) (11,8%), и рак легкого (9,7%) [2].
Высокая заболеваемость и смертность от рака являются основной мотивацией для разработки и применения новых противоопухолевых лекарственных средств. Несмотря на значительные успехи в лечении рака, многие виды опухолей остаются сложными для лечения и имеют высокую степень сопротивляемости к существующим методам терапии. Для преодоления сложностей в лечении рака и снижения заболеваемости и смертности от этого заболевания важна дальнейшая научная исследовательская работа и разработка перспективных противоопухолевых соединений с улучшенными свойствами и эффективностью.
Тест на жизнеспособность является важной методикой, которая позволяет определить, какие новые противоопухолевые соединения способны оказывать влияние на раковые клетки. Таким образом, данный тест является важным этапом в отборе перспективных соединений для дальнейшей разработки и исследования в области противоопухолевой терапии [3].
В ряду 2-гетарил-1,3-трополонов известен 2-(4h-1,3-бензоксазин-4-он-2-ил)-4,5,6-трихлор-1,3-трополон, обладающий антибактериальной активностью против госпитальных штаммов грамотрицательных и грамположительных бактерий [4]. Известны также 2-гетарилзамещенные 1,3-трополона, обладающие антимикробным действием [5].
Наиболее активны соединения в ряду 2-гетарил-1,3-трополонов против различных линий раковых клеток (H441, A549, OVCAR-3, OVCAR-8, HCT 116 , Panc-1) являются 1,3-трополоны, содержащие акцепторные группы (NO2, Cl) на периферии трополонового кольца, в том числе 5,7-ди(трет-бутил)-2-(4,7-дихлор-8-метил-2-хинолил)-4-нитро-1,3-трополон [6], 5,7-ди(трет-бутил)-2-(4,7-дихлор-8-метил-5-нитро-2-хинолил)-4-нитро-1,3-трополон [6,7] и полихлорированные производные - 2-(4,7-дихлор-8-метил-2-хинолил)-5,6,7-трихлор-1,3-трополон и их смеси [6].
Наиболее близким по выполнению и достигаемому результату является 2-(6,8-диметил-5-нитро-4-хлорхинолин-2-ил)-5,6,7-трихлор-1,3-трополон, обладающий цитотоксической активностью по отношению к культуре клеток рака легкого А549 [8].
Техническим результатом является новое соединение в ряду 2-гетарил-1,3-трополонов, в том числе в ряду 2-индолин-2-ил-производных 1,3-трополонов, обладающее цитотоксической активностью по отношению к культуре клеток рака кожи А431 и рака легкого Н1299.
Технический результат достигается соединением 1.
Синтез соединения 1 заключается в реакции расширения о-хинонового цикла, протекающей между 1,1,2-триметил-1H-бензо[е]индолином 2 и 3,4,5,6-тетрахлор-1,2-бензохиноном 3 при кипячении в диоксане:
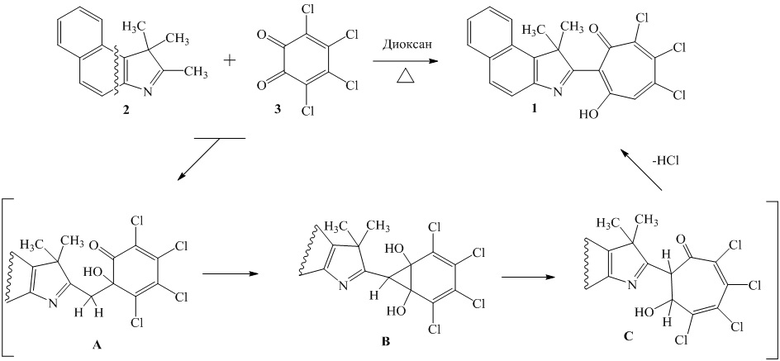
Механизм образования трополоновой системы 1 включает стадию альдольной конденсации с образованием интермедиата А, циклизацию А в норкарадиеновое производное B и перегруппировку B в дигидротрополон С. Окончательное формирование 1,3-трополонового фрагмента сопровождается дегидрохлорированием С, что ведет к основному продукту 1.
Строение соединения 1 установлено данными ЯМР 1Н и ИК-спектроскопии, масс-спектрометрии.
Ниже приведен пример синтеза 2-(1,1-диметил-1H-бензо[e]индолин-2-ил)-5,6,7-трихлор-1,3-трополона 1.
Пример. 2-(1,1-Диметил-1H-бензо[e]индолин-2-ил)-5,6,7-трихлор-1,3-трополон (1). Раствор 1.05 г (5 ммоль) 1,1,2-триметил-1H-бензо[e]индолина (2), 1.23 г (5 ммоль) о-хлоранила (3) в 10 мл диоксана кипятили 1,5 часа с обратным холодильником. Отгоняли растворитель и остаток растворяли в хлористом метилене. Раствор пропускали через хроматографическую колонку с силикагелем (элюент – гексан - СН2Cl2, 1 : 2), собирали жёлто-оранжевую фракцию (1) с Rf=0.4. Перекристаллизовывали из н-гексана. Оранжевые кристаллы. Выход 30%. Tпл. 164-165 ºС (н-гексан).
Спектр ЯМР 1H (CDCl3, δ, м.д., J/Гц): 1.96 (с, 6H, Me(1,1)), 6.90 (с, 1H, H(4)), 7.42 (д, 1Н, Наром., J = 8.6), 7.49 (м, 1H, Hаром.), 7.61 (м, 1H, Hаром.), 7.87 (д, 1H, Hаром., J = 8.6), 7.93 (д, 1H, Hаром., J = 8.2), 8.06 (д, 1H, Hаром., J = 8.5), 15.14 (уш. с, 1Н, ОН). Спектр ЯМР 13С (CDCl3, δ, м.д.): 23.4, 54.6, 77.0, 112.7, 122.5, 125.3, 127.6, 127.9, 130.1, 130.3, 132.6, 133.5, 135.0, 135.9, 180.7. ИК-спектр, ν/см-1: 3040, 2975, 2934, 2867, 1736, 1638, 1536, 1520, 1494, 1466, 1442, 1399, 1372, 1364, 1323, 1261, 1215, 1207, 1174, 1082, 1057, 945, 907, 874, 856, 815, 788, 763, 748, 689. Масс-спектр (ЭУ, 70 эВ), m/z (Iотн (%)): 419 (44) [M+], 417 (44), 389 (66), 378 (27), 374 (82), 353 (17), 339 (60), 304 (18), 275 (24), 241 (35), 194 (72), 191 (26), 165 (60), 152 (100), 147 (26), 139 (30), 127 (35), 121 (35), 115 (21), 106 (16), 87 (12), 84 (21), 77 (15), 63 (23). Найдено (%): C, 60.12; Н, 3.20; N, 3.22. C21H14Cl3NO2. Вычислено (%): C, 60.24; Н, 3.37; N, 3.35.
Исследование фармакологической активности.
Материалы и методы.
Эксперимент проведен на клеточных линиях рака кожи А431 и рака легкого Н1299. Для определения цитотоксической активности нового вещества в отношении данных культур применяли стандартный МТТ тест. МТТ-колориметрический тест для оценки жизнеспособности клеток основан на восстановлении при помощи НАДФ-H-зависимых клеточных оксидоредуктазных ферментов тетразолиевого красителя 3-(4,5-диметилтиазол-2-ил)-2,5-дифенил-тетразолиум бромида, имеющего жёлтую окраску, в пурпурно-синий формазан, с максимумом поглощения света в диапазоне 540-560 нм. Оптическая плотность раствора в данном диапазоне волн является косвенным показателем количества живых клеток в культуре. Цитотоксическую активность тестируемого вещества измеряют по уменьшению оптической плотности опытных проб по сравнению с контрольными пробами без воздействия [9].
Ход эксперимента. Клетки культур А431 и Н1299 высаживали в 96-луночный планшет в количестве 15 тыс/лунка в среде DMEM с добавлением 10% ЭТС и культивировали в стандартных условиях при 5,0 % CO2, 37 ºC. На следующий день среду заменяли и вносили тестируемое вещество в серии двукратных разведений от 0,12мкМ до 120 мкМ. В контрольных лунках производили замену среды без внесения вещества. Клетки далее инкубировали в тех же стандартных условиях в течение 24 ч, после чего среду заменяли и вносили 10% раствор МТТ в среде DMEM с добавлением 10% ЭТС, после чего инкубировали ещё 2 часа в условиях СО2-инкубатора. По окончании культивирования среду с МТТ полностью удаляли из лунок, а образовавшиеся кристаллы формазана растворяли в ДМСО, после чего измеряли оптическую плотность полученного раствора при 540 нм.
Определение значения IC50 проводили в среде разработки RStudio с использованием пакета drc [10].
Результаты исследований.
Об уровне цитотоксической активности судили по изменению оптической плотности на 540 нм в лунках, обработанных веществом по сравнению с контрольными лунками (без воздействия).
Ингибирующая концентрация IC50 2-(1,1-диметил-1H-бензо[e]индолин-2-ил)-5,6,7-трихлор-1,3-трополона в отношении культуры клеток рака кожи А431, при которой количество живых клеток уменьшалось на 50%, составила 0,172±0,029 мкМ. Для культуры H1299 этот параметр составил 2,18±0,7 мкМ. Для сравнения, ингибирующая концентрация IC50 стандартного противоопухолевого препарата цисплатина при инкубации 24 часа по данным литературы составляет 137±12мкМ для культуры А431 [11] и 34,9 мкМ для культуры H1299 [12], что существенно выше значений, полученных для 2-(1,1-диметил-1H-бензо[e]индолин-2-ил)-5,6,7-трихлор-1,3-трополона.
Таким образом, 2-(1,1-диметил-1H-бензо[e]индолин-2-ил)-5,6,7-трихлор-1,3-трополон проявляет высокую цитотоксическую активность в отношении клеточной линии рака кожи А431 и рака легкого Н1299, при этом концентрация IC50 предлагаемого соединения ниже, чем концентрация IC50 широко используемого в терапии опухолей, в том числе и рака легкого, Циспластина.
Литература
1. Sung H., Ferlay J., Siegel R.L., Laversanne M., Soerjomataram I., Jemal A., Bray F. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. // CA Cancer J Clin. - 2021. - Vol. 71. - № 3. – P. 209-249. doi: 10.3322/caac.21660.
2. Злокачественные новообразования в России в 2021 году (Заболеваемость и смертность). Под ред. Каприна А.Д., Старинского В.В., Шахзадовой А.О. – М.: МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России, 2022. – 252 с.
3. Linkui Bai, Chuanzhu Gao, Qinghua Liu, Congtao Yu, Zhuxin Zhang, Linxiang Cai, Bo Yang, Yunxu Qian, Jian Yang, Xiali Liao. Research progress in modern structure of platinum complexes. // Eur. J. Med. Chem. - 2017. - Vol. 140. – P. 349-382. https://doi.org/10.1016/j.ejmech.2017.09.034.
4. Ю. А. Саяпин, Е. А. Гусаков, И. В. Дороган, И. О. Тупаева, М. Г. Теймуразов, Н. К. Фурсова, К. В. Овчинников, В. И. Минкин. Новый 2- (4h-1,3-бензоксазин-4-он-2-ил)- 1,3-трополон: синтез, структура и антибактериальные свойства // Биоорганическая химия, 2016, том 42, № 2, с. 247–2522.
5. Патент на изобретение РФ № 2314295, МПК C07D215/14, 2008 г.
6. Gusakov E.A., Topchu I.A., Mazitova A.M., Dorogan I.V., Bulatov E.R., Serebriiskii I.G., Abramova Z.I., Tupaeva I.O., Demidov O.P., Duong N.T., Tran D.L., Duong N. B., Boumber Y.A., Sayapin Yu.A., Minkin V.I. Design, synthesis and biological evaluation of 2-quinolyl-1,3-tropolone derivatives as new anti-cancer agents // RSC Advances. – 2021. – Vol. 11. – Issue 8. – P. 4555. DOI: 10.1039/d0ra10610k.
7. Патент на изобретение РФ № 2702648, МПК C07D215/18, 2019 г.
8. Патент на изобретение РФ № 2741311, МПК C07D215/18, 2020 г.
9. Mosmann, Tim. Rapid colorimetric assay for cellular growth and survival: application to proliferation and cytotoxicity assays // Journal of Immunological Methods. — 1983. — V. 65(1-2). — P. 55—63. — ISSN 0022-1759. DOI: 10.1016/0022-1759(83)90303-4.
10. Ritz C, Baty F, Streibig JC, Gerhard D // Dose-Response Analysis Using R. PLoS ONE. — 2015. — V.10. — № 12. — P. e0146021. https://doi.org/10.1371/journal.pone.0146021.
11. Bannon J. H., Fichtner I., O'Neill A., Pampillón C., Sweeney N. J., Strohfeldt K., Watson R. W., Tacke M., Mc Gee M. M. Substituted titanocenes induce caspase-dependent apoptosis in human epidermoid carcinoma cells in vitro and exhibit antitumour activity in vivo. // Br J. Cancer. — 2007. — P. 1234–1241. doi: 10.1038/sj.bjc.6604021.
12. Tang Z., Du W., Xu F., Sun X., Chen W., Cui J., Tang W., Yang F., Teng F., Lin J., Liu B., Dong J. Icariside II enhances cisplatin-induced apoptosis by promoting endoplasmic reticulum stress signalling in non-small cell lung cancer cells. // International journal of biological sciences. — 2022. — V. 18. — № 5. — P. 2060–2074. https://doi.org/10.7150/ijbs.66630.
| название | год | авторы | номер документа |
|---|---|---|---|
| Средство, обладающее цитотоксической активностью в отношении культуры клеток глиомы U87MG | 2024 |
|
RU2839886C1 |
| Средство, обладающее цитотоксической активностью в отношении культуры клеток немелкоклеточного рака легких А 549 | 2020 |
|
RU2741311C1 |
| 5,7-Ди(трет-бутил)-2-(4,7-дихлор-8-метил-5-нитрохинолин-2-ил)-4-нитро-1,3-трополон, обладающий цитотоксической активностью | 2019 |
|
RU2702648C1 |
| N-(2-(2-(2-азидоэтокси)этокси)этил)-4,6-ди(азиридин-1-ил)-1,3,5-триазин-2-амин, обладающий цитотоксическим действием | 2023 |
|
RU2825828C1 |
| ПРОТИВООПУХОЛЕВОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ В ФОРМЕ САШЕ | 2018 |
|
RU2695326C1 |
| ТЕТРАЭТИЛ-2-(2,2,6,6-ТЕТРАМЕТИЛПИПЕРИДИН-4-ИЛАМИНО)-ЭТИЛЕН-1,1-БИСФОСФОНАТ, ОБЛАДАЮЩИЙ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2506085C1 |
| Новые лекарственные средства с цитотоксической активностью на основе производных азолоазинов для химиотерапии рака молочной железы | 2022 |
|
RU2814965C2 |
| ПРОИЗВОДНЫЕ ХИНАЗОЛИНА, ИНДУЦИРУЮЩИЕ ФЕРРОПТОЗ В МЕТАСТАТИЧЕСКИХ КЛЕТКАХ МЕЛАНОМЫ И РАКА ТОЛСТОЙ КИШКИ | 2019 |
|
RU2722308C1 |
| (17S)-N-БЕНЗИЛ-5-((3β-АЦЕТОКСИ-28-НОР-УРС-12-ЕН)-17-ИЛ)-1,3,4-ОКСАДИАЗОЛ-2-АМИН, ОБЛАДАЮЩИЙ СЕЛЕКТИВНОЙ ЦИТОТОКСИЧНОСТЬЮ В ОТНОШЕНИИ КЛЕТОК РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ MCF-7 | 2019 |
|
RU2708400C1 |
| Разнолигандные комплексы меди(II) с 1H-тетразол-5-уксусной кислотой и производными олигопиридина, проявляющие цитотоксичную активность | 2023 |
|
RU2818953C1 |
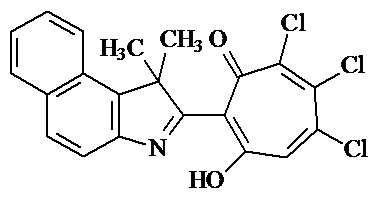
Изобретение относится к области органической химии, а именно к 2-(1,1-диметил-1H-бензо[e]индолин-2-ил)-5,6,7-трихлор-1,3-трополону формулы 1, который обладает цитотоксической активностью в отношении культуры клеток рака кожи А431 и рака легкого Н1299 и может найти применение при производстве противоопухолевых лекарственных средств. 1 з.п. ф-лы, 1 пр.
 (1)
(1)
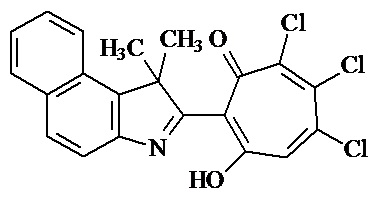
1. 2-(1,1-Диметил-1H-бензо[e]индолин-2-ил)-5,6,7-трихлор-1,3-трополон формулы 1
 (1).
(1).
2. 2-(1,1-Диметил-1H-бензо[e]индолин-2-ил)-5,6,7-трихлор-1,3-трополон по п. 1, обладающий цитотоксической активностью в отношении культуры клеток рака кожи А431 и рака легкого Н1299.
| Средство, обладающее цитотоксической активностью в отношении культуры клеток немелкоклеточного рака легких А 549 | 2020 |
|
RU2741311C1 |
| 5,7-Ди(трет-бутил)-2-(4,7-дихлор-8-метил-5-нитрохинолин-2-ил)-4-нитро-1,3-трополон, обладающий цитотоксической активностью | 2019 |
|
RU2702648C1 |
| 2-ГЕТАРИЛЗАМЕЩЕННЫЕ 1,3-ТРОПОЛОНА, СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ АНТИМИКРОБНОГО ДЕЙСТВИЯ | 2006 |
|
RU2314295C2 |
| E | |||
| A | |||
| GUSAKOV ET AL., Design, synthesis and biological evaluation of 2-quinolyl-1,3-tropolone derivatives as new anti-cancer agents, RSC ADVANCES, 2021, 11, pp | |||
| ПРОФИЛАКТИЧЕСКОЕ СРЕДСТВО ОТ НАСЕКОМЫХ | 1922 |
|
SU4555A1 |
Авторы
Даты
2023-12-27—Публикация
2023-11-08—Подача