Область техники, к которой относится изобретение
Настоящее изобретение относится к области фармацевтической технологии. Более конкретно, настоящее изобретение относится к производным михелиолида и их солям, фармацевтической композиции, содержащей указанные соединения в качестве активного ингредиента, для лечения рака, способу их получения и к применению для получения противораковых средств или вспомогательного противоракового средства.
Предшествующий уровень техники
Опухоль имеет большую угрозу для здоровья человека, в настоящее время количество раковых больных около 200 миллионов и каждый год количество новых раковых больных составляет 1,6 миллиона. В настоящее время противоопухолевое исследование является очень важным и имеет большое значение в науке. В настоящее время, обычно используемыми клиническими противораковыми препаратами являются цитотоксические препараты. Данные препараты обладают плохой селективностью, сильными побочными эффектами, устойчивостью к препарату и т.д. Они представляют собой типичные двойственные препараты и трудно уничтожают рак, что приводит к высокому проценту рецидива рака. Высокая скорость рецидива рака является проблемой для врачей, и все больше и больше исследований подтверждают то, что существуют небольшое количество стволовых раковых клеток в популяции раковых клеток, которые могут увеличить клеточные раковые группы. Стволовые раковые клетки обычно находятся в медленном циклическом статусе и имеют низкую чувствительность к химиотерапевтическим препаратам. Они и являются источником рецидива рака. Найденная стволовая опухолевая клетка делает новую цель для лечения рака и исследования препарата, сосредоточенного на стволовой опухолевой клетке, может привести к полному излечению рака.
В последние годы, исследования в отношении противораковых соединений из натуральных продуктов стали очень распространенными в области исследования и разработки противораковых препаратов. В течение прошлых 20 лет, 61% препарат в виде новой маленькой молекулы могли быть получены из натуральных продуктов. Натуральные продукты очень распространены в некоторых терапевтических областях: 78% антибактериальных соединений и 74% противораковых соединений являются натуральными продуктами или получены из натуральных продуктов. Практика доказала, что уникальная роль натуральных продуктов в открытии противораковых препаратов снова привлекает большое внимание.
Традиционное противоопухолевое химиотерапевтическое лекарство имеет проблему устойчивости, в частности низкую чувствительность к опухолевой стволовой клетке. Традиционная китайская медицина (ТСМ) является основательной в противораковой области, имеет высокую эффективность и низкую токсичность. Соответственно, существует высокий шанс обнаружить препараты, уничтожающие стволовые раковые клетки для лечения злокачественной опухоли в ТСМ.
Партенолид (Parthenolide), сесквитерпеновый лактон, экстрагированный из Tanacetum Parthenium, традиционно использовались для лечения кожных инфекций, ревматизма и мигрени. Последние исследования показали, что партенолид может ингибировать рост раковых клеток, таких как рак простаты, рак молочных желез, рак желудка, лейкемия, рак почки, рак легких, ободочный железистый рак, медуллобластома. Более того, партенолид является эффективным при лечении рака кожи, вызванного УФ-лучами на животной модели. Исследования его механизма обнаружило, что партенолид может ингибировать активацию фактора транскрипции NF-кВ. Активность, главным образом, получали из тиола на субъединице p65/NF-кB, которая сопровождает реакцию Михаэля с партенолидом. NF-кВ является ключевым геном в регулировании опухолевого развития, метастаз и генов устойчивости к препаратам, и поэтому ингибирование активации NF-кВ может увеличить чувствительность апоптоза опухоли к ингибитору опухоли. Недавно, профессор Jordan СТ. и его коллеги из медицинского института обнаружили, что партенолид может селективно устранять стволовые раковые клетки без поражения нормальных стволовых клеток, которые позволяют подавить повторение острого миелобластного лейкоза (АМЛ). Этот уникальный механизм партенолид привлек широкое внимание.
Михелиолид относится к сесквитерпеновому лактону из гваякового типа. Как указано в литературе [J. Nat. Prod. 1993, 56, 90-98; Bioorg. Med. Chem. Lett. 2003, 11, 1503-1510]. На основании полученных результатов, настоящее изобретения относится к использованию производных михелиолида и их солей для лечения рака.
Сущность изобретения
Вариант осуществления настоящего изобретения касается производного михелиолида, противораковой фармацевтической композиции, содержащей эффективное количество производного михелиолида формулы (I) или ее солей, способа ее получения и применение производного михелиолида формулы (I) или ее солей, или фармацевтической композиции для получения противоракового средства.
Воплощение данного изобретения обеспечивают указанные объекты изобретения:
Предлагается соединение формулы (I) или его соль:

где
R1 представляет собой Р, -C(О)R4 или -C(О)NR5R6, где R5 и R6 могут быть одинаковыми или различными, R4, R5 и R6 представляют собой водород, алкил, циклоалкил, алкенил, алкинил, арил, алкиларил, арилалкил, арилалкенил, арилалкинил и гетероцикл;
R2=R3 представляет собой двойную связь, или
R3 представляет собой Р, a R2 представляет собой алкил, имеющий от 1 до 8 атомов углерода и содержащий заместитель, где заместитель выбирают из циклоалкила, гетероциклоалкила, арила, гетероарила, фрагмента аминокислоты или -NR7R8, и его фармацевтически приемлемые соли, образованные с неорганической и/или органической кислотой и его четвертичные аммониевые соли, образованные с R9Z, предпочтительно, заместителем является фрагмент аминокислоты и метилен, замещенный -NR7R8;
где R7 и R8 могут быть одинаковыми или различными и представляют собой водород, алкил, циклоалкил, алкил, замещенный гидроксилом, алкенил, алкинил, арил, алкиларил, арилалкил, арилалкенил, арилалкинил, гетероцикл, трифторметил, перфторалкил, циано, цианометил, карбоксил, карбамат, сульфонил, сульфонамид или арилоксиалкил; или R7 и R8, взятые вместе с атомом N, образуют кольцо, предпочтительно 3-9-членное кольцо, где кольцо может содержать один или несколько заместителей, выбранных из водорода, алкила, циклоалкила, алкенила, алкинила, арила, алкиларила, арилалкила, арилалкенила, арилалкинила или гетероцикла, предпочтительно R7 и R8 выбирают из водорода, алкила, имеющего от 1 до 8 атомов углерода, или циклоалкила;
Z представляет собой фтор, хлор, бром, иод, тозилат, метансульфонат, бензолсульфонат, трифторметансульфонат; R9 представляет собой алкил, циклоалкил, алкил, замещенный гидроксилом, алкенил, алкинил, арил, гетероцикл, арилалкил, арилалкенил, арилалкинил, цианометил, алкокси или арилоксиалкил; неорганическая или органическая кислота представляет собой фтористоводородные кислоты, соляную кислоту, бромистоводородную кислоту, иодистоводородную кислоту, серную кислоту, азотную кислоту, фосфорную кислоту, угольную кислоту, борную кислоту, селенистые кислоты, фосфорно-кислоты, фосфорные кислоты, сернистую кислоту, лимонную кислоту, малеиновую кислоту, D-яблочную кислоту, L-яблочную кислоту, DL-яблочную кислоту, L-молочную кислоту, D-молочную кислоту, DL-молочную кислоту, щавелевую кислоту, метансульфокислоту, валериановые кислоты, олеиновые кислоты, лауриновые кислоты, п-метил бензолсульфокислоту, 1-нафталинсульфокислоты, 2-нафталинсульфокислоты, фталевые кислоты, винные кислоты, малоновые кислоты, янтарную кислоту, фумаровую кислоту, гликолевую кислоту, тиоловую кислоту, глицин, саркоцин, сульфокислоту, никотиновую кислоту, пиколиновую кислоту, изоникотиновую кислоту, бензойную кислоту или замещенную бензойную кислоту;
X представляет собой кислород или R10N, где R10 представляет собой водород, алкил, циклоалкил, алкенил, алкинил, арил, алкиларил, арилалкил, арилалкенил, арилалкинил или гетероцикл;
Y представляет собой одинарную связь, O, R11N, R12R13C, где R11 представляет собой водород, алкил, циклоалкил, алкенил, алкинил, арил, алкиларил, арилалкил, арилалкенил, арилалкинил или гетероцикл; R12 и R13 могут быть одинаковыми или различными и представляют собой водород, фтор, хлор, бром, иод, алкил, циклоалкил, алкил, замещенный гидроксилом, алкенил, алкинил, арил, гетероцикл, арилалкил, арилалкенил, арилалкинил, цианометил, алкокси или арилоксиалкил.
Предпочтительно, если R1 представляет собой H, Y является одинарной связью, то R2=R3 не является двойной связью.
Предпочтительно, R2 представляет собой метилен, замещенный NR7R8 или фрагментом аминокислоты, где R7 и R8 могут быть одинаковыми или различными и представляют собой водород, алкил, циклоалкил, алкил, замещенный гидроксилом, алкенил, алкинил, арил, алкиларил, арилалкил, арилалкенил, арилалкинил, гетероцикл, трифторметил, перфторалкил, циано, цианометил, карбоксил, карбамат, сульфонил, сульфонамид или арилоксиалкил; или R7 и R8, взятые вместе с атом N, образуют кольцо, предпочтительно 3-9-членное кольцо, где кольцо может содержать один или несколько заместителей, выбранных из водорода, алкила, циклоалкила, алкенила, алкинила, арила, алкиларила, арилалкила, арилалкенила, арилалкинила или гетероцикла, предпочтительно R7 и R8 выбирают из водорода, алкила, имеющего от 1 до 8 атомов углерода, или циклоалкила.
Настоящее изобретение также касается способа получения соединения формулы (I) или его соли, включающего обеспечение михелиолидом в качестве исходного материала, добавление катализатора в органический растворитель, и взаимодействие органического растворителя с катализатором и исходным материалом с получением целевого соединения.
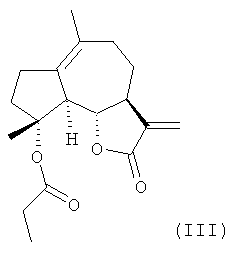
Предпочтительно, соединение формулы (I) или его соль могут быть представлены формулой (II), формулой (III), формулой (IV) или формулой (V):



В частности, изобретение касается способа получения производного михелиолида формулы (II), включающего взаимодействие исходных соединений с получением целевого соединения, где исходными соединениями являются михелиолид и диметиламид.
Также изобретение касается способа получения производного михелиолида формулы (III), включающего взаимодействие исходных соединений, растворителя и катализатора с получением целевого соединения, где исходными соединениями являются михелиолид и пропионилхлорид, катализатором является триэтиламин, растворителем является СН2С12.
Также изобретение касается способа получения производного михелиолида формулы (IV), включающего взаимодействие исходных соединений и растворителя с получением целевого соединения, где исходными соединениями являются михелиолид и 3-хлорпербензойная кислота, растворителем является CH2Cl2.
В частности, настоящее изобретение касается способа получения соединения формулы (V), включающего растворение исходного материала в CH2Cl2, где исходным соединением является соединение формулы (V), доведение pH до значения 4-5 с помощью соляной кислоты и лиофилизация водного раствора с получением целевого соединения.
Настоящее изобретение также касается применения соединения формулы (I) или его соли для лечения рака, где рак включает лейкемию, рак грудной железы, рак предстательной железы, рак носоглотки, рак толстой кишки, рак легких, рак печени, рак пищевода, рак желудка, рак кишки, рак почки, рак полости рта, лимфому Ходжкина, рак поджелудочной железы, рак прямой и ободочной кишки, рак шейки матки, лимфому не-Ходжкина, глиому, меланоматоз, цистокарциному, рак яичника, рак щитовидной железы или саркому Капоши.
Настоящее изобретение также касается применения соединения формулы (I) или его соли для вспомогательного лечения рака, где рак включает лейкемию, рак грудной железы, рак предстательной железы, рак носоглотки, рак толстой кишки, рак легких, рак печени, рак пищевода, рак желудка, рак кишки, рак почки, рак полости рта, лимфому Ходжкина, рак поджелудочной железы, рак прямой и ободочной кишки, рак шейки матки, лимфому не-Ходжкина, глиому, меланоматоз, цистокарциному, рак яичника, рак щитовидной железы или саркому Капоши.
Настоящее изобретение также касается применения соединения формулы (I) или его соли в качестве лекарственного средства, где указанное лекарственное средство используют для лечения рака, где рак включает лейкемию, рак грудной железы, рак предстательной железы, рак носоглотки, рак толстой кишки, рак легких, рак печени, рак пищевода, рак желудка, рак кишки, рак почки, рак полости рта, лимфому Ходжкина, рак поджелудочной железы, рак прямой и ободочной кишки, рак шейки матки, лимфому не-Ходжкина, глиому, меланоматоз, цистокарциному, рак яичника, рак щитовидной железы или саркому Капоши.
Настоящее изобретение также касается применения соединения формулы (I) или его соли в качестве лекарственного средства, где указанное лекарственное средство используют для вспомогательного лечения рака, где рак включает лейкемию, рак грудной железы, рак предстательной железы, рак носоглотки, рак толстой кишки, рак легких, рак печени, рак пищевода, рак желудка, рак кишки, рак почки, рак полости рта, лимфому Ходжкина, рак поджелудочной железы, рак прямой и ободочной кишки, рак шейки матки, лимфому не-Ходжкина, глиому, меланоматоз, цистокарциному, рак яичника, рак щитовидной железы или саркому Капоши.
Настоящее изобретение также касается фармацевтической композиции для лечения рака, содержащей эффективное количество производного михелиолида формулы (I) или его соли, в комбинации с фармацевтически приемлемым носителем или другим противораковым лекарственным средством.
Настоящее изобретение также касается применения соединения формулы (II), (III), (IV), (V) или его соли для лечения рака, где рак включает лейкемию, рак грудной железы, рак предстательной железы, рак носоглотки, рак толстой кишки, рак легких, рак печени, рак пищевода, рак желудка, рак кишки, рак почки, рак полости рта, лимфому Ходжкина, рак поджелудочной железы, рак прямой и ободочной кишки, рак шейки матки, лимфому не-Ходжкина, глиому, меланоматоз, цистокарциному, рак яичника, рак щитовидной железы или саркому Капоши.
Настоящее изобретение также касается применения соединения формулы (II), (III), (IV), (V) или его соли для вспомогательного лечения рака, где рак включает лейкемию, рак грудной железы, рак предстательной железы, рак носоглотки, рак толстой кишки, рак легких, рак печени, рак пищевода, рак желудка, рак кишки, рак почки, рак полости рта, лимфому Ходжкина, рак поджелудочной железы, рак прямой и ободочной кишки, рак шейки матки, лимфому не-Ходжкина, глиому, меланоматоз, цистокарциному, рак яичника, рак щитовидной железы или саркому Капоши.
Настоящее изобретение также касается применения соединения формулы (II), (III), (IV), (V) или его соли для лечения рака, где рак включает лейкемию, рак грудной железы, рак предстательной железы, рак носоглотки, рак толстой кишки, рак легких, рак печени, рак пищевода, рак желудка, рак кишки, рак почки, рак полости рта, лимфому Ходжкина, рак поджелудочной железы, рак прямой и ободочной кишки, рак шейки матки, лимфому не-Ходжкина, глиому, меланоматоз, цистокарциному, рак яичника, рак щитовидной железы или саркому Капоши.
Настоящее изобретение также касается применения соединения формулы (II), (III), (IV), (V) или его соли в качестве лекарственного средства, где лекарственное средство используют для лечения рака, где рак включает лейкемию, рак грудной железы, рак предстательной железы, рак носоглотки, рак толстой кишки, рак легких, рак печени, рак пищевода, рак желудка, рак кишки, рак почки, рак полости рта, лимфому Ходжкина, рак поджелудочной железы, рак прямой и ободочной кишки, рак шейки матки, лимфому не-Ходжкина, глиому, меланоматоз, цистокарциному, рак яичника, рак щитовидной железы или саркому Капоши.
Настоящее изобретение также касается применения соединения формулы (II), (III), (IV), (V) или его соли в качестве лекарственного средства, где лекарственное средство используют для вспомогательного лечения рака, где рак включает лейкемию, рак грудной железы, рак предстательной железы, рак носоглотки, рак толстой кишки, рак легких, рак печени, рак пищевода, рак желудка, рак кишки, рак почки, рак полости рта, лимфому Ходжкина, рак поджелудочной железы, рак прямой и ободочной кишки, рак шейки матки, лимфому не-Ходжкина, глиому, меланоматоз, цистокарциному, рак яичника, рак щитовидной железы или саркому Капоши.
Настоящее изобретение также касается фармацевтической композиции для лечения рака, содержащей эффективное количество производного михелиолида формулы II), (III), (IV), (V) или его соли, в комбинации с фармацевтически приемлемым носителем или другим противораковым лекарственным средством.
Соединения настоящего изобретения могут быть непосредственно или в виде фармацевтической композиции использованы в качестве лекарственного средства. Фармацевтические композиции содержат 0,1-99%, предпочтительно 0,5-90%, соединений настоящего изобретения, и фармацевтически приемлемые носители и/или эксципиенты, которые не опасны для животных и человека, или в комбинации с другими противораковыми лекарственными средствами. Композиции могут быть получены в виде инъекции, таблетки и капсулы.
Фармацевтически приемлемые носители и экципиенты являются твердыми, полутвердыми и жидкими. Доза фармацевтической композиции настоящего изобретения зависит от единицы веса. Фармацевтические композиции могут быть введены в виде инъекции и пероральной формы. Инъекции включают инъекции для внутривенного и внутримышечного введения, а пероральная форма представляет таблетку и капсулу.
Производные михелиолида и их соли демонстрируют хороший эффект в лечении рака и не показывают очевидное ингибирование нормальных клеток.
Примеры
Настоящее изобретение далее описано со ссылкой на примеры, которые не ограничивают настоящее изобретение.
Пример 1
Получение 11βH, 13-гидро,13-диметиламиномихелиолида (соединение II):

Михелиолид (106 мг, 0,40 ммоль), триэтиламин (2,0 мл), Me2NH-HCl (41 мг, 0,5 ммоль) и метанол (30 мл) добавляют в 100-миллилитровую круглодонную колбу. Полученную смесь нагревают и кипятят с обратным холодильником в течение 3 часов, и затем после концентрируют при пониженном давлении с получением сырого осадка, который очищают на колонке с силикагелем (петролейный эфир:этилацетат:триэтиламин=50:50:0,5) с получением 107,4 мг твердого вещества белого цвета, с выходом 86%.
Формула: C17H27NO3
Молекулярный вес: 293
Характеристика: Белый аморфный порошок
Спектральные данные:
1H-ЯМР (CDCl3, 400 МГц) δ 3,76 (т, J=10,0 Гц, 1H), 2,96 (с, 1H), 2,49-2,67 (м, 3H), 2,28-2,34 (м, 1H), 2,30-2,34 (м, 2H), 2,18 (с, 6H), 2,09 (ушир.с, 2Н), 1,96 (д, J=11,2 Гц, 1Н), 1,67-1,73(м, 2Н), 1,60 (с, 3H) 1,22 (ушир.с, 3H), 1,18 (ушир.с, 2Н);
13C-ЯМР (CDCl3, 100 МГц) δ 177,0, 131,8, 131,3, 84,0, 80,2, 58,3, 58,1, 50,9, 46,0, 44,6, 38,4, 35,3, 30,0, 27,2, 23,7, 22,8.
Пример 2
Получение 4-пропионилмихелиолида (соединение III):

Михелиолид (106 мг, 0,40 ммоль), триэтиламин (2,0 мл), пропионилхлорид (0,2 мл) и CH2Cl2 (5 мл) добавляют в 20-миллилитровую круглодонную колбу. Полученную смесь перемешивают в течение 24 часов при комнатной температуре, и затем концентрируют при пониженном давлении, и очищают на колонке с силикагелем (петролейный эфир:этилацетат=90:10), с получением 87 мг твердого вещества белого цвета, с выходом: 72%.
Формула: C18H24NO4
Молекулярный вес: 304
Характеристика: Белый аморфный порошок
Спектральные данные:
1H-ЯМР (CDCl3, 400 МГц) δ 6,14 (с, 1Н), 5,42 (с, 1Н), 3,74 (т, J=10,0 Гц, J=10,0 Гц, 1Н), 1,80-2,74 (м, 12Н), 1,67 (с, 3H), 1,50 (с, 3H), 1,07 (т, J=4,0 Гц, 3H);
13C-ЯМР (CDCl3, 100 МГц) δ 173,8, 170,1, 139,5, 131,5, 130,4, 118,6, 88,4, 83,0, 56,6, 50,1, 36,5, 34,9, 30,4, 28,7, 25,9, 24,1, 18,8, 9.1.
Пример 3
Получение 1,10-эпоксимихелиолида (соединение IV):

Михелиолид (106 мг, 0,40 ммоль), м-хлорпербензойной кислоты (0,45 ммоль) и метиленхлорид (5 мл) добавляли в 20-миллимилитровую круглодонную колбу. Полученную смесь перемешивают в течение 6 часов при комнатной температуре, и затем после концентрируют при пониженном давлении, и очищают на колонке с силикагелем (петролейный эфир:этилацетат=80:20) с получением 96 мг твердого вещества белого цвета, с выходом: 91%.
Формула: C15H20NO4
Молекулярный вес: 264
Характеристика: Белый аморфный порошок
Спектральные данные:
1H-ЯМР (CDCl3, 400 МГц) δ 6,13 (д, J=3,2 Гц, 1Н), 5,44 (д, J=2,8 Гц, 1Н), 3,73 (т, J=10,4 Гц, 1Н), 1,30-2,46 (м, 11Н), 1,29 (с, 3H), 1,28 (с, 3H);
13C-ЯМР (CDCl3, 100 МГц) δ 168,7, 137,8, 118,6, 79,2, 77,3, 74,2, 66,7, 52,6, 48,4, 37,1, 33,8, 29,0, 24,6, 22,5, 21,3.
Пример 4
Получение гидрохлорида 11βH,13-гидро,13-диметиламиномихелиолида (соединение V):

Соединение (II) (293 мг, 1 ммоль) растворяют в метиленхлориде (2 мл) и перемешивают при комнатной температуре, затем добавляют соляную кислоту до доведения pH=4-5. Полученную смесь экстрагируют дихлорметаном (2×10 мл). Полученный водный слой лиофилизируют с получением твердого вещества белого цвета, с выходом: 82%.
Формула: C17H28ClNO3
Молекулярный вес: 328.5
Характеристика: Белый аморфный порошок
Спектральные данные:
[a]D 20=-42, О (С=10, H2O);
ИК (см-1): 3334,25, 2927,18, 2856,17, 1767,94, 1467,25, 992,801, 967,371, 874,796, 831,311, 719,915, 669,783, 626,854, 5 04,24;
1H-ЯМР (D2O, 400 МГц) δ 4,14 (т, J=10,3 Гц, 1Н), 3,51 (кв, J=12,6 Гц, 1Н), 3,40 (дд, J=13,3, 2,9 Гц, 1Н), 3,18-3,04 (м, 1Н), 2,96 (д, J=10,6 Гц, 6Н), 2,67 (д, J=10,2 Гц, 1Н), 2,37 (дд, J=16,2, 8,1 Гц, 1Н), 2,27-2,05 (м, 4Н), 1,87 (д, J=12,9 Гц, 1Н), 1,73 (дд, J=19,5, 11,7 Гц, 2Н), 1,66 (с, 3H), 1,46-1,31 (м, 2Н), 1,26 (с, 3H);
13C-ЯМР (CDCl3, 100 МГц) δ 178,4, 132,6, 131,4, 85,1, 80,7, 56,9, 55,6, 49,9, 45,1, 42,3, 41,5, 39,2, 34,4, 29,5, 25,9, 23,2, 21,4.
Пример 5
Фармакологическая активность производных михелиолида
Раковые клетки суспендируют в 2х105/мл, и затем добавляют в 24-луночный планшет с круглодонными лунками для тканевой культуры. Затем добавляют михелиолид и его производные, где один тест с одной плотностью занимает 5 лунок. Полученную суспензию инкубируют (при 37°C, 5%-ном CO2) в течение 18 часов, чтобы соединения вступили во взаимодействие. Значение коэффициента поглощения (A) измеряют с использованием МТТ-теста (используется для оценки цитотоксичности потенциально противоопухолевых соединений) и на фермент-связанном детекторе при длине волны 570 нм и измеряют ингибирующую активность соединений. Полученные результаты ингибирующей активности представлены в Таблице 1.
В Таблице 1 HL-60, К562, MCF-7, CNE-1, CNE-2, SW620, А549, HepG-2, Ес9706, SGC7901, SW1116, А498, ASPC-1, НТ-29, HeLa, GL15, B16F1, Т24, SKOV3, SW579, РС-3 представляют собой линии клеток острой лейкемии, линии клеток хронической лейкемии, линии клеток рака молочной железы, линии клеток высокодифференцированной носоглоточной карциномы, линии клеток беднодифференцированной носоглоточной карциномы, линии клеток рака ободочной и прямой кишки, линии клеток рака легких, линии клеток гепатоцеллюлярной карциномы, линии клеток рака пищевода, линии клеток рака желудка, линии клеток рака толстой кишки, линии клеток почечно-клеточнного рака, линии клеток рака поджелудочной железы, линии клеток рака толстой кишки, линии клеток рака шейки матки, линии клеток роговой человеческой нейробластомы, линии клеток меланомы, линии клеток мочевого пузыря, линии клеток рака яичника, линии клеток рака щитовидной железы, линии клеток рака простаты.
Полученные результаты демонстрируют, что соединения настоящего изобретения обладают сильной активностью против тестируемых клеток, однако также обладают неочевидным ингибированием на клетки при значении 50 мкМ.
Пример 6
Инъекция
Соединения II, III, IV, V, полученные в Примерах 1-4, растворяют в малом количестве ДМСО. Затем воду для инъекции добавляют в полученную смесь, фильтруют и затем заливают и стерилизуют с получением инъекции.
Пример 7
Таблетка
Соединения II, III, IV, V, полученные в Примерах 1-4, смешивают с эксципиентами в соответствии с весовым соотношением 5:1, и затем таблетируют с получением таблеток.
Пример 8
Капсула
Соединения II, III, IV, V, полученные в Примерах 1-4, смешивают с эксципиентами в соответствии с весовым соотношением 5:1, с получением капсул.
Соединения настоящего изобретения, использование и способы были описаны с помощью конкретных примеров осуществления изобретения. Для специалиста в данной области техники очевидно, что соответствующие изменения исходных материалов, условий способа и т.д. приведут к достижению соответствующих целей. Любые модификации, эквивалентные замены и улучшения являются содержанием настоящего изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| АМИНОПИРИМИДИНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗ | 2006 |
|
RU2427578C2 |
| СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ РАКА | 2015 |
|
RU2805949C2 |
| КОМБИНИРОВАННЫЙ ИММУНОТЕРАПЕВТИЧЕСКИЙ ПОДХОД К ЛЕЧЕНИЮ РАКА | 2015 |
|
RU2716821C2 |
| ПРОМЕЖУТОЧНЫЕ ХИМИЧЕСКИЕ СОЕДИНЕНИЯ И СПОСОБЫ ПОЛУЧЕНИЯ СОЕДИНЕНИЙ | 2013 |
|
RU2635359C2 |
| СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ РАКА | 2015 |
|
RU2733393C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И СПОСОБЫ ЛЕЧЕНИЯ РАКА И ЕГО МЕТАСТАЗОВ | 2006 |
|
RU2401662C2 |
| КОМБИНАЦИЯ ИНОТУЗУМАБА ОЗОГАМИЦИНА И ТОРИЗЕЛА ДЛЯ ЛЕЧЕНИЯ РАКА | 2012 |
|
RU2607594C2 |
| НОВЫЕ ПИРАЗОЛОПИРИМИДИНЫ КАК ИНГИБИТОРЫ ЦИКЛИН-ЗАВИСИМОЙ КИНАЗЫ | 2003 |
|
RU2380369C9 |
| ТЕТРАГИДРОПИРАНИЛ АМИНО-ПИРРОЛОПИРИМИДИНОН И СПОСОБЫ ЕГО ПРИМЕНЕНИЯ | 2015 |
|
RU2715421C2 |
| СУЛЬФОКСИМИНЗАМЕЩЕННЫЕ ПИРИМИДИНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ CDK И/ИЛИ VEGF, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2004 |
|
RU2410378C2 |
Изобретение относится к производным михелиолида формулы (I), фармацевтической композиции на их основе и их применению для лечения рака. В формуле (I) R1 представляет собой Н, -C(O)R4, где R4 представляет собой C1-8алкил; R2=R3 представляет собой двойную связь, или R3 представляет собой Н, а R2 представляет собой замещенный алкил, имеющий от 1 до 8 атомов углерода, где заместитель представляет собой -NR7R8; и его фармацевтически приемлемые соли; где R7 и R8 могут быть одинаковыми или различными и представляют собой C1-8алкил; Х представляет собой кислород; Y представляет собой одинарную связь. 4 н. и 2 з.п. ф-лы, 1 табл., 8 пр.
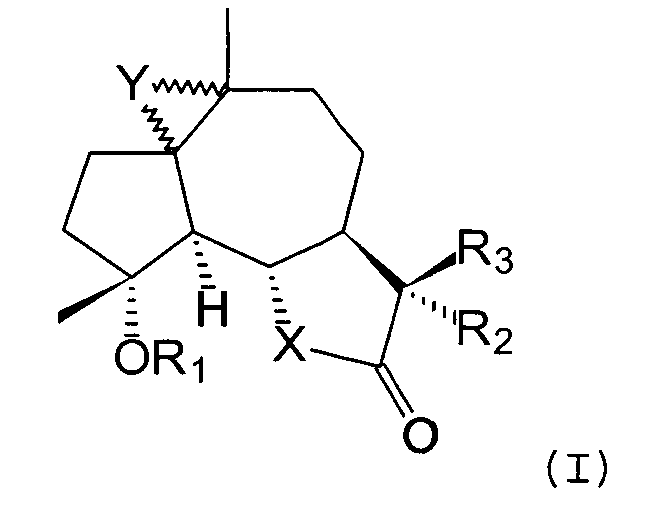
1. Соединение формулы (I):

где
R1 представляет собой Н, -C(O)R4, где R4 представляет собой C1-8алкил;
R2=R3 представляет собой двойную связь, или
R3 представляет собой Н, а R2 представляет собой замещенный алкил, имеющий от 1 до 8 атомов углерода, где заместитель представляет собой -NR7R8;
и его фармацевтически приемлемые соли;
где R7 и R8 могут быть одинаковыми или различными и представляют собой C1-8алкил;
Х представляет собой кислород;
Y представляет собой одинарную связь О;
если R1 представляет собой Н, Y является одинарной связью, то R2=R3 не является двойной связью.
2. Соединение по п.1, где R2 представляет собой метилен, замещенный -NR7R8, где R7 и R8 могут быть одинаковыми или различными и представляют собой С1-8алкил.
3. Соединение по п.1, где формула (I) представляет формулу, выбранную из формулы (II), формулы (III), формулы (IV), формулы (V):

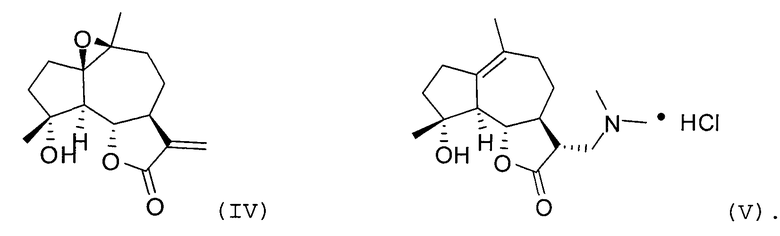
4. Применение соединения по любому из пп.1-3 или его соли для получения лекарственного средства для лечения рака, где рак представляет собой лейкемию, рак молочной железы, рак предстательной железы, рак носоглотки, рак толстой кишки, рак легких, рак печени, рак пищевода, рак желудка, рак кишечника, рак почки, рак ротовой полости, лимфому Ходжкина, рак панкреаса, рак прямой и ободочной кишки, рак шейки матки, лимфому не-Ходжкина, глиому, меланому, рак мочевого пузыря, рак яичников, рак щитовидной железы или саркому Капоши.
5. Применение соединения по любому из пп.1-3 или его соли для получения вспомогательного лекарственного средства для лечения рака, где рак представляет собой лейкемию, рак молочной железы, рак предстательной железы, рак носоглотки, рак толстой кишки, рак легких, рак печени, рак пищевода, рак желудка, рак кишечника, рак почки, рак ротовой полости, лимфому Ходжкина, рак панкреаса, рак прямой и ободочной кишки, рак шейки матки, лимфому не-Ходжкина, глиому, меланому, рак мочевого пузыря, рак яичников, рак щитовидной железы или саркому Капоши.
6. Фармацевтическая композиция для лечения рака, содержащая эффективное количество соединения по любому из пп.1-3 или его соли и фармацевтически приемлемый носитель.
| WO 2009122447 A1, 08.10.2009 | |||
| WO 1999043314 A1, 02.09.1999 | |||
| US 3196164 A, 20.07.1965 | |||
| Приспособление для навески заслонок рабочих окон мартеновских печей | 1929 |
|
SU19239A1 |
Авторы
Даты
2015-01-10—Публикация
2011-04-14—Подача