ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Настоящая заявка на изобретение испрашивает приоритет на основании предварительной заявки на патент США, серийный номер 60/835574, поданной 4 августа 2006 года, полное описание которой включено в настоящую заявку посредством ссылки.
УРОВЕНЬ ТЕХНИКИ
[0002] Опиоиды широко применяются при лечении пациентов с прогрессирующими раковыми заболеваниями и другими заболеваниями в терминальной стадии с целью облегчения страданий. Опиоиды являются наркотическими медицинскими препаратами, которые активируют опиоидные рецепторы, локализованные в центральной нервной системе, что приводит к облегчению боли. Однако опиоиды также взаимодействуют с рецепторами, расположенными вне центральной нервной системы, что приводит к возникновению побочных эффектов, в том числе запоров, тошноты, рвоты, задержке мочи и сильному зуду. Наиболее существенному воздействию подвергается желудочно-кишечный тракт (ЖКТ), где опиоиды вызывают затруднение опорожнения желудка и подавляют пропульсивную активность кишечника, тем самым уменьшая скорость продвижения содержимого через кишечник, что может вызвать запор. Эффективность опиоидов при уменьшении боли часто ограничена из-за возникающих побочных эффектов, которые могут приводить к ухудшению состояния здоровья пациента и часто вынуждают пациентов прекратить применение опиоидных анальгетиков.
[0003] Результаты проведенных исследований позволяют предположить, что помимо побочных эффектов, вызванных приемом болеутоляющих опиоидов, на активность желудочно-кишечного тракта (ЖКТ) могут также оказывать воздействие эндогенные опиоидные соединения, которые также могут участвовать в нормальном регулировании перистальтики кишечника и переноса жидкостей через слизистые оболочки как у животных, так и у человека (Koch, Т. R, et al., Digestive Diseases and Sciences 1991, 36, 712-728; Schuller, A.G.P., et al., Society of Neuroscience Abstracts 1998. 24, 524, Reisine, Т., и Pasternak, G., Goodman & Gilman's The Pharmacological Basis of Therapeutics Ninth Edition 1996, 521-555 и Bagnol, D., et al., Regul. Pept. 1993, 47, 259-273). Таким образом, отклонения от нормального физиологического содержания эндогенных соединений и/или рецепторной активности могут приводить к дисфункции кишечника.
[0004] Например, пациенты, перенесшие хирургические операции, особенно операции на брюшной полости, часто страдают от дисфункции кишечника, например, послеоперационной кишечной непроходимости, которая может быть вызвана колебаниями естественных уровней опиоидов. Аналогичным образом, женщины после родов зачастую страдают от послеродовой кишечной непроходимости, которая, как полагают, вызвана аналогичными колебаниями естественного уровня опиоидов в результате родового стресса. Дисфункция кишечника, связанная с послеоперационной или послеродовой кишечной непроходимостью, обычно может продолжаться в течение 3-5 дней, достигая недели и более в некоторых серьезных случаях. Введение опиоидных анальгетиков пациенту после хирургической операции, являющееся в настоящее время почти всеобщей практикой, может усилить дисфункцию кишечника, замедляя тем самым восстановление нормального функционирования кишечника, продлевая время пребывания в больнице и увеличивая стоимость медицинского обслуживания.
[0005] Были проведены исследования опиоидных антагонистов, таких как налоксон, налтрексон и налмефен, в качестве средств, уменьшающих нежелательное воздействие опиоидов на периферическую нервную систему. Однако эти вещества воздействуют не только на периферические опиоидные рецепторы, но также и на участки центральной нервной системы, так что иногда они аннулируют положительные анальгетические эффекты опиоидов или вызывают синдром отмены опиоидов. Предпочтительные подходы к контролированию побочных эффектов, вызванных опиоидами, включают применение соединений, являющихся антагонистами периферически действующих опиоидов, которые не сразу преодолевают гематоэнцефалический барьер. Например, было показано, что метилналтрексон, являющийся периферически действующим µ-опиоидным антагонистом, и родственные соединения можно применять с целью сдерживания у пациентов побочных эффектов, вызываемых опиоидами (например, запора, зуда, тошноты и/или рвоты). См., например, патенты США 5972954, 5102887, 4861781 и 4719215; и Yuan, С.-S. et al. Drug и Alcohol Dependence 1998, 52. 161.
[0006] Были описаны составы на основе метилналтрексона в качестве периферически действующего антагониста µ-опиоидного рецептора (см., например, патенты США 6608075, 6274591 и 6559158). Однако было обнаружено, что метилналтрексон в некоторых средах и при некоторых условиях образует продукты разложения. См., например, US 2004266806A1. Таким образом, требуется получение лекарственных форм, обеспечивающих эффективную доставку метилналтрексона без значительного разложения метилналтрексона при охлаждении и/или при комнатной температуре.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0007] В настоящем изобретении предложены некоторые составы на основе метилналтрексона. Согласно некоторым вариантам реализации в изобретении предложены составы, имеющие улучшенные характеристики стабильности при длительных сроках хранения активного соединения при охлаждении, а также при комнатной температуре. Предложенные составы можно применять для парентерального введения метилналтрексона. Изобретение включает способы получения и применения указанных составов, а также продукты и наборы, содержащие предложенные составы.
[0008] Согласно некоторым вариантам реализации изобретения предложена фармацевтическая композиция, содержащая эффективное количество по меньшей мере одного активного соединения, выбранного из по меньшей мере метилналтрексона или его фармацевтически приемлемой соли, и кальциевую соль хелатирующего агента в водном растворе.
[0009] Согласно другим вариантам реализации изобретения предложены жидкие составы, содержащие метилналтрексон или его фармацевтически приемлемую соль, кальциевую соль, хелатирующий агент, изотонический агент и водный растворитель. Согласно некоторым вариантам реализации изобретения кальциевая соль и хелатирующий агент представляют собой одно соединение в виде кальциевой соли хелатирующего агента. Согласно некоторым вариантам реализации изобретения, кальциевую соль хелатирующего агента выбирают из кальциевой соли этилендиаминтетрауксусной кислоты (EDTA), кальциевой соли диэтилентриаминпентауксусной кислоты (DTPA), кальциевой соли гидроксиэтилендиаминтриуксусной кислоты (HEDTA), кальциевой соли этиленгликоль-бис-(2-аминоэтил)-N,N,N',N'-тетрауксусной кислоты (EGTA), кальциевой соли нитрилотриуксусной кислоты (NTA), цитрата кальция и производных их кальциевых солей. Согласно некоторым вариантам реализации изобретения кальциевая соль хелатирующего агента представляет собой кальциевую соль EDTA.
[0010] Согласно некоторым вариантам реализации изобретения составы также дополнительно содержат стабилизатор. Согласно некоторым вариантам реализации изобретения стабилизатор выбирают из глицина, бензойной кислоты, лимонной, гликолевой, молочной, яблочной и малеиновой кислоты. Согласно некоторым вариантам реализации изобретения стабилизатор представляет собой глицин.
[0011] Согласно некоторым вариантам реализации изобретения, состав содержит метилналтрексон или его фармацевтически приемлемую соль, кальциевый хелатирующий агент, стабилизатор, изотонический агент и водный растворитель. Согласно некоторым вариантам реализации изобретения, состав содержит метилналтрексон или его фармацевтически приемлемую соль, кальциевую соль EDTA, глицин и хлорид натрия в водном растворе.
[0012] В целом, предложенные составы можно применять для предотвращения, лечения или уменьшения степени тяжести побочных эффектов, возникающих в результате применения опиоидов, в том числе для ингибирования желудочно-кишечной дисфункции (например, запора, гипоперистальтики кишечника, закупорки, гипоперистальтики желудка, сужения сфинктера ЖКТ, увеличения тонуса сфинктера, ингибирования желудочно-кишечной перистальтики, ингибирования перистальтики кишечника, ингибирования опорожнения желудка, замедления опорожнения желудка, неполного опорожнения, тошноты, рвоты, вспучивания, вздутия живота), покраснения кожных покровов, потоотделения, дисфории, зуда, задержки мочи и т.д. Предложенные составы можно применять для введения пациентам, проходящим краткий курс лечения опиоидами (например, пациентам, восстанавливающимся после хирургической операции (на брюшной полости, ортопедической, операции после травмы и т.д.), пациентам, восстанавливающимся после травм, и пациентам, восстанавливающимся после рождения ребенка). Составы также можно применять для введения пациентам, постоянно принимающим опиоиды (например, неизлечимо больным пациентам, принимающим опиоидную терапию (например, пациентам с диагнозом СПИД, пациентам с раковыми заболеваниями или пациентам с сердечно-сосудистыми заболеваниями); пациентам, постоянно принимающим опиоидную терапию с целью обезболивания (например, от боли в спине); пациентам, принимающим опиоидную терапию с целью облегчения синдрома отмены опиоидов).
[0013] Дополнительные применения предложенных составов включают предотвращение, лечение или уменьшение степени тяжести симптомов, связанных с расстройствами или состояниями, возникающими в результате нормальной или аберрантной активности эндогенных опиоидов. Указанные расстройства или состояния включают, среди прочего, кишечную непроходимость (например, послеродовую кишечную непроходимость, кишечную непроходимость при параличе), желудочно-кишечную дисфункцию, которая развивается после операции на брюшной полости (например, колэктомии, в том числе, без ограничения, правосторонней гемиколэктомии, левосторонней гемиколэктомии, поперечной гемиколэктомии, подготовке в колэктомии и низкой передней резекции), такую как послеоперационная кишечная непроходимость и идиопатический запор. Предложенные составы также можно применять при лечении состояний, включающих, например, раковые заболевания, связанные с ангиогенезом, воспалительные заболевания (например, синдром раздраженного кишечника), иммуносупрессию, сердечно-сосудистые заболевания (например, брадикардию, гипотонию), хронические воспаления и/или хронические боли, серповидноклеточную анемию, повреждения сосудов и ретинопатию, пониженную секрецию желчи, пониженную секреторную активность поджелудочной железы, спазм желчевыводящих путей и повышенный гастроэзофагеальный рефлюкс.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0014] Фиг.1А и фиг.1В: Влияние CaEDTA и NaEDTA на образование 2',2-бис-метилналтрексона в присутствии железа при 40°С (фиг.1А) и комнатной температуре, 25° (фиг.1В). Как кальциевая соль ЭДТА, так и натриевая соль ЭДТА являются эффективными ингибиторами образования продукта разложения в виде 2',2'-бис-метилналтрексона.
[0015] Фиг.2А, 2В, 2С и 2D: Влияние CaEDTA на образование 7-дигидроксиметилналтрексона в растворах. Оценивали влияние CaEDTA и NaEDTA на образование 7-дигидроксиметилналтрексона в присутствии железа при 40°С (фиг.2А) и комнатной температуре, 25°С (фиг.2В). Эффективным ингибитором образования продукта разложения в виде 7-дигидроксиметилналтрексона является кальциевая соль ЭДТА, а не натриевая соль ЭДТА. Оценивали влияние CaEDTA на образование 7-дигидроксиметилналтрексона в растворе после хранения в течение месяца при комнатной температуре (фиг.2С) и при 40°С (фиг.2D). Присутствие CaEDTA уменьшало образование 7-дигидроксиметилналтрексона при обеих температурах. Через один месяц при комнатной температуре содержание продукта разложения уменьшалось от 0.34% до 0.11%; и при 40°С /относительной влажности (OВ) 75% указанное содержание уменьшалось от 0.64% до 0.14%. Присутствие NaEDTA в пробах может даже приводить к увеличению содержания образующегося 7-дигидроксиметилналтрексона.
[0016] Фиг.3А и фиг.3В: Влияние CaEDTA в растворе метилналтрексона на образование продукта разложения метилналтрексона, имеющего RRT (относительное время удерживания), равное 0.79 ("продукт разложения 0.79"). Оценивали влияние CaEDTA и NaEDTA на образование продукта разложения 0.79 при комнатной температуре, 25°С (фиг.3А), и при 40°С (фиг.3В). Кальциевая соль ЭДТА не являлась эффективной в отношении ингибирования образования продукта разложения 0.79 и могла приводить к увеличению содержания образующегося продукта разложения.
[0017] На фиг.4 представлены идентифицированные продукты разложения метилналтрексона, соответствующие относительные времена удерживания (RRT) и соответствующие катализаторы и/или ингибиторы их образования, которые были идентифицированы.
ПОДРОБНОЕ ОПИСАНИЕ НЕКОТОРЫХ ВАРИАНТОВ РЕАЛИЗАЦИИ ИЗОБРЕТЕНИЯ
[0018] В изобретении предложены фармацевтические составы, имеющие улучшенные характеристики стабильности при некоторых условиях. Композиции, наборы и продукты, содержащие предложенные составы, характеризуются длительными сроками хранения и также могут храниться при благоприятных условиях при комнатной температуре. Таким образом, композиции, наборы и продукты, содержащие предлагаемые составы, обеспечивают улучшенную доставку терапевтических препаратов пациентам, на которых применение метилналтрексона оказывает лечебное воздействие.
[0019] Например, предлагаемые составы подходят для лечения, предотвращения, замедления или уменьшения степени тяжести или частоты возникновения побочных эффектов, связанных с введением опиоидов, в том числе желудочно-кишечной дисфункции (например, запора, гипоперистальтики кишечника, закупорки, желудочной гипоперистальтики, сужения сфинктера ЖКТ, увеличения тонуса сфинктера, ингибирования желудочно-кишечной перистальтики, ингибирования перистальтики кишечника, ингибирования опорожнения желудка, замедления опорожнения желудка, неполного опорожнения, тошноты, рвоты, вспучивания, вздутия живота), дисфории, зуда, задержки мочи, подавления дыхания, спазма папиллярной мышцы, сердечно-сосудистых эффектов, ригидности грудных стенок и подавления кашля, депрессии стрессовой реакции и иммуносупрессии, связанной с применением наркотического обезболивания и т.д. Дополнительные эффекты от введения опиоидов могут включать, например, аберрантную миграцию или пролиферацию эндотелиальных клеток (например, васкулярных эндотелиальных клеток), увеличение ангиогенеза, и приводить к повышению смертности за счет продуцирования условно-патогенных возбудителей инфекции (например, Pseudomonas aeruginosa). Составы можно применять для введения пациентам, проходящим краткосрочный курс лечения опиоидами (например, пациентам, страдающим от послеоперационной желудочно-кишечной дисфункции и принимающим опиоиды в течение непродолжительного периода времени). Составы также можно применять для введения пациентам, постоянно принимающим опиоиды (например, неизлечимо больным пациентам, подвергающимся опиоидной терапиии, таким как больные СПИДом, пациенты с раковыми заболеваниями, пациенты с сердечно-сосудистыми заболеваниями; пациенты, постоянно принимающие опиоиды с целью обезболивания; пациенты, принимающие опиоиды с целью облегчения синдрома отмены опиоидов).
[0020] Кроме того, применение предлагаемых составов включает, например, предотвращение, замедление, лечение или уменьшение степени тяжести симптомов, связанных с расстройствами или состояниями, возникающими в результате нормальной или аберрантной активности эндогенных опиоидов. Указанные расстройства или состояния включают, помимо прочего, кишечную непроходимость (например, послеродовую кишечную непроходимость, кишечную непроходимость при параличе), желудочно-кишечную дисфункцию, которая развивается после операции на брюшной полости (например, колэктомии, в том числе, без ограничения, правосторонней гемиколэктомии, левосторонней гемиколэктомии, поперечной гемиколэктомии, подготовке к колэктомии и низкой передней резекции), такую как послеоперационная кишечная непроходимость и идиопатический запор. Предлагаемые составы также можно применять при лечении состояний, включающих раковые заболевания, связанные с ангиогенезом, иммуносупрессию, серповидноклеточную анемию, сосудистые повреждения и ретинопатию, и при лечении заболеваний, вызванных воспалением (например, синдрома раздраженного кишечника), иммуносупрессии и хронического воспаления.
Определения
[0021]Термин "концентрат" относится к фармацевтической композиции, содержащей предложенный состав, в которой концентрация активного вещества (веществ) выше, чем концентрация в обычной стандартной лекарственной форме, подходящей для непосредственного введения пациенту. Концентрат можно непосредственно применять для введения пациенту, но, как правило, при приготовлении для введения пациенту его дополнительно разбавляют до концентрации обычной стандартной лекарственной формы. Весь объем концентрата или его аликвоту можно применять при приготовлении стандартной лекарственной формы (форм) для лечения, например, согласно способам, предложенным в настоящем изобретении. Согласно некоторым вариантам реализации изобретения концентрат является примерно в 2 раза, примерно в 5 раз, примерно в 10 раз, примерно в 25 раз, примерно в 50 раз, примерно в 100 раз или примерно в 200 раз более концентрированным, чем стандартная лекарственная форма. Согласно некоторым вариантам реализации изобретения концентрат является примерно в 50 раз, примерно в 100 раз или примерно в 200 раз более концентрированным, чем стандартная лекарственная форма.
[0022] Применяемый в настоящем описании термин "эффективное количество" соединения или фармацевтически приемлемого состава представляет собой количество, обеспечивающее требуемый терапевтический и/или профилактический эффект. Согласно некоторым вариантам реализации изобретения, "эффективное количество" представляет собой по меньшей мере минимальное количество соединения, или состава, содержащего соединение, которое является достаточным для лечения одного или нескольких симптомов заболевания или состояния, связанного с модулированием периферийных µ-опиоидных рецепторов, например, побочных эффектов, вызванных опиоидной обезболивающей терапией (например, желудочно-кишечной дисфункции (например, нарушения перистальтики кишечника, запора и т.д.), тошноты, рвоты и т.д.). Согласно некоторым вариантам реализации изобретения "эффективное количество" соединения или состава, содержащего указанное соединение, является достаточным для лечения симптомов, связанных с заболеванием, вызванным аберрантной эндогенной активностью периферийных опиоидов или µ-рецепторов опиоидов (например, идиопатического запора, кишечной непроходимости и т.д.).
[0023] Термин "состав" относится к композиции для введения пациенту, которая содержит по меньшей мере одно фармацевтически активное соединение (например, по меньшей мере метилналтрексон) в комбинации с одним или несколькими наполнителями или другими фармацевтическими добавками. В общем случае, конкретные наполнители и/или другие фармацевтические добавки, как правило, выбирают с целью достижения требуемой стабильности, высвобождения, распределения и/или активности активного соединения (соединений) при применении.
[0024] Термин "субъект", применяемый в настоящем описании, означает млекопитающее, которому вводят состав или композицию, содержащую указанный состав, и включает людей и животных, таких как домашние животные (например, лошади, собаки, кошки и т.д.).
[0025] Термин "терапевтически активное соединение" или "активное соединение" относится к веществу, в том числе биологически активному веществу, которое можно применять с целью терапии (например, терапии человека или в ветеринарии), в том числе для профилактического и/или терапевтического лечения. Терапевтически активные соединения могут представлять собой органические молекулы, которые являются лекарственными соединениями, пептидами, белками, карбогидратами, моносахаридами, олигосахаридами, полисахаридами, нуклеопротеином, мукопротеином, липопротеином, синтетическим полипептидом или белком, молекулами небольшого размера, связанными с белком; гликопротеином, стероидом, нуклеиновой кислотой, ДНК, РНК, нуклеотидом, нуклеозидом, олигонуклеотидами, антисмысловым олигонуклеотидами, липидом, гормоном и витамином. Альтернативным образом или дополнительно терапевтически активные соединения могут представлять собой любое вещество, применяемое в качестве лекарственного препарата для лечения, предотвращения, замедления, уменьшения или облегчения заболевания, состояния или расстройства. Терапевтически активные соединения, которые можно применять в составах, предложенных в настоящем изобретении, включают опиоидные антагонисты, опиоидные болеутоляющие соединения и т.п. Дополнительное подробное описание соединений, применяемых в качестве терапевтически активных соединений, приведено ниже. Терапевтически активное соединение включает соединение, которое усиливает действие или эффективность второго соединения, например, путем усиления активности или уменьшения нежелательных эффектов второго соединения. Термины "лечить" или "лечение", применяемые в настоящем описании, относятся к частичному или полному облегчению, подавлению, задержке наступления, уменьшению частоты случаев, улучшению и/или облегчению расстройства или состояния или одного или нескольких симптомов расстройства, заболевания или состояния.
[0026] Применяемое в настоящем описании выражение "стандартная доза" относится к физически отдельной дозе состава, подходящего для лечения субъекта. Однако следует иметь в виду, что суммарное ежедневное применение состава, предлагаемого в настоящем изобретении, определяется лечащим врачом в рамках тщательного медицинского обследования. Величина индивидуальной эффективной дозы для любого конкретного субъекта или организма зависит от множества факторов, в том числе конкретного заболевания, подвергаемого лечению, и степени тяжести заболевания; активности применяемого конкретного активного соединения; применяемой конкретной композиции; возраста, массы тела, общего состояния здоровья, пола и режима питания субъекта; времени введения и скорости выведения применяемого конкретного активного соединения; продолжительности лечения; лекарственных препаратов и/или дополнительных курсов лечения, применяемых в сочетании или одновременно с конкретным применяемым соединением (соединениями) и других подобных факторов, хорошо известных в области медицины.
[0027] Выражение "лекарственная форма" относится к средствам, обеспечивающим возможность хранения и/или введения состава субъекту. Например, состав можно хранить во флаконе или шприце. Состав также можно хранить в контейнере, который защищает состав от света (например, УФ-излучения). Альтернативным образом, контейнер или флакон, который сам не обязательно защищает состав от света, можно хранить во втором контейнере для хранения (например, поместив в коробку, пакет и т.д.), который защищает состав от света.
[0028] В настоящем изобретении предложены составы и лекарственные формы для парентерального введения метилналтрексона, в том числе его фармацевтически приемлемых солей. Применяемый в настоящем описании термин "метилналтрексон" включает N-метилналтрексон и его соли. Метилналтрексон описан, например, в патентах США 4176186; 4719215; 4861781; 5102887; 5972954; 6274591; заявках на патент, опубликованных в США под номерами 20020028825 и 20030022909; и публикациях WO 99/22737 и WO 98/25613, содержание которых включено в настоящее описание посредством ссылок.
[0029] В общем случае, фармацевтически приемлемые соли включают без ограничения хлорид, бромид, иодид, нитрат, сульфат, бисульфат, фосфат, кислую соль фосфорной кислоты, соли изоникотиновой кислоты, ацетат, лактат, салицилат, цитрат, тартрат, пантотенат, битартрат, карбонат, аскорбат, сукцинат, малеат, гентизинат, фумарат, глюконат, глюкаронат, сахарат, формиат, карбоксилат, бензоат, глутамат, сульфонат, метансульфонат, этансульфонат, бензолсульфонат, п-толуолсульфонат, селенати памоат(т.е. 1,1'-метилен-бис-(2-гидрокси-3-нафтоат). Согласно некоторым вариантам реализации изобретения соли применяемые в составах согласно настоящему изобретению, представляют собой ранее описанные соли метилналтрексона, например метилналтрексона бромид и т.д. Однако изобретение не ограничивается этими конкретными солями. Другие соли и их смеси можно адаптировать для применения в лекарственном составе согласно изобретению с тем, чтобы достичь подходящей совокупности параметров, характеризующей доставку соединения в организме, предлагаемую в настоящем изобретении (например, хлориды, сульфаты, бисульфаты, тартраты, нитраты, цитраты, битартраты, фосфаты, соли яблочной кислоты, соли малеиновой кислоты, бромиды, иодиды, соли фумаровой кислоты, сульфонаты, карбоксилаты или сукцинаты и т.д.). Альтернативным образом или дополнительно периферически действующий антагонист опиоидного рецептора (например, метилналтрексон) можно при необходимости применять в виде основания, его химических и хиральных производных и других солей.
[0030] К бромидной соли метилналтрексона также относятся, например, N-метилналтрексона бромид, N-метилналтрексона гидробромид, метилналтрексона бромид, метилналтрексона гидробромид, налтрексона метобромид, N-метилналтрексон, MNTX, SC-37359, MRZ-2663-BR и N-циклопропилметилнорокси-морфина метобромид. Метилналтрексон можно приобрести в порошковой форме в компании Mallinckrodt Pharmaceuticals, St. Louis, Mo., где его выпускают в виде белого кристаллического порошка, хорошо растворимого в воде. Температура плавления метилналтрексона составляет 254-256°С. Согласно некоторым вариантам реализации изобретения составы содержатся во флаконе. Согласно некоторым вариантам реализации изобретения, состав содержится во флаконе, содержащем стандартную дозу метилналтрексона. Согласно указанным вариантам реализации состав может содержать примерно от 0.5 мг до примерно 200 мг бромида метилналтрексона. Согласно некоторым вариантам реализации изобретения, стандартная доза может содержать от примерно 1 мг до примерно 80 мг, от примерно 5 мг до примерно 40 мг, или от примерно 8 мг до 12 мг, от примерно 18 мг до примерно 24 мг.
[0031] Метилналтрексон имеет хиральные центры и, следовательно, может встречаться в виде стереохимических изомеров при размещении заместителей у этих хиральных центров. Указанные стереохимические изомеры относятся к соединениям, подходящим для применения в настоящих составах. Соединения, применяемые в композициях и способах согласно настоящему изобретению, могут представлять собой индивидуальные стереоизомеры, а также смеси стереоизомеров. Согласно некоторым аспектам в способах, предлагаемых в настоящем изобретении, применяют соединения, которые по существу представляют собой чистые стереоизомеры. Предполагается, что композиции, предлагаемые в настоящем изобретении, также включают все таутомеры.
[0032] Применяемые в настоящем документе термины "R" и "S" обычно используют в номенклатуре органической химии для обозначения определенной конфигурации хирального центра. Термин "R" относится к "правовращающим изомерам" и применяется для обозначения конфигурации хирального центра, в котором, если смотреть вдоль связи по направлению к группе с самым низким старшинством, группы располагаются по старшинству по часовой стрелке (от самого высокого старшинства к самому низкому). Термин "S" или "левовращающий изомер" применяют для обозначения конфигурации хирального центра, в котором, если смотреть вдоль связи по направлению к группе с самым низким старшинством, группы располагаются по старшинству против часовой стрелки (от самого высокого старшинства к самому низкому). Старшинство групп основано на их атомном номере (самый тяжелый изотоп является первым). Неполный перечень групп с различным старшинством и обсуждение стереохимии приведены в книге: The Vocabulary of Organic Chemistry, Orchin, et a!., John Wiley and Sons Inc., page 126 (1980), содержание которой полностью включено в настоящее описание посредством ссылки.
[0033] Согласно некоторым вариантам реализации изобретения отдельные R-N изомеры метилналтрексона можно применять в составах и способах. Применяемое в настоящем документе обозначение "R-N-изомер" метилналтрексона относится к указанным соединениям с (R) конфигурацией относительно атома азота. Отдельные изомерные соединения включают без ограничения R-N изомерные метилналтрексоновые соединения, описанные в заявке на патент США с серийным номером 11/441395, поданной 25 мая 2006 года, опубликованной под номером WO 2006/127899, содержание которой включено в настоящий документ посредством ссылки. Согласно некоторым вариантам реализации изобретения, активное соединение представляет собой R-N изомер метилналтрексона или его соль. R-N изомер метилналтрексона, как было показано в USSN 11/441395, представляет собой опиоидный антагонист.
[0034] Согласно некоторым вариантам реализации изобретения отдельные S-N изомеры метилналтрексона можно применять в составах и способах. Применяемое в настоящем документе обозначение "S-N-изомер" метилналтрексона относится к указанным соединениям с (S) конфигурацией относительно атома азота. Отдельные изомерные соединения включают без ограничения S-N изомер соединений метилналтрексона, описанный в заявке на патент США, с серийным номером 11/441452, поданной 25 мая 2006 года, опубликованной под номером WO 2006/127898, содержание которой включено в настоящее описание посредством ссылки. Согласно некоторым вариантам реализации изобретения активное соединение представляет собой S-N изомер метилналтрексона или его соли. S-N изомер метилналтрексона, как было показано в USSN 11/441452, представляет собой опиоидный антагонист.
[0035] Согласно некоторым вариантам реализации изобретения составы на основе метилналтрексона, предложенные в настоящем изобретении, представляют собой смесь стереоизомеров, характеризующуюся действием опиоидного антагониста. Например, метилналтрексон может представлять собой смесь R-N и S-N метилналтрексона, так что сама смесь имеет эффект антагониста и может применяться в способах, описанных в настоящем изобретении для опиоидных антагонистов. В некоторых вариантах реализации изобретения применяют R-N метилналтрексон, который по существу не содержит S-N метилналтрексон.
[0036] Согласно некоторым вариантам реализации изобретения по меньшей мере примерно 99.6%, 99.7%, 99.8%, 99.85%, 99.9%, или 99.95% метилналтрексона находится в (R) конфигурации относительно атома азота. Способы определения количества (R)-N-изомера, присутствующего в пробе по сравнению с количеством (S)-N-изомера, присутствующего в той же самой пробе, подробно описаны в публикации W02006/127899, которая включена в настоящий документ посредством ссылки. Согласно другим вариантам реализации изобретения метилналтрексон содержит 0.15%, 0.10% или меньше (S)-N-изомера.
[0037] Точное количество метилналтрексона (или комбинации метилналтрексона и любого другого конкретного активного вещества), которое необходимо для достижения фармацевтически эффективного количества, варьируется в зависимости от конкретного субъекта, биологического вида субъекта, его возраста и общего состояния здоровья, степени тяжести побочных эффектов или заболевания, конкретного соединения (соединений), способа введения и т.п. Суммарная ежедневная доза метилналтрексона (например, бромида метилналтрексона), как правило, находится в диапазоне 10-200 мг, предпочтительно 20-100 мг, для взрослого человека массой 70 кг. Стандартный лекарственный состав согласно изобретению обычно содержит 1-250 мг активного соединения (например, бромида метилналтрексона) на дозу, 5-100 мг активного соединения на дозу, 10-50 мг активного соединения на дозу или примерно 8 мг или примерно 12 мг или примерно 24 мг активного соединения на дозу. Согласно некоторым вариантам реализации изобретения эффективное количество метилналтрексона для введения взрослому человеку массой 70 кг может содержать от примерно 10 мг до примерно 50 мг соединения (например, бромида метилналтрексона) на стандартную дозу, при введении один или несколько раз в день. Следует принимать во внимание, что диапазоны доз, приведенные выше, только дают представление о введении активного соединения взрослому человеку. Количество, которое следует ввести, например, ребенку или младенцу, может быть определено практикующим врачом или специалистом в данной области техники и может быть ниже или таким же, как при введении взрослому.
Составы
[0038] В настоящем изобретении предложены составы, обеспечивающие сохранность метилналтрексона без существенного образования продуктов разложения при хранении, в том числе хранении при комнатной температуре. Таким образом, предложенные составы способны обеспечивать улучшенные характеристики стабильности метилналтрексона при хранении. Например, согласно некоторым вариантам реализации изобретения состав содержит метилналтрексон, кальциевую соль хелатирующего агента, изотонический агент и носитель. Согласно некоторым вариантам реализации изобретения состав содержит метилналтрексон, кальциевую соль хелатирующего агента, изотонический агент, стабилизатор и носитель. Согласно некоторым вариантам реализации изобретения рН состава находится в интервале между примерно 2 и примерно 5.
[0039] В настоящем изобретении предложены составы и способы доставки метилналтрексона, обеспечивающие улучшенные характеристики при хранении и лучшую сохранность фармацевтических композиций на основе метилналтрексона. В частности, в настоящем изобретении предложены составы, которые являются стабильными и подоходят для парентерального введения композиций на основе метилналтрексона. Предложенные составы для парентерального введения могут включать стерильный раствор для инъекции, стерильную суспензию для инъекции, стерильные эмульсии и дисперсии.
[0040] Например, согласно некоторым вариантам реализации изобретения, составы содержат метилналтрексон и кальциевую соль хелатирующего агента в изотоническом растворе. Согласно некоторым вариантам реализации изобретения составы содержат метилналтрексон, кальциевую соль хелатирующего агента и стабилизатор в изотоническом растворе.
[0041] Как правило, предлагаемые составы содержат одно или несколько активных соединений вместе с одним или несколькими наполнителями, такими как, например, один или несколько хелатирующих агентов, ион кальция, изотонические вещества, носители, буферные вещества, вспомогательные растворители, разбавители, консерванты и/или поверхностно-активные вещества или их комбинации. Специалисту в данной области техники известно, что один и тот же ингредиент может иногда выполнять более одной функции или может выполнять различные функции в различных составах и/или частях составов в зависимости от количества ингредиента и/или присутствия других ингредиентов и/или активного соединения (соединений). Активное соединение может содержать от примерно 0.5 мг до примерно 200 мг бромида метилналтрексона. Согласно некоторым вариантам реализации изобретения активное соединение может содержать от примерно 1 мг до примерно 80 мг, от примерно 5 мг до примерно 40 мг, или примерно 8, или примерно 12 мг, примерно 16 мг, примерно 18 мг, или примерно 24 мг бромида метилналтрексона.
[0042] Согласно некоторым вариантам реализации изобретения состав содержит хелатирующий агент. Согласно некоторым вариантам реализации изобретения хелатирующий агент может присутствовать в составе в количестве от примерно 0.01 мг/мл до примерно 2 мг/мл или от примерно 0.1 мг/мл до примерно 1 мг/мл, или от примерно 0.2 мг/мл до примерно 0.8 мг/мл состава. Согласно некоторым вариантам реализации изобретения хелатирующий агент может присутствовать в составе в количестве от примерно 0.2 мг/мл, примерно 0.3 мг/мл, примерно 0.4 мг/мл, примерно 0.5 мг/мл, или примерно 0.6 мг/мл.
[0043] Авторами настоящего изобретения было обнаружено, что применение хелатирующего агента является эффективным для ингибирования образования по меньшей мере одного продукта разложения. Таким образом, добавление по меньшей мере одного хелатирующего агента является чрезвычайно полезным в составах, которые содержат метил налтрексон, и обеспечивает защиту от образования продуктов разложения, катализируемого металлами, и/или от выпадения осадка. Подходящие хелатирующие агенты включают любые фармацевтически приемлемые хелатирующие агенты и их соли. Примеры хелатирующих агентов включают, но не ограничиваются ими, этилендиаминтетрауксусную кислоту (также известная как EDTA (ЭДТА), эдетиновая кислота, версеновая кислота и секвестрен (sequestrene)) и производные EDTA, такие как натриевая соль EDTA и калиевая соль EDTA, диаммониевая соль EDTA, дикалиевая соль EDTA, динатриевая соль EDTA, триэтиламинная (TEA) соль EDTA, тетранатриевая соль EDTA, трикалиевая соль EDTA, тринатриевая соль EDTA, HEDTA, и тринатриевая соль HEDTA, и родственные соли. Другие хелатирующие агенты включают ниацинамид и его производные и натрия дезоксихолат и его производные, этиленгликоль-бис-(2-аминоэтил)-N,N,N",N'-тетрауксусную кислоту (EGTA) и ее производные, диэтилентриаминпентауксусную кислоту (DTPA) и ее производные, N,N-бис(карбоксиметил)глицин (NTA) и его производные, нитрилотриуксусную кислоту и ее производные. Кроме того, другие хелатирующие агенты включают лимонную кислоту и ее производные. Лимонная кислота также известна в виде моногидрата лимонной кислоты. Производные лимонной кислоты включают безводную лимонную кислоту и тринатрийцитрат-дигидрат. Согласно некоторым вариантам реализации изобретения хелатирующие агенты выбирают из EDTA или производного EDTA, или EGTA или производного EGTA. Согласно некоторым вариантам реализации изобретения хелатирующий агент представляет собой динатриевую соль EDTA, например, гидрат динатриевой соли EDTA.
[0044] Согласно некоторым вариантам реализации изобретения, предложенный состав содержит кальциевую соль. Согласно некоторым вариантам реализации изобретения кальциевая соль может присутствовать в составе в количестве от примерно 0.01 мг/мл до примерно 2 мг/мл или от примерно 0.1 мг/мл до примерно 1 мг/мл, или примерно от 0.2 мг/мл до примерно 0.8 мг/мл состава. Согласно некоторым вариантам реализации изобретения кальциевая соль может присутствовать в составе в количестве от примерно 0.2 мг/мл, примерно 0.3 мг/мл, примерно 0.4 мг/мл, примерно 0.5 мг/мл, или примерно 0.6 мг/мл.
[0045] Авторами настоящего изобретения было обнаружено, что присутствие иона кальция эффективно ингибирует образование по меньшей мере одного продукта разложения. Таким образом, добавление по меньшей мере одной кальциевой соли является особенно полезным в составах, которые включают метилналтрексон, и обеспечивает защиту от образования продуктов разложения катализируемого металлами, и/или от выпадения осадка. Подходящие кальциевые соли включают любые фармацевтически приемлемые кальциевые соли. Примеры кальциевых солей включают без ограничения хлорид кальция, ацетат кальция, цитрат кальция, сульфат кальция и т.д.
[0046] Согласно некоторым вариантам реализации изобретения состав содержит ион кальция и хелатирующий агент в виде одного из компонентов состава. Таким образом, согласно некоторым вариантам реализации изобретения кальциевая соль хелатирующего агента может содержаться в составе в количестве от примерно 0.01 мг/мл до примерно 2 мг/мл или от примерно 0.1 мг/мл до примерно 1 мг/мл, или от примерно 0.2 мг/мл до примерно 0.8 мг/мл состава. Согласно некоторым вариантам реализации изобретения кальциевая соль хелатирующего агента может содержаться в составе в количестве от примерно 0.2 мг/мл, примерно 0.3 мг/мл, примерно 0.4 мг/мл, примерно 0.5 мг/мл, или примерно 0.6 мг/мл.
[0047] Авторами настоящего изобретения было обнаружено, что применение хелатирующего агента на основе кальциевой соли особенно эффективно ингибирует образование по меньшей мере одного продукта разложения. Таким образом, добавление по меньшей мере одной кальциевой соли хелатирующего агента особенно полезно в составах, которые содержат метилналтрексон, и обеспечивает защиту от катализируемого металлами образования 2,2' бис-метилналтрексона и 7-дигидроксиметилналтрексона и/или от выпадения осадка. Согласно некоторым вариантам реализации изобретения состав содержит кальциевую соль хелатирующего агента.
[0048] Подходящие кальциевые соли хелатирующих агентов включают любые фармацевтически приемлемые хелатирующие агенты и их кальциевые соли. Обычные кальциевые соли хелатирующих агентов включают без ограничения кальциевую соль этилендиаминтетрауксусной кислоты (EDTA) и производные кальциевой соли EDTA, кальциевую соль этиленгликоль-бис-(2-аминоэтил)-N,N,N',N'-тетрауксусной кислоты (EGTA) и производные кальциевой соли EGTA, кальциевую соль диэтилентриаминпентауксусной кислоты (DTPA) и производные кальциевой соли DTPA, кальциевую соль N,N-бис(карбоксиметил)глицина (NTA) и производные кальциевой соли NTA и цитрат кальция и его производные. Согласно некоторым вариантам реализации изобретения хелатирующий агент выбирают из кальциевой соли EDTA или производного кальциевой соли EDTA, или кальциевой соли EGTA или производного кальциевой соли EGTA. Согласно некоторым вариантам реализации изобретения хелатирующий агент представляет собой кальциево-динатриевую соль EDTA, например, гидрат кальциево-динатриевой соли EDTA.
[0049] Согласно некоторым вариантам реализации изобретения предложенный состав содержит по меньшей мере метилналтрексон, кальциевую соль хелатирующего агента и изотонический агент. Применяемый в настоящих составах изотонический агент может представлять собой любой фармацевтически приемлемый изотонический агент. Обычные изотонические агенты включают вещества, выбранные из группы, включающей хлорид натрия, маннит, лактозу, декстрозу (водную или безводную), сахарозу, глицерин и сорбит и растворы вышеупомянутых веществ. Согласно некоторым вариантам реализации изобретения состав содержит метилналтрексон, изотонический агент, который представляет собой хлорид натрия, и кальциевую соль хелатирующего агента, представляющую собой кальциевую соль EDTA или производное кальциевой соли EDTA. Согласно некоторым вариантам реализации изобретения EDTA представляет собой кальциево-натриевую соль EDTA.
[0050] Согласно некоторым вариантам реализации изобретения состав содержит по меньшей мере метилналтрексон, изотонический агент, кальциевую соль хелатирующего агента и носитель. Согласно некоторым вариантам реализации изобретения носитель представляет собой водный носитель. Водные носители хорошо известны в данной области техники и включают без ограничения стерильную воду, воду для инъекций, хлорид натрия, инъекционный раствор Рингера, изотонический инъекционный раствор декстрозы, декстрозный и лактатный инъекционный раствор Рингера. Согласно некоторым вариантам реализации изобретения состав содержит воду для инъекций. Согласно некоторым вариантам реализации изобретения составы содержат метилналтрексон или его фармацевтически приемлемую соль, кальциевую соль EDTA или производное кальциевой соли EDTA, воду для инъекции и хлорид натрия в таком количестве, что конечный раствор является изотоническим (например, 0.1%, 0.25%, 0.45% 0.65%, 0.9% хлорида натрия). Согласно некоторым вариантам реализации изобретения, хлорид натрия присутствует в изотоническом количестве в таком количестве, что конечная концентрация хлорида натрия составляет 0.65%.
[0051] Кроме того, предложенные составы могут быть введены дополнительные компоненты, такие как стабилизаторы, буферные вещества, вспомогательные растворители, разбавители, консерванты и/или поверхностно-активные вещества и т.д. Согласно некоторым вариантам реализации изобретения содержание в составах указанных дополнительных веществ может составлять от примерно 1% до примерно 30% или примерно от 1% до примерно 12% состава, или от примерно 1% до примерно 10% от общей массы состава. Согласно некоторым вариантам реализации изобретения, содержание дополнительных веществ может составлять от примерно 1%, примерно 2%, примерно 5%, примерно 8% или примерно 10% от общей массы состава. Ниже приведены примеры дополнительных ингредиентов, которые могут быть введены в составы.
[0052] Согласно некоторым вариантам реализации изобретения предложенные составы содержат стабилизатор. Согласно некоторым вариантам реализации изобретения, стабилизатор может присутствовать в составе в количестве от примерно 0.01 мг/мл до примерно 2 мг/мл или от примерно 0.05 мг/мл до примерно 1 мг/мл, или от примерно 0.1 мг/мл до примерно 0.8 мг/мл. Согласно некоторым вариантам реализации изобретения стабилизатор может присутствовать в количестве от примерно 0.15 мг/мл, примерно 0.2 мг/мл, примерно 0.25 мг/мл, примерно 0.3 мг/мл, примерно 0.35 мг/мл, или примерно 0.4 мг/мл.
[0053] Подходящие стабилизаторы, применяемые в составах согласно настоящему изобретению, включают без ограничения глицин, бензойную кислоту, лимонную, гликолевую, молочную, яблочную и малеиновую кислоту. Согласно некоторым вариантам реализации изобретения, состав содержит глицин. Согласно некоторым вариантам реализации изобретения глицин включает глицин-HCl. Согласно некоторым вариантам реализации изобретения составы содержат метилналтрексон, кальциевую соль EDTA или производное кальциевой соли EDTA, воду для инъекций, хлорид натрия в таком количестве, что конечная концентрация изотонического хлорида натрия составляет 6.5 мг/мл, и глицин в виде глицина-НСl.
[0054] Согласно некоторым вариантам реализации изобретения к составу добавляют стабилизатор в количестве, достаточном для установления и поддержания заданного значения рН состава. Таким образом, согласно некоторым вариантам реализации изобретения, стабилизатор помимо своей основной функции выполняет функцию буфера. Согласно некоторым вариантам реализации изобретения стабилизатор может выступать в качестве буферного вещества, поддерживающего заданный рН состава. Согласно некоторым вариантам реализации изобретения значение рН находится в интервале между примерно 2.0 и примерно 6.0. Согласно некоторым вариантам реализации изобретения значение рН состава находится в интервале между примерно 2.6 и примерно 5.0. Согласно некоторым вариантам реализации изобретения значение рН состава находится в интервале между примерно 3.0 и примерно 4.0. Согласно некоторым вариантам реализации изобретения значение рН состава находится в интервале между примерно 3.4 и примерно 3.6. Согласно некоторым вариантам реализации изобретения значение рН состава составляет примерно 3.5.
[0055] Согласно некоторым вариантам реализации изобретения предложенные составы содержат метилналтрексон, кальциевую соль EDTA или производное кальциевой соли EDTA, воду для инъекций, хлорид натрия в таком количестве, что конечная концентрация изотонического хлорида натрия составляет 6.5 мг/мл, и глицин, при этом рН состава находится в интервале между примерно 3.0 и примерно 4.0. Согласно некоторым вариантам реализации изобретения составы содержат метилналтрексон или его фармацевтически приемлемую соль, кальциевую соль EDTA или производное кальциевой соли EDTA, воду для инъекций, хлорид натрия в таком количестве, что конечная концентрация изотонического хлорида натрия составляет 6.5 мг/мл, глицин, при этом рН состава находится в интервале между примерно 3.4 и примерно 3.6. Согласно некоторым вариантам реализации изобретения составы содержат бромид метилналтрексона, кальциевую соль EDTA или производное кальциевой соли EDTA, воду для инъекций, хлорид натрия в таком количестве, что конечная концентрация изотонического хлорида натрия составляет 6.5 мг/мл, и глицин, при этом рН состава составляет примерно 3.5. Согласно некоторым вариантам реализации изобретения рН регулируют с помощью глицина. Согласно некоторым вариантам реализации изобретения, глицин представляет собой глицин-НСl.
[0056] Согласно некоторым вариантам реализации изобретения предложенные составы содержат бромид метилналтрексона, кальциевую соль EDTA, воду для инъекций, изотонический хлорид натрия и глицин-НСl, при этом рН состава находится в интервале между примерно 3.4 и примерно 3.6. Согласно некоторым вариантам реализации изобретения предложенные составы содержат бромид метилналтрексона с концентрацией примерно 20 мг/мл, кальциевую соль EDTA с концентрацией примерно 0.4 мг/мл, хлорид натрия в таком количестве, что конечная концентрация изотонического хлорида натрия составляет 6.5 мг/мл, и глицин-НСl с концентрацией примерно 0.3 мг/мл, при этом рН состава равен примерно 3.5. Согласно некоторым вариантам реализации изобретения составы содержат бромид метилналтрексона с концентрацией примерно 10 мг/мл, кальциевую соль EDTA с концентрацией примерно 0.2 мг/мл, хлорид натрия в таком количестве, что конечная концентрация изотонического хлорида натрия составляет 3.25 мг/мл, и глицин-НСl с концентрацией примерно 0.15 мг/мл, при этом рН состава равен примерно 3.5.
[0057] Для специалиста в данной области техники очевидно, что для обеспечения требуемого рН предложенного состава может потребоваться дополнительное регулирование рН. Таким образом, согласно некоторым вариантам реализации изобретения дальнейшее установление рН осуществляют с помощью соляной кислоты и/или гидроксида натрия.
Дополнительные компоненты
[0058] Согласно некоторым вариантам реализации изобретения составы могут содержать одно или несколько дополнительных веществ для изменения и/или оптимизации характеристик высвобождения и/или всасывания. Например, как упомянуто выше, включение буферных веществ, вспомогательных растворителей, разбавителей, консервантов и/или поверхностно-активных веществ может способствовать растворению, всасыванию, стабильности и/или повышению активности активного соединения (соединений) и может применяться в составах, предложенных в изобретении. Согласно некоторым вариантам реализации изобретения при включении дополнительных веществ в состав количество дополнительных веществ в составе может составлять: буферных веществ - примерно от 10% до примерно 90%, вспомогательных растворителей - от примерно 1% до примерно 50%, разбавителей - от примерно 1% до примерно 10%, консервантов - от примерно 0.1% до примерно 8% и/или поверхностно-активных веществ - от примерно 1% до примерно 30% от общей массы состава в зависимости от конкретного случая.
[0059] Подходящие вспомогательные растворители (т.е. смешивающиеся с водой растворители) хорошо известны в данной области техники. Например, подходящие вспомогательные растворители включают без ограничения этиловый спирт и пропиленгликоль.
[0060] Для улучшения характеристик продукта можно добавлять физиологически приемлемые разбавители. Физиологически приемлемые разбавители хорошо известны в данной области техники и включают без ограничения сахара, неорганические соли и аминокислоты и растворы любых из вышеупомянутых веществ. Представительные примеры приемлемых разбавителей включают декстрозу, маннит, лактозу и сахарозу, хлорид натрия, фосфат натрия и хлорид кальция, аргинин, тирозин и лейцин и т.п., и их водные растворы.
[0061] Подходящие консерванты хорошо известны в данной области техники и включают, например, бензиловый спирт, метилпарабен, пропилпарабен, натриевые соли метилпарабена, тимерозал, хлорбутанол, фенол. Подходящие консерванты включают без ограничения хлорбутанол (0.3-0.9% вес/об.), парабены (0.01-5.0% вес/об.), тимерозал (0.004-0.2% вес/об.), бензиловый спирт (0.5-5% вес/об.), фенол (0.1-1.0% вес/об.) и т.п.
[0062] Подходящие поверхностно-активные вещества известны в данной области техники и включают, например, полоксамер, полиоксиэтиленовые эфиры, полиоксиэтиленовые эфиры сорбита и жирных кислот, полиоксиэтиленовые эфиры жирных кислот, полиэтиленгликолевые эфиры жирных кислот, полиоксиэтиленовое гидрогенизированное касторовое масло, полиоксиэтиленалкиловый эфир, эфиры полиоксиэтиленовой жирной кислоты, цетиловый спирт, глицериновые эфиры жирных кислот (например, триацетин, глицерин моностеарат и т.п.), полиоксиметиленстеарат, лаурилсульфат натрия, эфиры сорбита и жирных кислот, эфиры сахарозы и жирных кислот, бензалкония хлорид, полиэтоксилированное касторовое масло, и докузат натрия и т.п. и их комбинации. Согласно некоторым вариантам реализации изобретения состав может также содержать поверхностно-активное вещество.
Дозированные формы
[0063] Как было указано, в настоящем изобретении предложены лекарственные формы, в том числе стандартные лекарственные формы, концентраты дозированных количеств препарата и т.д. для парентерального введения. Парентеральное введение предложенных составов может включать любую внутривенную инъекцию, внутривенную инфузию, интрадермальную инъекцию, инъекцию в пораженные ткани, внутримышечную, подкожную инъекцию или введение стандартной дозы с помощью депо. Стандартная доза может являться или может не являться однократной "дозой" активного соединения (соединений), так как лечащий врач может выбрать для введения более одной, менее одной или ровно одну стандартную дозу при каждой приеме (т.е. при каждом введении). Например, стандартные дозы можно вводить один раз, менее одного раза или более одного раза в день, например, раз в неделю, через день (QOD), раз в день или 2, 3 или 4 раза в день, более предпочтительно 1 или 2 раза в день.
[0064] Согласно некоторым вариантам реализации изобретения, предложенную лекарственную форму вводят субъекту при реабилитации (пациентам, проходящим курс реабилитации после ортопедической операции, например, замены суставов) через день или каждый день. Согласно другим вариантам реализации изобретения предложенная дозировка составляет 12 мг метилналтрексона.
[0065] Согласно некоторым вариантам реализации изобретения, предложенную лекарственную форму вводят субъекту, страдающему от хронической боли, через день или каждый день. Согласно некоторым вариантам реализации изобретения, боль связана или не связана со злокачественным новообразованием. Согласно другим вариантам реализации изобретения предложенная дозировка составляет 12 мг метилналтрексона.
[0066] В настоящем изобретении предложены разнообразные лекарственные формы, применяемые для парентерального введения, в том числе, например, состав на основе метилналтрексона в контейнере (например, во флаконе, ампуле, шприце, пакете, дозаторе и т.д.).
[0067] Согласно одному варианту реализации состав находится во флаконе, заполненном раствором метилналтрексона, при этом раствор содержит по меньшей мере одно активное соединение, которое представляет собой метилналтрексон, и кальциевую соль хелатирующего агента в изотоническом растворе. Согласно одному варианту реализации предлагаемый состав находится во флаконе, при этом флакон заполняют предлагаемым составом, как описано здесь и выше. Согласно некоторым вариантам реализации изобретения предлагаемый состав находится во флаконе вместимостью от примерно 1 мл до примерно 50 мл. Согласно некоторым вариантам реализации изобретения объем флакона составляет примерно 1 мл, примерно 2 мл примерно 5 мл, примерно 10 мл, примерно 25 мл или примерно 50 мл.
[0068] Согласно одному варианту реализации предлагаемый состав находится в шприце или другом дозаторе, заполненном предлагаемым составом, как описано здесь и выше. Согласно некоторым вариантам реализации изобретения вместимость шприца или дозатора составляет от примерно 1 мл до примерно 20 мл. Согласно некоторым вариантам реализации изобретения, шприц или дозатор имеет объем примерно 1 мл, примерно 2 мл, примерно 2.5 мл, примерно 5 мл, примерно 7.5 мл, примерно 10 мл, примерно 15 мл или примерно 20 мл. Согласно некоторым вариантам реализации изобретения в шприце или дозаторе применяют иглу для подкожных инъекций для введения субъекту содержимого шприца или дозатора. Согласно некоторым вариантам реализации изобретения в шприце или дозаторе применяют безыгольный наконечник для введения содержимого контейнера субъекту или, альтернативным образом, для переноса во второй контейнер для смешивания и/или разбавления содержимого с другим раствором. Концентрат предлагаемого состава может находиться в герметичном контейнере, содержащем фармацевтический состав, предложенный в настоящем изобретении, в течение стандартного времени лечения, например, сразу же после разбавления, или вплоть до 24 часов после разбавления, при необходимости. Раствор для внутривенного введения можно приготовить, например, путем добавления концентрата состава в контейнер (например, стеклянные или пластиковые бутылки, флаконы, ампулы) в комбинации с разбавителем, так чтобы обеспечить необходимую для введения концентрацию. Количество концентрата, добавляемого к разбавителю, представляет собой количество, достаточное для лечения субъекта в течение периода, варьирующегося от примерно 6 часов до примерно 1 недели, но предпочтительно от примерно 6 или 12 часов до примерно 24 часов. Предпочтительно, если контейнер также содержит незаполненное пространство, объем которого позволяет (i) добавить водный растворитель, а также (ii) дополнительное пространство, позволяющее, при необходимости, взболтать и полностью перемешать разбавленный концентрат с добавленным водным растворителем. Контейнер можно оборудовать проницаемой или прокалываемой крышкой, например, резиновым уплотнением, чтобы можно было добавить водный растворитель, прокалывая уплотнение с помощью подкожного шприца или другим проницаемым уплотнением, основанным на безыгольном способе проникновения, с целью переноса содержащегося концентрата. Согласно некоторым вариантам реализации изобретения, предлагаемые составы находятся в прокалываемом флаконе. Согласно некоторым вариантам реализации изобретения предлагаемые составы находятся в 10 мл прокалываемом флаконе.
[0069] Добавление водного растворителя в жидкий концентрат можно успешно применять для получения стандартных доз жидких фармацевтических составов путем отбора аликвотных частей или всего содержимого концентрата для разбавления. Концентраты можно добавить в контейнер для внутривенного (ВВ) введения, содержащий подходящий водный растворитель. Подходящие растворители представляют собой стандартные растворы для инъекции, описанные ранее (например, 5% раствор декстрозы, физиологический раствор, лактатный раствор Рингера или стерильная вода для инъекций, и т.д.). Обычные пакеты со стандартной дозой для внутривенного введения (ВВ) представляют собой обыкновенные стеклянные или пластиковые контейнеры стандартного объема (например, 25 мл, 50 мл, 100 мл и 150 мл), имеющие входные и выходные отверстия. Растворы концентрата фармацевтического состава, предлагаемого в изобретении, помещают в контейнер для внутривенного введения стандартной дозы в количестве, необходимом для обеспечения концентрации примерно от 0.1 до примерно 1.0 мг метилналтрексона на мл и предпочтительно от примерно 0.24 до примерно 0.48 мг на мл.
[0070] Согласно другим вариантам реализации изобретения контейнер с предлагаемой лекарственной формой до употребления желательно защищать от воздействия света. Согласно некоторым вариантам реализации изобретения применение такого светозащитного контейнера может подавлять протекание одной или несколько реакций разложения. Например, флакон может представлять собой светонепроницаемый контейнер, который защищает содержимое от воздействия света. Дополнительно и/или альтернативным образом, флакон можно упаковать в контейнер любого типа, который защищает состав от воздействия света (дополнительная вторая упаковка флакона). Аналогичным образом, контейнер любого другого типа может сам представлять собой светозащитный контейнер или может находиться внутри другого светозащитного контейнера.
Приготовление составов согласно изобретению
[0071] Составы, предлагаемые в настоящем изобретении, можно приготовить любым из известных способов, например, как описано М. Е. Aulton в монографии "Pharmaceutics: The Science of Dosage Form Design" (1988) (Churchill Livingstone), соответствующие разделы которой включены в настоящее описание посредством ссылки.
[0072] Согласно одному варианту реализации предлагаемый состав получают следующим образом: сухие компоненты состава, в том числе активное соединение (например, метилналтрексона бромид) и кальциевую соль хелатирующего агента (например, кальциевую соль EDTA) растворяют в подходящем растворителе (например, изотоническом растворе (например, изотоническом хлориде натрия для инъекций)). Дополнительные сухие и/или жидкие ингредиенты (например, растворитель (например, воду)), стабилизатор или поверхностно-активное вещество добавляются по выбору. Дополнительные компоненты, такие как стабилизаторы или поверхностно-активные вещества добавляются по выбору перед растворением других компонентов. Предлагаемый состав может быть приготовлен в условиях низкого содержания кислорода.
[0073] Согласно еще одному варианту реализации изобретения предлагаемый состав получают следующим образом: сухие компоненты состава, в том числе активное соединение (например, метилналтрексона бромид) и кальциевую соль хелатирующего агента (например, кальциевую соль EDTA) растворяют в подходящем растворителе (например, изотоническом растворе (например, изотоническом растворе хлорида натрия предназначенного для инъекций)). Альтернативным образом, сухие компоненты состава, в том числе активное соединение (например, метилналтрексона бромид) и изотонический агент (например, хлорид натрия) растворяют в водном растворителе (например, воде для инъекции) для получения активного соединения в изотоническом растворе (например, метилналтрексона в изотоническом хлориде натрия, предназначенного для инъекций), с последующим дополнительным добавлением и растворением кальциевой соли хелатирующего агента (например, кальциевой соли EDTA). Далее, можно установить рН раствора. Например, добавление глицина позволяет установить заданное значение рН. Например, добавление в раствор глицин-НСl можно применять для установления требуемого рН (например, рН 3-4, рН 3.4-3.6, рН 3.5). Дополнительные сухие и/или жидкие ингредиенты (например, растворитель (например, вода), стабилизатор (например, глицин) или поверхностно-активное вещество добавляются по выбору. К растворителю до растворения других компонентов по выбору можно добавить дополнительные компоненты, такие как стабилизаторы, поверхностно-активные вещества. Предлагаемые составы могут быть приготовлены в условиях низкого содержания кислорода.
[0074] Согласно одному варианту реализации приготовленные составы помещают во флаконы, ампулы, шприцы или дозаторы, в отдельности или с дополнительными наполнителями. Типичные наполнители, добавляемые к предлагаемым составам, включают без ограничения поверхностно-активные вещества, консерванты, разбавители, буферные вещества, вспомогательные растворители и т.д. Типичное количество дополнительных наполнителей, добавляемых к раствору, может включать, например, от примерно 10% до примерно 90% буферных веществ, от примерно 1% до примерно 50% вспомогательных растворителей, от примерно 1% до примерно 10% разбавителей, от примерно 0.1% до примерно 8% консервантов, и от примерно 1% до примерно 30% поверхностно-активных веществ, относительно общей массы.
[0075] Перед упаковкой приготовленный состав может подвергаться процессу фильтрации. Процесс фильтрации перед упаковкой может включать, например, в случае препаратов для инъекции, стерилизующую фильтрацию и/или ультрафильтрацию обрабатываемого раствора с целью уничтожения микроорганизмов или других загрязняющих веществ, содержащихся в обрабатываемом растворе.
[0076] Приготовленный состав можно расфасовать по флаконам (например, по прозрачным стеклянным флаконам, флаконам из желтого стекла), ампулам, шприцам или дозаторам (например, автодозаторам). Процесс распределения включает, например, в случае расфасовки во флаконы, процесс распределения подходящего объема раствора во флаконы с учетом концентрации метилналтрексона, с тем чтобы обеспечить заданное содержание метилналрексона во флаконе.
Выделение и идентификация продуктов разложения
[0077] Авторами настоящего изобретения была проведена идентификация продуктов разложения, обнаруженных в растворах метилналтрексона, а также исследования некоторых каталитических реакций, образуются указанные продукты разложения. Более того, среди прочего, авторами изобретения были установлены способы контроля образования продуктов разложения, что позволило понизить содержание продуктов разложения в жидких составах, содержащих метилналтрексон. В приведенном далее примере 1 подробно описаны способы и результаты такой идентификации, в том числе структуры образовавшихся при разложении соединений. В дополнительных примерах также дана характеристика приготовленных растворов и идентификация механизмов каталитического образования и/или ингибирования образования продуктов разложения.
[0078] Таким образом, в изобретении предложены способы обнаружения одного или нескольких продуктов разложения в составах на основе метилналтрексона. Согласно некоторым вариантам реализации изобретения, способы обнаружения продуктов разложения при их содержании ниже указанного предела являются предпочтительными при производстве состава на основе метилналтрексона. Обнаружение образования конкретного продукта разложения в составе на основе метилналтрексона с помощью ВЭЖХ, а также анализ состава, содержащего один или несколько продуктов разложения при их содержании ниже определенного уровня, являются предпочтительными. Согласно некоторым вариантам реализации изобретения, способ предусматривает анализ состава на основе метилналтрексона методом ВЭЖХ и установление отсутствия превышения уровня одного или нескольких конкретных продуктов разложения. Предпочтительные концентрации, которые не должны быть превышены для одного или нескольких продуктов разложения, описаны в нижеследующих параграфах, касающихся содержания продуктов разложения в предлагаемых составах.
[0079] Кроме того, в изобретении предложены составы, которые ингибируют образование продуктов разложения метилналтрексона и обеспечивают улучшенные характеристики стабильности составов, композиций и продуктов, содержащих составы на основе метилналтрексона. Согласно некоторым вариантам реализации в изобретении предложены составы на основе метилналтрексона, в которых концентрация всех продуктов разложения не превышает примерно 2% от содержания метилналтрексона в препарате после двенадцати или восемнадцати месяцев хранения. Согласно некоторым вариантам реализации в изобретении предложены составы на основе метилналтрексона, в которых концентрация всех продуктов разложения не превышает примерно 1.5% от содержания метилналтрексона в препарате после двенадцати или восемнадцати месяцев хранения. Согласно конкретным вариантам реализации, в изобретении предложены составы на основе метилналтрексона, в которых концентрация всех продуктов разложения не превышает примерно 1% от содержания метилналтрексона в препарате после двенадцати или восемнадцати месяцев хранения. Предпочтительные условия хранения включают хранение при комнатной температуре.
[0080] Согласно некоторым вариантам реализации в изобретении предложены составы на основе метилналтрексона, в которых концентрация всех продуктов разложения не превышает примерно 1.5% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре. Согласно некоторым вариантам реализации в изобретении предложены составы на основе метилналтрексона, в которых концентрация всех продуктов разложения не превышает примерно 1% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре. Согласно конкретным вариантам реализации в изобретении предложены составы на основе метилналтрексона, в которых концентрация всех продуктов разложения не превышает примерно 0.5% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре.
[0081] Согласно некоторым вариантам реализации в изобретении предложены составы на основе метилналтрексона, в которых концентрация продукта разложения в виде 2,2' бис-метилналтрексона (RRT 1.55) не превышает примерно 0.5% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре. Согласно некоторым вариантам реализации в изобретении предложены составы на основе метилналтрексона, в которых концентрация продукта разложения в виде 2,2'-бис-метилналтрексона (RRT 1.55) не превышает примерно 0.2% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре. Согласно более конкретным вариантам реализации в изобретении предложены составы на основе метилналтрексона, в которых концентрация продукта разложения в виде 2,2' бис-метилналтрексона (RRT 1.55) не превышает примерно 0.1% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре.
[0082] Согласно некоторым вариантам реализации в изобретении предложены составы на основе метилналтрексона, в которых концентрация продукта разложения в виде 7-дигидроксиметилналтрексона (RRT 0.67) не превышает примерно 0.5% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре. Согласно некоторым вариантам реализации в изобретении предложены составы на основе метилналтрексона, в которых концентрация продукта разложения в виде 7-дигидроксиметилналтрексона (RRT 0.67) не превышает примерно 0.2% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре. Согласно более конкретным вариантам реализации в изобретении предложены составы на основе метилналтрексона, в которых концентрация продукта разложения в виде 7-дигидроксиметилналтрексона (RRT 0.67) не превышает примерно 0.1% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре.
[0083] Согласно некоторым вариантам реализации в изобретении предложены составы на основе метилналтрексона, в которых концентрация продукта разложения в виде метилналтрексона с суженным циклом (RRT 0.79) не превышает примерно 0.5% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре. Согласно некоторым вариантам реализации в изобретении предложены составы на основе метилналтрексона, в которых концентрация продукта разложения в виде метилналтрексона с суженным циклом (RRT 0.79) не превышает примерно 0.2% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре. Согласно конкретным вариантам реализации в изобретении предложены составы на основе метилналтрексона, в которых концентрация продукта разложения в виде метилналтрексона с суженным циклом (RRT 0.79) не превышает примерно 0.1% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре.
[0084] Согласно некоторым вариантам реализации в изобретении предложены составы на основе метилналтрексона, в которых концентрация продукта разложения метилналтрексона в виде альдольного димера (RRT 1.77) не превышает примерно 0.5% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре. Согласно некоторым вариантам реализации в изобретении предложены составы на основе метилналтрексона, в которых концентрация продукта разложения метилналтрексона в виде альдольного димера (RRT 1.77) не превышает примерно 0.2% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре. Согласно конкретным вариантам реализации в изобретении предложены составы на основе метилналтрексона, в которых концентрация продукта разложения метилналтрексона в виде альдольного димера (RRT 1.77) не превышает примерно 0.1% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре.
[0085] Согласно некоторым вариантам реализации в изобретении предложены составы на основе метилналтрексона, в которых концентрация продукта разложения метилналтрексона, образующегося в результате протекания реакции разложения Гофмана (RRT 2.26), не превышает примерно 0.5% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре. Согласно некоторым вариантам реализации в изобретении предложены составы на основе метилналтрексона, в которых концентрация продукта разложения метилналтрексона, образующегося в результате протекания реакции разложения Гофмана (RRT 2.26), не превышает примерно 0.2% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре. Согласно конкретным вариантам реализации в изобретении предложены составы на основе метилналтрексона, в которых концентрация продукта разложения метилналтрексона, образующегося в результате протекания реакции разложения Гофмана (RRT 2.26), не превышает примерно 0.1% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре.
[0086] Согласно некоторым вариантам реализации в изобретении предложены составы на основе метилналтрексона, в которых концентрация O-метилметилналтрексона (RRT 1.66) не превышает примерно 0.5% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре. Согласно некоторым вариантам реализации в изобретении предложены составы на основе метилналтрексона, в которых концентрация O-метил-метилналтрексона (RRT 1.66) не превышает примерно 0.25% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре. Согласно конкретным вариантам реализации в изобретении предложены составы на основе метилналтрексона, в которых концентрация O-метилметилналтрексона (RRT 1.66) не превышает примерно 0.15% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре.
[0087] Согласно некоторым вариантам реализации, в изобретении предложены составы на основе метилналтрексона, в которых количество S-N-метилналтрексона в исходном составе составляет менее 0.5 масс.% (относительно суммарного количества метилналтрексона), при этом концентрация продукта разложения в виде S-метилналтрексона (RRT 0.89) не превышает примерно 0.5% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре. Согласно некоторым вариантам реализации в изобретении предложены составы на основе метилналтрексона, в которых концентрация продукта разложения в виде S-метилналтрексона (RRT 0.89) не превышает примерно 0.2% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре. Согласно конкретным вариантам реализации в изобретении предложены составы на основе метилналтрексона, в которых концентрация продукта разложения в виде S-метилналтрексона (RRT 0.89) не превышает примерно 0.1% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре.
[0088] Согласно некоторым вариантам реализации, в изобретении предложены составы на основе метилналтрексона, в которых концентрация всех продуктов разложения не превышает примерно 1.25% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре, концентрация продукта разложения в виде 2,2' бис-метилналтрексона (RRT 1.55) не превышает примерно 0.2% от содержания метилналтрексона, в которых концентрация продукта разложения в виде 7-дигидроксиметилналтрексона (RRT 0.67) не превышает примерно 0.2% от содержания метилналтрексона, концентрация продукта разложения в виде метилналтрексона с суженным циклом (RRT 0.79) не превышает примерно 0.2% от содержания метилналтрексона, концентрация продукта разложения метилналтрексона в виде альдольного димера (RRT 1.77) не превышает примерно 0.2% от содержания метилналтрексона, концентрация продукта разложения метилналтрексона, образующегося в результате протекания реакции разложения Гофмана (RRT 2.26), не превышает примерно 0.2% от содержания метилналтрексона, и концентрация 0-метилметилналтрексона (RRT 1.66) не превышает примерно 0.25% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре.
[0089] Согласно некоторым вариантам реализации в изобретении предложены составы на основе метилналтрексона, в которых концентрация всех продуктов разложения не превышает примерно 0.75% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре, концентрация продукта разложения в виде 2,2'-бис-метилналтрексона (RRT 1.55) не превышает примерно 0.1% от содержания метилналтрексона, при этом концентрация продукта разложения в виде 7-дигидроксиметилналтрексона (RRT 0.67) не превышает примерно 0.1% от содержания метилналтрексона, концентрация продукта разложения в виде метилналтрексона с суженным циклом (RRT 0.79) не превышает примерно 0.15% от содержания метилналтрексона, концентрация разложения метилналтрексона в виде альдольного димера (RRT 1.77) не превышает примерно 0.05% от содержания метилналтрексона, концентрация продукта разложения метилналтрексона, образующегося в результате протекания реакции разложения Гофмана (RRT 2.26), не превышает примерно 0.1% от содержания метилналтрексона, и концентрация O-метилметилналтрексона (RRT 1.66) не превышает примерно 0.15% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре.
[0090] Согласно другим вариантам реализации в изобретении предложены составы на основе метилналтрексона, в которых концентрация продукта разложения в виде 2,2'-бис-метилналтрексона (RRT 1.55) не превышает примерно 0.2% от содержания метилналтрексона, в которых концентрация продукта разложения в виде 7-дигидроксиметилналтрексона (RRT 0.67) не превышает примерно 0.2% от содержания метилналтрексона, концентрация продукта разложения в виде метилналтрексона с суженным циклом (RRT 0.79) не превышает примерно 0.2% от содержания метилналтрексона, и концентрация продукта разложения метилналтрексона, образующегося в результате протекания реакции разложения Гофмана (RRT 2.26), не превышает примерно 0.2% от содержания метилналтрексона в препарате после шести месяцев хранения при комнатной температуре.
Комбинированные продукты и совместное введение
[0091] Согласно некоторым вариантам реализации изобретения помимо метилналтрексона предложенные составы содержат одно или несколько других активных соединений. В таких комбинированных составах дополнительное соединение (соединения) может содержаться в одной или нескольких порциях состава, содержащих метилналтрексон, может отсутствовать в одной или нескольких порциях, содержащих метилналтрексон, и/или может содержаться в одной или нескольких порциях, не содержащих метилналтрексон. В частности, изобретение включает составы, которые обеспечивают доставку по меньшей мере метилналтрексона и по меньшей мере одного другого активного соединения. Кроме того, настоящее изобретение включает составы, которые обеспечивают доставку по меньшей мере двух независимых порций метилналтрексона, и которые также обеспечивают доставку по меньшей мере одного другого активного соединения (соединений).
[0092] Согласно некоторым вариантам реализации изобретения составы содержат как опиоид, так и метилналтрексон (например, антагонист µ-опиоидного рецептора). Такие комбинированные продукты, содержащие как опиоид, так и антагонист опиоида, позволяют одновременно добиться облегчения боли и уменьшения связанных с приемом опиоидов побочных эффектов (например, воздействия на желудочно-кишечный тракт (например, замедления опорожнения желудка, изменения перистальтики ЖК тракта), и т.д.).
[0093] Опиоиды, применяемые при лечении с целью анастезии, хорошо известны в данной области техники. Например, опиоидные соединения включают без ограничения альфентанил, анилеридин, азимадолин, бремазоцин, бурпренорфин, буторфанол, кодеин, дезоцин, диацетилморфин (героин), дигидрокодеин, дифеноксилат, этилморфин, федотоцин, фентанил, фуналтрексамин, гидрокодон, гидроморфон, леваллорфан, левометадил ацетат, леворфанол, лоперамид, меперидин (петидин), метадон, морфин, морфин-6-глюкоронид, налбуфин, налорфин, никоморфин, опиум, оксикодон, оксиморфон, папаверетум, пентазоцин, пропирам, пропоксифен, ремифентанил, суфентанил, тилидин, тримебутин и трамадол.
Согласно некоторым вариантам реализации изобретения опиоид представляет собой по меньшей мере один опиоид, выбранный из альфентанила, бупренорфина, буторфанола, кодеина, дезоцина, дигидрокодеина, фентанила, гидрокодона, гидроморфона, леворфанола, меперидина (петидина), метадона, морфина, налбуфина, никоморфина, оксикодона, оксиморфона, папаверетума, пентазоцина, пропирама, пропоксифена, суфентанила и/или трамадола. Согласно некоторым вариантам реализации изобретения опиоид выбирают из морфина, кодеина, оксикодона, гидрокодона, дигидрокодеина, пропоксифена, фентанила, трамадола и их смесей. Согласно конкретному варианту реализации изобретения, опиоид представляет собой лоперамид. Согласно другому конкретному варианту реализации, опиоид представляет собой гидроморфон. Согласно другим вариантам реализации изобретения опиоид представляет собой смешанный агонист, такой как буторфанол. Согласно некоторым вариантам реализации изобретения пациентам вводят более одного опиоида, например, морфин и героин или метадон и героин.
[0094] Количество дополнительного активного соединения (соединений), содержащегося в комбинированных композициях согласно настоящему изобретению, как правило, не превышает количество, обычно вводимое в составе композиции, содержащей указанное активное соединение в качестве единственного терапевтического препарата. Согласно некоторым вариантам реализации изобретения количество дополнительного активного соединения находится в диапазоне от примерно 50% до 100% от количества, обычно содержащегося в композиции, содержащей указанное активное соединение в качестве единственного терапевтического препарата.
[0095] Согласно некоторым вариантам реализации изобретения составы также можно применять в сочетании и/или в комбинации с дополнительными активными соединениями и/или традиционными способами лечения желудочно-кишечной дисфункции с целью уменьшения запора и дисфункции кишечника. Традиционные терапевтические способы лечения, например, включают без ограничения функциональное стимулирование кишечного тракта, препараты, смягчающие стул, слабительные средства (например, дифелиметановые слабительные средства, очистительные слабительные средства, осмотические слабительные средства, солевые слабительные средства и т.д.), препараты и слабительные средства, способствующие увеличению объема содержимого кишечника, смазывающие вещества, внутривенную гидратацию и назогастральную декомпрессию.
Наборы и применение составов
Применение
[0096] Как обсуждалось выше, в настоящем изобретении предложены составы, которые можно применять в качестве антагонистов для подавления нежелательных побочных эффектов опиоидной обезболивающей терапии (например, воздействия на желудочно-кишечный тракт (например, замедления опорожнения желудка, изменения перистальтики ЖК тракта) и т.д.). Кроме того, составы, предлагаемые в изобретении, можно применять для лечения субъектов с болезненными состояниями, которые улучшаются при связывании µ-опиоидных рецепторов или при любом лечении, где необходимо временное подавление системы µ-опиоидных рецепторов (например, лечении кишечной непроходимости и т.д.). Согласно некоторым вариантам реализации изобретения составы применяют для лечения человека.
[0097] Соответственно, введение предлагаемых составов может обеспечивать преимущества при лечении, предотвращении, облегчении, замедлении или уменьшении побочных эффектов, возникающих при введении опиоидов, таких как, например, желудочно-кишечная дисфункция (например, ингибирование кишечной перистальтики, запор, сужение сфинктера ЖКТ, тошнота, рвота, спазм желчевыводящих путей, опиоидная дисфункция кишечника, колики) дисфория, зуд, задержка мочи, подавление дыхания, спазм папиллярной мышцы, воздействие на сердечно-сосудистую систему, ригидность грудных стенок и подавление кашля, подавление стрессовой реакции и подавление иммунитета, связанное с применением наркотических анальгетиков и т.д., или их комбинации. Таким образом, применение предложенных составов может быть полезным с точки зрения улучшения качества жизни субъектов, принимающих опиоиды, а также уменьшения осложнений, возникающих из-за хронического запора, таких как геморрой, потеря аппетита, разрушение слизистой оболочки, сепсис, риск развития рака толстой кишки и инфаркт миокарда.
[0098] Согласно некоторым вариантам реализации изобретения предлагаемые составы можно применять для введения субъекту, проходящему краткосрочный курс лечения опиоидами. Согласно некоторым вариантам реализации изобретения предлагаемые составы можно применять для введения субъектам, страдающим от послеоперационной желудочно-кишечной дисфункции.
[0099] Согласно другим вариантам реализации изобретения предлагаемые составы также можно применять для введения субъектам, принимающим опиоиды в течение длительного времени (например, неизлечимо больным субъектам, проходящим опиоидную терапию, таким как субъекты, больные СПИДом, раком, страдающие от сердечно-сосудистых заболеваний; субъекты, постоянно проходящие опиоидную терапию с целью обезболивания; субъекты, проходящие опиоидную терапию с целью облегчения синдрома отмены опиоидов). Согласно некоторым вариантам реализации изобретения субъект принимает опиоид для облегчения хронической боли. Согласно некоторым вариантам реализации изобретения субъект является неизлечимо больным субъектом. Согласно другим вариантам реализации изобретения субъект является человеком, подвергаемым опиоидной терапии с целью уменьшения синдрома отмены опиоидов.
[00100] Дополнительное применение составов, описанных в настоящем изобретении, может быть направлено на лечение, уменьшение, ингибирование или предотвращение побочных эффектов от введения опиоидов, в том числе, например, аберрантной миграции или пролиферации эндотелиальных клеток (например, васкулярных эндотелиальных клеток), роста ангиогенеза и роста смертности в результате продуцирования условно-патогенных возбудителей инфекции (например, Pseudomonas aeruginosa). Дополнительное применение предложенных составов, которое обеспечивает преимущество, включает лечение иммуносупрессии, вызванной опиоидами, ингибирование ангиогенеза, ингибирование васкулярной пролиферации, лечение боли, лечение воспалительных состояний, таких как синдром воспаления кишечника, лечение инфекционных заболеваний и заболеваний костно-мышечной системы, таких как остеопороз, артрит, остит, периостит, миопатия, и лечение аутоиммунных заболеваний.
[00101] Согласно некоторым вариантам реализации составы, предлагаемые в изобретении, можно применять для предотвращения, ингибирования, снижения, замедления, уменьшения или лечения желудочно-кишечной дисфункции, в том числе, без ограничения синдрома раздраженной толстой кишки, дисфункции кишечника, вызванной опиоидами, колита, послеоперационной или связанной с параличом кишечной непроходимости или послеродовой кишечной непроходимости, тошноты и/или рвоты, ухудшения желудочной перистальтики и опорожнения, ингибирования желудочной пропульсии и пропульсии тонкой и/или толстой кишки, роста амплитуды непропульсивных сегментообразных сокращений, сужения сфинктера Одди, увеличения тонуса анального сфинктера, нарушения рефлекторной релаксации с растяжением прямой кишки, снижения желудочной, печеночной, панкреатической или кишечной секреции, увеличения всасывания воды из содержимого кишечника, гастроэзофагеального рефлюкса, пареза желудка, спазма, вздутия, брюшной или подложечной боли и дискомфорта, запора, идиопатического запора, послеоперационной желудочно-кишечной дисфункции после операции на брюшной полости (например, колэктомии (например, правосторонней гемиколэктомии, левосторонней гемиколэктомии, поперечной гемиколэктомии, подготовке в колэктомии, низкой передней резекции) или грыжесечении), и замедления всасывания перорально введенных лекарственных препаратов или питательных веществ.
[00102] Предлагаемые составы также можно применять при лечении состояний, в том числе раковых заболеваний, связанных с ангиогенезом, иммуносупрессии, серповидноклеточной анемии, сосудистых повреждений и ретинопатии, при лечении заболеваний, вызванных воспалением (например, синдрома раздраженного кишечника), иммуносупрессии, хронического воспаления.
[00103] Согласно дополнительным вариантам реализации в изобретении предложено применение указанных составов в ветеринарных целях (например, при лечении домашних животных, например, лошадей, собак, кошек и т.д.). Соответственно, предполагается применение предложенных составов в ветеринарных целях, аналогичных тем, что обсуждались выше и применяются для лечения человека. Например, ингибирование желудочно-кишечной перистальтики у лошадей, такой как колики и запор, может быть фатальным для лошади. Боль, возникающая при страдании лошади от колик, может привести к вызывающему смерть шоку, хотя длительный запор может также вызвать смерть лошади. Лечение лошадей антагонистами периферийных опиоидов было описано, например, в публикации патента США No.20050124657 от 20 января 2005 г.
[00104] Следует также иметь в виду, что составы, предлагаемые в настоящем изобретении, можно применять в ходе комбинированной терапии, то есть метилналтрексон и его композиции можно вводить одновременно, до или после введения одного или нескольких других требуемых лекарственных препаратов или перед осуществлением медицинских процедур. В случае конкретных комбинированных способов лечения (лекарственных препаратах или процедурах), применяемых в комбинированных режимах, также учитывают совместимость требуемых лекарственных средств и/или процедур и необходимый терапевтический эффект, который должен быть достигнут. Также следует иметь в виду, что применяемые лекарственные средства могут обеспечивать желаемый эффект в отношении одного и того же заболевания (например, состав можно ввести одновременно с другим соединениями, применяемыми для лечения этого же заболевания), или они могут обеспечивать разные эффекты (например, сдерживание любых неблагоприятных эффектов). Применяемые согласно настоящему изобретению дополнительные терапевтические соединения, которые обычно вводят для лечения или предотвращения конкретного заболевания или состояния, известны как "подходящие для лечения заболевания или состояния".
[00105] Согласно другим вариантам реализации изобретения, предлагаемые составы и лекарственные формы можно применять при приготовлении медицинских препаратов, в том числе без ограничения препаратов, подходящих для лечения побочных эффектов от введения опиоидов (например, желудочно-кишечных побочных эффектов (например, ингибирования перистальтики кишечника, сужение сфинктера ЖКТ, запора, тошноты, рвоты) дисфории, зуда и т.д.) или их комбинаций. Предлагаемые составы можно использовать при приготовлении медицинских препаратов, применяемых при лечении субъектов, проходящих краткосрочную опиоидную терапию (например, субъектов, страдающих от послеоперационной желудочно-кишечной дисфункции, краткосрочно принимающих опиоиды), или субъектов, применяющих опиоиды в течение длительного времени (например, неизлечимо больных субъектов, проходящих опиоидную терапию, таких как субъекты, больные СПИДом, ракомсубъект, субъекты с сердечно-сосудистыми заболеваниями; субъекты, постоянно проходящие опиоидную терапию с целью обезболивания; или субъекты, проходящие опиоидную терапию с целью облегчения синдрома отмены опиоидов). Кроме того, в изобретении предложены способы приготовления лекарственных препаратов, применяемых при лечении боли, лечении воспалительных состояний, таких как синдром воспаления кишечника, при лечении инфекционных заболеваний, лечении заболеваний костно-мышечной системы, таких как остеопороз, артрит, остит, периостит, миопатия, при лечении аутоиммунных заболеваний и иммуносупрессии, при терапии послеоперационной желудочно-кишечной дисфункции после операции на брюшной полости (например, колэктомии (например, правосторонней гемиколэктомии, левосторонней гемиколэктомии, поперечной гемиколэктомии, подготовке в колэктомии, низкой передней резекции), идиопатического запора и кишечной непроходимости), и при лечении таких заболеваний, как раковые заболевания, связанные с ангиогенезом, хроническое воспаление и/или хроническая боль, серповидноклеточная анемия, сосудистые повреждения и ретинопатия.
Фармацевтические наборы и упаковка
100106] Кроме того, настоящее изобретение также включает фармацевтические упаковки и/или наборы. Предлагаемые фармацевтические упаковки и/или наборы могут содержать состав и контейнер (например, флакон, ампулу, бутыль, шприц и/или дозировочную упаковку или другой подходящий контейнер). Согласно некоторым вариантам реализации изобретения предлагаемые наборы могут также дополнительно содержать второй контейнер, содержащий подходящий водный носитель для разбавления с целью восстановления влагосодержания препарата для внутривенного введения субъекту. Согласно некоторым вариантам реализации изобретения содержимое предлагаемого контейнера с составом и контейнера с растворителем объединяют для получения стандартной лекарственной формы.
[00107] Согласно некоторым вариантам реализации изобретения состав, предлагаемый в изобретении, можно применять в сочетании с устройствами для обезболивания, управляемыми субъектом (patient controlled analgesia devices, PCA), при этом субъект может управлять опиоидной аналгезией по мере необходимости. В указанных примерах совместное введение предлагаемых составов можно применять для предотвращения нежелательных побочных эффектов, возникающих при введении опиоидов. Таким образом, наборы, предлагаемые в изобретении, могут содержать состав для введения метилналтрексона, содержащийся внутри картриджа для применения совместно с PCA устройством.
[00108] Согласно некоторым вариантам реализации изобретения состав, предлагаемый в изобретении, можно применять в сочетании с контейнером с разбавителем, подходящим для хранения в замороженном состоянии, при этом состав разбавляют подходящим разбавителем и хранят в контейнере, подходящем для замораживания. Согласно некоторым вариантам реализации изобретения указанные контейнеры для хранения в замороженном состоянии можно разморозить перед внутривенным введением метилналтрексона субъекту. Таким образом, наборы, предлагаемые в изобретении, могут содержать состав для введения метилналтрексона в контейнере, подходящем для хранения в замороженном состоянии, который размораживают перед введением состава субъекту. Согласно одному варианту реализации изобретения указанный контейнер представляет собой пакет для хранения препарата для внутривенного введения в замороженном состоянии.
[00109] Контейнер может иметь одно или несколько отделений для хранения лиофилизированного состава и/или подходящего водного носителя для разбавления. Согласно некоторым вариантам реализации изобретения контейнер может быть модифицирован, т.е. может подвергаться физическому изменению с тем, чтобы обеспечить возможность объединения отделений и/или компонентов из разных отделений. Например, пакет из фольги или пластика может содержать два или несколько отделений, разделенных перфорированной перемычкой, которую можно разрушить для объединения содержимого двух отдельных отделений, как только появится сигнал сломать перемычку. Таким образом, фармацевтическая упаковка или набор может содержать указанные контейнеры с несколькими отделениями, содержащими лиофилизированный состав и подходящий растворитель для восстановления влагосодержания и/или подходящий водный носитель для разбавления состава. К указанным наборам могут быть приложены инструкции по применению.
[00110] Согласно некоторым вариантам реализации изобретения фармацевтический набор содержит состав в пакете или контейнере для разбавления, при этом механизм безыгольного обмена позволяет смешивать состав с изотоническим раствором с целью приготовления продукта для внутривенного введения. Например, согласно некоторым неограничивающим примерам, состав, предлагаемый в изобретении, можно применять в сочетании с системой (Baxter) контейнеров для разбавления MINIBAG®Plus или системой контейнеров для разбавления ADD VANTAGE® (Hospira).
[00111] К наборам, предлагаемым в изобретении, могут быть дополнительно приложены инструкции по применению. Эти инструкции могут представлять собой, например, инструкции по дозированию и введению. Согласно другим вариантам реализации изобретения инструкции могут также содержать дополнительные подробности, касающиеся специализированных инструкций для конкретных контейнеров и/или систем введения. Кроме того, инструкции могут содержать специализированные инструкции по применению препарата в сочетании и/или в комбинации с дополнительной терапией. Согласно одному неограничивающему примеру, составы, предлагаемые в изобретении, можно использовать в сочетании с применением опиоидной аналгезии, что может включать применение устройства для обезболивания, управляемого субъектом (РСА). Таким образом, инструкции по применению предлагаемых составов могут содержать инструкции по применению препарата в сочетании с устройством введения РСА.
[00112] Для более подробного описания настоящего изобретения далее приведены следующие примеры. Следует иметь в виду, что данные примеры являются иллюстративными и никоим образом не ограничивают настоящее изобретение.
ПРИМЕРЫ
ЧАСТЬ I: Стабильность составов согласно изобретению
Пример 1
Идентификация и характеристика продуктов разложения составов на основе метилналтрексона
[00113] Выше, с помощью результатов анализа методом ВЭЖХ были охарактеризованы по меньшей мере три продукта разложения в 20 мг/мл изотоническом солевом растворе (идентифицированы с помощью анализа методом ВЭЖХ в виде пиков с RRT примерно 0.72, 0.89, и 1.48). См., например, публикацию заявки на патент США №20040266806А1, опубликованную 30 декабря 2004 г. Авторы настоящего изобретения исследовали 20 мг/мл солевые растворы метилналтрексона с целью исследования образования продуктов разложения и идентификации продуктов разложения, а также идентификации ингибиторов образования различных продуктов разложения. Авторы настоящего изобретения идентифицировали и определили характеристики продуктов разложения, которые накапливаются в некоторых растворах метилналтрексона. В этих экспериментах по исследованию разложения и в составах, используемых в примерах, применяли R-N-метилналтрексон, содержащий менее 0.15 весовых процентов S-N-метилналтрексона от общей массы метилналтрексона.
[00114] Для проведения ВЭЖХ анализа с целью получения представленных в настоящем документе данных применяли два (2) различных способа. Указанные способы кратко представлены ниже:
Способ А:
Колонка: Prodigy ODS-3 15 см × 2.0 мм, 3 мкм частицы (Phenomenex)
Скорость потока: 0.25 мл/мин
Детектирование: УФ, 280 нм
Подвижная фаза: концентрации: изократические: 75:25 (по объему) 0.1% ТФК (трифторуксусная кислота) в воде/метанол
Подвижная фаза: чистота: градиент, как указано ниже:
Растворитель А: 95:5 (по объему) 0.1% ТФК в воде/метанол
Растворитель В: 35:65 (по объему) 0.1% ТФК в воде/метанол
Растворитель для пробы: 0.05 М двухосновный фосфат натрия, рН 6.8
Программа изменения градиента:
Температура колонки: 50°С
Способ В: (чистота)
Колонка: Prodigy ODS-3 15 см × 4.6 Мм, 3 мкм частицы (Phenomenex)
Скорость потока: 1.5 мл/мин
Детектирование: УФ, 280 нм
Подвижная фаза: градиент, как указано ниже:
Растворитель А: 95:5 (по объему) 0.1% ТФК в воде/метанол
Растворитель В: 25:75 (по объему) 0.1% ТФК в воде/метанол
Растворитель для проб: 0.05М двухосновный фосфат натрия, рН 6.8
Программа изменения градиента:
Способ В: (концентрациия)
Колонка: Prodigy ODS-3 15 см × 4.6 Мм, 3 мкм частицы (Phenomenex)
Скорость потока: 1.0 мл/мин
Обнаружение: УФ, 280 нм
Подвижная фаза: градиент, как указано ниже:
Растворитель А: 95:5 (по объему) 0.1% ТФК в воде/метанол
Растворитель В: 25:75 (по объему) 0.1% ТФК в воде/метанол
Растворитель для проб: 0.05 М двухосновный фосфат натрия, рН 6.8
Программа изменения градиента:
[00115] При исследовании стабильности с помощью анализа методом ВЭЖХ (способ А) проб в указанных условиях хранения были идентифицированы следующие соединения, которые, если не указано иное, имели следующие соответствующие расчетные относительные времена удерживания:
Метилналтрексона бромид RRT 1.00
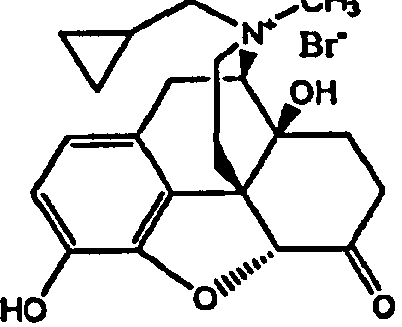
Основание натрексона RRT 1.17

S -метилналтрексон RRT 0.86 или 0.89

Хинон RRT 0.89 (для таблиц 11 С-2, 11С-3, 12А-2, 12 В-2, 12С-2, 12D-2)

8-кетометилналтрексона бромид RRT 0.49
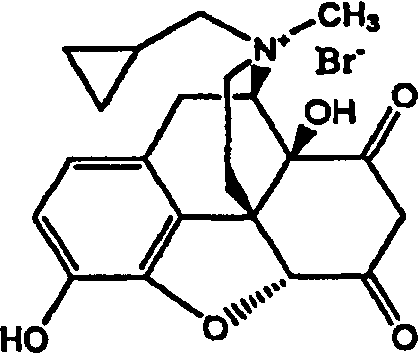
Альдольный димер RRT 1.77

O-метилметилналтрексон RRT 1.66 (3-метиоксиналтрексонметобромид)

2,2-бис-метилналтрексон RRT 1.55

[00116] Каждый из основания налтрексона, S-метилналтрексона и O-метил метилналтрексона является соединением, найденным в исходных пробах. Дополнительные примеси/продукты разложения, образовавшиеся и идентифицированные в составах на основе метилналтрексона, включают 8-кетометилналтрексона бромид (RRT 0.49), альдольный димер (RRT 1.77), O-метилметилналтрексон (RRT 1.66), и 2,2-бис-метилналтрексон (RRT 1.55), а также дополнительные продукты разложения, имеющие относительное время удерживания 0.67, 0.79 и 2.26.
[00117] Каждый из трех дополнительных продуктов разложения был идентифицированы с помощью ЯМР анализа после выделения из пропущенных через колонку элюатов и дополнительно охарактеризованы, как указано в настоящем описании. Продукт разложения 0.67 был идентифицирован как 7-дигидроксиметилналтрексон; продукт разложения 0.79 был идентифицирован как форма с суженным циклом ((3R,4R,4aS,6aR,11bS)-6-карбокси-3-(циклопропилметил)-4а,6,8-тригидрокси-3-метил-1,2,3,4,4а,5,6,6а-октагидро-4,11-метан[1]бензофуро[3',2':2,3]циклопента[1,2-с]пиридин-3-иума); и продукт разложения 2.26 был идентифицирован как продукт реакции разложения Гофмана (см. названия следующих соединений, относительные времена удерживания и соответствующие структуры; см. также, фиг.4). 7-дигидроксиметилналтрексон RRT 0.67 ХН3

Продукт реакции сужения цикла RRT 0.79 (3R,4R,4aS,6aR,11bS)-6-карбокси-3-(циклопропилметил)-4а,6,8-тригидрокси-3-метил-1,2,3,4,4а,5,6,6а-октагидро-4,11-метан[1]бензофуро[3',2':2)3]циклопента[1,2-с]пиридин-3-иум)

Продукт реакции разложения Гофмана RRT 2.26

[00118] Результаты исследования стабильности, представленные в таблицах в нижеследующих примерах, демонстрируют содержание каждого из образующихся продуктов разложения, идентифицированных в пробах с помощью анализа методом ВЭЖХ. Методики проведения исследования стабильности, применяемые в нижеследующих примерах, включают стандартные фармацевтические исследования стабильности в соответствии с руководством ICH в условиях 25°С/ 60% относительной влажности, 40°С/ 65% относительной влажности и/или при 70°С. На фиг.4 представлены три основных образующихся продукта разложения и соответствующий предложенный механизм каталитического образования и/или способов ингибирования образования, которые были идентифицированы и затем описаны в нижеследующих примерах.
[00119] Для специалиста в данной области техники очевидно, что незначительные модификации в проведении анализа методом ВЭЖХ или пробоподготовки могут приводить к сдвигу RRT. Таким образом, следует иметь в виду, что значения RRT, приведенные в настоящем описании, могут смещаться в зависимости от фактических условий.
Пример 2
Ингибирование разложения составов на основе метилналтрексона, опосредуемого металлом и кальцием.
[00120] Ингибирование образования 2.2'-бис-метилналтрексона, катализируемого металлом. Авторы настоящего изобретения обнаружили, что Fe3+ способствует протеканию разложения бромида метилналтрексона в растворе, приводящего к образованию продукта разложения в виде 2,2'-бис-метилналтрексона. С помощью ВЭЖХ анализа (способ В) авторы настоящего изобретения обнаружили, что продукт разложения в виде 2,2'-бис-метилналтрексона имеет пик с RRT примерно 1.55. Fe3+ является ионом, который может поступать в жидкий состав из нескольких источников. Например, он может выщелачиваться из технологического оборудования из нержавеющей стали, игл шприцов, пробок и флаконов из желтого стекла. EDTA, как вещество, образующее хелаты с металлами, связывает доступные ионы Fe3+ в растворе, тем самым предотвращая протекание нежелательных реакций, катализируемых металлом. Растворы метилналтрексона были приготовлены в 0.9% NaCl в присутствии железа и различных концентраций натриевой соли EDTA и кальциевой соли EDTA. Применяемый при описании всех экспериментов термин «натриевая соль EDTA» обозначает дигидрат динатриевой соли EDTA, и термины «натриевая соль EDTA», «EDTA динатрия дигидрат» и «NaEDTA» в настоящем описании являются взаимозаменяемыми. Применяемый при описании всех экспериментов термин «кальциевая соль EDTA» представляет собой кальциево-динатриевую соль EDTA, и термины «кальциевая соль EDTA», кальциево-динатриевая соль EDTA и «CaEDTA» в настоящем описании являются взаимозаменяемыми. Образование 2,2'-бис-метилналтрексона оценивали при комнатной температуре, а также при 40°С.
Добавление раствора натриевой или кальциевой соли EDTA было эффективным в отношении ингибирования образования продукта разложения в виде 2,2'-бис-метилналтрексона, см. фиг.1А и фиг.1В. Таким образом, хелатирующее действие способствует стабильности бромида метилналтрексона в растворе при комнатной температуре.
[00121] Ингибирование катализируемого металлом образования 7-дигидроксиметилналтрексона. Авторы настоящего изобретения обнаружили, что EDTA ингибирует катализируемое металлом образование продукта разложения в виде 7-дигидроксиметилналтрексона в растворе метилналтрексона. С помощью ВЭЖХ анализа (способ В) авторы настоящего изобретения обнаружили, что продукт разложения с пиком при 0.67 свидетельствует о присутствии 7-дигидроксиметилналтрексона. Готовили растворы метилналтрексона в 0.9% NaCl в присутствии железа и различных концентраций EDTA и оценивали образование 7-дигидроксиметилналтрексона. Добавление любого раствора EDTA было эффективным в отношении ингибирования образования продукта разложения в виде 7-дигидроксиметилналтрексона, см. таблицу 1.
ТАБЛИЦА 1. Площадь пика продукта разложения метилналтрексона (MNTX) с относительным временем удерживания (RRT), равным 0.67, при концентрации MNTX 20 мг/мл при комнатной температуре в присутствии 1 мМ Fe+3
[00122] Авторы настоящего изобретения обнаружили, что вещество, образующее хелаты с Са (Са-хелатирующий агент), обеспечивает дополнительное ингибирование образования продукта разложения в виде 7-дигидроксиметилналтрексона по сравнению с Na+-хелатирующим агентом. Готовили растворы метилналтрексона в 0.9% NaCl в присутствии железа и различных концентраций натриевой соли EDTA и кальциевой соли EDTA. Образование 7-дигидроксиметилналтрексона оценивали при комнатной температуре, а также при 40°С. Добавление раствора кальциевой соли EDTA было высокоэффективным в отношении ингибирования образования продукта разложения в виде 7-дигидроксиметилналтрексона при обеих температурах. См. фиг.2А и фиг.2В. Применение кальция способствует повышению стабильности бромида метилналтрексона в растворе при комнатной температуре. Более того, при длительном хранении раствора при комнатной температуре или при 40°С/ 75% относительной влажности также наблюдали повышение стабильности и ингибирование образования продукта разложения в виде 7-дигидроксиметилналтрексона в присутствии кальциевой соли EDTA. После хранения в течение одного месяца при комнатной температуре суммарное образование 7-дигидроксиметилналтрексона уменьшилось с 0.34% до 0.11% в присутствии кальциевой соли EDTA. Более того, при 40°С/ 75% относительной влажности содержание продукта разложения уменьшилось с 0.64% в чистом солевом растворе до 0.14% в пробе, содержащей кальциевую соль EDTA. См. фиг.2С и фиг.2D.
[00123] Получение состава на основе метилналтрексона, обладающего улучшенными характеристиками при хранении при комнатной температуре. Результаты исследований, проведенных авторами настоящего изобретения показали, что состав на основе метилналтрексона, содержащий солевой раствор активного соединения и кальциевую соль хелатирующего агента, обладает улучшенными характеристиками стабильности при комнатной температуре. Получение таких улучшенных составов включает применение следующих типичных компонентов:
Изотонический носитель 0.9% нормальный физиологический раствор (от 1 до 1.25 мл)
[00124] Для получения объема 0.6 мл или 1.25 мл 20 или 30 мг бромида метилналтрексона растворяли в 0.9% хлориде натрия; и 0.24 мг или 0.5 мг кальциевой соли EDTA также растворяли в этом растворе. Приготавливали конечные растворы и стерилизовали посредством фильтрации в условиях окружающей среды, затем полученными составами заполняли чистые стеклянные флаконы, ампулы, шприцы или автодозаторы.
Пример 3
Ингибирование рН-зависимого разложения составов на основе метилналтрексона
[00125] Ингибирование рН-зависимого образования продуктов разложения метилналтрексона. Авторы настоящего изобретения обнаружили, что в присутствии Са2+ и EDTA при определенных показателях стабильности происходит разложение бромида метилналтрексона в растворе, что приводит к образованию третьего продукта разложения метилналтрексона. С помощью ВЭЖХ анализа (способ В) авторы изобретения обнаружили, что продукт разложения характеризуется пиком с RRT примерно 0.79. Идентификация и получение продукта разложения 0.79 описаны в предварительной заявке на патент США 60/835687, поданной 4 августа 2006 года одновременно с настоящей заявкой, содержание которой включено в настоящее описание во всей полноте посредством ссылки.
[00126] Образование продукта разложения метилналтрексона 0.79 при комнатной температуре в составе, содержащем CaEDTA, описанном выше в примере 2, уменьшалось по сравнению с охлажденным раствором метилналтрексона в солевом растворе. Раствор метилналтрексона, описанный в примере 2, содержащий CaEDTA, сравнивали с контрольным охлажденным солевым раствором метилналтрексона и оценивали составы с точки зрения образования продукта разложения 0.79 (комнатная температура, 0.03% CaEDTA относительно охлажденного контрольного солевого 0.06% раствора). См. фиг.3А и фиг.3В. Применение кальциевой соли EDTA, по-видимому, способствует образованию продукта разложения 0.79 в достигнутых условиях улучшенной стабильности, однако, как было найдено, при 40°С/ 75% ОВ (относительной влажности) содержание продукта разложения 0.79 возрастает относительно контрольной пробы с 0.19% до 0.38% в присутствии CaEDTA. Более того, содержание продукта разложения с пиком RRT при 0.79 увеличивается с 0.03% при комнатной температуре до 0.4% при 40°С/ 75% ОВ после хранения в течение 1 месяца. Таким образом, в то время как в составе, описанном выше в примере 2, можно контролировать образование продуктов разложения с RRT 0.67 и RRT 1.55, продукт разложения с RRT 0.79 сохраняется в условиях улучшенной стабильности при 40°С/75% RH.
[00127] Авторы настоящего изобретения обнаружили, что уменьшение рН, а также присутствие глицина приводило к повышению стабильности продукта разложения 0.79. В таблице 4 приведены обобщенные данные по стабильности составов в отсутствие рН-контроля при 70°С. рН состава равен 5.6. Эти данные подтверждают, что состав, содержащий Ca-EDTA, действительно ограничивает образование продуктов разложения RRT 0.67 и 1.55, но не уменьшат образование продукта разложения RRT 0.79. Только за несколько дней содержание продукта разложения RRT 0.79 увеличилось до более чем 1.0%. В таблице представлен каждый из пиков ВЭЖХ. Для продуктов, идентифицированных по пикам, RRT 0.89 представляет собой S-MNTX; RRT 1.17 представляет собой основание налтрексона; RRT 1.55 представляет собой 2,2-бис-метилналтрексон; RRT 1.66 представляет собой O-метилметилналтрексон; RRT 1.77 представляет собой альдольную димерную структуру; и RRT 2.26 представляет собой продукт разложения, образовавшийся в результате реакции разложения Гофмана. BRL=ниже предела обнаружения.
[00128] Авторы настоящего изобретения исследовали зависимость образования продукта разложения 0.79 от рН и оптимальный диапазон рН раствора. В таблице 5 приведены обобщенные данные о стабильности приготовленных растворов. Дополнительно в таблице 6 приведены обобщенные данные о стабильности приготовленных растворов при 40°С/ 75% относительной влажности и при 70°С при регулировании рН с помощью глицина и без него. Авторы изобретения обнаружили, что при добавлении к раствору дополнительного количества глицин-HCl, количество образующегося продукта разложения с RRT 0.79 значительно уменьшается, и подтвердили, что стабильность состава с точки зрения образования RRT 0.79 остается неизменной благодаря присутствию глицина. См. таблицы 5 и 6.
Приготовление состава с заданным рН и улучшенными характеристиками при хранения при комнатной температуре. Ниже, в таблице 7 и таблице 8, представлены разработанные составы, содержащие глицин-HCl, при этом получение указанных составов включает стадию регулирования рН, причем диапазон изменения рН в ходе процесса получения составляет 3.4-3.6, а заданное значение рН составляет 3.5. Не желая быть связанными какой-либо теорией, при разработке рецептуры составов авторы изобретения руководствовались соображениями, что хотя рН 3.0 обеспечивает требуемую стабильность, раздражение и острая боль в месте инъекции являются нежелательными. Более того, при рН 4.0 начинается образование продукта разложения RRT 0.79. Глицин-HCl обычно применяют в составах для подкожного введения для регулирования рН, и он проявляет меньшую склонность вызывать жжение в месте инъекции в результате использования цитратного буфера. Когда глицин-НСl применяют для установления рН состава, содержащего метилналтрексон, контролирование разложения также является очевидным. Раствор, содержащий метилналтрексон, а также CaEDTA и 0.3 мг/мл глицин-HCl, в котором рН устанавливают равным 3.4-3.6, обеспечивает ингибирование образования RRT 1.55 и значительное уменьшение образования продуктов разложения RRT 0.67 и RRT 0.79. Жидкий состав, подходящий для хранения при комнатной температуре, содержащий метилналтрексон, CaEDTA, 0.65% NaCl и 0.3 мг/мл глицин-HCl, с рН 3.5 может представлять собой состав для подкожного введения или внутривенного введения.
[00129] Приготовление указанных составов с улучшенными характеристиками включает применение следующих типичных компонентов:
рН 3.4-3.6
Достаточное количество растворителя (QS) до конечного объема
А3 мл флакон West из флинтгласа с 13 мм пробкой West 4432/50 Fluorotec и West 13 FO CS ТЕ 3769 Blue Cap.
[00130] Например, для приготовления раствора с концентрацией 12 мг/флакон, 12 мг бромида метилналтрексона и 3.9 мг хлорида натрия растворяли в воде для инъекций; затем добавляли 0.24 мг кальциевой соли EDTA и доводили объем раствора до конечного объема 0.6 мл. рН устанавливали с помощью глицин-НСl в интервале 3.4-3.6, оптимально - 3.5. Готовили конечный раствор и фильтровали через 0.45 и 0.22 микронные поливинилиденфторидные фильтры. Полученным раствором наполняли чистые стеклянные флаконы в условиях низкого содержания кислорода. Можно применять любые подходящие контейнеры, в том числе флаконы, ампулы, шприцы или автодозаторы. Полученные препараты хранили при комнатной температуре или ниже, не замораживая. Полученный состав можно применять для парентерального введения, для подкожного введения или для внутривенного введения. См. таблицу 7.
[00131] Аналогичным образом, содержание ингредиентов можно адаптировать к конечному объему 0.8 (или любому другому предпочтительному конечному объему) и получить те же самые концентрации. См. Таблицу 7.
A3 мл флакон West из флинтгласа с 13 мм пробкой West 4432/50 Fluorotec и West 13FOCS ТЕ 3769 Blue Cap.
[00132] В случае альтернативного типичного состава для получения концентрации 12 мг/флакон 12 мг бромида метилналтрексона и 3.9 мг хлорида натрия растворяли в воде для инъекций; затем добавляли 0.24 мг кальциевой соли EDTA и доводили объем раствора до конечного объема 1.2 мл. рН устанавливали с помощью глицин-НСl в интервале 3.4-3.6, оптимально - рН 3.5. Приготавливали конечный раствор и фильтровали через 0.45 и 0.22 микронные поливинилиденфторидные фильтры. Полученным раствором наполняли чистые стеклянные флаконы в условиях низкого содержания кислорода. Можно применять любые подходящие контейнеры, в том числе флаконы, ампулы, шприцы или автодозаторы. Полученные препараты хранили при комнатной температуре или ниже, не замораживая. Полученный состав можно применять для парентерального введения, для подкожного введения или для внутривенного введения. См. Таблицу 8.
[00133] Аналогичным образом, содержание ингредиентов можно адаптировать к конечному объему 1.6 (или любому другому предпочтительному конечному объему) и получить те же самые концентрации. См. таблицу 8.
Пример 4
Сравнение и оценка буферной совместимости
[00134] Оценка стабильности растворов фосфатных буферов. Авторы настоящего изобретения также оценивали различные буферы, чтобы определить совместимость и установить влияние различных условий на возможность обеспечения дополнительной стабильности растворам метилналтрексона. В таблице 9 и таблице 10 (ВЭЖХ, способ А) показаны результаты образования всех продуктов разложения в течение длительного периода времени в растворах метилналтрексона, приготовленных в фосфатном растворе (таблица 9) и растворе глицина (Таблица 10). Авторы изобретения обнаружили, что при рН 7 глицин обеспечивает лучшие характеристики стабильности проб, чем фосфат.
*Фосфатный буфер: КН2РO4 и Na2НРО4
*Глициновый буфер: глицин и NaOH
[00135] Приготовление состава на основе метилналтрексона, содержащего натриевую соль EDTA и цитратный буфер. Составы на основе метилналтрексона, содержащие метилналтрексон, натриевую соль EDTA и хлорид натрия в цитратном буфере, известны и описаны (см. публикацию заявки на патент США US2004/0266806A1, опубликованную 30 декабря 2004 г.). Авторы настоящего изобретения приготовили растворы, содержащие те же компоненты, с целью сравнительного исследования их стабильности относительно составов согласно настоящему изобретению.
[00136] Были приготовлены составы, содержащие 20 мг/мл бромида метилналтрексона в а) 0.7 мг/мл NaEDTA с рН 3.5, установленном с помощью цитратного буфера; и б) 0.4 мг/мл CaEDTA / 0.65% NaCl с рН 3.5, установленном с помощью глицинового буфера. Все составы оценивали в течение длительного периода времени с точки зрения образования продуктов разложения; результаты представлены в таблице 11.
[00137] Составы, содержащие 5 мг/мл бромида метилналтрексона (12 мг/флакон или 24 мг/флакон) были приготовлены, как описано ниже в примере 12. Все составы оценивали в течение длительного периода времени с точки зрения образования продуктов разложения; результаты представлены в таблице 12.
[00138] В агрессивных условиях, в растворах, содержащих натриевую соль EDTA, даже при высоком содержании натриевой соли EDTA происходит увеличение содержания продуктов разложения 0.67 и 0.79. Полагают, что составы и способы, предлагаемые в настоящем изобретении для приготовления растворов метилналтрексона, обеспечивают сохранение стабильности композиции и приемлемые содержания продуктов разложения в течение длительного времени.
ТАБЛИЦА 11. Сравнение стабильности состава на основе метилналтрексона концентрацией 20 мг/мл


ТАБЛИЦА 12. Сравнительное исследование стабильности состава на основе метилналтрексона с концентрацией 5 мг/мл (12 мг/флакон или 24 мг/флакон)
Прямой
Прямой
Прямой
Пример 5
[00139] Стабильность состава для внутривенного введения, содержащего 5.0 мг/мл вещества (12 мг/флакон или 24 мг/флакон) исследовали для определения влияния воздействия света. Составы оценивали на протяжении длительного периода времени с точки зрения присутствия продуктов разложения (ВЭЖХ, способ А). Результаты исследования на устойчивость к свету представлены в таблицах 13А и 13 В.
7-дигидрокси MNTX mz 388
Суженный цикл
7-дигидрокси MNTX mz 388
Суженный цикл
Пример 6. Оценка совместимости пробок
[00140] Авторы настоящего изобретения оценивали различные имеющиеся пробки, применяемые для закрывания флаконов, с точки зрения их совместимости с растворами метилналтрексона и определяли их влияние на образование продуктов разложения в растворе.
[00141] Идентичные препараты, приготовленные, как описано в примере 4, хранили одновременно во флаконах с пробкой диаметром 13 мм WPS S2-F451 4432/50 Gray B2-40 Westar RS (West Pharmaceutical Services) или пробкой диаметром 13 мм S2-F451 RS D 777-1 RB2-40 (Daikyo Seiko, Ltd) при различных условиях. Каждая из пробок имела фторуглеродную пленку FluoroTec®; пробка Westar 4432/50 сделана из хлорбутиловой резины, тогда как пробка RB2-40 RS D 777-1 сделана из бромбутиловой резины. В каждом случае оценивали накопление продукта разложения (ВЭЖХ, способ А). В таблице 14 представлены результаты этих исследований. В условиях хранения пробка, содержащая бромбутиловую резину, по-видимому, аккумулирует состав с альдольным димером с более высокой скоростью, чем сравниваемая хлорбутиловая пробка.
Пример 7
Стабильность замороженных пакетов с составами для внутривенного введения
[00142] Следующий состав, содержащий метилналтрексона 5 мг/мл, 0.8 мг NaCL, 0.1 мг CaEDTA, 0.1 мг гидрохлорида глицина и воду для инъекций, вливали в 100 мл пакеты для препаратов для внутривенных инъекций, содержащие 0.9% нормальный солевой раствор, и замораживали при -200 ОС. Исследование проводили для двух концентраций метилналтрексона: 12 мг/100 мл и 24 мг/100 мл. Применяли пакеты B/Braun NDC 0264-1800-32 с 0.9% нормальным солевым раствором.
[00143] Приготавливали две партии состава и определяли их стабильность. Первая партия представляла собой вышеупомянутый состав на основе метилналтрексона для внутривенного введения: 5 мг/мл метилналтрексона, 0.8 мг NaCl, 0.1 мг CaEDTA, 0.1 мг гидрохлорида глицина, помещенный в пакет для внутривенного введения с 0.9% нормальным солевым раствором. Вторая партия представляла собой раствор, содержащий лишь 5 мг/мл метилналтрексона, помещенный в пакет для внутривенного введения с 0.9% нормальным солевым раствором. Пакеты замораживали и хранили при -20°С. Данные по стабильности показывали, что на протяжении 2 месяцев продукт в обоих пакетах сохранял стабильность и не происходило образования продуктов разложения. Дополнительным преимуществом хранения в замороженном виде в пакетах является отсутствие необходимости защиты от света.
[00144] Исследование стабильности в течение двух месяцев (ВЭЖХ, способ А) показало отсутствие разложения, продемонстрировав тем самым, что состав является стабильным в условиях заморозки, а также что продолжительность применения и срок годности состава могут быть больше 6 месяцев; кроме того, в этом случае отсутствует необходимость заполнения пакетов для внутривенного введения лекарственным препаратом больничным персоналом. Пакеты поступают к потребителю уже в готовом виде, их необходимо только разморозить. В таблице 15 приведены обобщенные результаты вышеуказанных исследований.
24 мг/100 мл пакет с 0.9% нормальным солевым раствором
Пример 8
[00145] Обобщенные данные по влиянию вольфрамата натрия (ВЭЖХ, способ А) на состав для подкожного введения, предложенный в настоящем изобретении, приведены ниже в таблице 16.
ЧАСТЬ II: Составы для подкожного введения
Пример 9
[00146] Раствор для подкожной инъекции, содержащий 20 мг/мл состава на основе метилналтрексона при комнатной температуре и CaEDTA, содержал 20 мг/мл бромида метилналтрексона, 0.4 мг/мл кальций-динатрий эдетата (CaEDTA), 0.3 мг/мл гидрохлорида глицина и 0.65% хлорида натрия в воде для инъекций. Этот продукт, который является стабильным при хранении при комнатной температуре, асептически помещали во флаконы для однократного применения объемом 0.6 мл, или 12 мг метилналтрексона на флакон, с целью подкожного введения.
[00147] Содержание хлорида натрия устанавливают равным 0.65% для обеспечения заданной тоничности состава.
[00148] Указанный состав, подходящий для хранения комнатной температуре, для подкожного введения, был приготовлен, как указано ниже в таблицах 17А, 17 В и 17С:

[00149] Согласно некоторым вариантам реализации изобретения, вышеуказанный состав для подкожного введения можно дозировать согласно следующей таблице. Субъектам, чей вес не попадает в указанные диапазонов, препарат может быть введен в количестве 0.15 мг/кг.
[00150] Согласно другим вариантам реализации изобретения, для субъектов с тяжелой почечной недостаточностью (клиренс креатинина менее 30 мл/мин) доза вышеуказанного состава для подкожного введения может быть сокращена наполовину.
Пример 10
[00151] Как указано в настоящем описании, в изобретении предложен предварительно заполненный шприц, содержащий состав на основе метилналтрексона согласно настоящему изобретению. Такой предварительно заполненный шприц описан ниже в таблице 18.
Таблица 18. Предварительно заполненный шприц
Пример 11. Состав для подкожного введения - изучение биоэквивалентности
[00152] Исследование биоэквивалентности для сравнения состава для подкожного введения, описанного в примере 9, и состава, содержащего только метилналтрексон в солевом растворе, было выполнено без контроля плацебо, с применением однократных доз при рандомизированном, с 2 периодами, перекрестном с 2 последовательностями, стационарном/амбулаторном исследовании здоровых субъектов, которое проводилось в одном исследовательском центре. Дозы вводили после воздержания от еды в течение ночи в течение по меньшей мере 10 часов. В исследованиях участвовали здоровые мужчины и не кормящие и небеременные женщины в возрасте от 18 до 50 лет, если они удовлетворяли всем другим квалификационным критериям. Приблизительно в 800 в день 1 периодов 1 и 2 каждому субъекту делали подкожную инъекцию, содержащую 0.15 мг/кг метилналтрексона (период 1, день 1, для определения вводимой дозы учитывали вес). Стандартную пищу средней жирности, подаваемую согласно расписанию в данной клинике, можно было съесть через 3 часа после введения тестируемого продукта. Основные показатели состояния организма, ЭКГ, лабораторные анализы и отбор фармакокинетической (ФК) пробы осуществляли в назначенное время в 1, 2, и 3 дни периода 1 и 2 согласно графику исследований.
[00153] Каждому субъекту делали однократную подкожную инъекцию, содержащую дозу в 0.15 мг/кг назначенного состава метилналтрексона в день 1 каждого периода после воздержание от еды в течение ночи по меньшей мере в течение 10 часов. Инъекцию делали подкожно в верхнюю часть руки, и каждую инъекцию делали в одну и ту же руку. Место инъекции должно было выглядеть здоровым участком кожи. Желательно, чтобы один и тот же человек вводил оба состава каждому субъекту. Дозу определяли в зависимости от веса субъекта в день 1 периода 1. Шприцы взвешивали до и после введения тестируемого продукта с целью контроля вводимого объема.
Каждая однократная доза отделялась интервалом выведения в по меньшей мере 7 дней. Пробы крови отбирали для определения фармакокинетики метилналтрексона. Пробы крови (6 мл) отбирали из постоянного катетера или путем прямой венепункции. Если для отбора крови применяли катетер, то каждый раз перед отбором пробы следовало отбросить приблизительно 0.5 мл крови. Пробы крови собирали в течение каждого периода в день 1 в пределах 2 часов до введения тестируемого продукта и через 0.083, 0.25, 0.5, 0.75, 1, 1.5, 2, 3, 4, 6, 8, 12, 16, 24, 36 и 48 часов после введения тестируемого продукта. Результаты фармакокинетического исследования представлены ниже в таблице 19.
[00154] Как показано выше в таблице 19, профиль средней концентрация метилналтрексона в зависимости от времени после подкожного введения состава, описанного в примере 9, был по существу идентичен профилю, наблюдаемому при введении солевого состава. Концентрации метилналтрексона в плазме резко возрастали в ответ на подкожное введение и того и другого состава, при этом Смакс составляла 127 нг/мл для состава согласно изобретению и 119 нг/мл для солевого состава, что наблюдалось в основном в течение первого часа (среднее t макс составляло 0.34 ч и 0.41 ч соответственно).
Пример 12
Фармакокинетические исследования составов для подкожного введения на основе метилналтрексона на собаках
[00155] Оценивали три различных состава на основе метилналтрексона, которые вводили подкожно собакам. Исследовали фармакокинетику метилналтрексона после введения однократной дозы в 0.15 мг/кг подкожно гончим собакам мужского пола. Восемь собак мужского пола (9.4-15 кг) разделили на две группы, по четыре собаки на группу. Собакам обеих групп подкожно вводили 0.15 мг/кг метилналтрексона в нормальном солевом растворе (партия 1) в качестве эталонного состава в течение периода 1. Неделей позже, во время периода 2, группе 1 (SAN 1-4) подкожно вводили 0.15 мг/кг метилналтрексона в солевом растворе, содержащем 0.5 мг/флакон Na EDTA и 0.6 мМ цитрата (партия 2), и группе 2 (SAN 5-8) подкожно вводили 0.15 мг/кг метилналтрексона в солевом растворе, содержащем 0.5 мг/флакон Са EDTA (партия 3). Пробы крови отбирали через 0 (до дозирования), 0.0833, 0.167, 0.25, 0.5, 0.75, 1, 2, 4, 6, 8 и 12 часов после дозирования, плазму отделяли и оценивали с точки зрения содержания метилналтрексона.
[00156] На основании полученных биоаналитических результатов осуществляли оценку фармакокинетики (ФК). Профили зависимости концентрации метилналтрексона в плазме конкретной собаки от времени подвергали некомпартментному ФК-анализу (WinNonlin, Model 200). Для каждой собаки определяли нижеследующие фармакокинетические параметры, и рассчитывали требуемые статистические показатели с целью сравнения составов: AUC, Смакc, t макс и t1/2. См. таблицу 20.
ЧАСТЬ III.
Составы для внутривенного введения Пример 13
[00157] Согласно некоторым вариантам реализации, в настоящем изобретении предложен состав на основе метилналтрексона для внутривенного введения. Предложенные составы для внутривенного введения можно приготовить с концентрацией 12 мг/флакон или 24 мг/флакон. При обеих концентрациях, 12 мг/флакон и 24 мг/флакон, применяют 5 мг/мл метилналтрексона. Согласно некоторым вариантам реализации изобретения, предложенные составы для внутривенного введения помещают в 10 мл прокалываемый флакон, сконструированный с возможностью совместного применения с мини-пакетами Baxter или любыми другими прокалываемыми инфузионными системами. Согласно некоторым вариантам реализации изобретения предложенные составы подвергают заключительной стерилизации путем нагревания при 121°С в течение 15 минут.
[00158] Составы, приготовленные с концентрациями 12 мг/флакон или 24 мг/флакон, представлены ниже в таблицах 20А и 20В, соответственно. Указанные составы можно вводить при дозах 24 мг, или, например, 0.3 мг/кг каждые 6 часов в виде 20-минутных вливаний. Согласно некоторым вариантам реализации изобретения, такое введение продолжается в течение 3 дней (всего 12 доз). Каждый состав на основе метилналтрексона разбавляют до 50 мл и вводят с помощью калиброванного насоса.
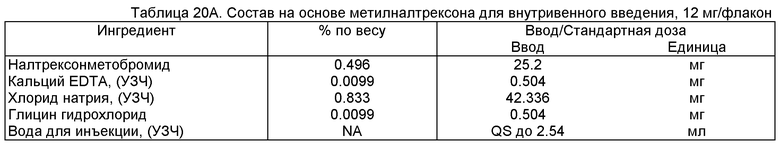
[00159] Согласно некоторым вариантам реализации изобретения заполняемый объем составляет по меньшей мере 2.6 мл для 2.4 мл извлекаемого объема, и по меньшей мере 5.1 мл для 4.8 мл извлекаемого объема. Ниже в таблице 20С приведено разбавление содержания флаконов при применении традиционного шприца или прокалываемого флакона.
Пример 14
[00160] Согласно некоторым вариантам реализации изобретения предложенный состав для внутривенного введения вводят субъекту через 90 минут после операции, когда операция представляет собой удаление грыжи. Согласно некоторым вариантам реализации изобретения субъектам после удаления грыжи вводят опиоиды с помощью насоса, контролируемого субъектом. Указанные составы можно ввести при дозе 12 мг или 24 мг, или, например, 0.3 мг/кг каждые 6 часов в виде 20-минутных вливаний. Согласно некоторым вариантам реализации изобретения, такое введение продолжается в течение 10 дней, после чего субъекта выписывают, или через 24 часа после опорожнения кишечника.
[00161] Для специалиста в данной области техники не вызовет затруднений определение существенных признаков настоящего изобретения, при этом для специалиста в данной области техники очевидно, что вышеприведенное описание и примеры иллюстрируют варианты реализации предложенного изобретения. Для специалиста в данной области техники очевидно, что путем проведения обычных экспериментов может быть установлено множество возможных частных вариантов реализации настоящего изобретения, при этом каждый из таких вариантов также находится в рамках настоящего изобретения.
[00162] В настоящей заявке приведены ссылки на патенты, заявки на патенты, публикации и др., при этом описание каждого из этих документов включено в настоящую заявку во всей полноте посредством ссылки.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ ПРЕПАРАТИВНАЯ ФОРМА | 2004 |
|
RU2362560C2 |
| СОСТАВЫ НА ОСНОВЕ ТИГЕЦИКЛИНА И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2006 |
|
RU2428190C2 |
| СТАБИЛЬНАЯ ПРИ ОКИСЛЕНИИ, ПРОЧНАЯ НА ИЗЛОМ ЛЕКАРСТВЕННАЯ ФОРМА | 2010 |
|
RU2567723C2 |
| КОНЦЕНТРАТ ЛЕЧЕБНОГО РАСТВОРА | 2011 |
|
RU2576026C2 |
| СОСТАВ ДЛЯ ОПТИЧЕСКОЙ ВИЗУАЛИЗАЦИИ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ | 2019 |
|
RU2802481C2 |
| КОМПОЗИЦИИ ЖИДКОЙ ПЕРОРАЛЬНОЙ ЛЕКАРСТВЕННОЙ ФОРМЫ МЕТИЛНАЛТРЕКСОНА | 2020 |
|
RU2827066C2 |
| ПРИМЕНЕНИЕ МЕТИЛНАЛТРЕКСОНА ДЛЯ ЛЕЧЕНИЯ СИНДРОМА РАЗДРАЖЕННОГО КИШЕЧНИКА | 2004 |
|
RU2373936C2 |
| НОВАЯ КОМПОЗИЦИЯ ЗАМЕДЛЕННОГО ВЫСВОБОЖДЕНИЯ ТОФАЦИТИНИБА, ЕГО ПРОИЗВОДНЫХ И СОЛЕЙ | 2021 |
|
RU2839277C1 |
| ВОДНЫЙ СОСТАВ, СОДЕРЖАЩИЙ 1-(4-{ [4-(ДИМЕТИЛАМИНО)ПИПЕРИДИН-1-ИЛ]КАРБОНИЛ} ФЕНИЛ)-3-[4-(4,6-ДИМОРФОЛИН-4-ИЛ-1,3,5-ТРИАЗИН-2-ИЛ)ФЕНИЛ]МОЧЕВИНУ | 2019 |
|
RU2772287C1 |
| НОВЫЕ И ЭФФЕКТИВНЫЕ ЛЕКАРСТВЕНЫЕ ФОРМЫ ТАПЕНТАДОЛА | 2009 |
|
RU2599846C2 |
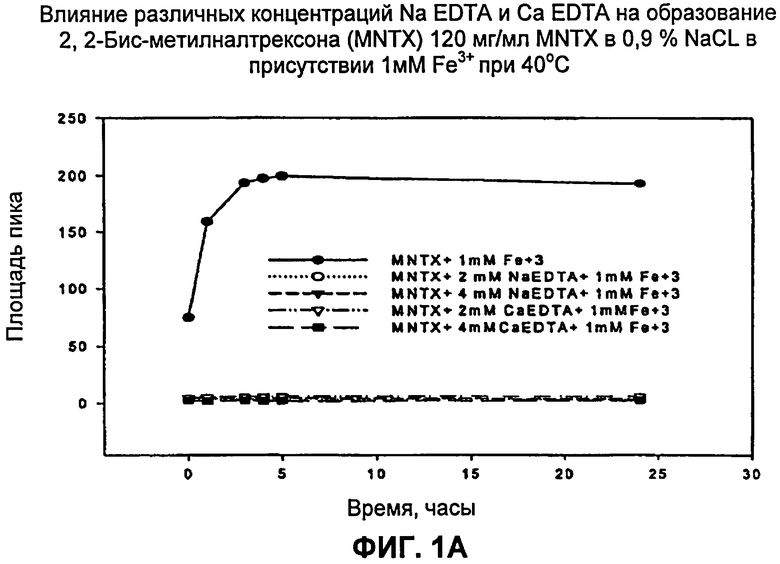
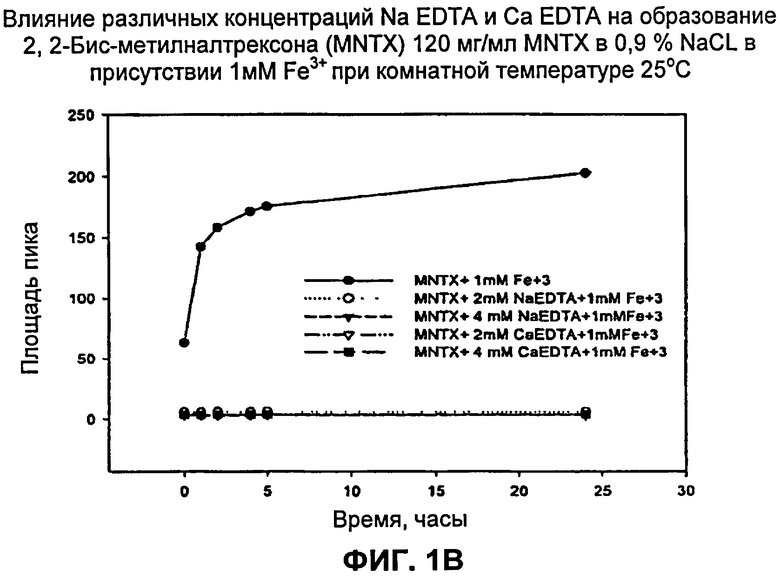
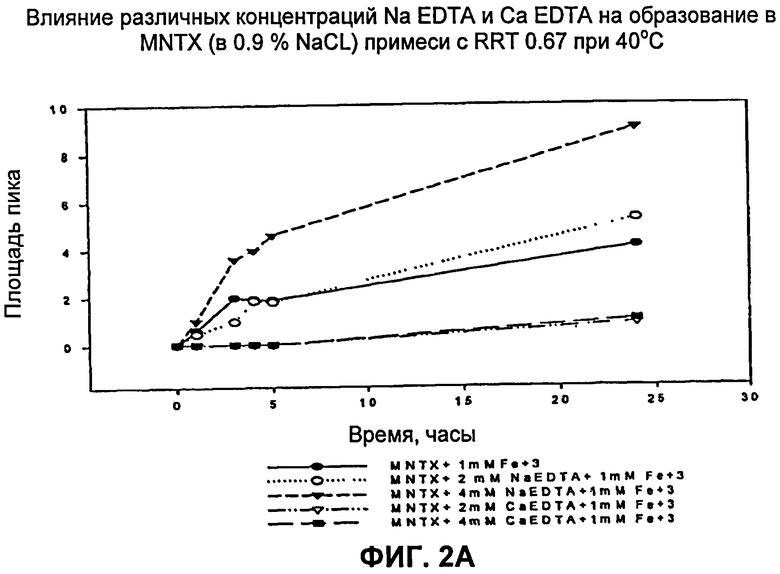

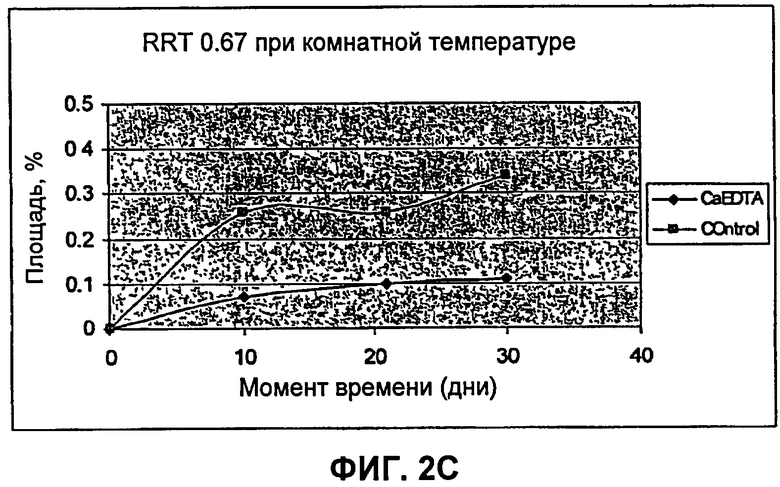
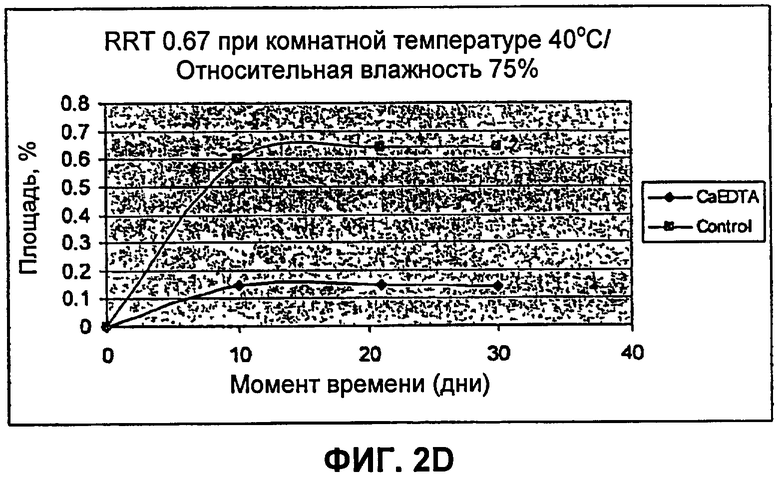



В настоящем изобретении предложены составы, обеспечивающие эффективную доставку композиций на основе метилналтрексона. Фармацевтическая композиция по изобретению содержит эффективное количество метилналтрексона, кальцийэтилендиаминтетрауксусную кислоту (ЭДТА) или кальциево-динатриевую соль ЭДТА и гидрохлорида глицин в водном растворе. Указанный раствор имеет рН от примерно 3 до примерно 4. Также описан способ получения состава метилналтрексона. Предложенные составы подходят для предотвращения, лечения, замедления, ослабления или снижения степени тяжести побочных эффектов, возникающих в результате применения болеутоляющих опиоидов. Композиция характеризуется высокой стабильностью при длительном хранении в жестких условиях. 2 н. и 28 з.п. ф-лы, 4 ил., 20 табл., 14 пр.
1. Фармацевтическая композиция, содержащая эффективное количество метилналтрексона или его фармацевтически приемлемой соли, кальций этилендиаминтетрауксусную кислоту (ЭДТА) или кальциевую соль производного ЭДТА и гидрохлорида глицин в водном растворе, причем pH указанного раствора составляет от примерно 3 до примерно 4.
2. Фармацевтическая композиция по п.1, отличающаяся тем, что указанная соль метилналтрексона содержит бромид метилналтрексона.
3. Фармацевтическая композиция по п.1 или 2, отличающаяся тем, что указанная композиция содержит от примерно 5 мг до примерно 40 мг метилналтрексона или его фармацевтически приемлемой соли.
4. Фармацевтическая композиция по п.1 или 2, отличающаяся тем, что указанная композиция содержит от примерно 8 мг до примерно 12 мг метилналтрексона или его фармацевтически приемлемой соли.
5. Фармацевтическая композиция по любому из пп.1 или 2, отличающаяся тем, что кальциевая соль производного ЭДТА включает кальциево-динатриевую соль ЭДТА.
6. Фармацевтическая композиция по любому из пп.1 или 2, отличающаяся тем, что указанная композиция содержит от примерно 0,2 до примерно 0,8 мг/мл кальцийэтилендиаминтетрауксусной кислоты (ЭДТА) или кальциевой соли производного ЭДТА.
7. Фармацевтическая композиция по любому из пп.1 или 2, отличающаяся тем, что указанная композиция содержит примерно 0,4 мг/мл кальцийэтилендиаминтетрауксусной кислоты (ЭДТА) или кальциевой соли производного ЭДТА.
8. Фармацевтическая композиция по любому из пп.1 или 2, отличающаяся тем, что указанная композиция содержит примерно 0,3 мг/мл глицина.
9. Фармацевтическая композиция по любому из пп.1 или 2, отличающаяся тем, что pH указанного раствора составляет от примерно 3,4 до примерно 3,6.
10. Фармацевтическая композиция по любому из пп.1 или 2, отличающаяся тем, что pH указанного раствора составляет примерно 3,5.
11. Фармацевтическая композиция по любому из пп.1 или 2, отличающаяся тем, что фармацевтическая композиция дополнительно содержит хлорид натрия.
12. Фармацевтическая композиция по любому из пп.1 или 2, отличающаяся тем, что фармацевтическая композиция представляет собой стандартную дозу, содержащуюся во флаконе, ампуле или шприце, для подкожного введения субъекту.
13. Фармацевтическая композиция по любому из пп.1 или 2, отличающаяся тем, что концентрация продуктов разложения в указанной композиции после шести месяцев хранения при комнатной температуре характеризуется одним или несколькими из следующих признаков:
a. общее содержание продуктов разложения не превышает примерно 1,25% от содержания метилналтрексона или его фармацевтически приемлемой соли;
b. концентрация продукта разложения, представляющего собой 2,2′-бис-метилналтрексон (RRT 1.55), не превышает примерно 0,2% от содержания метилналтрексона или его фармацевтически приемлемой соли;
c. концентрация продукта разложения, представляющего собой 7-дигидроксиметилналтрексон (RRT 0.67), не превышает примерно 0,2% от содержания метилналтрексона или его фармацевтически приемлемой соли;
d. концентрация продукта разложения метилналтрексона с меньшим количеством атомов в кольце (RRT 0.79) не превышает примерно 0,2% от содержания метилналтрексона или его фармацевтически приемлемой соли;
e. концентрация продукта разложения метилналтрексона, представляющего собой альдольный димер (RRT 1.77), не превышает примерно 0,2% от содержания метилналтрексона или его фармацевтически приемлемой соли;
f. концентрация продукта разложения метилналтрексона, образующегося в результате протекания реакции разложения Гофмана (RRT 2.26), не превышает примерно 0,2% от содержания метилналтрексона или его фармацевтически приемлемой соли;
g. концентрация О-метилметилналтрексона (RRT 1.66) не превышает примерно 0,25% от содержания метилналтрексона или его фармацевтически приемлемой соли.
14. Фармацевтическая композиция по п.13, характеризующаяся каждым из признаков (a)-(g).
15. Способ получения состава метилналтрексона для парентерального введения, включающий следующие стадии:
- смешивание кальций-ЭДТА или соли его производного и гидрохлорида глицина с раствором метилналтрексона или его фармацевтически приемлемой соли;
- доведение pH указанного раствора до значения от примерно 3,0 до примерно 4,0; и
- стерилизация полученного раствора.
16. Способ по п.15, отличающийся тем, что указанная соль метилналтрексона включает бромид метилналтрексона.
17. Способ по п.15 или 16, отличающийся тем, что указанный состав метилналтрексона содержит от примерно 5 мг до примерно 40 мг метилналтрексона или его фармацевтически приемлемой соли.
18. Способ по п.15 или 16, отличающийся тем, что указанный состав метилналтрексона содержит от примерно 8 мг до примерно 12 мг метилналтрексона или его фармацевтически приемлемой соли.
19. Способ по любому из пп.15 или 16, отличающийся тем, что кальциевая соль производного ЭДТА включает кальциево-динатриевую соль ЭДТА.
20. Способ по любому из пп.15 или 16, отличающийся тем, что указанный состав содержит от примерно 0,2 до примерно 0,8 мг/мл кальцийэтилендиаминтетрауксусной кислоты (ЭДТА) или кальциевой соли производного ЭДТА.
21. Способ по любому из пп.15 или 16, отличающийся тем, что указанный состав содержит примерно 0,4 мг/мл кальцийэтилендиаминтетрауксусной кислоты (ЭДТА) или кальциевой соли производного ЭДТА.
22. Способ по любому из пп.15 или 16, отличающийся тем, указанный состав содержит примерно 0,3 мг/мл глицина.
23. Способ по любому из пп.15 или 16, отличающийся тем, что pH доводят до значения от примерно 3,4 до примерно 3,6.
24. Способ по любому из пп.15 или 16, отличающийся тем, что pH доводят до значения примерно 3,5.
25. Способ по любому из пп.15 или 16, дополнительно включающий добавление хлорида натрия к указанному раствору метилналтрексона или его фармацевтически приемлемой соли.
26. Применение фармацевтической композиции по любому из пп.1-14 для уменьшения побочных эффектов опиоидной терапии у субъекта, подвергаемого лечению опиоидами.
27. Продукт, содержащий фармацевтическую композицию по любому из пп.1-11 или 13-14 в герметичном контейнере.
28. Продукт по п.27, отличающийся тем, что указанный контейнер выбирают из флакона, ампулы, пакета, бутыли, шприца и дозирующей упаковки.
29. Продукт по п.28, отличающийся тем, что указанный контейнер представляет собой флакон.
30. Продукт по п.28, отличающийся тем, что указанный контейнер представляет собой шприц.
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| US 2004266806 A1, 30.12.2004 | |||
| RU 2005134359 A, 10.06.2006 | |||
Авторы
Даты
2015-01-20—Публикация
2007-08-03—Подача