Изобретение относится к электролитическим способам получения неорганических соединений, в частности соединений церия, используемых в ядерной энергетике, атомной технике, а также в различных областях современной техники.
Известны способы получения гексаборида церия электролизом расплавленных сред [Самсонов Г.В. Тугоплавкие соединения редкоземельных металлов М, Изд-во «Металлургия», 1964, стр.53-55]. Электролиз осуществляют в графитовых тиглях, служащих одновременно анодом; катод изготовляют из графита или молибдена. В состав ванны для электролиза входят окислы редкоземельных металлов и борный ангидрид с добавками фторидов щелочных и щелочноземельных металлов для снижения температуры и вязкости ванны. Температура электролиза смесей составляет 950-1000°C, напряжение на ванне 8,54÷12B, плотность тока 2,5÷2,6 А/см2. Состав ванны для получения гексаборида церия:
CeO2+2B2O3+CeF2,
или 1/3CeO2+B2O3+CaF2,
или 1/10CeO2+2B2O3+MgO+MgF2.
Недостатком данного технического решения являются высокая температура синтеза и сложность отделения целевого продукта от расплавленного электролита из-за низкой растворимости боратов и фторидов, загрязнение побочными продуктами, в частности боратами, а также невозможность получения ндивидуальной боридной фазы.
Наиболее близким является способ электролитического получения гексаборида церия по патенту РФ №2466090. Электролиз осуществляют в стеклоуглеродных тиглях, служащих одновременно анодом; катодом служит серебряный стержень. В состав ванны для электролиза входят:
хлорид церия 1,0÷4,0;
фторборат калия 1,0÷3,0;
остальное - эвтектическая смесь хлоридов калия, натрия и цезия.
Температура электролиза 550°C при плотностях тока от 0,1 до 1,0 А/см2 и потенциалах электролиза относительно стеклоуглеродного электрода сравнения от -2,0 до -3,0B.
Недостатком данного способа является получение побочного продукта СеВ4 за счет низких температур и сложность отделения его от целевого продукта гексаборида церия.
Задачей настоящего изобретения является получение наноразмерного порошка чистого гексаборида церия, повышение скорости синтеза целевого продукта из расплавленного электролита за счет увеличения температуры процесса синтеза.
Сущность изобретения заключается в том, что осуществляют совместное электровыделение церия и бора из галогенидного расплава на катоде и последующее взаимодействие их на атомарном уровне с образованием ультрадисперсных порошков гексаборида церия. Процесс осуществляется в трехэлектродной кварцевой ячейке, где катодом служит вольфрамовый стержень; анодом и одновременно контейнером - стеклоуглеродный тигель; электродом сравнения - стеклоуглеродная пластина. Синтез ультрадисперсного порошка гексаборида церия проводят посредством потенциостатического электролиза из эквимольного расплава KCl-NaCl, содержащего трихлорид церия и фторборат калия в атмосфере очищенного и осушенного аргона. Потенциостатический электролиз эквимольного расплава KCl-NaCl, содержащего трихлорид церия и фторборат калия, проводят на вольфрамовом катоде при потециалах в пределах от -2,0 до -3,1B относительно стеклоуглеродного электрода сравнения. Полученную катодно-солевую грушу, состоящую из гексаборида церия, отмывают от фторида церия фторидом калия.
Электрохимические процессы, происходящие при образовании боридов церия, можно представить следующими уравнениями:
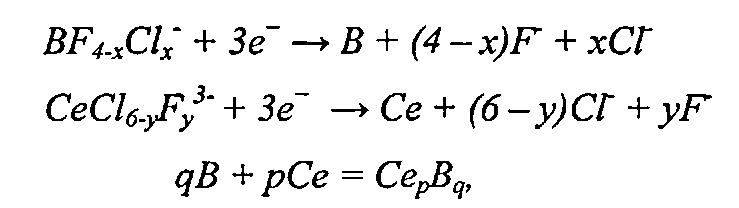
В качества источника церия используют безводный трихлорид церия, в качестве источника бора - фторборат калия, в качестве растворителя - эквимольную смесь хлоридов калия и натрия при следующем соотношении компонентов, мас.%:
хлорид церия 1,0÷4,0;
фторборат калия 1,0÷3,0;
остальное - эквимольная смесь хлоридов калия и натрия.
Электролиз ведут в потенциостатическом режиме при температуре 700°C. Оптимальная продолжительность ведения процесса электролиза составляет 50÷60 мин.
Выбор компонентов электролитической ванны произведен на основании термодинамического анализа и кинетических измерений совместного электровыделения церия и бора из галогенидных расплавов. Из соединений церия и бора, не содержащих кислород, хлорид церия и фторборат калия являются достаточно низкоплавкими и хорошо растворимыми в эквимольном расплаве KCl-NaCl. Растворитель (эквимольный расплав KCl-NaCl) выбран из следующих соображений: напряжение разложения расплавленной смеси KCl-NaCl больше таковых для расплавов CeCl3 и KBF4; хорошая растворимость в воде.
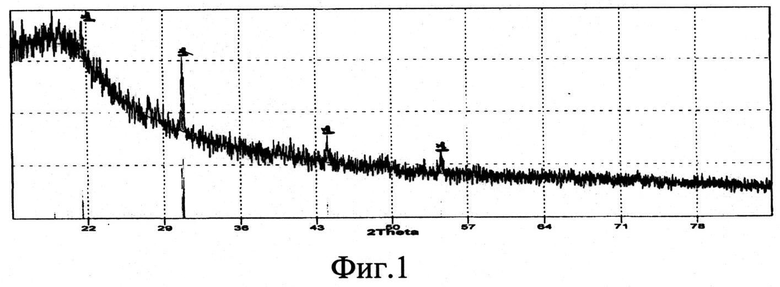
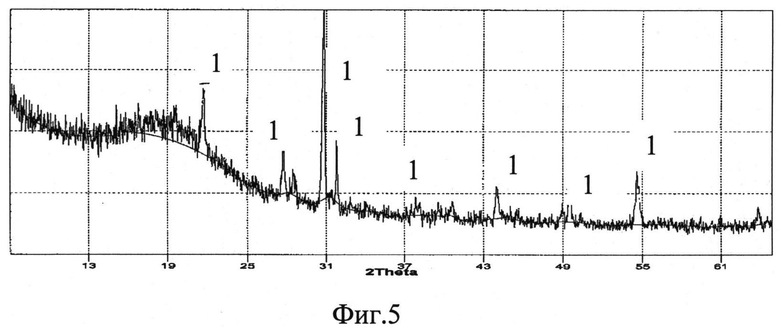
Фазовый состав идентифицирован методом рентгенофазового анализа на дифрактометре ДРОН-6, который показал наличие только фазы CeB6 (изображение на фиг.1, 3, 5).
Фиг.1 - Рентгенограмма порошка борида церия CeB6 (линия 1), полученного из расплава KCl-NaCl на вольфрамовом катоде при φ=-2,3B.
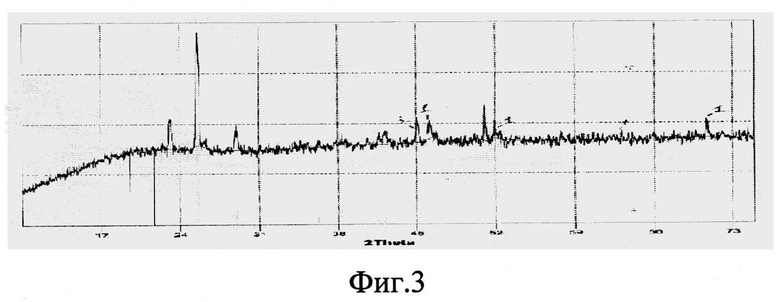
Фиг.3 - Рентгенограмма порошка борида церия CeB6 (линия 1), полученного из расплава KCl-NaCl на вольфрамовом электроде при φ=-3,1B.
Фиг.5 - Рентгенограмма порошка борида церия CeB6 (линия 1), полученного на вольфрамовом катоде при φ=-2,5B.
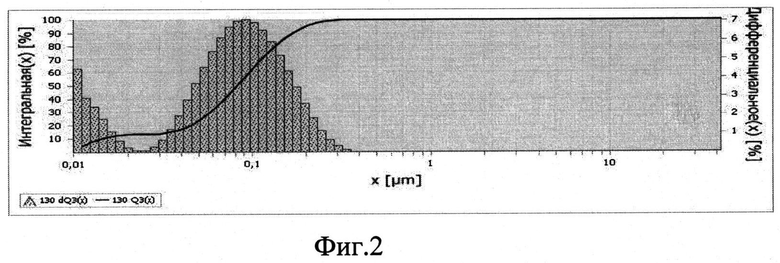
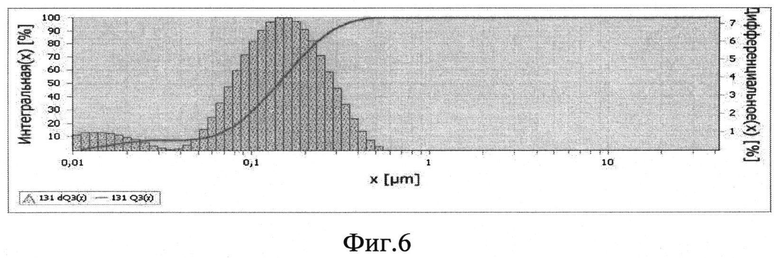
Размер частиц определяли лазерным дифракционным анализатором Fritsch Analysette-22 (изображение на фиг.2, 4, 6).
Фиг.2 - Диаграмма распределения по размерам частиц, полученных при 973K электрохимическим синтезом при i=0,5A/см2.
Фиг.4 - Электронный снимок, частиц, полученных при 973K электрохимическим синтезом при i=0,3A/см2.
Фиг.6 - Диаграмма распределения по размерам частиц, полученных при 973K электрохимическим синтезом при i=0,7A/см2.
Пример 1
В стеклоуглеродный тигель объемом 40 мл помещают солевую смесь массой 31,67 г, содержащую 0,66 г CeCl3 (2,1 мас.%); 1,01 г KBF4 (3,18 мас.%); 16,8 г KCl (53,04 мас.%); 13,2 г NaCl (41,68 мас.%). Тигель с солевой смесью помещают в кварцевую ячейку и в атмосфере сухого аргона выдерживают до температуры расплавления системы. По достижении рабочей температуры 700°C в расплав опускают вольфрамовый катод, электролиз проводят при потенциале -2,3B относительно стеклоуглеродного электрода сравнения (плотность тока 0,5А/см2). Катодно-солевую грушу, состоящую из гексаборида церия, отмывают от фторида церия фторидом калия. Размер частиц полученного порошка гексаборида церия 10-30 нм.
Пример 2
В стеклоуглеродный тигель объемом 40 мл помещают солевую смесь массой 34,2 г, содержащую 2,78 г CeCl3 (8,11 мас.%); 1,42 г KBF4 (4,15 мас.%); 16,8 г KCl (49,12 мас.%); 13,2 г NaCl (38,6 мас.%). Тигель с солевой смесью помещают в кварцевую ячейку и в атмосфере сухого аргона выдерживают до температуры расплавления системы. По достижении рабочей температуры 700°C в расплав опускают вольфрамовый катод, электролиз проводят при потенциале -3,1B относительно стеклоуглеродного электрода сравнения (плотность тока 0,3 А/см2). Катодно-солевую грушу, состоящую из гексаборида церия, отмывают от фторида церия фторидом калия. Размер частиц полученного порошка гексаборида церия 50-70 нм.
Пример 3
В стеклоуглеродный тигель объемом 40 мл помещают солевую смесь массой 33,74 г содержащую 1,13 г CeCl3 (3,37 мас.%); 2,61 г KBF4 (7,72 мас.%); 16,8 г KCl (49,79 мас.%); 13,2 г NaCl (39,12 мас.%). Тигель с солевой смесью помещают в кварцевую ячейку и в атмосфере сухого аргона выдерживают до температуры расплавления системы. По достижении рабочей температуры 700°C в расплав опускают вольфрамовый катод, электролиз проводят при потенциале -2,5B относительно стеклоуглеродного электрода сравнения (плотность тока 0,7 А/см2). Катодно-солевую грушу, состоящую из гексаборида церия, отмывают от фторида церия фторидом калия. Размер частиц полученного порошка гексаборида церия 100 нм.
Техническим результатом является:
- получение наноразмерных частиц гексаборида церия;
- получение целевого продукта в чистом виде за счет хорошей растворимости эквимольного расплава хлорида калия и хлорида натрия в воде, растворимости образующегося фторида церия фторидом калия.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭЛЕКТРОЛИТИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ НАНОРАЗМЕРНЫХ ПОРОШКОВ ГЕКСАБОРИДА НЕОДИМА | 2008 |
|
RU2389684C2 |
| ЭЛЕКТРОЛИТИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ УЛЬТРАДИСПЕРСНОГО ПОРОШКА ГЕКСАБОРИДА ГАДОЛИНИЯ | 2011 |
|
RU2466217C1 |
| ЭЛЕКТРОЛИТИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ УЛЬТРАДИСПЕРСНОГО ПОРОШКА ГЕКСАБОРИДА ГАДОЛИНИЯ | 2012 |
|
RU2507314C1 |
| ЭЛЕКТРОЛИТИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ УЛЬТРАДИСПЕРСНОГО ПОРОШКА ГЕКСАБОРИДА ЛАНТАНА | 2011 |
|
RU2477340C2 |
| ЭЛЕКТРОЛИТИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ УЛЬТРАДИСПЕРСНОГО ПОРОШКА ГЕКСАБОРИДА ДИСПРОЗИЯ | 2012 |
|
RU2510630C1 |
| ЭЛЕКТРОЛИТИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ УЛЬТРАДИСПЕРСНОГО ПОРОШКА ГЕКСАБОРИДА ЦЕРИЯ | 2011 |
|
RU2466090C1 |
| ЭЛЕКТРОЛИТИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ ГЕКСАБОРИДА ПРАЗЕОДИМА | 2008 |
|
RU2393115C2 |
| ЭЛЕКТРОЛИТИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ НАНОРАЗМЕРНОГО ПОРОШКА ДИСИЛИЦИДА ЦЕРИЯ | 2013 |
|
RU2539523C1 |
| Электролитический способ получения ультрадисперсного порошка двойного борида церия и кобальта | 2018 |
|
RU2695346C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОДИСПЕРСНОГО ПОРОШКА ГЕКСАБОРИДА ИТТРИЯ | 2009 |
|
RU2448044C2 |

Изобретение относится к электролитическому способу получения наноразмерного порошка гексаборида церия, включающему синтез гексаборида церия из расплавленных сред в атмосфере очищенного и осушенного аргона. При этом синтез проводят из галогенидного расплава, в качества источника церия используют безводный хлорид церия, в качестве источника бора - фторборат калия, в качестве растворителя - эквимольную смесь хлоридов калия и натрия при следующем соотношении компонентов, мас.%: хлорид церия 1,0÷4,0; фторборат калия 1,0÷3,0; остальное - эквимольная смесь хлоридов калия и натрия, процесс ведут при температуре 700°С, плотностях тока от 0,3 до 0,7 А/см2 и потенциалах электролиза относительно стеклоуглеродного электрода сравнения от -2,0 до -3,1 B. Использование настоящего способа позволяет получать целевой продукт в чистом виде при высокой скорости получения. 6 ил., 3 пр.
Электролитический способ получения наноразмерного порошка гексаборида церия, включающий синтез гексаборида церия из расплавленных сред в атмосфере очищенного и осушенного аргона, отличающийся тем, что синтез проводят из галогенидного расплава, в качества источника церия используют безводный хлорид церия, в качестве источника бора - фторборат калия, в качестве растворителя - эквимольную смесь хлоридов калия и натрия при следующем соотношении компонентов, мас.%:
хлорид церия 1,0÷4,0;
фторборат калия 1,0÷3,0;
остальное - эквимольная смесь хлоридов калия и натрия,
процесс ведут при температуре 700°С, плотностях тока от 0,3 до 0,7 А/см2 и потенциалах электролиза относительно стеклоуглеродного электрода сравнения от -2,0 до -3,1 B.
| ЭЛЕКТРОЛИТИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ УЛЬТРАДИСПЕРСНОГО ПОРОШКА ГЕКСАБОРИДА ЦЕРИЯ | 2011 |
|
RU2466090C1 |
| ПНЕВМОСЕПАРИРУЮЩАЯ КАМЕРА | 0 |
|
SU318362A1 |
| CN 101891216 A, 24.11.2010 | |||
| CN 101948117 A, 19.01.2011 | |||
| CN 101434395 A, 20.05.2009 | |||
Авторы
Даты
2015-02-10—Публикация
2013-09-27—Подача