Изобретение относится к электролитическим способам получения неорганических соединений, в частности соединений церия, и может быть использовано в качестве магнитных материалов.
В последние десятилетия физика магнитных явлений и некоторые области техники получили мощный импульс для своего развития благодаря тому, что было обнаружено магнитное упорядочение у редкоземельных металлов (РЗМ), а также сплавов и соединений на их основе. Поскольку РЗМ являются основой для синтеза различных сплавов и соединений, их изучение является исходным этапом в становлении физических представлений о магнетизме редкоземельных веществ. РЗМ обладают необычными магнитными свойствами: гигантскими значениями магнитной анизотропии и магнитострикции, высокой магнитной индукцией и др. [1-2].
В сплавах и соединениях эти свойства проявляются не только при низких, но и при высоких температурах.
Другой особенностью РЗМ и их сплавов является наличие большого числа разнообразных периодических магнитных структур и магнитных фазовых переходов между различными магнитоупорядоченными состояниями [3-4].
В работе [5] рассмотрено взаимодействие фаз в четверной системе Се-№-Со-Мо в области, богатой кобальтом по разрезу СеМв5 (где Ме: Со, №), содержащей 3 ат. % молибдена.
Установлены фазовые равновесия в системе кобальт-никель-молибден. Установлен характер взаимодействия фаз в части четверной системы Се-№-Со-Мо в области существования соединений СеСо5 и СегСоп при содержании в системе 3 ат. % Мо. На основании полученных результатов построена схема распределения фазовых областей в системе Се-М-Со-Мо при 773 К. Установлена область существования ферромагнетизма.
Известен электролитический способ получения ультрадисперсного порошка гексаборида диспрозия [6]. Изобретение относится к электролитическим способам получения чистого гексаборида диспрозия. В качестве источника диспрозия используют безводный трихлорид диспрозия, источника бора - фторборат калия, фонового электролита - эквимольную смесь хлоридов калия и натрия. Электролиз ведут в потенциостатическом режиме при температуре 700±10°С, плотностях тока от 0,1 до 1,0 А/см2 и потенциалах электролиза от 2,5 до 2,8 В относительно стеклоуглеродного квазистационарного электрода сравнения.
Известен электролитический способ получения ультрадисперсного порошка гексаборида гадолиния [7]. Изобретение относится к электролитическим способам получения чистого ультрадисперсного порошка гексаборида гадолиния. Порошок синтезируют электролизом из расплавленной среды, включающей хлорид гадолиния и фторборат калия в фоновом электролите при температуре 550±10°С в атмосфере очищенного и осушенного аргона. В качестве фонового электролита используют эвтектическую смесь хлоридов калия, натрия и цезия при следующем соотношении компонентов, мас.%: хлорид гадолиния 3,0^-7,0, фторборат калия 6,0-^-10,0, эвтектическая смесь хлоридов калия, натрия и цезия -остальное. Изобретение позволяет получить чистый ультрадисперсный порошок гексаборида гадолиния, повысить скорость синтеза целевого продукта из расплавленного электролита и снизить энергозатраты.
Известен способ получения ультрадисперсных порошков интерметаллидов иттрия с кобальтом [8]. Изобретение относится к электрохимическому получению ультрадисперсных порошков интерметаллидов иттрия с кобальтом для создания магнитных материалов и ячеек хранения информации. Порошок получают путем электролиза расплава при температуре 700°С и плотностях катодного тока 2,6-3,2 А/см2, в среде четыреххлористого углерода, где в качестве источника иттрия используется растворимый иттриевый анод. В качестве расплава используют электролит,
содержащий хлорид натрия, хлорид калия и хлорид кобальта при следующем соотношении компонентов, мол.%: КС1 - 47,5-49,5; ЫаС1 - 47,5-49,5; СоСЬ -1,0-5,0. Способ позволяет получать изотропные по составу ультрадисперсные порошки интерметаллидов иттрия и кобальта при повышении скорости синтеза целевого продукта.
Известен способ совместного электровосстановления ионов церия с ионами кобальта и бора и электрохимический синтез двойных боридов церия и кобальта из галогенидных расплавов [9].
Известен также способ совместного электровосстановления ионов церия, кобальта и бора из галогенидных расплавов [10].
Общим недостатком приведенных аналогов является высокая длительность и многостадийность процесса, а также энергозатратность, сложность отделения целевого продукта от расплавленного электролита, загрязнение побочными продуктами.
Наиболее близким является способ получения гексаборида церия электролизом расплавленных сред [11].
Процесс осуществляется в трехэлектродной кварцевой ячейке, где катодом служит вольфрамовый стержень; анодом и одновременно контейнером - стеклоуглеродный тигель; электродом сравнения -стеклоуглеродная пластина. Синтез ультрадисперсного порошка гексаборида церия проводят посредством потенциостатического электролиза из эквимольного расплава КС1-ИаС1, содержащего трихлорид церия и фторборат калия в атмосфере очищенного и осушенного аргона. Потенциостатический электролиз эквимольного расплава КС1-ЫаС1, содержащего трихлорид церия и фторборат калия, проводят на вольфрамовом катоде при потенциалах в пределах от -2,0 до -3,1 В относительно стеклоуглеродного электрода сравнения. Полученную катодно-солевую грушу, состоящую из гексаборида церия, отмывают от фторида церия фторидом калия.
Недостатком прототипа является загрязнение побочными продуктами.
В основу настоящего изобретения положена задача: получение чистого ультрадисперсного порошка двойного борида церия и кобальта, обладающего магнитными свойствами, из галогенидных расплавов путем снижения температуры процесса синтеза и увеличение выхода целевого продукта.
Сущность изобретения заключается в том, что осуществляют совместное электровыделение церия, кобальта и бора из галогенидного расплава на катоде и последующее взаимодействие их на атомарном уровне с образованием ультрадисперсных порошков двойных боридов церия и кобальта. Процесс осуществляется в трехэлектродной кварцевой ячейке, где катодом служит молибденовый электрод; электродом сравнения -стеклоуглеродная пластина; анодом и одновременно контейнером -стеклоуглеродный тигель. Синтез ультрадисперсного порошка двойного борида церия и кобальта проводят посредством потенциостатического электролиза из эквимольного расплава КС1-ИаС1, содержащего трихлорид церия, дихлорид кобальта и фторборат калия в атмосфере очищенного и осушенного аргона. Потенциостатический электролиз эквимольного расплава КС1-ШС1, содержащего трихлорид церия, дихлорид кобальта и фторборат калия, проводят на вольфрамовом электроде при потенциалах в пределах от -2,2 до -2,4 В относительно стеклоуглеродного электрода сравнения. Полученную катодно-солевую грушу, содержащего двойной борид церия и кобальта, отмывают от рабочего электролита раствором фторида калия (10%).
В качестве источника церия используют безводный трихлорид церия, в качестве источника кобальта - безводный дихлорид кобальта, в качестве источника бора - фторборат калия, в качестве растворителя - эквимольную смесь хлоридов калия и натрия при следующем соотношении компонентов, моль/см3, х10"4:
хлорид церия 1,7 3,0;
хлорид кобальта 0,8 + 7,0 фторборат калия 1,5 ч- 3,5.
Электролиз ведут в потенциостатическом режиме при температуре 700°С±5°. Оптимальная продолжительность ведения процесса электролиза составляет 60ч-120 мин.
Выбор компонентов электролитической ванны произведен на основании термодинамического анализа и кинетических измерений совместного электровыделения церия, кобальта и бора из галогенидных расплавов. Из соединений церия, кобальта и бора, не содержащих кислород, хлорид церия, хлорид кобальта и фторборат калия являются достаточно низкоплавкими и хорошо растворимыми в эквимольном расплаве КС1-ИаС1. Растворитель (эквимольный расплав КС1-МаСГ) выбран из следующих соображений: напряжение разложения расплавленной смеси КС1-ИаС1 больше таковых для расплавов СеС1з, СоСЬ и КВР4', хорошая растворимость в воде.
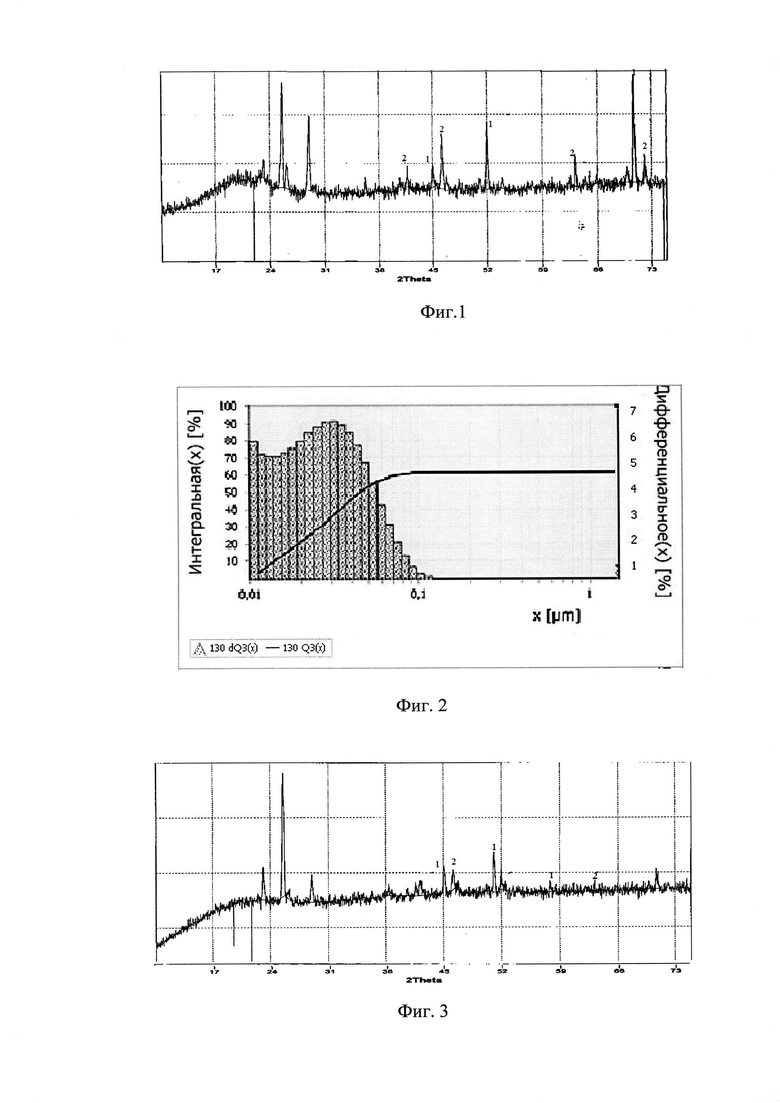
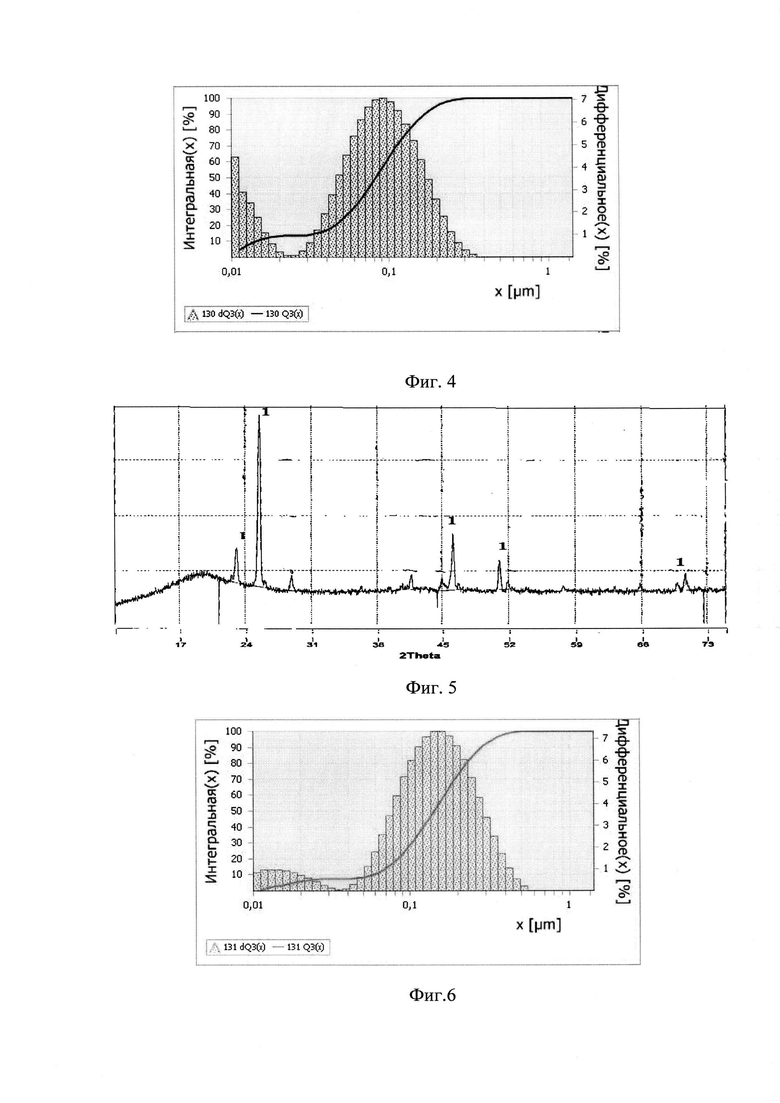
Фазовый состав идентифицирован методом рентгенофазового анализа на дифрактометре ДРОН-6, который показал наличие фаз СеСо4В, СеСозВг, Се2Со7В3 (фиг. 1,3,5/
Фиг. 1 .Рентгенограмма порошка двойного борида церия и кобальта, полученного из эквимольного расплава КС1-ИаС1, содержащего моль/см3, хЮ"4: СеСЬ - 1,73; СоСЬ - 0,85; КВР4 - 1,55 на молибденовом катоде при Ф = - 2,2 В. Линии: 1 - Се2Со7В3; 2 - СеСо4В.
Фиг. 3. Рентгенограмма порошка двойного борида церия и кобальта, полученного из эквимольного расплава КС1-ИаС1, содержащего моль/см3, хЮ"4: СеСЬ - 2,35; СоСЬ- 5,14; КВР4- 2,85 на молибденовом катоде при Ф = - 2,3 В. Линии: 1 - СеСо3В2; 2 - Се2Со7В3.
Фиг. 5. Рентгенограмма порошка двойного борида церия и кобальта, полученного из эквимольного расплава КС1-ЫаС1, содержащего моль/см3, хЮ-4: СеСЬ - 2,98; СоСЬ - 6,87; КВР4 - 3.49 на молибденовом катоде при Ф = - 2,4 В. Линии: 1 - СеСо3В2.
Лазерным дифракционным анализатором Ргкзсп Апа1узеп.е-22 определены размер частиц и составляет 0,01- 0,3 мкм (фиг. 2,4,6).
Фиг. 2. Диаграмма распределения по размерам частиц двойного борида церия и кобальта, полученных при 700°С из эквимольного расплава КС1-ЫаС1, содержащего моль/см3, х10"4: СеС13- 1,73; СоС12- 0,85; КВР4- 1,55.
Фиг. 4. Диаграмма распределения по размерам частиц двойного борида церия и кобальта, полученных при 700°С из эквимольного расплава КС1-ЫаС1, содержащего моль/см3, хЮ"4: СеС13-2,35; СоС12-5,14; КВР4-2,85.
Фиг. 6. Диаграмма распределения по размерам частиц двойного борида церия и кобальта, полученных при 700 °С из эквимольного расплава КС1-ИаС1 содержащего моль/см3, хЮ4: СеС13- 2,98; СоС12 - 6,87; КВР4 - 3.49.
Пример 1. Электролитический способ получения ультрадисперсного порошка двойного борида церия и кобальта осуществляют в стеклоуглеродном тигле объемом 20 мл, куда помещают эквимольную смесь КС1-ЫаС1 массой ЗОг, содержащую в моль/см3, хЮ"4: СеС13- 1,73; СоС12-0,85; КВР4- 1,55. Тигель с солевой смесью помещают в кварцевую ячейку и в атмосфере сухого аргона выдерживают до температуры расплавления системы. По достижении рабочей температуры 700°С в расплав опускают молибденовый катод, электролиз проводят при потенциале -2,2 В относительно стеклоуглеродного электрода сравнения. Катодно-солевую грушу, содержащую двойной борид церия и кобальта, отмывают от рабочего электролита раствором фторида калия 10%. Размер частиц полученного порошка двойного борида церия и кобальта 0,01-0,06 мкм.
Пример 2. Электролитический способ получения ультрадисперсного порошка двойного борида церия и кобальта осуществляют в стеклоуглеродном тигле объемом 20 мл, куда помещают эквимольную смесь КС1-ИаС1 массой 30 г, содержащую в моль/см3, хЮ"4: СеС13 - 2,35; СоСЛг— 5,14; КВР4- 2,85. Тигель с солевой смесью помещают в кварцевую ячейку и в атмосфере сухого аргона выдерживают до температуры расплавления
системы. По достижении рабочей температуры 700°С в расплав опускают молибденовый катод, электролиз проводят при потенциале - 2,3 В относительно стеклоуглеродного электрода сравнения. Катодно-солевую грушу, содержащую двойной борид церия и кобальта, отмывают от рабочего электролита раствором фторида калия 10%. Размер частиц полученного порошка двойного борида церия и кобальта 0,01-0,1 мкм.
Пример 3. Электролитический способ получения ультрадисперсного порошка двойного борида церия и кобальта осуществляют в стеклоуглеродном тигле объемом 20 мл, куда помещают эквимольную смесь КС1-ИаС1 массой ЗОг, содержащую в моль/см3, х10"4: СеСЬ - 2,98; СоСЬ — 6,87; КВР4 - 3,49. Тигель с солевой смесью помещают в кварцевую ячейку и в атмосфере сухого аргона выдерживают до температуры расплавления системы. По достижении рабочей температуры 700°С в расплав опускают молибденовый катод, электролиз проводят при потенциале - 2,4 В относительно стеклоуглеродного электрода сравнения. Катодно-солевую грушу, содержащую двойной борид церия и кобальта, отмывают от рабочего электролита раствором фторида калия 10%. Размер частиц полученного порошка двойного борида церия и кобальта 0,07-0,3 мкм.
Техническим результатом является: получение ультрадисперсных порошков двойного борида церия и кобальта при сравнительно низкой температуре (700°С) и использованием недорогих, доступных реагентов.
Литература
1. Никитин С.А. М., Магнитные свойства редкоземельных металлов и их сплавов. Изд.МГУ, 1989, 248с.
2. Белов К.П. Редкоземельные металлы, сплавы и соединения - новые магнитные материалы для техники. Соросовский образовательный журнал, М., Международная Соросовская программа образования в области точных наук, 1996, с94-99.
3. Тейлор К., Дарби М. Физика редкоземельных соединений, М., изд.
Мир, 1974,с.374.
1. Звездин А.К., Матвеев В.М., Мухин А.А., Попов А.И. Редкоземельные ионы в магнитоупорядоченных кристаллах. М., Наука, 1985 , с.294.
2. Фазовый состав и свойства сплавов системы Се-№-Со-Мо. Р. В. Калагова, Н. И. Калоев, А. И. Мартирян, Г.Г. Григорян и Л.Г. Арустамова. Журнал неорганической химии. №3 2002г. Ст. 45-50.
3. Патент РФ №2510630.
4. Патент РФ №2507314.
5. Патент РФ №2514237.
6. Исследование совместного электровосстановления ионов церия с ионами кобальта и бора и электрохимический синтез двойных боридов церия и кобальта из галогенидных расплавов. Х.Б. Кушхов, А.Х. Абазова, М.К. Виндижева, Р.А. Мукожева, А.А. Кяров, З.Х. Кярова // Известия КБГУ. - Нальчик, -2016, - Том IV. - №1. С. 60-66.
Ю.Исследование совместного электровосстановления ионов церия, кобальта и бора из галогенидных расплавов. Х.Б. Кушхов, А.А. Мукожева, М.К. Виндижева, А.Х. Абазова, М.Н. Калибатова, Б.В. Бала // XVI Российская конференция (с международным участием). Материалы докладов том I - Екатеринбург -2013. С. 172-173.
11 .Патент РФ № 2466090.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭЛЕКТРОЛИТИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ НАНОРАЗМЕРНОГО ПОРОШКА ГЕКСАБОРИДА ЦЕРИЯ | 2013 |
|
RU2540277C1 |
| ЭЛЕКТРОЛИТИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ УЛЬТРАДИСПЕРСНОГО ПОРОШКА ГЕКСАБОРИДА ЦЕРИЯ | 2011 |
|
RU2466090C1 |
| ЭЛЕКТРОЛИТИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ УЛЬТРАДИСПЕРСНОГО ПОРОШКА ГЕКСАБОРИДА ГАДОЛИНИЯ | 2011 |
|
RU2466217C1 |
| ЭЛЕКТРОЛИТИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ УЛЬТРАДИСПЕРСНОГО ПОРОШКА ГЕКСАБОРИДА ДИСПРОЗИЯ | 2012 |
|
RU2510630C1 |
| ЭЛЕКТРОЛИТИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ УЛЬТРАДИСПЕРСНОГО ПОРОШКА ГЕКСАБОРИДА ГАДОЛИНИЯ | 2012 |
|
RU2507314C1 |
| ЭЛЕКТРОЛИТИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ УЛЬТРАДИСПЕРСНОГО ПОРОШКА ГЕКСАБОРИДА ЛАНТАНА | 2011 |
|
RU2477340C2 |
| ЭЛЕКТРОЛИТИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ ГЕКСАБОРИДА ПРАЗЕОДИМА | 2008 |
|
RU2393115C2 |
| ЭЛЕКТРОЛИТИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ НАНОРАЗМЕРНЫХ ПОРОШКОВ ГЕКСАБОРИДА НЕОДИМА | 2008 |
|
RU2389684C2 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОДИСПЕРСНОГО ПОРОШКА ГЕКСАБОРИДА ИТТРИЯ | 2009 |
|
RU2448044C2 |
| Электрохимический способ получения микродисперсных порошков гексаборидов металлов лантаноидной группы | 2019 |
|
RU2722753C1 |
Изобретение относится к электролитическому способу получения ультрадисперсных порошков двойного борида церия и кобальта, включающему синтез двойного борида церия и кобальта из расплавленных сред. Способ характеризуется тем, что синтез проводят из галогенидного расплава на молибденовом катоде в атмосфере очищенного и осушенного аргона при температуре 700°C и потенциалах электролиза относительно стеклоуглеродного электрода сравнения от -2,2 до -2,4 В, где в качестве источника церия используют безводный хлорид церия, в качестве источника кобальта - безводный дихлорид кобальта, в качестве источника бора - фторборат калия, в качестве растворителя - эквимольную смесь хлоридов калия и натрия при следующем соотношении компонентов, моль/см3, × 10-4: хлорид церия 1,7÷3,0; хлорид кобальта 0,8÷7,0; фторборат калия 1,5÷3,5. Техническим результатом является получение ультрадисперсного порошка двойного борида церия и кобальта; получение целевого продукта в чистом виде и с повышенным выходом. 3 пр., 6 ил.
Электролитический способ получения ультрадисперсных порошков двойного борида церия и кобальта, включающий синтез двойного борида церия и кобальта из расплавленных сред, отличающийся тем, что синтез проводят из галогенидного расплава на молибденовом катоде в атмосфере очищенного и осушенного аргона при температуре 700°C и потенциалах электролиза относительно стеклоуглеродного электрода сравнения от -2,2 до -2,4 В, где в качестве источника церия используют безводный хлорид церия, в качестве источника кобальта - безводный дихлорид кобальта, в качестве источника бора - фторборат калия, в качестве растворителя - эквимольную смесь хлоридов калия и натрия при следующем соотношении компонентов, моль/см3, × 10-4:
| АБАЗОВА Азида Хасановна | |||
| ЭЛЕКТРОХИМИЧЕСКИЙ СИНТЕЗ ФУНКЦИОНАЛЬНЫХ МАТЕРИАЛОВ НА ОСНОВЕ ЦЕРИЯ В ГАЛОГЕНИДНЫХ РАСПЛАВАХ | |||
| ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ОБРАЗОВАНИЯ "КАБАРДИНО-БАЛКАРСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ им | |||
| Х.М | |||
| БЕРБЕКОВА" | |||
| ДИССЕРТАЦИЯ на соискание ученой степени кандидата химических наук, Екатеринбург, 2017 | |||
| ЭЛЕКТРОЛИТИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ НАНОРАЗМЕРНОГО ПОРОШКА ГЕКСАБОРИДА ЦЕРИЯ | 2013 |
|
RU2540277C1 |
| СПОСОБ ПОЛУЧЕНИЯ БОРИДОВ РЕДКОЗЕМЕЛЬНЫХ МЕТАЛЛОВ | 1997 |
|
RU2123975C1 |
| US 3902973 A, 02.09.1975 | |||
| ЭЛЕКТРОЛИТИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ НАНОРАЗМЕРНОГО ПОРОШКА ГЕКСАБОРИДА ЦЕРИЯ | 2013 |
|
RU2540277C1 |
Авторы
Даты
2019-07-23—Публикация
2018-10-08—Подача