Заявляемое техническое решение относится к аффинным сорбентам, полученным на основе техногенного сырья, в частности магнитных микросфер летучих энергетических зол, и может быть использовано в биохимии, медицинской диагностике и биотехнологии для выделения и детекции рекомбинантных белков, содержащих полигистидиновые последовательности.
Экспрессия рекомбинантных белков, меченных полигистидиновыми фрагментами (от 6 остатков гистидина и более), широко применяется для упрощения их выделения из различных прокариотических и эукариотических систем. Для этого используют металл-ионные аффинные сорбенты, содержащие на своей поверхности хелатносвязанные ионы переходных металлов (Cu2+, Ni2+, Zn2+, Со2+) [Porath J., Carlsson J., Olsson I., Belfrage G. Metal chelate affinity chromatography, a new approach to protein fractionation, Nature 258 (1975) 598-599; Schmitt J., Hess H., Stunnenberg H.G. Affinity purification of histidine-tagged proteins, Mol. Biol. Rep. 18 (1993) 223-230; Gabert-Porecar V., Menart V. Perspectives of immobilized-metal affinity chromatography, J. Biochem. Biophys. Methods 49 (2001) 335-360]. Адсорбция белков на металл-хелатных сорбентах протекает за счет образования координационной связи между иммобилизованным ионом металла и электронодонорными атомами азота, входящими в состав имидазольного кольца гистидина в молекуле белка.
Усовершенствование аффинных сорбентов с координационно-связанными ионами металлов ведется в направлении придания им магнитных свойств, что обеспечивает возможность манипулирования сорбентами с использованием магнитного поля и таким образом упрощает процедуру извлечения рекомбинантных белков из гетерогенных смесей. Так, известны такие коммерчески доступные магнитоуправляемые аффинные сорбенты, как Ni2+-NTA MABs (Qiagen, Германия) [Schafer F., Romer U., Emmerlich M., Blumer J., Steinert K. Automated high-throughput purification of 6xHis-tagged proteins, J. Biomol. Tech. 13 (2002) 131-142], которые состоят из магнитного ядра на основе оксидов железа и полисахаридной оболочки на основе поперечно-сшитой агарозы с ковалентно привитыми остатками нитрилотриуксусной кислоты (NTA), хелатирующей ионы Ni2+. Частицы сорбента Ni2+-NTA MABs представляют собой микросферы размером 45-165 мкм с емкостью по 6His-меченным белкам (~20 кДа) 5-10 мг/мл. Известны также наноразмерные (~10 нм) металл-хелатные сорбенты с магнитным ядром на основе FePt [Xu С., Xu K., Gu H., Zhong X., Guo Z., Zheng R., Zhang X., Xu B. Nitrilotriacetic Acid-Modified Magnetic Nanoparticles as a General Agent to Bind Histidine-Tagged Proteins, J. Am. Chem. Soc., 126 (2004) 3392-3393], в которых ионы Ni2+ закреплены на поверхности наночастиц FePt также посредством связи с нитрилотриуксусной кислотой. К недостаткам такого рода сорбентов можно отнести многостадийность и сложность их синтеза, требующего применения широкого набора органических реагентов, а также низкую химическую устойчивость в условиях высоких концентраций денатурирующих и хелатирующих реагентов, используемых на стадии сорбции (ЭДТА, мочевина) и регенерации сорбента (имидазол). В частности, при совместном присутствии с Ni2+-NTA MABs допустима концентрация ЭДТА не выше 10-3 М. Более высокие концентрации ЭДТА, благоприятные для выделения белков, чувствительных к присутствию в растворе двухвалентных катионов металлов, вызывают вымывание ионов Ni2+ с поверхности носителя и инактивацию сорбента. Кроме того, инактивация сорбента происходит также на стадии десорбции в процессе элюирования His-меченных белков в условиях высокой концентрации имидазола, что делает необходимым введение ионов Me2+ после каждого цикла адсорбции-десорбции.
Для повышения устойчивости магнитных твердофазных систем с иммобилизованным ионом Me2+ к воздействию более высоких концентраций комплексообразователей (>10-3 М) в ряде работ предложены магнитоуправляемые сорбенты, состоящие из магнитного ядра на основе синтетического магнетита или маггемита и кремнеземной оболочки, в которую без участия хелатирующего полидентатного лиганда инкорпорированы ионы Ni2+ (Ni2+ -SiMAG, Chemicell, Berlin, Germany) [Frenzel A., Bergemann C., Kohl G., Reinard T. Novel purification system for 6His-tagged proteins by magnetic affinity separation // J. Chromatogr. В 793 (2003) 325-329] или Zn2+ [Bele M., Hribar G., Campelj S., Macovec D., Gabert-Porecar V., Zorko M., Gaberscek M., Jamnik J., Venturini P. Zn-decorated silicacoated magnetic nanoparticles for protein binding and controlled release // J. Chromatogr. В 867 (2008) 160-164]. Полученный сорбент характеризуется прочным связыванием ионов Ni2+ в кремнеземной матрице, что позволяет многократное использование сорбента без промежуточной реактивации. Однако сложность процесса получения магнитного компонента удорожает стоимость сорбента.
В работе [Л.А. Франк, В.В. Борисова, Т.А. Верещагина, Е.В. Фоменко, А.Г. Аншиц, И.И. Гительзон. Выделение рекомбинантных белков с использованием аффинных магнитных сорбентов на основе микросфер энергетических зол // Прикладная биохимия и микробиология 45 (2009) 237-242] получен магнитный сорбент Ni2+-SiO2/MM на основе магнитных микросфер энергетических зол от сжигания угля с иммобилизованным ионом Ni2+ на поверхности кремнеземного слоя, синтезированного золь-гель методом. Отсутствие стадии синтеза магнитного компонента существенно упрощает процедуру получения композитного сорбента, а относительно невысокие затраты на выделение узкой фракции микросфер из магнитных концентратов, являющихся фактически отходами производства электроэнергии, и низкая стоимость являются достоинствами сорбента.
Согласно данному способу на первой стадии получают кремнеземный компонент в виде гидрогеля при взаимодействии жидкого силикатного стекла с раствором азотнокислого аммония при выбранном соотношении NH4 +/Na+=1,2 в присутствии азотной кислоты с целью поддерживания в суспензии заданного постоянного значения pH=1. Затем осадок отфильтровывают, тщательно промывают дистиллированной водой, подвергают катионному обмену с солями аммония для освобождения от хемосорбированных ионов натрия, затем снова отфильтровывают и промывают. На следующей стадии осуществляют нанесение кремнеземного компонента на поверхность магнитных микросфер путем смешивания полученного гидрогеля с магнитными микросферами в соотношении 1:3, тщательно перемешивают, затем сушат в сушильном шкафу при 120°C в течение 6 часов. Из сухого образца методом магнитной сепарации отбирают магнитную фракцию, которую многократно подвергают процедуре очистки от немагнитного кремнеземного компонента промывкой дистиллированной водой и последующей мокрой магнитной сепарацией. Выделенный магнитный продукт отфильтровывают и сушат при 120°C. Для модифицирования поверхности композитных микросфер введением ионов никеля микросферы пропитывают 10%-ным раствором ацетата никеля в соотношении 0,6 г микросфер на 2 мл раствора Ni(CH3COO)2. Образцы сушат при комнатной температуре, затем прокаливают при 500°C в течение 6 часов, после чего подвергают мокрой магнитной сепарации и сушке при 120°C.
В качестве магнитного ядра композитного сорбента используют узкую фракцию магнитных микросфер, выделенную из летучих зол от сжигания ирша-бородинского угля, которая характеризовалась следующим составом (мас.%):SiO2 - 4,30; Fe2O3 - 83,17. Содержание феррошпинельной фазы в микросферах составляло 76,4 мас.%, а силикатной стеклофазы - 16,5 мас.%.
В случае тестового выделения рекомбинантного зеленого флуоресцентного белка, имеющего в своем составе фрагмент из 6 повторяющихся гистидиновых остатков по NH2-концу (6His-CLGFP), адсорбционная специфическая емкость указанного аффинного сорбента составила 1-3,5 мг на грамм сорбента.
К недостаткам данного способа получения следует отнести многостадийность создания кремнеземного слоя на поверхности магнитных микросфер и низкую адгезионную прочность силикатного покрытия, вызывающую снижение адсорбционной емкости сорбента в многоцикловом процессе сорбции-десорбции белка. Способ принят за прототип.
Поставлена задача упростить синтез сорбента и повысить адгезионную прочность кремнеземной оболочки на поверхности магнитных микросфер без ухудшения сорбционной емкости в отношении белков среднего размера (20-30 кДа).
Эта задача решена следующим образом. Для достижения поставленного технического результата при получении сорбента в качестве магнитного компонента используют магнитные микросферы летучих зол от сжигания углей, содержащие аморфную силикатную фазу. На поверхность микросфер нанесят пористый кремнеземный слой, в который вводят ионы Ni2+ методом пропитки солью никеля с последующим ее термическим разложением. В отличие от прототипа содержание силикатной стеклофазы в магнитных микросферах составляет около 40 мас.%, а создание пористого кремнеземного покрытия проводят методом гидротермального синтеза при совместном присутствии в реакционной среде микросфер, гексадецилтриметиламмония бромида и тетраэтоксисилана с последующей высокотемпературной обработкой продукта. Затем продукт синтеза подвергают активации кипячением в водных средах с различным pH. Гидротермальный синтез проводят в динамических или статических условиях, в кислой или аммиачно-спиртовой среде при температурах 60-120°C в течение 2-120 часов.
Сущность заявляемого технического решения заключается в следующем. Разделение концентратов магнитных микросфер энергетических зол с использованием комбинированной схемы, включающей стадии гранулометрической классификации, гравитационной и магнитной сепарации, позволяет получать магнитные микросферические продукты стабилизированного состава и морфологии [Шаронова О.М., Аншищ Н.Н., Оружейников А.И., Акимочкина Г.В., Саланов А.Н., Низовский А.И., Семенова О.Н., Аншиц А.Г. Состав и морфология магнитных микросфер энергетической золы каменных углей Экибастузского и Кузнецкого бассейнов // Химия в интересах устойчивого развития 11 (2003) 673-682]. Текстура магнитных микросфер образована кристаллитами феррошпинели с примесью минорных фаз, капсулированных в силикатном стекле разного состава. Различия в содержании железа, стеклофазы и других компонентов приводят к формированию магнитных глобул различной морфологии. Стеклофаза служит своего рода защитной оболочкой, препятствующей окислению магнитного компонента и его потенциально возможному растворению в случае контактирования с водными средами. Наряду с этим, силикатное стекло содержит на своей поверхности реакционноспособные силанольные группы ≡Si-OH, которые могут служить якорными группами для закрепления катионов d-металлов по типу координационного взаимодействия или, в случае их невысокого содержания, для связывания дополнительного функционального слоя SiO2 высокой поверхности. Учитывая, что ионы никеля имеют 6 центров связывания лигандов в своей координационной сфере, которые могут быть полностью насыщены взаимодействием с атомами кислорода ОH-групп при их высокой плотности, важным является обеспечение ненасыщенности как минимум 2-х координационных связей Me2+ для сохранения величины связывания белков на уровне сорбентов-аналогов (до 3,5 мг/г). Как показано в способе получения сорбента-прототипа, координационная ненасыщенность связей инкорпорированных ионов Ni2+ может быть обеспечена при введении избытка ионов Ni2+ методом пропитки поверхности водным раствором соли никеля с последующим ее термическим разложением.
Достижение заявленных преимуществ обеспечивается выбором магнитных микросфер с высоким содержанием силикатной составляющей, способа получения силикатного покрытия с оптимальными пористой структурой и концентрацией поверхностных гидроксильных групп и способом нанесения ионов Ni2+.
На рисунке 1 приведен электронно-микроскопический снимок магнитных микросфер фракции -0,063+0,05 мм.
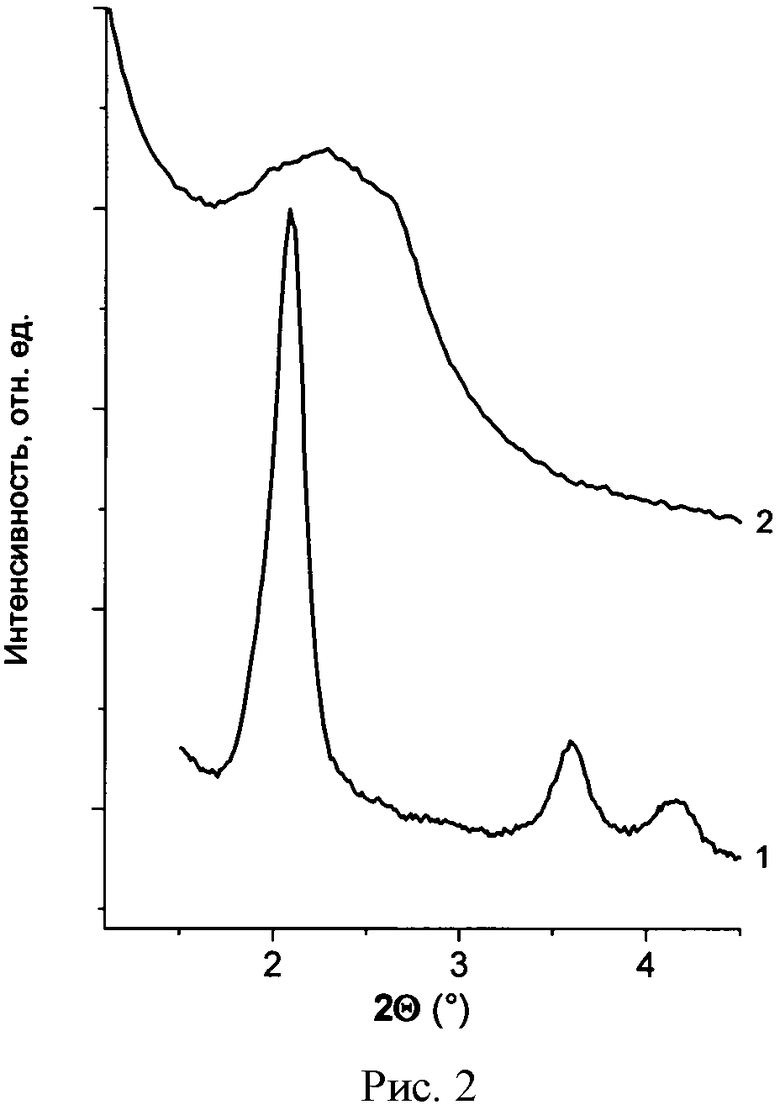
На рисунке 2 приведены рентгенограммы эталонного МСМ-41 (1) и модифицированных микросфер (2).
Сущность изобретения демонстрируется следующими примерами.
ПРИМЕР 1. Для получения аффинного сорбента используют узкую фракцию магнитных микросфер (Рис.1), выделенную из летучих зол от сжигания экибастузского угля, характеристики которой приведены в таблице 1. Условия получения сорбента приведены в таблице 2.
Синтез пористого кремнеземного покрытия на поверхности магнитных микросфер проводят «темплатным» методом в водной кислой среде в стационарном режиме при 80°C в течение 120 часов. Использовались реагенты в следующем мольном соотношении: 100 H2O:0,9 HCl:0,11 гексадецилтриметиламмония бромид (HTABr):0,13 тетраэтоксисилан (TEOS) при объемном соотношении твердая фаза (микросферы):жидкая фаза = 1:20. По окончании синтеза микросферы отделяют и промывают дистиллированной водой до отрицательной реакции на хлорид-ионы раствором 0,1 н AgNO3, сушат при 80°C, прокаливают в течение 4 часов при 540°C. По данным рентгенофазового анализа (Рис.2) и низкотемпературной адсорбции азота в составе модифицированных микросфер присутствует фаза мезопористого силиката с диаметром пор 36 Å, аналогичная материалу МСМ-41 [Meynen, V., Cool, Р., Vansant, E.F. Verified syntheses of mesoporous materials // Micropor. Mesopor. Mater. 125 (2009) 170-223]. Слабовыраженный рефлекс в области основного пика МСМ-41 на дифрактограмме полученного материала (Рис.2, рентгенограмма 2) свидетельствует о низком содержании синтезированного силикатного компонента и/или низкой упорядоченности его структуры по сравнению с эталонным образцом МСМ-41. Исходя из сопоставления величин удельной поверхности полученного материала (~10 м2/г) и МСМ-41 (~1000 м2/г), оценочное содержание мезопористого SiO2 в составе микросферического композитного материала составило около 1 мас.%.
Активацию поверхности мезопористого покрытия микросфер проводят при кипячении в воде в течение 4 часов.
Магнитный сорбент тестируют на примере выделения рекомбинантного белка размером 27 кДа, имеющего в своем составе фрагмент из шести повторяющихся гистидиновых остатков по NH2-концу - зеленого флуоресцентного белка медузы Clytia gregaria (6His-CLGFP). Рекомбинантные клетки E.coli BL21-gold, экспрессирующие этот белок, суспендируют в трис-HCl - солевом буфере (0,02М ТрисНСl, pH 7, 0,15М NaCl - TBS) и разрушают с помощью ультразвукового дезинтегратора UD-20 (Techpan, Польша) (6 импульсов по 20 сек, 0°C). Смесь центрифугируют и полученный супернатант («лизат»), содержащий 6His-CLGFP, используют для тестирования образцов сорбента.
В пробирку с навеской частиц сорбента вносят 1 мл «лизата» и перемешивают в течение 2 минут. Частицы сорбента фиксируют у стенки пробирки с помощью магнита, а раствор белка удаляют пипеткой и записывают спектр поглощения на спектрофотометре UVIKON 943 («Kontron Instruments», Италия). Оценку сорбционной емкости сорбента проводят по разнице оптических плотностей растворов при длине волны 485 нм до и после поглощения с использованием значения молярной экстинкции 6His-CLGFP в зеленой области (Е485=63·103 M-1 см-1) [S.V. Markova, L.P. Burakova, L.A. Frank, S. Golz, K.A. Korostileva, E.S. Vysotski. Green-fluorescent protein from the bioluminescent jellyfish Clytia gregaria: cDNA cloning, expression, and characterization of novel recombinant protein // Photochem. Photobiol Sci. 9 (2010) 757-765].
Сорбент без введения катионов Ni2+ характеризуется сорбционной активностью в отношении белка, не превышающей 0,6 мг/г, которая, скорее всего, связана с участием ионов железа, вошедших в структуру мезопористого силиката в процессе синтеза в кислых условиях, способствующих выщелачиванию железа из магнитных микросфер в жидкую фазу. Для сравнения в таблице 2 приведены результаты сорбционной емкости сорбента, взятого за прототип.
После модифицирования поверхности образца нанесением катионов Ni2+ пропиткой 10%-ным раствором Ni(CH3COO)2 при соотношении 0,3 г микросфер: 1 мл раствора Ni(CH3COO)2 с последующим прокаливанием при 500°C в течение 4 часов (как в прототипе), адсорбционная емкость полученного сорбента ЕМТ1-H2O-Ni2+ составила 1,3 мг/г.
ПРИМЕР 2. Условия получения сорбента (EMT1-H2O-S, Ni2+) и тестирования те же, что и в примере 1, за исключением того, что модифицирование силикатного покрытия катионами Ni2+ проводят сорбцией из 10% водного раствора Ni(CH3COO)2 при перемешивании при 50°C в течение 8 часов с последующей сушкой и прокалкой при 500°C в течение 4 часов. Как следует из приведенных в таблице 2 данных, сорбент характеризуется низкой адсорбционной емкостью в отношении белка (0,7 мг/г), близкой к величине адсорбционной емкости композитного носителя без нанесения ионов никеля. Вероятно, это связано с низкой сорбцией катионов Ni2+ на поверхности микросфер и/или с инактивацией сорбированных форм Ni2+ за счет полного насыщения координационных связей Ni2+ при взаимодействии с силанольным покрытием.
ПРИМЕР 3. Получение сорбента (EMT1-HCl-Ni2+) и его тестирование проводят как в примере 1, кроме того, что активацию поверхности мезопористого покрытия осуществляют кипячением в 1М растворе HCl в течение 4-х часов.
ПРИМЕР 4. Получение сорбента EMT1-NH4 +-Ni2+, модифицирование поверхности и его тестирование проводили, как в примере 1, за исключением того, что активацию поверхности мезопористого покрытия микросфер осуществляют кипячением в 1М растворе NH4OH в течение 4 часов.
ПРИМЕР 5. Синтез мезопористого силикатного покрытия на поверхности микросфер проводят в аммиачно-спиртовом растворе в динамическом режиме в тефлоновом автоклаве в течение 2 часов при температуре 120°C с использованием реагентов в следующем мольном соотношении: 1 TEOS:0,2 HTABr:22 NH3:52 EtOH:475 H2O, при объемном соотношении твердая фаза:жидкая фаза = 1:20. Вращение автоклава, закрепленного перпендикулярно оси вала, осуществлялось со скоростью 30 об/мин. После проведения синтеза отделенную твердую фазу промывают, сушат при 80°C, затем прокаливают при 540°C в течение 4 часов. Активацию, модификацию SiO2-оболочки катионами Ni и тестирование проводят по методу, приведенному в примере 1.
ПРИМЕР 6. Получение сорбента (EMT4-H2O-Ni2+) включает те же стадии, что и в примере 5, за исключением того, что синтез мезопористого покрытия проводят в статическом режиме при температуре 80°C в течение 120 часов, а активацию, модификацию кремнеземной оболочки и тестирование проводят, как в примере 1.
ПРИМЕР 7. Получение сорбента (EMT-7-NH4+-Ni2+) проводят, как в примере 5, но при температуре 60°C в течение 72 часов. Активацию и модификацию кремнеземной оболочки проводят, как в примере 4, а тестирование сорбента, как в примере 1.
ПРИМЕР 8. Получение сорбента (EMT5-NH4 +-Ni2+) проводят, как в примере 5, только при температуре 80°C в течение 15 часов. Активацию и модификацию кремнеземной оболочки осуществляют по методу, описанному в примере 4. Тестирование сорбента проводят, как в примере 1.
ПРИМЕР 9. Получение сорбента (EMT8-NH4 +-Ni2+) проводят, как в примере 5, только при температуре 60°C в течение 15 часов. Активацию и модификацию силикатного покрытия проводят, как в примере 4, а тестирование - как в примере 1. Для элюирования адсорбированного белка, частицы промывают фосфатным буфером, содержащим 0,25 М имидазола. В результате целевой белок элюировался практически полностью. После обработки сорбента раствором имидазола количество белка, перешедшего в раствор, составило 4,3 мг/г сорбента. Наблюдаемые потери белка (0,1 мг/г) находятся в пределах ошибки определения.
Была исследована стабильность сорбционных свойств сорбента при многократном использовании, результаты приведены в таблице 3. Установлено, что адсорбционная емкость магнитного сорбента EMT8-NH4 +-Ni2+ сохранялась при 3-кратном использовании. После 7-кратного использования емкость снижалась в 1,5 раза. В аналогичных условиях адсорбционная емкость сорбента-прототипа уменьшалась в 5 раз. Стабильность сорбционных свойств в отношении зеленого флуоресцентного белка в многоцикловом сорбционном процессе свидетельствует о повышенной прочности силикатного покрытия по сравнению с сорбентом, полученным по способу-прототипу.
Приведенные примеры подтверждают возможность получения магнитного аффинного сорбента с иммобилизованными ионами Ni2+ в процессе синтеза, содержащем меньшее число стадий по сравнению со способом-прототипом. Достигнутым техническим результатом является также повышенная прочность силикатного покрытия и сопоставимая с сорбентом-прототипом адсорбционная емкость в отношении рекомбинантного белка размером 20-30 кДа (1,3-4,4 мг/г).
Реализация заявленного технического решения не ограничивается приведенными примерами. В качестве магнитного компонента могут быть использованы ферросферы других источников с высоким содержанием аморфной силикатной фазы. Высокое сродство сорбента к белкам, имеющим полигистидиновые последовательности, может быть обеспечено введением не только катионов никеля, но и других катионов переходных металлов, таких как Fe3+, Cu2+, Со2+, Zn2+. Гидротермальный синтез пористого силикатного покрытия может проводиться с использованием других органических структуроформирующих реагентов, требующих применения близких условий синтеза и последующей термической обработки.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ МЕЗОПОРИСТОГО ДИОКСИДА КРЕМНИЯ | 2009 |
|
RU2409423C1 |
| СПОСОБ КОНЦЕНТРИРОВАНИЯ И РАЗДЕЛЕНИЯ ФЛАВОНОИДОВ | 2016 |
|
RU2646805C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТЕРМОСТАБИЛЬНОГО МИКРОПОРИСТОГО ПОКРЫТИЯ НА ОСНОВЕ СМЕШАННОГО ОКСИДА ТИТАНА-КРЕМНИЯ | 2020 |
|
RU2733936C1 |
| ПОЛИДЕНТАТНЫЙ ФУНКЦИОНАЛЬНЫЙ МОНОМЕР N,O-ТИПА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ В МАТЕРИАЛЕ С ИОННЫМ ОТПЕЧАТКОМ | 2020 |
|
RU2839651C1 |
| КАТАЛИЗАТОР ПРЕВРАЩЕНИЯ УГЛЕВОДОРОДОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2005 |
|
RU2276621C1 |
| СПОСОБ ПОЛУЧЕНИЯ NaSn(PO) СО СТРУКТУРОЙ NASICON | 2021 |
|
RU2777643C1 |
| Способ получения наноструктурированного рентгеноаморфного сорбента цезия | 2023 |
|
RU2831541C1 |
| МИКРОПОРИСТАЯ МЕМБРАНА ДЛЯ МОЛЕКУЛЯРНОГО РАЗДЕЛЕНИЯ С ВЫСОКОЙ ГИДРОТЕРМАЛЬНОЙ СТАБИЛЬНОСТЬЮ | 2007 |
|
RU2424044C2 |
| Способ получения однофазного циркона | 2023 |
|
RU2819814C1 |
| СПОСОБ УСКОРЕННОГО ПОЛУЧЕНИЯ МЕЗОПОРИСТЫХ МЕЗОСТРУКТУРИРОВАННЫХ СИЛИКАТНЫХ МАТЕРИАЛОВ ТИПА МСМ-41 | 2005 |
|
RU2287485C1 |

Изобретение относится к получению сорбентов для выделения и детекции рекомбинантных белков, содержащих полигистидиновые последовательности. Предложен способ получения магнитного аффинного сорбента для выделения рекомбинантных белков. Способ включает нанесение пористого кремнеземного слоя на поверхность магнитных микросфер летучих зол от сжигания угля и пропитку раствором, содержащим ионы переходных металлов. В качестве микросфер используют фракцию магнитных микросфер, содержащую 40-41 мас.% стеклофазы. Нанесение пористого кремнеземного слоя осуществляют в гидротермальных условиях. Магнитные микросферы контактируют с жидкой реакционной смесью, содержащей тетраэтоксисилан и гексадецилтриаммоний бромид в качестве структуроформирующего агента. После нанесения кремнезёмного слоя твердую фазу отделяют, промывают, термообрабатывают и активируют при кипячении в водной среде. Изобретение позволяет повысить прочность кремнезёмной оболочки на поверхности микросфер без снижения сорбционной ёмкости по белкам среднего размера. 6 з.п. ф-лы, 2 ил., 3 табл., 9 пр.
1.Способ получения магнитного аффинного сорбента для выделения рекомбинантных белков, включающий нанесение пористого кремнеземного слоя на поверхность магнитных микросфер летучих зол от сжигания угля и последующую пропитку раствором, содержащим ионы переходных металлов, отличающийся тем, что в качестве микросфер используют фракцию магнитных микросфер, содержащую 40-41 мас.% стеклофазы, а нанесение пористого кремнеземного слоя осуществляют в гидротермальных условиях, подвергая микросферы контактированию с жидкой реакционной смесью, содержащей тетраэтоксисилан и гексадецилтриаммоний бромид в качестве структуроформирующего агента, с последующим выделением полученной твердой фазы, ее промывкой, термообработкой и активацией кипячением в водной среде.
2. Способ получения по п.1, отличающийся тем, что гидротермальный синтез проводят в водной кислой среде в статическом режиме при температуре 80°С в течение 120 часов при соотношении реагентов (мол.): 100 H2O:0,9 HCl:0,11 гексадецилтриметиламмоний бромид: 0,13 тетраэтоксисилан и объемном соотношении твердая фаза (микросферы):жидкая фаза = 1:20, а активацию поверхности микросфер проводят при кипячении в воде в течение 4 часов, либо в 1 М растворе соляной кислоты, либо в 1 М растворе гидроксида аммония.
3. Способ получения по п.1, отличающийся тем, что гидротермальный синтез проводят в аммиачно-спиртовой среде в динамическом режиме при температуре 120°С в течение 2 часов при соотношении реагентов (мол.): 1 тетраэтоксисилан:0,2 гексадецилтриметиламмоний бромид:22 NH3:52 этиловый спирт:475 H2O и объемном соотношении твердая фаза (микросферы):жидкая фаза = 1:20, а активацию поверхности микросфер проводят при кипячении в воде в течение 4 часов.
4. Способ получения по п.1, отличающийся тем, что гидротермальный синтез проводят в аммиачно-спиртовой среде в статическом режиме при температуре 80°С в течение 120 часов при соотношении реагентов (мол.): 1 тетраэтоксисилан:0,2 гексадецилтриметиламмоний бромид:22 NH3:52 этиловый спирт:475 Н2О и объемном соотношении твердая фаза (микросферы):жидкая фаза = 1:20, а активацию поверхности микросфер проводят при кипячении в воде в течение 4 часов.
5. Способ получения по п.1, отличающийся тем, что гидротермальный синтез проводят в аммиачно-спиртовой среде в статическом режиме при температуре 60°С в течение 72 часов при соотношении реагентов (мол.): 1 тетраэтоксисилан:0,2 гексадецилтриметиламмоний бромид:22 NH3:52 этиловый спирт: 475 H2O и объемном соотношении твердая фаза (микросферы):жидкая фаза=1:20, а активацию поверхности микросфер проводят при кипячении в 1 М растворе NH4OH в течение 4 часов.
6. Способ получения по п.1, отличающийся тем, что гидротермальный синтез проводят в аммиачно-спиртовой среде в динамическом режиме при температуре 80°С в течение 15 часов при соотношении реагентов (мол.): 1 тетраэтоксисилан:0,2 гексадецилтриметиламмоний бромид:22 NH3:52 этиловый спирт:475 Н2О и объемном соотношении твердая фаза (микросферы):жидкая фаза = 1:20, а активацию поверхности микросфер проводят при кипячении в 1 М растворе NH4OH в течение 4 часов.
7. Способ получения по п.1, отличающийся тем, что гидротермальный синтез проводят в аммиачно-спиртовой среде в динамическом режиме при температуре 60°С в течение 15 часов при соотношении реагентов (мол.):1 тетраэтоксисилан:0,2 гексадецилтриметиламмоний бромид:22 NH3:52 этиловый спирт:475 Н2О и объемном соотношении твердая фаза (микросферы):жидкая фаза = 1:20, а активацию поверхности микросфер проводят при кипячении в 1 М растворе NH4OH в течение 4 часов.
Авторы
Даты
2015-02-10—Публикация
2013-10-22—Подача