ПЕРЕКРЕСНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Данная заявка заявляет приоритет предварительной заявки США сер. №61/074464, поданной 20 июня 2008 года, раскрытие которой включено в данный документ по ссылке в ее полном объеме для каких-либо целей.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
[0002] Основной задачей разработки и превращения в источник прибыли лекарственных форм с контролируемым высвобождением для показаний, таких как сердечно-сосудистые заболевания, хроническая боль, ослабление мышечного спазма и связанные симптомы, особенно у пожилых людей, является доставка лекарственного средства так, чтобы поддерживать лекарственное средство в терапевтически эффективных концентрациях в течение длительного периода времени, что, таким образом, повышает степень согласия пациента с предписанным режимом и терапевтическую эффективность, что, таким образом, уменьшает как стоимость лечения, так и побочные эффекты.
[0003] Многие терапевтические средства наиболее эффективны, когда предоставляются при постоянной скорости в или поблизости места абсорбции. Абсорбция терапевтических средств, предоставляемая таким образом, обычно дает в результате необходимые концентрации в плазме, приводя к максимальной эффективности и минимальным побочным эффектам. Множество усилий было посвящено разработке систем доставки лекарственного средства на основе матричной таблетки и на основе капсулы с множеством частиц для пероральных применений.
[0004] Патент США №4839177, Colombo и др., принадлежащий Jagotec AG, относится, в общих чертах, к контролируемому высвобождению активных веществ, включая лекарственные препараты и какой-либо тип вещества, который должен высвобождаться при контролируемой скорости в жидкость на водной основе. Патент направлен на систему для высвобождения с контролируемой скоростью активных веществ, включающую ядро-хранилище, содержащее активное вещество и, по меньшей мере, одно из: (а) полимерный материал, обладающий высокой степенью набухания при контакте с водой, и желатинирующийся полимерный материал или (b) отдельный полимерный материал, обладающий свойствами как набухания, так и желатинирования, и опорную платформу, нанесенную на ядро-хранилище, где опорная платформа включает водонерастворимый полимерный материал.
[0005] Патенты США №4851228 и №4968507, оба Zentner и др., принадлежащие Merck & Company, относятся к осмотическому насосу множества частиц для контролируемого высвобождения фармацевтически активного средства, при этом каждый элемент осмотического насоса включает в основном ядро, содержащее активное средство и контролирующую скорость водонерастворимую стенку, содержащую полупроницаемый полимер и, по меньшей мере, одну нечувствительную к рН порообразующую добавку, диспергированную по стенке. Патент США №4590062, Jang, принадлежащий Tech Trade Corporation и патент США №4882167, Jang, направлены на спрессованный продукт, содержащий активную, полученную сухим смешиванием с матрицей комбинацию гидрофобного полимера (например, этилцеллюлозы) и воска, жирной кислоты, нейтрального липида или их сочетания.
[0006] Патент США №4996047, Kelleher, принадлежащий Richardson-Vicks, направлен на пероральную фармацевтическую композицию в стандартной лекарственной форме частиц ионообменной смолы, которые имеют связанное с ними фармакологически активное лекарственное средство, где частицы комплекса лекарственное средство-смола покрыты водонепроницаемым диффузионным барьером для обеспечения контролируемого высвобождения активного лекарственного средства. Патент США №5120548, McClelland и др., принадлежащий Merck & Company, направлен на устройство доставки лекарственного средства с контролируемым высвобождением, содержащее композицию полимера, который набухает при воздействии водного окружения, несколько модуляторов набухания с контролируемым высвобождением, по меньшей мере, одно активное средство и либо водонерастворимое полимерное покрытие, окружающее композицию, либо микропористую стенку, окружающую композицию. Патент США №5350584, McClelland и др, принадлежащий Merck & Company, относится к способу получения микрокристаллических, не содержащих целлюлозу множественных частиц, содержащих лекарственный препарат и заряженную смолу. Получаемые в результате сферонизированные гранулы можно применять в определенных лекарственных формах с контролируемым высвобождением.
[0007] Патент США №5366738, Rork и др., принадлежащий Merck & Company, направлен на устройство доставки лекарственного средства для контролируемого высвобождения активного средства. Устройство доставки лекарственного средства включает спрессованное ядро с активным средством и полимер, который при гидратации образует желатинозные микроскопические частицы и водонерастворимое, водонепроницаемое полимерное покрытие, содержащее полимер и пластификатор, который окружает ядро и прилипает к нему.
[0008] Патент США 5582838, Rork и др., принадлежащий Merck & Company, относится к устройству доставки лекарственного средства для контролируемого высвобождения целебного средства. Устройство доставки лекарственного средства включает спрессованное ядро, имеющее, по меньшей мере, два слоя: по меньшей мере, один слой представляет собой смесь целебного средства и полимера, который при гидратации образует микроскопические полимерные гелевые гранулы, и, по меньшей мере, один внешний слой содержит полимер, который при гидратации образует микроскопические полимерные гелевые гранулы. Водонерастворимое, водонепроницаемое покрытие наносят на ядро, и покрытие имеет отверстия, оставляя открытым приблизительно 5-75% поверхности ядра.
[0009] Патент США №5874418, Stella и др., принадлежащий Cydex, направлен на фармацевтическую композицию, содержащую носитель и смесь сульфоалкилового эфира-циклодекстрина и терапевтического средства, где основная доля терапевтического средства не связана в комплекс с сульфоалкилэфирным-циклодекстриновым производным. Также описываются составы с отсроченным, непрерывным или контролируемым высвобождением, где фармацевтическое ядро покрыто пленочным покрытием, содержащим пленкообразующее средство и порообразующее средство. Патент США №5882682, Rork и др., принадлежащий Merck & Company, направлен на способ доставки лекарственного средства, включающий этапы получения однородной смеси полимера, который при гидратации образует желатинозные микроскопические частицы, целебное средство и другие формообразующие, применяемые при получении ядра; прессования смеси в ядра; покрытия всего ядра водонерастворимым, водонепроницаемым полимерным покрытием, включающим полимер и пластификатор; и образования отверстий сквозь покрытие.
[0010] Патент США №5952451, Zhao, принадлежащий Guilford Pharmaceuticals, направлен на способ получения высокомолекулярных поли (фосфоэфирных) композиций, содержащих биологически активное вещество и поли (фосфоэфир), и высокомолекулярные композиции, полученные таким образом. Полученные таким образом полимеры пригодны в системах доставки лекарственного средства с пролонгированным высвобождением. Патент США №6004582, Faour и др., принадлежащий Laboratories Phoenix U.S.A., направлен на многослойное осмотическое устройство, содержащее спрессованное ядро, включающее первое активное средство и осмотическое средство, полупроницаемую мембрану, окружающую ядро и имеющую предварительно образованные в ней проходы, где мембрана является проницаемой для жидкости в окружающей среде применения и, по существу, непроницаемой для первого активного средства. Полупроницаемая мембрана предпочтительно состоит в основном из ацетилцеллюлозы и поли(этиленгликоля). Внешнее покрытие может включать поли(винилпирролидон) и поли(этиленгликоль) и может дополнительно включать материалы, такие как НРМС, этилцеллюлозу, гидроксилэтилцеллюлозу, CMC, сополимер диметиламиноэтилметакрилата и сложного эфира метакриловой кислоты, сополимер этилакрилата и метилметакрилата и их сочетания.
[0011] WO 99/18937, Kleinbart и др. (Merck & Company), направлена на композицию, содержащую фармацевтически эффективное количество циклобензаприна и водного двухосновного фосфата кальция, где таблетка высвобождает большую часть активного компонента в течение часа. WO 99/30671, Ron E.S., направлена на пероральную среду доставки, включающую аспектированную частицу, содержащую фармацевтически активный компонент и формообразующие, где среда составлена для обеспечения контролируемой доставки фармацевтически активного компонента. Среда может дополнительно содержать покрытие для обеспечения непрерывной доставки лекарственного средства к частице. WO 98/53802, Faour и др. (Laboratories Phoenix USA), направлена на многослойное осмотическое устройство, которое способно доставлять первое активное средство во внешнем тонком слое в одну среду применения, а второе активное средство в ядре - в другую среду применения. Разрушаемое полимерное покрытие между внутренней полупроницаемой мембраной и внешним покрытием, содержащим второе активное средство, содержит сополимер поли(винилпирролидон)а и винилацетат)а. Активное средство в ядре доставляется через пору, содержащую разрушаемую пробку.
[0012] WO 98/18610, Van Lengerich, направлена на частицы, содержащие активное средство, которые обеспечивают контролируемое высвобождение активного ингредиента без существенного разрушения материала матрицы. Компонент, контролирующий скорость высвобождения, включен в матрицу для контроля скорости высвобождения герметика из частицы. Гидрофобный компонент или компонент с высокой способностью связывать воду можно применять для увеличения времени высвобождения. Свойства высвобождения можно также контролировать предварительным покрытием герметика и/или покрытием частиц пленкообразующим компонентом. WO 98/06439, Oedemoed, (Osteotech), направлена на композицию, содержащую биологически активное средство, инкапсулированное в матрицу, содержащую сополимер полиэфира и сложного эфира, такой как сополимер полиэтиленгликоля терефталата/полибутилентерефталата. Сополимер полиэфира и сложного эфира защищает активное средство от разрушения и таким образом способствует доставке лекарственного средства.
[0013] Циклобензаприна гидрохлорид, миорелаксант скелетных мышц, является лекарственным средством центрального действия, которое уменьшает или прекращает избыточную тоническую мышечную активность при гипертонических, в отличие от фазических спастических, расстройствах. Flexeril® является циклобензаприновой композицией немедленного высвобождения в форме покрытой таблетки. Таблетки Flexeril® получают путем смешивания и прессованния циклобензаприна и формообразующих (лактоза, крахмал, стеарат магния и красящие вещества), затем покрытия полученной таблетки раствором водорастворимого, фармацевтически приемлемого полимера (гидроксипропилцеллюлоза/гидроксипропилметилцеллюлоза). Таблетки Flexeril® доступны в дозировках или 5 мг, или 10 мг, и, как правило, вводятся три раза в день для получения необходимого терапевтического эффекта. IR (немедленного высвобождения) таблетки Flexeril®, содержащие 10 мг циклобензаприна НСl, вводятся три раза в день для ослабления мышечного спазма локального происхождения без препятствования мышечной функции. Пероральное введение трижды в день является вопросом степени согласия пациента с предписанным режимом, особенно в отношении пожилых людей. Следовательно, существует необходимость в миорелаксанте скелетных мышц с модифицированным высвобождением, подходящем для введения один раз в день, особенно в лекарственных формах 15 мг и 30 мг для того, чтобы в значительной степени минимизировать межличностную вариабельность и улучшить качество жизни, особенно у пожилого населения.
[0014] К тому же, важно обладать технологией, которая воспроизводимо и согласованно обеспечивает фармацевтические лекарственные формы с определенными фармакокинетическими свойствами и характеристиками при реальных условиях транспортировки и хранения. Способ, который не способен последовательно предоставлять продукт, отвечающий утвержденным техническим требованиям, не является практичным для коммерческих целей. Продукты, не отвечающие техническим требованиям, должны быть отбракованы, так как они не гарантируют предоставление фармакокинетических качеств и качеств стабильности, которые утверждены контролирующими органами. Технологии, как правило, включают множество этапов, какой-либо один из которых может повлиять на фармакокинетические эксплуатационные характеристики полученного продукта.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0015] В одном варианте осуществления данное изобретение относится к способу получения фармацевтической композиции, включающему: а) получение гранул немедленного высвобождения (IR), включающих циклобензаприн или его фармацевтически приемлемую соль, сольват и/или сложный эфир; и b) покрытие IR гранул ER кроющей композицией, включающей фармацевтически приемлемый водонерастворимый полимер, в атмосфере с точкой росы в диапазоне приблизительно 5-20°С, с формированием, таким образом, ER гранул. В другом варианте осуществления способ дополнительно включает покрытие IR гранул этапа а) изолирующей кроющей композицией, включающей фармацевтически приемлемый водорастворимый полимер, перед указанным этапом b) ER покрытия.
[0016] В одном варианте осуществления данное изобретение относится к способу получения фармацевтической композиции, включающему: а) покрытие инертных частиц композицией наслаивания лекарственного средства, включающей циклобензаприн или его фармацевтически приемлемую соль, сольват и/или сложный эфир и фармацевтически приемлемый растворитель, с формированием, таким образом, гранул с наслоенным лекарственным средством; и b) покрытие IR гранул ER кроющей композицией, включающей фармацевтически приемлемый водонерастворимый полимер, в атмосфере с точкой росы в диапазоне приблизительно 5-20°С, с формированием, таким образом, ER гранул. В другом варианте осуществления способ дополнительно включает покрытие IR гранул этапа а) изолирующей кроющей композицией, включающей фармацевтически приемлемый водорастворимый полимер, перед указанным этапом b) ER покрытия.
[0017] В одном варианте осуществления данное изобретение относится к способу получения фармацевтической композиции, включающему: а) покрытие инертных частиц композицией наслаивания лекарственного средства, включающей циклобензаприн или его фармацевтически приемлемую соль, сольват и/или сложный эфир и фармацевтически приемлемый растворитель, с формированием, таким образом, гранул с наслоенным лекарственным средством; b) покрытие гранул с наслоенным лекарственным средством изолирующей кроющей композицией, включающей фармацевтически приемлемый водорастворимый полимер, с формированием, таким образом, IR гранул; и с) покрытие IR гранул ER кроющей композицией, включающей фармацевтически приемлемый водонерастворимый полимер, в атмосфере с точкой росы в диапазоне приблизительно 5-20°С, с формированием, таким образом, ER гранул.
[0018] В одном варианте осуществления данное изобретение относится к способу получения фармацевтической композиции, включающему: а) покрытие инертных частиц композицией наслаивания лекарственного средства, включающей циклобензаприн или его фармацевтически приемлемую соль, сольват и/или сложный эфир и фармацевтически приемлемый растворитель, с формированием, таким образом, гранул с наслоенным лекарственным средством; b) покрытие IR гранул ER кроющей композицией, включающей фармацевтически приемлемый водонерастворимый полимер, в атмосфере с точкой росы в диапазоне приблизительно 5-20°С, с формированием, таким образом, ER гранул; и с) выдерживание ER гранул при приблизительно 60°С в течение приблизительно 4-12 часов в атмосфере с точкой росы в диапазоне приблизительно 5-20°С.
[0019] В одном варианте осуществления данное изобретение относится к способу получения фармацевтической композиции, включающему покрытие приблизительно 20-25 меш инертных частиц композицией наслаивания лекарственного средства, содержащий циклобензаприн или его фармацевтически приемлемую соль, сольват и/или сложный эфир и фармацевтически приемлемый растворитель, например водный органический растворитель; высушивание покрытых инертных частиц с формированием, таким образом, гранул с наслоенным лекарственным средством; покрытие гранул с наслоенным лекарственным средством изолирующей кроющей композицией, включающей фармацевтически приемлемый водорастворимый полимер и воду; высушивание покрытых гранул с наслоенным лекарственным средством с формированием, таким образом, IR гранул; и покрытие IR гранул ER кроющей композицией, включающей фармацевтически приемлемый водонерастворимый полимер, в атмосфере с точкой росы в диапазоне приблизительно 5-20°С, с формированием, таким образом, ER гранул. В другом варианте осуществления данный способ направлен на способ получения фармацевтической композиции, включающий покрытие приблизительно 20-25 меш инертных частиц композицией наслаивания лекарственного средства с содержанием твердых веществ приблизительно 25 вес.%, содержащей циклобензаприн или его фармацевтически приемлемые соли, сольваты и/или сложные эфиры и водный органический растворитель; высушивание покрытых инертных частиц с формированием, таким образом, гранул с наслоенным лекарственным средством; покрытие гранул с наслоенным лекарственным средством изолирующей кроющей композицией с содержанием твердых веществ приблизительно 8-10 вес.%, содержащей фармацевтически приемлемый водорастворимый полимер и воду; высушивание покрытых гранул с наслоенным лекарственным средством с формированием, таким образом, IR гранул (например, загрузка лекарственного средства: 25 процентного соотношения веса); покрытие IR гранул ER кроющей композицией с содержанием твердых веществ приблизительно 6 вес.%, содержащей фармацевтически приемлемый водонерастворимый полимер и факультативный пластификатор; высушивание покрытых IR гранул в атмосфере с точкой росы в диапазоне приблизительно 5-20°С с формированием, таким образом, ER гранул; и факультативно выдерживание просеянных ER гранул при приблизительно 60°С в течение до приблизительно 4 часов в атмосфере с точкой росы в диапазоне приблизительно 5-20°С.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[0020] Данное изобретение будет описано более детально со ссылкой на прилагаемые Фигуры, где:
[0021] ФИГ.1 показывает предполагаемый целевой профиль высвобождения для MR (модифицированного высвобождения) капсул циклобензаприна гидрохлорида.
[0022] ФИГ.2 показывает смоделированный уровень в плазме на День 1 после дозирования 1×10 мг Flexeril®, который давали 3 раза в день, и 1×30 мг MR капсулы циклобензаприна НСl, которую давали раз в день.
[0023] ФИГ.3 показывает блок-схему способа производства MR капсул циклобензаприна НСl.
[0024] ФИГ.4 показывает профили концентрация в плазме - время капсул модифицированного высвобождения (MR) циклобензаприна НСl, 30 мг, против Fexeril (таблетки немедленного высвобождения (IR) циклобензаприна НСl, 10 мг) × трижды в день, протестированные в базовом РК клиническом исследовании.
[0025] ФИГ.5 показывает действительные и смоделированные in-vitro профили высвобождения для CMR 30 мг (смоделированный профиль получили с помощью РК параметров, полученных из клинического исследования).
[0026] ФИГ.6 показывает профили высвобождения лекарственного средства капсул модифицированного высвобождения (MR) циклобензаприна НСl, 30 мг, хранящегося в загерметизированных от индукции HDPE бутылках при 40°С/75%ОВ.
ДЕТАЛЬНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0027] Все документы, процитированные в данном документе, включены по ссылке в их полном объеме для каких-либо целей. Цитирование какого-либо документа не следует истолковывать как признание того, что это известный уровень техники по отношению к данному изобретению.
[0028] Выражения "лекарственное средство", "активное", "активный фармацевтический ингредиент" и т.д. применяются взаимозаменяемо.
[0029] Все ссылки на конкретное лекарственное средство или активное в данном документе включают их фармацевтически приемлемые соли, сольваты, сложные эфиры, изомеры и т.д., если явно не указано иное.
[0030] В своих различных вариантах осуществления данное изобретение направлено на способы получения фармацевтических композиций, как описано в данном документе, т.е. способы получения пероральных лекарственных форм миорелаксантов скелетных мышц, например циклобензаприна.
[0031] В одном варианте осуществления данное изобретение относится к способу получения фармацевтической композиции, включающему: а) получение гранул немедленного высвобождения (IR), включающих циклобензаприн или его фармацевтически приемлемую соль, сольват и/или сложный эфир; и b) покрытие IR гранул ER кроющей композицией, включающей фармацевтически приемлемый водонерастворимый полимер, в атмосфере с точкой росы в диапазоне приблизительно 5-20°С, с формированием, таким образом, ER гранул. В другом варианте осуществления способ дополнительно включает покрытие IR гранул этапа а) изолирующей кроющей композицией, включающей фармацевтически приемлемый водорастворимый полимер, перед указанным этапом b) ER покрытия.
[0032] В одном варианте осуществления, данное изобретение относится к способу получения фармацевтической композиции, включающему: а) покрытие инертных частиц композицией наслаивания лекарственного средства, включающей циклобензаприн или его фармацевтически приемлемую соль, сольват и/или сложный эфир и фармацевтически приемлемый растворитель, с формированием, таким образом, гранул с наслоенным лекарственным средством; и b) покрытие IR гранул ER кроющей композицией, включающей фармацевтически приемлемый водонерастворимый полимер, в атмосфере с точкой росы в диапазоне приблизительно 5-20°С, с формированием, таким образом, ER гранул. В другом варианте осуществления способ дополнительно включает покрытие IR гранул этапа а) изолирующей кроющей композицией, включающей фармацевтически приемлемый водорастворимый полимер, перед указанным этапом b) ER покрытия.
[0033] В одном варианте осуществления данное изобретение относится к способу получения фармацевтической композиции, включающему: а) покрытие инертных частиц композицией наслаивания лекарственного средства, включающей циклобензаприн или его фармацевтически приемлемую соль, сольват и/или сложный эфир и фармацевтически приемлемый растворитель, с формированием, таким образом, гранул с наслоенным лекарственным средством; b) покрытие гранул с наслоенным лекарственным средством изолирующей кроющей композицией, включающей фармацевтически приемлемый водорастворимый полимер, с формированием, таким образом, IR гранул; и с) покрытие IR гранул ER кроющей композицией, включающей фармацевтически приемлемый водонерастворимый полимер, в атмосфере с точкой росы в диапазоне приблизительно 5-20°С, с формированием, таким образом, ER гранул. В одном варианте осуществления инертные частицы имеют размер частиц приблизительно 20-25 меш. В другом варианте осуществления фармацевтически приемлемый растворитель в композиции наслаивания лекарственного средства включает водный органический растворитель. В другом варианте осуществления изолирующая кроющая композиция дополнительно включает воду в качестве растворителя.
[0034] В одном варианте осуществления данное изобретение относится к способу получения фармацевтической композиции, включающему: а) покрытие инертных частиц композицией наслаивания лекарственного средства, включающей циклобензаприн или его фармацевтически приемлемую соль, сольват и/или сложный эфир и фармацевтически приемлемый растворитель, с формированием, таким образом, гранул с наслоенным лекарственным средством; b) покрытие IR гранул ER кроющей композицией, включающей фармацевтически приемлемый водонерастворимый полимер, в атмосфере с точкой росы в диапазоне приблизительно 5-20°С, с формированием, таким образом, ER гранул; и с) выдерживание ER гранул при приблизительно 60°С в течение приблизительно 4-12 часов в атмосфере с точкой росы в диапазоне приблизительно 5-20°С.
[0035] В одном варианте осуществления данное изобретение относится к способу получения фармацевтической композиции, включающему: а) покрытие инертных частиц композицией наслаивания лекарственного средства, включающей циклобензаприн или его фармацевтически приемлемую соль, сольват и/или сложный эфир и фармацевтически приемлемый растворитель, с формированием, таким образом, гранул с наслоенным лекарственным средством; b) покрытие гранул с наслоенным лекарственным средством изолирующей кроющей композицией, включающей фармацевтически приемлемый водорастворимый полимер, с формированием, таким образом, IR гранул; и с) покрытие IR гранул ER кроющей композицией, включающей фармацевтически приемлемый водонерастворимый полимер, в атмосфере с точкой росы в диапазоне приблизительно 5-20°С, с формированием, таким образом, ER гранул. В еще одном варианте осуществления данное изобретение дополнительно включает выдерживание ER гранул из вышеупомянутого этапа с) при приблизительно 60°С в атмосфере с точкой росы в диапазоне приблизительно 5-20°С. Процесс выдерживания может осуществляться в течение приблизительно 12 часов, приблизительно 10 часов, приблизительно 8 часов, приблизительно 6 часов, приблизительно 4 часов или приблизительно 2 часов.
[0036] В другом варианте осуществления данное изобретение дополнительно включает этап высушивания после формирования гранулы с наслоенным лекарственным средством. Например, способ включает получение фармацевтической композиции, при котором включает: (а) покрытие инертных частиц композицией наслаивания лекарственного средства, включающей циклобензаприн или его фармацевтически приемлемую соль, сольват и/или сложный эфир и фармацевтически приемлемый растворитель, с формированием, таким образом, гранул с наслоенным лекарственным средством; (а1) высушивание гранул с наслоенным лекарственным средством; (b) покрытие гранул с наслоенным лекарственным средством изолирующей кроющей композицией, включающей фармацевтически приемлемый водорастворимый полимер, с формированием, таким образом, IR гранул; и (с) покрытие IR гранул ER кроющей композицией, включающей фармацевтически приемлемый водонерастворимый полимер, в атмосфере с точкой росы в диапазоне приблизительно 5-20°С, с формированием, таким образом, ER гранул. В другом варианте осуществления этап высушивания (а1) осуществляют в атмосфере с точкой росы в диапазоне приблизительно 5-20°С.
[0037] В другом варианте осуществления данное изобретение дополнительно содержит этап высушивания после формирования IR гранул. Например, способ включает получение фармацевтической композиции, при котором включает: (а) покрытие инертных частиц композицией наслаивания лекарственного средства, включающей циклобензаприн или его фармацевтически приемлемую соль, сольват и/или сложный эфир и фармацевтически приемлемый растворитель, с формированием, таким образом, гранул с наслоенным лекарственным средством; (b) покрытие гранул с наслоенным лекарственным средством изолирующей кроющей композицией, включающей фармацевтически приемлемый водорастворимый полимер, с формированием, таким образом, IR гранул; (b1) высушивание IR гранул; и (с) покрытие IR гранул ER кроющей композицией, включающей фармацевтически приемлемый водонерастворимый полимер, в атмосфере с точкой росы в диапазоне приблизительно 5-20°С, с формированием, таким образом, ER гранул. В другом варианте осуществления этап высушивания (Ы) проводят в атмосфере с точкой росы в диапазоне приблизительно 5-20°С.
[0038] В другом варианте осуществления данное изобретение дополнительно включает этап высушивания после формирования ER гранул. Например, способ включает получение фармацевтической композиции, при котором включает: (а) покрытие инертных частиц композицией наслаивания лекарственного средства, включающей циклобензаприн или его фармацевтически приемлемую соль, сольват и/или сложный эфир и фармацевтически приемлемый растворитель, с формированием, таким образом, гранул с наслоенным лекарственным средством; (b) покрытие гранул с наслоенным лекарственным средством изолирующей кроющей композицией, включающей фармацевтически приемлемый водорастворимый полимер, с формированием, таким образом, IR гранул; и (с) покрытие IR гранул ER кроющей композицией, включающей фармацевтически приемлемый водонерастворимый полимер, в атмосфере с точкой росы в диапазоне приблизительно 5-20°С; (с1) высушивание покрытых гранул немедленного высвобождения, с формированием, таким образом, ER гранул.
[0039] В одном варианте осуществления данное изобретение относится к способу получения фармацевтической композиции, включающему: (а) покрытие приблизительно 20-25 меш инертных частиц композицией наслаивания лекарственного средства, включающей циклобензаприн или его фармацевтически приемлемую соль, сольват и/или сложный эфир и водный органический растворитель; b) высушивание покрытых инертных частиц с формированием, таким образом, гранул с наслоенным лекарственным средством; с) покрытие гранул с наслоенным лекарственным средством изолирующей кроющей композицией, включающей фармацевтически приемлемый водорастворимый полимер и воду; d) высушивание покрытых гранул с наслоенным лекарственным средством с формированием, таким образом, IR гранул; е) покрытие IR гранул ER кроющей композицией, включающей фармацевтически приемлемый водонерастворимый полимер; f) высушивание покрытых гранул немедленного высвобождения в атмосфере с точкой росы в диапазоне приблизительно 5-20°С с формированием, таким образом, ER гранул.
[0040] В одном варианте осуществления фармацевтически приемлемые инертные частицы сначала покрывают композицией наслаивания лекарственного средства. Неограничивающие примеры подходящих фармацевтически приемлемых частиц включают сахарные сферы или гранулы (например, Celphere®), целлюлозные сферы, сферы из диоксида кремния, частицы кислого буфера, частицы щелочного буфера, или подобные, с подходящим размером частиц или распределением размеров частиц, например, приблизительно 20-25 меш. В одном варианте осуществления инертные частицы представляют собой сахарные гранулы (зерна нонпарель) с размером частиц приблизительно 20-25 меш. В другом варианте осуществления частицы, включающие лекарственное средство, можно получить гранулированием и размалыванием, контролируемым сферонизацией в Granurex 40 или грануляцией и экструзией/сферонизацией для формирования IR пеллет.
[0041] Композиция наслаивания лекарственного средства содержит лекарственное средство (например, циклобензаприн и фармацевтически приемлемые соли, сольваты и/или их сложные эфиры), растворенное или диспергированное в водно- органическом растворителе. Неограничивающие водные органические растворители включают водные кетоны или водные спирты, например водный ацетон. В одном варианте осуществления водный органический растворитель представляет собой 1:1 вода/ацетон, и лекарственное средство представляет собой циклобензаприна гидрохлорид, например, растворенный до содержания твердых веществ приблизительно 25 вес.%.
[0042] В других вариантах осуществления композиция наслаивания лекарственного средства дополнительно содержит факультативное связующее вещество, например фармацевтически приемлемый водорастворимый полимер, такой как поливинилпирролидон (PVP), карбоксиалкилцеллюлозы, полиэтилена оксид, полисахариды, такие как декстран, кукурузный крахмал, целлюлозные производные, такие как гидроксипропилметилцеллюлоза (НРМС) и гидроксипропилцеллюлоза. В одном варианте осуществления композиция наслаивания лекарственного средства содержит связующее вещество, как описано в данном документе. В другом варианте осуществления композиция наслаивания лекарственного средства не содержит связующее вещество.
[0043] Вес покрытия композиции наслаивания лекарственного средства (т.е. вес твердых веществ, растворенных в водном органическом растворителе, размещенном на инертных частицах, выраженный как повышение весового процента гранул после покрытия и высушивания) может варьировать в зависимости от необходимой дозировки лекарственного средства и может варьировать в диапазоне от приблизительно 5 вес.% до приблизительно 30 вес.%, включая приблизительно 5 вес.%, приблизительно 10 вес.%, приблизительно 15 вес.%, приблизительно 20 вес.%, приблизительно 25 вес.% или приблизительно 30 вес.%. В одном варианте осуществления вес покрытия композиции наслаивания лекарственного средства составляет приблизительно 25 вес.%.
[0044] Композицию наслаивания лекарственного средства можно наносить каким-либо подходящим способом, включая аппарат псевдоожиженного слоя для нанесения покрытий непрерывного или периодического типа, такой как выпускаемый Glatt. Например, наслаивание лекарственного средства можно проводить на Glatt GPCC 120, оснащенном 18 дюймовой вставкой Wurster для нанесения снизу вверх (например, с помощью воздушного пароприемного листа типа "С" с 1,5 мм отверстиями в центре и 2,0 мм отверстиями, которые по наружной окружности, или воздушного пароприемного листа типа "D" с 2,0 мм отверстиями в центре и 3,5 мм на наружной окружности). Аппаратом псевдоожиженного слоя для нанесения покрытий можно управлять при каких-либо подходящих условиях, которые минимизируют спекание гранул с наслоенным лекарственным средством во время покрытия и которые обеспечивают вес покрытия, описанный в данном документе. Например, высота сектора от пароприемного листа может составлять приблизительно 53 мм, варьируя в диапазоне от приблизительно 45 мм до приблизительно 55 мм. В одном варианте осуществления, высота сектора от пароприемного листа составляет приблизительно 53±2 мм. Аналогично, скорость, при которой композиция наслаивания лекарственного средства распыляется на инертные частицы, и объем технологического воздуха (и другие рабочие параметры) можно модифицировать, например, для получения необходимого веса покрытия. Например, в одном варианте осуществления скорость распыления варьирует в диапазоне от 100 г/мин до приблизительно 400 г/мин, а объем технологического воздуха варьирует в диапазоне приблизительно 800-1500 куб. фут/мин.
[0045] В одном варианте осуществления высушенные гранулы с наслоенным лекарственным средством можно затем покрыть изолирующей кроющей композицией, например, для улучшения механической прочности гранул с наслоенным лекарственным средством. Можно применять какую-либо подходящую изолирующую кроющую композицию, которая не препятствует свойствам покрытия продолжительного высвобождения, добавляемого в последующих этапах. Подходящие изолирующие покрывающие композиции содержат фармацевтически приемлемый водорастворимый полимер, растворенный или диспергированный в воде. Неограничивающие примеры водорастворимых полимеров включают полиэтиленгликоль, гидроксипропилметилцеллюлозу, гидроксипропилцеллюлозу, гидроксиэтилцеллюлозу, метилцеллюлозу, поливинилпирролидон и их смеси. В одном варианте осуществления водорастворимым полимером является гидроксипропилметилцеллюлоза (например, Opadry® Clear). Содержание твердых веществ изолирующей кроющей композиции может варьировать в диапазоне от приблизительно 2 вес.% до приблизительно 10 вес.%, например приблизительно 2 вес.%, приблизительно 3 вес.%, приблизительно 4 вес.%, приблизительно 5 вес.%, приблизительно 6 вес.%, приблизительно 7 вес.%, приблизительно 8 вес.%, приблизительно 9 вес.% или приблизительно 10 вес.%. В одном варианте осуществления содержание твердых веществ изолирующей кроющей композиции составляет приблизительно 8-10 вес.%. В другом варианте осуществления содержание твердых веществ изолирующей кроющей композиции составляет приблизительно 8 вес.%.
[0046] В одном варианте осуществления этап изолирующего покрытия можно осуществить, например, с помощью аппарата псевдоожиженного слоя для нанесения покрытий, как описано в данном документе, и можно высушить при подходящих условиях, например, в аппарате псевдоожиженного слоя для нанесения покрытий при температурных условиях, как описано в данном документе. Например, изолирующую кроющую композицию можно нанести до скорости распыления приблизительно 200 г/мин и высушить при температуре продукта, варьирующей в диапазоне от приблизительно 35°С до приблизительно 60°С. В одном варианте осуществления температура продукта составляет приблизительно 42°С. Получаемые покрытые изоляцией гранулы с наслоенным лекарственным средством затем называют гранулы "немедленного высвобождения" (IR) по причине того, что лекарственное средство высвобождается по существу немедленно после растворения или введения.
[0047] После наслаивания композицией наслаивания лекарственного средства получаемые гранулы с наслоенным лекарственным средством высушивают для удаления водного органического растворителя. Можно применять какие-либо подходящие условия высушивания, которые не разрушают лекарственное средство (например, циклобензаприн или его фармацевтически приемлемые соли, сольваты и/или сложные эфиры). Например, гранулы с наслоенным лекарственным средством можно высушить в аппарате для нанесения покрытий (например, аппарате псевдоожиженного слоя для нанесения покрытий, таком как устройство псевдоожиженного слоя для нанесения покрытий Glatt, оснащенном вставкой Wurster). Подходящие температуры высушивания составляют приближенно 50°С, например в диапазоне от приблизительно 45°С до приблизительно 55°С.
[0048] При необходимости после высушивания IR гранулы можно факультативно "отсортировать по величине" для удаления мелких фракций (т.е. очень мелких частиц) или агломератов. Например, IR гранулы можно "просеять" с помощью 14-меш и 24-меш сит для удаления нежелательных и превышающих размер частиц.
[0049] IR гранулы затем покрывают кроющей композицией "продолжительного высвобождения" (ER), включающей фармацевтически приемлемый водонерастворимый полимер. Неограничивающие примеры подходящих фармацевтически приемлемых водонерастворимых полимеров включают воски, водонерастворимые производные целлюлозы (например, этилцеллюлоза, простые эфиры целлюлозы, сложные эфиры целлюлозы, ацетилцеллюлоза, бутираты целлюлозы, пропионат целлюлозы, сложные эфиры целлюлозы и этилцеллюлозы и т.д.), высокомолекулярную гидроксипропилметилцеллюлозу с вязкостью 2 вес.% водного раствора 3000-5600 сП или выше, ацилированные полисахариды, полиуретаны, поливинилацетат (например, Kollicoat SR30D от BASF), полиакрилатные и полиметакрилатные полимеры и производные, нейтральные сополимеры, содержащие повторяющиеся единицы этилакрилата и/или метилметакрилата (такие как Eudragit NE), нечувствительные к рН сополимеры аммонио и метакриловой кислоты, водонерастворимые сополимеры сложных эфиров акриловой и метакриловой кислот с группами четвертичного аммония, такие как Eudragit RS, RS30D, RL или RL30D и подобное, и их сочетания. Водонерастворимые полимеры в ER кроющих композициях можно пластифицировать или не пластифицировать.
[0050] В другом варианте осуществления данного изобретения ER кроющая композиция содержит водонерастворимый полимер и пластификатор. Неограничивающие примеры подходящих пластификаторов включают глицерин и его сложные эфиры (например, ацетилированные моно- или диглицериды, включая коммерчески доступный Myvacet® 9-45), глицерилмоностеарат, глицерилтриацетат, глицерилтрибутират, дибутилфталат, диэтилфталат, диметилфталат, диоктилфталат, сложный трибутиловый эфир ацетиллимонной кислоты, сложный триэтиловый эфир ацетиллимонной кислоты, трибутилцитрат, ацетилтрибутилцитрат, триэтилцитрат, глицеринтрибутират; диэтилсебацат, дибутилсебацат, дибутиладипаты, дибутилазелаинаты, дибутилбензоаты, хлорбутанол, полиэтиленгликоли растительные масла, диэтилфумарат, диэтилмалаты, диэтилоксалат, дибутилсукцинат, дибутилбутират, сложные эфиры цетилового спирта, диэтилмалонат, касторовые масла, полисорбаты, N-бутилбензенсульфонамид, N-метилпирролидон и их смеси. Пластификатор может содержать приблизительно 3-30 вес.% (например, приблизительно 3 вес.%, приблизительно 5 вес.%, приблизительно 10 вес.%, приблизительно 15 вес.%, приблизительно 20 вес.%, приблизительно 25 вес.% или приблизительно 30 вес.%) и более типично приблизительно 10-25 вес.% ER покрытия (относительно количества водонерастворимого полимера).
[0051] ER кроющая композиция может быть в форме раствора (например, водонерастворимого полимера и факультативного пластификатора в подходящем фармацевтически приемлемом растворителе) или в форме дисперсии (например, водонерастворимого полимера и/или факультативного пластификатора в подходящей фармацевтически приемлемой жидкости). В одном варианте осуществления ER кроющая композиция содержит водную дисперсию этилцеллюлозы и пластификатор (например, дибутилсебацат). В другом варианте осуществления ER кроющая композиция содержит раствор этилцеллюлозы (например, Ethocel Premium Standard 10 сП) и пластификатор (например, диэтилфталат) в ацетоне/воде. В еще одном варианте осуществления ER покрытие содержит раствор этилцеллюлозы и диэтилфталата в 98:2 ацетон:вода. В еще одном варианте осуществления ER покрытие содержит приблизительно 90% этилцеллюлозы и приблизительно 10 вес.% диэтилфталата. В еще одном другом варианте осуществления ER кроющая композиция содержит раствор этилцеллюлозы и диэтилфталата в смеси ацетон:вода, содержащей приблизительно от 85 вес.% до 98 вес.% ацетона и от 15 вес.% до 2 вес.% воды, включая весовые соотношения ацетон/вода приблизительно 88/12, приблизительно 90/10, приблизительно 92/8 и приблизительно от 95/5 до приблизительно 98/2. В еще одном дополнительном варианте осуществления ER кроющая композиция содержит раствор этилцеллюлозы и диэтилфталата в приблизительно 98:2 ацетон: вода. В другом варианте осуществления ER кроющая композиция содержит раствор этилцеллюлозы в приблизительно 98:2 ацетоне.
[0052] Содержание твердых веществ ER кроющей композиции может варьировать от приблизительно 5 вес.% до приблизительно 10 вес.%. В одном варианте осуществления содержание твердых веществ ER кроющей композиции составляет приблизительно 6-7 вес.%. В еще одном варианте осуществления содержание твердых веществ ER кроющей композиции составляет приблизительно 6,5 вес.%. В еще другом варианте осуществления ER кроющая композиция содержит раствор этилцеллюлозы и диэтилфталата в ацетон/вода с приблизительно 6 вес.% содержанием твердых веществ.
[0053] ER кроющую композицию получают перемешиванием смеси фармацевтически приемлемого водонерастворимого полимера, как описано в данном документе (например, этилцеллюлозы), факультативно пластификатора, как описано в данном документе, и фармацевтически приемлемого растворителя (как описано в данном документе, например, водного органического растворителя). В одном варианте осуществления ER кроющую композицию получают перемешиванием смеси фармацевтически приемлемого водонерастворимого полимера (например, этилцеллюлозы), пластификатора (например, диэтилфталата) и фармацевтически приемлемого растворителя (например, ацетон/вода), где получаемый раствор перемешивают после добавления пластификатора в течение до 8 часов, но не менее чем одного часа (например, в течение приблизительно 1-2 часов, в течение приблизительно 2-6 часов, в течение приблизительно 3-4 часов или приблизительно 1 час) для обеспечения необходимой гомогенизации.
[0054] Этап покрытия ER композицией можно осуществить, например, с помощью аппарата псевдоожиженного слоя для нанесения покрытий при скорости распыления приблизительно 75-700 г/мин, используя объем технологического воздуха 700-1500 куб. фут/мин. Покрытые ER гранулы можно высушить при подходящих условиях, например, в аппарате псевдоожиженного слоя для нанесения покрытий при температурных и влажностных условиях, как описано в данном документе, например при температуре продукта 27-40°С (как правило, 33-34°С в установившемся состоянии) и точке росы приблизительно 5-20°С (включая приблизительно 5°С, приблизительно 6°С, приблизительно 7°С, приблизительно 8°С, приблизительно 9°С, приблизительно 10°С, приблизительно 11°С, приблизительно 12°С, приблизительно 13°С, приблизительно 14°С, приблизительно 15°С, приблизительно 16°С, приблизительно 17°С, приблизительно 18°С, приблизительно 19°С или приблизительно 20°С, включающие все значения, диапазоны и поддиапазоны между ними; как правило, 10°С в установившемся состоянии).
[0055] При необходимости после высушивания ER гранулы можно факультативно "отсортировать по величине" для удаления мелких фракций (т.е. очень мелких частиц) или агломератов. Например, ER гранулы можно "просеять" с помощью 14-меш и 24-меш сит для удаления нежелательных и превышающих размер частиц.
[0056] Факультативно, выдерживание или дополнительное высушивание ER гранул можно осуществить, например, в традиционной сушилке, конкретнее - в лотковом сушильном шкафу. Также можно применять другие способы высушивания или выдерживания, известные в данном уровне техники (например, высушивание под потоком газа). В одном варианте осуществления ER гранулы высушивают в точке росы, определенной для придания необходимого профиля высвобождения лекарственного средства (например, через 2 часа высвобождается не более чем приблизительно 40% общего активного; через 4 часа высвобождается от приблизительно 40-65% общего активного; через 8 часов высвобождается от приблизительно 60-85% общего активного; и факультативно через 12 часов высвобождается от приблизительно 75-85% общего активного). В другом варианте осуществления ER гранулы высушивают в точке росы приблизительно 5-20°С (включая приблизительно 5°С, приблизительно 6°С, приблизительно 7°С, приблизительно 8°С, приблизительно 9°С, приблизительно 10°С, приблизительно 11°С, приблизительно 12°С, приблизительно 13°С, приблизительно 14°С, приблизительно 15°С, приблизительно 16°С, приблизительно 17°С, приблизительно 18°С, приблизительно 19°С или приблизительно 20°С, включая все значения, диапазоны и поддиапазоны между ними), например приблизительно 6-17°С или приблизительно 8-10°С. Какой-либо соответственно оснащенный аппарат для высушивания может применяться для высушивания при условиях с контролируемой точкой росы. Например, в аппарат для высушивания можно добавить установку кондиционирования, которая отслеживает и регулирует точку росы. Другой подходящий способ включает применение сушильного газа, высушенного с помощью какого-либо аппарата для высушивания/удаления влаги, где сушильный газ высушивают до необходимой точки росы.
[0057] Более низкая точка росы коррелирует с более сухим воздухом. Таким образом, альтернативно, процесс высушивания можно отслеживать и регулировать для поддержания необходимой относительной влажности. В другом варианте осуществления ER гранулы высушивают при относительной влажности, определенной для придания необходимого профиля высвобождения лекарственного средства (например, через 2 часа высвобождается не более чем приблизительно 40% общего активного; через 4 часа высвобождается от приблизительно 40-65% общего активного; через 8 часов высвобождается от приблизительно 60-85% общего активного; и факультативно через 12 часов высвобождается от приблизительно 75-85% общего активного). В другом варианте осуществления ER гранулы высушивают при относительной влажности приблизительно 0-20%, включая приблизительно 2-10% и приблизительно 4-8% при атмосферном давлении.
[0058] К тому же время и температуры высушивания или выдерживания можно варьировать до тех пор, пока условия производят ER гранулы с необходимым профилем высвобождения лекарственного средства. В одном варианте осуществления температура выдерживания составляет приблизительно 60°С±5°С. Также можно применять другие температуры выдерживания, такие как приблизительно 50±5°С. Аналогично, время выдерживания может варьировать, включая, например, до 24 часов, приблизительно 2-24 часа, приблизительно 2-12 часов, приблизительно 2-6 часов и приблизительно 4 часа. В одном варианте осуществления ER гранулы выдерживают при приблизительно 60°С в течение приблизительно 4 часов. В другом варианте осуществления ER гранулы выдерживают при псевдоожижении при температуре внутреннего воздуха приблизительно 60°С в течение приблизительно 15 минут в собственно устройстве псевдоожиженного слоя.
[0059] ER гранулы, полученные, как описано выше, имеют профиль высвобождения лекарственного средства при тестировании с помощью Аппарата 2 по Фармакопее США (перемешивает при 50 rpm (оборотов в минуту)) в 900 мл 0,1 N НСl (или подходящей среде для растворения) при 37°С, в основном соответствующий следующей схеме: через 2 часа высвобождается не более чем приблизительно 40% общего активного;
через 4 часа высвобождается от приблизительно 40-65% общего активного;
через 8 часов высвобождается от приблизительно 60-85% общего активного;
и
факультативно через 12 часов высвобождается от приблизительно 75-85% общего активного.
[0060] Если IR гранулы покрывают ER кроющей композицией при условиях покрытия (например, в аппарате псевдоожиженного слоя для нанесения покрытий), в которых температуру и влажность поддерживают для обеспечения точки росы приблизительно 5-20°С, и факультативно выдерживают в точке росы приблизительно 5-20°С (например, 7-16°С), получаемые ER гранулы проявляют улучшенные свойства стабильности. Например, ER гранулы из коммерческих капсул, полученные таким образом и упакованные в бутылки, подвергнутые условиям теста долговременной стабильности (например, при 25% ОВ после хранения в течение до 48 месяцев), постоянно обеспечивают в основном равномерные профили растворения при тестировании в условиях in vitro. В одном варианте осуществления ER гранулы, полученные таким образом, обеспечивают профили растворения, где концентрация лекарственного средства не отклоняется на более чем 10% в любой момент времени, измеренная по сравнению с изначальным профилем растворения через приблизительно 3 месяца, 6 месяцев, 12 месяцев, 24 месяца, 36 месяцев или 48 месяцев хранения. Гранулы продолжительного высвобождения, которые получают с помощью других условий обработки, не проявляют постоянные сопоставимые свойства стабильности. Например, ER гранулы, которые получают покрытием IR гранул ER кроющей композицией и факультативно выдерживают при условиях, в которых точка росы не контролируется, или при атмосфере за пределом диапазона точки росы приблизительно 5-20°С (например, 7-16°С), не обеспечивают постоянные профили растворения, которые стабильны в течение ожидаемой длительности срока годности (например, через 12 месяцев, 24 месяца, 36 месяца или до 48 месяцев хранения на складах или в аптеках).
[0061] К тому же однородность профиля высвобождения для ER гранул, в которые включено ER покрытие, пластификатор, как было обнаружено, зависит от того, как был получен раствор для нанесения ER покрытия. В одном варианте осуществления ER покрытие получают растворением водонерастворимого полимера (например, этилцеллюлозы) в подходящем растворителе (например, водном органическом растворителе, таком как водный ацетон), затем добавлением пластификатора к раствору и перемешиванием раствора водонерастворимого полимера и пластификатора в течение, по меньшей мере, одного часа после добавления пластификатора. В некоторых вариантах осуществления, раствор водонерастворимого полимера и пластификатора перемешивают в течение, по меньшей мере, приблизительно 2 часов, по меньшей мере, приблизительно 3 часов, по меньшей мере, приблизительно 4 часов, по меньшей мере, приблизительно 5 часов после добавления пластификатора. Если раствор водонерастворимого полимера и пластификатора перемешивают в течение менее чем одного часа после добавления пластификатора, получаемые ER гранулы не будут обеспечивать постоянные профили растворения, которые стабильны во времени (например, при условиях хранения).
[0062] Циклобензаприновые композиции, полученные способом данного изобретения, являются пригодными для лечения мышечных спазмов и боли, связанной с мышечными спазмами, а также фибромиалгии (хронический синдром, характеризующийся рассеянной или характерной мышечной, суставной или костной болью, или другими симптомами) и для лечения боли нижних отделов спины.
[0063] Активное ядро лекарственной формы данного изобретения может включать инертную частицу или кристалл кислого или щелочного буфера, которые покрывают пленкообразующим составом, содержащим лекарственное средство, и предпочтительно водорастворимой пленкообразующей композицией для формирования водорастворимой/диспергируемой частицы. Альтернативно, активное можно получить гранулированием и размалыванием и/или экструзией и сферонизацией полимерной композиции, содержащей лекарственное вещество. Количество лекарственного средства в ядре будет зависеть от дозы, которая необходима, и, как правило, варьирует от приблизительно 5 до 60 вес.%. В целом, полимерное покрытие на активном ядре будет составлять от приблизительно 4 до 20% по весу покрытой частицы в зависимости от типа необходимого профиля высвобождения и/или выбранных полимеров и растворителей покрытия. Специалисты в данной области техники смогут выбрать соответствующее количество лекарственного средства для покрытия на или включения в ядро для достижения необходимой дозировки. В одном варианте осуществления неактивным ядром может быть сахарная сфера или кристалл буфера или инкапсулированный кристалл буфера, такой как карбонат кальция, бикарбонат натрия, фумаровая кислота, винная кислота и т.д., которые изменяют микроокружение лекарственного средства для того, чтобы способствовать его высвобождению.
[0064] Частицу, содержащую лекарственное средство, можно покрыть покрытием продолжительного высвобождения (ER), содержащим водонерастворимый полимер или сочетание водонерастворимого полимера и водорастворимого полимера, для получения ER гранул. В соответствии с определенными вариантами осуществления водонерастворимый полимер и водорастворимый полимер могут присутствовать в весовом соотношении от 100/0 до 65/35, более конкретно от приблизительно 95/5 до 70/30 и еще более конкретно в соотношении от приблизительно 85/15 до 75/25. Покрытие продолжительного высвобождения наносят в количестве, необходимом для обеспечения необходимого профиля высвобождения. Покрытие продолжительного высвобождения, как правило, содержит от приблизительно 1% до 15%, более конкретно, от приблизительно 7% до 12% по весу покрытых гранул.
[0065] Данное изобретение также обеспечивает способ изготовления лекарственной формы модифицированного высвобождения, включающей смесь двух совокупностей гранул. В соответствии с одним вариантом осуществления способ включает этапы:
получения ядра, содержащего лекарственное средство, путем покрытия инертной частицы, такой как зерно нонпарель, кристалл кислого буфера или кристалл щелочного буфера, лекарственным средством и полимерным связующим веществом или грануляцией и размалыванием, или экструзией/сферонизацией для формирования гранулы немедленного высвобождения (IR);
покрытие IR гранулы только водонерастворимым полимером (факультативно пластифицированным) (таким как этилцеллюлоза) или в сочетании с водорастворимым полимером (таким как гидроксипропилметилцеллюлоза) для формирования гранулы продолжительного высвобождения (ER);
заполнение в твердые желатиновые капсулы только ER гранул или в сочетании с IR гранулами при соответствующем соотношении для получения MR (модифицированного высвобождения) капсул, обеспечивающих необходимый профиль высвобождения.
[0066] IR гранулы при тестировании в соответствии со следующей процедурой высвобождают, по меньшей мере, приблизительно 70%, более точно, по меньшей мере, приблизительно 90% активного в течение 30 минут.
[0067] Процедура растворения:
[0068] Аппарат для растворения: Аппарат 2 по Фармокопее США (перемешивает при 50 rpm), среда-растворитель: 900 мл 0,1 N НСl (или подходящая среда-растворитель) при 37°С и определение высвобождения лекарственного средства с помощью HPLC).
[0069] Водную или фармацевтически приемлемую среду-растворитель можно применять для получения частиц-ядер, содержащих лекарственное средство. Тип пленкообразующего связующего вещества, которое применяется для связывания лекарственного средства с инертными сахарными сферами, не является критичным, но обычно применяют водорастворимые, спирторастворимые или растворимые в ацетон/вода связующие вещества. Связующие вещества, такие как поливинилпирролидон (PVP), полиэтиленоксид, гидроксипропилметилцеллюлоза (НРМС), гидроксипропилцеллюлоза (НРС), полисахариды, такие как декстран, кукурузный крахмал, можно применять при концентрациях от приблизительно 0,5 до 5 вес.%, хотя могут быть пригодны другие концентрации. Лекарственное вещество может присутствовать в этом кроющей составе в форме раствора или может быть диспергировано при содержании твердого вещества до приблизительно 35 вес.% в зависимости от вязкости кроющего состава.
[0070] Примеры соответствующих полимеров для нанесений покрытий включают воски, водонерастворимые производные целлюлозы (например, этилцеллюлозу, простые эфиры целлюлозы, сложные эфиры целлюлозы, ацетилцеллюлозу, бутираты целлюлозы, пропионат целлюлозы, этилцеллюлозу, смешанные сложные эфиры целлюлозы и т.д.), ацилированные полисахариды, полиуретаны, поливинилацетат (например, Kollicoat SR30D от BASF), полиакрилатные и полиметакрилатные полимеры и производные, нейтральные сополимеры, содержащие повторяющиеся единицы этилакрилата и/или метилметакрилата (такие как Eudragit NE), нечувствительные к рН сополимеры аммонио и метакриловой кислоты, водонерастворимые сополимеры сложных эфиров акриловой и метакриловой кислот с группами четвертичного аммония, такие как Eudragit RS, RS30D, RL или RL30D и подобное, и их сочетания. Предпочтительные толщины покрытия изменяются в диапазоне от приблизительно 1 до приблизительно 1000 микрон, наиболее предпочтительно от приблизительно 20 до приблизительно 500 микрон.
[0071] В соответствии с определенными вариантами осуществления лекарственное вещество, факультативно связующее вещество, такое как PVP, полимер, контролирующий скорость растворения (если применяется), и факультативно другие фармацевтически приемлемые формообразующие смешивают вместе в планетарном смесителе или грануляторе с высоким усилием сдвига, таком как Fielder, и гранулируют путем добавления/распыления гранулирующей жидкости, такой как вода или спирт. Влажную массу можно экструдировать и сферонизировать для получения сферических частиц (гранул) с помощью экструдера/марумерайзера. В этих вариантах осуществления загрузка лекарственного средства может достигать 90 вес.% от общего веса экструдированного/сферонизированного ядра.
[0072] Типичные миорелаксанты включают циклобензаприн, дантролен натрия, метокарбамол, метаксалон, каризопродол, диазепам и их фармацевтически приемлемые соли, сольваты и/или сложные эфиры. Циклобензаприна гидрохлорид является особенно пригодным миорелаксантом. Как используется в данном документе, пригодные миорелаксанты включают основание, его фармацевтически приемлемые соли, такие как гидрохлорид, их стереоизомеры и их смеси.
[0073] Типичные примеры водонерастворимых полимеров, применимых в ER покрытии, включают воски, (например, сложные эфиры жирных кислот, такие как бегенат глицерина или карнаубский воск), этилцеллюлозный порошок или этилцеллюлозную водную дисперсию (такую как AQUACOAT® ECD-30), ацетилцеллюлозу, поливинилацетат (Kollicoat SR#30D от BASF), нейтральные сополимеры на основе этилакрилата и метилметакрилата (такие как Eudragit NE) водонерастворимые сополимеры сложных эфиров акриловой и метакриловой кислот с группами четвертичного аммония, такие как Eudragit RS и RS30D, RL или RL30D, и подобное. Типичные примеры водорастворимых полимеров, пригодных тут, включают низкомолекулярную гидроксипропилметилцеллюлозу (НРМС), метилцеллюлозу, гидроксипропилцеллюлозу, поливинилпирролидон, полиэтиленгликоль (PEG с молекулярным весом>3000) и их смеси. Покрытие продолжительного высвобождения будут, как правило, наносить при толщине, варьирующей в диапазоне от приблизительно 1 вес.% до 15 вес.%, в зависимости от растворимости активного в воде и применяемого растворителя или кроющего состава на основе латексной суспензии.
[0074] Кроющие композиции, применяемые при формировании мембраны, факультативно пластифицируют. Типичные примеры пластификаторов, которые могут применяться для пластификации мембран, включают триацетин, трибутилцитрат, триэтилцитрат, диэтилфталат ацетилтри-n-бутилпитрат, полиэтиленгликоль, полипропиленгликоль, касторовое масло, дибутилсебацат, ацетилированные моноглицериды и подобное или их смеси. Пластификатор может содержать приблизительно 3-30 вес.% и более типично приблизительно 10-25 вес.% на основе полимера. Тип пластификатора и его содержание зависит от полимера или полимеров, природы системы покрытия (например, водная или на основе растворителя, раствор или на основе дисперсии и общее содержание твердых веществ).
[0075] В основном желательно грунтовать поверхность частицы перед нанесением мембранного покрытия продолжительного высвобождения или разделать различные мембранные слои нанесением тонкой гидроксипропилметилцеллюлозной (НРМС) (OPADRY® Clear) пленки. В то время как обычно применяют НРМС, также можно применять другие грунтовки, такие как гидроксипропилцеллюлоза (НРС).
[0076] Мембранные покрытия можно наносить на ядро с помощью какой-либо техники покрытия, обычно применяемой в фармацевтической промышленности, однако особенно пригодным является псевдоожиженное покрытие.
[0077] Данное изобретение применяют к формам с множественными дозами, т.е. лекарственным продуктам в форме лекарственных форм с множеством частиц (пеллеты, гранулы, крупинки или мини-таблетки) или в других формах, подходящих для перорального введения. Как используется в данном документе, эти выражения применяются взаимозаменяемо для отсылки к лекарственным формам с множеством частиц.
[0078] Данное изобретение также обеспечивает способ изготовления лекарственной формы продолжительного высвобождения, которая включает смесь двух или более совокупностей гранул. В соответствии с одним аспектом данного изобретения способ включает этапы:
[0079] покрытия инертной частицы, такой как зерно нонпарель, кристалл кислого буфера или кристалл щелочного буфера, лекарственным средством и полимерным связующим веществом для формирования частицы активного лекарственного средства (IR гранул), которая может присутствовать в стандартной лекарственной форме для действия в качестве болюсной дозы;
[0080] покрытие частицы активного лекарственного средства раствором или суспензией водонерастворимого полимера или смеси водорастворимых и водонерастворимых полимеров для формирования покрытой частицы лекарственного средства с продолжительным высвобождением (ER гранул);
[0081] заполнение в твердую желатиновую капсулу только ER гранул и факультативно в сочетании с IR гранулам в соответствующем соотношении, варьирующем в диапазоне от 95/5 до 70/30 (ER гранулы/IR гранулы), для получения MR (модифицированного высвобождения) капсулы, проявляющей целевой профиль высвобождения лекарственного средства.
[0082] Способы данного изобретения обеспечивают лекарственную форму с множеством частиц и модифицированным высвобождением миорелаксанта скелетных мышц, содержащую одну или более совокупности гранул, которая обеспечивает профиль продолжительного высвобождения активного в условиях in vitro, близко подражая профилю, сымитированному из фармакокинетического моделирования. По меньшей мере, одна из совокупностей гранул является совокупностью ER (продолжительного высвобождения) гранул, как правило, содержащей покрытие только из водонерастворимого полимера или в сочетании с водорастворимым полимером, нанесенное на ядра, содержащие активное. Активное ядро лекарственной формы данного изобретения может содержать инертную частицу, такую как сахарная сфера, или кристалл кислого или щелочного буфера, которую покрывают миорелаксантом скелетных мышц, таким как пленкообразующий состав циклобензаприна гидрохлорида, предпочтительно водорастворимая пленкообразующая композиция. Первый кроющий состав может содержать, в дополнение к активному, связующее вещество, такое как гидроксипропилцеллюлоза. Гранулы с наслоенным лекарственным средством можно покрыть защитным изолирующим покрытием OPADRY® Clear для получения IR гранул. Альтернативно, частицу-ядро можно сформировать гранулированием и сухим размалываним и/или с помощью экструзии и сферонизации фармацевтической композиции, содержащей активное. Количество лекарственного средства в ядре будет зависеть от необходимой дозы и, как правило, варьирует от приблизительно 5 до приблизительно 60 вес.%.
[0083] ER гранулы, полученные способами данного изобретения, содержат функциональную мембрану (например, мембрану продолжительного высвобождения), содержащую только водонерастворимый полимер или в сочетании с водорастворимым полимером на IR гранулах. Состав капсулы для перорального введения один раз в день миорелаксанта скелетных мышц, полученный в соответствии с данным изобретением, включает ER гранулы, содержащие активное вещество и факультативно IR гранулы. IR (немедленного высвобождения) гранулы обеспечивают немедленное высвобождение активного, в то время как ER гранулы обеспечивают профиль продолжительного высвобождения активного через несколько часов. После перорального введения такой состав капсулы обеспечивает профили терапевтически эффективного содержания в плазме в течение продолжительного периода времени, таким образом, приводя к повышенной степени согласия пациента с предписанным режимом.
[0084] Лекарственные формы, полученные способами данного изобретения, включают одну или более совокупностей гранул и обеспечивают модифицированный профиль высвобождения. По меньшей мере одна из совокупностей гранул включает гранулы продолжительного высвобождения (ER), где ER гранулы включают частицу-ядро (IR (немедленного высвобождения) гранулу), содержащую миорелаксант скелетных мышц и ER (продолжительное высвобождение) покрытие, включающее водонерастворимый полимер, окружающий ядро. Лекарственная форма, в соответствии с определенными вариантами осуществления, при тестировании на растворение с помощью Аппарата 2 Фармакопеи США (перемешивает при 50 rpm) в 900 мл 0,1 N НСl (или подходящей среде-растворителе) при 37°С проявляет профиль высвобождения лекарственного средства, в основном соответствующий следующей схеме:
через 2 часа высвобождается не более чем приблизительно 40% общего активного;
через 4 часа высвобождается от приблизительно 40-65% общего активного;
через 8 часов высвобождается от приблизительно 60-85% общего активного;
и
факультативно через 12 часов высвобождается от приблизительно 75-85% общего активного.
[0085] Лекарственная форма, таким образом, обеспечивает терапевтически эффективную концентрацию в плазме в течение продолжительного периода времени, как правило, в течение периода 24 часов для лечения мышечного спазма, связанного с болезненными скелетно-мышечными состояниями у людей. Альтернативно, лекарственные формы, полученные способами данного изобретения, можно применять для лечения фибромиалгии или инсомнии.
[0086] Следующие неограничивающие примеры иллюстрируют капсульные лекарственные формы, произведенные в соответствии с данным изобретением, с применением циклобензаприна гидрохлорида в качестве контрольного примера, который проявляет in vitro профили высвобождения лекарственного средства, сходные с прогнозируемым путем проведения модельных экспериментов. Такие лекарственные формы при пероральном введении будут способны поддерживать концентрации лекарственного средства в плазме на терапевтически эффективных уровнях в течение продолжительных периодов времени, таким образом, значительно улучшая степень согласия пациента с предписанным режимом.
Пример 1
[0087] Циклобензаприн хорошо абсорбируется после перорального введения, но существует большая межличностная вариация в плазменных уровнях. Он выводится достаточно медленно с периодом полураспада до одного-трех дней. Настоящая схема лечения 10 мг три раза в день является вопросом степени согласия пациента с предписанным режимом, особенно у пожилых людей. Таким образом, лекарственная форма (капсула) модифицированного высвобождения была разработана с профилем высвобождения, показанным на Фигуре 1. Для определения того, является ли это соответствующим профилем высвобождения, из литературы взяли данные фармакокинетики циклобензаприна после одной дозы 10 мг Flexeril" таблеток, которые вводили 3 раза в день. Фармакокинетическую модель разработали из этих данных, используя WinNonlin™ версии 1.5.
Полученные в результате модельные параметры приведены ниже:
[0088] Теоретические плазменные уровни моделировали с помощью фармакокинетической модели, приведенной выше, а целевая скорость высвобождения in vitro приведена на Фигуре 1. Фигура 2 показывает смоделированые плазменные уровни на день первый после дозировки 1 х 10 мг Flexeril® таблетки, которую давали 3 раза в день, и предложенной MR капсулы циклобензаприна НСl, 30 мг, которую давали один раз в день.
Пример 2А
[0089] Блок-схема способа производства показана на Фигуре 3, применяется для получения MR капсул циклобензаприна НСl. (См. патент США 7387793, включенный в данный документ по ссылке во всей его полноте для каких-либо целей.) Капсулы, применяемые для различных клинических исследований (например, базовое исследование и поэтапные клинические испытания), и серии для испытания стабильности для регистрации были также получены согласно способу Примера 2А.
[0090] Раствор лекарственного средства (25 вес.% твердых веществ), содержащий циклобензаприна гидрохлорид (20,0 кг), полученный в 50/50 ацетон/очищенная вода (30,0 кг каждого) и покрытый на 20-25 меш сахарные сферы (58,4 кг) в устройстве псевдоожиженного слоя для нанесения покрытий Glatt, GPCG 120, оснащенном 18" вставкой Wurster для нанесения снизу вверх, воздушным пароприемным листом D (100 меш сито), высотой сектора от пароприемного листа приблизительно 53 мм, при следующих условиях: диаметр наконечника: 3,0 мм; точка росы приблизительно 8°С; давление воздуха пульверизации: 2 бара; начальная скорость распыления: 100 г/мин, линейно увеличивающаяся до приблизительно 400 г/мин; температура продукта: 49°С, понижающаяся до 43°С; объем технологического воздуха: 950-1100 куб. фут/мин. Полученные в результате гранулы с наслоенным лекарственным средством обеспечили защитным изолирующим покрытием OPADRY® Clear с уровнем покрытия 2 вес.% в устройстве псевдоожиженного слоя для нанесения покрытий Glatt посредством распыления водного раствора (8 вес.% твердых веществ) при скорости распыления приблизительно 200 г/мин, при температуре продукта 42°С при точке росы 8°С, затем высушили при приблизительно 50°С в течение 5 минут при точке росы 8°С для получения гранул "немедленного высвобождения" (IR).
[0091] ER кроющую композицию (6,0 вес.% твердых веществ), содержащую этилцеллюлозу (6,9 кг, Ethocel Premium Std, 10 сП) и диэтилфталат (0,75 кг) в растворе 98/2 ацетон/вода, получили путем перемешивания при 850±25 rpm в течение не менее чем одного часа. Это означает, что время перемешивания может изменяться по усмотрению оператора в производственной среде. Эту кроющую композицию затем нанесли на IR гранулы (77,4 кг) при точке росы 10°С при начальной скорости распыления приблизительно 250 г/мин, линейно увеличивающейся до 500 г/мин, объеме технологического воздуха 1000 куб. фут/мин), температуре технологического воздуха 46°С, давлении воздуха пульверизации 2,5 бар, в Glatt GPCG 120, оснащенном 18" вставкой Wurster для нанесения снизу вверх, воздушным пароприемным листом С (100 меш сито), высотой сектора от пароприемного листа приблизительно 50 мм, размером отверстия наконечника 3 мм. ER покрытие наносили при точке росы 10°С для обеспечения 9% веса покрытия. Полученные в результате ER гранулы высушили в устройстве при 50°С в течение приблизительно 5 минут при точке росы 10°С для удаления остаточных растворителей.
[0092] ER гранулы затем пропустили через 14-меш и 24-меш сита, отбрасывая какие-либо гранулы, оставшиеся на 14 меш сите, затем высушили в сушилке при 60°С в течение 4 часов. Необходимые количества гранул продолжительного высвобождения (131,9 мг, эквивалентные 30 мг пиклобензаприна НСl) затем наполнили в капсулы 4 размера (вес пустой капсулы: 37 мг) для получения MR капсул пиклобензаприна НСl, 30 мг, в качестве базового материала для клинического испытания (СТМ), используя промышленное оборудование для заполнения капсул, MG Futura. Необходимые количества гранул продолжительного высвобождения (65,9 мг, эквивалентные 15 мг пиклобензаприна НСl) и эквивалентные количества 20-25 меш сахарных сфер также заполнили в белые непрозрачные капсулы 4-го размера для получения MR капсул пиклобензаприна НСl, 15 мг, в качестве базового СТМ, используя такой же заполнитель капсул. Твердые желатиновые капсулы 4 размера с различно окрашенными телом и шляпкой и идентифицирующий знак применяли для получения коммерческих продуктов в виде MR капсул циклобензаприна НСl, 15 и 30 мг.
Пример 2В
[0093] Согласно примеру 2А разработали модифицированный способ с модификациями для этапов ER покрытия и выдерживания в сушилке. В модифицированном способе IR гранулы получали, как в Примере 2А. На этапе ER покрытия ER кроющую композицию (полученная, как в Примере 2А), включающую этилцеллюлозу и диэтилфталат в растворе ацетон/вода, получили путем перемешивания при 850±25 rpm в течение не менее чем 1 часа после добавления диэтилфталата. Эту кроющую композицию затем наносили на IR гранулы при точке росы 10°С для получения 9% веса покрытия. Полученные в результате ER гранулы сушили в устройстве при 50°С в течение приблизительно 5 минут при точке росы 10°С для удаления остаточных растворителей. После просеивания (14- и 24-меш сита) ER гранулы выдержали в сушилке при 60°С в течение 4 часов при точке росы 8-10°С (целевая 10°С).
Пример 3
[0094] Композиции, полученные согласно процедуре Примера 2А, протестировали в клинических исследованиях фармакокинетики (РК) и Фазы 3 и (исследования состояний натощак против после приема пищи, используя CMR 30 мг дозы), исследовании по безопасности и биодоступности множественных дозировок MR циклобензаприна НСl 30 мг и циклобензаприна НСl 10 мг три раза в день у здоровых добровольцев, исследовании эффективности и безопасности MR циклобензаприна НСl 15 мг и 30 мг против плацебо у субъектов с болью из-за мышечных спазмов локального происхождения и рандомизированном, двойном слепом, перекрестном исследовании с двумя периодами у здоровых добровольцев (каждый 7-дневный оцениваемый период). Последнее исследование сравнивало безопасность и фармакокинетику модифицированного высвобождения (CMR) циклобензаприна НСl 30 мг один раз в день и Flexeril (циклобензаприна НСl 10 мг три раза в день в двух подгруппах 18 здоровых добровольцев возрастом 18-45 лет и возрастом 65-75 лет. Каждый 7-дневный оцениваемый период состоял из забора крови и оценок безопасности в момент до приема дозы, 0,5, 1, 1,5, 2, 2,5, 3, 4, 5, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 36, 48, 72, 96, 120, 144 и 168 часов после дозировки и биоаналитического тестирования аттестованным LC-MS/MS. Фигура 4 показывает профили плазменная концентрация - время MR циклобензаприна НСl (CMR 30 мг) и Flexeril® (10 мг ×3 раза), которые вводили здоровым взрослым добровольцам, которые не ели в течение ночи.
[0095] Соответственно, один аспект данного изобретения относится к способу получения лекарственных форм циклобензаприна НС1 для обеспечения фармакокинетических (РК) параметров, перечисленных в Таблице 1А, полученных в клинических исследованиях, описанных выше, и, в другом аспекте, биоэквивалентных лекарственных форм, обеспечивающих 80%-125% одного или более из средних фармакокинетических параметров, перечисленных в Таблице 1А (например, Смакс, и AUC). Каждая из MR лекарственных форм, содержащих циклобензаприна гидрохлорид, которую необходимо произвести для коммерческого распространения после разрешения контролирующего органа, при тестировании на здоровых добровольцах должна обеспечивать максимальную концентрацию в плазме крови (Смакс) в диапазоне приблизительно 80%-125% 19,851±5,8765 нг/мл циклобензаприна НСl и AUC0-168 в диапазоне приблизительно 80%-125% 736,60±259,414 нг·час/мл после перорального введения единичной MR капсулы 30 мг циклобензаприна НСl. Аналогично, MR лекарственные формы циклобензаприна должны обеспечивать максимальную концентрацию в плазме крови (Смакс) в диапазоне приблизительно 80%-125% 8,315±2,1635 нг/мл циклобензаприна НСl и AUC0-168 в диапазоне приблизительно 80%-125% 318,30±114,657 нг·час/мл после перорального введения единичной MR капсулы 15 мг циклобензаприна НСl.
[0096] MR капсулы 30 мг циклобензаприна НСl получили в соответствии с Примером 2А, обеспечивая 80%-125% средние фармакокинетические значения, показанные в Таблице 1 В у здоровых взрослых субъектов возрастом 18-45 лет в условиях натощак, и в Таблице 1 С у здоровых взрослых субъектов возрастом 65-75 в условиях натощак. AUC0-168 относится к площади под кривой плазменная концентрация-время до последней измеряемой точки времени (168 часов), подсчитанное по линейному правилу трапеции, AUC0-168 относится к площади под кривой концентрация-время до бесконечности, Смакс, относится к максимальной концентрации в плазме крови и Тмакс относится к времени до максимальных плазменных уровней циклобензаприна. Значения Смакс(первый) и Тмакс(первый) оценивали с помощью плазменных уровней после первой дозы и перед второй дозой для 10 мг циклобензаприна трижды в день, в то время как для CMR 30 мг использовали весь период исследования, и значение было доза-скорректированным к 10 мг дозе. Тмакс оценили с помощью плазменных уровней в течение всего периода исследования для обоих медикаментов исследования.
аОцененные с помощью плазменных уровней после первой дозы и перед второй дозой для циклобензаприна 10 мг трижды в день; для CMR 30 мг использовали весь период исследования, и значение было дозаскорректированным к 10 мг дозе.
bОцененные с помощью плазменных уровней в течение всего периода исследования для обоих медикаментов.
[0097] Фигура 5 показывает фактический профиль высвобождения лекарственного средства in vitro по сравнению со смоделированным профилем высвобождения лекарственного средства in vitro, подсчитанного с помощью программного обеспечения Gastro-Plus, и PK параметры, полученные в результате исследований, описанных выше. Два профиля являются исключительно очень близкими. Фигура 6 показывает профили высвобождения лекарственного средства первичной биосерии (30 мг, полученные согласно Примеру 2А), которую хранили в 60 куб. см запаянных индукционным нагревом HDPE бутылках при ускоренных условиях стабильности (40С/75%ОВ (относительная влажность)). 15 мг (PF307EA001) и все серии для испытания стабильности для регистрации (PF312 (15 мг) и PF313 (30 мг), также полученные согласно Примеру 2А), проявляли схожие тесные профили высвобождения лекарственного средства при хранении в 60 куб. см запаянных индукционным нагревом HDPE бутылках при ICH условиях стабильности (например, при 25°С/60%ОВ в течение 36 месяцев, 30°С/65%ОВ в течение 12 месяцев и 40°С/75%ОВ в течение 6 месяцев).
Пример 4
[0098] Таблица 2 подытоживает результаты стабильности для ряда предназначенных для аттестации способа серий MR капсул циклобензаприна НСl, 15 и 30 мг (например, PF312EA001V - PF312EA003V (15 мг) и PF313EA001V -PF313EA003V, полученные согласно Примеру 2А). Первая серия для аттестации (PF313EA001) и другая серия (PF313EA006) имели сравнительно высокую и низкую растворимости при высвобождении (т.е. в нулевой момент времени) соответственно (смотри Таблицу 3). Партия №PF3130001V не выдержала тест на растворение в 1-, 3- и 6-месячных 40°С/75%ОВ (относительная влажность), 3-, 6-месячной 25°С/60%ОВ и 3 месячном при 30°С/65%ОВ моментах времени. Точки растворения, не соответствующие характеристикам, были моментом времени 4 часа и/или 8 часов. Другие пять серий для аттестации при высвобождении (т.е. в нулевой момент времени) соответствовали характеристикам растворения, количественного анализа, расщеплению (смотри Таблицу 2). Кроме того, данные по стабильности для этих серий для аттестации также соответствовали характеристикам продукта. Изучение показало, что не соответствующие характеристикам (OOS) результаты растворения, наблюдаемые для PF3130001V, были не из-за проблемы стабильности продукта, но скорее из-за более высокого, чем типичный, профиля растворения для этой конкретной партии при высвобождении (т.е. в нулевой момент времени). Данные растворения нулевого момента времени и последующего времени не показали восходящей тенденции у значений растворения, а скорее типичную аналитическую и/или от серии к серии вариабельность.
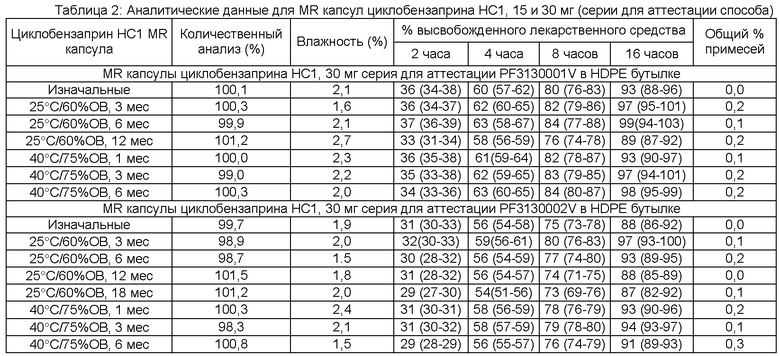
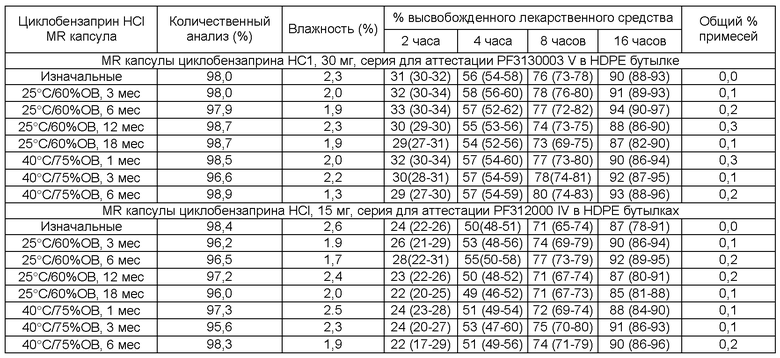
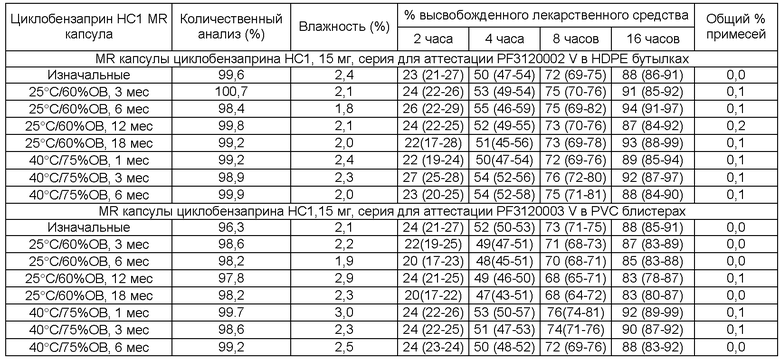
[0099] Были сделаны две модификации для способа Примера 2А. Первая: время перемешивания после добавления пластификатора в ER кроющий раствор постоянно контролировали, чтобы соответствовало, по меньшей мере, одному часу с верхним пределом, например, 2 часа. Вторая: установили сушильный механизм для жесткого контроля точки росы во время высушивания/выдерживания. Целевую точку росы для наслаивания лекарственного средства, покрытия ER гранул и выдерживания ER гранул выставили на 8-10°С.
[00100] Таблица 3 подытоживает средние значения со стандартными отклонениями, максимальные и минимальные значения количественных данных, растворения, влажность, общие расщепления и однородность единиц дозирования для коммерческих серий после последовательного принятия новых контролей (т.е. контроля времени перемешивания и точки росы выдерживания Примера 2В): 7 серий MR капсул циклобензаприна НС1, 30 мг (PF313) и 32 серии MR капсул циклобензаприна НС1, 15 мг (PF312). Предшествующая серия для аттестации способа PF3130001V и одна из первых 3 коммерческих серий (PF313 0006), упомянутых выше (произведенные согласно Примеру 2А), которые показали атипичные (т.е. высокие или низкие) значения растворения, показаны отдельно в Таблице 3. Очевидно, что значения количественного анализа и растворения близки, указывая на то, что способ производства достаточно надежен.
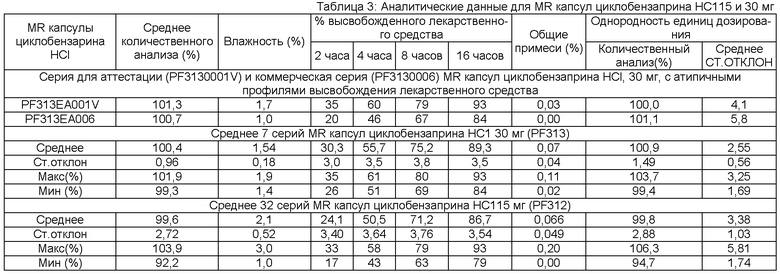
[00101] Несмотря на то что данное изобретение описано детально и со ссылками на его конкретные примеры, для специалиста в данной области будет очевидно, что можно сделать различные изменения и модификации без отступления от его сущности и объема.
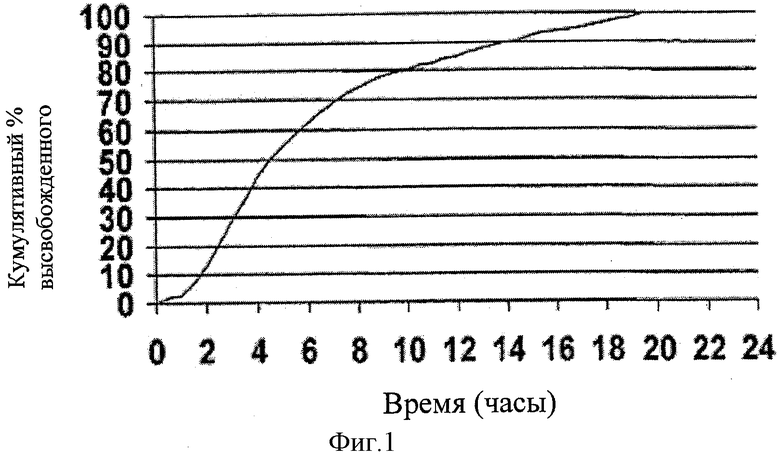
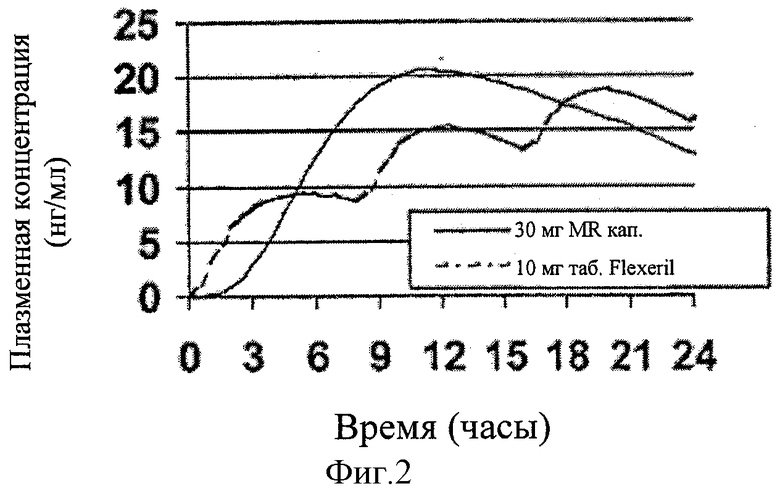
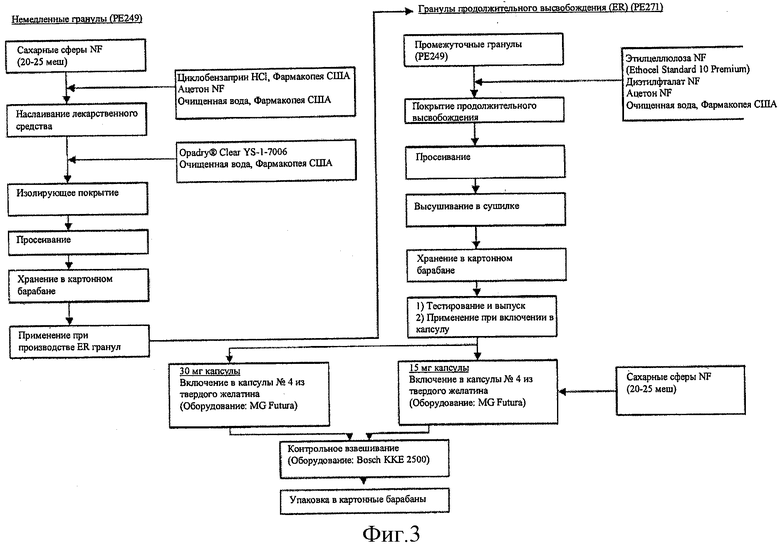
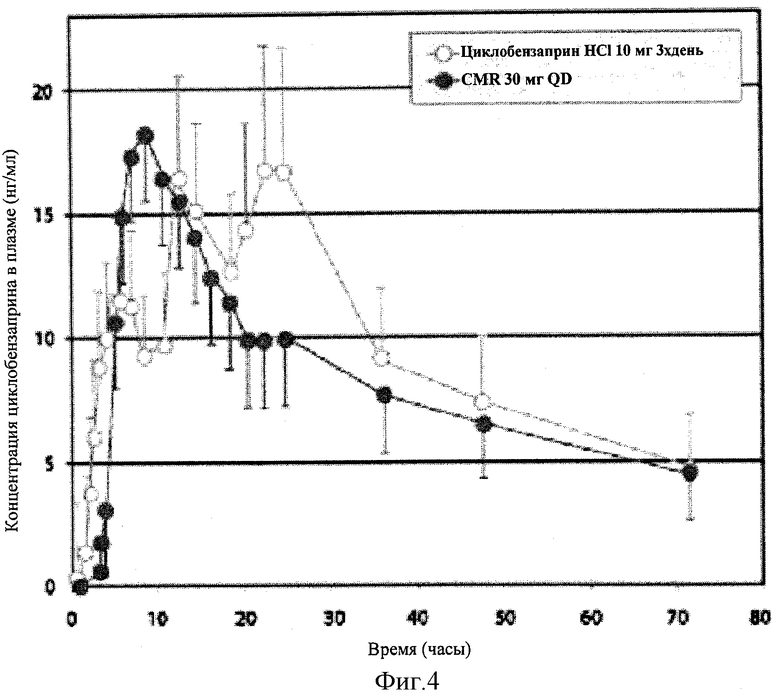
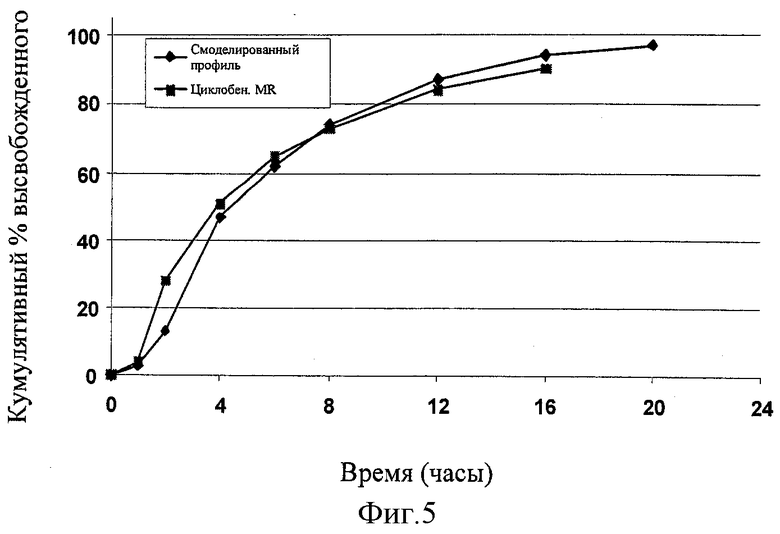
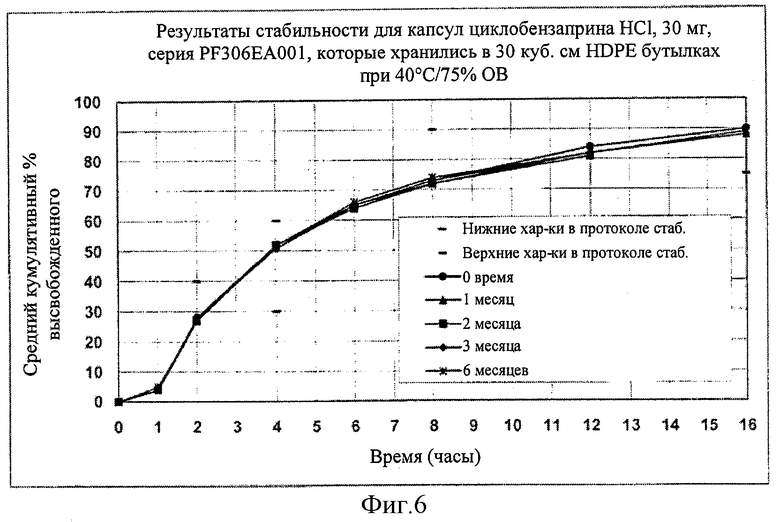
Изобретение относится к фармацевтической промышленности, а именно представляет собой способ обеспечения равномерного профиля растворения фармацевтической композиции, включающей циклобензаприн, включающей покрытые инертные частицы с содержащей циклобензаприн композицией наслаивания лекарственного средства, для формирования IR гранул, затем покрытия IR гранул покрытием продолжительного высвобождения для формирования ER гранул. 2 н. и 51 з.п. ф-лы, 6 ил., 5 пр., 4 табл.
1. Способ обеспечения равномерного профиля растворения фармацевтической композиции, включающей циклобензаприн или его фармацевтически приемлемую соль, сольват и/или сложный эфир, где указанный профиль растворения является воспроизводимым и тесным, включающий:
a) покрытие инертных частиц композицией наслаивания лекарственного средства, включающей циклобензаприн или его фармацевтически приемлемую соль, сольват и/или сложный эфир и фармацевтически приемлемый растворитель, с формированием, таким образом, гранул немедленного высвобождения;
b) покрытие гранул немедленного высвобождения кроющей композицией продолжительного высвобождения, включающей фармацевтически приемлемый водонерастворимый полимер, в атмосфере с точкой росы в диапазоне 5-20°C, с формированием, таким образом, гранул продолжительного высвобождения; где указанный способ отличается тем, что
c) гранулы продолжительного высвобождения выдерживают при 60°C в течение 4-12 часов в атмосфере с точкой росы в диапазоне 5-20°C.
2. Способ по п.1, дополнительно включающий покрытие гранул немедленного высвобождения этапа a) изолирующей кроющей композицией, включающей фармацевтически приемлемый водорастворимый полимер, перед указанным этапом b) покрытия продолжительного высвобождения.
3. Способ по п.2, где указанные инертные частицы имеют размер частиц 20-25 меш.
4. Способ по п.2, где указанная изолирующая кроющая композиция дополнительно включает воду.
5. Способ по п.1, где указанный этап покрытия а) осуществляют в атмосфере с точкой росы в диапазоне 5-20°C.
6. Способ по п.1, где кроющая композиция продолжительного высвобождения дополнительно включает пластификатор.
7. Способ по п.6, где кроющую композицию продолжительного высвобождения получают перемешиванием фармацевтически приемлемого водонерастворимого полимера, пластификатора и фармацевтически приемлемого растворителя в течение, по меньшей мере, 1 часа после добавления пластификатора к фармацевтически приемлемому водонерастворимому полимеру и фармацевтически приемлемому растворителю.
8. Способ по п.7, где фармацевтически приемлемый водонерастворимый полимер, пластификатор и фармацевтически приемлемый растворитель перемешивают в течение, по меньшей мере, 3 часов после добавления пластификатора к фармацевтически приемлемому водонерастворимому полимеру и фармацевтически приемлемому растворителю.
9. Способ по п.1, где композиция наслаивания лекарственного средства дополнительно включает циклобензаприна гидрохлорид и 50:50 ацетон:вода.
10. Способ по п.2, где фармацевтически приемлемый водонерастворимый полимер включает гидроксипропилметилцеллюлозу.
11. Способ по п.1, где фармацевтически приемлемый водонерастворимый полимер выбирают из группы, включающей этилцеллюлозу, простые эфиры целлюлозы, сложные эфиры целлюлозы, ацетилцеллюлозу, бутират целлюлозы, пропионат целлюлозы, поливинилацетат, нейтральные сополимеры на основе этилакрилата и метилметакрилата, сополимеры сложных эфиров акриловой и метакриловой кислоты с группами четвертичного аммония, нечувствительные к pH сополимеры аммонио и метакриловой кислоты, воски, ацилированные полисахариды, полиуретаны, высокомолекулярную гидроксипропилметилцеллюлозу, полиакрилатные и полиметакрилатные полимеры и их смеси.
12. Способ по п.1, где фармацевтически приемлемый водонерастворимый полимер включает этилцеллюлозу.
13. Способ по п.6, где пластификатор выбирают из группы, включающей глицерин и его сложные эфиры (например, ацетилированные моно- или диглицериды, включая коммерчески доступный Myvacet® 9-45), глицерилмоностеарат, глицерилтриацетат, глицерилтрибутират, дибутилфталат, диэтилфталат, диметилфталат, диоктилфталат, сложный трибутиловый эфир ацетиллимонной кислоты, сложный триэтиловый эфир ацетиллимонной кислоты, трибутилцитрат, ацетилтрибутилцитрат, триэтилцитрат, глицеринтрибутират; диэтилсебацат, дибутилсебацат, дибутиладипаты, дибутилазелаинаты, дибутилбензоаты, хлорбутанол, полиэтиленгликоли, растительные масла, оливковое масло, минеральное масло, диэтилфумарат, диэтилмалаты, диэтилоксалат, дибутилсукцинат, дибутилбутират, сложные эфиры цетилового спирта, диэтилмалонат, касторовые масла, полисорбаты, N-бутилбензенсульфонамид, N-метилпирролидон и их смеси.
14. Способ по п.6, где пластификатор включает диэтилфталат.
15. Способ по п.6, где кроющая композиция продолжительного высвобождения включает этилцеллюлозу и диэтилфталат, растворенные в растворителе, включающем ацетон и воду в весовом соотношении ацетон/вода в диапазоне от 85/15 до 98/2.
16. Способ по п.6, где соотношение водонерастворимого полимера к пластификатору составляет 9:1.
17. Способ по п.1, где композиция наслаивания лекарственного средства включает циклобензаприна гидрохлорид, и после высушивания гранулы с наслоенным лекарственным средством включают от 5 вес.% до 30 вес.% циклобензаприна гидрохлорида.
18. Способ по п.17, где композиция наслаивания лекарственного средства включает циклобензаприна гидрохлорид, и после высушивания гранулы с наслоенным лекарственным средством включают 25 вес.% циклобензаприна гидрохлорида.
19. Способ по п.2, где гранулы немедленного высвобождения включают 2% фармацевтически приемлемого водорастворимого полимера.
20. Способ по п.1, где гранулы продолжительного высвобождения включают от 7% до 12% фармацевтически приемлемого водонерастворимого полимера.
21. Способ по п.6, где гранулы продолжительного высвобождения включают 9% фармацевтически приемлемого водонерастворимого полимера и пластификатор.
22. Способ по п.1, где гранулы продолжительного высвобождения обеспечивают профиль высвобождения лекарственного средства, который не отклоняется более чем на 10% в любой момент времени в следующей схеме растворения:
через 2 часа высвобождается не более чем 40% общего активного;
через 4 часа высвобождается от 40-65% общего активного;
через 8 часов высвобождается от 60-85% общего активного; и факультативно через 12 часов высвобождается от 75-85% общего активного,
при тестировании с помощью Аппарата 2 по Фармакопее США (перемешивает при 50 rpm) в 900 мл 0,1 N HCl при 37°C.
23. Способ по п.1, где указанный этап покрытия b) осуществляют в атмосфере с точкой росы в диапазоне 6-17°C.
24. Способ по п.1, где указанный этап выдерживания с) осуществляют в атмосфере с точкой росы в диапазоне 6-17°C.
25. Способ по п.1, где указанный этап покрытия а) осуществляют в атмосфере с точкой росы в диапазоне 6-17°C.
26. Способ по п.1, где фармацевтическая композиция включает 30 мг циклобензаприна HCl и обеспечивает максимальную концентрацию в плазме крови (Cmax) в диапазоне 80%-125% 19,9 нг/мл циклобензаприна HCl и AUC0-168 в диапазоне 80%-125% 736,6 нг·час/мл после ее единичного перорального введения.
27. Способ по п.1, где фармацевтическая композиция включает 15 мг циклобензаприна HCl и обеспечивает максимальную концентрацию в плазме крови (Cmax) в диапазоне 80%-125% 8,3 нг/мл циклобензаприна HCl и AUC0-168 в диапазоне 80%-125% 318,3 нг·час/мл после ее единичного перорального введения.
28. Способ получения фармацевтической композиции, включающий:
a) покрытие инертных частиц композицией наслаивания лекарственного средства, включающей циклобензаприн или его фармацевтически приемлемую соль, сольват и/или сложный эфир и фармацевтически приемлемый растворитель, с формированием, таким образом, гранул немедленного высвобождения;
b) покрытие гранул немедленного высвобождения кроющей композицией продолжительного высвобождения, включающей фармацевтически приемлемый водонерастворимый полимер и пластификатор, в атмосфере с точкой росы в диапазоне 5-20°C, с формированием, таким образом, гранул продолжительного высвобождения; где покрытие гранул немедленного высвобождения кроющей композицией продолжительного высвобождения включает перемешивание смеси фармацевтически приемлемого водонерастворимого полимера, пластификатора и фармацевтически приемлемого растворителя в течение по меньшей мере одного часа после добавления пластификатора к фармацевтически приемлемому водонерастворимому полимеру и фармацевтически приемлемому растворителю.
29. Способ по п.28, дополнительно включающий:
c) выдерживание гранул продолжительного высвобождения при 60°C в течение 4-12 часов в атмосфере с точкой росы в диапазоне 5-20°C.
30. Способ по п.28, дополнительно включающий покрытие гранул немедленного высвобождения этапа а) изолирующей кроющей композицией, включающей фармацевтически приемлемый водорастворимый полимер, перед указанным этапом b) покрытия продолжительного высвобождения.
31. Способ по п.30, где указанные инертные частицы имеют размер частиц 20-25 меш.
32. Способ по п.30, где указанная изолирующая кроющая композиция дополнительно включает воду.
33. Способ по п.28, где указанные этапы покрытия а) и b) осуществляют в атмосфере с точкой росы в диапазоне 5-20°C.
34. Способ по п.28, где фармацевтически приемлемый водонерастворимый полимер, пластификатор и фармацевтически приемлемый растворитель перемешивают в течение по меньшей мере 3 часов после добавления пластификатора к фармацевтически приемлемому водонерастворимому полимеру и фармацевтически приемлемому растворителю.
35. Способ по п.28, где композиция наслаивания лекарственного средства дополнительно включает циклобензаприна гидрохлорид и приблизительно 50:50 ацетон: вода.
36. Способ по п.28, где фармацевтически приемлемый водонерастворимый полимер включает гидроксипропилметилцеллюлозу.
37. Способ по п.28, где фармацевтически приемлемый водонерастворимый полимер выбирают из группы, включающей этилцеллюлозу, простые эфиры целлюлозы, сложные эфиры целлюлозы, ацетилцеллюлозу, бутират целлюлозы, пропионат целлюлозы, поливинилацетат, нейтральные сополимеры на основе этилакрилата и метилметакрилата, сополимеры сложных эфиров акриловой и метакриловой кислоты с группами четвертичного аммония, нечувствительные к pH сополимеры аммонио и метакриловой кислоты, воски, ацилированные полисахариды, полиуретаны, высокомолекулярную гидроксипропилметилцеллюлозу, полиакрилатные и полиметакрилатные полимеры и их смеси.
38. Способ по п.28, где фармацевтически приемлемый водонерастворимый полимер включает этилцеллюлозу.
39. Способ по п.28, где пластификатор выбирают из группы, состоящей из диэтилфталата, триацетина, трибутилцитрата, триэтилцитрата, ацетилтри-n-бутилцитрата, дибутилсебацата, полиэтиленгликоля, полипропиленгликоля, касторового масла, ацетилированных моно- и диглицеридов, глицерилмоностеарата, глицерилтриацетата, глицерилтрибутирата, фталатов, цитратов, глицеринтрибутиратов; себацатов, адипатоы, азелаинатов, бензоатов, хлорбутанола, полиэтиленгликолей, растительных масел, оливкового масла, касторового масла, минерального масла, фумаратов, малатов, оксалатов, сукцинатов, бутиратов, сложных эфиров цетилового спирта, малонатов, полисорбатов, глицерина, N-бутилбензолсульфонамида, N-метилпирролидона и их смесей.
40. Способ по п.28, где пластификатор включает диэтилфталат.
41. Способ по п.28, где кроющая композиция продолжительного высвобождения включает этилцеллюлозу и диэтилфталат, растворенные в растворителе, включающем ацетон и воду в весовом соотношении ацетон/вода в диапазоне от приблизительно 85/15 до приблизительно 98/2.
42. Способ по п.28, где соотношение водонерастворимого полимера к пластификатору составляет приблизительно 9:1.
43. Способ по п.28, где композиция наслаивания лекарственного средства включает циклобензаприна гидрохлорид, и после высушивания гранулы с наслоенным лекарственным средством включают от приблизительно 20 вес.% до приблизительно 30 вес.% циклобензаприна гидрохлорида.
44. Способ по п.43, где композиция наслаивания лекарственного средства включает циклобензаприна гидрохлорид, и после высушивания гранулы с наслоенным лекарственным средством включают приблизительно 25 вес.% циклобензаприна гидрохлорида.
45. Способ по п.28, где гранулы немедленного высвобождения включают приблизительно 2% фармацевтически приемлемого водорастворимого полимера.
46. Способ по п.28, где гранулы продолжительного высвобождения включают от приблизительно 7% до приблизительно 12% фармацевтически приемлемого водонерастворимого полимера.
47. Способ по п.28, где гранулы продолжительного высвобождения включают приблизительно 9% фармацевтически приемлемого водонерастворимого полимера и пластификатор.
48. Способ по п.28, где гранулы продолжительного высвобождения обеспечивают профиль высвобождения лекарственного средства, который не отклоняется более чем на приблизительно 10% в любой момент времени в следующей схеме растворения:
через 2 часа высвобождается не более чем приблизительно 40% общего активного;
через 4 часа высвобождается от приблизительно 40-65% общего активного;
через 8 часов высвобождается от приблизительно 60-85% общего активного; и
факультативно через 12 часов высвобождается от приблизительно 75-85% общего активного,
при тестировании с помощью Аппарата 2 по Фармакопее США (перемешивает при 50 rpm) в 900 мл 0,1 N HCl при 37°C.
49. Способ по п.28, где указанный этап покрытия b) осуществляют в атмосфере с точкой росы в диапазоне приблизительно 6-17°C.
50. Способ по п.29, где указанный этап выдерживания c) осуществляют в атмосфере с точкой росы в диапазоне приблизительно 6-17°C.
51. Способ по п.28, где указанный этап покрытия a) осуществляют в атмосфере с точкой росы в диапазоне приблизительно 6-17°C.
52. Способ по п.28, где фармацевтическая композиция включает 30 мг циклобензаприна HCl и обеспечивает максимальную концентрацию в плазме крови (Cmax) в диапазоне приблизительно 80%-125% приблизительно 19,9 нг/мл циклобензаприна HCl и AUC0-168 в диапазоне приблизительно 80%-125% 736,6 нг·час/мл после ее единичного перорального введения.
53. Способ по п.28, где фармацевтическая композиция включает 15 мг циклобензаприна HCl и обеспечивает максимальную концентрацию в плазме крови (Cmax) в диапазоне приблизительно 80%-125% приблизительно 8,3 нг/мл циклобензаприна HCl и AUC0-168 в диапазоне приблизительно 80%-125% 318,3 нг·час/мл после ее единичного перорального введения.
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| Паросиловая установка с промежуточным перегревом пара | 1926 |
|
SU7504A1 |
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| Муравьева И.А | |||
| "Технология лекарств", Изд.3-е, перераб | |||
| и доп | |||
| Т | |||
| I,М., "Медицина", 1980, с370-371 | |||
Авторы
Даты
2015-02-10—Публикация
2009-06-18—Подача