Область техники, к которой относится изобретение
Область относится к заживлению ран и репарации тканей, и к коннексинам, коннексиновым полуканалам и щелевидным контактам, в том числе к композициям, включающим одно или несколько антиконнексиновых средств и одно или несколько лекарственных средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты, изделиям и наборам и средствам доставки, содержащим такие композиции, и составам, включающим такие композиции, а также к способам лечения ран и заболеваний, нарушений или состояний, характеризуемых полностью или частично быстрым, медленным или аномальным заживлением ран, которые были бы полезны для репарации или заживления тканей.
Уровень техники
Текст, приведенный ниже, включает информацию, которая может быть полезной для понимания настоящего изобретения. Это не означает, что любая информация, представленная в этом документе, является предшествующем уровнем техники или релевантной информацией в отношении описанного или заявленного изобретения, или что какая-либо публикация или документ, на которые конкретно или косвенно ссылаются, являются предшествующим уровнем техники.
У людей или других млекопитающих раневое повреждение запускает сложноорганизованный каскад клеточных и биохимических событий, которые в большинстве случаев будут приводить к заживлению раны. Идеально зажившая рана представляет собой рану, которая восстановила обычную анатомическую структуру, функцию и внешний вид на клеточном, тканевом, органном и организменном уровнях. Заживление ран, будь то инициировано травмой, микробами или чужеродными веществами, происходит с помощью сложного процесса, включающего множество перекрывающихся фаз, включая воспаление, эпителизацию, ангиогенез и отложение внеклеточного матрикса. Обычно, эти процессы приводят к созревшей ране и образованию рубца в определенной степени. Хотя воспаление и репарация происходят, главным образом, параллельно описанному ходу событий, чувствительность процесса зависит от баланса между разнообразными молекулами, участвующими в заживлении ран, включающими, например, систему регуляторных цитокинов и факторов роста.
Щелевидные контакты представляют собой мембранные клеточные структуры, которые облегчают прямое взаимодействие клетка-клетка. Канал щелевидного контакта образован двумя коннексонами (полуканалами), каждый из которых состоит из шести субъединиц коннексина. Каждый гексамерный коннексон стыкуется с коннексоном в противоположной мембране, образуя общий щелевидный контакт. Показано, что каналы щелевидного контакта обнаруживаются во всем организме. Ткани, такие как эпителий роговицы, имеют в своем составе от шести до восьми клеточных слоев, тем не менее, они экспрессируют различные каналы щелевидных контактов в различных слоях с помощью коннексина 43 в базальном слое и коннексина 26 от базального слоя до срединных слоев крылатых клеток. В основном, коннексины представляют собой семейство белков, обычно называемых в соответствии с их молекулярной массой или классифицированных на филогенетической основе на альфа-, бета- и гамма-подклассы. Идентифицировано, по меньшей мере, 20 человеческих изоформ и 19 мышиных изоформ. Сообщалось, что различные ткани и типы клеток имеют характерные особенности экспрессии коннексиновых белков, и было показано, что в тканях меняется тип экспрессии коннексиновых белков вследствие повреждения или трансплантации (Qui, С. et al., (2003) Current Biology, 13:1967-1703; Brander et al., (2004), J. Invest Dermatol. 122:1310-20).
Для модуляции экспрессии генов, вовлеченных в вирусные, грибковые и метаболические заболевания, предполагали использование антисмысловых технологий. Смотри, например, U.S. Pat. No. 5,166,195, (олигонуклеотидные ингибиторы HIV) и U.S. Pat. No. 5,004,810 (олигомеры для гибридизации с Vmw65 мРНК вируса простого герпеса и ингибирования репликации). Смотри также U.S. Pat. No. 7,098,190, выданный Becker и Green («Составы, включающие антисмысловые нуклеотиды к коннексинам»). Также сообщалось о пептидных ингибиторах щелевидных контактов и полуканалов. Смотри, например, Berthoud, V.M. et al., Am J. Physiol. Lung Cell Mol. Physiol. 279: L619 - L622 (2000); Evans, W.H. and Boitano, S. Biochem. Soc. Trans. 29:606-612, и De Vriese A.S., et al., Kidney Int. 61:177-185 (2001). Смотри также Becker and Green PCT/US06/04131 («Антиконнексиновые соединения и их применение»).
Различные цитокины и факторы роста исследовали, чтобы определить их потенциал при терапевтическом воздействии на заживление ран. Однако за исключением тромбоцитарного фактора роста, активного ингредиента в Regranex®, ни один из препаратов не одобрен для продажи в США. И, несмотря на успехи в понимании принципов, лежащих в основе процесса заживления ран, остается неудовлетворенной необходимость в подходящих терапевтических средствах для ухода за раной и в улучшении и/или стимулировании заживления ран, в том числе медленного или аномального заживления ран, таких как хронические раны, а также для лечения припухлости, воспаления и рубцевания, ассоциированного с ранами, включающими острые и подострые раны.
Раскрытие изобретения
Изобретения, раскрытые и заявленные в этом документе, обладают многими характеристиками и воплощениями, включающими, но не ограниченными теми, которые изложены или описаны, или которые упоминаются в этом разделе «Раскрытие изобретения». Этот раздел не является всеобъемлющим, и изобретения, описанные и заявленные в этом документе, не ограничивают ни предметы изобретения, ни воплощения, определенные в этом разделе «Раскрытие изобретения», и они включены в целях иллюстрации, но не ограничения.
Изобретение, главным образом, относится к применению одного или нескольких антиконнексиновых средств (например, ингибиторов коннексинов, таких как олигодезоксинуклеотиды альфа-1 коннексина и альфа-1 антиконнексиновых пептидов или пептидомиметики) в комбинации с одним или несколькими терапевтическими средствами, средствами, полезными для заживления ран, и/или средствами, модифицирующими щелевидные контакты, для лечения ран, в том числе острых, подострых, медленно заживающих и хронических ран.
Настоящее изобретение обеспечивает повышение скорости, типа и/или качества заживления ран с помощью применения одного или нескольких антиконнексиновых средств и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты. В предпочтительном воплощении комбинированное применение одного или нескольких антиконнексиновых средств и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты, обладает аддитивным, синергическим или сверхаддитивным эффектом в стимуляции заживления ран. В другом предпочтительном воплощении комбинированное применение одного или нескольких антиконнексиновых средств и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты, обеспечивает применение сниженных доз таких средств в сравнении с дозой или дозами, которые могут быть эффективными, если применяют только одно средство само по себе. В другом предпочтительном воплощении комбинированное применение одного или нескольких антиконнексиновых средств и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты, обеспечивает сокращенную частоту введения в сравнении с частотой введения, если применяют только одно средство само по себе.
Раскрыты и заявлены композиции и способы изобретения, в которых применяют антиконнексиновые средства в комбинации с другими терапевтическими средствами, средствами, полезными для заживления ран, и/или средствами, модифицирующими щелевидные контакты.
Изобретение включает фармацевтические композиции, включающие (а) терапевтически эффективное количество антиконнексинового средства и (b) терапевтически эффективное количество другого терапевтического средства, полезного при лечении раны или для стимуляции заживления ран. Изобретение включает фармацевтические композиции, включающие (а) терапевтически эффективное количество антиконнексинового средства и (b) терапевтически эффективное количество средства, модифицирующего щелевидные контакты. Предпочтительно фармацевтические композиции дополнительно включают фармацевтически приемлемый носитель, разбавитель или эксципиент.
Фармацевтические композиции предоставляют для комбинированного, одновременного, раздельного, последовательного или долговременного введения. В одном воплощении композицию, включающую одно или несколько антиконнексиновых средств, вводят в одно и то же время или в приблизительно одно и то же время в виде одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты.
Фармацевтические композиции также предоставляют в форме комбинированного препарата, например, в виде смеси одного или нескольких антиконнексиновых средств и одного или нескольких других средств, полезных для заживления ран, например, таких как ростовые факторы, которые эффективны для стимуляции или улучшения заживления ран, например тромбоцитарный фактор роста, эпидермальный фактор роста, фактор роста фибробластов (например, FGF2), фактор роста сосудистого эндотелия и трансформирующий фактор роста β3 и/или цитокины, которые эффективны для стимуляции или улучшения заживления ран, такие как IL-7 и IL-10, и/или другие средства, которые эффективны для стимуляции или улучшения заживления ран, такие как IGF (например, IGF-1) и IGFBP (например, IGFBP-2).
Термин «комбинированный препарат» включает «набор частей» в том смысле, что компоненты комбинации, как было определено выше, можно дозировать независимо или путем применения различных фиксированных комбинаций с различающимися количествами компонентов комбинации (а) и (b), т.е. одновременно, раздельно или последовательно. Части набора затем можно вводить, например, одновременно или со смещением по времени, то есть в различные моменты времени и с равными или различными временными интервалами для любой части набора, состоящего из частей.
В предпочтительном воплощении введение комбинированного препарата будет состоять из нескольких временных моментов введения и/или увеличенных интервалов между введением в результате такого комбинированного применения.
В одном аспекте изобретение включает фармацевтические композиции, в том числе формы для местной доставки и составы, включающие фармацевтически приемлемый носитель и терапевтически эффективные количества антиконнексинового средства и одного или нескольких средств, описанных в этом документе. Примеры антиконнексиновых средств включают антиконнексиновые олигодезоксинуклеотиды («ODN»), включающие антисмысловые (в том числе модифицированный и немодифицированный антисмысловой остов молекулы) олигонуклеотиды, РНКи (интерферирующие РНК) и миРНК (малые интерферирующие РНК), а также антиконнексиновые пептиды и пептидомиметики. Подходящие антиконнексиновые средства включают, например, антисмысловые ODN, пептиды и пептидомиметики, направленные против коннексинов 43, 26, 37, 30 и 31.1 и 32. В некоторых воплощениях подходящие композиции включают многочисленные антиконнексиновые средства в комбинации, включающей, например, коннексин 43, 26, 30, и 31.1 вместе с одним или несколькими другими средствами, полезными при заживлении ран и/или репарации ткани. Предпочтительные антиконнексиновые средства направлены на коннексин 43. Предпочтительные средства для применения при заживлении ран в комбинации с одним или несколькими антиконнексиновыми средствами включают некоторые факторы роста, в том числе, например, тромбоцитарный фактор роста, эпидермальный фактор роста, фактор роста фибробластов альфа, фактор роста фибробластов бета, фактор роста сосудистого эндотелия и трансформирующий фактор роста β3, а также инсулиноподобный ростовой фактор. Другие предпочтительные средства для применения при заживлении ран в комбинации с одним или несколькими антиконнексиновыми средствами включают определенные цитокины, в том числе, например, IL-7 и IL-10. Другие предпочтительные средства для применения при заживлении ран в комбинации с одним или несколькими антиконнексиновыми средствами включают тимозин бета-4, ингибитор секреторных лейкоцитарных протеаз, бета-адренергические антагонисты (например, тимоптик), антагонисты рецептора интерлейкина-1 (например, анакинра), ловушки для свободных радикалов (например, N-ацетилцистеин) и векторы для генной терапии, включающие кодирующую последовательность для белка, полезного для стимуляции или улучшения заживления ран (например, аденовирусный вектор, включающий последовательность, кодирующую тромбоцитарный фактор роста-В). Предпочтительные терапевтические средства, вводимые в комбинации с одним или несколькими антиконнексиновыми средствами, включают, например, противовоспалительные средства, антимикробные средства (например, триметоприм), локальные и местные анестетики и местные опиоиды (например, морфин, гидроморфон и фентанил).
В другом аспекте изобретение включает способы введения терапевтически эффективного количества одного или нескольких фармацевтически приемлемых антиконнексиновых средств и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты, составленных в виде препарата с замедленным высвобождением, препарата пролонгированного высвобождения, препарата с контролируемым высвобождением и/или в виде препарата повторного действия субъекту, имеющего рану, в том числе раны, полностью или частично характеризуемые замедленным или неполным заживлением.
В некоторых других аспектах изобретение также относится к способам применения таких композиций для лечения субъекта, страдающего от заболевания, или для лечения субъекта с риском различных заболеваний, нарушений и состояний, ассоциированных с раной, в том числе острыми или подострыми ранами и медленно заживающими или хроническими ранами.
В еще одном аспекте изобретение включает способы лечения субъекта, страдающего любыми заболеваниями, нарушениями и/или состояниями, характеризуемыми полностью или частично наличием раны или ткани, нуждающейся в заживлении, или субъекта с подозрением, или предрасположенностью, или риском таких заболеваний, нарушений и/или состояний. Такие композиции включают, например, формы или составы для местной доставки.
Предпочтительные способы включают последовательное или одновременное введение одного или нескольких антиконнексиновых средств и одного или нескольких средств, полезных для заживления ран, любое из них или все вместе предоставляют в количествах или дозах, которые меньше тех, которые применяют, если средство или средства вводят по отдельности, т.е., если их не вводят в составе комбинации как в физическом смысле, так и во время курса лечения раны. Эти уменьшенные количества вводимых средств обычно составляют примерно от одной двадцатой до примерно одной десятой части от количества или количеств средства, если его вводят по отдельности само по себе, и может составлять примерно одну восьмую часть количества, примерно одну шестую часть количества, примерно одну пятую часть количества, примерно одну четвертую часть количества, примерно одну третью часть количества и примерно одну вторую часть количества, если средство вводят по отдельности само по себе. Предпочтительно введение является последовательным. Предпочтительно средства вводят последовательно друг за другом в пределах, по меньшей мере, получаса. Средства также можно вводить одно за другим в пределах примерно часа, одно за другим в интервале, составляющем примерно от одних суток до одной недели, или другим подходящим образом. Предпочтительно антиконнексиновое средство вводят первым. Предпочтительно, если применяют одно или несколько антиконнексиновых средств, то антиконнексиновый пептид или антиконнексиновый пептидомиметик, например антиконнексиновое средство, которое блокирует или тормозит открытие полуканалов, вводят до антиконнексинового средства, которое блокирует или снижает экспрессию коннексина или образование полуканалов или щелевидных контактов, например, путем регулирующего торможения экспрессии белка коннексина. Предпочтительно антиконнексиновое средство или средства является/являются средством (средствами), направленным (направленными) против коннексина 43.
В следующем аспекте изобретение включает трансдермальные пластыри, повязки, прокладки, компрессы, матриксы и бинты, способные прилипать или связываться с кожей пациента другим способом, указанные изделия способны доставлять субъекту терапевтически эффективное количество одного или нескольких фармацевтически приемлемых антиконнексиновых средств и одного или нескольких дополнительных фармацевтически приемлемых лекарственных средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты.
В другом аспекте изобретение включает готовое изделие, включающее емкость, содержащую терапевтически эффективное количество одного или нескольких фармацевтически приемлемых антиконнексиновых средств и одного или нескольких фармацевтически приемлемых терапевтических средств для стимулирования заживления ран, и инструкции по применению, в том числе по применению для лечения субъекта.
В другом аспекте изобретение включает готовое изделие, включающее емкость, содержащую терапевтически эффективное количество одного или нескольких фармацевтически приемлемых антиконнексиновых средств и одного или нескольких фармацевтически приемлемых средств, полезных для стимулирования заживления ран, и инструкции по применению, в том числе по применению для лечения субъекта.
В другом аспекте изобретение включает готовое изделие, включающее емкость, содержащую терапевтически эффективное количество одного или нескольких фармацевтически приемлемых антиконнексиновых средств и одного или нескольких фармацевтически приемлемых средств, модифицирующих щелевидные контакты, и инструкции по применению, в том числе по применению для лечения субъекта.
Изобретение включает готовое изделие, включающее упаковочный материал, содержащий одно или несколько лекарственных форм, содержащих одно или несколько фармацевтически приемлемых антиконнексиновых средств и одно или несколько фармацевтически приемлемых терапевтических средств, средства, полезные для заживления ран, и/или средства, модифицирующие щелевидные контакты, где упаковочный материал содержит метку, которая указывает на то, что лекарственную форму можно применять субъекту, страдающему любыми заболеваниями, нарушениями и/или состояниями, описанными или упоминаемыми в этом документе, в том числе заболеваниями, нарушениями и/или состояниями, характеризуемыми полностью или частично наличием раны или ткани, нуждающейся в заживлении, или субъекту с подозрением, или предрасположенностью, или риском таких заболеваний, нарушений и/или состояний. Такие лекарственные формы включают, например, формы и композиции для местной доставки.
Изобретение включает композицию, включающую фармацевтически приемлемое антиконнексиновое средство и фармацевтически приемлемое средство, полезное для заживления ран, в количествах, эффективных для того, чтобы стимулировать у субъекта заживление или репарацию тканей. Изобретение включает композицию, включающую фармацевтически приемлемое антиконнексиновое средство и фармацевтически приемлемое лекарственное средство в количествах, эффективных для того, чтобы стимулировать у субъекта заживление ран. Изобретение включает композицию, включающую фармацевтически приемлемое антиконнексиновое средство и фармацевтически приемлемое средство, модифицирующее щелевидные контакты, в количествах, эффективных для того, чтобы стимулировать у субъекта заживление ран. Такие составы включают, например, формы и композиции для местной доставки. Предпочтительные композиции включают одно или несколько антиконнексиновых средств и одно или несколько средств, полезных для заживления ран, любое из них или все вместе предоставляют в количествах или дозах, которые меньше тех, которые применяют, если средство или средства вводят по отдельности, т.е., если их вводят не в составе комбинации как в физическом смысле, так и во время курса лечения раны. Эти уменьшенные количества вводимых или предоставляемых в комбинации средств обычно составляют примерно от одной двадцатой до примерно одной десятой части от количества или количеств средства, если его вводят по отдельности само по себе, и может составлять примерно одну восьмую часть количества, примерно одну шестую часть количества, примерно одну пятую часть количества, примерно одну четвертую часть количества, примерно одну третью часть количества и примерно одну вторую часть количества, если его вводят по отдельности само по себе.
Изобретение включает способы применения терапевтически эффективных количеств композиций, включающих одно или несколько фармацевтически приемлемых антиконнексиновых средств и одно или несколько фармацевтически приемлемых терапевтических средств, средства, полезные для заживления ран, и/или средства, модифицирующие щелевидные контакты, при изготовлении лекарственного средства. Такие лекарственные средства включают, например, формы и композиции для местной доставки. Такие лекарственные средства включают средства для лечения субъекта, как описано в этом документе. Такие лекарственные средства предпочтительно включают сниженные количества одного или нескольких антиконнексиновых средств и одного или нескольких фармацевтически приемлемых терапевтических средств, средства, полезные для заживления ран, и/или средства, модифицирующих щелевидные контакты, как было отмечено в этом документе.
Изобретение включает способы применения терапевтически эффективного количества одного или нескольких антиконнексиновых средств и одного или нескольких фармацевтически приемлемых терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты, при изготовлении лекарственной формы. Такие лекарственные формы включают, например, формы и композиции для местной доставки. Такие лекарственные формы включают формы для лечения субъекта, как было описано в этом документе. Такие лекарственные формы предпочтительно включают сниженные количества одного или нескольких антиконнексиновых средств и одного или нескольких фармацевтически приемлемых терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующие щелевидные контакты, как было отмечено в этом документе.
В другом аспекте изобретение обеспечивает способ лечения, включающий введение субъекту фармацевтической композиции изобретения для применения при лечении раны, в том числе, например, острой, подострой, медленно заживающей и хронической раны.
В другом аспекте изобретение обеспечивает применение антиконнексинового средства (например, анти-альфа-1 ODN, пептида или пептидомиметика) и терапевтического средства, средства, полезного для заживления ран, и/или средства, модифицирующего щелевидные контакты, для изготовления фармацевтического продукта для стимулирования заживления ран у пациента, которому это необходимо.
В еще одном аспекте изобретение обеспечивает способ стимулирования или улучшения заживления ран или лечения, или профилактики, или уменьшения интенсивности симптомов фиброза или других фиброзных состояний, способ, включающий введение одного или нескольких антиконнексиновых средств и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты, у пациента, которому это необходимо.
В другом аспекте изобретение обеспечивает: (i) упаковку, включающую антиконнексиновое средство вместе с инструкцией по применению в комбинации с терапевтическими средствами, средствами, полезными для заживления ран, и/или средствами, модифицирующими щелевидные контакты, для стимулирования (например, для уменьшения времени заживления, для более благоприятного результата лечения раны) заживления ран, (ii) упаковку, включающую одно или несколько терапевтических средств, средства, полезные для заживления ран, и/или средства, модифицирующие щелевидные контакты, вместе с инструкцией по применению в комбинации с одним или несколькими антиконнексиновыми средствами для стимулирования заживления ран; и (iii) упаковку, включающую одно или несколько антиконнексиновых средств и одно или несколько терапевтических средств, средства, полезные для заживления ран, и/или средства, модифицирующие щелевидные контакты, вместе с инструкциями по применению при стимулировании заживления ран или ослабления фиброза, связанного с ранами.
В одном воплощении фармацевтический продукт изобретения предоставляют в комбинации с повязкой для ран или матриксом для стимулирования заживления ран. Соответственно, повязку для ран или матрикс предоставляют в том числе в форме твердого субстрата с антиконнексиновым средством и одним или несколькими терапевтическими средствами, средствами, полезными для заживления ран, и/или средствами, модифицирующими щелевидные контакты, диспергированными на поверхности или внутри твердого субстрата.
Антиконнексиновое средство и терапевтические средства, средства, полезные для заживления ран, и/или средства, модифицирующие щелевидные контакты, можно вводить в одной и той же композиции или в различных композициях. Предпочтительно средства вводят в уменьшенных количествах одного или нескольких антиконнексиновых средств и одного или нескольких фармацевтически приемлемых терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты, как было отмечено в этом документе.
Антиконнексиновое средство и терапевтические средства, средства, полезные для заживления ран, и/или средства, модифицирующие щелевидные контакты, можно вводить пациенту одновременно, последовательно или по отдельности. Если средства вводят по отдельности, предпочтительно антиконнексиновое средство и лечебное средство, средство, полезное для заживления ран и/или средство, модифицирующее щелевидные контакты, вводят последовательно. Предпочтительно средства вводят последовательно друг за другом, по меньшей мере, в пределах получаса. Средства также можно вводить одно за другим примерно через час, одно за другим через интервал, составляющий примерно от одних суток до одной недели, или иным подходящим способом. Предпочтительно антиконнексиновое средство вводят первым. Предпочтительно, если применяют одно или несколько антиконнексиновых средств, то антиконнексиновый пептид или антиконнексиновый пептидомиметик, например антиконнексиновое средство, которое блокирует или тормозит открытие полуканалов, вводят до антиконнексинового средства, которое блокирует или снижает экспрессию коннексина или образование полуканалов или щелевидных контактов, например, путем регулирующего торможения экспрессии белка коннексина. Предпочтительно антиконнексиновое средство или средства является/являются средством (средствами), направленным (направленными) против коннексина 43.
Эти и другие аспекты настоящих изобретений, которые не ограничены объемом информации, приведенной в разделе «Раскрытие изобретения», представлены ниже.
Краткое описание фигур
Фигуры 1A-1I показывают экспрессию Сх43 в областях раны. Фигура 1А показывает результаты ПЦР-анализа в режиме реального времени экспрессии гена Сх43 в областях раны. Фигура 1А показывает уровень экспрессии Сх43 относительно экспрессии GAPDH в 1-ый и на 7-ой день в области раны, обработанной контрольными sODN (n=4; неокрашенные столбцы) и Сх43 asODN (n=4; закрашенные столбцы); результаты выражены в виде среднего значения ± стад.ош.средн. *Р<0,05. Фигуры 1B-1F показывают окрашивание на Сх43 (зеленое) совместно с ядерным окрашиванием бис-бензимидом (синее) раны, обработанной Сх43 asODN (фигура 1В: 1-ый день, фигура 1D: 2-ой день и фигура 1F: 7-ой день) или контролями (фигура 1C: 1-ый день, фигура 1Е: 2-ой день и фигура 1G: 7-ой день). Фигуры 1Н и 1I показывают схему изображенных участков на краю раны. Фигура 1Н изображает В-Е. Фигура 1I изображает F и G.
Фигуры 2А-2Н показывают пролиферацию клеток после нанесения раны. Фигуры 2A-2D показывают анализ пролиферации клеток в областях раны с помощью иммуногистохимического окрашивания с помощью моноклонального антитела к BrdU для контрольных ODN (фигура 2А: 2-ой день и фигура 2С: 7-ой день) и для Сх43 asODN (фигура 2В: 2-ой день и фигура 2D: 7-ой день). Острие стрелки и стрелка указывают на границу раны и переднюю кромку, соответственно. Фигуры 2Е-2Н показывают BrdU-окрашенные клетки; (i) и количество BrdU-позитивных клеток в поле в границах раны в эпидермисе (фигура 2Е: n=5) и зарождающемся эпидермисе (фигура 2F: n=5); (ii) количество BrdU-позитивных клеток на дермальной кромке раны (фигура 2G: n=5) и в формирующейся грануляционной ткани (фигура 2Н: n=5). Количества выражают в виде среднего значения ± стад.ош.средн. *Р<0,05. Графический масштаб соответствует 200 мкм.
Фигуры 3А-3С показывают рекрутинг нейтрофилов в зону раны. Фигура 3А и фигура 3В показывают рекрутинг нейтрофилов в кожные раны, обработанные контрольными sODN (фигура 3А) и Сх43 (фигура 3В), анализированные с помощью антитела к МРО в 1-ый день. Фигура 3С показывает количество МРО-позитивных клеток в зоне раны после обработки контрольными sODN (неокрашенные столбцы: n=4 в 1-ый день; n=5 во 2-ой день) и Сх43 asODN (закрашенные столбцы: n=3 в 1-ый день; n=4 во 2-ой день). Результаты выражены в виде среднего значения ± стад.ош.средн. *Р<0,05. Графический масштаб соответствует 50 мкм.
Фигуры 4А-4С показывают рекрутинг макрофагов в зону раны. Фигура 4А и фигура 4В показывают рекрутинг макрофагов в кожные раны, обработанные контрольными sODN (фигура 4А) и Сх43 asODN (фигура 4В), анализированные с помощью антитела к F4/80 на 7-ой день. Фигура 4С показывает рекрутинг макрофагов в кожные раны на 2-ой и 7-ой день после обработки контрольными sODN (неокрашенные столбцы: n=4 на 2-ой день; n=7 на 7-ой день) и Сх43 asODN (закрашенные столбцы: n=4 на 2-ой день; n=6 на 7-ой день). Результаты выражены в виде среднего значения ± стад.ош.средн. *Р<0,01. Графический масштаб соответствует 50 мкм.
Фигуры 5А-5В показывают экспрессию Cc12 и TNF-α в областях раны. Фигура 5А и Фигура 5В показывают ПЦР-анализ экспрессии гена Cc12 и TNF-α в режиме реального времени в областях раны. Уровень экспрессии Cc12 (фигура 5А) и TNF-α (фигура 5В) относительно экспрессии GAPDH на 1-ый, 2-ой и 7-ой день (для каждого n=5) после обработки контрольными sODN (неокрашенные столбцы) или Сх43 asODN (закрашенные столбцы) оценивали количественно. Результаты выражены в виде среднего значения ± стад.ош.средн. *Р<0,05.
Фигуры 6А-6K показывают экспрессию TGF-β1. Фигуры 6A-6J показывают иммуногистохимический анализ TGF-β1 в зонах раны, обработанной контрольными sODN (фигуры 6А-6Е) и Сх43 asODN (фигуры 6F-6J). Графический масштаб соответствует 200 мкм (фигуры 6А и 6F) и 50 мкм (фигуры 6В-6Е и 6G-6J). Черные стрелки указывают на зарождающийся край эпидермиса. Окрашивание TGF-β1 значительно сильнее в эпидермисе ран, обработанных Сх43 asODN (фигуры 6I и 6J), в сравнении с ранами, обработанными контрольными sODN (фигуры 6D и 6Е). Красные и черные концы стрелок показывают типичные TGF-β1-удлиненные фибробластоподобные клетки и округлые клетки, предположительно, лейкоциты, соответственно. Фигура 6K показывает ПЦР-анализ в режиме реального времени экспрессии мРНК TGF-β1 на 1-ый, 2-ой и 7-ой день (для каждого n=5) в зонах раны, обработанной контрольными sODN (неокрашенные столбцы) или Сх43 asODN (закрашенные столбцы). Результаты выражены в виде среднего значения ± стад.ош.средн. *Р<0,05.
Фигуры 7A-7F показывают образование грануляционной ткани и миграцию фибробластов. Фигуры 7А и 7В показывают рекрутинг фибробластоподобных клеток в кожные раны, обработанные контрольными sODN (фигура 7А) и Сх43 asODN (фигура 7В), анализируемые с помощью TRITC-фаллоидина и ядерного окрашивания с помощью DAPI на 2-ой день. Фигура 7С показывает количество фибробластоподобных клеток в каждом участке раны в поле зрения раны, обработанной контрольными sODN (неокрашенные столбцы: n=5) или Сх43 asODN (закрашенные столбцы: n=5). Фигура 7D показывает результаты анализа заживления ран для миграции фибробластов, которые демонстрируют, что миграция происходит значительно быстрее после обработки Сх43 asODN. Фигуры 7Е и 7F показывают изображения ран в культурах фибробластов в момент нанесения раны (фигура 7Е) и 4 часа спустя после нанесения раны (фигура 7F). Результаты выражены в виде среднего значения ± стад.ош.средн. *Р<0,02, **Р<0,01. Графический масштаб соответствует 50 мкм.
Фигуры 8А-8В показывают экспрессию коллагена в зоне раны. Фигура 8А показывает содержание коллагена, оцененное с помощью количественного измерения гидроксипролина (HP) на 7-ой, 10-ый и 14-ый день после нанесения раны, в областях раны, обработанной контрольными sODN (неокрашенные столбцы) и Сх43 asODN (закрашенные столбцы), и в неповрежденной коже (n=5). Результаты выражены в виде среднего значения ± стад.ош.средн. Р<0,05. Фигура 8В показывает ПЦР-анализ в режиме реального времени экспрессии мРНК на 1-й, 2-й и 7-й день (для каждого n=5) для Co11α1 в областях раны, обработанной контрольными sODN (неокрашенные столбцы) и Cx43 asODN (закрашенные столбцы). Результаты выражены в виде среднего значения ± стад.ош.средн. *Р<0,05.
Фигуры 9А-9С показывают сокращение грануляционной ткани. Фигуры 9А и 9В показывают Н&Е-окрашивание грануляционной ткани через 14 дней после нанесения повреждения в ранах, обработанных контрольными sODN (фигура 9А) и asODN (фигура 9В). Фигура 9С показывает поверхность грануляционной ткани после обработки контрольными sODN (неокрашенные столбцы) или Cx43 asODN (закрашенные столбцы), анализируемой на 5-ый день (контроль; n=7, asODN; n=6), 7-ой день (контроль; n=5, asODN; n=5), 10-ый день (контроль; n=5, asODN; n=6) и 14-ый день (контроль; n=5, asODN; n=6). Измерение поверхности грануляционной ткани на 5-й день показывает немного меньшую поверхность после обработки с помощью asODN, но уменьшение становится значительным на 7-й, 10-й и 14-й день (*Р<0,05. **Р<0,01). Результаты выражены в виде среднего значения ± стад.ош.средн. Графический масштаб соответствует 1 мм.
Фигуры 10А-10С показывают апоптоз в области ран. Фигура 10А и 10В показывают TUNEL-окрашивание грануляционной ткани в ранах, обработанных контрольными sODN (фигура 10А) и Cx43 asODN (фигура 10В), на 7-ой день. Апоптотические клетки появляются в виде ярких зеленых пятен, некоторые из них выделены с помощью острия стрелок. Графический масштаб соответствует 50 мкм. Фигура 10С показывает количество апоптотических клеток в поле зрения на 5-й, 7-й и 10-й день (для каждого n=6) в области ран, обработанных контрольными sODN (неокрашенные столбцы) и Cx43 asODN (закрашенные столбцы). Результаты выражены в виде среднего значения ± стад.ош.средн. Графический масштаб соответствует 50 мкм.
Фигуры 11A-11F показывают созревание миофибробластов в области ран. Фигуры 11А и 11D показывают окрашивание с помощью антител к гладкомышечному α-актину (SMA) (зеленое окрашивание) с совместным окрашиванием ядер бис-бензимидом (синее окрашивание) кромки грануляционной ткани на 7-й день после нанесения раны (фигуры 11А и 11В) и центра грануляционной ткани на 10-й день после нанесения раны (фигуры 11С и 11D). Фигура 11Е показывает количественную оценку уровня окрашивания, демонстрирующую более значительное SMA-окрашивание в ранах, обработанных Cx43 asODN, по сравнению с контролями на 7-й день (P=0,004), что указывает на более раннее созревание и дифференцировку миофибробластов. Это более развившееся созревание все еще присутствовало на 10-ый день, когда большая часть SMA-окрашивания и миофибробластов утрачена в ранах, обработанных Cx43 asODN, но окрашивание все еще было сильным в контрольных ранах (Р=0,000002). Фигура 11F показывает схему изображенных участков в грануляционной ткани: зона I (фигуры 11А и 11В) и зона II (фигуры 11С и 11D). Результаты выражены в виде среднего значения ± стад.ош.средн. Графический масштаб соответствует 25 мкм.
Фигуры 12А-12Н показывают ангиогенез в области ран. Фигуры 12A-12F показывают окрашивание грануляционной ткани зарождающихся кровеносных сосудов на фактор фон Виллебранда (зеленое окрашивание) совместно с окрашиванием ядер бис-бензимидом (синее окрашивание) на 7-й день (фигуры 12А и 12В), 10-й день (фигуры 12С и 12D) и 14-й день (фигуры 12Е и 12F) после нанесения раны. В обработанных антисмысловым соединением ранах (фигуры 12А, 12С и 12Е) кровеносные сосуды были более распространенными в начальные моменты времени (7-й день, фигуры 12А и 12В, и 10-й день, фигуры 12С и 12D), но значительно более выражено, чем в ранах, обработанных контрольными ODN (фигуры 12В, 12D и 12F), что приводило к значительно слабому окрашиванию по сравнению с контролями (7-й день *Р=0,0019; 10-й день **Р=0,015). К 14-му дню кровеносные сосуды увеличивались в размере в asODN-группе и были тех же самых размеров, что сосуды в контрольной группе (фигура 12G). Фигура 12Н показывает схему изображенных участков в грануляционной ткани: зона I (фигуры 12А и 12В) и зона II (фигуры 12С-12Е). Результаты выражены в виде среднего значения ± стад.ош.средн. Графический масштаб соответствует 25 мкм.
Фигуры 13А-13В показывают макроскопические изображения заживления ран (фигура 13А) и изменения поверхности раны (фигура 13В) после обработки с помощью asODN относительно контрольной обработки.
Фигура 14 показывает химеру лимбального кольца человека - денудированного стромального матрикса свиньи.
Фигура 15 показывает примеры связывания факторов роста и цитокинов с матрицей антител, применяемой для детекции уровня белков для 120 различных ростовых факторов и цитокинов. На каждой из двух матричных мембран проводили анализ четырех образцов (60 факторов роста/цитокинов на мембрану с повторами и как с позитивными, так и с негативными контролями).
Фигура 16 показывает анализ уровня факторов роста в химерной строме в сравнении с участками лимбального кольца спустя две недели. Это контрольная роговица (без обработки антисмысловым соединением). Два ростовых фактора представляют особый интерес (указано стрелками). Это очень высокий уровень IGFBP-2 в химерной строме и повышенный уровень IGF-1 в лимбальном кольце. Было сообщено, что первый важен для стимулирования миграции клеток (которые могут важными для повторного заселения стромы стромальными кератиноцитами из лимбального кольца), а последний важен для стимулирования пролиферации клеток (которые могут быть важными в лимбальном кольце для обеспечения источника клеток, повторно заселяющих строму).
Фигура 17 показывает результаты анализа уровня факторов роста в химерной строме по сравнению с участками лимбального кольца спустя две недели культивирования (на основе данных, полученных для роговицы, обработанной Сх43 asODN). Два ростовых фактора представляют особый интерес (указано стрелками). Это высокий уровень IGF-7 в химерной строме, обработанной антисмысловым соединением, в сравнении с необработанными контролями, и повышенный уровень IGFBP-2 как в лимбальном кольце, так и в строме в сравнении с необработанными контролями, в особенности, с контрольными лимбальными кольцами. Было сообщено, что первый важен для стимулирования эпителиального роста (в соответствии с повышенной реэпитализацией, обнаруженной в химерах, обработанных антисмысловым соединением), а последний важен для стимулирования миграции клеток (в соответствии с повышенным повторным заселением эпителия из лимбального кольца после обработки антисмысловым соединением).
Фигура 18 иллюстрирует группу типичных цитокинов, которые были идентифицированы на основе повышенного уровня их экспрессии при воспалении в сравнении с моделями ран с незначительным воспалением. Эти типичные цитокины могут служить подходящими мишенями для модулирования заживления ран.
Фигура 19 иллюстрирует группу типичных цитокинов, которые были идентифицированы на основе повышенного уровня их экспрессии в модели ран с незначительным воспалением в сравнении с воспалительной моделью. Эти типичные цитокины могут служить подходящими мишенями для модулирования заживления ран.
Осуществление изобретения
Определения
Используемый в этом документе термин «нарушение» означает любое нарушение, заболевание или состояние, при котором полезным будет средство, которое стимулирует заживление ран и/или ослабляет припухлость, воспаление и/или образование рубцов. Например, сюда включены раны, возникающие в результате хирургической операции или травмы, и рана, ассоциированная с патологиями в связи с невропатической, ишемической, микрососудистой патологией, давлением на поверхность костей (копчиковая (крестцовая), бедренная (вертлужная), ягодичная (седалищная) или пяточная область ступни), реперфузионным повреждением и этиологией рефлекса клапана и состояниями.
Используемый в этом документе термин «субъект» относится к любому млекопитающему, в том числе к людям, ручным и сельскохозяйственным животным и животным, связанным с зоопарком, спортом, или домашним животным, таким как собаки, лошади, кошки, овцы, свиньи, коровы и т.д. Предпочтительное млекопитающее - человек, в том числе взрослые, дети и пожилые люди.
Используемый в этом документе термин «предупреждение» означает полное или частичное предупреждение или улучшение, или регулирование симптомов.
Используемый в этом документе термин «терапевтически эффективное количество» в отношении соединений или композиций рассматриваемого изобретения относится к количеству, достаточному для того, чтобы получить желаемый биологический, фармацевтический или терапевтический результат. Этим результатом может быть улучшение признаков, симптомов или причин заболевания, или нарушения, или состояния, или любое другое желаемое изменение биологической системы. В настоящем изобретении результат будет включать полное или частичное стимулирование заживления ран и уменьшение припухлости, воспаления и/или образования рубцов.
Используемый в этом документе термин «лечение» относится как к терапевтическому лечению, так и к профилактике или предупредительным мерам. Такое лечение необходимо при расстройствах с уже существующими ранами или другого родственного нарушения, а также при расстройствах с предрасположенным возникновением раны или родственного нарушения, или при расстройствах с диагностированным нарушением, или при расстройствах, при которых нарушение следует предупреждать.
Используемый в этом документе термин «антиконнексиновые средства» представляют собой соединения, которые затрагивают или модулируют активность, экспрессию или образование коннексина, коннексинового полуканала (коннексона) или щелевидного контакта. Антиконнексиновые средства включают, без ограничения, антисмысловые соединения (например, антисмысловые полинуклеотиды), соединения РНКи и миРНК, антитела и их связывающие фрагменты и пептиды и полипептиды, которые включают «пептидомиметики» и аналоги пептидов. Предпочтительные антиконнексиновые средства представляют собой средства, направленные против коннексина 43. Примеры антиконнексиновых средств обсуждаются в этом документе более детально далее.
Используемый в этом документе термин «лечение» относится как к терапевтическому лечению, так и к профилактике или предупредительным мерам. Такое лечение необходимо при расстройствах с уже существующим нарушением, а также при расстройствах с предрасположенным возникновением нарушения, или при расстройствах с диагностированным нарушением, или при расстройствах, при которых нарушение следует предупреждать.
Термины «пептидомиметик» и «миметик» включают природные и синтетические химические соединения, которые могут иметь в значительной степени сходные структурные и функциональные свойства с участками белка, которые они имитируют. В случае коннексинов они могут имитировать, например, внеклеточные петли противостоящих коннексинов, вовлеченных в соединение коннексон-коннексон и образование каналов между клетками.
«Пептидные аналоги» относятся к соединениям со свойствами, аналогичными свойствам пептида-эталона, и могут быть непептидными лекарственными средствами. «Пептидомиметики» (также известные как «миметические пептиды»), которые включают соединения на пептидной основе, также включают непептидные соединения, такие как пептидные аналоги. Пептидомиметики, которые структурно сходны с терапевтически полезными пептидами, могут применяться для достижения эквивалентного или улучшенного терапевтического или профилактического эффекта. Обычно пептидомиметики структурно идентичны или похожи на эталонный полипептид (т.е. полипептид, который имеет биологическую или фармакологическую функцию или активность), но также могут иметь одну или несколько пептидных связей, необязательно замененных связями, выбираемыми из группы, состоящей, например, из -CH2NH-, -CH2S-, -СН2-СН2-, - СН-СН- (цис и транс), -СОСН2-, -СН(ОН)СН2- и -CH2SO-. Миметик может быть полностью состоящим из природных аминокислот или из неприродных аналогов аминокислот, или представляет собой химерную молекулу, состоящую частично из пептида с природными аминокислотами и частично из неприродных аналогов аминокислот. Миметик также может включать некоторое количество консервативных аминокислотных замен, если только такие замены действительно не изменяют миметическую активность. Например, миметическая композиция может быть полезной в качестве антиконнексинового средства, если она способна к регулирующему торможению биологического действия или активностей коннексиновых белков или коннексонов, таких как, например, предотвращение соединения коннексонов для создания опосредованного щелевыми контактами межклеточного информационного взаимодействия или предотвращение открытия коннексонов для экспонирования цитоплазмы клеток во внеклеточную среду. Пептидомиметики, миметические пептиды и пептиды, модулирующие коннексин, охватывают соединения, раскрытые как пептидомиметики, миметические пептиды и пептиды, модулирующие коннексин, и предложенные в этом документе, а также те, которые могут быть известны в этой области техники, будь то соединения, известные в настоящее время или те, которые будут разработаны в будущем.
Термины «модулятор» и «модулирование активности коннексинов», используемые в этом документе в различном виде, относятся к полному или частичному ингибированию коннексина или коннексинового полуканала, и они могут функционировать в качестве антиконнексиновых средств.
Обычно термин «белок» относится к любому полимеру из двух или более индивидуальных аминокислот (независимо от того, встречаются ли они в природе), связанных между собой с помощью пептидных связей, которые образованы, если углеродный атом карбоксильной группы, связанной с альфа-углеродом одной аминокислоты (или аминокислотного остатка) ковалентно связывается с атомом азота аминогруппы, связанной с альфа-углеродом соседней аминокислоты. Эти пептидные связи и атомы, включающие их (например, альфа-углеродные атомы, атомы углерода карбоксильной группы (и замещающие их атомы кислорода) и атомы азота аминогрупп (и замещающие их атомы водорода)), образуют «полипептидный скелет» белка. Кроме того, используемый в этом документе термин «белок» включает термины «полипептид» и «пептид» (которые, время от времени могут использоваться в этом документе взаимозаменяемо). Сходным образом, белковые фрагменты, аналоги, производные и варианты могут быть отнесены в этом документе к «белкам» и будут считаться «белком», если только не будет оговорено противное. Термин «фрагмент» белка относится к полипептиду, включающему не все аминокислотные остатки белка. «Домен» белка также является фрагментом и включает аминокислотные остатки белка, часто необходимые для предоставления активности или функции.
Используемый в этом документе термин «одновременно» применяют для обозначения того, что одно или несколько средств изобретения вводят параллельно, тогда как термин «в комбинации» применяют для обозначения того, что их вводят, если не одновременно или физически вместе, то «последовательно» в пределах промежутка времени, за который оба средства доступны для терапевтического действия. Таким образом, «последовательное» введение может обеспечить введение одного средства в течение минут (например, в течение 1, 2, 3, 4, 5, 10, 15, 20, 25, 30 минут) или примерно за часы, дни, недели или месяцы после другого средства, обеспечивая чтобы одно или несколько антиконнексиновых средств и одно или несколько терапевтических средств, средства, полезные для заживления ран, и/или средства, модифицирующие щелевидные контакты, одновременно присутствовали в эффективных количествах. Время интервала между введением или введениями компонентов будет различаться в зависимости от точной природы компонентов, их взаимодействия и соответствующего времени их полураспада.
Термин «рана» означает повреждение любой ткани, в том числе, например, острые, подострые, медленно заживающие или трудно заживающие раны и хронические раны. Примеры ран могут включать как открытые, так и закрытые раны. Раны включают, например, ожоги, резаные раны, резекции, разрывы, царапины, колотые раны или проникающие раны, хирургические раны, ушибы, гематомы, раздробленные повреждения и язвы.
Как было описано в этом документе, медленно заживающая или трудно заживающая рана может включать, например, рану, которая характеризуется, по меньшей мере, частично одним или несколькими признаками: 1) продолжительной воспалительной фазой, 2) медленным образованием внеклеточного матрикса (ЕСМ) и 3) замедленной или сниженной скоростью эпителизации.
Используемый в этом документе термин «хронические раны» может относиться, например, к ране, которая характеризуется, по меньшей мере, частично одним или несколькими признаками: 1) хроническим непроходящим состоянием воспаления раны, 2) неполноценным или дефектным ЕСМ раны, 3) слабо реагирующими (стареющими) клетками в ране, в частности фибробластами, ограничивающими образование ЕСМ, и 4) нарушением реэпителизации частично из-за потери необходимого взаимодействия ЕСМ и потери матрикса для миграции. Хронические раны включают венозные язвы, артериальные язвы, пролежни, васкулитные язвы и диабетические язвы.
Термин «повязка» относится к повязке на рану для местного применения и исключает композиции, подходящие для системного введения. Например, одно или несколько антиконнексиновых средств и/или одно или несколько средств, полезных для заживления ран, терапевтические средства и/или средства, модифицирующие щелевидные контакты, можно диспергировать внутри или на поверхности плотной прослойки из материала, контактирующего с раной, такого как тканый или нетканый текстильный материал, или можно диспергировать в слой пены, такой как полиуретановая пена, или в гидрогель, такой как полиуретановый гидрогель, полиакрилатный гидрогель, желатин, карбоксиметилцеллюлоза, пектин, альгинат и/или гидрогель гиалуроновой кислоты, например, в гель или мазь. В некоторых воплощениях антиконнексиновое средство и/или указанное одно или несколько средств, полезных для заживления ран, терапевтические средства и/или средства, модифицирующие щелевидные контакты, диспергируют внутри или на поверхности биодеградируемого прослоечного материала, который обеспечивает замедленное высвобождение активных ингредиентов в рану, например прослойки из лиофилизированного коллагена, смесей лиофилизированного коллагена/альгината (доступных в продаже под зарегистрированной торговой маркой FIBRACOL от фирмы Johnson & Johnson Medical Limited) или лиофилизированного коллагена/окисленной регенерированной целлюлозы (доступных в продаже под зарегистрированной торговой маркой PROMOGRAN от фирмы Johnson & Johnson Medical Limited).
Используемый в этом документе термин «матрикс» включает, например, матриксы, такие как коллаген, бесклеточный матрикс, поперечно-сшитые биологические каркасные молекулы, биоинженерный структурный каркас на основе тканей, биопротезы промышленного изготовления и другие имплантированные структуры, такие как, например, сосудистые трансплантаты, пригодные для включения клеток и пролиферации, полезной при стимулировании заживления ран. Дополнительный подходящий биоматриксный материал может включать химически модифицированную коллагеновую ткань для снижения антигенности и иммуногенности. Другие подходящие примеры включают коллагеновые прослойки для повязок на раны, бесклеточный матрикс, не содержащий антигены или с пониженным содержанием антигенов (Wilson et al., Trans Am Soc Artif Intern 1990; 36:340-343), или другой биоматрикс, который сконструирован, чтобы уменьшить антигенную реакцию на ксенотрансплантатный материал. Другой матрикс, полезный для стимулирования заживления ран, может включать, например, белки переработанного бычьего перикарда, включающие нерастворимый коллаген и эластин (Courtman et al., J Biomed Mater Res 1994; 28:655-666) и другую бесклеточную ткань, которая может быть полезной для обеспечения естественного микроокружения при миграции клеток хозяина для стимулирования регенерации тканей (Malone et al., J Vase Surg 1984; 1:181-91). В некоторых воплощениях матриксный материал может быть дополнен средствами, полезными для заживления ран, такими как факторы роста, или другие средства, стимулирующие заживление ран, предназначенные для высвобождения в специфических участках, терапевтические средства и/или средства, модифицирующие щелевидные контакты.
Раны и классификация ран
В дополнение к уже данному ранее определению термин «рана» может также включать, например, повреждения кожи и подкожной ткани, вызванные различными способами (например, пролежнями из-за продолжительного постельного режима и ранами, вызванными травмой) и имеющие различные характеристики. Раны можно классифицировать на четыре типа в зависимости от глубины раны: i) тип I: раны, ограниченные эпителием; ii) тип II: раны, простирающиеся внутрь дермы; iii) тип III: раны, простирающиеся в подкожную ткань; и iv) тип IV (или раны на всю толщу кожи): раны с выставленными наружу костями (например, точка пережатия кости, такой как большой вертел или крестец). Термин «рана на неполную толщину кожи» относится к ранам, которые охватывают типы I-III; примеры ран на полную толщину кожи включают ожоговые раны, пролежни, застойные венозные язвы и диабетические язвы. Термин «глубокая рана» включает как раны типа III, так и раны типа IV. Композиции и способы настоящего изобретения предполагают лечение ран всех типов, в том числе и глубоких ран и хронических ран. Термин «хроническая рана» относится к ране, которая не была вылечена. Предпочтительно ее выбирают из группы, состоящей из венозных язв, пролежней, васкулитных язв, диабетических язв и пролежневых язв. Хронические кожные раны включают, например, пролежневые язвы, диабетические язвы, венозные язвы, васкулитные язвы, артериальные язвы и смешанные язвы. Хроническая рана может быть артериальной язвой, которая включает изъязвления, возникающие в результате полной или частичной блокады артерий. Хроническая рана может быть застойной венозной язвой, которая включает изъязвления, возникающие в результате дефекта венозного клапана и ассоциированного сосудистого заболевания. Хроническая рана может быть язвой, вызванной травмой, диабетической язвой или васкулитной язвой.
Пролежневая язва: пролежневую язву можно классифицировать на 4 стадии в соответствии с руководящими положениями AHCPR (Агентство по политике и исследованиям в области здравоохранения, Министерство здравоохранения и социальных служб США): стадия 1: пролежневая язва стадии 1 представляет собой заметное изменение интактной кожи, связанное со сжатием, показатели которого в сравнении с соседней или противолежащей поверхностью тела могут включать изменение одного или нескольких следующих признаков: температура кожи (ощущение теплоты или прохлады), степень плотности ткани (ощущение твердости или дряблости) и/или чувствительность (боль, кожный зуд). Язва возникает как определенная поверхность устойчивого покраснения в слегка пигментированной коже, тогда как на коже темных тонов язва может появляться в виде непроходящего красного, синего или фиолетового окрашивания. Язва стадии 1 может включать эритему интактной кожи, которая не бледнеет при надавливании, и поражение, предвещающее изъязвление кожи. У субъектов с темным цветом кожи изменение цвета кожи, ощущение тепла, отек, уплотнение и твердость также могут быть указанием на изъязвление стадии 1. Стадия 2: изъязвление стадии 2 может характеризоваться частичным уменьшением толщины кожных покровов, включающих эпидермис, дерму или и то, и другое вместе. Язва является неглубокой и клинически присутствует в виде царапины, волдыря или небольшой вмятины. Стадия 3: изъязвление на стадии 3 может характеризоваться утратой кожи на всю толщину, включающей от повреждения до некроза подкожной ткани, которые могут распространяться внутрь, но не сквозь расположенную ниже фасцию. Язва клинически присутствует в виде глубокой вмятины с разрушением или без разрушения соседней ткани. Стадия 4: изъязвление на стадии 4 может характеризоваться утратой кожи на всю толщину с обширным разрушением, некрозом тканей или повреждением мышцы, кости или поддерживающих структур (например, сухожилия, суставной сумки). В некоторых воплощениях предоставляют композиции и способы лечения хронической раны, где хроническая рана характеризуется одной или несколькими следующими стадиями пролежневого изъязвления в соответствии с AHCPR: стадией 1, стадией 2, стадией 3 и/или стадией 4.
Пролежни: Пролежень может появляться в результате продолжительного и непрекращающегося давления на костный выступ, что приводит к ишемии. Рана имеет тенденцию к появлению у пациентов, которые сами не могут изменять положение тела из-за бездействующего состояния, например у парализованных, находящихся без сознания, или тяжело истощенных людей. Как определено Министерством здравоохранения и социальных служб США, основные профилактические меры включают идентификацию пациентов с повышенным риском; частое обследование и профилактические меры, такие как регулярная репозиция, подходящие постельные принадлежности, ограничивающие давление, гидроизолирующие прокладки и полноценное питание. Параметры лечения могут включать, например, разгрузку давления, хирургическую и энзиматическую санацию раневой полости, влажный уход за раной и контроль за бактериальной нагрузкой. В некоторых воплощениях предоставляют композиции и способы лечения хронической раны, где хроническая рана характеризуется пролежнем или изъязвлением, которые возникают в результате продолжительного и непрекращающегося давления на костный выступ, что приводит к ишемии.
Артериальные язвы: Артериальные язвы могут характеризоваться полной или частичной блокадой артерий, которая может приводить к некрозу тканей и/или изъязвлению. Признаки артериальной язвы могут включать, например, отсутствие пульса в конечностях; болезненное изъязвление; небольшие, точечные язвы, которые обычно имеют четкую границу; прохладную или холодную кожу; замедленное время восстановления капилляров (кратковременно нажмите на кончик большого пальца стопы и отпустите, нормальный цвет должен возвратиться в течение примерно 3 секунд и менее); атрофический вид кожи (например, лоснящаяся, тонкая, сухая кожа); и потеря волос на пальцах и стопе. В некоторых воплощениях предоставляют композиции и способы лечения хронической раны, где хроническая рана характеризуется присутствием артериальной язвы или изъязвления из-за полной или частичной блокады артерий.
Венозные язвы: Венозные язвы представляют собой наиболее распространенный тип язвы, затрагивающий нижние конечности, и они могут характеризоваться наличием дефекта венозного клапана. Нормальная вена имеет клапаны, которые не допускают обратный отток крови. Если эти клапаны становятся недееспособными, то обратный отток венозной крови вызывает закупорку вен. Гемоглобин выходит из эритроцитов и вытекает в пространство, расположенное вне сосуда, что вызывает обычно отмечаемое коричневатое изменение окраски. Было показано, что чрескожное давление кислорода в коже, окружающей венозную язву, уменьшается, что указывает на то, что существуют силы, нарушающие нормальную васкуляризацию поверхности. Лимфатический дренаж и количество проходящей жидкости также играют роль в развитии этих язв. Венозная язва может появляться рядом с внутренней лодыжкой и обычно встречается в комбинации с отечностью и затвердением нижних конечностей; она может быть неглубокой, несильно болезненной и из пораженного места может происходить выделение жидкости. В некоторых воплощениях предоставляют композиции и способы лечения хронической раны, где хроническая рана характеризуется присутствием венозной язвы или изъязвления из-за дефекта венозного клапана и ассоциированного сосудистого заболевания.
Застойные венозные язвы: Застойная венозная язва может характеризоваться наличием хронической пассивной закупорки вен в нижних конечностях, которая приводит к локальной гипоксии. Один из возможных механизмов патогенеза этих ран включает задержку диффузии кислорода в ткани сквозь толстые периваскулярные фибриновые муфты. Другой механизм состоит в том, что макромолекулы, вытекающие в периваскулярную ткань, захватывают факторы роста, необходимые для поддержания целостности кожи. Кроме того, поток крупных лейкоцитов замедляется из-за закупорки вен, окклюдирования капилляров, приводя к их активации и повреждению эндотелия сосудов, что предрасполагает к образованию язв. Таким образом, в некоторых воплощениях предоставляют композиции и способ лечения хронической раны, где хроническая рана характеризуется присутствием застойной венозной язвы или изъязвления из-за хронической пассивной закупорки вен в нижних конечностях и/или возникающей в результате этого локальной гипоксии.
Диабетические язвы: Пациенты, больные диабетом, предрасположены к изъязвлению стопы или другому изъязвлению как из-за неврологических, так и сосудистых осложнений. Периферическая нейропатия может вызывать изменение или полную потерю чувствительности в стопе и/или голени. Пациенты, больные диабетом, с выраженной нейропатией полностью теряют способность распознавать острое и тупое. У пациента с нейропатией любые порезы или травма стопы могут протекать полностью незамеченными в течение дней или недель. Пациент с выраженной нейропатией теряет способность чувствовать длительное повреждение под действием давления, в результате могут возникать ишемия тканей и некроз, приводящие, например, к подошвенному изъязвлению. Микрососудистое заболевание является одним из важнейших осложнений у больных диабетом, которое может привести к изъязвлению. В некоторых воплощениях предоставляют композиции и способы лечения хронической раны, где хроническая рана характеризуется наличием диабетической язвы стопы и/или изъязвлением из-за неврологических и/или сосудистых осложнений диабета.
Травматические язвы: Образование травматических язв может происходить в результате травматических повреждений тела. Эти повреждения включают, например, нарушения артериальной, венозной или лимфатической систем; изменения структуры костей скелета; утрату тканевых слоев - эпидермиса, дермы, подкожных мягких тканей, мышц и костей; повреждение частей тела или органов и потерю частей тела и органов. В некоторых воплощениях предоставляют композиции и способы лечения хронической раны, где хроническая рана характеризуется изъязвлением, ассоциированным с травматическими повреждениями тела.
Ожоговые язвы: Изъязвление может возникать в результате ожогового повреждения, в том числе ожога 1-ой степени (т.е. неглубокой покрасневшей поверхности кожи); ожога 2-ой степени (участок повреждения, покрытый волдырями, который может спонтанно заживать после того, как из волдыря удалили жидкость); ожога 3-ьей степени (ожог, проникающий через весь слой кожи и обычно требующий хирургического вмешательства для заживления ран); ошпаривания (может возникать при ошпаривании горячей водой, горячим жиром или жидкостью из радиатора); термального ожога (может возникать в результате контакта с огнем, обычно это глубокие ожоги); химического ожога (может вызываться кислотой и щелочью, обычно это глубокие ожоги); электрического ожога (вызываемого током низкого напряжения в домашних условиях или током высокого напряжения на работе); ожога в результате воспламенения (обычно это поверхностные повреждения); и контактных ожогов (обычно глубоких, они могут быть вызваны контактом с выхлопными трубами, горячими утюгами и печками). В некоторых воплощениях предоставляют композиции и способы лечения хронической раны, где хроническая рана характеризуется изъязвлением, ассоциированным с ожоговыми повреждениями тела.
Антиконнексиновые средства
Антиконнексиновые средства изобретения, описанные в этом документе, способны модулировать или влиять на транспорт молекул внутрь клеток и из них (например, путем блокирования или ингибирования, или регуляторного торможения). Таким образом, определенные антиконнексиновые средства, описанные в этом документе, модулируют клеточную коммуникацию (например, от клетки к клетке). Определенные антиконнексиновые средства модулируют или влияют на передачу молекул между цитоплазмой клеток и периплазматическим или внеклеточным пространством. Такие антиконнексиновые средства в основном нацелены на коннексины и/или коннексиновые полуканалы (коннексоны). Полуканалы и образующиеся щелевидные контакты, которые включают коннексины, независимо вовлечены в высвобождение и обмен небольшими молекулами между цитоплазмой клеток и внеклеточным пространством или тканью в случае открытых полуканалов, и между цитоплазмой соседней клетки в случае открытых щелевидных контактов. Таким образом, антиконнексиновые средства, предоставляемые в этом документе, которые могут прямо или косвенно уменьшать сопряжение и коммуникацию между клетками или уменьшать или блокировать коммуникацию (или передачу молекул) между клеткой и внеклеточным пространством или тканью, и модулирование транспорта молекул из клетки во внеклеточное пространство или ткань (или из внеклеточного пространства или ткани в клетку) или между соседними клетками, составляют объем антиконнексиновых средств и воплощений изобретения.
Любое антиконнексиновое средство, которое способно вызывать желаемое торможение переноса (например, транспорта) молекул через щелевидный контакт или коннексиновый полуканал, может быть полезным в воплощениях изобретения. В определенных воплощениях также предоставляют некоторые антиконнексиновые средства, которые модулируют перенос молекул через щелевидный контакт или коннексиновый полуканал (например, те средства, которые модулируют, блокируют или снижают перенос молекул из цитоплазмы клетки во внеклеточное пространство или цитоплазму соседней клетки). Такие антиконнексиновые средства могут модулировать перенос молекул через щелевидный контакт или коннексиновый полуканал с разъединением или без разъединения щелевидного контакта (блокирование транспорта молекул через щелевидные контакты). Такие соединения включают, например, белки и полипептиды, полинуклеотиды и другие органические соединения, и они могут, например, полностью или частично блокировать функцию или экспрессию щелевидного контакта или полуканала, или полностью или частично регуляторно подавлять образование коннексина. Определенные ингибиторы щелевидных контактов перечислены в работе Evans, W.H. and Boitano, S. Biochem. Soc. Trans. 29:606-612 (2001).
Определенные антиконнексиновые средства обеспечивают регуляторное торможение экспрессии коннексинов (например, с помощью регуляторного торможения транскрипции или трансляции мРНК) или же снижают или ингибируют активность белка коннексина, коннексинового полуканала или щелевидного контакта. В случае регуляторного торможения это будет иметь эффект ослабления коммуникации между клетками с помощью щелевидных контактов или экспонирования цитоплазмы клеток во внеклеточное пространство с помощью полуканалов, там, где регуляторно тормозится экспрессия коннексинов.
Примеры антиконнексиновых средств включают средства, которые уменьшают или ингибируют экспрессию или функцию мРНК коннексинов и/или белка, который уменьшает активность, экспрессию или образование коннексина, коннексинового полуканала или щелевидного контакта. Антиконнексиновые средства включают антиконнексиновые полинуклеотиды, такие как антисмысловые полинуклеотиды и другие полинуклеотиды (такие как полинуклеотиды, имеющие миРНК- или рибозимные функции), а также антитела и их связывающие фрагменты, и пептиды и полипептиды, в том числе пептидомиметики и пептидные аналоги, которые модулируют активность или функцию полуканала или щелевидного контакта.
Антиконнексиновые полинуклеотиды
Антиконнексиновые полинуклеотиды включают коннексиновые антисмысловые полинуклеотиды, а также полинуклеотиды, которые обладают функциями, которые обеспечивают их способность осуществлять регуляторное торможение экспрессии коннексинов. Другие подходящие антиконнексиновые полинуклеотиды включают РНКи-полинуклеотиды и миРНК-полинуклеотиды.
Синтез антисмысловых полинуклеотидов и других антиконнексиновых полинуклеотидов, таких как РНКи, миРНК и рибозимные полинуклеотиды, а также полинуклеотиды, имеющие модифицированные и смешанные остовы, известен специалистам в этой области техники. Смотри, например, Stein C.A. and Krieg A.M. (eds), Applied Antisense Oligonucleotide Technology, 1998 (Wiley-Liss). Способы синтеза антител и связывающих фрагментов, а также пептидов и полипептидов, в том числе пептидомиметиков и пептидных аналогов, известны специалистам в этой области техники. Смотри, например, Lihu Yang et al., Proc. Natl. Acad. Sci. U.S.A., 1; 95(18):10836-10841 (Sept 1 1998); Hariow and Lane (1988) «Antibodies: A Laboratory Manuel» Cold Spring Harbor Publications, New York; Hariow and Lane (1999) «Using Antibodies» A Laboratory Manuel, Cold Spring Harbor Publications, New York.
В соответствии с одним аспектом, регуляторное торможение экспрессии коннексинов может базироваться в основном на антисмысловом подходе с применением антисмысловых полинуклеотидов (таких как полинуклеотиды ДНК или РНК), и, в частности, на применении антисмысловых олигодезоксинуклеотидов (ODN). Эти полинуклеотиды (например, ODN) нацелены на регуляторное торможение белка коннексина (белков). Обычно полинуклеотиды являются одноцепочечными, но могут быть и двухцепочечными.
Антисмысловой полинуклеотид может ингибировать транскрипцию и/или трансляцию коннексина. Предпочтительно полинуклеотид является специфическим ингибитором транскрипции и/или трансляции гена коннексина или мРНК и не ингибирует транскрипцию и/или трансляцию других генов или мРНК. Продукт может связываться с геном коннексина или мРНК как (i) с 5'-концом кодирующей последовательности, и/или (ii) с кодирующей последовательностью, и/или (iii) с 3'-концом кодирующей последовательности.
Антисмысловой полинуклеотид обычно является антисмысловым относительно мРНК коннексина. Такой полинуклеотид может быть способным гибридизоваться с мРНК коннексина и может, таким образом, ингибировать экспрессию коннексина, препятствуя одной или нескольким фазам метаболизма мРНК коннексина, в том числе транскрипции, процессингу мРНК, транспорту мРНК из ядра, трансляции или разрушению мРНК. Антисмысловой полинуклеотид обычно гибридизуется с мРНК коннексина с образованием двойной спирали, которая может вызывать прямое ингибирование трансляции/или дестабилизацию мРНК. Такая двойная спираль может быть подвержена деградации нуклеазами.
Антисмысловой полинуклеотид может гибридизоваться со всей мРНК или с частью мРНК коннексина. Обычно антисмысловой полинуклеотид гибридизуется с участком, связывающимся с рибосомой или кодирующим участком мРНК коннексина. Полинуклеотид может быть комплементарным ко всей мРНК или к части мРНК коннексина. Например, полинуклеотид может быть полностью комплементарным ко всей мРНК или к части мРНК коннексина. Однако в абсолютной комплементарности нет необходимости, и полинуклеотиды, которые обладают достаточной комплементарностью, чтобы образовать двойную спираль, имеющую в физиологическом состоянии температуру плавления более, чем примерно 20°C, 30°C или 40°C, особенно подходят для применения в настоящем изобретении.
Таким образом, полинуклеотид обычно является гомологом последовательности, комплементарной по отношению к мРНК. Полинуклеотид может быть полинуклеотидом, который гибридизуется с мРНК коннексина в умеренно строгих или строгих условиях, таких как 0,03 М хлорид натрия и 0,03 М цитрат натрия при температуре примерно от 50°C до примерно 60°C.
Для определенных аспектов подходящие полинуклеотиды обычно имеют примерную длину от 6 до 40 нуклеотидов. Предпочтительно полинуклеотид может иметь примерную длину от 12 до примерно 35 нуклеотидов или альтернативно примерно от 12 до примерно 20 нуклеотидов, или более предпочтительно примерно от 18 до примерно 32 нуклеотидов. В соответствии с альтернативным аспектом полинуклеотид может иметь длину, по меньшей мере, около 40, например, по меньшей мере, около 60 или, по меньшей мере, около 80 нуклеотидов и до примерно 100, примерно 200, примерно 300, примерно 400, примерно 500, примерно 1000, примерно 2000 или примерно 3000 или более нуклеотидов.
Белок коннексин или белки, на который нацелен полинуклеотид, будет зависеть от того, на какой участок будет воздействовать регуляторное торможение. Это отражает неоднородную структуру щелевидного контакта (контактов) в различных частях организма в терминах субъединичного состава коннексина. Коннексин - это природный коннексин, который встречается у человека или животного в одном аспекте или встречается в тканях, в которых экспрессия или активность коннексина должна снижаться. Ген коннексина (в том числе и кодирующая последовательность) обычно имеет гомологию с кодирующей последовательностью одного или нескольких специфических коннексинов, которые были упомянуты в этом документе, например гомологию с кодирующей последовательностью коннексина 43, показанной в таблице 8. Коннексин обычно является α- или β-коннексином. Предпочтительно коннексин является α-коннексином и он экспрессируется в ткани, которую подвергают лечению.
Некоторые коннексиновые белки, однако, более распространены по сравнению с другими в терминах распределения в ткани. Одним из широко распространенных коннексинов является коннексин 43. Полинуклеотиды, нацеленные на коннексин 43, в особенности подходят для применения в настоящем изобретении. В других аспектах мишенью являются другие коннексины.
Антиконнексиновые полинуклеотиды включают антисмысловые полинуклеотиды коннексина, а также полинуклеотиды, которые имеют функциональные группы, которые обеспечивают им возможность регуляторно тормозить экспрессию коннексинов. Другие подходящие антиконнексиновые полинуклеотиды включают РНКи-полинуклеотиды и миРНК-полинуклеотиды.
В одном предпочтительном аспекте антисмысловые полинуклеотиды нацелены на миРНК только одного белка коннексина. Более предпочтительно этот коннексиновый белок является коннексином 43. В другом аспекте коннексиновый белок является коннексином 26, 30, 31.1, 32, 36, 37, 40 или 45. В других аспектах коннексиновый белок является коннексином 30.3, 31, 40.1 или 46.6.
Также предусмотрено применение комбинаций полинуклеотидов, нацеленных на отдельные коннексиновые белки (например, целью могут быть 1, 2, 3, 4 или более различных коннексинов). Например, полинуклеотиды, нацеленные на коннексин 43 и один или несколько других членов семейства коннексинов (таких как коннексин 26, 30, 30.3, 31.1, 32, 36, 37, 40, 40.1, 45 и 46.6), могут быть использованы в комбинации.
Альтернативно, антисмысловые полинуклеотиды могут быть частью композиции, которая может включать полинуклеотиды, направленные на более чем один белок коннексин. Предпочтительно один из коннексиновых белков, на который направлены полинуклеотиды, является коннексином 43. Другие коннексиновые белки, на которые направлены олигодезоксинуклеотиды, могут включать, например, коннексины 26, 30, 30.3, 31.1, 32, 36, 37, 40, 40.1, 45 и 46.6. Подходящие примеры полинуклеотидов (и ODN), направленные на различные коннексины, представлены в таблице 1.
Отдельные антисмысловые полинуклеотиды могут быть специфичными к определенному коннексину или могут быть нацелены на 1, 2, 3 или более различных коннексинов. Специфичные полинуклеотиды в основном будут нацелены на последовательности в гене коннексина или на мРНК, которые не являются консервативными среди коннексинов, тогда как неспецифичные полинуклеотиды будут нацелены на консервативные последовательности различных коннексинов.
Полинуклеотиды для применения в изобретения могут соответственно быть немодифицированными фосфодиэфирными олигомерами. Такие олигодезоксинуклеотиды могут различаться по длине. Было обнаружено, что 30-мерный полинуклеотид является особенно подходящим.
Описано много аспектов изобретения, в которых упоминаются олигодезоксинуклеотиды. Однако следует понимать, что и другие подходящие полинуклеотиды (такие как РНК-полинуклеотиды) могут применяться в этих аспектах.
Антисмысловые полинуклеотиды могут быть химически модифицированными. Это может улучшить их устойчивость к нуклеазам и может улучшить их способность проникать в клетки. Например, можно применять фосфоротиоатные олигонуклеотиды. Другие дезоксинуклеотидные аналоги включают метилфосфонаты, фосфорамидаты, фосфородитиоаты, N3'P5'-фосфорамидаты и олигорибонуклеотидфосфоротиоаты и их 2'-O-алкильные аналоги, и 2'-O-метилрибонуклеотидметилфосфонаты. Альтернативно можно применять олигонуклеотиды со смешанным остовом молекулы («МВО»). МВО содержат сегменты из фосфоротиоатных олигодезоксинуклеотидов и расположенные соответствующим образом сегменты модифицированных олигодезокси- или олигорибонуклеотидов. МВО имеют сегменты фосфоротиоатных связей и другие сегменты других модифицированных олигонуклеотидов, такие как метилфосфонат, который является неионной группой и очень устойчив к нуклеазам, или 2'-O-алкилолигорибонуклеотиды. Способы получения олигонуклеотидов с модифицированным остовом и смешанным остовом известны в этой области техники.
Точная последовательность антисмыслового полинуклеотида, применяемого в изобретении, будет зависеть от целевого белка коннексина. В одном воплощении подходящие коннексиновые антисмысловые полинуклеотиды могут включать полинуклеотиды, например олигодезоксинуклеотиды, выбираемые из следующих последовательностей, приведенных в таблице 1:
Подходящие полинуклеотиды для получения комбинированных полинуклеотидных композиций, описанных в этом документе, включают, например, полинуклеотиды, направленные на коннексин Сх43, и полинуклеотиды, направленные на коннексины 26, 30, 31.1, 32 и 37, как было описано выше в таблице 1.
Хотя точная последовательность антисмыслового полинуклеотида, полезного в изобретении, будет зависеть от целевого белка коннексина, было обнаружено, что для коннексина 43 особенно подходят антисмысловые полинуклеотиды, имеющие следующие последовательности: GTA ATT GCG GCA AGA AGA ATT GTT TCT GTC (SEQ ID NO:1); GTA ATT GCG GCA GGA GGA ATT GTT TCT GTC (SEQ ID NO:2) и GGC AAG AGA CAC CAA AGA CAC TAC CAG CAT (SEQ ID NO:3).
Например, подходящие антисмысловые полинуклеотиды для коннексинов 26, 31.1 и 32 имеют следующие последовательности:
5' TCC TGA GCA ATA CCT AAC GAA CAA ATA (коннексин 26) (SEQ ID NO:4); 5' CGT CCG AGC CCA GAA AGA TGA GGT С (коннексин 31.1) (SEQ ID NO:9) и 5' TTT CTT TTC TAT GTG CTG TTG GTG А (коннексин 32) (SEQ ID NO:12).
Другие последовательности антисмысловых полинуклеотидов для коннексина, полезные в соответствии со способами настоящего изобретения, включают:
5' CAT CTC CTT GGT GCT САА СС 3' (коннексин 37) (SEQ ID NO:5);
5' СТО AAG TCG ACT TGG CTT GG 3' (коннексин 37) (SEQ ID NO:6);
5' CTC AGA TAG TGG CCA GAA TGC 3' (коннексин 30) (SEQ ID NO:7);
5' TTG TCC AGG TGA CTC CAA GG 3' (коннексин 30) (SEQ ID NO:8);
5' AGA GGC GCA CGT GAG АСА С 3' (коннексин 31.1) (SEQ ID NO:10) и
5' TGA AGA САА TGA AGA TGT Т 3' (коннексин 31.1) (SEQ ID NO:11).
Полинуклеотиды, включающие ODN, направленные на коннексиновые белки, можно выбирать в соответствии с их нуклеотидной последовательностью с помощью любого удобного и традиционного подхода. Например, можно использовать компьютерные программы Mac Vector и OligoTech (Oligos etc. Eugene, Oregon, USA). После отбора ODN's можно синтезировать с помощью ДНК-синтезатора.
Гомологи полинуклеотидов
Гомология и гомологи обсуждаются в этом документе (например, полинуклеотид может быть гомологом последовательности, комплементарной к последовательности мРНК коннексина). Такой полинуклеотид обычно имеет, по меньшей мере, около 70% гомологии, предпочтительно, по меньшей мере, около 80%, по меньшей мере, около 90%, по меньшей мере, около 95%, по меньшей мере, около 97% или, по меньшей мере, около 99% гомологии с соответствующей последовательностью, например, относительно участка, по меньшей мере, примерно из 15, по меньшей мере, примерно 20, по меньшей мере, примерно 40, по меньшей мере, примерно 100 и более соседних нуклеотидов (гомологичной последовательности).
Гомологию можно рассчитать с помощью любого метода, известного в этой области техники. Например, пакет UWGCG предоставляет программу BESTFIT, которую можно использовать для расчета гомологии (например, используя ее установки по умолчанию) (Devereux et al. (1984) Nucleic Acids Research 12, p.387-395). Алгоритмы PILEUP и BLAST можно использовать для расчета гомологии или выравнивания последовательностей (обычно, исходя из их собственных установок по умолчанию), например, как было описано в работе Altschul S. F. (1993) J Mol Evol 36:290-300; Altschul, S, F et al. (1990) J Mol Biol 215:403-10.
Программное обеспечение для выполнения анализов BLAST общедоступно в Национальном центре биотехнологической информации (http://www.ncbi.nlm.nih.gov/). Этот алгоритм включает, во-первых, идентификацию пары сегментов с максимальным сходством (high scoring sequence pair, HSP) с помощью идентификации «коротких слов», имеющих длину W во входной последовательности, которые или совпадают, или удовлетворяют некоторому положительно оцененному пороговому значению Т при выравнивании со «словом» такой же длины в базе данных последовательностей. Т рассматривается как пороговая величина веса выравнивания для соседних слов (Altschul et al., supra). Эти исходные совпадения соседних слов действуют как затравка для начала поиска для нахождения HSP, содержащих их. Совпадения слов расширяют в обоих направлениях вдоль каждой последовательности по мере того, как накопленный вес выравнивания может увеличиваться. Продолжение процесса поиска совпадений слов в каждом направлении прекращают, если: накопленный вес выравнивания снижается в соответствии с величиной Х по сравнению с ее максимально достигнутым значением; накопленный вес выравнивания приходит к нулю или становится отрицательным из-за накопления одного или нескольких остатков с негативным баллом; или если достигнут конец последовательности.
Параметры алгоритма BLAST W, Т и Х определяют чувствительность и скорость выравнивания. Программа BLAST использует по умолчанию длину «слова» (W), матрицу BLOSUM62 (see Henikoff and Henikoff (1992) Proc. Natl. Acad. Sci. USA 89:10915-10919), выравнивания (В) - 50, ожидаемое значение (Е) - 10, М=5, N=4 и сравнение обеих цепей.
Алгоритм BLAST выполняет статистический анализ сходства между двумя последовательностями; смотри, например, Karlin and Altschul (1993) Proc. Natl. Acad. Sci. USA 90:5873-5787. Один показатель сходства, предоставляемый алгоритмом BLAST, представляет собой наименьшую сумму вероятностей (P(N)), которая является обозначением вероятности, с которой случайным образом будет возникать совпадение между двумя нуклеотидными или аминокислотными последовательностями. Например, последовательность считают сходной с другой последовательностью, если наименьшая сумма вероятности при сравнении первой последовательности со второй последовательностью будет меньше чем примерно 1, предпочтительно меньше чем примерно 0,1, более предпочтительно меньше чем примерно 0,01 и наиболее предпочтительно меньше чем примерно 0,001.
Гомологичные последовательности обычно отличаются от рассматриваемой последовательности, по меньшей мере, примерно (или не более чем примерно) на 2, 5, 10, 15, 20 и более мутаций (которые могут быть заменами, делениями или вставками). Эти мутации могут распределяться по любым участкам, упомянутым выше, в связи с рассчитываемой гомологией.
Гомологичная последовательность обычно селективно гибридизуется с исходной последовательностью на уровне, существенно превышающем фоновый уровень. Селективную гибридизацию обычно достигают, используя условия от умеренных до строгих (например, 0,03 М хлорид натрия и 0,03 М цитрат натрия при температуре от примерно 50°C до примерно 60°C). Однако такая гибридизация может быть проведена в любых подходящих условиях, известных в этой области техники (смотри Sambrook et al., (1989), Molecular Cloning: A Laboratory Manual). Например, если необходимы строгие условия, то подходящие условия включают 0,2×SSC при 60°C. Если необходимы менее строгие условия, то подходящие условия включают 2×SSC при 60°C.
Пептидные и полипептидные антиконнексиновые средства
Связывающие белки, в том числе пептиды, пептидомиметики, антитела, фрагменты антител и т.п., также являются подходящими модуляторами щелевидных контактов и полуканалов.
Связывающие белки включают, например, моноклональные антитела, поликлональные антитела, фрагменты антител (в том числе, например, фрагменты Fab, F(ab')2 и Fv; одноцепочечные антитела; одноцепочечные Fvs и одноцепочечные связывающие молекулы, те, которые включают, например, связывающий домен, шарнирный домен, СН2- и СН3-домены, рекомбинантные антитела и фрагменты антител, которые способны связывать антигенную детерминанту (т.е. ту часть молекулы, которую обычно относят к эпитопу), которая обеспечивает контакт с определенным антителом или другими связывающими молекулами. Такие связывающие белки, включающие антитела, фрагменты антител и т.д., могут быть химерными или гуманизированными, или созданными другим способом для того, чтобы быть менее иммуногенными для субъекта, которому их должны вводить, и могут быть синтезированы, получены рекомбинантным способом или получены в экспрессионных библиотеках. Рассматривается любая связывающая молекула, известная в этой области техники или та, которая будет открыта в будущем, например, такие молекулы, которые были упомянуты в этом документе и/или детально описаны в этой области техники. Например, связывающие белки включают не только антитела и т.п., но также лиганды, рецепторы, пептидомиметики или другие связывающие фрагменты или молекулы (например, получаемые с помощью фагового дисплея), которые связываются с мишенью (например, с коннексином, полуканалом или ассоциированными молекулами).
Связывающие молекулы обычно будут обладать желаемой специфичностью, включающей, но не ограниченной специфичностью связывания и желаемой аффинностью. Аффинность, например, может соответствовать Ka, которая больше или равна примерно 104 М-1, больше или равна примерно 106 М-1, больше или равна примерно 107 М-1, больше или равна примерно 108 М-1. Аффинности, составляющие больше чем примерно 108 М-1, являются подходящими, например аффинности, которые больше или равны примерно 109 М-1, примерно 1010 М-1, примерно 1011 М-1 и примерно 1012 М-1. Аффинности связывающих белков в соответствии с настоящим изобретением могут быть легко определены с помощью традиционных методик, например, таких, которые были описаны Scatchard et al., 1949 Ann. N.Y. Acad. Sci. 51:660.
С помощью результатов, полученных из графиков гидрофобности, было предположено, что коннексин содержит четыре трансмембранных участка и две короткие внеклеточные петли. Расположение первого и второго внеклеточного участка коннексина было дополнительно охарактеризовано путем сообщенного в литературе получения антител к пептидам, которые применяли для имунолокализации соответствующих эпитопов в зазоре щелевидных контактов. Goodenough D.A. J Cell Biol 107:1817-1824 (1988); Meyer R.A., J Cell Biol 119:179-189 (1992).
Внеклеточные домены полуканала образованы «соединением» двух соседних клеток друг с другом, которое приводит к образованию каналов щелевидных контактов. Реагенты, которые мешают взаимодействию этих внеклеточных доменов, могут нарушать межклеточную коммуникацию. Сообщалось о пептидных ингибиторах щелевидных контактов и полуканалов. Смотри, например, Berthoud, V.M. et al., Am J. Physiol. Lung Cell Mol. Physiol. 279: L619 - L622 (2000); Evans, W.H. and Boitano, S. Biochem. Soc. Trans. 29:606-612, и De Vriese A.S., et al. Kidney Int. 61:177-185 (2001). Было показано, что короткие пептиды, соответствующие последовательностям внеклеточных петель коннексинов, ингибируют межклеточную коммуникацию. Boitano S. and Evans W. Am J Physiol Lung Cell Mol Physiol 279: L623-L630 (2000). Также было сообщено о применении пептидов в качестве ингибиторов формирования межклеточных каналов, образованных с помощью коннексина (Сх) 32, экспрессированного в сдвоенных ооцитах Xenopus. Dahl G, et al., Biophys J 67:1816-1822 (1994). Berthoud, V.M. and Seul, K.H., суммировавшие некоторые из этих результатов. Am J., Physiol. Lung Cell Mol. Physiol. 279: L619 - L622 (2000).
Антиконнексиновые средства включают пептиды, включающие аминокислотную последовательность, соответствующую трансмембранному участку (например, с первого по четвертый) коннексина (например, коннексина 45, 43, 26, 30, 31.1 и 37). Антиконнексиновые средства могут включать пептид, включающий аминокислотную последовательность, соответствующую части трансмембранного участка коннексина 45. Антиконнексиновые средства включают пептид, имеющий аминокислотную последовательность, которая включает примерно от 5 до 20 расположенных рядом аминокислот последовательности SEQ ID NO:13, пептид, имеющий аминокислотную последовательность, которая включает примерно от 8 до 15 расположенных рядом аминокислот последовательности SEQ ID NO:13, или пептид, имеющий аминокислотную последовательность, которая включает примерно от 11 до 13 расположенных рядом аминокислот последовательности SEQ ID NO:13. Другие воплощения направлены на антиконнексиновое средство, которое является пептидом, имеющим аминокислотную последовательность, которая включает, по меньшей мере, примерно 5, по меньшей мере, примерно 6, по меньшей мере, примерно 7, по меньшей мере, примерно 8, по меньшей мере, примерно 9, по меньшей мере, примерно 10, по меньшей мере, примерно 11, по меньшей мере, примерно 12, по меньшей мере, примерно 13, по меньшей мере, примерно 14, по меньшей мере, примерно 15, по меньшей мере, примерно 20, по меньшей мере, примерно 25 или, по меньшей мере, примерно 30 расположенных рядом аминокислот последовательности SEQ ID NO:13. У некоторых антиконнексиновых средств, предоставляемых в этом документе, внеклеточные домены коннексина 45, соответствующие аминокислотам в положениях 46-75 и 199-228 последовательности SEQ ID NO:13, могут применяться для усовершенствования последовательностей специфических пептидов. Специфические пептиды, описанные в этом документе, имеют аминокислотную последовательность, соответствующую участкам в положениях 46-75 и 199-228 последовательности SEQ ID NO:13. Нет необходимости в том, чтобы пептиды имели аминокислотную последовательность, идентичную этим участкам в последовательности SEQ ID NO:13, и можно делать замены консервативных аминокислот так, чтобы пептиды сохраняли связывающую активность или функциональную активность. Альтернативно, пептид может быть нацелен на участки белка коннексина, не входящие во внеклеточные домены (например, части последовательности SEQ ID NO:13, не соответствующие положениям 46-75 и 199-228).
Также подходящие антиконнексиновые средства включают пептид, включающий аминокислотную последовательность, соответствующую части трансмембранного участка коннексина 43. Антиконнексиновые средства включают пептиды, имеющие аминокислотную последовательность, которая включает примерно от 5 до 20 расположенных рядом аминокислот последовательности SEQ ID NO:14, пептиды, имеющие аминокислотную последовательность, которая включает примерно от 8 до 15 расположенных рядом аминокислот последовательности SEQ ID NO:14, или пептиды, имеющие аминокислотную последовательность, которая включает примерно от 11 до 13 расположенных рядом аминокислот последовательности SEQ ID NO:14. Другие антиконнексиновые средства включают пептид, имеющий аминокислотную последовательность, которая включает, по меньшей мере, примерно 5, по меньшей мере, примерно 6, по меньшей мере, примерно 7, по меньшей мере, примерно 8, по меньшей мере, примерно 9, по меньшей мере, примерно 10, по меньшей мере, примерно 11, по меньшей мере, примерно 12, по меньшей мере, примерно 13, по меньшей мере, примерно 14, по меньшей мере, примерно 15, по меньшей мере, примерно 20, по меньшей мере, примерно 25 или, по меньшей мере, примерно 30 расположенных рядом аминокислот последовательности SEQ ID NO:14. Другие антиконнексиновые средства включают внеклеточные домены коннексина 43, соответствующие аминокислотам в положениях 37-76 и 178-208 последовательности SEQ ID NO:14. Антиконнексиновые средства включают пептиды, описанные в этом документе, которые имеют аминокислотную последовательность, соответствующую участкам в положениях 37-76 и 178-208 последовательности SEQ ID NO:14. Нет необходимости в том, чтобы пептиды имели аминокислотную последовательность, идентичную этим участкам в последовательности SEQ ID NO:13, и можно делать замены консервативных аминокислот так, чтобы пептиды сохраняли связывающую активность или функциональную активность. Альтернативно, пептид может быть нацелен на участки белка коннексина, не входящие во внеклеточные домены (например, части последовательности SEQ ID NO:14, не соответствующие положениям 37-76 и 178-208).
Коннексин 45 (SEQ ID NO:13)




Антиконнексиновые пептиды могут включать последовательности, соответствующие части внеклеточных доменов коннексинов с заменами консервативных аминокислот, так чтобы пептиды представляли собой функционально активные антиконнексиновые средства. Примеры замен консервативных аминокислот включают, например, замену неполярной аминокислоты на другую неполярную аминокислоту, замену ароматической аминокислоты на другую ароматическую аминокислоту, замену алифатической аминокислоты на другую алифатическую аминокислоту, замену полярной аминокислоты на другую полярную аминокислоту, замену кислой аминокислоты на другую кислую аминокислоту, замену основной аминокислоты на другую основную аминокислоту и замену ионизируемой аминокислоты на другую ионизируемую аминокислоту.
Типичные пептиды, нацеленные на коннексин 43, показаны ниже в таблице 2. M1, 2, 3 и 4 обозначают с первого по четвертый трансмембранные участки белка коннексина 43, соответственно. Е1 и Е2 относятся к первой и второй внеклеточным петлям, соответственно.
Таблица 3 представляет дополнительные примеры пептидов коннексина, применяемых для ингибирования функции полуканалов или щелевидных контактов. В других воплощениях замены консервативных аминокислот делают в пептидах или их фрагментах.
В таблице 4 представлены внеклеточные петли членов семейства коннексинов, которые используют для усовершенствования пептидных ингибиторов для применения, описанного в этом документе. Пептиды и представленные в таблице 4 соединения и их фрагменты применяют в качестве пептидных ингибиторов в некоторых воплощениях, которые не ограничивают объем изобретения. В других неограничивающих воплощениях пептиды, включающие примерно от 8 до примерно 15, или примерно от 11 до примерно 13 расположенных рядом аминокислотных остатков пептидов, представленных в таблице 4, являются пептидными ингибиторами. Можно проводить замены консервативных аминокислот в пептидах или их фрагментах.
В таблице 5 показан внеклеточный домен представителей семейства коннексинов, который может быть использован для усовершенствования пептидных антиконнексиновых средств. Пептиды и соединения, представленные в таблице 5, и их фрагменты также могут применяться в качестве пептидных антиконнексиновых средств. Такие пептиды могут включать от примерно 8 до примерно 15 или от примерно 11 до примерно 13 расположенных рядом аминокислот последовательности пептидов, представленных в таблице 5. Можно проводить замены консервативных аминокислот в пептидах или их фрагментах.
В таблице 6 представлены пептидные ингибиторы коннексина 40, показанные в сравнении с внеклеточными петлями (Е1 и Е2) коннексина 40. Полужирным шрифтом выделены аминокислоты, относящиеся к трансмембранным участкам коннексина 40.
В таблице 7 представлены пептидные ингибиторы коннексина 45, показанные в сравнении с внеклеточными петлями (Е1 и Е2) коннексина 45. Полужирным шрифтом выделены аминокислоты, относящиеся к трансмембранным участкам коннексина 45.
В некоторых воплощениях предпочтительно, чтобы определенные пептидные ингибиторы блокировали полуканалы без нарушения существующих щелевидных контактов. Без намерения быть связанным рамками определенной теории или механизма также полагают, что определенные пептидомиметики (например VCYDKSFPISHVR, (SEQ ID NO:23) блокируют полуканалы, не вызывая разъединения щелевидных контактов (смотри Leybeart et al., Cell Commun. Adhes. 10:251-257 (2003)), или делают это при пониженных дозах. Также можно применять пептид SRPTEKTIFII (SEQ ID NO: 19), например, чтобы блокировать полуканалы, не вызывая разъединения щелевидных контактов. Пептид SRGGEKNVFIV (SEQ ID NO:107) можно использовать как контрольную последовательность (DeVriese et al., Kidney Internal 61:177-185 (2002)). Примеры пептидных ингибиторов для коннексина 45 - YVCSRLPCHP (SEQ ID NO:108), QVHPFYVCSRL (SEQ ID NO:109), FEVGFLIGQYFLY (SEQ ID NO:110), GQYFLYGFQVHP (SEQ ID NO:111), GFQVHPFYVCSR (SEQ ID NO:112), AVGGESIYYDEQ (SEQ ID NO), YDEQSKFVCNTE (SEQ ID NO:114), NTEQPGCENVCY (SEQ ID NO:115), CYDAFAPLSHVR (SEQ ID NO:116), FAPLSHVRFWVF (SEQ ID NO:117) и LIGQY (SEQ ID NO:118), QVHPF (SEQ ID NO:119), YVCSR (SEQ ID NO:120), SRLPC (SEQ ID NO:121), LPCHP (SEQ ID NO:122) и GESIY (SEQ ID NO:123), YDEQSK (SEQ ID NO:124), SKFVCN (SEQ ID NO:125), TEQPGCEN (SEQ ID NO:126), VCYDAFAP (SEQ ID NO:127), LSHVRFWVFQ (SEQ ID NO:128). Пептиды по длине могут состоять всего из 3 аминокислот, в том числе SRL, РСН, LCP, СНР, IYY, SKF, QPC, VCY, APL, HVR, или быть длиннее, например, как LIQYFLYGFQVHPF (SEQ ID NO:129), VHPFYCSRLPCHP (SEQ ID NO:130), VGGESIYYDEQSKFVCNTEQEG (SEQ ID NO:131), TEQPGCENVCYDAFAPLSHVRF (SEQ ID NO:132), AFAPLSHVRFWVFQ (SEQ ID NO:133).
Терапевтические средства
Терапевтические средства включают фармацевтически приемлемые средства, полезные для лечения раны или стимулирования заживления ран, независимо от того, существуют ли они или известны в настоящий момент, или будут разработаны в будущем. Терапевтические средства включают, например, противоинфекционные средства, анестетики, анальгетики, антибиотики, наркотические средства и стероидные и нестероидные противовоспалительные средства. Предпочтительные терапевтические средства включают местные стероидные противовоспалительные средства, антимикробные средства, локальные и местные анестетики и местные опиоиды. В некоторых воплощениях одно, два, три, четыре, пять или шесть терапевтических средств можно применять в комбинации.
Средства, полезные для заживления ран
Применяемые в этом документе средства, полезные для заживления ран, включают стимуляторы, энхансеры или позитивные медиаторы каскада заживления ран, которые 1) стимулируют или ускоряют естественный процесс заживления ран или 2) снижают эффекты, ассоциированные с неправильным или медленным заживлением ран, где эффекты включают, например, осложненное воспаление, эпителизацию, ангиогенез и отложение матрикса, и образование рубцов и фиброз.
Позитивные медиаторы, энхансеры и стимуляторы включают, например, средства, которые могут стимулировать, усиливать, способствовать или ускорять (т.е. быть агонистами) количество, качество или эффективность заживления ран, или активный процесс заживления ран, или активацию ассоциированного с заживлением ран фактора роста или цитокина в области раны, или активацию ассоциированного с заживлением ран фактора роста или цитокинового рецептора. Такие средства могут включать ассоциированный с заживлением ран фактор роста или цитокин, или частично модифицированную форму ассоциированного с заживлением ран фактора роста или, например, цитокина. Частично модифицированная форма ассоциированного с заживлением ран фактора роста или цитокина может, например, иметь более продолжительное время полураспада в сравнении с природным ассоциированным с заживлением ран фактора роста или цитокина. Альтернативно, она может быть ингибитором метаболизма ассоциированного с заживлением ран фактора роста или цитокина.
Частичную модификацию такого средства можно проводить с помощью присоединения, делеции или замены аминокислотных остатков. Замена, например, может быть консервативной заменой. В результате частично модифицированная молекула может быть гомологом молекулы, из которой она произошла. Она может иметь, по меньшей мере, около 40%, например, около 50, 60, 70, 80, 90 или 95% гомологии с молекулой, из которой она происходит.
Применяемые в этом документе средства, полезные для заживления ран, могут включать, например, средства, стимулирующие заживление ран или уменьшающие рубцевание, для методов лечения ран, известных в настоящий момент в этой области техники или тех, которые будут развиваться в будущем; типовые факторы, средства или методы лечения, включающие природные и синтетические факторы роста, цитокины или их модуляторы, применяемые для стимулирования заживления ран, сконструированный биоинженерными способами матрикс, стимулирующий заживление ран, повязки, бинты и т.п. Подходящие примеры могут включать без ограничения 1) местно действующие средства и повязки и относящиеся к этому виды терапии и средства для очищения ран (такие как, например, Santyl® коллагеназа) и Iodosorb® (кадексомер иод); 2) антимикробные средства, включающие кремы и гели для системного или местного применения, включающие, например, средства, содержащие серебро, такие как SAGs (серебряные антимикробные гели), CollaGUARD(TM), Innocoll, Inc (повязка на основе очищенного белка коллагена I типа), CollaGUARD Ag (биоактивная повязка на основе коллагена, импрегнированная серебром, для инфицированных ран или ран с риском инфицирования), DermaSIL(TM) (синтетическая композитная пенная коллагеновая повязка для глубоких ран и ран, интенсивно выделяющих жидкость); 3) клеточную терапию или кожу, сконструированную биоинженерными методами, заменители кожи и эквиваленты кожи, включающие, например, Dermograft (3-мерный матрикс для культивирования человеческих фибробластов, которые секретируют цитокины и факторы роста), Apligraf® (человеческие кератиноциты и фибробласты), Graftskin® (бислой эпидермальных клеток и фибробластов, который гистологически сходен с нормальной кожей и продуцирует факторы роста, сходные с теми, которые продуцируются нормальной кожей), TransCyte (временный заменитель кожи из фибробластов человека) и Oasis® (активный биоматериал, который включает как факторы роста, так и компоненты внеклеточного матрикса, такие как коллаген, протеогликаны и гликозаминогликаны); 4) цитокины, факторы роста или гормоны (как природные, так и синтетические), вводимые в рану для стимулирования заживления ран, включающие, например, NGF, NT3, BDGF, интегрины, плазмин, семафорин, фактор роста крови, фактор роста кератиноцитов, тканевой фактор роста, TGF-альфа, TGF-бета, PDGF (можно применять один или несколько из трех подтипов: АА, АВ и В), PDGF-BB, TGF-бета 3, факторы, которые модулируют относительный уровень TGFβ3, TGFβ1 и TGFβ2 (например, маннозо-6-фосфат), половые стероиды, включающие, например, эстроген, эстрадиол или агонист рецептора эстрогена, выбираемый из группы, состоящей из этинилэстрадиола, диеноэстрола, местранола, эстрадиола, эстриола, конъюгированного эстрагена, пиперазина эстронсульфата, диэтилстильбэстрола, фосфэстрола тетранатрия, полиэстрадиол-фосфата, тиболона, фитоэстрогена, 17-бета-эстрадиола; гормоны тимуса, такие как тимозин-бета-4, EGF, HB-EGF, факторы роста фибробластов (например, FGF1, FGF2, FGF7), фактор роста кератиноцитов, TNF, семейство интерлейкинов, модуляторов воспалительного ответа, таких как, например, IL-10, IL-1, IL-2, IL-6, IL-8 и IL-10 и их модуляторы; INF (INF-альфа, -бета и -дельта); стимуляторы активина или ингибина и ингибиторы интерферона гамма, простагландин Е2 (PGE2) и медиаторы метаболического пути, связанного с циклическим аденозин-3',5'-монофосфатом (цАМФ); агонист аденозиновых рецепторов A1, агонист аденозиновых рецепторов А2 или 5) другие средства, полезные для заживления ран, включающие, например, как природные, так и синтетические гомологи, агонист и антагонист VEGF, VEGFA, IGF; IGF-1, провоспалительные цитокины, GM-CSF и лептины и 6) кДНК IGF-1 и KGF, аутологический тромбоцитарный гель, хлорноватистую кислоту (Sterilox®), липоевую кислоту, NO-синтазу 3, металлопротеиназу 9 матрикса (ММР-9), ССТ-ЕТА, интегрин альфа 5 бета 6, фактор роста примированных фибробластов и декорин, повязки на рану, содержащие серебро, Xenaderm™, средства очищения раны, содержащие папаин, лактоферрин, субстанцию Р, коллаген и ORC-серебро, плацентарную щелочную фосфатазу или плацентарный фактор роста, модуляторы hedgehog-сигналинга, модуляторы метаболического пути синтеза холестерина и АРС (активированный белок С), фактор роста кератиноцитов, TNF, тромбоксан А2, NGF, морфогенетический белок кости BMP, CTGF (фактор роста соединительной ткани), хемокины заживления ран, декорин, модуляторы неоваскуляризации, индуцируемой лактатом, рыбий жир, плацентарную щелочную фосфатазу или плацентарный фактор роста и тимозин бета 4. В некоторых воплощениях в комбинации можно применять одно, два, три, четыре, пять и шесть средств, полезных для заживления ран.
Следует понимать, что средства, полезные для заживления ран (в том числе, например, факторы роста и цитокины), указанные выше, охватывают все существующие в природе полиморфы (например, полиморфы факторов роста или цитокинов). Также изобретение охватывает функциональные фрагменты, химерные белки, включающие одно из указанных средств, полезных для заживления ран, или их функциональные фрагменты, гомологи, полученные с помощью аналогичной замены одной или нескольких аминокислот, средства для заживления ран и видовые гомологи. Предусмотрено, что одно или несколько средств, полезных для заживления ран, могут быть продуктом технологии рекомбинантных ДНК, и одно или несколько средств, полезных для заживления ран, могут быть продуктом трансгенной технологии. Например, тромбоцитарный фактор роста может предоставляться в форме рекомбинантного PDGF или вектора для генной терапии, включающего кодирующую последовательность PDGF.
Фрагмент или его частично модифицированная форма относится к фрагменту или частично модифицированной форме средства для заживления ран, которые сохраняют биологическую или ранозаживляющую функцию фактора, хотя он, конечно же, может иметь дополнительную функцию. Частичную модификацию можно, например, проводить с помощью присоединения, делеции или замены аминокислотных остатков. Замена, например, может быть консервативной заменой. В результате, частично модифицированная молекула может быть гомологом средства для заживления ран. Они могут, например, иметь, по меньшей мере, около 40% гомологии с указанным фактором. Они могут, например, иметь, по меньшей мере, около 50, 60, 70, 80, 90 или 95% гомологии с указанным фактором. Например, в некоторых воплощениях IL-10 или его фрагмент, или его частично модифицированную форму можно вводить в концентрации в диапазоне от примерно 1 мкМ до примерно 10 мкМ. Его можно вводить в концентрации в диапазоне от примерно 2,5 мкМ до примерно 5 мкМ. В некоторых других воплощениях IL-10 или его фрагмент, или его частично модифицированную форму можно вводить немедленно перед заживлением раны, но он может быть эффективным при введении в пределах примерно 7 дней после нанесения раны. Его можно вводить, по меньшей мере, в два приема.
Средства, модифицирующие щелевидные контакты
Используемый в этом документе термин «средства, модифицирующие щелевидные контакты» может широко включать такие средства или соединения, которые предупреждают, снижают или модулируют, полностью или частично, активность, функцию или образование полуканала или щелевидного контакта.
В других воплощениях средство, модифицирующее щелевидные контакты, предупреждает или снижает, полностью или частично, образование или активность полуканала или щелевидного контакта.
В некоторых воплощениях средство, модифицирующее щелевидные контакты, вызывает полное или частичное закрытие полуканала или щелевидного контакта. В других воплощениях средство, модифицирующее щелевидные контакты, блокирует, полностью или частично, полуканал или щелевидный контакт. В некоторых воплощениях средство, модифицирующее щелевидные контакты, снижает или предупреждает, полностью или частично, открытие полуканала или щелевидного контакта.
В некоторых воплощениях указанное блокирование или закрытие щелевидного контакта или полуканала с помощью средства, модифицирующего щелевидные контакты, может уменьшить или затормозить коммуникацию через внеклеточные полуканалы путем предупреждения или снижения потока небольших молекул через открытый канал во внеклеточное или периплазматическое пространство или из него.
В некоторых воплощениях средство, модифицирующее щелевидные контакты, препятствует, снижает или изменяет активность или функцию коннексина, полуканала или щелевидного контакта. Использованный в этом документе термин «модификация активности или функции щелевидного контакта» может включать открытие или закрытие щелевидных контактов, открытие или закрытие коннексонового полуканала и/или перенос молекул или ионов через щелевидные контакты.
В другом определенном аспекте средство, модифицирующее щелевидные контакты, может включать, например, алифатические спирты; октанол; гептанол; анестетики (например, галотан), этран, флуотан, пропофол и тиопентал; анандамид; ариламинобензоат (FFA: флуфенамовую кислоту и аналогичные производные, которые являются липофильными соединениями); карбеноксолон; халькон: (2',5'-дигидроксихалькон); CHFs (хлоргидроксифураноны); CMCF (3-хлор-4-(хлорметил)-5-гидрокси-2(5Н)-фуранон); дексаметазон; доксорубицин (и другие производные антрахинона); миметики эйкозаноида тромбоксана А(2) (ТХА(2)); NO (окись азота); жирные кислоты (например, арахидоновую кислоту, олеиновую кислоту и метаболиты липоксигеназы; фенаматы (флуфенамовую (FFA), нифлумовую (NFA) и меклофенамовую кислоты (MFA)); генистеин; глицирретиновую кислоту (GA): 18а-глицирретиновую кислоту и 18-бета-глицирретиновую кислоту и их производные; линдан; лизофосфатидную кислоту; мефлоквин; менадион; 2-метил-1,4-нафтохинон, витамин K(3); нафенопин; окадаевую кислоту; олеамид; олеиновую кислоту; РН, регулируемый с помощью внутриклеточного закисления; например, закисляющие средства; полиненасыщенные жирные кислоты; жирнокислотные GJIC-ингибиторы (например, олеиновую и арахидоновую кислоты); хинидин; хинин; полностью транс-ретиноевую кислоту; и тамоксифен.
Типичные соединения, применяемые для изменения функций щелевидных контактов (например, средства, блокирующие щелевидные контакты, средства, фосфорилирующие и дефосфорилирующие белки щелевидных контактов) были ранее описаны Jensen et al., смотри U.S. Pat. No. 7,153,822, Larsen et al., смотри U.S. Pat. No. 7,250,397, Gourdie et al., смотри WO 2006069181 and Tudor et al., смотри WO 2003032964 и другие многообразные опубликованные патентные заявки.
Используемый в этом документе термин «средство, фосфорилирующее щелевидные контакты» или «средство, дефосфорилирующее щелевидные контакты» может включать те средства или соединения, которые способны вызывать фосфорилирование или дефосфорилирование остатков коннексина. Типичные участки фосфорилирования или дефосфорилирования включают один или несколько остатков тирозина, серина или треонина в белке коннексине. В некоторых воплощениях модулирование фосфорилирования может происходить на одном или нескольких остатках одного или нескольких белков коннексинов. Примеры средства, фосфорилирующего и дефосфорилирующего щелевидные контакты, хорошо известны в этой области техники и могут включать, например, тирозинкиназу c-Src или другие агонисты рецепторов, связанных с G белками. Смотри Giepmans В, J. Biol. Chem., Vol.276, Issue 11, 8544-8549, March 16, 2001. В одном воплощении модулирование фосфорилирования одного или нескольких таких остатков воздействует на функцию полуканалов, в частности, путем закрытия полуканала. В другом воплощении модулирование фосфорилирования одного или нескольких таких остатков воздействует на функцию щелевидных контактов, в частности, путем закрытия щелевидного контакта.
Лекарственные формы и композиции и их введение
Терапевтически эффективное количество каждого из компонентов комбинации (например, антиконнексинового средства и средства для заживления ран) можно вводить одновременно, по отдельности или последовательно и в любом порядке. Средства можно вводить по отдельности или в виде комбинации с постоянным составом. Если их не вводят в виде комбинации с постоянным составом, то предпочтительные способы включают последовательное введение одного или нескольких антиконнексиновых средств и одного или нескольких средств, полезных для заживления ран, каждое из которых, или оба средства, предоставляют в количествах или дозах, которые меньше чем те, которые применяют в случае, если средство или средства вводят сами по себе по отдельности, т.е., если их не вводят в комбинации как в физическом смысле, так и в процессе лечения раны. Такие сниженные количества вводимых средств обычно составляют от примерно одной двадцатой до примерно одной десятой части от количества или количеств средства, если средство вводят по отдельности само по себе, и может составлять примерно одну восьмую часть количества, примерно одну шестую часть количества, примерно одну пятую часть количества, примерно одну четвертую часть количества, примерно одну третью часть количества и примерно одну вторую часть количества, если средство вводят по отдельности само по себе. Предпочтительно введение бывает последовательным. Предпочтительно средства вводят последовательно друг за другом, по меньшей мере, в пределах получаса. Средства также можно вводить одно за другим примерно через час, одно за другим через примерный интервал, составляющий от одних суток до примерно одной недели, или другим подходящим образом. Предпочтительно антиконнексиновое средство вводят первым. Предпочтительно, если применяют одно или несколько антиконнексиновых средств, то антиконнексиновый пептид или антиконнексиновый пептидомиметик, например антиконнексиновое средство, которое блокирует или тормозит открытие полуканалов, вводят до антиконнексинового средства, которое блокирует или снижает экспрессию коннексина или образование полуканалов или щелевидных контактов, например, путем регулирующего торможения экспрессии белка коннексина. Предпочтительно антиконнексиновое средство или средства является/являются средством (средствами), направленным (направленными) против коннексина 43.
Средства изобретения можно вводить субъекту, которому необходимо такое лечение, такому как субъект с любым из заболеваний или состояний, упомянутых в этом документе. Состояние субъекта, таким образом, может быть улучшено. Антиконнексиновое средство и партнер по комбинации могут, таким образом, применяться при лечении организма субъекта с помощью терапии. Их можно применять для изготовления лекарственного средства для лечения любого из состояний, упомянутых в этом документе. Таким образом, в соответствии с изобретением предоставляют композиции, с помощью которых можно будет временно и специфическим образом регуляторно тормозить межклеточную коммуникацию.
Антиконнексиновое средство может быть выделенным, главным образом, в чистом виде. Следует понимать, что продукт может быть смешан с носителями или разбавителями, которые не будут препятствовать намеченной цели создания продукта, но он все еще будет рассматриваться как выделенный, главным образом, в чистом виде. Продукт изобретения также может быть в значительно очищенной форме, в этом случае он обычно будет включать около 90%, например, по меньшей мере, около 95%, по меньшей мере, около 98% или, по меньшей мере, около 99% полинуклеотида (или другого антиконнексинового средства) или всю сухую массу препарата.
В зависимости от предполагаемого пути введения фармацевтические продукты, фармацевтические композиции, комбинированные препараты и лекарственные средства изобретения могут, например, быть в форме растворов, суспензий, инстилляций, бальзамов, кремов, гелей, пен, мазей, эмульсий, лосьонов, красителей, составов с замедленным высвобождением или порошков и обычно содержат примерно 0,1%-95% активного ингредиента (активных ингредиентов), предпочтительно около 0,2%-70%. Другие подходящие композиции включают композиции на основе плюроновых гелей, композиции на основе карбоксиметилцеллюлозы (КМЦ) и композиции на основе гидроксипропилметилцеллюлозы (ГПМЦ). Другие полезные композиции включают препараты с медленным или отсроченным высвобождением.
Гели или желе можно получать с помощью подходящего гелеобразующего средства, включающего без ограничения желатин, трагакант или производное целлюлозы и может включать глицерин в качестве увлажняющего вещества, смягчающее средство и консервант. Мази представляют собой полутвердые препараты, которые состоят из активного ингредиента, который включен в жирную, восковую или синтетическую основу. Примеры подходящих кремов включают без ограничения эмульсии вода-в-масле и масло-в-воде. Кремы вода-в-масле можно составить с помощью подходящего эмульгирующего средства, обладающего свойствами, сходными, но не ограниченными только ими, со свойствами жирных спиртов, таких как цетиловый спирт или цетостеариловый спирт, и эмульгирующего воска. Кремы масло-в-воде можно составить с помощью эмульгирующего средства, такого как цетомакроголовый эмульгирующий воск. Подходящие свойства включают способность модифицировать вязкость эмульсии и как физическую, так и химическую стабильность в широком диапазоне рН. Водорастворимая или смешиваемая основа крема может содержать систему консервантов и может также быть забуференной, чтобы поддерживать приемлемое физиологическое значение рН.
Пенные препараты могут быть составлены таким образом, чтобы их можно было доставлять из контейнера с аэрозолем, находящимся под давлением, с помощью подходящего аппликатора, используя инертные газы-вытеснители. Подходящие эксципиенты для состава пенной основы включают, но не ограничиваются только ими, пропиленгликоль, эмульгирующий воск, цетиловый спирт и глицерилстеарат. Возможные консерванты включают метилпарабен и пропилпарабен.
Предпочтительно средства изобретения смешивают с фармацевтически приемлемым носителем или разбавителем, чтобы получить фармацевтическую композицию. Подходящие носители и разбавители включают изотонические растворы солей, например фосфатно-солевой буфер. Подходящие разбавители и эксципиенты также включают, например, воду, физиологический раствор, декстрозу, глицерин и т.п. и их комбинации. Кроме того, при необходимости также могут присутствовать вещества, такие как увлажняющие или эмульгирующие средства, стабилизирующие или забуферивающие средства.
Термин «фармацевтически приемлемый носитель» относится к любому фармацевтическому носителю, который сам по себе не вызывает образование антител, вредных для человека, получающего композицию, и введение которого не вызывает токсичности. Подходящие носители могут быть крупными, медленно метаболизирующимися макромолекулами, такими как белки, полисахариды, полимолочные кислоты, полигликолевые кислоты, полимерные аминокислоты и сополимеры аминокислот.
Также могут присутствовать фармацевтически приемлемые соли, например соли минеральных кислот, такие как гидрохлориды, гидробромиды, фосфаты, сульфаты и т.п.; и соли органических кислот, такие как ацетаты, пропионаты, малонаты, бензоаты и т.п.
Подходящие вещества-носители включают любой носитель или среду, обычно применяемые в качестве основы для кремов, лосьонов, гелей, эмульсий, лосьонов или красителей для местного нанесения. Примеры включают эмульгирующие средства, инертные носители, включающие углеводородные основы, эмульгирующие основы, нетоксичные растворители или водорастворимые основы. Особенно подходящие примеры включают плюроники, ГПМЦ, КМЦ и другие ингредиенты на основе целлюлозы, ланолин, твердый парафин, жидкий парафин, мягкий желтый парафин или мягкий белый парафин, белый пчелиный воск, желтый пчелиный воск, цетостеариловый спирт, цетиловый спирт, диметиконы, эмульгирующие воска, изопропилмиристат, микрокристаллический воск, олеиловый спирт и стеариловый спирт.
Предпочтительно фармацевтически приемлемый носитель или среда представляет собой гель, подходящий неионный полиоксиэтилен-полиоксипропиленовый сополимерный гель, например плюроновый гель, предпочтительно Pluronic F-127 (BASF Corp.). Этот гель является особенно предпочтительным, так как он жидкий при низких температурах, но быстро затвердевает при физиологических температурах, что ограничивает высвобождение средства в участке нанесения или в участке, находящемся в непосредственной близости.
В композицию изобретения также могут быть включены вспомогательное средство, такое как казеин, желатин, альбумин, связующее средство, альгинат натрия, карбоксиметилцеллюлоза, метилцеллюлоза, гидроксиэтилцеллюлоза или поливиниловый спирт.
Другие подходящие композиции включают композиции на основе плюронового геля, композиции на основе карбоксиметилцеллюлозы (КМЦ) и композиции на основе гидроксипропилметилцеллюлозы (ГПМЦ).
Композицию можно составлять в любой желаемой форме доставки, включая местное, инстилляционное, парентеральное, внутримышечное, подкожное или трансдермальное введение. Другие полезные композиции включают препараты медленного или пролонгированного высвобождения.
Если антиконнексиновое средство представляет собой нуклеиновую кислоту, такую как полинуклеотид, поглощение нуклеиновой кислоты клетками млекопитающих усиливается с помощью нескольких известных методов трансфекции, например, тех, которые включают применение средств трансфекции. Такие методы можно применять, используя определенные антиконнексиновые средства, в том числе полинуклеотиды. Вводимая композиция может содержать такие средства трансфекции. Примеры этих средств включают катионные средства (например, фосфат кальция и ДЭАЭ-декстран) и липофектанты (например, lipofectam™ и transfectam™) и поверхностно-активные соединения.
Если антиконнексиновое средство включает полинуклеотид, обычно композиция дополнительно включает поверхностно-активное соединение, чтобы содействовать проникновению полинуклеотида в клетку, или композиция может содержать любой подходящий наполнитель. Может быть включено любое подходящее нетоксичное поверхностно-активное соединение, такое как ДМСО. Альтернативно, может быть включено средство для трансдермального проникновения, такое как мочевина.
Эффективную дозу для данного субъекта или состояния можно определить с помощью общепринятого экспериментального исследования или с помощью других способов, известных в этой области техники или тех, которые будут открыты в будущем. Например, чтобы разработать рецептуру с диапазоном значений дозировок, можно использовать анализы клеточных культур и исследования на животных. Дозировка таких соединений предпочтительно находится в пределах дозы, которая терапевтически эффективна, по меньшей мере, на 50% популяции и которая обладает небольшой токсичностью или не обладает ей на таком уровне.
Эффективная дозировка каждого из антиконнексиновых средств, применяемых в способах и композициях изобретения, может различаться в зависимости от целого ряда факторов, включающих специфичность антиконнексинового средства или применяемых средств, партнеры по комбинации, способы введения, частоту введения, состояние, подвергающееся лечению, тяжесть состояния, подвергающегося лечению, путь введения, необходимость в лечении у группы пациентов или необходимость в лечении у отдельного пациента с иными потребностями, которые могут быть в силу его возраста, пола, массы тела, соответствующего медицинского состояния, специфичного для пациента.
Доза, в которой вводят антиконнексиновое средство пациенту, будет зависеть от многих факторов, таких как возраст, масса тела и общее состояние пациента, от состояния, которое подвергается лечению и специфического антиконнексинового средства, которое ему вводят.
Подходящая доза может составлять примерно от 0,001 до примерно 100 мг/кг массы тела, например, примерно от 0,01 до примерно 40 мг/кг массы тела. Подходящая доза может, однако, составлять примерно от 0,001 до примерно 0,1 мг/кг массы тела, например, примерно от 0,01 до примерно 0,050 мг/кг массы тела. Применимы дозы примерно от 1 до 100, 200, 300,400 и 500 микрограммов.
Например, в некоторых воплощениях композицию антиконнексиновых средств можно наносить в конечной концентрации около 0,01 микромолярной (мкМ) или примерно от 0,05 мкМ до примерно 200 мкМ при обработке участка, выбранного для лечения и/или соседствующего с ним участка. Предпочтительно композицию антисмысловых полинуклеотидов наносят в конечной концентрации от примерно 0,05 мкМ до примерно 100 мкМ, более предпочтительно композицию антиконнексиновых средств наносят в конечной концентрации от примерно 1,0 мкМ до примерно 50 мкМ и более предпочтительно композицию антиконнексиновых средств наносят в конечной концентрации от примерно 5-10 мкМ до примерно 30-50. Кроме того, комбинированную композицию антиконнексиновых средств наносят в конечной концентрации от примерно 8 мкМ до примерно 20 мкМ и, альтернативно, композицию антиконнексиновых средств наносят в конечной концентрации от примерно 10 мкМ до примерно 20 мкМ или в конечной концентрации от примерно 10 до примерно 15 мкМ. В некоторых других воплощениях антиконнексиновое средство наносят в конечной концентрации около 10 мкМ. В еще одном воплощении композицию антиконнексиновых средств наносят в конечной концентрации, составляющей примерно 1-15 мкМ. Количество антиконнексиновых средств в дозе включает, например, примерно 0, 1-1, 1-2, 2-3, 3-4 или 4-5 микрограммов (мкг), примерно от 5 до примерно 10 мкг, примерно от 10 до примерно 15 мкг, примерно от 15 до примерно 20 мкг, примерно от 20 до примерно 30 мкг, примерно от 30 до примерно 40 мкг, примерно от 40 до примерно 50 мкг, примерно от 50 до примерно 75 мкг, примерно от 75 до примерно 100 мкг, примерно от 100 мкг до примерно 250 мкг и от 250 мкг до примерно 500 мкг. Также предоставляют дозовые количества от 0,5 до примерно 1,0 миллиграмма или более, как было указано выше. Объемы доз будут зависеть от размера обрабатываемого участка и могут разниться, например, примерно от 25-100 мкл до примерно 100-200 мкл, примерно от 200-500 мкл до примерно 500-1000 мкл. Для более обширных обрабатываемых участков также пригодны дозы объемом несколько миллилитров.
Другие дозировки поддерживают на уровне примерно от 1 нанограмма (нг)/кг до примерно 100 мг/кг массы тела в день каждого из средств, описанных в этом документе. В некоторых воплощениях дозировка каждого из соединений для обработки будет обычно составлять диапазон от примерно 1 нг до примерно 1 микрограмма на кг массы тела, примерно от 1 нг до примерно 0,1 микрограмма на кг массы тела, примерно от 1 нг до примерно 10 нг на кг массы тела, примерно от 10 нг до примерно 0,1 микрограмма на кг массы тела, примерно от 0,1 микрограмма до примерно 1 микрограмма на кг массы тела, примерно от 20 нг до примерно 100 нг на кг массы тела, примерно от 0,001 мг до примерно 100 мг на кг массы тела, примерно от 0,01 мг до примерно 10 мг на кг массы тела или примерно от 0,1 мг до примерно 1 мг на кг массы тела. В некоторых воплощениях дозировка каждого из соединений, предназначенных для обработки, будет обычно составлять диапазон примерно от 0,001 мг до примерно 0,01 мг на кг массы тела, примерно от 0,01 мг до примерно 0,1 мг на кг массы тела, примерно от 0,1 мг до примерно 1 мг на кг массы тела, примерно от 1 мг до примерно 10 мг на кг массы тела или примерно от 10 мг до примерно 100 мг на кг массы тела. Если применяют более одного антиконнексинового средства, то нет необходимости дозировку каждого из антиконнексиновых средств поддерживать в том же диапазоне, что и для других средств. Например, дозировка одного антиконнексинового средства может составлять примерно от 0,01 мг до примерно 10 мг на кг массы тела, а дозировка другого антиконнексинового средства может составлять от 0,1 мг до примерно 1 мг на кг массы тела. Специалистам в этой области техники известны и другие количества и их без труда можно будет определить.
Условно антиконнексиновое средство вводят в количестве, достаточном для регуляторного подавления экспрессии белка коннексина или модулирования образования щелевидных контактов, или открытия коннексонов в течение, по меньшей мере, примерно от 0,5 до 1 часа, по меньшей мере, около 1-2 часов, по меньшей мере, около 2-4 часов, по меньшей мере, около 4-6 часов, по меньшей мере, около 6-8 ЧАСОВ, по меньшей мере, около 8-10 часов, по меньшей мере, около 12 часов или, по меньшей мере, около 24 часов после введения.
Дозировка каждого из антиконнексиновых средств в композиции и способах, связанных с предметом изобретения, может также быть определена на основании концентрации композиции относительно размера, протяженности, глубины, площади и объема, на которые его наносят. Например, в определенных местных и других способах практического применения, например при инсталляции, дозировку фармацевтических композиций можно рассчитать на основе массы (например, микрограммов) или концентрации в фармацевтической композиции (например, мкг/мкл) в пересчете на длину, глубину, площадь или объем участка нанесения.
Средства, полезные для заживления ран, подходящие для получения фармацевтических композиций, описанных в этом документе, можно получать и вводить с помощью способов, известных в этой области техники (смотри, например, U.S. Patent No. 7,098,190, 6,319,907, 6,331,298, 6,387,364, 6,455,569, 6,566,339, 6,696,433, 6,855,505, 6,900,181, 7,052,684 и ЕР 1100529 В1. Нет необходимости дозировку каждого из антиконнексиновых средств, полезных для заживления ран, поддерживать в том же диапазоне, что и для других средств. Специалистам в этой области техники известны и другие количества и их без труда можно будет определить. Например, подходящие дозировки комбинаций и композиций в соответствии с различными аспектами и воплощениями, как было описано в этом документе, можно вводить в соответствии с режимом, описанным в патенте US 6903078, выданным Lewis, «Комбинация PDGF, KGF, IGF и IGFBP для заживления ран».
Исходная и любые последующие вводимые дозировки будут зависеть от возраста, состояния и заболевания, раны, нарушения или биологического состояния, которое подвергают лечению. В зависимости от средства заживления ран дозировка и протокол введения будут различаться, и дозировка также будет зависеть от выбранного способа введения, например локального или системного введения.
Средство для заживления ран можно применять внутрь или снаружи, и можно применять в отношении любой ткани, в которой обнаруживается рана. Для местного введения IGF, например, можно применять композицию с окисью цинка, которая вызывает локальное образование IGF, как было описано в работе Tamow et al., Scand J. Plast Reconstr Hand Surg. 28:255-259 (1994). Сообщалось, что эффективная доза PDGF составляет 5 нг/мм2 или выше при местном применении, как было описано в патенте U.S. Pat. No. 4,861,757, и локальная концентрация изоформы PDGF (например, PDGF-AA, PDGF-BB или PDGF-AB), применяемая в отношении популяции фибробластов, по меньшей мере, составляет от 1 нг/мл и до примерно 30 нг/мл, как было описано в работе Lepisto et al., Biochem Biophys Res. Comm 209:393-399 (1995). PDGF можно вводить в композиции карбоксиметилцеллюлозного геля в концентрациях, составляющих примерно от 10 мкг/г до примерно 500 мкг/г геля, примерно от 20 мкг/г до примерно 200 мкг/г и примерно от 30 мкг/г до примерно 100 мкг/г геля, оптимально примерно 100 мкг/г геля. Эффективности PDGF достигали при введении раствора с концентрацией в примерном диапазоне от 3 мкг/мл до 300 мкг/мл.
Около 50 мкл раствора KGF с концентрацией около 5 мкг/мл может быть эффективным для заживления ран с помощью местного нанесения на ткань эпителия, как было описано в работе Sotozono et al., Invest. Opthal. Vis. Science 36:1524-29 (1995). Как было описано в патенте U.S. Pat. No. 4,861,757, эффективное количество IGF при совместном введении с PDGF составляет диапазон, по меньшей мере, от 2,5 нг/мм2 до примерно 5 нг/мм2, при соотношении PDGF и IGF в примерном диапазоне от 1:10 до 25:1 по массе, с наиболее эффективными соотношениями PDGF и IGF, составляющими примерно от 1:1 до примерно 2:1 по массе. Было показано, что IGFBP, вводимый в комбинации с IGF, усиливает заживление ран в дозах примерно от 5 мкг IGF примерно с 1,5 мкг фосфорилированного IGFBP в молярном соотношении, приблизительно равном 11:1 IGF:IGFBP, как было описано в работе Jyung et al., Surgery 115:233-239 (1994).
Для введения полипептидных терапевтических средств, например полипептидов PDGF, KGF, IGF и IGFBP, дозировка может составлять примерный диапазон от 5 мкг до 50 мкг/кг ткани, на которую направлено нанесение, также примерно от 50 мкг до примерно 5 мг/кг, также примерно от 100 мкг до примерно 500 мкг/кг ткани и примерно от 200 до примерно 250 мкг/кг. Для полинуклеотидных терапевтических средств, например, в протоколе введения при генной терапии, в зависимости от эффективности экспрессии полинуклеотида у пациента, в ткани, на которые нацелено введение средств, согласно протоколу генной терапии можно вводить векторы, содержащие экспрессируемые конструкции, включающие кодирующие последовательности PDGF, KTF, IGF и IGFBP, в примерном диапазоне от 100 нг до 200 мг ДНК при местном введении, также примерно от 500 нг до примерно 50 мг, также примерно от 1 мкг до примерно 2 мг ДНК, примерно от 5 мкг ДНК до примерно 500 мкг ДНК и примерно от 20 мкг до примерно 100 мкг во время местного нанесения согласно протоколу генной терапии и примерно 250 мкг на инъекцию или введение. Такие факторы, как механизм действия и эффективность трансформации и экспрессии, представляют собой причину, которая будет влиять на дозировку, необходимую для максимальной эффективности терапевтических средств на основе ДНК. Если необходим более высокий уровень экспрессии на более протяженном участке ткани, то чтобы добиться необходимого положительного результата в последующем протоколе введения могут понадобиться увеличенные количества ДНК или повторное введение тех же количеств, или несколько введений в различные соседние или близко прилегающие участки ткани, например в области раны.
Терапевтические средства и средства, модифицирующие щелевидные контакты, подходящие для получения фармацевтических композиций, описанных в этом документе, можно составлять и вводить с помощью методов, известных в этой области техники. Исходные и любые последующие вводимые дозировки будут зависеть от возраста пациента, состояния и заболевания, раны, нарушения или биологического состояния, которое подвергают лечению. В зависимости от терапевтического средства дозировка и протокол введения будут различаться, и дозировка также будет зависеть от выбранного способа введения, например локального или системного введения.
Как было отмечено в этом документе, дозы как антиконнексинового средства, так и другого средства, вводимого в комбинации, можно отрегулировать в сторону низких количеств по сравнению с дозами, которые вводят при раздельном применении средств.
Комбинированное применение некоторых средств может уменьшить требуемую дозировку для любого индивидуального средства, так как начало и продолжительность эффекта различных средств могут быть взаимодополняющими. В предпочтительном воплощении комбинированное применение одного или нескольких антиконнексиновых средств и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты, обладает аддитивным, синергическим или сверхаддитивным эффектом.
В некоторых случаях комбинация одного или нескольких антиконнексиновых средств и одного или нескольких терапевтических средств, и/или одного или нескольких средств, полезных для заживления ран, и/или одного или нескольких средств, модифицирующих щелевидные контакты, имеет аддитивный эффект. В других случаях комбинация может обладать более чем аддитивным эффектом. Такой эффект называют в этом документе «сверхаддитивным» эффектом и он может происходить из-за синергического или усиливающего взаимодействия.
Термин «сверхаддитивное стимулирование заживления ран» относится к среднему значению показателя заживления ран, вызванного введением комбинации антиконнексинового средства и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средства, модифицирующего щелевидные контакты, если оно статистически более значимо, чем суммарный эффект заживления ран, вызываемый индивидуальным введением любого из средств. Определить, является ли эффект, вызванный или введением комбинации антиконнексинового средства и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты, «статистически более значимым», чем ожидаемое аддитивное значение для индивидуальных соединений, можно с помощью множества статистических способов, как это описано в этом документе и/или известно специалисту среднего звена в этой области техники. Термин «синергический» относится к типу сверхаддитивного ингибирования, в котором как антиконнексиновое средство, так и одно или несколько терапевтических средств, средства, полезные для заживления ран, и/или средства, модифицирующие щелевидные контакты, по отдельности обладают способностью стимулировать заживление ран или уменьшать фиброз и образование рубцов. Термин «усиливающий» относится к типу сверхаддитивного ингибирования, в котором одно из антиконнексиновых средств или одно или несколько терапевтических средств, средства, полезные для заживления ран, и/или средства, модифицирующие щелевидные контакты, по отдельности обладают повышенной способностью стимулировать заживление ран.
В основном усиливающий эффект можно оценить, определяя, вызывает ли обработка комбинацией в лечебной группе увеличение среднего показателя заживления ран, который является статистически значимым сверхаддитивным, при сравнении с увеличением суммы средних показателей заживления ран, вызванного индивидуальной обработкой в обрабатываемых группах, соответственно. Увеличение среднего показателя заживления ран можно рассчитать как разницу средних показателей заживления ран между контрольной группой и обрабатываемой группой. Долевое увеличение показателей при заживлении ран, «долю воздействия» (Fa) можно рассчитать путем деления увеличения среднего показателя заживления ран в обрабатываемой группе на средний показатель заживления ран в контрольной группе. Тестирование на статистически значимое усиление эффекта требует расчета Fa для каждой обрабатываемой группы. Ожидаемое аддитивное значение Fa при обработке комбинацией может быть выведено из суммы средних значений Fas для групп, получавших каждый из элементов комбинации. Чтобы оценить, насколько вероятно, что результат, полученный с помощью эксперимента, является случайным, можно использовать двухсторонний t-тест для одной выборки, измеряя значение р. Значение р, которое меньше чем 0,05, считают статистически значимым, то есть маловероятным, что результат случаен. Таким образом, значение Fa для группы, обработанной комбинацией, должно быть статистически более значимым, чем ожидаемые аддитивные значения Fa для каждой группы, обрабатываемой отдельным компонентом, чтобы считать комбинацию, способной вызывать усиленный сверхаддитивный эффект.
Результаты синергического эффекта от лечения комбинацией можно оценивать по медианному эффекту/комбинационному индексу методом изоболограмм (Chou, Т., and Talalay, P. (1984) Ad. Enzyme Reg. 22:27-55). В этом методе значения комбинационного индекса (CI) рассчитывают для различных значений доза-эффект на основе параметров, полученных из графиков медианных эффектов антиконнексинового средства самого по себе, одного или нескольких средств, полезных для заживления ран самих по себе и комбинации двух средств при фиксированных молярных соотношениях. Значения CI & 1t; 1 указывает на синергизм, CI-1 указывает на аддитивный эффект и СР1 указывает на антагонистический эффект. Этот анализ можно проводить с помощью компьютерных программных средств, таких как CalcuSyn, Windows Software for Dose Effect Analysis (Biosoft(D, Cambridge UK).
Для использования при скрининге подходящих антиконнексиновых средств, предназначенных для применения в комбинации с одним или несколькими терапевтическими средствами, средствами, полезными для заживления ран, и/или средствами, модифицирующими щелевидные контакты, изобретение предлагает любой метод анализа, известный в настоящий момент или открытый впоследствии в этой области техники, выясняющий, существует ли сверхаддитивный эффект для комбинационной терапии.
В другом предпочтительном воплощении комбинированное применение одного или нескольких антиконнексиновых средств и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты, снижает эффективную дозу любого такого средства в сравнении с эффективной дозой, когда указанное средство вводят само себе. В некоторых воплощениях эффективная доза средства, если его применяют в комбинации с одним или несколькими антиконнексиновыми средствами, составляет примерно от 1/15 до примерно 1/2, примерно от 1/10 до примерно 1/3, примерно от 1/8 до примерно 1/6, примерно 1/5, примерно 1/4, примерно 1/3 или примерно 1/2 дозы средства, если его применяют само по себе.
В другом предпочтительном воплощении комбинированное применение одного или нескольких антиконнексиновых средств и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты, снижает частоту, с которой указанное средство вводят, в сравнении с частотой, когда указанное средство вводят само по себе. Таким образом, эти комбинации обеспечивают применение более низких и/или более редких доз каждого средства, чем требовалось ранее для того, чтобы достигнуть желаемой терапевтической цели.
Дозы можно вводить однократно или делить их на части для нескольких применений. Дозы можно вводить один раз или повторять применение в течение нескольких раз.
Одно или несколько антиконнексиновых средств и одно или несколько терапевтических средств, средства, полезные для заживления ран, и/или средства, модифицирующие щелевидные контакты, можно вводить одним и тем же или разными путями. Различные средства изобретения можно вводить по отдельности в различные моменты времени курса терапии или одновременно в раздельных формах или в форме единой комбинации.
В одном аспекте изобретения антиконнексиновое средство вводят в одной композиции, а лечебное средство, ранозаживляющее средство и/или средство, модифицирующее щелевидные контакты, вводят во второй композиции. В одном воплощении первую композицию, включающую одно или несколько антиконнексиновых средств, вводят перед второй композицией, включающей одно или несколько терапевтических средств, средства, полезные для заживления ран, и/или средства, модифицирующие щелевидные контакты. В одном воплощении первую композицию, включающую одно или несколько антиконнексиновых средств, вводят после второй композиции, включающей одно или несколько терапевтических средств, средства, полезные для заживления ран, и/или средства, модифицирующие щелевидные контакты. В одном воплощении первую композицию, включающую одно или несколько антиконнексиновых средств, вводят перед и после второй композиции, включающей одно или несколько терапевтических средств, средства, полезные для заживления ран, и/или средства, модифицирующие щелевидные контакты. В одном воплощении первую композицию, включающую одно или несколько антиконнексиновых средств, вводят примерно в то же время, что и вторую композицию, включающую одно или несколько терапевтических средств, средства, полезные для заживления ран, и/или средства, модифицирующие щелевидные контакты.
Предпочтительно одно или несколько антиконнексиновых средств и одно или несколько терапевтических средств, средства, полезные для заживления ран, и/или средства, модифицирующие щелевидные контакты, высвобождаются при помощи местного введения (на периферическую часть или непосредственно в пораженный участок), включающего, но не ограниченного только ими, местное введение с помощью твердофазных подложек (таких как повязки и другие основы) и медицинских композиций (таких как гели, смеси, суспензии и мази). В одном воплощении твердофазная подложка включает биологически совместимую мембрану или вставку в обрабатываемый участок. В другом воплощении твердофазная подложка включает повязку или матрикс. В одном воплощении изобретения композиция для твердофазной подложки может быть медленно высвобождающейся композицией для твердофазной подложки, в которой одно или несколько антиконнексиновых средств и одно или несколько терапевтических средств, средства, полезные для заживления ран, и/или средства, модифицирующие щелевидные контакты, диспергированы в медленно высвобождающем твердом матриксе, таком как матрикс, представляющий собой альгинат, коллаген или синтетический биологически рассасываемый полимер. Предпочтительно композиция для твердофазной подложки является стерильной или имеет низкое содержание микрофлоры. В одном воплощении можно применять раствор для промывания, включающий одно или несколько антиконнексиновых средств.
При более тяжелых повреждениях и состояниях может быть особенно полезной доставка одного или нескольких антиконнексиновых средств и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты, композиции в течение периода времени, в некоторых случаях составляющего примерно 1-2 часа, примерно 2-4 часа, примерно 4-6 часов, примерно 6-8 или примерно 24 часа или больше. В некоторых случаях потеря клеток может распространяться далеко за пределы обрабатываемого участка на окружающие клетки. Такая потеря может происходить в пределах 24 часов после исходной процедуры и опосредуется межклеточной коммуникацией посредством щелевидных контактов. Введение антиконнексинового средства (средств), например, для регуляторного подавления экспрессии коннексинов или блокады открытия коннексонов, поэтому, будет модулировать коммуникацию между клетками или уход клеток во внеклеточное пространство в случае регулирования коннексонов и минимизировать дополнительную потерю клеток или повреждение клеток или последствия повреждения.
Хотя период доставки будет зависеть как от места, в котором необходимо индуцировать регуляторное торможение, так и от желаемого терапевтического эффекта, изобретение обеспечивает продолжительную доставку или доставку с замедленным высвобождением в течение примерно 1-2 часов, примерно 2-4 часов, примерно 4-6 часов, примерно 6-8 или примерно 24 часов или дольше. В соответствии с настоящим изобретением этого достигают с помощью включения антиконнексиновых средств и/или одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты, в композицию вместе с фармацевтически приемлемым носителем или средой, в частности, в форме композиции для продолжительного введения или введения с замедленным высвобождением.
Как было отмечено, одно или несколько средств изобретения можно вводить перед, во время, сразу же после нанесения раны, например, или в пределах примерно 180, примерно 120, примерно 90, примерно 60, или примерно 30 дней, но предпочтительно в пределах примерно 10, примерно 9, примерно 8, примерно 7, примерно 6, примерно 5, примерно 4, примерно 3 или примерно 2 дней или меньше, и наиболее предпочтительно в пределах примерно 24, примерно 12, примерно 10, примерно 9, примерно 8, примерно 7, примерно 6, примерно 5, примерно 4, примерно 3, примерно 2 часов или, например, в пределах примерно 60, примерно 45, примерно 30, примерно 15, примерно 10, примерно 5, примерно 4, примерно 3, примерно 2, примерно 1 минуты после нанесения раны.
Способы введения и дозировки, описанные в этом документе, являются лишь ориентировочными, так как опытный врач-терапевт сам сможет определить оптимальный способ введения и дозировку для любого конкретного пациента и состояния.
В любом из способов лечения субъекта, у которого есть заболевание, нарушение и/или состояние, упоминаемые или описанные в этом документе, или у которого есть риск или предрасположенность к возникновению заболевания, нарушения и/или состояния, упоминаемых или описанных в этом документе, можно использовать введение любых доз, лекарственных форм, составов и/или композиций, описанных в этом документе.
Повязки и матриксы
В одном аспекте одно или несколько антиконнексиновых средств, одно или несколько терапевтических средств, средства, полезные для заживления ран, и/или средства, модифицирующие щелевидные контакты, предоставляют в форме повязки или матрикса. В некоторых воплощениях одно или несколько средств изобретения предоставляют в форме жидкой, полутвердой или твердой композиции для непосредственного нанесения, или композицию наносят на поверхность или включают внутрь твердого контактирующего слоя, такого как перевязочная марля или матрикс. Композиция для повязки может предоставляться, например, в форме жидкости или геля. Одно или несколько антиконнексиновых средств и одно или несколько терапевтических средств, средства, полезные для заживления ран, и/или средства, модифицирующие щелевидные контакты, могут предоставляться в комбинации с традиционными фармацевтическими эксципиентами для местного применения. Подходящие носители включают: плюроновые гели, полаксамеровые гели, гидрогели, содержащие производные целлюлозы, в том числе гидроксиэтилцеллюлозу, гидроксиметилцеллюлозу, карбоксиметилцеллюлозу, гидроксипропилметилцеллюлозу и их смеси; и гидрогели, содержащие полиакриловую кислоту (карбополы). Подходящие носители также включают кремы/мази, применяемые для местных фармацевтических препаратов, например для кремов на основе цетомакроголовой эмульгирующей мази. Указанные выше носители могут включать альгинат (как загуститель или стимулятор), консерванты, такие как бензиловый спирт, буферы для контролирования рН, такие как двузамещенный фосфорнокислый натрий/однозамещенный фосфорнокислый натрий, средства для регулирования осмолярности, такие как хлорид натрия, и стабилизаторы, такие как ЭДТА.
Подходящие повязки или матриксы могут включать, например, нижеперечисленные приспособления вместе с одним или несколькими антиконнексиновыми средствами, вместе с одним или несколькими терапевтическими средствами, средствами, полезными для заживления ран, и/или средствами, модифицирующими щелевидные контакты:
1) Впитывающие средства: подходящие впитывающие средства могут включать, например, впитывающие повязки, которые могут обеспечивать, например, полуприлипающие свойства, или предоставлять неприлипающий слой, объединенный вместе с хорошо впитываемыми слоями волокон, таких как, например, целлюлоза, хлопок или вискоза. Альтернативно, впитывающие средства можно использовать в качестве первичной или вторичной повязки.
2) Альгинаты: подходящие альгинаты включают, например, повязки, которые представляют собой нетканые, неприлипающие прокладки и полоски, состоящие из природных полисахаридных волокон или ксерогелей из морских водорослей. Подходящие альгинатные повязки могут, например, при контакте с эксудатом с помощью ионного обмена образовать влажный гель. В некоторых воплощениях альгинатные повязки сконструированы таким образом, чтобы быть мягкими и комфортными, чтобы их было легко накладывать, заправлять или накладывать на поверхности неправильной формы. В некоторых воплощениях альгинатные повязки можно применять вместе со второй повязкой.
3) Антимикробные повязки: подходящие антимикробные повязки могут включать, например, повязки, которые могут облегчать доставку биоактивных средств, таких как, например, серебро и полигексаметиленбигуанидин (РНМВ), для того, чтобы поддержать противоинфекционную активность, если это необходимо или желательно. В некоторых воплощениях подходящие антимикробные повязки могут быть доступны, например, в виде тампонов, импрегнированной плетеной марли, пленочных повязок, впитывающих изделий, секционных повязок, нейлоновой ткани, нелипнущих изолирующих слоев или комбинации материалов.
4) Биологические и биосинтетические средства: подходящие биологические повязки или биосинтетические повязки могут включать, например, гели, растворы или полупроницаемые прослойки из природных источников. В некоторых воплощениях гель или раствор наносят на обрабатываемый участок и покрывают повязкой для изоляции. В другом воплощении прослойку помещают in situ, она может действовать как мембрана, оставаясь на месте после однократного применения.
5) Коллагены: подходящие коллагеновые повязки могут включать, например, гели, прокладки, частицы, пасты, порошки, прослойки или растворы, например, из препаратов, выделенных из быка, свиньи или птиц, или других природных источников, или доноров. В некоторых воплощениях коллагеновая повязка может взаимодействовать с эксудатом из обрабатываемого участка с образованием геля. В некоторых воплощениях коллагеновая повязка может применяться в комбинации с вторичной повязкой.
6) Композиты: подходящие композитные повязки могут включать, например, повязки, которые объединяют физически различающиеся компоненты в единое изделие, чтобы обеспечить многообразные функции, такие как, например, бактериальный барьер, абсорбцию и адгезию. В определенном воплощении композитные повязки состоят, например, из множественных слоев и включают полу- или неприлипающую прокладку. В определенном воплощении композит также может включать, например, прилипающий край нетканой матерчатой ленты или прозрачной пленки. В другом определенном воплощении композитная повязка может функционировать, например, в качестве как первичной, так и вторичной повязки, а в еще одном воплощении повязки можно применять в комбинации с фармацевтической композицией для местного применения.
7) Контактные слои: подходящие повязки с контактным слоем могут включать, например, тонкое, нелипнущее полотно, помещаемое на поверхность для защиты ткани, например, от непосредственного контакта с другими средствами или повязками, нанесенными на обрабатываемый участок. В некоторых воплощениях контактные слои могут разворачиваться, чтобы приспосабливаться к форме поверхности обрабатываемого участка, и могут быть пористыми, чтобы обеспечивать возможность экссудату проходить через поры для впитывания вышележащей вторичной повязкой. В еще одном воплощении повязка с контактным слоем может применяться в комбинации с фармацевтической композицией для местного применения.
8) Эластичные бинты: подходящие эластичные бинты могут включать, например, повязки, которые растягиваются и приспосабливаются под контуры тела. В определенном воплощении матерчатая композиция может включать, например, хлопок, полиэстер, вискозу или нейлон. В некоторых других воплощениях эластичные бинты могут, например, обеспечивать впитывание в качестве второго слоя или повязки, сохранять покрытие на своем месте, прикладывать давление или амортизировать обрабатываемый участок.
9) Пены: подходящие пенные повязки могут включать, например, листовые и другие формы растворов пенных полимеров (в том числе полиуретана) с небольшими, открытыми полостями, способными удерживать жидкости. Типичные пены могут быть, например, импрегнированными материалами или могут образовывать слои в комбинации с другими материалами. В определенном воплощении емкость впитывания можно регулировать на основе толщины и композиции пены. В некоторых других воплощениях поверхность контакта с обрабатываемым участком может быть нелипнущей для легкого удаления. В еще одном воплощении пену можно применять в комбинации с прилипающим краем и/или прозрачным пленочным покрытием, которое может служить противоинфекционным барьером.
10) Марлевые и нетканые повязки: подходящие марлевые повязки и тканые повязки могут включать, например, сухие тканые или нетканые губки и компрессы с различной степенью впитываемости. Типичная матерчатая композиция может включать, например, хлопок, полиэстер или вискозу. В определенном воплощении марлевая и нетканая повязка может быть доступна в стерильном или полностью нестерильном виде и с липнущим краем или без него. Типичные марлевые повязки и тканые повязки можно применять для очистки, тампонирования и покрытия различных обрабатываемых участков.
11) Гидроколлоиды: подходящие гидроколлоидные повязки могут включать, например, пластинки, порошки или пасты, состоящие из желатина, пектина или карбоксиметилцеллюлозы. В определенном воплощении пластинки являются самоприклеивающимися и имеются в готовом виде с прилипающим краем или без него и в широком разнообразии форм и размеров. Типичные гидроколлоиды полезны на поверхностях, для которых необходимо формирование контура. В некоторых воплощениях порошковые и пастообразные гидроколлоиды могут применяться в комбинации с вторичной повязкой.
12) Гидрогели (неупорядоченные): подходящие повязки с неупорядоченными гидрогелями могут включать, например, композиции воды, полимеров и других бесформенных ингредиентов, разработанных для того, чтобы отдавать влагу и поддерживать окружение заживляющегося участка во влажном состоянии и/или регидратировать обрабатываемый участок. В определенном воплощении гидрогели можно применять в комбинации с покрытием вторичной повязки.
13) Гидрогели: импрегнированные повязки: подходящие импрегнированные гидрогелевые повязки могут включать, например, марлевые или нетканые губки, жгуты и полоски, насыщенные аморфным гидрогелем. Аморфные гидрогели могут включать, например, композиции воды, полимеров и других бесформенных ингредиентов, разработанных для того, чтобы отдавать влагу сухому обрабатываемому участку и поддерживать окружение заживляющегося участка во влажном состоянии.
14) Гидрогелевые полотна: подходящие гидрогелевые полотна могут включать, например, трехмерные сетки из поперечно-сшитых гидрофильных полимеров, которые нерастворимы в воде и взаимодействуют с водными растворами путем набухания. Типичные гидрогели высокопластичны и проницаемы и могут впитывать различные количества отделяемой жидкости, в зависимости от своего состава. В определенном воплощении гидрогель не липнет к обрабатываемому участку или обработан для легкого удаления.
15) Импрегнированные повязки: подходящие импрегнированные повязки могут включать, например, марлевые или нетканые губки, жгуты и полоски, насыщенные раствором, эмульсией, маслом, гелем или некоторым другим фармацевтически активным соединением или носителем, в том числе, например, физиологическим раствором, маслом, солями цинка, вазелином, ксероформом и азокрасителем, а также соединениями, описанными в этом документе.
16) Полотна силикагеля: подходящие повязки из полотна силикагеля могут включать, например, мягкие покрытия, состоящие из поперечно-сшитых полимеров, укрепленных или связанных с сеткой или тканью.
17) Растворы: подходящие жидкие повязки могут включать, например, смеси мультибелкового материала и других элементов, обнаруженных во внеклеточном матриксе. В определенном воплощении типичные растворы могут наноситься на обрабатываемый участок после санации и очистки раневой поверхности и затем покрываться впитывающей повязкой или нелипнущим тампоном.
18) Прозрачные пленки: подходящая прозрачная пленка может включать полимерные мембраны различной толщины, покрытые с одной стороны клейким материалом. В некоторых воплощениях прозрачные пленки непроницаемы для жидкости, воды и бактерий, но проницаемы для влажных испарений и атмосферных газов. В некоторых воплощениях прозрачность позволяет видеть обрабатываемый участок.
19) Наполнители: подходящие повязки с наполнителями могут включать, например, гранулы, кремы, пены, гели, мази, прокладки, пасты, подушки, порошки, нити и другие композиции. В определенном воплощении наполнители являются нелипнущими и могут включать антимикробные средства, высвобождающиеся во времени. Типичные наполнители могут быть полезными, чтобы поддерживать влажное окружение, справляться с экссудатом и обрабатывать, например, раны почти на всю или на всю толщину кожи, инфицированные раны, дренированные и глубокие раны, которым необходимо заполнение.
Комбинированное лечение ран
Основные характеристики
Настоящее изобретение направлено на фармацевтические композиции и способы их применения, где композиция включает терапевтически эффективные количества одного или нескольких антиконнексиновых средств и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты. Композиции полезны для улучшения или стимулирования заживления ран, такие раны включают раны, которые могут быть медленно заживающими или упорно не поддаются обычному лечению или стимулирующей ранозаживляющей терапии.
В равной мере, в случае повреждения другой ткани (в частности, в случае ран) способы и композиции изобретения эффективны для стимулирования процесса заживления ран, уменьшения припухлости и воспаления и ограничения до минимума образования рубцов. Композиции обладают очевидной выгодой при лечении ран, будь то результат внешней травмы (в том числе ожогов), внутренней травмы или хирургического вмешательства, а также при лечении хронических ран.
Композиции
Соответственно, в одном аспекте изобретение обеспечивает композиции для применения при терапевтической обработке, которая включает: по меньшей мере, одно антиконнексиновое средство и, по меньшей мере, одно лечебное средство, и/или средство для заживлении ран и/или средство, модифицирующее щелевидные контакты. В предпочтительном воплощении композиция дополнительно включает фармацевтически приемлемый носитель или среду.
В одной предпочтительной форме композиция содержит только один или несколько антисмысловых полинуклеотидов в отношении мРНК одного коннексинового белка. В другой предпочтительной форме композиция включает один или несколько антиконнексиновых пептидов или пептидомиметиков. Наиболее предпочтительно этот коннексиновый белок - коннексин 43.
Композиции могут включать полинуклеотиды или антиконнексиновые пептиды более чем к одному коннексиновому белку. Предпочтительно один из коннексиновых белков, на которые направлены полинуклеотиды или антиконнексиновых пептиды, представляет собой коннексин 43. Другие коннексины, на которые направлены полинуклеотиды или антиконнексиновые пептиды, могут включать, например, коннексины 26, 30, 30.3, 31.1, 32, 36, 37, 40, 40.1, 44.6, 45 и 46. Подходящие примеры полинуклеотидов (и ODN), направленных на различные коннексины, приведены в таблице 1. Подходящие антиконнексиновые пептиды также представлены в этом документе.
Типичные комбинации
Типичные комбинации антиконнексинового средства и ранозаживляющего средства в соответствии с композициями и способами настоящего изобретения включают следующие примеры:
(a) одно из следующих антиконнексиновых средств:
антисмысловой полинуклеотид для коннексина 43;
антисмысловой ODN для коннексина 43;
полинуклеотид, включающий SEQ ID NO:2;
ODN, включающий SEQ ID NO:2;
полинуклеотид, включающий SEQ ID NO:1;
ODN, включающий SEQ ID NO:1;
РНКи-полинуклеотид для коннексина 43; или
миРНК-полинуклеотид для коннексина 43; и
(b) одно из следующих средств, полезных для заживления ран:
активин;
FGF-2 или фактор роста фибробластов 2;
FGF-1 или фактор роста фибробластов 1;
VEGF или фактор роста сосудистого эндотелия;
GM-SF или колониестимулирующий фактор гранулоцитов/моноцитов;
тромбоцитарный фактор 4;
EGF или эпидермальный фактор роста;
TGF или трансформирующий фактор роста (например, TGF-1,2,3);
TNF-альфа или фактор некроза опухолей альфа;
IL-1 интерлейкин-1;
IL-4 интерлейкин-4;
IL-7 интерлейкин-7;
IL-8 интерлейкин-8;
IL-10 интерлейкин-10;
GMCSF или колониестимулирующий фактор гранулоцитов/макрофагов;
CTGF или фактор роста соединительной ткани;
тимозин бета 4;
IGF-1 или инсулиноподобный фактор роста-1;
PDGF или тромбоцитарный фактор роста;
PDGF-BB или тромбоцитарный фактор роста ВВ;
маннозо-6-фосфат;
(aFGF) кислый фактор роста фибробластов;
(bFGF) основной фактор роста фибробластов;
(HB-EGF) гепарин-связывающий эпидермальный фактор роста;
(hGH) гормон роста человека;
(KGF) фактор роста кератиноцитов;
(KGF-2) фактор роста кератиноцитов 2;
(ММР) металлопротеиназа матрикса;
(PDECGF) тромбоцитарный эндотелиальный фактор роста;
(PDEGF) тромбоцитарный эпидермальный фактор роста;
(rbbFGF) рекомбинантный бычий основной фактор роста фибробластов;
(rhbFGF) рекомбинантный человеческий основной фактор роста фибробластов;
(rhPDGF-BB) рекомбинантный человеческий тромбоцитарный фактор роста (ВВ-димер);
(TGF-альфа) трансформирующий фактор роста-альфа;
(TGF-бета) трансформирующий фактор роста-бета;
(TIMP) тканевой ингибитор металлопротеиназы матрикса;
(VEGF) фактор роста сосудистого эндотелия;
(IGFBP) белок, связывающий инсулиноподобный фактор роста (например, IGFBP-2, IGFBP-3, IGFBP-4); и,
(FGF) или факторы роста фибробластов (например, FGF-1, FGF-2).
Этот список комбинаций является по своей природе примерным. Также включены другие комбинации антиконнексиновых средств и терапевтических средств, описанных в этом документе. Также включены другие комбинации антиконнексиновых средств и средств, полезных для заживления ран, описанных в этом документе. Также включены другие комбинации антиконнексиновых средств и средств, модифицирующих щелевидные контакты, описанных в этом документе.
Наборы, лекарственные средства и готовые промышленные изделия
Необязательно, для изготовления лекарственного средства также могут быть использованы одно или несколько антиконнексиновых средств и одно или несколько средств, полезных для заживления ран, терапевтические средства, и/или средства, модифицирующие щелевидные контакты (например, пептиды, ингибиторы протеолиза, компоненты внеклеточного матрикса, фрагменты и пептиды, стероиды, цитокины, доноры кислорода или витамины).
В одном аспекте изобретение обеспечивает набор, включающий одну или несколько композиций или описанные выше составы. Например, набор может включать композицию, включающую эффективное количество одного или нескольких антиконнексиновых средств и одного или нескольких терапевтических средств, средства, полезные для заживления ран, и/или средства, модифицирующие щелевидные контакты.
Также предоставляют готовые изделия от производителя, включающие емкость, содержащую композицию или состав изобретения, как было описано в этом документе, и инструкции по применению для лечения субъекта. Например, в другом аспекте изобретение включает готовое изделие, включающее емкость, содержащую терапевтически эффективное количество одного или нескольких фармацевтически приемлемых антиконнексиновых средств и одного или нескольких фармацевтически приемлемых терапевтических средств для стимулирования или улучшения заживления ран и инструкции по применению, в том числе по применению для лечения субъекта.
Обработка
Композиции и составы изобретения можно применять вместе или в комбинации с композицией для стимулирования заживления раны или чтобы уменьшить припухлость, воспаление и/или образование рубцов. Композиции и составы изобретения можно также применять вместе или в комбинации с композицией для стимулирования и/или улучшения заживления острых или хронических ран. В одном аспекте рана может быть результатом хирургической операции или травмы.
Подходящие терапевтические средства, средства, полезные для заживления ран, и/или средства, модифицирующие щелевидные контакты, применяемые в комбинации с одним или несколькими антиконнексиновых средствами для лечения раны, описаны в этом документе. В одном аспекте антиконнексиновые средства можно вводить в комбинации со средством, полезным для заживления ран, таким как хемокин, цитокин, фактор роста или их комбинация. В одном воплощении хемокин представляет собой антагонист хемокинового лиганда 2 (Сс12). В другом воплощении цитокин представляет собой антагонист фактора некроза опухолей альфа (TNF-α). В другом воплощении цитокин представляет собой IL-10. В одном воплощении фактор роста представляет собой TGF-бета-3. В соответствии с другим воплощением ранозаживляющее средство представляет собой тимозин β4. В еще одном воплощении антиконнексиновые средства можно вводить в комбинации с одним или несколькими IGFBP-2, IGF-7, IGF-1 или в комбинации с их модуляторами, чтобы увеличить синтез гидроксипролина и коллагена типа 1α1 для стимулирования заживления ран.
Подходящие антиконнексиновые средства для применения в комбинации со средством, полезным для заживлении ран, лечебным средством или средством, модифицирующим щелевидные контакты, описаны в этом документе и могут включать, например, полинуклеотид, такой как ODN, блокатор или другое средство, связывающее коннексины, такое как, например, рецепторный миметический пептид; абсорбент для устранения активности, такой как, например, молекулы или миметики синтетически экспрессированного рецептора; или антитела; а также, например, другие средства, полезные для регулирования закрытия/открытия щелевидных контактов, такие как соединения, которые фосфорилируют или дефосфорилируют щелевидные контакты.
В одном аспекте изобретение направлено на способ стимулирования или улучшения заживления ран у субъекта, включающий введение терапевтически эффективного количества одного или нескольких антиконнексиновых средств и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты, или соединений, полезных для стимулирования или улучшения заживления. В некоторых воплощениях введение одного или нескольких антиконнексиновых средств и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты, эффективно для того, чтобы уменьшить воспаление, снизить инфильтрацию нейтрофилов и/или макрофагов в рану, снизить отложение грануляционной ткани, стимулировать миграцию клеток для того, чтобы ускорить затягивание и заживление ран, способствовать росту эпителия, построению ткани и восстановлению поверхности ожогов или для любой их комбинации. В некоторых воплощениях введение одного или нескольких антиконнексиновых средств и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты, эффективно для того, чтобы уменьшить или предотвратить образование рубцов. В способах для стимулирования или улучшения образования рубцов антиконнексиновое средство предпочтительно вводят в комбинации или после, или до введения TGF-бета-3, или IL-10, или маннозо-6-фосфата.
В одном аспекте изобретение направлено на способ стимулирования или улучшения заживлении ран у субъекта, включающий введение одного или нескольких антиконнексиновых средств и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты, в количестве, эффективном для того, чтобы регулировать деление и рост базальных эпителиальных клеток. В одном воплощении антиконнексиновое средство представляет собой антисмысловой полинуклеотид для коннексина, эффективный для того, чтобы регулировать деление и рост базальных эпителиальных клеток. В одном воплощении антисмысловой полинуклеотид для коннексина представляет собой антисмысловой полинуклеотид для коннексина 26, антисмысловой полинуклеотид для коннексина 43 или их смесь.
В одном аспекте изобретение направлено на способ стимулирования или улучшения заживления ран, включающий введение одного или нескольких антиконнексиновых средств и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты, в количестве, эффективном для того, чтобы регулировать внешний слой секреции кератина. В одном воплощении антиконнексиновое средство представляет собой антисмысловой полинуклеотид для коннексина, эффективный для того, чтобы регулировать внешний слой секреции кератина. В одном воплощении антисмысловой полинуклеотид для коннексина представляет собой антисмысловой полинуклеотид для коннексина 43, антисмысловой полинуклеотид для коннексина 31.1 или их смесь.
В еще одном аспекте изобретение обеспечивает способ уменьшения образования рубцов и/или улучшения внешнего вида рубцов у пациента, который страдает присутствием раны, например раны, приобретенной в результате хирургической операции (такой как, например, косметическая операция или другие хирургические операции), который включает стадию введения одного или нескольких антиконнексиновых средств и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты, в указанную рану для того, чтобы тормозить экспрессию одного или нескольких коннексиновых белков в участке указанной раны или в непосредственно примыкающих участках раны. Кроме того, рана может быть результатом травмы или хирургической операции, и состав можно наносить на рану сразу же перед хирургическим вмешательством и/или после закрытия раны. Как было отмечено в этом документе, в способах для уменьшения образования рубцов или улучшения их внешнего вида антиконнексиновое средство предпочтительно вводят в комбинации после или перед введением подходящего количества TGF-бета-3, или IL-10, или маннозо-6-фосфата.
В одном аспекте изобретение направлено на способ снижения, предупреждения или улучшения признаков повреждения тканей у субъекта, включающий введение одного или нескольких антиконнексиновых средств и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты.
В следующем аспекте изобретение направлено на способ уменьшения припухлости и/или воспаления как части лечения раны и/или ткани, подвергнутой физическому травмированию, который включает стадию введения антиконнексиновой композиции или состава, как было определено выше, и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты, в указанную рану или ткань или в непосредственной близости от нее. В одном воплощении рана является результатом физической травмы ткани, включающей нейрональные ткани, такие как мозг, спинной мозг или зрительный нерв, или кожу и глаз.
В одном аспекте изобретение направлено на продолжительное введение одного или нескольких антиконнексиновых средств и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты. В одном воплощении антиконнексиновое средство вводят, по меньшей мере, примерно 1-24 часа, по меньшей мере, примерно 2 часа, по меньшей мере, примерно 3 часа, по меньшей мере, примерно 4 часа, по меньшей мере, примерно 5 часов, по меньшей мере, примерно 6 часов, по меньшей мере, примерно 7 часов, по меньшей мере, примерно 8 часов, по меньшей мере, примерно 9 часов, по меньшей мере, примерно 10 часов, по меньшей мере, примерно 11 часов, по меньшей мере, примерно 12 часов или, по меньшей мере, примерно 24 часа. В одном воплощении экспрессию коннексинов регуляторно подавляют в течение продолжительного периода времени. Предпочтительно экспрессию коннексина 43 подавляют в течение продолжительного периода времени. Обычно экспрессию коннексина 43 подавляют в течение, по меньшей мере, примерно 2, 4, 6, 8, 10, 12 или 24 часов. В соответствии с одним воплощением рана является хронической раной. Подходящие субъекты включают субъектов, страдающих диабетом.
В одном аспекте настоящее изобретение обеспечивает способ лечения субъекта, имеющего рану, который включает продолжительное введение в рану эффективного количества антиконнексинового средства и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты. В следующем аспекте настоящее изобретение обеспечивает способ стимулирования или улучшения заживления ран у субъекта, который включает продолжительное введение в рану одного или нескольких антиконнексиновых средств и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты. В следующем аспекте настоящее изобретение обеспечивает способ снижения, предупреждения или улучшения признаков припухлости и/или воспаления у субъекта, который включает продолжительное введение в рану одного или нескольких антиконнексиновых средств и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты. В следующем аспекте настоящее изобретение обеспечивает способ снижения, предупреждения или улучшения признаков образования рубцов у субъекта, который включает продолжительное введение в рану одного или нескольких антиконнексиновых средств и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты.
В соответствии со следующим аспектом настоящее изобретение обеспечивает способ стимулирования или улучшения заживления ран у субъекта, имеющего рану, который включает продолжительное введение в область раны антиконнексиновой композиции или состава настоящего изобретения и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты, в количестве, эффективном для увеличения скорости реэпителизации в области раны. В одном воплощении способ включает продолжительное введение антисмыслового полинуклеотида для коннексина 43 и/или антисмыслового полинуклеотида для коннексина 31.1 и одного или нескольких терапевтических средств, ранозаживляющих средств и/или средств, модифицирующих щелевидные контакты. В одном воплощении композицию или композиции вводят в форме состава с замедленным высвобождением. В другом воплощении композицию или композиции вводят в течение продолжительного периода времени. Обычно композиция эффективна для того, чтобы снизить уровень или активность коннексина 43 и/или 31.1 (например, активность полуканалов или щелевидных контактов) в течение, по меньшей мере, примерно 24 часов. В соответствии с одним воплощением рана является хронической раной. Субъекты, которых можно лечить, включают субъектов, больных диабетом.
В еще одном аспекте настоящее изобретение обеспечивает способ стимулирования или улучшения заживлении ран у субъекта, имеющего рану, который включает продолжительное введение в область раны антиконнексиновой композиции или состава настоящего изобретения и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты, в количестве, эффективном для того, чтобы регулировать деление и рост базальных эпителиальных клеток, и/или эффективном для того, чтобы регулировать внешний слой секреции кератина. В одном воплощении композиция включает антисмысловой полинуклеотид для коннексина, эффективный для того, чтобы регулировать деление или рост базальных эпителиальных клеток, предпочтительно антисмысловой полинуклеотид для коннексина 26, антисмысловой полинуклеотид для коннексина 43 или их смесь. В одном воплощении композиция включает антисмысловой полинуклеотид для коннексина, эффективный для того, чтобы регулировать внешний слой кератинизации, предпочтительно антисмысловой полинуклеотид для коннексина 31.1. В одном воплощении композицию или композиции вводят в виде состава для замедленного высвобождения. В другом воплощении композицию или композиции вводят в течение продолжительного периода времени. Обычно, композиция эффективна для того, чтобы снижать уровень коннексинов 43, 26 и/или 31.1 в течение, по меньшей мере, примерно 24 часов. В соответствии с одним воплощением рана является хронической раной. Субъекты, которых можно лечить, включают субъектов, больных диабетом.
В другом аспекте предоставляют способы лечения субъекта, имеющего хроническую рану. Такие способы включают введение субъекту антиконнексинового средства, способного тормозить экспрессию, образование или активность коннексина или коннексинового полуканала, в комбинации с одним или несколькими терапевтическими средствами, ранозаживляющими средствами и/или средствами, модифицирующими щелевидные контакты.
В одном аспекте изобретение направлено на способ лечения или профилактику хронической раны, включающие введение субъекту, которому это необходимо, эффективного количества антиконнексинового средства, которое вводят в указанную хроническую рану или ткань, связанную с указанной раной, в комбинации с одним или несколькими терапевтическими средствами, средствами, полезными для заживления ран, и/или средствами, модифицирующими щелевидные контакты. В другом воплощении хроническая рана является хронической кожной раной, и композицию настоящего изобретения вводят на кожу или в ткань, связанную с кожей указанного субъекта, в течение эффективного промежутка времени. Хроническая кожная рана, подходящая для лечения, может, например, быть выбрана из группы, состоящей из пролежневой язвы, диабетической язвы, венозной язвы, артериальной язвы, васкулитной язвы и смешанной язвы. Хроническая рана может быть артериальной язвой, которая включает изъязвления, возникающие в результате полной или частичной артериальной блокады. Хроническая рана может быть застойной венозной язвой, которая включает изъязвления, возникающие в результате дефекта венозного клапана и ассоциированного сосудистого заболевания. Хроническая рана может быть язвой, вызванной травмой.
В одном воплощении антиконнексиновое средство вводят в комбинации с фактором роста. Предпочтительно фактор роста представляет собой PDGF, EGF или FGF (например, FGF-2).
Если введение происходит не в виде комбинации с постоянным составом, предпочтительные способы включают последовательное введение одного или нескольких антиконнексиновых средств и одного или нескольких факторов роста. Предпочтительно средства вводят последовательно одно за другим в пределах, по меньшей мере, примерно получаса. Средства также можно вводить одно за другим примерно через один час, одно за другим через примерный интервал, составляющий от одного дня и до одной недели, или другим подходящим способом. Предпочтительно антиконнексиновое средство вводят первым. Предпочтительно, если применяют одно или несколько антиконнексиновых средств, антиконнексиновый пептид или антиконнексиновый пептидомиметик, например антиконнексиновое средство, которое блокирует или уменьшает открытие полуканалов, вводят до введения антиконнексинового средства, которое блокирует или уменьшает экспрессию коннексинов или образование полуканалов или щелевидных контактов, например, путем регуляторного торможения экспрессии коннексинового белка. Предпочтительно антиконнексиновое средство или средства является/являются средством/средствами, направленным/направленными против коннексина 43.
В другом воплощении для лечения раны, в том числе и хронических ран, предоставляют или одно или несколько антиконнексиновых средств и один или несколько факторов роста, или и то, и другое в количествах или дозах, которые меньше тех, которые применяют в случае, если средство или средства вводят по отдельности, т.е. если их вводят не в комбинации, или в физическом смысле или в курсе лечения раны. Такие сниженные количества вводимых средств обычно составляют примерно от 1/20 до примерно 1/10 количества или количеств средства, если его вводят отдельно само по себе, и может составлять примерно 1/8 количества, примерно 1/6 количества, примерно 1/5 количества, примерно 1/4 количества, примерно 1/3 количества и примерно 1/2 количества, если средство вводят отдельно само по себе.
В одном воплощении способ лечения или профилактики хронической раны включает продолжительное введение одного или нескольких антиконнексиновых средств и одного или нескольких терапевтических средств, средств, полезных для заживления ран, и/или средств, модифицирующих щелевидные контакты. В одном воплощении композицию или композиции вводят в виде состава с замедленным высвобождением. В другом воплощении композицию или композиции вводят в течение продолжительного промежутка времени. Обычно композиция эффективна для того, чтобы снижать уровень коннексина 43 или блокировать или уменьшать открытие полуканала коннексина 43 в течение, по меньшей мере, примерно 1-2 часов, примерно 2-4 часов, примерно 4-6 часов, примерно 4-8 часов, примерно 12 часов, примерно 18 часов или примерно 24 часов. Субъекты, которых можно лечить, включают субъектов, больных диабетом, и пациентов с другими язвами, в том числе с венозными язвами и другими язвами, описанными в этом документе и известных в этой области техники.
Приведенные ниже примеры, которые, как следует понимать, предоставлены только в целях иллюстрации, не ограничивают объем изобретения.
Примеры
Пример 1
Заживление ран оценивали с помощью модели на 8-недельных мышах с иссеченными ранами диаметром 1,6 мм на всю толщину кожи. Проводили иммуногистохимический и гистологический анализ совместно с RT-ПЦР-анализом экспрессии генов.
Кожные раны восстанавливали с помощью комбинации реэпителизирующего действия и сокращения соединительной ткани с последующим ангиогенным ответом, который приводит к образованию густой сети кровеносных сосудов в грануляционной ткани раны (Grose, R. and Werner, S. (2004). Wound-healing studies in transgenic and knockout mice. Mol Biotechnol 28, 147-66.). Устойчивый воспалительный ответ начинался сразу же после любого повреждения ткани. Это как защищало рану от микробной инфекции, так и приводило к образованию многих типов биоактивных веществ, которые действуют на клетки хозяина в области раны. Множество воспалительных клеток перемещается в рану, выполняя несколько различных функций. Нейтрофилы являются лейкоцитами самого раннего ответа, привлекаемыми в рану, и их главная роль состоит в том, чтобы защищать хозяина от инвазии микробами, что они делают, выделяя токсичные активные радикалы кислорода и секретируя провоспалительные цитокины. Впоследствии макрофаги убирают истощенные нейтрофилы и другие продукты разрушения клеток и внеклеточного матрикса в области раны. Макрофаги также являются главными продуцентами цитокинов, хемокинов и факторов роста, которые направляют последовательную миграцию клеток и ткани во время восстановительных реакций. В то время как многие из сигналов, регулирующих процесс воспаления и восстановления тканей, отчетливо рассеяны и действуют на значительном расстоянии, оказалось, что локальная межклеточная коммуникация посредством адгезионных молекул и межклеточных контактов также играет значительную роль.
Одним связующим звеном между клетками, которое может играть значительную регуляторную роль, является щелевидный контакт, который представляет собой гексамерный канал, образованный белками, относящимися к семейству коннексинов. Сообщалось, что щелевидные контакты экспрессируются почти всеми клетками организма (Wei, С.J., Xu, X. and Lo, С.W. (2004). Annu Rev Cell Dev Biol 20, 811-38.), и они опосредуют изменения в миграции клеток.
Сообщалось, что уровень белка коннексина 43 (Сх43) на краю эпидермальной раны естественным образом повышается в течение 24-48 часов. Было показано, что регуляторное снижение уровня белка Сх43 после применения антисмысловых олигодезоксинуклеотидов (asODN) на кожной ране и на участках ожогового повреждения приводит к значительно ускоренному заживлению по сравнению с ранами, обработанными контрольными смысловыми олигодезоксинуклеотидами (sODN) (Qiu, С., Coutinho, P., Frank, S., Franke, S., Law, L.Y., Martin, P., Green, C.R. and Becker, D.L. (2003). Targeting connexin 43 expression accelerates the rate of wound repair. Curr Biol 13, 1697-703; Coutinho, P., Qiu, C., Frank, S., Wang, C.M., Brown, Т., Green, C.R. and Becker, D.L. (2005). Limiting bum extension by transient inhibition of connexin 43 expression at the site of injury. Br J Plast Surg 58, 658-67).
Эксперименты показали, что резкое регуляторное торможение белка Сх43 в области раны приводит к повышению пролиферации и миграции кератиноцитов и повышению скорости, с которой фибробласты мигрируют в рану и нижележащий слой коллагенового матрикса. Мы обратили внимание на уменьшение инфильтрации нейтрофилов и сопутствующее уменьшение мРНК хемокинового лиганда 2 (Сс12) и цитокина фактора некроза опухоли альфа (TNF-α). Впоследствии мы также обратили внимание на сниженный рекрутинг макрофагов, который может быть результатом уменьшения исходного воспалительного ответа, который, как известно, обладает регуляторно тормозящим эффектом на процесс последующего заживления ран. Вместе эти измененные ответы приводят к значительному улучшению заживления ран.
Модель раны и лечение с помощью ODN
В последующих экспериментах использовали 8-недельных мышей-самцов ICR. Всех мышей содержали в специфических беспатогенных условиях в экологически чистой кондиционируемой комнате Университетского колледжа Лондона, и все эксперименты проводили в соответствии с правилами, утвержденными Министерством внутренних дел Великобритании. Мышей обезболивали с помощью галотановой ингаляции. На выбритых задних частях с каждой стороны средней линии спины с помощью 6-миллиметрового дерматома (Kai Industries) делали четыре иссеченные раны на всю толщину кожи диаметром 6 мм. Для каждой пары ран на одну рану однократно наносили 50 мкл 1 мкМ Сх43 asODN (SEQ ID No. 2) (Sigma-Genosys) в 30%-ном геле Pluronic F-127 (Sigma-Aldrich), охлажденном на льду, а на другую рану делали идентичное нанесение 1 мкМ контрольных смысловых sODNs. Нанесение Сх43 asODNs приводит к значительному снижению белка Сх43 в области доставки в пределах двух часов (Becker, D.L., McGonnell, I., Makarenkova, H.P., Patel, K., Tickle, С., Lorimer, J. and Green, C.R. (1999). Roles for alpha 1 connexin in morphogenesis of chick embryos revealed using a novel antisense approach. Dev Genet 24, 33-42; McGonnell, I.M., Green, C.R., Tickle, C. and Becker, D.L. (2001). Connexin 43 gap junction protein plays an essential role in morphogenesis of the embryonic chick face. Dev Dyn 222, 420-38; Qiu, C., Coutinho, P., Frank, S., Franke, S., Law, L.Y., Martin, P., Green, C.R. and Becker, D.L. (2003). Targeting connexin 43 expression accelerates the rate of wound repair. Curr Biol 13, 1697-703). Участок каждой раны снимали на цифровой фотоаппарат в указанные интервалы времени и подсчитывали площади ран. Все площади ран выражали в процентах от исходных площадей ран. В некоторых сериях экспериментов раны и поверхность, окружающую их, в том числе струп и края эпителия, собирали с помощью 8-миллиметрового дерматома (Kai Industries) в указанные интервалы времени после того, как мышей умерщвляли увеличенной дозой хлороформа. Для каждой исследованной временной точки использовали минимум восемь мышей.
Гистологический анализ и иммуноокрашивание
Ткани раны фиксировали в 4%-ном формальдегиде, забуференном с помощью PBS, и погружали в парафин. Срезы (толщиной 6 мкм) окрашивали с помощью гематоксилина и эозина или с помощью иммуноокрашивания. Измерение площади грануляционной ткани в Н&Е проводили с помощью программного обеспечения Improvision Openlab™ 4.0.2 software (Improvision). Для иммуногистохимического анализа депарафинизированные срезы обрабатывали реагентом, блокирующим эндогенные пероксидазы (Dako Cytomation A/S), и протеиназой K (Dako Cytomation A/S) в течение 20 минут и 6 минут при комнатной температуре, соответственно. Затем их инкубировали в течение ночи при 4°C после блокировки с помощью 15%-ного обезжиренного молока в течение 1 часа при комнатной температуре с кроличьим поликлональным антителом к миелопероксидазе (МРО) (NeoMarkers), разведенным 1:200, крысиным моноклональным антителом к мышиным иммуноглобулинам F4/80 (mAb) (Abcom Limited), разведенным 1:400, или крысиным моноклональным антителом к мышиному CD31 (молекула адгезии тромбоцитов к клеткам эндотелия-1, РЕСАМ-1) (PharMingen) или кроличьим поликлональным антителом к мышиному TGF-β1 (Santa Cruz Biotechnology, Inc), оба антитела были разведены 1:200. Кроме того, некоторые срезы подвергали реакции с изоцианатом фаллоидин-тетраметилродамина В (Sigma-Aldrich), разведенным 1:500, в течение 1 часа при комнатной температуре. Антитела подходящим образом разводили в разбавителе для антител с компонентами, снижающими фон (Dako Cytomation A/S). Срезы, прореагировавшие с антителом к МРО и антителом к TGF-β1, окрашивали с помощью EnVision+™ (Dako Cytomation A/S) для усиления сигнала в соответствии с инструкциями фирмы-производителя. Срезы затем подвергали реакции с антителами к F4/80, и антитела к CD31 инкубировали с биотинилированными кроличьими антителами к крысиным иммуноглобулинам (Dako Cytomation A/S), разведенными 1:200, в течение 1 часа при 37°C. Затем сигнал усиливали с помощью системы Catalyzed Signal Amplification System® (Dako Cytomation A/S) в соответствии с инструкциями фирмы-производителя. Затем проводили контрастное окрашивание с помощью Метилового зеленого (Dako Cytomation A/S) с последующим прокращиванием на МРО, TGF-β1, F4/80 и CD31, или окрашивание 4',6-диамидино-2-фенилиндолом (DAPI) с последующим окрашиванием фаллоидином.
Иммуноокрашивание коннексина 43, кровеносных сосудов или гладкомышечного α-актина проводили на криостатных срезах раны. Срезы фиксировали в ацетоне при 4°C в течение 5 минут до блокировки в течение 45 минут. Инкубацию с первичным антителом проводили при комнатной температуре в течение одного часа при следующих разведениях: кроличье антитело к Сх43 (Sigma) 1:3000; изолектин B_FITC 1:2000; фактор фон Виллебранда (кролик, Dako) 1:400; антитело к гладкомышечному α-актину (Sigma) 1:400. Срезы промывали 3 раза по 5 минут в PBS перед одночасовой инкубацией с вторичным антителом к кроличьим иммуноглобулинам, меченным FITC (Dako) 1:200 при комнатной температуре. Промывали 3 раза по 5 минут с помощью PBS, в некоторых случаях с 1 мкМ бис-бензимидом (Sigma) при первой промывке для контрастного окрашивания ядер, и монтировали в Citifluor (Citifluor, London, UK). Срезы рассматривали с помощью конфокальной микроскопии, сохраняя все параметры постоянными, для того, чтобы обеспечить прямое сравнение цифровых изображений.
TUNEL-окрашивание
Ткани раны фиксировали в 4%-ном формальдегиде, забуференном с помощью PBS, и погружали в парафин и делали срезы. Депарафинированные срезы обрабатывали протеиназой K (Dako Cytomation A/S) в течение 5 минут при комнатной температуре. Затем их окрашивали с помощью набора In Situ Cell Death Detection Kit (Roche) в соответствии с инструкциями фирмы-производителя. Затем проводили контрастное окрашивание с помощью 4',6-диамидино-2-фенилиндола (DAPI). Рассматривали TUNEL-окрашенные срезы и в грануляционной ткани подсчитывали позитивные клетки в трех случайно выбранных полях, на двух сторонах и в центре каждой раны (каждое поле размером 0,332 мм2).
Детекция пролиферирующих клеток с помощью мечения 5'-бром-2'дезоксиуридином (BrdU)
В другом эксперименте раненным мышам делали внутрибрюшинную инъекцию 1 мл BrdV (Sigma) в растворе PBS (1 мг/мл) за 2 часа до получения препаратов в 1-ый, 2-ой и 7-ой день. Ткани ран фиксировали в 4%-ном формальдегиде, забуференном с помощью PBS, и погружали в парафин. Депарафинированные срезы (толщиной 6 мм) обрабатывали с помощью набора HistoMouse™-Plus Kit (ZYMED Laboratories, Inc), чтобы уменьшить фоновые сигналы в соответствии с инструкциями фирмы-производителя. Срезы окрашивали с помощью набора BrdU Detection Kit (BD Bioscience Pharmingen) в соответствии с инструкцией фирмы-производителя. Затем проводили контрастное окрашивание с помощью Метилового зеленого (Dako Cytomation A/S).
Измерение нейтрофилов, макрофагов, фибробластов, BrdU-положительных клеток и ангиогенеза
Специалист слепым методом подсчитывал МРО-позитивные нейтрофилы и F4/80-позитивные макрофаги в основании раны (определяемом как поверхность, окруженную неповрежденной кожей, фасцией, регенерированным эпидермисом и струпом) в 3 случайных полях, размером 0,332 мм2, при большом увеличении. Подсчитывали BrdU-позитивные клетки на краю раны и на участках зарождающегося эпидермиса каждого среза, окрашенного иммуногистохимически, как было описано ранее, и пересчитывали на 100 мкм эпидермиса (Mori, R., Kondo, Т., Nishie, Т., Ohshima, Т. and Asano, M. (2004). Impairment of skin wound healing in beta-l,4-galactosyltransferase-deficient mice with reduced leukocyte recruitment. Am J Pathol 164, 1303-14). Количество фибробластоподобных клеток (фаллоидин-позитивные клетки с веретенообразной формой) на краю раны также подсчитывали при большом увеличении (каждое поле размером 0,332 мм2). За неоваскуляризацией следили с помощью флуоресцентного окрашивания эндотелиальных клеток на фактор фон Виллебранда на 5-ый, 7-ой, 10-ый и 14-ый день после нанесения раны. Миофибробласты идентифицировали с помощью окрашивания антителами к гладкомышечному α-актину. Для количественной оценки обоих флуоресцентных окрашиваний применяли конфокальный микроскоп, чтобы получать изображения одиночных срезов из сравниваемых зон (минимально от шести животных на каждую временную точку). Все параметры для получения изображений держали постоянными, чтобы обеспечить сравнение. Изображения делали бинарными при стандартном пороге, и позитивные пиксели подсчитывали с помощью Image J (NIH Image).
Анализ гидроксипролина
Содержание коллагена на поверхности раны оценивали путем определения гидроксипролина (HP), основного компонента коллагена. Образцы гомогенизировали в 1 мл реагента T-PER® Tissue Protein Extraction Reagent (PIERCE Biotechnology Inc.), включающего набор ингибиторов протеаз Halt™ Protease Inhibitor Cocktail, EDTA-Free (PIERCE Biotechnology Inc.), и центрифугировали при 15000 об/мин в течение 20 минут при 4°C для удаления дебриса. Концентрации белка измеряли с помощью набора ВСА™ Protein Assay Kit (PIERCE Biotechnology Inc.), а количества HP определяли с помощью набора Sircol™ Soluble Collagen Assay Kit (Biocolor Ltd.). Для каждого образца результаты выражали в количестве НР/общий белок (нг/мкг).
Культура клеток
Фибробласты Swiss 3T3 выращивали в среде Игла в модификации Дюльбекко (DMEM; Gibco), дополненной 10% фетальной сывороткой теленка (Labtech) и 1% раствора пенициллина/стрептомицина (Sigma, Poole) в CO2-инкубаторе с 5% СО2 при 37°C. Если не указано особо, клетки содержали в этой среде в большинстве экспериментов. Клетки пассировали путем трипсинизации и использовали после 6-10 пассажей при достижении конфлюентности ≈ 90%. Клетки высевали на 13-миллиметровые покровные стекла в 24-луночные планшеты (Nunc) в количестве 4-5×105 клеток на лунку, содержащую 1 мл среды. Клетки достигали конфлюентности через 72 часа и затем их использовали в экспериментах.
Анализ миграции клеток в результате нанесения раны
Анализ клеток фибробластов включал нанесение «раны» в конфлюэнтном монослое фибробластных клеток. Эта широко используемая в опытах in vitro методика имитирует поведение клеток, мигрирующих in vivo (Lampugnani, M.G. (1999) Cell Migration into a wounded area in vitro. Methods Mol Biol 96:177-182). Нанесение раны проводили с помощью протаскивания микроэлектрода вдоль покровного стекла, создавая повреждение стандартной ширины. Фазово-контрастные изображения получали с помощью 5-кратного объектива инвертированного микроскопа Zeiss при инкубации в камере при 37° и 5% СО2. Изображение определенной поверхности на краю покровного стекла получали сразу же после нанесения раны, и затем изображение той же поверхности делали через 4 часа, во время, при котором можно отчетливо видеть, что миграция происходит (фигура 7Е, 7F). Получали изображения как минимум восьми покровных стекол для каждого контроля и каждой обрабатываемой группы. Миграцию количественно оценивали с помощью анализа изображений, измеряя изменение в области раны (пиксели) с помощью программного Image J обеспечения (NEH).
Чтобы снизить экспрессию Сх43 в фибробластах, среду заменяли на DMEM без сыворотки, содержащую или 20 мкМ asODNs, или 20 мкМ контрольные sODN. Инкубацию проводили в течение двух часов перед тем, как среду заменяли на DMEM, содержащую сыворотку. Затем проводили анализ раны, как было описано выше. Предварительный опыт показал, что два часа было достаточно для значительного падения содержания белка Сх43 (Qiu, С., Coutinho, P., Frank, S., Franke, S., Law, L.Y., Martin, P., Green, C.R. and Becker, D. L. (2003). Targeting connexin 43 expression accelerates the rate of wound repair. Curr Biol 13, 1697-703) и процесс падения продолжается во время анализа миграции в ране.
Выделение РНК и количественная оценка уровня экспрессии с помощью ПЦР в режиме реального времени
Суммарную РНК экстрагировали из образцов кожной раны с помощью реагента TRIzol Reagent (bivitrogen) в соответствии с инструкциями фирмы-производителя. Десять микрограммов суммарной РНК подвергли обратной транскрипции с получением кДНК с помощью системы Superscript First-Strand Synthesis System for RT-PCR (Invitrogen).
Специфические праймеры генов и зонд получали с помощью TaqMan® Gene Expression Assays (Applied Biosystems) для Сх43, Cc12, Co1α1, TNF-α и TGF-β1. Ферментную и буферную систему приобретали как TaqMan® Universal PCR Master Mix (Applied Biosystemes). Каждый образец анализировали в двойных повторах. Амплификацию и детекцию в режиме реального времени проводили в DNA Engine Opticon®2 (MJ Research Inc.). Экспрессию целевых генов сравнивали с экспрессией GAPDH.
Статистический анализ
Статистические различия определяли с помощью непарного теста Стьюдента или, при необходимости, с помощью U-теста Манна-Уитни. Все данные представлены в виде среднего значения ± стад.ош.средн. Критерии уровня значимости для индивидуальных тестов представлены в разделе Результаты.
Регудяторное снижение уровня Сх43 в области раны с помощью Сх43 asODN
Было обнаружено, что Сх43 преимущественно экспрессируется в нижнем и среднем слоях шиповатых клеток эпидермиса и в фибробластах, кровеносных сосудах и дермальных придатках интактной кожи. Через 6 часов после повреждения Сх43 экспрессировался в гиперпролиферативном эпидермисе, но начинал подвергаться регуляторному торможению на ведущем крае кератиноцитов. Доставка Сх43 asODN с момента поражения значительно снижала уровень белка Сх43 в эпидермисе и дерме в пределах двух часов после обработки. Такое быстрое снижение, возможно, происходит потому, что белок Сх43 быстро обновляется, иногда в пределах 1,5-2 часов. Чтобы более точно количественно оценить степень снижения уровня белка Сх43 и мРНК и восстановления после обработки asODN, мы сравнили уровни экспрессии Сх43 мРНК в обработанных областях раны относительно уровней экспрессии в необработанных областях раны с помощью ПЦР в режиме реального времени (RT-ПЦР; фигура 1). Через один день после повреждения экспрессия Сх43 мРНК в ранах, обработанных Сх43 asODN, была значительно снижена по сравнению с контрольными ранами, обработанными sODN (2,95 против 4,7 единиц, соответственно, 37%-ное снижение; Р<0,05). Через 7 дней после повреждения, однако, уровни экспрессии были сходными в двух условиях обработки ран (4,6 против 5,2 единиц для ран, обработанных asODN и контрольными sODN, соответственно). Иммуноокрашивание ран на Сх43 в 1-ый, 2-ой и 7-ой день после нанесения раны выявило очень низкие уровни белка Сх43 в эпидермисе и дерме края раны, обработанной Сх43 asODN в 1-ый день, по сравнению с контролями (фигура 1). На 2-ой день в дерме раны, обработанной Сх43 asODN, восстановилось некоторое окрашивание на Сх43, но уровень окрашивания в эпидермисе все еще оставался очень низким. На 7-ой день в соответствии с результатами RT-ПЦР не было очевидного различия в окрашивании на Сх43 между обработанными и необработанными ранами. Эти результаты подтверждают, что Сх43 asODN при доставке с помощью плюронового геля действительно ингибирует экспрессию Сх43 мРНК в ранние моменты времени после нанесения раны.
Ускоренное затягивание и ускоренная пролиферация ран, обработанных Сх43 asODN
Были сделаны макроскопические фотоснимки ран в идентичных условиях, и их площадь измеряли цифровым способом (Qiu, С., Coutinho, P., Frank, S., Franke, S., Law, L.Y., Martin, P., Green, C.R. and Becker, D.L. (2003). Targeting connexin 43 expression accelerates the rate of wound repair. Curr Biol 13, 1697-703), раны, обработанные Сх43 asODN, были значительно меньших размеров, более сухими, менее воспаленными и более быстро затягивающимися по сравнению с контрольными ранами в 1-ый и 2-ой день. На 7-ой день раны покрылись корками, и это дало возможность сделать точные измерения затягивания ран. Вскоре после повреждения с края раны началась реэпителизация, закрывающая оголенную область. Обработка как иссеченных, так и разрезанных ран с помощью Сх43 asODN приводит к более быстрой реэпителизации по сравнению с ранами, обработанными контрольными ODN. Поэтому мы выяснили, может ли это частично происходить из-за повышенной пролиферации кератиноцитов и фибробластов в заживающей коже ран, обработанных Сх43 asODN (фигуры 2А-2Н). Хотя между контрольной и обработанной группами было обнаружено небольшое различие в пролиферации кератиноцитов на краю эпидермиса раны (фигура 2Е), мы показали, что через 2 дня и через 7 дней действительно существует значительно повышенное количество BrdU-позитивных клеток в нарождающемся эпидермисе раны, обработанной Сх43 asODN (фигура 2F). Сходным образом, на 1-ый и 2-ой день подсчет BrdU-позитивных клеток на краю дермы раны выявил немного больше клеток после обработки asODN и значительно больше в грануляционной ткани (фигура 2G и 2Н). Эти результаты находятся в соответствии с результатами наших предварительных микроскопических наблюдений и предполагают, что кратковременное регуляторное торможение уровня Сх43 в областях раны приводит к всплеску пролиферации кератиноцитов на краю раны, который сохраняется, так как кератиноциты вызывают реэпителизацию раны. Такая повышенная пролиферация может вносить вклад в ускорение реэпителизации и усиление созревания грануляционной ткани в ранах, обработанных asODN.
Сниженный приток воспалительных клеток в раны, обработанные Сх43 asODN - нейтрофилы и макрофаги
Несколько линий лейкоцитов проникают в область раны с различающейся динамикой во время воспалительного ответа на повреждение тканей. Две первичные клеточные линии представлены нейтрофилами и макрофагами, каждые из них может вызывать сильные эффекты на различные аспекты процесса репарации. Ранее мы оценили проникновение нейтрофилов в раны, обработанные Сх43 asODN, и в этих опытах с помощью антител к МРО мы подтверждаем, что число нейтрофилов значительно снижено в 1-ый и во 2-ой день, на стадии, когда число нейтрофилов достигает наивысшего значения в контрольных обработанных ранах (фигура 3). В настоящий момент есть четкое доказательство того, что проникновение макрофагов в область раны может быть связано со скоростью реэпителизации и последующим распространением рубцевания в области раны, поэтому мы исследовали количество макрофагов с помощью иммуногистохимического анализа F4/80 (фигуры 4А-4С). Мы обнаружили, что число макрофагов в области раны, обработанной Сх43 asODN, было значительно снижено на 2-ой и 7-ой день после повреждения по сравнению с контрольными ранами, обработанными sODN, это снижение составляло 33% на 2-ой день и 32% на 7-ой день (фигура 4С). Эти результаты отчетливо указывают на то, что резкое падение уровня Сх43 в момент нанесения раны приводит к последующему драматическому ослаблению как ранней нейтрофильной, так и более поздней макрофаговой фазы и фаз воспаления.
Сниженная экспрессия Сс12 и TNF-α в ранах, обработанных Сх43 asODN
Нейтрофилы и макрофаги в области раны высвобождают огромное разнообразие провоспалительных цитокинов и хемокинов, которые непосредственно действуют на клетки в этом участке (кератиноциты, фибробласты и эндотелиальные клетки) и усиливают воспалительную реакцию в ране. Чтобы исследовать, как сокращенное проникновение воспалительных клеток после падения уровня Сх43 влияет на уровень этих сигналов, мы анализировали Сс12 и TNF-α, типичных представителей хемокинов и цитокинов, соответственно. Чтобы количественно оценить уровень экспрессии Сс12 и TNF-α, мы проводили RT-ПЦР-анализ на поврежденной ране в 1-ый, 2-ой и 7-ой день (фигуры 5А и 5В). В 1-ый день обе мРНК регуляторно повышались в значительной степени в участках ран, обработанных контрольными sODN, и обе достигали максимального уровня экспрессии на 2-ой день, после чего их уровень снижался. Для сравнения, уровень экспрессии Сс12 и TNF-α в ранах, обработанных Сх43 asODN, был значительно сниженным (Р<0,05) на 2-ой день (Сс12) и 7-ой день (TNF-α). Эти результаты указывают на то, что сниженный рекрутинг нейтрофилов и макрофагов в раны, обработанные Сх43 asODN, действительно сопровождался снижением экспрессии этих сигнальных молекул, которая не компенсировалась за счет клеток других типов.
Чтобы оценить уровень экспрессии Сс12 и TNF-α, проводили RT-ПЦР-анализ тканей раны в 1-ый, 2-ой и 7-ой день. В 1-ый день обе мРНК регуляторно повышались в значительной степени в участках ран, обработанных контрольными sODN, и обе достигали максимального уровня экспрессии на 2-ой день, после чего их уровень снижался. Для сравнения, уровень экспрессии Сс12 и TNF-α в ранах, обработанных Сх43 asODN, был значительно сниженным (Р<0,05) на 2-ой день (Сс12) и 7-ой день (TNF-α). Эти результаты указывают на то, что пониженный рекрутинг нейтрофилов и макрофагов в раны, обработанные Сх43 asODN, действительно сопровождался снижением экспрессии этих сигнальных молекул, которая не компенсировалась за счет клеток других типов.
Повышенная экспрессия TGF-β1 в области ран, обработанных Сх43 asODN
Было сообщено, что ассоциированный с ранами фактор роста TGF-β1 играет важную роль в различных стадиях процесса заживления ран. Поэтому мы анализировали уровень экспрессии TGF-β1 в участках ран, обработанных контрольными sODN и Сх43 asODN, с помощью RT-ПЦР в 1-ый, 2-ой и 7-ой день после нанесения раны (фигура 6). В 1-ый и 7-ой день TGF-β1 был на низком уровне и не было выявлено различий между контрольными и опытными ранами. Однако на 2-ой день после повреждения экспрессия TGF-β1 в ранах, обработанных asODN, была значительно повышена (Р<0,05) по сравнению с ранами, обработанными контрольными sODN. Иммуноокрашивание на TGF-β1 во 2-ой день выявило TGF-β1-позитивные клетки в дерме как в области раны, так и в прилегающих тканях. Большая часть клеток была округлой формы и имела внешнее сходство с лейкоцитами. Однако в ткани, обработанной Сх43 asODN, на дермальных краях раны можно было видеть дополнительный TGF-β1-позитивный клеточный тип в большом количестве. Эти клетки были вытянуты и по морфологии больше походили на фибробласты. Интересно, что в эпидермисе ран, обработанных Сх43 asODN, TGF-β1, как оказалось, окрашивается намного более интенсивно, чем в эпидермисе контрольных ран (фигура 6). Эти результаты позволяют предположить, что повышенная экспрессия TGF-β1 может давать вклад в некоторые изменения, которые мы видим при заживлении ран после обработки Сх43 asODN.
Образование и созревание грануляционной ткани
Как было указано, сжатие соединительной ткани раны является ключевым компонентом процесса репарации кожи. Эта стадия тесным образом связана с миграцией фибробластов в основание раны и их дифференцировкой в сокращающиеся миофибробласты с последующей их утратой (Martin, P. (1997). Science 276, 75-81). С помощью контрастного окрашивания родамин-фаллоидином совместно с DAPI на 2-ой день мы обнаружили значительное увеличение (среднее значение 39,4 в контроле и 99,2 после обработки asODN; Р<0,01) числа продолговатых фибробластоподобных клеток на краях раны, обработанной Сх43 asODN, по сравнению с контрольными ранами (фигуры 7А и 7В). Эти результаты позволяют предположить, что проникновение фибробластов для образования грануляционной ткани раны усиливается в ранах, если снижен уровень белка Сх43. Это может происходить из-за увеличенной миграции и значительно более выраженной пролиферации клеток, которую мы видим в грануляционной ткани ран, обработанных asODN.
Чтобы исследовать, происходит ли повышенная скорость миграции фибробластов из-за снижения экспрессии белка Сх43, мы использовали анализ фибробластов при заживлении ран. В этом анализе мы снижали уровень белка Сх43 путем нанесения Сх43 asODN на конфлюэнтную культуру фибробластов за два часа до анализа соскобов раны. Так как белок Сх43 быстро обновляется (со временем полураспада, составляющим менее 1,5-2 часов), этого было достаточно, чтобы обеспечить 95%-ое падение уровня белка в пределах двух часов, которое продолжается от 8 до 48 часов в зависимости от типа клеток. Культуры фибробластов, которые были обработаны Сх43 asODN, демонстрировали значительно (Р=0,02) увеличенную скорость затягивания раны по сравнению с контролями (фигура 7D), что полностью соответствует нашим результатам, полученным in vivo. Это убедительно доказывает, что резкое падение уровня белка Сх43 повышает скорость миграции фибробластов как in vitro, так и in vivo, и поэтому стимулирует скорость образования грануляционной ткани.
При измерении площади грануляционной ткани мы обнаружили, что на 5-ый день обработанная ткань была немного меньше, чем необработанная ткань, но это различие не было значительным. Однако мы обнаружили, что на 7-ой, 10-ый и 14-ый день после повреждения обработанные Сх43 asODN раны имеют значительно (*Р<0,05; **Р<0,01) меньшие площади грануляционной ткани, чем раны, обработанные контрольными sODN.
При измерении площади грануляционной ткани мы обнаружили, что на 5-ый день обработанная ткань была немного меньше, чем необработанная ткань, но это различие не было значительным. Однако мы обнаружили, что на 7-ой, 10-ый и 14-ый день после повреждения обработанные Сх43 asODN раны имеют значительно (*Р<0,05; **Р<0,01) меньшие площади грануляционной ткани, чем раны, обработанные контрольными sODN (фигура 9). Чтобы исследовать, как происходит более быстрое сжатие грануляционной ткани, мы окрашивали срезы с помощью набора TUNEL, чтобы увидеть гибель апоптотических клеток, или с помощью антител к гладкомышечному актину (SMA) в качестве маркера миофибробластов. Хотя в обработанной грануляционной ткани всегда было немного меньше апоптотических клеток, мы не обнаружили значимых различий в числе TUNEL-позитивных клеток между контрольными и обработанными животными на 5-ый, 7-ой и 10-ый день после нанесения раны (фигура 10). Однако мы обнаружили значительное различие между двумя группами во всех временных точках при окрашивании на SMA (фигура 11). На 5-ый день на краях грануляционной ткани ран, обработанных Сх43 asODN, можно было обнаружить окрашивание на SMA, но в контрольных ранах окрашивания пока еще не было видно. На 7-ой день окрашивание на SMA можно было обнаружить на краях грануляционной ткани контрольных ран и по всей грануляционной ткани ран, обработанных Сх43 asODN (фигуры 11А и 11В). Количественная оценка окрашивания на краях грануляционной ткани выявила, что оно было более значимо (Р=0,004) в ранах, обработанных Сх43 asODN (фигура 11 Е). На 10-ый день после нанесения раны большая часть окрашивания на SMA исчезла с краев грануляционной ткани ран, обработанных Сх43 asODN, немного оставаясь только в центре раны. Это сильно отличалось (Р=0,000002) от контрольных ран, которые демонстрировали мощную экспрессию SMA по всей грануляционной ткани (фигуры 11C и 11D). Эти результаты означают, что дифференцировка фибробластов в миофибробласты происходит раньше в ранах, обработанных Сх43 asODN, и что эти клетки продолжают сокращать рану и исчезают значительно быстрее, чем в контрольных ранах. Можно предположить, что раны, обработанные Сх43 asODN, на 2-3 дня опережают контроли по созреванию их грануляционной ткани.
Ангиогенез
В дополнение к проникающим фибробластам, другими основными клеточными компонентами грануляционной ткани ран являются эндотелиальные клетки новых кровеносных сосудов. Поэтому мы провели иммуногистохимическое окрашивание с помощью антител к CD31 и антител к фактору фон Виллебранда или с помощью изолектин В-FITC, чтобы оценить ангиогенез в области обработанных ран на 5-ый, 7-ой, 10-ый и 14-ый день после нанесения раны (фигуры 12А-12Н). На 5-ый день в грануляционной ткани контрольных ран нельзя было увидеть окрашивание кровеносных сосудов, тогда как на краях грануляционной ткани всех ран, обработанных Сх43 asODN, было видно такое окрашивание. На 7-ой день были отчетливо обнаружены кровеносные сосуды по всей грануляционной ткани в пяти из шести ран, обработанных Сх43 asODN, но они только начинали проникать в края грануляционной ткани в контролях. Однако, если кровеносные сосуды ран, обработанных asODN, были более широко распространены, оказалось, что в те же самые интервалы времени они были значительно меньше и тоньше, чем в контролях (фигура 12А). Это означает, что если окрашивание кровеносных сосудов количественно оценивали на 7-ой и 10-ый день, то наблюдалось более интенсивное окрашивание (7-ой день, Р=0,0019; 10-ый день Р=0,015) в контролях, где сосуды были крупнее. На 14-ый день размер кровеносных сосудов и интенсивность окрашивания были сходными как в опытной, так и в контрольной группах (фигуры 12Е, 12F). Эти результаты позволяют предположить, что ангиогенез происходит значительно раньше после обработки Сх43 asODN. Вместе с другими результатами, имеющими отношение к созреванию грануляционной ткани, можно думать, что обработка увеличивает скорость созревания раны на 2-3 дня.
Как было показано в результатах, здесь представлены типичные патологические и биологические последствия кратковременного торможения уровня Сх43 в участках заживления кожных ран с помощью Сх43 asODN, доставляемых из медленно высвобождающего плюронового геля Pluronic F-127. Обработка быстро снижает уровень белка Сх43 в поврежденных участках эпидермиса и дермы в течение, по меньшей мере, 24 часов с некоторым возвратом уровня экспрессии в дерме не позднее 48 часов и без очевидной разницы между группами через 7 дней. Мы демонстрируем, что обработка Сх43 asODN приводит к заметному ускорению заживления кожных ран, что соответствует пониженной инфильтрации лейкоцитов, сниженному уровню цитокинов, повышенной реэпителизации и более интенсивному сокращению раны.
Воспаление
Начальный ответ на нанесение раны обычно состоит в образовании кровяного сгустка, который вместе с локально поврежденными тканями высвобождает провоспалительные сигналы, которые запускают инфильтрацию клеток в виде нейтрофилов, а затем макрофагов в участок раны. Эти сигналы и сигналы от проникающих воспалительных клеток влияют как на реэпителизацию, так и на сокращение соединительной ткани раны (Martin, P. (1997). Science 276, 75-81). Миграция и инфильтрация воспалительных клеток в рану связана с межклеточными взаимодействиями и взаимодействиями между клеткой и внеклеточным матриксом и с расширением кровеносных сосудов в непосредственной близости от раны. Недавно было показано, что Сх43 экспрессируется в активированных лейкоцитах и в участках клеточных контактов типа лейкоцит-лейкоцит и лейкоцит-эндотелиальная клетка в процессе их выхода из сосудов в ткани в условиях воспаления, и что функциональные каналы Сх43 вовлечены в высвобождение цитокинов и иммуноглобулинов (проанализировано в работе: Oviedo-Orta, E. and Evans, W.H. (2004). Biochim Biophys Acta 1662, 102-12). Результаты, полученные в этом исследовании, показывают, что количество и нейтрофилов, и макрофагов значительно снижалось в ранах, обработанных Сх43 asODN, что находится в соответствии с необходимостью экспрессии Сх43 для выхода нейтрофилов из сосудов в ткани и высвобождением провоспалительных цитокинов. Кроме того, результаты показывают, что уровень хемокина Сс12 и цитокина TNF-α, которые, как сообщалось, являются хемоатрактантами для нейтрофилов и моноцитов/макрофагов (Rossi, D. and Zlotnik, A. (2000). Annu Rev Immunol 18, 217-42), также снижается после обработки Сх43 asODN на 2-ой и 7-ой день, соответственно. Ясно, что пониженный уровень этих и других факторов роста, хемокинов и цитокинов в участке раны является показателем того, что эти вещества, полезные для заживления ран, являются важными медиаторами (как тормозящими, так и активирующими) сниженного проникновения нейтрофилов и других воспалительных клеток.
В некоторых недавних сообщениях было постулировано, что обычная воспалительная реакция не является необходимой для заживления кожных ран (Martin, Р. and Leibovich, S.J. (2005). Trends Cell Biol.). Сообщалось, что PU.1-нулевые мыши, которые генетически утратили нейтрофилы и макрофаги, восстанавливают повреждения кожи без образования рубцов и с той же скоростью или быстрее, чем их сибсы дикого типа (Martin, Р., D'Souza, D., Martin, J., Grose, R., Cooper, L., Maid, R. and McKercher, S.R. (2003). Curr Biol 13, 1122-8). Сходным образом, было показано, что уменьшение количества нейтрофилов в областях раны путем нанесения антител к нейтрофилам приводит к более быстрой реэпителизации (Dovi, J.V., He, L.K. and DiPietro, L.A. (2003). J Leukoc Biol 73, 448-55). Существует корреляция между увеличением миграции в эпидермисе и способного к пролиферации и снижением воспалительной реакции и возможной ролью падения уровня Сх43 в переднем крае кератиноцитов и фибробластов. Кроме того, падение уровня Сх43 может приводить к уменьшению проникновения лейкоцитов. Ткани, на которые нацелено действие Сх43 asODN, могут включать эндотелиальные клетки или лейкоциты, сообщалось, что для эффективного выхода и тех, и других из сосудов в ткани и для выраженного воспалительного ответа необходима экспрессия Сх43 (Oviedo-Orta, В., Hoy, Т. and Evans, W.H. (2000). Immunology 99, 578-90; Oviedo-Orta, E., Gasque, P. and Evans, W.H. (2001). FASEB J 15, 768-74). На основании этих результатов можно предположить, что изменение экспрессии белка Сх43 в эндотелиальных клетках или лейкоцитах также может регулировать воспалительную реакцию.
TGF-β1
В ранах, обработанных Сх43 asODN, мы обнаружили, что уровень мРНК для TGF-β1 значительно повышается на 2-ой день по сравнению с контролями, но находится на относительно низком уровне как в опытной, так и контрольной группах в 1-ый и 7-ой день. Сообщалось, что экспрессия TGF-β1 связана со многими ключевыми событиями в процессе заживления ран. Эти описанные активности включают иммуносупрессию, стимулирование миграции и пролиферации фибробластов, улучшение сокращения ран, улучшение образования грануляционной ткани, улучшение синтеза и отложения коллагена, стимулирование ангиогенеза и стимулирование реэпителизации. Было показано, что эффект TGF-β1 на рану до некоторой степени зависит от дозировки и использованной модели раны. Также были представлены различные результаты исследования перемещения различных частей сигнальных путей TGF-β1 и эксперименты с использованием генетических модификаций. Например, у нокаутных по TGF-β1 мышей, которые дефицитны по Т-клеткам и В-клеткам (мыши Scid-/-), заживление ран сильно замедленно (Crowe, M.J., Doetschman, Т. and Greenhaigh, D.G. (2000) J. Invest. Dermatol 115:3-11). Однако, если сигнальный путь с участием TGF-β1 нарушен, как в случае нокаутных по Smad3 мышей, заживление ран ускоряется (Ashcroft, G.S., Yang, X, Glick, А.В., Weinstein, M., Letterio, J.L., Mizel, D.E., Anzano, M., Greenwell-Wild, Т., Wahl, S.M., Deng, C. and Roberts, А.В. (1999) Nat Cell Biol. 1:260-6). Сходным образом, экспрессия доминантно-негативного рецептора TGF-β II типа в кератиноцитах приводит к реэпителизации, которая опять является ускоренной. Трансгенные мыши с суперэкспрессией TGF-β1 демонстрируют более высокое качество заживления ран с пониженным образованием рубцов (Shah, M., Revis, D., Herrick, S., Baillie, R., Thorgeirson, S., Ferguson, M. and Roberts, A. (1999) Am. J. Pathol. 154:1115-24). Также трансгенные мыши, лишенные бета 3-интегрина, демонстрируют повышенный уровень TGF-β1, что ассоциировано с улучшенным заживлением и ускоренной миграцией фибробластов в раны (Reynolds, L.E., Conti, F.J., Lucas, M., Grose, R., Robinson, S., Stone, M., Saunders, G., Dickson, C, Hynes, R.O., Lacy-Hulbert, A. and Hodivala-DUke, K. (2005) Nat. Med. 11:167-74). Нокаутные по CD18 мыши демонстрируют пониженную экспрессию TGF-β1 и характеризуются медленным заживлением ран, которое может быть восстановлено с помощью инъекции TGF-β1 в края раны (Peters, Т., Sindrilaru, A., Hinz, В., Hinrichs, R., Menke, A., Al-Azzeh, E.A., Holzwarth, K., Oreshkova, Т., Wang, H., Kess, D., Walzog, В., Sulyok, S., Sunderkotter, C., Friedrich, W., Wlaschek, M., Krieg, T. and Scharffetter-Kochanek, K. (2005) EMBO J. 24:3400-10).
Повышенный уровень окрашивания на TGF-β1, который мы видим на 2-ой день, оказывается более интенсивным в вытянутых фибробластоподобных клетках на краях раны и в кератиноцитах на краях раны. Это согласуется с описанными ранее эффектами TGF-β1 на усиление пролиферации и миграции (Postlethwaite, A.E., Keski-Oja, J., Moses, H.L. and Kang, A.H. (1987) J Exp Med 165:251-6), каждую из которых мы обнаруживаем на ранних стадиях репарации тканей. Действительно, повышение уровня TGF-β1 может быть одним из факторов, которые в этих условиях вносят вклад в стимулирование заживления в контексте повышения скорости пролиферации и миграции фибробластов и повышения скорости синтеза коллагена, которые мы видим в эти ранние моменты времени.
Было показано, что как активное снижение уровня белка Сх43, так и действие фактора роста TGF-β1, связанного с ранами, активирует экспрессию Col1α1 (Cutroneo, K.R. (2003). How is Type I procollagen synthesis regulated at the gene level during tissue fibrosis. J Cell Biochem 90, 1-5; Waggett, A.D., Benjamin, M. and Ralphs, J.R. (2006) Eur J Cell Biol. 2006 Jul 19; [Epub ahead of print]). Повышенный уровень экспрессии Col1α1 и отложение коллагена, которые мы видим после обработки, могут иметь отношение к повышенной экспрессии TGF-β1 на 2-ой день или к снижению уровня белка Сх43, или и к тому, и к другому событию вместе.
Фактор роста, ассоциированный с ранами (TGF-β1), выполняет очень разнообразные функции на многих стадиях процесса заживления ран. TGF-β1 был на низком уровне на 1-ый и 7-ой день без особых различий между контрольными и опытными ранами. Однако на 2-ой день после повреждения экспрессия TGF-β1 в ранах, обработанных asODN, была значительно повышена (Р<0,05) по сравнению с ранами, обработанными контрольными sODN. Иммуноокрашивание на TGF-β1 на 2-ой день выявило TGF-β1-позитивные клетки в дерме как в области раны, так и в прилегающих тканях. Наибольшее количество клеток имело округлую форму и внешнее сходство с лейкоцитами. Однако в ткани, обработанной Сх43 asODN, на дермальных краях раны можно было видеть дополнительный TGF-β1-позитивный клеточный тип в большом количестве. Эти клетки были вытянуты и по морфологии больше походили на фибробласты. Интересно, что в эпидермисе ран, обработанных Сх43 asODN, TGF-β1, как оказалось, окрашивается намного более интенсивно, чем в эпидермисе контрольных ран (фигура 6). Эти результаты позволяют предположить, что повышенная экспрессия TGP-β1 может давать вклад в некоторые изменения, которые мы видим при заживлении ран после обработки Сх43 asODN.
Хотя было предположено, что TGF-β1 подавляет воспаление, маловероятно, что он является главным фактором, приводящим к уменьшению воспаления, которое мы наблюдаем и которое уже очевидно в 1-ый день до того как повышается уровень TGF-β1. Также, хотя показано, что TGF-β1 стимулирует ангиогенез и созревание грануляционной ткани на последних стадиях процесса заживления ран, мы не видим повышение уровня TGF-β1 в эти моменты времени; скорее он находится на том же низком уровне, что и в контролях. Поэтому стимулировать ускорение созревания грануляционной ткани, которое мы видим после обработки, должны другие факторы.
Эти эксперименты поддерживают предположение о том, что TGF-β1 был вовлечен в подавление воспаления, стимулирование ангиогенеза и созревания грануляционной ткани в процессе заживления ран, и указывают на то, что модулирование TGF-β1 в комбинации с другими способами обработки ран могут быть полезными для стимулирования процесса заживления ран.
Миграция и пролиферация
Миграция и пролиферация фибробластов и кератиноцитов является неотъемлемой частью заживления кожных ран, они вносят вклад как в сокращение раны, так и в затягивание раны. В этом исследовании мы демонстрируем повышенную миграцию фибробластов в участок раны и ускоренную реэпителизацию после обработки Сх43 asODN. Эти результаты указывают на то, что Сх43 может играть важную роль в модулировании перемещения клеток. Другими авторами были сообщены противоречащие результаты о роли Сх43 в перемещении клеток, согласно которым в эмбриональном развитии дефицитные по Сх43 проэпикардиальные клетки мигрировали быстрее, чем клетки, экспрессирующие Сх43 (Li, W.E., Waldo, K., Linask, K.L., Chen, Т., Wessels, A., Parmacek, M.S., Kirby, M.L. and Lo, C.W. (2002). Development 129, 2031-42). Однако та же группа ранее уже сообщала о том, что Сх43-дефицитные клетки нервного гребня демонстрировали сниженные скорости миграции (Huang, G.Y., Cooper, E.S., Waldo, K., Kirby, M.L., Gilula. N.B. and Lo, C.W. (1998). J Cell Biol 143, 1725-34). Последний результат согласуется с низкими скоростями миграции ретинальных нейроэпителиальных клеток, которые обладали нарушенной коммуникацией или сниженной экспрессией Сх43 (Pearson R., Luneborg, N., Becker, D.L. and Mobbs P. (2005) J. Neurosci 25 (46), 10803-10814). Эти различия во влиянии коммуникации на миграцию, возможно, могут отражать вовлеченность различных типов клеток и то, что клетки мигрируют или независимо, или в виде сообщающейся группы.
Более быстрая реэпителизация и повышенная скорость образования грануляционной ткани могут также быть приписаны повышенной пролиферации в группе, обработанной asODN, которую мы обнаружили в зарождающемся эпидермисе и грануляционной ткани как на 2-ой, так и 7-ой день после нанесения раны. Как и в случае со скоростями миграции, есть противоречивые сообщения относительно экспрессии Сх43 и пролиферации. Пролиферация Сх43-дефицитных проэпикардиальных клеток усиливается, но этого не наблюдают в Сх43-дефицитных сердечных клетках нервного гребня или в развивающейся невральной ретине, обработанных Сх43 asODN, где снижена пролиферация (Huang, G.Y., Cooper, E.S., Waldo, K., Kirby, M.L., Gilula, N.B. and Lo, C.W. (1998). J Cell Biol 143, 1725-34; Becker, D.L. and Mobbs, P. (1999) Exp. Neurology, 156, 326-332; Li, W.E., Waldo, K., Linask, K.L., Chen, Т., Wessels, A., Parmacek, M.S., Kirby, M.L. and Lo, C.W. (2002). Development 129, 2031-42). Интересно, что эффекты снижения уровня Сх43 на проэпикардиальные клетки вызывают как пролиферацию, так и миграцию, тогда как эффект на клетки нервного гребня и ретинальные нейроэпителиальные клетки состоит в нарушении пролиферации и миграции. Наши эксперименты в этой работе демонстрируют, что экспрессия Сх43, сниженная под влиянием asODN, в анализе фибробластов при заживлении ран значительно ускоряет скорость их миграции. Снижение уровня белка Сх43 может, таким образом, способствовать более быстрой реэпителизации и миграции фибробластов в грануляционную ткань, которые мы здесь видим. Альтернативно, влияние может происходить из-за повышенного уровня TGF-β1, который мы наблюдаем на 2-ой день в ранах, обработанных Сх43 asODN, который, как было предположено, усиливает пролиферацию клеток и повышает скорости миграции фибробластов (Mustoe, T.A., Pierce, G.F., Thomason, A., Gramates, P., Spom, M.B. and Deuel, T.F. (1987). Science 237, 1333-6: Postlethwaite, A.E., Keski-Oja, J., Moses, H.L. and Kang, A.H. (1987) J Exp Med 165:251-6), или из-за комбинации обеих возможностей.
Ангиогенез
Ангиогенез является другим важнейшим признаком образования и созревания грануляционной ткани, в том числе заселения, распространения и последующей перестройки. В этом исследовании кровеносные сосуды, прорастающие в грануляционную ткань раны, обработанной Сх43 asODN, были намного более развитыми, чем в контролях.
На 5-ый день можно было отчетливо наблюдать кровеносные сосуды, проникающие в грануляционную ткань всех обработанных ран, но в любой контрольной грануляционной ткани сосудов видно не было. К 7-му дню кровеносные сосуды можно было наблюдать по всей грануляционной ткани в большинстве обработанных ран, но в контрольных ранах они были видны только по краям. Интересно, что кровеносные сосуды в контрольных ранах были толще на этих ранних стадиях и поэтому давали значительно большую площадь окрашивания как на 7-ой, так и 10-ый день. К 14-му дню кровеносные сосуды в обработанных ранах развивались до больших размеров и были похожи на сосуды в контролях. Известно, что Сх43 вовлечен в коронарный васкулогенез и ангиогенез (Walker, D.L., Vacha, S.J., Kirby, M.L. and Lo, C.W. (2005). Dev Biol 284, 479-98). Однако обнаружение того, что уровень белка Сх43 к 7-му дню после повреждения сходен в контрольных и обработанных ранах, позволяет предположить, что ангиогенез в ранах, обработанных Сх43 asODN, на этой стадии наиболее вероятно находится под непрямым воздействием изменений, опосредованных антисмысловым соединением, которые мы видим на ранних стадиях. Возможно, что ангиогенез стимулируется ранним повышением уровня TGF-β1, так как этот фактор роста, как было показано, стимулирует ангиогенез (Roberts, A.B., Sporn, M.B., Assoian, R.K., Smith, J.M., Roche, N.S., Wakefield, L.M., Heine, U.I., Liotta, L.A., Falanga, V., Kehrl, J.H. et al., (1986). Proc Natl Acad Sci USA 83, 4167-71), но временные рамки этих процессов не соответствуют друг другу.
Созревание грануляционной ткани, сокращение и клеточная смерть
Площадь грануляционной ткани после обработки Сх43 asODN неизменно меньше, чем в контрольных ранах. Это, вероятно, может происходить из-за нескольких факторов. Уменьшение воспалительной реакции вызывало в свою очередь несколько эффектов на последующие стадии процесса заживления. Сокращенное проникновение нейтрофилов приведет к уменьшению повреждений в окружающей ткани, и наиболее иссеченные раны увеличиваются в размерах первые несколько дней заживления, так как вносит вклад воспалительный процесс, тогда как в тот же период времени обработанные раны значительно сокращаются. Таким образом, уменьшение воспаления, как можно было ожидать, приводит к значительно меньшей площади, которую заполняют фибробласты. Так как одним из многих ключевых эффектов, которые мы наблюдаем, является усиление пролиферации фибробластов и миграция, раны меньшего размера могут заполняться намного быстрее и грануляционная ткань может начать созревать значительно быстрее.
Таким образом, эти исследования представляют наши первые результаты проведенного анализа механизма, лежащего в основе биологического клеточного регуляторного снижения уровня белка Сх43 в областях раны. Локальное торможение сильно влияет на очень ранние события при заживлении ран. В частности, оно ограничивает распространение иммунной реакции и развития процесса и скорость реэпителизации и на уровень и скорость образования грануляционной ткани. Грануляционная ткань поэтому имеет меньшую площадь для заполнения и делает это быстрее, что приводит к более раннему сокращению раны и созреванию. Этот подход, очевидно, предоставляет потенциал для новых методов лечения для улучшения заживления ран в различных клинических ситуациях.
На основании этих результатов экспериментальное снижение экспрессии коннексина 43 в местах кожных ран заметно улучшает скорость и качество заживления. Физиологические и клеточно-биологические аспекты процесса репарации сравнивают при обработке с помощью типичного антиконнексинового средства - антисмыслового олигодезоксинуклеотида, направленного против коннексина 43 - и без него. Обработанные раны демонстрировали ускоренное заживление кожи со значительно усиленной пролиферацией и миграцией кератиноцитов и фибробластов. Резкое снижение in vitro уровня коннексина 43 в фибробластной модели заживления ран также приводило к значительно ускоренному заживлению, ассоциированному с повышением уровня мРНК для трансформирующего фактора роста бета 1 и коллагена альфа1, и общего содержания коллагена в участке раны. Обработанные раны демонстрировали усиленное образование и созревание грануляционной ткани с более быстрым ангиогенезом, дифференцировкой миофибробластов, и сокращение раны, очевидно, происходило ко 2-3 дню. Рекрутинг как нейтрофилов, так и макрофагов был значительно снижен в обработанных ранах, с сопутствующим снижением инфильтрации лейкоцитов. В свою очередь уровень мРНК для хемокинового лиганда 2 и фактора некроза опухоли альфа был снижен в обработанных ранах. Эти результаты показывают, что в этих условиях на ранней стадии процесса заживления кожи снижение уровня белка коннексина 43 с помощью специфического к коннексину 43 антисмыслового соединения в месте раны усиливает репарацию, по меньшей мере, частично, путем ускорения миграции и пролиферации клеток, и ослабления воспаления, и дополнительного повреждения, которое он может вызывать.
Резкое снижение уровня белка Сх43 в месте раны приводит к усилению пролиферации и миграции кератиноцитов и скорости, с которой фибробласты мигрируют в рану и нижележащий слой коллагеновой основы. Это коррелирует со снижением инфильтрации нейтрофилов и сопутствующим снижением уровня мРНК хемокинового лиганда 2 (Сс12) и цитокинового фактора некроза опухоли альфа (TNF-α). Затем наблюдают сниженный рекрутинг макрофагов, возможно, как следствие кратковременного снижения исходной воспалительной реакции. В противоположность этому в ранах, обработанных Cx43AsODN, наблюдали повышенную экспрессию TGF-β1 с увеличением содержания гидроксипролина и коллагена типа 1α1. Вместе эти видоизмененные ответы приводили к значительно улучшенному заживлению ран.
Пример 2
Химеры денудированной стромы свиньи культивировали в течение двух недель и затем оценивали с помощью матрицы антител к факторам роста/цитокинам (измеряет уровень белков 120 различных факторов роста/цитокинов).
Лимбальные кольца человека, полученные после хирургического удаления центральной роговицы для кератопластики (трансплантат), помещали на раздел фаз между воздушной средой и жидкостью органотипической культуры, и в центральную часть помещали денудированный свиной внеклеточный стромальный матрикс (фигура 14). Стромальный матрикс свиньи денудировали (удаляли клетки) с помощью замораживания в жидком азоте и оттаивания.
Химеры выращивали до 2 недель, в течение которых лимбальные эпителиальные клетки человека вызывали реэпителизацию стромы свиньи 5-7 слоями клеток нормального полностью дифференцированного эпителия. Кроме того, лимбальные стромальные кератиноциты человека пролиферировали и мигрировали сквозь лимбальное кольцо - стромальную вставку, чтобы вновь заселить стромальный матрикс свиньи человеческими кератиноцитами.
В следующем эксперименте в 1-ый день химеры обрабатывали антисмысловым ODN, специфичным к коннексину 43. Это приводило к значительному увеличению скорости реэпителизации и полному покрытию эпителием стромы свиньи в течение 3 дней по сравнению с 7-14 днями для контролей.
Через две недели культивирования химеры разрезали пополам: одну половину использовали для гистологического анализа, а другую - для анализа на матрице антител к факторам роста и цитокинам. Для анализа факторов роста и цитокинов центральный участок стромы (с эпителием, полностью восстановленным клетками человека) и частично повторно заселенную строму (кератиноциты человека) удаляли и гомогенизировали раздельно от лимбального кольца человека, которое содержало популяции стволовых клеток. Гомогенаты исследовали на матрице антител к факторам роста/цитокинам (фигура 15) и проводили анализ уровня факторов роста с помощью денситометрического анализа мембран матрицы. Анализ ключевых факторов роста выявил количество интересующих факторов (фигура 16 и фигура 17).
Анализ уровня факторов роста в химерной строме в сравнении с участками лимбальных колец химер через две недели культивирования (контрольные роговицы - без обработки антисмысловым соединением) выявил два фактора роста, представляющие особый интерес (фигура 16). Это был очень высокий уровень IGFBP-2 в химерной строме и повышенный уровень IGF-1 в лимбальном кольце. Как утверждают, первый фактор стимулирует клеточную миграцию (необходимую для повторного заселения стромы стромальными кератиноцитами лимбального кольца), а последний фактор стимулирует пролиферацию клеток (необходима в лимбальном кольце для обеспечения источника клеток, вновь заселяющих строму).
Анализ уровня факторов роста в химерной строме в сравнении с участками лимбальных колец химер, обработанных Cx43As ODN, через две недели культивирования выявил два фактора роста, представляющие особый интерес (фигура 17). Это был очень высокий уровень IGF-7 в химерной строме, обработанной антисмысловым соединением, по сравнению с необработанными контролями, и повышенный уровень IGFBP-2 как в лимбальном кольце, так и в строме по сравнению с необработанными контролями, в особенности, контрольными лимбальными кольцами. Как утверждают, первый фактор стимулирует эпителиальный рост (согласующийся с повышенной реэпителизацией, наблюдаемой в химерах, обработанных антисмысловым соединением), а последний фактор стимулирует миграцию клеток (согласующуюся с повышенным повторным заселением эпителия из лимбального кольца в результате обработки антисмысловым соединением).
Пример 3
Ожоги второй степени обрабатывали с помощью распыления состава, включающего антиконнексиновое средство, 10 мкг/мл KGF, 30 нг/мл изоформы PDGF, 10 нг/мл IGF-1 и 30 нг/мл IGFBP-1. Распыляемый раствор оставляли сохнуть на воздухе. Повторное нанесение рекомендуют проводить каждые два часа.
Пример 4
Сшитую рану закрывали и перед накладыванием повязки на шов наносили мазь, приготовленную из антиконнексинового средства, 10% KGF и/или 5% PDGF. При необходимости может потребоваться повторное нанесение мази, что способствует или улучшает заживление раны, например, до 2-3 раз в день в течение примерно 4-7 дней или по обстоятельствам.
Пример 5
Состав 20%-ной окиси цинка, содержащий антиконнексиновое средство и один или несколько компонентов, приведенных ниже: 5% KGF, 2,5% PDGF, 10% IGFBP, наносят на небольшие царапины, солнечные ожоги и опрелости для ускоренного заживления этих ран.
Пример 6
Получали состав, содержащий антиконнексиновое средство и один или несколько активных антибиотических ингредиентов, например один или несколько приведенных ниже компонентов: бацитрацин, неомицин и полимиксин. В одном таком составе каждый грамм содержит полимиксина В сульфат (5000 единиц), бацитрацин цинка (400 единиц) и/или неомицин (3,5 мг). Неактивные ингредиенты состава могут включать масло какао, хлопковое масло, оливковое масло, пируват натрия, токоферола ацетат и медицинский вазелин в необходимых количествах. Предпочтительным антиконнексиновым средством является агент, направленный против коннексина 43. Такие составы наносят, например, на небольшие порезы, царапины, солнечные ожоги и опрелости для ускоренного/улучшенного заживления этих ран.
Пример 7
Состав, содержащий антиконнексиновое средство, как представлено в примере 6, получают таким образом, чтобы он также содержал местный анальгетик (например, прамоксин).
Пример 8
Состав, содержащий антиконнексиновое средство, который представлен в примере 6 или примере 7, получают таким образом, чтобы он содержал грамицидин.
Пример 9
Получают состав, содержащий антиконнексиновое средство и один или несколько активных противогрибковых ингредиентов, например миконазола нитрат. Один такой состав содержит 2% миконазола нитрата. Неактивные ингредиенты могут включать пропиленгликоль 300, полисорбат 20 (и), SD спирт 40В. Продукт можно составлять в виде крема, геля, распыляемого раствора или жидкости. Подходящие газы-вытеснители для распыляемого раствора включают диметиловый эфир. Предпочтительным антиконнексиновым средством является агент, направленный против коннексина 43. Такие составы наносят, например, для обработки атлетической стопы, паховой эпидермофитии и дерматомикоза.
Пример 10
Этот пример демонстрирует способ идентификации потенциальных цитокинов, полезных при лечении раны с помощью роговичной модели. Роговица содержит дендритные клетки, известные как клетки Лангерганса, которые активируются в ответ на повреждение. Дополнительные воспалительные клетки затем рекрутируются в лимб из кровеносных сосудов. Наши модельные роговицы культивируют изолированно от кровоснабжения, таким образом становится невозможным рекрутинг макрофагов, Т-клеток и полиморфоядерных клеток.
Модельные роговицы применяют для того, чтобы определить, достаточно ли присутствия клеток Лангерганса, чтобы помешать воспалительному ответу, и можно ли отличить этот ответ от реакции заживления. Две равноценные роговицы человека были повреждены с помощью различных методов. Одну роговицу иссекли на глубину 80 мкм по поверхности, диметром 7 мм путем экстирпации с помощью эксимерной лазерной фототерапевтической кератоктоэктомии, методики, которая стимулирует очень низкий уровень воспаления. Другую роговицу повреждали с помощью 7-миллиметрового кружка фильтровальной бумаги, смоченного в NaOH, в течение 1 минуты - известной методики для индукции воспаления. После культивирования в течение 24 часов роговицы разделяли пополам (одну половину использовали для иммуногистохимического анализа, а вторую - для анализа цитокинов). Затем перед подготовкой для анализа цитокинов с помощью матрицы антител роговицу делили на части, находящиеся в зоне заживления, и части, находящиеся вне этой зоны.
Воспалительный ответ идентифицировали в обеих половинах роговицы, но он был сильнее выражен при ожоге щелочью. Профиль цитокинов между двумя группами отличался из-за более выраженного воспаления в образце с ожогом щелочью, и потому что заживление начиналось раньше в роговице, обработанной лазером, так как требовалось удалить меньше некротической ткани. Фигура 18 показывает группу цитокинов, уровень которых повышен в ранах обоих типов, но значительно сильнее в воспалительной модели раны. Эта группа включала интерлейкины. Фигура 19 показывает группу цитокинов, уровень которых повышен в ранах обоих типов, но особенно в модели с низким уровнем воспаления, и, таким образом, представлены цитокины, которые могут быть мишенью для улучшения заживления.
Эффективность различных цитокинов в модели заживления ран определяли путем оценки эффекта прироста цитокинов в модели заживления ран. Кроме того, оценивали способность различных цитокинов, представляющих интерес, увеличивать скорость заживления ран и улучшать качество заживления.
Пример 11
Этот пример демонстрирует способ определения цитокинов для терапевтического применения. Цитокины в этом исследовании можно выбирать для практического применения на основании изменения их уровня, вызванного обработкой Cx43asODN. Эти цитокины могут влиять на заживление ран в роговице, например, если их вводят экзогенно в кератопластической модели заживления ран
Модель: Парные лимбальные кольца человека с вставленными стромальными имплантатами свиньи тестируют в культивируемой кератопластической модели на различия в уровне цитокинов. Уровень добавленных цитокинов в ткани измеряли с помощью результатов, полученных на матрицах антител. Для исследования во времени цитокины добавляют в начале процесса заживления. Оптимальные периоды обработки при необходимости определяют с помощью дополнительных временных точек. В случае если заживление во времени происходит точно так же, как и в модели с использованием Cx43asODN, то длительность культивирования оценивают на 3-ий и 7-ой день. Динамику заживления определяют с помощью темнопольной микроскопии и при необходимости корректируют.
Методика: используют 5 пар лимбальных колец на один цитокин в повышающихся дозах, чтобы построить кривую зависимости доза-ответ.
Можно использовать те же самые способы исследования заживления ран в роговице, как было отмечено выше в примере 9, с одним лишь исключением - для того, чтобы отделить эпителиальное заживление раны от стромального заживления раны используют эпителиальную пробку, которая образуется при заживлении раны в роговице без наложения шва. Факторы, которые влияют на восстановление эпителия, оценивают независимо от влияния клеток стромы. В некоторых случаях можно предпочтительно усилить корнеальное эпителиальное заживление ран, чтобы защитить барьер проницаемости, но не усиливать стромальное заживление ран, которое может индуцировать помутнение.
Идентифицируют цитокины, представляющие интерес при корнеальном заживлении ран. Кандидаты включают, например, IGF и IGFBP2 в исследованиях на нормальных тканях и FGF-7 при исследовании антисмысловых соединений.
Все патенты, публикации, научные статьи, веб-сайты и другие документы, и материалы, упомянутые или указанные в этом документе, отражают уровень специалистов в этой области техники, к которой относится изобретение, и каждый такой ссылочный документ включен сюда путем отсылки в том же объеме, как если бы он был включен путем отсылки в индивидуальном порядке во всей полноте или изложен во всей своей полноте. Заявители оставляют за собой право физически включать в это описание любой или весь материал и информацию из любых таких патентов, публикаций, научных статей, веб-сайтов, информации, доступной в электронном виде и других ссылочных материалов или документов.
Специфические способы и композиции, описанные в этом документе, представляют собой типичные примеры предпочтительных воплощений и являются иллюстративным материалом, который не должен рассматриваться как ограничение объема изобретения. У специалистов в этой области техники будут возникать другие цели, аспекты и воплощения на основании оценки этого описания, и они также будут охватывать сущность изобретения, которая определена объемом формулы изобретения. Для специалистов в этой области техники очевидно, что в изобретении, раскрытом в этом документе, могут быть сделаны различные замены и модификации без отклонения от смысла и объема изобретения. Изобретение, иллюстративно описанное в этом документе, может подходящим образом применяться на практике в отсутствии любого элемента или элементов, или ограничения или ограничений, которые не раскрыты в этом документе как существенные. Поэтому, например, в каждом случае в этом документе, в воплощениях или примерах настоящего изобретения, любой из терминов «включающий», «состоящий главным образом из» и «состоящий из» в этом описании может быть заменен на любой другой из двух терминов. Также термины «включающий», «в том числе», «содержащий» и т.д. должны читаться расширительно и без ограничений. Способы и процессы, иллюстративно описанные в этом документе, подходящим образом могут применяться на практике в различном порядке стадий, и они в силу необходимости не являются ограниченными порядком стадий, указанных в этом документе или в формуле изобретения. Кроме того, как описано в этом документе и в приложенной формуле изобретения, формы в единственном числе («a», «an» и «the» в английском тексте) включают ссылку на формы во множественном числе, до тех пор пока контекст не диктует другое. Ни при каких обстоятельствах патент не может быть интерпретирован как ограниченный специфическими примерами и воплощениями или способами, специфически раскрытыми в этом документе. Ни при каких обстоятельствах патент не может быть интерпретирован как ограниченный любым утверждением, сделанным любым экспертом или другими официальными или наемными Патентными и торговыми ведомствами, если только такое утверждение специальным образом и без квалификации или условий было принято в ответном документе заявителями.
Термины и выражения, которые были употреблены, используют в целях описания, но не ограничения, и без намерений применять такие термины и выражения для того, чтобы исключить любые эквивалентные признаки, показанные и описанные, или их части, но признается, что в объеме заявленного изобретения возможны различные модификации. Таким образом, следует понимать, что хотя настоящее изобретение было специфическим образом раскрыто с помощью предпочтительных воплощений и необязательных признаков, специалисты в этой области техники могут прибегнуть к модификациям и вариантам принципов, раскрытых в этом документе, и такие модификации и вариации рассматривают в объеме этого изобретения, определенном в прилагаемой формуле изобретения.
Изобретение в этом документе было раскрыто широко и в общих чертах. Каждая из узких категорий и субгенерических групп, попадающих в пределы основного описания, также является частью изобретения. Оно включает основное описание изобретения с условием или отрицательным ограничением удаления любого объекта изобретения из класса объектов, независимо от того, упоминался ли или нет удаленный в этом документе материал.
Другие воплощения находятся в рамках формулы изобретения. Кроме того, если признаки и аспекты описаны в терминах групп Маркуша, специалистам в этой области техники будет ясно, что изобретение также описано в терминах любого индивидуального представителя или подгруппы группы Маркуша.






































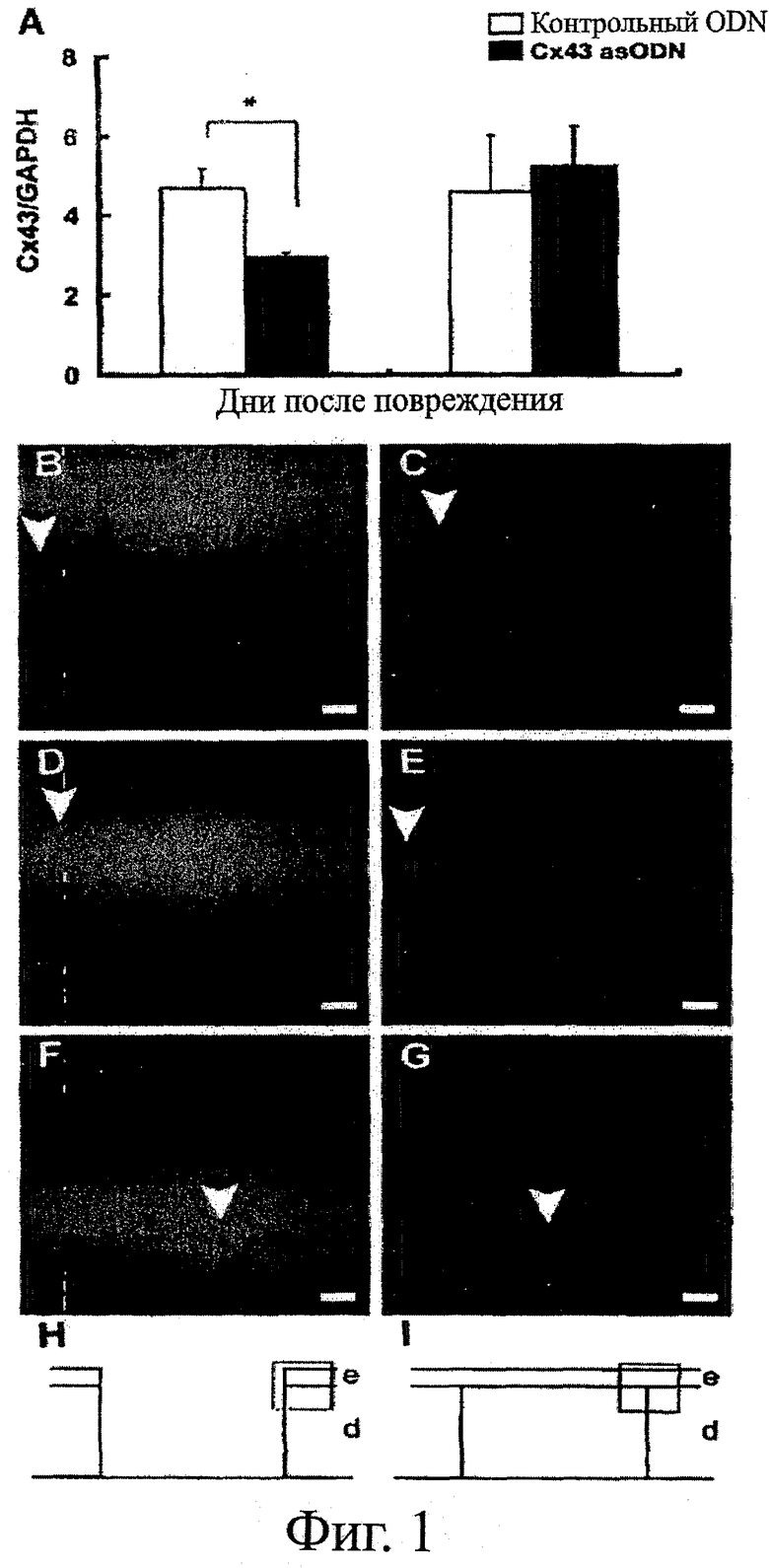
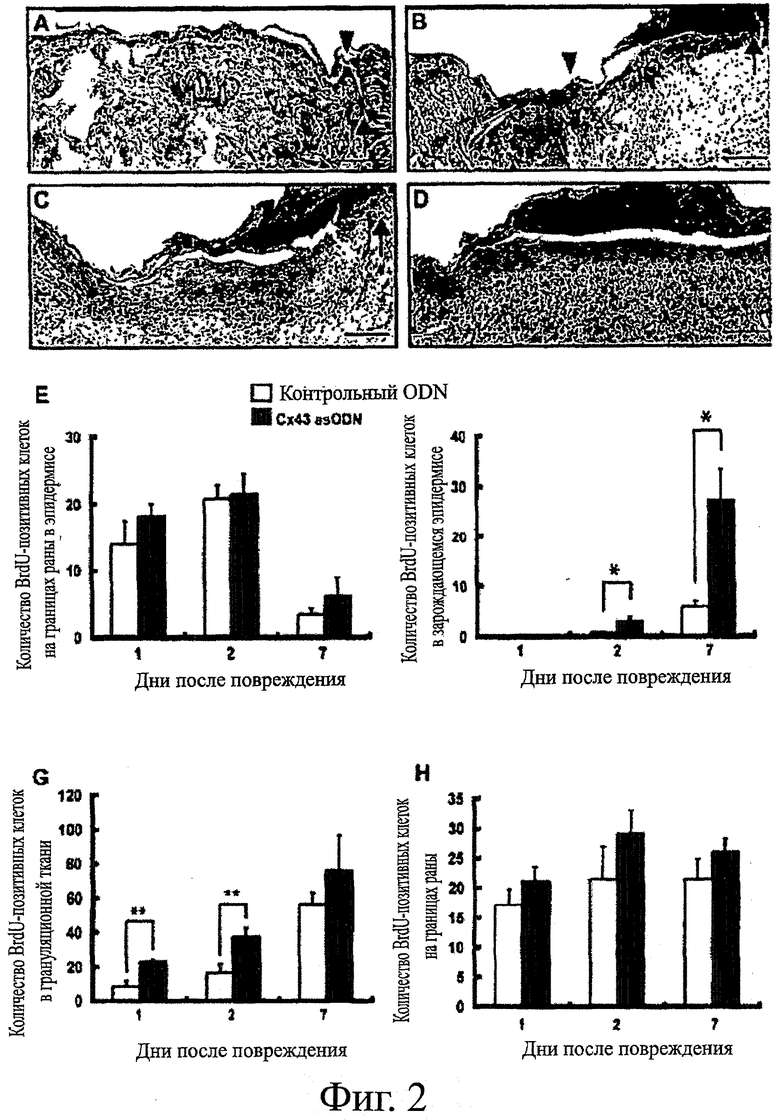
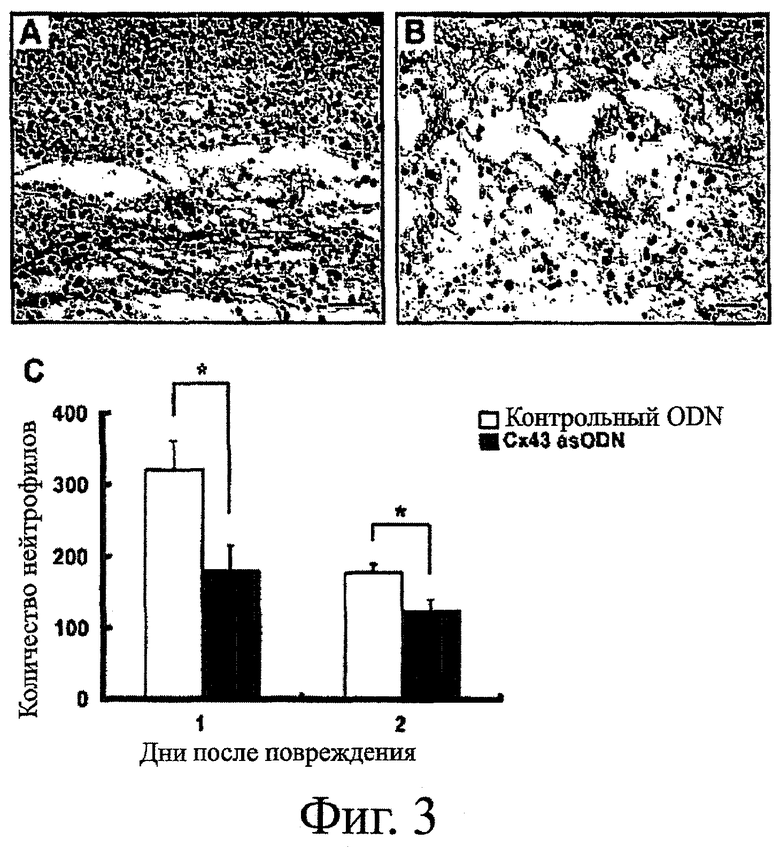
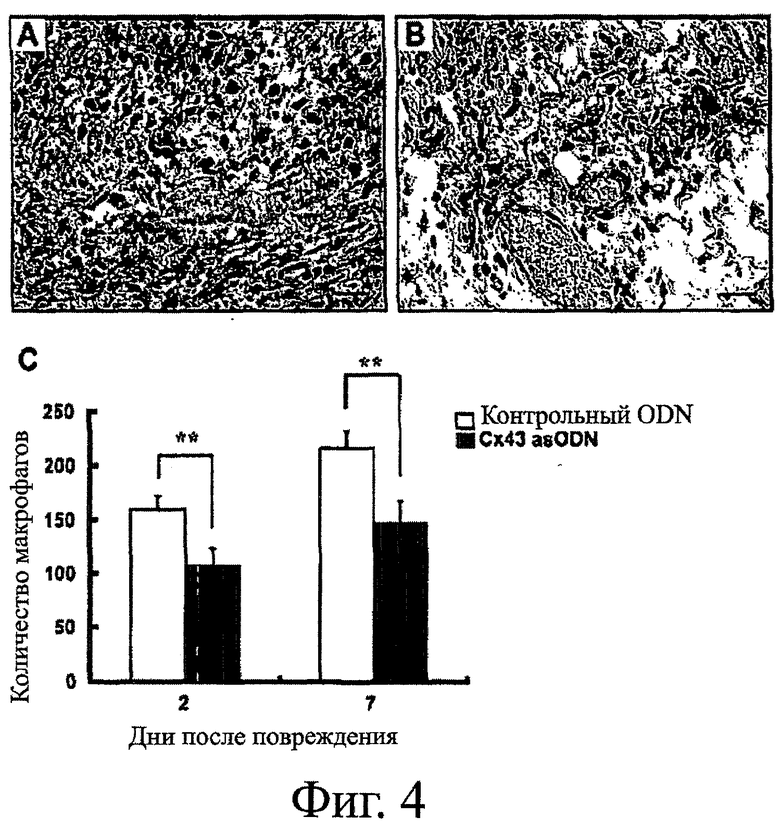
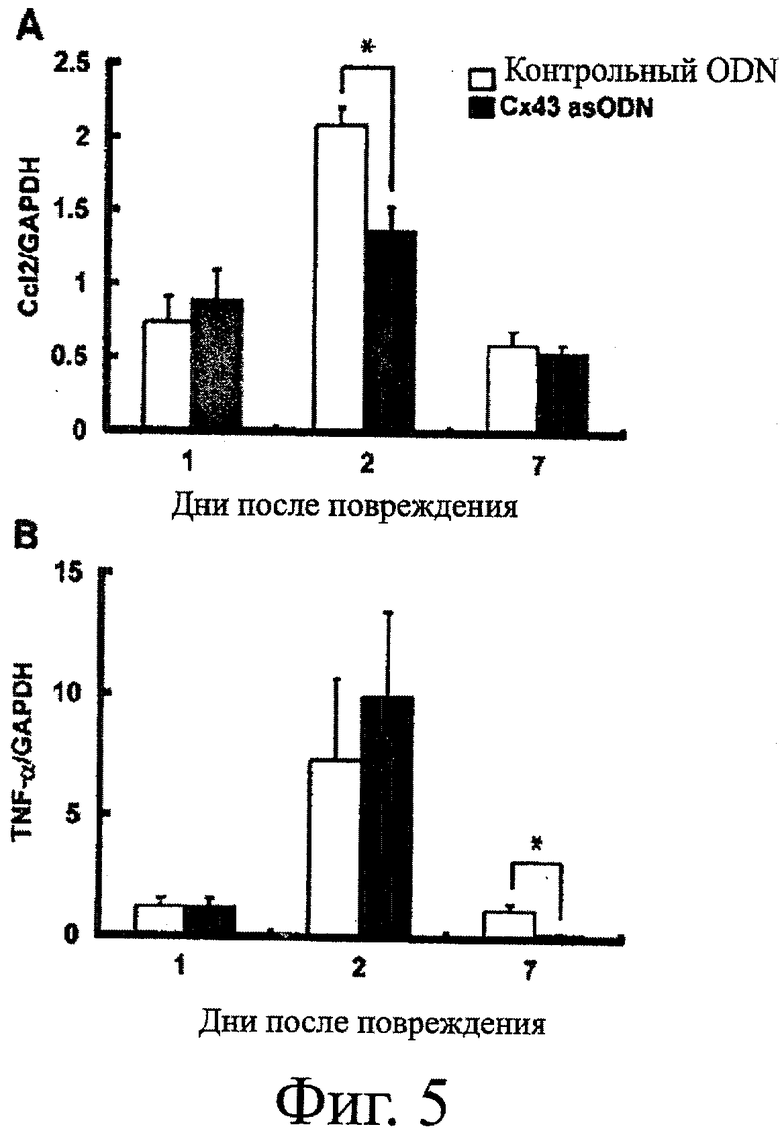

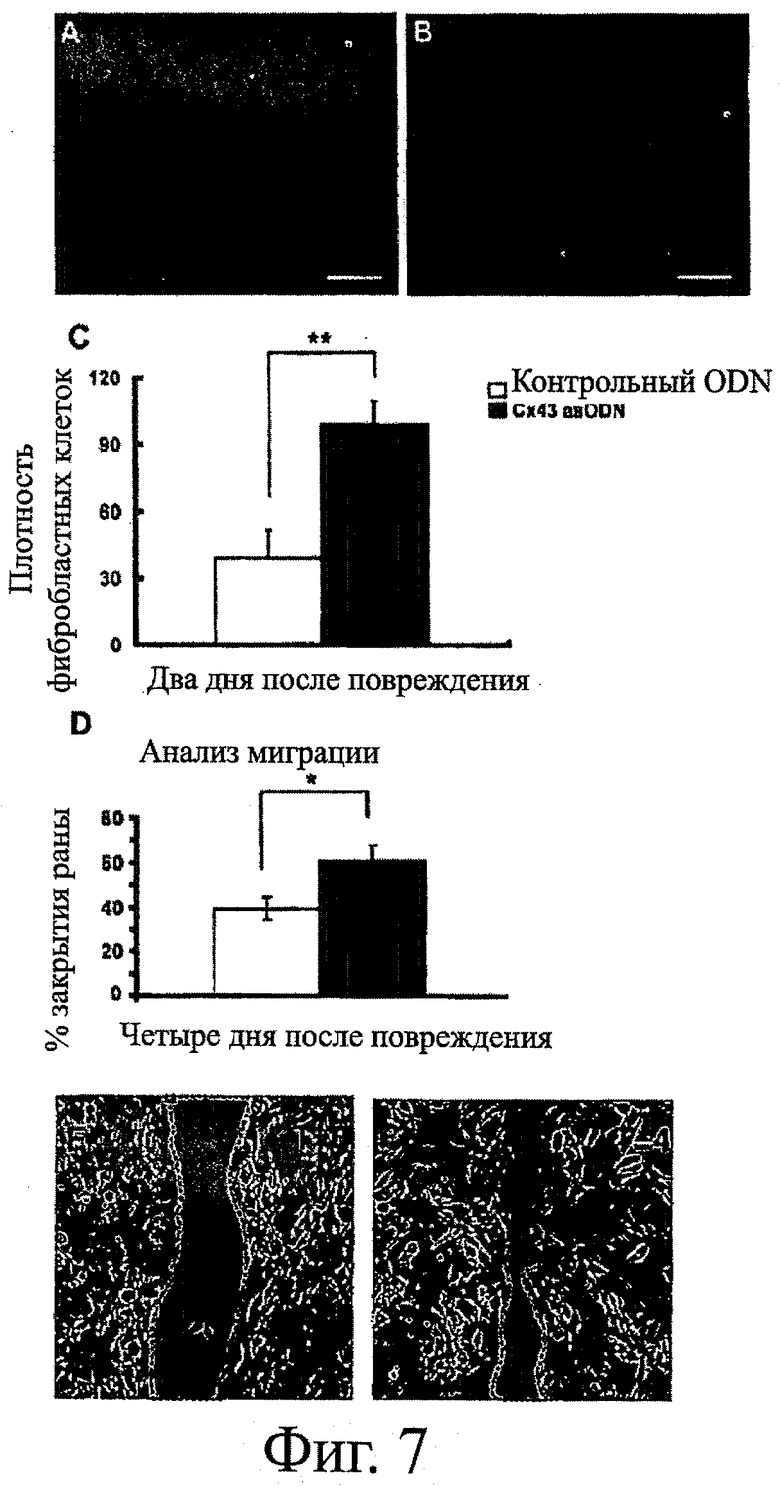
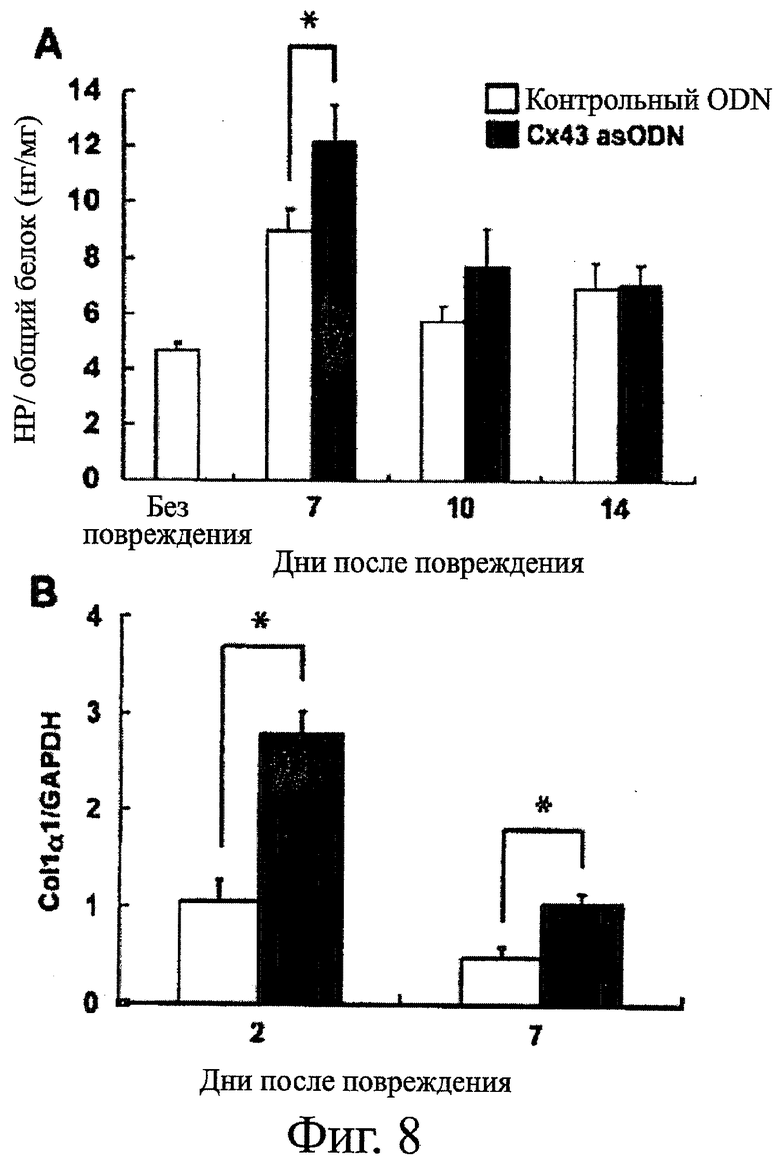

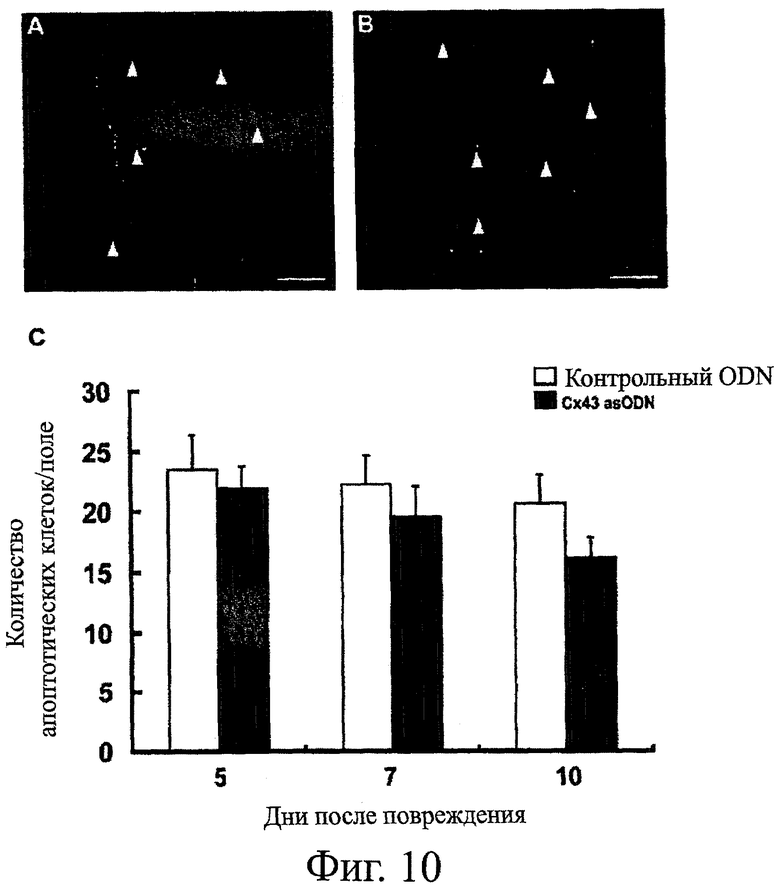
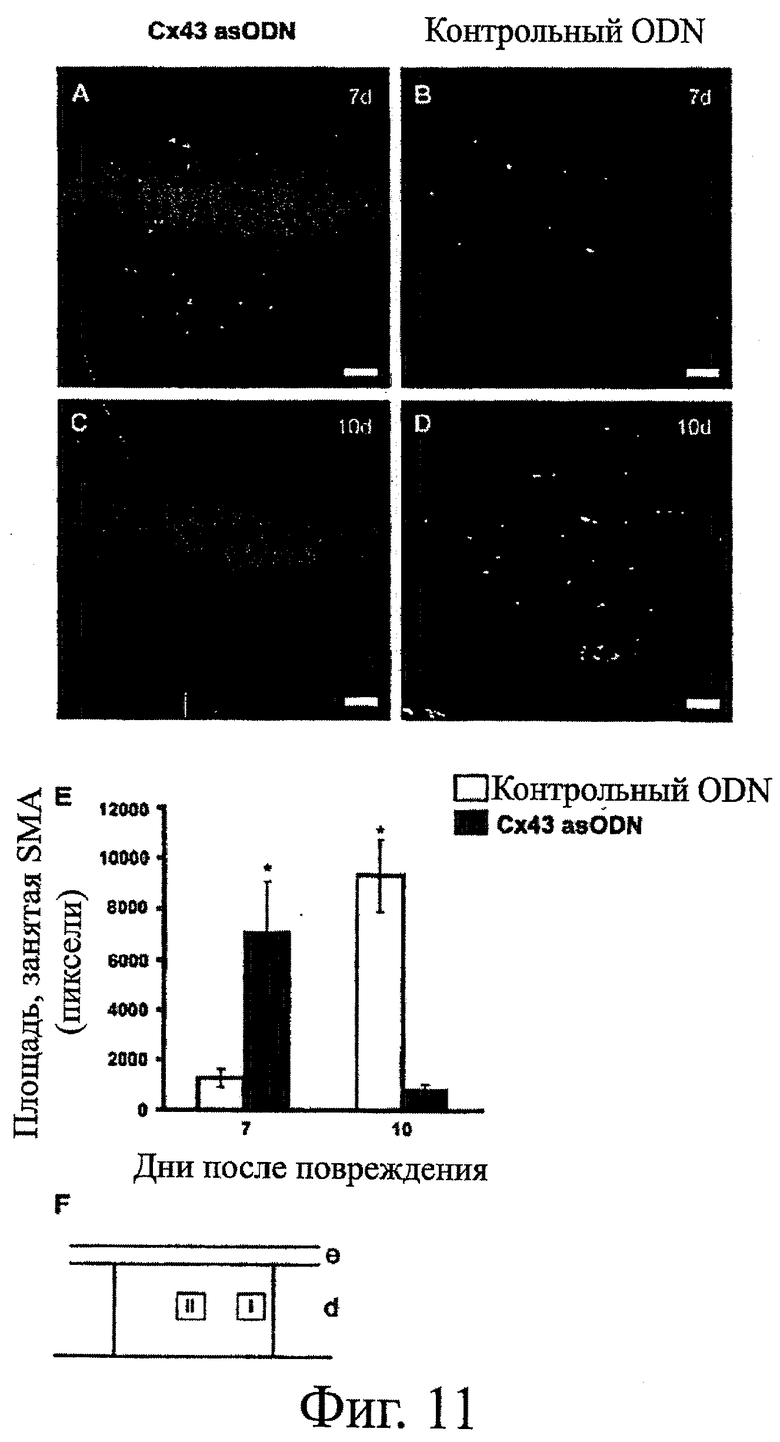
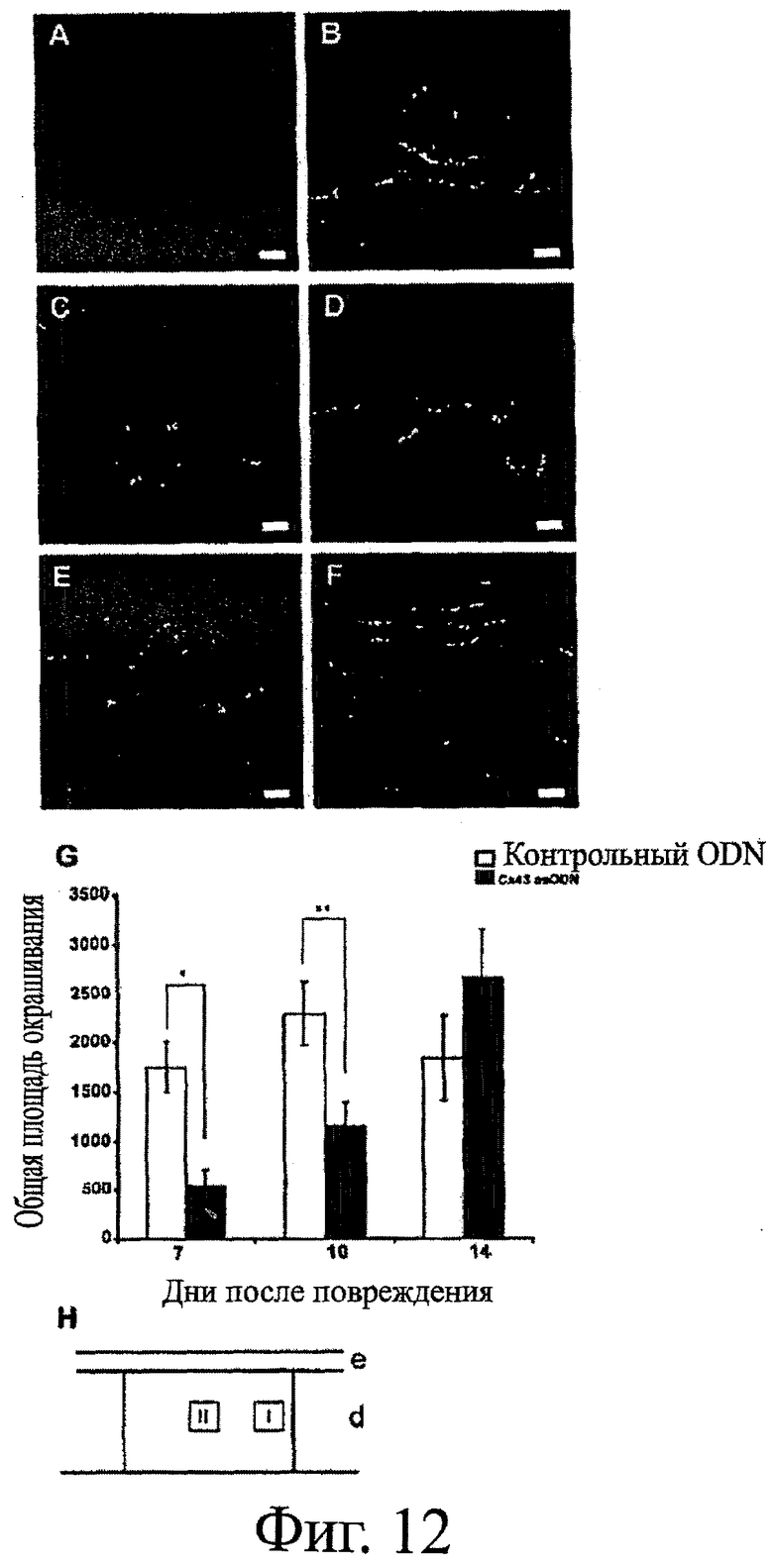
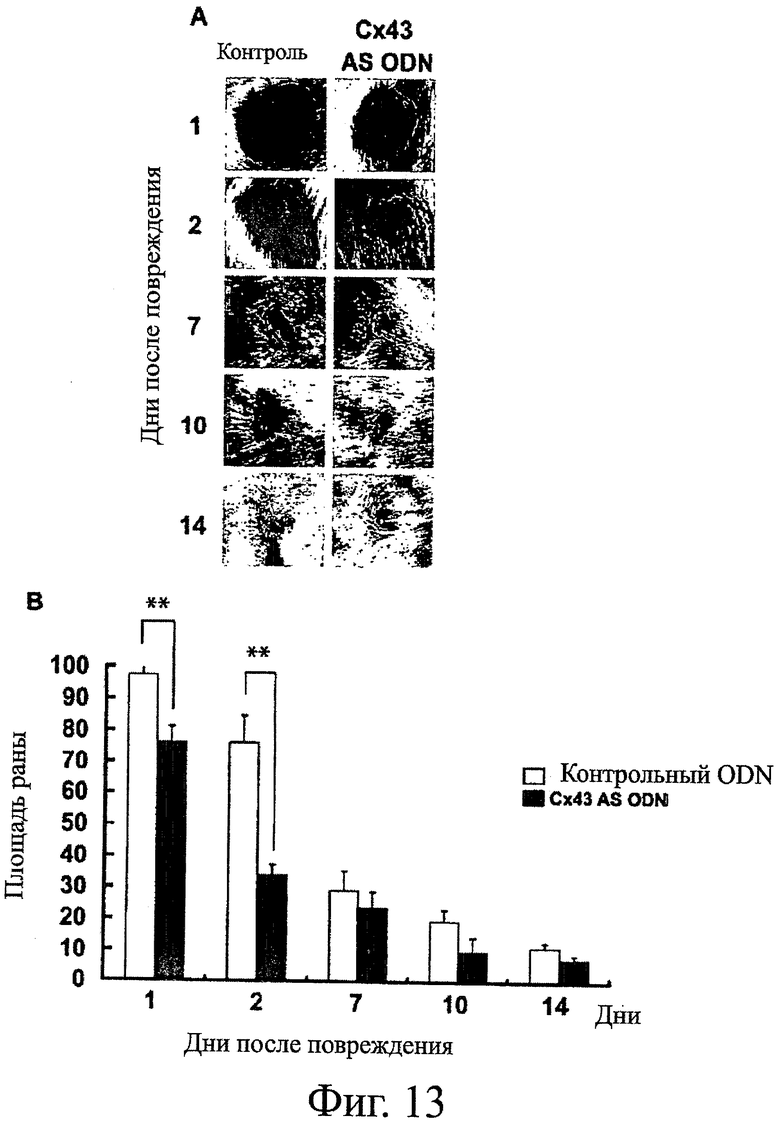

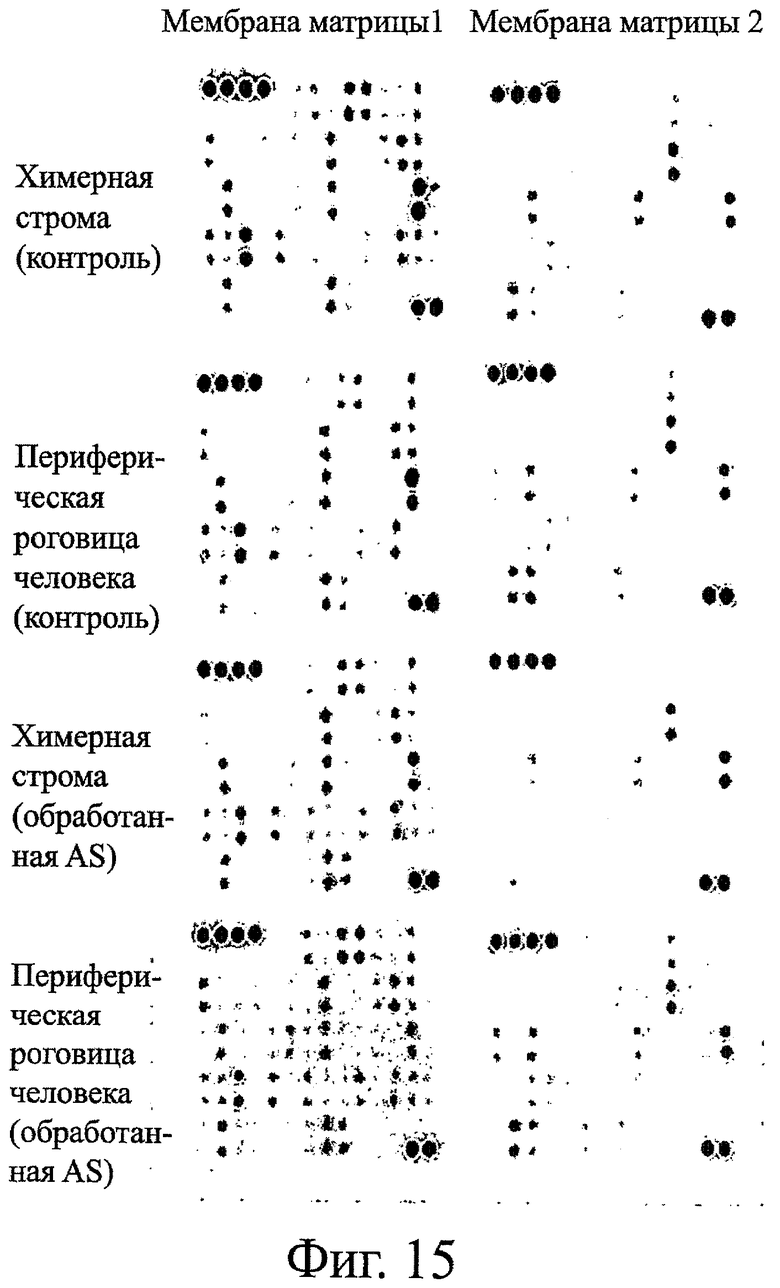
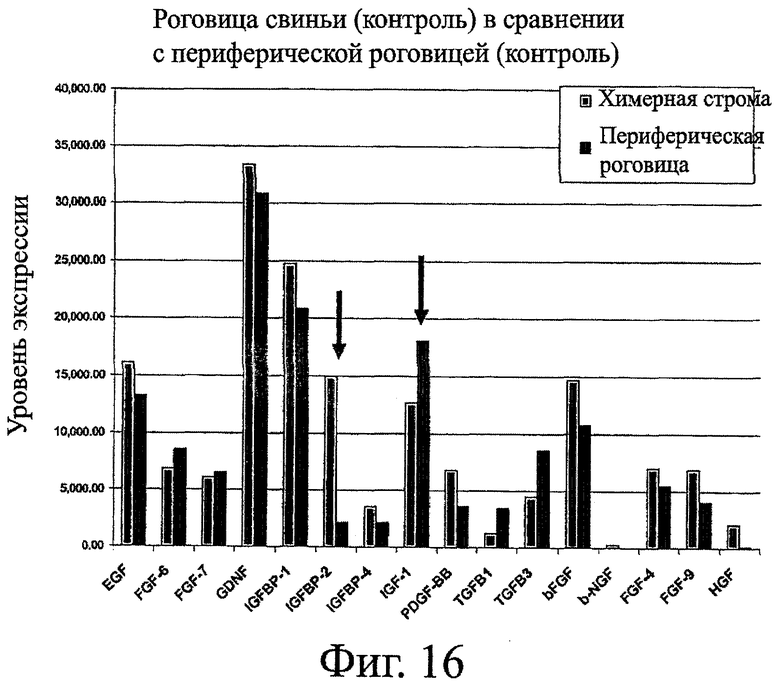
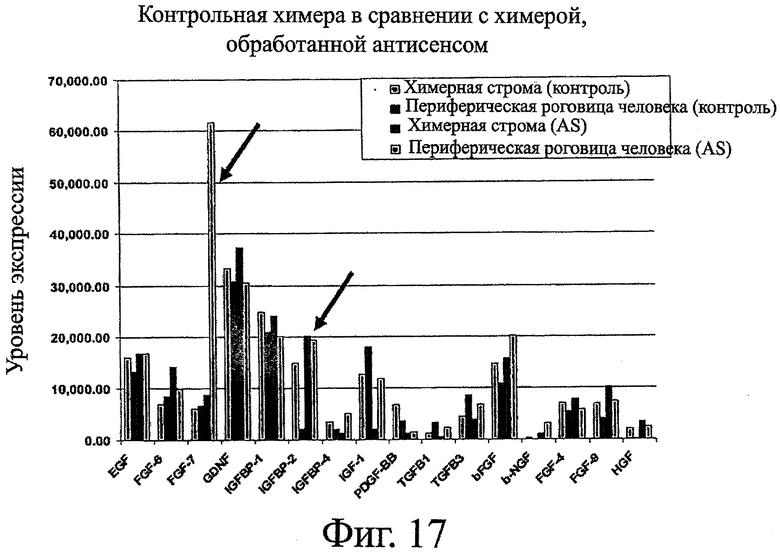
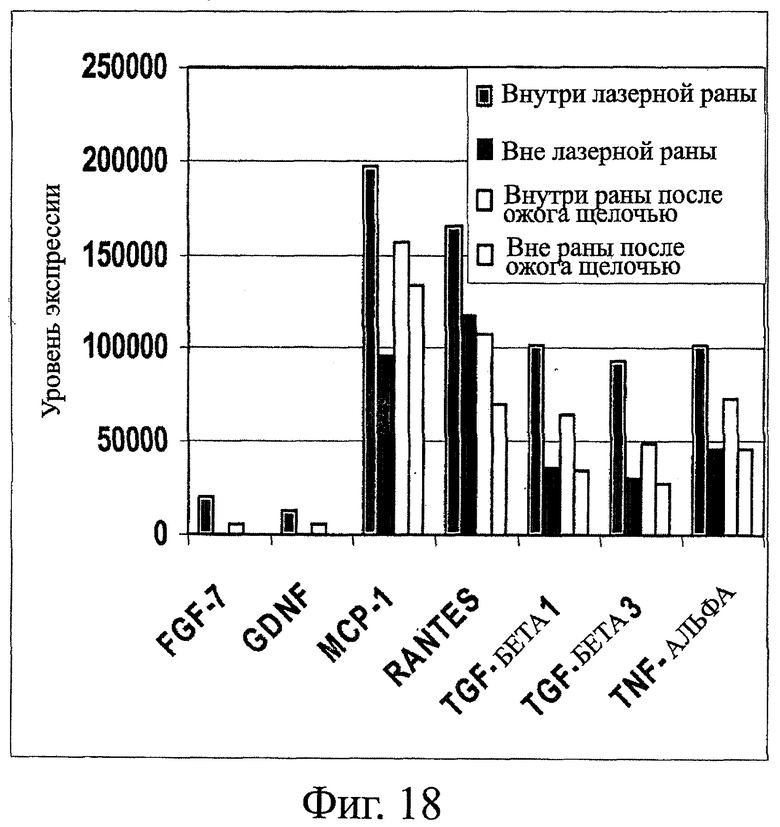
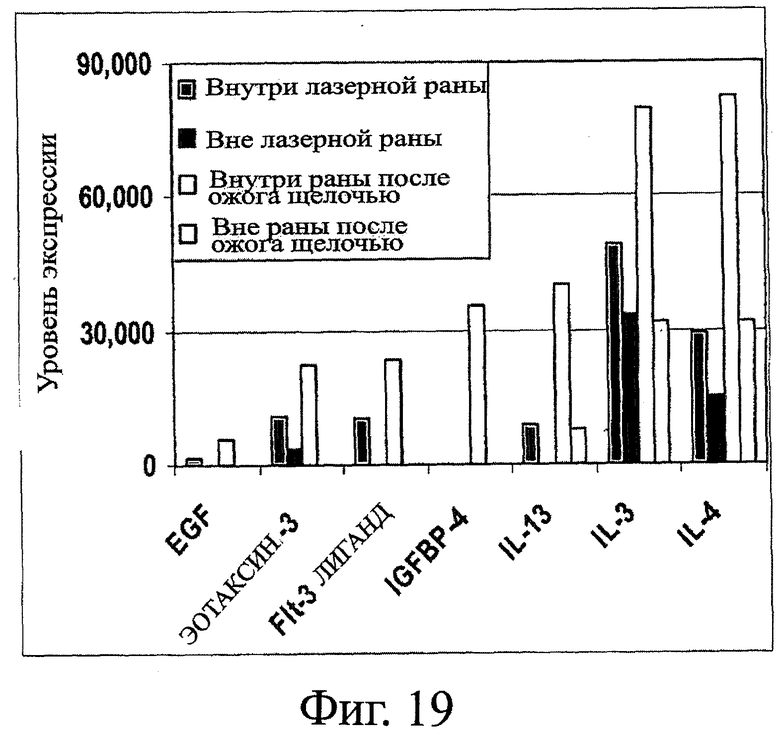
Группа изобретений относится к медицине и может быть использована для лечения субъекта, имеющего медленно заживающую, трудно заживающую или хроническую рану. Для этого субъекту, нуждающемуся в этом, вводят композицию, включающую терапевтически эффективные количества средства, направленного против коннексина 43, и белка или пептида, эффективного для стимулирования или улучшения заживления ран. Также предложено использование терапевтически эффективного количества первого ранозаживляющего соединения и второго ранозаживляющего соединения, где указанное первое соединение представляет собой средство, направленное против коннексина 43, а указанное второе соединение выбирают из группы, состоящей из бета-адренергических антагонистов, антагонистов рецептора интерлейкина-1, ловушек свободных радикалов, противовоспалительных и антимикробных средств, опиоидов, средств, фосфорилирующих коннексин. Группа изобретений обеспечивает повышение скорости и/или качества заживления ран с помощью применения указанного комбинирования терапевтических средств при возможности снижения дозы и частоты введения таких средств. 6 н. и 40 з.п. ф-лы, 19 ил., 8 табл., 11 пр.
1. Способ лечения субъекта, имеющего медленно заживающую, трудно заживающую или хроническую рану, включающий введение субъекту, нуждающемуся в этом, композиции, включающей терапевтически эффективные количества средства, направленного против коннексина 43, и белка или пептида, эффективного для стимулирования или улучшения заживления ран.
2. Способ лечения субъекта, имеющего медленно заживающую, трудно заживающую или хроническую рану, включающий введение субъекту, нуждающемуся в этом, композиции, включающей терапевтически эффективные количества первого ранозаживляющего соединения и второго ранозаживляющего соединения, где указанное первое соединение представляет собой средство, направленное против коннексина 43, а указанное второе соединение выбирают из группы, состоящей из бета-адренергических антагонистов, антагонистов рецептора интерлейкина-1 и ловушек свободных радикалов.
3. Способ лечения субъекта, имеющего медленно заживающую, трудно заживающую или хроническую рану, включающий введение субъекту, нуждающемуся в этом, композиции, включающей терапевтически эффективные количества первого ранозаживляющего соединения и второго ранозаживляющего соединения, где указанное первое соединение представляет собой средство, направленное против коннексина 43, а указанное второе соединение выбирают из группы, состоящей из противовоспалительных средств и антимикробных средств.
4. Способ лечения субъекта, имеющего медленно заживающую, трудно заживающую или хроническую рану, включающий введение субъекту, нуждающемуся в этом, композиции, включающей терапевтически эффективные количества первого ранозаживляющего соединения и второго ранозаживляющего соединения, где указанное первое соединение представляет собой средство, направленное против коннексина 43, а указанное второе соединение представляет собой опиоид.
5. Способ лечения субъекта, имеющего медленно заживающую, трудно заживающую или хроническую рану, включающий введение субъекту, нуждающемуся в этом, композиции, включающей терапевтически эффективные количества первого ранозаживляющего соединения и второго ранозаживляющего соединения, где указанное первое соединение представляет собой средство, направленное против коннексина 43, а указанное второе соединение представляет собой средство, фосфорилирующее коннексин.
6. Способ лечения субъекта, имеющего медленно заживающую, трудно заживающую или хроническую рану, включающий последовательное введение субъекту, нуждающемуся в этом, первой ранозаживляющей композиции и второй ранозаживляющей композиции, причем указанная первая ранозаживляющая композиция включает терапевтически эффективное количество средства, направленного против коннексина 43, и указанная вторая ранозаживляющая композиция включает терапевтически эффективное количество белка или пептида, эффективного для стимулирования или улучшения заживления ран.
7. Способ по любому из пп.1-6, в котором средство, направленное против коннексина 43, представляет собой полинуклеотид.
8. Способ по п.7, в котором указанный полинуклеотид представляет собой антисмысловой полинуклеотид.
9. Способ по п.8, в котором указанный антисмысловой полинуклеотид включает последовательность, выбираемую из SEQ ID NO:1-12.
10. Способ по п.8, в котором указанный антисмысловой полинуклеотид выбирают из:

11. Способ по п.8, в котором указанный антисмысловой полинуклеотид содержит примерно от 15 до примерно 35 нуклеотидов и достаточно комплементарен мРНК коннексина 43, чтобы в физиологических условиях образовать дуплекс с точкой плавления выше чем 20°C.
12. Способ по п.8, в котором полинуклеотид коннексина 43 содержит примерно от 15 до примерно 35 нуклеотидов и имеет, по меньшей мере, около 70 процентов гомологии с антисмысловой последовательностью мРНК коннексина 43.
13. Способ по п.1, в котором ранозаживляющая композиция включает примерно от 0,1 до примерно 1000 микрограммов указанного средства, направленного против коннексина 43, и средство, направленное против коннексина 43, представляет собой антисмысловой полинуклеотид.
14. Способ по п.1 или 6, в котором белок или пептид выбирают из группы, состоящей из факторов роста, которые эффективны для стимулирования или улучшения заживления ран.
15. Способ по п.1 или 6, в котором белок или пептид представляет собой тромбоцитарный фактор роста-В.
16. Способ по п.1 или 6, в котором белок или пептид представляет собой эпидермальный фактор роста.
17. Способ по п.1 или 6, в котором белок или пептид представляет собой фактор роста фибробластов.
18. Способ по п.1 или 6, в котором белок или пептид представляет собой фактор роста сосудистого эндотелия.
19. Способ по п.1 или 6, в котором белок или пептид представляет собой трансформирующий фактор роста.
20. Способ по п.6, в котором первую и вторую ранозаживляющие композиции вводят одновременно.
21. Способ по п.6, в котором первую и вторую ранозаживляющие композиции вводят последовательно.
22. Способ по п.6, в котором первую и вторую ранозаживляющие композиции вводят друг за другом в пределах, по меньшей мере, примерно получаса.
23. Способ по п.6, в котором первую и вторую ранозаживляющие композиции вводят друг за другом в пределах примерно одного часа, в пределах примерно одного дня, или в пределах примерно одной недели.
24. Способ по п.6, в котором первую ранозаживляющую композицию вводят первой.
25. Способ по п.6, дополнительно включающий введение третьей ранозаживляющей композиции, где третья ранозаживляющая композиция включает пептид или пептидомиметик, направленные против коннексина 43.
26. Способ по п.25, в котором третью ранозаживляющую композицию вводят первой.
27. Способ по любому из пп.1-6, в котором хроническая рана представляет собой диабетическую язву.
28. Способ по любому из пп.1-6, в котором хроническая рана представляет собой венозную язву.
29. Способ по любому из пп.1-6, в котором хроническая рана представляет собой пролежневую язву.
30. Способ по любому из пп.1-6, в котором хроническая рана представляет собой артериальную язву.
31. Способ по любому из пп.1-6, в котором хроническая рана представляет собой васкулитную язву.
32. Способ по п.6, в котором первую ранозаживляющую композицию или вторую ранозаживляющую композицию или обе композиции вводят местно.
33. Способ по любому из пп.1-6, в котором субъект представляет собой млекопитающее.
34. Способ по п.33, в котором млекопитающее представляет собой человека.
35. Способ по п.33, в котором млекопитающее выбирают из группы, состоящей из домашних животных, сельскохозяйственных животных, животных, связанных с зоопарком, животных, связанных со спортом, и комнатных животных.
36. Способ по п.33, в котором животное представляет собой лошадь, собаку или кошку.
37. Способ по п.6, в котором ранозаживляющая композиция включает примерно от 0,1 до примерно 1000 микрограммов указанного средства, направленного против коннексина 43, и средство, направленное против коннексина 43, представляет собой антисмысловой полинуклеотид.
38. Способ по любому из пп.2-5, в котором первое и второе ранозаживляющие соединения вводят одновременно.
39. Способ по любому из пп.2-5, в котором первое и второе ранозаживляющие соединения вводят последовательно.
40. Способ по любому из пп.2-5, в котором первое и второе ранозаживляющие соединения вводят друг за другом в пределах, по меньшей мере, примерно получаса.
41. Способ по любому из пп.2-5, в котором первое и второе ранозаживляющие соединения вводят друг за другом в пределах примерно одного часа, в пределах примерно одного дня или в пределах примерно одной недели.
42. Способ по любому из пп.2-5, в котором первое ранозаживляющее соединение вводят первым.
43. Способ по любому из пп.2-5, дополнительно включающий введение третьего ранозаживляющего соединения, где третье ранозаживляющее соединение включает пептид или пептидомиметик, направленные против коннексина 43.
44. Способ по любому из пп.2-5, в котором первое и второе ранозаживляющее соединение вводят местно.
45. Способ по п.1, в котором композицию вводят местно.
46. Способ по любому из пп.2-5, в котором первое ранозаживляющее соединение включает примерно от 0,1 до примерно 1000 микрограммов средства, направленного против коннексина 43, и средство, направленное против коннексина 43, представляет собой антисмысловой полинуклеотид.
| US 7098190 B1, 29.08.2006 | |||
| ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ ДЛИТЕЛЬНО НЕЗАЖИВАЮЩИХ ИНФИЦИРОВАННЫХ ЯЗВ И РАН | 1998 |
|
RU2147240C1 |
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| WO2005053600 A2, 16.06.2005 | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Зубчатое колесо со сменным зубчатым ободом | 1922 |
|
SU43A1 |
| Насос | 1917 |
|
SU13A1 |
Авторы
Даты
2015-02-20—Публикация
2007-11-15—Подача