Изобретение относится к области органической химии и медицины и касается биологически активных химических соединений, обладающих цитотоксической активностью.
Известно соединение 1-бензил-4,9-диоксо-1H-нафто[2,3-d][1,2,3]триазол-2-оксид, обладающее цитотоксической активностью [Радаева Н.Ю., Долгушина Л.В., Сакилиди В.Т., Горностаев Л.М. Циклизация 2-азидо-3-N-нитрозо-алкиламино-1,4-нафтохинонов в 1-алкил-4,9-диоксо-1Н-нафто[2,3][1,2,3]триазол-2-оксиды // Журнал Органическая Химия, 2005, т. 41, вып. 6, с. 926-927].
Наиболее близким к заявляемому соединению по механизму действия является соединение 1-R-4,9-диоксо-1H-нафто[2,3-d][1,2,3]триазол-2-оксид, обладающее цитотоксическим действием (прототип) [Долгушина Л.В. Синтез 1-R-4,9-диоксо-1H-нафто[2,3-d][1,2,3]триазол-2-оксидов и 3-R-5-ариламино-6H,11H-6,11-диоксоантра[1,2-d][1,2,3]триазол-2-оксидов: Дис. канд. хим. наук, Новосибирск, 2011, 125 с.].
Задачей заявляемого изобретения является расширение арсенала химических соединений 1-R-4,9-диоксо-1H-нафто[2,3-d][1,2,3]триазол-4-оксим-2-оксидов, обладающих цитотоксической активностью.
Задача решается получением новых биологически активных химических соединений, а именно 1-R-4,9-диоксо-1H-нафто[2,3-d][1,2,3]триазол-4-оксим-2-оксидов, обладающих цитотоксической активностью.
Общая химическая структура соединений представлена формулой 1
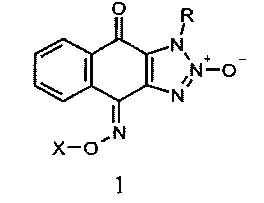
R=Alk, бензил; X=H, -C(=O)R′, где R′=метил, фенил.
Технический результат заявляемого изобретения заключается в расширении арсенала новых биологически активных химических соединений, а именно l-R-4,9-диоксо-1H-нафто[2,3-d][1,2,3]триазол-4-оксим-2-оксидов, которые обладают цитотоксической активностью в наномолярных и субмикромолярных концентрациях.
Способ получения новых биологически активных химических соединений l-R-4,9-
диоксо-1H-нафто[2,3-d][1,2,3] триазол-4-оксим-2-оксидов.
Биологические активные химические соединения 1-R-4,9-диоксо-1H-нафто[2,3-d][1,2,3]триазол-2-оксиды получали путем циклизации 2-азидо-3-N-нитрозо-алкиламино-1,4-нафтохинонов в 1-алкил-4,9-диоксо-1H-нафто[2,3][1,2,3]триазол-2-оксиды с добавлением гидрохлорида гидроксиламина при нагревании в пиридине. Продукты реакции 1-R-4,9-диоксо-1H-нафто [2,3-d][1,2,3]триазол-4-оксим-2-оксиды далее ацилировали уксусным ангидридом или бензоилхлоридом в пиридине с образованием соответствующих 1-R-4,9-диоксо-1H-нафто[2,3-d][1,2,3]триазол-4-(O-ацил)-2-оксидов. Заявляемое изобретение иллюстрируется примерами 1-4.
Пример 1
Способ получения 1-метил-4,9-диоксо-1H-нафто[2,3-d][1,2,3]триазол-4-оксим-2-оксида (1)
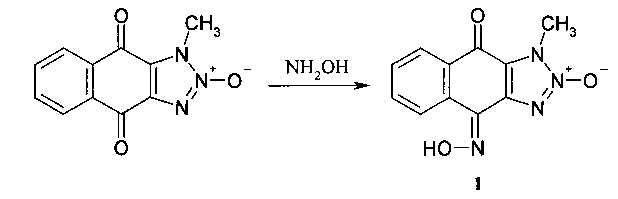
2,29 г (0,01 моль) 1-Метил-4,9-диоксо-1H-нафто[2,3-d][1,2,3]триазол-2-оксида и 2,3 г (0,033 моль) гидрохлорида гидроксиламина кипятили в 20 мл пиридина в течение 20 минут. После охлаждения к загустевшей массе добавляли 20 мл воды, осадок фильтровали, промывали водой, высушивали, нагревали до кипения в минимальном количестве 96%-ного этилового спирта. Кипящий раствор отфильтровывали для отделения нерастворимых примесей. Выпавший после охлаждения фильтрата осадок целевого продукта фильтровали и высушивали при t=20-22°C. Выход 2,3 г (94%). Т.пл. 250-252°C. Спектр ЯМР 1Н, δ, м.д., J (Гц): 4.09 (3Н, с), 7.67 (1H, дт, J=7.6, J=1.3), 7.77 (1H, дт, J=7.6, J=1.3), 8.13 (1H, дд, J=7.9, J=1.3), 8.31 (1H, дд, J=7.9, J=1.3), 13.50 (1H, с). Масс-спектр, m/z (I отн, %): 244 (18.3) [M +], 130 (35.8), 102 (31.4), 32 (38.8), 30 (100) [NO +]. Найдено, %: С, 54.09; Η, 3.09; Ν, 22.77. C11H8N4O3. Вычислено, %: С, 54.10; Η, 3.30; Ν, 22.94.
Пример 2
Способ получения 1-метил-4,9-диоксо-1H-нафто[2,3-d][1,2,3]триазол-4-(O-ацетилоксим)-2-оксида (2)
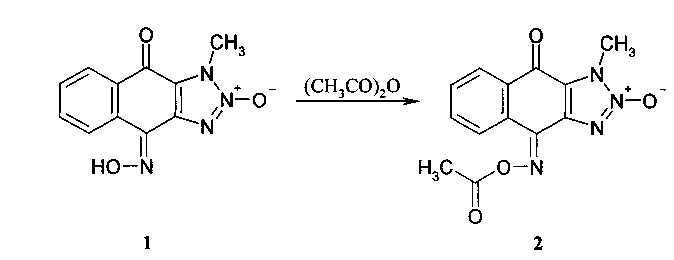
0,5 г (0,002 моль) 1-Метил-4,9-диоксо-1H-нафто[2,3-d][1,2,3]триазол-4-оксим-2-оксида в 5 мл пиридина перемешивали с 0,4 мл (0,004 моль) уксусного ангидрида при t=20-22°C в течение 20 минут, а затем высушивали до образования кристаллов желтого цвета. Полученный продукт реакции промывали водой, фильтровали, высушивали, нагревали до кипения в минимальном количестве 96%-ного этилового спирта. Кипящий раствор отфильтровывали для отделения нерастворимых примесей. Выпавший после охлаждения фильтрата осадок целевого продукта фильтровали и высушивали при t=20-22°C. Выход 0,42 г (72%). Т. пл. 200-202°C. Спектр ЯМР 1H, δ, м.д., J (Гц): 2.38 (3Н, с), 4.09 (3Н, с), 7.82 (1Н, т, J=7.4), 7.88 (1H, т, J=7.4), 8.19 (1Н, д, J=7.8), 8.41 (1H, д, J=7.8). Масс-спектр, m/z (I отн, %): 286 (8.5) [M +], 244 (48.4), 43 (100) [C 2 H 3 O +], 32 (41.0), 30 (24.2) [NO +]. Найдено, %: C, 54.64; H, 3.26; N, 19.41. C13H10N4O4. Вычислено, %: C, 54.55; Н, 3.52; N, 19.57.
Пример 3
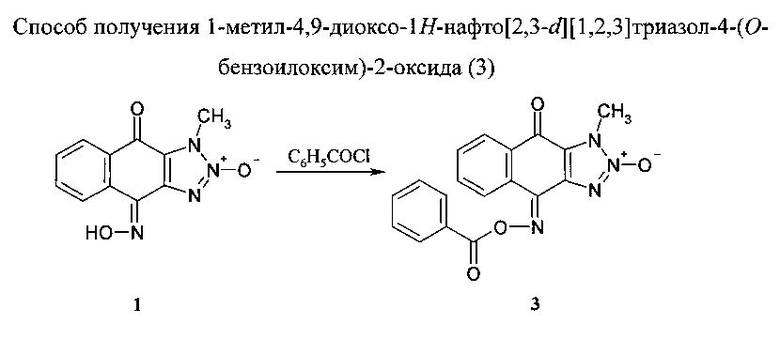
0,5 г (0,002 моль) 1-Метил-4,9-диоксо-1H-нафто[2,3-d][1,2,3]триазол-4-оксим-2-оксида в 5 мл пиридина перемешивали с 0,5 мл (0,004 моль) бензоилхлорида при t=20-22°C в течение 20 минут, а затем высушивали до образования кристаллов желтого цвета. Полученный продукт реакции фильтровали, промывали водой, высушивали, нагревали до кипения в минимальном количестве 96%-ного этилового спирта. Кипящий раствор отфильтровывали для отделения нерастворимых примесей. Выпавший после охлаждения фильтрата осадок целевого продукта фильтровали и высушивали при t=20-22°C. Выход 0,62 г (90%). Т. пл. 225-227°C. Спектр ЯМР 1H, δ, м.д., J (Гц): 4.12 (3Н, с), 7.65-7.70 (2Н,м), 7.80 (1H, т, J=7.5), 7.85 (1H, т, J=7.5), 7.92 (1H, т, J=7.5), 8.21 (1H, д, J=8.0), 8.40 (2H, д, J=7.5), 8.49 (1H, д, J=8.0). Масс-спектр, m/z (I отн., %): 348 (3.7) [M +], 105 (100) [C 7 H 5 O +], 77 (54.8), 51 (30.7), 32 (82.2), 30 (15.5) [NO +]. Найдено, %: С, 61.68; H, 3.30; Ν, 15.99. C18H12N4O4. Вычислено, %: С, 62.07; H, 3.47; Ν, 16.08.
Пример 4
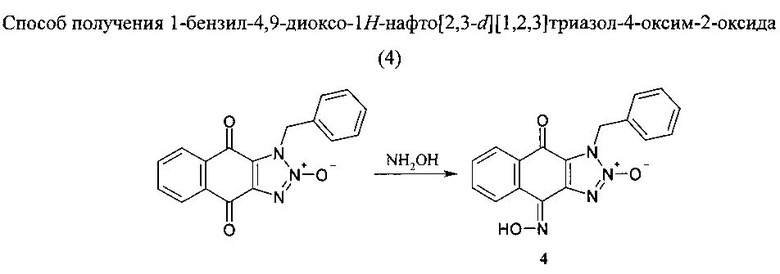
0,61 г (0,002 моль) 1-Бензил-4,9-диоксо-1H-нафто[2,3-d][1,2,3]триазол-2-оксида и 0,5 г (0,007 моль) гидрохлорида гидроксиламина кипятили в 8 мл пиридина в течение 20 минут. После охлаждения к загустевшей массе добавляли 20 мл воды, осадок фильтровали, промывали водой, высушивали, нагревали до кипения в минимальном количестве 96%-ного этилового спирта. Кипящий раствор отфильтровывали для отделения нерастворимых примесей. Выпавший после охлаждения фильтрата осадок целевого продукта фильтровали и высушивали при t=20-22°C. Выход 0,62 г (97%). Т. пл. 236-238°C. Спектр ЯМР 1H, δ, м.д., J (Гц): 5.84 (2H, с), 7.33-7.43 (5H, м) 7.70 (1H, дт, J=7.5, J=1.3), 7.80 (1H, дт, J=7.5, J=1.3), 8.18 (1H, дд, J=8, J=l), 8.35 (1H, дд, J=8, J=l), 13.56 (1H, c). Масс-спектр, m/z (I отн., %): 320 (3.6) [M +], 91 (100) [C 7 H 7 +]. Найдено, %: C, 63.68; H, 3.67; Ν, 17.72. C11H8N4O3. Вычислено, %: C, 63.75; H, 3.78; Ν, 17.49.
Исследование цитотоксической активности 1-R-4,9-диоксо-1H-нафто[2,3-d][1,2,3]триазол-4-оксим-2-оксидов.
Клетки аденокарциномы толстой кишки человека линии НСТ116 рассевали на 96-луночные планшеты в количестве 104 клеток в 190 мкл культуральной среды (ДМЕМ) на одну лунку. Далее вносили соединения 1-4, а в качестве контроля использовали 0,5% водный раствор диметилсульфоксида. Объем вносимых веществ не превышал 5% объема культуральной среды в лунках. Каждую концентрацию соединения вносили трижды. Культуру клеток аденокарциномы толстой кишки человека линии НСТ116 инкубировали при t=37°C, 5% СО2 в течение 72 часов. Затем вносили по 20 мкл водного раствора (2,5 мг/мл) 3-4,5-диметилтиазол-2-ил-2,5-дифенилтераразола и помещали в СО2-инкубатор на 2 часа. Жизнеспособность клеток определяли по цветной реакции, характерной при восстановлении тетразолия в формазан дегидрогеназами митохондрий. Окраску регистрировали на спектрофотометре при длине волны возбуждения 540 нм. Оптическую плотность в контрольной культуре клеток аденокарциномы толстой кишки человека линии НСТ116 принимали за 100%. Показатели оптической плотности в культуре клеток каждой концентрации соединений 1-4 усредняли и вычисляли процент выживших клеток. Затем вычисляли IC50-концентрацию каждого исследуемого соединения, при которой гибель культуры клеток аденокарциномы толстой кишки человека линии НСТ116 составляла 50%.
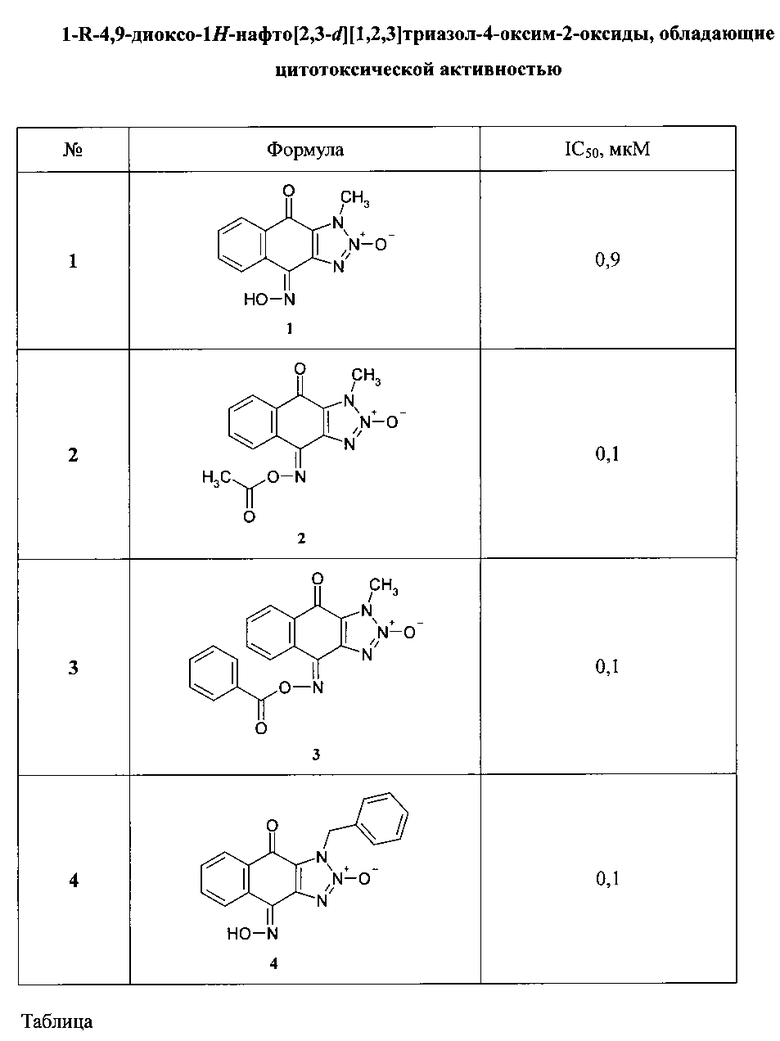
Изобретение иллюстрируется таблицей.
В таблице приведены результаты исследования цитотоксической активности биологически активных химических соединений 1-R-4,9-диоксо-1H-нафто[2,3-d][1,2,3]триазол-4-оксим-2-оксидов для культуры клеток аденокарциномы толстой кишки человека линии НСТ116.
Показано, что для соединения 1 IC50 равна 0,9 мкМ, а для соединений 2, 3 и 4 IC50 составила 0,1 мкМ. Цитотоксическая активность соединений 2, 3, 4 в девять раз превышала цитотоксическую активность соединения 1, что свидетельствовало о высокой активности соединений в субмикромолярных и наномолярных концентрациях.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 1-(2-пропаргил)-1Н-нафто[2,3-d][1,2,3]триазол-4,9-дион-4-оксим-2-оксида | 2022 |
|
RU2791249C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАФТО[1,2,3-cd]ИНДОЛ-6(2Н)-ОНОВ | 2013 |
|
RU2552521C2 |
| СПОСОБ ПОЛУЧЕНИЯ НАФТО[1,2,3-cd]ИНДОЛ-6(2Н)-ОНОВ | 2013 |
|
RU2552416C2 |
| Производное класса N-гликозидов индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-дионов - N-{ 12-(β-D-ксилопиранозил)-5,7-диоксо-индоло[2,3-а]пирроло[3,4-с] карбазол-6-ил} пиридин-2-карбоксамид, обладающее цитотоксической и противоопухолевой активностью | 2017 |
|
RU2667906C1 |
| 6-ГИДРОКСИНАФТОХИНОНЫ ЛАБДАНОВОГО ТИПА, ОБЛАДАЮЩИЕ ЦИТОТОКСИЧЕСКОЙ АКТИВНОСТЬЮ ПО ОТНОШЕНИЮ К ОПУХОЛЕВЫМ КЛЕТКАМ ЧЕЛОВЕКА | 2012 |
|
RU2479582C1 |
| N-ГЛИКОЗИДЫ ИНДОЛО[2,3-a]ПИРРОЛО[3,4-c]КАРБАЗОЛОВ, ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2014 |
|
RU2548045C1 |
| Способ получения аминокислотных аналогов противоопухолевого антибиотика ребеккамицина | 2020 |
|
RU2755572C1 |
| ПРОИЗВОДНЫЕ ИНДОЛОКАРБАЗОЛОВ, БЛОКИРУЮЩИЕ ВАСКУЛОГЕННУЮ МИМИКРИЮ В ОПУХОЛИ | 2014 |
|
RU2557554C1 |
| 2-(1,2,3-ТРИАЗОЛИЛ)ЗАМЕЩЕННЫЕ ЛИНЕЙНЫЕ ФУРОКУМАРИНЫ, ОБЛАДАЮЩИЕ АНТИВИРУСНОЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ ВИРУСА ГРИППА A/Н1N1 | 2024 |
|
RU2841063C1 |
| 7-ТРИАЗОЛИЛ-ЗАМЕЩЕННЫЕ ГИДРОКСИСПИРОСТАНЫ, ОБЛАДАЮЩИЕ ЦИТОТОКСИЧЕСКОЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ ОПУХОЛЕВЫХ КЛЕТОК ЧЕЛОВЕКА | 2023 |
|
RU2798105C1 |
Изобретение относится к 1-R-4,9-диоксо-1H-нафто[2,3-d][1,2,3]триазол-4-оксим-2-оксидам, обладающим цитотоксической активностью, общей формулы 1
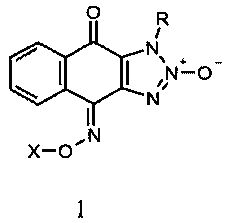
где R=Alk, бензил; X=H, -C(=O)R′, где R′=метил, фенил. Технический результат: получены новые биологически активные соединения. 1 табл., 4 пр.
1-R-4,9-диоксо-1H-нафто[2,3-d][1,2,3]триазол-4-оксим-2-оксиды, обладающие цитотоксической активностью, общей формулы 1

где
R=Alk, бензил; X=H, -C(=O)R′, где R′=метил, фенил.
| Н.Ю | |||
| Радаева и др | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| ИСПОЛЬЗОВАНИЕ ТРИЦИКЛИЧЕСКИХ ПРИЗВОДНЫХ 1,4-ДИГИДРО-1,4-ДИОКСО-1Н-НАФТАЛИНА И НОВЫЕ ЕГО СОЕДИНЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И ПРОИЗВОДНЫЕ ЗАМЕЩЕННЫХ НАФТАЛИНОВ В КАЧЕСТВЕ ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ | 1996 |
|
RU2178791C2 |
| US 20100267671 A1, 21.10.2010 | |||
Авторы
Даты
2015-03-27—Публикация
2014-03-18—Подача