Предлагаемое изобретение относится к способам получения новых фосфорорганических соединений, конкретно к способу получения полициклических 3-фенилфосфолан-3-сульфидов формулы 1а-г,


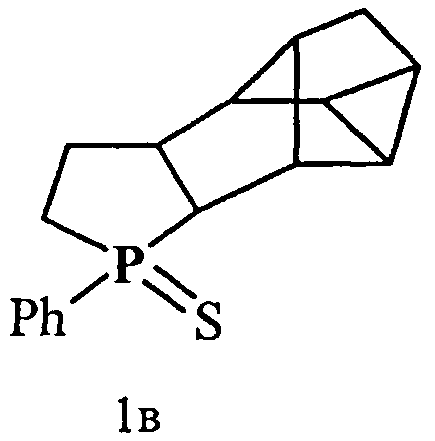

которые могут найти применение в качестве промежуточных реагентов для тонкого органического и металлорганического синтеза [Keglevich, G., Forintos, Н., Keseru, G.M., Hegedus, L., Toke, L. Tetrahedron 2000, 56, 4823], материалов для производства светоизлучающих диодов [Fave, С, Cho, T.-Y., Hissler, М., Chen, Ch.-W., Luh, T.-Y., Wu, Ch.-Ch., Reau, R., J. Am. Chem. Soc, 2003, 125, 9254] и потенциальных биологически активных соединений [Baraniak, J., Kaszmarek, R., Stec, W.J. Tetrahedron Lett. 2000, 41, 9139].
Известен способ [Hydrio, J., Gouygou, M., Dallemer, F., Daran, J.-C, Balavoine, G.A. Gilbert. Convenient route for the preparation of unsymmetrical phospholes via zirconacyclopentadienes. // J. Organomet. Chem., 2000, 595, 261-267] синтеза несимметричных фосфолсульфидов реакцией элементной серы с фосфолами, образующимися в результате взаимодействия дихлорфенилфосфина с соответствующими несимметричными цирконациклопентадиенами. Реакции протекают по схеме 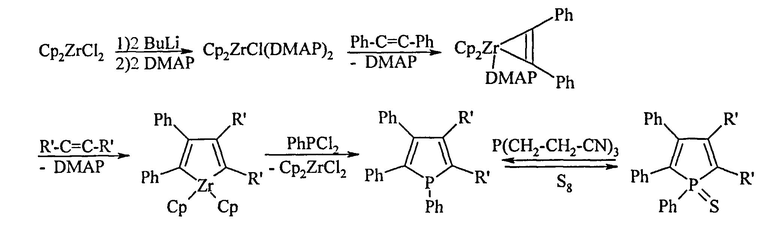
Известный способ не позволяет получать полициклические фосфолансульфиды 1а-г.
Известен способ [Tomioka, Н., Miura, Sh., Izawa, Y. Synthesis and photochemical reaction of Diels-Alder adduct of phosphole oxide and cyclopentadiene. // Tetrahedron Lett., 1983, 24, 3353-3356] получения фосфол-1-сульфида, исходя из 1,2,5-трифенилфосфола, полученного взаимодействием дифенил-1,3-бутадиена с фенилдихлорфосфином. Последующая конденсация незамещенного фосфол-1-сульфида с циклопентадиеном дает полициклический фосфол-1-сульфид. Реакции протекают по схеме

Известен способ [Zhou, Y., Yan, X., Xi, Ch. Preparation of 2-phospholene derivatives from zirconacyclopentenes. // Tet. Lett., 2010, 51, 6136-6138] получения замещенных фосфоленсульфидов реакцией соответствующих цирконациклопентенов с дихлорфенилфосфином, с последующим взаимодействием образующихся фосфоленов с элементной серой. Реакции протекают по схеме 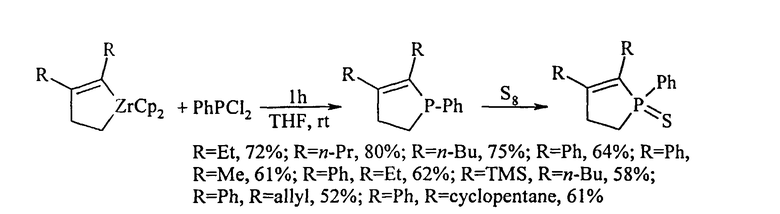
Известным способом не могут быть получены полициклические фосфолансульфиды 1а-г.
Таким образом, в литературе отсутствуют сведения по синтезу полициклических фосфолан-3-сульфидов 1а-г.
Предлагается способ синтеза полициклических 3-фенилфосфолан-3-сульфидов.
Сущность предлагаемого способа заключается во взаимодействии каркасных углеводородов норборненового ряда, таких как бицикло[2.2.1]гептен-2, или экзо-трицикло[3.2.1.02,4]октен-6, или тетрацикло[4.3.0.02,4.03,7]нонен-8, или дициклопентадиен, с триэтилалюминием при мольном соотношении реагентов непредельное соединение:AlEt3=1:1.05-1.2 в присутствии катализатора цирконоцендихлорида (Cp2ZrCl2), взятого в количестве 1-10 мол.% по отношению к исходному непредельному соединению, предпочтительно 5 мол.%, в атмосфере аргона при 15-25°C в течение 12 ч с последующим добавлением растворителя и при -10°C - галогенида трехвалентного фосфора RPCl2 (где R=Ph) в количестве 1:1 (моль/моль) по отношению к AlEt3, после чего реакционную массу перемешивают в течение 30 мин при 15-25°C. Затем в реакцию вовлекают серу (S8) в эквимольном по отношению к PhPCl2 количестве и перемешивают при 15-25°C в течение 12 ч. В качестве растворителя используют толуол, бензол или гексан. Выход полициклических фосфолан-3-сульфидов (1а-г), определенный по продуктам гидролиза с помощью ГЖХ, составляет 78-88%. Реакция протекает по схеме:

На первой стадии реакции триэтилалюминий AlEt3 и дихлорфенилфосфин берут в эквимольных количествах, с целью предотвращения образования побочных продуктов. Снижение количества AlEt3 по отношению к непредельному соединению на первой стадии реакции либо снижение количества дихлорфенилфосфина по отношению к образующемуся алюминациклопентану на второй стадии приводит к снижению конверсии непредельного соединения либо алюминациклопентана соответственно и, как следствие, вызывает уменьшение выхода целевого продукта. Изменение соотношения исходных реагентов в сторону увеличения содержания триэтилалюминия, PhPCl2 и серы приводит к образованию побочного диэтилфенилфосфинсульфида и снижению селективности реакции, а также в реакционной массе остается непрореагировавшая сера.
Проведение указанной реакции в присутствии катализатора Cp2ZrCl2 более 5 мол.% не приводит к существенному увеличению выхода целевых продуктов. Использование катализатора Cp2ZrCl2 менее 1 мол.% снижает выход алюминациклопентана, что связано, возможно, со снижением каталитически активных центров в реакционной массе. Опыты проводят при температуре 15-25°C. При более высокой температуре, например 50°C, уменьшается селективность реакции, при меньшей температуре, например 0°C, снижается скорость реакции.
Существенные отличия предлагаемого способа
Предлагаемый способ базируется на использовании в качестве исходных реагентов AlEt3, каркасных углеводородов норборненового ряда и дихлорфенилфосфина, а в качестве катализатора - Cp2ZrCl2. В литературе отсутствуют сведения о синтезе полициклических 3-фенилфосфолан-3-сульфидов.
Предлагаемый способ обладает следующими преимуществами:
1. Способ позволяет получать с высокой селективностью полициклические 3-фенилфосфолан-3-сульфиды формулы 1а-г, синтез которых в литературе не описан.
Способ поясняется следующими примерами.
Пример 1. В стеклянный реактор объемом 50 мл, установленный на магнитной мешалке, в атмосфере сухого аргона при 0°C и перемешивании последовательно помещают 0.0584 г (0.20 ммоль) Cp2ZrCl2, 0.376 г (4 ммоль) норборнена и 0.66 мл (4.4 ммоль (92%)) AlEt3. Температуру доводят до комнатной (~20°C) и перемешивают 12 ч. Затем в реакционную смесь добавляют 5 мл толуола и охлаждают до -10°C, прикапывают 0.6 мл (4.4 ммоль) дихлорфенилфосфина PhPCl2 и перемешивают при комнатной температуре 30 мин. Затем добавляют 0.1408 г (4.4 ммоль) молекулярной серы S8 и перемешивают при комнатной температуре 12 ч. Реакционную массу обрабатывают насыщенным водным раствором NH4Cl, продукты реакции экстрагируют диэтиловым эфиром, сушат над MgSO4. Растворитель упаривают, целевой 3-фенил-3-фосфатрицикло[5.2.1.02,6]декан-3-сульфид 1а выделяют колоночной хроматографией. Элюент - гексан:этилацетат:метанол=5:3:1. Другие примеры, подтверждающие способ, приведены в таблице.
Реакции проводят при 15-25°C.
В качестве растворителя используют толуол, бензол либо гексан.
Для соединений 1а-г выделены изомеры, образующиеся в преимущественном количестве.
Спектральные характеристики соединений 1а-г
3-Фенил-3-фосфатрицикло[5.2.1.02,6]декан-3-сульфид (1а)

Спектр ЯМР 1Н (δ, м.д., J/Гц, CDCl3): 1.10-1.24 (м, 3Н, С(5)На, С(8)На, С(10)На), 1.52-1.70 (м, 3Н, С(5)Нб, С(9)На, С(8)Нб), 1.78-1.94 (м, 2Н, С(9)Нб, С(10)Нб), 1.98-2.48 (м, 5Н, С(2)Н, С(4)Н2, С(6)Н, С(1)Н), 2.61-2.73 (м, 1Н, С(7)Н), 7.40-7.60, 7.77-7.96 (м, 5Н, Ph). Спектр ЯМР 13С (δ, м.д., J/Гц): 28.52 (С(8)), 29.35 (С(5), JCP=12.1), 29.63 (С(9), JCP=15.1), 29.91, 35.33 (С(10)), 35.68 (С(4), JCP=54.3), 38.33 (С(7)), 40.92 (С(1)), 49.21 (С(2), JCP=50.3), 50.76 (С(6), JCP=4), 128.56 (Ph, JCP=11.1), 130.59 (Ph, JCP=10.05), 130.95(Ph, JCP=9.05), 131.27. Спектр ЯМР 31P (δ, м.д.): 65.62. Rf=0.35.
3-Фенил-3-фосфа-экзо-тетрацикло[5.3.1.02,6.08,10]ундекан-3-сульфид (1б)
Спектр ЯМР 1Н (δ, м.д., J/Гц, CDCl3): 0.02-0.18 (м, 1H, С(9)На), 0.56-0.65 (м, 1Н, С(9)Нб), 0.70-1.20 (м, 3Н, С(11)На, С(10)Н, С(8)Н), 1.30-1.40 (м, 1Н, С(11)Нб), 1.70-1.80 (м, 1Н, С(5)На), 2.02-2.33 (м, 5Н, С(4)На, С(1)Н, С(5)Нб, С(2)Н, С(4)Нб), 2.49-2.65 (м, 2Н, С(6)Н, С(7)Н), 7.33-7.56, 7.73-7.80 (м, 5Н, Ph). Спектр ЯМР 13С (δ, м.д., J/Гц): ЯМР 13С (δ, м.д., J/Гц): 4.63 (С(9), JCP=2), 16.36 (С(10), JCP=16.1), 16.74 (С(8)), 23.64 (С(11)), 28.37 (С(5), JCP=10.05), 36.70 (С(4), JCP=53.3), 38.17 (С(7)), 40.72 (С(1)), 50.58 (С(2), JCP=51.1), 51.52 (С(6), JCP=6), 128.74 (Ph, JCP=12.1), 130.35 (Ph, JCP=10.05), 131.78 (Ph, JCP=2), 132.78 (Ph, JCP=89.5). Спектр ЯМР 31P (δ, м.д.): 60.50. Rf=0.33.
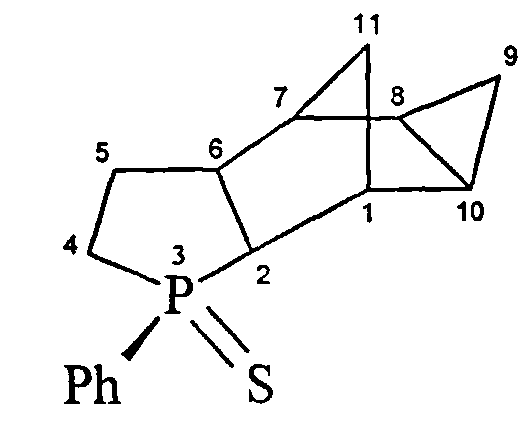
3-Фенил-3-фосфапентацикл[6.4.0.02,6.08.10]додекан-3-сульфид (1в)
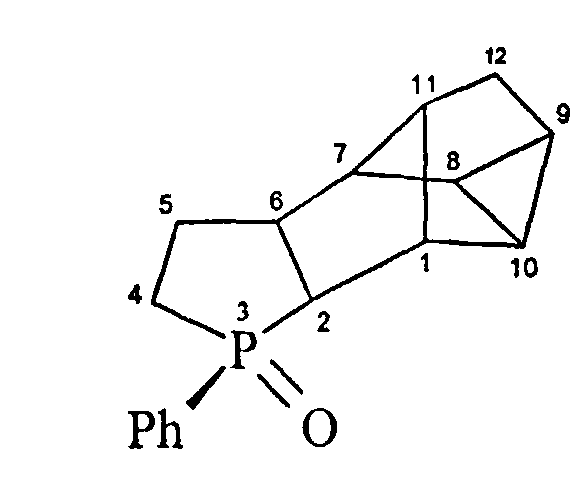
Спектр ЯМР 1Н (δ, м.д., J/Гц, CDCl3): 0.95-1.06 (м, 2Н, С(10)Н, С(8)Н), 1.19-1.24 (м, 1Н, (С(9)Н), 1.57-1.63 (м, 1Н, (С(12)На), 1.67-1.73 (С(12)Нб), 1.84-1.93 (м, 1H, (С(5)На), 1.98-2.01 (м, 1Н, С(1)Н), 2.10-2.17 (м, 1H, С(4)На), 2.20-2.34 (м, 3Н, С(5)Нб, С(4)Нб, С(11)Н), 2.46-2.52 (м, 2Н, С(7)Н), 2.67-2.72 (м, 1H, С(2)Н), 2.81-2.89 (м, 1Н, С(6)Н), 7.45-7.55, 7.86-7.96 (м, 5Н, Ph).
Спектр ЯМР 13С (δ, м.д., J/Гц): 14.90 (С(9)), 16.29 (С(10), JCP=15.1), 16.31 (С(8)), 29.49 (С(5), JCP=11.1), 31.79 (С(12)), 35.82 (С(4), JCP=533), 39.07 (С(11)), 44.38 (С(7)), 47.54 (С(2), JCP=50.1), 48.31 (С(6), JCP=6), 48.45 (С(1)), 128.57 (Ph, JCP=11.1), 130.62 (Ph, JCP=10.1), 131.27, 131.46. Спектр ЯМР 31Р (δ, м.д.): 63.51. Rf=0.35.
1-Фенил-1-фосфатетрацикло[5.5.1.02,6.08,12]тридец-10-ен-3-сульфид (1г)
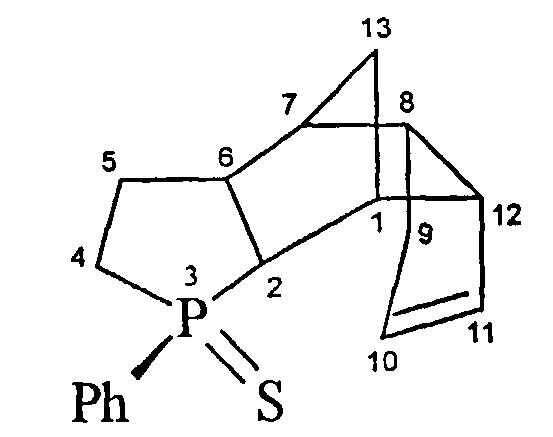
Спектр ЯМР 1Н (δ, м.д., J/Гц, CDCl3): 1.45-1.53 (м, 1Н, (С(13)На), 1.80-1.91 (м, 1Н, С(5)На), 2.09-2.37 (м, 8Н, (С(1)Н, С(13)Нб, С(4)Н2, С(5)Нб, С(9)Н2, С(2)Н), 2.44-2.52 (м, 1Н, С(6)Н), 2.58-2.69 (м, 1Н, С(8)Н), 2.75-2.80 (м, 1H, С(7)Н), 3.16-3.23 (м, 1Н, С(12)Н), 5.40-5.45 (м, 1H, С(10)Н), 5.72-5.76 (м, 1H, С(11)Н), 7.45-7.55, 7.80-7.90 (м, 5Н, Ph). Спектр ЯМР 13С (δ, м.д., J/Гц): 29.74 (С(5), JCP=12.1), 32.06 (С(9)), 36.12 (С(4), JCP=53.3), 38.72 (С(13)), 41.66 (С(7)), 41.69 (С(8)), 42.48 (С(6), JCP=5), 44.50 (С(2), JCP=52.3), 45.98 (С(1)Н), 52.96 (С(12), JCP=13.1), 131.73 (С(10)), 132.12 (С(11)), 128.54 (Ph, JCP=11.1), 130.45 (Ph, JСР=12.1), 131.13 (Ph, JCP=3), 131.98. Спектр ЯМР 31Р (δ, м.д.): 67.19. Rf=0.30.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИЦИКЛИЧЕСКИХ 3-ФЕНИЛФОСФОЛАНОВ | 2013 |
|
RU2551650C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИЦИКЛИЧЕСКИХ 3-АЛКИЛ(ФЕНИЛ)ФОСФОЛАН-3-ОКСИДОВ | 2013 |
|
RU2551684C1 |
| СПОСОБ ПОЛУЧЕНИЯ 3-ЭТИЛ-3-АЛЮМИНАТЕТРАЦИКЛО[12.2.1.0.0]ГЕПТАДЕЦ-4-ЕНА | 2008 |
|
RU2375367C2 |
| Способ получения 3-алкил(арил)-1-дихлорметилфосфолан оксидов | 2023 |
|
RU2812208C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛ-1-ФЕНИЛ(АЛКИЛ)ЗАМЕЩЕННЫХ ФОСФОЛ-2-ЕН-1-СУЛЬФИДОВ | 2014 |
|
RU2556008C1 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ 3-ЭТИЛ-3-АЛЮМИНАПЕНТАЦИКЛО-[12.5.1.0.0.0]-ИКОЗА-4,16-ДИЕНА И 3-ЭТИЛ-3-АЛЮМИНАПЕНТАЦИКЛО-[12.5.1.0.0.0]-ИКОЗА-4,17-ДИЕНА | 2008 |
|
RU2375369C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПИРИДИНАТОВ 1-ФТОР(ХЛОР)-3-АЛКИЛ(АРИЛ)БОРОЛАНОВ | 2013 |
|
RU2532925C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ФТОР-3-АЛКИЛБОРОЦИКЛОПЕНТАНОВ | 2010 |
|
RU2440356C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-БРОМ-3-АЛКИЛБОРОЛАНОВ | 2012 |
|
RU2507208C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛ-1-ФЕНИЛ(АЛКИЛ)ЗАМЕЩЕННЫХ ФОСФОЛ-2-ЕН-1-ОКСИДОВ | 2014 |
|
RU2570205C2 |
Изобретение относится к способу получения соединений, пригодных в области органического синтеза формул 1а-г,
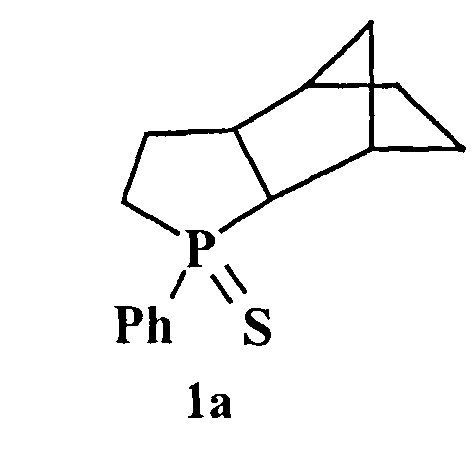
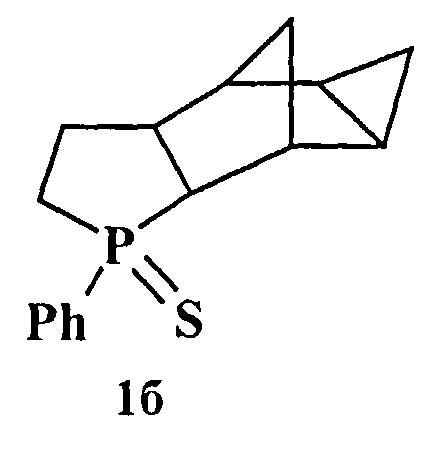


Способ заключается во взаимодействии каркасного углеводорода норборненового ряда бицикло[2.2.1]гептена-2, или экзо-трицикло[3.2.1.02,4]октена-6, или тетрацикло[4.3.02,4.03,7]нонена-8, или дициклопентадиена с триэтилалюминием при мольном соотношении непредельное соединение:AlEt3=1:1.05-1.2, в присутствии 1-10 мол.% катализатора цирконоцендихлорида (Cp2ZrCl2) в атмосфере аргона при 15-25°C и атмосферном давлении с последующим добавлением толуола, бензола или гексана и галогенида трехвалентного фосфора RPCl2 (где R=Ph) в количестве 1:1 (моль/моль) по отношению к триэтилалюминию и перемешиванием реакционной массы в атмосфере аргона при 15-25°C, после чего вносят эквимольное к фенилдихлорфосфину количество молекулярной серы S8. Предложен эффективный способ получения полициклических фосфолансульфидов. 1 з.п. ф-лы, 1 табл., 1 пр.
1. Способ получения полициклических фосфолан-3-сульфидов формулы 1а-г




взаимодействием каркасного непредельного соединения с триэтилалюминием в присутствии катализатора Cp2ZrCl2, отличающийся тем, что в качестве каркасного непредельного соединения используют бицикло[2.2.1]гептен-2, или экзо-трицикло[3.2.1.02,4]октен-6, или тетрацикло[4.3.0.02,4.03,7]нонен-8, или дициклопентадиен, реакцию проводят при мольном соотношении реагентов Cp2ZrCl2:непредельное соединение:AlEt3=0.05:1:1.05-1.2, в атмосфере аргона при температуре 15-25°С и атмосферном давлении в течение 12 ч, с последующим добавлением растворителя, затем дихлорфенилфосфина PhPCl2 при -10°С в количестве 1:1 по отношению к триэтилалюминию, после чего реакционную смесь перемешивают при температуре 15-25°С в атмосфере аргона 30 мин, по истечении которого вносят эквимольное по отношению к дихлорфенилфосфину количество молекулярной серы S8 и реакцию продолжают еще 12 ч.
2. Способ по п.1, отличающийся тем, что в качестве растворителя используют толуол, бензол или гексан.
Авторы
Даты
2015-05-27—Публикация
2013-10-31—Подача