Область изобретения
Настоящее изобретение относится к антителам человека и антигенсвязывающим фрагментам антител человека, которые специфическим образом связывают человеческую пропротеинконвертазу субтилизин/кексин тип 9 (PCSK9), и к терапевтическим методам применения указанных антител.
Известный уровень техники
Пропротеинконвертаза субтилизин/кексин тип 9 (PCSK9) относится к пропротеинконвертазам, входящим в подсемейство протеиназ К семейства секреторных субтилаз. Кодируемый белок синтезируется в виде растворимого зимогена, который проходит автокаталитическую внутримолекулярную трансформацию в эндоплазматическом ретикулуме. Имеющиеся данные свидетельствуют о том, что PCSK9 повышает ЛНП холестерин в плазме за счет стимулирования распада рецептора ЛНП, который опосредует эндоцитоз ЛНП в печени, являющийся основным каналом клиренса ЛНП из обращения. Структура белка PCSK9 указывает на наличие сигнальной последовательности, за которой идет продомен, каталитический домен, содержащий консервативную триаду остатков (D186, H226 и S386) и С-терминальный домен. Она синтезируется в виде растворимого предшественника 74 кДа, который претерпевает автокаталитический распад в ЭР с образованием продомена 14 кДа и каталитического фрагмента 60 кДа. Была продемонстрирована необходимость наличия автокаталитической активности для секреции. После распада продомен остается жестко связанным с каталитическим доменом.
Антитела к PCSK9 описаны, например, в заявках WO 2008/057457, WO 2008/057458, WO 2008/057459, WO 2008/063382, WO 2008/125623 и патенте US 2008/0008697.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В первом аспекта изобретения предлагаются полностью человеческие моноклональные антитела (mAb) и их антигенсвязывающие фрагменты, которые специфически связываются и нейтрализуют активность человеческой PCSK9 (hPCSK9).
В одном осуществлении настоящее изобретение включает антитело или антигенсвязывающий фрагмент антитела, которые специфически связывает hPCSK9 и характеризуется по крайней мере одним из следующих признаков:
(i) способностью снижать суммарный сывороточный холестерин не менее чем на 25-35% и поддерживать сниженный уровень в течение не менее чем 24-дневного периода по сравнению с уровнем до введения, предпочтительное снижение суммарного уровня холестерина составляет не менее чем приблизительно 30-40%;
(ii) способностью снижать сывороточный ЛНП холестерин не менее чем на приблизительно 65-80% и поддерживать сниженный уровень в течение не менее чем 24-дневного периода по сравнению с уровнем до введения;
(iii) способностью снизить уровень сывороточных триглицеридов не менее чем на приблизительно 25-40% по сравнению с уровнем до введения;
(iv) не приводит к снижению уровня сывороточного ЛВП холестерина или снижает уровень сывороточного ЛВП холестерина не более чем на 5% по сравнению с уровнем до введения.
В одном осуществлении настоящее изобретение включает антитело или антигенсвязывающий фрагмент антитела, которые специфически связывает hPCSK9 и характеризуется по крайней мере одним из следующих признаков:
(i) способностью снижать сывороточный ЛНП холестерин не менее чем на приблизительно 40-70% и поддерживать сниженный уровень в течение не менее чем 60-дневного периода по сравнению с уровнем до введения;
(ii) способностью снизить уровень сывороточных триглицеридов не менее чем на приблизительно 25-40% по сравнению с уровнем до введения;
(iii) не приводит к снижению уровня сывороточного ЛВП холестерина или снижает уровень сывороточного ЛВП холестерина не более чем на 5% по сравнению с уровнем до введения.
В одном из осуществлений антитело или его фрагмент характеризуются как связывающие эпитоп, включающий аминокислотный остаток 238 от hPCSK9 (SEQ ID №: 755). В одном из более конкретных осуществлений антитело или его фрагмент связывают эпитоп, включающий один или несколько аминокислотных остатков 238, 153, 159 и 343 от hPCSK9 (SEQ ID №: 755). В более конкретном осуществлении антитело или его фрагмент характеризуются как связывающие эпитоп, не содержащий аминокислотный остаток в положениях 192, 194, 197 и/или 237 последовательности SEQ ID №: 755.
В одном из осуществлений антитело или его фрагмент характеризуются как связывающие эпитоп, включающий аминокислотный остаток 366 от hPCSK9 (SEQ ID №: 755). В одном из более конкретных осуществлений антитело или его фрагмент связывают эпитоп, включающий один или несколько аминокислотных остатков 147, 366 и 380 SEQ ID №: 755. В более конкретном осуществлении антитело или его фрагмент характеризуются как связывающие эпитоп, не содержащий аминокислотный остаток в положениях 215 и/или 238 последовательности SEQ ID №: 755.
В одном осуществлении антитело или его фрагмент характеризуются как проявляющие повышенную аффинность связывания (KD) для hPCSK9 при pH 5,5 по сравнению с KD при pH 7,4, как показывают результаты измерения поверхностным плазмонным резонансом. В одном конкретном осуществлении антитело или его фрагмент проявляют не менее чем 20-кратную, не менее чем 40-кратную или не менее чем 50-кратную повышенную аффинность к PCSK9 при кислом pH по сравнению с нейтральным pH, как показывают данные поверхностного плазмонного резонанса.
В одном осуществлении антитело или его фрагмент характеризуются как не проявляющие повышенную аффинность связывания для PCSK9 при кислом pH по сравнению с нейтральным pH, как показывают результаты измерения поверхностным плазмонным резонансом. В одном конкретном осуществлении связывание при кислом рН слабее, а T1/2 короче, чем при нейтральном pH.
В другом осуществлении антитело или антигенсвязывающий фрагмент связываются с PCSK9 человека, человека с GOF-мутацией D374Y, яванского макака, макаки-резуса, мыши, крысы и хомяка.
В одном осуществлении антитело или антигенсвязывающий фрагмент связываются с PCSK9 человека и обезьяны, но не связывается с PCSK9 мыши, крысы и хомяка.
mAb могут быть полноразмерными (например, антитела IgG1 или IgG4) или включать только антигенсвязывающую часть (например, фрагмент Fab, F(ab')2 или scFv) и могут быть модифицированы с целью воздействовать на функциональность, например, удалять остаточные эффекторные функции (Reddy et al. (2000) J. Immunol. 164:1925-1933).
В одном осуществлении настоящее изобретение включает антитело или антигенсвязывающий фрагмент антитела, содержащие вариабельную область тяжелой цепи (HCVR), выбираемую из группы SEQ ID №: 2, 18, 22, 26, 42, 46, 50, 66, 70, 74, 90, 94, 98, 114, 118, 122, 138, 142, 146, 162, 166, 170, 186, 190, 194, 210, 214, 218, 234, 238, 242, 258, 262, 266, 282, 286, 290, 306, 310, 314, 330, 334, 338, 354, 358, 362, 378, 382, 386, 402, 406, 410, 426, 430, 434, 450, 454, 458, 474, 478, 482, 498, 502, 506, 522, 526, 530, 546, 550, 554, 570, 574, 578, 594, 598, 602, 618, 622, 626, 642, 646, 650, 666, 670, 674, 690, 694, 698, 714, 718, 722, 738 и 742, или ее существенно аналогичную последовательность, имеющую идентичность последовательности не менее 90%, не менее 95%, не менее 98% или не менее 99%. В одном осуществлении HCVR является аминокислотной последовательностью, выбираемой из группы SEQ ID №: 50, 66, 70, 74, 90, 94, 122, 138, 142, 218, 234, 238, 242, 258, 262, 314, 330 и 334. В более конкретном осуществлении HCVR содержит SEQ ID №: 90 или 218.
В одном осуществлении антитело или его фрагмент далее содержит вариабельную область легкой цепи (LCVR), выбираемую из группы SEQ ID №: 10, 20, 24, 34, 44, 48, 58, 68, 72, 82, 92, 96, 106, 116, 120, 130, 140, 144, 154, 164, 168, 178, 188, 192, 202, 212, 216, 226, 236, 240, 250, 260, 264, 274, 284, 288, 298, 308, 312, 322, 332, 336, 346, 356, 360, 370, 380, 384, 394, 404, 408, 418, 428, 432, 442, 452, 456, 466, 476, 480, 490, 500, 504, 514, 524, 528, 538, 548, 552, 562, 572, 576, 586, 596, 600, 610, 620, 624, 634, 644, 648, 658, 668, 672, 682, 692, 696, 706, 716, 720, 730, 740 и 744, или ее существенно аналогичную последовательность, имеющую идентичность последовательности не менее 90%, не менее 95%, не менее 98% или не менее 99%. В одном осуществлении LCVR является аминокислотной последовательностью, выбираемой из группы SEQ ID №: 58, 68, 72, 82, 92, 96, 130, 140, 144, 226, 236, 240, 250, 260, 264, 322, 332 и 336. В более конкретном осуществлении LCVR содержит SEQ ID №: 92 или 226.
В конкретных осуществлениях антитело или его фрагмент содержит пару последовательностей HCVR и LCVR (HCVR/LCVR), выбираемую из группы, включающей SEQ ID №: 2/10, 18/20, 22/24, 26/34, 42/44, 46/48, 50/58, 66/68, 70/72, 74/82, 90/92, 94/96, 98/106, 114/116, 118/120, 122/130, 138/140, 142/144, 146/154, 162/164, 166/168, 170/178, 186/188, 190/192, 194/202, 210/212, 214/216, 218/226, 234/236, 238/240, 242/250, 258/260, 262/264, 266/274, 282/284, 286/288, 290/298, 306/308, 310/312, 314/322, 330/332, 334/336, 338/346, 354/356, 358/360, 362/370, 378/380, 382/384, 386/394, 402/404, 406/408, 410/418, 426/428, 430/432, 434/442, 450/452, 454/456, 458/466, 474/476, 478/480, 482/490, 498/500, 502/504, 506/514, 522/524, 526/528, 530/538, 546/548, 550/552, 554/562, 570/572, 574/576, 578/586, 594/596, 598/600, 602/610, 618/620, 622/624, 626/634, 642/644, 646/648, 650/658, 666/668, 670/672, 674/682, 690/692, 694/696, 698/706, 714/716, 718/720, 722/730, 738/740 и 742/744. В одном осуществлении HCVR и LCVR выбираются из пар аминокислотных последовательностей SEQ ID №: 50/58, 66/68, 70/72, 74/82, 90/92, 94/96, 122/130, 138/140, 142/144, 218/226, 234/236, 238/240, 242/250, 258/260, 262/264, 314/322, 330/332 и 334/336. В более конкретном осуществлении пара HCVR/LCVR содержит SEQ ID №: 90/92 или 218/226.
Во втором аспекте настоящего изобретения приводится антитело или антигенсвязывающий фрагмент антитела, содержащие домен CDR3 (HCDR3) тяжелой цепи, выбираемый из группы, включающей SEQ ID №: 8, 32, 56, 80, 104, 128, 152, 176, 200, 224, 248, 272, 296, 320, 344, 368, 392, 416, 440, 464, 488, 512, 536, 560, 584, 608, 632, 656, 680, 704 и 728, или его существенно аналогичную последовательность, имеющую идентичность последовательности не менее 90%, не менее 95%, не менее 98% или не менее 99%; и домен CDR3 (LCDR3) легкой цепи, выбираемый из группы, включающей SEQ ID №: 16, 40, 64, 88, 112, 136, 160, 184, 208, 232, 256, 280, 304, 328, 352, 376, 400, 424, 448, 472, 496, 520, 544, 568, 592, 616, 640, 664, 688, 712 и 736, или его существенно аналогичную последовательность, имеющую идентичность последовательности не менее 90%, не менее 95%, не менее 98% или не менее 99%. В одном осуществлении пары последовательностей HCVR/LCVR являются SEQ ID №: 56/64, 80/88, 128/136, 224/232, 248/256 или 320/328. В более конкретном осуществлении HCDR3/LCDR3 содержит SEQ ID №: 80/88 или 224/232.
В дальнейшем осуществлении настоящего изобретения приводится антитело или его фрагмент, дополнительно содержащие домен CDR1 (HCDR1) тяжелой цепи, выбираемый из группы, включающей SEQ ID №: 4, 28, 52, 76, 100, 124, 148, 172, 196, 220, 244, 268, 292, 316, 340, 364, 388, 412, 436, 460, 484, 508, 532, 556, 580, 604, 628, 652, 676, 700 и 724, или его существенно аналогичную последовательность, имеющую идентичность последовательности не менее 90%, не менее 95%, не менее 98% или не менее 99%; домен CDR2 (HCDR2) тяжелой цепи, выбираемый из группы, включающей SEQ ID №: 6, 30, 54, 78, 102, 126, 150, 174, 198, 222, 246, 270, 294, 318, 342, 366, 390, 414, 438, 462, 486, 510, 534, 558, 582, 606, 630, 654, 678, 702 и 726, или его существенно аналогичную последовательность, имеющую идентичность последовательности не менее 90%, не менее 95%, не менее 98% или не менее 99%; домен CDR1 (HCDR1) легкой цепи, выбираемый из группы, включающей SEQ ID №: 12, 36, 60, 84, 108, 132, 156, 180, 204, 228, 252, 276, 300, 324, 348, 372, 396, 420, 444, 468, 492, 516, 540, 564, 588, 612, 636, 660, 684, 708 и 732, или его существенно аналогичную последовательность, имеющую идентичность последовательности не менее 90%, не менее 95%, не менее 98% или не менее 99%; и домен CDR2 (HCDR2) легкой цепи, выбираемый из группы, включающей SEQ ID №: 14, 38, 62, 86, 110, 134, 158, 182, 206, 230, 254, 278, 302, 326, 350, 374, 398, 422, 446, 470, 494, 518, 542, 566, 590, 614, 638, 662, 686, 710 и 734, или его существенно аналогичную последовательность, имеющую идентичность последовательности не менее 90%, не менее 95%, не менее 98% или не менее 99%. В одном осуществлении последовательностями CDR тяжелой и легкой цепей являются SEQ ID №: 52, 54, 56, 60, 62, 64; 76, 78, 80, 84, 86, 88; 124, 126, 128, 132, 134, 136; 220, 222, 224, 228, 230, 232; 244, 246, 248, 252, 254, 256; и 316, 318, 320, 324, 326, 328. В более конкретных осуществлениях последовательностями CDR тяжелой и легкой цепей являются SEQ ID №: 76, 78, 80, 84, 86, 88; or 220, 222, 224, 228, 230, 232.
В связанном осуществлении настоящего изобретения приводится антитело или антигенсвязывающий фрагмент антитела, содержащие домен, который специфическим образом связывает hPCSK9, где антитело или его фрагмент содержит домены тяжелой и легкой цепей CDR, находящиеся в парах последовательностей тяжелой и легкой цепей, выбираемых из группы, включающей SEQ ID №: 2/10, 18/20, 22/24, 26/34, 42/44, 46/48, 50/58, 66/68, 70/72, 74/82, 90/92, 94/96, 98/106, 114/116, 118/120, 122/130, 138/140, 142/144, 146/154, 162/164, 166/168, 170/178, 186/188, 190/192, 194/202, 210/212, 214/216, 218/226, 234/236, 238/240, 242/250, 258/260, 262/264, 266/274, 282/284, 286/288, 290/298, 306/308, 310/312, 314/322, 330/332, 334/336, 338/346, 354/356, 358/360, 362/370, 378/380, 382/384, 386/394, 402/404, 406/408, 410/418, 426/428, 430/432, 434/442, 450/452, 454/456, 458/466, 474/476, 478/480, 482/490, 498/500, 502/504, 506/514, 522/524, 526/528, 530/538, 546/548, 550/552, 554/562, 570/572, 574/576, 578/586, 594/596, 598/600, 602/610, 618/620, 622/624, 626/634, 642/644, 646/648, 650/658, 666/668, 670/672, 674/682, 690/692, 694/696, 698/706, 714/716, 718/720, 722/730, 738/740 и 742/744. В одном осуществлении последовательности CDR, содержащиеся в HCVR и LCVR, выбираются из пар аминокислотных последовательностей SEQ ID №: 50/58, 66/68, 70/72, 74/82, 90/92, 94/96, 122/130, 138/140, 142/144, 218/226, 234/236, 238/240, 242/250, 258/260, 262/264, 314/322, 330/332 и 334/336. В более конкретных осуществлениях последовательности CDR, содержащиеся в HCVR и LCVR, выбираются из пар аминокислотных последовательностей SEQ ID №: 90/92 или 218/226.
В одном осуществлении настоящего изобретения приводится полное моноклональное антитело человека, или его антиген-связывающий фрагмент, которое специфическим образом связывает и нейтрализует активность hPCSK9, при этом антитело или его фрагмент демонстрирует одну или более из следующих характеристик:
(i) способность снижать суммарный сывороточный холестерин не менее чем на 25-35% и поддерживать сниженный уровень в течение не менее чем 24-дневного периода по сравнению с уровнем до введения, предпочтительное снижение суммарного уровня сывороточного холестерина составляет не менее чем приблизительно 30-40%;
(ii) способность снижать сывороточный ЛНП холестерин не менее чем на приблизительно 65-80% и поддерживать сниженный уровень в течение не менее чем 24-дневного периода по сравнению с уровнем до введения;
(iii) способность снизить уровень сывороточных триглицеридов не менее чем на приблизительно 25-40% по сравнению с уровнем до введения;
(iv) не приводит к снижению уровня сывороточного ЛВП холестерина или снижает уровень сывороточного ЛВП холестерина не более чем на 5% по сравнению с уровнем до введения;
(v) связывает эпитоп, содержащий аминокислотные остатки 238 hPCSK9 (SEQ ID №: 755);
(vi) проявляет повышенную аффинность связывания (KD) для hPCSK9 при pH 5,5 по сравнению с KD при pH 7,4, как показывают измерения с помощью поверхностного плазмонного резонанса, причем такая повышенная аффинность представляет собой не менее чем 20-50-кратное повышение аффинности;
(vii) связывает с PCSK9 человека, человека с GOF-мутацией D374Y, яванского макака, макаки-резуса, мыши, крысы и хомяка;
(viii) содержит последовательности CDR3 тяжелой и легкой цепи, содержащие SEQ ID №: 80 и 88;
(ix) содержит последовательности CDR из SEQ ID №: 90 и 92.
В одном осуществлении настоящего изобретения приводится полное моноклональное антитело человека, или его антиген-связывающий фрагмент, которое специфическим образом связывает и нейтрализует активность hPCSK9, при этом антитело или его фрагмент демонстрирует одну или более из следующих характеристик:
(i) способность снижать сывороточный ЛНП холестерин не менее чем на приблизительно 40-70% и поддерживать сниженный уровень в течение не менее чем 60-дневного периода по сравнению с уровнем до введения;
(ii) способность снизить уровень сывороточных триглицеридов не менее чем на приблизительно 25-40% по сравнению с уровнем до введения;
(iii) не приводит к снижению уровня сывороточного ЛВП холестерина или снижает уровень сывороточного ЛВП холестерина не более чем на 5% по сравнению с уровнем до введения;
(iv) связывает эпитоп, содержащий аминокислотные остатки 366 hPCSK9 (SEQ ID №: 755);
(v) не проявляет повышенную аффинность связывания для PCSK9 при кислом pH по сравнению с нейтральным pH, как показывают результаты измерения поверхностного плазмонного резонанса;
(vi) связывает с PCSK9 человека и обезьяны, но не связывает с PCSK9 мыши, крысы и хомяка;
(vii) содержит последовательности CDR3 тяжелой и легкой цепи, содержащие SEQ ID №: 224 и 232; и
(viii) содержит последовательности CDR из SEQ ID №: 218 и 226.
В третьем аспекте настоящего изобретения приводятся молекулы нуклеиновой кислоты, кодирующие антитела анти-PCSK9 или их фрагменты. Настоящее изобретение также охватывает рекомбинантные векторы экспрессии, несущие нуклеиновые кислоты настоящего изобретения, и клетки-хозяева, в которые включаются такие векторы, а также способы получения антител путем культивирования клеток-хозяев в условиях, допускающих продуцирование антител и получение продуцированных антител.
В одном осуществлении настоящего изобретения приводится антитело или его фрагмент, содержащие HCVR, кодируемую последовательностью нуклеиновой кислоты, выбираемой из группы, включающей SEQ ID №: 1, 17, 21, 25, 41, 45, 49, 65, 69, 73, 89, 93, 97, 113, 117, 121, 137, 141, 145, 161, 165, 169, 185, 189, 193, 209, 213, 217, 233, 237, 241, 257, 261, 265, 281, 285, 289, 305, 309, 313, 329, 333, 337, 353, 357, 361, 377, 381, 385, 401, 405, 409, 425, 429, 433, 449, 453, 457, 473, 477, 481, 497, 501, 505, 521, 525, 529, 545, 549, 553, 569, 573, 577, 593, 597, 601, 617, 621, 625, 641, 645, 649, 665, 669, 673, 689, 693, 697, 713, 717, 721, 737 и 741, или существенно аналогичную последовательность с гомологией не менее 90%, не менее 95%, не менее 98% или не менее 99%. В одном осуществлении HCVR кодируется последовательностью нуклеиновой кислоты, выбираемой из группы, включающей SEQ ID №: 49, 65, 69, 73, 89, 93, 121, 137, 141, 217, 233, 237, 241, 257, 261, 313, 329 и 333. В более конкретных осуществлениях HCVR кодируется последовательностью нуклеиновой кислоты, выбираемой из группы, включающей SEQ ID №: 89 и 217.
В одном осуществлении антитело или его фрагмент дополнительно содержит LCVR, кодируемую последовательностью нуклеиновой кислоты, выбираемой из группы, включающей SEQ ID №: 99, 19, 23, 33, 43, 47, 57, 67, 71, 81, 91, 95, 105, 115, 119, 129, 139, 143, 153, 163, 167, 177, 187, 191, 201, 211, 215, 225, 235, 239, 249, 259, 263, 273, 283, 287, 297, 307, 311, 321, 331, 335, 345, 355, 359, 369, 379, 383, 393, 403, 407, 417, 427, 431, 441, 451, 455, 465, 475, 479, 489, 499, 503, 513, 523, 527, 537, 547, 551, 561, 571, 575, 585, 595, 599, 609, 619, 623, 633, 643, 647, 657, 667, 671, 681, 691, 695, 705, 715, 719, 729, 739 и 743, или существенно аналогичную последовательность с гомологией не менее 90%, не менее 95%, не менее 98% или не менее 99%. В одном осуществлении LCVR кодируется последовательностью нуклеиновой кислоты, выбираемой из группы, включающей SEQ ID №: 57, 67, 71, 81, 91, 95, 129, 139, 143, 225, 235, 239, 249, 259, 263, 321, 331 и 335. В более конкретных осуществлениях LCVR кодируется последовательностью нуклеиновой кислоты, выбираемой из группы, включающей SEQ ID №: 91 и 225.
В одном осуществлении настоящего изобретения приводится антитело или антигенсвязывающий фрагмент антитела, содержащие домен HCDR3, кодируемый нуклеотидной последовательностью, выбираемой из группы, включающей SEQ ID №: 7, 31, 55, 79, 103, 127, 151, 175, 199, 223, 247, 271, 295, 319, 343, 367, 391, 415, 439, 463, 487, 511, 535, 559, 583, 607, 631, 655, 679, 703 и 727, или существенно аналогичную последовательность с гомологией не менее 90%, не менее 95%, не менее 98% или не менее 99%; и домен LCDR3, кодируемый нуклеотидной последовательностью, выбираемой из группы, включающей SEQ ID №: 15, 39, 63, 87, 111, 135, 159, 183, 207, 231, 255, 279, 303, 327, 351, 375, 399, 423, 447, 471, 495, 519, 543, 567, 591, 615, 639, 663, 687, 711 и 735, или существенно аналогичную последовательность с гомологией не менее 90%, не менее 95%, не менее 98% или не менее 99%. В одном осуществлении последовательности HCDR3 и LCDR3 кодируются последовательностью нуклеиновой кислоты SEQ ID №: 55/63, 79/87, 127/135, 223/231, 247/255 и 319/327 соответственно. В более конкретных осуществлениях пара последовательностей HCDR3 и LCDR3 кодируется последовательностью нуклеиновой кислоты SEQ ID №: 79/87 и 223/231.
В еще одном осуществлении антитело или его фрагмент дополнительно содержит домен HCDR1, кодируемый нуклеотидной последовательностью, выбираемой из группы, включающей SEQ ID №: 3, 27, 51, 75, 99, 123, 147, 171, 195, 219, 243, 267, 291, 315, 339, 363, 387, 411, 435, 459, 483, 507, 531, 555, 579, 603, 627, 651, 675, 699 и 723, или существенно аналогичную последовательность с гомологией не менее 90%, не менее 95%, не менее 98% или не менее 99%; домен HCDR2, кодируемый нуклеотидной последовательностью, выбираемой из группы, включающей SEQ ID №: 5, 29, 53, 77, 101, 125, 149, 173, 197, 221, 245, 269, 293, 317, 341, 365, 389, 413, 437, 461, 485, 509, 533, 557, 581, 605, 629, 653, 677, 701 и 725, или существенно аналогичную последовательность с гомологией не менее 90%, не менее 95%, не менее 98% или не менее 99%; домен LCDR1, кодируемый нуклеотидной последовательностью, выбираемой из группы, включающей SEQ ID №: 11, 35, 59, 83, 107, 131, 155, 179, 203, 227, 251, 275, 299, 323, 347, 371, 395, 419, 443, 467, 491, 515, 539, 563, 587, 611, 635, 659, 683, 707 и 731, или существенно аналогичную последовательность с гомологией не менее 90%, не менее 95%, не менее 98% или не менее 99%; домен LCDR2, кодируемый нуклеотидной последовательностью, выбираемой из группы, включающей SEQ ID №: 13, 37, 61, 85, 109, 133, 157, 181, 205, 229, 253, 277, 301, 325, 349, 373, 397, 421, 445, 469, 493, 517, 541, 565, 589, 613, 637, 661, 685, 709 и 733, или существенно аналогичную последовательность с гомологией не менее 90%, не менее 95%, не менее 98% или не менее 99%. В одном осуществлении последовательности CDR тяжелой и легкой цепей кодируются последовательностями нуклеиновой кислоты SEQ ID №: 51, 53, 55, 59, 61, 63; 75, 77, 79, 83, 85, 87; 123, 125, 127, 131, 133, 135; 219, 221, 223, 227, 229, 231; 243, 245, 247, 251, 253, 255; и 315, 317, 319, 323, 325, 327. В более конкретных осуществлениях последовательности CDR тяжелой и легкой цепей кодируются последовательностями нуклеиновой кислоты SEQ ID №: 75, 77, 79, 83, 85, 87; и 219, 221, 223, 227, 229, 231.
В четвертом аспекте настоящего изобретения приводится изолированное антитело или антигенсвязывающий фрагмент антитела, которые специфическим образом связывают hPCSK9, содержащий HCDR3 и LCDR3, где HCDR3 содержит аминокислотную последовательность формулы X1-X2-X3-X4-X5-X6-X7-X8-X9-X10-X11-X12-X13-X14-X15-X16-X17-X18-X19-X20 (SEQ ID №: 747), где X1 - Ala, X2 - Arg или Lys, X3 - Asp, X4 - Ser или Ile, X5 - Asn или Val, X6 - Leu или Trp, X7 - Gly или Met, X8 - Asn или Val, X9 - Phe или Tyr, X10 - Asp, X11 - Leu или Met, X12 - Asp или отсутствует, X13 - Tyr или отсутствует, X14 - Tyr или отсутствует, X15 - Tyr или отсутствует, X16 - Tyr или отсутствует, X17 - Gly или отсутствует, X18 - Met или отсутствует, X19 - Asp или отсутствует и X20 - Val или отсутствует; и LCDR3 содержит аминокислотную последовательность формулы X1-X2-X3-X4-X5-X6-X7-X8-X9 (SEQ ID №: 750), где X1 - Gln или Met, X2 - Gln, X3 - Tyr или Thr, X4 - Tyr или Leu, X5 - Thr или Gln, X6 - Thr, X7 - Pro, X8 - Tyr или Leu и X9 - Thr.
В еще одном осуществлении антитело или его фрагмент дополнительно содержит последовательность HCDR1 формулы X1-X2-X3-X4-X5-X6-X7-X8 (SEQ ID №: 745), где X1 - Gly, X2 - Phe, X3 - Thr, X4 - Phe, X5 - Ser или Asn, X6 - Ser или Asn, X7 - Tyr или H- и X8 - Ala или Trp; последовательность HCDR2 формулы X1-X2-X3-X4-X5-X6-X7-X8 (SEQ ID №: 746), где X1 - Ile, X2 - Ser или Asn, X3 - Gly или Gln, X4 - Asp или Ser, X5 - Gly, X6 - Ser или Gly, X7 - Thr или Glu и X8 - Thr или Lys; последовательность LCDR1 формулы X1-X2-X3-X4-X5-X6-X7-X8-X9-X10-X11-X12 (SEQ ID №: 748), где X1 - Gln, X2 - Ser, X3 - Val или Leu, X4 - Leu, X5 - H- или Tyr, X6 - Arg или Ser, X7 - Ser или Asn, X8 - Asn или Gly, X9 - Asn, X10 - Arg или Asn, X11 - Asn или Tyr и X12 - Phe или отсутствует; последовательность LCDR2 формулы X1-X2-X3 (SEQ ID №: 749), где X1 - Trp или Leu, X2 - Ala или Gly и X3 - Ser. На фиг.1 приводится совмещение последовательностей вариабельных участков тяжелой и легкой цепи для 316P и 300N mAb.
В пятом аспекте настоящего изобретения приводится антитело анти-PCSK9 человека или антигенсвязывающий фрагмент антитела, содержащие вариабельную область тяжелой цепи (HCVR), кодируемую сегментами нуклеотидной последовательности, полученными из последовательностей зародышевых линий VH, DH и JH, и вариабельную область легкой цепи (LCVR), кодируемую сегментами нуклеотидной последовательности, полученными из последовательностей зародышевых линий VK и JK, где зародышевыми линиями являются генный сегмент VH 3-23, генный сегмент DH 7-27, генный сегмент JH 2, генный сегмент VK 4-1 и генный сегмент JK 2; или (b) генный сегмент VH 3-7, генный сегмент DH 2-8, генный сегмент JH 6, генный сегмент VK 2-28 и генный сегмент JK 4.
В шестом аспекте настоящего изобретения приводится антитело или его антигенсвязывающий фрагмент, которые связываются с белком PCSK9 SEQ ID №: 755, где связывание антитела или его фрагмента с вариантом белка PCSK9 составляет меньше 50% связи между антителом или его фрагментом с белком PCSK9 SEQ ID №: 755. В конкретном осуществлении антитело или его фрагмент связываются с вариантом белка PCSK9, имеющим аффинность связывания (KD) менее 50%, менее 60%, менее 70%, менее 80%, менее 90% или менее 95%, по сравнению со связыванием с PCSK9 (SEQ ID №: 755).
В одном осуществлении вариант белка PCSK9 содержит не менее одной мутации в позиции 238 SEQ ID №: 755. В более конкретном осуществлении мутацией является D238R. В одном осуществлении аффинность связывания антитела или фрагмента антитела для варианта белка PCSK9 не менее чем на 90% меньше по сравнению с нативным белком SEQ ID №: 755, где вариант белка содержит мутацию в остатке 238. В одном осуществлении аффинность связывания антитела или фрагмента антитела для варианта белка PCSK9 не менее чем на 80% меньше по сравнению с нативным белком последовательности SEQ ID №: 755, где вариант белка содержит мутацию одного или более остатков 153, 159, 238 и 343. В более конкретном осуществлении мутацией является один из S153R, E159R, D238R и D343R.
В одном осуществлении вариант белка PCSK9 содержит не менее одной мутации в позиции 366 SEQ ID №: 755. В более конкретном осуществлении мутацией является E366K. В одном осуществлении аффинность связывания антитела или фрагмента антитела для варианта белка PCSK9 не менее чем на 95% меньше по сравнению с нативным белком последовательности SEQ ID №: 755, где вариант белка содержит мутацию в остатке 366. В одном осуществлении аффинность связывания антитела или фрагмента антитела для варианта белка PCSK9 не менее чем на 70%, 80% или 90% меньше по сравнению с нативным белком последовательности SEQ ID №: 755, где вариант белка содержит мутацию одного или более остатков 147, 366 и/или 380. В более конкретном осуществлении мутацией является один из S147F, E366K и V380M.
Настоящее изобретение включает антитела анти-PCSK9 с модифицированной структурой гликозилирования. В некоторых приложениях может оказаться полезным удалить нежелательные сайты гликозилирования, например, удалить фукозный фрагмент для усиления функции антителозависимой клеточно-обусловленной цитотоксичности (ADCC) (см. Shield et al. (2002) JBC 277:26733). В других приложениях может осуществляться модификация галактозилирования, с тем чтобы изменить комплементзависимую цитотоксичность (CDC).
В седьмом аспекте настоящего изобретения приводится фармацевтический состав, включающий рекомбинантное антитело человека или его фрагмент, которое специфически связывает hPCSK9 и фармацевтически приемлемый носитель. В одном осуществлении настоящего изобретения приводится состав, представляющий собой сочетание антитела или антигенсвязывающего фрагмента антитела настоящего изобретения, и второй терапевтический агент. Вторым терапевтическим агентом может быть любой агент, который с положительным эффектом сочетается с антителом или его фрагментом настоящего изобретения, например, агент, который в состоянии вызвать нарушение синтеза холестерина на клеточном уровне посредством ингибирования 3-гидрокси-3-метилглутарил (HMG)-коэнзим A (CoA) редуктазы, например, из числа таких, как церивастатин, аторвастатин, симвастатин, питавастатин, розувастатин, флувастатин, ловастатин, правастатин и пр.; который в состоянии ингибировать захват холестерина и/или реабсорбции желчных кислот; в состоянии повышать катаболизм липопротеинов (например, ниацина); и/или активаторы фактора транскрипции LXR, который играет роль в удалении холестерина, например, 22-гидроксихолестерина.
В восьмом аспекте настоящего изобретения приводятся способы ингибирования активности hPCSK9 с помощью антитела анти-PCSK9 или антиген-связывающей области антитела настоящего изобретения, где терапевтические методы предусматривают введение терапевтически эффективного количества фармацевтического состава, содержащего антитело или антиген-связывающий фрагмент антитела настоящего изобретения. Подлежащим лечению нарушением является любое заболевание или состояние, которое улучшается, облегчается, подавляется или предупреждается за счет устранения, ингибирования или снижения активности PCSK9. Конкретные группы населения, которые могут проходить лечение с использованием терапевтических методов настоящего изобретения, включают пациентов, которым показан аферез ЛНП, пациентов с мутациями, активирующими PCSK9 (мутаций с усилением функций, в дальнейшем «GOF»), пациентов с гетерозиготной наследственной гиперхолестеринемией (heFH); пациентов с первичной гиперхолестеринемией, которые не переносят статины или неконтролируемы статинами; а также пациенты с риском развития гиперхолестеринемии, которые могут получать профилактическое лечение. К другим показаниям относятся дислипидемия, связанная с вторичными причинами, например, сахарный диабет II-го типа, холестатические заболевания печени (первичный билиарный цирроз), нефротический синдром, гипотироидизм, ожирение; а также профилактика и лечение атеросклероза и сердечно-сосудистых заболеваний.
В конкретных осуществлениях способа настоящего изобретения анти-hPCSK9 антитело или фрагмент антитела настоящего изобретения используются для снижения повышенного уровня общего холестерина, не-ЛВП холестерина, ЛНП холестерина и/или аполипопротеина B (аполипопротеина B100).
Антитело или антигенсвязывающий фрагмент настоящего изобретения могут использоваться индивидуально или в сочетании со вторым агентом, например, ингибитором HMG-CoA редуктаз и/или другими лекарствами, снижающими уровень липидов.
Дополнительные осуществления предусматривают использование описанного выше антитела или антигенсвязывающего фрагмента антитела для смягчения или ингибирования заболевания или состояния, опосредованного PCSK9.
Настоящее изобретение предусматривает использование антитела или антигенсвязывающего фрагмента антитела в соответствии с приведенным выше описанием при производстве лекарственных препаратов, применяемых для смягчения или ингибирования заболевания или состояния, опосредованного PCSK9. В конкретных осуществлениях, при которых опосредованным PCSK9 заболеванием или состоянием является гиперхолестеринемия, гиперлипидемия, аферез ЛВП, гетерозиготная наследственная гиперхолестеринемия, непереносимость статинов, неконтролируемость статинами, риск развития гиперхолестеринемии, дислипидемия, холестатические заболевания печени, нефротический синдром, гипотироидизм, ожирение, атеросклероз и сердечно-сосудистые заболевания.
Другие осуществления станут очевидными при ознакомлении с приведенным ниже подробным описанием.
КРАТКОЕ ОПИСАНИЕ ФИГУР
Фиг.1. Таблицы сравнения последовательностей вариабельных участков тяжелой цепи (A) и легкой цепи (B) и CDR антител H1H316P и H1M300N.
Фиг.2. Концентрация антител в сыворотке во времени. 316P 5 мг/кг (□); 300N 5 мг/кг (σ); 316P 15 мг/кг (ν); 300N 15 мг/кг (●).
Фиг.3. Уровень общего сывороточного холестерина в процентах изменения по сравнению с контролем по буферу. Контроль (Т); 316P 5 мг/кг (ν); 300N 5 мг/кг (σ); 316P 15 мг/кг (□); 300N 15 мг/кг (Δ).
Фиг.4. Уровень сывороточного ЛНП холестерина в процентах изменения по сравнению с контролем по буферу. Контроль (Т); 316P 5 мг/кг (ν); 300N 5 мг/кг (σ); 316P 15 мг/кг (□); 300N 15 мг/кг (Δ).
Фиг.5. Уровень сывороточного ЛНП холестерина, нормализованный по контрольному буферу. Контроль по буферу (Т); 316P 5 мг/кг (ν); 300N 5 мг/кг (σ); 316P 15 мг/кг (□); 300N 15 мг/кг (Δ).
Фиг.6. Уровень сывороточного ЛВП холестерина в процентах изменения по сравнению с контролем по буферу. Контроль (Т); 316P 5 мг/кг (ν); 300N 5 мг/кг (σ); 316P 15 мг/кг (□); 300N 15 мг/кг (Δ).
Фиг.7. Уровень сывороточного триглицерида в процентах изменения по сравнению с контролем по буферу. Контроль по буферу (Т); 316P 5 мг/кг (ν); 300N 5 мг/кг (σ); 316P 15 мг/кг (□); 300N 15 мг/кг (Δ).
Фиг.8. Уровень сывороточного ЛНП холестерина в процентах изменения по сравнению с исходным после разового подкожного введения. 316P 5 мг/кг (ν); 300N 5 мг/кг (●).
Фиг.9. Концентрация антител в сыворотке во времени после разового подкожного введения. 316P 5 мг/кг (●); 300N 5 мг/кг (σ).
Фиг.10. Вестерн-блот для рецептора ЛНП мышей в суммарных гомогенатах печени. Образцы были взяты через 24 часа после введения ФСБ (полоски 1-3), 5 мг/кг 316P (полоски 4-6) или 5 мг/кг неспецифических hPCSK9 mAb (полоски 7-8) и 4 часа после введения 1,2 мг/кг hPCSK9-mmh (все полоски).
Фиг.11. Воздействие 316P на уровень сывороточного ЛНП холестерина у мышей PCSK9
hu/hu. Контроль по буферу ( ( ); 316P 1 мг/кг ( ); 316P 5 мг/кг (
); 316P 5 мг/кг ( ); 316P 10 мг/кг (
); 316P 10 мг/кг ( ).
).
Фиг.12. Сывороточный фармакокинетический профиль анти-hPCSK9 mAb у мышей C57BL/6. Разовая доза контроля I mAb (λ) при 10 мг/кг; 316P (σ) при 10 мг/кг и 300N (ν) при 10 мг/кг.
Фиг.13. Сывороточный фармакокинетический профиль анти-hPCSK9 mAb у гетерозиготных мышей hPCSK9. Разовая доза 10 мг/кг: Контроль I mAb (λ); 316P (σ) и 300N (ν).
Фиг.14. Воздействие 316P на уровень сывороточного ЛНП холестерина у сирийских хомяков, получавших нормальное питание. Контроль по буферу (●); 316P 1 мг/кг (ν); 316P 3 мг/кг (σ); 316P 5 мг/кг (τ).
ПОЛНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Прежде чем приступить к описанию представляемого способа, необходимо отметить, что настоящее изобретение не ограничивается конкретными способами и изложенными экспериментальными условиями, поскольку такие способы и условия могут меняться. Следует также понимать, что используемая в настоящем документе терминология предназначена исключительно для описания конкретных осуществлений и не носит ограничительного характера, поскольку охват настоящего изобретения ограничивается только прилагаемой формулой изобретения.
Если не указано иное, все технические и научные термины, используемые в настоящем документе, имеют такое же значение, которое общеизвестно рядовым специалистам в области, к которой относится настоящее изобретение. Хотя на практике или при проверке настоящего изобретения могут использоваться любые способы и материалы, аналогичные или идентичные описанным в настоящем документе способам и материалам, ниже приводится описание предпочтительных способов и материалов.
Определения
Термин «человеческая пропротеинконвертаза субтилизин/кексин тип 9», или «hPCSK9», используемый в настоящем документе, означает hPCSK9 с последовательностью нуклеиновой кислоты, показанной в SEQ ID №: 754, и аминокислотную последовательность SEQ ID №: 755, или его биологически активный фрагмент.
Используемый в настоящем документе термин «антитело» предназначен для обозначения молекул иммуноглобулина, составленных из четырех полипептидных цепей, при этом две тяжелые (Н) цепи и две легкие (L) цепи связываются друг с другом дисульфидными связями. Каждая тяжелая цепь содержит вариабельную область тяжелой цепи («HCVR», или «VH») и константную область тяжелой цепи (содержащую домены CH1, CH2 and CH3). Каждая легкая цепь содержит вариабельную область легкой цепи («LCVR», или «VL») и константную область легкой цепи. Области VH и VL могут подразделяться на области гипервариабельности, которые называются определяющими комплементарность областями (CDR), перемежающимися с областями с более высоким уровнем консервативности, называемые остовными областями (FR). Каждая область VH и VL образована тремя CDR и четырьмя FR, расположенными от амино-терминального конца к карбокси-терминальному концу в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4.
Также возможно замещение одного или нескольких остатков CDR или пропуск одной или нескольких CDR. В научной литературе описаны антитела, в которых для связывания можно обойтись без одной или двух CDR. В работе Padlan et al. (1995 FASEB J. 9:133-139) анализировались контактные области между антителами и их антигенами на основании опубликованных кристаллических структур, и был сделан вывод о том, что только примерно треть остатков CDR на самом деле вступает в контакт с антигеном. В этой работе также обнаружено множество антител, в которых одна или две CDR не содержат аминокислот, контактирующих с антигеном (см. также, Vajdos et al. 2002 J Mol Biol 320:415-428).
Остатки CDR, не контактирующие с антигеном, можно определить на основании предыдущих исследований (например, остатки H60-H65 в CDRH2 часто не требуются), по областям CDR Кабата, лежащих вне CDR Чотиа, с помощью молекулярного моделирования и/или эмпирическим путем. Если CDR или его остатки пропущены, они обычно замещаются аминокислотами, занимающими аналогичное положение в другой последовательности человеческого антитела, или консенсусе таких последовательностей. Положения для замещения CDR и аминокислотами могут также выбираться эмпирически. Эмпирические замещения могут быть консервативными или неконсервативными.
Используемый в настоящем документе термин «антитело человека» предназначен для обозначения антител с вариабельной и константной областями, полученных из иммуноглобулиновых последовательностей зародышевых линий человека. Описываемые в данном изобретении моноклональные антитела (mAb) могут включать аминокислотные остатки, не кодируемые иммуноглобулиновыми последовательностями зародышевых линий человека (например, мутации, вызванные случайным или сайт-специфическим мутагенезом in vitro или соматическими мутациями in vivo), например, в областях CDR, особенно в области CDR3. Однако используемый в настоящем документе термин «антитело человека» не подразумевает включения mAb, в которых на базовые последовательности человека привиты CDR последовательности, полученные из зародышевых линий другого вида млекопитающих, например, мыши.
Термин «специфически связываются» или ему подобные означает, что антитело или его антигенсвязывающий фрагмент образует комплекс с антигеном, который сравнительно стабилен в физиологических условиях. Специфическое связывание может характеризоваться равновесной константой диссоциации не менее примерно 1×10-6 M и менее (то есть меньшая KD обозначает более прочное связывание). Методы определения специфического связывания молекул известны специалистам в области и включают, например, равновесный диализ, поверхностный плазмонный резонанс и пр. Изолированное антитело, которое специфическим образом связывает hPCSK9, тем не менее, может проявлять перекрестную реактивность к другим антигенам, например, молекулам PCSK9 из других видов. Кроме того, мультиспецифические антитела (например, биспецифические), которые связываются с hPCSK9 и одним или несколькими дополнительными антигенами, тем не менее, рассматриваются как антитела, которые «специфически связывают» hPCSK9 в соответствии с терминологией настоящего документа.
Используемый в настоящем документе термин антитело «высокой аффинности» относится к mAb, имеющим аффинность связывания с hPCSK9 не менее 10-10 M; предпочтительно 10-11 M; еще более предпочтительно 10-12 M, по результатам измерения методом поверхностного плазмонного резонанса, например, BIACORE™, или результатам измерения аффинности в растворе методом иммуноферментного анализа (ELISA).
Под используемым в настоящем документе термином “медленно диссоциирующее”, “Koff” или “kd” подразумевается антитело, комплекс которого с hPCSK9 диссоциирует с константой скорости 1×10-3 с-1 или ниже, предпочтительно 1×10-4 с-1 или ниже, по результатам измерения методом поверхностного плазмонного резонанса, например, BIACORE™.
Используемый в настоящем документе термин «антигенсвязывающая область» антитела (или просто «фрагмент антитела») обозначает один или несколько фрагментов антитела, которые сохраняют способность к специфическому связыванию с hPCSK9. Фрагмент антитела может включать фрагмент Fab, фрагмент F(ab')2, фрагмент Fv, фрагмент dAb, фрагмент, содержащий CDR или изолированную CDR.
Конкретные осуществления, антитело или фрагменты антитела настоящего изобретения могут конъюгироваться с терапевтическим агентом («иммуноконъюгат»), например, цитотоксином, химиотерапевтическим препаратом, иммунодепрессантом или радиоактивным изотопом.
Используемый в настоящем документе термин "изолированное антитело" предназначен для обозначения антитела, существенно свободного от других mAb, обладающих иной антигенной специфичностью (например, изолированное антитело, которое специфическим образом связывает hPCSK9, существенно свободно от mAb, которые специфическим образом связывают антигены, отличные от hPCSK9). Изолированное антитело, которое специфическим образом связывает hPCSK9, тем не менее, может проявлять перекрестную реактивность к другим антигенам, например, молекулам PCSK9 из других видов.
Используемый в настоящем документе термин «нейтрализующее антитело» (или «антитело, нейтрализующее активность PCSK9») предназначен для обозначения антитела, связывание которого с PCSK9 приводит к ингибированию как минимум одной биологической активности PCSK9. Данное ингибирование биологической активности PCSK9 может быть оценено путем измерения одного или более показателей биологической активности PCSK9 при помощи одного или нескольких стандартных методов анализа in vitro или in vivo, известных специалистам (см. примеры ниже).
Используемый в настоящем документе термин «поверхностный плазмонный резонанс» относится к оптическому явлению, которое позволяет проводить анализ биоспецифических взаимодействий в реальном времени за счет детектирования изменений концентраций белка в биосенсорной матрице, например, с помощью системы BIACORE™ (Pharmacia Biosensor AB, Uppsala, Sweden and Piscataway, N.J.).
Используемый в настоящем документе термин «KD» предназначен для обозначения равновесной константы диссоциации конкретного взаимодействия антитело-антиген.
Термин «эпитоп» обозначает область антигена, в которой происходит связывание с антителом. Эпитопы могут быть структурными или функциональными. Функциональные эпитопы обычно представляют собой подмножество структурных эпитопов и содержат такие остатки, которые непосредственно способствуют аффинности взаимодействия. Эпитопы также могут быть конформационными, то есть состоящими из разветвленных аминокислот. В ряде осуществлений эпитопы могут включать детерминанты, представляющие собой на химически активные поверхностные группировки молекул, такие как аминокислоты, боковые цепи сахаров, фосфорильные группы или сульфонильные группы, и в ряде осуществлений могут иметь специфические трехмерные структурные характеристики и/или специфические зарядовые характеристики.
Термин «существенная идентичность» или «по существу идентичны» в отношении нуклеиновой кислоты или ее фрагменту означает, что при оптимальном выравнивании вставок и делеций соответствующих нуклеотидов нуклеиновых кислот (или их комплементарных цепей) наблюдается идентичность нуклеотидных последовательностей не менее примерно 90% и, более предпочтительно, не менее 95%, 96%, 97%, 98% или 99% оснований нуклеотидов, что измеряется с помощью любого известного алгоритма идентичности последовательностей, например, FASTA, BLAST или GAP, которые обсуждаются ниже.
Применяемый в отношении полипептидов термин «существенное сходство» или «по существу подобные» означает, что две пептидные последовательности при их оптимальном выравнивании, например, с помощью программ GAP или BESTFIT с учетом веса пропусков по умолчанию демонстрируют идентичность последовательностей не менее 90%, и еще более предпочтительно, не менее 95%, 98% или 99%. Предпочтительно положение неидентичных остатков отличается консервативным замещением аминокислот. «Консервативное замещение аминокислот» - это такое замещение, при котором один аминокислотный остаток замещается другим аминокислотным остатком, имеющим боковую цепь (группу R) с аналогичными химическими свойствами (например, заряд или гидрофобность). В общем случае консервативное замещение аминокислот не будет приводить к существенным изменениям функциональных свойств белка. В случае если две или более аминокислотные последовательности отличаются друг от друга консервативными замещениями, процент или степень аналогичности может корректироваться в сторону увеличения, с тем чтобы учесть консервативный характер замещения. Способы такой корректировки хорошо известны специалистам в данной области. См. например, Pearson (1994) Methods Mol. Biol. 24: 307-331. К примерам групп аминокислот, имеющих боковые цепи с аналогичными химическими свойствами, относятся 1) алифатические боковые цепи: глицин, аланин, валин, лейцин и изолейцин; 2) алифатические гидроксилированные боковые цепи: серин и треонин; 3) боковые цепи с амидной группой: аспарагин и глутамин; 4) ароматические боковые цепи: фенилаланин, тирозин и триптофан; 5) боковые цепи со свойствами основания: лизин, аргинин и гистидин; 6) боковые цепи со свойствами кислоты: аспартат и глутамат; и 7) серосодержащие боковые цепи: цистеин и метионин. Предпочтительными группами для консервативного замещения аминокислот являются: валин-лейцин-изолейцин, фенилаланин-тирозин, лизин-аргинин, аланин-валин, глутамат-аспартат и аспарагин-глутамин. В альтернативном варианте консервативное замещение представляет собой любое изменение, не имеющее отрицательное значение в логарифмической матрице вероятностей PAM250, описанной в работе Gonnet et al. (1992) Science 256: 1443 45. «Умеренно консервативным» замещением называется любое изменение, приводящее к неотрицательному значению в логарифмической матрице правдоподобия PAM250.
Подобие последовательностей полипептидов обычно определяют с помощью программного обеспечения для анализа последовательности. Программа для анализа белков сопоставляет подобные последовательности с использованием показателей аналогичности, задаваемых для различных замещений, делеций и других модификаций, в том числе для консервативного замещения аминокислот. Например, программное обеспечение GCG содержит такие программы как GAP и BESTFIT, которые могут использоваться с параметрами по умолчанию для определения гомологии или идентичности последовательности между близкородственными полипептидами, например, гомологичными полипептидами различных видов организмов или между исходным белком и его мутантом. См., например, GCG Вер. 6.1. Полипептидные последовательности могут также сопоставляться с помощью FASTA - программы, включенной в GCG Вер. 6.1, - с использованием параметров по умолчанию или рекомендуемых параметров. FASTA (например, FASTA2 и FASTA3) обеспечивает выравнивание и определяет процент идентичности последовательностей в областях с наибольшим перекрыванием между заданной и исследуемой последовательностями (см. выше Pearson (2000)). Другим предпочтительным алгоритмом сопоставления последовательности настоящего изобретения с базой данных, содержащей большое число последовательностей различных организмов, является компьютерная программа BLAST, особенно BLASTP или TBLASTN, которая использует параметры по умолчанию. См., например, Altschul et al. (1990) J. Mol. Biol. 215: 403 410 и Altschul et al. (1997) Nucleic Acids Res. 25:3389 402.
В конкретных осуществлениях антитело или фрагмент антитела, применяемый в способе настоящего изобретения может быть моноспецифическим, биспецифическим или мультиспецифическим. Мультиспецифические антитела могут быть специфичны по отношению к различным эпитопам одного целевого полипептида или могут содержать антиген-связывающие домены, специфические по отношению к эпитопам нескольких целевых полипептидов. Примером формата приготовления биспецифического антитела, которое может использоваться в контексте настоящего изобретения, может быть использование первого домена иммуноглобулина (Ig) CH3 и второго домена Ig CH3, где первый и второй домены Ig CH3 отличаются друг от друга не менее чем одной аминокислотой и где такое различие не менее чем на одну аминокислоту уменьшает связывание биспецифического антитела с белком A по сравнению с биспецифическим антителом, в котором такое аминокислотное различие отсутствует. В одном из осуществлений первый домен Ig CH3 связывается с белком A, а второй домен содержит мутацию, которая уменьшает или блокирует связывание белка А, например, модификацию H95R (по номенклатуре экзонов IMGT; H435R по номенклатуре ЕС). Второй CH3 может также содержать модификацию Y96F (по IMGT; Y436F по ЕС). Во втором модуле CH3 могут присутствовать дополнительные модификации: D16E, L18M, N44S, K52N, V57M и V82I (по IMGT; D356E, L358M, N384S, K392N, V397M и V422I по ЕС) в случае IgG1 mAb; N44S, K52N и V82I (IMGT; N384S, K392N и V422I по ЕС) в случае IgG2 mAb; и Q15R, N44S, K52N, V57M, R69K, E79Q и V82I (по IMGT; Q355R, N384S, K392N, V397M, R409K, E419Q и V422I по ЕС) в случае IgG4 mAb. Вариации по формату биспецифических антител, описанные выше, относятся к сфере охвата настоящего изобретения.
Определение «терапевтически эффективное количество» означает количество, которое оказывает желаемый эффект воздействия, для достижения которого оно вводится. Точное количество будет зависеть от целей лечения и может оцениваться специалистом в области на основе известных методик (см., например, Lloyd (1999) The Art, Science and Technology of Pharmaceutical Compounding).
Получение антител человека
Методы генерирования человеческих антител в трансгенных мышах общеизвестны (смотрите, например, US 6596541, Regeneron Pharmaceuticals, VELOCIMMUNE™). Технология VELOCIMMUNE™ предполагает получение трансгенных мышей с геномом, содержащим вариабельные области тяжелой и легкой цепи человека, которые функционально связаны с эндогенными локусами константной области мыши, так что в ответ на антигенную стимуляцию мышь продуцирует антитело, содержащее вариабельную область человека и константную область мыши. ДНК, кодирующая вариабельные области тяжелой и легкой цепи антитела, изолируется и функционально связывается с ДНК, кодирующей константные тяжелые и легкие цепи человека. Затем ДНК экспрессируется в клетке, которая в состоянии экспрессировать полное антитело человека. В конкретном осуществлении такой клеткой является клетка СНО.
Антитела могут использоваться в терапевтических целях для блокирования лиганд-рецепторного взаимодействия или ингибирования рецепторной компоненты взаимодействия вместо уничтожения клеток путем фиксации комплемента и участия в комплементзависимой цитотоксичности (CDC) или уничтожения клеток за счет антителозависимой клеточно-обусловленной цитотоксичности (ADCC). Константная область антитела, таким образом, важна для обеспечения способности антитела фиксировать комплемент и опосредовать клеточно-обусловленную цитотоксичность. Поэтому изотип антитела можно выбирать в зависимости от того, желательно ли, чтобы антитело опосредовало цитотоксичность.
Антитела человека могут существовать в двух формах, которые связаны с гетерогенностью шарнирной области. В одной из форм молекула антитела содержит стабильную четырехцепочечную конструкцию с весом примерно 150-160 кДа, в которой димеры удерживаются связывающим тяжелые цепи дисульфидным мостиком. Во второй форме димеры не связаны межцепочечными дисульфидными связями, и образуется молекула с приблизительным весом 75-80 кДА, включающая ковалентно сочлененные легкую и тяжелые цепи (половина антитела). Эти формы было исключительно сложно разделить, даже после аффинной очистки.
Частота проявлений второй формы в различных изотипах интактного IgG вызвана, кроме прочего, структурными различиями, связанными с изотипом шарнирной области антитела. Замена одной аминокислоты в шарнирной области человеческого IgG4 может существенно снизить долю второй формы (Angal et al. 1993 Molecular Immunology 30:105) до уровней, обычно характерных при использовании шарнирной области человеческого IgG1. В сферу охвата настоящего изобретения входят антитела, имеющие одну или несколько мутаций в шарнирной области, областях CH2 или CH3, которые могут быть желательны, например, при продуцировании антител для повышения выхода нужной формы антитела.
Обычно мышь VELOCIMMUNE™ стимулируется представляющим интерес антигеном, и у мыши, экспрессирующей антитела, берутся лимфатические клетки (например, В-клетки). Лимфатические клетки могут сливаться с линией клеток миеломы для получения иммортализованных линий клеток гибридомы, и такие линии клеток гибридомы проходят скрининг и селекцию для идентификации тех линий клеток гибридомы, которые продуцируют антитела к представляющему интерес антигену. ДНК, кодирующая вариабельные области тяжелой и легкой цепи антитела, можно изолировать и связывать с нужными изотипическими константными областями тяжелой и легкой цепей. Такой белок антитела можно продуцировать в клетке, например, в клетке СНО. В альтернативном варианте ДНК, кодирующая антигенспецифические химерные антитела или вариабельные домены легкой и тяжелой цепей, можно изолировать непосредственно из антигенспецифических лимфоцитов.
Первоначально изолировали химерные антитела с высокой аффинностью, имеющие вариабельную область человека и константную область мыши. Как описано ниже, антитела характеризуются и выбираются по нужным свойствам, в том числе по аффинности, селективности, эпитопу и т.п. Константные области мыши заменяются желаемыми константными областями человека, с тем чтобы получить полные антитела человека, описанные в настоящем изобретении, например, немутантный или модифицированный IgG1 или IgG4 (например, SEQ ID №: 751, 752, 753). В то время как выбранная константная область может различаться в зависимости от конкретного осуществления, свойства высокой аффинности антиген-связывания и необходимая специфичность определяются вариабельной областью.
Эпитопное картирование и связанные с ним технологии
Для скрининга антител, которые связываются с конкретным эпитопом (например, антител, блокирующих связывание IgE с соответствующим рецептором, обладающим высокой аффинностью), можно проводить стандартный кросс-блокинг, подобно описанному в Antibodies, Harlow and Lane (Cold Spring Harbor Press, Cold Spring Harb., NY). К другим методам относятся мутанты сканирования аланина, пептидный блоттинг (Reineke (2004) Methods Mol Biol 248:443-63), и анализ расщепления пептидов. Кроме того, могут использоваться такие методы, как вырезание эпитопа, экстракция эпитопа и химическая модификация антигенов (Tomer (2000) Protein Science 9: 487-496).
Используемый в настоящем документе термин «эпитоп» относится к сайту антигена, на который реагируют B и/или T клетки. Эпитопы B-клеток могут быть образованы как непрерывной последовательностью аминокислот, так и разрозненными аминокислотами, оказавшимися рядом в результате фолдинга белка в третичную структуру. Эпитопы, образованные непрерывной последовательностью аминокислот, как правило, сохраняются при воздействии денатурирующих растворителей, тогда как эпитопы, возникшие в результате фолдинга белка в третичную структуру, разрушаются при обработке денатурирующими растворителями. Эпитоп, как правило, формируется не менее чем тремя, а обычно не менее чем пятью или 8-10 аминокислотами во вполне конкретной пространственной конформации.
Определение профиля с помощью модификации (MAP), также известное как определение профиля антител на основе структуры антигена (ASAP) представляет собой метод классификации большого числа моноклональных антител (mAb) к одному и тому же антигену в соответствии со сходствами профиля связывания каждого антитела с химически или энзиматически модифицированными антигенными поверхностями (US 2004/0101920). Каждая категория может отражать уникальный эпитоп, который либо четко отличается от эпитопа, представленного в любой другой категории, либо частично перекрывается с ним. Подобная технология позволяет быстро отделять генетически идентичные mAb и, таким образом, сосредоточиться на идентификации генетически отличающихся mAb. В случае применения для скрининга гибридомы, MAP может способствовать идентификации редких клонов гибридомы, производящих mAb с нужными характеристиками. MAP может использоваться для сортировки mAb анти-PCSK9 настоящего изобретения в группы mAb, связывающих различные эпитопы.
В различных осуществлениях антитело hPCSK9 или антиген-связывающий фрагмент антитела связывает эпитоп с каталитическим доменом, который равен примерно 153 по 425 SEQ ID №: 755); более конкретно эпитоп от примерно 153 до примерно 250 или от примерно 250 до примерно 425; более конкретно антитело или фрагмент антитела настоящего изобретения связывает эпитоп в фрагменте с примерно 153 до примерно 208, с примерно 200 до примерно 260, с примерно 250 до примерно 300, с примерно 275 до примерно 325, с примерно 300 до примерно 360, с примерно 350 до примерно 400, и/или с примерно 375 до примерно 425.
В различных осуществлениях антитело анти-hPCSK9 или антиген-связывающий фрагмент антитела связывает эпитоп с доменом пропептида (остатки 31 - по 152 SEQ ID №: 755); более конкретно, эпитоп от примерно остатка 31 до примерно остатка 90 или от остатка примерно 90 до примерно остатка 152; более конкретно, антитело или фрагмент антитела настоящего изобретения связывает эпитоп в фрагменте с примерно 31 до примерно 60, с примерно 60 до примерно 90, с примерно 85 до примерно 110, с примерно 100 до примерно 130, с примерно 125 до примерно 150, с примерно 135 до примерно 152, и/или с примерно 140 до примерно 152.
В некоторых осуществлениях антитело анти-hPCSK9 или антиген-связывающий фрагмент антитела связывает эпитоп в С-терминальном домене (остатки 426 - по 692 SEQ ID №: 755); более конкретно, эпитоп от примерно остатка 426 до примерно остатка 570 или от остатка примерно 570 до примерно остатка 692; более конкретно, антитело или фрагмент антитела настоящего изобретения связывает эпитоп в фрагменте с примерно 450 до примерно 500, с примерно 500 до примерно 550, с примерно остатка 550 до примерно 600, и/или с примерно 600 до примерно 692.
В некоторых осуществлениях антитело или фрагменты антитела связываются с эпитопом, который содержит более одного из перечисленных эпитопов в каталитическом, пропептидном или С-терминальном домене, и/или в пределах двух или трех различных доменов (например, эпитопы в каталитическом и С-терминальном доменах или пропептидном и каталитическом доменах, или в пропептидном, каталитическом и С-терминальном доменах).
В некоторых осуществлениях антитело или его фрагмент связываются с эпитопом hPCSK9, содержащим аминокислотный остаток 238 hPCSK9 (SEQ ID №: 755). Экспериментальные результаты (таблица 27) показывают, что в случае мутации D238 KD mAb 316P демонстрировала >400-кратное снижение аффинности связывания (с ~1×10-9 M до ~410×10-9 M), а T1/2 снижалось >30-раз (с ~37 до ~1 минуты). В конкретном осуществлении использовалась мутация D238R. В конкретных осуществлениях антитело или его фрагмент связываются с эпитопом hPCSK9, содержащим один или несколько аминокислотных остатков 153, 159, 238 и 343.
Как показано ниже мутация аминокислотных остатков 153, 159 или 343 приводила к от 5- до 10-кратному снижению аффинности или аналогичному сокращению T1/2. В конкретных осуществлениях мутация была S153R, E159R и/или D343R.
В некоторых осуществлениях антитело или его фрагмент связываются с эпитопона hPCSK9, содержащим аминокислотный остаток 366 hPCSK9 (SEQ ID №: 755). Экспериментальные результаты (таблица 27) показывают, что в случае мутации Е366 аффинность mAb 300N демонстрировала примерно 50-кратное снижение (с ~0,7×10-9 M до ~36×10-9 M) при аналогичном снижении T1/2 (с ~120 до ~2 минут). В конкретном осуществлении использовалась мутация E366K.
Настоящее изобретение включает анти-PCSK9 антитела, которые связываются с тем же эпитопом, что и любые из конкретных примеров антител, описанных в настоящем документе. Точно также, настоящее изобретение включает анти-PCSK9 антитела, которые конкурируют за связывание с фрагментом PCSK9 или PCSK9 с любыми из конкретных примеров антител, описанных в настоящем документе.
Легко установить, связывается ли то или иное антитело с тем же эпитопом, что и контрольное анти-PCSK9 антитело, или конкурирует за связывание с ним, воспользовавшись стандартными методами, известными специалистам в области. Например, чтобы определить, связывается ли испытуемое антитело с тем же эпитопом, что и контрольное анти-PCSK9 антитело настоящего изобретения, контрольному антителу дают связаться с белком PCSK9 или пептидом в условиях насыщения. Затем оценивается способность испытуемого антитела связываться с молекулой PCSK9. Если испытуемое антитело в состоянии связываться с PCSK9 после связывания в условиях насыщения с контрольным анти-PCSK9 антителом, можно сделать вывод о том, что испытуемое антитело связывается с эпитопом, отличным от контрольного анти-PCSK9 антитела. С другой стороны, если испытуемое антитело не в состоянии связываться с молекулой PCSK9 после связывания в условиях насыщения с контрольным анти-PCSK9 антителом, тогда испытуемое антитело может связываться с тем же эпитопом, что и эпитоп, связывающийся с контрольным анти-PCSK9 антителом настоящего изобретения.
Чтобы определить, конкурирует ли антитело при связывании с контрольным анти-PCSK9 антителом, представленная выше методология связывания использовалась в двух вариантах: В первом случае контрольному антителу давали связываться с молекулой PCSK9 в условиях насыщения с последующей оценкой связывания контрольного антитела с молекулой PCSK9. Во втором случае испытуемому антителу давали связываться с молекулой PCSK9 в условиях насыщения с последующей оценкой связывания контрольного антитела с молекулой PCSK9. Если в обоих случаях только первое (насыщающее) антитело в состоянии связываться с молекулой PCSK9, то делается вывод о том, что испытуемое антитело и контрольное антитело конкурируют за связывание с PCSK9. Специалисту в области будет очевидно, что антитело, которое конкурирует за связывание с контрольным антителом, необязательно будет связываться с тем же эпитопом, что и контрольное антитело, но может стерически блокировать контрольное антитело посредством связывания с перекрывающимся или соседним эпитопом.
Два антитела связываются с одним и тем же или перекрывающимся эпитопом, если каждое конкурентно ингибирует (блокирует) связывание другого антитела с антигеном. То есть 1-, 5-, 10-, 20- или 100-кратный избыток одного антитела ингибирует связывание другого не менее чем на 50%, но предпочтительно, на 75%, 90% или даже 99% по результатам анализа конкурентного связывания (см., например, Junghans et al., Cancer Res. 1990 50: 1495-1502). В качестве альтернативы, два антитела имеют один и тот же эпитоп, если по существу все аминокислотные мутации в антигене, которые снижают или блокируют связывание одного антитела, также снижают или блокируют связывание другого. Два антитела имеют перекрывающиеся эпитопы, если некоторые аминокислотные мутации, которые снижают или блокируют связывание одного антитела, также снижают или блокируют связывание другого.
Затем можно провести дополнительные стандартные эксперименты (например, пептидную мутацию или анализ связывания), чтобы подтвердить, вызвано ли, на самом деле, отмеченное отсутствие связывания испытуемого антитела тем, что испытуемое антитело связалось с тем же самым эпитопом, что и контрольное антитело, или же отсутствие отмеченного связывания происходит по причине стерического блокирования (или иного явления). Эксперименты такого рода могут проводиться с использованием ELISA, RIA, поверхностного плазмонного резонанса, проточной цитометрии или любого другого количественного или качественного анализа связывания антител, доступного специалистам в области.
В конкретном осуществлении изобретение включает анти-PCSK9 антитело или антигенсвязывающий фрагмент антитела, которые связываются с белком PCSK9 последовательности SEQ ID №: 755, причем связывание между антителом или его фрагментом с PCSK9 и вариантом белка PCSK9 составляет менее 50% связывания между антителом или фрагментом и белком PCSK9 последовательности SEQ ID №: 755. В одном конкретном осуществлении вариант белка PCSK9 содержит не менее одной мутации остатка в позиции, выбираемой из группы, включающей 153, 159, 238 и 343. В более конкретном осуществлении одной мутацией является S153R, E159R, D238R и D343R. В другом конкретном осуществлении вариант белка PCSK9 содержит не менее одной мутации остатка в позиции, выбираемой из группы, включающей 366. В одном конкретном осуществлении вариант белка PCSK9 содержит не менее одной мутации остатка в позиции, выбираемой из группы, включающей 147, 366 и 380. В более конкретном осуществлении мутацией является один из S147F, E366K и/или V380M.
Иммуноконъюгаты
В сферу охвата настоящего изобретения входит анти-PCSK9 моноклональное антитело человека, конъюгированное с терапевтическим агентом («иммуноконъюгат»), например, цитотоксином, химиотерапевтический препарат, иммунодепрессант или радиоактивный изотоп. К цитотоксическим агентам относятся любые вещества, которые оказывают разрушительное воздействие на клетки. Примеры пригодных для применения цитотоксических агентов и химиотерапевтических агентов для образования иммуноконъюгатов известны специалистам в области, см., например, WO 05/103081.
Биспецифичность
Антитела настоящего изобретения могут быть моноспецифическими, биспецифическими или мультиспецифическими. Мультиспецифические mAb могут быть специфичны по отношению к различным эпитопам одного целевого полипептида или могут содержать антиген-связывающие домены, специфические по отношению к нескольким целевым полипептидам. См., например, Tutt et al. (1991) J. Immunol. 147:60-69. mAb анти-PCSK9 человека могут быть связаны с другой функциональной молекулой или экспрессироваться одновременно с ней, например, с другим пептидом или белком. Например, антитело или его фрагмент могут быть функционально связаны (например, химической связью, генетическим слиянием, нековалентной ассоциацией или иным образом) с одной или несколькими молекулярными структурами, например, с другим антителом или фрагментом антитела, с образованием биспецифического или мультиспецифического антитела с дополнительной специфичностью связывания.
Примером формата биспецифического антитела, которое может использоваться в контексте настоящего изобретения, может быть использование первого домена иммуноглобулина (Ig) CH3 и второго домена Ig CH3, где первый и второй домены Ig CH3 отличаются друг от друга не менее чем одной аминокислотой и где такое различие не менее чем на одну аминокислоту уменьшает связывание биспецифического антитела с белком A по сравнению с биспецифическим антителом, в котором такое аминокислотное различие отсутствует. В одном из осуществлений первый домен Ig CH3 связывается с белком A, а второй домен содержит мутацию, которая уменьшает или блокирует связывание белка А, например, модификацию H95R (по номенклатуре экзонов IMGT; H435R по номенклатуре ЕС). Второй CH3 может также содержать модификацию Y96F (по IMGT; Y436F по ЕС). Во втором модуле CH3 могут присутствовать дополнительные модификации: D16E, L18M, N44S, K52N, V57M и V82I (по IMGT; D356E, L358M, N384S, K392N, V397M и V422I по ЕС) в случае антител IgG1; N44S, K52N и V82I (IMGT; N384S, K392N и V422I по ЕС) в случае антител IgG2; и Q15R, N44S, K52N, V57M, R69K, E79Q и V82I (по IMGT; Q355R, N384S, K392N, V397M, R409K, E419Q и V422I по ЕС) в случае в случае антител IgG4. Вариации по формату биспецифических антител, описанные выше, входят в сферу охвата настоящего изобретения.
Биоэквиваленты
Анти-PCSK9 антитела и фрагменты антител настоящего изобретения включают белки, содержащие аминокислотные последовательности, которые отличаются от описанных mAb, но сохраняют способность связывать человеческий PCSK9. Такие вариантные mAb и фрагменты антител содержат одно или несколько добавлений, делеций или замещений аминокислот по сравнению с материнской последовательностью, но проявляют биологическую активность, которая в значительной мере эквивалентна активности описанных mAb. Аналогичным образом, последовательности ДНК, кодирующие анти-PCSK9 антитела настоящего изобретения, включают последовательности, которые содержат одно или несколько добавлений, делеций или замещений нуклеотидов по сравнению с раскрываемой последовательностью, однако они кодируют анти-PCSK9 антитела или фрагмент антитела, которые в значительной мере биоэквивалентны анти-PCSK9 антителу или фрагменту антитела настоящего изобретения. Примеры таких вариантных аминокислотных последовательностей и последовательностей ДНК обсуждаются выше.
Два антигенсвязывающих белка или антитела считаются биоэквивалентными, если, например, они являются фармацевтическими эквивалентами или фармацевтическими альтернативами, для которых скорость и степень абсорбции не проявляют существенных различий при введении в одинаковых молярных дозах в аналогичных экспериментальных условиях, как при разовой дозировке, так и в многократных дозах. Некоторые антитела будут считаться эквивалентными или фармацевтическими альтернативами, если они эквивалентны по степени своей абсорбции, но не по скорости такой абсорбции, но, тем не менее, могут рассматриваться как биоэквивалентные, поскольку такие различия в скорости абсорбции, вносимые намеренно и отраженные на маркировке, не являются существенными для достижения эффективных концентраций лекарства в организме при, например, продолжительном применении и считаются незначительными с медицинской точки зрения для конкретного исследуемого лекарственного препарата. В одном осуществлении два антигенсвязывающих белка являются биоэквивалентными, если для них отсутствуют значимые клинические различия в плане безопасности, чистоты и активности.
В одном осуществлении два антигенсвязывающих белка являются биоэквивалентными, если пациенту можно вводить контрольный и биологический продукт поочередно, один или несколько раз, без ожидаемого нарастания риска побочных эффектов, в том числе клинических значимых изменений в иммуногенности или снижения эффективности, по сравнению с непрерывной терапией одним продуктом.
В одном из осуществлений два антигенсвязывающих белка являются биоэквивалентными, если они оба действуют по одинаковому механизму или механизму действия при данном заболевании или условиях применения в той мере, в которой такие механизмы известны.
Биоэквивалентность может быть продемонстрирована и методиками in vivo и in vitro. К методам измерения биоэквивалентности относятся, например, (a) испытания in vivo на человеке или других млекопитающих, при которых концентрация антитела или его метаболитов измеряется в крови, плазме, сыворотке или другой биологической жидкости в зависимости от времени; (b) испытания in vitro, которые коррелируют с данными биодоступности для человека in vivo и с обоснованной степенью достоверности предсказывают их; (c) испытания in vivo на человеке или других млекопитающих, в которых надлежащий острый фармакологический эффект антитела (или его мишени) измеряются в зависимости от времени; и (d) строго контролируемые клинические испытания, в ходе которых устанавливается безопасность, эффективность воздействия, биодоступность или биоэквивалентность антитела.
Биоэквивалентные варианты анти-PCSK9 антител настоящего изобретения могут конструироваться, например, посредством введения различных замещений остатков или последовательностей, или делеций терминальных или внутренних остатков или последовательностей, не нужных для биологической активности. Например, остатки цистеина, не имеющие существенного значения для биологической активности, можно удалять или замещать другими аминокислотами, чтобы не допустить образования ненужных или неправильных внутримолекулярных дисульфидных мостиков в ходе ренатурации.
Группы пациентов
В настоящем изобретении предлагаются терапевтические методы для лечения человека, нуждающегося в применении состава настоящего изобретения. Несмотря на то, что изменения образа жизни и лечение стандартными препаратами часто обеспечивают успех в снижении уровня холестерина, не все пациенты в состоянии добиться рекомендуемых целевых уровней холестерина в рамках таких подходов. Различные состояния, например, наследственная гиперхолестеринемия (FH), оказываются устойчивыми в плане снижения уровня ЛНП-Х, несмотря на агрессивное применение стандартной терапии. Гомозиготная и гетерозиготная наследственная гиперхолестеринемия (hoFH, heFH) является состоянием, которое связывают с преждевременным сосудистым атеросклерозом. Вместе с тем у пациентов с поставленным диагнозом hoFH чаще всего отсутствует ответ на стандартную лекарственную терапию, и возможности их лечения весьма ограничены. В частности, лечение статинами, которые снижают ЛНП-Х за счет ингибирования синтеза холестерина и повышения функции рецепторов ЛНП печени, могут оказывать несущественный эффект на пациентов, у которых нет ЛНП рецепторов, или же их функционирование нарушено. Недавно было показано, что у пациентов с подтвержденной по генотипу hoFH, получавших максимальные дозы статинов, отмечается среднее снижение ЛНП-Х всего лишь менее чем на примерно 20%. Добавление к этой схеме лечение эзетимиба в дозе 10 мг/день привело к суммарному снижению уровней ЛНП-Х на 27%, что по-прежнему далеко от оптимального показателя. Аналогичным образом, многие пациенты невосприимчивы к статинам, плохо контролируются при статиновой терапии или не в состоянии переносить лечение статинами; в общем случае, такие пациента не могут добиться контроля за уровнем холестерина в условиях альтернативного лечения. Существует огромная неудовлетворенная медицинская потребность в новых методах лечения, которые в состоянии учесть недостатки существующих вариантов лечения.
Конкретные группы населения, которые могут проходить лечение с использованием терапевтических методов настоящего изобретения, включают пациентов, которым показан аферез ЛНП, пациентов с мутациями, активирующими PCSK9 («GOF»), гетерозиготной наследственной гиперхолестеринемией (heFH); пациентов с первичной гиперхолестеринемией, которые не переносят статины или неконтролируемы статинами; а также пациенты с риском развития гиперхолестеринемии, которые могут получать профилактическое лечение.
Терапевтическое применение и составы препаратов
В изобретении приводятся терапевтические препараты, включающие антитела анти-PCSK9 или их антиген-связывающие фрагменты, входящие в сферу охвата настоящего изобретения. Введение терапевтических препаратов в соответствии с настоящим изобретением будет осуществляться в подходящих носителях, формообразующих и прочих веществах, которые включаются в состав препаратов, чтобы обеспечить более эффективное распространение, доставку, переносимость и пр. Множество соответствующих составов можно найти в формулярах, известных всем специалистам в области фармацевтической химии: Remington's Pharmaceutical Sciences, Mack Publishing Company, Easton, PA. К таким препаратам относятся, например, порошки, пасты, мази, желе, воски, масла, липиды, липид-содержащие (катионные или анионные) везикулы (например, LIPOFECTIN™), конъюгаты ДНК, безводные абсорбционные пасты, эмульсии масла в воде и воды в масле, эмульсии Carbowax (полиэтиленгликоли различного молекулярного веса), полутвердые гели и полутвердые смеси, содержащие Carbowax. См. также Powell et al. "Compendium of excipients for parenteral formulations" PDA (1998) J Pharm Sci Technol 52:238-311.
Дозу можно менять в зависимости от возраста и веса объекта, получающего лечение, заболевания, на которое направлено лечение, условий, способа введения и пр. При использовании антитела настоящего изобретения для лечения различных болезней и заболеваний, связанных с PCSK9, включая гиперхолестеринемию, расстройства, связанные с липопротеином низкой плотности (ЛНП) и аполипопротеином B, и нарушения липидного метаболизма и т.п. у взрослых пациентов, целесообразно вводить антитело настоящего изобретения внутривенно, как правило, в разовой дозе примерно от 0,01 до 20 мг на кг веса тела, более предпочтительно примерно от 0,02 до 7 мг, примерно от 0,03 до 5 мг, или примерно от 0,05 до 3 мг на кг веса тела. В зависимости от тяжести состояния можно корректировать частоту и продолжительность лечения.
Известны различные системы доставки, и они могут использоваться для введения фармацевтического препарата настоящего изобретения, например, инкапсуляция в липосомы, микрочастицы, микрокапсулы, рекомбинантные клетки, способные экспрессировать мутантные вирусы, опосредованный рецепторами эндоцитоз (см., например, Wu et al. (1987) J. Biol. Chem. 262:4429-4432). К методам введения, среди прочих, относятся чрескожный, внутримышечный, внутрибрюшинный, внутривенный, подкожный, интраназальный, эпидуральный и пероральный. Препарат может вводиться любым подходящим способом, например, вливанием или болюсной инъекцией, абсорбцией через эпиталиальные или кожно-слизистые оболочки (например, слизистую ротовой полости, слизистую прямой кишки и кишечника и пр.) и может применяться совместно с другими биологически-активными агентами. Введение может быть системным или локальным.
Фармацевтический препарат может также доставляться в везикуле, в частности в липосоме (см. Langer (1990) Science 249:1527-1533; Treat et al. (1989) в Liposomes in the Therapy of Infectious Disease and Cancer, Lopez Berestein and Fidler (eds.), Liss, New York, сс. 353-365; Lopez-Berestein, там же, сс. 317-327; см. в целом там же).
В определенных ситуациях фармацевтический препарат может доставляться в системе контролируемого высвобождения. В одном осуществлении может использоваться насос (см. Sefton (1987) CRC Crit. Ref. Biomed. Eng. 14:201). В другом осуществлении могут использоваться полимерные материалы; см. Medical Applications of Controlled Release, Langer and Wise (eds.), CRC Pres., Boca Raton, Florida (1974). В еще одном осуществлении система контролируемого высвобождения может располагаться в непосредственной близости от цели препарата, а потому потребуется лишь некоторая доля от системной дозы (см., например, Goodson, in Medical Applications of Controlled Release, vol. 2, сс. 115-138, 1984).
К инъекционным препаратам могут относиться формы дозировки для внутривенных, подкожных, чрескожных и внутримышечных инъекций, капельных вливаний и пр. Такие инъекционные препараты можно приготовить с помощью известных методов. Например, инъекционные препараты можно приготовить, в частности, посредством растворения, суспендирования или эмульгирования описанного выше антитела или его соли в стерильной водной среде или в масляной среде, которые обычно применяются для инъекций. В качестве водной среды для инъекций предлагаются, например, физиологический раствор, изотонический раствор, содержащий глюкозу, и другие вспомогательные вещества и пр., которые могут использоваться в сочетании с соответствующим солюбилизирующим агентом, например, спиртом (в частности этанолом), многоосновным спиртом (например, пропиленгликолем, полиэтиленгликолем), неионогенным поверхностно-активным соединением [например, полисорбатом 80, НСО-50 (аддуктом полиоксиэтилена (50 моль) и гидрогенизированного касторового масла] и пр. В качестве масляной среды используются, например, кунжутное масло, соевое масло и пр., которые могут применяться в сочетании с солюбилизирующим агентом, например, бензилбензоатом, бензиловым спиртом и пр. Приготовленный таким образом препарат для инъекций предпочтительно фасовать в соответствующие ампулы. Фармацевтический состав настоящего изобретения может вводиться подкожно или внутривенно с помощью стандартной иглы и шприца. Кроме того, что касается подкожного введения, в случае применения фармацевтического препарата настоящего изобретения вполне можно использовать шприц-ручку. Такой шприц-ручка может быть многоразового или одноразового использования. В многоразовом шприце-ручке обычно используется сменный картридж, который содержит фармацевтический состав. После того как весь фармацевтический состав внутри картриджа был введен, и картридж пуст, отработанный картридж можно легко выбросить и заменить его на новый картридж, в котором содержится фармацевтический состав. После этого шприц-ручка может использоваться повторно. В разовом шприце-ручке сменный картридж не предусмотрен. Напротив, разовый шприц-ручка поставляется уже заполненным фармацевтическим составом, который помещается в резервуаре внутри устройства. После того как в резервуаре не остается лекарственного состава, все устройство выбрасывают.
Для подкожного введения фармацевтического состава настоящего изобретения могут применяться самые различные конструкции многоразовых шприцов-ручек и устройств для автоматической инъекции. Примеры включают, без ограничения, AUTOPEN™ (Owen Mumford, Inc., Woodstock, UK), DISETRONIC™ pen (Disetronic Medical Systems, Burghdorf, Switzerland), HUMALOG MIX 75/25™ pen, HUMALOG™ pen, HUMALIN 70/30™ pen (Eli Lilly and Co., Indianapolis, IN), NOVOPEN™ I, II и III (Novo Nordisk, Copenhagen, Denmark), NOVOPEN JUNIOR™ (Novo Nordisk, Copenhagen, Denmark), BD™ pen (Becton Dickinson, Franklin Lakes, NJ), OPTIPEN™, OPTIPEN PRO™, OPTIPEN STARLET™, and OPTICLIK™ (sanofi-aventis, Frankfurt, Germany). К примерам разовых шприцов-ручек, которые могут применяться для подкожного введения фармацевтического состава настоящего изобретения, среди прочих, относятся шприц-ручка SOLOSTAR™ (sanofi-aventis), FLEXPEN™ (Novo Nordisk) и KWIKPEN™ (Eli Lilly).
Фармацевтические препараты для перорального или парентерального введения, описанные выше, предпочтительно готовить в лекарственных формах с разовой дозой, подбираемой в соответствии с дозировкой активных ингредиентов. К таким лекарственным формам с разовой дозой относятся, например, таблетки, пилюли, капсулы, инъекции (ампулы), суппозитории и пр. Количество указанного антитела, содержащегося в разовой дозе, обычно составляет от 5 до 500 мг на лекарственную форму; особенно в виде инъекции, предпочтительно, чтобы количество указанного антитела составляло примерно от 5 до примерно 100 мг и примерно от 10 до примерно 250 мг в случае других лекарственных форм.
В изобретении предлагаются терапевтические способы, в рамках которых антитело или фрагмент антитела настоящего изобретения применяется для лечения гиперхолестеринемии, связанной с самыми различными заболеваниями с участием hPCSK9. Антитела анти-PCSK9 или их фрагменты, описанные в настоящем изобретении, особенно эффективны для лечения гиперхолестеринемии и аналогичных нарушений. Комбинационная терапия может включать анти-PCSK9 антитело настоящего изобретения, например, с одним или несколькими агентами, которые (1) индуцируют нарушение синтеза холестерина на клеточном уровне посредством ингибирования 3-гидрокси-3-метилглутарил (HMG)-коэнзим A (CoA) редуктазы, например, церивастатин, аторвастатин, симвастатин, питавастатин, розувастатин, флувастатин, ловастатин, правастатин; (2) ингибируют захват холестерина и/или реабсорбцию желчных кислот; (3) повышают катаболизм липопротеинов (например, ниацина); а также активаторами фактора транскрипции LXR, который играет роль в удалении холестерина, например, 22-гидроксихолестерина, или фиксированные комбинации, например, эзетимиб плюс симвастатин; статин с секвестрантом желчных кислот на ионообменной смоле (например, холестирамин, колестипол, колесевелам), фиксированная комбинация ниацин плюс статин (например, ниацин с ловастатином); или с другими агентами, снижающими концентрацию липидов, например, этиловыми эфирами омега-3 жирных кислот, (например, омакор).
ПРИМЕРЫ
Приведенные ниже примеры призваны дать специалистам в области полную информацию и описание того, как следует формулировать и использовать способы и препараты настоящего изобретения, и не призваны ограничивать сферу охвата того, что изобретатели рассматривают как предмет своего изобретения. Прилагались усилия обеспечить точность используемых показателей, но при этом необходимо учитывать некоторые экспериментальные ошибки и отклонения. Если не указано иначе, под молекулярным весом понимается усредненный молекулярный вес, температура приводится в градусах Цельсия, а давление находится на уровне атмосферного или близко к этому уровню.
Пример 1. Получение антител человека к PCSK9 человека.
Мышей VELOCIMMUNE™ иммунизировали человеческой PCSK9, и иммунный ответ антител отслеживали с помощью антигенспецифического иммуноанализа с использованием сыворотки, взятой у таких мышей. В-клетки, экспрессирующие анти-hPCSK9, взятые из селезенки иммунизированных мышей, которые демонстрировали повышенные титры анти-hPCSK9 антител, сливали с клетками мышиной миеломы с образованием гибридом. Гибридомы проходят скрининг и селекцию для идентификации тех линий клеток, которые экспрессируют hPCSK9-специфические антитела, используя анализы, описанные ниже. Анализ позволил идентифицировать несколько клеточных линий, которые продуцируют химерные анти-hPCSK9 антитела, обозначаемые как H1M300, H1M504, H1M505, H1M500, H1M497, H1M498, H1M494, H1M309, H1M312, H1M499, H1M493, H1M496, H1M503, H1M502, H1M508, H1M495 и H1M492.
PCSK9-специфические антитела человека также выделяли напрямую из антиген-иммунизированных B-клеток без слияния с клетками миеломы, как описано в патенте США 2007/0280945A1. Вариабельные области тяжелой и легкой цепей клонировали, чтобы получить полностью человеческие анти-hPCSK9 антитела, обозначаемые как H1H313, H1H314, H1H315, H1H316, H1H317, H1H318, H1H320, H1H321 и H1H334. Были установлены стабильные клеточные линии CHO, экспрессирующие такие антитела.
Пример 2. Анализ использования генов
Для анализа структуры продуцируемых mAb клонировали и секвенировали нуклеиновые кислоты, кодирующие вариабельные области антител. Предсказанные аминокислотные последовательности вариабельных областей подтверждали N-терминальным аминокислотным секвенированием. На основании последовательности нуклеиновой кислоты и прогнозируемой последовательности аминокислот в mAb для каждой цепи антитела определяли степень использования генов.
Пример 3. Определение антигенсвязывающей аффинности
Равновесные константы диссоциации (KD) для связывания hPCSK9 с mAb, полученные из линий клеток гибридомы, описанных выше, определяли поверхностной кинетикой методом плазмонного резонанса на поверхности биосенсора в реальном времени (BIACORE™ T100). Каждое антитело захватывали при скорости потока 4 мкл/мин в течение 90 секунд на поверхности поликлонального антимышиного антитела козы IgG, образованной посредством прямого химического связывания на чипе BIACORE™, с формированием поверхности захваченного антитела. Человеческую PCSK9-mmh в концентрации 50 нМ или 12,5 нМ наносили на поверхность захваченных антител со скоростью потока 50 мкл/мин в течение 300 секунд, после чего отслеживали диссоциацию антиген-антитело в течение 15 минут при 25°C или 37°C (KD=пМ; T1/2=мин).
Равновесные константы диссоциации (KD) для связывания hPCSK9 с mAb, полученные прямым выделением спленоцитов, определяли поверхностной кинетикой методом плазмонного резонанса на поверхности биосенсора в реальном времени (BIACORE™ T100). Каждое выбранное антитело захватывали при скорости потока 2 мкл/мин в течение 6 минут на поверхности поликлонального античеловеческого антитела козы IgG, образованной посредством прямого химического связывания на чипе BIACORE™, с формированием поверхности захваченного антитела. Человеческую PCSK9-mmh в концентрации 50 нМ или 12,5 нМ наносили на поверхность захваченных антител со скоростью потока 70 мкл/мин в течение 5 минут, после чего отслеживали диссоциацию антиген-антитело в течение 15 минут при 25°C или 37°C (KD=пМ; T1/2=мин).
Скорость диссоциации (kd) для отдельных mAb для меченых макак-резусов (Macaca mulata) PCSK9 (mmPCSK9; SEQ ID №: 756) (mmPCSK9-mmh) при 25°C определяли в соответствии с описанными выше методиками.
Пример 4. Эффект воздействия рН на аффинность связывания антигена
Эффекты воздействия рН на аффинность связывания антигена для продуцируемых клетками СНО полностью человеческих анти-hPCSK9 mAb оценивали с помощью описанных выше методов. Испытуемые mAb представляли собой полностью человеческие варианты Н1Н316Р («316Р») (HCVR/LCVR SEQ ID №:90/92; CDR последовательности SEQ ID №:76/78/80 и 84/86/88) и H1M300N («300N») (HCVR/LCVR SEQ ID №:218/226; CDR последовательности SEQ ID №:220/222/224 и 228/230/232). hPCSK9-mmh захватывалась на поверхности анти-myc mAb при высокой плотности (примерно от 35 до 45 резонансных единиц) (RU) или при низкой плотности (примерно от 5 до 14 RU). Каждое антитело в концентрации 50 нМ в HBST (рН 7,4 или рН 5,5) вводили на поверхность захваченной hPCSK9 со скоростью потока 100 мкл/мин в течение 1,5 минуты при 25°С, и диссоциацию антиген-антитело отслеживали в течение 10 минут. Контроль I: анти-hPCSK9 mAb SEQ ID №:79/101 (WO 2008/063382) (KD=пМ; T1/2=мин).
Антигенсвязывающие свойства 316Р и 300N при рН 7,4 или рН 5,5 определяли с помощью модифицированного анализа BIACORE™, как это описано выше. Коротко говоря, mAb иммобилизовали на сенсорных чипах BIACORE™ CM5 посредством сочетания с амином. Различные концентрации меченной myc-myc-his hPCSK9, мышиной PCSK9 (mPCSK9, SEQ ID №:757), hPCSK9 с точечной мутацией с появлением новых патологических функций (GOF) D374Y (hPCSK9(D374Y)), PCSK9 (mfPCSK9, SEQ ID №:761) (mfPCSK9) яванского макака (Масаса fascicularis), крысиной (Rattus norvegicus) PCSK9 (rPCSK9, SEQ ID №:763) и his-меченной PCSK9 (maPCSK9, SEQ ID №:762) (maPCSK9) сирийского золотистого хомяка (Mesocricetus auratus) в пределах от 11 до 100 нМ вводили на поверхность антител со скоростью потока 100 мкл/мин в течение 1,5 минуты, и диссоциацию антиген-антитело отслеживали в реальном времени в течение 5 минут при 25°С (таблица 6) или при 37°С (таблица 7). Контроль II: aHTH-hPCSK9 mAb SEQ ID №:67/12 (WO 2009/026558). НС: в экспериментальных условиях связывания не наблюдалось (KD=пМ; Т1/2=мин).
Эффект pH при 25°C
Эффект pH при 37°C
Пример 5. Связывание анти-hPCSK9 mAb с hPCSK9 с точечной мутацией D374Y
Аффинность связывания некоторых анти-hPCSK9 mAb с hPCSK9 с точечной мутацией с появлением новых патологических функций (GOF) D374Y (hPCSK9(D374Y)-mmh) определяли с помощью описанных выше методов. Каждое антитело захватывали при скорости потока 40 мкл/мин в течение 8-30 секунд на поверхности поликлонального антимышиного антитела козы IgG, образованной посредством прямого химического связывания на чипе BIACORE™, с формированием поверхности захваченного антитела. Человеческую PCSK9(D374Y)-mmh в различных концентрациях от 1,78 нM до 100 нM наносили на поверхность захваченных антител со скоростью потока 50 мкл/мин в течение 5 минут, после чего отслеживали диссоциацию человеческой PCSK9(D374Y)-mmh - антитело в течение 15 минут при 25°C. Контроль III: анти-hPCSK9 mAb SEQ ID №: 49/23 (WO 2009/026558) (KD=пM; T1/2=мин).
Пример 6. Специфичность связывания анти-hPCSK9 mAb
316P, 300N и контроль I анти-hPCSK9 mAb фиксировали на аминосвязанном анти-hFc CM5 чипе на BIACORE™2000. Меченная (myc-myc-his) человеческая PCSK9, человеческая PCSK1 (hPCSK1) (SEQ ID №: 759), человеческая PCSK7 (hPCSK7) (SEQ ID №: 760) или мышиная PCSK9 наносились (100 нM) на поверхность захваченных mAb и выдерживались для связывания при 25°C в течение 5 минут. Регистрировали изменения в RU. Результаты: 300N и контроль I связывались только с hPCSK9, а 316P связывались и с hPCSK9, и с mPCSK9.
Специфичность связывания анти-hPCSK9 mAb определяли с помощью ELISA. Коротко говоря, анти-hPCSK9 антитело наносили на поверхность 96-луночной планшеты. Человеческие PCSK9-mmh, mPCSK9-mmh, maPCSK9-h, hPCSK1-mmh или hPCSK7-mmh в концентрации 1,2 нM добавляли в покрытые антителами планшеты и инкубировали при комнатной температуре в течение 1 часа. Связанный с планшетой белок PCSK затем определяли по HRP-конъюгированному анти-His антителу. Результаты показывают, что 316P связывает человеческую, мышиную и хомячковую PCSK9, тогда как 300N и контроль I связывают только hPCSK9. Ни одно из анти-hPCSK9 mAb не проявляло существенного связывания с hPCSK1 или hPCSK7.
Пример 7. Перекрестная реактивность анти-hPCSK9 mAb
Перекрестная реактивность анти-hPCSK9 mAb с mmPCSK9, mfPCSK9, mPCSK9, maPCSK9 или rPCSK9 определяли с использованием BIACORE™ 3000. Анти-hPCSK9 mAb фиксировали на поверхности анти-hFc, которую формировали посредством реакции прямого химического сочетания на чипе BIACORE™. Очищенную меченную hPCSK9, hPCSK9(D374Y), mmPCSK9, mfPCSK9, mPCSK9, maPCSK9 или rPCSK9, каждую в концентрации от 1,56 нM до 50 нM, наносили на поверхность антител при 25°C или 37°C. Определяли связывание между 316P, 300N, контролем I, контролем II или контролем III и белками PCSK9 (KD=пM; T1/2=мин).
316P mAb
300N mAb
Контроль I mAb
Контроль II mAb
Контроль III mAb
Пример 8. Ингибирование связывания между hPCSK9 и доменами hLDLR
Способность некоторых анти-hPCSK9 mAb блокировать связывание hPCSK9 с внеклеточным доменом человека LDLR полной длины (hLDLR-экто SEQ ID №: 758), доменом hLDLR EGF-A (аминокислоты 313-355 SED ID №: 758) или доменами hLDLR EGF-AB (аминокислоты 314-393 SEQ ID №: 758) (LDLR Genbank номер NM_000527) определяли с помощью BIACORE™ 3000. Коротко говоря, белки hLDLR-экто, EGF-A-hFc или EGF-AB-hFc фиксировали на чипе CM5 посредством сочетания с амином, чтобы образовать поверхность рецептора или фрагмента рецептора. Некоторые анти-hPCSK9 mAb в концентрации 62,5 нM (2,5-кратный избыток по сравнению с антигеном) предварительно смешивали с 25 нM hPCSK9-mmh с последующей инкубацией в течение 40 минут при 25°C, с тем чтобы обеспечить достижение равновесия антитело-антиген связывания с образованием равновесных растворов. Равновесные растворы наносили на поверхность рецепторов или фрагментов рецепторов со скоростью 2 мкл/мин в течение 40 минут при 25°C. Определяли изменения в RU из-за связывания анти-hPCSK9 mAb с hLDLR-экто, EGF-A-hFc или EGF-AB-hFc. Результаты показывают, что H1H316P и H1M300N блокировали связывание hPCSK9-mmh с hLDLR-экто, доменом hLDLR EGF-A и доменами hLDLR EGF-AB; H1H320P блокировало связывание hPCSK9-mmh с hLDLR-экто и доменом hLDLR EGF-A; а H1H321P блокировало связывание hPCSK9-mmh с доменом hLDLR EGF-A.
Способность mAb блокировать связывание hPCSK9 с hLDLR-экто, доменом hLDLR EGF-A или доменами hLDLR EGF-AB также оценивали по результатам иммуноферментного анализа на основе ELISA. Вкратце, hLDLR-экто, hLDLR EGF-A-hFc или hLDLR EGF-AB-hFc, каждый по 2 мкг/мл, наносили на 96-луночный планшет в ФСБ-буфере в течение ночи при температуре 4°C, и неспецифические сайты связывания блокировали обработкой БСА. Данный планшет использовали для измерения свободного hPCSK9-mmh в растворе PCSK9-mmh, предварительно приведенного в равновесие различными концентрациями mAb анти-hPCSK9. Одинаковое количество hPCSK9-mmh (500 пМ) предварительно смешивали с различными дозами антитела в диапазоне концентраций от 0 до ~50 нМ в последовательных разбавлениях, затем проводили одночасовое инкубирование при комнатной температуре для достижения равновесия связывания антитело-антиген. После достижения равновесия образцы растворов переносили на покрытые рецептором или фрагментами рецептора планшеты. После одного часа связывания планшеты промывали, и связанные hPCSK9-mmh детектировали при помощи HRP-конъюгированного анти-myc антитела. Значения IC50 (в пМ) определяли как количество антитела, требуемое для 50% снижения hPCSK9-mmh, связанного с нанесенным на планшет рецептором или фрагментами рецептора. Результаты показывают, что специфические mAb функционально блокируют связывание PCSK9 с тремя рецепторами при нейтральном pH (7,2) и кислом pH (5,5).
Способность mAb блокировать связывание мутанта hPCSK9 GOF -hPCSK9(D374Y)-mmh с доменом hLDLR EGF-A или доменом hLDLR EGF-AB (значения IC50 в области пM) также определяли с помощью описанного выше иммуноферментного анализа на основе ELISA, для чего использовали фиксированное количество 0,05 нM hPCSK9(D374Y)-mmh.
Способность mAb блокировать связывание mmPCSK9 или mPCSK9 с доменом hLDLR-экто, доменом hLDLR EGF-A или доменом hLDLR EGF-AB (значения IC50 в области пM) оценивали при нейтральном рН с помощью описанного выше иммуноферментного анализа на основе ELISA, для чего использовали фиксированное количество 1 нM mmh-меченой mmPCSK9 или 1 нM mPCSK9.
Способность mAb блокировать связывание hPCSK9, mmPCSK9, rPCSK9, maPCSK9, mfPCSK9 или mPCSK9 с доменом hLDLR EGF-A (значения IC50 в области пM) оценивали при нейтральном pH (7,2) (таблица 17) или кислом pH (5,5, таблица 18) с помощью описанного выше иммуноферментного анализа на основе ELISA, для чего использовали фиксированное количество 0,5 нM hPCSK9-mmh, 1 нM mmPCSK9-mmh, 1 нM rPCSK9-mmh, 1 нM maPCSK9-h, 0,3 нM mfPCSK9-mmh или 1 нM mPCSK9-mmh.
Также определяли способность 316P и контроля I блокировать связывание hPCSK9 с hLDLR. Коротко говоря, посредством сочетания с амином рекомбинантные hLDLR или hLDLR-EGFA-mFc иммобилизовали на чипах BIACORE™ CM5. Смесь антиген-антитело из 100 нМ hPCSK9-mmh и 316Р, контроль I mAb или неспецифического hPCSK9 mAb (каждое пр 250 нМ) инкубировали при комнатной температуре в течение 1 часа, а затем наносили на поверхность hLDLR или hLDLR-EGFA со скоростью потока 10 мкл/мин в течение 15 минут при 25°С. Регистрировали изменения в RU из-за связывания между свободной hPCSKS-mmh в смеси с hLDLR или hLDLR-EGFA. Связывание hPCSK9 с hLDLR или hLDLR-EGFA полностью блокировалось 316Р и 300N, но не контролем I mAb.
Пример 9. Эпитопное картирование
Для определения специфичности связывания с эпитопом приготовили группу из трех химерных белков PCSK9-mmh, в которых специфические домены человеческого PCSK9 были замещены доменами PCSK9 мыши. Химерный белок #1 содержал мышиный продомен PCSK9 (аминокислотные остатки 1-155 SEQ ID №:757), за которым следовал человеческий каталитический домен PCSK9 (остатки 153-425 SEQ ID №:755) и мышиный С-терминальный домен PCSK9 (остатки 429-694 SEQ ID №:757) (mPro-hCat-mC-term-mmh). Химерный белок #2 содержал человеческий продомен PCSK9 (аминокислотные остатки 1-152 SEQ ID №:755), за которым следовал мышиный каталитический домен PCSK9 (остатки 156-428 SEQ ID №:757) и мышиный С-терминальный домен PCSK9 (остатки 429-694 SEQ ID №:757) (hPro-mCat-mC-term-mmh). Химерный белок #3 содержит мышиный продомен PCSK9 и мышиный каталитический домен PCSK9, за которым следует человеческий С-терминальный домен PCSK9 (остатки 426-692 SEQ ID №:755) (mPro-mCat-hC-term-mmh). Кроме того, была получена hPCSK9 с точечной мутацией D374Y (hPCSK9(D374Y)-mmh).
Специфичность связывания mAb с исследуемыми белками hPCSK9-mmh, мышиной PCSK9-mmh, химерными белками #1, #2 и #3, а также hPCSK9(D374Y)-mmh проверяли следующим образом: mAb наносили на 96-луночную планшету в течение ночи при 4°C, затем на планшету добавляли каждый из испытуемых белков (1,2 нM). После 1 часа связывания при комнатной температуре планшету промывали и связанный испытуемый белок определяли с помощью поликлонального HRP-конъюгированного антитела анти-myc (++ = OD >1,0; + = OD 0,4-1,0; - = OD <0,4).
Специфичность связывания 316P, 300N и контрольных анти-hPCSK9 mAb с hPCSK9-mmh, mPCSK9-mmh, mmPCSK9-mmh, mfPCSK9-mmh, rPCSK9-mmh, химерными белками #1, #2 и #3, а также с hPCSK9(D374Y)-mmh проверяли, как описано выше, но концентрация белка составляла 1,7 нM (- = OD <0,7; + = OD 0,7-1,5; ++ = OD >1,5).
Аналогичные результаты для некоторых mAb были получены с помощью анализа связывания BIACORE™. Коротко говоря, 316P, 300N или контроль I mAb фиксировали на аминосвязанном чипе СМ5 с анти-hFc CM5, и 100 нM каждого белка, наносили на поверхность с фиксированными mAb. Определяли изменения RU в результате связывания каждого белка с поверхностью mAb.
Чтобы далее оценить специфичность связывания 316P, которое перекрестно реагирует с mPCSK9-mmh, был разработан перекрестный конкурентный анализ ELISA, позволяющий оценить специфичность связывания домена. Коротко говоря, mAb, специфические к химерным белкам #1, #2 или #3, вначале наносили на поверхность 96-луночной планшеты в течение ночи при концентрации 1 мкг/мл. В каждую лунку затем добавляли человеческую PCSK9-mmh (2 мкг/мл) с последующим инкубированием в течение 1 часа при комнатной температуре. 316P (1 мкг/мл) добавляли и инкубировали еще час при комнатной температуре. Связанный с планшетой 316З затем определяли по HRP-конъюгированному анти-hFc поликлональному антителу. Несмотря на то что связывание 316P с hPCSK9-mmh не зависело от присутствие mAb, специфических по отношению к химерному белку #2 или химерному белку #3, связывание 316P с hPCSK9-mmh в значительной мере снижалось из-за наличия антитела, специфического к химерному белку #1.
Пример 10. Оценка профиля связывания антигена на основе BIACORE™
Профили связывания антитела также определяли для 316P, 300N, контроля I, II и III mAb с помощью BIACORE™1000. Коротко говоря, hPCSK9-mmh фиксировали на поверхности анти-myc. Первое анти-hPCSK9 mAb (50 мкг/мл) наносили на поверхность со связанной PCSK9 в течение 10 минут со скоростью потока 10 мкл/мин при 25°C. Затем наносили второе анти-hPCSK9 mAb (50 мкг/мл) на поверхность с фиксированным первым mAb в течение 10 минут со скоростью потока 10 мкл/мин при 25°C. Оценивали способность первого mAb блокировать связывание второго mAb, которую выражали в процентах ингибирования.
Пример 11. Повышение захвата ЛНП антителами анти-hPCSK9
Способность анти-hPCSK9 mAb увеличивать захват ЛНП in vitro определяли с использованием клеточной линии гепатоклеточной карциномы печени человека (HepG2). Клетки HepG2 высевали на 96-луночные планшеты по 9×104 клеток на лунку в полной среде DMEM и инкубировали при 37°C, 5% CO2 в течение 6 часов для получения монослоев HepG2. Добавляли человеческую PCSK9-mmh в концентрации 50 нМ в липопротеин-дефицитной среде (LPDS) и испытуемое mAb в различных концентрациях от 500 нМ до 0,98 нМ в среде LPDS. Данные выражали в виде значений IC50 для каждого эксперимента (IC50 = концентрация антитела, при которой происходит увеличение захвата ЛНП на 50%). Кроме того, было также экспериментально продемонстрировано, что 316P и 300N были в состоянии полностью обратить ингибирующий эффект hPCSK9 на захват ЛНП, тогда как для контроля I mAb или H1M508 анти-hPCSK9 mAb обращение ингибирующего воздействия достигалось примерно на 50%.
Способность анти-hPCSK9 mAb обращать ингибирующий эффект на захват ЛНП белком PCSK9 у различных видов млекопитающих также тестировали на клеточной линии HepG2, как это описано выше. Коротко говоря, клетки HepG2 инкубировали в течение ночи с последовательными разбавлениями антитела в среде LPDS (начиная с концентрации 500 нМ) и 50 нM hPCSK9-mmh, mfPCSK9-mmh, mPCSK9-mmh, rPCSK9-mmh или maPCSK9-h. Клетки HepG2 также инкубировали в течение ночи с последовательными разбавлениями антитела в LPDS (начиная с 50 нM) и 1 нM hPCSK9(D374Y). Как показано в таблице 24, в то время как 316P было в состоянии полностью обратить ингибирующее воздействие на ЛНП всеми испытываемыми белками PCSK9, 300N смогло обратить только ингибирующий эффект hPCSK9, hPCSK9(D374Y) и mfPCSK9 на захват ЛНП. Значения выражены в нМ IC50.
Пример 12. Нейтрализация биологического эффекта hPCSK9 in vivo
Для оценки биологического эффекта нейтрализации PCSK9 проводили сверхэкспрессию hPCSK9 у мышей C57BL/6 посредством гидродинамической доставки (HDD) конструкций ДНК, кодирующих полную длину hPCSK9-mmh. 4 мыши (C57BL/6) получали инъекцию холостым вектором/физраствором (контроль), а 16 мышей получали инъекцию 50 мкг смеси hPCSK9-mmh-ДНК/физраствор в хвостовую вену в объеме, равном 10% от массы их тела. На 7 день после HDD доставка hPCSK9 приводила к 1,6-кратному повышению общего холестерина, 3,4-кратному повышению ЛНП холестерина (ЛНП-Х) и 1,9-кратному повышению холестерина без ЛВП (по отношению к контролю). Уровни hPCSK9 в сыворотке на 7 день были всегда выше 1 мкг/мл, как показывали данные количественного ELISA.
Введение H1M300N на 6 день после HDD в 3 экспериментальных группах (1, 5 или 10 мг/кг) (n=4 на группу) посредством внутрибрюшинной инъекции (в/б) привело к значительному сглаживанию уровня сывороточного холестерина. Через 18 часов после введения общий холестерин снизился на 9,8%, 26,3% и 26,8%, ЛНП-Х упал на 5,1%, 52,3% и 56,7%, а холестерин без ЛВП сократился на 7,4%, 33,8% и 28,6% в группах, получавших 1, 5 или 10 мг/кг H1M300N, соответственно.
Пример 13. Фармакокинетическое и химическое исследование сыворотки у обезьян
Фармакокинетическое исследование (ФК) проводили на интактных самцах яванского макака (Macaca fascicularis) с массой тела в интервале 5-7 кг и возрасте от 3 до 5 лет.
Распределение по группам. Обезьян распределяли на 5 групп лечения: Лечебная группа 1 (n=3) получала контрольный буфер (10 мM фосфат натрия, pH 6, 1 мл/кг); лечебная группа 2 (n=3) получала 1 мл/кг 316P (5 мг/мл); лечебная группа 3 (n=3) получала 1 мл/кг 300N (5 мг/мл); лечебная группа 4 (n=3) получала 1 мл/кг 316P (15 мг/мл); а лечебная группа 5 (n=3) получала 1 мл/кг 300N (15 мг/мл). Все лекарства вводили посредством в/в болюса с последующим смывом 1 мл физраствора. Объем суммарной дозы (мл) рассчитывался по самому последнему показателю массы тела (каждое животное дважды взвешивали в период акклиматизации и раз в неделю в течение всего исследования. В 1 день вводили разовую дозу испытуемого mAb или контрольного буфера.
Уход за животными. Животных содержали в условиях с контролем температуры и влажности. Целевой показатель температуры и относительной влажности лежал в промежутке 18-29°C и 30-70%, соответственно. Автоматическая система освещения обеспечивала 12-часовой суточный цикл. Темновой цикл можно было прерывать для мероприятий, связанных с исследованиями или обслуживанием помещения. Животных размещали в индивидуальных клетках, которые соответствовали Закону о защите прав животных и рекомендациям, приведенным в Руководстве по содержанию и использованию лабораторных животных (National Research Council 1996).
Диета и питание. Животные получали пищу дважды в день в соответствии со стандартными процедурами работы SNBL USA. Животным не давали пищу, если этого требовали конкретные процедуры (например, перед забором крови на биохимический анализ сыворотки, забором мочи, или если проводились процедуры, требовавшие введения седативных средств). Состав продуктов питания проходил стандартную процедуру анализа на предмет наличия загрязнителей, и было установлено, что он соответствует показателям изготовителя.
Схема эксперимента. Необходимое число животных отбирали из вивария SNBL USA. Состояние здоровья животных анализировали ветеринарным персоналом, и проводили биохимический анализ сыворотки, гематологическое исследование и скрининг коагуляции. Для исследования б отобрали 16 здоровых самцов. 15 самцов распределили между конкретными исследовательскими группами, а оставшееся животное содержали в качестве запасного. Для распределения животных по группам для исследований использовали стратифицированную рандомизированную схему, включающую проверку уровня сывороточного холестерина (на основании двух заборов в течение акклиматизации).
Период акклиматизации. Прошедшие предварительный карантин животные акклиматизировались к условиям исследовательского помещения как минимум в течение 14 дней до начала введения препаратов. Данные на этапе акклиматизации собирались у всех животных, в том числе у запасного. Для всех животных проводили оценку на предмет аномального поведения, которое могло бы повлиять на результаты исследования. После 1 дня запасное животное вернули в виварий.
Забор крови. Забор крови производили посредством венопункции из периферической вены у фиксированных, находящихся в сознании животных. Там где возможно, кровь забирали разовым образом, а затем делили на необходимые порции.
ФК исследование. Образцы крови (1,5 мл) собирали в пробирки для отделения сыворотки (SST) до введения, через 2 минуты, 15 минут, 30 минут, 1 час, 2 часа, 4 часа, 8 часов, 12 часов, 24 часа, а затем каждые 24 часа. Образцы сыворотки для хранения переносили в два флакона и хранили при -60°C или ниже.
Пробы сыворотки анализировали с использованием оптимизированной процедуры ELISA (твердофазный иммуноферментный анализ). Коротко говоря, планшеты для микротитрования вначале покрывали hPCSK9-mmh. Затем испытуемые mAb 316P или 300N наносили на планшету hPCSK9-mmh. Фиксированные 316P или 300N детектировали с использованием биотинилированного мышиного анти-hIgG4 с последующим связыванием с NeutrAvidin-HRP. В качестве стандартных использовали различные концентрации 316P или 300N в интервале от 100 до 1,56 нг/мл. В качестве нулевого стандарта (0 мг/мл) использовали однопроцентную сыворотку обезьян (аналитическая матрица) в отсутствие 316P или 300N. Результаты, приведенные на фиг.2, указывают на зависимое от дозы увеличение уровня 316P и 300N в сыворотке. Параметры ФК анализировали с помощью программного обеспечения WinNonlin (бескомпартментный анализ, модель 201 - в/в болюсное введение).
Биохимический анализ сыворотки. Образцы крови собирали до введения, через 12 часов, 48 часов, а затем каждые 48 часов для клинического биохимического анализа, в частности, липидных профилей (то есть холестерин, ЛНП-Х, ЛВП-Х, триглицериды). За исключением образца, отбираемого через 12 часов после введения, до забора крови все животные не получали питания в течение ночи. Объем образца составлял около 1 мл. Параметры химического состава определяли с использованием автоматического анализатора Olympus. Измеренные параметры (код Xybion): альбумин (ALB); щелочная фосфатаза (ALP); аланинаминотрансфераза (ALT); аспартаттрансаминаза (AST); общий билирубин (TBIL); кальций (Ca); общий холестерин (TCho); креатинкиназа (CK); креатинин (CRN); гамма-глутамилтрансаминаза (GGT); глюкоза (GLU); неорганический фосфор (IP); общий белок (TP); триглицериды (TRIG); азот мочевины крови (BUN); глобулин (GLOB); отношение альбумин/глобулин (A/G); хлорид (Cl); калий (K); натрий (Na); ЛНП и ЛВП холестерин. Остатки сыворотки хранили при -20°C или ниже и удаляли в отходы не ранее чем через неделю после анализа.
Результаты для образцов до 105 дня после введения дозы приводятся на фиг.3-7. Отмечалось снижение общего холестерина и ЛНП-Х у животных, получавших 316P и 300N, независимо от дозы в течение 24 часов после первой дозы. Общий сывороточный холестерин снижался быстро и сильно (~35%, фиг.3). Сильное снижение ~80% отмечалось по ЛНП-Х (фиг.4-5) на 6 день. У животных, которые получали дозу 15 мг/кг 300N, снижение общего холестерина (снижение ~10-15%) и ЛНП-Х (снижение ~40%) продолжалось не менее чем до 80-го дня исследования. Кроме того, ЛВП-Х был повышен у животных, которые получали 316P при 15 мг/кг (фиг.6). Животные, которые получали более высокую дозу (15 мг/кг) либо 316P, либо 300N, также демонстрировали снижение триглицеридов в ходе исследования (фиг.7). 316P проявляло максимальное подавление уровней ЛНП-Х до 80% по сравнению с исходным уровнем. Продолжительность периода такого подавления зависела от дозы, причем не менее чем 60% подавления (по сравнению с исходными уровнями ЛНП-Х) продолжалось примерно 18 дней (доза 5 мг/кг) и примерно 45 дней (доза 15 мг/кг). 300N демонстрирует четкий фармакодинамический профиль, отличающийся от 316P. Подавление уровня ЛНП-Х введением 300N поддерживалось в течение существенно более продолжительного периода времени при сопоставимых дозах (50% подавления ЛНП-Х в течение 28 дней после дозы 5 мг/кг и 50% подавления ЛНП-Х в течение примерно 90 дней после дозы 15 мг/кг). По данным измерения ALT и AST не отмечалось заметных или поддающихся измерению изменений в функциях печени. Все животные, получавшие анти-PCSK9 антитело в ходе исследования, демонстрировали быстрое снижение ЛНП-Х и общего холестерина.
Аналогичный эффект снижения ЛНП-Х при воздействии 316P и 300N также наблюдался в яванских макаках, которые получали разовую подкожную (п/к) инъекцию 5 мг/кг 316P или 5 мг/кг 300N (фиг.8). И 316P, и 300N резко подавляют уровни ЛНП-Х и поддерживают эффект снижения ЛНП-Х в течение примерно 15 и 30 дней, соответственно (фиг.8). Фармакодинамический эффект (примерно 40% подавление ЛНП-Х), по-видимому, коррелирует с функциональными уровнями антител в сыворотке обезьян (фиг.9). По мере снижения уровня антител ниже 10 мкг/мл подавление ЛНП-Х также сокращается. Кроме того, 300N демонстрировало существенно более высокий уровень полувыведения из обращения по сравнению с 316P, а значит, более продолжительное наблюдаемое подавление ЛНП-Х.
Пример 14. Снижение распада ЛНП рецепторов антителами анти-hPCSK9
Для оценки биологического воздействия PCSK9 на уровень активности гепаторецепеторов и последующего воздействия на уровни сывороточного ЛНП-Х, hPCSK9 вводили внутривенно мышам, экспрессирующим hPCSK9, но не mPCSK9 (мыши PCSK9 hu/hu). В частности, мышам PCSK9 hu/hu через хвостовую вену вводили ФСБ (контроль) или 1,2 мг/кг hPCSK9-mmh. Через шесть часов после введения hPCSK9 наблюдалось 1,4-кратное увеличение (относительно исходного уровня) по общему холестерину и 2,3-кратное повышение сывороточного ЛНП-Х. Анализ уровней гепаторецепторов ЛНП в отдельной когорте (n=3) животных через 4 часа после введения hPCSK9 продемонстрировал существенное снижение регистрируемых рецепторов ЛНП в гомогенатах печени.
Для оценки биологического воздействия анти-hPCSK9 на уровни гепаторецепторов ЛНП и последующего влияния на уровни сывороточного ЛНП-Х, 316P и неспецифические к hPCSK9 mAb вводили мышам PCSK9 hu/hu в эквивалентной дозе (5 мг/кг в/б) за 20 часов до упомянутого выше введения белка hPCSK9-mmh. Через четыре часа после введения hPCSK9 мышей умерщвляли и брали пробы восьми видов тканей (печень, мозг, легкие, почки, сердце, подвздошная кишка, надпочечники и поджелудочная железа), в которых уровни рецепторов ЛНП определяли вестерн-блоттингом. Изменения в уровнях рецепторов ЛНП наблюдались только в печени. По сравнению с контрольной дозировкой ФСБ введение 316P существенно блокировало опосредованные PCSK9 увеличения общего холестерина и ЛНП холестерина (ЛНП-Х=2,49 мг/дл исходно и 3,1 мг/дл через 6 часов после PCSK9; что соответствует повышению на 25% по сравнению с 135% в присутствии носителя). Предварительное введение неспецифического к hPCSK9 mAb блокировало увеличение ЛНП-Х примерно на 27% по сравнению с чистым ФСБ (ЛНП-Х=4,1 мг/дл по сравнению с наблюдавшихся для ФСБ 5,6 мг/дл). Анализ уровней рецепторов ЛНП в отдельной когорте мышей (n=3 в группе) продемонстрировал существенное снижение уровней ЛНП рецепторов при введении PCSK9, которое блокировалось 316P, но не блокировалось неспецифическим к hPCSK9 mAb (фиг.10).
Эффект воздействия различных доз 316P также оценивали для мышей PCSK9 hu/hu с повышенными уровнями ЛНП-Х и повышенными уровнями hPCSK9. Мыши PCSK9 hu/hu вначале переводили на диету с высоким содержанием углеводов на 8 недель, что приводило к ~2-кратному повышению уровней ЛНП-Х и hPCSK9. Мышам вводили либо 316P, либо неспецифические к hPCSK9 mAb, каждое в дозе 1 мг/кг, 5 мг/кг или 10 мг/кг. Сыворотку собирали через 24 часа после этого и анализировали уровни ЛНП-Х. 316P эффективно снижало уровни ЛНП-Х зависимым от дозы образом (фиг.11). Кроме того, 316P в дозе 10 мг/кг в течение 24 часов быстро снижало уровни ЛНП-Х до исходных (до диеты) (данные не приводятся).
Пример 15. Исследования ФК у мышей
Исследование ФК проводили на мышах C57BL/6 в возрасте 6 недель и на гетерозиготных мышах hPCSK9 в возрасте 11-15 недель. Разовую инъекцию контроля I, 316P или 300N, каждое в дозе 10 мг/кг, проводили п/к. Пробы сыворотки измеряли на предмет уровней hIgG в моменты времени 0 часов (до отбора), 6 часов, день 1, 3, 6, 10, 14, 21, 28, 35, 42 и 56, всего 12 точек по времени с использованием методик захвата анти-hFc и детектирование анти-hFc с помощью сэндвич-ELISA (фиг.12 и 13). Все mAb достигали своего Tmax примерно через 3 дня при соответствующих уровнях Cmax примерно 47-115 мкг/мл для мышей C57BL/6 и 55-196 мкг/мл для гетерозиготных мышей hPCSK9. На 56 день уровни mAb контроля I были примерно 12 мкг/мл, а уровни 300N были примерно 11 мкг/мл, тогда как уровни 316P были несколько меньше 0,02 мкг/мл у мышей C57BL/6. На 56 день у гетерозиготных мышей hPCSK9 уровни mAb контроля I составляли примерно 29 мкг/мл, тогда как уровни 300N и 316P были ниже регистрируемого лимита (BQL) 0,02 мкг/мл.
Пример 16. Связывание анти-hPCSK9 mAb с мутантом/вариантом hPCSK9
Для дальнейшей оценки связывания между hPCSK9 и анти-hPCSK9 mAb получали 21 вариантный белок hPCSK9, каждый из которых содержал одноточечную мутацию, а также два вариантных белка hPCSK9, каждый из которых содержал двойную мутацию. Каждое выбранное антитело удерживалось на поверхности F(ab')2 анти-hIgGп, образованной посредством прямого химического сочетания с чипом BIACORE™ для формирования поверхности связанного антитела. Каждый mmh-меченный вариант hPCSK9 при различных концентрациях от 100 нM до 25 нM затем наносили на поверхность фиксированных антител со скоростью потока 60 мкл/мин в течение 240 секунд, и диссоциацию вариантного hPCSK9 и антитела отслеживали в реальном времени в течение 20 минут при 25°C. НС: в этих экспериментальных условиях связывания не наблюдалось (KD=M×10-9; T1/2=мин; WT=нативный).
Результаты показывают, что в случае мутации остатка D238 аффинность связывания 316Р с hPCSK9 снижалась примерно в >400 раз, с KD примерно 1×10-9 M до 410×10-9 M, а T1/2 укорачивалось примерно в 30 раз, с 37 до 1 минуты, что свидетельствует о связывании 316Р с эпитопом на hPCSK9, содержащим D238 от hPCSK9 (SEQ ID №: 755). Кроме того, анализ по методикам BIACORE™ показывает, что аффинность связывания 316P и T1/2 снижались примерно от 5 до 10 раз, если происходила мутация по остаткам 153, 159 или 343. Конкретно, KD снижалась с примерно 1×10-9 M до примерно 5-8×10-9 M, если происходила мутация любого из остатков S153, E159 или D343; тогда как T1/2 снижалось с примерно 37 минут до примерно 4-6 минут.
Связывание 300N с hPCSK9 снижалось примерно в 50 раз, если происходила мутация остатка в положении 366, что приводило к снижению KD с примерно 0,7×10-9 M до примерно 36×10-9 M и более короткому T1/2 с примерно 120 до 2 минут. Эти результаты свидетельствуют о связывании 300N с эпитопом на hPCSK9, содержащим E366 от hPCSK9 (SEQ ID №: 755). Кроме того, анализ по методикам BIACORE™ показывает, что аффинность связывания 300N и T1/2 снижались от 2 до >10 раз, если происходила мутация по остаткам 147 или 380. В частности, KD снижалась с примерно 0,69×10-9 M до примерно 2-9×10-9 M, если происходила мутация любого из остатков S147 или V380; тогда как T1/2 снижалось с примерно 120 минут до примерно 24-66 минут. По сравнению с 316P связывание 300N с hPCSK9 не ослаблялось из-за мутации по остатку 238.
Напротив, антитело контроля I не проявляло изменения аффинности связывания или T1/2 в результате каких-либо мутаций в испытуемых положениях; антитело контроля II демонстрировало сниженную в 40 раз аффинность при мутации остатка 215 (R215E) (с ~0,1×10-9 до ~4,5×10-9), а T1/2 было примерно в 27 раз короче (с ~333 до 12 минут); тогда как антитело контроля III проявляло пониженную аффинность при мутации остатка 237 (KD уменьшилась с ~0,6×10-9 до ~5,9×10-9, а T1/2 понизилось с ~481 до ~43 минут).
Специфичность связывания 316P, 300N и контрольных анти-hPCSK9 mAb с вариантами hPCSK9-mmh проверяли с использованием иммуноанализа на основе ELISA. Анти-PCSK9 mAb наносили на 96-луночную планшету в течение ночи при 4°C. Каждый mmh-меченный вариант hPCSK9 в супернатантах лизата транзиентной трансфекции CHO-k1 наносили на покрытую антителами планшету при различных концентрациях в диапазоне от 0 до 5 нМ. После 1 часа связывания при комнатной температуре планшету промывали и связанный вариант hPCSK9 определяли с помощью поликлонального HRP-конъюгированного антитела анти-myc (- = OD <0,7; + = OD 0,7-1,5; ++ = OD >1,5).
Пример 17. Воздействие 316P на нормолипидимических и гиперлипидемических хомяков
Способность анти-PCSK9 mAb 316P снижать уровень сывороточного ЛНП-Х испытывали на нормолипидемических или гиперлипидемических золотистых сирийских хомяках (Mesocricetus auratus). Самцы сирийских хомяков в возрасте 6-8 недель весом в интервале 80-100 грамм проходили акклиматизацию в течение 7 дней до начала исследования. Всех животных переводили на диету со стандартным кормом или гиперлипидемическую диету, в ходе которой в корм добавляли 0,1% холестерина и 10% кокосового масла. 316P mAb вводили хомякам в форме разовой подкожной инъекции в дозах 1, 3 или 10 мг/кг нормолипидемических хомяков и в дозах 3, 10 или 30 мг/кг для гиперлипидемических хомяков. Пробы сыворотки отбирали у всех групп через 24 часа и 7, 14 и 22 дня после введения, проводя анализ уровня сывороточных липидов на тот момент времени и сопоставляя его с исходными уровнями в пробах, взятых за 7 дней до введения mAb. Общий холестерин в системе кровообращения и ЛНП-Х у нормолипидемических хомяков был существенно снижен зависимым от дозы образом по сравнению с введением носителя. Как показано на фиг.14, введение 316P эффективно снижало уровни ЛНП-Х почти на 60% через семь дней после введения самой высокой из испытываемых доз (10 мг/кг). Подобный эффект снижения холестерина при введении 316P у гиперлипидемических хомяков не наблюдался.
| название | год | авторы | номер документа |
|---|---|---|---|
| ВЫСОКОАФФИННЫЕ ЧЕЛОВЕЧЕСКИЕ АНТИТЕЛА К PCSK9 | 2009 |
|
RU2697773C2 |
| АНТИТЕЛА ЧЕЛОВЕКА К PCSK9 ДЛЯ ПРИМЕНЕНИЯ В СПОСОБАХ ЛЕЧЕНИЯ КОНКРЕТНЫХ ГРУПП ИНДИВИДУУМОВ | 2012 |
|
RU2603481C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ АНТИТЕЛА К PCSK9 ЧЕЛОВЕКА | 2012 |
|
RU2604139C2 |
| АНТИТЕЛА АНТИ-ANGPTL3 И ИХ ПРИМЕНЕНИЕ | 2012 |
|
RU2620064C2 |
| АНТАГОНИСТЫ PCSK9 | 2009 |
|
RU2528735C2 |
| АНТИТЕЛА ЧЕЛОВЕКА К PCSK9 ДЛЯ ПРИМЕНЕНИЯ В СПОСОБАХ ЛЕЧЕНИЯ КОНКРЕТНЫХ ГРУПП ИНДИВИДУУМОВ | 2012 |
|
RU2721279C2 |
| АНТАГОНИСТЫ PCSK9 | 2014 |
|
RU2618869C2 |
| АНТАГОНИСТЫ | 2019 |
|
RU2839429C2 |
| АНТИТЕЛА С РН-ЗАВИСИМЫМ СВЯЗЫВАНИЕМ АНТИГЕНА | 2011 |
|
RU2570729C2 |
| АНТИ-PCSK9 АНТИТЕЛО, ЕГО АНТИГЕНСВЯЗЫВАЮЩИЙ ФРАГМЕНТ И ИХ МЕДИЦИНСКОЕ ПРИМЕНЕНИЕ | 2016 |
|
RU2739208C2 |
































































































































































































































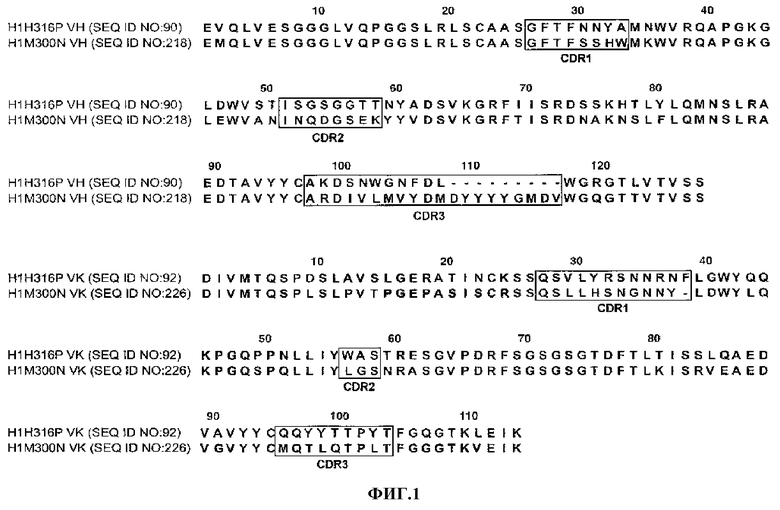
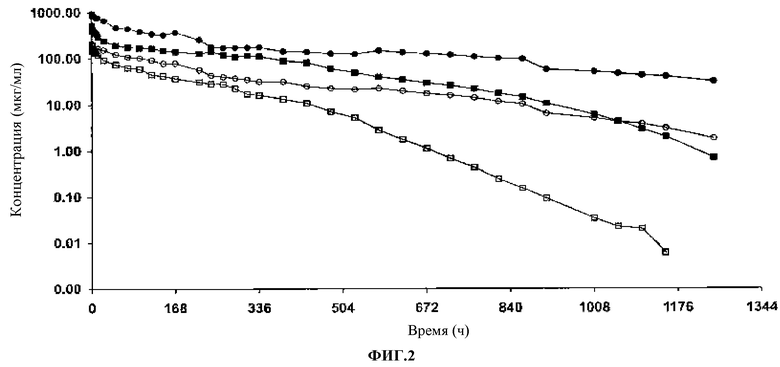
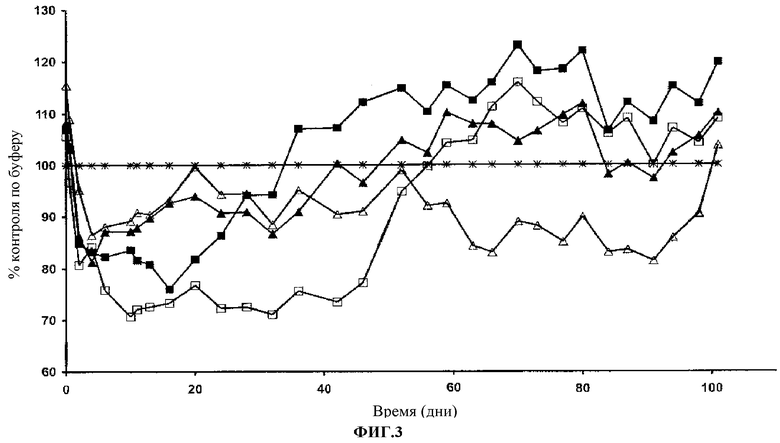
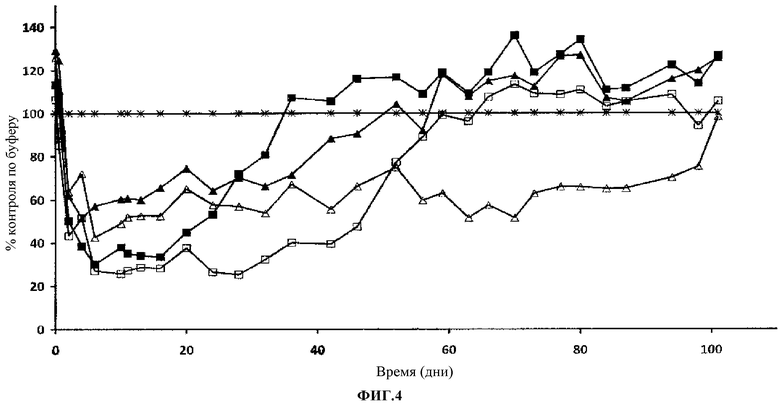
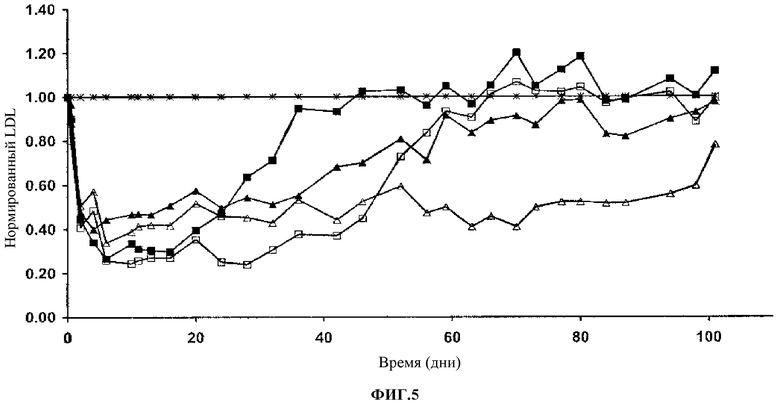
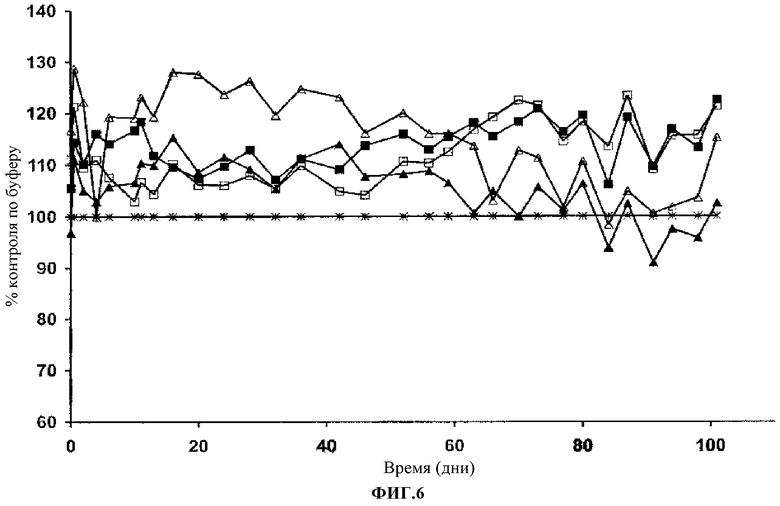
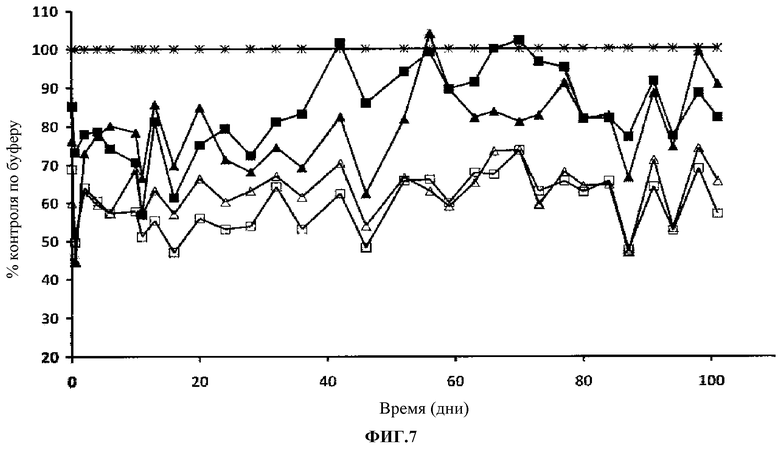
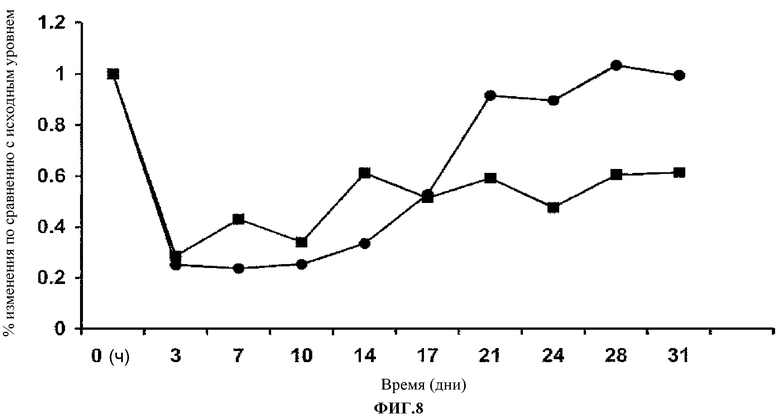
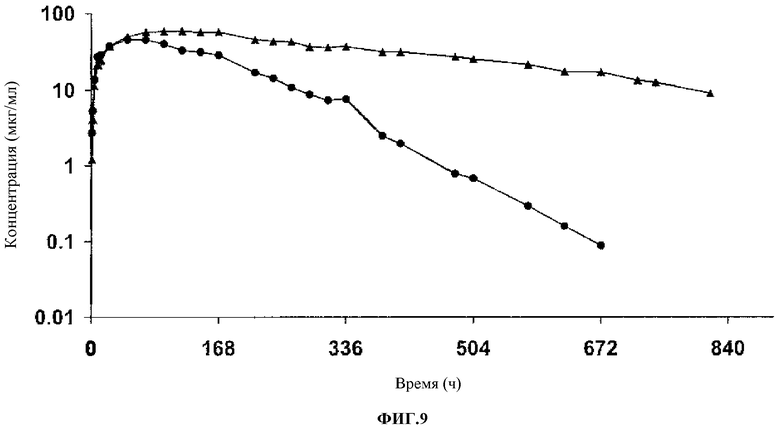
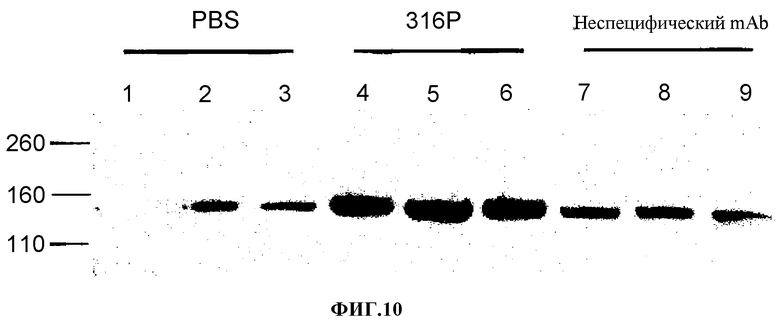
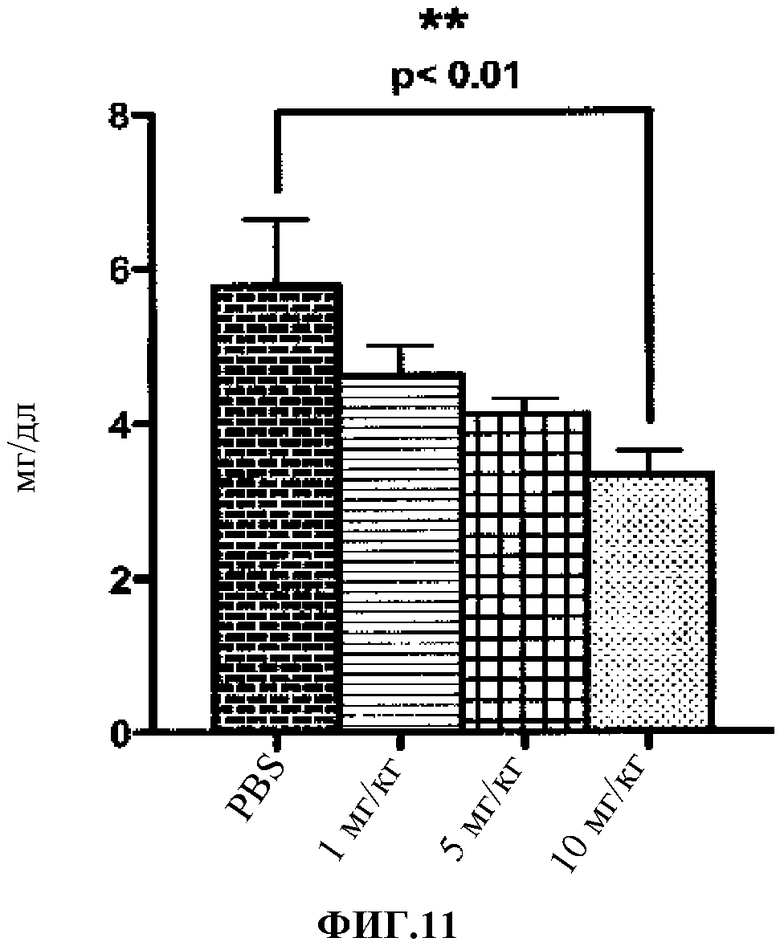
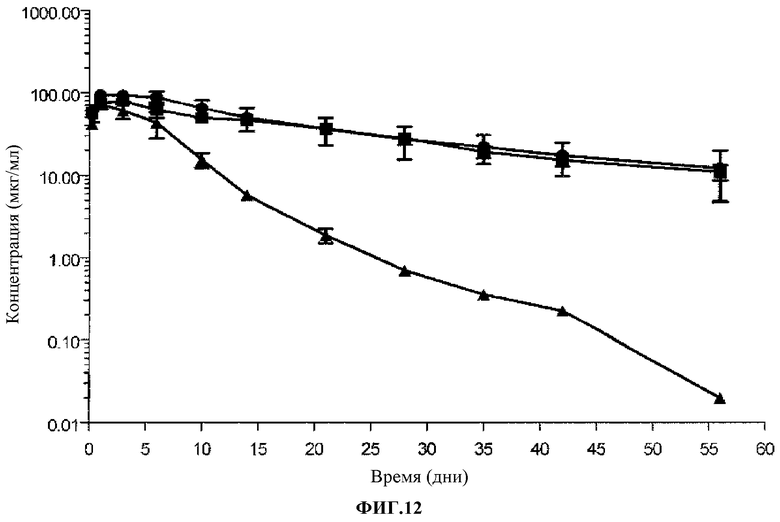
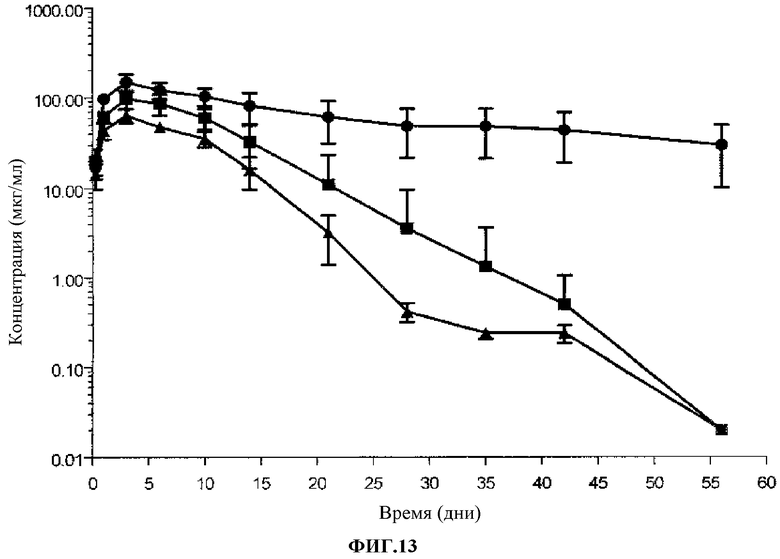
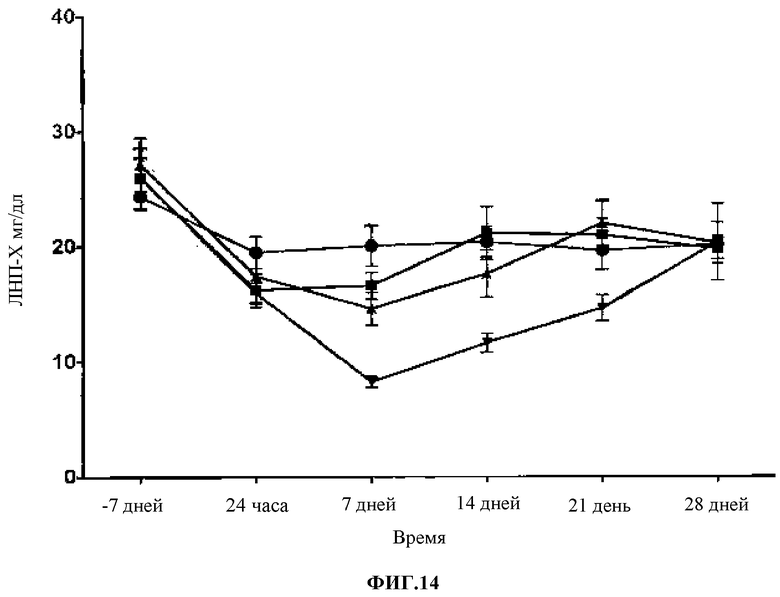
Предложенное изобретение относится к области иммунологии. Раскрыты варианты антитело человека или антиген-связывающий фрагмент антитела человека, которые специфическим образом связывают и ингибируют человеческую пропротеинконвертазу субтилизин/кексин тип 9 («hPCSK9»). Каждый вариант характеризуется тем, что содержит 6 CDR тяжелой и легкой цепи. Описаны: изолированная кодирующая нуклеиновая кислота, вектор экспрессии и способ получения антитела с использованием указанного вектора. Предложен фармацевтический состав на основе антитела для лечения заболевания или состояния, которое поддается смягчению, улучшению, подавлению или предотвращению с помощью антитела к PCSK9. Использование изобретения обеспечивает новые варианты антител, способные снижать сывороточный ЛНП холестерин при незначительных изменениях или отсутствии воздействия на функции печени, по данным измерения AЛТ и AСT. 5 н. и 3 з.п. ф-лы, 14 ил., 28 табл., 17 пр.
1. Антитело человека или антигенсвязывающий фрагмент антитела человека, который специфическим образом связывает человеческую пропротеинконвертазу субтилизин/кексин тип 9 («hPCSK9»), где антитело или антигенсвязывающий фрагмент содержит CDR последовательности тяжелой и легкой цепи, представленные последовательностями SEQ ID NO:76, 78, 80, 84, 86, 88 или SEQ ID NO: 220, 222, 224, 228, 230, 232.
2. Антитело или антигенсвязывающий фрагмент по п.1, содержащее пару аминокислотных последовательностей вариабельной области тяжелой цепи/вариабельной области лёгкой цепи (HCVR/LCVR), представленной последовательностями SEQ ID №: 90/92 или 218/226.
3. Изолированная молекула нуклеиновой кислоты, кодирующая антитело или антигенсвязывающий фрагмент по п.1 или 2.
4. Вектор экспрессии для получения антитела по п.1, содержащий молекулу нуклеиновой кислоты по п.3.
5. Способ производства антитела анти-PCSK9 человека или антигенсвязывающего фрагмента антитела по п.1, состоящий из стадий введения вектора экспрессии по п.4 в изолированную клетку-хозяина, выращивания клетки в условиях, допускающих производство антитела или его фрагмента, и получения антитела или его фрагмента, произведенного таким образом.
6. Фармацевтический состав для лечения заболевания или состояния, которое поддается смягчению, улучшению, подавлению или предотвращению с помощью антагониста PCSK9, включающий антитело или антигенсвязывающий фрагмент по п.1 или 2 в терапевтически эффективном количестве и фармацевтически приемлемый носитель.
7. Фармацевтический состав по п.6, дополнительно включающий второй терапевтический агент, где второй терапевтический агент выбран из группы, состоящей из одного из ингибиторов 3-гидрокси-3-метилглутарил (HMG)-коэнзима A (CoA) редуктазы, статина, ингибитора захвата холестерина или реабсорбции желчных кислот, агента, повышающего катаболизм липопротеинов, и активатора фактора транскрипции LXR.
8. Фармацевтический состав по п.6, где опосредованное PCSK9 заболевание или состояние выбрано из группы, состоящей из гиперхолестеринемии, гиперлипидемии, афереза ЛВП, гетерозиготной наследственной гиперхолестеринемии, непереносимости статинов, неконтролируемости статинами, риска развития гиперхолестеринемии, дислипидемии, холестатического заболевания печени, нефротического синдрома, гипотироидизма, ожирения, атеросклероза и сердечно-сосудистых заболеваний.
| WO2008125623 A2, 23.10.2008 | |||
| WO2008057459 A2, 15.05.2008 | |||
| LAGACE et al., "Secreted PCSK9 decreases the number of LDL receptors in hepatocytes and in livers of parabiotic mice", J | |||
| Clin | |||
| Invest, 116:2995-3005 (2006), doi:10.1172/JCI29383 | |||
| РОЙТ и др | |||
| "Иммунология", М.: Мир, 2000, стр.111, 150-151 |
Авторы
Даты
2015-06-10—Публикация
2009-12-15—Подача