ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Изобретение относится к антагонистам пропротеиновой конвертазы субтилизин-кексинового типа 9 (PCSK9), таким как антитела и их фрагменты, а также к способам, применению и комбинациям.
УРОВЕНЬ ТЕХНИКИ
Пропротеиновая конвертаза субтилизин-кексинового типа 9 (PCSK9) представляет собой сериновую протеазу, участвующую в регуляции уровней белка рецептора липопротеинов низкой плотности (LDLR) (Horton et al., 2007; Seidah and Prat, 2007). Эксперименты in vitro показали, что добавление PCSK9 к клеткам HepG2 снижает уровни LDLR на клеточной поверхности (Benjannet et al., 2004; Lagace et al., 2006; Maxwell et al., 2005; Park et al., 2004). Эксперименты на мышах показали, что повышение уровней белка PCSK9 снижает уровени белка LDLR в печени (Benjannet et al., 2004; Lagace et al., 2006; Maxwell et al., 2005; Park et al., 2004), тогда как мыши, нокаутные по PCSK9, имеют повышенные уровни LDLR в печени (Rashid et al., 2005). Кроме того, были идентифицированы различные мутации PCSK9 человека, которые приводят либо к увеличению, либо к снижению уровней ЛПНП в плазме (Kotowski et al., 2006; Zhao et al., 2006). PCSK9, как было показано, напрямую взаимодействует с белком LDLR, подвергается эндоцитозу вместе с LDLR и коиммунофлуоресцирует с LDLR по всему эндосомальному пути (Lagace et al., 2006).
PCSK9 представляет собой прогормональную пропротеиновую конвертазу из семейства сериновых протеаз субтилизина (S8) (Seidah et al., 2003). У людей есть девять прогормональных пропротеиновых конвертаз, которые можно разделить на подсемейства S8A и S8B (Rawlings et al., 2006). В подсемействе S8B выделяют фурин, РС1/РС3, РС2, РАСЕ4, РС4, РС5/РС6 и PC7/PC8/LPC/SPC7. Кристаллические и ЯМР-структуры различных доменов фурина и РС1 мыши выявляют субтилизин-подобные про- и каталитические домены, а также Р-домен непосредственно на С-конце каталитического домена (Henrich et al., 2003; Tangrea et al., 2002). На основании сходства аминокислотных последовательностей внутри этого подсемейства предполагается, что все семь членов имеют сходные структуры (Henrich et al., 2005). В подсемействе S8A выделяют SKI-1/S1P и PCSK9. Сравнение последовательностей этих белков также указывает на присутствие субтилизин-подобных про- и каталитических доменов (Sakai et al., 1998; Seidah et al., 2003; Seidah et al., 1999). В этих белках аминокислотная последовательность С-конца каталитического домена более вариабельна и не предполагает наличия Р-домена.
Конвертазы прогормона-пропротеина экспрессируются в виде зимогенов и созревают в многоэтапном процессе. Функция продомена в этом процессе двоякая. Продомен сначала действует как шаперон и необходим для правильной укладки каталитического домена (Ikemura et al., 1987). Как только каталитический домен свернут, между продоменом и каталитическим доменом происходит автокатализ. После этой начальной реакции расщепления продомен остается связанным с каталитическим доменом, где он затем действует как ингибитор каталитической активности (Fu et al., 2000). Когда условия подходящие, созревание протекает со вторым автокаталитическим явлением на сайте внутри продомена (Anderson et al., 1997). После этого второго явления расщепления продомен и каталитический домен диссоциируют, давая начало активной протеазе.
Автокатализ зимогена PCSK9 происходит между Gln152 и Ser153 (VFAQ|SIP (SEQ ID №67)) (Naureckiene et al., 2003), и было показано, что он необходим для его секреции из клеток (Seidah et al., 2003). Второго автокаталитического явления на сайте в продомене PCSK9 не наблюдалось. Очищенный PCSK9 состоит из двух типов молекул, которые можно разделить с помощью невосстанавливающего электрофореза ДСН-ПААГ (SDS-PAGE); продомена с массой 17 кДа и каталитических плюс С-концевых доменов с массой 65 кДа. PCSK9 не был выделен без своего ингибирующего продомена, а измерения каталитической активности PCSK9 были различными (Naureckiene et al., 2003; Seidah et al., 2003).
В некоторых вариантах осуществления изобретения полипептид PCSK9 включает концевые остатки, такие как, но не ограничиваясь ими, остатки лидерной последовательности, целевые остатки, аминоконцевые остатки метионина, остатки лизина, остатки метки и/или остатки слитого белка. «PCSK9» также обозначается как FH3, NARC1, HCHOLA3, пропротеиновая конвертаза субтилизин/кексинового типа 9 и регулируемая нейрональным апоптозом конвертаза 1. Ген PCSK9 кодирует белок пропротеиновой конвертазы, который принадлежит к подсемейству протеиназы К семейства секреторных субтилаз.
Термин «PCSK9» обозначает как пропротеин, так и продукт, образованный после автокатализа пропротеина. Когда упоминается только продукт, полученный в результате автокатализа (например, в случае антигенсвязывающего белка или лиганда, который связывается с расщепленным PCSK9), белок может называться «зрелым», «расщепленным», «процессированным» или «активным» PCSK9. Когда упоминается только неактивная форма, белок может называться «неактивной», «про-формой» или «непроцессированной» формой PCSK9. Термин PCSK9 также включает молекулы PCSK9, включающие посттрансляционные модификации аминокислотной последовательности PCSK9, такие как гликозилированные последовательности PCSK9, последовательности PCSK9, от которых отщеплена его сигнальная последовательность, последовательность PCSK9, в которой его продомен был отщеплен от каталитического домена, но которая не отделена от каталитического домена (см., например, Фиг. 1А и 1В в US 20120093818 А1).
PCSK9 контролирует экспрессию рецептора липопротеинов низкой плотности (ЛПНП) в печени, способствуя лизосомальной деградации рецептора. Ингибирование PCSK9 приводит к повышенной экспрессии рецептора ЛПНП в гепатоцитах и к снижению уровня холестерина в плазме за счет увеличения клиренса частиц ЛПНП печенью. Лечение моноклональными антителами к PCSK9 является клинически успешным терапевтическим вмешательством у пациентов с диагнозом гиперлипидемия или гиперхолестеринемия, которые не отвечают на лечение статинами. Антитело к PCSK9 алирокумаб продается Regeneron Pharmaceuticals, Inc под названием Praluent™. Антитело к PCSK9 эволокумаб продается Amgen, Inc под названием Repatha™.
ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
В первой конфигурации в изобретении предложены:
Антитело или фрагмент, содержащий сайт связывания, который специфически связывается с пропротеиновой конвертазой субтилизин-кексинового типа 9 (PCSK9), причем сайт связывания включает домен VH, который кодируется нуклеотидной последовательностью, полученной в результате рекомбинации сегмента гена VH, сегмента гена DH и сегмента гена JH человека, при этом сегмент гена VH выбран из IGHV4-31, IGHV4-59, IGHV4-4 и IGHV3-9.
Во второй конфигурации в изобретении предложены:
Антитело или фрагмент, которые специфически связываются с PCSK9 и содержат последовательность CDRH3 антитела к PCSK9 по изобретению или указанную последовательность CDRH3, содержащую 3, 2 или 1 аминокислотную замену(-ы).
В третьей конфигурации в изобретении предложены:
Антитело или фрагмент (необязательно по любому предыдущему пункту), которые специфически связывается с PCSK9 и содержат домен VH, который содержит последовательность CDRH3 антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или указанную последовательность, содержащую 3, 2 или 1 аминокислотную замену(-ы).
В четвертой конфигурации в изобретении предложены:
Антитело или фрагмент, содержащие сайт связывания, который специфически связывается с PCSK9, причем сайт связывания содержит домен VH, который содержит аминокислотную последовательность домена VH антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или аминокислотную последовательность, которая идентична ей по меньшей мере на 70%.
В пятой конфигурации в изобретении предложены:
Антитело или фрагмент (необязательно по любому предыдущему пункту), содержащие сайт связывания, который специфически связывается с PCSK9, причем сайт связывания содержит домен VL, который кодируется нуклеотидной последовательностью, полученной путем рекомбинации сегмента гена VL и сегмента гена JL человека, причем сегмент гена VL выбран из IGKV3-11, IGKV2-28 и IGKV2-29.
В шестой конфигурации в изобретении предложены:
Антитело или фрагмент, которые специфически связываются с PCSK9 и содержат последовательность CDRL3 антитела к PCSK9 по изобретению или указанную последовательность CDRL3, содержащую 3, 2 или 1 аминокислотную замену(-ы).
В седьмой конфигурации в изобретении предложены:
Антитело или фрагмент, которые специфически связываются с PCSK9 и содержат домен VL, который содержит последовательность CDRL3 (и необязательно CDRH3) антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или указанную последовательность(-и), каждая из которых содержит 3, 2 или 1 аминокислотную замену(-ы).
В восьмой конфигурации в изобретении предложены:
Антитело или фрагмент, содержащие сайт связывания, который специфически связывается с PCSK9, причем сайт связывания содержит домен VL, который содержит аминокислотную последовательность домена VL антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или аминокислотную последовательность, которая идентична ей по меньшей мере на 70%.
В девятой конфигурации в изобретении предложены:
Антитело или фрагмент, которые специфически связываются с PCSK9 и содержат аминокислотную последовательность тяжелой цепи антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или аминокислотную последовательность, которая идентична ей по меньшей мере на 70%.
В десятой конфигурации в изобретении предложены:
Антитело или фрагмент, которые специфически связываются с PCSK9 и содержат аминокислотную последовательность легкой цепи антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или аминокислотную последовательность, которая идентична ей по меньшей мере на 70%.
В одиннадцатой конфигурации в изобретении предложены:
Антитело или фрагмент, которые специфически связываются с эпитопом PCSK9 человека, идентичным эпитопу, с которым связывается антитело по изобретению (например, CL-274711 или CL-148219QLT).
В двенадцатой конфигурации в изобретении предложены:
Антитело или фрагмент, которые конкурируют за связывание с PCSK9 человека с антителом по изобретению.
В тринадцатой конфигурации в изобретении предложены:
Антитело или фрагмент к PCSK9 по изобретению для лечения или профилактики PCSKS-опосредованного заболевания или патологического состояния (необязательно гиперлипидемии или гиперхолестеринемии) у субъекта.
В четырнадцатой конфигурации в изобретении предложена: Комбинация количества антитела или фрагмента к PCSK9 и количества статина (необязательно включающая несколько доз указанного антитела и/или статина), причем указанное антитело или фрагмент соответствуют изобретению.
Комбинация количества антитела или фрагмента к PCSK9 и количества ингибитора ANGPTL3 (например, антитела к ANGPTL3, например эвинакумаба) (необязательно включающая несколько доз указанного антитела и/или статина), причем указанное антитело или фрагмент соответствуют изобретению. Необязательно комбинация также включает статин.
В пятнадцатой конфигурации в изобретении предложено:
Применение антитела, фрагмента или комбинации по изобретению при производстве лекарственного препарата для введения субъекту для лечения или профилактики PCSK9-опосредованного заболевания или патологического состояния, необязательно гиперлипидемии или гиперхолестеринемии.
В шестнадцатой конфигурации в изобретении предложен:
Способ лечения или профилактики PCSK9-опосредованного заболевания или патологического состояния у субъекта (необязательно гиперлипидемии или гиперхолестеринемии), включающий введение указанному субъекту терапевтически эффективного количества антитела, фрагмента или комбинации по изобретению, при этом тем самым лечится или предотвращается PCSK9-опосредованное заболевание или патологическое состояние.
В семнадцатой конфигурации в изобретении предложена:
Фармацевтическая композиция, содержащая антитело, фрагмент или комбинацию по изобретению и фармацевтически приемлемое вспомогательное вещество, разбавитель или носитель.
В восемнадцатой конфигурации в изобретении предложена:
Нуклеиновая кислота, кодирующая домен VH и/или домен VL антитела или фрагмента по изобретению.
В девятнадцатой конфигурации в изобретении предложена:
Нуклеиновая кислота, которая кодирует домен VH, содержащий аминокислотную последовательность домена VH антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или аминокислотную последовательность, которая идентична ей по меньшей мере на 70%.
В двадцатой конфигурации в изобретении предложена:
Нуклеиновая кислота, кодирующая тяжелую цепь и/или легкую цепь антитела или фрагмента по изобретению.
В двадцать первой конфигурации в изобретении предложен:
Вектор, содержащий нуклеиновую кислоту(-ы); при этом необязательно вектор представляет собой вектор СНО или HEK293.
В двадцать второй конфигурации в изобретении предложена:
Клетка-хозяин, содержащая нуклеиновую кислоту(-ы) или вектор.
В двадцать третьей конфигурации в изобретении предложены:
Антитело, фрагмент, комбинация, вектор, клетка-хозяин, применение или способ, как описано в данном документе.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Фигура 1: нейтрализация hPCSK9 с помощью CL-148219 в сравнении с контрольными антителами.
Фигура 2: восстановление захвата ЛПНП с помощью CL-148219 по сравнению с контрольными антителами.
Фигура 3: аффинность CL-148219 в сравнении с контрольными антителами.
Фигура 4: снижение уровня не-ЛПВП в плазме крови с помощью CL-148219 по сравнению с контрольными антителами.
Фигура 5: нейтрализация hPCSK9 с помощью CL-148489 в сравнении с контрольными антителами.
Фигура 6: восстановление захвата ЛПНП с помощью CL-148489 по сравнению с контрольными антителами.
Фигура 7: аффинность CL-148489 в сравнении с контрольными антителами.
Фигура 8: снижение уровня не-ЛПВП в плазме крови с помощью CL-148489 по сравнению с контрольными антителами.
Фигура 9: дизайн исследования.
Фигура 10: общий холестерин.
Фигура 11: общий холестерин, не относящийся кЛПВП.
Фигура 12: холестерин ЛПВП.
Фигура 13: триглицериды.
Фигура 14: профиль фосфолипидов и холестерина.
Фигура 15: показывает влияние однократной подкожной дозы 1 мг/кг CL-148219 QLT, контрольного антитела F (коммерчески продаваемое антитело) или однократной подкожной дозы 10 мг/кг изотипического контроля на уровни общего холестерина (±SEM) трансгенных мышей APOE*3Leiden.CETP, которые находились на диете западного типа, содержащей 0,15% холестерина и 15% насыщенных жиров.
Фигура 16: показывает влияние однократной подкожной дозы 3 мг/кг CL-148219 QLT, контрольного антитела F или однократной подкожной дозы 10 мг/кг изотипического контроля на уровни общего холестерина (±SEM) трансгенных мышей APOE*3Leiden.CETP, которые находились на диете западного типа, содержащей 0,15% холестерина и 15% насыщенных жиров.
Фигура 17: показывает влияние однократной подкожной дозы 10 мг/кг CL-148219 QLT, контрольного антитела F или изотипического контроля на уровни общего холестерина (±SEM) трансгенных мышей APOE*3Leiden.CETP, которые находились на диете западного типа, содержащей 0,15% холестерина и 15% насыщенных жиров.
Фигура 18: сравнение эффектов однократной подкожной дозы 1 мг/кг CL-148219 QLT с дозой 1 и 3 мг/кг контрольного антитела F на уровни общего холестерина (±SEM) у трансгенных мышей APOE*3Leiden.CETP, которые находились на диете западного типа, содержащей 0,15% холестерина и 15% насыщенных жиров.
Фигура 19: сравнение эффектов однократной подкожной дозы 3 мг/кг CL-148219 QLT с дозой 3 и 10 мг/кг контрольного антитела F на уровни общего холестерина (±SEM) у трансгенных мышей APOE*3Leiden.CETP, которые находились на диете западного типа, содержащей 0,15% холестерина и 15% насыщенных жиров.
Фигура 20: показывает эффекты однократной подкожной дозы 1 (А), 3 (В) или 10 мг/кг (С) CL-148219 QLT/контрольного антитела F, 1 и 3 мг/кг CL-274711 (А, В) или 10 мг/кг изотипического контроля на уровни холестерина, не относящегося к ЛПВП, (±SEM) у трансгенных мышей APOE*3Leiden.CETP, которые находились на диете западного типа, содержащей 0,15% холестерина и 15% насыщенных жиров.
Фигура 21: Сравнение эффектов однократной подкожной дозы 1 (А) и 3 мг/кг (В) CL-148219 QLT с дозами 1 и 3 (А) или 3 и 10 мг/кг (В) контрольного антитела F на уровни холестерина, не относящегося к ЛПВП, (±SEM) у трансгенных мышей APOE*3Leiden.CETP, которые находились на диете западного типа, содержащей 0,15% холестерина и 15% насыщенных жиров.
Фигура 22: показаны профили липопротеинов (А - холестерин ЛПОНП, В - фосфолипиды ЛПОНП, С - холестерин ЛПНП, D - фосфолипиды ЛПНП) после однократного подкожного введения дозы 1, 3 или 10 мг/кг контрольного антитела F/CL-148219 QLT, дозы 3 или 10 мг/кг CL-274711 или 10 мг/кг изотипического контроля у трансгенных мышей APOE*3Leiden.CETP, которые находились на диете западного типа, содержащей 0,15% холестерина и 15% насыщенных жиров; и
Фигура 23: показывает концентрации антител (±SEM) с течением времени после однократного подкожного введения 3 мг/кг контрольного антитела F, CL-148219 QLT или CL-274711 самцам мышей C57/BI6.
Фигура 1. CL-148219 нейтрализовал интернализацию PCSK9 человека больше, чем контрольные антитела в клеточном анализе in vitro. Клетки HepG2 обрабатывали АР647-меченным мутантным вариантом человека PCSK9 с увеличенной функцией в присутствии изотипического контроля, контрольных антител или CL-148219 с последующей обработкой ЛПНП BODIPY. Затем клетки собирали и детектировали флуоресцентные сигналы AF647 проточным цитометром CytoFlex™.
Фигура 24: CL-148219 нейтрализовал интернализацию PCSK9 человека больше, чем контрольные антитела в клеточном анализе in vitro. Клетки HepG2 обрабатывали АР647-меченным мутантным вариантом человека PCSK9 с увеличенной функцией в присутствии изотипического контроля, контрольных антител или CL-148219 с последующей обработкой ЛПНП BODIPY. Затем клетки собирали и детектировали флуоресцентные сигналы AF647 проточным цитометром CytoFlex™.
Фигура 25: CL-148219 увеличивал захват ЛПНП лучше, чем контрольные антитела в клеточном анализе in vitro. Клетки HepG2 обрабатывали AF647-меченным мутантным вариантом человека PCSK9 с увеличенной функцией в присутствии изотипического контроля, контрольных антител или CL-148219 с последующей обработкой ЛПНП BODIPY. Затем клетки собирали и детектировали флуоресцентные сигналы BODIPY с помощью проточного цитометра CytoFlex.
Фигура 26: Аффинность CL-148219. Аффинность определяли по KD. KD CL-148219 измеряли по отношению к PCSK9 человека и мыши при рН 7,6 с помощью системы анализа SPR Proteon™.
Фигура 27: CL-148219 продемонстрировал превосходную функцию снижения холестерина, не относящегося к ЛПВП, по сравнению с контрольными антителами в мышиной модели гиперлипидемии (мыши E3L.CETP). Мыши E3L.CETP находились на диете западного типа в течение 4 недель с последующей инъекцией антител. В разное время после инъекции АЬ собирали кровь и измеряли количество ЛПВП и общего холестерина в плазме. Затем рассчитывали количество холестерина, не относящегося к ЛПВП, в плазме путем вычитания ЛПВП из общего холестерина.
Фигура 28: CL-148219 QLT нейтрализовал интернализацию PCSK9 человека больше, чем контрольные антитела в клеточном анализе in vitro. Клетки HepG2 обрабатывали АР647-меченным мутантным вариантом человека PCSK9 с увеличенной функцией в присутствии изотипического контроля, контрольных антител или CL-148219 QLT с последующей обработкой ЛПНП BODIPY. Затем клетки собирали и детектировали флуоресцентные сигналы AF647 проточным цитометром CytoFlex.
Фигура 29: CL-148219 QLT увеличивал захват ЛПНП лучше, чем контрольные антитела в клеточном анализе in vitro. Клетки HepG2 обрабатывали AF647-меченным мутантным вариантом человека PCSK9 с увеличенной функцией в присутствии изотипического контроля, контрольных антител или CL-148219 QLT с последующей обработкой ЛПНП BODIPY. Затем клетки собирали и детектировали флуоресцентные сигналы BODIPY с помощью проточного цитометра CytoFlex.
Фигура 30: Аффинность CL-148219 QLT. Аффинность определяли по KD. KD CL-148219 QLT измеряли по отношению к PCSK9 человека и мыши при рН 7,6 с помощью системы анализа SPR Proteon.
Фигура 31: CL-148219 QLT продемонстрировал превосходную функцию снижения холестерина, не относящегося к ЛПВП, по сравнению с контрольными антителами в мышиной модели гиперлипидемии (мыши E3L.CETP). Мыши E3L.CETP находились на диете западного типа в течение 4 недель с последующей инъекцией антител. В разное время после инъекции Ab собирали кровь и измеряли количество ЛПВП и общего холестерина в плазме. Затем рассчитывали количество холестерина, не относящегося к ЛПВП, в плазме путем вычитания ЛПВП из общего холестерина.
Фигура 32: CL-148489 умеренно нейтрализовал интернализацию PCSK9 человека в клеточном анализе in vitro. Клетки HepG2 обрабатывали АР647-меченным мутантным вариантом человека PCSK9 с увеличенной функцией в присутствии изотипического контроля, контрольных антител или CL-148489 с последующей обработкой ЛПНП BODIPY. Затем клетки собирали и детектировали флуоресцентные сигналы AF647 проточным цитометром CytoFlex.
Фигура 33: CL-148489 увеличивал захват ЛПНП лучше, чем контрольные антитела в клеточном анализе in vitro. Клетки HepG2 обрабатывали AF647-меченным мутантным вариантом человека PCSK9 с увеличенной функцией в присутствии изотипического контроля, контрольных антител или CL-148489 с последующей обработкой ЛПНП BODIPY. Затем клетки собирали и детектировали флуоресцентные сигналы BODIPY с помощью проточного цитометра CytoFlex.
Фигура 34: Аффинность CL-148489. Аффинность определяли по KD. KD CL-148489 измеряли по отношению к PCSK9 человека и мыши при рН 7,6 с помощью системы анализа SPR Proteon.
Фигура 35: CL-148489 продемонстрировал превосходную функцию снижения холестерина, не относящегося к ЛПВП, по сравнению с контрольными антителами в мышиной модели гиперлипидемии (мыши E3L.CETP). Мыши E3L.CETP находились на диете западного типа в течение 4 недель с последующей инъекцией антител. В разное время после инъекции АЬ собирали кровь и измеряли количество ЛПВП и общего холестерина в плазме. Затем рассчитывали количество холестерина, не относящегося к ЛПВП, в плазме путем вычитания ЛПВП из общего холестерина.
Фигура 36: CL-274698 нейтрализовал интернализацию PCSK9 человека больше, чем контрольные антитела в клеточном анализе in vitro. Клетки HepG2 обрабатывали АР647-меченным мутантным вариантом человека PCSK9 с увеличенной функцией в присутствии изотипического контроля, контрольных антител или CL-274698 с последующей обработкой ЛПНП BODIPY. Затем клетки собирали и детектировали флуоресцентные сигналы AF647 проточным цитометром CytoFlex.
Фигура 37: CL-274698 увеличивал захват ЛПНП лучше, чем контрольные антитела в клеточном анализе in vitro. Клетки HepG2 обрабатывали AF647-меченным мутантным вариантом человека PCSK9 с увеличенной функцией в присутствии изотипического контроля, контрольных антител или CL-274698 с последующей обработкой ЛПНП BODIPY. Затем клетки собирали и детектировали флуоресцентные сигналы BODIPY с помощью проточного цитометра CytoFlex.
Фигура 38: Аффинность CL-274698. Аффинность определяли по KD. KD CL-274698 измеряли по отношению к PCSK9 человека и мыши при рН 7,6 с помощью системы анализа SPR Proteon.
Фигура 39: CL-274698 продемонстрировал превосходную функцию снижения холестерина, не относящегося к ЛПВП, по сравнению с контрольными антителами в мышиной модели гиперлипидемии (мыши E3L.CETP). Мыши E3L.CETP находились на диете западного типа в течение 4 недель с последующей инъекцией антител. В разное время после инъекции Ab собирали кровь и измеряли количество ЛПВП и общего холестерина в плазме. Затем рассчитывали количество холестерина, не относящегося к ЛПВП, в плазме путем вычитания ЛПВП из общего холестерина.
Фигура 40: CL-274711 нейтрализовал интернализацию PCSK9 человека сильнее, чем контрольные антитела в клеточном анализе in vitro. Клетки HepG2 обрабатывали АР647-меченным мутантным вариантом человека PCSK9 с увеличенной функцией в присутствии изотипического контроля, контрольных антител или CL-274711 с последующей обработкой ЛПНП BODIPY. Затем клетки собирали и детектировали флуоресцентные сигналы AF647 проточным цитометром CytoFlex.
Фигура 41: CL-274711 увеличивал захват ЛПНП лучше, чем контрольные антитела в клеточном анализе in vitro. Клетки HepG2 обрабатывали AF647-меченным мутантным вариантом человека PCSK9 с увеличенной функцией в присутствии изотипического контроля, контрольных антител или CL-274711 с последующей обработкой ЛПНП BODIPY. Затем клетки собирали и детектировали флуоресцентные сигналы BODIPY с помощью проточного цитометра CytoFlex.
Фигура 42: Аффинность CL-274711. Аффинность определяли по KD. KD CL-274711 измеряли по отношению к PCSK9 человека и мыши при рН 7,6 с помощью системы анализа SPR Proteon.
Фигура 43: CL-274711 продемонстрировал превосходную функцию снижения холестерина, не относящегося к ЛПВП, по сравнению с контрольными антителами в мышиной модели гиперлипидемии (мыши E3L.CETP). Мыши E3L.CETP находились на диете западного типа в течение 4 недель с последующей инъекцией антител. В разное время после инъекции Ab собирали кровь и измеряли количество ЛПВП и общего холестерина в плазме. Затем рассчитывали количество холестерина, не относящегося к ЛПВП, в плазме путем вычитания ЛПВП из общего холестерина.
ПОДРОБНОЕ ОПИСАНИЕ
Определения
Если в данном документе не определено иное, научные и технические термины имеют значения, которые обычно понимаются специалистами в данной области техники. Кроме того, если иное не требуется по контексту, термины в единственном числе должны включать множественное число, а термины во множественном числе должны включать единственное число. Термины в единственном числе включают в себя эквиваленты во множественном числе, если контекст явно не указывает иное. Аналогично, слово «или» подразумевает включение «и», если контекст явно не указывает иное. Хотя способы и материалы, аналогичные или эквивалентные описанным в данном документе, могут быть использованы при практическом осуществлении или при тестировании данного раскрытия, подходящие способы и материалы описаны ниже. Слово «например» аналогично латинскому exempli gratia и используется в данном документе для обозначения неограничивающего примера. Таким образом, слово «например» является синонимом термина «к примеру». В описании и формуле изобретения термин «около» используется для модификации, например, количества ингредиента в композиции, концентрации, объема, температуры процесса, времени процесса, выхода, скорости потока, давления и подобных величин, а также их диапазонов, используемых при описании вариантов осуществления изобретения. Термин «около» относится к изменению числового количества, которое может происходить, например, в результате типичных процедур измерения и обработки, используемых для изготовления соединений, композиций, концентратов или составов для использования; из-за непреднамеренной ошибки в этих процедурах; из-за различий в производстве, источнике или чистоте исходных материалов или ингредиентов, используемых для реализации способов, и тому подобного. Термин «около» также охватывает количества, которые различаются из-за старения состава с конкретной начальной концентрацией или смесью, и количества, которые различаются из-за смешивания или обработки состава с конкретной начальной концентрацией или смесью. При модификации термином «около» прилагаемая формула изобретения включает эквиваленты этих количеств.
Используемый в данном документе термин «применение» или «введение» относится к осуществлению инъекции или иной физической доставки вещества в том виде, в каком оно существует вне тела (например, антитела к hPCSK9, представленного в данном документе), у пациента, например, через слизистую оболочку, с помощью внутрикожной, внутривенной, внутримышечной доставки и/или любого другого способа физической доставки, описанного в данном документе или известного в данной области техники. Когда лечат заболевание или его симптом, введение вещества обычно происходит после начала заболевания или его симптомов. Когда предотвращают заболевание или его симптомы, введение вещества обычно происходит до начала заболевания или его симптомов.
Термин «антитело», «иммуноглобулин» или «Ig» можно использовать в данном документе взаимозаменяемо, и он означает молекулу иммуноглобулина, которая распознает и специфически связывается с мишенью, такой как белок, полипептид, пептид, углевод, полинуклеотид, липид или их комбинации, по меньшей мере через один сайт распознавания антигена в вариабельной области молекулы иммуноглобулина. При использовании в данном документе, термин «антитело» включает интактные поликлональные антитела, интактные моноклональные антитела, фрагменты антител (такие как фрагменты Fab, Fab', F(ab')2 и Fv), одноцепочечные мутанты Fv (scFv), мультиспецифические антитела, такие как биспецифические антитела (включая антитела с двойным связыванием), химерные антитела, гуманизированные антитела, человеческие антитела, слитые белки, содержащие часть антитела, определяющую антиген, и любую другую модифицированную молекулу иммуноглобулина, содержащую сайт распознавания антигена, при условии, что антитела проявляют желаемую биологическую активность. Термин «антитело» может также относиться к Y-образному гликопротеину с молекулярной массой приблизительно 150 кДа, который состоит из четырех полипептидных цепей: двух легких (L) цепей и двух тяжелых (Н) цепей. Существует пять изотипов тяжелой цепи lg млекопитающих, обозначаемых греческими буквами альфа (α), дельта (δ), эпсилон (ε), гамма (γ) и мю (μ). Тип тяжелой цепи определяет класс антитела, т.е. IgA, IgD, IgE, IgG и IgM, соответственно. Классы у и а далее делятся на подклассы на основе различий в последовательности и функции константного домена, например, IgG1, hIgG2, mIgG2A, mIgG2B, IgG3, IgG4, IgA1 и IgA2. У млекопитающих существует два типа легких цепей иммуноглобулина, А и к. «Вариабельная область» или «вариабельный домен» антитела относится к аминоконцевым доменам тяжелой или легкой цепи антитела. Вариабельные домены тяжелой цепи и легкой цепи можно обозначать как «VH» и «VL», соответственно. Эти домены обычно являются наиболее вариабельными частями антитела (по сравнению с другими антителами того же класса) и содержат сайты связывания антигена. Примером антител являются антитела, состоящие только из тяжелых цепей (т.е. Н2), которые содержат димер тяжелой цепи (5'-\/Н-(необязательный шарнир)-СН2-СН3-3') и лишены легкой цепи.
Описанные в данном документе антитела могут быть олигоклональными, поликлональными, моноклональными (включая моноклональные антитела полной длины), верблюжьими, химерными, CDR-привитыми, мультиспецифическими, биспецифическими (включая антитела с двойным связыванием), каталитическими, химерными, гуманизированными, полностью человеческими, антиидиотипическими, включая антитела, которые могут быть помечены в растворимой или связанной форме, а также их фрагменты, варианты или производные, отдельно или в комбинации с другими аминокислотными последовательностями, полученными известными методами. Антитело может происходить от любого вида. Описанные в данном документе антитела могут быть неконъюгированными или конъюгированными с другими молекулами, такими как токсины, радиоизотопы и т.д.
Термины «антигенсвязывающий сайт», «антигенсвязывающий домен», «антигенсвязывающая область», «антигенсвязывающий фрагмент» и аналогичные термины относятся к той части антитела, которая содержит аминокислотные остатки, которые взаимодействуют с антигеном и придают связывающему агенту его специфичность и аффинность к антигену (например, области, определяющие комплементарность (CDR)). Область связывания антигена может происходить от любого вида животных, таких как грызуны (например, кролик, крыса или хомяк) и люди. Предпочтительно, чтобы область связывания антигена была человеческого происхождения.
Описанные в данном документе антигенсвязывающие фрагменты могут включать одноцепочечные Fv (scFv), одноцепочечные антитела, однодоменные антитела, доменные антитела, фрагменты Fv, фрагменты Fab, фрагменты F(ab'), фрагменты F(ab')2, фрагменты антител, которые проявляют желаемую биологическую активность, стабилизированную дисульфидом вариабельную область (dsFv), димерную вариабельную область (диатело), антиидиотипические (анти-Id) антитела (включая, например, анти-Id антитела к антителам), интратела, линейные антитела, одноцепочечные молекулы антител и мультиспецифические антитела, образованные из фрагментов антител и эпитоп-связывающих фрагментов любого из вышеперечисленного. В частности, описанные в данном документе антитела и фрагменты антител могут включать молекулы иммуноглобулинов и иммунологически активные фрагменты молекул иммуноглобулинов, т.е. молекулы, которые содержат антигенсвязывающий сайт. Расщепление антител ферментом папаином приводит к образованию двух идентичных антигенсвязывающих фрагментов, известных также как «Fab»-фрагменты, и «Fcs-фрагмента, не обладающего антигенсвязывающей активностью, но способного кристаллизоваться. «Fab» в контексте настоящего описания относится к фрагменту антитела, который включает один константный и один вариабельный домен каждой из тяжелой и легкой цепей. Термин «область Fc» в данном документе используется для определения С-концевой области тяжелой цепи иммуноглобулина, включая области Fc с нативной последовательностью и варианты областей Fc. «Фрагмент Fc» относится к карбоксиконцевым частям обеих Н-цепей, удерживаемых вместе дисульфидами. Эффекторные функции антител определяются последовательностями в области Fc, области, которая также распознается рецепторами Fc (FcR), находящимися на определенных типах клеток. Расщепление антител ферментом пепсином приводит к образованию фрагмента F(ab')2, в котором два плеча молекулы антитела остаются связанными и содержат два антигенсвязывающих сайта. Фрагмент F(ab')2 обладает способностью сшивать антиген.
Термин «полученный в результате рекомбинации» в отношении генных сегментов будет очевиден для специалиста в данной области техники, который поймет, что В-клетки рекомбинируют свои генные сегменты вариабельной области для получения кодирующей последовательности для вариабельных доменов. Например, «полученный в результате рекомбинации сегмента гена VH, сегмента гена DH и сегмента гена JH человека» относится к рекомбинации одного сегмента гена VH с одним сегментом гена DH и одним сегментом гена JH человека с образованием перегруппированной последовательности VDJ, которая кодирует вариабельный домен тяжелой цепи антитела. Соединительная и соматическая гипермутация также могут быть особенностями процесса, в результате чего результирующая рекомбинированная последовательность VDJ включает одно или несколько добавлений, замен или делеций нуклеотидов (например, р-добавления и/или n-добавления), которые не входят в последовательности зародышевого типа V, D и J. Эквивалент будет называться генными сегментами Vк и Jк для вариабельного домена легкой цепи каппа и Vλ и Jλ для вариабельного домена легкой цепи лямбда. Предполагается, что в вариабельные домены могут быть дополнительно включены любые посттрансляционные модификации.
«Fv», при использовании в данном документе, относится к минимальному фрагменту антитела, который сохраняет как сайты распознавания антигена, так и сайты связывания антигена. Эта область состоит из димера вариабельного домена одной тяжелой и одной легкой цепи в жестком, нековалентном или ковалентном соединении. Именно в такой конфигурации три CDR каждого вариабельного домена взаимодействуют для определения антигенсвязывающего сайта на поверхности димера VH-VL В совокупности шесть CDR придают антителу антигенсвязывающую специфичность. Однако даже один вариабельный домен (или половина Fv, содержащая только три CDR, специфичных к антигену) обладает способностью распознавать и связывать антиген, хотя и с более низким сродством, чем весь сайт связывания.
Термин «моноклональное антитело», при использовании в данном документе, относится к антителу, полученному из популяции по существу гомогенных антител, т.е. отдельные антитела, составляющие популяцию, идентичны, за исключением возможных встречающихся в природе мутаций и/или посттрансляционных модификаций (например, изомеризации, амидирования), которые могут присутствовать в незначительных количествах. Моноклональные антитела являются высокоспецифичными и направлеными против одной антигенной детерминанты или эпитопа. Напротив, препараты поликлональных антител обычно включают различные антитела, направленные против различных антигенных детерминант (или эпитопов). Термин «моноклональное антитело», при использовании в данном документе, охватывает как интактные, так и полноразмерные моноклональные антитела, а также фрагменты антител (такие как Fab, Fab', F(ab')2, Fv), одноцепочечные мутанты (scFv), слитые белки, содержащие часть антитела, и любую другую модифицированную молекулу иммуноглобулина, содержащую сайт распознавания антигена. Кроме того, «моноклональное антитело» относится к таким антителам, полученным любым количеством способов, включая, но не ограничиваясь ими, гибридому, фаговую селекцию, рекомбинантную экспрессию и трансгенных животных. Моноклональные антитела в данном документе могут включать «химерные» антитела (иммуноглобулины), в которых часть тяжелой и/или легкой цепи идентична или гомологична соответствующим последовательностям в антителах, происходящих от определенного вида или принадлежащих к конкретному классу или подклассу антител, в то время как остальная часть цепи (цепей) идентична(-ы) или гомологична(-ы) соответствующим последовательностям в антителах, происходящих от другого вида или принадлежащих к другому классу или подклассу антител, а также фрагменты таких антител, которые проявляют желаемую биологическую активность.
Термин «гуманизированное антитело» относится к подгруппе химерных антител, в которых «гипервариабельная область» иммуноглобулина нечеловеческого происхождения (донорское антитело) заменяет остатки гипервариабельной области человеческого иммуноглобулина (реципиентного антитела). В общем, гуманизированное антитело будет включать практически все из по меньшей мере одного, а обычно двух вариабельных доменов, в которых все или практически все гипервариабельные петли соответствуют таковым с последовательностью иммуноглобулина нечеловеческого происхождения, и все или практически все из каркасных областей представляют собой области с последовательностью человеческого иммуноглобулина, хотя каркасные области могут включать одну или более замен, которые улучшают характеристики антитела, такие как аффинность связывания, изомеризация, иммуногенность и т.д.
Термин «биспецифическое антитело» означает антитело, которое обладает специфичностью к двум целевым молекулам и включает, помимо прочего, такие форматы, как DVD-Ig (см. DiGiammarino et al., "Design and generation of DVD-Ig™ molecules for dual-specific targeting", Meth. Mo. Biol., 2012, 889, 145-156), mAb2 (см. WO2008/003103, описание формата mAb2 включено в данный документ посредством ссылки), FIT-lg (см. WO 2015/103072, описание остова FIT-Ig включено в данный документ посредством ссылки), mAb-dAb, «dock and lock», обмен Fab-фрагментами, SEED-тело, трифункциональное антитело Triomab, LUZ-Y, Fcab, кλ-тело, ортогональный Fab, зс-диатело-Fc, диатело-Fc, тандемный scFv-Fc, Fab-scFv-Fc, Fab-scFv, интратело, BiTE, диатело, DART, тандемное диатело, sc-диатело, sc-диатело-СН3, диатело-СН3, триатело, миниантитело, минитело, минитело TriBi, scFv-CH3 KIH, scFv-CH-CL-scFv, F(ab')2-scFv, scFv-KIH, Fab-scFv-Fc, четырехвалентный HCab, ImmTAC, выступы-во-впадины, выступы-во-впадины с общей легкой цепью, выступы-во-впадины с общей легкой цепью и заряженными парами, заряженные пары, заряженные пары с общей легкой цепью, DT-IgG, DutaMab, IgG(H)-scFv, scFv-(H)IgG, IgG(L)-scFv, scFv-(L)IgG, IgG(L,H)-Fv, IgG(H)-V, V(H)-IgG, IgG(L)-V, V (L)-IgG, KIH IgG-scFab, 2scFv-IgG, IgG-2scFv, scFv4-lg и Zybody. Обзор биспецифических форматов см. в Spiess, С, et al., Mol. Immunol. (2015). В другом варианте осуществления изобретения биспецифическая молекула включает антитело, которое слито с другим форматом, отличным от lg, например, с доменом связывания рецептора Т-клетки; доменом суперсемейства иммуноглобулинов; вариабельным рецептором лимфоцитов агнатана; доменом фибронектина (например, Adnectin™); константным доменом антитела (например, домен СН3, например, СН2 и/или СН3 Fcab™), причем константный домен не является функциональным доменом СН1; scFv; (scFv)2; sc-диателом; scFab; центирином и эпитоп-связывающим доменом, происходящим из остова, выбранного из CTLA-4 (Evibody™); доменом липокалина; белком А, таким KaKZ-домен белка А (например, Affibody™ или SpA); А-доменом (например, Avimer™ или Maxibody™); белком теплового шока (таким как эпитоп-связывающий домен, полученный из GroE1 и GroES); доменом трансферрина (например, транс-тело); белком с анкириновым повтором (например, DARPin™); пептидным аптамером; лектиновым доменом С-типа (например, Tetranectin™); γ-кристаллином человека или убиквитином человека (аффилин); доменом PDZ; токсином скорпиона; и доменом типа Кунитца ингибитора протеазы человека. См., например, в US 5731568 и WO 98/50431 (обе включены в данный документ посредством ссылки) неограничивающие примеры технологии «выступ-во-впадину».
Принцип состоит в конструировании парных доменов СН3 гетеродимерных тяжелых цепей так, чтобы один домен СН3 содержал «выступ», а другой домен СН3 содержал «впадину» в стерически противоположном положении. Выступы создаются путем замены небольшой боковой цепи аминокислоты на границе раздела между доменами СН3, в то время как впадины создаются путем замены больших боковых цепей на меньшие. Выступ предназначен для вставки во впадину, чтобы способствовать гетеродимеризации различных доменов СН3, дестабилизируя образование гомодимера. Таким образом, в смеси тяжелых и легких цепей антитела, которые собираются с образованием биспецифического антитела, увеличивается доля молекул IgG, имеющих парные гетеродимерные тяжелые цепи, что увеличивает выход и степень извлечения активной молекулы.
Для образования «выступов» в домене СН3 IgG могут быть включены мутации Y349C и/или T366W. Для образования «впадин» в домене СН3 IgG могут быть включены мутации Е356С, T366S, L368A и/или Y407V. Выступы и впадины могут быть введены в любой домен СН3 IgG человека, например домен СН3 IgG1, IgG2, IgG3 или IgG4. Предпочтительным примером является IgG4. Как уже отмечалось, IgG4 может включать дополнительные модификации, такие как мутации «Р» и/или «Е». Последовательность IgG4 типа а («ra») содержит замены Y349C и T366W («выступы»), а последовательность IgG4 типа b («yb») содержит замены Е356С, T366S, L368A и Y407V («впадины»). Как ra, так и yb также содержат замену «Р» в положении 228 в шарнирной области (S228P) для стабилизации шарнирной области тяжелой цепи. Как ra, так и yb также содержат замену «Е» в области СН2 в положении 235 (L235S) для устранения связывания с FcγR. Таким образом, релевантной последовательностью тяжелой цепи IgG4-РЕ является ppcpPcpapefEggps.
Дальнейшим прогрессом в биспецифической инженерии IgG стала идея использования общей легкой цепи, как описано в WO 98/50431. Были описаны биспецифические антитела, содержащие две пары тяжелой-легкой цепи, в которых вариабельные легкие цепи обеих пар тяжелой-легкой цепи имели общую последовательность. В WO 98/50431 описано комбинирование подхода общей легкой цепи со специфическими комплементарными взаимодействиями на границе гетеродимеризации тяжелой цепи (такими как выступы во впадины), чтобы способствовать образованию гетеродимера и препятствовать образованию гомодимера. В комбинации эти подходы усиливают образование требуемого гетеродимера по сравнению с нежелательными гетеродимерами и гомодимерами.
В то время как технология «выступы-во-впадины» включает в себя конструирование боковых цепей аминокислот для создания комплементарных молекулярных форм на границе спаренных доменов СН3 в биспецифическом гетеродимере, другой способ стимулировать образование гетеродимера и препятствовать образованию гомодимера состоит в том, чтобы сконструировать боковые цепи аминокислот таким образом, чтобы они имели противоположные заряды. Ассоциации доменов СН3 в гетеродимерах тяжелой цепи способствует спаривание противоположно заряженных остатков, в то время как парные положительные заряды или парные отрицательные заряды могут сделать образование гомодимера менее энергетически выгодным. В WO 2006/106905 описан способ получения гетеромультимера, состоящего из более чем одного типа полипептида (такого как гетеродимер двух разных тяжелых цепей антитела), включающий замену в аминокислотном остатке, образующем поверхность раздела между указанными полипептидами, так что гетеромультимерная ассоциация будет регулироваться, причем способ включает:
(a) модификацию нуклеиновой кислоты, кодирующей аминокислотный остаток, образующий поверхность раздела между полипептидами из исходной нуклеиновой кислоты, так что ассоциация между полипептидами, образующими один или более мультимеров, будет ингибироваться в гетеромультимере, который может образовывать два или более типов мультимеров;
(b) культивирование клеток-хозяев таким образом, чтобы экспрессировалась последовательность нуклеиновой кислоты, модифицированная на стадии (а); и
(c) выделение указанного гетеромультимера из культуры клеток-хозяев, причем модификация стадии (а) представляет собой модификацию исходной нуклеиновой кислоты так, чтобы один или более аминокислотных остатков были заменены на границе раздела, так что два или более аминокислотных остатка, включая мутантный остаток(-и), образующие границу раздела, будут нести тот же тип положительного или отрицательного заряда.
Примером этого является подавление ассоциации между тяжелыми цепями путем введения электростатического отталкивания на границе раздела гомодимеров тяжелой цепи, например, путем модификации аминокислотных остатков, которые контактируют друг с другом на границе раздела доменов СН3, в том числе:
положения 356 и 439
положения 357 и 370
положения 399 и 409,
нумерация остатков соответствует системе нумерации EU.
За счет модификации одной или более из этих пар остатков так, чтобы они имели одинаковые заряды (как положительные, так и отрицательные) в домене СН3 первой тяжелой цепи, спаривание гомодимеров тяжелой цепи ингибируется электростатическим отталкиванием. За счет конструирования одних и тех же пар или пар остатков в домене СН3 второй (другой) тяжелой цепи так, чтобы они имели противоположный заряд по сравнению с соответствующими остатками в первой тяжелой цепи, гетеродимерное спаривание первой и второй тяжелых цепей стимулируется электростатическим притяжением.
Аминокислоты на границе СН3 константной области тяжелой цепи были модифицированы для введения пар зарядов, мутации перечислены в Таблице 1 WO 2006/106905. Сообщалось, что изменение аминокислот в положениях тяжелой цепи 356, 357, 370, 399, 409 и 439 для введения индуцированного зарядом молекулярного отталкивания на границе раздела СН3 приводило к повышению эффективности образования предполагаемого биспецифического антитела. Например, одна константная область тяжелой цепи может представлять собой константную область IgG4, содержащую мутацию К439Е (положительно заряженный Lys заменен отрицательно заряженным Glu), а другая константная область тяжелой цепи может представлять собой константную область IgG4, содержащую мутацию E356K (отрицательно заряженный Glu заменен положительно заряженным Lys), на основе нумерации EU. «Спаривание зарядов» является результатом пространственной близости остатков 439 и 356 в Fc-области, собранной в результате гетеродимеризации этих двух константных областей.
Если используются две различные константные области тяжелой цепи, они могут быть связаны с двумя различными доменами VH антитела в любой ориентации.
В WO 2006/106905 также приведены примеры биспецифических антител IgG, в которых домены СН3 IgG4 были сконструированы с мутациями типа «выступы-во-впадины». Тип a (IgG4γa) представлял собой IgG4, замещенный по Y349C и T366W, а тип b (IgG4γb) представлял собой IgG4, замещенный по Е356С, T366S, L368A и Y407V.
В другом примере введение пар зарядов в домены VH и VL антитела использовали для ингибирования образования «неправильных» пар VH-VL (спаривание VH одного антитела с VL другого антитела). В одном примере остатки Q в VH и VL были изменены на K или R (положительные) или на Е или D (отрицательные), чтобы ингибировать водородную связь между боковыми цепями Q и ввести электростатическое отталкивание.
Дополнительные примеры заряженных пар были раскрыты в WO 2013/157954, в котором описан способ получения гетеродимерной молекулы, содержащей домен СН3, из одной клетки, причем молекула содержит два домена СН3, способных образовывать границу раздела. Способ включал введение в клетку
(a) первой молекулы нуклеиновой кислоты, кодирующей первую полипептидную цепь, содержащую домен СН3, причем эта цепь содержит остаток K в положении 366 в соответствии с системой нумерации EU, и
(b) второй молекулы нуклеиновой кислоты, кодирующей вторую полипептидную цепь, содержащую домен СН3, причем эта цепь содержит остаток D в положении 351 в соответствии с системой нумерации EU,
способ дополнительно включает стадию культивирования клетки-хозяина, обеспечивающую экспрессию двух молекул нуклеиновых кислот и сбор гетеродимерной молекулы, содержащей домен СН3, из культуры.
Дополнительные способы конструирования электростатических взаимодействий в полипептидных цепях для ускорения образования гетеродимера по сравнению с образованием гомодимера описаны в WO 2011/143545.
Другой пример конструирования на границе раздела СН3-СН3 представляет собой гетеродимеры домена СН3, сконструированного путем обмена между цепями (SEED). Домены СН3 состоят из чередующихся сегментов последовательностей СН3 IgA и IgG человека, которые образуют пары комплементарных гетеродимеров SEED, называемых «SEED-телами» [WO 2007/110205].
Также были получены биспецифические антитела с гетеродимеризованными тяжелыми цепями, которые дифференцированно модифицированы в домене СН3 для изменения их аффинности связывания с реагентом очистки, таким как белок А. В WO 2010/151792 описан гетеродимерный биспецифический антигенсвязывающий белок, содержащий первый полипептид, содержащий от N-конца к С-концу первую эпитоп-связывающую область, которая избирательно связывает первый эпитоп, константную область иммуноглобулина, которая содержит первую область СН3 IgG человека, выбранную из IgG1, IgG2 и IgG4; и второй полипептид, содержащий от N-конца к С-концу вторую эпитоп-связывающую область, которая избирательно связывает второй эпитоп, константную область иммуноглобулина, которая содержит вторую область СН3 IgG человека, выбранную из IgG1, IgG2 и IgG4, причем вторая область СН3 содержит модификацию, которая снижает или устраняет связывание второго домена СН3 с белком А.
Таким образом, область Fc может содержать одну или более мутаций, способствующих дифференциальной очистке активного гетеродимера от гомодимерных молекул. СН3 одной константной области тяжелой цепи может содержать мутации His435Arg и/или Tyr436Phe (нумерация EU) [], тогда как СН3 другой константной области тяжелой цепи не содержит указанных мутаций. Эмицизумаб, например, содержит область Fc, в которой один СН3 содержит His435, а другой СН3 содержит His435Arg.
В биспецифических молекулах по данному изобретению могут использоваться любые из этих биспецифических методов и молекулярных форматов по желанию.
В одном варианте осуществления изобретения биспецифическое антитело представляет собой mAb2. mAb2 содержит домен VH и VL интактного антитела, слитый с модифицированной константной областью, которая была сконструирована для образования антигенсвязывающего сайта, известного как «Fcab». Технология, лежащая в основе формата Fcab/mAb2, описана более подробно в WO 2008/003103, и описание формата mAb2 включено в данный документ посредством ссылки.
В другом варианте осуществления изобретения биспецифическое антитело представляет собой «антитело с двойным связыванием». При использовании в данном документе, термин «антитело с двойным связыванием» означает биспецифическое антитело, в котором оба антигенсвязывающих домена образованы парой VH/VL, и включает FIT-Ig (см. WO 2015/103072, включенный в данный документ посредством ссылки), mAb-dAb, «dock and lock», обмен Fab-фрагментами, SEED-тело, трифункциональное антитело Triomab, LUZ-Y, Fcab, кλ-тело, ортогональный Fab, зс-диатело-Fc, диатело-Fc, тандемный scFv-Fc, Fab-scFv-Fc, Fab-scFv, интратело, BiTE, диатело, DART, тандемное диатело, sc-диатело, sc-диатело-СН3, диатело-СН3, триатело, миниантитело, минитело, scFv-СН3 KIH, scFv-CH-CL-scFv, F(ab')2-scFv, scFv-KIH, Fab-scFv-Fc, четырехвалентный HCab, ImmTAC, выступы-во-впадины, выступы-во-впадины с общей легкой цепью, выступы-во-впадины с общей легкой цепью и заряженными парами, заряженные пары, заряженные пары с общей легкой цепью, DT-IgG, DutaMab, IgG(H)-scFv, scFv-(H)IgG, IgG(L)-scFv, scFv-(L)IgG, IgG(L,H)-Fv, IgG(H)-V, V(H)-IgG, IgG(L)-V, V (L)-IgG, KIH IgG-scFab, 2scFv-IgG, IgG-2scFv и scFv4-Ig.
Термин «гипервариабельная область», «область CDR» или «CDR» относится к областям вариабельного домена антитела, которые являются гипервариабельными по последовательности и/или образуют структурно определенные петли. В общем, антигенсвязывающие сайты антитела включают шесть гипервариабельных областей: три в VH (CDRH1, CDRH2, CDRH3) и три в VL (CDRL1, CDRL2, CDRL3). Эти области тяжелой и легкой цепей антитела придают антителу антигенсвязывающую специфичность. CDR могут быть определены в соответствии с системой Кабата (см. Kabat, Е.A. et al., 1991, "Sequences of Proteins of Immunological Interest", 5th edit., NIH Publication no. 91-3242, U.S. Department of Health and Human Services). Для определения CDR можно использовать другие системы, такие как система, разработанная Chothia et al. (см. Chothia, С. & Lesk, А.М., 1987, "Canonical structures for the hypervariable regions of immunoglobulins", J. Mol. Biol., 196, 901-917) и система IMGT (см. Lefranc, M.P., 1997, "Unique database numbering system for immunogenetic analysis", Immunol. Today, 18, 50). Антитело обычно содержит 3 CDR тяжелой цепи и 3 CDR легкой цепи. Термин CDR или несколько CDR используется в данном документе для обозначения одной или нескольких из этих областей. Специалист в данной области может легко сравнить различные системы номенклатуры и определить, может ли конкретная последовательность быть определена как CDR.
«Человеческое антитело» представляет собой антитело, которое обладает аминокислотной последовательностью, соответствующей аминокислотной последовательности антитела, продуцируемого человеком, и/или было получено с использованием любого из методов получения человеческих антител и, в частности, исключает гуманизированное антитело, содержащее антигенсвязывающие остатки нечеловеческого происхождения. Термин «специфически связывается с» относится к измеримым и воспроизводимым взаимодействиям, таким как связывание между мишенью и антителом, которое является определяющим для присутствия мишени в присутствии гетерогенной популяции молекул, включая биологические молекулы. Например, антитело, которое специфически связывается с мишенью (которая может представлять собой эпитоп), представляет собой антитело, которое связывает эту мишень с большей аффинностью, авидностью, более легко и/или с большей продолжительностью, чем оно связывается с другими мишенями. В одном варианте осуществления изобретения степень связывания антитела с неродственной мишенью составляет менее около 10% связывания антитела с мишенью, что измерено, например, с помощью радиоиммуноанализа (RIA).
Антитело или его фрагмент, которые специфически связываются с антигеном hPCSK9, могут иметь перекрестную реакцию с родственными антигенами.
Предпочтительно антитело или его фрагмент, которые специфически связываются с антигеном hPCSK9, не реагируют перекрестно с другими антигенами (но могут необязательно перекрестно реагировать с PCSK9 другого вида, например макака-резуса или мыши). Антитело или его фрагмент, которые специфически связываются с антигеном hPCSK9, можно идентифицировать, например, с помощью иммуноанализов, BIAcore™ или других методов, известных специалистам в данной области техники. Антитело или его фрагмент специфически связывается с антигеном PCSK9, когда оно связывается с антигеном hPCSK9 с более высокой аффинностью, чем с любым перекрестно-реагирующим антигеном, как определено с помощью экспериментальных методов, таких как радиоиммуноанализы (RIA) и иммуноферментные анализы (ELISA). Как правило, специфическая или селективная реакция будет давать сигнал по меньшей мере вдвое больший, чем фоновый сигнал или шум и, как правило, более чем в 10 раз больший (например, более чем в 15 раз, более чем в 20 раз, более чем в 50 раз или более чем в 100 раз), чем фон. Обсуждение специфичности антител см., например, в Paul, ed., 1989, Fundamental Immunology Second Edition, Raven Press, New York, на страницах 332-336.
Термин «алифатическая аминокислота» означает, что группы R аминокислоты являются неполярными и гидрофобными. Гидрофобность увеличивается с увеличением числа атомов С в углеводородной цепи. Глицин, аланин, валин, лейцин и изолейцин являются алифатическими аминокислотами.
Термин «ароматическая аминокислота» означает, что группы R аминокислоты содержат ароматическую кольцевую систему. Фенилаланин, тирозин и триптофан являются ароматическими аминокислотами.
Термин «гидроксилсодержащая аминокислота» означает, что группы R аминокислоты содержат гидроксильную группу и являются гидрофильными. Серии, цистеин, треонин и метионин являются гидроксилсодержащими аминокислотами.
Термин «основная аминокислота» означает, что группы R аминокислоты являются азотсодержащими и являются основными при нейтральном рН. Гистидин, лизин и аргинин являются основными аминокислотами.
Термин «циклическая аминокислота» означает, что группы R аминокислоты имеют алифатическую циклическую структуру. Пролин является единственной циклической алифатической аминокислотой.
Термин «кислая аминокислота» означает, что группы R аминокислоты являются полярными и имеют отрицательный заряд при физиологическом рН. Аспартат и глутамат являются кислыми аминокислотами.
Термин «амидная аминокислота» означает, что группы R аминокислоты содержат амидную группу. Аспарагин и глутамин являются амидными аминокислотами.
При использовании в данном документе, термин «номер разрешения» или «номер разрешения на продажу» относится к номеру, выданному регулирующим органом после того, как этот орган определит, что конкретный медицинский продукт и/или композиция может продаваться и/или предлагаться для продажи в регионе, подпадающем под действие юрисдикции этого органа. При использовании в данном документе, термин «регулирующий орган» относится к одному из агентств, ответственных за оценку, например, безопасности и эффективности медицинского продукта и/или композиции, а также за контроль продаж/маркетинга таких продуктов и/или композиций в данном регионе. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) в США и Европейское агентство по лекарственным средствам (ЕРА) в Европе являются лишь двумя примерами таких регулирующих органов. Другие неограничивающие примеры могут включать SDA, МРА, MHPRA, IMA, ANMAT, Департамент здравоохранения Гонконга - Управление по лекарственным препаратам, CDSCO, Medsafe и KFDA.
При использовании в данном документе, термин «буфер» относится к химическому агенту, который способен поглощать определенное количество кислоты или основания, не подвергаясь сильному изменению рН.
При использовании в данном документе, термин «носитель» относится к разбавителю, адъюванту (например, адъюванту Фрейнда (полному и неполному)), вспомогательному веществу или среде, с которыми вводят терапевтическое средство. Такие фармацевтические носители могут быть стерильными жидкостями, такими как вода и масла, включая масла нефтяного, животного, растительного или синтетического происхождения, такие как арахисовое масло, соевое масло, минеральное масло, кунжутное масло и т.п. Вода является предпочтительным носителем при внутривенном введении фармацевтической композиции. Солевые растворы и водные растворы декстрозы и глицерина также можно использовать в качестве жидких носителей, особенно для растворов для инъекций.
При использовании в данном документе, термин «композиция» предназначен для охвата продукта, содержащего указанные ингредиенты (например, антитело по изобретению), необязательно в определенных количествах, а также любой продукта, который прямо или косвенно является результатом комбинации указанных ингредиентов, необязательно, в указанных количествах.
При использовании в данном документе, термин «содержащий» или «содержит» используется в отношении антител, фрагментов, применений, композиций, способов и их соответствующих компонентов(-а), которые являются существенными для способа или композиции, но открыты для включения неуказанных элементов, существенных или нет.
Термин «состоящий из» относится к антителам, фрагментам, применениям, композициям, способам и их соответствующим компонентам, как описано в данном документе, при этом исключен любой элемент, не указанный в этом описании варианта осуществления.
При использовании в данном документе, термин «состоящий по существу из» относится к тем элементам, которые необходимы для данного варианта осуществления. Этот термин допускает наличие элементов, которые существенно не влияют на основные и новые или функциональные характеристики (-у) этого варианта осуществления.
В контексте полипептида термин «производное», при использовании в данном документе, включает полипептид, который содержит аминокислотную последовательность полипептида hPCSK9, фрагмента полипептида hPCSK9 или антитело или фрагмент, которые специфически связываются с полипептидом hPCSK9, который был изменен введением замен, делеций или добавлений аминокислотных остатков. Термин «производное», при использовании в данном документе, также включает полипептид hPCSK9, фрагмент полипептида hPCSK9 или антитело, которое специфически связывается с полипептидом hPCSK9, который был химически модифицирован, например, путем ковалентного присоединения молекулы любого типа к полипептиду. Например, но не в качестве ограничения, полипептид hPCSK9, фрагмент полипептида hPCSK9 или антитело к hPCSK9 можно химически модифицировать, например, путем гликозилирования, ацетилирования, пегилирования, фосфорилирования, амидирования, дериватизации известными защитными/блокирующими группами, протеолитического расщепления, связывания с клеточным лигандом или другим белком и т.д. Производные модифицируют так, что они отличается от встречающихся в природе или исходных пептидов или полипептидов либо по типу, либо по расположению присоединенных молекул. Производные дополнительно включают делецию одной или более химических групп, которые обычно присутствуют в пептиде или полипептиде. Производное полипептида hPCSK9, фрагмента полипептида hPCSK9 или антитела к hPCSK9 можно химически модифицировать химическими модификациями с использованием методов, известных специалистам в данной области, включая, но не ограничиваясь ими, специфическое химическое расщепление, ацетилирование, формилирование, метаболический синтез туникамицина и т.д. Кроме того, производное полипептида hPCSK., фрагмент полипептида hPCSK9 или антитело к hPCSK9 может содержать одну или более неклассических аминокислот. Производное полипептида обладает функцией, аналогичной или идентичной полипептиду hPCSK9, фрагменту полипептида hPCSK9 или антитела к hPCSK9, описанного в данном документе.
Термин «эффекторная функция» (или «активированный эффектором»), при использовании в данном документе, относится к одному или более ответам, опосредованным антителозависимой клеточно-опосредованной цитотоксической активностью (ADCC), комплемент-зависимой цитотоксической активностью (CDC), опосредованному Fc фагоцитозу или антителозависимому клеточному фагоцитозу (ADCP) и рециклингу антител посредством рецептора FcRn.
«Эффективное количество» относится к количеству, эффективному в дозировках и в течение необходимых периодов времени, для достижения желаемого эффекта, включая терапевтический или профилактический результат.«Терапевтически эффективное количество» относится к минимальной концентрации, необходимой для достижения измеримого улучшения или профилактики конкретного расстройства. Терапевтически эффективное количество в данном изобретении может варьироваться в зависимости от таких факторов, как состояние болезни, возраст, пол и масса пациента, а также способность антитела вызывать желаемый ответ у индивида. Терапевтически эффективное количество также представляет собой такое количество, при котором токсические или вредные эффекты антитела перевешиваются терапевтически полезными эффектами. «Профилактически эффективное количество» относится к количеству, эффективному при дозировках и в течение необходимых периодов времени для достижения желаемого профилактического результата. В некоторых вариантах осуществления изобретения эффективное количество антитела по изобретению составляет от около 0,1 мг/кг (мг антитела на кг массы субъекта) до около 100 мг/кг. В некоторых вариантах осуществления изобретения эффективное количество предоставляемого антитела составляет около 0,1 мг/кг, около 0,5 мг/кг, около 1 мг/кг, 3 мг/кг, 5 мг/кг, около 10 мг/кг, около 15 мг/кг, около 20 мг/кг, около 25 мг/кг, около 30 мг/кг, около 35 мг/кг, около 40 мг/кг, около 45 мг/кг, около 50 мг/кг, около 60 мг/кг, около 70 мг/кг, около 80 мг/кг, около 90 мг/кг или около 100 мг/кг (или диапазон между ними). В некоторых вариантах осуществления изобретения термин «эффективное количество», при использовании в данном документе, также относится к количеству антитела по изобретению для достижения определенного результата (например, ингибирования биологической активности hPCSK9 клетки).
При использовании в данном документе, термин «эпитоп» относится к локализованной области на поверхности антигена, такой как полипептид hPCSK9 или фрагмент полипептида hPCSK9, которая способна связываться с одной или более антигенсвязывающими областями антитела и которая имеет антигенную или иммуногенную активность у животного, предпочтительно у млекопитающего и наиболее предпочтительно у человека, которая способна вызывать иммунный ответ. Эпитоп, обладающий иммуногенной активностью, представляет собой часть полипептида, которая вызывает у животного ответ виде антител. Эпитоп, обладающий антигенной активностью, представляет собой часть полипептида, с которой специфически связывается антитело, как определено любым методом, хорошо известным в данной области, например, с помощью описанных в данном документе иммуноанализов. Эпитопы антигенов не обязательно должны быть иммуногенными. Эпитопы обычно состоят из химически активных поверхностных групп молекул, таких как аминокислоты или боковые цепи Сахаров, и обладают определенными трехмерными структурными характеристиками, а также определенными характеристиками заряда. Участок полипептида, вносящий вклад в эпитоп, может представлять собой непрерывные аминокислоты полипептида, или эпитоп может образовываться из двух или более не непрерывных участков полипептида. Эпитоп может быть или не быть трехмерным поверхностным элементом антигена. В некоторых вариантах осуществления изобретения эпитоп hPCSK9 представляет собой трехмерный поверхностный элемент полипептида hPCSK9 (например, в тримерной форме полипептида hPCSK9). В других вариантах осуществления изобретения эпитоп hPCSK9 является линейным элементом полипептида hPCSK9 (например, в тримерной форме или мономерной форме полипептида hPCSK9). Представленные в данном документе антитела могут специфически связываться с эпитопом мономерной (денатурированной) формы hPCSK9, эпитопом тримерной (нативной) формы hPCSK9 или как мономерной (денатурированной) формы, так и тримерной (нативной) формы hPCSK9. В конкретных вариантах осуществления изобретения антитела, представленные в данном документе, специфически связываются с эпитопом тримерной формы hPCSK9, но не связываются специфически с мономерной формой hPCSK9.
Термин «вспомогательные вещества», при использовании в данном документе, относится к инертным веществам, которые обычно используются в качестве разбавителя, носителя, консервантов, связующих веществ или стабилизирующего агента для лекарственных средств, и включает, но не ограничиваясь ими, белки (например, сывороточный альбумин и т.д.), аминокислоты (например, аспарагиновая кислота, глутаминовая кислота, лизин, аргинин, глицин, гистидин и т.д.), жирные кислоты и фосфолипиды (например, алкилсульфонаты, каприлат и т.д.), поверхностно-активные вещества (например, ДСН, полисорбат, неионогенное поверхностно-активное вещество и т.д.), сахариды (например, сахароза, мальтоза, трегалоза и т.д.) и полиолы (например, маннит, сорбит и т.д.). См. также Remington's Pharmaceutical Sciences (1990) Mack Publishing Co., Easton, Pa., которая включена в данный документ в полном объеме посредством ссылки.
При использовании в данном документе, термин «номер разрешения» или «номер разрешения на продажу» относится к номеру, выданному регулирующим органом после того, как этот орган определит, что конкретный медицинский продукт и/или композиция может продаваться и/или предлагаться для продажи в регионе, подпадающем под действие юрисдикции этого органа. При использовании в данном документе, термин «регулирующий орган» относится к одному из агентств, ответственных за оценку, например, безопасности и эффективности медицинского продукта и/или композиции, а также за контроль продаж/маркетинга таких продуктов и/или композиций в данном регионе. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) в США и Европейское агентство по лекарственным средствам (ЕРА) в Европе являются лишь двумя примерами таких регулирующих органов. Другие неограничивающие примеры могут включать SDA, МРА, MHPRA, IMA, ANMAT, Департамент здравоохранения Гонконга - Управление по лекарственным препаратам, CDSCO, Medsafe и KFDA.
При использовании в данном документе, «инъекционное устройство» относится к устройству, которое предназначено для проведения инъекций, причем инъекция включает этапы временного гидравлического соединения инъекционного устройства с тканью человека, обычно с подкожной тканью. Инъекция дополнительно включает введение некоторого количества жидкого лекарственного средства в ткань и отсоединение или удаление инъекционного устройства от ткани. В некоторых вариантах осуществления изобретения инъекционное устройство может быть внутривенным или в/в устройством, которое представляет собой тип инъекционного устройства, используемого, когда целевой тканью является кровь в системе кровообращения, например кровь в вене. Распространенным, но не ограничивающим примером инъекционного устройства является игла и шприц.
При использовании в данном документе, термин «буфер» относится к химическому агенту, который способен поглощать определенное количество кислоты или основания, не подвергаясь сильному изменению рН.
При использовании в данном документе, «упаковка» относится к тому, как компоненты собраны и/или заключены в единичный элемент, пригодный для распространения и/или использования. Упаковка может включать, например, коробки, пакеты, шприцы, ампулы, флаконы, пробирки, двухстворчатую упаковку, барьеры и/или контейнеры для поддержания стерильности, маркировку и т.д.
При использовании в данном документе, «инструкции» относятся к отображению письменных, печатных или графических материалов на непосредственном контейнере изделия, например письменный материал, отображаемый на флаконе, содержащем фармацевтически активный агент, или подробности о составе и применении интересующего продукта, включенные в набор, содержащий интересующий состав. В инструкциях изложено предполагаемое применение или проведение способа лечения.
В контексте пептида или полипептида термин «фрагмент», при использовании в данном документе, относится к пептиду или полипептиду, который содержит неполную аминокислотную последовательность. Такой фрагмент может возникать, например, в результате усечения на амино-конце, усечения на карбокси-конце и/или внутренней делеции остатка(-ов) из аминокислотной последовательности. Фрагменты могут, например, возникать в результате альтернативного сплайсинга РНК или протеазной активности in vivo. В некоторых вариантах осуществления изобретения фрагменты PCSK9 включают полипептиды, содержащие аминокислотную последовательность из по меньшей мере 5 аминокислотных остатков подряд, по меньшей мере 10 аминокислотных остатков подряд, по меньшей мере 15 аминокислотных остатков подряд, по меньшей мере 20 аминокислотных остатков подряд, по меньшей мере 25 аминокислотных остатков подряд, по меньшей мере 40 аминокислотных остатков подряд, по меньшей мере 50 аминокислотных остатков подряд, по меньшей мере 60 аминокислотных остатков подряд, по меньшей мере 70 аминокислотных остатков подряд, по меньшей мере 80 аминокислотных остатков подряд, по меньшей мере 90 аминокислотных остатков подряд, по меньшей мере 100 аминокислотных остатков подряд, по меньшей мере 125 аминокислотных остатков подряд, по меньшей мере 150 аминокислотных остатков подряд, по меньшей мере 175 аминокислотных остатков подряд, по меньшей мере 200 аминокислотных остатков подряд или по меньшей мере 250 аминокислотных остатков подряд аминокислотной последовательности полипептида hPCSK9 или антитела, которое специфически связывается с полипептидом hPCSK9. В конкретном варианте осуществления изобретения фрагмент полипептида hPCSK9 или антитела, которое специфически связывается с антигеном hPCSK9, сохраняет по меньшей мере 1, по меньшей мере 2 или по меньшей мере 3 функции полипептида или антитела.
Термин «свободный» может относиться к полипептиду, например PCSK9 или его фрагментам и вариантам, который объединен с буфером, при этом полипептид не связан с клеточной поверхностью или клеточной мембраной. Таким образом, термин «свободный» может относиться к полипептиду, который способен к поверхностной экспрессии (т.е. включает один или более трансмембранных доменов или доменов мембранной ассоциации), но который в своем нынешнем состоянии не экспрессируется на поверхности клетки или не связан с белком, который экспрессируется на поверхности клетки. Свободный полипептид также может относиться к свободному рекомбинантному, нативному или несвязанному полипептиду. В контексте фагового дисплея свободный антиген может быть выбран в растворе (называемый в данном документе «отбором растворением») или адсорбирован на поверхности, например адсорбирован на поверхности 96-луночного планшета (называемый в данном документе «биопэннинг-отбор»).
Термин «слитый белок», при использовании в данном документе, относится к полипептиду, который включает аминокислотную последовательность антитела и аминокислотную последовательность гетерологичного полипептида или белка (т.е. полипептид или белок, обычно не являющийся частью антитела (например, не являющийся частью антитела к антигену PCSK9)). Термин «слияние», когда он используется по отношению к PCSK9 или к антителу к PCSK9, относится к объединению пептида или полипептида, или их фрагмента, варианта и/или производного, с гетерологичным пептидом или полипептидом. Слитый белок предпочтительно сохраняет биологическую активность PCSK9 или антитела к PCSK9. В некоторых вариантах осуществления изобретения слитый белок содержит домен VH, домен VL, CDR VH (одна, две или три CDR VH) и/или CDR VL (одна, две или три CDR VL) антитела к PCSK9, причем слитый белок специфически связывается с эпитопом PCSK9.
Термин «тяжелая цепь», когда он используется в отношении антитела, относится к пяти различным типам, называемым альфа (α), дельта (δ), эпсилон (ε), гамма (γ) и мю (μ) в зависимости от аминокислотной последовательности константного домена тяжелой цепи. Эти отдельные типы тяжелых цепей хорошо известны и дают начало пяти классам антител IgA, IgD, IgE, IgG и IgM, соответственно, включая четыре подкласса IgG, а именно IgG1, IgG2, IgG3 и IgG4. Предпочтительно тяжелая цепь представляет собой тяжелую цепь человека. В человеческой популяции существует множество аллелей константной области тяжелой цепи каждого иммуноглобулина или подкласса иммуноглобулинов. Нуклеотидные и аминокислотные последовательности этих аллельных вариантов доступны в общедоступных базах данных, таких как IMGT, ENSEMBL Swiss-Prot и Uniprot. Аллельные варианты также могут быть идентифицированы в различных проектах секвенирования генома. В одном варианте осуществления изобретения антитела и фрагменты антител, раскрытые в данном документе, содержат тяжелую цепь, кодируемую аллелем константной области IgG1, которая включает, но не ограничиваясь этим, IGHG1*01 (Seq ID №340, 341 и 537), IGHG1*02 (SEQ ID №340, 341 и 537), IGHG1*03 (SEQ ID №523 и 524), IGHG1*04 (SEQ ID №525 и 526) и IGHGT05 (SEQ ID №340, 341 и 537) человека. В одном варианте осуществления изобретения антитела и фрагменты антител, раскрытые в данном документе, содержат белок, кодируемый аллелем константной области IgG2, который включает, но не ограничиваясь этим, IGHG2*01 (Seq ID №527 и 528), IGHG2*02 (Seq ID №529 и 530), IGHG2*03 (SEQ ID №527 и 528), IGHG2*04 (SEQ ID №531 и 532), IGHG2*05 (SEQ ID №527 и 528) и IGHG2*06 (SEQ ID №533 и 534) человека. Водном варианте осуществления изобретения антитела или фрагменты антител, раскрытые в данном документе, содержат белок, кодируемый аллелем константной области IgG3, который включает, но не ограничиваясь этим, IGHG3*01, IGHG3*02, IGHG3*03, IGHG3*04, IGHG3*05, IGHG3*06, IGHG3*07, IGHG3*08, IGHG3*09, IGHG3*10, IGHG3*11, IGHG3*12, IGHG3*13, IGHG3*14, IGHG3*15, IGHG3*16, IGHG3*17, IGHG3*18 и IGHG3*19 человека. В одном варианте осуществления изобретения антитела или фрагменты антител, раскрытые в данном документе, содержат белок, кодируемый аллелем константной области IgG4, который включает, но не ограничиваясь этим, IGHG4*01 (см., например, таблицу последовательностей в данном документе), IGHG4*02 (см., например, таблицу последовательностей в данном документе), IGHG4*03 (см., например, таблицу последовательностей в данном документе) и IGHG4*04 (см., например, таблицу последовательностей в данном документе) человека. В другом примере тяжелая цепь представляет собой отключенный изотип IgG, например отключенный IgG4. В некоторых вариантах осуществления изобретения антитела по изобретению содержат константную область гамма-4 человека. В другом варианте осуществления изобретения константная область тяжелой цепи не связывает рецепторы Fc-γ и, например, содержит мутацию Leu235Glu. В другом варианте осуществления изобретения константная область тяжелой цепи содержит мутацию Ser228Pro для повышения стабильности. В другом варианте осуществления изобретения константная область тяжелой цепи представляет собой IgG4-PE (см., например, таблицу последовательностей в данном документе). В другом варианте осуществления изобретения антитела и фрагменты антител, раскрытые в данном документе, содержат константную область тяжелой цепи, кодируемую аллелем константной области IgG1 мыши, которая включает, но не ограничиваясь этим, IGHG1 *01 или IGHG1*02 мыши. В одном варианте осуществления изобретения антитела и фрагменты антител, раскрытые в данном документе, содержат константную область тяжелой цепи, кодируемую аллелем константной области IgG2 мыши, которая включает, но не ограничиваясь этим, IGHG2A*01, IGHG2A*02, IGHG2B*01, IGHG2B*02, IGHG2C*01, IGHG2C*02 или IGHG2C*03 мыши. В одном варианте осуществления изобретения антитела или фрагменты антител, раскрытые в данном документе, содержат белок, кодируемый аллелем константной области IgG3 мыши, который включает, но не ограничиваясь им, IGHG3*01 мыши.
Термин «хозяин», при использовании в данном документе, относится к животному, предпочтительно к млекопитающему и наиболее предпочтительно к человеку.
Термин «клетка-хозяин», при использовании в данном документе, относится к конкретной целевой клетке, трансфицированной молекулой нуклеиновой кислоты, и потомству или потенциальному потомству такой клетки. Потомство такой клетки может не быть идентичным родительской клетке, трансфицированной молекулой нуклеиновой кислоты из-за мутаций или влияний окружающей среды, которые могут иметь место в последующих поколениях, или интеграции молекулы нуклеиновой кислоты в геном клетки-хозяина.
Термин «в комбинации» в контексте применения других терапий относится к использованию более чем одной терапии. Использование термина «в комбинации» не ограничивает порядок, в котором терапии проводятся субъекту с заболеванием. Первая терапия может быть проведена раньше (например, на 1 минуту, 45 минут, 30 минут, 45 минут, 1 час, 2 часа, 4 часа, 6 часов, 12 часов, 24 часа, 48 часов, 72 часа, 96 часов, 1 неделю, 2 недели, 3 недели, 4 недели, 5 недель, 6 недель, 8 недель или 12 недель), одновременно или после (например, через 1 минуту, 45 минут, 30 минут, 45 минут, 1 час, 2 часа, 4 часа, 6 часов, 12 часов, 24 часа, 48 часов, 72 часа, 96 часов, 1 неделю, 2 недели, 3 недели, 4 недели, 5 недель, 6 недель, 8 недель или 12 недель) проведения второй терапии субъекту, у которого было, есть или который предрасположен к заболеванию, опосредованному PCSK9. Любая дополнительная терапия может проводиться в любом порядке с другими дополнительными терапиями. В некоторых вариантах осуществления изобретения антитела по изобретению можно вводить в комбинации с одним или несколькими видами лечения (например, с терапиями, которые не являются антителами по изобретению, которые в настоящее время вводят для профилактики, лечения, контроля и/или облегчения заболевания, опосредованного PCSK9). Неограничивающие примеры терапий, которые можно вводить в комбинации с антителом по изобретению, включают анальгетики, анестетики, антибиотики или иммуномодулирующие агенты или любые другие агенты, перечисленные в Фармакопее США и/или Настольном справочнике врача.
При использовании в данном документе, «инъекционное устройство» относится к устройству, которое предназначено для проведения инъекций, причем инъекция включает этапы временного гидравлического соединения инъекционного устройства с тканью человека, обычно с подкожной тканью. Инъекция дополнительно включает введение некоторого количества жидкого лекарственного средства в ткань и отсоединение или удаление инъекционного устройства от ткани. В некоторых вариантах осуществления изобретения инъекционное устройство может быть внутривенным или в/в устройством, которое представляет собой тип инъекционного устройства, используемого, когда целевой тканью является кровь в системе кровообращения, например кровь в вене. Распространенным, но не ограничивающим примером инъекционного устройства является игла и шприц.
При использовании в данном документе, «инструкции» относятся к отображению письменных, печатных или графических материалов на непосредственном контейнере изделия, например письменный материал, отображаемый на флаконе, содержащем фармацевтически активный агент, или подробности о составе и применении интересующего продукта, включенные в набор, содержащий интересующий состав. В инструкциях изложено предполагаемое применение или проведение способа лечения.
«Выделенное» или «очищенное» антитело или белок представляют собой соединения, которые были идентифицированы, отделены и/или выделены из компонентов среды его получения (например, природной или рекомбинантной). Например, антитело или белок практически не содержат клеточного материала или других загрязняющих белков из источника клетки или ткани, из которого происходит антитело, или практически не содержат химических прекурсоров или других химических реагентов при химическом синтезе. Выражение «практически без клеточного материала» включает препараты антитела, в которых антитело отделено от клеточных компонентов клеток, из которых оно выделено или получено рекомбинантно. Таким образом, антитело, которое практически не содержит клеточного материала, включает препараты антитела, содержащие менее около 30%, 20%, 10% или 5% (по массе сухого вещества) гетерологичного белка (также называемого в данном документе «загрязняющим белком»). Когда антитело получают рекомбинантным способом, оно также предпочтительно по существу не содержит культуральной среды, т.е. культуральная среда составляет менее около 20%, 10% или 5% от объема белкового препарата. Когда антитело получают путем химического синтеза, оно предпочтительно по существу не содержит химических прекурсоров или других химических реагентов, т.е. оно отделено от химических прекурсоров или других химических реагентов, которые участвуют в синтезе белка. Соответственно, такие препараты антитела содержат менее около 30%, 20%, 10%, 5% (по массе сухого вещества) химических прекурсоров или соединений, отличных от представляющего интерес антитела. В предпочтительном варианте осуществления изобретения антитела по изобретению выделяют или очищают.
Термины «нумерация по Кабату» и подобные термины известны в данной области и относятся к системе нумерации аминокислотных остатков, которые являются более вариабельными (т.е. гипервариабельными), чем другие аминокислотные остатки в вариабельных областях тяжелой цепи антитела или его антигенсвязывающей части (Kabat et al., (1971) Ann. NY Acad. Sci., 190:382-391 and, Kabat et al. (1991) Sequences of Proteins of Immunological Interest, Fifth Edition, U.S. Department of Health and Human Services, NIH Publication No. 91-3242). Для вариабельной области тяжелой цепи гипервариабельная область обычно находится в диапазоне положений аминокислот 31-35 для CDR1, положений аминокислот 50-65 для CDR2 и положений аминокислот 95-102 для CDR3.
«Метка» или «меченый», при использовании в данном документе, относится к добавлению детектируемого фрагмента к полипептиду, например, радиоактивной метки, флуоресцентной метки, ферментативной метки, хемилюминесцентной метки или биотинильной группы или золота. Радиоизотопы или радионуклиды могут включать 3Н, 14С, 15N, 35S, 90Y, 99Тс, 115In, 125I, 131I, флуоресцентные метки могут включать родамин, люминофоры на основе комплексов лантаноидов или FITC, а ферментные метки могут включать пероксидазу хрена, β-галактозидазу, люциферазу, щелочную фосфатазу. Дополнительные метки включают, в качестве иллюстрации, но не ограничения: ферменты, такие как глюкозо-6-фосфатдегидрогеназа («G6PDH»), альфа-D-галактозидаза, глюкозооксидаза, глюкозоамилаза, карбоангидраза, ацетилхолинэстераза, лизоцим, малатдегидрогеназа и пероксидаза; красители (например, цианиновые красители, например Су5™, Су5.5™ или Су7™); дополнительные флуоресцентные метки или флуоресцентные агенты включают, например, флуоресцеин и его производные, флуорохром, GFP (GFP для «зеленого флуоресцентного белка»), другие флуоресцентные белки (например, mCherry, mTomato), дансил, умбеллиферон, фикоэритрин, фикоцианин, аллофикоцианин, о-фталевый альдегид и флуорескамин; флуорофоры, такие как криптаты и хелаты лантаноидов, например европия и т.д. (анализы Perkin Elmer и Cisbio); хемолюминесцентные метки или хемилюминесцентные агенты, такие как изолюминол, люминол и диоксетаны; сенсибилизаторы; коферменты; ферментные субстраты; частицы, такие как частицы латекса или углерода; золь металлов; кристаллит; липосомы; клетки и т.д., которые могут быть дополнительно помечены красителем, катализатором или другой детектируемой группой; молекулы, такие как биотин, дигоксигенин или 5-бромдезоксиуридин; фрагменты токсина, такие как, например, фрагмент токсина, выбранного из группы экзотоксина синегнойной палочки (РЕ или его цитотоксический фрагмент или его мутант), дифтерийного токсина или его цитотоксического фрагмента или мутанта, токсин ботулина А, В, С, D, Е или F, рицина или его цитотоксического фрагмента, например рицина А, абрина или его цитотоксического фрагмента, сапорина или его цитотоксического фрагмента, противовирусного токсина из лаконоса или его цитотоксического фрагмента и бриодина 1 или его цитотоксического фрагмента.
Термин «легкая цепь», когда он используется в отношении антитела, относится к легким цепям иммуноглобулина, которые у млекопитающих бывают двух типов: лямбда (λ) и каппа (к). Легкая цепь предпочтительно представляет собой легкую цепь человека. Константная область легкой цепи предпочтительно представляет собой константную область человека. В человеческой популяции существует множество аллелей константной области легкой цепи. Нуклеотидные и аминокислотные последовательности этих аллельных вариантов доступны в общедоступных базах данных, таких как IMGT, ENSEMBL, Swiss-Prot и Uniprot. В одном варианте осуществления изобретения антитела или фрагменты антител, раскрытые в данном документе, содержат белок, кодируемый аллелем константной области к человека, который включает, но не ограничиваясь ими, IGKC*01 (см., например, таблицу последовательностей в данном документе), IGKC*02 (см., например, таблицу последовательностей в данном документе), IGKC*03 (см., например, таблицу последовательностей в данном документе), IGKC*04 (см., например, таблицу последовательностей в данном документе) и IGKC*05 (см., например, таблицу последовательностей в данном документе). В одном варианте осуществления изобретения антитела или фрагменты антител, раскрытые в данном документе, содержат белок, кодируемый аллелем константной области λ человека, который включает, но не ограничиваясь ими, IGLC1 *01 (см., например, таблицу последовательностей в данном документе), IGLC1*02 (см., например, таблицу последовательностей в данном документе), IGLC2*01 (см., например, таблицу последовательностей в данном документе), IGLC2*02 (см., например, таблицу последовательностей в данном документе), IGLC2*03 (см., например, таблицу последовательностей в данном документе), IGLC3*01 (см., например, таблицу последовательностей в данном документе), IGLC3*02 (см., например, таблицу последовательностей в данном документе), IGLC3*03 (см., например, таблицу последовательностей в данном документе), IGLC3*04 (см., например, таблицу последовательностей в данном документе), IGLC6*01 (см., например, таблицу последовательностей в данном документе), IGLC7*01 (см., например, таблицу последовательностей в данном документе), IGLC7*02 (см., например, таблицу последовательностей в данном документе), IGLC7*03 (см., например, таблицу последовательностей в данном документе). В другом варианте осуществления изобретения антитела и фрагменты антител, раскрытые в данном документе, содержат константную область легкой цепи, кодируемую аллелем константной области к мыши, который включает, но не ограничиваясь ими, IGKC*01, IGKC*03 или IGKC*03. В другом варианте осуществления изобретения антитела и фрагменты антител, раскрытые в данном документе, содержат константную область легкой цепи, кодируемую аллелем константной области λ мыши, который включает, но не ограничиваясь ими, IGLC1*01, IGLC2*01 или IGLC3*01.
«Процент (%) идентичности аминокислотной последовательности» и «гомология» по отношению к последовательности пептида, полипептида или антитела определяются как процент аминокислотных остатков в рассматриваемой последовательности, которые идентичны аминокислотным остаткам в конкретной пептидной или полипептидной последовательности после выравнивания последовательностей и введения пробелов, если необходимо, для достижения максимального процента идентичности последовательностей и без учета каких-либо консервативных замен как части идентичности последовательностей. Выравнивание для определения процента идентичности аминокислотной последовательности может быть достигнуто различными способами, которые известны специалистам в данной области техники, например, с использованием общедоступного компьютерного программного обеспечения, такого как программное обеспечение BLAST, В LAST-2, ALIGN или MEG ALIGN™ (DNASTAR). В одном варианте осуществления изобретения процент % гомологии составляет около 70%. В одном варианте осуществления изобретения процент % гомологии составляет около 75%. В одном варианте осуществления изобретения процент % гомологии составляет около 80%. В одном варианте осуществления изобретения процент % гомологии составляет около 85%. В одном варианте осуществления изобретения процент % гомологии составляет около 90%. В одном варианте осуществления изобретения процент % гомологии составляет около 92%. В одном варианте осуществления изобретения процент % гомологии составляет около 95%. В одном варианте осуществления изобретения процент % гомологии составляет около 97%. В одном варианте осуществления изобретения процент % гомологии составляет около 98%. В одном варианте осуществления изобретения процент % гомологии составляет около 99%. В одном варианте осуществления изобретения процент % гомологии составляет 100%.
Термин «встречающийся в природе» или «нативный» при использовании в связи с биологическими материалами, такими как молекулы нуклеиновых кислот, полипептиды, клетки-хозяева и т.п., относится к тем, которые встречаются в природе и не обработаны человеком.
При использовании в данном документе, «упаковка» относится к тому, как компоненты собраны и/или заключены в единичный элемент, пригодный для распространения и/или использования. Упаковка может включать, например, коробки, пакеты, шприцы, ампулы, флаконы, пробирки, двухстворчатую упаковку, барьеры и/или контейнеры для поддержания стерильности, маркировку и т.д. Термин «фармацевтически приемлемый», при использовании в данном документе, означает одобренный регуляторным органом Федерального правительства или правительства штата, или приведенный в Фармакопее США, европейской фармакопеи или другой общепризнанной фармакопее для применения у животных и более конкретно у людей.
При использовании в данном документе, термин «полинуклеотид», «нуклеотид», «нуклеиновая кислота», «молекула нуклеиновой кислоты» и другие подобные термины используются взаимозаменяемо и включают ДНК, РНК, мРНК и т.п. При использовании в данном документе, термины «предотвращать», «предотвращающий» и «профилактика» относятся к полному или частичному ингибированию развития, рецидива, начала или распространения опосредованного hPCSK9 заболевания и/или симптома, связанного с ним, врезультате применения терапии или комбинации терапий, представленных в данном документе (например, комбинации профилактических или терапевтических агентов, таких как антитело по изобретению). Термин «растворимый» относится к полипептиду, такому как PCSK9 и его варианты или фрагменты, в котором отсутствуют один или несколько трансмембранных или цитоплазматических доменов, обнаруженных в нативной или ассоциированной с мембраной форме. В одном варианте осуществления изобретения «растворимая» форма PCSK9 лишена как трансмембранного домена, так и цитоплазматического домена.
Термин «субъект» или «пациент» относится к любому животному, включая, помимо прочего, млекопитающих. При использовании в данном документе, термин «млекопитающее» относится к любому позвоночному животному, которое вскармливает молоком своих детенышей и либо рожает живого детеныша (нормальные или плацентарные млекопитающие), либо откладывает яйца (метатерий или неплацентарные млекопитающие). Примеры видов млекопитающих включают, но не ограничиваясь ими, людей и других приматов, включая обезьян, таких как шимпанзе и другие виды человекообразных обезьян и мартышек; сельскохозяйственных животных, таких как крупный рогатый скот, овцы, свиньи, козы и лошади; домашние млекопитающие, такие как собаки и кошки; лабораторные животные, включая грызунов, таких как мыши, крысы (включая хлопковых хомяков) и морские свинки; птицы, включая домашних, диких и охотничьих птиц, таких как куры, индейки и другие куриные, утки, гуси и т.п.
При использовании в данном документе, термин «практически все» относится к по меньшей мере около 60%, по меньшей мере около 70%, по меньшей мере около 75%, по меньшей мере около 80%, по меньшей мере около 85%, по меньшей мере около 90%, по меньшей мере около 95%, по меньшей мере около 98%, по меньшей мере около 99% или около 100%.
При использовании в данном документе, термин «терапевтический агент» относится к любому агенту, который можно использовать для лечения, ведения или облегчения опосредованного PCSK9 заболевания и/или симптома, связанного с ним. В некоторых вариантах осуществления изобретения термин «терапевтический агент» относится к антителу по изобретению. В некоторых других вариантах осуществления изобретения термин «терапевтический агент» относится к агенту, отличному от антитела по изобретению. Терапевтическое средство предпочтительно представляет собой средство, которое, как известно, пригодно, или использовалось или используется в данное время для лечения, ведения или облегчения заболевания, опосредованного PCSK9, или одного или нескольких симптомов, связанных с ним. В конкретных вариантах осуществления изобретения терапевтический агент представляет собой полностью человеческое антитело к PCSK9, такое как полностью человеческое моноклональное антитело к PCSK9.
При использовании в данном документе, термин «терапия» относится к любому протоколу, методу и/или агенту, которые можно использовать для профилактики, ведения, лечения и/или облегчения заболевания, опосредованного PCSK9 (например, рака). В некоторых вариантах осуществления изобретения термины «терапии» и «терапия» относятся к биологической терапии, поддерживающей терапии и/или другим видам терапии, применимым для профилактики, ведения, лечения и/или облегчения опосредованного PCSK9 заболевания, известного специалисту в данной области техники, например медицинскому персоналу. Термины «лечить», «лечение» и «лечащий» относятся к снижению или облегчению прогрессирования, тяжести и/или продолжительности опосредованного hPCSK9 заболевания (например, рака), возникающего в результате применения одного или более видов лечения (включая, но не ограничиваясь этим, введение одного или более профилактических или терапевтических агентов, таких как антитело по изобретению). В конкретных вариантах осуществления изобретения такие термины относятся к снижению или ингибированию связывания hPCSK9 с рецептором BMP или HJV и/или ингибированию или ослаблению одного или более симптомов, связанных с заболеванием, опосредованным PCSK9, таким как гиперлипидемия или гиперхолестеринемия.
Термин «вариабельная область» или «вариабельный домен» относится к части легкой и тяжелой цепей, обычно от около 120 до 130 аминокислот на амино-конце тяжелой цепи и от около 100 до 110 аминокислот на амино-конце легкой цепи, которые сильно различаются по последовательности среди антител и используются при связывании и специфичности каждого конкретного антитела в отношении его конкретного антигена. Вариабельность последовательности сосредоточена в тех областях, которые называются определяющими комплементарность областями (CDR), в то время как более высококонсервативные области в вариабельном домене называются каркасными областями (FR). CDR PCSK9 и тяжелых цепей в первую очередь ответственны за взаимодействие антитела с антигеном. Используемая в данном документе нумерация аминокислотных положений соответствует индексу EU, как в Kabat et al. (1991) Sequences of proteins of immunological interest. (U.S. Department of Health and Human Services, Washington, D.C.) 5th ed. («Kabat et al.»). В предпочтительных вариантах осуществления изобретения вариабельная область представляет собой вариабельную область человека.
Определения общих терминов в клеточной биологии и молекулярной биологии можно найти в "The Merck Manual of Diagnosis and Therapy", 19th Edition, published by Merck Research Laboratories, 2006 (ISBN 0-911910-19-0); Robert S. Porter et al. (eds.), The Encyclopedia of Molecular Biology, published by Blackwell Science Ltd., 1994 (ISBN 0-632-02182-9); Benjamin Lewin, Genes X, published by Jones & Bartlett Publishing, 2009 (ISBN-10: 0763766321); Kendrew et al. (Eds.), Molecular Biology and Biotechnology: a Comprehensive Desk Reference, published by VCH Publishers, Inc., 1995 (ISBN 1-56081-569-8) и Current Protocols in Protein Sciences 2009, Wiley lntersciences, Coligan et al., eds.
Если не указано иное, данное изобретение было выполнено с использованием стандартных процедур, как описано, например, в Sambrook et al., Molecular Cloning: A Laboratory Manual (4 ed.), Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y., USA (2012); Davis et al., Basic Methods in Molecular Biology, Elsevier Science Publishing, Inc., New York, USA (1995); or Methods in Enzymology: Guide to Molecular Cloning Techniques Vol. 152, S.L. Berger and A.R. Kimmel Eds., Academic Press Inc., San Diego, USA (1987); Current Protocols in Protein Science (CPPS) (John E. Coligan, et al., ed., John Wiley and Sons, Inc.), Current Protocols in Cell Biology (CPCB) (Juan S. Bonifacino et al., ed., John Wiley and Sons, Inc.), и Culture of Animal Cells: A Manual of Basic Technique by R. Ian Freshney, Publisher: Wiley-Liss; 5th edition (2005), Animal Cell Culture Methods (Methods in Cell Biology, Vol. 57, Jennie P. Mather and David Barnes editors, Academic Press, 1st edition, 1998), которые включены в данный документ в полном объеме посредством ссылки.
Другие термины определены в данном документе в описании различных аспектов изобретения.
Антитела и фрагменты к PCSK9
В изобретении предложены различные антитела и фрагменты к PCSK9 (такие как фрагменты Fab или scFv), применения, способы и комбинации (например, со статином). Примеры приведены в следующих пронумерованных пунктах.
1. Антитело или фрагмент, содержащий сайт связывания, который специфически связывается с пропротеиновой конвертазой субтилизин-кексинового типа 9 (PCSK9), причем сайт связывания включает домен VH, который кодируется нуклеотидной последовательностью, полученной в результате рекомбинации сегмента гена VH, сегмента гена DH и сегмента гена JH человека, при этом сегмент гена VH выбран из IGHV4-59 и IGHV3-9.
Например, сегмент гена VH представляет собой IGHV4-59*01, а сегмент гена DH и сегменты гена JH представляют собой сегменты гена человека. Например, сегмент гена VH представляет собой IGHV3-9*01, а сегмент гена DH и сегменты гена JH представляют собой сегменты гена человека.
В одном примере специфическое связывание происходит с KD, Koff и/или Kon, как описано дополнительно ниже. В одном примере специфическое связывание происходит с KD от 1 пМ до 5 нМ.
Специалист в данной области техники знаком с базами данных и другими источниками сегментов генов антител человека и других видов. Например, база данных IMGT (www.IMGT.org) является подходящим источником, например, версия по состоянию на 1 сентября 2018 г.
Ссылка сделана на Примеры, показывающие антитела, основанные на IGHV4-59 и IGHV3-9. Неожиданно этот сегмент гена VH человека продуцирует антитела к PCSK9, которые обладают желаемыми свойствами против PCSK9, такими как те, что описаны, например, в Примерах.
Например, антитело или фрагмент по данному изобретению предназначены для введения субъекту для снижения общего холестерина в плазме и холестерина, не относящегося к ЛПВП, у субъекта дозозависимым образом.
Например, антитело или фрагмент по изобретению предназначены для введения субъекту для снижения общего холестерина в плазме у субъекта.
Например, антитело или фрагмент по изобретению предназначены для введения субъекту для снижения уровня холестерина, не относящегося к ЛПВП, в плазме (необязательно дозозависимым образом) у субъекта.
Например, антитело или фрагмент по изобретению предназначены для введения субъекту для снижения уровней триглицеридов в плазме у субъекта.
В варианте осуществления любого из этих примеров уровень холестерина ЛПВП у субъекта не снижается или существенно не снижается.
Примеры показывают пользу от введения антител по изобретению по сравнению с контрольным алирокумабом. Например, антитело или фрагмент по изобретению предназначены для введения субъекту для лечения или профилактики PCSK9-опосредованного заболевания или патологического состояния (например, гетерозиготной семейной гиперхолестеринемии (HeFH) или гомозиготной семейной гиперхолестеринемии (HoFH)), причем антитело или фрагмент вводят в дозе менее 75 мг каждые 2 недели или 300 мг каждые 4 недели. Например, антитело или фрагмент по изобретению предназначены для введения субъекту для лечения или профилактики PCSK9-опосредованного заболевания или патологического состояния (например, гетерозиготной семейной гиперхолестеринемии (HeFH) или гомозиготной семейной гиперхолестеринемии (HoFH)), причем антитело или фрагмент вводят в дозе менее 140 мг каждые 2 недели или менее 420 мг каждые 4 недели. Например, антитело или фрагмент по изобретению предназначены для введения субъекту для лечения или профилактики PCSK9-опосредованного заболевания или патологического состояния (например, гетерозиготной семейной гиперхолестеринемии (HeFH) или гомозиготной семейной гиперхолестеринемии (HoFH)), причем антитело или фрагмент вводят в дозе менее чем доза пралуэнта или репаты каждые 2 недели. Например, антитело или фрагмент по изобретению предназначены для введения субъекту для лечения или профилактики PCSK9-опосредованного заболевания или патологического состояния (например, гетерозиготной семейной гиперхолестеринемии (HeFH) или гомозиготной семейной гиперхолестеринемии (HoFH)), причем антитело или фрагмент вводят в дозе менее чем доза пралуэнта или репаты каждые 4 недели. Например, антитело или фрагмент по изобретению предназначены для введения субъекту для лечения или профилактики PCSK9-опосредованного заболевания или патологического состояния (например, гетерозиготной семейной гиперхолестеринемии (HeFH) или гомозиготной семейной гиперхолестеринемии (HoFH)), причем антитело или фрагмент вводят раз в 2 недели или 4 недели в дозе, которая менее 70, 65, 60, 50, 40, 30 или 25 мг.
Рекомендуемая начальная доза Praluent™ составляет 75 мг один раз в 2 недели, вводимая подкожно, поскольку у большинства пациентов достигается достаточное снижение уровня XC-ЛПНП при этой дозировке, или 2×150 мг каждые 4 недели.
Рекомендуемая подкожная дозировка Repatha™ у взрослых с установленным сердечно-сосудистым заболеванием или у взрослых с первичной гиперлипидемией (включая гетерозиготную семейную гиперхолестеринемию [HeFH] составляет 140 мг каждые 2 недели или 420 мг один раз в месяц, в зависимости от предпочтений пациента в отношении частоты дозирования и объема инъекции. Рекомендуемая подкожная доза Repatha™ для пациентов с HoFH составляет 420 мг один раз в месяц.
Например, антитело или фрагмент содержат последовательность CDRH3 антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT), и необязательно CDRL3 указанного выбранного антитела. Например, антитело или фрагмент содержат последовательности CDRH1 и CDRH3 антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT), и необязательно CDRL2 указанного выбранного антитела. Например, антитело или фрагмент содержат последовательности CDRH1 и CDRH2 антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT). Например, антитело или фрагмент содержат последовательности CDRH2 и CDRH3 антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT). Например, антитело или фрагмент содержат сайт связывания с PCSK9, причем сайт связывания содержит домен VH, содержащий последовательность CDRH3 CL-58838, спаренный с доменом VL CL-58838.
Например, антитело или фрагмент содержат сайт связывания с PCSK9, причем сайт связывания содержит домен VH, содержащий SEQ ID №1, необязательно спаренный с доменом VL, содержащим соответственно SEQ ID №33. Например, антитело или фрагмент содержат сайт связывания с PCSK9, причем сайт связывания содержит домен VH, содержащий SEQ ID №65, спаренный с доменом VL, содержащим SEQ ID №95.
Например, антитело или фрагмент содержат сайт связывания с PCSK9, причем сайт связывания включает домен VH антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT), необязательно спаренный с доменом VL выбранного антитела. Например, антитело или фрагмент содержат сайт связывания с PCSK9, причем сайт связывания содержит домен VH CL-58838, спаренный с доменом VL CL-58838.
2. Антитело или фрагмент по п. 1, в которых (i) сегмент гена VH представляет собой IGHV4-59 (например, IGHV4-59*01), а сегмент гена DH представляет собой сегмент гена человека IGHD3-10 (например, IGHD3-10*01); или (ii) сегмент гена VH представляет собой IGHV3-9 (например, IGHV3-9*01), а сегмент гена DH представляет собой сегмент гена человека IGHD3-9 (например, IGHD3-9*01).
3. Антитело или фрагмент по п. 1 или 2, в котором сегмент гена JH представляет собой сегмент гена человека JH6 (например, JH6*02).
4. Антитело или фрагмент, которые специфически связываются с пропротеиновой конвертазой субтилизин-кексинового типа 9 (PCSK9) и содержат последовательность CDRH3 антитела к PCSK9 по любому из предыдущих пунктов.
5. Антитело или фрагмент, которые специфически связываются с пропротеиновой конвертазой субтилизин-кексинового типа 9 (PCSK9) и содержат домен VH, который содержит последовательность CDRH3 любого антитела к PCSK9, описанного в данном документе (например, CL-148219 или CL-148489), или указанную последовательность CDRH3, содержащую 3, 2 или 1 аминокислотную замену(-ы).
6. Антитело или фрагмент (необязательно по любому предыдущему пункту), которые специфически связывается с пропротеиновой конвертазой субтилизин-кексинового типа 9 (PCSK9) и содержат домен VH, который содержит последовательность CDRH3 антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или указанную последовательность, содержащую 3, 2 или 1 аминокислотную замену(-ы).
Необязательно, домен VH содержит последовательность CDRH3, выбранную из последовательностей CDRH3, раскрытых в данном документе, или указанную выбранную последовательность, содержащую 3, 2 или 1 аминокислотную замену(-ы).
7. Антитело или фрагмент по п. 6, в которых домен VH содержит (i) последовательность CDRH3 антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или указанную последовательность CDRH3, содержащую 3, 2 или 1 аминокислотную замену(-ы); и (ii) последовательность CDRH1 указанного выбранного антитела; или указанную последовательность CDRH1, содержащую 3, 2 или 1 аминокислотную замену(-ы).
8. Антитело или фрагмент по п. 6 или 7, в которых домен VH содержит (iii) последовательность CDRH3 антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или указанную последовательность CDRH3, содержащую 3, 2 или 1 аминокислотную замену(-ы); и (iv) последовательность CDRH2 указанного выбранного антитела; или указанную последовательность CDRH2, содержащую 3, 2 или 1 аминокислотную замену(-ы).
9. Антитело или фрагмент (необязательно по любому предыдущему пункту), содержащие сайт связывания, который специфически связывается с пропротеиновой конвертазой субтилизин-кексинового типа 9 (PCSK9), причем сайт связывания содержит домен VH, который содержит аминокислотную последовательность домена VH антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или аминокислотную последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%.
Например, идентичность составляет по меньшей мере 85%. Например, идентичность составляет по меньшей мере 90%. Например, идентичность составляет по меньшей мере 95%.
Необязательно домен VH антитела или фрагмента содержит аминокислотную последовательность VH, описанную в данном документе, или аминокислотную последовательность вариабельного домена тяжелой цепи, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%. Например, идентичность составляет по меньшей мере 85%. Например, идентичность составляет по меньшей мере 90%. Например, идентичность составляет по меньшей мере 95%.
10. Антитело или фрагмент по любому из предыдущих пунктов, содержащий первую и вторую копии указанного домена VH.
В одном примере антитело или фрагмент содержат сайт связывания, содержащий домен VH по изобретению, спаренный с доменом VL по изобретению, причем сайт связывания способен специфически связываться с PCSK9 (например, зрелая PCSK9, например PCSK9 человека и/ил и яванского макака). Например, антитело или фрагмент содержат два таких сайта связывания.
11. Антитело или фрагмент (необязательно по любому предыдущему пункту), содержащие сайт связывания, который специфически связывается с пропротеиновой конвертазой субтилизин-кексинового типа 9 (PCSK9), причем сайт связывания содержит домен VL, который кодируется нуклеотидной последовательностью, полученной путем рекомбинации сегмента гена VL и сегмента гена JL человека, причем сегмент гена VL выбран из IGKV2-28 (например, IGKV2-28*01) и IGKV2-29 (например, IGKV2-29*01).
12. Антитело или фрагмент по п. 11, в которых VL представляет собой Vк, а сегмент гена JL представляет собой сегмент гена человека, выбранный из IGKJ3 и IGKJ4.
Необязательно, сегмент гена JL выбран из IGKJ3*01 и IGKJ4*01.
13. Антитело или фрагмент, которые специфически связываются с пропротеиновой конвертазой субтилизин-кексинового типа 9 (PCSK9) и содержат последовательность CDRL3 антитела к PCSK9 в соответствии с п. 11 или 12.
14. Антитело или фрагмент (необязательно по любому предыдущему пункту), которые специфически связываются с пропротеиновой конвертазой субтилизин-кексинового типа 9 (PCSK9) и содержат домен VL, который содержит последовательность CDRL3 любого антитела к PCSK9, описанного в данном документе (например, CL-148219 или CL-148489), или указанную выбранную последовательность CDRL3, содержащую 3, 2 или 1 аминокислотную замену(-ы).
15. Антитело или фрагмент по п. 14, содержащие домен VH, который содержит последовательность CDRH3 указанного выбранного антитела.
16. Антитело или фрагмент (необязательно по любому предыдущему пункту), которые специфически связываются с пропротеиновой конвертазой субтилизин-кексинового типа 9 (PCSK9) и содержат домен VL, который содержит последовательность CDRL3, выбранную из последовательности CDRL3, раскрытой в данном документе, или указанной выбранной последовательности CDRL3, содержащей 3, 2 или 1 аминокислотную замену(-ы).
17. Антитело или фрагмент (необязательно по любому предыдущему пункту), которые специфически связываются с пропротеиновой конвертазой субтилизин-кексинового типа 9 (PCSK9) и содержат домен VL, который содержит последовательность CDRL3 (и необязательно CDRH3) антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или указанную последовательность(-и), каждая из которых содержит 3, 2 или 1 аминокислотную замену(-ы).
18. Антитело или фрагмент по п. 17, в которых домен VL содержит (i) последовательность CDRL3 (и необязательно CDRH3) антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или указанную последовательность(-и) CDR3, каждая из которых содержит 3, 2 или 1 аминокислотную замену(-ы); и (ii) последовательность CDRL1 (и необязательно CDRH1) указанного выбранного антитела; или указанную последовательность(-и) CDR1, каждая из которых содержит 3, 2 или 1 аминокислотную замену(-ы).
19. Антитело или фрагмент по п. 17 или 18, в которых домен VL содержит (iii) последовательность CDRL3 (и необязательно CDRH3) антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или указанную последовательность(-и) CDR3, каждая из которых содержит 3, 2 или 1 аминокислотную замену(-ы); и (iv) последовательность CDRL2 (и необязательно CDRH2) указанного выбранного антитела; или указанную последовательность(-и) CDR2, каждая из которых содержит 3, 2 или 1 аминокислотную замену(-ы).
20. Антитело или фрагмент (необязательно по любому предыдущему пункту), содержащие сайт связывания, который специфически связывается с пропротеиновой конвертазой субтилизин-кексинового типа 9 (PCSK9), причем сайт связывания содержит домен VL, который содержит аминокислотную последовательность домена VL антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или аминокислотную последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%.
Например, идентичность составляет по меньшей мере 85%. Например, идентичность составляет по меньшей мере 90%. Например, идентичность составляет по меньшей мере 95%.
21. Антитело или фрагмент по любому из предыдущих пунктов, содержащий первую и вторую копии указанного домена VL.
В одном примере антитело или фрагмент содержат сайт связывания, содержащий домен VL по изобретению, спаренный с доменом VH, причем сайт связывания способен специфически связываться с PCSK9 (например, зрелая PCSK9, например, PCSK9 человека и/или яванского макака). Например, антитело или фрагмент содержат два таких сайта связывания.
22. Антитело или фрагмент (необязательно по любому предыдущему пункту), которые специфически связываются с пропротеиновой конвертазой субтилизин-кексинового типа 9 (PCSK9) и содержат аминокислотную последовательность тяжелой цепи антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или аминокислотную последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%.
В одном примере последовательность тяжелой цепи содержит аминокислотную последовательность VH CL-148219 или CL-148489, слитую с константной областью тяжелой цепи антитела, описанной в данном документе, например константной областью lgG4-PE, например SEQ ID №3. Дополнительно или альтернативно, в качестве примера последовательность легкой цепи содержит аминокислотную последовательность VL CL-148219 или CL-148489, слитую с константной областью легкой цепи антитела, описанной в данном документе, например константной областью каппа, например SEQ ID №156.
Например, идентичность составляет по меньшей мере 85%. Например, идентичность составляет по меньшей мере 90%. Например, идентичность составляет по меньшей мере 95%.
23. Антитело или фрагмент (необязательно по любому предыдущему пункту), которые специфически связываются с пропротеиновой конвертазой субтилизин-кексинового типа 9 (PCSK9) и содержат аминокислотную последовательность легкой цепи антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или аминокислотную последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%.
Например, идентичность составляет по меньшей мере 85%. Например, идентичность составляет по меньшей мере 90%. Например, идентичность составляет по меньшей мере 95%.
24. Антитело или фрагмент по п. 23, содержащие аминокислотную последовательность легкой цепи указанного выбранного антитела; или аминокислотную последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%.
Например, идентичность составляет по меньшей мере 85%. Например, идентичность составляет по меньшей мере 90%. Например, идентичность составляет по меньшей мере 95%.
25. Антитело или фрагмент (необязательно по любому предыдущему пункту), которые специфически связываются с эпитопом PCSK9 человека, идентичным эпитопу, с которым связывается антитело по любому предыдущему пункту.
26. Антитело или фрагмент по п. 25, в которых эпитоп идентифицируют сканированием неродственными аминокислотами или рентгеновской кристаллографией.
Контактные аминокислотные остатки, участвующие во взаимодействии антитела и антигена, могут быть определены различными методами, известными специалистам в данной области техники.
В одном варианте осуществления изобретения последовательная замена аминокислот в последовательности антигена (с использованием стандартных методов молекулярной биологии для мутации ДНК кодирующей последовательности антигена), в этом случае PCSK9 с аланином (также известный как аланиновое сканирование) или другой неродственной аминокислотой, может давать остатки, мутация которых будет снижать или устранять способность антитела распознавать рассматриваемый антиген. Связывание можно оценить с использованием стандартных методов, таких как, но не ограничиваясь ими, SPR, HTRF, ELISA (которые описаны в другом месте в данном документе). Для усиления нарушения связывания могут быть осуществлены другие замены, такие как изменение заряда боковой цепи аминокислот последовательности антигена (например, замена лизина на глутаминовую кислоту), переключение полярных и неполярных остатков (например, замена серина на лейцин). Аланиновое сканирование или другой метод замены аминогруппы можно проводить либо с рекомбинантным растворимым антигеном, либо, если мишенью является мишень клеточной мембраны, непосредственно на клетках с использованием временной или стабильной экспрессии мутированных версий.
В одном варианте осуществления изобретения можно использовать кристаллографию белка для определения контактных остатков между антителом и антигеном (т.е. для определения эпитопа, с которым связывается антитело), кристаллография позволяет напрямую визуализировать контактные остатки, участвующие во взаимодействии антитело-антиген. Помимо стандартной рентгеновской кристаллографии для определения контактных остатков между антителами и капсидным белком ВИЧ использовали криоэлектронную микроскопию (см. Lee, Jeong Hyun, et al. "Antibodies to a conformational epitope on gp41 neutralize HIV-1 by destabilizing the Env spike.", Nature communications, 6, (2015)).
В одном варианте осуществления изобретения, если антитело распознает линейный эпитоп, могут быть получены короткие пептиды на основе последовательности антигена, и связывание антитела с этими пептидами может быть оценено с использованием стандартных методов, таких как, но не ограничиваясь ими, SPR, HTRF, ELISA (которые описаны в другом месте в данном документе). Дальнейшее исследование эпитопа может быть проведено путем аланинового сканирования любых пептидов, которые демонстрируют связывание. В качестве альтернативы линейным пептидам конформационное сканирование может быть выполнено с помощью технологии Pepscan (http://www.pepscan.com/) с использованием химического связывания пептидов с остовами, что было использовано для определения прерывистых эпитопов на антителах, нацеленных на CD20 (Niederfellner, Gerhard, et al. "Epitope characterization and crystal structure of GA101 provide insights into the molecular basis for type I/II distinction of CD20 antibodies.", Blood, 118.2, (2011), 358-367).
В одном варианте осуществления изобретения для идентификации связывающих эпитопов можно использовать ограниченное протеолитическое расщепление и масс-спектрометрию. Комплекс антитело-антиген расщепляется протеазой, такой как, но не ограничиваясь им, трипсин. Расщепленные комплексные пептиды сравнивают с помощью масс-спектрометрии с расщеплением только антитела и только антигена, чтобы определить, защищен ли конкретный эпитоп комплексообразованием. Затем для сужения до отдельных аминокислотных остатков, участвующих во взаимодействии, может быть осуществлено дальнейшее исследование, включающее замену аминокислот, конкурентное связывание (см., например, Suckau, Detlev, et al. "Molecular epitope identification by limited proteolysis of an immobilized antigen-antibody complex and mass spectrometric peptide mapping.", Proceedings of the National Academy of Sciences, 87.24, (1990), 9848-9852).
Таким образом, в одном варианте осуществления изобретения контактные остатки эпитопа идентифицируют с помощью сканирования неродственными аминокислотами (например, аланинового сканирования). В другом варианте осуществления изобретения сканирование неродственными аминокислотами (например, аланиновое сканирование) проводят с использованием метода, выбранного из SPR, HTRF, ELISA, рентгеновской кристаллографии, криоэлектронной микроскопии и комбинации ограниченного протеолитического расщепления и масс-спектрометрии. В одном варианте осуществления изобретения сканирование неродственными аминокислотами (например, аланиновое сканирование) проводят с использованием HTRF. В одном варианте осуществления изобретения сканирование неродственными аминокислотами (например, аланиновое сканирование) проводят с использованием ELISA. Когда аланиновое сканирование выполняют с помощью ELISA или HTRF, аминокислотный остаток идентифицируют как вносящий вклад в эпитоп, если снижение сигнала составляет по меньшей мере 25%. В одном варианте осуществления изобретения снижение сигнала составляет по меньшей мере 30%. В одном варианте осуществления изобретения снижение сигнала составляет по меньшей мере 35%. В одном варианте осуществления изобретения снижение сигнала составляет по меньшей мере 40%. В одном варианте осуществления изобретения снижение сигнала составляет по меньшей мере 45%. В одном варианте осуществления изобретения снижение сигнала составляет по меньшей мере 50%. В одном варианте осуществления изобретения снижение сигнала составляет по меньшей мере 55%. В одном варианте осуществления изобретения снижение сигнала составляет по меньшей мере 60%. В одном варианте осуществления изобретения снижение сигнала составляет по меньшей мере 70%. В одном варианте осуществления изобретения снижение сигнала составляет по меньшей мере 75%. В одном варианте осуществления изобретения снижение сигнала составляет по меньшей мере 80%. В одном варианте осуществления изобретения снижение сигнала составляет по меньшей мере 85%. В одном варианте осуществления изобретения снижение сигнала составляет по меньшей мере 90%.
Когда аланиновое сканирование выполняют с помощью SPR1 аминокислотный остаток идентифицируется как вносящий вклад в эпитоп, если наблюдается по меньшей мере 10-кратное снижение аффинности. В одном варианте осуществления изобретения снижение аффинности происходит по меньшей мере в 15 раз. В одном варианте осуществления изобретения снижение аффинности происходит по меньшей мере в 20 раз. В одном варианте осуществления изобретения снижение аффинности происходит по меньшей мере в 30 раз. В одном варианте осуществления изобретения снижение аффинности происходит по меньшей мере в 40 раз. В одном варианте осуществления изобретения снижение аффинности происходит по меньшей мере в 50 раз. В одном варианте осуществления изобретения снижение аффинности происходит по меньшей мере в 100 раз.
В одном варианте осуществления изобретения контактные остатки эпитопа идентифицируют с помощью рентгеновской кристаллографии. В одном варианте осуществления контактные остатки эпитопа идентифицируют с помощью криоэлектронной микроскопии. В одном варианте осуществления изобретения контактные остатки эпитопа идентифицируют с помощью комбинации ограниченного протеолитического расщепления и масс-спектрометрии.
27. Антитело или фрагмент по п. 26, в которых контактные остатки эпитопа определены по снижению аффинности по меньшей мере в 10 раз при сканировании неродственными аминокислотами, например аланиновом сканировании, что определено с помощью SPR.
В одном варианте осуществления изобретения снижение аффинности происходит по меньшей мере в 15 раз. В одном варианте осуществления изобретения снижение аффинности происходит по меньшей мере в 20 раз. В одном варианте осуществления изобретения снижение аффинности происходит по меньшей мере в 30 раз. В одном варианте осуществления изобретения снижение аффинности происходит по меньшей мере в 40 раз. В одном варианте осуществления изобретения снижение аффинности происходит по меньшей мере в 50 раз. В одном варианте осуществления изобретения снижение аффинности происходит по меньшей мере в 100 раз. SPR можно проводить, как описано в данном документе.
28. Антитело или фрагмент (необязательно по любому предыдущему пункту), которые конкурируют за связывание с PCSK9 человека с антителом по любому предыдущему пункту.
Необязательно, конкуренция определяется поверхностным плазмонным резонансом (SPR) или ELISA. Специалист в данной области техники знаком, например, с этими методами и стандартными условиями.
В одном варианте осуществления изобретения антитело или фрагмент конкурируют (например, дозозависимым образом) с hPCSK9 (или его слитым белком) за связывание с hPCSK9, экспрессируемым на клеточной поверхности. В одном варианте осуществления изобретения антитело или фрагмент конкурирует (например, дозозависимым образом) с hPCSK9 (или его слитым белком) за связывание с растворимым hPCSK9.
Необязательно, конкуренцию за связывание с hPCSK9 изучают с использованием SPR. SPR можно проводить, как описано в данном документе.
29. Антитело или фрагмент по любому предыдущему пункту, которые специфически связывается с PCSK9 человека, содержащей любую из SEQ ID №189-192; и/или PCSK9 яванского макака, содержащей SEQ ID №193; и/или PCSK9 мыши, содержащей SEQ ID №194.
Необязательно, антитело или фрагмент по изобретению специфически связываются с аминокислотной последовательностью SEQ ID №189. Необязательно, антитело или фрагмент по изобретению специфически связываются с аминокислотной последовательностью SEQ ID №193. Необязательно, антитело или фрагмент по изобретению специфически связываются с аминокислотной последовательностью SEQ ID №194.
В одном примере PCSK9 в данном документе представляет собой PCSK9 человека, мыши или яванского макака.
В одном варианте осуществления изобретения антитело или фрагмент связываются с PCSK9 яванского макака с аффинностью менее 1 нМ (например, от 1 нМ до 0,01 пМ, или от 1 нМ до 0,1 пМ, или от 1 нМ до 1 пМ). В одном варианте осуществления изобретения антитело или фрагмент связываются с PCSK9 яванского макака с аффинностью менее 10 нМ (например, от 10 нМ до 0,01 пМ, или от 10 нМ до 0,1 пМ, или от 10 нМ до 1 пМ). В одном варианте осуществления изобретения антитело или фрагмент связываются с PCSK9 яванского макака с аффинностью менее 0,1 нМ (например, от 0,1 нМ до 0,01 пМ, или от 0,1 нМ до 0,1 пМ, или от 0,1 нМ до 1 пМ). В одном варианте осуществления изобретения антитело или фрагмент связываются с PCSK9 яванского макака с аффинностью менее 0,01 нМ (например, от 0,011 нМ до 0,01 пМ или от 0,01 нМ до 0,1 пМ).
В одном варианте осуществления изобретения антитело или фрагмент связываются с PCSK9 яванского макака с аффинностью в пределах 2-кратной аффинности к hPCSK9. В одном варианте осуществления изобретения антитело или фрагмент связываются с PCSK9 яванского макака с аффинностью в пределах 4-кратной аффинности к hPCSK9. В одном варианте осуществления изобретения антитело или фрагмент связываются с PCSK9 яванского макака с аффинностью в пределах 5-кратной аффинности к hPCSK9. В одном варианте осуществления изобретения антитело или фрагмент связываются с PCSK9 яванского макака с аффинностью в пределах 6-кратной аффинности к hPCSK.9. В одном варианте осуществления изобретения антитело или фрагмент связываются с PCSK9 яванского макака с аффинностью в пределах 8-кратной аффинности к hPCSK9. В одном варианте осуществления изобретения антитело или фрагмент связываются с PCSK9 яванского макака с аффинностью в пределах 10-кратной аффинности к hPCSK9.
«hPCSK9» в данном документе представляет собой PCSK9 человека, например PCSK9 человека, раскрытый в данном документе, например содержащий SEQ ID №562.
В одном варианте осуществления изобретения антитело или фрагмент обнаружимо не связываются с PCSK9 яванского макака. В одном варианте осуществления изобретения антитело или фрагмент не связываются с PCSK9 мыши (например, мыши и/или крысы).
В одном варианте осуществления изобретения антитело или фрагмент связываются с PCSK9 мыши (например, мыши и/или крысы) с аффинностью менее 1 нМ (например, от 1 нМ до 0,01 пМ, или от 1 нМ до 0,1 пМ, или от 1 нМ до 1 пМ). В одном варианте осуществления изобретения антитело или фрагмент связываются с PCSK9 мыши с аффинностью менее 10 нМ (например, от 10 нМ до 0,01 пМ, или от 10 нМ до 0,1 пМ, или от 10 нМ до 1 пМ). В одном варианте осуществления изобретения антитело или фрагмент связываются с PCSK9 мыши с аффинностью менее 0,1 нМ (например, от 0,1 нМ до 0,01 пМ, или от 0,1 нМ до 0,1 пМ, или от 0,1 нМ до 1 пМ). В одном варианте осуществления изобретения антитело или фрагмент связываются с PCSK9 мыши с аффинностью менее 0,01 нМ (например, от 0,011 нМ до 0,01 пМ или от 0,01 нМ до 0,1 пМ).
Необязательно, антитело или фрагмент содержат константную область, активируемую или деактивируемую эффектором, такую как константная область человека, например безэффекторная константная область человека, например константная область lgG4 или константная область lgG1, при этом необязательно константная область область представляет собой lgG4-PE или отключенный lgG1. Необязательно, антитело или фрагмент содержат константную область мыши (например, мыши и/или крысы). Необязательно, антитело или фрагмент содержат любую из описанных в данном документе последовательностей константной области тяжелой цепи.
Необязательно, константная область имеет активность CDC и/или ADCC.
30. Антитело или фрагмент по любому из предыдущих пунктов, причем антитело или фрагмент содержат константную область человека, например константную область lgG4 или константную область lgG1.
Например, константная область включает описанную в данном документе константную область тяжелой цепи.
В одном примере (необязательно в дополнение к области тяжелой цепи, как указано в абзаце непосредственно выше), константная область включает константную область легкой цепи, константная область легкой цепи содержит аминокислотную последовательность константной области легкой цепи, описанную в данном документе.
31. Антитело или фрагмент по п. 30, в которых константная область представляет собой константную область lgG4-PE.
Антитело или фрагмент к PCSK9 по изобретению могут содержать константную область, такую как константная область человека, например константная область человека без эффекторной функции, например константная область lgG4 или константная область lgG1, при этом необязательно константная область представляет собой lgG4-PE или отключенный lgG1, как определено в таблице последовательностей в данном документе.
В других вариантах осуществления изобретения антитело или фрагмент представляет собой любой из изотипов или константных областей, как определено в данном документе. В одном варианте осуществления изобретения константная область представляет собой lgG1 человека дикого типа. Например, константная область представляет собой активируемую эффектором константную область lgG1, необязательно имеющую активность ADCC и/или CDC В одном варианте осуществления изобретения константная область сконструирована для усиления ADCC, и/или CDC, и/или ADCP. В другом варианте осуществления изобретения константная область сконструирована для усиления эффекторной функции.
Константная область lgG4 может представлять собой любую из аминокислотных последовательностей константной области lgG4 или кодироваться любой из последовательностей нуклеиновых кислот из приведенной в данном документе таблицы последовательностей. Константная область тяжелой цепи может представлять собой lgG4, содержащий как мутацию Leu235Glu, так и мутацию Ser228Pro. Эта константная область тяжелой цепи «lgG4-PE» (см. пример в таблице последовательностей) не имеет эффекторной функции.
Альтернативной константной областью человека без эффекторной функции является отключенный lgG1, представляющий собой аллель lgG1*01, содержащий мутации L235A и/или G237A (например, LAGA, см. таблицу последовательностей). В одном варианте осуществления изобретения антитела или фрагменты антител, раскрытые в данном документе, содержат константную область тяжелой цепи lgG1, причем последовательность содержит аланин в положении 235 и/или 237 (индексная нумерация в соответствии с EU).
Эффективность Fc-опосредованных эффектов может быть увеличена путем конструирования Fc-домена любым из способов, которые будут очевидны специалисту в данной области техники. В другом варианте осуществления изобретения антитела и фрагменты, раскрытые в данном документе, могут содержать тройную мутацию (M252Y/S254T/T256E), которая усиливает связывание с FcRn.
32. Антитело или фрагмент по любому предыдущему пункту (например, биспецифическое антитело), дополнительно содержащие антигенсвязывающий сайт, который специфически связывает другой антиген-мишень (например, ANGPTL3, например ANGPTL3 человека).
В одном примере дополнительный сайт связывания представляет собой сайт связывания агониста для указанного другого антигена. В одном примере дополнительный сайт связывания представляет собой сайт связывания антагониста для указанного другого антигена.
В одном примере дополнительный сайт связывания представляет собой сайт связывания антитела, содержащий VH и VL; сайт связывания, содержащий константный домен антитела (например, сайт связывания Fcab) или сайт связывания неиммуноглобулина (например, домен фибронектина). Необязательно, антигенсвязывающий сайт представляет собой любой антигенсвязывающий сайт, раскрытый в данном документе.
Например, антитело или фрагмент представляют собой биспецифическое антитело или фрагмент.Например, антитело или фрагмент представляют собой антитело или фрагмент с двойным связыванием, или слитый белок, содержащий антитело или его фрагмент, как определено в любом предыдущем пункте. Антитело с двойным связыванием имеет значение, представленное выше.
В одном примере антитело или фрагмент имеют биспецифический формат, выбранный из DVD-lg, mAb2, FIT-lg, mAb-dAb, «dock and lock», SEED-тела, sc-диатело-Fc, диатело-Fc, тандемного scFv-Fc, Fab-scFv-Fc, Fab-scFv, интратела, BiTE, диатела, DART, TandAb, sc-диатела, sc-диатело-СН3, диатело-СН3, минитела, выступов-во-впадины, выступов-во-впадины с общей легкой цепью, выступов-во-впадины с общей легкой цепью и заряженными парами, заряженных пар, заряженных пар с общей легкой цепью, в частности mAb2, выступов-во-впадины, выступов-во-впадины с общей легкой цепью, выступов-во-впадины с общей легкой цепью и заряженными парами и FIT-lg, например mAb2 и FIT-lg.
В одном варианте осуществления изобретения биспецифический формат выбран из DVD-lg, mAb2, FIT-lg, mAb-dAb, «dock and lock», обмена Fab-фрагментами, SEED-тела, трифункциональных антител Triomab, LUZ-Y, Fcab, кλ-тел, ортогонального Fab, sc-диатело-Fc, диатело-Fc, тандемного scFv-Fc, Fab-scFv-Fc, Fab-scFv, интратела, BiTE, диатела, DART, тандемных диател, sc-диатела, sc-диатело-СН3, диатело-СН3, триатела, миниантитела, минитела, минитела TriBi, scFv-СН3 KIH, scFv-CH-CL-scFv, F(ab')2-scFv, scFv-KIH, Fab-scFv-Fc, четырехвалентного HCab, ImmTAC, выступов-во-впадины, выступов-во-впадины с общей легкой цепью, выступов-во-впадины с общей легкой цепью и заряженными парами, заряженных пар, заряженных пар с общей легкой цепью, DT-lgG, DutaMab, lgG(H)-scFv, scFv-(H)lgG, lgG(L)-scFv, scFv-(L)lgG, lgG(L,H)-Fv, lgG(H)-V, V(H)-lgG, lgG(L)-V, V (L)-lgG, KIH lgG-scFab, 2scFv-lgG, lgG-2scFv, scFv4-lg и Zybody.
В одном варианте осуществления изобретения биспецифический формат выбран из DVD-lg, FIT-lg, mAb-dAb, «dock and lock», обмена Fab-фрагментами, SEED-тела, трифункциональных антител Triomab, LUZ-Y, Fcab, кλ-тел, ортогонального Fab, sc-диатело-Fc, диатело-Fc, тандемного scFv-Fc, Fab-scFv-Fc, Fab-scFv, интратела, BiTE, диатела, DART, тандемных диател, sc-диатела, sc-диатело-СН3, диатело-СН3, триатела, миниантитела, минитела, минитела TriBi, scFv-CH3 KIH, scFv-CH-CL-scFv, F(ab')2-scFv, scFv-KIH, Fab-scFv-Fc, четырехвалентного HCab, ImmTAC, выступов-во-впадины, выступов-во-впадины с общей легкой цепью, выступов-во-впадины с общей легкой цепью и заряженными парами, заряженных пар, заряженных пар с общей легкой цепью, DT-lgG, DutaMab, lgG(H)-scFv, scFv-(H)lgG, lgG(L)-scFv, scFv-(L)lgG, lgG(L,H)-Fv, lgG(H)-V, V(H)-lgG, lgG(L)-V, V (L)-lgG, KIH lgG-scFab, 2scFv-lgG, lgG-2scFv, scFv4-lg и Zybody, например DVD-lg, FIT-lg, mAb-dAb, «dock and lock», SEED-тела, sc-диатело-Fc, диатело-Fc, тандемного scFv-Fc, Fab-scFv-Fc, Fab-scFv, интратела, BiTE, диатела, DART, тандемного диатела, sc-диатела, sc-диатело-СН3, диатело-СН3, минитела, выступов-во-впадины, выступов-во-впадины с общей легкой цепью, выступов-во-впадины с общей легкой цепью и заряженными парами, заряженных пар, заряженных пар с общей легкой цепью, в частности выступов-во-впадины, выступов-во-впадины с общей легкой цепью, выступов-во-впадины с общей легкой цепью и заряженными парами зарядов и FIT-lg, например FIT-lg.
В одном варианте осуществления изобретения биспецифический формат выбран из DVD-lg, mAb2, mAb-dAb, «dock and lock», обмена Fab-фрагментами, SEED тела, трифункциональных антител Triomab, LUZ-Y, Fcab, кλ-тел, ортогонального Fab, sc-диатело-Fc, диатело-Fc, тандемного scFv-Fc, Fab-scFv-Fc, Fab-scFv, интратела, BiTE, диатела, DART, тандемных диател, sc-диатела, sc-диатело-СН3, диатело-СН3, триатела, миниантитела, минитела, минитела TriBi, scFv-CH3 KIH, scFv-CH-CL-scFv, F(ab')2-scFv, scFv-KIH, Fab-scFv-Fc, четырехвалентного HCab, ImmTAC, выступов-во-впадины, выступов-во-впадины с общей легкой цепью, выступов-во-впадины с общей легкой цепью и заряженными парами, заряженных пар, заряженных пар с общей легкой цепью, DT-lgG, DutaMab, lgG(H)-scFv, scFv-(H)lgG, lgG(L)-scFv, scFv-(L)lgG, lgG(L,H)-Fv, lgG(H)-V, V(H)-lgG, lgG(L)-V, V (L)-lgG, KIH lgG-scFab, 2scFv-lgG, lgG-2scFv, scFv4-lg и Zybody, например DVD-lg, mAb2, mAb-dAb, «dock and lock», SEED-тела, sc-диатело-Fc, диатело-Fc, тандемного scFv-Fc, Fab-scFv-Fc, Fab-scFv, интратела, BiTE, диатела, DART, тандемного диатела, sc-диатела, sc-диатело-СН3, диатело-СН3, минитела, выступов-во-впадины, выступов-во-впадины с общей легкой цепью, выступов-во-впадины с общей легкой цепью и заряженными парами, заряженных пар, заряженных пар с общей легкой цепью, в частности mAb2, выступов-во-впадины, выступов-во-впадины с общей легкой цепью и заряженными парами зарядов и выступов-во-впадины с общей легкой цепью, например mAb2.
В одном варианте осуществления изобретения биспецифический формат выбран из DVD-lg, mAb-dAb, «dock and lock», обмена Fab-фрагментами, SEED-тела, трифункциональных антител Triomab, LUZ-Y, Fcab, кλ-тел, ортогонального Fab, sc-диатело-Fc, диатело-Fc, тандемного scFv-Fc, Fab-scFv-Fc, Fab-scFv, интратела, BiTE, диатела, DART, тандемных диател, sc-диатела, sc-диатело-CH3, диатело-CH3, триатела, миниантитела, минитела, минитела TriBi, scFv-CH3 KIH, scFv-CH-CL-scFv, F(ab')2-scFv, scFv-KIH, Fab-scFv-Fc, четырехвалентного HCab, ImmTAC, выступов-во-впадины, выступов-во-впадины с общей легкой цепью, выступов-во-впадины с общей легкой цепью и заряженными парами, заряженных пар, заряженных пар с общей легкой цепью, DT-lgG, DutaMab, lgG(H)-scFv, scFv-(H)lgG, lgG(L)-scFv, scFv-(L)lgG, lgG(L,H)-Fv, lgG(H)-V, V(H)-lgG, lgG(L)-V, V (L)-lgG, KIH lgG-scFab, 2scFv-lgG, lgG-2scFv, scFv4-lg и Zybody, например DVD-lg, mAb-dAb, «dock and lock», SEED-тела, sc-диатело-Fc, диатело-Fc, тандемного scFv-Fc, Fab-scFv-Fc, Fab-scFv, интратела, BiTE, диатела, DART, тандемного диатела, sc-диатела, sc-диатело-CH3, диатело-СН3, минитела, выступов-во-впадины, выступов-во-впадины с общей легкой цепью, выступов-во-впадины с общей легкой цепью и заряженными парами, заряженных пар, заряженных пар с общей легкой цепью, в частности выступов-во-впадины, выступов-во-впадины с общей легкой цепью и заряженными парами зарядов и выступов-во-впадины с общей легкой цепью.
33. Антитело или фрагмент к PCSK9, как определено в любом предыдущем пункте, для лечения или профилактики PCSK9-опосредованного заболевания или патологического состояния (например, гиперлипидемии или гиперхолестеринемии) у субъекта.
Например, субъект представляет собой человек. В альтернативном варианте субъект представляет собой животное, отличное от человека. Например, субъект представляет собой взрослого человека. Например, субъект представляет собой ребенка. Например, субъект представляет собой пациента-человека с ХБП, находящегося на лечение диализом. Например, субъект представляет собой человека с терминальной стадией почечной недостаточности.
Например, антитело или фрагмент в данном документе предназначены для лечения или профилактики заболевания или патологического состояния, выбранного из гиперхолестеринемии, гиперлипидемии, гиперхолестеринемии, дислипидемии, холестатического заболевания печени, нефротического синдрома, гипотиреоза, ожирения, диабета, атеросклероза или сердечнососудистого заболевания. Например, заболевание или патологическое состояние выбрано из расстройства липидного обмена, гиперлипопротеинемии, гиперлипидемии; дислипидемии; гиперхолестеринемии, сердечного приступа, инсульта, ишемической болезни сердца, атеросклероза, заболевания периферических сосудов, хромоты, диабета II типа, высокого кровяного давления и сердечно-сосудистого заболевания или патологического состояния. Например, заболевание или патологическое состояние представляет собой гиперлипидемию. Например, заболевание или патологическое состояние представляет собой гиперхолестеринемию. Например, заболевание или патологическое состояние представляет собой диабет. Например, заболевание или патологическое состояние представляет собой инсульт. Например, заболевание или патологическое состояние представляет собой атеросклероз. Например, заболевание или патологическое состояние представляет собой расстройство ЦНС. Например, заболевание или патологическое состояние представляет собой неврологическое расстройство. Например, заболевание или патологическое состояние представляет собой депрессию.
Например, заболевание или патологическое состояние возникает у человека. Например, заболевание или патологическое состояние возникает у животного.
Например, заболевание или патологическое состояние, опосредованное PCSK9, представляет собой нейродегенеративное заболевание, нарушение или патологическое состояние, например, выбранное из болезни Альцгеймера, бокового амиотрофического склероза, болезни Паркинсона, болезни Хантингтона, первичного прогрессирующего рассеянного склероза, вторичного прогрессирующего рассеянного склероза, кортикобазальной дегенерации, синдрома Ретта, дегенерации сетчатки, выбранной из возрастной дегенерации желтого пятна и пигментного ретинита; передней ишемической оптической нейропатии, глаукомы, увеита, депрессии, стресса, связанного с травмой, или посттравматического стрессового расстройства, лобно-височной деменции, деменции с тельцами Леви, легких когнитивных нарушений, задней корковой атрофии, первичной прогрессирующей афазии и прогрессирующего надъядерного паралича или старческой деменции, в частности нейродегенеративное заболевание, нарушение или патологическое состояние выбрано из болезни Альцгеймера, бокового амиотрофического склероза, болезни Паркинсона и болезни Хантингтона, например болезни Альцгеймера.
Например, антитело, фрагмент, комбинацию по изобретению вводят субъекту внутривенно; или они предназначены для внутривенного введения субъекту. Например, антитело, фрагмент, комбинацию по изобретению вводят субъекту подкожно; или они предназначены для введения субъекту подкожно.
34. Антитело или фрагмент по п. 33, причем антитело или фрагмент вводят субъекту одновременно или последовательно со статином.
35. Комбинация количества антитела или фрагмента к PCSK9 и количества статина (например, включающего несколько доз указанного антитела и/или статина), причем указанное антитело или фрагмент соответствует любому из пп. 1-34.
Также предложены: медицинский набор, содержащий комбинацию, первый стерильный контейнер, содержащий указанное количество антитела или фрагмента, и второй стерильный контейнер, содержащий указанное количество статина, и необязательно инструкции по применению комбинации для лечения гиперлипидемии или гиперхолестеринемии у субъекта.
Также предложены: медицинский набор, содержащий комбинацию, первый стерильный контейнер, содержащий указанное количество антитела или фрагмента, и второй стерильный контейнер, содержащий указанное количество ингибитора ANGPTL3, и необязательно инструкции по применению комбинации для лечения гиперлипидемии или гиперхолестеринемии у субъекта.
Например, комбинация предназначена для лечения или профилактики гиперлипидемии или гиперхолестеринемии у субъекта, причем в течение 4 недель подряд общую дозу антитела и общую дозу статина вводят указанному субъекту в соотношении X:Y, где X составляет от 10 до 2×106 и Y=4, например, X составляет от 10 до 2×106 микрограммов, a Y=4 микрограмма.
36. Антитело, фрагмент или комбинация по изобретению для применения в способе лечения или профилактики гиперхолестеринемии у субъекта, который ранее находился на схеме лечения статинами в первой дозе, причем способ включает снижение дозы статина, вводимой субъекту, или отсутствие введения статина субъекту, при этом способ включает введение субъекту антитела или фрагмента.
37. Комбинация по п. 35 или 36, включающая статин в суточной дозе от 10 до 20 мг (например, 10 мг); или <60 мг (например, 40 мг).
38. Антитело, фрагмент или комбинация по любому из предыдущих пунктов для введения человеку или животному, страдающему повышенным уровнем холестерина, для снижения уровня холестерина липопротеинов низкой плотности (ХС-ЛПНП) в плазме у субъекта после того, как субъект получил антитело или фрагмент к PCSK9.
39. Применение антитела, фрагмента или комбинации, как определено в любом предыдущем пункте, при производстве лекарственного препарата для введения субъекту для лечения или профилактики PCSK9-опосредованного заболевания или патологического состояния, например гиперлипидемии или гиперхолестеринемии.
40. Способ лечения или профилактики PCSK9-опосредованного заболевания или патологического состояния у субъекта (например, гиперлипидемии или гиперхолестеринемии), включающий введение указанному субъекту терапевтически эффективного количества антитела, фрагмента или комбинации, как определено в любом из пп. 1-38, при этом тем самым лечится или предотвращается PCSK9-опосредованное заболевание или патологическое состояние.
Заболевание или патологическое состояние может представлять собой любое, описанное в данном документе.
41. Применение по п. 39 или способ по п. 40, причем заболевание или патологическое состояние, опосредованное PCSK9, представляет собой гиперлипидемию или гиперхолестеринемию.
42. Антитело, фрагмент, комбинация, применение или способ по любому из пунктов 33-41, дополнительно включающие применение к субъекту дополнительной терапии, например дополнительного терапевтического агента, при этом дополнительный терапевтический агент необязательно выбран из группы, состоящей из:
a. Статина;
b. Ингибитора ANGPTL3 (например, антитело к ANGPTL3, например эвинакумаб)
c. Фибрата;
d. Секвестранта желчных кислот;
e. Никотиновой кислоты; и
f. Ниацина.
Раскрытие включает дженереки брендовых лекарственных средств, и описание этих дженериков включено в данный документ посредством ссылки для возможного применения в изобретении, например, как часть комбинации.
43. Фармацевтическая композиция, содержащая антитело, фрагмент или комбинацию, как определено в любом из пп. 1-38 и 42, и фармацевтически приемлемое вспомогательное вещество, разбавитель или носитель и необязательно в комбинации с дополнительным терапевтическим агентом, выбранным из указанных выше (например, в п. 42).
44. Фармацевтическая композиция по п. 43 для лечения и/или профилактики патологического состояния или заболевания, опосредованного PCSK9, например гиперлипидемии или гиперхолестеринемии.
45. Фармацевтическая композиция по п. 43 или 44 в комбинации с этикеткой или инструкциями по применению для лечения и/или профилактики указанного заболевания или патологического состояния у человека; при этом этикетка или инструкции необязательно содержат номер разрешения на продажу (например, номер разрешения FDA или ЕМА); при этом набор необязательно содержит в/в или инъекционное устройство, которое содержит антитело или фрагмент.
46. Нуклеиновая кислота, которая кодирует домен VH и/или домен VL антитела или фрагмента, как определено в любом из пп. 1-32.
47. Нуклеиновая кислота, которая кодирует домен VH, содержащий аминокислотную последовательность домена VH антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или аминокислотную последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%.
Например, идентичность составляет по меньшей мере 85%. Например, идентичность составляет по меньшей мере 90%. Например, идентичность составляет по меньшей мере 95%.
Необязательно, предложена нуклеиновая кислота, которая кодирует домен VH, содержащий аминокислотную последовательность SEQ ID №114, или аминокислотную последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%. Например, идентичность составляет по меньшей мере 85%. Например, идентичность составляет по меньшей мере 90%. Например, идентичность составляет по меньшей мере 95%.
48. Нуклеиновая кислота, которая кодирует домен VL, содержащий аминокислотную последовательность домена VL антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или аминокислотную последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%.
Необязательно, нуклеиновая кислота также кодирует домен VH, содержащий аминокислотную последовательность домена VH выбранного антитела; или аминокислотную последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%. Например, идентичность составляет по меньшей мере 85%. Например, идентичность составляет по меньшей мере 90%. Например, идентичность составляет по меньшей мере 95%.
49. Нуклеиновая кислота (например, в клетке-хозяине, например в клетке СНО, или HEK293, или Cos), содержащая нуклеотидную последовательность, которая по меньшей мере на 70% идентична последовательности SEQ ID №2 или 66.
В данном документе в любом случае, в котором упоминается % идентичности, в примере наблюдается идентичность на 100%.
50. Нуклеиновая кислота, которая кодирует тяжелую цепь и/или легкую цепь антитела или фрагмента, как определено в любом из пп. 1-32.
51. Нуклеиновая кислота, кодирующая тяжелую цепь, содержащую аминокислотную последовательность VH, которая по меньшей мере на 70% идентична SEQ ID №22 или 66; и аминокислотную последовательность С-области, которая по меньшей мере на 70% идентична последовательности IGHG4, необязательно по меньшей мере на 70% идентична SEQ ID №3 или 152.
52. Нуклеиновая кислота, кодирующая легкую цепь, содержащую аминокислотную последовательность VL, которая по меньшей мере на 70% идентична SEQ ID №93 или 95; и аминокислотную последовательность С-области, которая по меньшей мере на 70% идентична последовательности IGKC, необязательно по меньшей мере на 70% идентична SEQ ID №156.
53. Нуклеиновая кислота (например, в клетке-хозяине, например в клетке СНО, или HEK293, или Cos), содержащая
a. нуклеотидную последовательность, которая по меньшей мере на 70% идентична последовательности тяжелой цепи антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); и/или
b. нуклеотидную последовательность, которая по меньшей мере на 70% идентична последовательности легкой цепи антитела, выбранного, соответственно, из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT).
54. Вектор, содержащий нуклеиновую кислоту(-ы) (например, нуклеиновую кислоту(-ы) по любому из пп. 46-53); при этом вектор необязательно представляет собой вектор СНО или HEK293.
Все нуклеиновые кислоты по данному изобретению могут экспрессироваться в клетке-хозяине, например в клетке СНО, или HEK293, или Cos, например, для экспрессии вариабельного домена или цепи антитела или фрагмента по изобретению.
55. Клетка-хозяин, содержащая нуклеиновую кислоту(-ы) (например, нуклеиновую кислоту(-ы) по любому из пп. 46-53) или вектор по п. 54.
Например, антитело или фрагмент содержат HCDR3 длиной 9, 10, 11 или 12 остатков, например 10, например 11. Например, антитело или фрагмент содержит LCDR3 длиной 7, 8 или 9 остатков, например 8, например 9. Например, каждый домен VH антитела или фрагмента содержит от 1 до 11 остатков, не относящихся к зародышевой линии, например 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или 11 остатков, не относящихся к зародышевой линии. Например, каждый домен VL антитела или фрагмента содержит от 3 до 8 остатков, не относящихся к зародышевой линии, например, 3, 4, 5, 6, 7 или 8 остатков, не относящихся к зародышевой линии.
В одном варианте осуществления изобретения последовательность CDR в данном документе определена в соответствии с Кабатом. В качестве альтернативы последовательность CDR определена в соответствии с IMGT.
Например, выбранное антитело представляет собой CL-148219. Например, выбранное антитело представляет собой CL-148489.
Например, выбранное антитело содержит тяжелую цепь CL-148219 или CL-148489.
Например, тяжелая цепь антитела или фрагмента по изобретению представляет собой гамма-1, гамма-2, гамма-3, гамма-4, мю, дельта, эпсилон или альфа-изотип человека, предпочтительно гамма-изотип (например, изотип lgG4). Например, легкая цепь антитела или фрагмента по изобретению содержит константную область каппа-цепи человека. Альтернативно, например, легкая цепь антитела или фрагмента по изобретению содержит константную область лямбда-цепи человека.
Необязательно, антитело представляет собой 4-цепочечное антитело, содержащее димер тяжелой цепи, связанный с димером легкой цепи. Например, тяжелая цепь содержит одну из CDR тяжелой цепи или комбинацию CDR, как раскрыто в данном документе, и/или легкая цепь содержит одну из CDR тяжелой цепи или комбинации CDR, как раскрыто в данном документе, например, из того же выбранного антитела. Например, тяжелая цепь содержит домен VH, как раскрыто в данном документе, и/или легкая цепь содержит VL, как раскрыто в данном документе, например, из того же выбранного антитела. Например, тяжелая цепь и легкая цепь происходят из одного и того же выбранного антитела, например, любого антитела, описанного в таблице последовательностей в данном документе или в таблицах в приведенных в данном документе Примерах.
Например, выбранное антитело содержит легкую (и необязательно тяжелую) цепь(-и) CL-148219 или CL-148489.
Например, выбранное антитело содержит вариабельные домены CL-148219 или CL-148489.
Например, выбранное антитело содержит домены VH CL-148219 или CL-148489.
Например, выбранное антитело содержит домены VH и VL CL-148219 или CL-148489.
Необязательно, VH кодируется нуклеотидной последовательностью, которая получена в результате рекомбинации IGHV4-59 человека (например, IGHV4-59*01), сегмента гена D (например, IGHD3-10, например IGHD3-10*01) и сегмента гена IGHJ6 (например, IGHJ6*02). Необязательно, дополнительно или альтернативно VL кодируется нуклеотидной последовательностью, которая получена в результате рекомбинации IGKV2-28 человека (например, IGKV2-28*01) и IGKJ3 (например, IGKJ3*01).
Необязательно, VH кодируется нуклеотидной последовательностью, которая получена в результате рекомбинации IGHV3-9 человека (например, IGHV3-9*01), сегмента гена D (например, IGHD3-9, например IGHD3-9*01) и сегмента гена IGHJ6 (например, IGHJ6*02). Необязательно, дополнительно или альтернативно VL кодируется нуклеотидной последовательностью, которая получена в результате рекомбинации IGKV2-29 человека (например, IGKV2-29*01 или IGKV2D-29*01) и IGKJ4 (например, IGKJ4*01).
Например, антитело или фрагмент содержат HCDR3 длиной 9-12 остатков и/или антитело или фрагмент содержат LCDR3 длиной 7-9 остатков. Например, антитело или фрагмент содержат HCDR3 длиной 9, 10, 11 или 12 остатков, например 10, например 11. Например, антитело или фрагмент содержит LCDR3 длиной 7, 8 или 9 остатков, например 8, например 9. Например, каждый домен VH антитела или фрагмента содержит от 1 до 11 остатков, не относящихся к зародышевой линии, например 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или 11 остатков, не относящихся к зародышевой линии. Например, каждый домен VL антитела или фрагмента содержит от 3 до 8 остатков, не относящихся к зародышевой линии, например, 3, 4, 5, 6, 7 или 8 остатков, не относящихся к зародышевой линии.
Необязательно, антитело или фрагмент конкурируют с CL-148219 (например, CL-148219 в формате lgG, например lgG4-PE) за связывание с PCSK9 (например, PCSK9 человека), что определено с помощью SPR.
Необязательно, антитело или фрагмент конкурируют с CL-148489 (например, CL-148489 в формате lgG, например lgG4-PE) за связывание с PCSK9 (например, PCSK9 человека), что определено с помощью SPR.
Необязательно, аминокислотные замены представляют собой консервативные аминокислотные замены, при этом каждая консервативная замена необязательно относится к группе (1)-(6):
1) аланин (А), серии (S), треонин (Т);
2) аспарагиновая кислота (D), глутаминовая кислота (Е);
3) аспарагин (N), глутамин (Q);
4) аргинин (R), лизин (K);
5) изолейцин (I), лейцин (L), метионин (М), валин (V); и
6) фенилаланин (F), тирозин (Y), триптофан (W).
Любой SPR в данном документе представляет собой, например, поверхностный плазмонный резонанс (SPR) при 37°С и рН 7,6.
Любой PCSK9 в данном документе необязательно представляет собой (например, при тестировании in vitro) PCSK9 человека.
Например, антитело или фрагмент по изобретению связывается с PCSK9 человека с Ka, составляющей, например, 5×106 М-1 × с-1; или около 5×106 М-1 × с-1. Например, антитело или фрагмент по изобретению связываются с PCSK9 человека с Kd, например, 4 или 5 с-1; или около 4 или 5 с-1. Например, антитело или фрагмент по изобретению связываются с PCSK9 человека с KD, например, 0,07 или 0,14 нМ; или около 0,07 или 0,14 нМ. В одном варианте осуществления изобретения фрагмент представляет собой Fab-фрагмент. В одном варианте осуществления изобретения фрагмент представляет собой scFv.
При использовании в данном документе, термины «ингибирует», «ингибирование», «ингибирующий» и т.п. в контексте данного описания относятся к способности антагониста (например, антитела или его фрагмента) связываться с эпитопом (например, hPCSK9), что либо частично, либо полностью предотвращает связывание другого антигена. Если эпитоп, с которым связывается антагонист, полностью блокирует сайт связывания лиганда, то связывание лиганда полностью предотвращается (что может представлять собой физическое блокирование - в случае перекрывающихся эпитопов - или стерическое блокирование - если антагонист является большим, так что он предотвращает связывание лиганда с его отдельным эпитопом), и лиганд не удаляется из кровотока. Следовательно, может казаться, что концентрация лиганда в кровотоке увеличивается. Если эпитоп, с которым связывается антагонист, частично блокирует сайт связывания лиганда, лиганд может связываться, но только слабо (в случае частичного ингибирования) или в другой ориентации по сравнению с естественным связывающим взаимодействием. В этом случае часть лиганда может быть удалена из кровотока, но не в такой степени, как когда сайт связывания лиганда полностью свободен и доступен для связывания. Таким образом, ингибирование относится к физическому взаимодействию лиганда и рецептора. Ингибирование можно измерить с помощью HTRF, который более подробно описан в другом месте в данном документе и в Mathis (1995) Clinical Chemistry 41(9), 1391-1397. Ингибирование также можно измерить с помощью проточной цитометрии, когда рецептор экспрессируется на клетках, или с помощью ELISA, когда рецептор адсорбируется на планшетах.
Необязательно, антитело по изобретению имеет аффинность (KD) связывания с PCSK9 от 1 пМ до 5 нМ, причем связывание необязательно определяют с помощью SPR с использованием Fab указанного антитела при 37°С и рН 7,6.
Необязательно, антитело имеет скорость диссоциации (Koff) при связывании с PCSK9 от 1×10-5 до 1×10-3 с-1, при этом необязательно связывание определяют с помощью SPR с использованием Fab указанного антитела при 37°С и рН 7,6.
Необязательно, антитело имеет скорость ассоциации (Kon) при связывании с PCSK9 от 1×105 до 1×107 М-1 с-1, при этом связывание необязательно определяют с помощью SPR с использованием Fab указанного антитела при 37°С и рН 7,6.
Например, антитело (например, в виде Fab) или фрагмент имеют аффинность (KD) связывания с PCSK9 (например, PCSK9 человека)
(a) от 2, 3, 4, 5 или 10 пМ до 3, 4 или 5 нМ;
(b) от 1-10 пМ до 5 нМ;
(c) от 10 пМ до 3, 4 или 5 нМ;
(d) от 50 или 80 пМ до 200 нМ;
(e) от 50 или 80 пМ до 150 нМ; или
(f) от 50 или 80 пМ до 100 нМ.
Например, KD составляет (или составляет около) 5-15 пМ (например, 10 пМ). Например, KD составляет (или составляет около) 2-5 нМ (например, 3 нМ). Например, KD составляет (или составляет около) 100-400 пМ (например, 140 или 390 пМ).
Например, антитело (например, в виде Fab) или фрагмент имеет скорость диссоциации (Koff) при связывании с PCSK9 (например, PCSK9 человека)
(a) от 1×10-5 до 5×10-4 с-1;
(b) от 1×10-5 до 6×10-4 с-1;
(c) от 1×10-5 до 7×10-4 с-1;
(d) от 1×10-5 до 8×10-4 с-1;
(e) от 2×10-5 до 1×10-3 с-1;
(f) от 2×10-5 до 5×10-4 с-1;
(д) от 2×10-5 до 6×10-4 с-1;
(h) от 2×10-5 до 7×10-4 с-1; или
(i) от 2×10-5 до 8×10-4 с-1.
Например, Koff составляет (или составляет около) 5×10-4 с-1 (например, когда KD составляет (или составляет около) от 2 нМ до 400 пМ; когда KD составляет (или составляет около) 2-5 нМ (например, 3 нМ), или когда KD составляет (или составляет около) 100-400 пМ (например, 140 или 390 пМ)). Например, Koff составляет (или составляет около) 3×10-5 с-1 (например, когда KD составляет (или составляет около) 5-15 пМ (например, 10 пМ)).
Например, антитело (например, в виде Fab) или фрагмент имеют скорость ассоциации (Kon) при связывании с PCSK9 (например, PCSK9 человека)
(a) от 1×105 до 1×106 М-1 с-1;
(b) от 1×105 до 2×106 М-1 с-1;
(c) от 1×105 до 3×106 М-1 с-1;
(d) от 1×105 до 4×106 М-1 с-1;
(е) от 1×105 до 5×106 М-1 с-1;
(f) от 2×105 до 5×106 М-1 с-1;
(g) от 3×105 до 5×106 М-1 с-1;
(h) от 4×105 до 5×106 М-1 с-1;
(i) от 5×105 до 5×106 М-1 с-1; или
(j) от 6×105 до 5×106 М-1 с-1.
Например, Kon составляет (или составляет около) 1 или 2×10-5 М-1 с-1 (например, когда KD составляет 2-5 нМ (например, 3 нМ)). Например, Kon составляет (или составляет около) 1-4, 1, 2, 3 или 4×10-6 M-1 c-1 (например, когда KD составляет (или составляет около) 5-400 пМ (например, 140 или 390 пМ) или 5-15 пМ (например, 10 пМ)).
Как предусмотрено в пунктах или других аспектах данного документа, антитело или фрагмент к PCSK9 могут связываться с PCSK9, например с PCSK9 человека, с KD менее 50 нМ, менее 40 нМ, менее 30 нМ, что определено с помощью поверхностного плазмонного резонанса. В другом варианте осуществления изобретения антитело или фрагмент к PCSK9 может связываться с PCSK9, например с PCSK9 человека, с KD менее 20 нМ, менее 15 нМ, менее 10 нМ, что определено с помощью поверхностного плазмонного резонанса. Антитело или фрагмент к PCSK9 могут связываться с PCSK9, например PCSK9 человека, с KD менее 8 нМ, менее 5 нМ, менее 4 нМ, менее 3 нМ, менее 2 нМ или менее 1 нМ, что определено с помощью поверхностного плазмонного резонанса. KD может составлять 0,9 нМ или меньше, 0,8 нМ или меньше, 0,7 нМ или меньше, 0,6 нМ или меньше, 0,5 нМ или меньше, 0,4 нМ или меньше, 0,3 нМ или меньше, 0,2 нМ или меньше или 0,1 нМ или меньше.
В другом варианте осуществления изобретения KD находится в диапазоне от 0,01 до 1 нМ, или в диапазоне от 0,05 до 2 нМ, или в диапазоне от 0,05 до 1 нМ. KD может относиться к hPCSK9, PCSK9 яванского макака (т.е. «супо») и/или PCSK9 мыши.
В другом варианте осуществления изобретения описанные в данном документе антитела к PCSK9 имеют скорость Kon (например, при измерении с помощью SPR, например, при 25°С или при 37°С) приблизительно 0,5-10 мкМ, например приблизительно 1-8 мкМ или приблизительно 1-7 мкМ. В другом варианте осуществления изобретения скорость Kon составляет приблизительно 1-5 мкМ, например приблизительно 1 мкМ, приблизительно 1,5 мкМ, приблизительно 2 мкМ, приблизительно 2,5 мкМ или приблизительно 3 мкМ. В другом варианте осуществления изобретения скорость Kon составляет приблизительно 3,5 мкМ, приблизительно 4 мкМ, приблизительно 4,5 мкМ, приблизительно 5 мкМ или приблизительно 5,5 мкМ.
В другом варианте осуществления изобретения описанные в данном документе антитела к PCSK9 имеют скорость Koff (например, измеренную с помощью SPR, например, при 25°С или при 37°С) приблизительно 0,01-100 мМ, например приблизительно 0,1-50 мМ или приблизительно 0,5-50 мМ. В другом варианте осуществления изобретения скорость Koff составляет приблизительно 0,5-10 мМ или приблизительно 0,5-10 мМ, например приблизительно 1 мМ, приблизительно 2 мМ, приблизительно 3 мМ, приблизительно 4 мМ или приблизительно 5 мМ. В другом варианте осуществления изобретения скорость Koff составляет приблизительно 0,6 мМ, приблизительно 0,7 мМ, приблизительно 0,8 мМ или приблизительно 0,9 мМ.
Необязательно, антитело по изобретению содержит константную область lgG4 человека.
Предпочтительно, антитело или его фрагмент, которые специфически связываются с hPCSK9, не реагируют перекрестно с другими антигенами (но могут необязательно перекрестно реагировать с PCSK9 различных видов, например макака-резуса, яванского макака или мыши). Антитело или его фрагмент, которые специфически связываются с антигеном PCSK9, можно идентифицировать, например, с помощью иммуноанализов, BIAcore™ или других методов, известных специалистам в данной области техники. Антитело или его фрагмент специфически связывается с антигеном hPCSK9, когда оно связывается с антигеном hPCSK9 с более высокой аффинностью, чем с любым перекрестно-реагирующим антигеном, как определено с помощью экспериментальных методов, таких как радиоиммуноанализы (RIA) и иммуноферментные анализы (ELISA). Как правило, специфическая или селективная реакция будет давать сигнал по меньшей мере вдвое больший, чем фоновый сигнал или шум и, как правило, более чем в 10 раз больший, чем фон. Обсуждение специфичности антител см., например, в Paul, ed., 1989, Fundamental Immunology Second Edition, Raven Press, New York, на страницах 332-336.
Контактные аминокислотные остатки, участвующие во взаимодействии антитела и антигена, такого как PCSK9, могут быть определены различными методами, известными специалистам в данной области техники.
В одном варианте осуществления изобретения, если антитело распознает линейный эпитоп, могут быть получены короткие пептиды на основе последовательности антигена, и связывание антитела с этими пептидами может быть оценено с использованием стандартных методов.
В одном варианте осуществления изобретения для идентификации связывающих эпитопов можно использовать ограниченное протеолитическое расщепление и масс-спектрометрию.
В одном варианте осуществления изобретения контактные остатки эпитопа идентифицируют с помощью рентгеновской кристаллографии. В одном варианте осуществления контактные остатки эпитопа идентифицируют с помощью криоэлектронной микроскопии. В одном варианте осуществления изобретения контактные остатки эпитопа идентифицируют с помощью комбинации ограниченного протеолитического расщепления и масс-спектрометрии.
В другом варианте осуществления изобретения антитела к PCSK9 (и фрагменты), описанные в данном документе, обеспечивают улучшение уровней временной экспрессии по сравнению с другими антителами и фрагментами к PCSK9. Таким образом, в одном варианте осуществления изобретения антитело (или фрагмент) к PCSK9 экспрессируется в клетке HEK293, например в клетке HEK293T, на уровне экспрессии приблизительно 100 мкг/мл или в диапазоне приблизительно 100-350 мкг/мл. В другом варианте осуществления изобретения уровень экспрессии превышает приблизительно 350 мкг/мл.
В другом варианте осуществления изобретения антитело (или фрагмент) к PCSK9 экспрессируется в клетке СНО, например в клетке Expi-CHO, на уровне экспрессии приблизительно 100 мкг/мл или в диапазоне приблизительно 100-350 мкг/мл. В другом варианте осуществления изобретения уровень экспрессии превышает приблизительно 350 мкг/мл.
В другом варианте осуществления изобретения антитело (или фрагмент) к PCSK9 экспрессируется в клетке СНО, например в клетке Expi-CHO или клетке СНО-Е7 EBNA, на уровне экспрессии приблизительно 100 мкг/мл или в диапазоне приблизительно 100-350 мкг/мл. В другом варианте осуществления изобретения уровень экспрессии превышает приблизительно 350 мкг/мл. Например, антитело содержит домены VH и VL любого из CL-58838 в формате lgG1 человека или lgG4 человека (например, lgG4-PE).
В любой из этих систем экспрессии экспрессия осуществляется в масштабе от приблизительно 0,5 мл до 3 мл, например от приблизительно 0,5 мл до 2 мл. В любой из этих систем экспрессии антитело (или фрагмент) к PCSK9 может быть экспрессировано из вектора рТТ5. В любой из этих систем экспрессии антитело (или фрагмент) к PCSK9 может экспрессироваться в сочетании с реагентом для липидной трансфекции и может необязательно экспрессироваться в клетке СНО, например в клетке Expi-CHO. В любой из этих систем экспрессии антитело (или фрагмент) к PCSK9 может экспрессироваться в сочетании с реагентом для трансфекции с помощью PEI и может необязательно экспрессироваться в клетке СНО, например в клетке СНО-Е7 EBNA. В любой из этих систем экспрессии антитело (или фрагмент) к PCSK9 может экспрессироваться в сочетании с плазмидой-помощником (например, плазмида-помощник АКТ) и может необязательно экспрессироваться в клетке СНО, например в клетке СНО-Е7 EBNA.
В любой из этих систем экспрессии уровень экспрессии составляет от приблизительно 100 мкг/мл до приблизительно 1500 мкг/мл, например от приблизительно 100 мкг/мл до приблизительно 1000 мкг/мл, или от приблизительно 200 мкг/мл до приблизительно 1000 мкг/ мл, или от приблизительно 350 мкг/мл до приблизительно 1000 мкг/мл. В любой из этих систем экспрессии нижний предел экспрессии может составлять приблизительно 100 мкг/мл, приблизительно 200 мкг/мл, приблизительно 300 мкг/мл или приблизительно 400 мкг/мл. В другом варианте осуществления изобретения нижний предел экспрессии может составлять приблизительно 500 мкг/мл, приблизительно 600 мкг/мл, приблизительно 700 мкг/мл или приблизительно 800 мкг/мл. В любой из этих систем экспрессии верхний предел экспрессии может составлять приблизительно 2000 мкг/мл, приблизительно 1800 мкг/мл, приблизительно 1600 мкг/мл или приблизительно 1500 мкг/мл. В другом варианте осуществления изобретения верхний предел экспрессии может составлять приблизительно 1250 мкг/мл, приблизительно 1000 мкг/мл, приблизительно 900 мкг/мл или приблизительно 800 мкг/мл.
В другом варианте осуществления изобретения система экспрессии представляет собой систему экспрессии Lonza, например систему Lonza X-Ceed®.
В системе экспрессии Lonza экспрессия может осуществляться в масштабе приблизительно от 30 мл до 2 л, например от 50 мл до 1 л или от 1 л до 2 л. В системе экспрессии Lonza антитело к PCSK9 (или фрагмент) можно экспрессировать в сочетании с электропорацией и, необязательно, без каких-либо плазмид-помощников. В системе экспрессии Lonza антитело к PCSK9 (или его фрагмент) может экспрессироваться на уровне приблизительно 1 г/л, или приблизительно 900 мг/л, или приблизительно 800 мг/л, или приблизительно 700 мг/л. В другом варианте осуществления изобретения в системе экспрессии Lonza антитело (или фрагмент) к PCSK9 может экспрессироваться на уровне приблизительно 600 мг/л, или приблизительно 500 мг/л, или приблизительно 400 мг/л. В системе экспрессии Lonza антитело (или фрагмент) к PCSK9 может экспрессироваться на уровне от приблизительно 400 мг/л до приблизительно 2 г/л, например от приблизительно 500 мг/л до приблизительно 1,5 г/л или от приблизительно 500 мг/л до приблизительно 1 г/л. В другом варианте осуществления изобретения уровень экспрессии выше 1 г/л. В другом варианте осуществления изобретения антитела к PCSK9 обеспечивают удлинение периода полужизни по сравнению с другими антителами к PCSK9.
В одном варианте осуществления изобретения антитело или фрагмент представляют собой антитело или фрагмент человека. В одном варианте осуществления изобретения антитело или фрагмент представляют собой полностью человеческое антитело или фрагмент. В одном варианте осуществления изобретения антитело или фрагмент представляет собой полностью человеческое моноклональное антитело или фрагмент.
В одном варианте осуществления изобретения антитело или фрагмент представляет собой гуманизированное антитело или фрагмент. В одном варианте осуществления изобретения антитело или фрагмент представляет собой гуманизированное моноклональное антитело или фрагмент.
Контактные аминокислотные остатки, участвующие во взаимодействии антитела и антигена, могут быть определены различными методами, известными специалистам в данной области техники, такими как аланиновое сканирование, кристаллография белков, масс-спектрометрия или любой другой метод, который будет очевиден специалисту в данной области.
В одном варианте осуществления изобретения указанный CDR содержит одну аминокислотную замену, которая может быть консервативной аминокислотной заменой. В одном варианте осуществления изобретения указанный CDR содержит две аминокислотные замены, которые могут быть консервативными аминокислотными заменами. В одном варианте осуществления изобретения указанный CDR содержит три аминокислотные замены, которые могут быть консервативными аминокислотными заменами. В одном варианте осуществления изобретения указанный CDR содержит четыре аминокислотные замены, которые могут быть консервативными аминокислотными заменами. В одном варианте осуществления изобретения указанный CDR содержит пять аминокислотных замен, которые могут быть консервативными аминокислотными заменами. В одном варианте осуществления изобретения указанный CDR содержит шесть аминокислотных замен, которые могут быть консервативными аминокислотными заменами.
Аминокислотные замены включают изменения, при которых аминокислота заменяется другим встречающимся в природе аминокислотным остатком. Такие замены можно классифицировать как «консервативные», и в этом случае аминокислотный остаток, содержащийся в полипептиде, заменяется другой встречающейся в природе аминокислотой с аналогичными свойствами в отношении полярности, функциональности боковой цепи или размера. Такие консервативные замены хорошо известны в данной области техники. Замены, охватываемые данным изобретением, также могут быть «неконсервативными», при которых аминокислотный остаток, содержащийся в пептиде, заменен аминокислотой, имеющей другие свойства, такой как встречающаяся в природе аминокислота из другой группы (например, замена заряженной или гидрофобной аминокислоты на аланин), или альтернативно, при которых встречающаяся в природе аминокислота заменена нетрадиционной аминокислотой.
В одном варианте осуществления изобретения консервативные аминокислотные замены являются такими, как описано в данном документе. Например, замена может представлять собой Y на F, Т на S или K, Р на А, Е на D или Q, N на D или G, R на K, G на N или А, Т на S или K, D на N или Е, I на L или V, F на Y, S на Т или A, R на K, G с N или А, K на R, А на S, K или Р. В другом варианте осуществления изобретения консервативные аминокислотные замены могут быть такими, при которых Y замещен на F, Т на А или S, I на L или V, W на Y, М на L, N на D, G на A, T на А или S, D на N, I на L или V, F на Y или L, S на А или Т и А на S, G, Т или V.
В одном варианте осуществления в данном изобретении предложена фармацевтическая композиция, содержащая антагонист к PCSK9 (например, антитело или его фрагмент, связывающий PCSK9) по данному изобретению и приемлемый носитель, разбавитель или вспомогательное вещество. Более конкретно, композиции по данному изобретению дополнительно содержат один или несколько дополнительных терапевтических агентов, например статин. Как упоминается в данном документе, «статины» (также известные как ингибиторы HMG-CoA-редуктазы) являются ингибиторами фермента HMG-coA-редуктазы, который опосредует выработку холестерина в печени. Статины, конкурентно связывая HMG-CoA-редуктазу, предотвращают связывание HMG-CoA с ферментом и тем самым ингибируют активность редуктазы (например, продукцию мевалоната). Неограничивающие примеры статинов могут включать аторвастатин (LIPITOR™), флувастатин (LESCOL™), ловастатин (MEVACOR™, ALTOCOR™), питавастатин (LIVALO™), правастатин (PRAVACHOL™), розувастатин (CRESTOR™) и симвастатин (ZOCOR™). Статины можно вводить в сочетании с другими агентами, например с комбинацией эзетимиба и симвастатина.
Например, антагонист, антитело или фрагмент к PCSK9 связывается с PCSK9 с KD менее около 1×10-8 М, предпочтительно менее около 1×10-9 М, что определено обычными методами, известными в данной области техники, например, с помощью биосенсора поверхностного плазмонного резонанса (SPR) при 37°С.
«Эффективное количество» означает количество антагониста (например, антитела) по данному изобретению или фармацевтической композиции по данному изобретению, которое вызовет биологический или медицинский ответ или желаемый терапевтический эффект у субъекта, млекопитающего или человека, которого добиваются исследователь, врач или другой клиницист. Эффективное количество может варьироваться в зависимости от таких факторов, как болезненное состояние, возраст, пол и масса индивида, а также способность антитела и/или статина вызывать желаемый ответ у индивида. Эффективным количеством также является такое количество, при котором любой токсический или вредный эффект перевешивается терапевтически полезными эффектами.
Антитело к антагонисту PCSK9 или его антигенсвязывающий фрагмент по данному изобретению, комбинацию или фармацевтическую композицию, содержащую их, можно вводить парентеральными путями (например, подкожным, внутривенным, внутрибрюшинным, внутримышечным или трансдермальным). Введение может осуществляться субъекту отдельно или в комбинации с фармацевтически приемлемым носителем и/или разбавителем в одной или нескольких дозах. Фармацевтические композиции, комбинации или антагонисты по данному изобретению могут быть получены способами, хорошо известными в данной области техники (например, Remington: The Science and Practice of Pharmacy, 19th ed. (1995), A. Gennaro et al., Mack Publishing Co.) и могут содержать или быть объединены с одним или более фармацевтически приемлемыми носителями, разбавителями или вспомогательными веществами.
В одном варианте осуществления изобретения субъектом является человек мужского пола, например взрослый или младенец. В одном варианте осуществления изобретения субъектом является человек женского пола, например взрослый или младенец, например небеременная женщина или беременная женщина. Например, человек является пациентом на диализе. Младенец может представлять собой человека возрастом >1 месяца. Например, субъект представляет собой взрослого человека с установленным сердечнососудистым заболеванием или с первичной гиперлипидемией (например, гетерозиготной семейной гиперхолестеринемией [HeFH]). Например, субъект представляет собой человека с HoFH, например взрослого человека.
Субъектом может быть тот, кому ранее был поставлен диагноз или кто был идентифицирован как страдающий от или имеющий состояние, требующее лечения, или одно или более осложнений, связанных с таким состоянием, и, необязательно, кто уже проходил лечение этого состояния или одного или более осложнений, связанных с указанным состоянием. Альтернативно, субъект также может быть тем, у кого ранее не было диагностировано состояние или одно или более осложнений, связанных с этим состоянием. Например, субъектом может быть тот, кто демонстрирует один или более факторов риска для патологического состояния или одно или несколько осложнений, связанных с патологическим состоянием, или субъект, который не демонстрирует факторов риска.
Изобретение может включать одновременное или последовательное введение антагониста к PCSK9 и статина. Например, антагонист и статин вводят с интервалом не более 1 месяца, 4 недель, 3 недель, 2 недель, 1 недели, 10 дней, 9 дней, 8 дней, 7 дней, 6 дней, 5 дней, 4 дней, 3 дней, 2 дней или 1 дня. Как проиллюстрировано в данном документе, введение антагониста и статина может быть эффективным, если интервал составляет не более 7 дней (например, не более одного дня). Например, антагонист к PCSK9 и статин вводят субъекту с интервалом не более 10, 14, 21 или 28 дней.
Например, статин вводят 2, 3 или 4 раза в неделю. В другом примере статин вводят 1, 2, 3 или 4 раза в месяц или в течение 8 недель.
Например, статин и/или антитело или фрагмент вводят субъекту внутривенно или подкожно.
Например, гиперлипидемия или гиперхолестеринемия наблюдается у субъекта, получающего или получавшего лечение статинами, например, у пациента, который плохо отвечает или не отвечает на лечение статинами.
В варианте осуществления в данном изобретении предложено применение антагониста к PCSK9 и статина для производства лекарственного средства. В дополнительном варианте осуществления в данном изобретении предложено применение антагониста к PCSK9 и статина для производства лекарственного средства для лечения или профилактики гиперлипидемии или гиперхолестеринемии, например гиперлипидемии или гиперхолестеринемии от умеренной до тяжелой степени, например, у субъекта, который плохо отвечает или не отвечает на лечение статинами.
Например, антитело к PCSK9 по изобретению представляет собой антитело, которое конкурирует с контрольным антителом в анализе HTRF. Например, в анализе HTRF антитело по изобретению представляет собой меченое антитело, которое предварительно инкубируют с PCSK9 человека и затем объединяют с немеченым контрольным антителом (в соответствии с частью I или II), при этом в ходе анализа устанавливают конкуренция между антителами. Например, в анализе используют антитело по изобретению, меченое AlexaFluor™ 647. В качестве альтернативы метят PCSK9 человека (например, с помощью AlexaFluor™ 647, тестируемое антитело метят биотином для связывания с криптат-стрептавидином Eu3+, а контрольное антитело не метят). Примеры контрольных антител предпочтительно представляют собой CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT). Альтернативой является алирокумаб или эволокумаб.
Необязательно, антитело к PCSK9 по изобретению (тестируемое антитело) конкурирует в анализе HTRF с контрольным антителом за связывание с PCSK9 человека (или связывает тот же эпитоп PCSK9 человека, что и контрольное антитело), при этом в анализе используется прямо или косвенно меченое тестируемое антитело, прямо или косвенно меченное донорным (например, криптатом Eu3+) или акцепторным флуорофором (например, AlexaFluor™ 647), и мишень PCSK9, меченая либо донорным, либо акцепторным флуорофором, чтобы обеспечить передачу энергии между донором и акцептором, посредством чего вырабатывается и детектируется сигнал флуоресценции. Например, если используется мечение с помощью AlexaFluor™ 647, конкуренция обнаруживается по снижению сигнала флуоресценции при 665 нМ по крайней мере на 20%, когда тестируемое антитело находится в присутствии контрольного антитела по сравнению с сигналом без контрольного антитела. Необязательно, уменьшение сигнала при 665 нм составляет по меньшей мере 20, 30, 40, 50, 60, 70, 80 или 90%.
Например, антитело или фрагмент предназначены для снижения общей дозы, вводимой в течение 4-недельного периода человеку или животному для лечения или профилактики гиперлипидемии или гиперхолестеринемии или любого другого заболевания или патологического состояния, описанного в данном документе.
Например, антитело или фрагмент предназначены для снижения до от  до 1/3 общей дозы, необходимой для контрольного субъекта, получающего идентичное лечение в течение 4-недельного периода, за исключением введения статина без введения антагониста к PCSK9 (например, антитела или фрагмента) человеку или животному для лечения или профилактики гиперлипидемии или гиперхолестеринемии или любого другого заболевания или патологического состояния, описанного в данном документе.
до 1/3 общей дозы, необходимой для контрольного субъекта, получающего идентичное лечение в течение 4-недельного периода, за исключением введения статина без введения антагониста к PCSK9 (например, антитела или фрагмента) человеку или животному для лечения или профилактики гиперлипидемии или гиперхолестеринемии или любого другого заболевания или патологического состояния, описанного в данном документе.
Например, антитело или фрагмент предназначены для уменьшения дозы статина на от  до 1/3, вводимой человеку или животному в течение периода лечения, например 4-недельного периода, для лечения или профилактики гиперлипидемии или гиперхолестеринемии, остеопороза или любого другого заболевания или патологического состояния, описанного в данном документе.
до 1/3, вводимой человеку или животному в течение периода лечения, например 4-недельного периода, для лечения или профилактики гиперлипидемии или гиперхолестеринемии, остеопороза или любого другого заболевания или патологического состояния, описанного в данном документе.
Необязательно, антитело представляет собой антитело IgG4.
Необязательно, доза статина, вводимая субъекту, не эффективна при введении в отсутствие антагониста к PCSK9 (например, антитела или фрагмента по изобретению).
Например, субъект, описанный в данном документе, невосприимчив к дозе статина, но отвечает на лечение гиперлипидемии или гиперхолестеринемии или другого заболевания или патологического состояния при введении антитела или фрагмента по изобретению и дозы статина.
Таким образом, например, антитело или фрагмент по изобретению предназначены для введения в комбинации с дозой статина человеку или животному для лечения связанного с PCSK9 заболевания или патологического состояния у субъекта, при этом субъекта лечат комбинацией, но заболевание или патологическое состояние не поддается лечению путем введения дозы статина в отсутствие введения указанного антитела или фрагмента.
Заболевание или патологическое состояние может представлять собой гиперлипидемию или гиперхолестеринемию или любое другое заболевание или патологическое состояние, раскрытое в данном документе, например выбранное из расстройства липидного обмена, гиперлипопротеинемии, гиперлипидемии; дислипидемии; гиперхолестеринемии, сердечного приступа, инсульта, ишемической болезни сердца, атеросклероза, заболевания периферических сосудов, хромоты, диабета II типа, высокого кровяного давления и сердечнососудистого заболевания или патологического состояния.
В изобретении предложено антитело или фрагмент, которые специфически связываются с PCSK9. Необязательно, антитело или фрагмент содержат последовательность CDRH1, как описано в данном документе, или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%. Необязательно, антитело или фрагмент содержат последовательность CDRH2, как описано в данном документе, или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%. Необязательно, антитело или фрагмент содержат последовательность CDRH3, как описано в данном документе, или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%. Необязательно, антитело или фрагмент содержат последовательность CDRL1, как описано в данном документе, или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%. Необязательно, антитело или фрагмент содержат последовательность CDRL2, как описано в данном документе, или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%. Необязательно, антитело или фрагмент содержат последовательность CDRL3, как описано в данном документе, или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%.
Необязательно, антитело или фрагмент содержат последовательность CDRH1 CL-148219 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%; последовательность CDRH2 CL-148219 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%; и последовательность CDRH3 CL-148219 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%. Необязательно, антитело или фрагмент содержат последовательность CDRL1 CL-148219 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%; последовательность CDRL2 CL-148219 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%; и последовательность CDRL3 CL-148219 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%.
Необязательно, антитело или фрагмент содержат последовательность CDRH1 CL-148489 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%; последовательность CDRH2 CL-148489 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%; и последовательность CDRH3 CL-148489 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%. Необязательно, антитело или фрагмент содержат последовательность CDRL1 CL-148489 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%; последовательность CDRL2 CL-148489 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%; и последовательность CDRL3 CL-148489 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%.
Необязательно, антитело или фрагмент содержат последовательность FR1 VH CL-148219 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%; последовательность FR2 VH CL-148219 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%; последовательность FR3 VH CL-148219 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%; и последовательность FR4 VH CL-148219 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%. Дополнительно или альтернативно, антитело или фрагмент необязательно содержат последовательность FR1 VL CL-148219 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%; последовательность FR2 VL CL-148219 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%; последовательность FR3 VL CL-148219 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%; и последовательность FR4 VL CL-148219 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%.
Необязательно, антитело или фрагмент содержат последовательность FR1 VH CL-148489 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%; последовательность FR2 VH CL-148489 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%; последовательность FR3 VH CL-148489 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%; и последовательность FR4 VH CL-148489 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%. Дополнительно или альтернативно, антитело или фрагмент необязательно содержат последовательность FR1 VL CL-148489 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%; последовательность FR2 VL CL-148489 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%; последовательность FR3 VL CL-148489 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%; и последовательность FR4 VL CL-148489 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%.
Например, каждый CDR и FR1-4 в данном документе соответствует номенклатуре IMGT. В качестве альтернативы каждый CDR и FR1-4 в данном документе соответствует номенклатуре Кабата.
Необязательно, антитело или фрагмент содержит константную область тяжелой цепи гамма-1 человека, например, содержащую последовательность константной области тяжелой цепи гамма-1, описанную в данном документе, или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%. Например, указанная область С содержит SEQ ID №126 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%.
Необязательно, антитело или фрагмент содержит константную область тяжелой цепи гамма-2 человека, например, содержащую последовательность константной области тяжелой цепи гамма-2, описанную в данном документе, или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%. Например, указанная область С содержит SEQ ID №136 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%.
Необязательно, антитело или фрагмент содержат константную область тяжелой цепи гамма-3 человека.
Необязательно, антитело или фрагмент содержат константную область тяжелой цепи гамма-4 человека, например, содержащую последовательность константной области тяжелой цепи гамма-4, описанную в данном документе, или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%. Например, указанная область С содержит SEQ ID №3, 144, 152 или 154 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%.
Необязательно, антитело или фрагмент содержат константную область легкой цепи каппа человека, например, содержащую последовательность константной области легкой цепи каппа, описанную в данном документе, или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%. Например, указанная область С содержит SEQ ID №156 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%. В варианте осуществления изобретения антитело или фрагмент содержат константную область тяжелой цепи гамма-4 человека, например константную область IgG4-PE.
Необязательно, антитело или фрагмент содержат константную область легкой цепи лямбда человека, например, содержащую последовательность константной области легкой цепи лямбда, описанную в данном документе, или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%. Например, указанная область С содержит SEQ ID №166 или последовательность, которая идентична ей по меньшей мере на 70, 80, 85, 90, 95, 96, 97, 98 или 99%. В варианте осуществления изобретения антитело или фрагмент содержат константную область тяжелой цепи гамма-4 человека, например константную область IgG4-PE.
Способность связывать мишень, специфичность и аффинность (Kd, Koff и/или Коп) можно определить любым стандартным методом в данной области техники, например, с помощью поверхностного плазмонного резонанса (SPR). Термин «Kd», при использовании в данном документе, предназначен для обозначения константы равновесной диссоциации конкретного взаимодействия антитело-антиген.
В одном варианте осуществления изобретения поверхностный плазмонный резонанс (SPR) проводят при 25°С. В другом варианте осуществления изобретения SPR проводят при 37°С.
В одном варианте осуществления изобретения SPR проводят при физиологическом рН, таком как рН 7 или рН 7,6 (например, с использованием забуференного солевым раствором Hepes при рН 7,6 (также называемого HBS-ЕР)).
В одном варианте осуществления изобретения SPR проводят при физиологическом уровне соли, например 150 мМ NaCI.
В одном варианте осуществления изобретения SPR проводят при уровне детергента не более 0,05% по объему, например, в присутствии Р20 (полисорбат 20; например, Tween-20™) в концентрации 0,05% и ЭДТА в концентрации 3 мМ.
В одном примере SPR проводят при 25°С или 37°С в буфере с рН 7,6, 150 мМ NaCl, 0,05% детергента (например, Р20) и 3 мМ ЭДТА. Буфер может содержать 10 мМ Hepes. В одном примере SPR проводят при 25°С или 37°С в HBS-EP. HBS-ЕР можно приобрести в Teknova Inc (Калифорния; номер в каталоге Н8022).
Например, аффинность лиганда (например, антитела) определяется с использованием SPR путем
1. связывания антител к IgG мыши (или другая подходящая константная область антитела человека, крысы или другого позвоночного животного с совпадением по видам) (например, Biacore™ BR-1008-38) с биосенсорным чипом (например, GLM-чипом), например, с помощью связывания с первичным амином;
2. воздействие на антитела к IgG мыши (или антитела другого подобранного вида) тестируемым антителом IgG для захвата тестируемого антитела на чипе;
3. пропускание тестируемого антигена через поверхность захвата чипа при 1024 нМ, 256 нМ, 64 нМ, 16 нМ, 4 нМ и 0 нМ (т.е. только буфер); и
4. определение аффинности связывания тестируемого антитела с тестируемым антигеном с использованием поверхностного плазмонного резонанса, например, в условиях SPR, описанных выше (например, при 25°С в физиологическом буфере). SPR может быть проведен с использованием любого стандартного устройства SPR, такого как Biacore™ или ProteOn XPR36™ (Bio-Rad®).
Регенерация поверхности захвата может быть проведена с помощью 10 мМ глицина при рН 1,7. Это удаляет захваченное антитело и позволяет использовать поверхность для другого взаимодействия. Данные связывания могут быть аппроксимированы моделью 1:1, присущей стандартным методам, например, с использованием модели, имеющейся в аналитическом программном обеспечении ProteOn XPR36™.
Например, антагонист (например, антитело или фрагмент) по изобретению содержится в медицинском контейнере, например флаконе, шприце, контейнере для внутривенного введения или устройстве для инъекций (например, устройстве для внутриглазной или интравитреальной инъекции). Например, антагонист находится in vitro, например в стерильном контейнере. Например, в изобретении предложен набор, содержащий антагонист по изобретению, упаковку и инструкции по применению для лечения, профилактики или диагностики у человека заболевания или состояния, опосредованного PCSK9. Например, в инструкциях указано, что человек должен быть генотипирован по варианту последовательности PCSK9 по данному изобретению перед введением антагониста человеку. Например, в инструкциях указано, что человек должен быть фенотипирован по варианту PCSK9 по данному изобретению перед введением лиганда человеку. Например, человек имеет китайскую (например, ханьскую) этническую принадлежность, а инструкции составлены на китайском языке (например, мандаринский диалект).
Например, антагонист является (или был определен как) нейтрализатором PCSK9. Например, определение проводят у человека (например, в клиническом испытании). Например, определение проводят не у человека, например у мыши, крысы, кролика, свиньи, собаки, овцы или примата, отличного от человека (например, яванского макака, макака-резуса или бабуина).
Варианты PCSK9 могут включать формы, описанные в WO 2015092393 как a, f, с, r, р, m, е h, aj и q. Последовательности этих вариантов представлены в нем, см., например, SEQ ID №1-27 и в Таблицах 1, 2 или 6. Раскрытие этого источника и этих последовательностей включено в данный документ посредством ссылки для возможного использования в данном изобретении. Например, антагонист специфически связывается с вариантом PCSK9, раскрытым в WO 2015092393. Например, дополнительно или альтернативно, субъект-человек экспрессирует такой вариант PCSK9.
Например, антагонист специфически связывается с вариантами PCSK9, содержащими аминокислоту E670G. Например, дополнительно или альтернативно, субъект-человек экспрессирует такой вариант PCSK9.
Например, антагонист специфически связывается с вариантами PCSK9, содержащими аминокислоту I474V. Например, дополнительно или альтернативно, субъект-человек экспрессирует такой вариант PCSK9.
Антагонисты по изобретению пригодны, например, в анализах специфического связывания, для генотипирования или фенотипирования людей, аффинной очистки PCSK9 и в анализах скрининга для определения активности других антагонистов PCSK9. Некоторые антагонисты по изобретению пригодны для ингибирования связывания PCSK9 с родственным рецептором или белком человека или для ингибирования активности, опосредованной PCSK9.
Изобретение охватывает антагонисты антител к PCSK9 (например, PCSK9), имеющие модифицированные характеристики гликозилирования. В некоторых применениях модификация может быть полезна для удаления нежелательных сайтов гликозилирования или, например, удаления фрагмента фукозы для усиления функции антителозависимой клеточной цитотоксичности (ADCC) (см. Shield et al. (2002) JBC 277:26733). В других применениях модификация галактозилирования может быть осуществлена для модификации комплемент-зависимой цитотоксичности (CDC).
Например, изобретение относится к фармацевтической композиции, содержащей антагонист по изобретению, причем антагонист представляет собой или включает рекомбинантное человеческое антитело или его фрагмент, которые специфически связываются с PCSK9 (например, редкий вариант, описанный в данном документе), и фармацевтически приемлемый носитель. В одном варианте осуществления изобретение относится к композиции, которая представляет собой комбинацию антагониста антитела или антигенсвязывающего фрагмента антитела по изобретению и второго терапевтического агента. Второе терапевтическое средство может представлять собой любое из противовоспалительного средства, средства против ангиогенеза, болеутоляющего, диуретика, химиотерапевтического средства, противоопухолевого средства, сосудорасширяющего средства, сосудосуживающего средства, статина, бета-блокатора, питательного вещества, адъюванта, средства против ожирения и средства против диабета.
Например, в изобретении предложен способ ингибирования активности PCSK9 с использованием антагониста против PCSK9 по изобретению (например, антитела или антигенсвязывающей части антитела по изобретению), при этом терапевтический способ включает введение терапевтически эффективного количества фармацевтической композиции, содержащей антагонист.Расстройство, которое лечат, представляет собой любое заболевание или патологическое состояние, которое улучшается, ослабляется, подавляется или предотвращается путем устранения, ингибирования или снижения активности PCSK9.
ПУНКТЫ:
В изобретении предложены следующие аспекты, изложенные в пунктах 1 и последующих.
1. Антитело или фрагмент, содержащие сайт связывания, который специфически связывается с пропротеиновой конвертазой субтилизин-кексинового типа 9 (PCSK9), причем сайт связывания включает домен VH, который кодируется нуклеотидной последовательностью, полученной в результате рекомбинации сегмента гена VH, сегмента гена DH и сегмента гена JH человека, при этом сегмент гена VH выбран из IGHV4-31, IGHV4-59, IGHV4-4 и IGHV3-9.
2. Антитело или фрагмент по п. 1, в которых (i) сегмент гена VH представляет собой IGHV4-31, а сегмент гена DH представляет собой сегмент гена человека IGHD3-9; или (ii) сегмент гена VH представляет собой IGHV4-59, а сегмент гена DH представляет собой сегмент гена человека IGHD3-10; или (iii) сегмент гена VH представляет собой IGHV4-4, а сегмент гена DH представляет собой сегмент гена человека IGHD2-15; или (iv) сегмент гена VH представляет собой IGHV3-9, а сегмент гена DH представляет собой сегмент гена человека IGHD3-9.
3. Антитело или фрагмент по п. 1 или 2, в которых сегмент гена JH представляет собой сегмент гена человека IGHJ6.
4. Антитело или фрагмент по любому предыдущему пункту, в которых сайт связывания содержит последовательность CDRH3, выбранную из SEQ ID №271, 285, 15, 77, 29, 91, 211 и 225.
5. Антитело или фрагмент по любому предыдущему пункту, в которых сайт связывания содержит домен VH, содержащий SEQ ID №259, 1, 65 или 199.
6. Антитело или фрагмент по любому предыдущему пункту, в которых сайт связывания содержит домен VH, содержащий SEQ ID №259, спаренный с доменом VL, содержащим SEQ ID №289.
7. Антитело или фрагмент по любому из пп. 1-5, в которых сайт связывания включает домен VH, содержащий SEQ ID №319, спаренный с доменом VL, содержащим SEQ ID №349.
8. Антитело или фрагмент, которые специфически связываются с PCSK9 и содержат последовательность CDRH3 антитела к PCSK9 по любому предыдущему пункту или указанную последовательность CDRH3, содержащую 3, 2 или 1 аминокислотную замену(-ы).
9. Антитело или фрагмент (необязательно по любому предыдущему пункту), которые специфически связывается с PCSK9 и содержат домен VH, который содержит последовательность CDRH3 антитела, выбранного из CL-274711, CL-148219QLT, CL- 274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или указанную последовательность, содержащую 3, 2 или 1 аминокислотную замену(-ы).
10. Антитело или фрагмент по п. 9, в которых домен VH содержит (i) последовательность CDRH3 антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или указанную последовательность CDRH3, содержащую 3, 2 или 1 аминокислотную замену(-ы); и (ii) последовательность CDRH1 указанного выбранного антитела; или указанную последовательность CDRH1, содержащую 3, 2 или 1 аминокислотную замену(-ы).
11. Антитело или фрагмент по п. 9 или 10, в которых домен VH содержит (iii) последовательность CDRH3 антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или указанную последовательность CDRH3, содержащую 3, 2 или 1 аминокислотную замену(-ы); и (iv) последовательность CDRH2 указанного выбранного антитела; или указанную последовательность CDRH2, содержащую 3, 2 или 1 аминокислотную замену(-ы).
12. Антитело или фрагмент (необязательно по любому предыдущему пункту), содержащие сайт связывания, который специфически связывается с PCSK9, причем сайт связывания содержит домен VH, который содержит аминокислотную последовательность домена VH антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или аминокислотную последовательность, которая идентична ей по меньшей мере на 70%.
13. Антитело или фрагмент по пп. 9, 10, 11 или 12, причем выбранное антитело представляет собой CL-274711 или CL-148219QLT.
14. Антитело или фрагмент по любому предыдущему пункту, содержащие первую и вторую копии указанного домена VH.
15. Антитело или фрагмент (необязательно по любому предыдущему пункту), содержащие сайт связывания, который специфически связывается с PCSK9, причем сайт связывания содержит домен VL, который кодируется нуклеотидной последовательностью, полученной путем рекомбинации сегмента гена VL и сегмента гена JL человека, причем сегмент гена VL выбран из IGKV3-11, IGKV2-28 и IGKV2-29.
16. Антитело или фрагмент по п. 15, причем сегмент гена JL представляет собой сегмент гена человека, выбранный из IGKJ4, IGJK3 и IGKJ1.
17. Антитело или фрагмент, которые специфически связываются с PCSK9 и содержат последовательность CDRL3 антитела к PCSK9 по любому предыдущему пункту или указанную последовательность CDRL3, содержащую 3, 2 или 1 аминокислотную замену(-ы).
18. Антитело или фрагмент (необязательно по любому предыдущему пункту), которые специфически связываются с PCSK9 и содержат домен VL, который содержит последовательность CDRL3, выбранную из SEQ ID №301, 315, 47, 107, 61, 121, 241 и 255, или указанную выбранную последовательность CDRL3, содержащую 3, 2 или 1 аминокислотную замену(-ы).
19. Антитело или фрагмент (необязательно по любому предыдущему пункту), которые специфически связываются с PCSK9 и содержат домен VL, который содержит последовательность CDRL3 (и необязательно CDRH3) антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или указанную последовательность(-и), каждая из которых содержит 3, 2 или 1 аминокислотную замену(-ы).
20. Антитело или фрагмент по п. 19, в которых домен VL содержит (i) последовательность CDRL3 (и необязательно CDRH3) антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или указанную последовательность(-и) CDR3, каждая из которых содержит 3, 2 или 1 аминокислотную замену(-ы); и (ii) последовательность CDRL1 (и необязательно CDRH1) указанного выбранного антитела; или указанную последовательность(-и) CDR1, каждая из которых содержит 3, 2 или 1 аминокислотную замену(-ы).
21. Антитело или фрагмент по п. 19 или 20, в которых домен VL содержит (iii) последовательность CDRL3 (и необязательно CDRH3) антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или указанную последовательность(-и) CDR3, каждая из которых содержит 3, 2 или 1 аминокислотную замену(-ы); и (iv) последовательность CDRL2 (и необязательно CDRH2) указанного выбранного антитела; или указанную последовательность(-и) CDR2, каждая из которых содержит 3, 2 или 1 аминокислотную замену(-ы).
22. Антитело или фрагмент (необязательно по любому предыдущему пункту), содержащие сайт связывания, который специфически связывается с PCSK9, причем сайт связывания содержит домен VL, который содержит аминокислотную последовательность домена VL антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или аминокислотную последовательность, которая идентична ей по меньшей мере на 70%.
23. Антитело или фрагмент (необязательно по любому предыдущему пункту), которые специфически связываются с PCSK9 и содержат аминокислотную последовательность тяжелой цепи антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или аминокислотную последовательность, которая идентична ей по меньшей мере на 70%.
24. Антитело или фрагмент (необязательно по любому предыдущему пункту), которые специфически связываются с PCSK9 и содержат аминокислотную последовательность легкой цепи антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или аминокислотную последовательность, которая идентична ей по меньшей мере на 70%.
25. Антитело или фрагмент по п. 23, содержащие аминокислотную последовательность легкой цепи указанного выбранного антитела; или аминокислотную последовательность, которая идентична ей по меньшей мере на 70%.
26. Антитело или фрагмент (необязательно по любому предыдущему пункту), которые специфически связываются с эпитопом PCSK9 человека, идентичным эпитопу, с которым связывается антитело по любому предыдущему пункту.
27. Антитело или фрагмент по п. 26, в которых эпитоп идентифицируют сканированием неродственных аминокислот или рентгеновской кристаллографией.
28. Антитело или фрагмент по п. 27, в которых контактные остатки эпитопа определены по снижению аффинности по меньшей мере в 10 раз при сканировании неродственными аминокислотами, например аланиновом сканировании, что определено с помощью SPR.
29. Антитело или фрагмент (необязательно по любому предыдущему пункту), которые конкурируют за связывание с PCSK9 человека с антителом по любому предыдущему пункту.
30. Антитело или фрагмент по любому предыдущему пункту, которые специфически связываются с PCSK9, содержащей аминокислотную последовательность, выбранную из SEQ ID №189-194.
31. Антитело или фрагмент по любому предыдущему пункту, причем антитело или фрагмент содержат константную область человека, необязательно константную область IgG4 или константную область IgG1.
32. Антитело или фрагмент по п. 31, в которых константная область представляет собой константную область IgG4-PE, необязательно константная область содержит аминокислотную последовательность SEQ ID №3 или 152.
33. Антитело или фрагмент по любому предыдущему пункту, дополнительно содержащие антигенсвязывающий сайт, который специфически связывает другой антиген-мишень, необязательно ANGPTL3.
34. Антитело или фрагмент к PCSK9, как определено в любом предыдущем пункте, для лечения или профилактики PCSK9-опосредованного заболевания или патологического состояния (необязательно гиперхолестеринемии) у субъекта.
35. Антитело или фрагмент к PCSK9 по п. 34, причем заболевание или патологическое состояние выбрано из гиперхолестеринемии, гиперлипидемии, гиперхолестеринемии, дислипидемии, холестатического заболевания печени, нефротического синдрома, гипотиреоза, ожирения, диабета, атеросклероза или сердечно-сосудистого заболевания.
36. Антитело или фрагмент по п. 34 или 35, в которых антитело или фрагмент вводят субъекту одновременно или последовательно со статином.
37. Комбинация количества антитела или фрагмента к PCSK9 и количества статина (необязательно включающего несколько доз указанного антитела и/или статина), причем указанное антитело или фрагмент соответствует любому из пп. 1-36.
38. Антитело, фрагмент или комбинация по любому из пп. 1 -37 для применения в способе лечения или профилактики гиперхолестеринемии у субъекта, который ранее находился на схеме лечения статинами в первой дозе, причем способ включает снижение дозы статина, вводимой субъекту, или отсутствие введения статина субъекту, при этом способ включает введение субъекту антитела или фрагмента.
39. Комбинация по п. 37 или 38, включающая статин в суточной дозе от 10 до 20 мг (например, 10 мг); или <60 мг (например, 40 мг).
40. Антитело, фрагмент или комбинация по любому предыдущему пункту для введения человеку или животному, страдающему повышенным уровнем холестерина, для снижения уровня холестерина липопротеинов низкой плотности (ХС-ЛПНП) в плазме у субъекта после того, как субъект получил антитело или фрагмент к PCSK9.
41. Применение антитела, фрагмента или комбинации, как определено в любом предыдущем пункте, при производстве лекарственного препарата для введения субъекту для лечения или профилактики PCSK9-опосредованного заболевания или патологического состояния, необязательно гиперхолестеринемии.
42. Способ лечения или профилактики PCSK9-опосредованного заболевания или патологического состояния у субъекта (необязательно гиперхолестеринемии), включающий введение указанному субъекту терапевтически эффективного количества антитела, фрагмента или комбинации, как определено в любом из пп. 1-40, при этом тем самым лечится или предотвращается PCSK9-опосредованное заболевание или патологическое состояние.
43. Применение по п. 41 или способ по п. 42, причем заболевание или патологическое состояние, опосредованное PCSK9, представляет собой гиперхолестеринемию.
44. Антитело, фрагмент, комбинация, применение или способ по любому из пп. 34-43, дополнительно включающие применение к субъекту дополнительной терапии, например дополнительного терапевтического агента, при этом дополнительный терапевтический агент необязательно выбран из группы, состоящей из:
a. Статина;
b. Ингибитора ANGPTL3 (например, антитело к ANGPTL3, например эвинакумаб)
c. Фибрата;
d. Секвестранта желчных кислот;
e. Никотиновой кислоты; и
f. Ниацина.
45. Фармацевтическая композиция, содержащая антитело, фрагмент или комбинацию, как определено в любом из пп. 1-40 и 44, и фармацевтически приемлемое вспомогательное вещество, разбавитель или носитель и необязательно в комбинации с дополнительным терапевтическим агентом, выбранным из агентов, перечисленных в п. 44.
46. Фармацевтическая композиция по п. 45 для лечения и/или профилактики патологического состояния или заболевания, опосредованного PCSK9, необязательно гиперхолестеринемии.
47. Фармацевтическая композиция по п. 45 или 46 в комбинации с этикеткой или инструкциями по применению для лечения и/или профилактики указанного заболевания или патологического состояния у человека; при этом этикетка или инструкции необязательно содержат номер разрешения на продажу (необязательно номер разрешения FDA или ЕМА); при этом набор необязательно содержит в/в или инъекционное устройство, которое содержит антитело или фрагмент.
48. Нуклеиновая кислота, которая кодирует домен VH и/ил и домен VL антитела или фрагмента, как определено в любом из пп. 1-33.
49. Нуклеиновая кислота, которая кодирует домен VH, содержащий аминокислотную последовательность домена VH антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или аминокислотную последовательность, которая идентична ей по меньшей мере на 70%.
50. Нуклеиновая кислота, которая кодирует домен VL, содержащий аминокислотную последовательность домена VL антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); или аминокислотную последовательность, которая идентична ей по меньшей мере на 70%.
51. Нуклеиновая кислота, содержащая нуклеотидную последовательность, которая по меньшей мере на 70% идентична последовательности SEQ ID №260 или 320.
Альтернативно:
Нуклеиновая кислота, содержащая нуклеотидную последовательность, которая по меньшей мере на 70% идентична последовательности SEQ ID №2, 66 или 200.
52. Нуклеиновая кислота, которая кодирует тяжелую цепь и/или легкую цепь антитела или фрагмента, как определено в любом из пп. 1-33.
53. Нуклеиновая кислота, кодирующая тяжелую цепь, содержащую аминокислотную последовательность VH, которая по меньшей мере на 70% идентична SEQ ID №259 или 319; и аминокислотную последовательность С-области, которая по меньшей мере на 70% идентична последовательности IGHG4, необязательно по меньшей мере на 70% идентична SEQ ID №3 или 152.
Альтернативно:
Нуклеиновая кислота, кодирующая тяжелую цепь, содержащую аминокислотную последовательность VH, которая по меньшей мере на 70% идентична SEQ ID №1, 65; и аминокислотную последовательность С-области, которая по меньшей мере на 70% идентична последовательности IGHG4, необязательно по меньшей мере на 70% идентична SEQ ID №3 или 152.
54. Нуклеиновая кислота, кодирующая легкую цепь, содержащую аминокислотную последовательность VL, которая по меньшей мере на 70% идентична SEQ ID №289 или 349; и аминокислотную последовательность С-области, которая по меньшей мере на 70% идентична последовательности IGKC, необязательно по меньшей мере на 70% идентична SEQ ID №156.
Альтернативно:
Нуклеиновая кислота, кодирующая легкую цепь, содержащую аминокислотную последовательность VL, которая по меньшей мере на 70% идентична SEQ ID №33, 95 или 229; и аминокислотную последовательность С-области, которая по меньшей мере на 70% идентична последовательности IGKC, необязательно по меньшей мере на 70% идентична SEQ ID №156.
55. Нуклеиновая кислота (например, в клетке-хозяине, например в клетке СНО, или НЕК293, или Cos), содержащая
a. нуклеотидную последовательность, которая по меньшей мере на 70% идентична последовательности тяжелой цепи антитела, выбранного из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT); и/или
b. нуклеотидную последовательность, которая по меньшей мере на 70% идентична последовательности легкой цепи антитела, выбранного, соответственно, из CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT).
56. Вектор, содержащий нуклеиновую кислоту(-ы) (например, нуклеиновую кислоту(-ы) по любому из пп. 48-55); при этом вектор необязательно представляет собой вектор СНО или НЕК293.
57. Клетка-хозяин, содержащая нуклеиновую кислоту(-ы) (например, нуклеиновую кислоту(-ы) по любому из пп. 48-55) или вектор по п. 56.
58. Антитело, фрагмент, комбинация, вектор, клетка-хозяин, применение или способ, как описано в данном документе.
В любом варианте осуществления в данном документе выбранное антитело предпочтительно представляет собой CL-274711.
Терапевтическое введение и составы
В изобретении предложены терапевтические композиции, содержащие антагонист к PCSK9, например антитела или их антигенсвязывающие фрагменты по данному изобретению. Введение терапевтических композиций в соответствии с изобретением будет осуществляться с подходящими носителями, вспомогательными веществами и другими агентами, которые включают в составы для обеспечения улучшенного переноса, доставки, переносимости и т.п. Множество подходящих составов можно найти в справочнике, известном всем химикам-фармацевтам: Remington's Pharmaceutical Sciences, Mack Publishing Company, Истон, Пенсильвания. Эти составы включают, например, порошки, пасты, мази, желе, воски, масла, липиды, везикулы, содержащие липиды (катионные или анионные), (такие как LIPOFECTINT™), конъюгаты ДНК, безводные абсорбирующие пасты, эмульсии «масло-в-воде» и «вода-в-масле», эмульсии карбовакса (полиэтиленгликоли различной молекулярной массы), полутвердые гели и полутвердые смеси, содержащие карбовакс. См. также Powell et al. "Compendium of excipients for parenteral formulations" PDA (1998) J Pharm Sci Technol 52:238-311.
Доза может варьироваться в зависимости от возраста и размера субъекта, которому вводят дозу, целевого заболевания, условий, пути введения и т.п. Когда антагонист, например антитело по данному изобретению, используется для лечения различных патологических состояний и заболеваний, связанных с PCSK9, у взрослого пациента, предпочтительно вводить антитело по данному изобретению внутривенно, как правило, в разовой дозе от около 0,01 до около 20 мг/кг массы тела, более предпочтительно от около 0,02 до около 7, от около 0,03 до около 5 или от около 0,05 до около 3 мг/кг массы тела. В зависимости от тяжести состояния можно регулировать частоту и продолжительность лечения.
Известны различные системы доставки, которые могут использоваться для введения антагониста или фармацевтической композиции по изобретению, например антагониста, обеспечиваемого, например, инкапсулированием в липосомы, микрочастицы, микрокапсулы, рекомбинантные клетки, способные экспрессировать мутантные вирусы, рецептор-опосредованным эндоцитозом (см., например, Wu et al. (1987) J. Biol. Chem. 262:4429-4432). Способы введения включают, но не ограничиваясь ими, внутрикожный, внутримышечный, внутрибрюшинный, внутривенный, подкожный, интраназальный, эпидуральный и пероральный пути. Антагонист или композицию можно вводить любым удобным путем, например, путем инфузии или болюсной инъекции, путем абсорбции через эпителиальные или кожно-слизистые оболочки (например, слизистую оболочку полости рта, слизистую оболочку прямой кишки и т.д.) и можно вводить вместе с другими биологически активными агентами. Введение может быть системным или местным.
Антагонист или фармацевтическая композиция также могут быть доставлены в везикуле, в частности в липосомах (см. Langer (1990) Science 249:1527-1533; Treat et al. (1989) in Liposomes in the Therapy of Infectious Disease and Cancer, Lopez Berestein and Fidler (eds.), Liss, New York, pp. 353-365; Lopez-Berestein, ibid., pp. 317-327; см. в общем там же).
В определенных ситуациях антагонист или фармацевтическая композиция могут быть доставлены в системе с контролируемым высвобождением. В одном варианте осуществления изобретения может использоваться насос (см. Langer, выше; Sefton (1987) CRC Grit. Ref. Biomed. Eng. 14:201). В другом варианте осуществления изобретения можно использовать полимерные материалы; см. Medical Applications of Controlled Release, Langer and Wise (eds.), CRC Pres., Boca Raton, Fla. (1974). В еще одном варианте осуществления изобретения система с контролируемым высвобождением может быть размещена в непосредственной близости от мишени композиции, что требует лишь части системной дозы (см., например, Goodson, в Medical Applications of Controlled Release, supra, vol. 2, pp.115-138, 1984).
Инъекционные препараты могут включать лекарственные формы для внутривенных, подкожных, внутрикожных и внутримышечных инъекций, капельных инфузий и т.д. Эти инъекционные препараты могут быть приготовлены общеизвестными способами. Например, инъекционные препараты можно приготовить, например, растворением, суспендированием или эмульгированием антитела или его соли, описанных выше, в стерильной водной среде или масляной среде, обычно используемой для инъекций. В качестве водной среды для инъекций используются, например, физиологический раствор, изотонический раствор, содержащий глюкозу и другие вспомогательные агенты и т.д., которые можно использовать в сочетании с подходящим солюбилизирующим агентом, таким как спирт (например, этанол), многоатомный спирт (например, пропиленгликоль, полиэтиленгликоль), неионогенное поверхностно-активное вещество [например, полисорбат 80, НСО-50 (полиоксиэтиленовый (50 моль) аддукт гидрогенизированного касторового масла)] и т.д. В качестве масляной среды используются, например, кунжутное масло, соевое масло и т.д., которые можно использовать в сочетании с солюбилизирующим агентом, таким как бензилбензоат, бензиловый спирт и т.д. Приготовленной таким образом инъекцией предпочтительно заполняют соответствующую ампулу. Фармацевтическая композиция по данному изобретению может быть введена подкожно или внутривенно с помощью стандартной иглы и шприца. Кроме того, что касается подкожной доставки, устройство для доставки в виде шприца-ручки легко может найти применение при доставке фармацевтической композиции по данному изобретению. Такое устройство доставки в виде шприца-ручки может быть многоразовым или одноразовым. В многоразовом устройстве доставки в виде шприца-ручки обычно используется сменный картридж, который содержит фармацевтическую композицию. После того, как вся фармацевтическая композиция в картридже введена и картридж опустеет, пустой картридж можно выбросить и заменить новым картриджем, содержащим фармацевтическую композицию. После этого устройство доставки в виде шприца-ручки можно использовать повторно. В одноразовом устройстве доставки в виде шприца-ручки сменный картридж отсутствует. Скорее, одноразовое устройство для доставки в виде шприца-ручки поставляется предварительно заполненным фармацевтической композицией, содержащейся в резервуаре внутри устройства. Как только резервуар опустошается от фармацевтической композиции, все устройство выбрасывается.
Многочисленные многоразовые шприцы-ручки и автоинжекторы используются для подкожной доставки антагониста или фармацевтической композиции по данному изобретению. Примеры включают, но не ограничиваются ими, AUTOPEN™ (Owen Mumford, Inc., Вудсток, Великобритания), шприц-ручку DISETRONIC™ (Disetronic Medical Systems, Бургдорф, Швейцария), шприц-ручку HUMALOG MIX 75/25™, шприц-ручку HUMALOG™, шприц-ручку HUMALIN 70/30™ (Eli Lilly and Co., Индианаполис, Индиана), NOVOPEN™ I, II и III (Novo Nordisk, Копенгаген, Дания), NOVOPEN JUNIOR™ (Novo Nordisk, Копенгаген, Дания), шприц-ручку BD™ (Becton Dickinson, Франклин Лейке, Нью-Джерси), OPTIPENT™, OPTIPEN PRO™, OPTIPEN STARLET™ и OPTICLIKT™ (Sanofi-Aventis, Франкфурт, Германия), и это лишь некоторые из них. Примеры одноразовых устройств для доставки в виде шприца-ручки, применяемых для подкожной доставки фармацевтической композиции по данному изобретению, включают, но не ограничиваясь ими, шприц-ручку SOLOSTAR™ (Sanofi-Aventis), FLEXPEN™ (Novo Nordisk) и KWIKPEN™ (Eli Lilly).
Преимущественно фармацевтические композиции для перорального или парентерального применения, описанные выше, готовят в виде лекарственных форм в стандартной дозе, подходящей для соответствия дозе антагониста(-ов). Такие лекарственные формы в стандартной дозе включают, например, таблетки, драже, капсулы, инъекции (ампулы), суппозитории и т.д. Количество содержащегося вышеупомянутого антитела обычно составляет от около 5 до около 500 мг на лекарственную форму в стандартной дозе; особенно в форме инъекции, предпочтительно, чтобы вышеуказанное антитело содержалось в количестве от около 5 до около 100 мг и от около 10 до около 250 мг для других лекарственных форм.
Для удобства ниже приведены значения некоторых терминов и фраз, используемых в описании, примерах и прилагаемой формуле изобретения. Если не указано иное или не вытекает из контекста, следующие термины и фразы имеют значения, указанные ниже. Определения предоставлены для помощи в описании конкретных вариантов осуществления изобретения и не предназначены для ограничения заявленного изобретения, поскольку объем изобретения ограничен только формулой изобретения. Если не указано иное, все технические и научные термины, используемые в данном документе, имеют то же значение, которое обычно понимается специалистом в области, к которой принадлежит это изобретение. Если есть очевидное несоответствие между использованием термина в данной области техники и его определением, приведенным в данном документе, определение, приведенное в описании, имеет преимущество.
Для удобства в данном документе собраны некоторые термины, используемые в данном документе, в описании, примерах и прилагаемой формуле изобретения.
Термины «уменьшение», «сниженный» или «снижение» используются в данном документе для обозначения уменьшения на статистически значимую величину. В некоторых вариантах осуществления изобретения «снизить», «снижение» или «уменьшение» обычно означает уменьшение по меньшей мере на 10% по сравнению с контрольным уровнем (например, отсутствие данного лечения) и может включать, например, уменьшение на по меньшей мере около 10%, по меньшей мере около 20%, по меньшей мере около 25%, по меньшей мере около 30%, по меньшей мере около 35%, по меньшей мере около 40%, по меньшей мере около 45%, по меньшей мере около 50%, по меньшей мере около 55%, по меньшей мере около 60%, по меньшей мере около 65%, по меньшей мере около 70%, по меньшей мере около 75%, по меньшей мере около 80%, по меньшей мере около 85%, по меньшей мере около 90%, по меньшей мере около 95%, по меньшей мере около 98%, по меньшей мере около 99% или более. Используемый в данном термин «снижение» не включает полное снижение по сравнению с контрольным уровнем. Предпочтительно, снижение может быть до уровня в пределах нормы, приемлемого для человека без данного расстройства. Однако, например, для целей понижения или снижения уровня холестерина, например, снижение на около 5-10 пунктов можно рассматривать как «уменьшение» или «снижение».
В некоторых аспектах всех вариантов осуществления изобретения используется термин «ингибирование». Ингибирование относится к уменьшению по меньшей мере на 10% по сравнению с контрольным уровнем (например, отсутствие данного лечения) и может включать, например, уменьшение на по меньшей мере около 10%, по меньшей мере около 20%, по меньшей мере около 25%, по меньшей мере около 30%, по меньшей мере около 35%, по меньшей мере около 40%, по меньшей мере около 45%, по меньшей мере около 50%, по меньшей мере около 55%, по меньшей мере около 60%, по меньшей мере около 65%, по меньшей мере около 70%, по меньшей мере около 75%, по меньшей мере около 80%, по меньшей мере около 85%, по меньшей мере около 90%, по меньшей мере около 95%, по меньшей мере около 98%, по меньшей мере около 99% или более, в том числе ингибирование на 100% по сравнению с контрольным уровнем. «Полное ингибирование» относится к ингибированию на 100% по сравнению с контрольным уровнем.
Термины «повышенный», «повышать», «усиливать» или «активировать» используются в данном документе для обозначения увеличения на статически значимую величину. В некоторых вариантах осуществления изобретения термины «повышенный», «повышать», «усиливать» или «активировать» могут означать увеличение по меньшей мере на 10% по сравнению с контрольным уровнем, например увеличение по меньшей мере на около 20%, или по меньшей мере на около 30%, или по меньшей мере на около 40%, или по меньшей мере на около 50%, или по меньшей мере на около 60%, или по меньшей мере на около 70%, или по меньшей мере на около 80%, или по меньшей мере на около 90%, или до и включая увеличение на 100% или любое увеличение на 10-100% по сравнению с контрольным уровнем, или по меньшей мере примерно в 2 раза, или по меньшей мере примерно в 3 раза, или по меньшей мере примерно в 4 раза, или по меньшей мере примерно в 5 раз, или по меньшей мере примерно в 10 раз, или любое увеличение от 2 до 10 раз или больше по сравнению с контрольным уровнем. В контексте маркера или симптома «повышать» представляет собой статистически значимое повышение такого уровня.
При использовании в данном документе, термин «по существу» относится к качественному состоянию проявления полной или почти полной степени или величины характеристики или свойства, представляющего интерес. Специалист в области биологии поймет, что биологические и химические явления редко, если вообще когда-либо, доходят до завершения и/или переходят к завершению или достигают или избегают абсолютного результата. Таким образом, термин «по существу» используется в данном документе для обозначения отсутствия полноты, присущей многим биологическим и химическим явлениям. Для устранения сомнений «по существу» может относиться к по меньшей мере 90% степени или величины интересующей характеристики или свойства, например по меньшей мере 90%, по меньшей мере 92%, по меньшей мере 95%, по меньшей мере 98%, по меньшей мере 99% или более.
Все патенты и другие публикации, включая ссылки на литературу, выданные патенты, опубликованные заявки на патенты и одновременно рассматриваемые заявки на патенты; процитированные в этой заявке явно включены в данный документ посредством ссылки с целью описания и раскрытия, например, методологий, описанных в таких публикациях, которые могут быть использованы в связи с описанной в данном документе технологией. Эти публикации приведены исключительно для их раскрытия до даты подачи данной заявки. Ничто в этом отношении не следует истолковывать как признание того, что авторы изобретения не имеют права датировать такое раскрытие задним числом на основании предшествующего изобретения или по любой другой причине. Все заявления относительно даты или представления содержания этих документов основаны на информации, доступной заявителям, и не являются признанием в отношении правильности дат или содержания этих документов.
Описание вариантов осуществления раскрытия не предназначено быть исчерпывающим или ограничивать раскрытие точной раскрытой формой. Хотя конкретные варианты осуществления и примеры раскрытия описаны в данном документе для иллюстративных целей, возможны различные эквивалентные модификации в пределах объема раскрытия, что будет понятно специалистам в соответствующей области техники. Например, хотя стадии или функции способа представлены в конкретном порядке, альтернативные варианты осуществления могут выполнять функции в другом порядке, или функции могут быть выполнены по существу одновременно. Идеи раскрытия, представленные в данном документе, могут быть применены к другим процедурам или способам, если это необходимо. Различные варианты осуществления, описанные в данном документе, могут быть объединены для получения дополнительных вариантов осуществления. Аспекты раскрытия могут быть изменены, если необходимо, для использования композиций, функций и концепций приведенных выше ссылок и заявки, чтобы получить еще дополнительные варианты осуществления раскрытия. Более того, из соображений биологической функциональной эквивалентности, некоторые изменения могут быть внесены в структуру белка без влияния на биологическое или химическое действие по типу или количеству. Эти и другие изменения могут быть внесены в раскрытие в свете подробного описания. Предполагается, что все такие модификации включены в объем прилагаемой формулы изобретения.
Конкретные элементы любого из вышеупомянутых вариантов осуществления могут быть объединены или заменены элементами в других вариантах осуществления. Кроме того, хотя преимущества, связанные с определенными вариантами осуществления раскрытия, были описаны в контексте этих вариантов осуществления, другие варианты осуществления также могут демонстрировать такие преимущества, и не все варианты осуществления обязательно должны демонстрировать такие преимущества, чтобы подпадать под объем раскрытия.
Следует понимать, что конкретные конфигурации, аспекты, примеры, пункты и варианты осуществления, описанные в данном документе, показаны в качестве иллюстрации, а не как ограничения изобретения. Основные признаки этого изобретения могут использоваться в различных вариантах осуществления, не выходя за рамки объема изобретения. Специалисты в данной области узнают или смогут установить, используя не более чем рутинное исследование, многочисленные эквиваленты конкретных процедур, описанных в данном документе. Такие эквиваленты считаются входящими в объем данного изобретения и охватываются формулой изобретения. Все публикации и заявки на патенты, упомянутые в описании, указывают на уровень квалификации специалистов в области, к которой относится это изобретение. Все публикации и патентные заявки включены в данный документ посредством ссылки в той же степени, как если бы каждая отдельная публикация или патентная заявка была специально и индивидуально указана для включения посредством ссылки. Использование слова в единственном числе вместе с термином «содержащий» в формуле изобретения и/или описании может означать «один», но это также согласуется со значением «один или более», «по меньшей мере один» и «один или более одного». Использование термина «или» в формуле изобретения используется для обозначения «и/или», если явно не указано, что он относится только к альтернативам или альтернативы являются взаимоисключающими, хотя раскрытие поддерживает определение, которое относится только к альтернативам и «и/или». В этой заявке термин «около» используется для обозначения того, что значение включает в себя вариацию погрешности, присущую устройству, методу, используемому для определения значения, или вариацию, существующую среди субъектов исследования.
При использовании в данном описании и пункте(-ах) формулы слова «содержащий» (и любая форма от содержащий, такая как «содержать» и «содержит»), «имеющий» (и любая форма от имеющий, такая как «иметь» и «имеет»), «включающий» (и любая форма от включающий, такая как «включает» и «включать») или «вмещающий» (и любая форма от вмещающий, такая как «вмещает» и «вмещать») являются исчерпывающими или открытыми и не исключают дополнительных, неперечисленных элементов или стадий способа.
Любая часть этого раскрытия может быть прочитана в сочетании с любой другой частью раскрытия, если иное не очевидно из контекста.
Все композиции и/или способы, раскрытые и заявленные в данном документе, могут быть изготовлены и выполнены без излишнего экспериментирования в свете данного раскрытия. Хотя композиции и способы по данному изобретению были описаны в терминах предпочтительных вариантов осуществления, специалистам в данной области будет очевидно, что к композициям и/или способам, а также к стадиям или последовательности стадий способа, описанного в данном документе, можно применять изменения без отклонения от концепции, сущности и объема изобретения. Все такие аналогичные замены и модификации, очевидные для специалистов в данной области техники, считаются находящимися в пределах сущности, объема и концепции изобретения, что определено прилагаемой формулой изобретения.
Данное изобретение описано более подробно в следующих неограничивающих примерах.
ПРИМЕРЫ
Холестерин ЛПНП в плазме (ХС-ЛПНП) является основным фактором риска сердечно-сосудистых заболеваний, от которых ежегодно умирают 4 миллиона человек в Европе. Клиренс ХС-ЛПНП в плазме в первую очередь осуществляется в печени с помощью рецептора ЛПНП (LDLR). LDLR постоянно захватывает ХС-ЛПНП из плазмы в гепатоциты и продолжает поглощать ХС-ЛПНП, возвращаясь обратно на поверхность клетки. Поверхностный уровень LDLR отрицательно регулируется PCSK9, который напрямую связывается с LDLR и способствует опосредованной лизосомами деградации LDLR. Уменьшение поверхностного воздействия LDLR на ХС-ЛПНП снижает интернализацию ХС-ЛПНП в гепатоциты и, таким образом, увеличивает ХС-ЛПНП в плазме, что может привести к образованию бляшек и закупориванию кровотока. Недавно нацеливание на PCSK9 стало многообещающей стратегией для контроля уровня ХС-ЛПНП в плазме.
Мы обнаружили моноклональные антитела, которые блокируют функцию PCSK9 и обладают терапевтическим потенциалом. Сначала мы иммунизировали Kymice™ (см., например, WO2011/004192 и Lee et al, Nat Biotechnol. 2014 Apr; 32(4):356-63. doi: 10.1038/nbt.2825. Epub 2014 Mar 16, "Complete humanization of the mouse immunoglobulin loci enables efficient therapeutic antibody discovery") человеческими и мышиными белками PCSK9 для генерации перекрестно-реактивных антител. Чтобы избежать нежелательного эффекта His-метки, мы создали клеточную линию, которая активно секретирует нативную форму человеческого и мышиного белка PCSK9 без His-метки для иммунизации. После иммунизации последовательности антител были извлечены из антигенспецифических В-клеток с помощью секвенирования следующего поколения и проанализированы in silico для идентификации антител, подходящих для дальнейшей работы. После экспрессии антитела подвергали скринингу и отбирали на основе перекрестного связывания, аффинности и функции с помощью последовательного каскадного скрининга in vitro. Было подтверждено связывание с вариантами PCSK9 человека для обеспечения эффективности у большинства людей. Биофизические особенности выбранных антител были охарактеризованы с точки зрения способности к развитию. В модели гиперлипидемии на мышах два наилучших антитела (CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT)) показали превосходную функцию в снижении холестерина, не относящегося к ЛПВП, без изменения холестерина ЛПВП и устойчивый эффект с большей продолжительностью по сравнению с контрольными антителами. В заключение, мы успешно выявили перекрестные антитела к PCSK9 и идентифицировали по меньшей мере два превосходных полностью человеческих моноклональных антитела для блокирования функции PCSK9 in vitro и in vivo.
Пример 1: Идентификация антител с помощью анализов in vitro
Было проведено пять кампаний иммунизации с использованием Kymice™ и анализы in vitro, включая следующие критерии отбора:
(a) были выбраны перекрестные связывающие соединения к PCSK9 человека (hPCSKS), PCSK9 яванского макака (cynoPCSK9) и PCSK9 мыши (mPCSK9);
(b) была определена аффинность антител к hPCSK9a и mPCSK9, и был отдан приоритет антителам с более высокой аффинностью;
(c) в клеточном анализе in vitro было продемонстрировано, что нейтрализация антител снижает интернализацию флуоресцентного hPCSK9 в линии клеток печени человека (HepG2); и
(d) одновременно с этим определяли функциональность антител по восстановлению захвата ЛПНП клетками HepG2 в том же клеточном анализе in vitro, что и в (с).
Два антитела (CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT)) показали особенно многообещающие функциональные свойства как in vitro, так и in vivo (Пример 2).
CL-148219
По сравнению с контрольными антителами, CL-148219 продемонстрировал более сильную нейтрализующую активность с более высокой способностью восстанавливать захват ЛПНП in vitro, что свидетельствует о том, что CL-148219 может напрямую блокировать взаимодействие между PCSK9 и LDLR. В модели гиперлипидемии на мышах (мыши E3L.CETP; de Knijff, Westerterp, Ason, van den Hoek and Kühnast) CL-148219 снижал уровень холестерина, не относящегося к ЛПВП, в плазме сильнее, чем контрольное антитело, с большей продолжительностью эффекта. См. Фигуры 1-4.
CL-148489
В клеточном анализе in vitro CL-148489 умеренно нейтрализовал hPCSK9, но обладал значительной способностью восстанавливать захват ЛПНП, что позволяет предположить, что это антитело может косвенно препятствовать связыванию PCSK9 с LDLR, возможно, посредством блокирования связывания HSPG с PCSK9. Это антитело также снижало уровень холестерина, не относящегося к ЛПВП, в плазме на мышиной модели гиперлипидемии (мыши E3L.CETP) лучше, чем контрольные образцы с аналогичной продолжительностью эффекта. См. Фигуры 5-8.
Контрольные антитела представляли собой: алирокумаб hIgG4-PE (SEQ ID №195 и 196) и «Regeneron рН-зависим.» (рН-зависимое (дифференциальное связывание PCSK9 внутри лизосомы по сравнению с внешней частью) антитело hIgG4-PE к PCSK9) (SEQ ID №197 и 198).
Области VH и VL антител были получены в результате рекомбинации следующих генных сегментов:
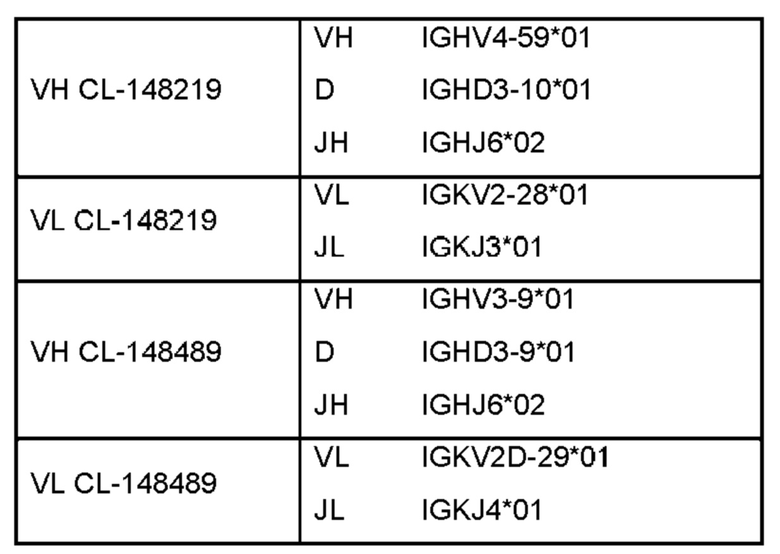
Список источников:
de Knijff, P. et al, 1991, "Familial dysbetalipoproteinemia associated with apo lipoprotein E3-Leiden in an extended multigeneration pedigree", J. Clin, Invest. 88: 643-655;
Westerterp, M. et al, 2006, "Cholesteryl ester transfer protein decreases high-density lipoprotein and severely aggravates atherosclerosis in APOE*3-Leidenmice", Arterioscler. Thromb. Vase. Biol. 26: 2552-2559;
Ason, B. et al, 2011, "PCSK9 inhibition fails to alter hepatic LDLR, circulating cholesterol, and atherosclerosis in the absence of ApoE", J Lipid Res. 2011 Apr, 52(4): 679-687;
van den Hoek AM. et al, 2014, "APOE*3Leiden.CETP transgenic mice as model for pharmaceutical treatment of the metabolic syndrome", Diabetes Obes Metab. 2014 Jun; 16(6):537-44; и
Kuhnast, S et al, 2014, "Alirocumab inhibits atherosclerosis, improves the plaque morphology, and enhances the effects of a statin", J Lipid Res. 2014 Oct, 55(10): 2103-2112.
Пример 2. Анализы in vivo
В этом исследовании мы использовали мышей APOE*3Leiden.CETP (транспортный белок холестериновых эфиров), которые содержат мышиный АроЕ, человеческий мутантный APOE3*Leiden и функциональный LDLR. Эти мыши показали отличную трансляционную ценность с увеличением холестерина, наблюдаемым в модели, которую можно лечить теми же методами лечения, которые эффективны для пациентов, и демонстрируют такое же максимальное снижение уровней ЛПНП, что и в клинических условиях.
Мыши СЕТР получали диету с высоким содержанием жиров в течение 4 недель, а затем получали однократную дозу антитела, изотипического контроля или стандарта лечения (алирокумаб, ингибитор PCSK9, одобренный FDA) в день 0. Затем мыши получали вторую более высокую дозу (половина log) на 18 день. Уровни холестерина у отдельных животных измеряли на 0, 3, 7, 14, 21 и 28 день. Полный липидный профиль был проведен на образце объединенной группы из крови, собранной в момент умерщвления, на 28 день.
Из 10 протестированных нами антител два (CL-148219 и CL148489) снижали уровень холестерина сильнее, чем эквивалентная доза алирокумаба, при этом одно антитело CL-148219 показало более длительный эффект. Таким образом, мы выделили два потенциально наилучших в своем классе ингибитора PCSK9.
Методы
См. схему исследования на Фиг. 9. Сто двадцать восемь самок трансгенных мышей APOE*3Leiden.CETP в возрасте 8-14 недель получали диету западного типа (WTD) с 0,15% холестерина и 15% насыщенных жиров. После 4-недельного вводного периода 24 мыши с низким уровнем ответа были исключены из исследования, и животные были разделены на группы (n=6-8), сопоставимые по возрасту, массе тела, холестерину в плазме, триглицеридам и холестерину ЛПВП после 4-часового голодания (t=0). Мышам вводили подкожно при t=0 3 мг/кг изотипического контроля, контрольного антитела или исследуемых антител к PCSK9. Для четырех из исследуемых антител, признанных превосходными по результатам предыдущего скрининга in vitro, была дополнительная группа с дозой 1 мг/кг при t=0. В t=18 дней мыши получили вторую подкожную дозу того же антитела, на ½ log более высокую дозу, чем первая доза (т.е. первая доза 3 мг/кг, вторая доза 10 мг/кг).
Массу тела и потребление пищи измеряли дважды в неделю. На 0, 3, 7, 14, 21 и 28 день после введения начальной дозы через 4 часа после приема пищи собирали образцы плазмы для определения общего холестерина в плазме, холестерина ЛПВП и триглицеридов. Были рассчитаны значения холестерина, не относящегося к ЛПВП, в плазме. В t=28 дней после последнего забора крови мышей умерщвляли и собирали плазму и ткань печени. Профили липопротеинов определяли в фракциях FPLC из объединенных для группы образцов плазмы. Статистика: двусторонний Annova и апостериорный анализ Даннетта - Graphpad Prism™.
Результаты
Общий холестерин (Фиг. 10)
В группе с изотипическим контролем во время исследования уровень общего холестерина в плазме составлял 16-22 ммоль/л.
Алирокумаб значительно снизил общий холестерин на 3-й день в дозе 3 мг/кг (-34,9%) и на 21-й и 28-й дни (соответственно через 3 и 10 дней после второй инъекции) в дозе 10 мг/кг (-33,2% и -32,3% соответственно) по сравнению с контрольным изотипическим антителом.
CL-148219 значительно снизил общий холестерин на 3-й день как в дозе 1, так и в дозе 3 мг/кг (-36,4% и -47,0%, соответственно), и на 7-й день в дозе 3 мг/кг (-32,6%). После второй дозы CL-148219 значительно снизил общий холестерин на 21 день как в дозе 3 мг/кг (-33,4% и -27,1%, соответственно), так и в дозе 10 мг/кг (-46,3% и -49,6%, соответственно).
CL-148489 значительно снизил общий холестерин на 3-й и 21-й день (3 дня после второй инъекции) в дозе 3 мг/кг (-47,3% и -32,3%, соответственно) и после второй дозы на 21-й и 28-й день в дозе 10 мг/кг (-42,9% и -56,0%, соответственно).
Общий холестерин, не относящийся кЛПВП (Фиг. 11)
В группе изотипического контроля во время исследования уровень холестерина, не относящегося к ЛПВП, составлял 15,2-21,3 ммоль/л.
Алирокумаб значительно снизил уровень холестерина, не относящегося к ЛПВП, на 3-й день в дозе 3 мг/кг (-36,5%) и на 21-й и 28-й дни (соответственно через 3 и 10 дней после второй инъекции) в дозе 10 мг/кг (-35,5% и 34,3%, соответственно) по сравнению с контрольным изотипическим антителом.
CL-148219 значительно снизил уровень холестерина, не относящегося к ЛПВП, на 3-й день как в дозе 1, так и в дозе 3 мг/кг (-37,7% и -49,1%, соответственно), и на 7-й день в дозе 3 мг/кг (-33,5%). После второй инъекции CL-148219 значительно снизил уровень холестерина, не относящегося к ЛПВП, на 21-й и 28-й день как в дозе 3 мг/кг (-34,4% и -29,2%, соответственно), так и в дозе 10 мг/кг (-49,6% и -51,8%, соответственно).
CL-148489 значительно снизил уровень холестерина, не относящегося к ЛПВП, на 3-й и 21-й день (3 дня после второй инъекции) в дозе 3 мг/кг (-49,4% и -35,0%, соответственно) и после второй инъекции на 21 и 28 день в дозе 10 мг/кг (-45,5% и -58,5%, соответственно).
Холестерин ЛПВП (Фиг. 12)
Ни одно из антител не влияло на холестерин ЛПВП.
Триглицериды (Фиг. 13)
Во время исследования уровни триглицеридов в плазме оставались стабильными в группе изотипического контроля. Хотя ни одно из антител существенно не влияло на триглицериды плазмы по сравнению с группой изотипического контроля, CL-148219, CI-148489 и алирокумаб показали тенденцию к более низким уровням триглицеридов на 28 день.
Профиль фосфолипидов и холестерина (Фиг. 14)
Профили фосфолипидов (А) и холестерина (В) для объединенных образцов показаны ниже: фракции 4-8 считаются ЛПОНП, 9-15 - ЛПНП и 16-24 - ЛПВП. Статистические исследования не проводились, поскольку измерения проводились на одной объединенной выборке на группу. Профили липопротеинов подтверждают, что алирокумаб, CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT) снижали уровень холестерина ЛПОНП и холестерина ЛПНП и не влияли на холестерин ЛПВП.
Выводы
• Наши антитела хорошо переносились животными, показывающими нормальное поведение и без признаков дискомфорта во время исследования.
• На разрезе тканей макроскопической патологии не выявлено.
• Ни одно из антител не оказало значительного влияния на массу тела и прием пищи.
• Ни одно из антител не повлияло на массу печени.
• CL-148219 и CL-148489 значительно снижали общий холестерин в плазме и холестерин, не относящийся к ЛПВП, дозозависимым образом по сравнению с группой изотипического контроля. Липопротеиновые профили показали снижение холестерина ЛПОНП в плазме у мышей, получавших эти антитела.
• Ни одно из исследуемых антител значительно не влияло на холестерин ЛПВП по сравнению с группой изотипического контроля.
• Ни одно из антител существенно не влияло на уровни триглицеридов в плазме, хотя алирокумаб, CL-274711, CL-148219QLT, CL-274698, CL-148219 и CL-148489 (например, CL-274711 или CL-148219QLT) показали тенденцию к снижению уровня триглицеридов в плазме по сравнению с группой изотипического контроля.
Примеры 3 и 4
Мыши
В Примере 3 использовали самок трансгенных мышей APOE*3Leiden.CETP. Мышей содержали в клетках из макролона (3 или 4 мыши на клетку) в комнатах для животных; относительная влажность 40-70%, температура 20-24°С, световой цикл с 7 утра до 7 вечера. Мышам давали корм и стерилизованную водопроводную воду в неограниченном количестве.
В примере 4 использовали мышей C57BL/6 массой 18-22 г в день эксперимента. Животных содержали группами по 2-4 в полисульфоновых клетках (площадь пола=1500 см2) в стандартных условиях: комнатная температура (22±2°С), гигрометрия (55±10%), цикл свет/темнота (12 ч/12 ч), замена воздуха (15-20 объемов/час), вода и еда в неограниченном количестве.
Анализ холестерина, липопротеинов и триглицеридов в плазме
Общий холестерин плазмы определяли с использованием набора Cholesterol CHOD-PAP (Roche, Мангейм, Германия), а триглицериды определяли с помощью набора Triglycerides GPO-PAP (Roche, Мангейм, Germany). Для определения холестерина ЛПВП в плазме липиды, содержащие АроВ, осаждали с использованием ПЭГ-6000/глицин с последующим количественным определением с использованием набора Cholesterol CHOD-PAP (Roche, Мангейм, Germany). Профили липопротеинов измеряли с помощью анализа FPLC с использованием устройства АКТА (GE Healthcare). Анализ проводили на объединенных по группе образцах. Фракции собирали на основании времени удерживания, и холестерин и фосфолипиды измеряли во фракциях с использованием набора Cholesterol CHOD-PAP (Roche, Мангейм, Германия) и набора Phospholipids (Instruchemie, Делфзейл, Нидерланды).
Концентрация антител в сыворотке
Концентрацию антител в сыворотке определяли с помощью иммуноферментного анализа (ELISA). Планшеты покрывали в течение ночи при 2-8°С антителом к IgG человека (Fc-специфическим). На следующий день аналитический планшет промывали три раза 300 мкл/лунка ФСБ+0,1% Твина (ФСБ-Т) с использованием устройства для промывки планшетов. Затем планшеты блокировали 250 мкл/лунка 2,5% молока в течение не менее 1 часа при комнатной температуре. Стандарты и контрольные образцы готовили в пробирках Эппендорфа. Затем стандарты, образцы и контрольные образцы разводили до 1:20 MRD в буфере для анализа в пробирках Эппендорфа. Планшеты трижды промывали 300 мкл/лунку ФСБ-Т с использованием устройства для промывки планшетов. 100 мкл на лунку стандарта, образца и контрольного образца добавляли в аналитический планшет в соответствии с картой планшета. Планшет инкубировали в течение 1 ч при кт, встряхивая при 300 об/мин. Планшеты промывали пять раз 300 мкл/лунка ФСБ-Т с использованием устройства для промывки планшетов и в каждую лунку добавляли 100 мкл антитела к IgG человека (Fc-специфического), конъюгированного с пероксидазой, разведенного 1:5000 в ФСБ, а затем планшет инкубировали в течение 1 ч при кт, встряхивая при 300 об/мин. Затем планшет промывали пять раз 300 мкл ФСБ-Т с использованием устройства для промывки планшетов. В каждую лунку добавляли 100 мкл субстрата ТМВ и планшет инкубировали в течение 15 минут при комнатной температуре в темноте. Затем в каждую лунку добавляли 100 мкл/лунка стоп-раствора (1 М серной кислоты) и определяли оптическую плотность с использованием считывающего устройства для микропланшетов, установленного на 450 нм с контрольным считыванием при 540 нм. Затем контрольное показание вычитали из показания при 450 нм с использованием программного обеспечения для считывания планшетов. Затем использовали Softmax Pro для анализа данных с помощью регрессионного анализа и аппроксимации кривой 4PL. Концентрации измеряли по стандартной кривой.
Пример 3
Самки трансгенных мышей APOE*3Leiden.CETP в возрасте 8-14 недель получали диету западного типа (WTD), содержащую 0,15% холестерина и 15% насыщенных жиров. После 4-недельного вводного периода мышей с низким ответом исключали из исследования. Остальные мыши были сопоставлены по возрасту, массе тела, холестерину и триглицеридам в плазме. Животных распределяли по группам по 6 (группа изотипического контроля) или по 10.
Животные получали подкожную инъекцию в день 0 (5 мл/кг). Антитела (изотипический контроль, контрольное антитело F, CL-148218 и CL-274711) вводили в дозе 1, 3 или 10 мг/кг. В дни 0, 3, 7, 14, 18, 21 и 28 после введения у животных брали образцы крови из хвостовой вены после 4-часового периода голодания. Кровь собирали с помощью систем Microvette СВ 300 К2Е (Sarstedt, Нюмбрехт, Германия), содержащих ЭДТА дикалия для определения общего холестерина, триглицеридов (день 0, 7 и 28) и холестерина ЛПВП. Пробирки или капилляры немедленно помещали на лед. Плазма с ЭДТА была получена после центрифугирования (10 мин при 6000 об/мин) при 4°С. Мышей умерщвляли на 28 день удушением CO2 сразу после последней точки отбора крови из хвостовой вены. Групповые профили липопротеинов были определены в образцах на 28 день.
Целью этого эксперимента было оценить фармакодинамические эффекты на профили общего холестерина/холестерина, не относящегося к ЛПВП, и липопротеинов в зависимости от дозы антител CL-274711, CL-148219 QLT и контрольного антитела F у трансгенных мышей APOE*3Leiden.CETP, находящихся на диете западного типа, содержащей 0,15% холестерина и 15% насыщенных жиров.
Все три антитела снижали уровень холестерина во всех испытанных дозах (см. Фиг. 15-17), а увеличение дозы увеличивало наблюдаемое снижение холестерина и продолжительность эффекта. При 1 и 3 мг/кг CL-148219 QLT был более эффективным, чем контрольное антитело F, в снижении уровней холестерина, и при всех испытанных дозах CL-148219 QLT имел более длительный эффект, чем контрольное антитело F (Фиг. 15-17). Дальнейший анализ показал, что CL-148219 QLT был также эффективен, как и в 3 раза более высокая доза контрольного антитела F в отношении снижения уровня холестерина, и имел ту же продолжительность эффекта, что и более высокая доза контрольного антитела F (Фиг. 18-19). CL-274711 снижал уровни холестерина до тех же уровней, что и аналогичная доза контрольного антитела F, но имел более длительный эффект (Фиг. 16-17).
Антитела показали эквивалентное снижение уровней холестерина, не относящегося к ЛПВП, при всех испытанных дозах (см. Фиг. 20), при этом увеличение дозы приводило к постепенному увеличению снижения уровня холестерина, не относящегося к ЛПВП, и продолжительности ответа. При 1 и 3 мг/кг CL-148219 QLT был более эффективным, чем контрольное антитело F, в снижении уровней холестерина, не относящегося к ЛПВП, и при всех испытанных дозах CL-148219 QLT имел более длительный эффект, чем контрольное антитело F (Фиг. 20). Дальнейший анализ также показал, что CL-148219 QLT был также эффективен, как и в 3 раза более высокая доза контрольного антитела F в отношении снижения уровня холестерина, не относящегося к ЛПВП, и имел ту же продолжительность эффекта, что и более высокая доза контрольного антитела F (Фиг. 21). CL-274711 снижал уровни холестерина до тех же уровней, что и аналогичная доза контрольного антитела F, но имел более длительный эффект (Фиг. 21).
Оценка профилей фосфолипидов на 28 день (Фиг. 22) показала, что как CL-274711, так и CL-148219 QLT снижали уровень холестерина ЛПОНП/ЛПНП и фосфолипидов дозозависимым образом. По сравнению с контрольным антителом F как CL-274711, так и CL-148219 QLT в дозе 10 мг/кг были более эффективны в снижении холестерина ЛПОНП/ЛПНП и фосфолипидов.
Пример 4
Для исследования использовали самцов мышей C57BL/6 (JANVIER LABS, C.S. 4105, Сен-Бертвен F-53941, Франция) массой 18-22 г в день эксперимента. Животные получали подкожную инъекцию 3 мг/кг CL-148219 QLT, CL-274711 или контрольного антитела F в день 0 (10 мл/кг). Забор крови проводили на 1, 3, 7, 14, 21 и 28 дни после введения дозы (n=3 на точку отбора). Затем из каждого образца крови готовили сыворотку, которую затем использовали для определения концентрации антител в каждый момент времени.
Целью эксперимента была оценка фармакокинетики CL-148219 QLT, CL-274711 и контрольного антитела F в течение 28 дней. Оценка профилей ФК показала, что как CL-274711, так и CL-148218 характеризовались более высокой исходной концентрацией антител в сыворотке, чем контрольное антитело F, и эта более высокая концентрация антител в сыворотке сохранялась в течение 28 дней исследования (Фиг. 23). CL-148219 QLT изначально характеризовался более высокой концентрацией антител в сыворотке, чем CL-274711, но CL-274711 имел более медленный клиренс из сыворотки.
Дополнительные данные:
Ссылка сделана на Фигуры 24 и далее, демонстрирующие эффективность антител по изобретению. Также сделана ссылка на Таблицу 1, показывающую аффинность антител к вариантам PCSK9 человека, PCSK9 яванского макака и PCSK9 мыши при нейтральном рН (7,6) по сравнению с кислым рН (5,8). KD измеряли с помощью системы анализа SPR ProteOn™.
Мы включили шесть контрольных антител к PCSK9 в качестве контролей для сравнения. Три контрольных антитела были вариантами продаваемых антител (контрольные антитела А, В и F), а три были выбраны из антител в клинических испытаниях (контрольные антитела С, D и Е). Контрольные антитела А, В, С, D и Е были выполнены в формате IgG4PE человека. Контрольное антитело F было в формате IgG1 человека.
Антигены, используемые для иммунизации и/или скрининга, включали 4 варианта PCSK9 человека, PCSK9 яванского макака и PCSK9 мыши. В данном документе мы назвали 4 варианта PCSK9 человека следующим образом: контрольное антитело к PCSK9 человека (hPCSK9 контр.), вариант a PCSK9 человека (hPCSKSa), вариант b PCSK9 человека (hPCSKSb) и мутант с усилением функции D374Y PCSK9 человека (hPCSK9 GOF). По сравнению с контрольной последовательностью PCSK9 человека вариант а человека имеет аминокислотные замены V474I и G670E, а вариант b человека имеет аминокислотные замены A53V, V474I и G670E. Мы включили эти 4 варианта человека для анализа, чтобы найти антитело, способное нейтрализовать все 4 варианта и мутант в человеческой популяции.
CL-148219
По сравнению с контрольными антителами CL-148219 показал более сильную нейтрализующую активность с большей способностью восстанавливать захват ЛПНП in vitro, что свидетельствует о том, что CL-148219 может напрямую блокировать взаимодействие между PCSK9 и LDLR. В модели гиперлипидемии на мышах (мыши E3L.CETP; de Knijff, Westerterp, Ason, van den Hoek and Kuhnast) CL-148219 снижал уровень холестерина, не относящегося к ЛПВП, в плазме сильнее, чем контрольное антитело, с большей продолжительностью эффекта. См. Фиг. 24-27 и Таблицу 1.
Мутант CL-148219 QLT
Посредством анализа последовательности путем компьютерного моделирования был обнаружен мотив N-гликозилирования в тяжелой цепи CL-148219. Мотив NLT, расположенный в каркасной области 3 тяжелой цепи, может быть гликозилирован и может оказывать неблагоприятное влияние на способность к развитию. Позже с помощью масс-спектрометрии было подтверждено, что мотив NLT в CL-148219 действительно был N-гликозилирован. Таким образом, мы ввели мутацию в мотив NLT, заменив остаток N на Q, создав мутант CL-148219 QLT, чтобы нарушить гликозилирование. Устранение гликозилирования было дополнительно подтверждено масс-спектрометрией. Мутант CL-148219 QLT продемонстрировал аналогичную аффинность и функциональность in vitro по сравнению с родительским CL-148219. Подобно родительскому CL-148219 мутант QLT снижал уровень холестерина, не относящегося к ЛПВП, в плазме, превосходя контрольные антитела с большей продолжительностью эффекта на мышиной модели гиперлипидемии (мыши E3L.CETP). См. Фиг. 27-31 и Таблицу 1.
CL-148489
В клеточном анализе in vitro CL-148489 умеренно нейтрализовал hPCSK9, но обладал значительной способностью восстанавливать захват ЛПНП, что позволяет предположить, что это антитело может косвенно препятствовать связыванию PCSK9 с LDLR, возможно, посредством блокирования связывания HSPG с PCSK9. Это антитело также снижало уровень холестерина, не относящегося к ЛПВП, в плазме на мышиной модели гиперлипидемии (мыши E3L.CETP) лучше, чем контрольные образцы с аналогичной продолжительностью эффекта. См. Фиг. 32-35 и Таблицу 1.
CL-274698
В отличие от CL-148219 и CL-148489, которые были получены от мыши с локусами гуманизированных антител и без нокаута гена PCSK9, CL-274698 был получен от мыши с нокаутом PCSK9. В отсутствие PCSK9 мыши продуцировали высокоаффинные антитела против иммуногенов, включая PCSK9 человека и мыши. Таким образом был получен и подвергнут скринингу CL-274698. CL-274698 не только продемонстрировал высокую аффинность к PCSK9 с KD в диапазоне субнМ, но также продемонстрировал превосходную функцию нейтрализации hPCSK9 и восстановления захвата ЛПНП in vitro. В исследовании эффективности in vivo с использованием мышей E3L.CETP, CL-274698 снижал уровень холестерина, не относящегося к ЛПВП, в плазме больше, чем контрольные антитела, в течение 3 дней после инъекции АЬ, при том, что уровень холестерина, не относящегося к ЛПВП, был аналогичен контрольным показателям после 7-го дня. См. Фиг. 36-39 и Таблицу 1.
CL-274711
Подобно CL-274698, CL-274711 был получен путем иммунизации мыши, нокаутированной по PCSK9. В клеточных анализах in vitro CL-274711 нейтрализовал hPCSK9 и восстанавливал захват ЛПНП лучше, чем в контрольные антитела. В тесте эффективности in vivo с использованием мышей E3L.CETP, CL-274711 продемонстрировал несколько лучшую функцию снижения холестерина, не относящегося к ЛПВП, в плазме с большей продолжительностью действия по сравнению с контрольными показателями. См. Фиг. 40-43 и Таблицу 1.
Методика
Функциональный клеточный анализ in vitro
Клетки HepG2 высевали из расчета 6×104 клеток/лунка в 96-луночные прозрачные планшеты с плоским дном для культивирования клеток (Costar) в полной культуральной среде, содержащей 10% ФБС, 1х пенициллина/стрептомицина и 1х NEAA в МЕМα. Чтобы обеспечить прикрепление, клетки инкубировали в инкубаторе с 5% CO2 при 37°С в течение 24 часов. На следующий день среды заменяли бессывороточной культуральной средой (1х NEAA и 1х пенициллина/стрептомицина в МЕМα), и клетки выдерживали в инкубаторе в течение ночи (16-18 часов). На следующий день клетки обрабатывали различными концентрациями моноклональных антител к PCSK9, которые предварительно инкубировали с 5 мкг/мл АР647-меченого антигена hPCSKS GOF. Антитела разбавляли от 60 мкг/мл 3-кратными последовательными разведениями. После 1 часа инкубации с hPCSK9 GOF и антителами к PCSK9 к клеткам добавляли BODIPY LDL (Invitrogen) до конечной концентрации 10 мкг/мл. Для поглощения ЛПНП клетки инкубировали в течение дополнительных 3 часов. В конце обработки клетки отделяли с помощью аккутазы (BD), а затем фиксировали 2% параформальдегидом, разведенным в ФСБ (Alfa Aesar), в течение ночи при 4°С. После промывания клетки ресуспендировали в ФСБ, содержащем 5 мМ ЭДТА, и флуоресцентные клетки детектировали с помощью проточной цитометрии CytoFlex.
Анализ SPR ProteOn
ProteOn™ XPR36 (Bio-Rad) использовали для измерения аффинности связывания антитела с антигеном (варианты PCSK9 человека, PCSK9 яванского макака и PCSK9 мыши) в нейтральном (HBS-EP+, рН 7,6) и кислом буфере (30 мМ ацетата натрия, 150 мМ NaCl, 0,05% Р20, рН 5,8) при 25°С. Анализ SPR выполняли с использованием чипа GLC (Bio-Rad), на котором были иммобилизованы антитела к Fc человека. Анализируемые антитела человека были захвачены на поверхности чипа в концентрации 2 мкг/мл. Белки PCSK9 вводили при 100 нМ, 25 нМ, 6,25 нМ, 1,56 нМ, 0,39 нМ в течение 180 секунд и наблюдали за диссоциацией в течение 600 секунд при скорости потока 30 мкл/мин. Поверхность чипа регенерировали с помощью двух инъекций 10 мМ глицина с рН 1,5 в течение 160 секунд при 30 мкл/мин. Затем сенсограммы аппроксимировали с помощью модели 1:1 (кинетическая модель Ленгмюра), где подобраны ka и kd, a KD рассчитана с помощью программного обеспечения ProteOn.

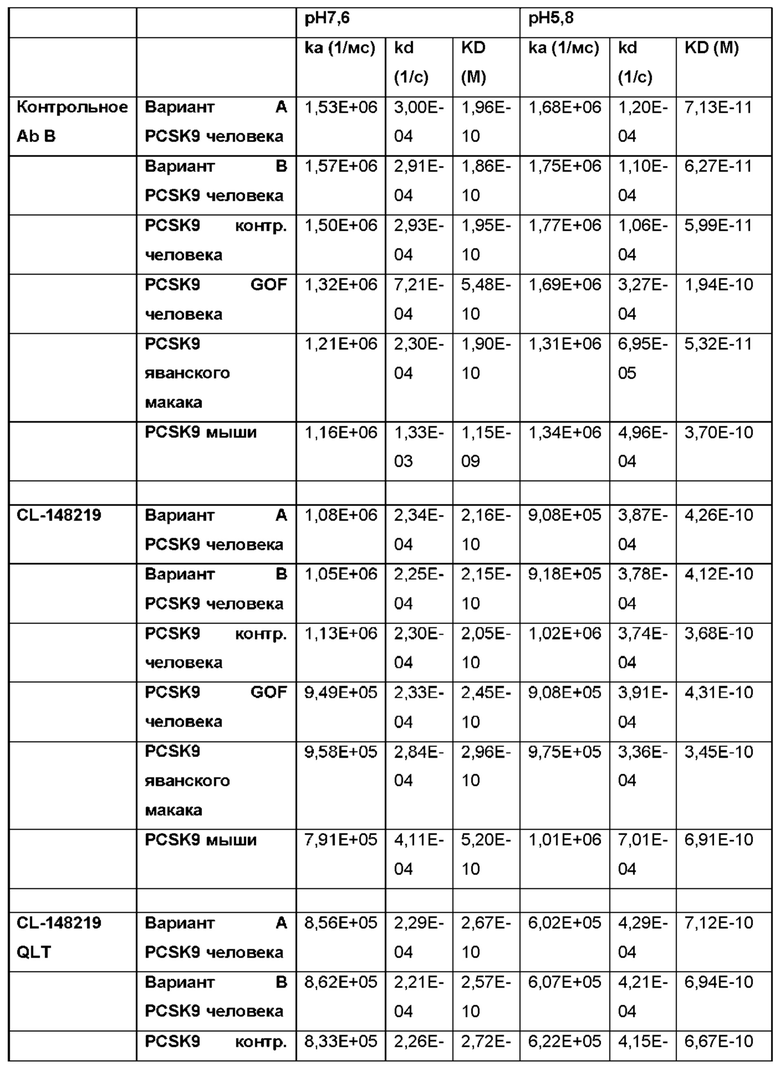
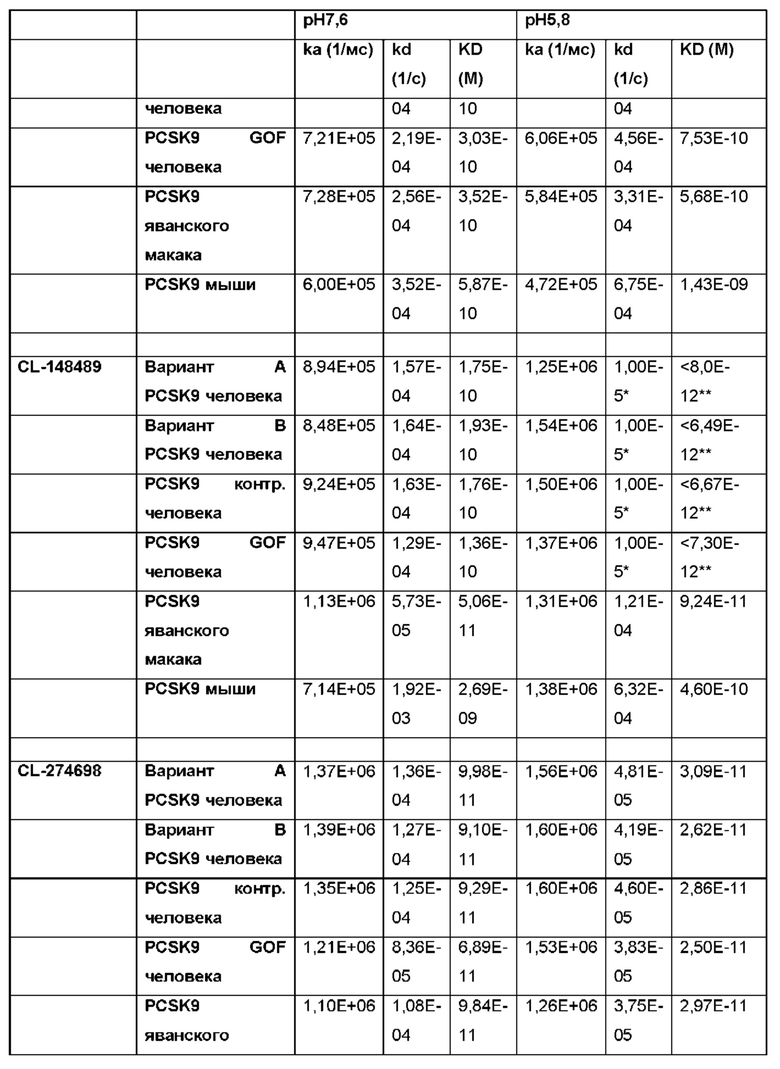
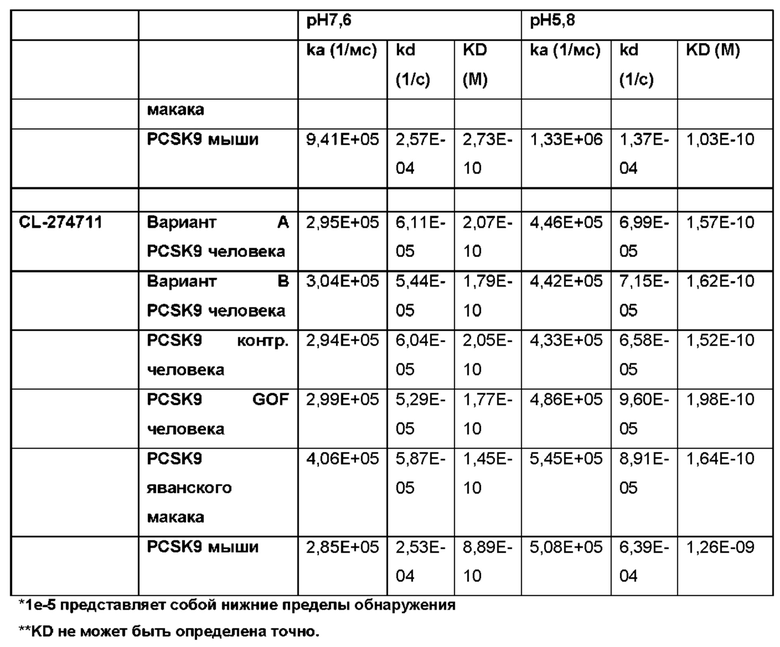
КРАТКИЙ ОБЗОР ПОСЛЕДОВАТЕЛЬНОСТЕЙ ВАРИАБЕЛЬНОЙ ОБЛАСТИ
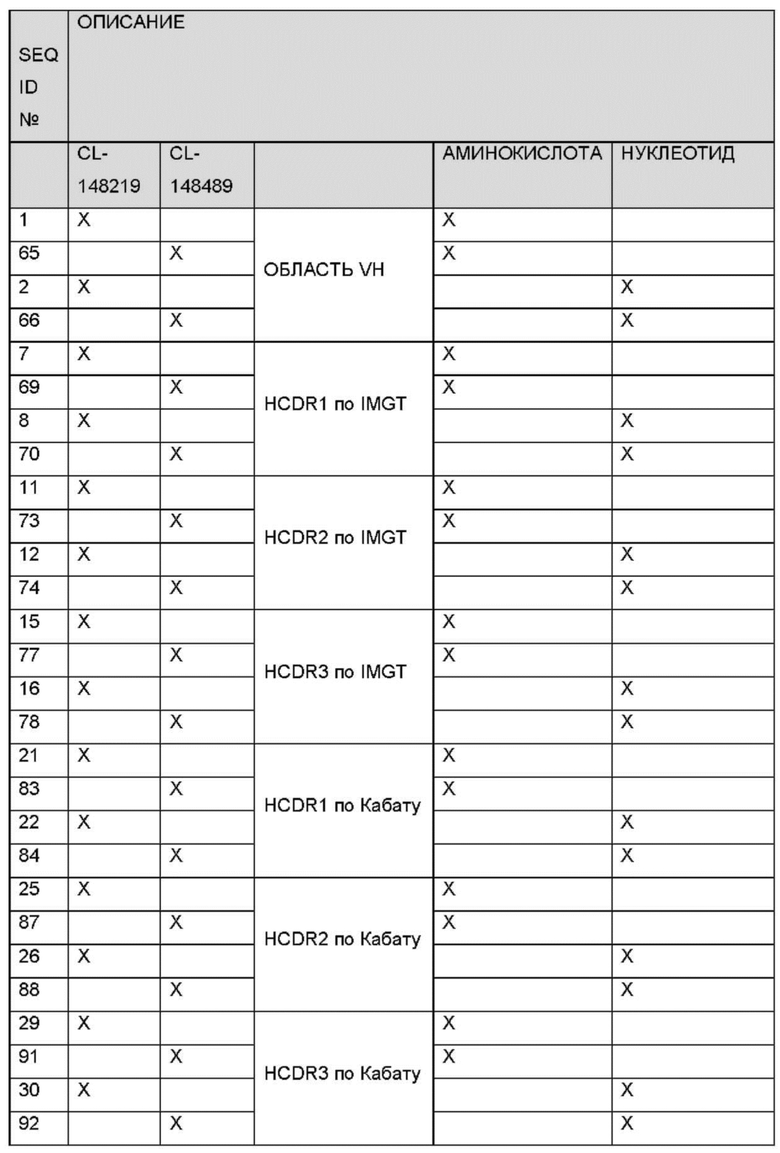
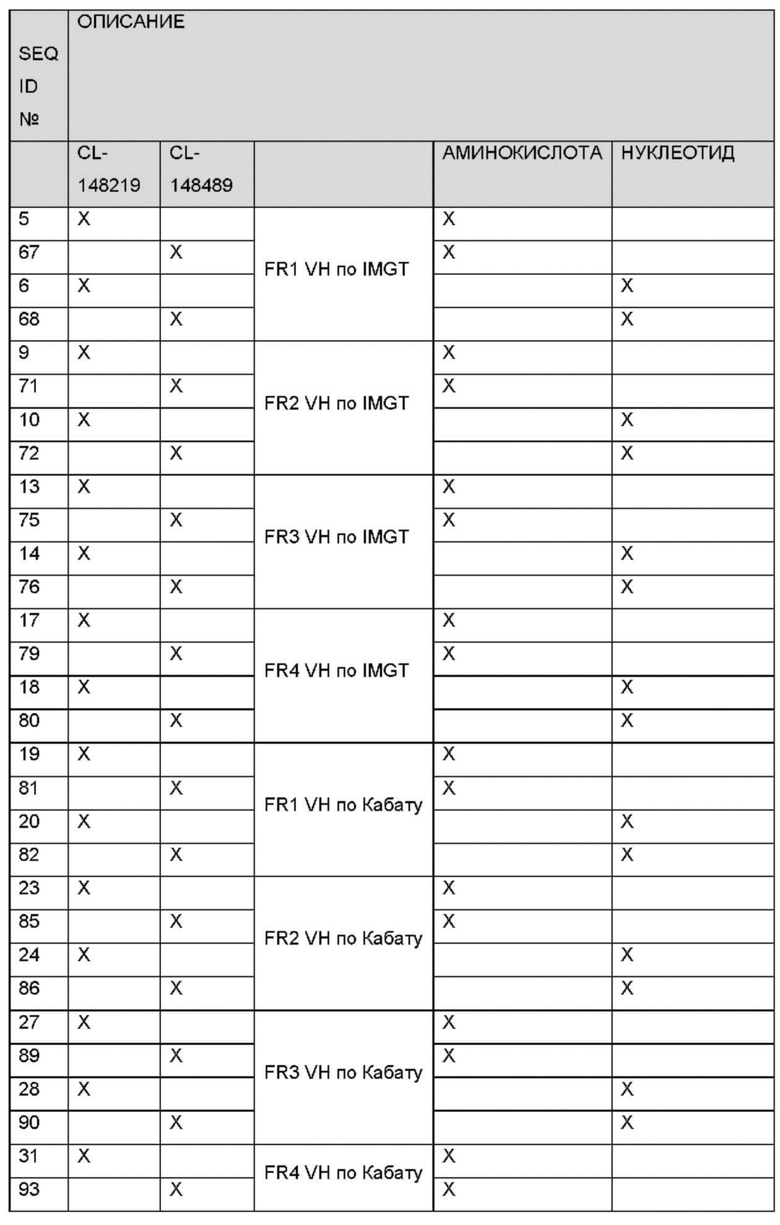
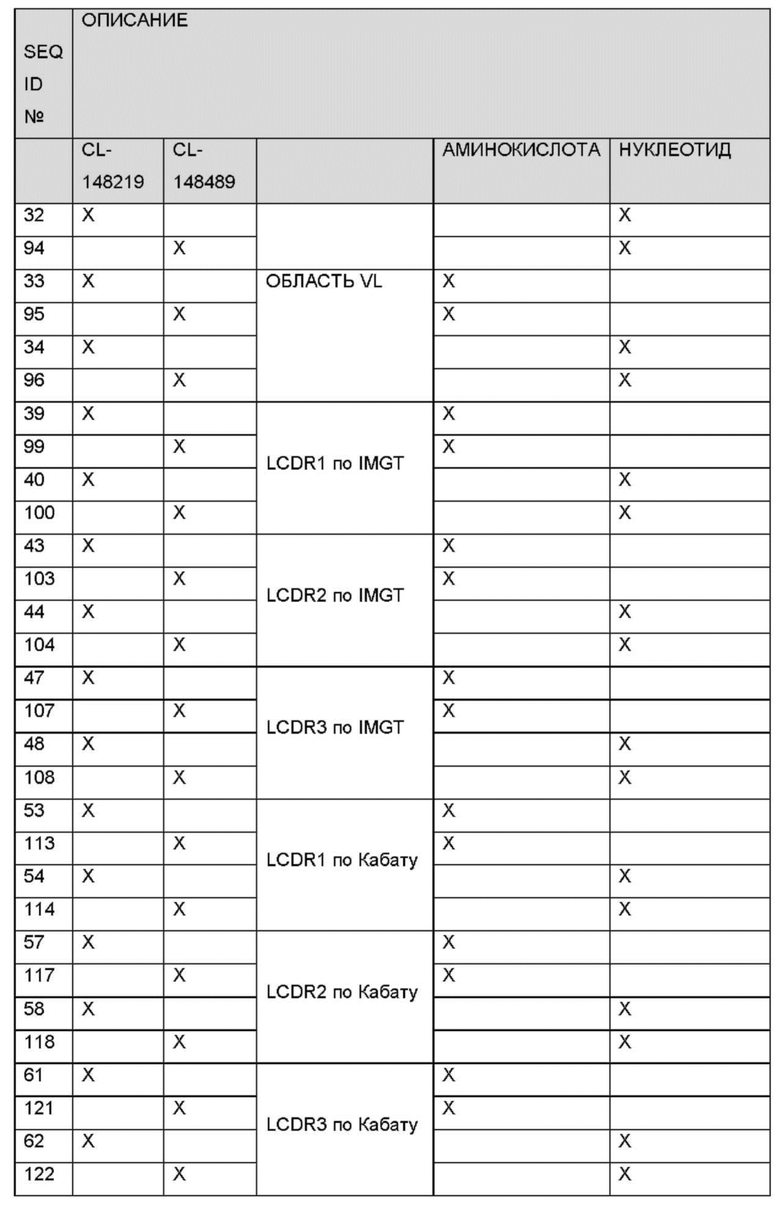
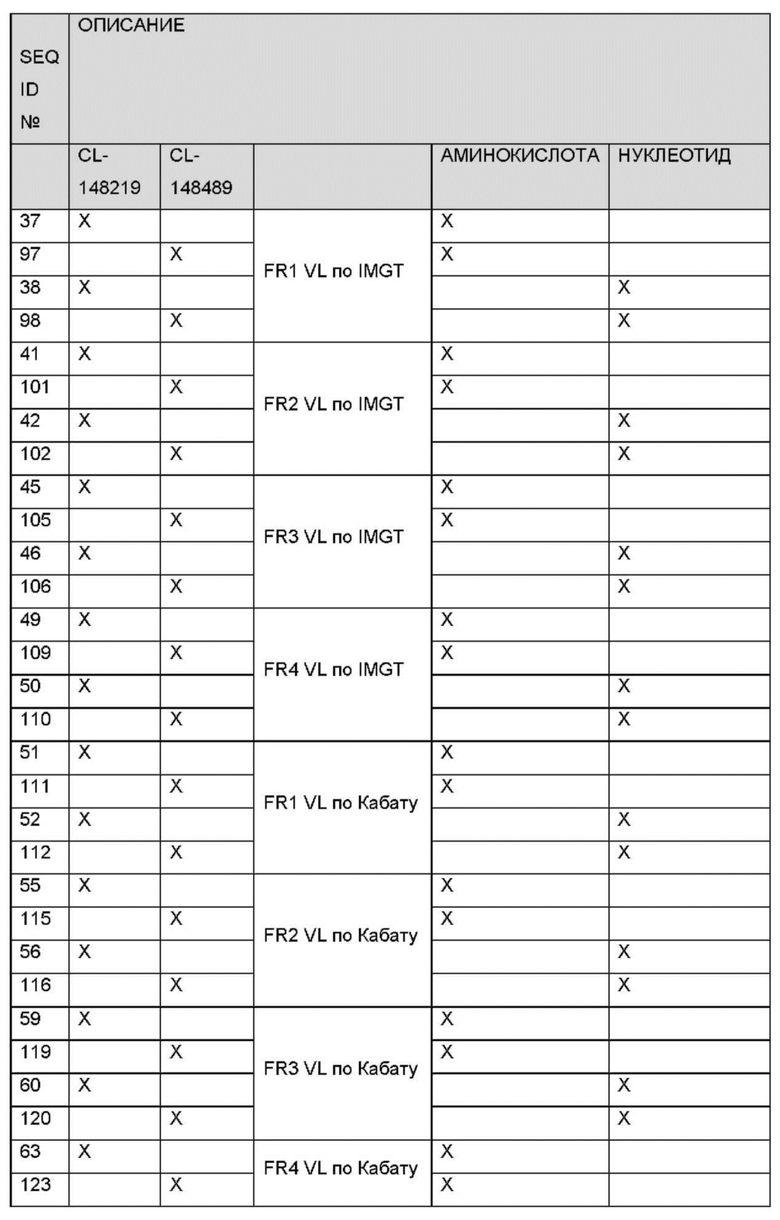
КРАТКИЙ ОБЗОР ПОСЛЕДОВАТЕЛЬНОСТЕЙ КОНСТАНТНОЙ ОБЛАСТИ
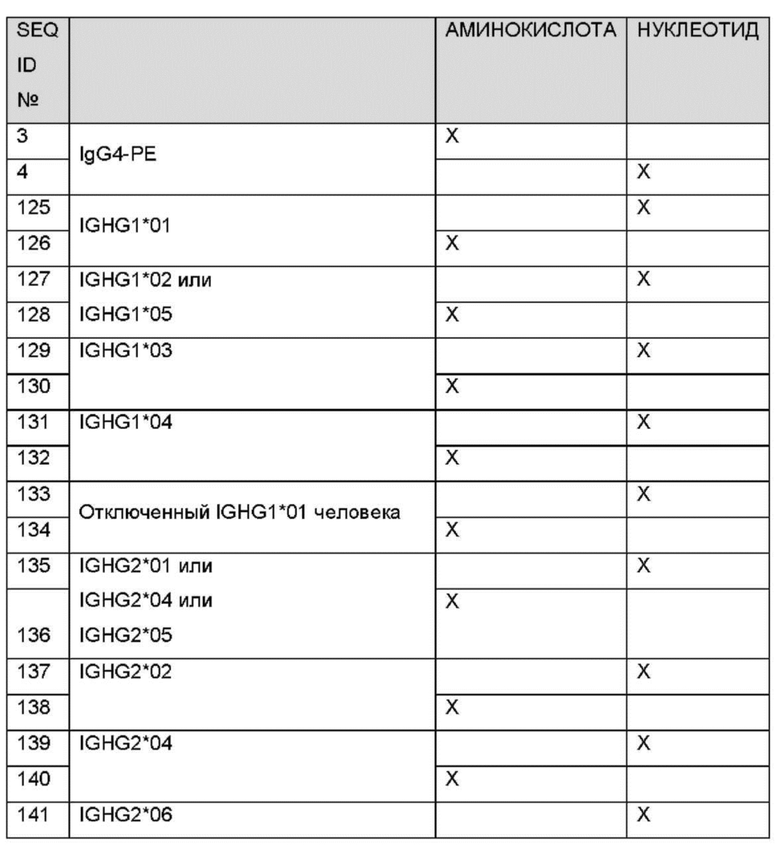
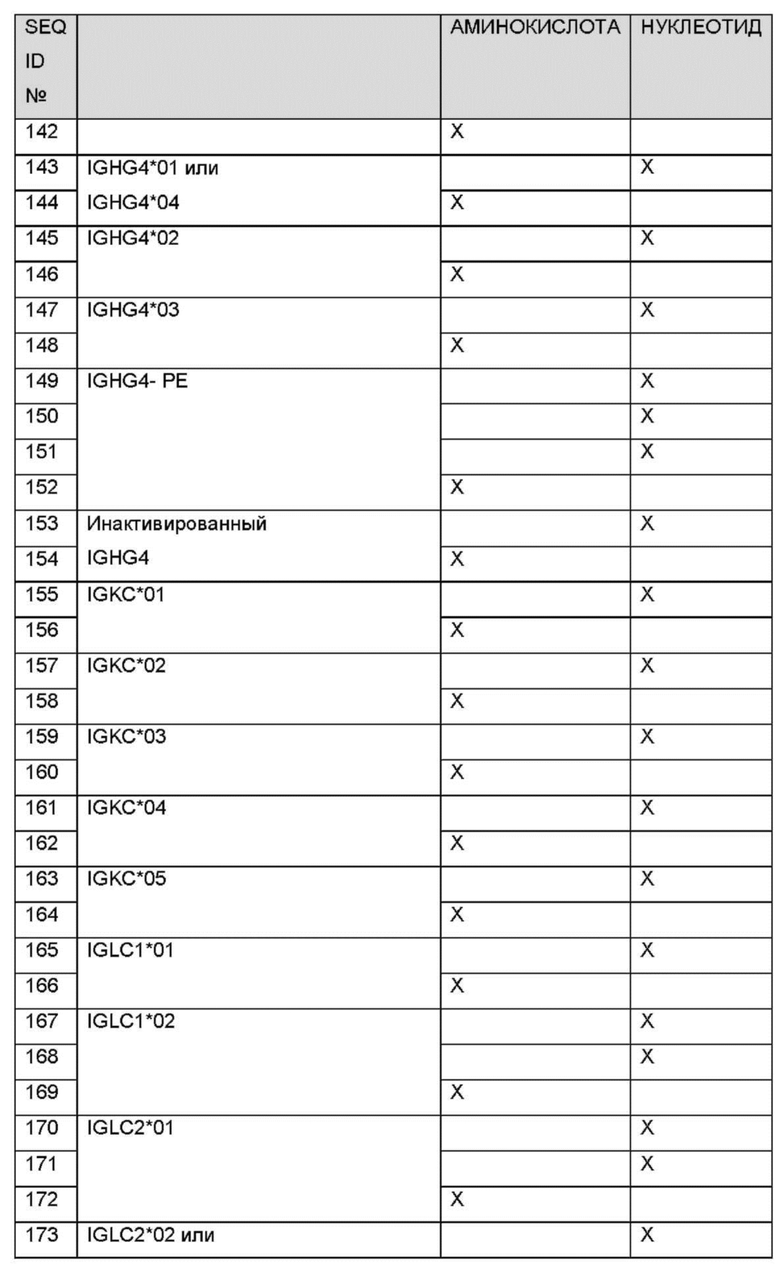
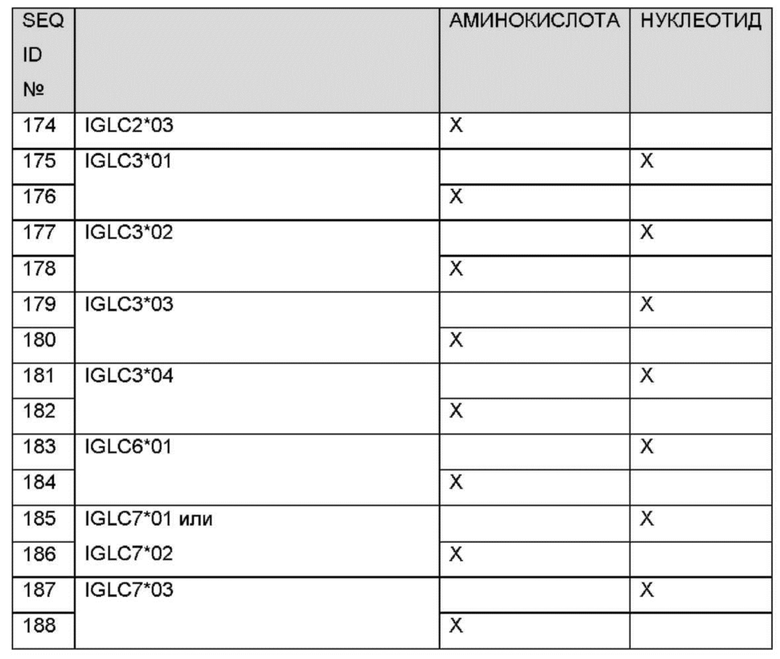




Аминокислотная последовательность FR4 по Кабату (SEQ ID №31)
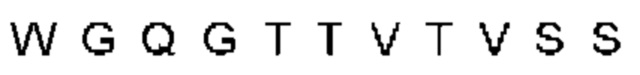
Нуклеотидная последовательность FR4 по Кабату (SEQ ID №32)
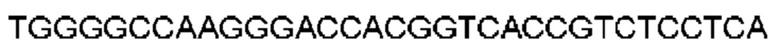
Легкая цепь каппа CL-148219
Аминокислотная последовательность вариабельной области (SEQ ID №33)

Нуклеотидная последовательность вариабельной области (SEQ ID №34)

Аминокислотная последовательность С-области (SEQ ID №35)

Нуклеотидная последовательность С-области (SEQ ID №36)

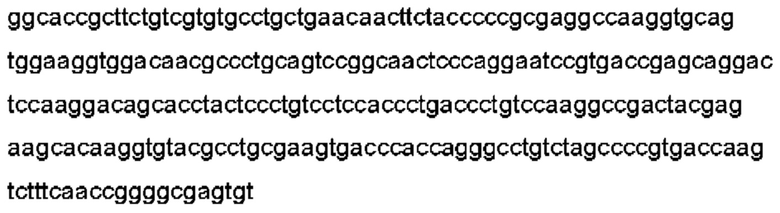
Аминокислотная последовательность FR1 по IMGT (SEQ ID №37)
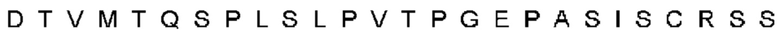
Нуклеотидная последовательность FR1 по IMGT (SEQ ID №38)
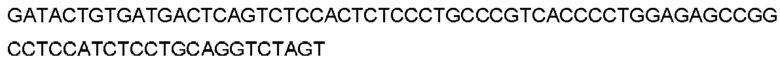
Аминокислотная последовательность CDR1 по IMGT (SEQ ID №39)
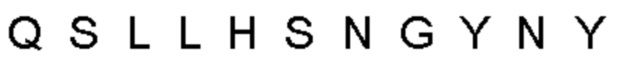
Нуклеотидная последовательность CDR1 по IMGT (SEQ ID №40)
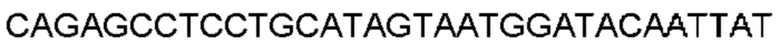
Аминокислотная последовательность FR2 по IMGT (SEQ ID №41)
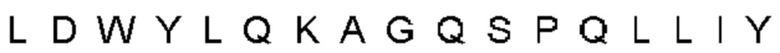
Нуклеотидная последовательность FR2 по IMGT (SEQ ID №42)
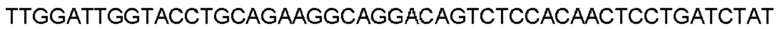
Аминокислотная последовательность CDR2 по IMGT (SEQ ID №43)
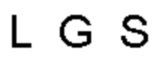
Нуклеотидная последовательность CDR2 по IMGT (SEQ ID №44)
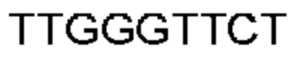
Аминокислотная последовательность FR3 по IMGT (SEQ ID №45)
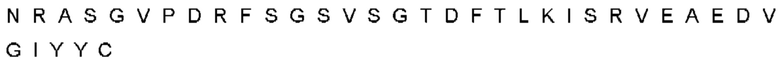
Нуклеотидная последовательность FR3 по IMGT (SEQ ID №46)
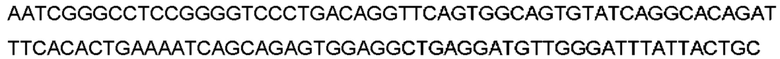
Аминокислотная последовательность CDR3 по IMGT (SEQ ID №47)

Нуклеотидная последовательность CDR3 по IMGT (SEQ ID №48)

Аминокислотная последовательность FR4 по IMGT (SEQ ID №49)

Нуклеотидная последовательность FR4 по IMGT (SEQ ID №50)

Аминокислотная последовательность FR1 по Кабату (SEQ ID №51)
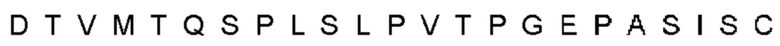
Нуклеотидная последовательность FR1 по Кабату (SEQ ID №52)
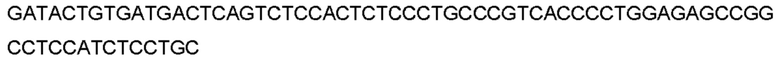
Аминокислотная последовательность CDR1 по Кабату (SEQ ID №53)
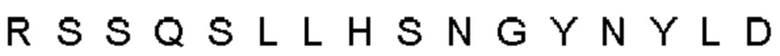
Нуклеотидная последовательность CDR1 по Кабату (SEQ ID №54)

Аминокислотная последовательность FR2 по Кабату (SEQ ID №55)
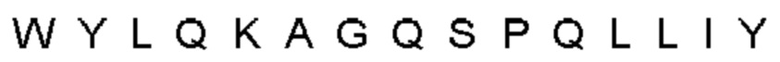
Нуклеотидная последовательность FR2 по Кабату (SEQ ID №56)
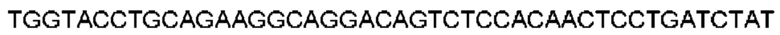
Аминокислотная последовательность CDR2 по Кабату (SEQ ID №57)
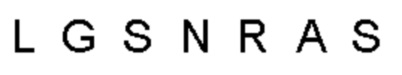
Нуклеотидная последовательность CDR2 по Кабату (SEQ ID №58)

Аминокислотная последовательность FR3 по Кабату (SEQ ID №59)

Нуклеотидная последовательность FR3 по Кабату (SEQ ID №60)
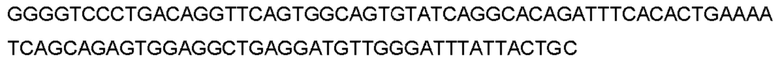
Аминокислотная последовательность CDR3 по Кабату (SEQ ID №61)
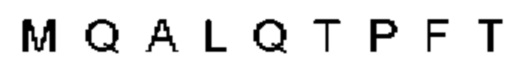
Нуклеотидная последовательность CDR3 по Кабату (SEQ ID №62)
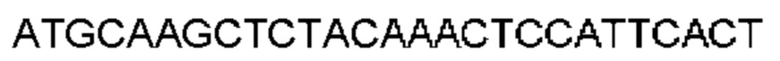
Аминокислотная последовательность FR4 по Кабату (SEQ ID №63)

Нуклеотидная последовательность FR4 по Кабату (SEQ ID №64)
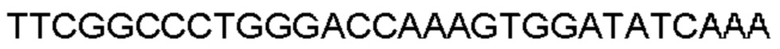
CL-148489
Тяжелая цепь CL-148489
Аминокислотная последовательность вариабельной области (SEQ ID №65)

Нуклеотидная последовательность вариабельной области (SEQ ID №66)

Аминокислотная последовательность FR1 по IMGT (SEQ ID №67)
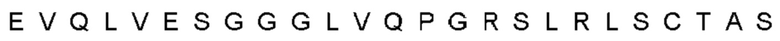
Нуклеотидная последовательность FR1 по IMGT (SEQ ID №68)
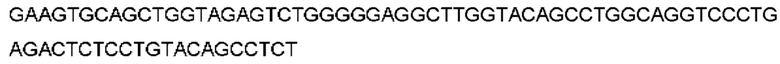
Аминокислотная последовательность CDR1 по IMGT (SEQ ID №69)
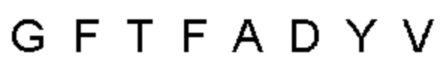
Нуклеотидная последовательность CDR1 по IMGT (SEQ ID №70)
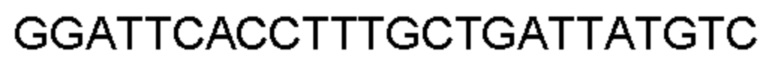
Аминокислотная последовательность FR2 по IMGT (SEQ ID №71)
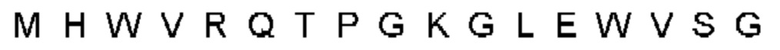
Нуклеотидная последовательность FR2 по IMGT (SEQ ID №72)
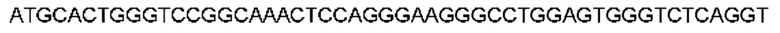
Аминокислотная последовательность CDR2 по IMGT (SEQ ID №73)
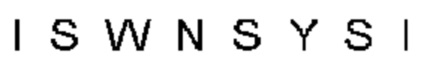
Нуклеотидная последовательность CDR2 по IMGT (SEQ ID №74)

Аминокислотная последовательность FR3 по IMGT (SEQ ID №75)
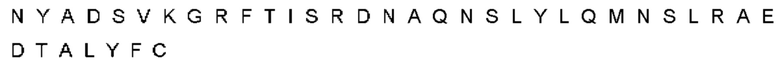
Нуклеотидная последовательность FR3 по IMGT (SEQ ID №76)
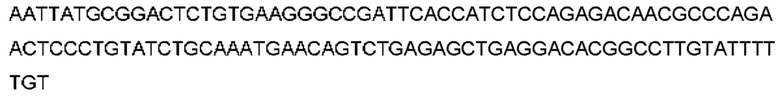
Аминокислотная последовательность CDR3 по IMGT (SEQ ID №77)
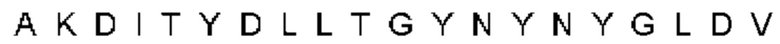
Нуклеотидная последовательность CDR3 по IMGT (SEQ ID №78)
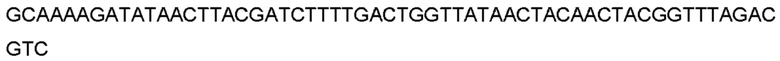
Аминокислотная последовательность FR4 по IMGT (SEQ ID №79)
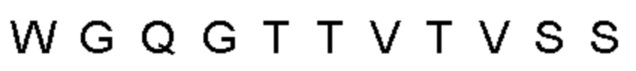
Нуклеотидная последовательность FR4 по IMGT (SEQ ID №80)
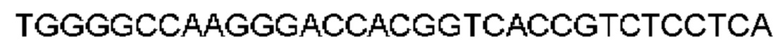
Аминокислотная последовательность FR1 по Кабату (SEQ ID №81)
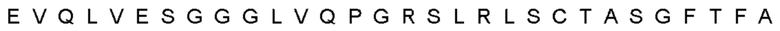
Нуклеотидная последовательность FR1 по Кабату (SEQ ID №82)
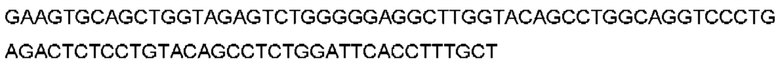
Аминокислотная последовательность CDR1 по Кабату (SEQ ID №83)
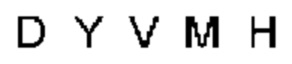
Нуклеотидная последовательность CDR1 по Кабату (SEQ ID №84)

Аминокислотная последовательность FR2 по Кабату (SEQ ID №85)
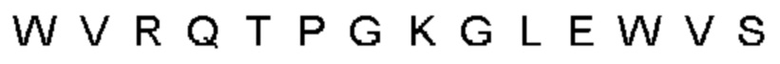
Нуклеотидная последовательность FR2 по Кабату (SEQ ID №86)
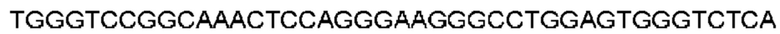
Аминокислотная последовательность CDR2 по Кабату (SEQ ID №87)
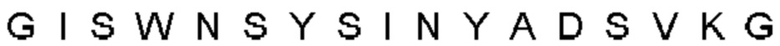
Нуклеотидная последовательность CDR2 по Кабату (SEQ ID №88)

Аминокислотная последовательность FR3 по Кабату (SEQ ID №89)
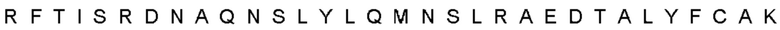
Нуклеотидная последовательность FR3 по Кабату (SEQ ID №90)
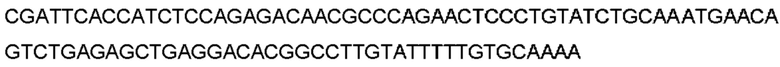
Аминокислотная последовательность CDR3 по Кабату (SEQ ID №91)
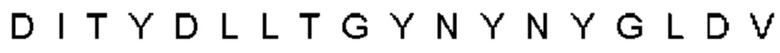
Нуклеотидная последовательность CDR3 по Кабату (SEQ ID №92)

Аминокислотная последовательность FR4 по Кабату (SEQ ID №93)

Нуклеотидная последовательность FR4 по Кабату (SEQ ID №94)
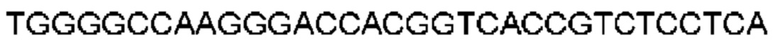
Легкая цепь каппа CL-148489
Аминокислотная последовательность вариабельной области (SEQ ID №95)

Нуклеотидная последовательность вариабельной области (SEQ ID №96)

Аминокислотная последовательность FR1 по IMGT (SEQ ID №97)

Нуклеотидная последовательность FR1 по IMGT (SEQ ID №98)
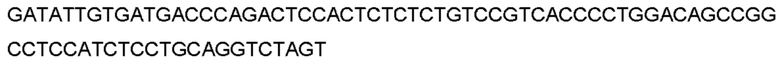
Аминокислотная последовательность CDR1 по IMGT (SEQ ID №99)
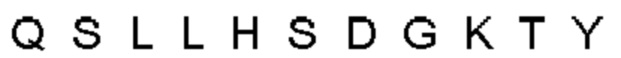
Нуклеотидная последовательность CDR1 по IMGT (SEQ ID №100)
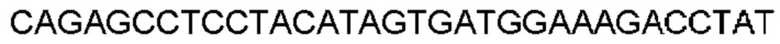
Аминокислотная последовательность FR2 по IMGT (SEQ ID №101)
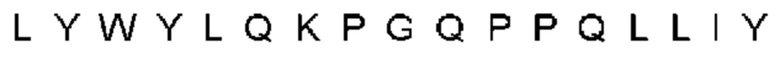
Нуклеотидная последовательность FR2 по IMGT (SEQ ID №102)
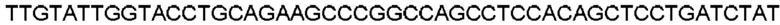
Аминокислотная последовательность CDR2 по IMGT (SEQ ID №103)
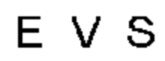
Нуклеотидная последовательность CDR2 по IMGT (SEQ ID №104)

Аминокислотная последовательность FR3 по IMGT (SEQ ID №105)
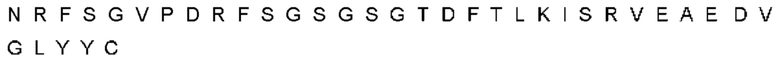
Нуклеотидная последовательность FR3 по IMGT (SEQ ID №106)
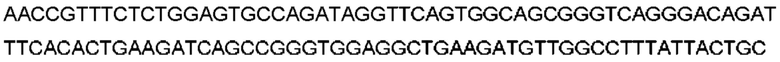
Аминокислотная последовательность CDR3 по IMGT (SEQ ID №107)

Нуклеотидная последовательность CDR3 по IMGT (SEQ ID №108)
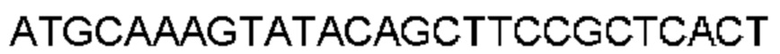
Аминокислотная последовательность FR4 по IMGT (SEQ ID №109)

Нуклеотидная последовательность FR4 по IMGT (SEQ ID №110)

Аминокислотная последовательность FR1 по Кабату (SEQ ID №111)
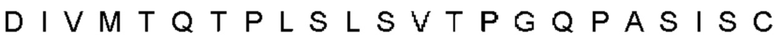
Нуклеотидная последовательность FR1 по Кабату (SEQ ID №112)
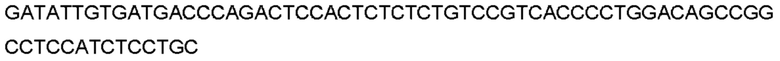
Аминокислотная последовательность CDR1 по Кабату (SEQ ID №113)
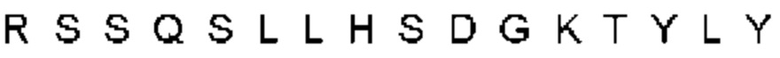
Нуклеотидная последовательность CDR1 по Кабату (SEQ ID №114)

Аминокислотная последовательность FR2 по Кабату (SEQ ID №115)
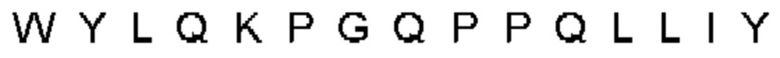
Нуклеотидная последовательность FR2 по Кабату (SEQ ID №116)

Аминокислотная последовательность CDR2 по Кабату (SEQ ID №117)
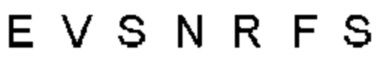
Нуклеотидная последовательность CDR2 по Кабату (SEQ ID №118)
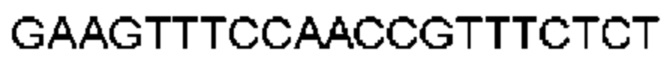
Аминокислотная последовательность FR3 по Кабату (SEQ ID №119)
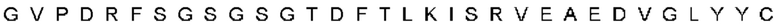
Нуклеотидная последовательность FR3 по Кабату (SEQ ID №120)
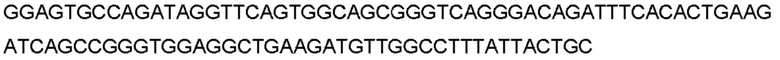
Аминокислотная последовательность CDR3 по Кабату (SEQ ID №121)
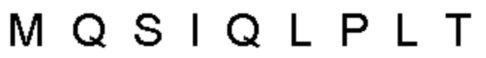
Нуклеотидная последовательность CDR3 по Кабату (SEQ ID №122)

Аминокислотная последовательность FR4 по Кабату (SEQ ID №123)
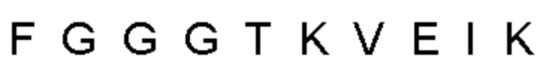
Нуклеотидная последовательность FR4 по Кабату (SEQ ID №124)
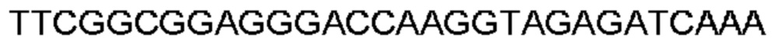
CL-274698
Тяжелая цепь CL-274698
Аминокислотная последовательность вариабельной области (SEQ ID №199)

Нуклеотидная последовательность вариабельной области (SEQ ID №200)

Аминокислотная последовательность FR1 по IMGT (SEQ ID №201)
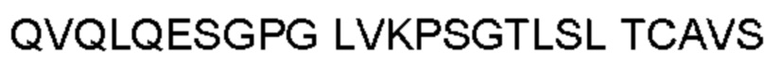
Нуклеотидная последовательность FR1 по IMGT (SEQ ID №202)
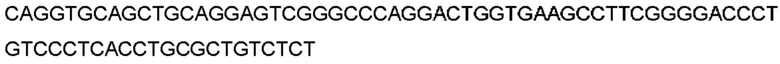
Аминокислотная последовательность CDR1 по IMGT (SEQ ID №203)
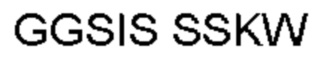
Нуклеотидная последовательность CDR1 по IMGT (SEQ ID №204)
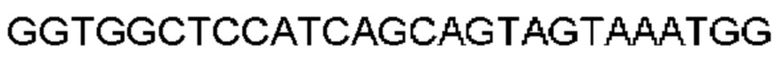
Аминокислотная последовательность FR2 по IMGT (SEQ ID №205)
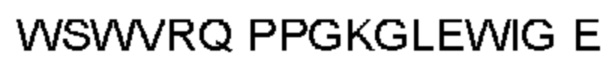
Нуклеотидная последовательность FR2 по IMGT (SEQ ID №206)
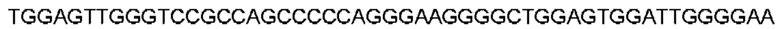
Аминокислотная последовательность CDR2 по IMGT (SEQ ID №207)
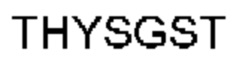
Нуклеотидная последовательность CDR2 по IMGT (SEQ ID №208)

Аминокислотная последовательность FR3 по IMGT (SEQ ID №209)

Нуклеотидная последовательность FR3 по IMGT (SEQ ID №210)
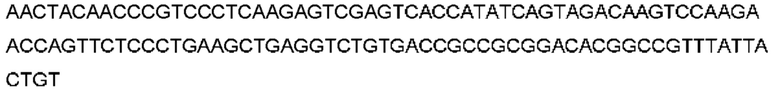
Аминокислотная последовательность CDR3 по IMGT (SEQ ID №211)

Нуклеотидная последовательность CDR3 по IMGT (SEQ ID №212)
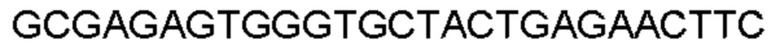
Аминокислотная последовательность FR4 по IMGT (SEQ ID №213)
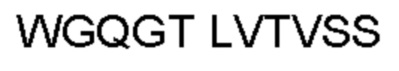
Нуклеотидная последовательность FR4 по IMGT (SEQ ID №214)

Аминокислотная последовательность FR1 по Кабату (SEQ ID №215)
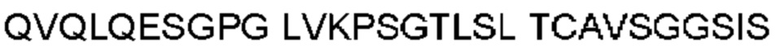
Нуклеотидная последовательность FR1 по Кабату (SEQ ID №216)
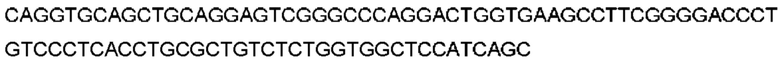
Аминокислотная последовательность CDR1 по Кабату (SEQ ID №217)
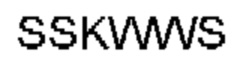
Нуклеотидная последовательность CDR1 по Кабату (SEQ ID №218)

Аминокислотная последовательность FR2 по Кабату (SEQ ID №219)
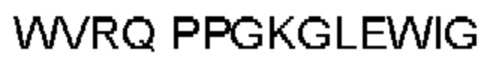
Нуклеотидная последовательность FR2 по Кабату (SEQ ID №220)

Аминокислотная последовательность CDR2 по Кабату (SEQ ID №221)

Нуклеотидная последовательность CDR2 по Кабату (SEQ ID №222)
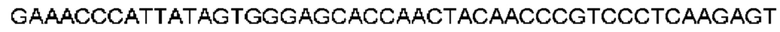
Аминокислотная последовательность FR3 по Кабату (SEQ ID №223)

Нуклеотидная последовательность FR3 по Кабату (SEQ ID №224)

Аминокислотная последовательность CDR3 по Кабату (SEQ ID №225)

Нуклеотидная последовательность CDR3 по Кабату (SEQ ID №226)
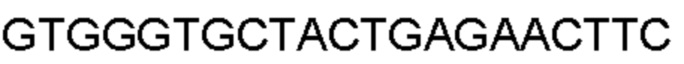
Аминокислотная последовательность FR4 по Кабату (SEQ ID №227)

Нуклеотидная последовательность FR4 по Кабату (SEQ ID №228)

Легкая цепь каппа CL-274698
Аминокислотная последовательность вариабельной области (SEQ ID №229)

Нуклеотидная последовательность вариабельной области (SEQ ID №230)

Аминокислотная последовательность FR1 по IMGT (SEQ ID №231)
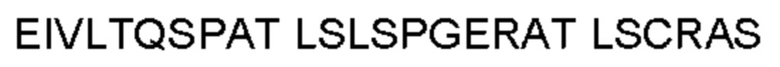
Нуклеотидная последовательность FR1 по IMGT (SEQ ID №232)
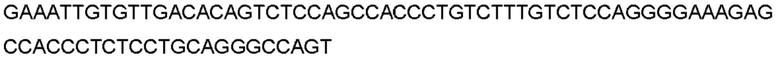
Аминокислотная последовательность CDR1 по IMGT (SEQ ID №233)

Нуклеотидная последовательность CDR1 по IMGT (SEQ ID №234)

Аминокислотная последовательность FR2 по IMGT (SEQ ID №235)
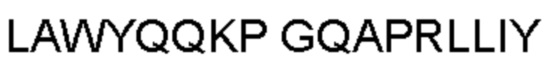
Нуклеотидная последовательность FR2 по IMGT (SEQ ID №236)
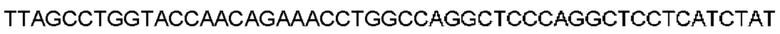 Аминокислотная последовательность CDR2 по IMGT (SEQ ID №237)
Аминокислотная последовательность CDR2 по IMGT (SEQ ID №237)
Нуклеотидная последовательность CDR2 по IMGT (SEQ ID №238)
Аминокислотная последовательность FR3 по IMGT (SEQ ID №239)
Нуклеотидная последовательность FR3 по IMGT (SEQ ID №240)
Аминокислотная последовательность CDR3 по IMGT (SEQ ID №241)

Нуклеотидная последовательность CDR3 по IMGT (SEQ ID №242)
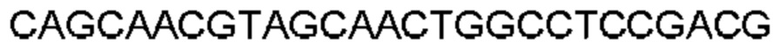
Аминокислотная последовательность FR4 по IMGT (SEQ ID №243)

Нуклеотидная последовательность FR4 по IMGT (SEQ ID №244)
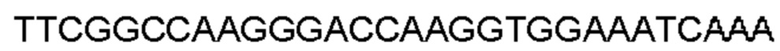
Аминокислотная последовательность FR1 по Кабату (SEQ ID №245)
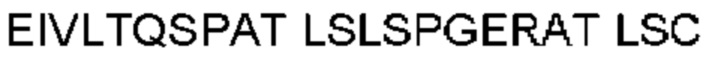
Нуклеотидная последовательность FR1 по Кабату (SEQ ID №246)
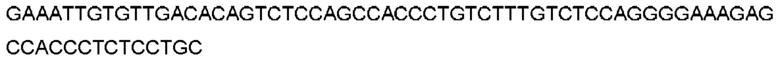
Аминокислотная последовательность CDR1 по Кабату (SEQ ID №247)

Нуклеотидная последовательность CDR1 по Кабату (SEQ ID №248)

Аминокислотная последовательность FR2 по Кабату (SEQ ID №249)

Нуклеотидная последовательность FR2 по Кабату (SEQ ID №250)

Аминокислотная последовательность CDR2 по Кабату (SEQ ID №251)

Нуклеотидная последовательность CDR2 по Кабату (SEQ ID №252)
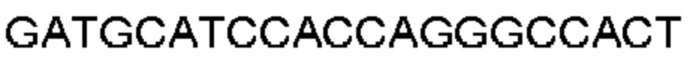
Аминокислотная последовательность FR3 по Кабату (SEQ ID №253)

Нуклеотидная последовательность FR3 по Кабату (SEQ ID №254)
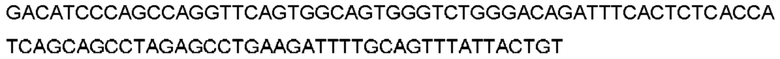
Аминокислотная последовательность CDR3 по Кабату (SEQ ID №255)

Нуклеотидная последовательность CDR3 по Кабату (SEQ ID №256)
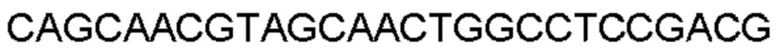
Аминокислотная последовательность FR4 по Кабату (SEQ ID №257)

Нуклеотидная последовательность FR4 по Кабату (SEQ ID №258)

CL-274711
Тяжелая цепь CL-274711
Аминокислотная последовательность вариабельной области (SEQ ID №259)

Нуклеотидная последовательность вариабельной области (SEQ ID №260)

Аминокислотная последовательность FR1 по IMGT (SEQ ID №261)
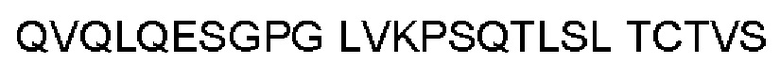
Нуклеотидная последовательность FR1 по IMGT (SEQ ID №262)
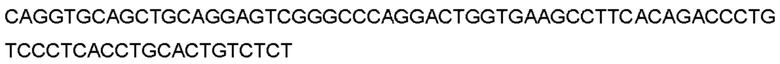
Аминокислотная последовательность CDR1 по IMGT (SEQ ID №263)
Нуклеотидная последовательность CDR1 по IMGT (SEQ ID №264)
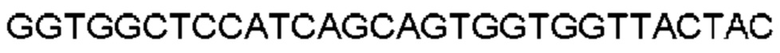
Аминокислотная последовательность FR2 по IMGT (SEQ ID №265)
Нуклеотидная последовательность FR2 по IMGT (SEQ ID №266)
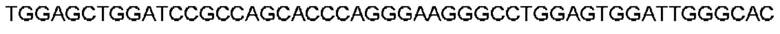
Аминокислотная последовательность CDR2 по IMGT (SEQ ID №267)

Нуклеотидная последовательность CDR2 по IMGT (SEQ ID №268)
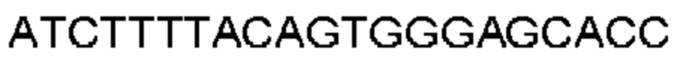
Аминокислотная последовательность FR3 по IMGT (SEQ ID №269)

Нуклеотидная последовательность FR3 по IMGT (SEQ ID №270)
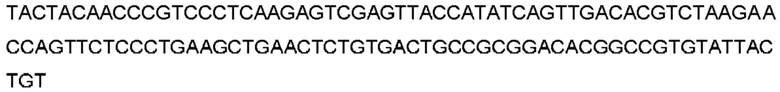
Аминокислотная последовательность CDR3 по IMGT (SEQ ID №271)
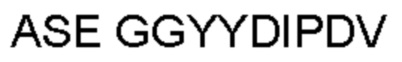
Нуклеотидная последовательность CDR3 по IMGT (SEQ ID №272)

Аминокислотная последовательность FR4 по IMGT (SEQ ID №273)

Нуклеотидная последовательность FR4 по IMGT (SEQ ID №274)
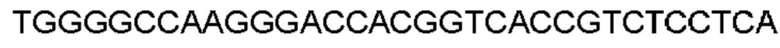
Аминокислотная последовательность FR1 по Кабату (SEQ ID №275)
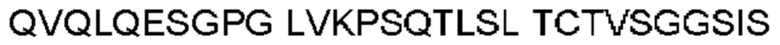
Нуклеотидная последовательность FR1 по Кабату (SEQ ID №276)
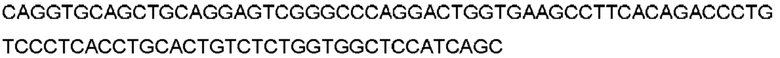
Аминокислотная последовательность CDR1 по Кабату (SEQ ID №277)
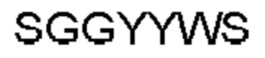
Нуклеотидная последовательность CDR1 по Кабату (SEQ ID №278)

Аминокислотная последовательность FR2 по Кабату (SEQ ID №279)
Нуклеотидная последовательность FR2 по Кабату (SEQ ID №280)
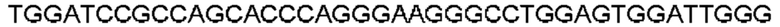
Аминокислотная последовательность CDR2 по Кабату (SEQ ID №281)

Нуклеотидная последовательность CDR2 по Кабату (SEQ ID №282)
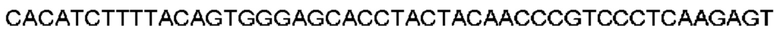
Аминокислотная последовательность FR3 по Кабату (SEQ ID №283)

Нуклеотидная последовательность FR3 по Кабату (SEQ ID №284)

Аминокислотная последовательность CDR3 по Кабату (SEQ ID №285)

Нуклеотидная последовательность CDR3 по Кабату (SEQ ID №286)
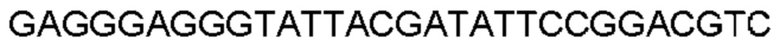
Аминокислотная последовательность FR4 по Кабату (SEQ ID №287)

Нуклеотидная последовательность FR4 по Кабату (SEQ ID №288)
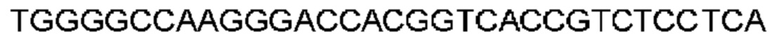
Легкая цепь каппа CL-274711
Аминокислотная последовательность вариабельной области (SEQ ID №289)

Нуклеотидная последовательность вариабельной области (SEQ ID №290)

Аминокислотная последовательность FR1 по IMGT (SEQ ID №291)
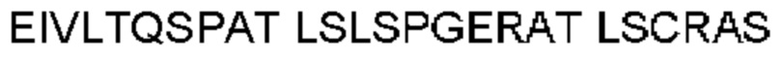
Нуклеотидная последовательность FR1 по IMGT (SEQ ID №292)
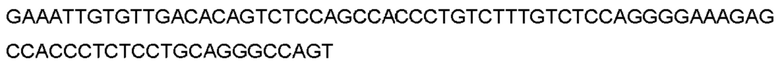
Аминокислотная последовательность CDR1 по IMGT (SEQ ID №293)
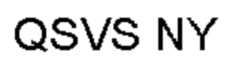
Нуклеотидная последовательность CDR1 по IMGT (SEQ ID №294)

Аминокислотная последовательность FR2 по IMGT (SEQ ID №295)
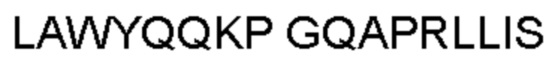
Нуклеотидная последовательность FR2 по IMGT (SEQ ID №236)
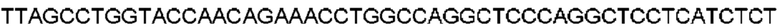
Аминокислотная последовательность CDR2 по IMGT (SEQ ID №297)
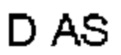
Нуклеотидная последовательность CDR2 по IMGT (SEQ ID №298)
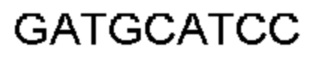
Аминокислотная последовательность FR3 по IMGT (SEQ ID №299)
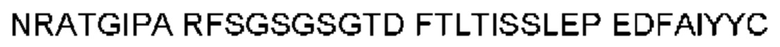
Нуклеотидная последовательность FR3 по IMGT (SEQ ID №300)
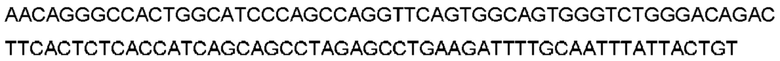
Аминокислотная последовательность CDR3 по IMGT (SEQ ID №301)

Нуклеотидная последовательность CDR3 по IMGT (SEQ ID №302)
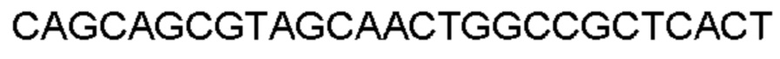
Аминокислотная последовательность FR4 по IMGT (SEQ ID №303)

Нуклеотидная последовательность FR4 по IMGT (SEQ ID №304)

Аминокислотная последовательность FR1 по Кабату (SEQ ID №305)
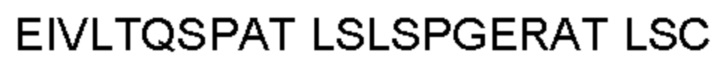
Нуклеотидная последовательность FR1 по Кабату (SEQ ID №306)
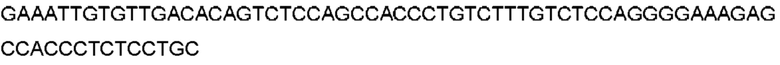
Аминокислотная последовательность CDR1 по Кабату (SEQ ID №307)
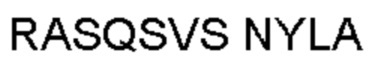
Нуклеотидная последовательность CDR1 по Кабату (SEQ ID №308)

Аминокислотная последовательность FR2 по Кабату (SEQ ID №309)

Нуклеотидная последовательность FR2 по Кабату (SEQ ID №310)
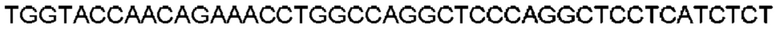
Аминокислотная последовательность CDR2 по Кабату (SEQ ID №311)

Нуклеотидная последовательность CDR2 по Кабату (SEQ ID №312)
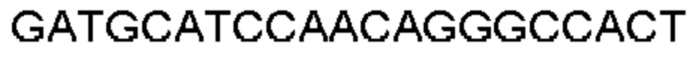
Аминокислотная последовательность FR3 по Кабату (SEQ ID №313)

Нуклеотидная последовательность FR3 по Кабату (SEQ ID №314)
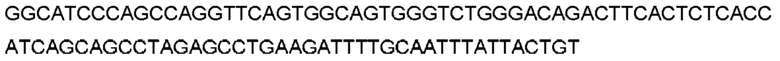
Аминокислотная последовательность CDR3 по Кабату (SEQ ID №315)
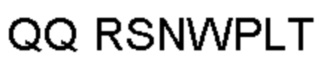
Нуклеотидная последовательность CDR3 по Кабату (SEQ ID №316)
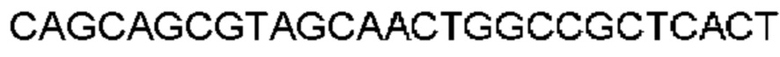
Аминокислотная последовательность FR4 по Кабату (SEQ ID №317)

Нуклеотидная последовательность FR4 по Кабату (SEQ ID №318)

CL-148219QLT
Тяжелая цепь CL-148219QLT
Аминокислотная последовательность вариабельной области (SEQ ID №319)

Нуклеотидная последовательность вариабельной области (SEQ ID №320)

Аминокислотная последовательность FR1 по IMGT (SEQ ID №321)
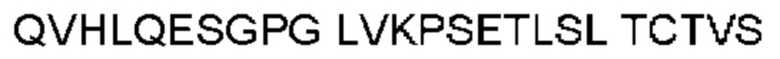
Нуклеотидная последовательность FR1 по IMGT (SEQ ID №322)
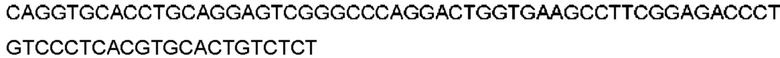
Аминокислотная последовательность CDR1 по IMGT (SEQ ID №323)

Нуклеотидная последовательность CDR1 по IMGT (SEQ ID №324

Аминокислотная последовательность FR2 по IMGT (SEQ ID №325)
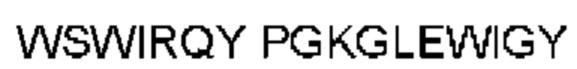
Нуклеотидная последовательность FR2 по IMGT (SEQ ID №326)
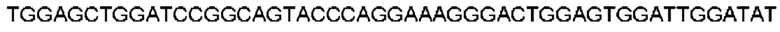
Аминокислотная последовательность CDR2 по IMGT (SEQ ID №327)
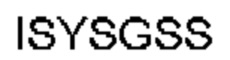
Нуклеотидная последовательность CDR2 по IMGT (SEQ ID №328)
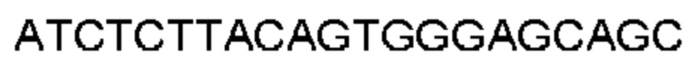
Аминокислотная последовательность FR3 по IMGT (SEQ ID №329)

Нуклеотидная последовательность FR3 по IMGT (SEQ ID №330)
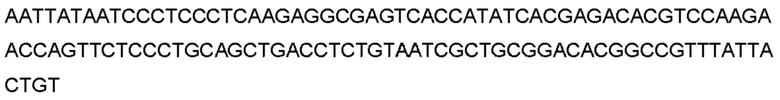
Аминокислотная последовательность CDR3 по IMGT (SEQ ID №331)
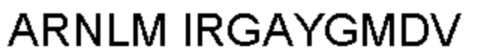
Нуклеотидная последовательность CDR3 по IMGT (SEQ ID №332)
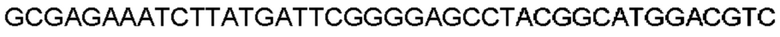
Аминокислотная последовательность FR4 по IMGT (SEQ ID №333)

Нуклеотидная последовательность FR4 по IMGT (SEQ ID №334)
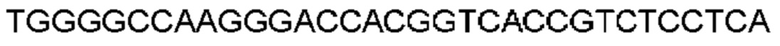
Аминокислотная последовательность FR1 по Кабату (SEQ ID №335)

Нуклеотидная последовательность FR1 по Кабату (SEQ ID №336)
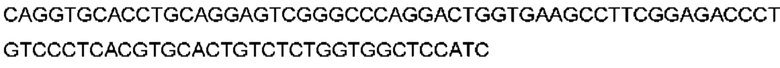
Аминокислотная последовательность CDR1 по Кабату (SEQ ID №337)
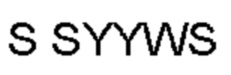
Нуклеотидная последовательность CDR1 по Кабату (SEQ ID №338)
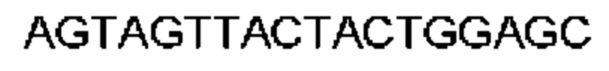
Аминокислотная последовательность FR2 по Кабату (SEQ ID №339)
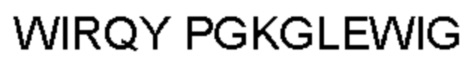
Нуклеотидная последовательность FR2 по Кабату (SEQ ID №340)
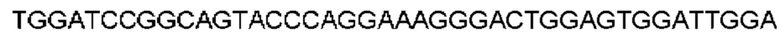
Аминокислотная последовательность CDR2 по Кабату (SEQ ID №341)

Нуклеотидная последовательность CDR2 по Кабату (SEQ ID №342)

Аминокислотная последовательность FR3 по Кабату (SEQ ID №343)
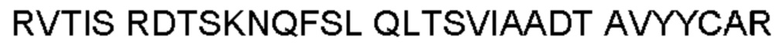
Нуклеотидная последовательность FR3 по Кабату (SEQ ID №344)

Аминокислотная последовательность CDR3 по Кабату (SEQ ID №345)

Нуклеотидная последовательность CDR3 по Кабату (SEQ ID №346)
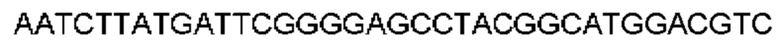
Аминокислотная последовательность FR4 по Кабату (SEQ ID №347)\

Нуклеотидная последовательность FR4 по Кабату (SEQ ID №348)
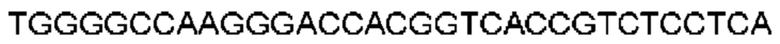
Легкая цепь каппа CL-148219QLT
Аминокислотная последовательность вариабельной области (SEQ ID №349)

Нуклеотидная последовательность вариабельной области (SEQ ID №350)

Аминокислотная последовательность FR1 по IMGT (SEQ ID №351)

Нуклеотидная последовательность FR1 по IMGT (SEQ ID №352)
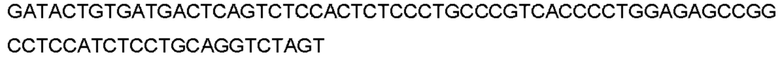
Аминокислотная последовательность CDR1 по IMGT (SEQ ID №353)
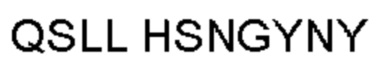
Нуклеотидная последовательность CDR1 по IMGT (SEQ ID №354)
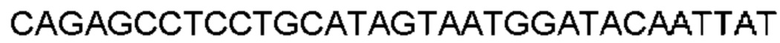
Аминокислотная последовательность FR2 по IMGT (SEQ ID №355)

Нуклеотидная последовательность FR2 по IMGT (SEQ ID №356)
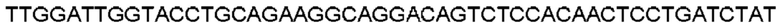
Аминокислотная последовательность CDR2 по IMGT (SEQ ID №357)
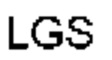
Нуклеотидная последовательность CDR2 по IMGT (SEQ ID №358)

Аминокислотная последовательность FR3 по IMGT (SEQ ID №359)

Нуклеотидная последовательность FR3 по IMGT (SEQ ID №360)
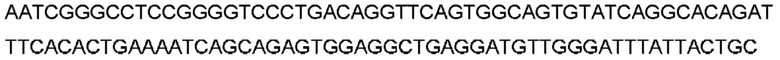
Аминокислотная последовательность CDR3 по IMGT (SEQ ID №361)
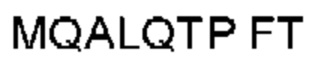
Нуклеотидная последовательность CDR3 по IMGT (SEQ ID №362)
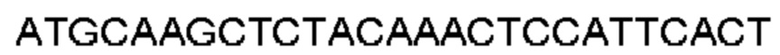
Аминокислотная последовательность FR4 по IMGT (SEQ ID №363)

Нуклеотидная последовательность FR4 по IMGT (SEQ ID №364)

Аминокислотная последовательность FR1 по Кабату (SEQ ID №365)
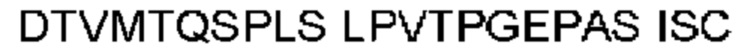
Нуклеотидная последовательность FR1 по Кабату (SEQ ID №366)
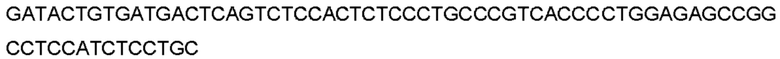
Аминокислотная последовательность CDR1 по Кабату (SEQ ID №367)

Нуклеотидная последовательность CDR1 по Кабату (SEQ ID №368)

Аминокислотная последовательность FR2 по Кабату (SEQ ID №369)

Нуклеотидная последовательность FR2 по Кабату (SEQ ID №370)

Аминокислотная последовательность CDR2 по Кабату (SEQ ID №371)

Нуклеотидная последовательность CDR2 по Кабату (SEQ ID №372)

Аминокислотная последовательность FR3 по Кабату (SEQ ID №373)

Нуклеотидная последовательность FR3 по Кабату (SEQ ID №374)
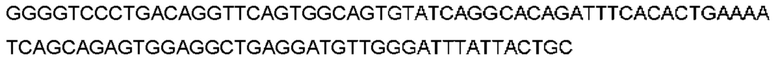
Аминокислотная последовательность CDR3 по Кабату (SEQ ID №375)
Нуклеотидная последовательность CDR3 по Кабату (SEQ ID №376)

Аминокислотная последовательность FR4 по Кабату (SEQ ID №377)

Нуклеотидная последовательность FR4 по Кабату (SEQ ID №378)

Константные области для антител и фрагментов по изобретению





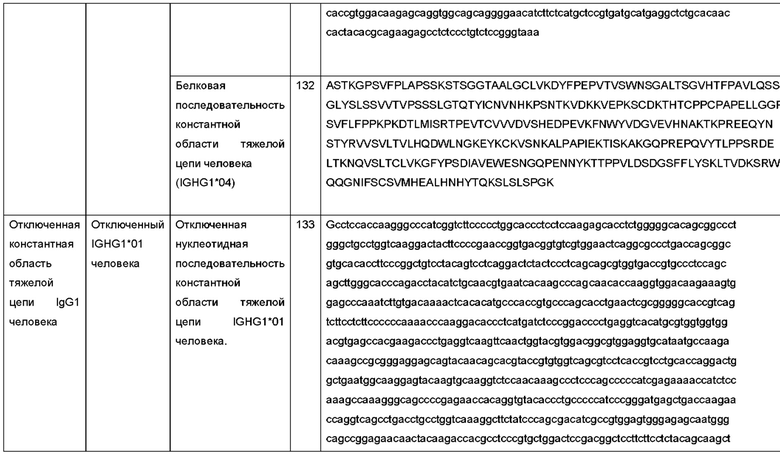




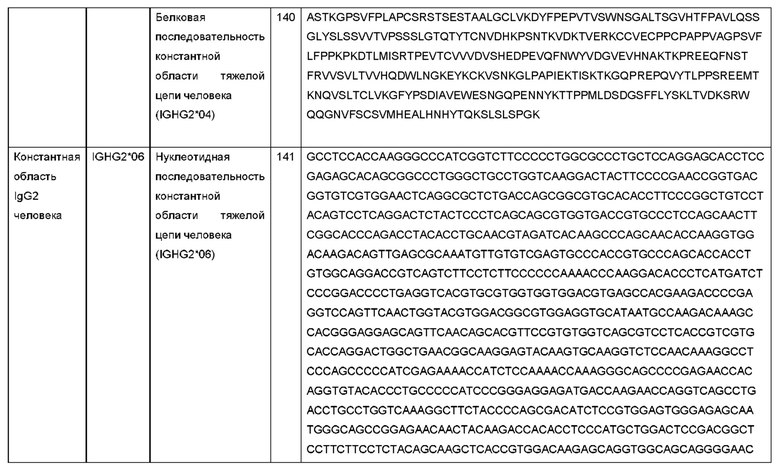









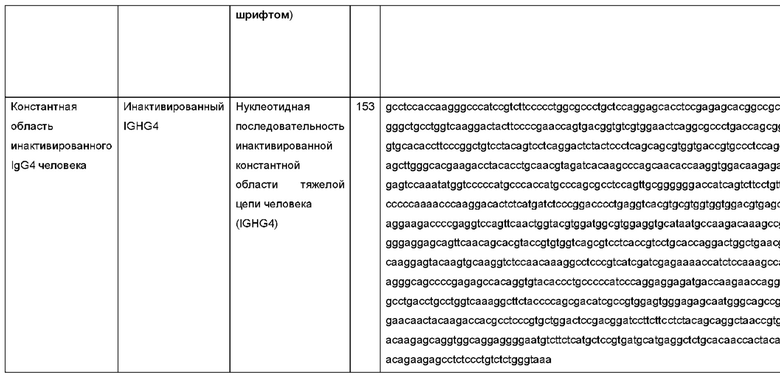




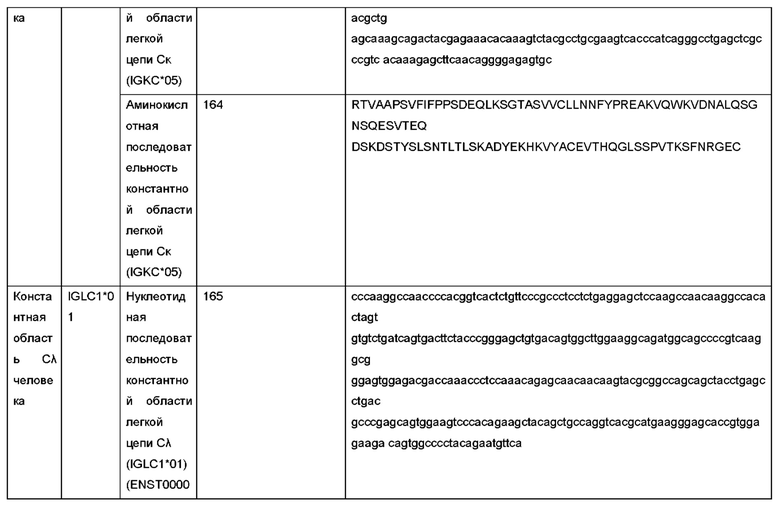

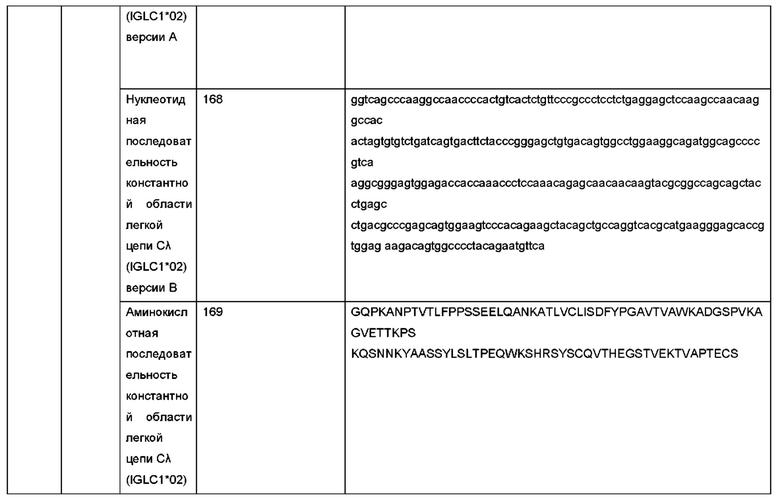







Аминокислотная последовательность С-области (SEQ ID №3)

Нуклеотидная последовательность С-области (SEQ ID №4)

>Контрольная последовательность PCSK9 (SEQ ID №189)

>Вариант a PCSK9 (SEQ ID №190)


>Вариант b PCSK9 (SEQ ID №191)

>Мутантный вариант PCSK9 GOF (SEQ ID №192)

>PCSK9 яванского макака (SEQ ID №193)


>PCSK9 мыши (SEQ ID №194)

Алирокумаб НС (lgG4 человека) (SEQ ID №195)
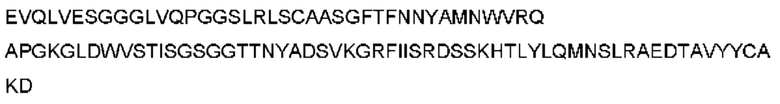

Алирокумаб LC (каппа человека) (SEQ ID №196)

рН-зависимое антитело НС (lqG4 человека) (SEQ ID №197)

рН-зависимое антитело LC (каппа человека) (SEQ ID №198)

--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> KYMAB LIMITED
<120> АНТАГОНИСТЫ
<130> KYMBN/P71233PC
<140> PCT/GB2019/053607
<141> 2019-12-18
<150> GB1820687.0
<151> 2018-12-19
<160> 378
<170> PatentIn версии 3.5
<210> 1
<211> 120
<212> Белок
<213> Homo Sapien
<400> 1
Gln Val His Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Tyr Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Ser Tyr Ser Gly Ser Ser Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Arg Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Asn Leu Thr Ser Val Ile Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Asn Leu Met Ile Arg Gly Ala Tyr Gly Met Asp Val Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 2
<211> 360
<212> ДНК
<213> Homo Sapien
<400> 2
caggtgcacc tgcaggagtc gggcccagga ctggtgaagc cttcggagac cctgtccctc 60
acgtgcactg tctctggtgg ctccatcagt agttactact ggagctggat ccggcagtac 120
ccaggaaagg gactggagtg gattggatat atctcttaca gtgggagcag caattataat 180
ccctccctca agaggcgagt caccatatca cgagacacgt ccaagaacca gttctccctg 240
aatctgacct ctgtaatcgc tgcggacacg gccgtttatt actgtgcgag aaatcttatg 300
attcggggag cctacggcat ggacgtctgg ggccaaggga ccacggtcac cgtctcctca 360
<210> 3
<211> 327
<212> Белок
<213> Homo Sapien
<400> 3
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro
100 105 110
Glu Phe Glu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
115 120 125
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
130 135 140
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
145 150 155 160
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
165 170 175
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
180 185 190
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
195 200 205
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
210 215 220
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
225 230 235 240
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
245 250 255
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
260 265 270
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
275 280 285
Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
290 295 300
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
305 310 315 320
Leu Ser Leu Ser Leu Gly Lys
325
<210> 4
<211> 981
<212> ДНК
<213> Homo Sapien
<400> 4
gccagcacca agggcccttc cgtgttcccc ctggcccctt gcagcaggag cacctccgaa 60
tccacagctg ccctgggctg tctggtgaag gactactttc ccgagcccgt gaccgtgagc 120
tggaacagcg gcgctctgac atccggcgtc cacacctttc ctgccgtcct gcagtcctcc 180
ggcctctact ccctgtcctc cgtggtgacc gtgcctagct cctccctcgg caccaagacc 240
tacacctgta acgtggacca caaaccctcc aacaccaagg tggacaaacg ggtcgagagc 300
aagtacggcc ctccctgccc tccttgtcct gcccccgagt tcgaaggcgg acccagcgtg 360
ttcctgttcc ctcctaagcc caaggacacc ctcatgatca gccggacacc cgaggtgacc 420
tgcgtggtgg tggatgtgag ccaggaggac cctgaggtcc agttcaactg gtatgtggat 480
ggcgtggagg tgcacaacgc caagacaaag ccccgggaag agcagttcaa ctccacctac 540
agggtggtca gcgtgctgac cgtgctgcat caggactggc tgaacggcaa ggagtacaag 600
tgcaaggtca gcaataaggg actgcccagc agcatcgaga agaccatctc caaggctaaa 660
ggccagcccc gggaacctca ggtgtacacc ctgcctccca gccaggagga gatgaccaag 720
aaccaggtga gcctgacctg cctggtgaag ggattctacc cttccgacat cgccgtggag 780
tgggagtcca acggccagcc cgagaacaat tataagacca cccctcccgt cctcgacagc 840
gacggatcct tctttctgta ctccaggctg accgtggata agtccaggtg gcaggaaggc 900
aacgtgttca gctgctccgt gatgcacgag gccctgcaca atcactacac ccagaagtcc 960
ctgagcctgt ccctgggaaa g 981
<210> 5
<211> 25
<212> Белок
<213> Homo Sapien
<400> 5
Gln Val His Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser
20 25
<210> 6
<211> 75
<212> ДНК
<213> Homo Sapien
<400> 6
caggtgcacc tgcaggagtc gggcccagga ctggtgaagc cttcggagac cctgtccctc 60
acgtgcactg tctct 75
<210> 7
<211> 8
<212> Белок
<213> Homo Sapien
<400> 7
Gly Gly Ser Ile Ser Ser Tyr Tyr
1 5
<210> 8
<211> 24
<212> ДНК
<213> Homo Sapien
<400> 8
ggtggctcca tcagtagtta ctac 24
<210> 9
<211> 17
<212> Белок
<213> Homo Sapien
<400> 9
Trp Ser Trp Ile Arg Gln Tyr Pro Gly Lys Gly Leu Glu Trp Ile Gly
1 5 10 15
Tyr
<210> 10
<211> 51
<212> ДНК
<213> Homo Sapien
<400> 10
tggagctgga tccggcagta cccaggaaag ggactggagt ggattggata t 51
<210> 11
<211> 7
<212> Белок
<213> Homo Sapien
<400> 11
Ile Ser Tyr Ser Gly Ser Ser
1 5
<210> 12
<211> 21
<212> ДНК
<213> Homo Sapien
<400> 12
atctcttaca gtgggagcag c 21
<210> 13
<211> 38
<212> Белок
<213> Homo Sapien
<400> 13
Asn Tyr Asn Pro Ser Leu Lys Arg Arg Val Thr Ile Ser Arg Asp Thr
1 5 10 15
Ser Lys Asn Gln Phe Ser Leu Asn Leu Thr Ser Val Ile Ala Ala Asp
20 25 30
Thr Ala Val Tyr Tyr Cys
35
<210> 14
<211> 114
<212> ДНК
<213> Homo Sapien
<400> 14
aattataatc cctccctcaa gaggcgagtc accatatcac gagacacgtc caagaaccag 60
ttctccctga atctgacctc tgtaatcgct gcggacacgg ccgtttatta ctgt 114
<210> 15
<211> 14
<212> Белок
<213> Homo Sapien
<400> 15
Ala Arg Asn Leu Met Ile Arg Gly Ala Tyr Gly Met Asp Val
1 5 10
<210> 16
<211> 42
<212> ДНК
<213> Homo Sapien
<400> 16
gcgagaaatc ttatgattcg gggagcctac ggcatggacg tc 42
<210> 17
<211> 11
<212> Белок
<213> Homo Sapien
<400> 17
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
1 5 10
<210> 18
<211> 33
<212> ДНК
<213> Homo Sapien
<400> 18
tggggccaag ggaccacggt caccgtctcc tca 33
<210> 19
<211> 30
<212> Белок
<213> Homo Sapien
<400> 19
Gln Val His Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser
20 25 30
<210> 20
<211> 90
<212> ДНК
<213> Homo Sapien
<400> 20
caggtgcacc tgcaggagtc gggcccagga ctggtgaagc cttcggagac cctgtccctc 60
acgtgcactg tctctggtgg ctccatcagt 90
<210> 21
<211> 5
<212> Белок
<213> Homo Sapien
<400> 21
Ser Tyr Tyr Trp Ser
1 5
<210> 22
<211> 15
<212> ДНК
<213> Homo Sapien
<400> 22
agttactact ggagc 15
<210> 23
<211> 14
<212> Белок
<213> Homo Sapien
<400> 23
Trp Ile Arg Gln Tyr Pro Gly Lys Gly Leu Glu Trp Ile Gly
1 5 10
<210> 24
<211> 42
<212> ДНК
<213> Homo Sapien
<400> 24
tggatccggc agtacccagg aaagggactg gagtggattg ga 42
<210> 25
<211> 16
<212> Белок
<213> Homo Sapien
<400> 25
Tyr Ile Ser Tyr Ser Gly Ser Ser Asn Tyr Asn Pro Ser Leu Lys Arg
1 5 10 15
<210> 26
<211> 48
<212> ДНК
<213> Homo Sapien
<400> 26
tatatctctt acagtgggag cagcaattat aatccctccc tcaagagg 48
<210> 27
<211> 32
<212> Белок
<213> Homo Sapien
<400> 27
Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser Leu Asn
1 5 10 15
Leu Thr Ser Val Ile Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg
20 25 30
<210> 28
<211> 96
<212> ДНК
<213> Homo Sapien
<400> 28
cgagtcacca tatcacgaga cacgtccaag aaccagttct ccctgaatct gacctctgta 60
atcgctgcgg acacggccgt ttattactgt gcgaga 96
<210> 29
<211> 12
<212> Белок
<213> Homo Sapien
<400> 29
Asn Leu Met Ile Arg Gly Ala Tyr Gly Met Asp Val
1 5 10
<210> 30
<211> 36
<212> ДНК
<213> Homo Sapien
<400> 30
aatcttatga ttcggggagc ctacggcatg gacgtc 36
<210> 31
<211> 11
<212> Белок
<213> Homo Sapien
<400> 31
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
1 5 10
<210> 32
<211> 33
<212> ДНК
<213> Homo Sapien
<400> 32
tggggccaag ggaccacggt caccgtctcc tca 33
<210> 33
<211> 112
<212> Белок
<213> Homo Sapien
<400> 33
Asp Thr Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Ala Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Val Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Ile Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Phe Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105 110
<210> 34
<211> 336
<212> ДНК
<213> Homo Sapien
<400> 34
gatactgtga tgactcagtc tccactctcc ctgcccgtca cccctggaga gccggcctcc 60
atctcctgca ggtctagtca gagcctcctg catagtaatg gatacaatta tttggattgg 120
tacctgcaga aggcaggaca gtctccacaa ctcctgatct atttgggttc taatcgggcc 180
tccggggtcc ctgacaggtt cagtggcagt gtatcaggca cagatttcac actgaaaatc 240
agcagagtgg aggctgagga tgttgggatt tattactgca tgcaagctct acaaactcca 300
ttcactttcg gccctgggac caaagtggat atcaaa 336
<210> 35
<211> 107
<212> Белок
<213> Homo Sapien
<400> 35
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 36
<211> 321
<212> ДНК
<213> Homo Sapien
<400> 36
cgtacggtgg ccgctccctc cgtgttcatc ttcccacctt ccgacgagca gctgaagtcc 60
ggcaccgctt ctgtcgtgtg cctgctgaac aacttctacc cccgcgaggc caaggtgcag 120
tggaaggtgg acaacgccct gcagtccggc aactcccagg aatccgtgac cgagcaggac 180
tccaaggaca gcacctactc cctgtcctcc accctgaccc tgtccaaggc cgactacgag 240
aagcacaagg tgtacgcctg cgaagtgacc caccagggcc tgtctagccc cgtgaccaag 300
tctttcaacc ggggcgagtg t 321
<210> 37
<211> 26
<212> Белок
<213> Homo Sapien
<400> 37
Asp Thr Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser
20 25
<210> 38
<211> 78
<212> ДНК
<213> Homo Sapien
<400> 38
gatactgtga tgactcagtc tccactctcc ctgcccgtca cccctggaga gccggcctcc 60
atctcctgca ggtctagt 78
<210> 39
<211> 11
<212> Белок
<213> Homo Sapien
<400> 39
Gln Ser Leu Leu His Ser Asn Gly Tyr Asn Tyr
1 5 10
<210> 40
<211> 33
<212> ДНК
<213> Homo Sapien
<400> 40
cagagcctcc tgcatagtaa tggatacaat tat 33
<210> 41
<211> 17
<212> Белок
<213> Homo Sapien
<400> 41
Leu Asp Trp Tyr Leu Gln Lys Ala Gly Gln Ser Pro Gln Leu Leu Ile
1 5 10 15
Tyr
<210> 42
<211> 51
<212> ДНК
<213> Homo Sapien
<400> 42
ttggattggt acctgcagaa ggcaggacag tctccacaac tcctgatcta t 51
<210> 43
<211> 3
<212> Белок
<213> Homo Sapien
<400> 43
Leu Gly Ser
1
<210> 44
<211> 9
<212> ДНК
<213> Homo Sapien
<400> 44
ttgggttct 9
<210> 45
<211> 36
<212> Белок
<213> Homo Sapien
<400> 45
Asn Arg Ala Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Val Ser Gly
1 5 10 15
Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly
20 25 30
Ile Tyr Tyr Cys
35
<210> 46
<211> 108
<212> ДНК
<213> Homo Sapien
<400> 46
aatcgggcct ccggggtccc tgacaggttc agtggcagtg tatcaggcac agatttcaca 60
ctgaaaatca gcagagtgga ggctgaggat gttgggattt attactgc 108
<210> 47
<211> 9
<212> Белок
<213> Homo Sapien
<400> 47
Met Gln Ala Leu Gln Thr Pro Phe Thr
1 5
<210> 48
<211> 27
<212> ДНК
<213> Homo Sapien
<400> 48
atgcaagctc tacaaactcc attcact 27
<210> 49
<211> 10
<212> Белок
<213> Homo Sapien
<400> 49
Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
1 5 10
<210> 50
<211> 30
<212> ДНК
<213> Homo Sapien
<400> 50
ttcggccctg ggaccaaagt ggatatcaaa 30
<210> 51
<211> 23
<212> Белок
<213> Homo Sapien
<400> 51
Asp Thr Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys
20
<210> 52
<211> 69
<212> ДНК
<213> Homo Sapien
<400> 52
gatactgtga tgactcagtc tccactctcc ctgcccgtca cccctggaga gccggcctcc 60
atctcctgc 69
<210> 53
<211> 16
<212> Белок
<213> Homo Sapien
<400> 53
Arg Ser Ser Gln Ser Leu Leu His Ser Asn Gly Tyr Asn Tyr Leu Asp
1 5 10 15
<210> 54
<211> 48
<212> ДНК
<213> Homo Sapien
<400> 54
aggtctagtc agagcctcct gcatagtaat ggatacaatt atttggat 48
<210> 55
<211> 15
<212> Белок
<213> Homo Sapien
<400> 55
Trp Tyr Leu Gln Lys Ala Gly Gln Ser Pro Gln Leu Leu Ile Tyr
1 5 10 15
<210> 56
<211> 45
<212> ДНК
<213> Homo Sapien
<400> 56
tggtacctgc agaaggcagg acagtctcca caactcctga tctat 45
<210> 57
<211> 7
<212> Белок
<213> Homo Sapien
<400> 57
Leu Gly Ser Asn Arg Ala Ser
1 5
<210> 58
<211> 21
<212> ДНК
<213> Homo Sapien
<400> 58
ttgggttcta atcgggcctc c 21
<210> 59
<211> 32
<212> Белок
<213> Homo Sapien
<400> 59
Gly Val Pro Asp Arg Phe Ser Gly Ser Val Ser Gly Thr Asp Phe Thr
1 5 10 15
Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Ile Tyr Tyr Cys
20 25 30
<210> 60
<211> 96
<212> ДНК
<213> Homo Sapien
<400> 60
ggggtccctg acaggttcag tggcagtgta tcaggcacag atttcacact gaaaatcagc 60
agagtggagg ctgaggatgt tgggatttat tactgc 96
<210> 61
<211> 9
<212> Белок
<213> Homo Sapien
<400> 61
Met Gln Ala Leu Gln Thr Pro Phe Thr
1 5
<210> 62
<211> 27
<212> ДНК
<213> Homo Sapien
<400> 62
atgcaagctc tacaaactcc attcact 27
<210> 63
<211> 10
<212> Белок
<213> Homo Sapien
<400> 63
Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
1 5 10
<210> 64
<211> 30
<212> ДНК
<213> Homo Sapien
<400> 64
ttcggccctg ggaccaaagt ggatatcaaa 30
<210> 65
<211> 127
<212> Белок
<213> Homo Sapien
<400> 65
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Thr Ala Ser Gly Phe Thr Phe Ala Asp Tyr
20 25 30
Val Met His Trp Val Arg Gln Thr Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Asn Ser Tyr Ser Ile Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Gln Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Phe Cys
85 90 95
Ala Lys Asp Ile Thr Tyr Asp Leu Leu Thr Gly Tyr Asn Tyr Asn Tyr
100 105 110
Gly Leu Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 66
<211> 381
<212> ДНК
<213> Homo Sapien
<400> 66
gaagtgcagc tggtagagtc tgggggaggc ttggtacagc ctggcaggtc cctgagactc 60
tcctgtacag cctctggatt cacctttgct gattatgtca tgcactgggt ccggcaaact 120
ccagggaagg gcctggagtg ggtctcaggt attagttgga atagttatag tataaattat 180
gcggactctg tgaagggccg attcaccatc tccagagaca acgcccagaa ctccctgtat 240
ctgcaaatga acagtctgag agctgaggac acggccttgt atttttgtgc aaaagatata 300
acttacgatc ttttgactgg ttataactac aactacggtt tagacgtctg gggccaaggg 360
accacggtca ccgtctcctc a 381
<210> 67
<211> 25
<212> Белок
<213> Homo Sapien
<400> 67
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Thr Ala Ser
20 25
<210> 68
<211> 75
<212> ДНК
<213> Homo Sapien
<400> 68
gaagtgcagc tggtagagtc tgggggaggc ttggtacagc ctggcaggtc cctgagactc 60
tcctgtacag cctct 75
<210> 69
<211> 8
<212> Белок
<213> Homo Sapien
<400> 69
Gly Phe Thr Phe Ala Asp Tyr Val
1 5
<210> 70
<211> 24
<212> ДНК
<213> Homo Sapien
<400> 70
ggattcacct ttgctgatta tgtc 24
<210> 71
<211> 17
<212> Белок
<213> Homo Sapien
<400> 71
Met His Trp Val Arg Gln Thr Pro Gly Lys Gly Leu Glu Trp Val Ser
1 5 10 15
Gly
<210> 72
<211> 51
<212> ДНК
<213> Homo Sapien
<400> 72
atgcactggg tccggcaaac tccagggaag ggcctggagt gggtctcagg t 51
<210> 73
<211> 8
<212> Белок
<213> Homo Sapien
<400> 73
Ile Ser Trp Asn Ser Tyr Ser Ile
1 5
<210> 74
<211> 24
<212> ДНК
<213> Homo Sapien
<400> 74
attagttgga atagttatag tata 24
<210> 75
<211> 38
<212> Белок
<213> Homo Sapien
<400> 75
Asn Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn
1 5 10 15
Ala Gln Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp
20 25 30
Thr Ala Leu Tyr Phe Cys
35
<210> 76
<211> 114
<212> ДНК
<213> Homo Sapien
<400> 76
aattatgcgg actctgtgaa gggccgattc accatctcca gagacaacgc ccagaactcc 60
ctgtatctgc aaatgaacag tctgagagct gaggacacgg ccttgtattt ttgt 114
<210> 77
<211> 20
<212> Белок
<213> Homo Sapien
<400> 77
Ala Lys Asp Ile Thr Tyr Asp Leu Leu Thr Gly Tyr Asn Tyr Asn Tyr
1 5 10 15
Gly Leu Asp Val
20
<210> 78
<211> 60
<212> ДНК
<213> Homo Sapien
<400> 78
gcaaaagata taacttacga tcttttgact ggttataact acaactacgg tttagacgtc 60
<210> 79
<211> 11
<212> Белок
<213> Homo Sapien
<400> 79
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
1 5 10
<210> 80
<211> 33
<212> ДНК
<213> Homo Sapien
<400> 80
tggggccaag ggaccacggt caccgtctcc tca 33
<210> 81
<211> 30
<212> Белок
<213> Homo Sapien
<400> 81
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Thr Ala Ser Gly Phe Thr Phe Ala
20 25 30
<210> 82
<211> 90
<212> ДНК
<213> Homo Sapien
<400> 82
gaagtgcagc tggtagagtc tgggggaggc ttggtacagc ctggcaggtc cctgagactc 60
tcctgtacag cctctggatt cacctttgct 90
<210> 83
<211> 5
<212> Белок
<213> Homo Sapien
<400> 83
Asp Tyr Val Met His
1 5
<210> 84
<211> 15
<212> ДНК
<213> Homo Sapien
<400> 84
gattatgtca tgcac 15
<210> 85
<211> 14
<212> Белок
<213> Homo Sapien
<400> 85
Trp Val Arg Gln Thr Pro Gly Lys Gly Leu Glu Trp Val Ser
1 5 10
<210> 86
<211> 42
<212> ДНК
<213> Homo Sapien
<400> 86
tgggtccggc aaactccagg gaagggcctg gagtgggtct ca 42
<210> 87
<211> 17
<212> Белок
<213> Homo Sapien
<400> 87
Gly Ile Ser Trp Asn Ser Tyr Ser Ile Asn Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 88
<211> 51
<212> ДНК
<213> Homo Sapien
<400> 88
ggtattagtt ggaatagtta tagtataaat tatgcggact ctgtgaaggg c 51
<210> 89
<211> 32
<212> Белок
<213> Homo Sapien
<400> 89
Arg Phe Thr Ile Ser Arg Asp Asn Ala Gln Asn Ser Leu Tyr Leu Gln
1 5 10 15
Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Phe Cys Ala Lys
20 25 30
<210> 90
<211> 96
<212> ДНК
<213> Homo Sapien
<400> 90
cgattcacca tctccagaga caacgcccag aactccctgt atctgcaaat gaacagtctg 60
agagctgagg acacggcctt gtatttttgt gcaaaa 96
<210> 91
<211> 18
<212> Белок
<213> Homo Sapien
<400> 91
Asp Ile Thr Tyr Asp Leu Leu Thr Gly Tyr Asn Tyr Asn Tyr Gly Leu
1 5 10 15
Asp Val
<210> 92
<211> 54
<212> ДНК
<213> Homo Sapien
<400> 92
gatataactt acgatctttt gactggttat aactacaact acggtttaga cgtc 54
<210> 93
<211> 11
<212> Белок
<213> Homo Sapien
<400> 93
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
1 5 10
<210> 94
<211> 33
<212> ДНК
<213> Homo Sapien
<400> 94
tggggccaag ggaccacggt caccgtctcc tca 33
<210> 95
<211> 112
<212> Белок
<213> Homo Sapien
<400> 95
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asp Gly Lys Thr Tyr Leu Tyr Trp Tyr Leu Gln Lys Pro Gly Gln Pro
35 40 45
Pro Gln Leu Leu Ile Tyr Glu Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Leu Tyr Tyr Cys Met Gln Ser
85 90 95
Ile Gln Leu Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 96
<211> 336
<212> ДНК
<213> Homo Sapien
<400> 96
gatattgtga tgacccagac tccactctct ctgtccgtca cccctggaca gccggcctcc 60
atctcctgca ggtctagtca gagcctccta catagtgatg gaaagaccta tttgtattgg 120
tacctgcaga agcccggcca gcctccacag ctcctgatct atgaagtttc caaccgtttc 180
tctggagtgc cagataggtt cagtggcagc gggtcaggga cagatttcac actgaagatc 240
agccgggtgg aggctgaaga tgttggcctt tattactgca tgcaaagtat acagcttccg 300
ctcactttcg gcggagggac caaggtagag atcaaa 336
<210> 97
<211> 26
<212> Белок
<213> Homo Sapien
<400> 97
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser
20 25
<210> 98
<211> 78
<212> ДНК
<213> Homo Sapien
<400> 98
gatattgtga tgacccagac tccactctct ctgtccgtca cccctggaca gccggcctcc 60
atctcctgca ggtctagt 78
<210> 99
<211> 11
<212> Белок
<213> Homo Sapien
<400> 99
Gln Ser Leu Leu His Ser Asp Gly Lys Thr Tyr
1 5 10
<210> 100
<211> 33
<212> ДНК
<213> Homo Sapien
<400> 100
cagagcctcc tacatagtga tggaaagacc tat 33
<210> 101
<211> 17
<212> Белок
<213> Homo Sapien
<400> 101
Leu Tyr Trp Tyr Leu Gln Lys Pro Gly Gln Pro Pro Gln Leu Leu Ile
1 5 10 15
Tyr
<210> 102
<211> 51
<212> ДНК
<213> Homo Sapien
<400> 102
ttgtattggt acctgcagaa gcccggccag cctccacagc tcctgatcta t 51
<210> 103
<211> 3
<212> Белок
<213> Homo Sapien
<400> 103
Glu Val Ser
1
<210> 104
<211> 9
<212> ДНК
<213> Homo Sapien
<400> 104
gaagtttcc 9
<210> 105
<211> 36
<212> Белок
<213> Homo Sapien
<400> 105
Asn Arg Phe Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly
1 5 10 15
Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly
20 25 30
Leu Tyr Tyr Cys
35
<210> 106
<211> 108
<212> ДНК
<213> Homo Sapien
<400> 106
aaccgtttct ctggagtgcc agataggttc agtggcagcg ggtcagggac agatttcaca 60
ctgaagatca gccgggtgga ggctgaagat gttggccttt attactgc 108
<210> 107
<211> 9
<212> Белок
<213> Homo Sapien
<400> 107
Met Gln Ser Ile Gln Leu Pro Leu Thr
1 5
<210> 108
<211> 27
<212> ДНК
<213> Homo Sapien
<400> 108
atgcaaagta tacagcttcc gctcact 27
<210> 109
<211> 10
<212> Белок
<213> Homo Sapien
<400> 109
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
1 5 10
<210> 110
<211> 30
<212> ДНК
<213> Homo Sapien
<400> 110
ttcggcggag ggaccaaggt agagatcaaa 30
<210> 111
<211> 23
<212> Белок
<213> Homo Sapien
<400> 111
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys
20
<210> 112
<211> 69
<212> ДНК
<213> Homo Sapien
<400> 112
gatattgtga tgacccagac tccactctct ctgtccgtca cccctggaca gccggcctcc 60
atctcctgc 69
<210> 113
<211> 16
<212> Белок
<213> Homo Sapien
<400> 113
Arg Ser Ser Gln Ser Leu Leu His Ser Asp Gly Lys Thr Tyr Leu Tyr
1 5 10 15
<210> 114
<211> 48
<212> ДНК
<213> Homo Sapien
<400> 114
aggtctagtc agagcctcct acatagtgat ggaaagacct atttgtat 48
<210> 115
<211> 15
<212> Белок
<213> Homo Sapien
<400> 115
Trp Tyr Leu Gln Lys Pro Gly Gln Pro Pro Gln Leu Leu Ile Tyr
1 5 10 15
<210> 116
<211> 45
<212> ДНК
<213> Homo Sapien
<400> 116
tggtacctgc agaagcccgg ccagcctcca cagctcctga tctat 45
<210> 117
<211> 7
<212> Белок
<213> Homo Sapien
<400> 117
Glu Val Ser Asn Arg Phe Ser
1 5
<210> 118
<211> 21
<212> ДНК
<213> Homo Sapien
<400> 118
gaagtttcca accgtttctc t 21
<210> 119
<211> 32
<212> Белок
<213> Homo Sapien
<400> 119
Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
1 5 10 15
Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Leu Tyr Tyr Cys
20 25 30
<210> 120
<211> 96
<212> ДНК
<213> Homo Sapien
<400> 120
ggagtgccag ataggttcag tggcagcggg tcagggacag atttcacact gaagatcagc 60
cgggtggagg ctgaagatgt tggcctttat tactgc 96
<210> 121
<211> 9
<212> Белок
<213> Homo Sapien
<400> 121
Met Gln Ser Ile Gln Leu Pro Leu Thr
1 5
<210> 122
<211> 27
<212> ДНК
<213> Homo Sapien
<400> 122
atgcaaagta tacagcttcc gctcact 27
<210> 123
<211> 10
<212> Белок
<213> Homo Sapien
<400> 123
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
1 5 10
<210> 124
<211> 30
<212> ДНК
<213> Homo Sapien
<400> 124
ttcggcggag ggaccaaggt agagatcaaa 30
<210> 125
<211> 990
<212> ДНК
<213> Homo Sapien
<400> 125
gcctccacca agggcccatc ggtcttcccc ctggcaccct cctccaagag cacctctggg 60
ggcacagcgg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 120
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacccagacc 240
tacatctgca acgtgaatca caagcccagc aacaccaagg tggacaagaa agttgagccc 300
aaatcttgtg acaaaactca cacatgccca ccgtgcccag cacctgaact cctgggggga 360
ccgtcagtct tcctcttccc cccaaaaccc aaggacaccc tcatgatctc ccggacccct 420
gaggtcacat gcgtggtggt ggacgtgagc cacgaagacc ctgaggtcaa gttcaactgg 480
tacgtggacg gcgtggaggt gcataatgcc aagacaaagc cgcgggagga gcagtacaac 540
agcacgtacc gggtggtcag cgtcctcacc gtcctgcacc aggactggct gaatggcaag 600
gagtacaagt gcaaggtctc caacaaagcc ctcccagccc ccatcgagaa aaccatctcc 660
aaagccaaag ggcagccccg agaaccacag gtgtacaccc tgcccccatc ccgggatgag 720
ctgaccaaga accaggtcag cctgacctgc ctggtcaaag gcttctatcc cagcgacatc 780
gccgtggagt gggagagcaa tgggcagccg gagaacaact acaagaccac gcctcccgtg 840
ctggactccg acggctcctt cttcctctac agcaagctca ccgtggacaa gagcaggtgg 900
cagcagggga acgtcttctc atgctccgtg atgcatgagg ctctgcacaa ccactacacg 960
cagaagagcc tctccctgtc tccgggtaaa 990
<210> 126
<211> 330
<212> Белок
<213> Homo Sapien
<400> 126
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
225 230 235 240
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
325 330
<210> 127
<211> 990
<212> ДНК
<213> Homo Sapien
<400> 127
gcctccacca agggcccatc ggtcttcccc ctggcaccct cctccaagag cacctctggg 60
ggcacagcgg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 120
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacccagacc 240
tacatctgca acgtgaatca caagcccagc aacaccaagg tggacaagaa agttgagccc 300
aaatcttgtg acaaaactca cacatgccca ccgtgcccag cacctgaact cctgggggga 360
ccgtcagtct tcctcttccc cccaaaaccc aaggacaccc tcatgatctc ccggacccct 420
gaggtcacat gcgtggtggt ggacgtgagc cacgaagacc ctgaggtcaa gttcaactgg 480
tacgtggacg gcgtggaggt gcataatgcc aagacaaagc cgcgggagga gcagtacaac 540
agcacgtacc gtgtggtcag cgtcctcacc gtcctgcacc aggactggct gaatggcaag 600
gagtacaagt gcaaggtctc caacaaagcc ctcccagccc ccatcgagaa aaccatctcc 660
aaagccaaag ggcagccccg agaaccacag gtgtacaccc tgcccccatc ccgggatgag 720
ctgaccaaga accaggtcag cctgacctgc ctggtcaaag gcttctatcc cagcgacatc 780
gccgtggagt gggagagcaa tgggcagccg gagaacaact acaagaccac gcctcccgtg 840
ctggactccg acggctcctt cttcctctac agcaagctca ccgtggacaa gagcaggtgg 900
cagcagggga acgtcttctc atgctccgtg atgcatgagg ctctgcacaa ccactacacg 960
cagaagagcc tctccctgtc tccgggtaaa 990
<210> 128
<211> 330
<212> Белок
<213> Homo Sapien
<400> 128
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
225 230 235 240
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
325 330
<210> 129
<211> 990
<212> ДНК
<213> Homo Sapien
<400> 129
gcctccacca agggcccatc ggtcttcccc ctggcaccct cctccaagag cacctctggg 60
ggcacagcgg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 120
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacccagacc 240
tacatctgca acgtgaatca caagcccagc aacaccaagg tggacaagag agttgagccc 300
aaatcttgtg acaaaactca cacatgccca ccgtgcccag cacctgaact cctgggggga 360
ccgtcagtct tcctcttccc cccaaaaccc aaggacaccc tcatgatctc ccggacccct 420
gaggtcacat gcgtggtggt ggacgtgagc cacgaagacc ctgaggtcaa gttcaactgg 480
tacgtggacg gcgtggaggt gcataatgcc aagacaaagc cgcgggagga gcagtacaac 540
agcacgtacc gtgtggtcag cgtcctcacc gtcctgcacc aggactggct gaatggcaag 600
gagtacaagt gcaaggtctc caacaaagcc ctcccagccc ccatcgagaa aaccatctcc 660
aaagccaaag ggcagccccg agaaccacag gtgtacaccc tgcccccatc ccgggaggag 720
atgaccaaga accaggtcag cctgacctgc ctggtcaaag gcttctatcc cagcgacatc 780
gccgtggagt gggagagcaa tgggcagccg gagaacaact acaagaccac gcctcccgtg 840
ctggactccg acggctcctt cttcctctat agcaagctca ccgtggacaa gagcaggtgg 900
cagcagggga acgtcttctc atgctccgtg atgcatgagg ctctgcacaa ccactacacg 960
cagaagagcc tctccctgtc cccgggtaaa 990
<210> 130
<211> 330
<212> Белок
<213> Homo Sapien
<400> 130
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu
225 230 235 240
Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
325 330
<210> 131
<211> 990
<212> ДНК
<213> Homo Sapien
<400> 131
gcctccacca agggcccatc ggtcttcccc ctggcaccct cctccaagag cacctctggg 60
ggcacagcgg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 120
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacccagacc 240
tacatctgca acgtgaatca caagcccagc aacaccaagg tggacaagaa agttgagccc 300
aaatcttgtg acaaaactca cacatgccca ccgtgcccag cacctgaact cctgggggga 360
ccgtcagtct tcctcttccc cccaaaaccc aaggacaccc tcatgatctc ccggacccct 420
gaggtcacat gcgtggtggt ggacgtgagc cacgaagacc ctgaggtcaa gttcaactgg 480
tacgtggacg gcgtggaggt gcataatgcc aagacaaagc cgcgggagga gcagtacaac 540
agcacgtacc gtgtggtcag cgtcctcacc gtcctgcacc aggactggct gaatggcaag 600
gagtacaagt gcaaggtctc caacaaagcc ctcccagccc ccatcgagaa aaccatctcc 660
aaagccaaag ggcagccccg agaaccacag gtgtacaccc tgcccccatc ccgggatgag 720
ctgaccaaga accaggtcag cctgacctgc ctggtcaaag gcttctatcc cagcgacatc 780
gccgtggagt gggagagcaa tgggcagccg gagaacaact acaagaccac gcctcccgtg 840
ctggactccg acggctcctt cttcctctac agcaagctca ccgtggacaa gagcaggtgg 900
cagcagggga acatcttctc atgctccgtg atgcatgagg ctctgcacaa ccactacacg 960
cagaagagcc tctccctgtc tccgggtaaa 990
<210> 132
<211> 330
<212> Белок
<213> Homo Sapien
<400> 132
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
225 230 235 240
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Ile Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
325 330
<210> 133
<211> 990
<212> ДНК
<213> Homo Sapien
<400> 133
gcctccacca agggcccatc ggtcttcccc ctggcaccct cctccaagag cacctctggg 60
ggcacagcgg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 120
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacccagacc 240
tacatctgca acgtgaatca caagcccagc aacaccaagg tggacaagaa agtggagccc 300
aaatcttgtg acaaaactca cacatgccca ccgtgcccag cacctgaact cgcgggggca 360
ccgtcagtct tcctcttccc cccaaaaccc aaggacaccc tcatgatctc ccggacccct 420
gaggtcacat gcgtggtggt ggacgtgagc cacgaagacc ctgaggtcaa gttcaactgg 480
tacgtggacg gcgtggaggt gcataatgcc aagacaaagc cgcgggagga gcagtacaac 540
agcacgtacc gtgtggtcag cgtcctcacc gtcctgcacc aggactggct gaatggcaag 600
gagtacaagt gcaaggtctc caacaaagcc ctcccagccc ccatcgagaa aaccatctcc 660
aaagccaaag ggcagccccg agaaccacag gtgtacaccc tgcccccatc ccgggatgag 720
ctgaccaaga accaggtcag cctgacctgc ctggtcaaag gcttctatcc cagcgacatc 780
gccgtggagt gggagagcaa tgggcagccg gagaacaact acaagaccac gcctcccgtg 840
ctggactccg acggctcctt cttcctctac agcaagctca ccgtggacaa gagcaggtgg 900
cagcagggga acgtcttctc atgctccgtg atgcatgagg ctctgcacaa ccactacacg 960
cagaagagcc tctccctgtc tccgggtaaa 990
<210> 134
<211> 330
<212> Белок
<213> Homo Sapien
<400> 134
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Ala Gly Ala Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
225 230 235 240
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
325 330
<210> 135
<211> 978
<212> ДНК
<213> Homo Sapien
<400> 135
gcctccacca agggcccatc ggtcttcccc ctggcgccct gctccaggag cacctccgag 60
agcacagccg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 120
tggaactcag gcgctctgac cagcggcgtg cacaccttcc cagctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcaacttcgg cacccagacc 240
tacacctgca acgtagatca caagcccagc aacaccaagg tggacaagac agttgagcgc 300
aaatgttgtg tcgagtgccc accgtgccca gcaccacctg tggcaggacc gtcagtcttc 360
ctcttccccc caaaacccaa ggacaccctc atgatctccc ggacccctga ggtcacgtgc 420
gtggtggtgg acgtgagcca cgaagacccc gaggtccagt tcaactggta cgtggacggc 480
gtggaggtgc ataatgccaa gacaaagcca cgggaggagc agttcaacag cacgttccgt 540
gtggtcagcg tcctcaccgt tgtgcaccag gactggctga acggcaagga gtacaagtgc 600
aaggtctcca acaaaggcct cccagccccc atcgagaaaa ccatctccaa aaccaaaggg 660
cagccccgag aaccacaggt gtacaccctg cccccatccc gggaggagat gaccaagaac 720
caggtcagcc tgacctgcct ggtcaaaggc ttctacccca gcgacatcgc cgtggagtgg 780
gagagcaatg ggcagccgga gaacaactac aagaccacac ctcccatgct ggactccgac 840
ggctccttct tcctctacag caagctcacc gtggacaaga gcaggtggca gcaggggaac 900
gtcttctcat gctccgtgat gcatgaggct ctgcacaacc actacacgca gaagagcctc 960
tccctgtctc cgggtaaa 978
<210> 136
<211> 326
<212> Белок
<213> Homo Sapien
<400> 136
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Asn Phe Gly Thr Gln Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Thr Val Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro Ala Pro
100 105 110
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
115 120 125
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
130 135 140
Val Ser His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly
145 150 155 160
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn
165 170 175
Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Val His Gln Asp Trp
180 185 190
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro
195 200 205
Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln Pro Arg Glu
210 215 220
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn
225 230 235 240
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
245 250 255
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
260 265 270
Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
275 280 285
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
290 295 300
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
305 310 315 320
Ser Leu Ser Pro Gly Lys
325
<210> 137
<211> 978
<212> ДНК
<213> Homo Sapien
<400> 137
gcctccacca agggcccatc ggtcttcccc ctggcgccct gctccaggag cacctccgag 60
agcacagcgg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 120
tggaactcag gcgctctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgacctcca gcaacttcgg cacccagacc 240
tacacctgca acgtagatca caagcccagc aacaccaagg tggacaagac agttgagcgc 300
aaatgttgtg tcgagtgccc accgtgccca gcaccacctg tggcaggacc gtcagtcttc 360
ctcttccccc caaaacccaa ggacaccctc atgatctccc ggacccctga ggtcacgtgc 420
gtggtggtgg acgtgagcca cgaagacccc gaggtccagt tcaactggta cgtggacggc 480
atggaggtgc ataatgccaa gacaaagcca cgggaggagc agttcaacag cacgttccgt 540
gtggtcagcg tcctcaccgt cgtgcaccag gactggctga acggcaagga gtacaagtgc 600
aaggtctcca acaaaggcct cccagccccc atcgagaaaa ccatctccaa aaccaaaggg 660
cagccccgag aaccacaggt gtacaccctg cccccatccc gggaggagat gaccaagaac 720
caggtcagcc tgacctgcct ggtcaaaggc ttctacccca gcgacatcgc cgtggagtgg 780
gagagcaatg ggcagccgga gaacaactac aagaccacac ctcccatgct ggactccgac 840
ggctccttct tcctctacag caagctcacc gtggacaaga gcaggtggca gcaggggaac 900
gtcttctcat gctccgtgat gcatgaggct ctgcacaacc actacacaca gaagagcctc 960
tccctgtctc cgggtaaa 978
<210> 138
<211> 326
<212> Белок
<213> Homo Sapien
<400> 138
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Thr Ser Ser Asn Phe Gly Thr Gln Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Thr Val Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro Ala Pro
100 105 110
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
115 120 125
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
130 135 140
Val Ser His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly
145 150 155 160
Met Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn
165 170 175
Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Val His Gln Asp Trp
180 185 190
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro
195 200 205
Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln Pro Arg Glu
210 215 220
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn
225 230 235 240
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
245 250 255
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
260 265 270
Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
275 280 285
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
290 295 300
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
305 310 315 320
Ser Leu Ser Pro Gly Lys
325
<210> 139
<211> 978
<212> ДНК
<213> Homo Sapien
<400> 139
gcctccacca agggcccatc ggtcttcccc ctggcgccct gctccaggag cacctccgag 60
agcacagcgg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 120
tggaactcag gcgctctgac cagcggcgtg cacaccttcc cagctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacccagacc 240
tacacctgca acgtagatca caagcccagc aacaccaagg tggacaagac agttgagcgc 300
aaatgttgtg tcgagtgccc accgtgccca gcaccacctg tggcaggacc gtcagtcttc 360
ctcttccccc caaaacccaa ggacaccctc atgatctccc ggacccctga ggtcacgtgc 420
gtggtggtgg acgtgagcca cgaagacccc gaggtccagt tcaactggta cgtggacggc 480
gtggaggtgc ataatgccaa gacaaagcca cgggaggagc agttcaacag cacgttccgt 540
gtggtcagcg tcctcaccgt tgtgcaccag gactggctga acggcaagga gtacaagtgc 600
aaggtctcca acaaaggcct cccagccccc atcgagaaaa ccatctccaa aaccaaaggg 660
cagccccgag aaccacaggt gtacaccctg cccccatccc gggaggagat gaccaagaac 720
caggtcagcc tgacctgcct ggtcaaaggc ttctacccca gcgacatcgc cgtggagtgg 780
gagagcaatg ggcagccgga gaacaactac aagaccacac ctcccatgct ggactccgac 840
ggctccttct tcctctacag caagctcacc gtggacaaga gcaggtggca gcaggggaac 900
gtcttctcat gctccgtgat gcatgaggct ctgcacaacc actacacgca gaagagcctc 960
tccctgtctc cgggtaaa 978
<210> 140
<211> 326
<212> Белок
<213> Homo Sapien
<400> 140
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Thr Val Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro Ala Pro
100 105 110
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
115 120 125
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
130 135 140
Val Ser His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly
145 150 155 160
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn
165 170 175
Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Val His Gln Asp Trp
180 185 190
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro
195 200 205
Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln Pro Arg Glu
210 215 220
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn
225 230 235 240
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
245 250 255
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
260 265 270
Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
275 280 285
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
290 295 300
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
305 310 315 320
Ser Leu Ser Pro Gly Lys
325
<210> 141
<211> 978
<212> ДНК
<213> Homo Sapien
<400> 141
gcctccacca agggcccatc ggtcttcccc ctggcgccct gctccaggag cacctccgag 60
agcacagcgg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 120
tggaactcag gcgctctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcaacttcgg cacccagacc 240
tacacctgca acgtagatca caagcccagc aacaccaagg tggacaagac agttgagcgc 300
aaatgttgtg tcgagtgccc accgtgccca gcaccacctg tggcaggacc gtcagtcttc 360
ctcttccccc caaaacccaa ggacaccctc atgatctccc ggacccctga ggtcacgtgc 420
gtggtggtgg acgtgagcca cgaagacccc gaggtccagt tcaactggta cgtggacggc 480
gtggaggtgc ataatgccaa gacaaagcca cgggaggagc agttcaacag cacgttccgt 540
gtggtcagcg tcctcaccgt cgtgcaccag gactggctga acggcaagga gtacaagtgc 600
aaggtctcca acaaaggcct cccagccccc atcgagaaaa ccatctccaa aaccaaaggg 660
cagccccgag aaccacaggt gtacaccctg cccccatccc gggaggagat gaccaagaac 720
caggtcagcc tgacctgcct ggtcaaaggc ttctacccca gcgacatctc cgtggagtgg 780
gagagcaatg ggcagccgga gaacaactac aagaccacac ctcccatgct ggactccgac 840
ggctccttct tcctctacag caagctcacc gtggacaaga gcaggtggca gcaggggaac 900
gtcttctcat gctccgtgat gcatgaggct ctgcacaacc actacacaca gaagagcctc 960
tccctgtctc cgggtaaa 978
<210> 142
<211> 326
<212> Белок
<213> Homo Sapien
<400> 142
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Asn Phe Gly Thr Gln Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Thr Val Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro Ala Pro
100 105 110
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
115 120 125
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
130 135 140
Val Ser His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly
145 150 155 160
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn
165 170 175
Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Val His Gln Asp Trp
180 185 190
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro
195 200 205
Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln Pro Arg Glu
210 215 220
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn
225 230 235 240
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
245 250 255
Ser Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
260 265 270
Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
275 280 285
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
290 295 300
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
305 310 315 320
Ser Leu Ser Pro Gly Lys
325
<210> 143
<211> 981
<212> ДНК
<213> Homo Sapien
<400> 143
gcttccacca agggcccatc cgtcttcccc ctggcgccct gctccaggag cacctccgag 60
agcacagccg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 120
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacgaagacc 240
tacacctgca acgtagatca caagcccagc aacaccaagg tggacaagag agttgagtcc 300
aaatatggtc ccccatgccc atcatgccca gcacctgagt tcctgggggg accatcagtc 360
ttcctgttcc ccccaaaacc caaggacact ctcatgatct cccggacccc tgaggtcacg 420
tgcgtggtgg tggacgtgag ccaggaagac cccgaggtcc agttcaactg gtacgtggat 480
ggcgtggagg tgcataatgc caagacaaag ccgcgggagg agcagttcaa cagcacgtac 540
cgtgtggtca gcgtcctcac cgtcctgcac caggactggc tgaacggcaa ggagtacaag 600
tgcaaggtct ccaacaaagg cctcccgtcc tccatcgaga aaaccatctc caaagccaaa 660
gggcagcccc gagagccaca ggtgtacacc ctgcccccat cccaggagga gatgaccaag 720
aaccaggtca gcctgacctg cctggtcaaa ggcttctacc ccagcgacat cgccgtggag 780
tgggagagca atgggcagcc ggagaacaac tacaagacca cgcctcccgt gctggactcc 840
gacggctcct tcttcctcta cagcaggcta accgtggaca agagcaggtg gcaggagggg 900
aatgtcttct catgctccgt gatgcatgag gctctgcaca accactacac acagaagagc 960
ctctccctgt ctctgggtaa a 981
<210> 144
<211> 327
<212> Белок
<213> Homo Sapien
<400> 144
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Ser Cys Pro Ala Pro
100 105 110
Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
115 120 125
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
130 135 140
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
145 150 155 160
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
165 170 175
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
180 185 190
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
195 200 205
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
210 215 220
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
225 230 235 240
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
245 250 255
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
260 265 270
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
275 280 285
Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
290 295 300
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
305 310 315 320
Leu Ser Leu Ser Leu Gly Lys
325
<210> 145
<211> 981
<212> ДНК
<213> Homo Sapien
<400> 145
gcttccacca agggcccatc cgtcttcccc ctggcgccct gctccaggag cacctccgag 60
agcacagccg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 120
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacgaagacc 240
tacacctgca acgtagatca caagcccagc aacaccaagg tggacaagag agttgagtcc 300
aaatatggtc ccccgtgccc atcatgccca gcacctgagt tcctgggggg accatcagtc 360
ttcctgttcc ccccaaaacc caaggacact ctcatgatct cccggacccc tgaggtcacg 420
tgcgtggtgg tggacgtgag ccaggaagac cccgaggtcc agttcaactg gtacgtggat 480
ggcgtggagg tgcataatgc caagacaaag ccgcgggagg agcagttcaa cagcacgtac 540
cgtgtggtca gcgtcctcac cgtcgtgcac caggactggc tgaacggcaa ggagtacaag 600
tgcaaggtct ccaacaaagg cctcccgtcc tccatcgaga aaaccatctc caaagccaaa 660
gggcagcccc gagagccaca ggtgtacacc ctgcccccat cccaggagga gatgaccaag 720
aaccaggtca gcctgacctg cctggtcaaa ggcttctacc ccagcgacat cgccgtggag 780
tgggagagca atgggcagcc ggagaacaac tacaagacca cgcctcccgt gctggactcc 840
gacggctcct tcttcctcta cagcaggcta accgtggaca agagcaggtg gcaggagggg 900
aatgtcttct catgctccgt gatgcatgag gctctgcaca accactacac gcagaagagc 960
ctctccctgt ctctgggtaa a 981
<210> 146
<211> 327
<212> Белок
<213> Homo Sapien
<400> 146
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Ser Cys Pro Ala Pro
100 105 110
Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
115 120 125
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
130 135 140
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
145 150 155 160
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
165 170 175
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Val His Gln Asp
180 185 190
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
195 200 205
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
210 215 220
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
225 230 235 240
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
245 250 255
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
260 265 270
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
275 280 285
Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
290 295 300
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
305 310 315 320
Leu Ser Leu Ser Leu Gly Lys
325
<210> 147
<211> 981
<212> ДНК
<213> Homo Sapien
<400> 147
gcttccacca agggcccatc cgtcttcccc ctggcgccct gctccaggag cacctccgag 60
agcacagccg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 120
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacgaagacc 240
tacacctgca acgtagatca caagcccagc aacaccaagg tggacaagag agttgagtcc 300
aaatatggtc ccccatgccc atcatgccca gcacctgagt tcctgggggg accatcagtc 360
ttcctgttcc ccccaaaacc caaggacact ctcatgatct cccggacccc tgaggtcacg 420
tgcgtggtgg tggacgtgag ccaggaagac cccgaggtcc agttcaactg gtacgtggat 480
ggcgtggagg tgcataatgc caagacaaag ccgcgggagg agcagttcaa cagcacgtac 540
cgtgtggtca gcgtcctcac cgtcctgcac caggactggc tgaacggcaa ggagtacaag 600
tgcaaggtct ccaacaaagg cctcccgtcc tccatcgaga aaaccatctc caaagccaaa 660
gggcagcccc gagagccaca ggtgtacacc ctgcccccat cccaggagga gatgaccaag 720
aaccaggtca gcctgacctg cctggtcaaa ggcttctacc ccagcgacat cgccgtggag 780
tgggagagca atgggcagcc ggagaacaac tacaagacca cgcctcccgt gctggactcc 840
gacggctcct tcttcctcta cagcaagctc accgtggaca agagcaggtg gcaggagggg 900
aacgtcttct catgctccgt gatgcatgag gctctgcaca accactacac gcagaagagc 960
ctctccctgt ctctgggtaa a 981
<210> 148
<211> 327
<212> Белок
<213> Homo Sapien
<400> 148
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Ser Cys Pro Ala Pro
100 105 110
Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
115 120 125
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
130 135 140
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
145 150 155 160
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
165 170 175
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
180 185 190
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
195 200 205
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
210 215 220
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
225 230 235 240
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
245 250 255
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
260 265 270
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
275 280 285
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
290 295 300
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
305 310 315 320
Leu Ser Leu Ser Leu Gly Lys
325
<210> 149
<211> 981
<212> ДНК
<213> Homo Sapien
<400> 149
gcctccacca agggcccatc cgtcttcccc ctggcgccct gctccaggag cacctccgag 60
agcacggccg ccctgggctg cctggtcaag gactacttcc ccgaaccagt gacggtgtcg 120
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacgaagacc 240
tacacctgca acgtagatca caagcccagc aacaccaagg tggacaagag agttgagtcc 300
aaatatggtc ccccatgccc accatgccca gcgcctgaat ttgagggggg accatcagtc 360
ttcctgttcc ccccaaaacc caaggacact ctcatgatct cccggacccc tgaggtcacg 420
tgcgtggtgg tggacgtgag ccaggaagac cccgaggtcc agttcaactg gtacgtggat 480
ggcgtggagg tgcataatgc caagacaaag ccgcgggagg agcagttcaa cagcacgtac 540
cgtgtggtca gcgtcctcac cgtcctgcac caggactggc tgaacggcaa ggagtacaag 600
tgcaaggtct ccaacaaagg cctcccgtca tcgatcgaga aaaccatctc caaagccaaa 660
gggcagcccc gagagccaca ggtgtacacc ctgcccccat cccaggagga gatgaccaag 720
aaccaggtca gcctgacctg cctggtcaaa ggcttctacc ccagcgacat cgccgtggag 780
tgggagagca atgggcagcc ggagaacaac tacaagacca cgcctcccgt gctggactcc 840
gacggatcct tcttcctcta cagcaggcta accgtggaca agagcaggtg gcaggagggg 900
aatgtcttct catgctccgt gatgcatgag gctctgcaca accactacac acagaagagc 960
ctctccctgt ctctgggtaa a 981
<210> 150
<211> 981
<212> ДНК
<213> Homo Sapien
<400> 150
gcctccacca agggacctag cgtgttccct ctcgccccct gttccaggtc cacaagcgag 60
tccaccgctg ccctcggctg tctggtgaaa gactactttc ccgagcccgt gaccgtctcc 120
tggaatagcg gagccctgac ctccggcgtg cacacatttc ccgccgtgct gcagagcagc 180
ggactgtata gcctgagcag cgtggtgacc gtgcccagct ccagcctcgg caccaaaacc 240
tacacctgca acgtggacca caagccctcc aacaccaagg tggacaagcg ggtggagagc 300
aagtacggcc ccccttgccc tccttgtcct gcccctgagt tcgagggagg accctccgtg 360
ttcctgtttc cccccaaacc caaggacacc ctgatgatct cccggacacc cgaggtgacc 420
tgtgtggtcg tggacgtcag ccaggaggac cccgaggtgc agttcaactg gtatgtggac 480
ggcgtggagg tgcacaatgc caaaaccaag cccagggagg agcagttcaa ttccacctac 540
agggtggtga gcgtgctgac cgtcctgcat caggattggc tgaacggcaa ggagtacaag 600
tgcaaggtgt ccaacaaggg actgcccagc tccatcgaga agaccatcag caaggctaag 660
ggccagccga gggagcccca ggtgtatacc ctgcctccta gccaggaaga gatgaccaag 720
aaccaagtgt ccctgacctg cctggtgaag ggattctacc cctccgacat cgccgtggag 780
tgggagagca atggccagcc cgagaacaac tacaaaacaa cccctcccgt gctcgatagc 840
gacggcagct tctttctcta cagccggctg acagtggaca agagcaggtg gcaggagggc 900
aacgtgttct cctgttccgt gatgcacgag gccctgcaca atcactacac ccagaagagc 960
ctctccctgt ccctgggcaa g 981
<210> 151
<211> 981
<212> ДНК
<213> Homo Sapien
<400> 151
gccagcacca agggcccttc cgtgttcccc ctggcccctt gcagcaggag cacctccgaa 60
tccacagctg ccctgggctg tctggtgaag gactactttc ccgagcccgt gaccgtgagc 120
tggaacagcg gcgctctgac atccggcgtc cacacctttc ctgccgtcct gcagtcctcc 180
ggcctctact ccctgtcctc cgtggtgacc gtgcctagct cctccctcgg caccaagacc 240
tacacctgta acgtggacca caaaccctcc aacaccaagg tggacaaacg ggtcgagagc 300
aagtacggcc ctccctgccc tccttgtcct gcccccgagt tcgaaggcgg acccagcgtg 360
ttcctgttcc ctcctaagcc caaggacacc ctcatgatca gccggacacc cgaggtgacc 420
tgcgtggtgg tggatgtgag ccaggaggac cctgaggtcc agttcaactg gtatgtggat 480
ggcgtggagg tgcacaacgc caagacaaag ccccgggaag agcagttcaa ctccacctac 540
agggtggtca gcgtgctgac cgtgctgcat caggactggc tgaacggcaa ggagtacaag 600
tgcaaggtca gcaataaggg actgcccagc agcatcgaga agaccatctc caaggctaaa 660
ggccagcccc gggaacctca ggtgtacacc ctgcctccca gccaggagga gatgaccaag 720
aaccaggtga gcctgacctg cctggtgaag ggattctacc cttccgacat cgccgtggag 780
tgggagtcca acggccagcc cgagaacaat tataagacca cccctcccgt cctcgacagc 840
gacggatcct tctttctgta ctccaggctg accgtggata agtccaggtg gcaggaaggc 900
aacgtgttca gctgctccgt gatgcacgag gccctgcaca atcactacac ccagaagtcc 960
ctgagcctgt ccctgggaaa g 981
<210> 152
<211> 327
<212> Белок
<213> Homo Sapien
<400> 152
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro
100 105 110
Glu Phe Glu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
115 120 125
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
130 135 140
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
145 150 155 160
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
165 170 175
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
180 185 190
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
195 200 205
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
210 215 220
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
225 230 235 240
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
245 250 255
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
260 265 270
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
275 280 285
Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
290 295 300
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
305 310 315 320
Leu Ser Leu Ser Leu Gly Lys
325
<210> 153
<211> 981
<212> ДНК
<213> Homo Sapien
<400> 153
gcctccacca agggcccatc cgtcttcccc ctggcgccct gctccaggag cacctccgag 60
agcacggccg ccctgggctg cctggtcaag gactacttcc ccgaaccagt gacggtgtcg 120
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacgaagacc 240
tacacctgca acgtagatca caagcccagc aacaccaagg tggacaagag agttgagtcc 300
aaatatggtc ccccatgccc accatgccca gcgcctccag ttgcgggggg accatcagtc 360
ttcctgttcc ccccaaaacc caaggacact ctcatgatct cccggacccc tgaggtcacg 420
tgcgtggtgg tggacgtgag ccaggaagac cccgaggtcc agttcaactg gtacgtggat 480
ggcgtggagg tgcataatgc caagacaaag ccgcgggagg agcagttcaa cagcacgtac 540
cgtgtggtca gcgtcctcac cgtcctgcac caggactggc tgaacggcaa ggagtacaag 600
tgcaaggtct ccaacaaagg cctcccgtca tcgatcgaga aaaccatctc caaagccaaa 660
gggcagcccc gagagccaca ggtgtacacc ctgcccccat cccaggagga gatgaccaag 720
aaccaggtca gcctgacctg cctggtcaaa ggcttctacc ccagcgacat cgccgtggag 780
tgggagagca atgggcagcc ggagaacaac tacaagacca cgcctcccgt gctggactcc 840
gacggatcct tcttcctcta cagcaggcta accgtggaca agagcaggtg gcaggagggg 900
aatgtcttct catgctccgt gatgcatgag gctctgcaca accactacac acagaagagc 960
ctctccctgt ctctgggtaa a 981
<210> 154
<211> 327
<212> Белок
<213> Homo Sapien
<400> 154
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro
100 105 110
Pro Val Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
115 120 125
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
130 135 140
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
145 150 155 160
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
165 170 175
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
180 185 190
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
195 200 205
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
210 215 220
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
225 230 235 240
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
245 250 255
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
260 265 270
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
275 280 285
Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
290 295 300
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
305 310 315 320
Leu Ser Leu Ser Leu Gly Lys
325
<210> 155
<211> 321
<212> ДНК
<213> Homo Sapien
<400> 155
cgtacggtgg ccgctccctc cgtgttcatc ttcccacctt ccgacgagca gctgaagtcc 60
ggcaccgctt ctgtcgtgtg cctgctgaac aacttctacc cccgcgaggc caaggtgcag 120
tggaaggtgg acaacgccct gcagtccggc aactcccagg aatccgtgac cgagcaggac 180
tccaaggaca gcacctactc cctgtcctcc accctgaccc tgtccaaggc cgactacgag 240
aagcacaagg tgtacgcctg cgaagtgacc caccagggcc tgtctagccc cgtgaccaag 300
tctttcaacc ggggcgagtg t 321
<210> 156
<211> 107
<212> Белок
<213> Homo Sapien
<400> 156
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 157
<211> 321
<212> ДНК
<213> Homo Sapien
<400> 157
cgaactgtgg ctgcaccatc tgtcttcatc ttcccgccat ctgatgagca gttgaaatct 60
ggaactgcct ctgttgtgtg cctgctgaat aacttctatc ccagagaggc caaagtacag 120
tggaaggtgg ataacgccct ccaatcgggt aactcccagg agagtgtcac agagcaggag 180
agcaaggaca gcacctacag cctcagcagc accctgacgc tgagcaaagc agactacgag 240
aaacacaaag tctacgccgg cgaagtcacc catcagggcc tgagctcgcc cgtcacaaag 300
agcttcaaca ggggagagtg t 321
<210> 158
<211> 107
<212> Белок
<213> Homo Sapien
<400> 158
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Glu Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Gly Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 159
<211> 321
<212> ДНК
<213> Homo Sapien
<400> 159
cgaactgtgg ctgcaccatc tgtcttcatc ttcccgccat ctgatgagca gttgaaatct 60
ggaactgcct ctgttgtgtg cctgctgaat aacttctatc ccagagaggc caaagtacag 120
cggaaggtgg ataacgccct ccaatcgggt aactcccagg agagtgtcac agagcaggag 180
agcaaggaca gcacctacag cctcagcagc accctgacgc tgagcaaagc agactacgag 240
aaacacaaag tctacgcctg cgaagtcacc catcagggcc tgagctcgcc cgtcacaaag 300
agcttcaaca ggggagagtg t 321
<210> 160
<211> 107
<212> Белок
<213> Homo Sapien
<400> 160
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Arg Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Glu Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 161
<211> 321
<212> ДНК
<213> Homo Sapien
<400> 161
cgaactgtgg ctgcaccatc tgtcttcatc ttcccgccat ctgatgagca gttgaaatct 60
ggaactgcct ctgttgtgtg cctgctgaat aacttctatc ccagagaggc caaagtacag 120
tggaaggtgg ataacgccct ccaatcgggt aactcccagg agagtgtcac agagcaggac 180
agcaaggaca gcacctacag cctcagcagc accctgacgc tgagcaaagc agactacgag 240
aaacacaaac tctacgcctg cgaagtcacc catcagggcc tgagctcgcc cgtcacaaag 300
agcttcaaca ggggagagtg t 321
<210> 162
<211> 107
<212> Белок
<213> Homo Sapien
<400> 162
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Leu Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 163
<211> 321
<212> ДНК
<213> Homo Sapien
<400> 163
cgaactgtgg ctgcaccatc tgtcttcatc ttcccgccat ctgatgagca gttgaaatct 60
ggaactgcct ctgttgtgtg cctgctgaat aacttctatc ccagagaggc caaagtacag 120
tggaaggtgg ataacgccct ccaatcgggt aactcccagg agagtgtcac agagcaggac 180
agcaaggaca gcacctacag cctcagcaac accctgacgc tgagcaaagc agactacgag 240
aaacacaaag tctacgcctg cgaagtcacc catcagggcc tgagctcgcc cgtcacaaag 300
agcttcaaca ggggagagtg c 321
<210> 164
<211> 107
<212> Белок
<213> Homo Sapien
<400> 164
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Asn Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 165
<211> 312
<212> ДНК
<213> Homo Sapien
<400> 165
cccaaggcca accccacggt cactctgttc ccgccctcct ctgaggagct ccaagccaac 60
aaggccacac tagtgtgtct gatcagtgac ttctacccgg gagctgtgac agtggcttgg 120
aaggcagatg gcagccccgt caaggcggga gtggagacga ccaaaccctc caaacagagc 180
aacaacaagt acgcggccag cagctacctg agcctgacgc ccgagcagtg gaagtcccac 240
agaagctaca gctgccaggt cacgcatgaa gggagcaccg tggagaagac agtggcccct 300
acagaatgtt ca 312
<210> 166
<211> 104
<212> Белок
<213> Homo Sapien
<400> 166
Pro Lys Ala Asn Pro Thr Val Thr Leu Phe Pro Pro Ser Ser Glu Glu
1 5 10 15
Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe Tyr
20 25 30
Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Gly Ser Pro Val Lys
35 40 45
Ala Gly Val Glu Thr Thr Lys Pro Ser Lys Gln Ser Asn Asn Lys Tyr
50 55 60
Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser His
65 70 75 80
Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu Lys
85 90 95
Thr Val Ala Pro Thr Glu Cys Ser
100
<210> 167
<211> 318
<212> ДНК
<213> Homo Sapien
<400> 167
ggtcagccca aggccaaccc cactgtcact ctgttcccgc cctcctctga ggagctccaa 60
gccaacaagg ccacactagt gtgtctgatc agtgacttct acccgggagc tgtgacagtg 120
gcctggaagg cagatggcag ccccgtcaag gcgggagtgg agaccaccaa accctccaaa 180
cagagcaaca acaagtacgc ggccagcagc tacctgagcc tgacgcccga gcagtggaag 240
tcccacagaa gctacagctg ccaggtcacg catgaaggga gcaccgtgga gaagacagtg 300
gcccctacag aatgttca 318
<210> 168
<211> 318
<212> ДНК
<213> Homo Sapien
<400> 168
ggtcagccca aggccaaccc cactgtcact ctgttcccgc cctcctctga ggagctccaa 60
gccaacaagg ccacactagt gtgtctgatc agtgacttct acccgggagc tgtgacagtg 120
gcctggaagg cagatggcag ccccgtcaag gcgggagtgg agaccaccaa accctccaaa 180
cagagcaaca acaagtacgc ggccagcagc tacctgagcc tgacgcccga gcagtggaag 240
tcccacagaa gctacagctg ccaggtcacg catgaaggga gcaccgtgga gaagacagtg 300
gcccctacag aatgttca 318
<210> 169
<211> 106
<212> Белок
<213> Homo Sapien
<400> 169
Gly Gln Pro Lys Ala Asn Pro Thr Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp
20 25 30
Phe Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Gly Ser Pro
35 40 45
Val Lys Ala Gly Val Glu Thr Thr Lys Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Thr Glu Cys Ser
100 105
<210> 170
<211> 318
<212> ДНК
<213> Homo Sapien
<400> 170
ggccagccta aggccgctcc ttctgtgacc ctgttccccc catcctccga ggaactgcag 60
gctaacaagg ccaccctcgt gtgcctgatc agcgacttct accctggcgc cgtgaccgtg 120
gcctggaagg ctgatagctc tcctgtgaag gccggcgtgg aaaccaccac cccttccaag 180
cagtccaaca acaaatacgc cgcctcctcc tacctgtccc tgacccctga gcagtggaag 240
tcccaccggt cctacagctg ccaagtgacc cacgagggct ccaccgtgga aaagaccgtg 300
gctcctaccg agtgctcc 318
<210> 171
<211> 318
<212> ДНК
<213> Homo Sapien
<400> 171
ggccagccta aagctgcccc cagcgtcacc ctgtttcctc cctccagcga ggagctccag 60
gccaacaagg ccaccctcgt gtgcctgatc tccgacttct atcccggcgc tgtgaccgtg 120
gcttggaaag ccgactccag ccctgtcaaa gccggcgtgg agaccaccac accctccaag 180
cagtccaaca acaagtacgc cgcctccagc tatctctccc tgacccctga gcagtggaag 240
tcccaccggt cctactcctg tcaggtgacc cacgagggct ccaccgtgga aaagaccgtc 300
gcccccaccg agtgctcc 318
<210> 172
<211> 106
<212> Белок
<213> Homo Sapien
<400> 172
Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp
20 25 30
Phe Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro
35 40 45
Val Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Thr Glu Cys Ser
100 105
<210> 173
<211> 318
<212> ДНК
<213> Homo Sapien
<400> 173
ggtcagccca aggctgcccc ctcggtcact ctgttcccgc cctcctctga ggagcttcaa 60
gccaacaagg ccacactggt gtgtctcata agtgacttct acccgggagc cgtgacagtg 120
gcctggaagg cagatagcag ccccgtcaag gcgggagtgg agaccaccac accctccaaa 180
caaagcaaca acaagtacgc ggccagcagc tatctgagcc tgacgcctga gcagtggaag 240
tcccacagaa gctacagctg ccaggtcacg catgaaggga gcaccgtgga gaagacagtg 300
gcccctacag aatgttca 318
<210> 174
<211> 106
<212> Белок
<213> Homo Sapien
<400> 174
Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp
20 25 30
Phe Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro
35 40 45
Val Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Thr Glu Cys Ser
100 105
<210> 175
<211> 312
<212> ДНК
<213> Homo Sapien
<400> 175
cccaaggctg ccccctcggt cactctgttc ccaccctcct ctgaggagct tcaagccaac 60
aaggccacac tggtgtgtct cataagtgac ttctacccgg gagccgtgac agttgcctgg 120
aaggcagata gcagccccgt caaggcgggg gtggagacca ccacaccctc caaacaaagc 180
aacaacaagt acgcggccag cagctacctg agcctgacgc ctgagcagtg gaagtcccac 240
aaaagctaca gctgccaggt cacgcatgaa gggagcaccg tggagaagac agttgcccct 300
acggaatgtt ca 312
<210> 176
<211> 104
<212> Белок
<213> Homo Sapien
<400> 176
Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser Glu Glu
1 5 10 15
Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe Tyr
20 25 30
Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro Val Lys
35 40 45
Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn Lys Tyr
50 55 60
Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser His
65 70 75 80
Lys Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu Lys
85 90 95
Thr Val Ala Pro Thr Glu Cys Ser
100
<210> 177
<211> 318
<212> ДНК
<213> Homo Sapien
<400> 177
ggtcagccca aggctgcccc ctcggtcact ctgttcccac cctcctctga ggagcttcaa 60
gccaacaagg ccacactggt gtgtctcata agtgacttct acccggggcc agtgacagtt 120
gcctggaagg cagatagcag ccccgtcaag gcgggggtgg agaccaccac accctccaaa 180
caaagcaaca acaagtacgc ggccagcagc tacctgagcc tgacgcctga gcagtggaag 240
tcccacaaaa gctacagctg ccaggtcacg catgaaggga gcaccgtgga gaagacagtg 300
gcccctacgg aatgttca 318
<210> 178
<211> 106
<212> Белок
<213> Homo Sapien
<400> 178
Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp
20 25 30
Phe Tyr Pro Gly Pro Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro
35 40 45
Val Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Lys Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Thr Glu Cys Ser
100 105
<210> 179
<211> 318
<212> ДНК
<213> Homo Sapien
<400> 179
ggtcagccca aggctgcccc ctcggtcact ctgttcccac cctcctctga ggagcttcaa 60
gccaacaagg ccacactggt gtgtctcata agtgacttct acccgggagc cgtgacagtg 120
gcctggaagg cagatagcag ccccgtcaag gcgggagtgg agaccaccac accctccaaa 180
caaagcaaca acaagtacgc ggccagcagc tacctgagcc tgacgcctga gcagtggaag 240
tcccacaaaa gctacagctg ccaggtcacg catgaaggga gcaccgtgga gaagacagtg 300
gcccctacag aatgttca 318
<210> 180
<211> 106
<212> Белок
<213> Homo Sapien
<400> 180
Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp
20 25 30
Phe Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro
35 40 45
Val Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Lys Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Thr Glu Cys Ser
100 105
<210> 181
<211> 318
<212> ДНК
<213> Homo Sapien
<400> 181
ggtcagccca aggctgcccc ctcggtcact ctgttcccgc cctcctctga ggagcttcaa 60
gccaacaagg ccacactggt gtgtctcata agtgacttct acccgggagc cgtgacagtg 120
gcctggaagg cagatagcag ccccgtcaag gcgggagtgg agaccaccac accctccaaa 180
caaagcaaca acaagtacgc ggccagcagc tacctgagcc tgacgcctga gcagtggaag 240
tcccacagaa gctacagctg ccaggtcacg catgaaggga gcaccgtgga gaagacagtg 300
gcccctacag aatgttca 318
<210> 182
<211> 106
<212> Белок
<213> Homo Sapien
<400> 182
Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp
20 25 30
Phe Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro
35 40 45
Val Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Thr Glu Cys Ser
100 105
<210> 183
<211> 318
<212> ДНК
<213> Homo Sapien
<400> 183
ggtcagccca aggctgcccc atcggtcact ctgttcccgc cctcctctga ggagcttcaa 60
gccaacaagg ccacactggt gtgcctgatc agtgacttct acccgggagc tgtgaaagtg 120
gcctggaagg cagatggcag ccccgtcaac acgggagtgg agaccaccac accctccaaa 180
cagagcaaca acaagtacgc ggccagcagc tacctgagcc tgacgcctga gcagtggaag 240
tcccacagaa gctacagctg ccaggtcacg catgaaggga gcaccgtgga gaagacagtg 300
gcccctgcag aatgttca 318
<210> 184
<211> 106
<212> Белок
<213> Homo Sapien
<400> 184
Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp
20 25 30
Phe Tyr Pro Gly Ala Val Lys Val Ala Trp Lys Ala Asp Gly Ser Pro
35 40 45
Val Asn Thr Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Ala Glu Cys Ser
100 105
<210> 185
<211> 318
<212> ДНК
<213> Homo Sapien
<400> 185
ggtcagccca aggctgcccc atcggtcact ctgttcccac cctcctctga ggagcttcaa 60
gccaacaagg ccacactggt gtgtctcgta agtgacttct acccgggagc cgtgacagtg 120
gcctggaagg cagatggcag ccccgtcaag gtgggagtgg agaccaccaa accctccaaa 180
caaagcaaca acaagtatgc ggccagcagc tacctgagcc tgacgcccga gcagtggaag 240
tcccacagaa gctacagctg ccgggtcacg catgaaggga gcaccgtgga gaagacagtg 300
gcccctgcag aatgctct 318
<210> 186
<211> 106
<212> Белок
<213> Homo Sapien
<400> 186
Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Val Ser Asp
20 25 30
Phe Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Gly Ser Pro
35 40 45
Val Lys Val Gly Val Glu Thr Thr Lys Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Arg Ser Tyr Ser Cys Arg Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Ala Glu Cys Ser
100 105
<210> 187
<211> 318
<212> ДНК
<213> Homo Sapien
<400> 187
ggtcagccca aggctgcccc ctcggtcact ctgttcccac cctcctctga ggagcttcaa 60
gccaacaagg ccacactggt gtgtctcgta agtgacttca acccgggagc cgtgacagtg 120
gcctggaagg cagatggcag ccccgtcaag gtgggagtgg agaccaccaa accctccaaa 180
caaagcaaca acaagtatgc ggccagcagc tacctgagcc tgacgcccga gcagtggaag 240
tcccacagaa gctacagctg ccgggtcacg catgaaggga gcaccgtgga gaagacagtg 300
gcccctgcag aatgctct 318
<210> 188
<211> 106
<212> Белок
<213> Homo Sapien
<400> 188
Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Val Ser Asp
20 25 30
Phe Asn Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Gly Ser Pro
35 40 45
Val Lys Val Gly Val Glu Thr Thr Lys Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Arg Ser Tyr Ser Cys Arg Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Ala Glu Cys Ser
100 105
<210> 189
<211> 662
<212> Белок
<213> Homo Sapien
<400> 189
Gln Glu Asp Glu Asp Gly Asp Tyr Glu Glu Leu Val Leu Ala Leu Arg
1 5 10 15
Ser Glu Glu Asp Gly Leu Ala Glu Ala Pro Glu His Gly Thr Thr Ala
20 25 30
Thr Phe His Arg Cys Ala Lys Asp Pro Trp Arg Leu Pro Gly Thr Tyr
35 40 45
Val Val Val Leu Lys Glu Glu Thr His Leu Ser Gln Ser Glu Arg Thr
50 55 60
Ala Arg Arg Leu Gln Ala Gln Ala Ala Arg Arg Gly Tyr Leu Thr Lys
65 70 75 80
Ile Leu His Val Phe His Gly Leu Leu Pro Gly Phe Leu Val Lys Met
85 90 95
Ser Gly Asp Leu Leu Glu Leu Ala Leu Lys Leu Pro His Val Asp Tyr
100 105 110
Ile Glu Glu Asp Ser Ser Val Phe Ala Gln Ser Ile Pro Trp Asn Leu
115 120 125
Glu Arg Ile Thr Pro Pro Arg Tyr Arg Ala Asp Glu Tyr Gln Pro Pro
130 135 140
Asp Gly Gly Ser Leu Val Glu Val Tyr Leu Leu Asp Thr Ser Ile Gln
145 150 155 160
Ser Asp His Arg Glu Ile Glu Gly Arg Val Met Val Thr Asp Phe Glu
165 170 175
Asn Val Pro Glu Glu Asp Gly Thr Arg Phe His Arg Gln Ala Ser Lys
180 185 190
Cys Asp Ser His Gly Thr His Leu Ala Gly Val Val Ser Gly Arg Asp
195 200 205
Ala Gly Val Ala Lys Gly Ala Ser Met Arg Ser Leu Arg Val Leu Asn
210 215 220
Cys Gln Gly Lys Gly Thr Val Ser Gly Thr Leu Ile Gly Leu Glu Phe
225 230 235 240
Ile Arg Lys Ser Gln Leu Val Gln Pro Val Gly Pro Leu Val Val Leu
245 250 255
Leu Pro Leu Ala Gly Gly Tyr Ser Arg Val Leu Asn Ala Ala Cys Gln
260 265 270
Arg Leu Ala Arg Ala Gly Val Val Leu Val Thr Ala Ala Gly Asn Phe
275 280 285
Arg Asp Asp Ala Cys Leu Tyr Ser Pro Ala Ser Ala Pro Glu Val Ile
290 295 300
Thr Val Gly Ala Thr Asn Ala Gln Asp Gln Pro Val Thr Leu Gly Thr
305 310 315 320
Leu Gly Thr Asn Phe Gly Arg Cys Val Asp Leu Phe Ala Pro Gly Glu
325 330 335
Asp Ile Ile Gly Ala Ser Ser Asp Cys Ser Thr Cys Phe Val Ser Gln
340 345 350
Ser Gly Thr Ser Gln Ala Ala Ala His Val Ala Gly Ile Ala Ala Met
355 360 365
Met Leu Ser Ala Glu Pro Glu Leu Thr Leu Ala Glu Leu Arg Gln Arg
370 375 380
Leu Ile His Phe Ser Ala Lys Asp Val Ile Asn Glu Ala Trp Phe Pro
385 390 395 400
Glu Asp Gln Arg Val Leu Thr Pro Asn Leu Val Ala Ala Leu Pro Pro
405 410 415
Ser Thr His Gly Ala Gly Trp Gln Leu Phe Cys Arg Thr Val Trp Ser
420 425 430
Ala His Ser Gly Pro Thr Arg Met Ala Thr Ala Val Ala Arg Cys Ala
435 440 445
Pro Asp Glu Glu Leu Leu Ser Cys Ser Ser Phe Ser Arg Ser Gly Lys
450 455 460
Arg Arg Gly Glu Arg Met Glu Ala Gln Gly Gly Lys Leu Val Cys Arg
465 470 475 480
Ala His Asn Ala Phe Gly Gly Glu Gly Val Tyr Ala Ile Ala Arg Cys
485 490 495
Cys Leu Leu Pro Gln Ala Asn Cys Ser Val His Thr Ala Pro Pro Ala
500 505 510
Glu Ala Ser Met Gly Thr Arg Val His Cys His Gln Gln Gly His Val
515 520 525
Leu Thr Gly Cys Ser Ser His Trp Glu Val Glu Asp Leu Gly Thr His
530 535 540
Lys Pro Pro Val Leu Arg Pro Arg Gly Gln Pro Asn Gln Cys Val Gly
545 550 555 560
His Arg Glu Ala Ser Ile His Ala Ser Cys Cys His Ala Pro Gly Leu
565 570 575
Glu Cys Lys Val Lys Glu His Gly Ile Pro Ala Pro Gln Glu Gln Val
580 585 590
Thr Val Ala Cys Glu Glu Gly Trp Thr Leu Thr Gly Cys Ser Ala Leu
595 600 605
Pro Gly Thr Ser His Val Leu Gly Ala Tyr Ala Val Asp Asn Thr Cys
610 615 620
Val Val Arg Ser Arg Asp Val Ser Thr Thr Gly Ser Thr Ser Glu Gly
625 630 635 640
Ala Val Thr Ala Val Ala Ile Cys Cys Arg Ser Arg His Leu Ala Gln
645 650 655
Ala Ser Gln Glu Leu Gln
660
<210> 190
<211> 662
<212> Белок
<213> Homo Sapien
<400> 190
Gln Glu Asp Glu Asp Gly Asp Tyr Glu Glu Leu Val Leu Ala Leu Arg
1 5 10 15
Ser Glu Glu Asp Gly Leu Ala Glu Ala Pro Glu His Gly Thr Thr Ala
20 25 30
Thr Phe His Arg Cys Ala Lys Asp Pro Trp Arg Leu Pro Gly Thr Tyr
35 40 45
Val Val Val Leu Lys Glu Glu Thr His Leu Ser Gln Ser Glu Arg Thr
50 55 60
Ala Arg Arg Leu Gln Ala Gln Ala Ala Arg Arg Gly Tyr Leu Thr Lys
65 70 75 80
Ile Leu His Val Phe His Gly Leu Leu Pro Gly Phe Leu Val Lys Met
85 90 95
Ser Gly Asp Leu Leu Glu Leu Ala Leu Lys Leu Pro His Val Asp Tyr
100 105 110
Ile Glu Glu Asp Ser Ser Val Phe Ala Gln Ser Ile Pro Trp Asn Leu
115 120 125
Glu Arg Ile Thr Pro Pro Arg Tyr Arg Ala Asp Glu Tyr Gln Pro Pro
130 135 140
Asp Gly Gly Ser Leu Val Glu Val Tyr Leu Leu Asp Thr Ser Ile Gln
145 150 155 160
Ser Asp His Arg Glu Ile Glu Gly Arg Val Met Val Thr Asp Phe Glu
165 170 175
Asn Val Pro Glu Glu Asp Gly Thr Arg Phe His Arg Gln Ala Ser Lys
180 185 190
Cys Asp Ser His Gly Thr His Leu Ala Gly Val Val Ser Gly Arg Asp
195 200 205
Ala Gly Val Ala Lys Gly Ala Ser Met Arg Ser Leu Arg Val Leu Asn
210 215 220
Cys Gln Gly Lys Gly Thr Val Ser Gly Thr Leu Ile Gly Leu Glu Phe
225 230 235 240
Ile Arg Lys Ser Gln Leu Val Gln Pro Val Gly Pro Leu Val Val Leu
245 250 255
Leu Pro Leu Ala Gly Gly Tyr Ser Arg Val Leu Asn Ala Ala Cys Gln
260 265 270
Arg Leu Ala Arg Ala Gly Val Val Leu Val Thr Ala Ala Gly Asn Phe
275 280 285
Arg Asp Asp Ala Cys Leu Tyr Ser Pro Ala Ser Ala Pro Glu Val Ile
290 295 300
Thr Val Gly Ala Thr Asn Ala Gln Asp Gln Pro Val Thr Leu Gly Thr
305 310 315 320
Leu Gly Thr Asn Phe Gly Arg Cys Val Asp Leu Phe Ala Pro Gly Glu
325 330 335
Asp Ile Ile Gly Ala Ser Ser Asp Cys Ser Thr Cys Phe Val Ser Gln
340 345 350
Ser Gly Thr Ser Gln Ala Ala Ala His Val Ala Gly Ile Ala Ala Met
355 360 365
Met Leu Ser Ala Glu Pro Glu Leu Thr Leu Ala Glu Leu Arg Gln Arg
370 375 380
Leu Ile His Phe Ser Ala Lys Asp Val Ile Asn Glu Ala Trp Phe Pro
385 390 395 400
Glu Asp Gln Arg Val Leu Thr Pro Asn Leu Val Ala Ala Leu Pro Pro
405 410 415
Ser Thr His Gly Ala Gly Trp Gln Leu Phe Cys Arg Thr Val Trp Ser
420 425 430
Ala His Ser Gly Pro Thr Arg Met Ala Thr Ala Ile Ala Arg Cys Ala
435 440 445
Pro Asp Glu Glu Leu Leu Ser Cys Ser Ser Phe Ser Arg Ser Gly Lys
450 455 460
Arg Arg Gly Glu Arg Met Glu Ala Gln Gly Gly Lys Leu Val Cys Arg
465 470 475 480
Ala His Asn Ala Phe Gly Gly Glu Gly Val Tyr Ala Ile Ala Arg Cys
485 490 495
Cys Leu Leu Pro Gln Ala Asn Cys Ser Val His Thr Ala Pro Pro Ala
500 505 510
Glu Ala Ser Met Gly Thr Arg Val His Cys His Gln Gln Gly His Val
515 520 525
Leu Thr Gly Cys Ser Ser His Trp Glu Val Glu Asp Leu Gly Thr His
530 535 540
Lys Pro Pro Val Leu Arg Pro Arg Gly Gln Pro Asn Gln Cys Val Gly
545 550 555 560
His Arg Glu Ala Ser Ile His Ala Ser Cys Cys His Ala Pro Gly Leu
565 570 575
Glu Cys Lys Val Lys Glu His Gly Ile Pro Ala Pro Gln Glu Gln Val
580 585 590
Thr Val Ala Cys Glu Glu Gly Trp Thr Leu Thr Gly Cys Ser Ala Leu
595 600 605
Pro Gly Thr Ser His Val Leu Gly Ala Tyr Ala Val Asp Asn Thr Cys
610 615 620
Val Val Arg Ser Arg Asp Val Ser Thr Thr Gly Ser Thr Ser Glu Glu
625 630 635 640
Ala Val Thr Ala Val Ala Ile Cys Cys Arg Ser Arg His Leu Ala Gln
645 650 655
Ala Ser Gln Glu Leu Gln
660
<210> 191
<211> 662
<212> Белок
<213> Homo Sapien
<400> 191
Gln Glu Asp Glu Asp Gly Asp Tyr Glu Glu Leu Val Leu Ala Leu Arg
1 5 10 15
Ser Glu Glu Asp Gly Leu Val Glu Ala Pro Glu His Gly Thr Thr Ala
20 25 30
Thr Phe His Arg Cys Ala Lys Asp Pro Trp Arg Leu Pro Gly Thr Tyr
35 40 45
Val Val Val Leu Lys Glu Glu Thr His Leu Ser Gln Ser Glu Arg Thr
50 55 60
Ala Arg Arg Leu Gln Ala Gln Ala Ala Arg Arg Gly Tyr Leu Thr Lys
65 70 75 80
Ile Leu His Val Phe His Gly Leu Leu Pro Gly Phe Leu Val Lys Met
85 90 95
Ser Gly Asp Leu Leu Glu Leu Ala Leu Lys Leu Pro His Val Asp Tyr
100 105 110
Ile Glu Glu Asp Ser Ser Val Phe Ala Gln Ser Ile Pro Trp Asn Leu
115 120 125
Glu Arg Ile Thr Pro Pro Arg Tyr Arg Ala Asp Glu Tyr Gln Pro Pro
130 135 140
Asp Gly Gly Ser Leu Val Glu Val Tyr Leu Leu Asp Thr Ser Ile Gln
145 150 155 160
Ser Asp His Arg Glu Ile Glu Gly Arg Val Met Val Thr Asp Phe Glu
165 170 175
Asn Val Pro Glu Glu Asp Gly Thr Arg Phe His Arg Gln Ala Ser Lys
180 185 190
Cys Asp Ser His Gly Thr His Leu Ala Gly Val Val Ser Gly Arg Asp
195 200 205
Ala Gly Val Ala Lys Gly Ala Ser Met Arg Ser Leu Arg Val Leu Asn
210 215 220
Cys Gln Gly Lys Gly Thr Val Ser Gly Thr Leu Ile Gly Leu Glu Phe
225 230 235 240
Ile Arg Lys Ser Gln Leu Val Gln Pro Val Gly Pro Leu Val Val Leu
245 250 255
Leu Pro Leu Ala Gly Gly Tyr Ser Arg Val Leu Asn Ala Ala Cys Gln
260 265 270
Arg Leu Ala Arg Ala Gly Val Val Leu Val Thr Ala Ala Gly Asn Phe
275 280 285
Arg Asp Asp Ala Cys Leu Tyr Ser Pro Ala Ser Ala Pro Glu Val Ile
290 295 300
Thr Val Gly Ala Thr Asn Ala Gln Asp Gln Pro Val Thr Leu Gly Thr
305 310 315 320
Leu Gly Thr Asn Phe Gly Arg Cys Val Asp Leu Phe Ala Pro Gly Glu
325 330 335
Asp Ile Ile Gly Ala Ser Ser Asp Cys Ser Thr Cys Phe Val Ser Gln
340 345 350
Ser Gly Thr Ser Gln Ala Ala Ala His Val Ala Gly Ile Ala Ala Met
355 360 365
Met Leu Ser Ala Glu Pro Glu Leu Thr Leu Ala Glu Leu Arg Gln Arg
370 375 380
Leu Ile His Phe Ser Ala Lys Asp Val Ile Asn Glu Ala Trp Phe Pro
385 390 395 400
Glu Asp Gln Arg Val Leu Thr Pro Asn Leu Val Ala Ala Leu Pro Pro
405 410 415
Ser Thr His Gly Ala Gly Trp Gln Leu Phe Cys Arg Thr Val Trp Ser
420 425 430
Ala His Ser Gly Pro Thr Arg Met Ala Thr Ala Ile Ala Arg Cys Ala
435 440 445
Pro Asp Glu Glu Leu Leu Ser Cys Ser Ser Phe Ser Arg Ser Gly Lys
450 455 460
Arg Arg Gly Glu Arg Met Glu Ala Gln Gly Gly Lys Leu Val Cys Arg
465 470 475 480
Ala His Asn Ala Phe Gly Gly Glu Gly Val Tyr Ala Ile Ala Arg Cys
485 490 495
Cys Leu Leu Pro Gln Ala Asn Cys Ser Val His Thr Ala Pro Pro Ala
500 505 510
Glu Ala Ser Met Gly Thr Arg Val His Cys His Gln Gln Gly His Val
515 520 525
Leu Thr Gly Cys Ser Ser His Trp Glu Val Glu Asp Leu Gly Thr His
530 535 540
Lys Pro Pro Val Leu Arg Pro Arg Gly Gln Pro Asn Gln Cys Val Gly
545 550 555 560
His Arg Glu Ala Ser Ile His Ala Ser Cys Cys His Ala Pro Gly Leu
565 570 575
Glu Cys Lys Val Lys Glu His Gly Ile Pro Ala Pro Gln Glu Gln Val
580 585 590
Thr Val Ala Cys Glu Glu Gly Trp Thr Leu Thr Gly Cys Ser Ala Leu
595 600 605
Pro Gly Thr Ser His Val Leu Gly Ala Tyr Ala Val Asp Asn Thr Cys
610 615 620
Val Val Arg Ser Arg Asp Val Ser Thr Thr Gly Ser Thr Ser Glu Glu
625 630 635 640
Ala Val Thr Ala Val Ala Ile Cys Cys Arg Ser Arg His Leu Ala Gln
645 650 655
Ala Ser Gln Glu Leu Gln
660
<210> 192
<211> 662
<212> Белок
<213> Homo Sapien
<400> 192
Gln Glu Asp Glu Asp Gly Asp Tyr Glu Glu Leu Val Leu Ala Leu Arg
1 5 10 15
Ser Glu Glu Asp Gly Leu Ala Glu Ala Pro Glu His Gly Thr Thr Ala
20 25 30
Thr Phe His Arg Cys Ala Lys Asp Pro Trp Arg Leu Pro Gly Thr Tyr
35 40 45
Val Val Val Leu Lys Glu Glu Thr His Leu Ser Gln Ser Glu Arg Thr
50 55 60
Ala Arg Arg Leu Gln Ala Gln Ala Ala Arg Arg Gly Tyr Leu Thr Lys
65 70 75 80
Ile Leu His Val Phe His Gly Leu Leu Pro Gly Phe Leu Val Lys Met
85 90 95
Ser Gly Asp Leu Leu Glu Leu Ala Leu Lys Leu Pro His Val Asp Tyr
100 105 110
Ile Glu Glu Asp Ser Ser Val Phe Ala Gln Ser Ile Pro Trp Asn Leu
115 120 125
Glu Arg Ile Thr Pro Pro Arg Tyr Arg Ala Asp Glu Tyr Gln Pro Pro
130 135 140
Asp Gly Gly Ser Leu Val Glu Val Tyr Leu Leu Asp Thr Ser Ile Gln
145 150 155 160
Ser Asp His Arg Glu Ile Glu Gly Arg Val Met Val Thr Asp Phe Glu
165 170 175
Asn Val Pro Glu Glu Asp Gly Thr Arg Phe His Arg Gln Ala Ser Lys
180 185 190
Cys Asp Ser His Gly Thr His Leu Ala Gly Val Val Ser Gly Arg Asp
195 200 205
Ala Gly Val Ala Lys Gly Ala Ser Met Arg Ser Leu Arg Val Leu Asn
210 215 220
Cys Gln Gly Lys Gly Thr Val Ser Gly Thr Leu Ile Gly Leu Glu Phe
225 230 235 240
Ile Arg Lys Ser Gln Leu Val Gln Pro Val Gly Pro Leu Val Val Leu
245 250 255
Leu Pro Leu Ala Gly Gly Tyr Ser Arg Val Leu Asn Ala Ala Cys Gln
260 265 270
Arg Leu Ala Arg Ala Gly Val Val Leu Val Thr Ala Ala Gly Asn Phe
275 280 285
Arg Asp Asp Ala Cys Leu Tyr Ser Pro Ala Ser Ala Pro Glu Val Ile
290 295 300
Thr Val Gly Ala Thr Asn Ala Gln Asp Gln Pro Val Thr Leu Gly Thr
305 310 315 320
Leu Gly Thr Asn Phe Gly Arg Cys Val Asp Leu Phe Ala Pro Gly Glu
325 330 335
Asp Ile Ile Gly Ala Ser Ser Tyr Cys Ser Thr Cys Phe Val Ser Gln
340 345 350
Ser Gly Thr Ser Gln Ala Ala Ala His Val Ala Gly Ile Ala Ala Met
355 360 365
Met Leu Ser Ala Glu Pro Glu Leu Thr Leu Ala Glu Leu Arg Gln Arg
370 375 380
Leu Ile His Phe Ser Ala Lys Asp Val Ile Asn Glu Ala Trp Phe Pro
385 390 395 400
Glu Asp Gln Arg Val Leu Thr Pro Asn Leu Val Ala Ala Leu Pro Pro
405 410 415
Ser Thr His Gly Ala Gly Trp Gln Leu Phe Cys Arg Thr Val Trp Ser
420 425 430
Ala His Ser Gly Pro Thr Arg Met Ala Thr Ala Val Ala Arg Cys Ala
435 440 445
Pro Asp Glu Glu Leu Leu Ser Cys Ser Ser Phe Ser Arg Ser Gly Lys
450 455 460
Arg Arg Gly Glu Arg Met Glu Ala Gln Gly Gly Lys Leu Val Cys Arg
465 470 475 480
Ala His Asn Ala Phe Gly Gly Glu Gly Val Tyr Ala Ile Ala Arg Cys
485 490 495
Cys Leu Leu Pro Gln Ala Asn Cys Ser Val His Thr Ala Pro Pro Ala
500 505 510
Glu Ala Ser Met Gly Thr Arg Val His Cys His Gln Gln Gly His Val
515 520 525
Leu Thr Gly Cys Ser Ser His Trp Glu Val Glu Asp Leu Gly Thr His
530 535 540
Lys Pro Pro Val Leu Arg Pro Arg Gly Gln Pro Asn Gln Cys Val Gly
545 550 555 560
His Arg Glu Ala Ser Ile His Ala Ser Cys Cys His Ala Pro Gly Leu
565 570 575
Glu Cys Lys Val Lys Glu His Gly Ile Pro Ala Pro Gln Glu Gln Val
580 585 590
Thr Val Ala Cys Glu Glu Gly Trp Thr Leu Thr Gly Cys Ser Ala Leu
595 600 605
Pro Gly Thr Ser His Val Leu Gly Ala Tyr Ala Val Asp Asn Thr Cys
610 615 620
Val Val Arg Ser Arg Asp Val Ser Thr Thr Gly Ser Thr Ser Glu Gly
625 630 635 640
Ala Val Thr Ala Val Ala Ile Cys Cys Arg Ser Arg His Leu Ala Gln
645 650 655
Ala Ser Gln Glu Leu Gln
660
<210> 193
<211> 662
<212> Белок
<213> Homo Sapien
<400> 193
Gln Glu Asp Glu Asp Gly Asp Tyr Glu Glu Leu Val Leu Ala Leu Arg
1 5 10 15
Ser Glu Glu Asp Gly Leu Ala Asp Ala Pro Glu His Gly Ala Thr Ala
20 25 30
Thr Phe His Arg Cys Ala Lys Asp Pro Trp Arg Leu Pro Gly Thr Tyr
35 40 45
Val Val Val Leu Lys Glu Glu Thr His Arg Ser Gln Ser Glu Arg Thr
50 55 60
Ala Arg Arg Leu Gln Ala Gln Ala Ala Arg Arg Gly Tyr Leu Thr Lys
65 70 75 80
Ile Leu His Val Phe His His Leu Leu Pro Gly Phe Leu Val Lys Met
85 90 95
Ser Gly Asp Leu Leu Glu Leu Ala Leu Lys Leu Pro His Val Asp Tyr
100 105 110
Ile Glu Glu Asp Ser Ser Val Phe Ala Gln Ser Ile Pro Trp Asn Leu
115 120 125
Glu Arg Ile Thr Pro Ala Arg Tyr Arg Ala Asp Glu Tyr Gln Pro Pro
130 135 140
Lys Gly Gly Ser Leu Val Glu Val Tyr Leu Leu Asp Thr Ser Ile Gln
145 150 155 160
Ser Asp His Arg Glu Ile Glu Gly Arg Val Met Val Thr Asp Phe Glu
165 170 175
Ser Val Pro Glu Glu Asp Gly Thr Arg Phe His Arg Gln Ala Ser Lys
180 185 190
Cys Asp Ser His Gly Thr His Leu Ala Gly Val Val Ser Gly Arg Asp
195 200 205
Ala Gly Val Ala Lys Gly Ala Gly Leu Arg Ser Leu Arg Val Leu Asn
210 215 220
Cys Gln Gly Lys Gly Thr Val Ser Gly Thr Leu Ile Gly Leu Glu Phe
225 230 235 240
Ile Arg Lys Ser Gln Leu Val Gln Pro Val Gly Pro Leu Val Val Leu
245 250 255
Leu Pro Leu Ala Gly Gly Tyr Ser Arg Val Phe Asn Ala Ala Cys Gln
260 265 270
Arg Leu Ala Arg Ala Gly Val Val Leu Val Thr Ala Ala Gly Asn Phe
275 280 285
Arg Asp Asp Ala Cys Leu Tyr Ser Pro Ala Ser Ala Pro Glu Val Ile
290 295 300
Thr Val Gly Ala Thr Asn Ala Gln Asp Gln Pro Val Thr Leu Gly Thr
305 310 315 320
Leu Gly Thr Asn Phe Gly Arg Cys Val Asp Leu Phe Ala Pro Gly Glu
325 330 335
Asp Ile Ile Gly Ala Ser Ser Asp Cys Ser Thr Cys Phe Val Ser Arg
340 345 350
Ser Gly Thr Ser Gln Ala Ala Ala His Val Ala Gly Ile Ala Ala Met
355 360 365
Met Leu Ser Ala Glu Pro Glu Leu Thr Leu Ala Glu Leu Arg Gln Arg
370 375 380
Leu Ile His Phe Ser Ala Lys Asp Val Ile Asn Glu Ala Trp Phe Pro
385 390 395 400
Glu Asp Gln Arg Val Leu Thr Pro Asn Leu Val Ala Ala Leu Pro Pro
405 410 415
Ser Thr His Arg Ala Gly Trp Gln Leu Phe Cys Arg Thr Val Trp Ser
420 425 430
Ala His Ser Gly Pro Thr Arg Met Ala Thr Ala Val Ala Arg Cys Ala
435 440 445
Gln Asp Glu Glu Leu Leu Ser Cys Ser Ser Phe Ser Arg Ser Gly Lys
450 455 460
Arg Arg Gly Glu Arg Ile Glu Ala Gln Gly Gly Lys Arg Val Cys Arg
465 470 475 480
Ala His Asn Ala Phe Gly Gly Glu Gly Val Tyr Ala Ile Ala Arg Cys
485 490 495
Cys Leu Leu Pro Gln Val Asn Cys Ser Val His Thr Ala Pro Pro Ala
500 505 510
Gly Ala Ser Met Gly Thr Arg Val His Cys His Gln Gln Gly His Val
515 520 525
Leu Thr Gly Cys Ser Ser His Trp Glu Val Glu Asp Leu Gly Thr His
530 535 540
Lys Pro Pro Val Leu Arg Pro Arg Gly Gln Pro Asn Gln Cys Val Gly
545 550 555 560
His Arg Glu Ala Ser Ile His Ala Ser Cys Cys His Ala Pro Gly Leu
565 570 575
Glu Cys Lys Val Lys Glu His Gly Ile Pro Ala Pro Gln Glu Gln Val
580 585 590
Ile Val Ala Cys Glu Asp Gly Trp Thr Leu Thr Gly Cys Ser Ala Leu
595 600 605
Pro Gly Thr Ser His Val Leu Gly Ala Tyr Ala Val Asp Asn Thr Cys
610 615 620
Val Val Arg Ser Arg Asp Val Ser Thr Thr Gly Ser Thr Ser Glu Glu
625 630 635 640
Ala Val Ala Ala Val Ala Ile Cys Cys Arg Ser Arg His Leu Val Gln
645 650 655
Ala Ser Gln Glu Leu Gln
660
<210> 194
<211> 660
<212> Белок
<213> Mus Musculus
<400> 194
Gln Asp Glu Asp Gly Asp Tyr Glu Glu Leu Met Leu Ala Leu Pro Ser
1 5 10 15
Gln Glu Asp Gly Leu Ala Asp Glu Ala Ala His Val Ala Thr Ala Thr
20 25 30
Phe Arg Arg Cys Ser Lys Glu Ala Trp Arg Leu Pro Gly Thr Tyr Ile
35 40 45
Val Val Leu Met Glu Glu Thr Gln Arg Leu Gln Ile Glu Gln Thr Ala
50 55 60
His Arg Leu Gln Thr Arg Ala Ala Arg Arg Gly Tyr Val Ile Lys Val
65 70 75 80
Leu His Ile Phe Tyr Asp Leu Phe Pro Gly Phe Leu Val Lys Met Ser
85 90 95
Ser Asp Leu Leu Gly Leu Ala Leu Lys Leu Pro His Val Glu Tyr Ile
100 105 110
Glu Glu Asp Ser Phe Val Phe Ala Gln Ser Ile Pro Trp Asn Leu Glu
115 120 125
Arg Ile Ile Pro Ala Trp His Gln Thr Glu Glu Asp Arg Ser Pro Asp
130 135 140
Gly Ser Ser Gln Val Glu Val Tyr Leu Leu Asp Thr Ser Ile Gln Gly
145 150 155 160
Ala His Arg Glu Ile Glu Gly Arg Val Thr Ile Thr Asp Phe Asn Ser
165 170 175
Val Pro Glu Glu Asp Gly Thr Arg Phe His Arg Gln Ala Ser Lys Cys
180 185 190
Asp Ser His Gly Thr His Leu Ala Gly Val Val Ser Gly Arg Asp Ala
195 200 205
Gly Val Ala Lys Gly Thr Ser Leu His Ser Leu Arg Val Leu Asn Cys
210 215 220
Gln Gly Lys Gly Thr Val Ser Gly Thr Leu Ile Gly Leu Glu Phe Ile
225 230 235 240
Arg Lys Ser Gln Leu Ile Gln Pro Ser Gly Pro Leu Val Val Leu Leu
245 250 255
Pro Leu Ala Gly Gly Tyr Ser Arg Ile Leu Asn Ala Ala Cys Arg His
260 265 270
Leu Ala Arg Thr Gly Val Val Leu Val Ala Ala Ala Gly Asn Phe Arg
275 280 285
Asp Asp Ala Cys Leu Tyr Ser Pro Ala Ser Ala Pro Glu Val Ile Thr
290 295 300
Val Gly Ala Thr Asn Ala Gln Asp Gln Pro Val Thr Leu Gly Thr Leu
305 310 315 320
Gly Thr Asn Phe Gly Arg Cys Val Asp Leu Phe Ala Pro Gly Lys Asp
325 330 335
Ile Ile Gly Ala Ser Ser Asp Cys Ser Thr Cys Phe Met Ser Gln Ser
340 345 350
Gly Thr Ser Gln Ala Ala Ala His Val Ala Gly Ile Val Ala Arg Met
355 360 365
Leu Ser Arg Glu Pro Thr Leu Thr Leu Ala Glu Leu Arg Gln Arg Leu
370 375 380
Ile His Phe Ser Thr Lys Asp Val Ile Asn Met Ala Trp Phe Pro Glu
385 390 395 400
Asp Gln Gln Val Leu Thr Pro Asn Leu Val Ala Thr Leu Pro Pro Ser
405 410 415
Thr His Glu Thr Gly Gly Gln Leu Leu Cys Arg Thr Val Trp Ser Ala
420 425 430
His Ser Gly Pro Thr Arg Thr Ala Thr Ala Thr Ala Arg Cys Ala Pro
435 440 445
Glu Glu Glu Leu Leu Ser Cys Ser Ser Phe Ser Arg Ser Gly Arg Arg
450 455 460
Arg Gly Asp Trp Ile Glu Ala Ile Gly Gly Gln Gln Val Cys Lys Ala
465 470 475 480
Leu Asn Ala Phe Gly Gly Glu Gly Val Tyr Ala Val Ala Arg Cys Cys
485 490 495
Leu Val Pro Arg Ala Asn Cys Ser Ile His Asn Thr Pro Ala Ala Arg
500 505 510
Ala Gly Leu Glu Thr His Val His Cys His Gln Lys Asp His Val Leu
515 520 525
Thr Gly Cys Ser Phe His Trp Glu Val Glu Asp Leu Ser Val Arg Arg
530 535 540
Gln Pro Ala Leu Arg Ser Arg Arg Gln Pro Gly Gln Cys Val Gly His
545 550 555 560
Gln Ala Ala Ser Val Tyr Ala Ser Cys Cys His Ala Pro Gly Leu Glu
565 570 575
Cys Lys Ile Lys Glu His Gly Ile Ser Gly Pro Ser Glu Gln Val Thr
580 585 590
Val Ala Cys Glu Ala Gly Trp Thr Leu Thr Gly Cys Asn Val Leu Pro
595 600 605
Gly Ala Ser Leu Thr Leu Gly Ala Tyr Ser Val Asp Asn Leu Cys Val
610 615 620
Ala Arg Val His Asp Thr Ala Arg Ala Asp Arg Thr Ser Gly Glu Ala
625 630 635 640
Thr Val Ala Ala Ala Ile Cys Cys Arg Ser Arg Pro Ser Ala Lys Ala
645 650 655
Ser Trp Val Gln
660
<210> 195
<211> 445
<212> Белок
<213> Homo Sapien
<400> 195
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Asn Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Asp Trp Val
35 40 45
Ser Thr Ile Ser Gly Ser Gly Gly Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Ile Ile Ser Arg Asp Ser Ser Lys His Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Ser Asn Trp Gly Asn Phe Asp Leu Trp Gly Arg Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys
210 215 220
Pro Pro Cys Pro Ala Pro Glu Phe Glu Gly Gly Pro Ser Val Phe Leu
225 230 235 240
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
245 250 255
Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln
260 265 270
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
275 280 285
Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu
290 295 300
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
305 310 315 320
Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys
325 330 335
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
340 345 350
Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
355 360 365
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
370 375 380
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
385 390 395 400
Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln
405 410 415
Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
420 425 430
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440 445
<210> 196
<211> 220
<212> Белок
<213> Homo Sapien
<400> 196
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Val Leu Tyr Arg
20 25 30
Ser Asn Asn Arg Asn Phe Leu Gly Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Asn Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Tyr Tyr Thr Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile
100 105 110
Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp
115 120 125
Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn
130 135 140
Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu
145 150 155 160
Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp
165 170 175
Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr
180 185 190
Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser
195 200 205
Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215 220
<210> 197
<211> 454
<212> Белок
<213> Homo Sapien
<400> 197
Glu Met Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser His
20 25 30
Trp Met Lys Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asn Ile Asn Gln Asp Gly Ser Glu Lys Tyr Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ile Val Leu Met Val Tyr His Met Asp Tyr Tyr Tyr Tyr
100 105 110
Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala
115 120 125
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser
130 135 140
Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
145 150 155 160
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
165 170 175
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
180 185 190
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr
195 200 205
Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg
210 215 220
Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu
225 230 235 240
Phe Glu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
260 265 270
Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly
275 280 285
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn
290 295 300
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
305 310 315 320
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro
325 330 335
Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
340 345 350
Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg
405 410 415
Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Leu Gly Lys
450
<210> 198
<211> 219
<212> Белок
<213> Homo Sapien
<400> 198
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu His His Ser
20 25 30
Asn Gly Asn Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Thr
85 90 95
Leu Gln Thr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 199
<211> 116
<212> Белок
<213> Homo Sapien
<400> 199
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gly
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Gly Ser Ile Ser Ser Ser
20 25 30
Lys Trp Trp Ser Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Glu Thr His Tyr Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Lys Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Arg Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Gly Ala Thr Glu Asn Phe Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 200
<211> 348
<212> ДНК
<213> Homo Sapien
<400> 200
caggtgcagc tgcaggagtc gggcccagga ctggtgaagc cttcggggac cctgtccctc 60
acctgcgctg tctctggtgg ctccatcagc agtagtaaat ggtggagttg ggtccgccag 120
cccccaggga aggggctgga gtggattggg gaaacccatt atagtgggag caccaactac 180
aacccgtccc tcaagagtcg agtcaccata tcagtagaca agtccaagaa ccagttctcc 240
ctgaagctga ggtctgtgac cgccgcggac acggccgttt attactgtgc gagagtgggt 300
gctactgaga acttctgggg ccagggaacc ctggtcaccg tctcctca 348
<210> 201
<211> 25
<212> Белок
<213> Homo Sapien
<400> 201
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gly
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser
20 25
<210> 202
<211> 75
<212> ДНК
<213> Homo Sapien
<400> 202
caggtgcagc tgcaggagtc gggcccagga ctggtgaagc cttcggggac cctgtccctc 60
acctgcgctg tctct 75
<210> 203
<211> 9
<212> Белок
<213> Homo Sapien
<400> 203
Gly Gly Ser Ile Ser Ser Ser Lys Trp
1 5
<210> 204
<211> 27
<212> ДНК
<213> Homo Sapien
<400> 204
ggtggctcca tcagcagtag taaatgg 27
<210> 205
<211> 17
<212> Белок
<213> Homo Sapien
<400> 205
Trp Ser Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
1 5 10 15
Glu
<210> 206
<211> 51
<212> ДНК
<213> Homo Sapien
<400> 206
tggagttggg tccgccagcc cccagggaag gggctggagt ggattgggga a 51
<210> 207
<211> 7
<212> Белок
<213> Homo Sapien
<400> 207
Thr His Tyr Ser Gly Ser Thr
1 5
<210> 208
<211> 21
<212> ДНК
<213> Homo Sapien
<400> 208
acccattata gtgggagcac c 21
<210> 209
<211> 38
<212> Белок
<213> Homo Sapien
<400> 209
Asn Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Lys
1 5 10 15
Ser Lys Asn Gln Phe Ser Leu Lys Leu Arg Ser Val Thr Ala Ala Asp
20 25 30
Thr Ala Val Tyr Tyr Cys
35
<210> 210
<211> 114
<212> ДНК
<213> Homo Sapien
<400> 210
aactacaacc cgtccctcaa gagtcgagtc accatatcag tagacaagtc caagaaccag 60
ttctccctga agctgaggtc tgtgaccgcc gcggacacgg ccgtttatta ctgt 114
<210> 211
<211> 9
<212> Белок
<213> Homo Sapien
<400> 211
Ala Arg Val Gly Ala Thr Glu Asn Phe
1 5
<210> 212
<211> 27
<212> ДНК
<213> Homo Sapien
<400> 212
gcgagagtgg gtgctactga gaacttc 27
<210> 213
<211> 11
<212> Белок
<213> Homo Sapien
<400> 213
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
1 5 10
<210> 214
<211> 34
<212> ДНК
<213> Homo Sapien
<400> 214
tggggccagg gaaccctggt caccgtctcc tcag 34
<210> 215
<211> 30
<212> Белок
<213> Homo Sapien
<400> 215
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gly
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Gly Ser Ile Ser
20 25 30
<210> 216
<211> 90
<212> ДНК
<213> Homo Sapien
<400> 216
caggtgcagc tgcaggagtc gggcccagga ctggtgaagc cttcggggac cctgtccctc 60
acctgcgctg tctctggtgg ctccatcagc 90
<210> 217
<211> 6
<212> Белок
<213> Homo Sapien
<400> 217
Ser Ser Lys Trp Trp Ser
1 5
<210> 218
<211> 18
<212> ДНК
<213> Homo Sapien
<400> 218
agtagtaaat ggtggagt 18
<210> 219
<211> 14
<212> Белок
<213> Homo Sapien
<400> 219
Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
1 5 10
<210> 220
<211> 42
<212> ДНК
<213> Homo Sapien
<400> 220
tgggtccgcc agcccccagg gaaggggctg gagtggattg gg 42
<210> 221
<211> 16
<212> Белок
<213> Homo Sapien
<400> 221
Glu Thr His Tyr Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys Ser
1 5 10 15
<210> 222
<211> 48
<212> ДНК
<213> Homo Sapien
<400> 222
gaaacccatt atagtgggag caccaactac aacccgtccc tcaagagt 48
<210> 223
<211> 32
<212> Белок
<213> Homo Sapien
<400> 223
Arg Val Thr Ile Ser Val Asp Lys Ser Lys Asn Gln Phe Ser Leu Lys
1 5 10 15
Leu Arg Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg
20 25 30
<210> 224
<211> 96
<212> ДНК
<213> Homo Sapien
<400> 224
cgagtcacca tatcagtaga caagtccaag aaccagttct ccctgaagct gaggtctgtg 60
accgccgcgg acacggccgt ttattactgt gcgaga 96
<210> 225
<211> 7
<212> Белок
<213> Homo Sapien
<400> 225
Val Gly Ala Thr Glu Asn Phe
1 5
<210> 226
<211> 21
<212> ДНК
<213> Homo Sapien
<400> 226
gtgggtgcta ctgagaactt c 21
<210> 227
<211> 11
<212> Белок
<213> Homo Sapien
<400> 227
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
1 5 10
<210> 228
<211> 34
<212> ДНК
<213> Homo Sapien
<400> 228
tggggccagg gaaccctggt caccgtctcc tcag 34
<210> 229
<211> 107
<212> Белок
<213> Homo Sapien
<400> 229
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Phe Arg Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Thr Arg Ala Thr Asp Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 230
<211> 321
<212> ДНК
<213> Homo Sapien
<400> 230
gaaattgtgt tgacacagtc tccagccacc ctgtctttgt ctccagggga aagagccacc 60
ctctcctgca gggccagtca gagtgttttc aggtacttag cctggtacca acagaaacct 120
ggccaggctc ccaggctcct catctatgat gcatccacca gggccactga catcccagcc 180
aggttcagtg gcagtgggtc tgggacagat ttcactctca ccatcagcag cctagagcct 240
gaagattttg cagtttatta ctgtcagcaa cgtagcaact ggcctccgac gttcggccaa 300
gggaccaagg tggaaatcaa a 321
<210> 231
<211> 26
<212> Белок
<213> Homo Sapien
<400> 231
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser
20 25
<210> 232
<211> 78
<212> ДНК
<213> Homo Sapien
<400> 232
gaaattgtgt tgacacagtc tccagccacc ctgtctttgt ctccagggga aagagccacc 60
ctctcctgca gggccagt 78
<210> 233
<211> 6
<212> Белок
<213> Homo Sapien
<400> 233
Gln Ser Val Phe Arg Tyr
1 5
<210> 234
<211> 18
<212> ДНК
<213> Homo Sapien
<400> 234
cagagtgttt tcaggtac 18
<210> 235
<211> 17
<212> Белок
<213> Homo Sapien
<400> 235
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
1 5 10 15
Tyr
<210> 236
<211> 51
<212> ДНК
<213> Homo Sapien
<400> 236
ttagcctggt accaacagaa acctggccag gctcccaggc tcctcatcta t 51
<210> 237
<211> 3
<212> Белок
<213> Homo Sapien
<400> 237
Asp Ala Ser
1
<210> 238
<211> 9
<212> ДНК
<213> Homo Sapien
<400> 238
gatgcatcc 9
<210> 239
<211> 36
<212> Белок
<213> Homo Sapien
<400> 239
Thr Arg Ala Thr Asp Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
1 5 10 15
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu Asp Phe Ala
20 25 30
Val Tyr Tyr Cys
35
<210> 240
<211> 108
<212> ДНК
<213> Homo Sapien
<400> 240
accagggcca ctgacatccc agccaggttc agtggcagtg ggtctgggac agatttcact 60
ctcaccatca gcagcctaga gcctgaagat tttgcagttt attactgt 108
<210> 241
<211> 9
<212> Белок
<213> Homo Sapien
<400> 241
Gln Gln Arg Ser Asn Trp Pro Pro Thr
1 5
<210> 242
<211> 27
<212> ДНК
<213> Homo Sapien
<400> 242
cagcaacgta gcaactggcc tccgacg 27
<210> 243
<211> 10
<212> Белок
<213> Homo Sapien
<400> 243
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
1 5 10
<210> 244
<211> 30
<212> ДНК
<213> Homo Sapien
<400> 244
ttcggccaag ggaccaaggt ggaaatcaaa 30
<210> 245
<211> 23
<212> Белок
<213> Homo Sapien
<400> 245
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys
20
<210> 246
<211> 69
<212> ДНК
<213> Homo Sapien
<400> 246
gaaattgtgt tgacacagtc tccagccacc ctgtctttgt ctccagggga aagagccacc 60
ctctcctgc 69
<210> 247
<211> 11
<212> Белок
<213> Homo Sapien
<400> 247
Arg Ala Ser Gln Ser Val Phe Arg Tyr Leu Ala
1 5 10
<210> 248
<211> 33
<212> ДНК
<213> Homo Sapien
<400> 248
agggccagtc agagtgtttt caggtactta gcc 33
<210> 249
<211> 15
<212> Белок
<213> Homo Sapien
<400> 249
Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
1 5 10 15
<210> 250
<211> 45
<212> ДНК
<213> Homo Sapien
<400> 250
tggtaccaac agaaacctgg ccaggctccc aggctcctca tctat 45
<210> 251
<211> 7
<212> Белок
<213> Homo Sapien
<400> 251
Asp Ala Ser Thr Arg Ala Thr
1 5
<210> 252
<211> 21
<212> ДНК
<213> Homo Sapien
<400> 252
gatgcatcca ccagggccac t 21
<210> 253
<211> 32
<212> Белок
<213> Homo Sapien
<400> 253
Asp Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
1 5 10 15
Leu Thr Ile Ser Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys
20 25 30
<210> 254
<211> 96
<212> ДНК
<213> Homo Sapien
<400> 254
gacatcccag ccaggttcag tggcagtggg tctgggacag atttcactct caccatcagc 60
agcctagagc ctgaagattt tgcagtttat tactgt 96
<210> 255
<211> 9
<212> Белок
<213> Homo Sapien
<400> 255
Gln Gln Arg Ser Asn Trp Pro Pro Thr
1 5
<210> 256
<211> 27
<212> ДНК
<213> Homo Sapien
<400> 256
cagcaacgta gcaactggcc tccgacg 27
<210> 257
<211> 10
<212> Белок
<213> Homo Sapien
<400> 257
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
1 5 10
<210> 258
<211> 30
<212> ДНК
<213> Homo Sapien
<400> 258
ttcggccaag ggaccaaggt ggaaatcaaa 30
<210> 259
<211> 120
<212> Белок
<213> Homo Sapien
<400> 259
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Gly
20 25 30
Gly Tyr Tyr Trp Ser Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly His Ile Phe Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Asn Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Ser Glu Gly Gly Tyr Tyr Asp Ile Pro Asp Val Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 260
<211> 360
<212> ДНК
<213> Homo Sapien
<400> 260
caggtgcagc tgcaggagtc gggcccagga ctggtgaagc cttcacagac cctgtccctc 60
acctgcactg tctctggtgg ctccatcagc agtggtggtt actactggag ctggatccgc 120
cagcacccag ggaagggcct ggagtggatt gggcacatct tttacagtgg gagcacctac 180
tacaacccgt ccctcaagag tcgagttacc atatcagttg acacgtctaa gaaccagttc 240
tccctgaagc tgaactctgt gactgccgcg gacacggccg tgtattactg tgcgagcgag 300
ggagggtatt acgatattcc ggacgtctgg ggccaaggga ccacggtcac cgtctcctca 360
<210> 261
<211> 25
<212> Белок
<213> Homo Sapien
<400> 261
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser
20 25
<210> 262
<211> 75
<212> ДНК
<213> Homo Sapien
<400> 262
caggtgcagc tgcaggagtc gggcccagga ctggtgaagc cttcacagac cctgtccctc 60
acctgcactg tctct 75
<210> 263
<211> 10
<212> Белок
<213> Homo Sapien
<400> 263
Gly Gly Ser Ile Ser Ser Gly Gly Tyr Tyr
1 5 10
<210> 264
<211> 30
<212> ДНК
<213> Homo Sapien
<400> 264
ggtggctcca tcagcagtgg tggttactac 30
<210> 265
<211> 17
<212> Белок
<213> Homo Sapien
<400> 265
Trp Ser Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu Trp Ile Gly
1 5 10 15
His
<210> 266
<211> 51
<212> ДНК
<213> Homo Sapien
<400> 266
tggagctgga tccgccagca cccagggaag ggcctggagt ggattgggca c 51
<210> 267
<211> 7
<212> Белок
<213> Homo Sapien
<400> 267
Ile Phe Tyr Ser Gly Ser Thr
1 5
<210> 268
<211> 21
<212> ДНК
<213> Homo Sapien
<400> 268
atcttttaca gtgggagcac c 21
<210> 269
<211> 38
<212> Белок
<213> Homo Sapien
<400> 269
Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr
1 5 10 15
Ser Lys Asn Gln Phe Ser Leu Lys Leu Asn Ser Val Thr Ala Ala Asp
20 25 30
Thr Ala Val Tyr Tyr Cys
35
<210> 270
<211> 114
<212> ДНК
<213> Homo Sapien
<400> 270
tactacaacc cgtccctcaa gagtcgagtt accatatcag ttgacacgtc taagaaccag 60
ttctccctga agctgaactc tgtgactgcc gcggacacgg ccgtgtatta ctgt 114
<210> 271
<211> 12
<212> Белок
<213> Homo Sapien
<400> 271
Ala Ser Glu Gly Gly Tyr Tyr Asp Ile Pro Asp Val
1 5 10
<210> 272
<211> 36
<212> ДНК
<213> Homo Sapien
<400> 272
gcgagcgagg gagggtatta cgatattccg gacgtc 36
<210> 273
<211> 11
<212> Белок
<213> Homo Sapien
<400> 273
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
1 5 10
<210> 274
<211> 33
<212> ДНК
<213> Homo Sapien
<400> 274
tggggccaag ggaccacggt caccgtctcc tca 33
<210> 275
<211> 30
<212> Белок
<213> Homo Sapien
<400> 275
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser
20 25 30
<210> 276
<211> 90
<212> ДНК
<213> Homo Sapien
<400> 276
caggtgcagc tgcaggagtc gggcccagga ctggtgaagc cttcacagac cctgtccctc 60
acctgcactg tctctggtgg ctccatcagc 90
<210> 277
<211> 7
<212> Белок
<213> Homo Sapien
<400> 277
Ser Gly Gly Tyr Tyr Trp Ser
1 5
<210> 278
<211> 21
<212> ДНК
<213> Homo Sapien
<400> 278
agtggtggtt actactggag c 21
<210> 279
<211> 14
<212> Белок
<213> Homo Sapien
<400> 279
Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu Trp Ile Gly
1 5 10
<210> 280
<211> 42
<212> ДНК
<213> Homo Sapien
<400> 280
tggatccgcc agcacccagg gaagggcctg gagtggattg gg 42
<210> 281
<211> 16
<212> Белок
<213> Homo Sapien
<400> 281
His Ile Phe Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser
1 5 10 15
<210> 282
<211> 48
<212> ДНК
<213> Homo Sapien
<400> 282
cacatctttt acagtgggag cacctactac aacccgtccc tcaagagt 48
<210> 283
<211> 32
<212> Белок
<213> Homo Sapien
<400> 283
Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys
1 5 10 15
Leu Asn Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Ser
20 25 30
<210> 284
<211> 96
<212> ДНК
<213> Homo Sapien
<400> 284
cgagttacca tatcagttga cacgtctaag aaccagttct ccctgaagct gaactctgtg 60
actgccgcgg acacggccgt gtattactgt gcgagc 96
<210> 285
<211> 10
<212> Белок
<213> Homo Sapien
<400> 285
Glu Gly Gly Tyr Tyr Asp Ile Pro Asp Val
1 5 10
<210> 286
<211> 30
<212> ДНК
<213> Homo Sapien
<400> 286
gagggagggt attacgatat tccggacgtc 30
<210> 287
<211> 11
<212> Белок
<213> Homo Sapien
<400> 287
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
1 5 10
<210> 288
<211> 33
<212> ДНК
<213> Homo Sapien
<400> 288
tggggccaag ggaccacggt caccgtctcc tca 33
<210> 289
<211> 107
<212> Белок
<213> Homo Sapien
<400> 289
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Asn Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Ser Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Ile Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 290
<211> 321
<212> ДНК
<213> Homo Sapien
<400> 290
gaaattgtgt tgacacagtc tccagccacc ctgtctttgt ctccagggga aagagccacc 60
ctctcctgca gggccagtca gagtgttagc aactacttag cctggtacca acagaaacct 120
ggccaggctc ccaggctcct catctctgat gcatccaaca gggccactgg catcccagcc 180
aggttcagtg gcagtgggtc tgggacagac ttcactctca ccatcagcag cctagagcct 240
gaagattttg caatttatta ctgtcagcag cgtagcaact ggccgctcac tttcggcgga 300
gggaccaagg tggagatcaa a 321
<210> 291
<211> 26
<212> Белок
<213> Homo Sapien
<400> 291
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser
20 25
<210> 292
<211> 78
<212> ДНК
<213> Homo Sapien
<400> 292
gaaattgtgt tgacacagtc tccagccacc ctgtctttgt ctccagggga aagagccacc 60
ctctcctgca gggccagt 78
<210> 293
<211> 6
<212> Белок
<213> Homo Sapien
<400> 293
Gln Ser Val Ser Asn Tyr
1 5
<210> 294
<211> 18
<212> ДНК
<213> Homo Sapien
<400> 294
cagagtgtta gcaactac 18
<210> 295
<211> 17
<212> Белок
<213> Homo Sapien
<400> 295
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
1 5 10 15
Ser
<210> 296
<211> 51
<212> ДНК
<213> Homo Sapien
<400> 296
ttagcctggt accaacagaa acctggccag gctcccaggc tcctcatctc t 51
<210> 297
<211> 3
<212> Белок
<213> Homo Sapien
<400> 297
Asp Ala Ser
1
<210> 298
<211> 9
<212> ДНК
<213> Homo Sapien
<400> 298
gatgcatcc 9
<210> 299
<211> 36
<212> Белок
<213> Homo Sapien
<400> 299
Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
1 5 10 15
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu Asp Phe Ala
20 25 30
Ile Tyr Tyr Cys
35
<210> 300
<211> 108
<212> ДНК
<213> Homo Sapien
<400> 300
aacagggcca ctggcatccc agccaggttc agtggcagtg ggtctgggac agacttcact 60
ctcaccatca gcagcctaga gcctgaagat tttgcaattt attactgt 108
<210> 301
<211> 9
<212> Белок
<213> Homo Sapien
<400> 301
Gln Gln Arg Ser Asn Trp Pro Leu Thr
1 5
<210> 302
<211> 27
<212> ДНК
<213> Homo Sapien
<400> 302
cagcagcgta gcaactggcc gctcact 27
<210> 303
<211> 10
<212> Белок
<213> Homo Sapien
<400> 303
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
1 5 10
<210> 304
<211> 30
<212> ДНК
<213> Homo Sapien
<400> 304
ttcggcggag ggaccaaggt ggagatcaaa 30
<210> 305
<211> 23
<212> Белок
<213> Homo Sapien
<400> 305
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys
20
<210> 306
<211> 69
<212> ДНК
<213> Homo Sapien
<400> 306
gaaattgtgt tgacacagtc tccagccacc ctgtctttgt ctccagggga aagagccacc 60
ctctcctgc 69
<210> 307
<211> 11
<212> Белок
<213> Homo Sapien
<400> 307
Arg Ala Ser Gln Ser Val Ser Asn Tyr Leu Ala
1 5 10
<210> 308
<211> 33
<212> ДНК
<213> Homo Sapien
<400> 308
agggccagtc agagtgttag caactactta gcc 33
<210> 309
<211> 15
<212> Белок
<213> Homo Sapien
<400> 309
Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Ser
1 5 10 15
<210> 310
<211> 45
<212> ДНК
<213> Homo Sapien
<400> 310
tggtaccaac agaaacctgg ccaggctccc aggctcctca tctct 45
<210> 311
<211> 7
<212> Белок
<213> Homo Sapien
<400> 311
Asp Ala Ser Asn Arg Ala Thr
1 5
<210> 312
<211> 21
<212> ДНК
<213> Homo Sapien
<400> 312
gatgcatcca acagggccac t 21
<210> 313
<211> 32
<212> Белок
<213> Homo Sapien
<400> 313
Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
1 5 10 15
Leu Thr Ile Ser Ser Leu Glu Pro Glu Asp Phe Ala Ile Tyr Tyr Cys
20 25 30
<210> 314
<211> 96
<212> ДНК
<213> Homo Sapien
<400> 314
ggcatcccag ccaggttcag tggcagtggg tctgggacag acttcactct caccatcagc 60
agcctagagc ctgaagattt tgcaatttat tactgt 96
<210> 315
<211> 9
<212> Белок
<213> Homo Sapien
<400> 315
Gln Gln Arg Ser Asn Trp Pro Leu Thr
1 5
<210> 316
<211> 27
<212> ДНК
<213> Homo Sapien
<400> 316
cagcagcgta gcaactggcc gctcact 27
<210> 317
<211> 10
<212> Белок
<213> Homo Sapien
<400> 317
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
1 5 10
<210> 318
<211> 30
<212> ДНК
<213> Homo Sapien
<400> 318
ttcggcggag ggaccaaggt ggagatcaaa 30
<210> 319
<211> 120
<212> Белок
<213> Homo Sapien
<400> 319
Gln Val His Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Tyr Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Ser Tyr Ser Gly Ser Ser Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Arg Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Gln Leu Thr Ser Val Ile Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Asn Leu Met Ile Arg Gly Ala Tyr Gly Met Asp Val Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 320
<211> 360
<212> ДНК
<213> Homo Sapien
<400> 320
caggtgcacc tgcaggagtc gggcccagga ctggtgaagc cttcggagac cctgtccctc 60
acgtgcactg tctctggtgg ctccatcagt agttactact ggagctggat ccggcagtac 120
ccaggaaagg gactggagtg gattggatat atctcttaca gtgggagcag caattataat 180
ccctccctca agaggcgagt caccatatca cgagacacgt ccaagaacca gttctccctg 240
cagctgacct ctgtaatcgc tgcggacacg gccgtttatt actgtgcgag aaatcttatg 300
attcggggag cctacggcat ggacgtctgg ggccaaggga ccacggtcac cgtctcctca 360
<210> 321
<211> 25
<212> Белок
<213> Homo Sapien
<400> 321
Gln Val His Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser
20 25
<210> 322
<211> 75
<212> ДНК
<213> Homo Sapien
<400> 322
caggtgcacc tgcaggagtc gggcccagga ctggtgaagc cttcggagac cctgtccctc 60
acgtgcactg tctct 75
<210> 323
<211> 8
<212> Белок
<213> Homo Sapien
<400> 323
Gly Gly Ser Ile Ser Ser Tyr Tyr
1 5
<210> 324
<211> 24
<212> ДНК
<213> Homo Sapien
<400> 324
ggtggctcca tcagtagtta ctac 24
<210> 325
<211> 17
<212> Белок
<213> Homo Sapien
<400> 325
Trp Ser Trp Ile Arg Gln Tyr Pro Gly Lys Gly Leu Glu Trp Ile Gly
1 5 10 15
Tyr
<210> 326
<211> 51
<212> ДНК
<213> Homo Sapien
<400> 326
tggagctgga tccggcagta cccaggaaag ggactggagt ggattggata t 51
<210> 327
<211> 7
<212> Белок
<213> Homo Sapien
<400> 327
Ile Ser Tyr Ser Gly Ser Ser
1 5
<210> 328
<211> 21
<212> ДНК
<213> Homo Sapien
<400> 328
atctcttaca gtgggagcag c 21
<210> 329
<211> 38
<212> Белок
<213> Homo Sapien
<400> 329
Asn Tyr Asn Pro Ser Leu Lys Arg Arg Val Thr Ile Ser Arg Asp Thr
1 5 10 15
Ser Lys Asn Gln Phe Ser Leu Gln Leu Thr Ser Val Ile Ala Ala Asp
20 25 30
Thr Ala Val Tyr Tyr Cys
35
<210> 330
<211> 114
<212> ДНК
<213> Homo Sapien
<400> 330
aattataatc cctccctcaa gaggcgagtc accatatcac gagacacgtc caagaaccag 60
ttctccctgc agctgacctc tgtaatcgct gcggacacgg ccgtttatta ctgt 114
<210> 331
<211> 14
<212> Белок
<213> Homo Sapien
<400> 331
Ala Arg Asn Leu Met Ile Arg Gly Ala Tyr Gly Met Asp Val
1 5 10
<210> 332
<211> 42
<212> ДНК
<213> Homo Sapien
<400> 332
gcgagaaatc ttatgattcg gggagcctac ggcatggacg tc 42
<210> 333
<211> 11
<212> Белок
<213> Homo Sapien
<400> 333
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
1 5 10
<210> 334
<211> 33
<212> ДНК
<213> Homo Sapien
<400> 334
tggggccaag ggaccacggt caccgtctcc tca 33
<210> 335
<211> 29
<212> Белок
<213> Homo Sapien
<400> 335
Gln Val His Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile
20 25
<210> 336
<211> 87
<212> ДНК
<213> Homo Sapien
<400> 336
caggtgcacc tgcaggagtc gggcccagga ctggtgaagc cttcggagac cctgtccctc 60
acgtgcactg tctctggtgg ctccatc 87
<210> 337
<211> 6
<212> Белок
<213> Homo Sapien
<400> 337
Ser Ser Tyr Tyr Trp Ser
1 5
<210> 338
<211> 18
<212> ДНК
<213> Homo Sapien
<400> 338
agtagttact actggagc 18
<210> 339
<211> 14
<212> Белок
<213> Homo Sapien
<400> 339
Trp Ile Arg Gln Tyr Pro Gly Lys Gly Leu Glu Trp Ile Gly
1 5 10
<210> 340
<211> 42
<212> ДНК
<213> Homo Sapien
<400> 340
tggatccggc agtacccagg aaagggactg gagtggattg ga 42
<210> 341
<211> 16
<212> Белок
<213> Homo Sapien
<400> 341
Tyr Ile Ser Tyr Ser Gly Ser Ser Asn Tyr Asn Pro Ser Leu Lys Arg
1 5 10 15
<210> 342
<211> 48
<212> ДНК
<213> Homo Sapien
<400> 342
tatatctctt acagtgggag cagcaattat aatccctccc tcaagagg 48
<210> 343
<211> 32
<212> Белок
<213> Homo Sapien
<400> 343
Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser Leu Gln
1 5 10 15
Leu Thr Ser Val Ile Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg
20 25 30
<210> 344
<211> 96
<212> ДНК
<213> Homo Sapien
<400> 344
cgagtcacca tatcacgaga cacgtccaag aaccagttct ccctgcagct gacctctgta 60
atcgctgcgg acacggccgt ttattactgt gcgaga 96
<210> 345
<211> 12
<212> Белок
<213> Homo Sapien
<400> 345
Asn Leu Met Ile Arg Gly Ala Tyr Gly Met Asp Val
1 5 10
<210> 346
<211> 36
<212> ДНК
<213> Homo Sapien
<400> 346
aatcttatga ttcggggagc ctacggcatg gacgtc 36
<210> 347
<211> 11
<212> Белок
<213> Homo Sapien
<400> 347
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
1 5 10
<210> 348
<211> 33
<212> ДНК
<213> Homo Sapien
<400> 348
tggggccaag ggaccacggt caccgtctcc tca 33
<210> 349
<211> 112
<212> Белок
<213> Homo Sapien
<400> 349
Asp Thr Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Ala Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Val Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Ile Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Phe Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105 110
<210> 350
<211> 336
<212> ДНК
<213> Homo Sapien
<400> 350
gatactgtga tgactcagtc tccactctcc ctgcccgtca cccctggaga gccggcctcc 60
atctcctgca ggtctagtca gagcctcctg catagtaatg gatacaatta tttggattgg 120
tacctgcaga aggcaggaca gtctccacaa ctcctgatct atttgggttc taatcgggcc 180
tccggggtcc ctgacaggtt cagtggcagt gtatcaggca cagatttcac actgaaaatc 240
agcagagtgg aggctgagga tgttgggatt tattactgca tgcaagctct acaaactcca 300
ttcactttcg gccctgggac caaagtggat atcaaa 336
<210> 351
<211> 26
<212> Белок
<213> Homo Sapien
<400> 351
Asp Thr Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser
20 25
<210> 352
<211> 78
<212> ДНК
<213> Homo Sapien
<400> 352
gatactgtga tgactcagtc tccactctcc ctgcccgtca cccctggaga gccggcctcc 60
atctcctgca ggtctagt 78
<210> 353
<211> 11
<212> Белок
<213> Homo Sapien
<400> 353
Gln Ser Leu Leu His Ser Asn Gly Tyr Asn Tyr
1 5 10
<210> 354
<211> 33
<212> ДНК
<213> Homo Sapien
<400> 354
cagagcctcc tgcatagtaa tggatacaat tat 33
<210> 355
<211> 17
<212> Белок
<213> Homo Sapien
<400> 355
Leu Asp Trp Tyr Leu Gln Lys Ala Gly Gln Ser Pro Gln Leu Leu Ile
1 5 10 15
Tyr
<210> 356
<211> 51
<212> ДНК
<213> Homo Sapien
<400> 356
ttggattggt acctgcagaa ggcaggacag tctccacaac tcctgatcta t 51
<210> 357
<211> 3
<212> Белок
<213> Homo Sapien
<400> 357
Leu Gly Ser
1
<210> 358
<211> 9
<212> ДНК
<213> Homo Sapien
<400> 358
ttgggttct 9
<210> 359
<211> 36
<212> Белок
<213> Homo Sapien
<400> 359
Asn Arg Ala Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Val Ser Gly
1 5 10 15
Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly
20 25 30
Ile Tyr Tyr Cys
35
<210> 360
<211> 108
<212> ДНК
<213> Homo Sapien
<400> 360
aatcgggcct ccggggtccc tgacaggttc agtggcagtg tatcaggcac agatttcaca 60
ctgaaaatca gcagagtgga ggctgaggat gttgggattt attactgc 108
<210> 361
<211> 9
<212> Белок
<213> Homo Sapien
<400> 361
Met Gln Ala Leu Gln Thr Pro Phe Thr
1 5
<210> 362
<211> 27
<212> ДНК
<213> Homo Sapien
<400> 362
atgcaagctc tacaaactcc attcact 27
<210> 363
<211> 10
<212> Белок
<213> Homo Sapien
<400> 363
Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
1 5 10
<210> 364
<211> 30
<212> ДНК
<213> Homo Sapien
<400> 364
ttcggccctg ggaccaaagt ggatatcaaa 30
<210> 365
<211> 23
<212> Белок
<213> Homo Sapien
<400> 365
Asp Thr Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys
20
<210> 366
<211> 69
<212> ДНК
<213> Homo Sapien
<400> 366
gatactgtga tgactcagtc tccactctcc ctgcccgtca cccctggaga gccggcctcc 60
atctcctgc 69
<210> 367
<211> 16
<212> Белок
<213> Homo Sapien
<400> 367
Arg Ser Ser Gln Ser Leu Leu His Ser Asn Gly Tyr Asn Tyr Leu Asp
1 5 10 15
<210> 368
<211> 48
<212> ДНК
<213> Homo Sapien
<400> 368
aggtctagtc agagcctcct gcatagtaat ggatacaatt atttggat 48
<210> 369
<211> 15
<212> Белок
<213> Homo Sapien
<400> 369
Trp Tyr Leu Gln Lys Ala Gly Gln Ser Pro Gln Leu Leu Ile Tyr
1 5 10 15
<210> 370
<211> 45
<212> ДНК
<213> Homo Sapien
<400> 370
tggtacctgc agaaggcagg acagtctcca caactcctga tctat 45
<210> 371
<211> 7
<212> Белок
<213> Homo Sapien
<400> 371
Leu Gly Ser Asn Arg Ala Ser
1 5
<210> 372
<211> 21
<212> ДНК
<213> Homo Sapien
<400> 372
ttgggttcta atcgggcctc c 21
<210> 373
<211> 32
<212> Белок
<213> Homo Sapien
<400> 373
Gly Val Pro Asp Arg Phe Ser Gly Ser Val Ser Gly Thr Asp Phe Thr
1 5 10 15
Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Ile Tyr Tyr Cys
20 25 30
<210> 374
<211> 96
<212> ДНК
<213> Homo Sapien
<400> 374
ggggtccctg acaggttcag tggcagtgta tcaggcacag atttcacact gaaaatcagc 60
agagtggagg ctgaggatgt tgggatttat tactgc 96
<210> 375
<211> 9
<212> Белок
<213> Homo Sapien
<400> 375
Met Gln Ala Leu Gln Thr Pro Phe Thr
1 5
<210> 376
<211> 27
<212> ДНК
<213> Homo Sapien
<400> 376
atgcaagctc tacaaactcc attcact 27
<210> 377
<211> 10
<212> Белок
<213> Homo Sapien
<400> 377
Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
1 5 10
<210> 378
<211> 30
<212> ДНК
<213> Homo Sapien
<400> 378
ttcggccctg ggaccaaagt ggatatcaaa 30
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Анти-PD-L1 и IL-2 цитокины | 2017 |
|
RU2769282C2 |
| PD-L1 специфические антитела | 2017 |
|
RU2756236C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ АНТИТЕЛА К PCSK-9, И ЕЕ ПРИМЕНЕНИЕ | 2018 |
|
RU2782792C2 |
| ВЫСОКОАФФИННЫЙ Т-КЛЕТОЧНЫЙ РЕЦЕПТОР ДЛЯ РАСПОЗНАВАНИЯ АНТИГЕНА AFP | 2019 |
|
RU2836365C2 |
| МОЛЕКУЛЫ, СВЯЗЫВАЮЩИЕСЯ С 4-1ВВ | 2011 |
|
RU2551963C2 |
| АНТИ-PRE-S1 HBV АНТИТЕЛА | 2016 |
|
RU2739955C2 |
| Антитело против PCSK9 и его применение | 2016 |
|
RU2756012C2 |
| АНТИ-PCSK9 АНТИТЕЛО, ЕГО АНТИГЕНСВЯЗЫВАЮЩИЙ ФРАГМЕНТ И ИХ МЕДИЦИНСКОЕ ПРИМЕНЕНИЕ | 2016 |
|
RU2739208C2 |
| ИСКУССТВЕННЫЕ АНТИГЕНПРЕЗЕНТИРУЮЩИЕ КЛЕТКИ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2763798C1 |
| Композиции и способы активации интегринов | 2020 |
|
RU2836262C1 |
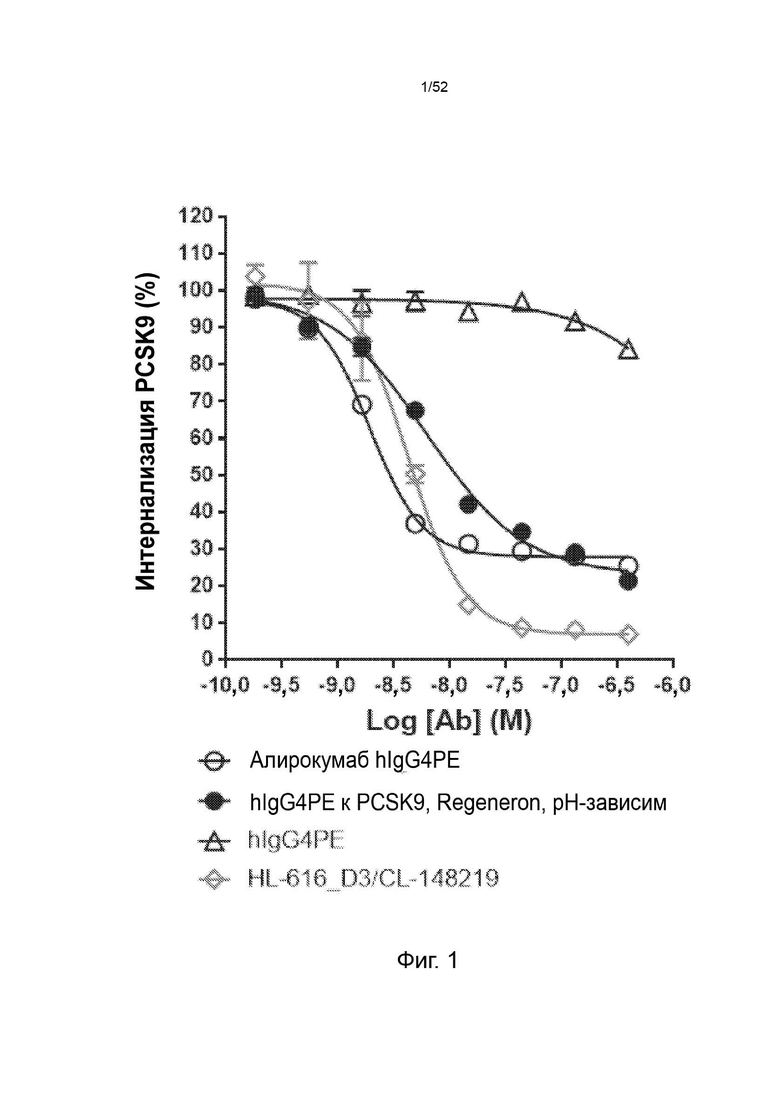
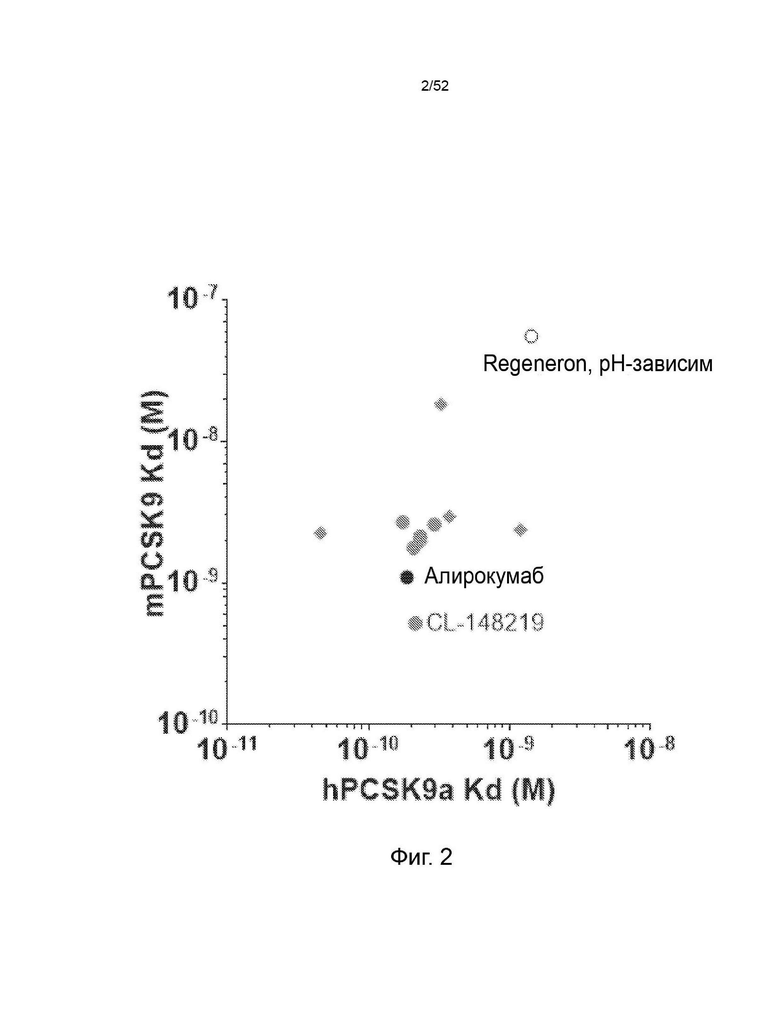
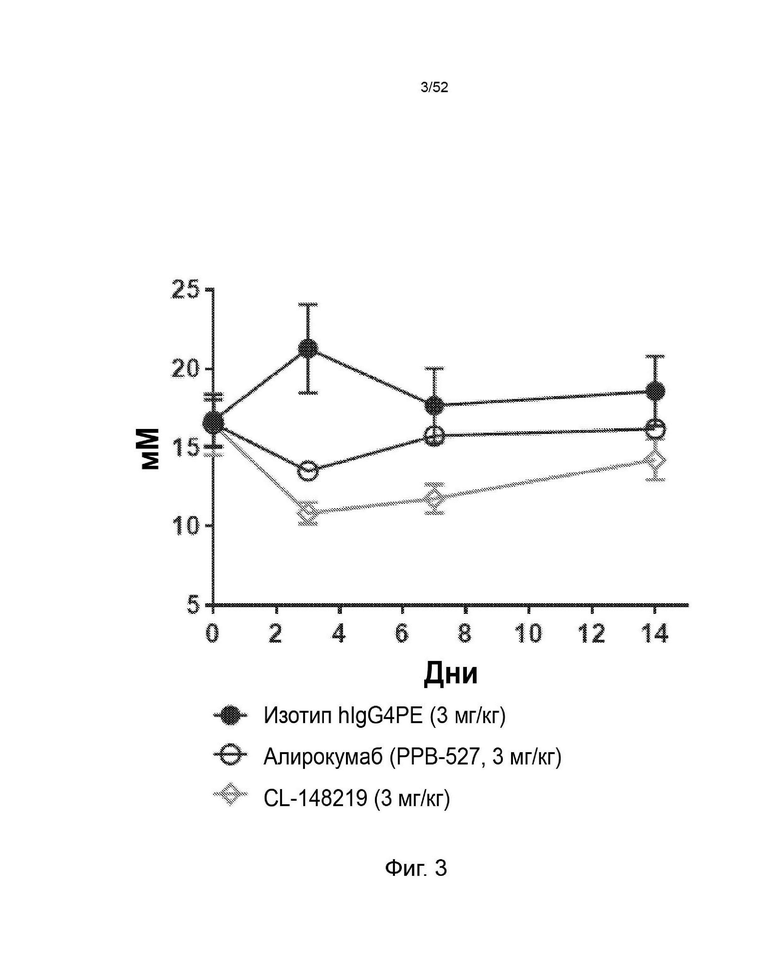
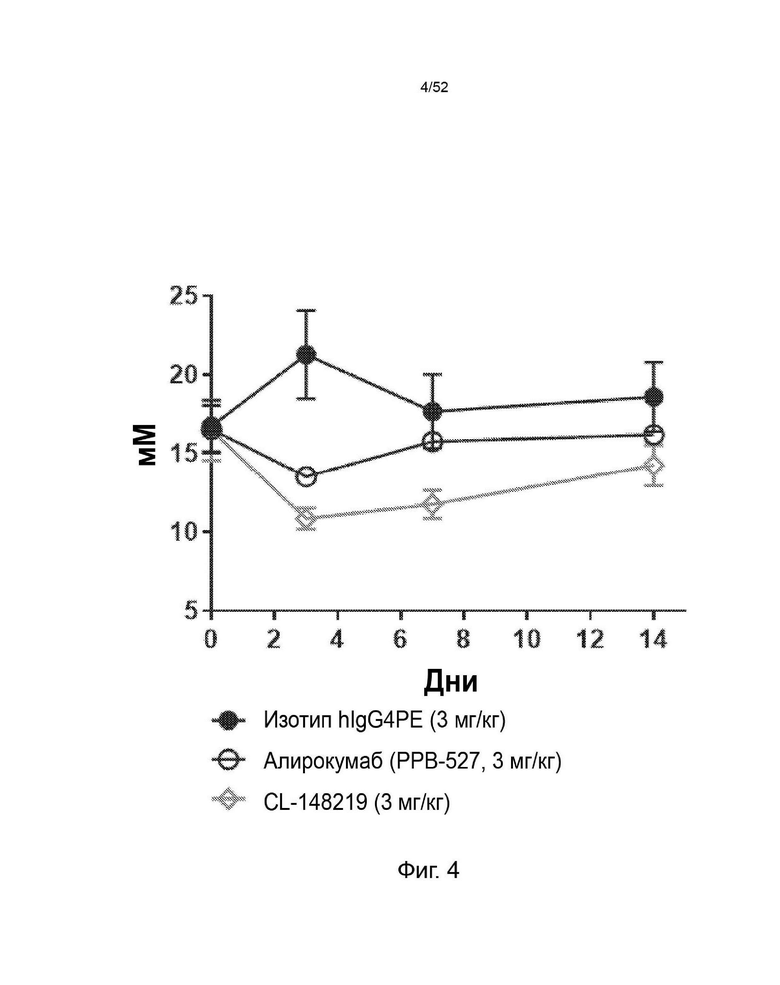
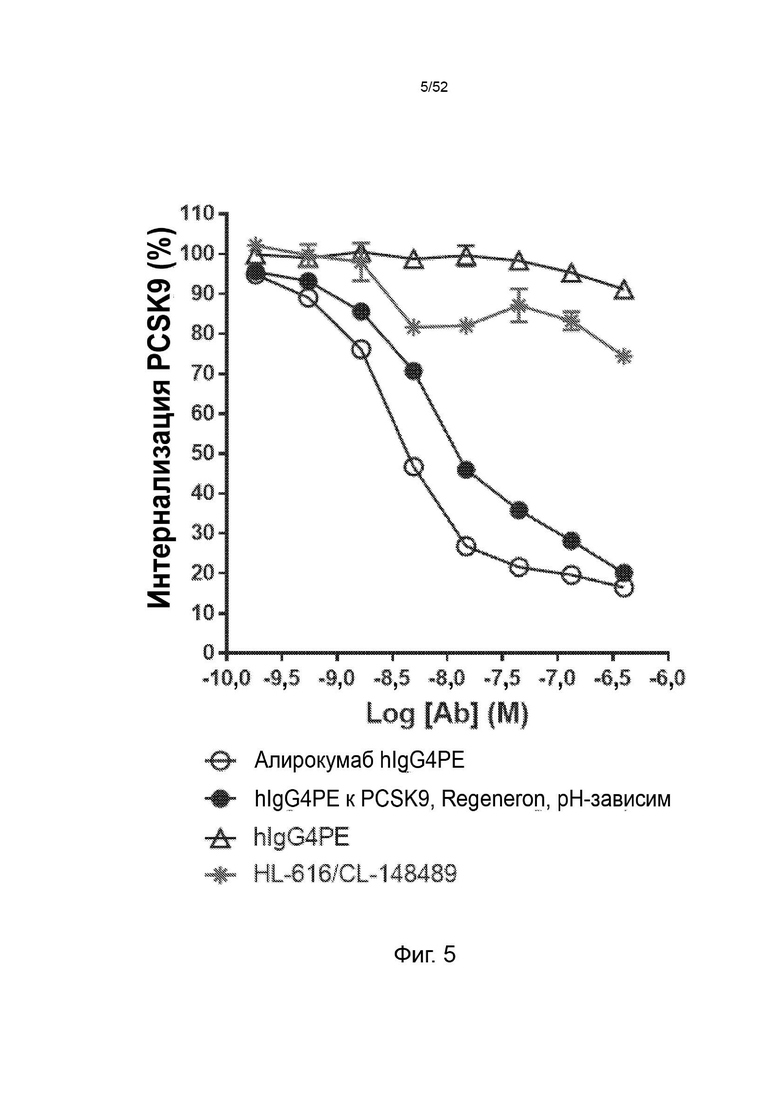
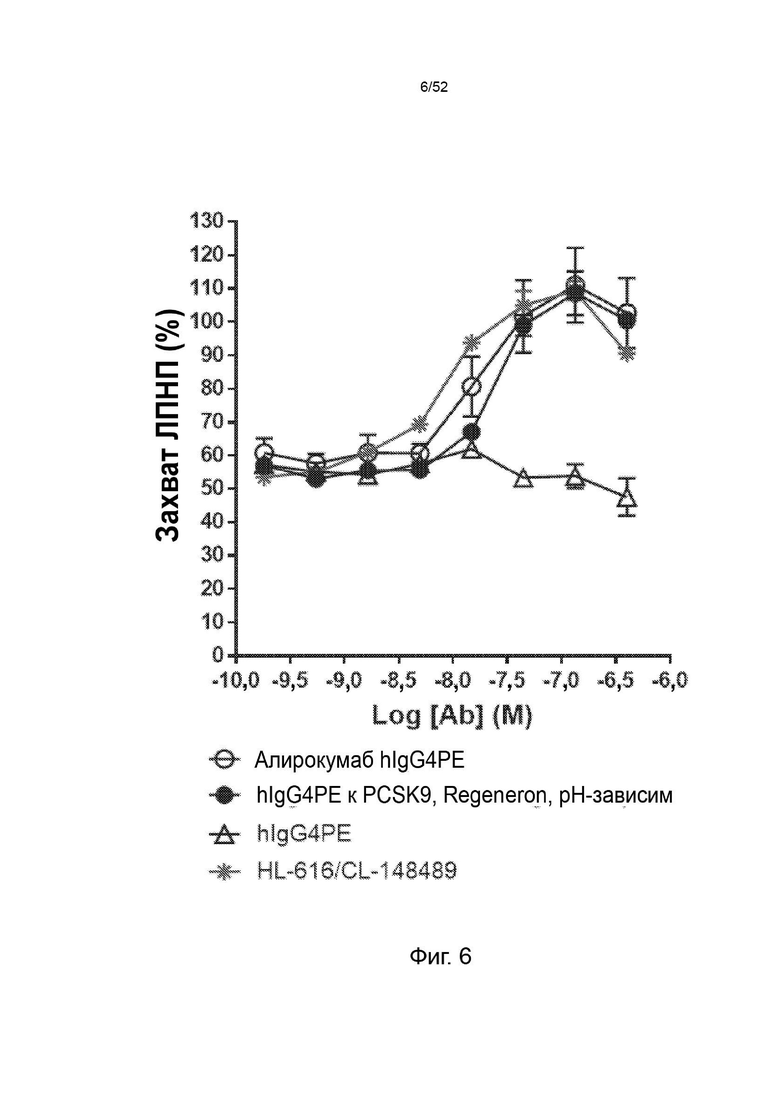
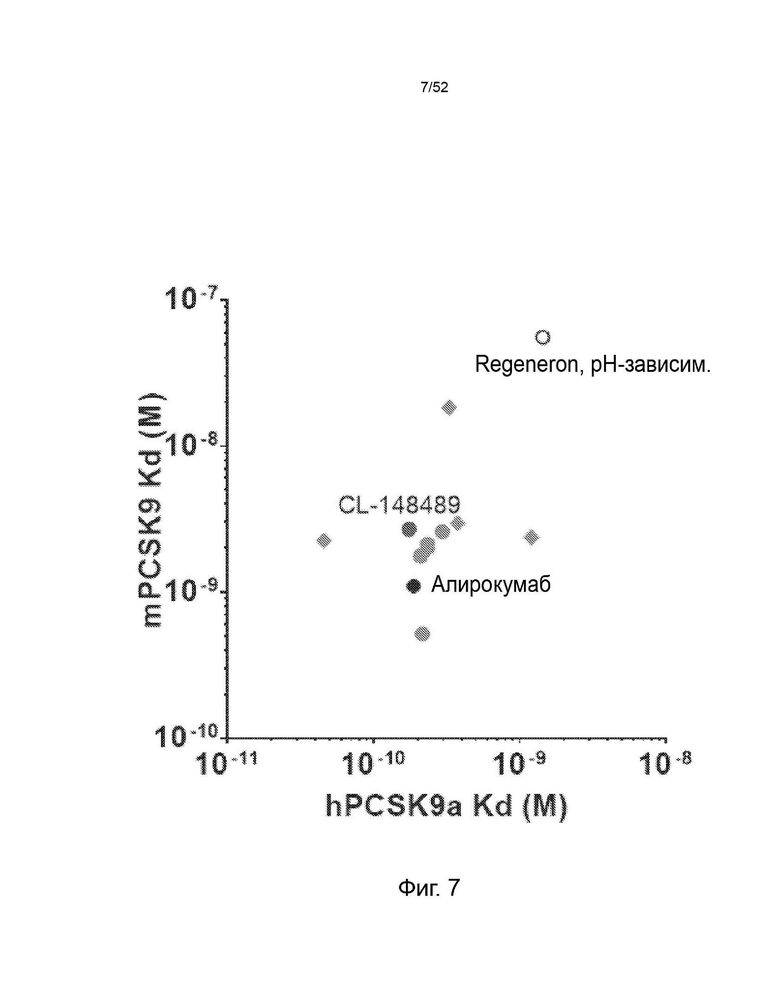
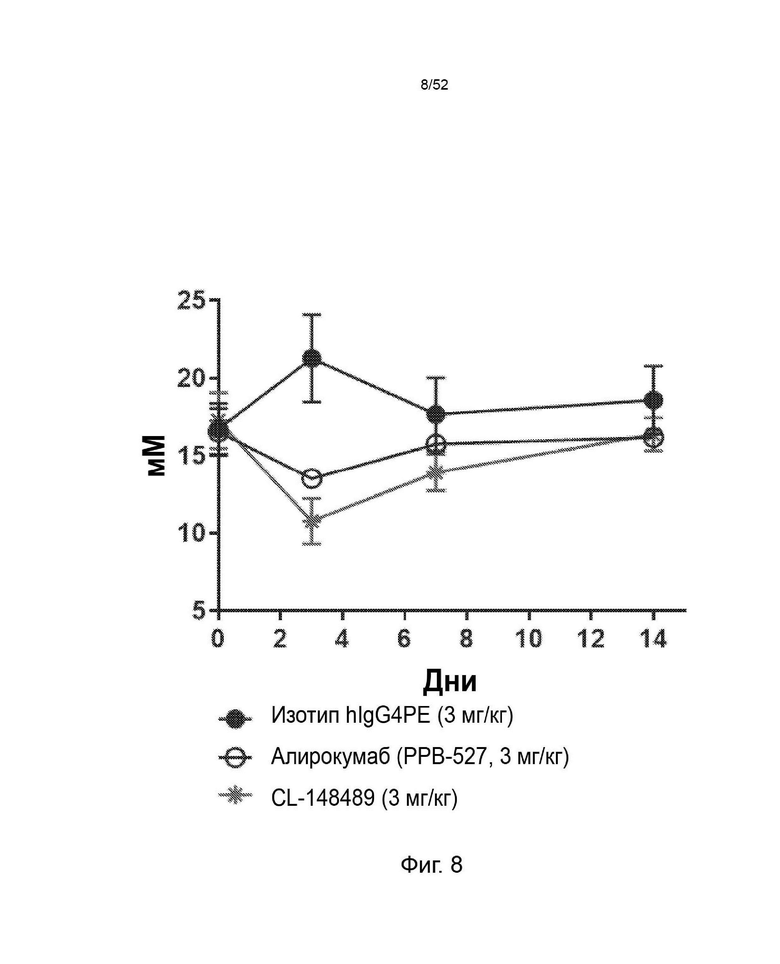
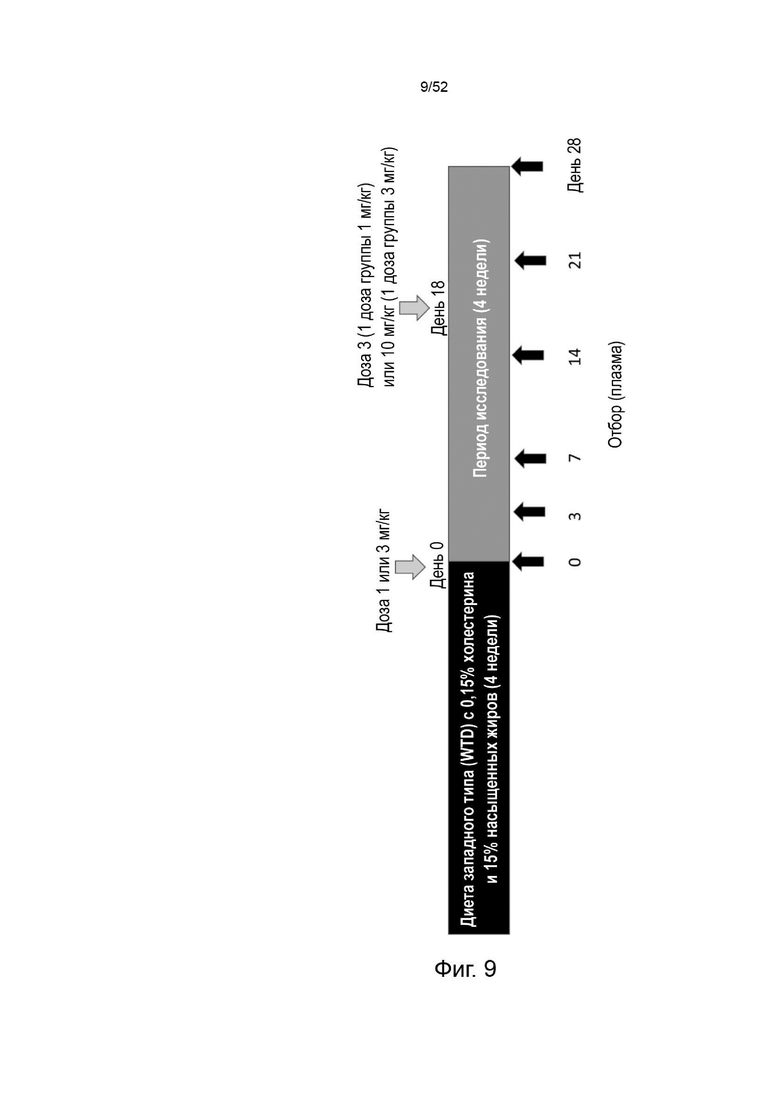
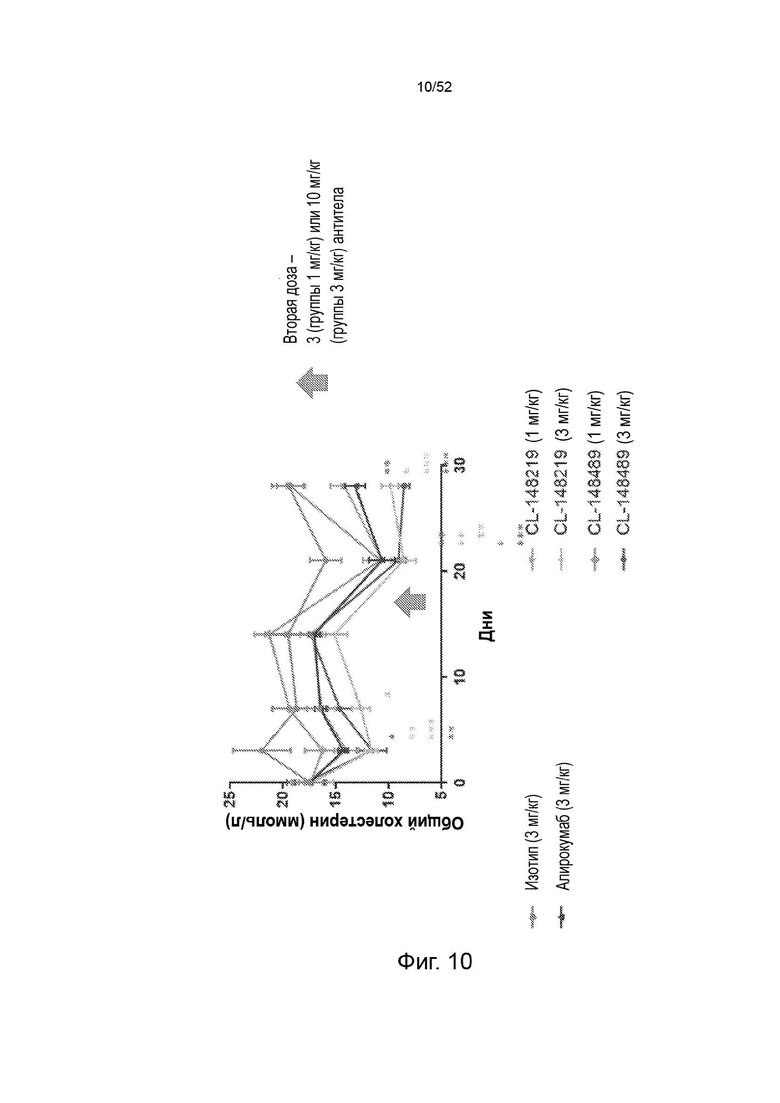
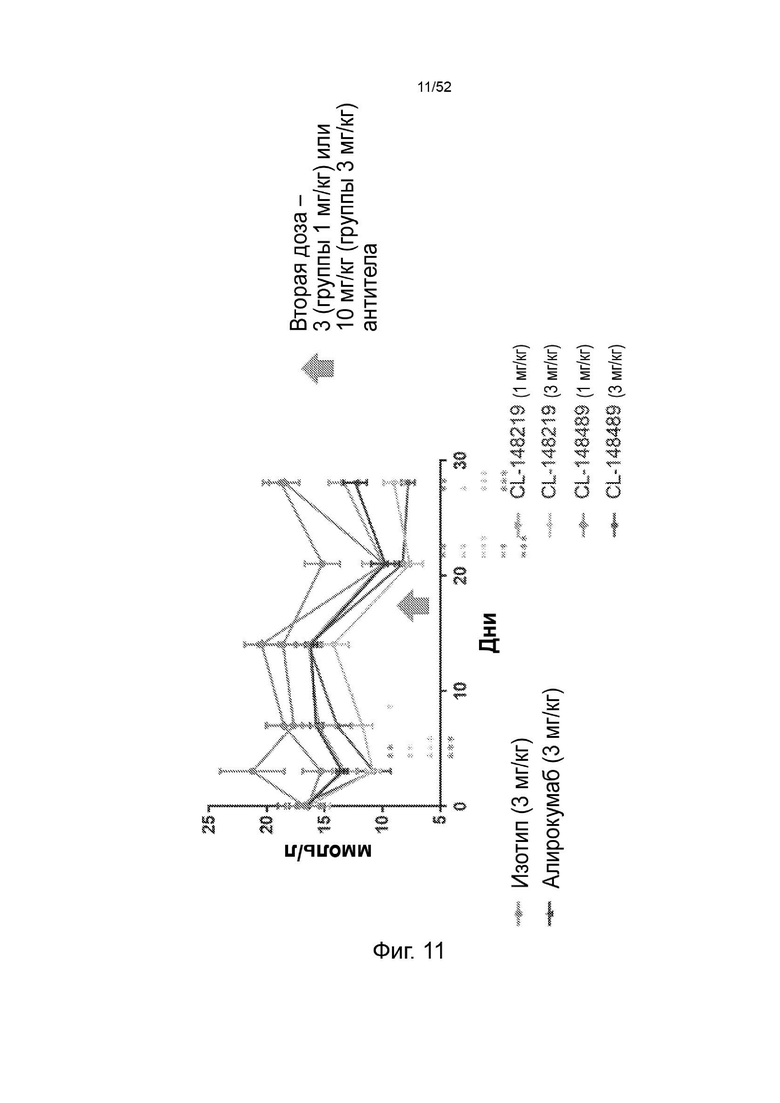
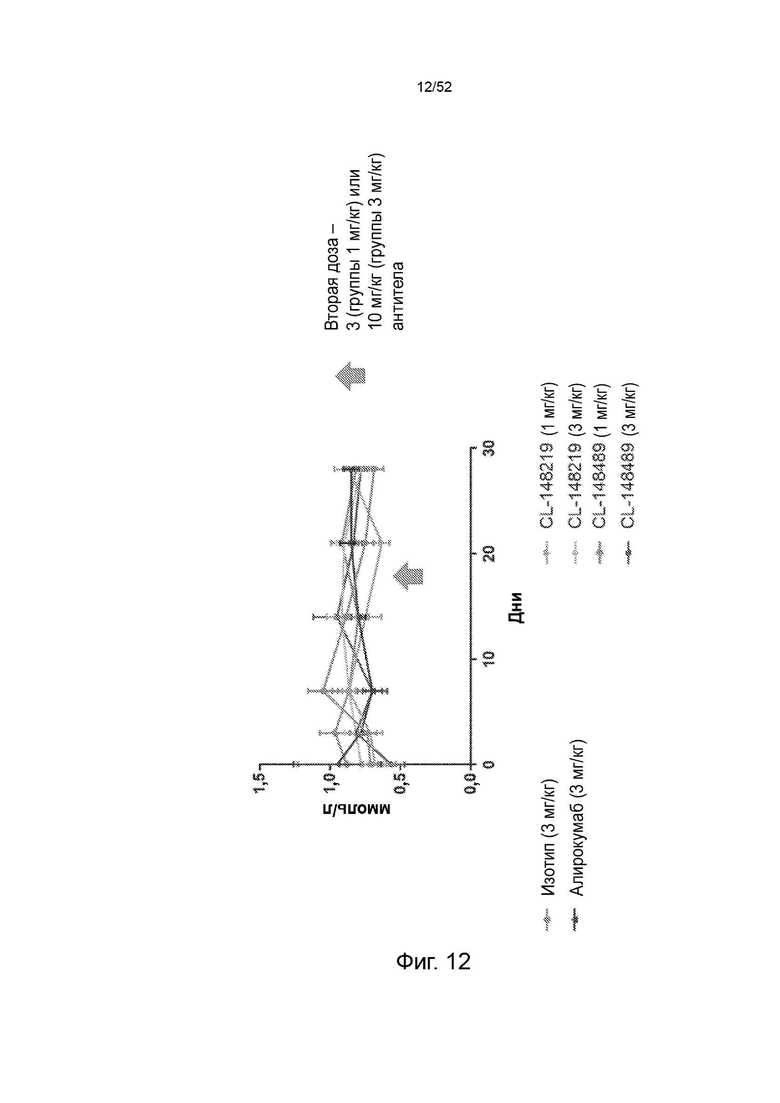
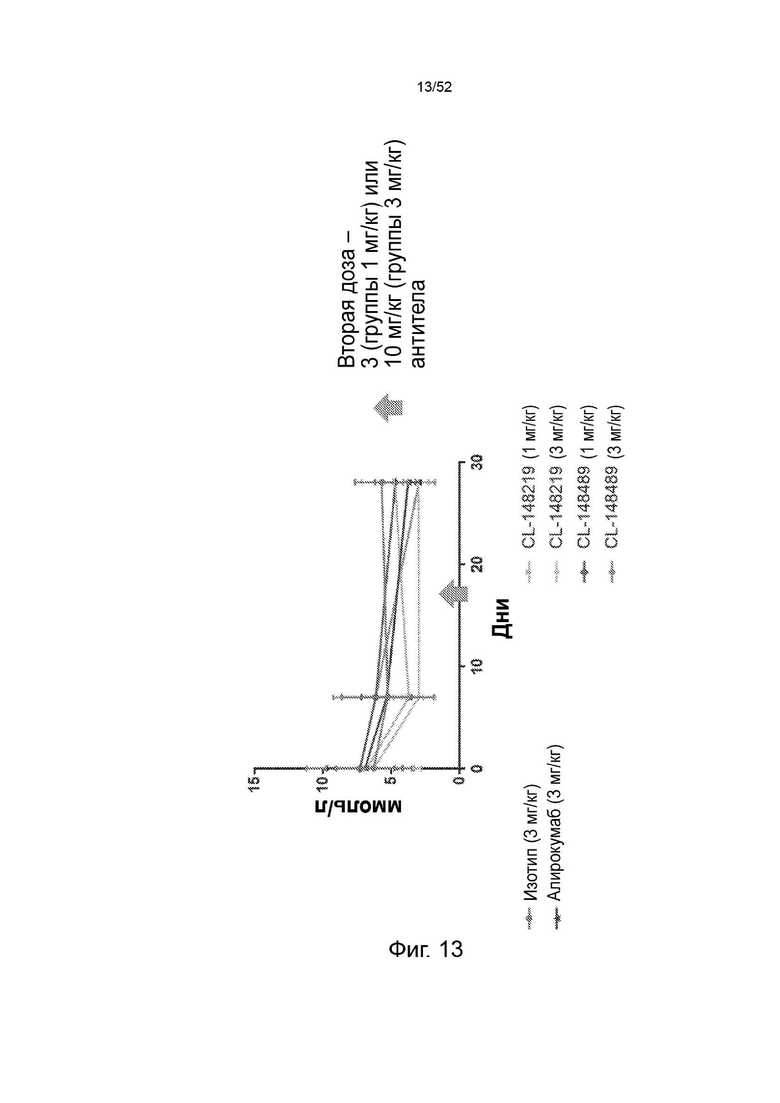
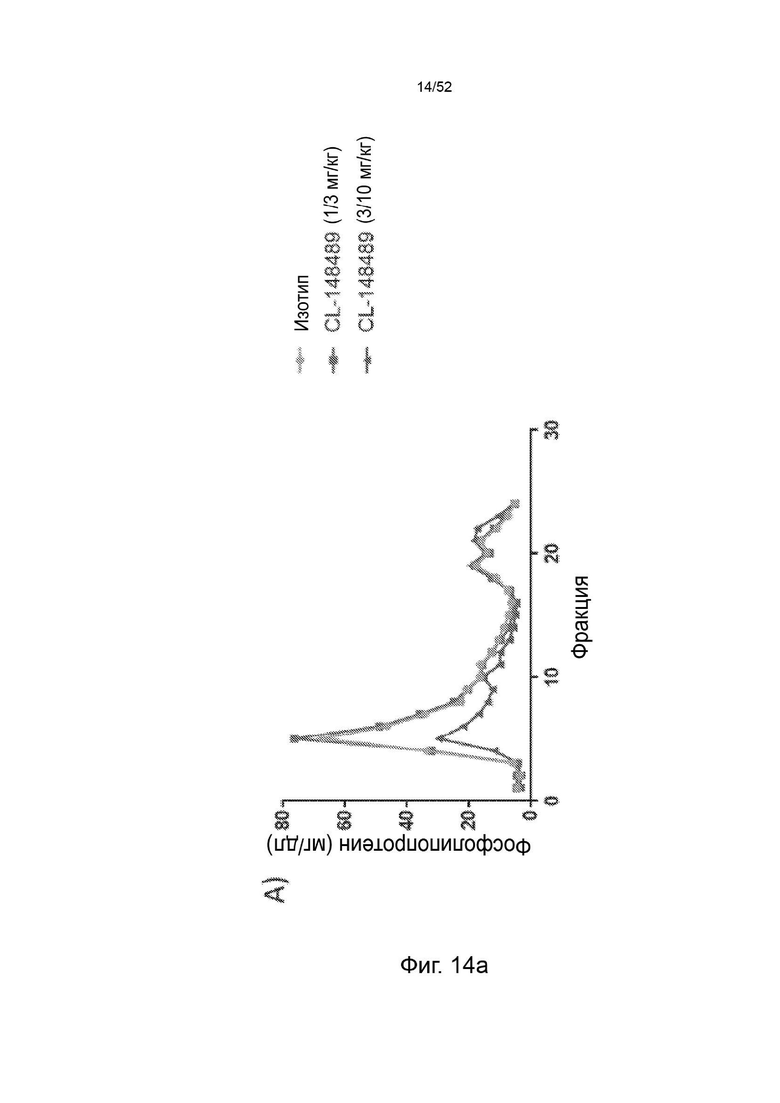
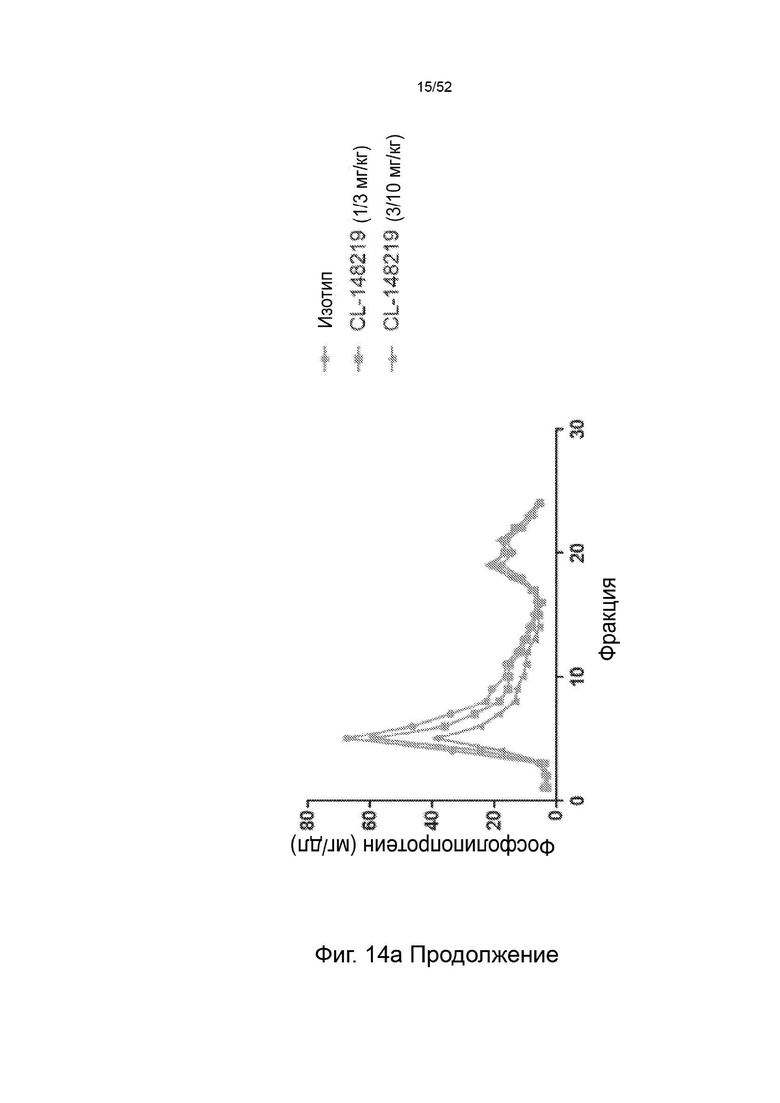
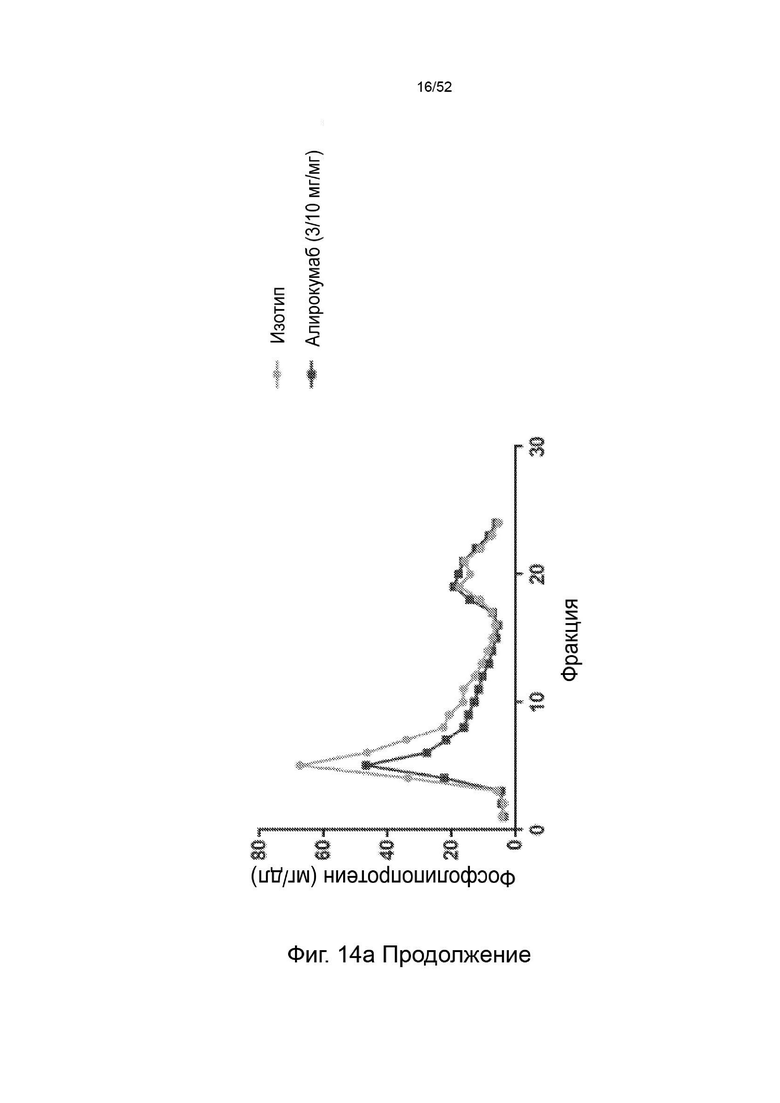
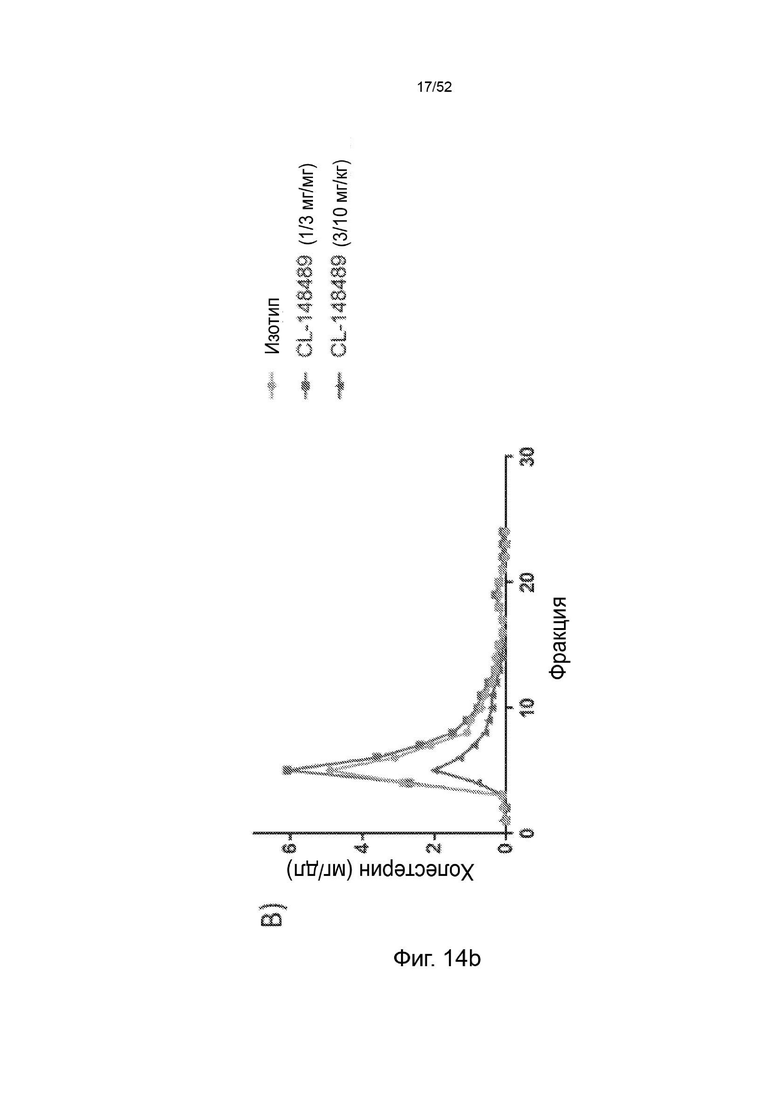
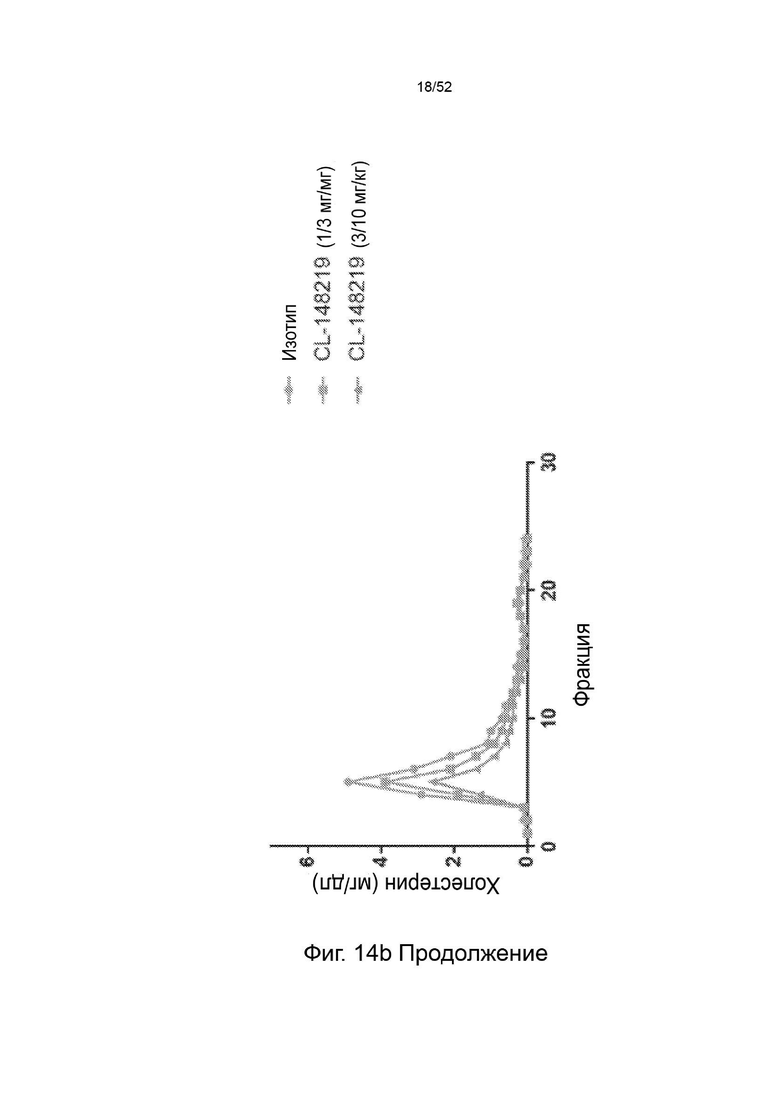
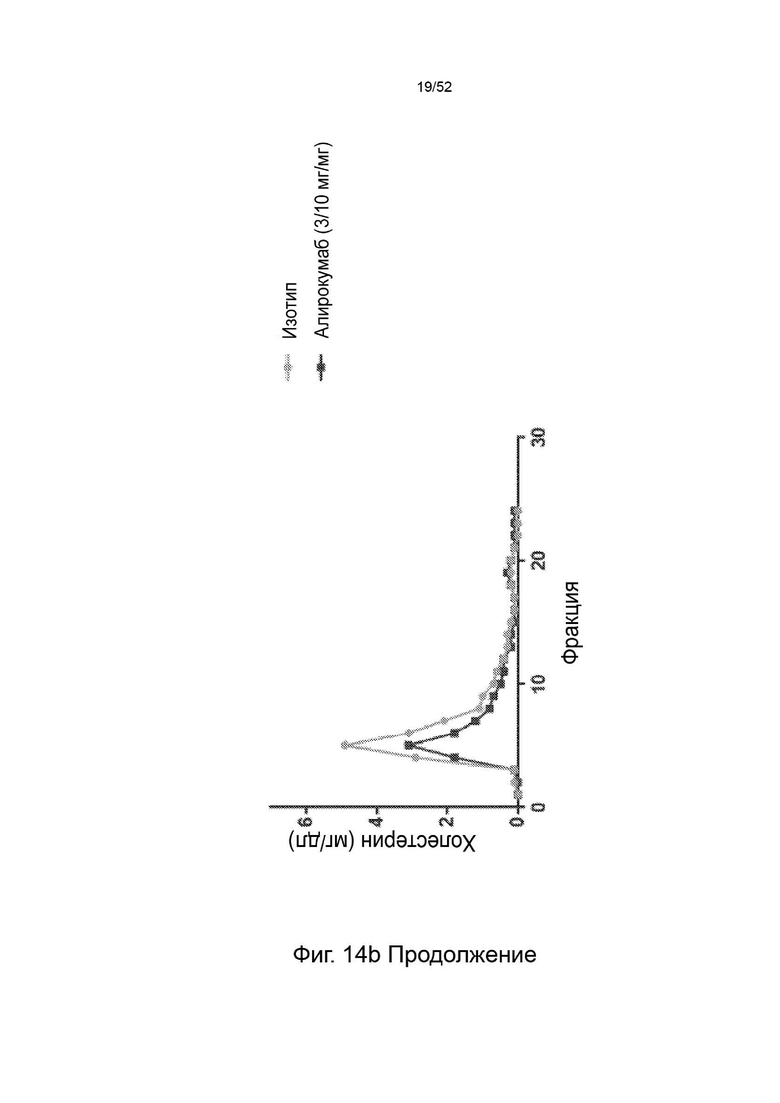
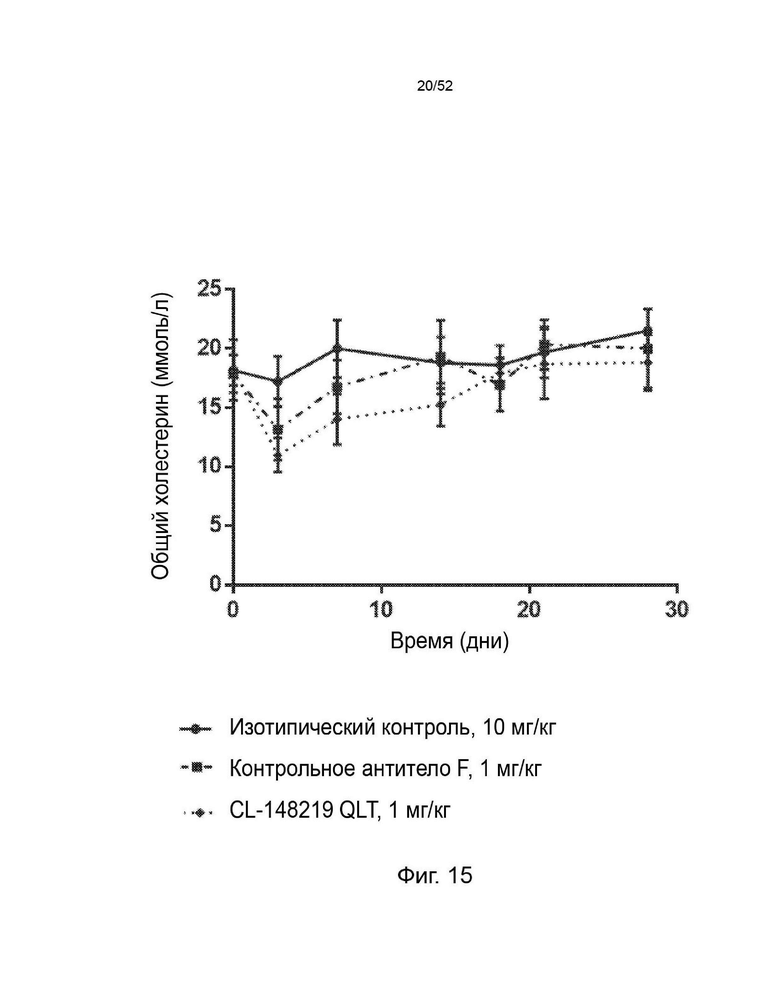
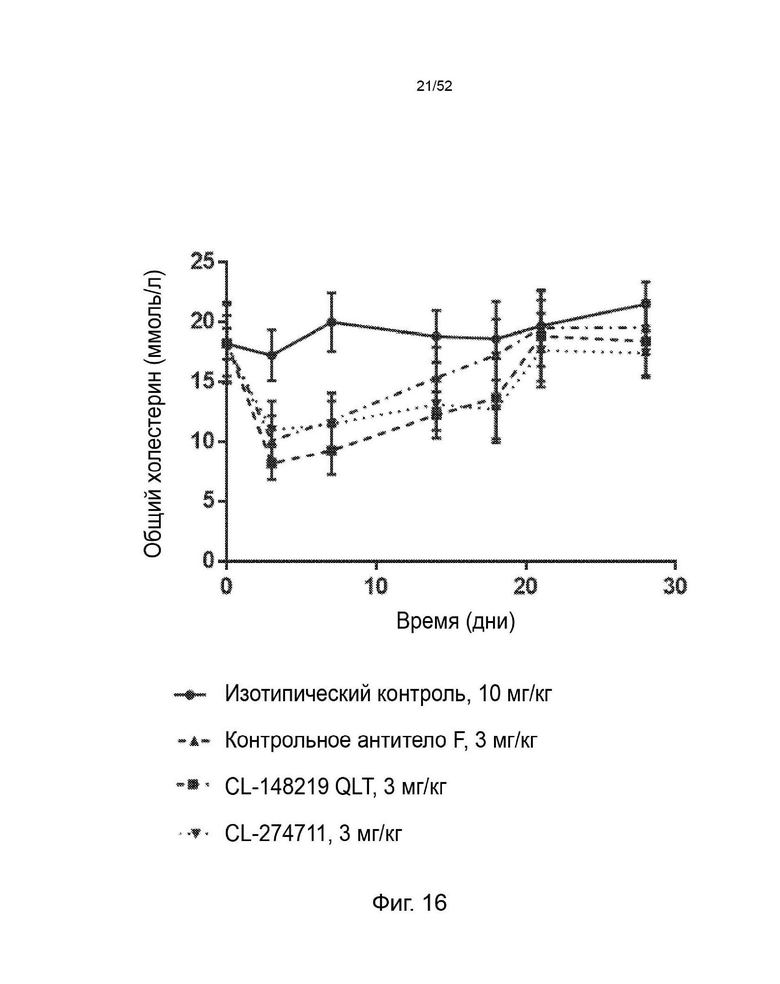
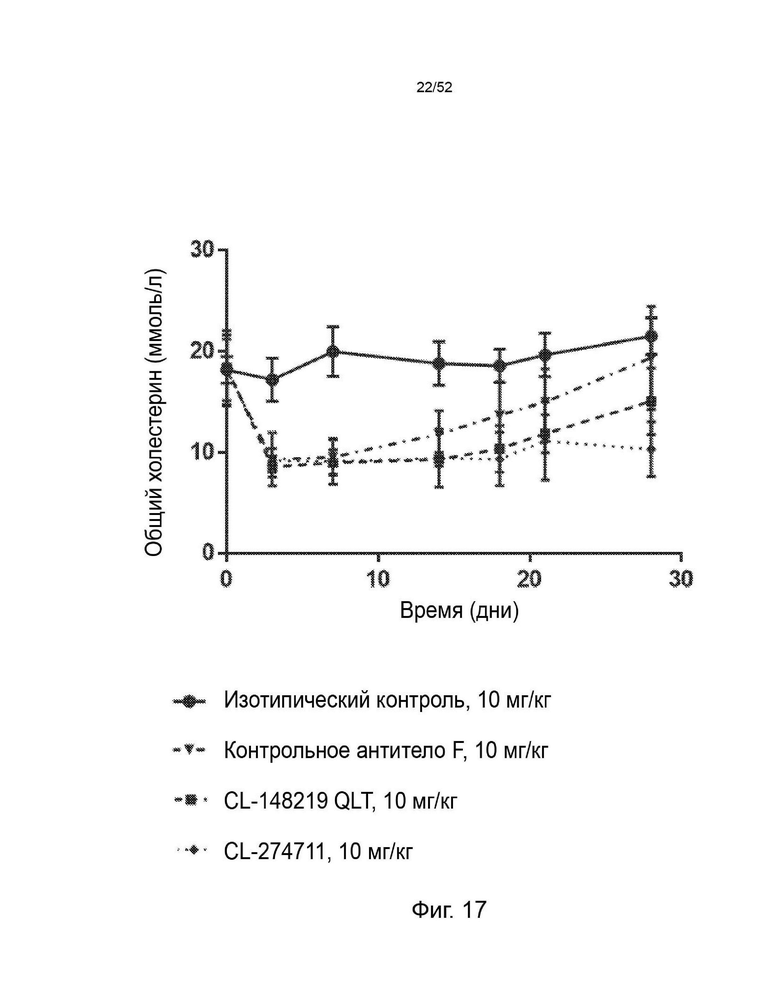
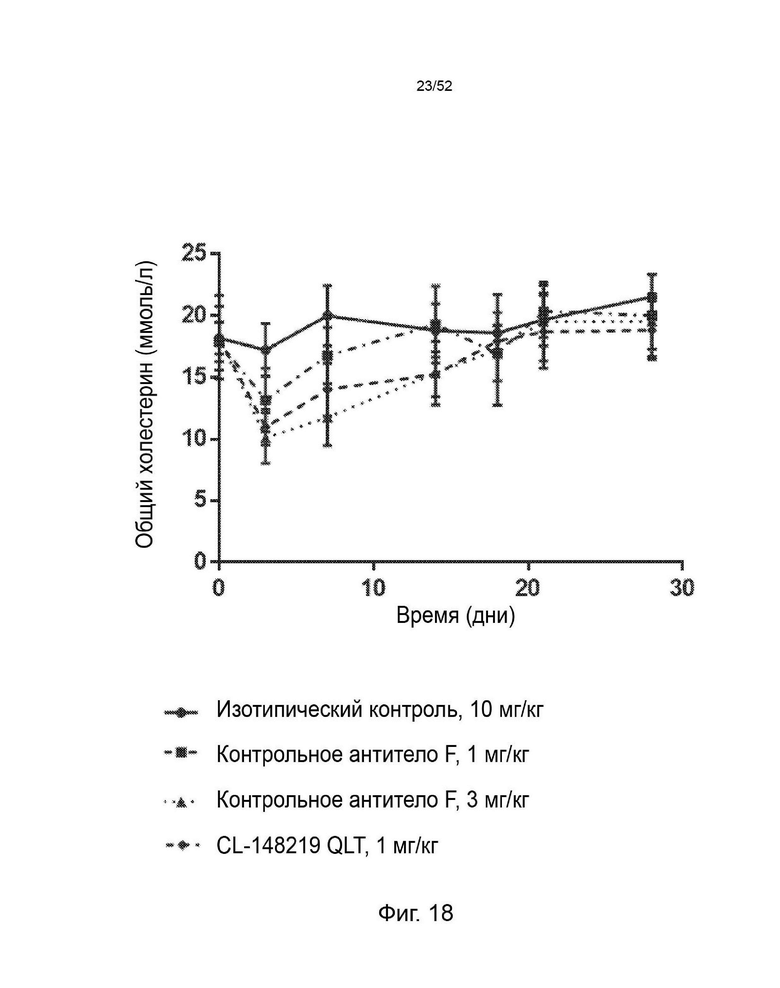
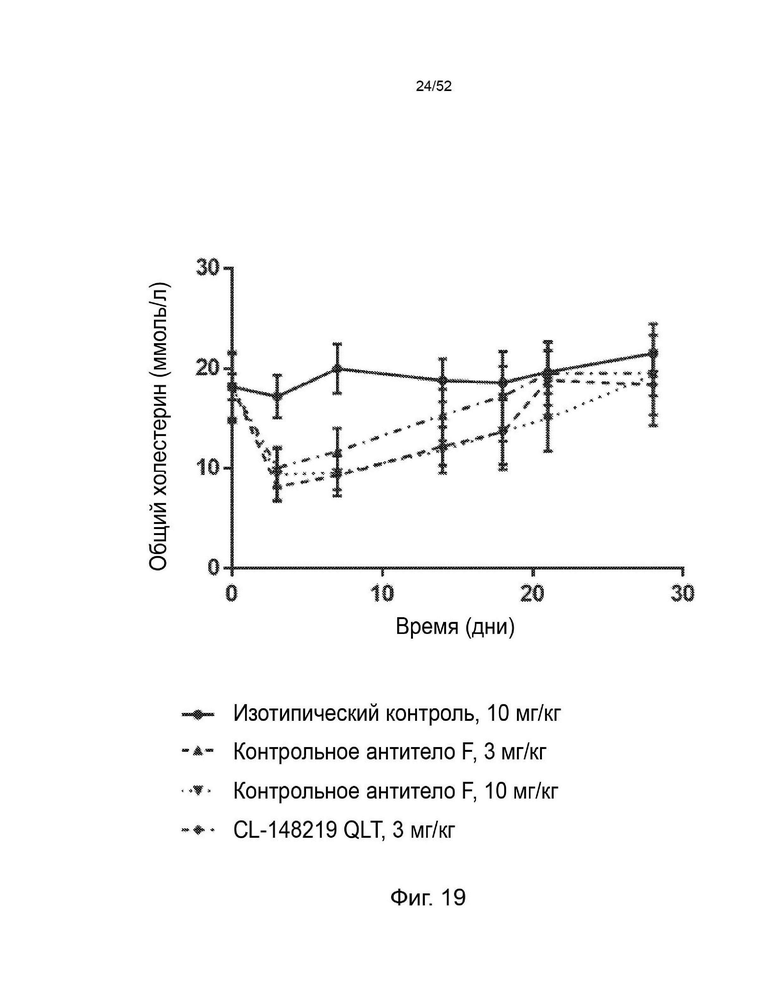
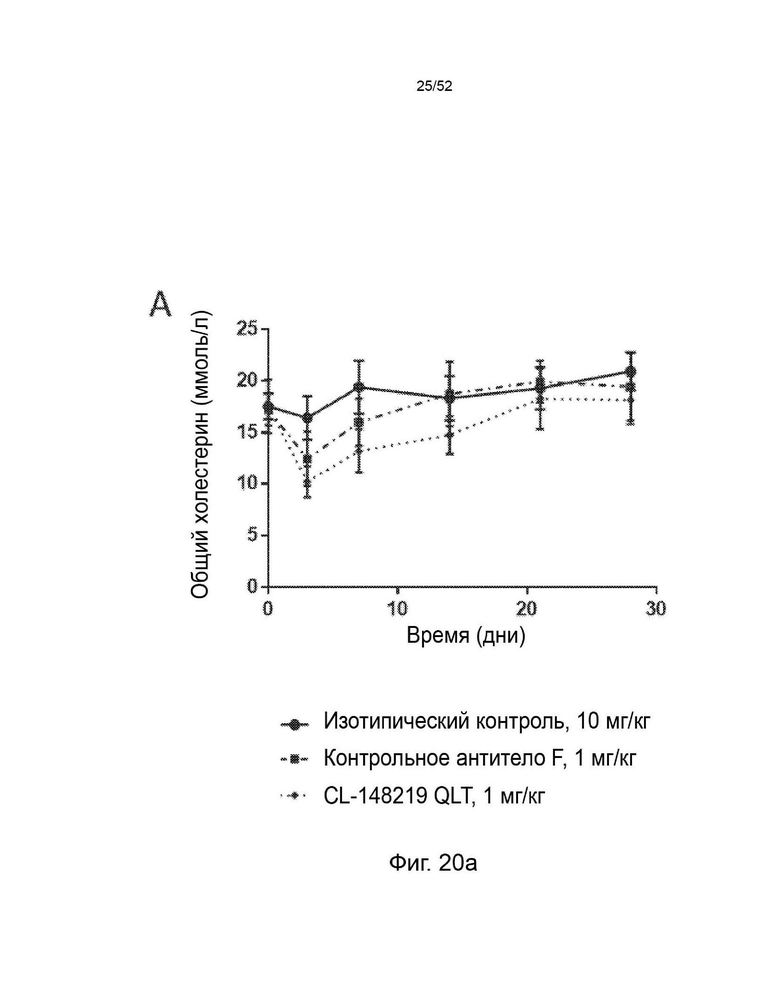
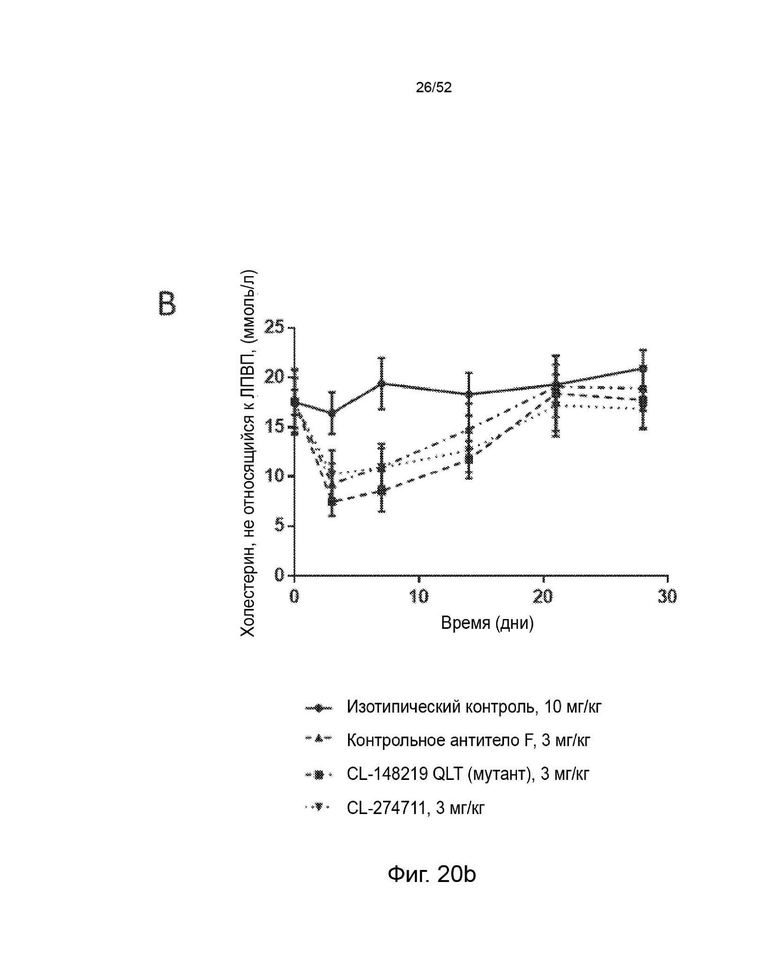
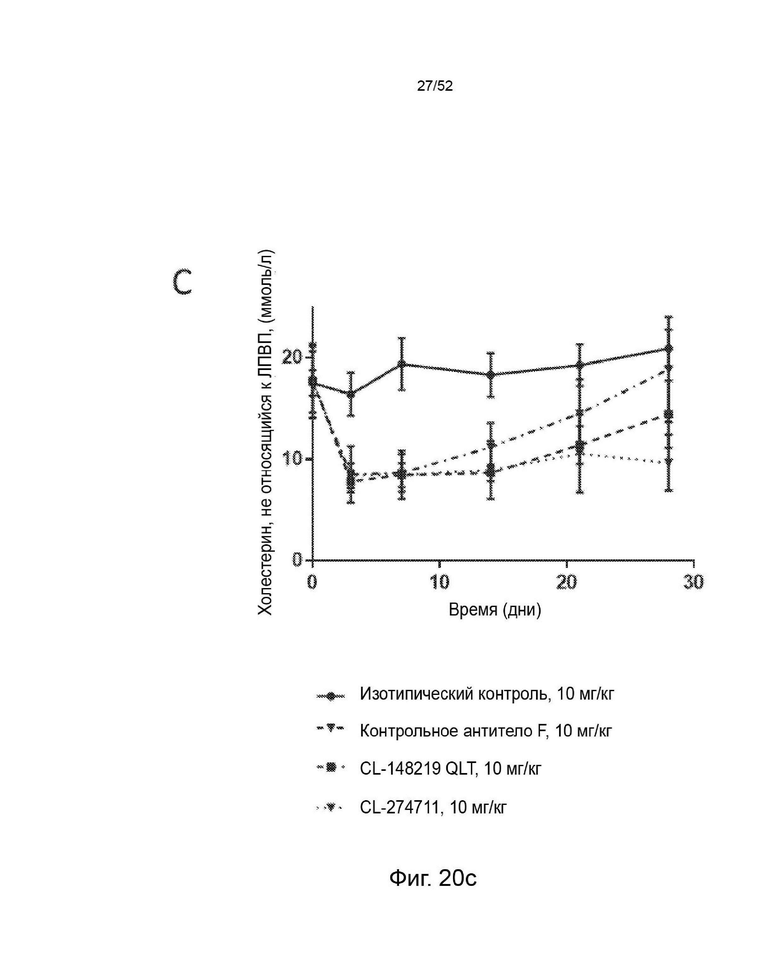
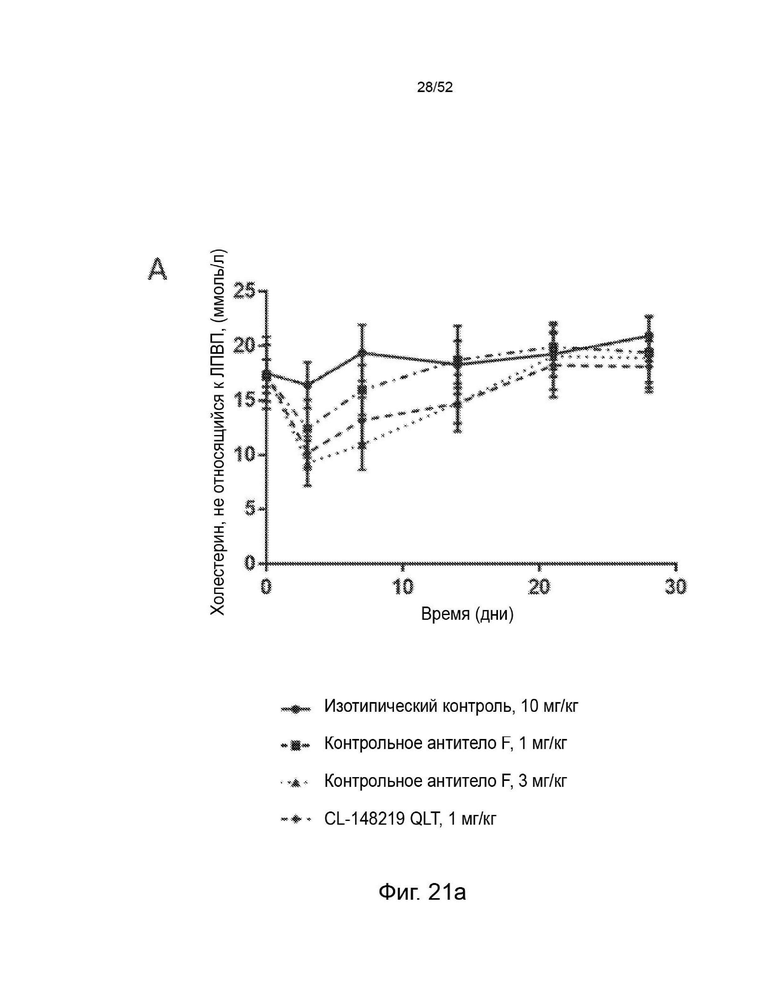
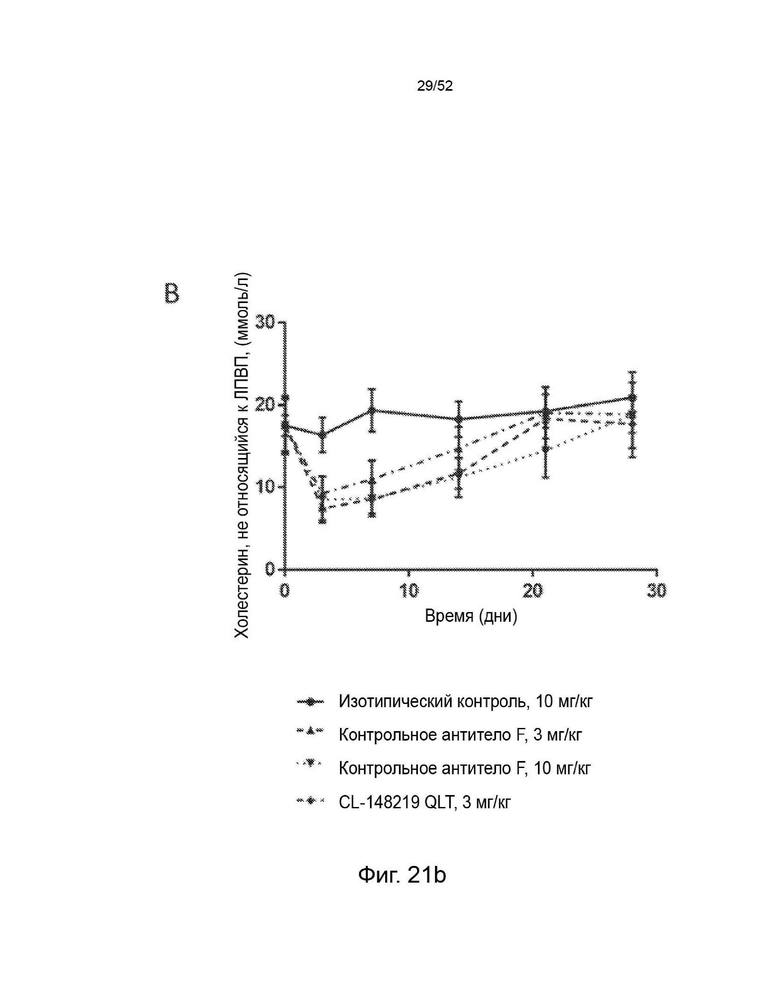
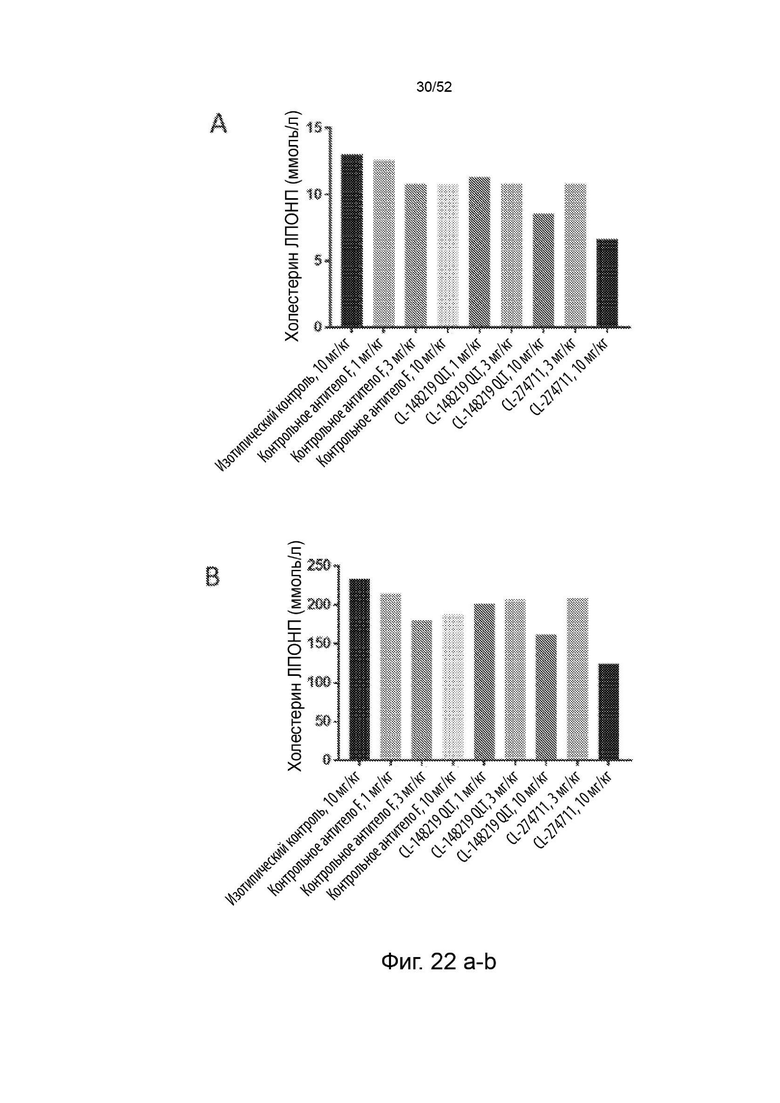
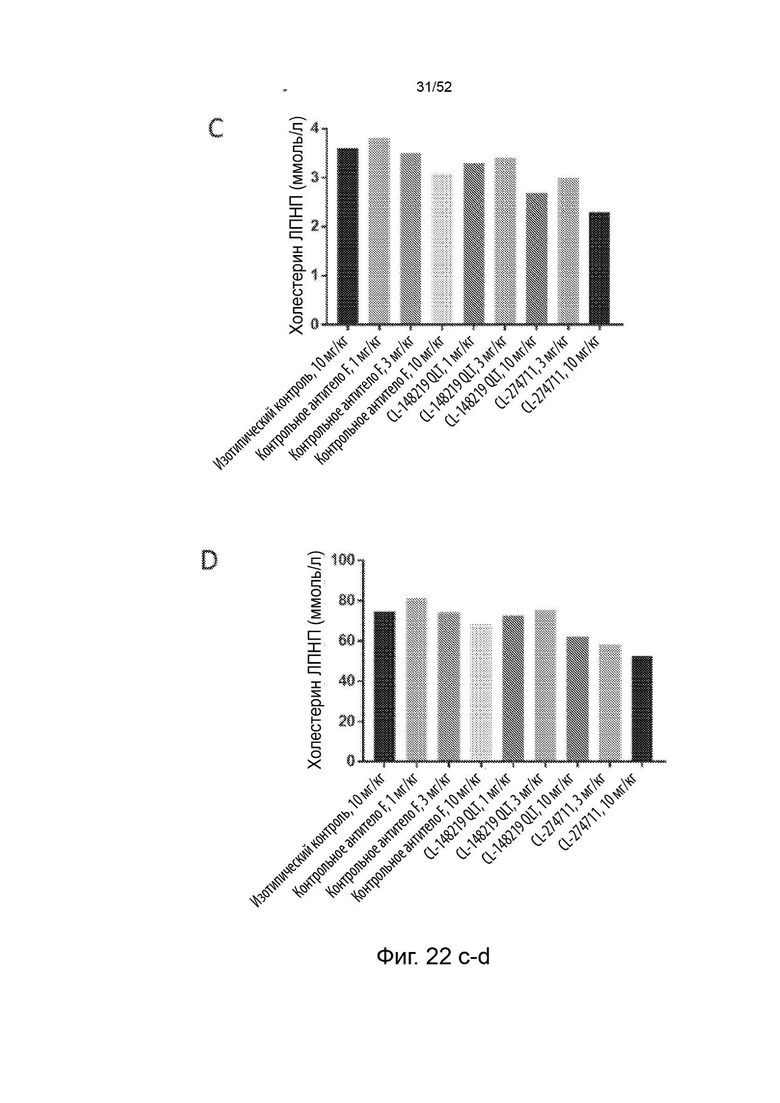
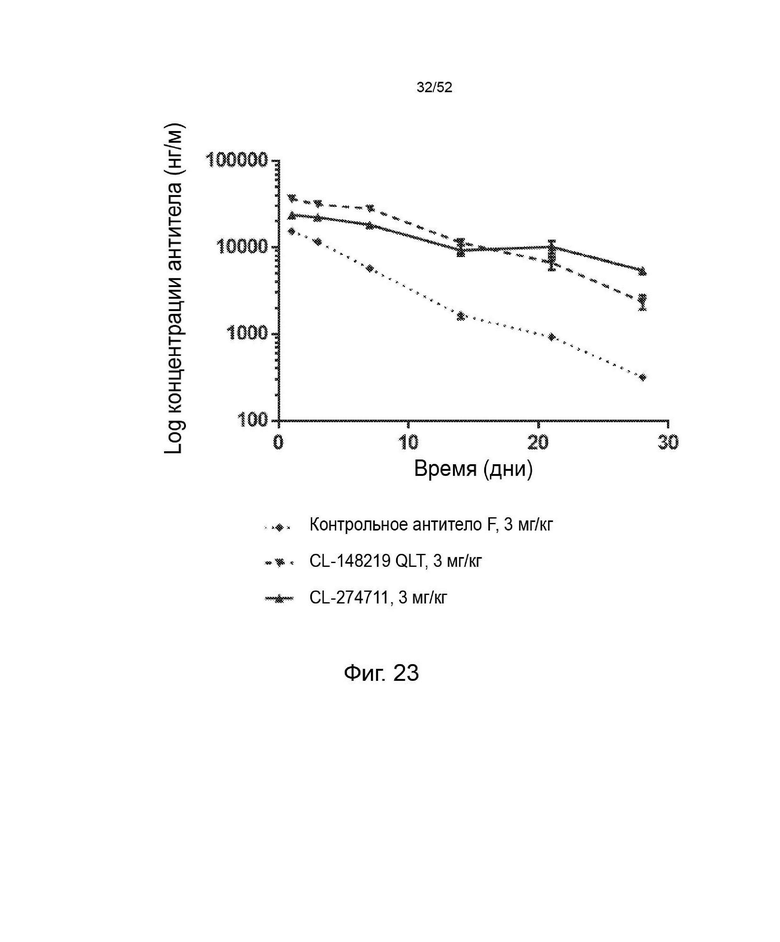
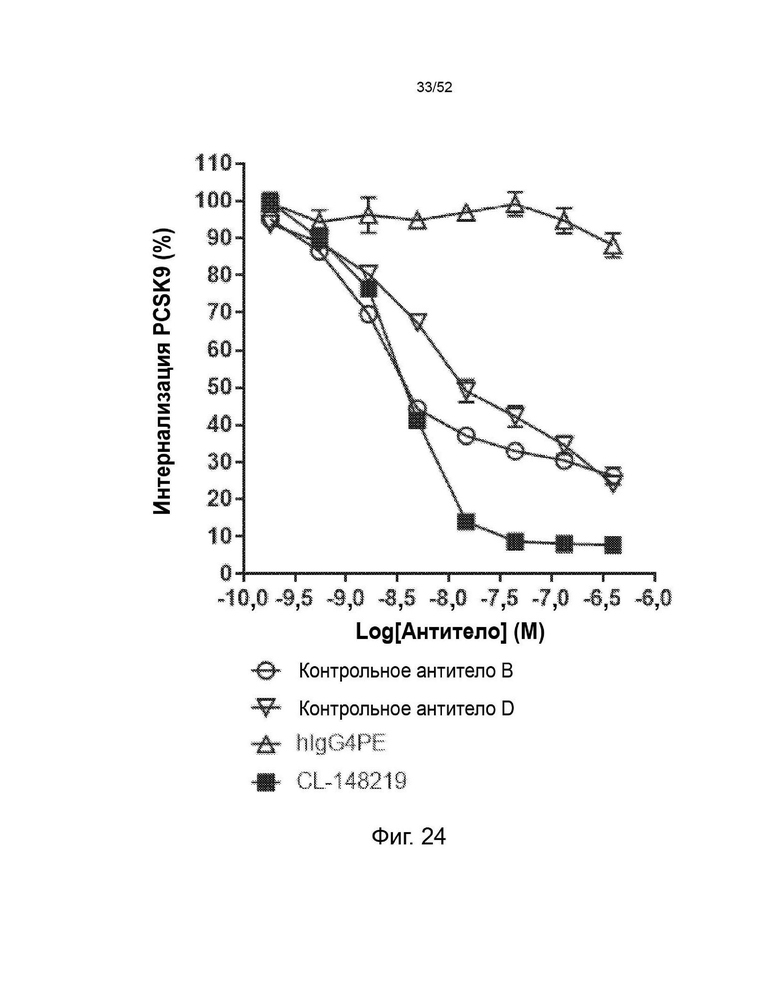
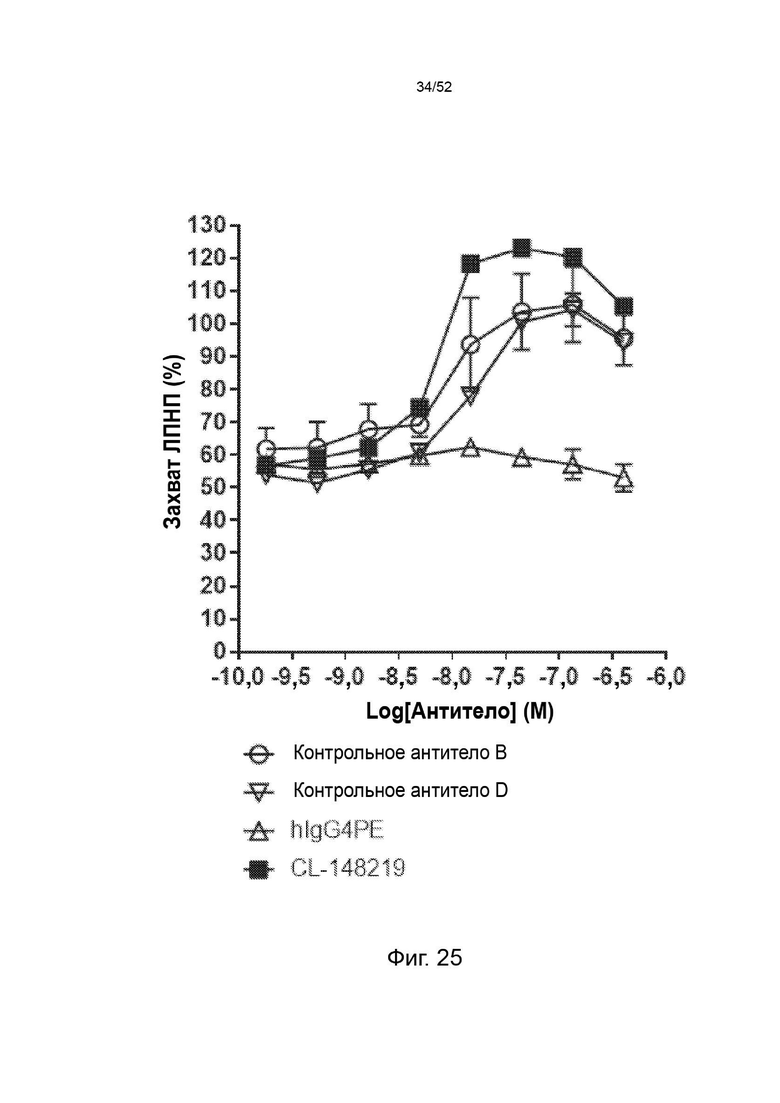
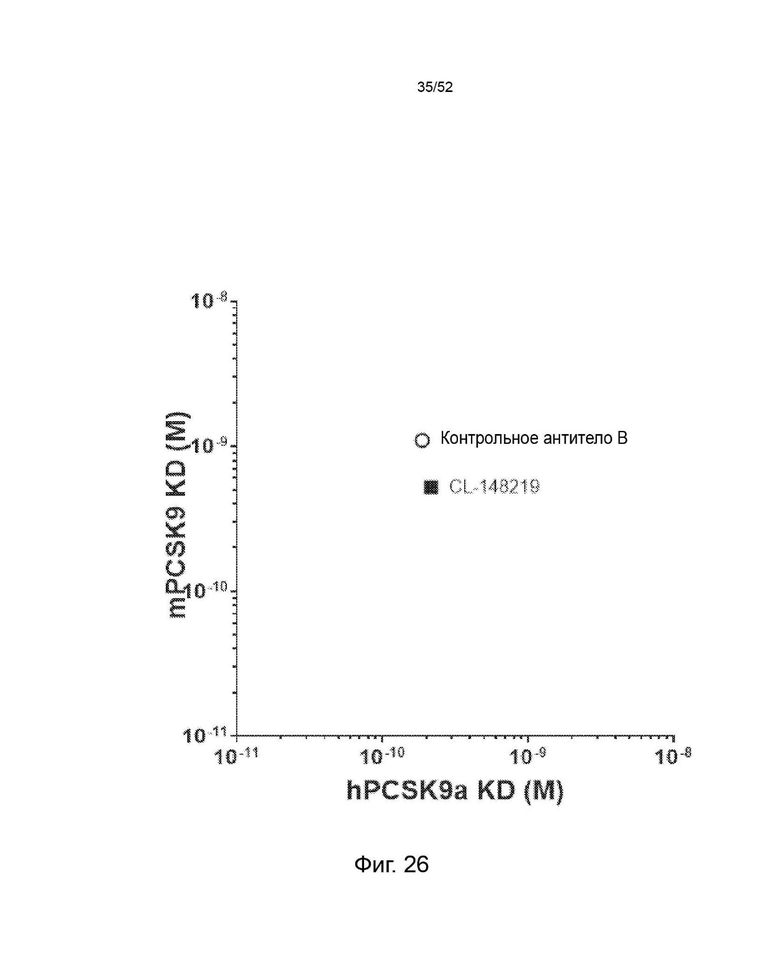
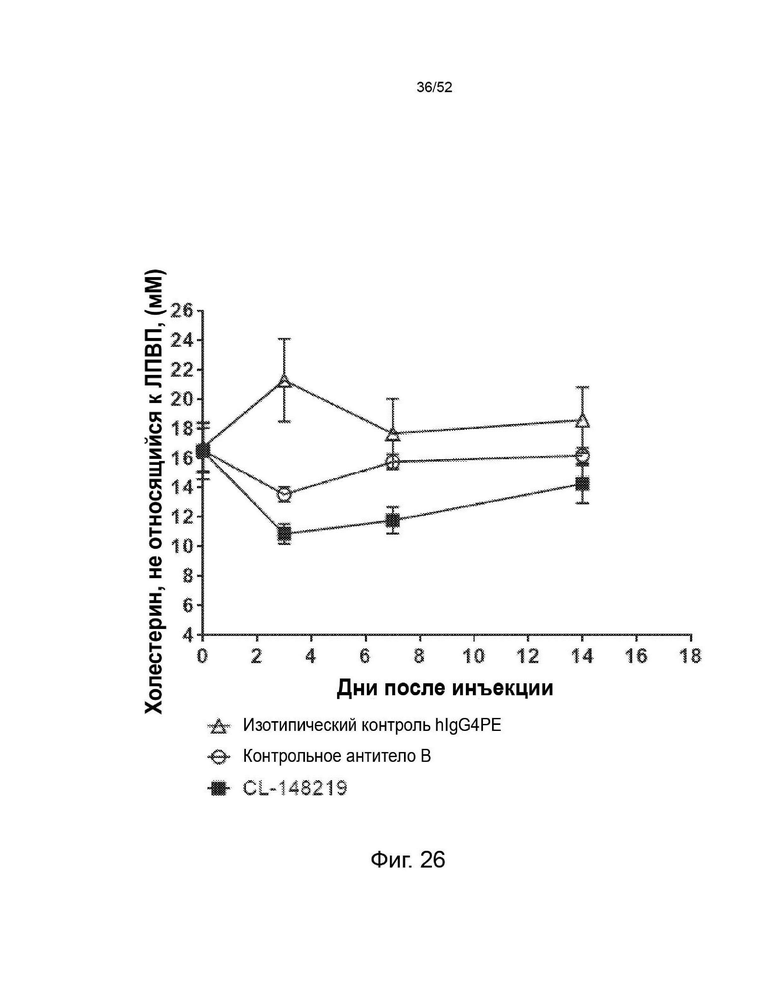
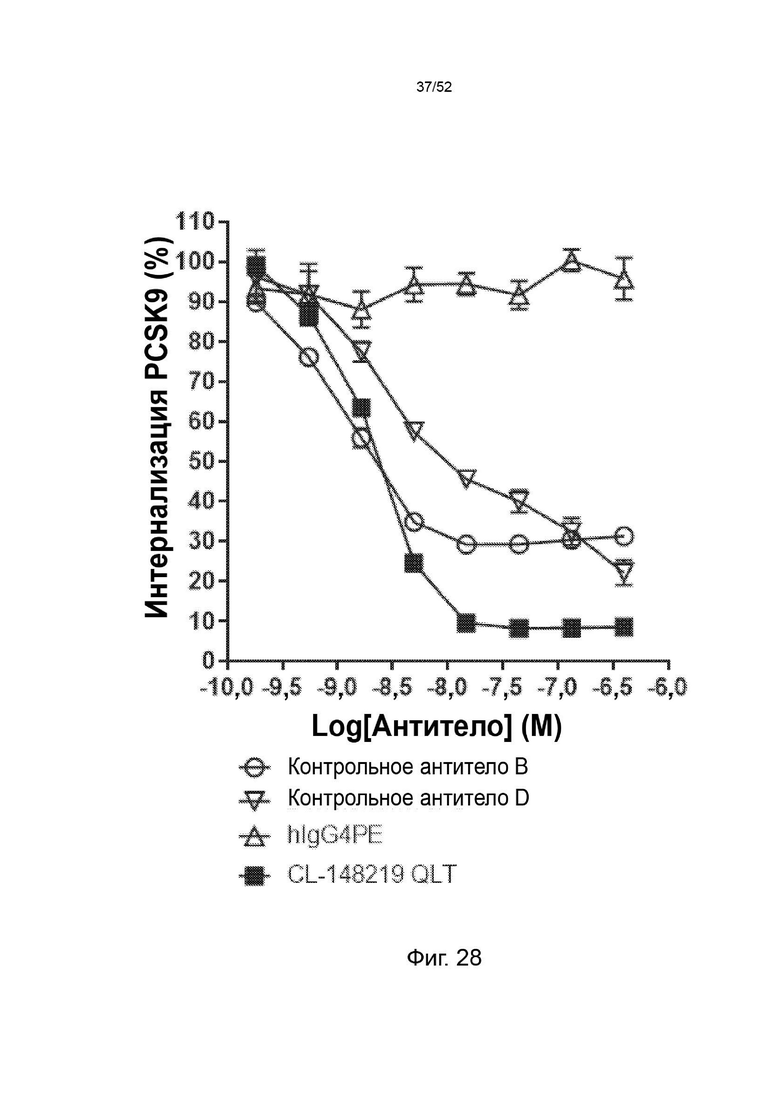
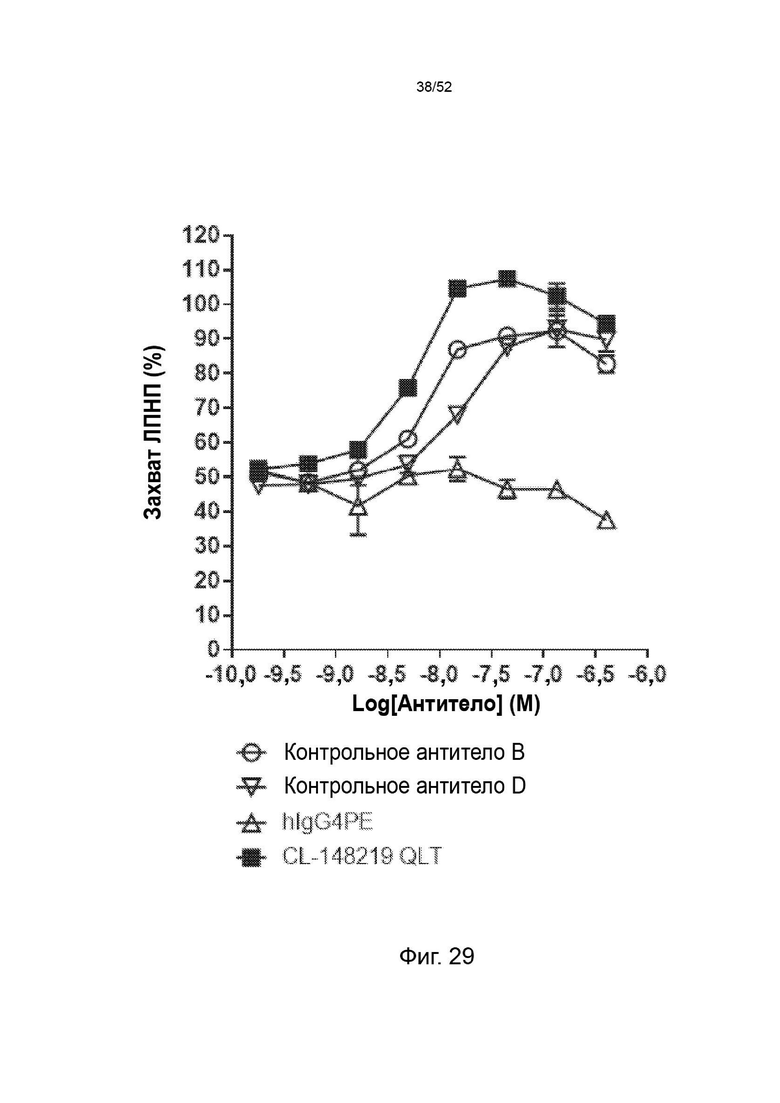
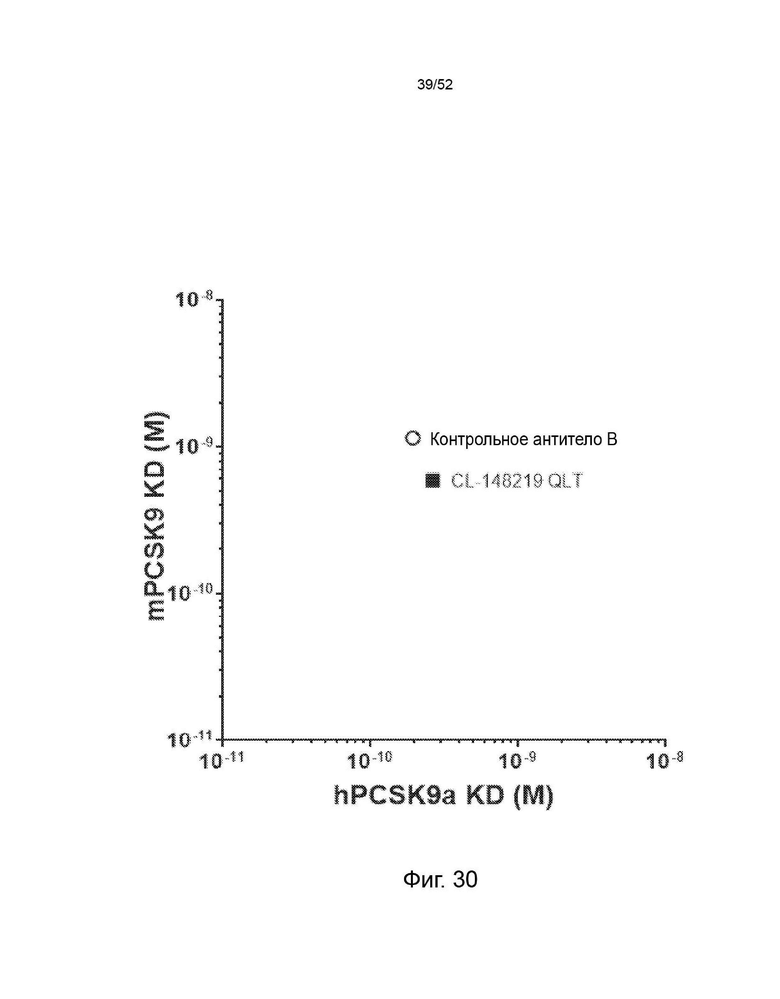
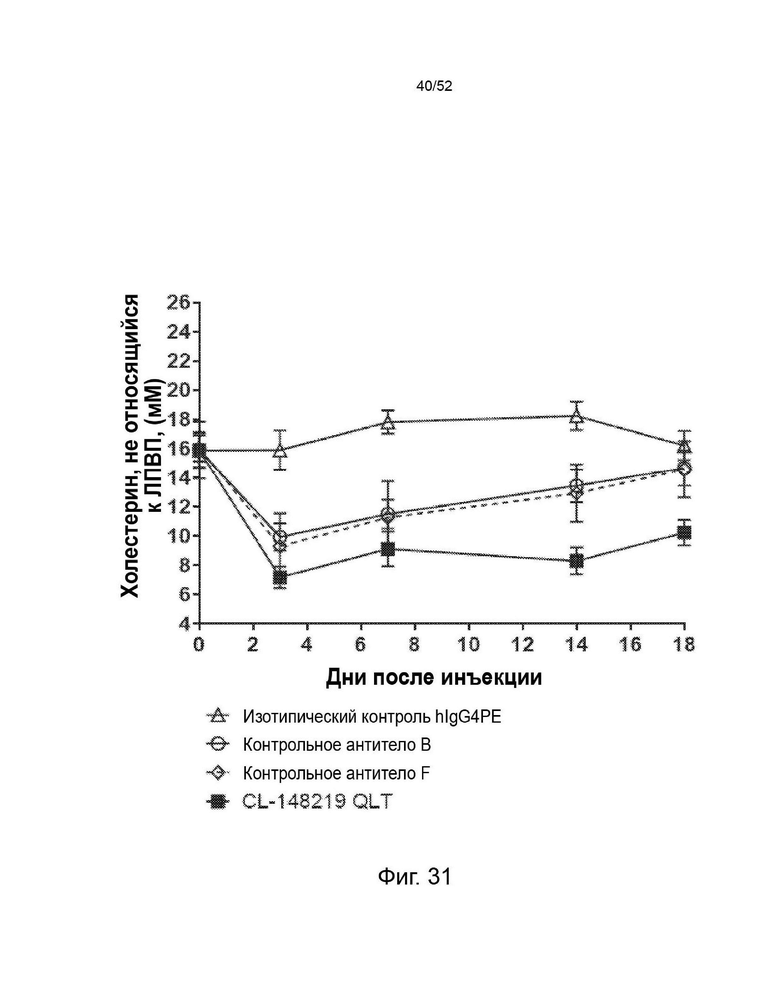
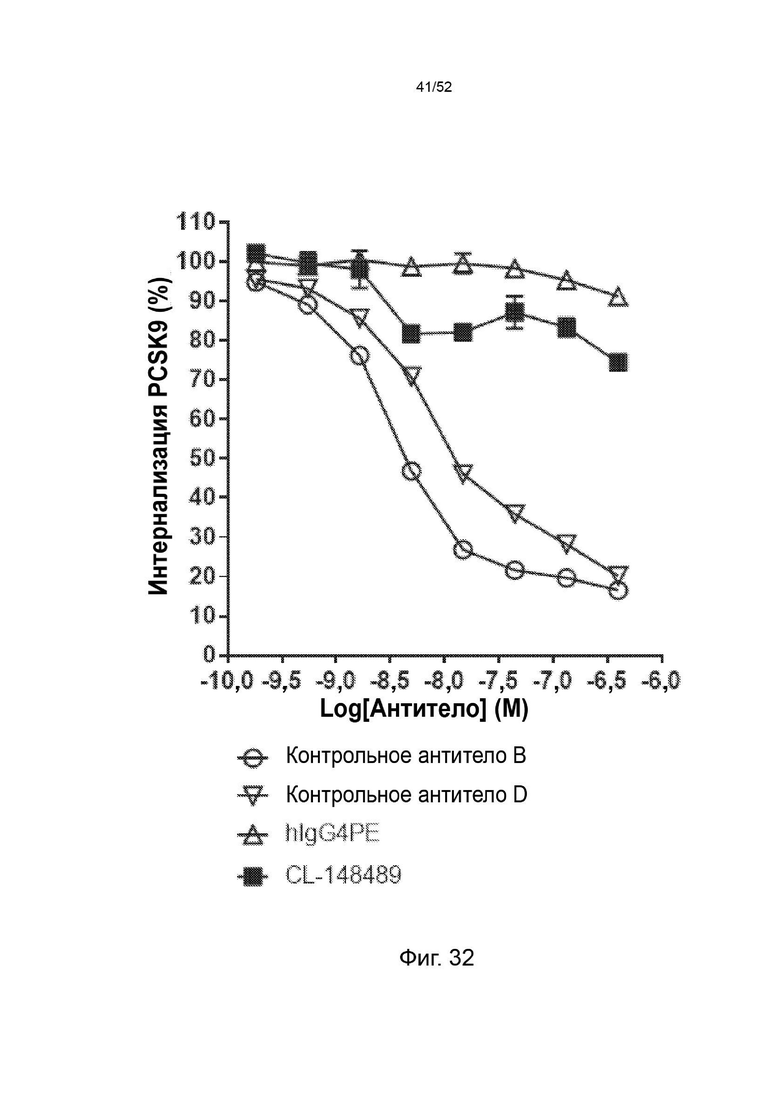
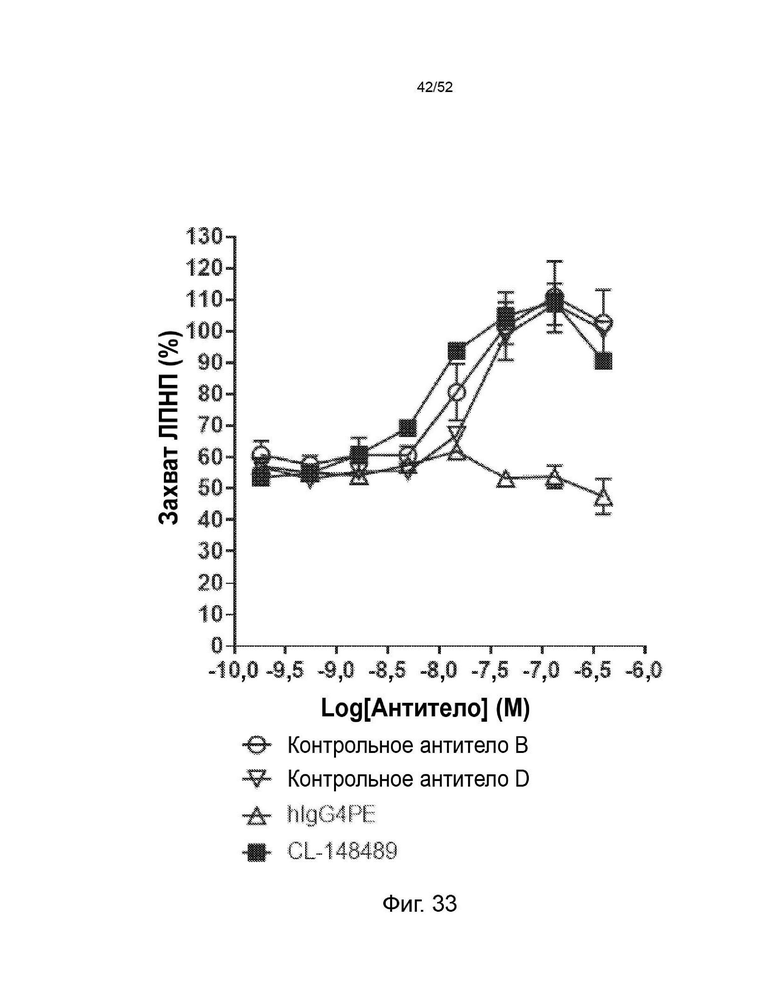
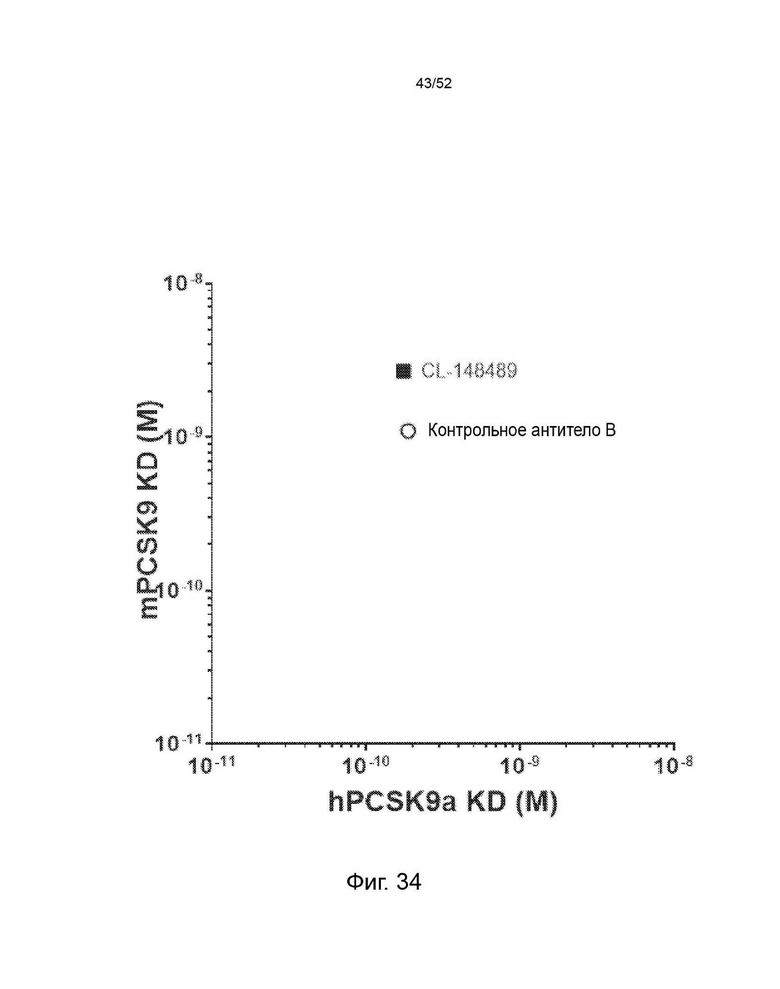
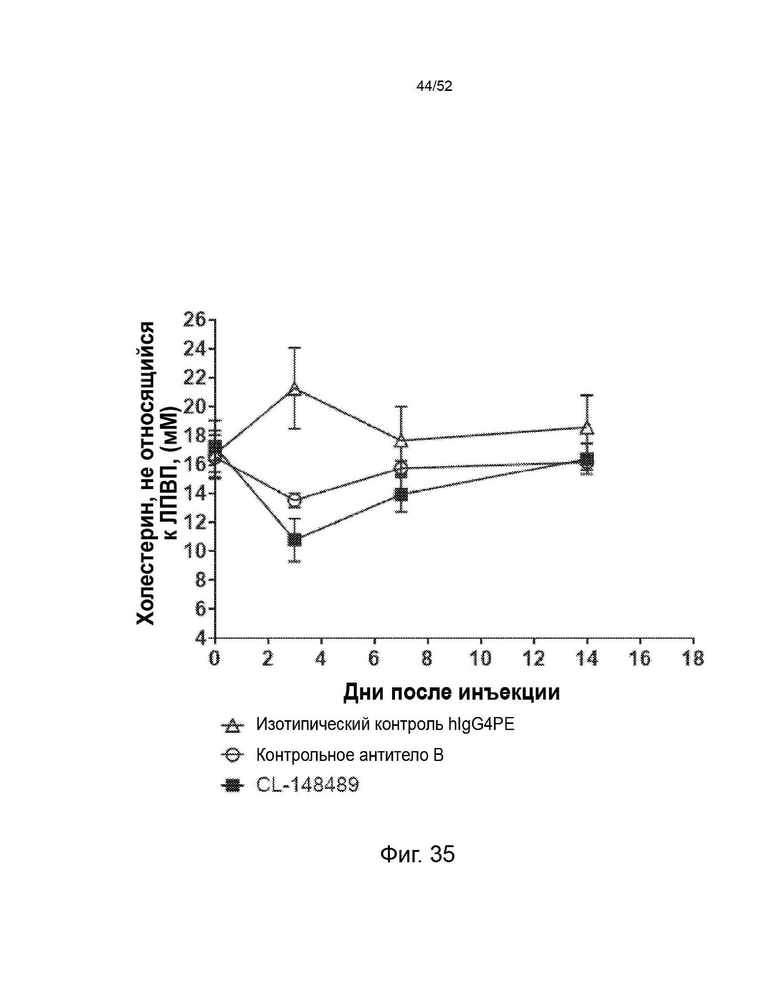
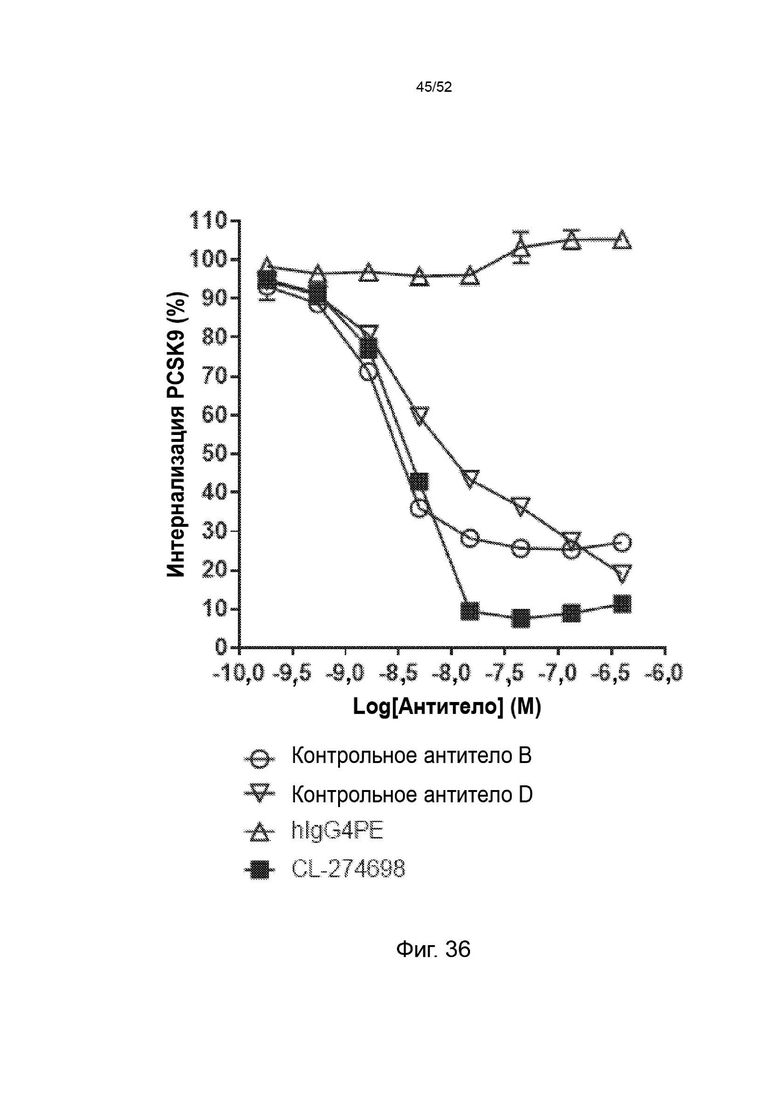
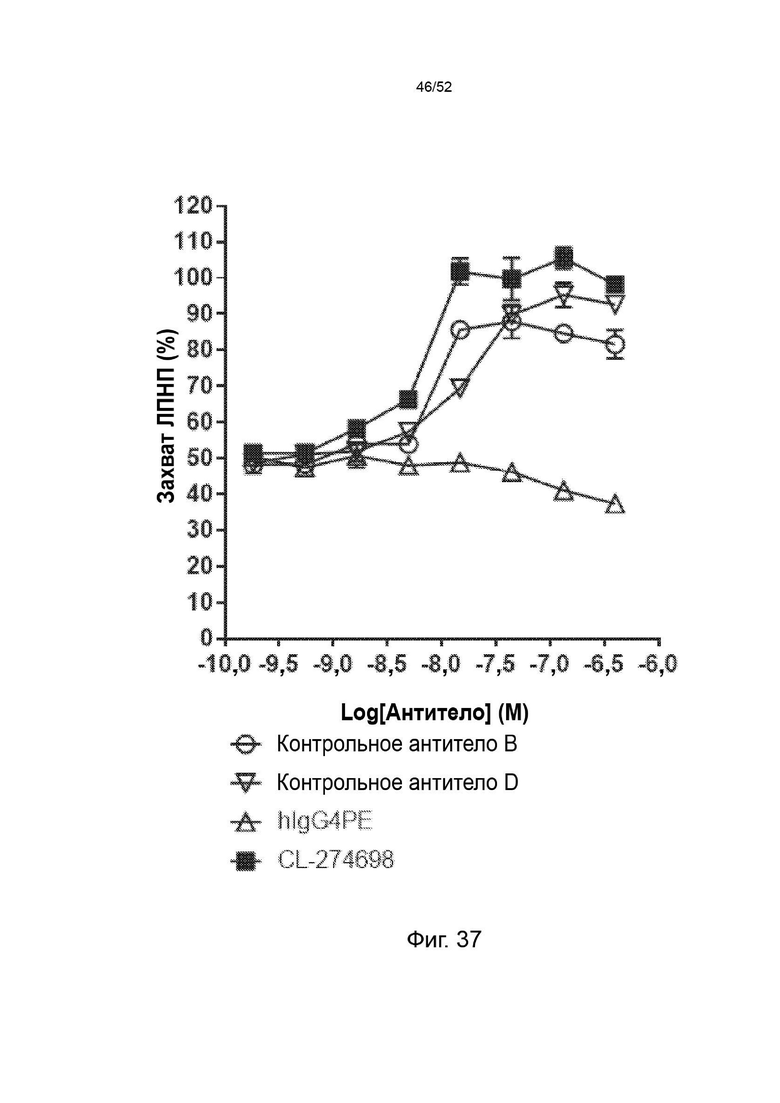
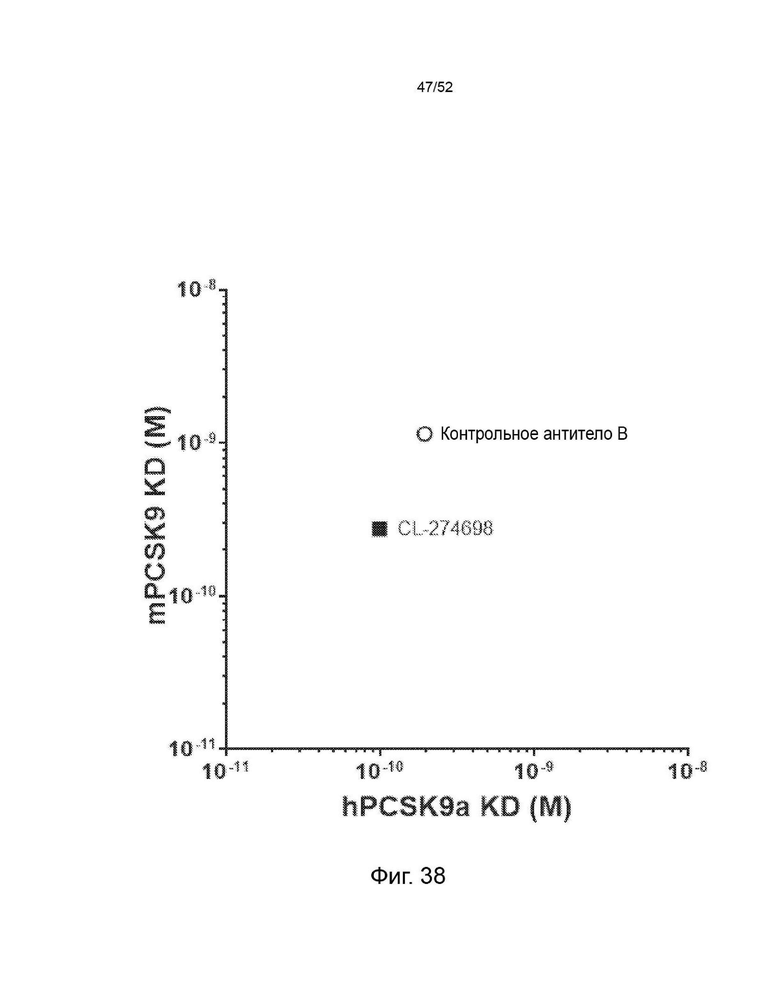
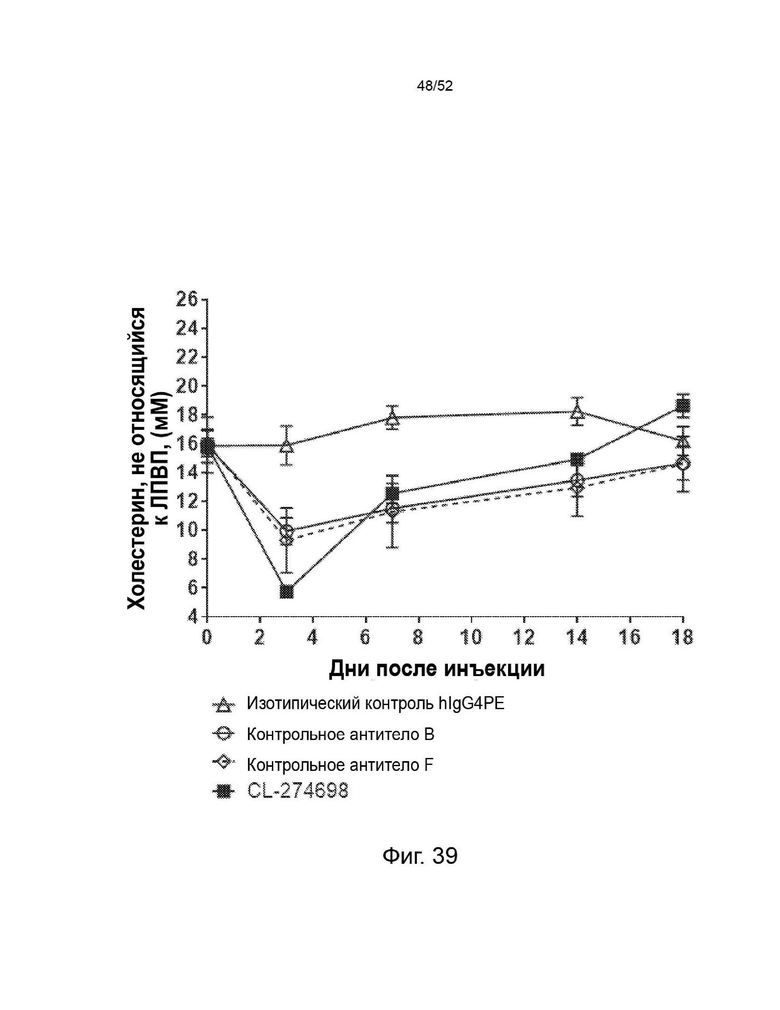
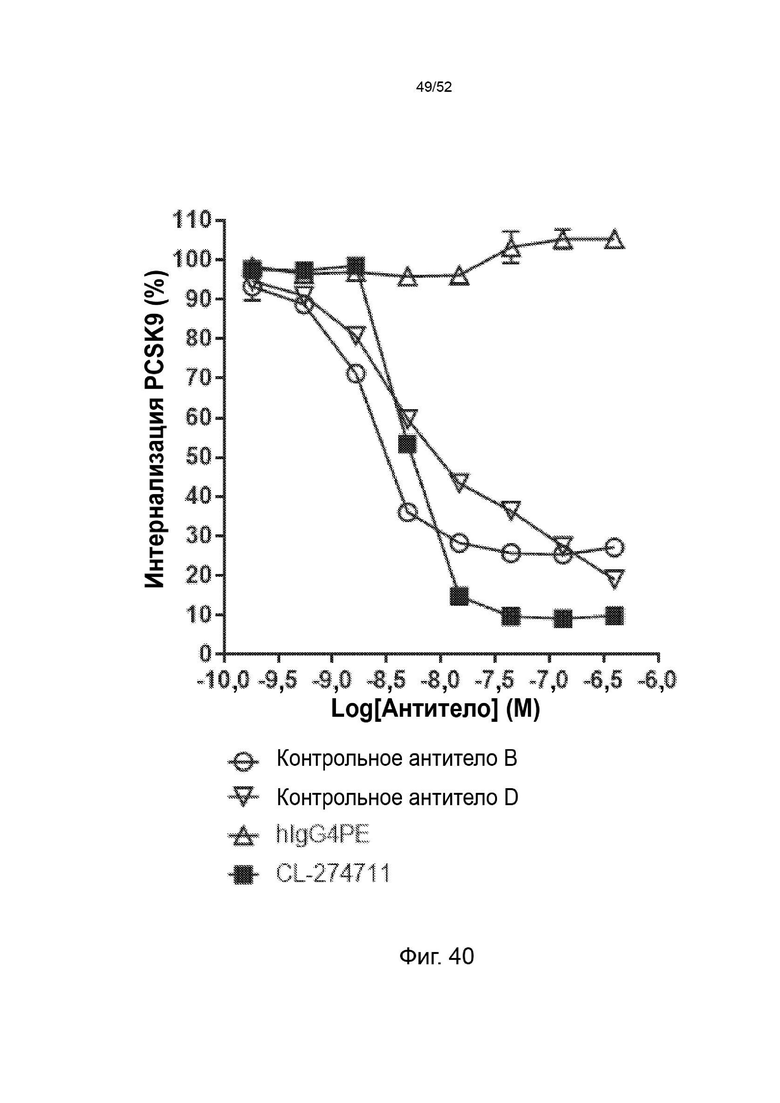
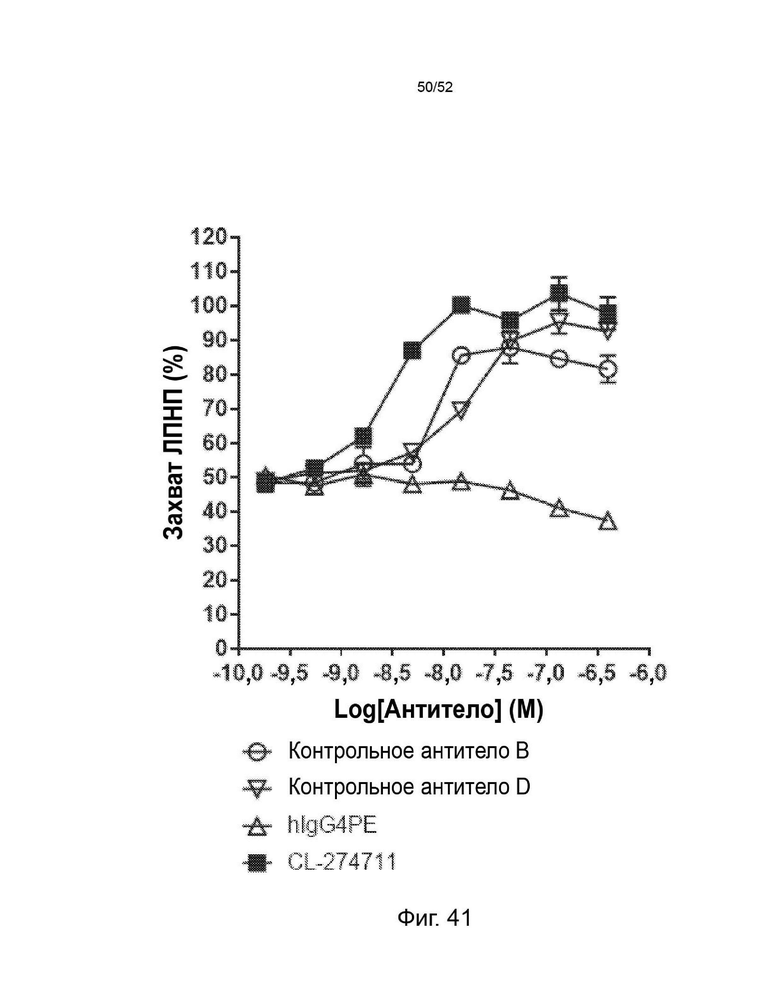
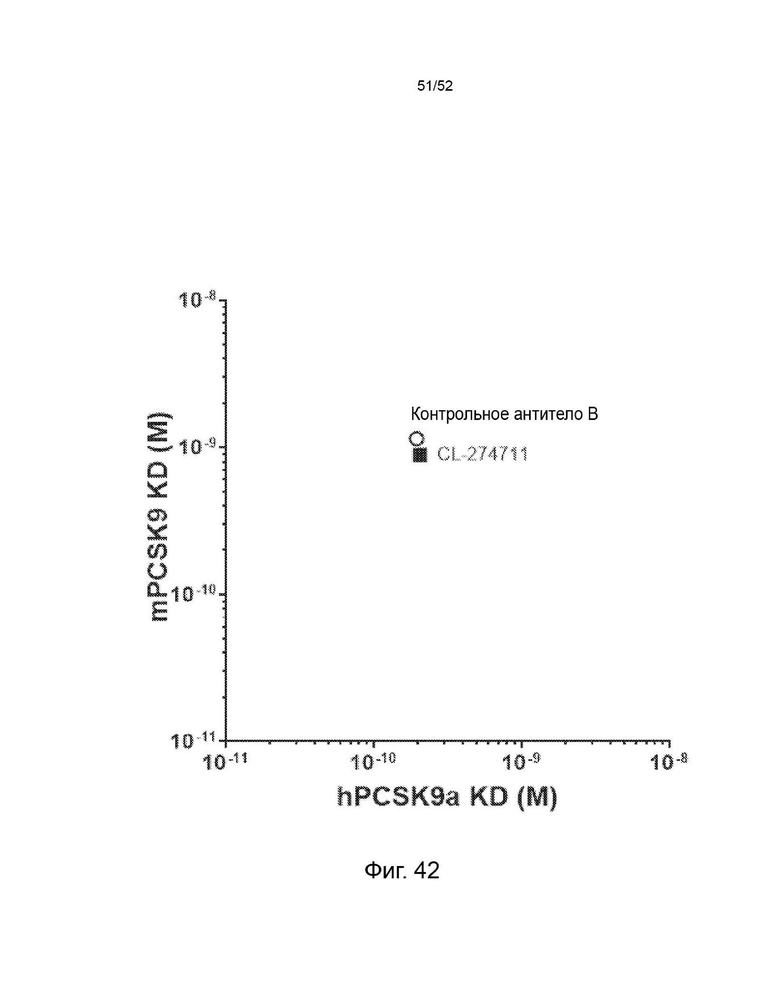
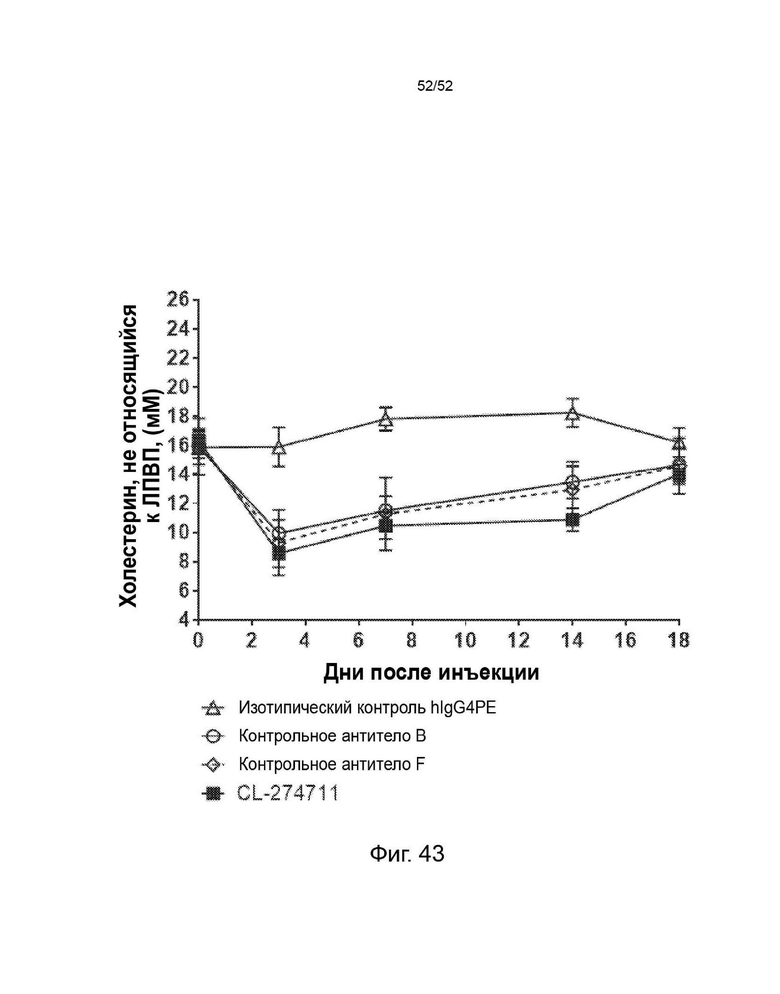
Изобретение относится к области биотехнологии. Предложены антитела и их антигенсвязывающие фрагменты, которые специфически связываются с пропротеиновой конвертазой субтилизин-кексинового типа 9 (PCSK9), кодирующие их нуклеиновые кислоты, экспрессионные векторы и клетки-хозяева. Также предложены фармацевтические композиции, комбинации и наборы, содержащие указанные антитела. Кроме того, изобретение относится к применению антител для лечения или профилактики PCSK9-опосредованного заболевания или патологического состояния. Изобретение обеспечивает улучшенную функцию снижения холестерина, не относящегося к ЛПВП, в плазме крови. 20 н. и 26 з.п. ф-лы, 48 ил., 1 табл., 4 пр.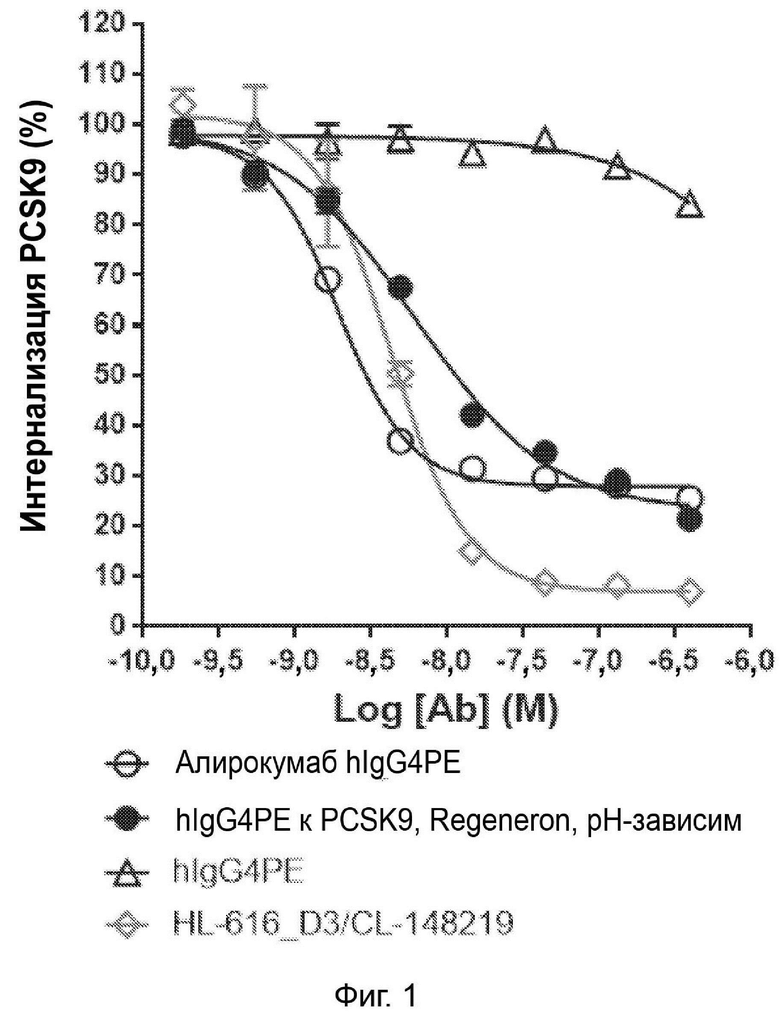
1. Антитело или его антигенсвязывающий фрагмент, которые специфически связываются с пропротеиновой конвертазой субтилизин-кексинового типа 9 (PCSK9), содержащие сайт связывания, который специфически связывается с указанной PCSK9,
где указанное антитело или антигенсвязывающий фрагмент содержит
(i) последовательности SEQ ID NO: 263, 267, 271, 293, 297 и 301 CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3 по IMGT, соответственно; или
последовательности SEQ ID NO: 277, 281, 285, 307, 311 и 315 CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3 по Кабату, соответственно; или
(ii) последовательности SEQ ID NO: 323, 327, 331, 353, 357 и 361 CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3 по IMGT, соответственно; или
последовательности SEQ ID NO: 337, 341, 345, 367, 371 и 375 CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3 по Кабату, соответственно; или
(iii) последовательности SEQ ID NO: 7, 11, 15, 39, 43 и 47 CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3 по IMGT, соответственно; или
последовательности SEQ ID NO: 21, 25, 29, 53, 57 и 61 CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3 по Кабату, соответственно; или
(iv) последовательности SEQ ID NO: 69, 73, 77, 99, 103 и 107 CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3 по IMGT, соответственно; или
последовательности SEQ ID NO: 83, 87, 91, 113, 117 и 121 CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3 по Кабату, соответственно; или
(v) последовательности SEQ ID NO: 203, 207, 211, 233, 237 и 241 CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3 по IMGT, соответственно; или
последовательности SEQ ID NO: 217, 221, 225, 247, 251 и 255 CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3 по Кабату, соответственно.
2. Антитело или его антигенсвязывающий фрагмент по п. 1, отличающиеся тем, что сайт связывания содержит домен VL, содержащий SEQ ID NO: 289, 349, 33, 95 или 229, или аминокислотную последовательность, которая идентична ей по меньшей мере на 70%.
3. Антитело или его антигенсвязывающий фрагмент по любому предыдущему пункту, отличающиеся тем, что сайт связывания содержит домен VH, содержащий SEQ ID NO: 259, 319, 1, 65 или 199, или аминокислотную последовательность, которая идентична ей по меньшей мере на 70%.
4. Антитело или его антигенсвязывающий фрагмент по любому предыдущему пункту, отличающиеся тем, что сайт связывания содержит домен VH, содержащий SEQ ID NO: 259, спаренный с доменом VL, содержащим SEQ ID NO: 289.
5. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-4, отличающиеся тем, что сайт связывания включает домен VH, содержащий SEQ ID NO: 319, спаренный с доменом VL, содержащим SEQ ID NO: 349.
6. Антитело или его антигенсвязывающий фрагмент по любому предыдущему пункту, содержащие первую и вторую копии указанного домена VH.
7. Антитело или его антигенсвязывающий фрагмент по любому предыдущему пункту, которые специфически связываются с PCSK9, содержащей аминокислотную последовательность, выбранную из SEQ ID NO: 189-194.
8. Антитело или его антигенсвязывающий фрагмент по любому предыдущему пункту, отличающиеся тем, что антитело или фрагмент содержат константную область человека.
9. Антитело или его антигенсвязывающий фрагмент по п. 8, отличающиеся тем, что константная область человека представляет собой константную область IgG4 или константную область IgG1.
10. Антитело или его антигенсвязывающий фрагмент по п. 8 или 9, отличающиеся тем, что константная область представляет собой константную область IgG4-PE.
11. Антитело или его антигенсвязывающий фрагмент по п. 8 или 9, отличающиеся тем, что константная область содержит аминокислотную последовательность SEQ ID NO: 3 или 152.
12. Антитело или его антигенсвязывающий фрагмент к PCSK9 как определены в любом предыдущем пункте, для лечения или профилактики PCSK9-опосредованного заболевания или патологического состояния у субъекта.
13. Антитело или его антигенсвязывающий фрагмент к PCSK9 по п. 12, отличающиеся тем, что заболевание или патологическое состояние выбрано из гиперхолестеринемии, гиперлипидемии, дислипидемии, холестатического заболевания печени, нефротического синдрома, гипотиреоза, ожирения, диабета, атеросклероза или сердечно-сосудистого заболевания.
14. Антитело или его антигенсвязывающий фрагмент по п. 12 или 13, отличающиеся тем, что антитело или фрагмент вводят субъекту одновременно или последовательно со статином.
15. Комбинация эффективного количества антитела или его антигенсвязывающего фрагмента к PCSK9 и эффективного количества статина, обладающая ингибирующей активностью в отношении PCSK9, причем указанное антитело или его антигенсвязывающий фрагмент соответствуют любому из пп. 1-11.
16. Комбинация по п. 15, отличающаяся тем, что указанная комбинация включает несколько доз указанного антитела и/или статина.
17. Антитело или его антигенсвязывающий фрагмент как определены в любом из пп. 1-14 или комбинация как определена в любом из пп. 15 или 16 для применения в способе лечения или профилактики гиперхолестеринемии у субъекта, который ранее находился на схеме лечения статинами в первой дозе, причем способ включает снижение дозы статина, вводимой субъекту, или отсутствие введения статина субъекту, при этом способ включает введение субъекту антитела или фрагмента.
18. Комбинация по любому из пп. 15-17, где доза статина, которую вводят субъекту, снижена относительно суточной дозы от 10 до 20 мг (например, 10 мг); или <60 мг (например, 40 мг).
19. Антитело или его антигенсвязывающий фрагмент как определены в любом из пп. 1-14 или комбинация как определена в любом из пп. 15-18 для введения человеку или животному, страдающему повышенным уровнем холестерина, для снижения уровня холестерина липопротеинов низкой плотности (ХС-ЛПНП) в плазме у субъекта после того, как субъект получил антитело или фрагмент к PCSK9.
20. Применение антитела или его антигенсвязывающего фрагмента как определены в любом из пп. 1-14 или комбинации как определена в любом из пп. 15-18 при производстве лекарственного препарата для введения субъекту для лечения или профилактики PCSK9-опосредованного заболевания или патологического состояния.
21. Способ лечения или профилактики PCSK9-опосредованного заболевания или патологического состояния у субъекта, включающий введение указанному субъекту терапевтически эффективного количества антитела или его антигенсвязывающего фрагмента как определены в любом из пп. 1-14 или комбинации как определена в любом из пп. 15-18, при этом тем самым лечится или предотвращается PCSK9-опосредованное заболевание или патологическое состояние.
22. Применение по п. 20 или способ по п. 21, отличающиеся тем, что заболевание или патологическое состояние, опосредованное PCSK9, представляет собой гиперхолестеринемию.
23. Антитело или его антигенсвязывающий фрагмент по любому из пп. 12-14, 17 и 19, комбинация по любому из пп. 15-19, применение по п. 20 или 22 или способ по п. 21 или 22, дополнительно включающие применение к субъекту дополнительной терапии, например, дополнительного терапевтического агента.
24. Антитело или его антигенсвязывающий фрагмент, комбинация, применение или способ по п. 23, отличающиеся тем, что дополнительный терапевтический агент выбран из группы, состоящей из:
a. Статина;
b. Ингибитора ANGPTL3 (например, антитело к ANGPTL3, например, эвинакумаб);
c. Фибрата;
d. Секвестранта желчных кислот;
e. Никотиновой кислоты; и
f. Ниацина.
25. Фармацевтическая композиция, обладающая ингибирующей активностью в отношении PCSK9, содержащая антитело или его антигенсвязывающий фрагмент как определены в любом из пп. 1-14, 17 и 19 или комбинацию как определена в любом из пп. 15-16 и 18, и фармацевтически приемлемое вспомогательное вещество, разбавитель или носитель.
26. Комбинация для лечения и/или профилактики патологического состояния или заболевания, опосредованного PCSK9, содержащая фармацевтическую композицию по п. 25 и дополнительный терапевтический агент, выбранный из группы, состоящей из:
a. Статина;
b. Ингибитора ANGPTL3 (например, антитело к ANGPTL3, например, эвинакумаб);
c. Фибрата;
d. Секвестранта желчных кислот;
e. Никотиновой кислоты; и
f. Ниацина.
27. Фармацевтическая композиция по п. 25 для лечения и/или профилактики патологического состояния или заболевания, опосредованного PCSK9.
28. Фармацевтическая композиция для применения по п. 27 или комбинация для применения по п. 26, отличающаяся тем, что патологическое состояние или заболевание, опосредованное PCSK9, представляет собой гиперхолестеринемию.
29. Набор для лечения и/или профилактики патологического состояния или заболевания, опосредованного PCSK9, содержащий фармацевтическую композицию по п. 25 или комбинацию для применения по п. 26, и этикетку или инструкции по применению для лечения и/или профилактики указанного заболевания или патологического состояния у человека.
30. Набор по п. 29, отличающийся тем, что этикетка или инструкции содержат номер разрешения на продажу.
31. Набор по п. 29, отличающийся тем, что номер разрешения на продажу представляет собой номер разрешения FDA или EMA.
32. Набор по любому из пп. 29-31, дополнительно содержащий в/в или инъекционное устройство, которое содержит антитело или его антигенсвязывающий фрагмент.
33. Нуклеиновая кислота, которая кодирует домен VH антитела или его антигенсвязывающего фрагмента как определены в любом из пп. 1-13.
34. Нуклеиновая кислота, которая кодирует домен VL антитела или его антигенсвязывающего фрагмента как определены в любом из пп. 1-13.
35. Нуклеиновая кислота, которая кодирует домен VH и домен VL антитела или его антигенсвязывающего фрагмента как определены в любом из пп. 1-13.
36. Нуклеиновая кислота, которая кодирует домен VH, содержащий аминокислотную последовательность домена VH, содержащего SEQ ID NO: 259, 319, 1, 65 или 199.
37. Нуклеиновая кислота, которая кодирует домен VL, содержащий аминокислотную последовательность домена VL, содержащего SEQ ID NO: 289, 349, 33, 95 или 229.
38. Нуклеиновая кислота, которая кодирует вариабельный домен тяжелой цепи антитела, содержащая нуклеотидную последовательность SEQ ID NO: 260 или 320.
39. Нуклеиновая кислота, кодирующая тяжелую цепь антитела или его антигенсвязывающего фрагмента как определены в любом из пп. 1-13.
40. Нуклеиновая кислота, кодирующая легкую цепь антитела или его антигенсвязывающего фрагмента как определены в любом из пп. 1-13.
41. Нуклеиновая кислота, кодирующая тяжелую цепь и легкую цепь антитела или его антигенсвязывающего фрагмента как определены в любом из пп. 1-13.
42. Нуклеиновая кислота, кодирующая тяжелую цепь, содержащую аминокислотную последовательность VH SEQ ID NO: 259 или 319; и аминокислотную последовательность C-области SEQ ID NO: 3 или 152.
43. Нуклеиновая кислота, кодирующая легкую цепь, содержащую аминокислотную последовательность VL SEQ ID NO: 289 или 349; и аминокислотную последовательность C-области SEQ ID NO: 156.
44. Экспрессионный вектор, содержащий нуклеиновую кислоту(-ы) по любому из пп. 33-43.
45. Экспрессионный вектор по п. 44, отличающийся тем, что вектор представляет собой вектор CHO или HEK293.
46. Клетка-хозяин для продуцирования антитела или его антигенсвязывающего фрагмента по любому из пп. 1-13, содержащая нуклеиновую кислоту(-ы) по п. 35 или 41 или нуклеиновую кислоту(-ы) по пп. 34 и 36 или нуклеиновую кислоту(-ы) по пп. 39 и 40 или нуклеиновую кислоту(-ы) по пп. 42 и 43; или вектор, содержащий нуклеиновую кислоту(-ы) по п. 35 или 41, вектор, содержащий нуклеиновую кислоту(-ы) по пп. 36 и 37, или вектор, содержащий нуклеиновую кислоту(-ы) по пп. 39 и 40, или вектор, содержащий нуклеиновую кислоту(-ы) по пп. 42 и 43.
| US 9017678 B1, 28.04.2015 | |||
| TSUYOSHI NOZUE, Lipid Lowering Therapy and Circulating PCSK9 Concentration, JOURNAL OF ATHEROSCLEROSIS AND THROMBOSIS, 2017, v | |||
| Пишущая машина для тюркско-арабского шрифта | 1922 |
|
SU24A1 |
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Способ многократной радиопередачи | 1922 |
|
SU895A1 |
| ВЫСОКОАФФИННЫЕ ЧЕЛОВЕЧЕСКИЕ АНТИТЕЛА К PCSK9 | 2009 |
|
RU2552169C2 |
| МАКАЕВ А.А., Фармакотерапия гиперлипидемии и атеросклероза с использованием моноклональных антител - ингибиторов PCSK9, Бюл | |||
| медицинских | |||
Авторы
Даты
2025-05-05—Публикация
2019-12-18—Подача