Предлагаемое изобретение относится к областям медицины и органической химии, а именно к способу получения и использованию в качестве лечебного кардиопротекторного средства динитрата изобутендиола.
2-Метилен-1,3-динитроксипропан (динитрат изобутендиола) описан в 1972 г. в работе [А.М. Королев, Л.Т. Еременко. Изв. АН СССР, Сер. хим., 1972, 663]. Авторы синтезировали это вещество с целью дополнить известный ранее ряд изомерных нитратов непредельных гликолей и сопоставить его физические свойства со свойствами известных изомеров. Сведения о возможных полезных свойствах вещества не приводятся.
Между тем, позднее нами была обнаружена по первичным тестам высокая кардиологическая активность 2-метилен-1,3-динитроксипропана, подтвержденная в последние годы в результате проведения углубленных исследований.
Описанный [А.М. Королев, Л.Т. Еременко. Изв. АН СССР, Сер. хим., 1972, 663] способ получения 2-метилен-1,3-динитроксипропана заключается в нитровании изобутендиола смесью азотной кислоты с уксусным ангидридом (Фиг.1).
Реакция нитрования в выбранных условиях протекает в течение короткого отрезка времени и дает высокий выход продукта (87%). Существенным недостатком этого способа является использование изобутендиола - труднодоступного соединения. Известно несколько способов получения изобутендиола [R. Lukes, J. Plesek, Chem. Listy, 1955, 49, 1826; A. Mooradian, J.B. Kloke. J.Am.Chem.Soc., 1945, 67, 942.; M.J. Konz. Пат. США №4059594, заявл. 16.01.75. РЖХим. 1978, 160339П.; H.-S. Byun, K.C. Redly, R. Bittman. Tetrahedron Lett., 1994, vol.35, 1371.; J. Grolig, G. Scharfe, W. Swodenk. Пат. ФРГ №1939142, заявл. 04.02.71. C.A. 1971, 74, 87373y.; C. Granow, W. Fogt, H. Glasser. Пат. ФРГ №2054987, заявл. 10.05.72. C.A. 1972, 77, 47880s.], из которых следует привести лишь два [R. Lukes, J. Plesek, Chem. Listy, 1955, 49, 1826; A. Mooradian, J.B. Kloke. J.Am. Chem. Soc., 1945, 67, 942]. Остальные способы не могут рассматриваться как сколько-нибудь пригодные для практического использования.
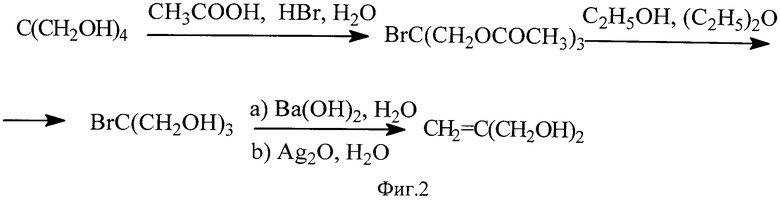
Авторами [А.М. Королев, Л.Т. Еременко. Изв. АН СССР, Сер. хим., 1972, 663] был использован трехстадийный способ получения изобутендиола [R. Lukes, J. Plesek, Chem. Listy, 1955, 49, 1826] (Фиг.2).
Хотя способ основан на применении доступного сырья - пентаэритрита, он страдает серьезными недостатками.
На первой стадии пентаэритрит превращается в триацетат бромгидрина пентаэритрита продолжительным кипячением (30 часов) в смеси уксусной кислоты с 66%-ной бромистоводородной кислотой (т.кип. - 120°C). На 2-й стадии триацетат омыляется кипящим этанолом, обрабатывается кипящим эфиром, а образовавшийся бромгидрин пентаэритрита расщепляется на третьей стадии до изобутендиола действием кипящего водного раствора гидроокиси бария (10 часов) или окиси серебра (4 часа). Суммарный выход изобутендиола (из расчета на исходный пентаэритрит) составляет 25-27%. При этом на всех стадиях выполняются дополнительные операции с использованием разного рода реактивов. Т.о. способ характеризуется повышенными трудоемкостью, энергоемкостью и пожароопасностью.
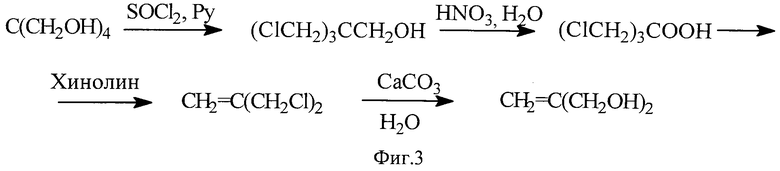
Другой, не менее трудоемкий, четырехстадийный способ получения изобутендиола [A. Mooradian, J.В. Kloke. J.Am. Chem. Soc., 1945, 67, 942], также из пентаэритрита, представлен Фиг.3.
На первой стадии получают трихлоргидрин пентаэритрита нагреванием с хлористым тионилом в присутствии пиридина (120°C, 7 часов). Полученный продукт фракционируют при пониженном давлении, отбирая фракцию с т.кип. 127,5-129°C/12 мм рт.ст. Выход трихлоргидрина 53-59%. На второй стадии трихлоргидрин окисляют нагреванием с 68-70%-ной азотной кислотой (50-90°C, несколько часов) до трис(хлорметил)уксусной кислоты (практически с количественным выходом), которую на третьей стадии разлагают нагреванием с хинолином (110°C, 1 час) до 3-хлор-2-хлорметил-1-пропена, а последний гидролизуют на четвертой стадии кипячением в течение трех суток в водном растворе карбоната кальция и получают изобутендиол. Таким образом, в итоге этот способ получения изобутендиола страдает теми же, в принципе, недостатками, что и предыдущий. Суммарный выход изобутендиола из расчета на исходный пентаэритрит составляет 14-18%.
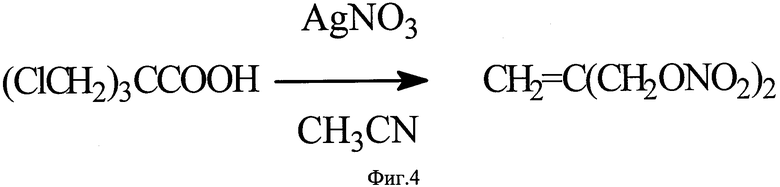
Задачей технического решения является разработка способа получения 2-метилен-1,3-динитроксипропана из доступного соединения. Таким соединением в предлагаемом способе выбрана вышеупомянутая трис(хлорметил)уксусная кислота [А. Mooradian, J.B. Kloke. J.Am. Chem. Soc.,1945, 67, 942], получаемая за две стадии из того же пентаэритрита, причем проведение этих стадий лишено тех недостатков, которые присущи трехстадийному способу получения изобутендиола. Использование трис(хлорметил)уксусной кислоты стало возможным благодаря открытой нами неизвестной ранее реакции превращения этой кислоты в 2-метилен-1,3-динитроксипропана под действием нитрата серебра в среде ацетонитрила (Фиг.4).
Превращение протекает в сравнительно мягких условиях (65-70°C, 10 часов) с удовлетворительным выходом (51-53%). Суммарный выход 2-метилен-1,3-динитроксипропана из расчета на пентаэритрит составляет 27-31%. Осуществление предложенного способа иллюстрируется примером.
Получение 2-метилен-1,3-динитроксипропана из трис(хлорметил)уксусной кислоты.
В трехгорлой колбе, снабженной механической мешалкой, термометром и капельной воронкой, готовят раствор 10,28 г (0,05 моля) трис(хлорметил)уксусной кислоты и 38,25 г (0.225 моля) нитрата серебра в 100 мл обезвоженного ацетонитрила и перемешивают его 10 часов при нагревании до 60-70°С. После охлаждения реакционной массы до комнатной температуры отфильтровывают осадок хлористого серебра, промывают его ацетонитрилом и получают 20 г (0,14 моля). Фильтрат с промывным ацетонитрилом упаривают в вакууме водоструйного насоса, к остатку добавляют 150 мл хлористого метилена, перемешивают, отфильтровывают осадок, получают 14 г (0,08 моля) непрореагировавшего нитрата серебра. Т.о. в виде нитрата и хлорида возвращают около 98% серебра. Хлористометиленовый фильтрат промывают водой и высушивают над сернокислым магнием. Растворитель удаляют в вакууме водоструйного насоса, а оставшийся продукт перегоняют на масляном насосе. Выход 4,65 г (52%), т.кип. 62-64°C/1 мм рт.ст., nD 20l,4638 (лит. [А.М. Королев, Л.Т. Еременко. Изв. АН СССР, Сер. хим., 1972, 663] данные: т.кип. 54-55°C/0,5 мм рт.ст., nD 201,4636).
Кардиологическая активность 2-метилен-1,3-динитроксипропана
Кардиологическая активность 2-метилен-1,3-динитроксипропана изучалась нами в сравнении с известным эффективным антиангинальным препаратом -N-(2-нитроксиэтил)никотинамидом (никорандилом) [Преображенский Д.В., Юркина М.Ю., Якутик В.В. Кардиология. 1994. N8. С.81-84; О.И. Писаренко, Л.И.Серебрякова, О.В. Цкитишвили, Д.А. Нестеренко. Л.Т. Еременко, В.П. Косилко, В.А. Гаранин. Кардиология. 2008. N5. С.36-40; Л.Ю. Бадриддинов, Н.В. Юргель, Л.И. Павлова, В.Г. Кукес. Фарматека. 2009. №8. С65-68].
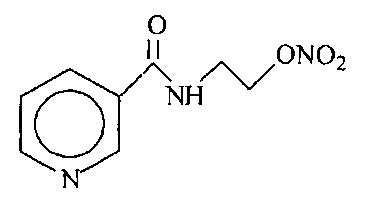
Действие никорандила реализуется за счет двух основных компонентов: 1) открытия K+-АТФ-чувствительных каналов с индуцированной гиперполяризацией клеточной мембраны; 2) нитратоподобного эффекта препарата и связанного с увеличения внутриклеточного содержания цГМФ.
2-метилен-1,3-динитроксипропан представляет собой новое противоишемическое средство для терапии ишемических повреждений миокарда, в механизме действия которого важную роль играет коронародилятация в результате активации K+-АТФ-каналов и блокады медленных Ca2+-каналов. При этом 2-метилен-1,3-динитроксипропан заметно или существенно превосходит никорандил по ряду эффектов.
1. Влияние исследуемых соединений на K+-АТФ-чувствительные каналы и медленные кальциевые каналы (МКК).
Определение характера влияния изучаемых веществ на K+-АТФ-каналы проводилось по результатам аналитических экспериментов на изолированных препаратах аорты крыс с регистрацией релаксации аорты после контрактуры норадреналином [Katsuo K., Noriyuki М., Yutaka K. Eur. Journal of Pharm. 1989. Vol.166. P.319-323].
Изучение влияние исследуемых нитросоединений на активность медленных кальциевых каналов осуществляли путем регистрации контрактуры изолированной аорты крыс, инкубируемой в безкальциевой среде, при добавлении в термостатируемую аэрируемую карбогеном кювету тестируемого раствора, содержащего хлорид кальция.
Результаты тестирования заявляемого соединения (ДНИ) и никорандила (НИК) приведены в табл.1 и 2.
C50 НИК
В результате оценки релаксирующей активности веществ на аорту после контрактуры норадреналином было выявлено, что 2-метилен-1,3-динитроксипропан обладает выраженным активирующим действием на K+-АТФ-чувствительные каналы, по эффективности в 14 раз превышающей никорандил.
Активность 2-метилен-1,3-динитроксипропана превышает таковую никорандила в отношении МКК в 3 раза.
2. Активность веществ на модели ишемии миокарда у крыс.
Полезный эффект активаторов K+-АТФ-чувствительных каналов при стенокардии зависит от их способности улучшать кровоснабжение в ишемизированной области сердечной мышцы. Определение способности ограничения размеров зоны некроза и ишемии у крыс определяли через 4 часа после окклюзии коронарной артерии при помощи дифференциального индикаторного метода [Сернов Л.Н., Гацура В.В. Бюлл. эксперим. биол. и мед. 1989. N5. С.534-535].
Согласно приведенным результатам 2-метилен-1,3-динитроксипропан в дозе 0,38 мг/кг уменьшает отношение зоны некроза к общей массе миокарда крысы статистически значимо (p<0,05) с 22,2±2,0 до 8,0±2,0%. Отношение зоны некроза к зоне ишемии 2-метилен-1,3-динитррксипропан уменьшает до 30,5±7,3% (p<0,05), по сравнению с контрольными данными - 68,0±4,3%.
2-Метилен-1,3-динитроксипропан в дозе 0,38 мг/кг по противоишемическому эффекту практически эквивалентен препарату сравнения никорандилу, но взятому в 6 раз большей дозе - 2,38 мг/кг. Дальнейшее повышение вводимой дозировки 2-метилен-1,3-динитроксипропана приводит к усилению антиишемической активности, что свидетельствует о прямом дозозависимом эффекте.
3. Антиаритмическая активность веществ.
Для регистрации сердечной деятельности, появления аритмий и вариабельности сердечного ритма пользовались электрокардиографическим программным комплексом «КАД-03» производства фирмы «ДНК и K0» (г.Тверь).
2-метилен-1,3-динитроксипропан в дозе 18,75 мг/кг не купирует появление фибрилляции сердца крысы. Фибрилляция возникает на 32±5 секунде эксперимента на фоне введенного вещества, что сопоставимо с контролем (20,3±0,6 с) и результатами с никорандилом (29±1,6 с), взятым в дозе 23,75 мг/кг (p<0,05). Летальность среди животных в экспериментах с 2-метилен-1,3-динитроксипропаном ниже и составляет 50% против 66,7% в группе никорандила. Повышение дозы 2-метилен-1,3-динитроксипропана до 37,5 мг/кг не приводит к изменению времени до появления фибрилляции сердца крысы, а летальность увеличивалась до 66,7%.
В дозе 18,75 мг/кг 2-метилен-1,3-динитроксипропан не купирует возникновение блокады AB-узла сердца крысы и экстрасистолии при введении адреналина гидрохлорида. Аритмии возникают практически сразу же после введения адреналина (через 69±20 с).
Так же как и никорандил в дозе 5% от ЛД50 2-метилен-1,3-динитроксипропан не проявляет антиаритмической активности и в экспериментах со строфантином. В дозе 18,75 мг/кг 2-метилен-1,3-динитроксипропан не изменяет время до появления аритмий, а также не влияет на сердечный ритм. В дозе 18,75 и 37,5 мг/кг не купирует появление аконитиновых аритмий, однако на фоне его действия не отмечалось появления трепетаний желудочков и появления аритмии по типу пируэта в отличие от никорандила.
Таким образом, 2-метилен-1,3-динитроксипропан не проявляет антиаритмических свойств, однако благоприятно влияет на течение и последствия фатальных аритмий.
4. Коронародилятаторные свойства соединений.
A. Влияние 2-метилен-1,3-динитроксипропана и никорандила на скорость оттока перфузата из изолированного по Лангендорфу сердца крыс.
1. Для определения коронародилятаторной активности изучаемых соединений использована стандартная методика изолированного перфузируемого сердца по Лангендорфу-Фаллену [Fallen Е.Т., Elliott W.G., Gorlin R.J. appl. physiol. 1967. Vol.22. №4. P.836-839].
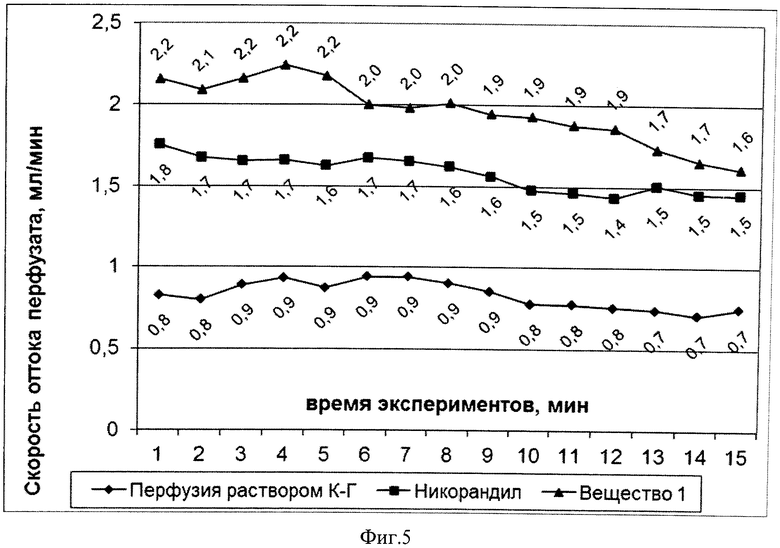
На фиг.5 представлена скорость оттока перфузата от изолированного сердца в первый 15-минутный период при действии 2-метилен-1,3-динитроксипропана (вещество 1) и никорандила. (Примечание: * P<0,01 по сравнению с контролем.)
2-Метилен-1,3-динитроксипропан имеет выраженное коронародилатирующее действие.
Препарат сравнения никорандил также увеличивает отток перфузата, однако менее выраженно, и не влияет на «выживаемость» изолированных гипоксических сердец крыс.
Б. Влияние исследуемых соединений на функциональные показатели изолированного гипоксического перфузируемого по Лангендорфу сердца крыс.
Согласно приведенным данным, 2-метилен-1,3-динитроксипропан имеет выраженное коронародилатирующее действие на сосуды перфузируемого гипоксического сердца крысы и достаточно длительное время поддерживает его сократительную функцию, причем эти эффекты проявляются сильнее, чем у никорандила.
Острая токсичность 2-метилен-1,3-динитроксипропана и никорандила.
Острую токсичность исследуемых соединений определяли на белых мышах массой 18-20 гр при внутрибрюшинном введении. Каждую дозу испытуемых веществ вводили группе из 4 животных в растворе, объем которого не превышал 0,5 мл. LD50 определяли табличным методом Личфилда-Уилкоксона (1980). Вещества растворяли в 0,9% растворе натрия хлорида и вводили животным однократно. Наблюдение за внешним видом, поведенческими реакциями и выживаемостью животных проводили в течение одной недели.
Как видно из данных табл.5, 2-метилен-1,3-динитроксипропан несколько токсичнее никорандила, что ни в какой степени не умаляет его достоинств. Согласно ГОСТ-у 12.1.007-76 оба соединения относятся к классу токсичности «3» - умеренно токсичные.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ 2-МЕТИЛЕН-1,3-ДИНИТРОКСИПРОПАНА В КАЧЕСТВЕ ПРОТИВОИШЕМИЧЕСКОГО СРЕДСТВА | 2015 |
|
RU2580929C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОИШЕМИЧЕСКОЙ АКТИВНОСТЬЮ В ЭКСПЕРИМЕНТАЛЬНОЙ КАРДИОЛОГИИ | 1988 |
|
RU2007985C1 |
| ПЕПТИДНОЕ СОЕДИНЕНИЕ, ВОССТАНАВЛИВАЮЩЕЕ ФУНКЦИЮ МИОКАРДА | 2004 |
|
RU2255756C1 |
| СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ИШЕМИИ МИОКАРДА ПРИ КОРОНАРОИНВАЗИВНЫХ ВМЕШАТЕЛЬСТВАХ | 1999 |
|
RU2146933C1 |
| КАРДИОПЛЕГИЧЕСКИЙ РАСТВОР "ИНФУЗОЛ" | 2002 |
|
RU2226093C1 |
| Способ определения реперфузионного повреждения миокарда после ишемии | 1988 |
|
SU1570707A1 |
| ПРОИЗВОДНЫЕ 2-МЕРКАПТОБЕНЗИМИДАЗОЛА, ОБЛАДАЮЩИЕ ПРОТИВОИШЕМИЧЕСКОЙ, АНТИАРИТМИЧЕСКОЙ И ПРОТИВОФИБРИЛЛЯТОРНОЙ АКТИВНОСТЬЮ | 1995 |
|
RU2136667C1 |
| СРЕДСТВО ДЛЯ ПРЕДУПРЕЖДЕНИЯ ПОСЛЕДСТВИЙ И ОСЛОЖНЕНИЙ ИНДУЦИРОВАННОЙ ИШЕМИИ СЕРДЦА | 1993 |
|
RU2083219C1 |
| ПРОИЗВОДНЫЕ 5-БРОМНИКОТИНОВОЙ КИСЛОТЫ, ОБЛАДАЮЩИЕ АНТИАРИТМИЧЕСКОЙ АКТИВНОСТЬЮ | 2015 |
|
RU2617428C2 |
| СПОСОБ ПРЕЗЕРВИРОВАНИЯ МИОКАРДА ПРИ ТРАНСПЛАНТАЦИИ | 2013 |
|
RU2535036C1 |
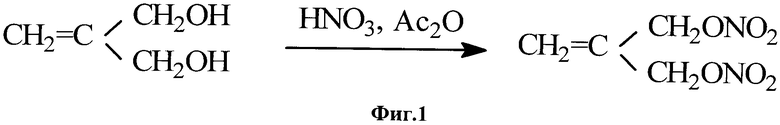
Изобретение относится к способу получения 2-метилен-1,3-динитроксипропана. Способ включает действие нитрата серебра на трис(хлорметил)уксусную кислоту в среде ацетонитрила. При этом реакцию проводят при нагревании до 60-70°С. Способ позволяет получать продукт с удовлетворительным выходом из доступного соединения в мягких условиях, а также сократить количество стадий. 5 ил., 5 табл.
Способ получения 2-метилен-1,3-динитроксипропана, заключающийся в действии нитрата серебра на трис(хлорметил)уксусную кислоту в среде ацетонитрила, отличающийся тем, что реакцию проводят при нагревании до 60-70°C.
| A.M | |||
| KOROLEV ET AL., Synthesis of isobutenediol dinitrate and some of its derivatives, Izvestiya Akademii Nauk SSSR, Seriya Khimicheskaya, 1972, 3, p | |||
| Рельсовое скрепление | 1923 |
|
SU663A1 |
| L.T | |||
| EREMENKO ET AL., | |||
Авторы
Даты
2015-06-10—Публикация
2013-09-05—Подача