Область изобретения
Настоящее изобретение относится к области биотехнологии, в частности, к белку, связанному с длиной зерен, весом зерен, количеством зерен в метелке и скрученностью листьев в культуре риса, генам, кодирующим указанный белок, и их применению.
Описание уровня техники
Рис является одной из основных зерновых культур, от которых зависит жизнь человека, и представляет собой основной продукт питания для почти половины населения земного шара. В Китае рис занимает первое место среди всех зерновых культур по объему производства и составляет 60% от потребляемого жителями Китая зерна; почти половина фермеров занимается производством риса. Соответственно, рис играет ведущую роль среди китайских продовольственных культур. На фоне роста мирового населения (темпы роста населения в потребляющих рис странах выше, чем средние темпы роста населения в мире) и бурного развития индустриализации и урбанизации, а также ущерба, причиняемого стихийными бедствиями и т.п., наблюдается тенденция к снижению площадей рисовых полей, порождающая растущее несоответствие между мировым предложением риса и спросом на него. Как производить больше продовольствия на меньших площадях рисовых полей, чтобы обеспечить достаточные поставки риса? Эта насущная проблема, с которой мы столкнулись и которую необходимо решить. Однако урожайность риса при больших масштабах производства, как правило, очень невелика. По данным исследования, проведенного Продовольственной и сельскохозяйственной организацией Объединенных Наций (ФАО) в 1999 году, среднемировой выход риса на единицу площади составляет всего 3,8 т/га (6,3 т/га в Китае). Поэтому в Китае в течение последних 30 лет был разработан проект селекции риса для получения сверхвысокой урожайности (проект селекции суперриса), направленный на развитие потенциала высокоурожайных сортов и, тем самым, существенное повышение урожайности риса. Вес зерна и количество зерен в метелке являются важными факторами, влияющими на объемы урожая, и увеличение размеров зерна, веса зерна или количества зерен в метелке является эффективным подходом к увеличению урожайности риса. Кроме того, длина зерна является важной морфологической характеристикой, определяющей качество риса. Для биологов и агрономов повышение как урожайности, так и качества риса представляет собой достойную цель.
Описание изобретения
Задача настоящего изобретения состоит в обеспечении белка риса, обозначаемого как OsXCL, представляющего собой один из белков 1) или 2):
1) белок, состоящий из аминокислотной последовательности, представленной в SEQ ID NO.2 в Перечне последовательностей;
2) белок, полученный из белка 1) путем введения в аминокислотную последовательность, представленную в SEQ ID NO.2 Перечня последовательностей путем замены, и/или делеции, и/или присоединения одной или нескольких аминокислот, который связан с длиной зерен, весом зерен, количеством зерен в метелке и формой листьев растения.
SEQ ID NO.2 представляет собой аминокислотную последовательность OsXCL, содержащую 255 аминокислот, в которой присутствует 72 гиброфобные аминокислоты (включая пролин), 183 гидрофильные аминокислоты, 34 кислых аминокислоты и 38 основных аминокислот. Белок имеет молекулярную массу 26.73 кДа и изоэлектрическую точку 9.8. Это новый белок, который ранее не был описан.
Маркеры, перечисленные в таблице 1, могут быть связаны с аминоконцевым или карбоксиконцевым участками белка, состоящего из аминокислотной последовательности, представленной в SEQ ID NO.2 в Перечне последовательностей для удобства выделения OsXCL согласно 1).
Белок OsXCL согласно вышеприведенному определению 2) может быть искусственно синтезирован или может быть получен путем синтеза гена, кодирующего указанный белок и его последующей биологической экспрессии. Ген, кодирующий белок OsXCL согласно вышеприведенному определению 2), может быть получен модификацией ДНК-последовательности, определенной основаниями в положениях 106-870, начиная от 5' конца последовательности SEQ ID NO.1 из Перечня последовательностей делецией кодонов одного или более аминокислотных остатков, и/или подвергая одну или более пар оснований миссенс-мутации, и/или присоединением маркерной кодирующей последовательности, выбранной из приведенных в таблице 1, по 5' концу и/или по 3' концу.
Кодирующий ген вышеописанного белка, обозначаемого как OsXCL, также входит в объем правовой охраны настоящего изобретения.
Вышеописанный кодирующий ген представляет собой 1) или 2) или 3) или 4):
1) ген, имеющий кодирующую последовательность, соответствующую положениям 106-870, начиная от 5' конца последовательности SEQ ID NO.1, представленной в
Перечне последовательностей;
2) ген, имеющий кодирующую последовательность, соответствующую положениям 50-873, начиная от 5' конца последовательности SEQ ID NO.1, представленной в Перечне последовательностей;
3) ген, гибридизованный с геном, определенным в 1) или 2) в жестких условиях и кодирующий указанный белок;
4) ген, на 80% или более чем на 80% гомологичный гену, определенному в 1) или 2), и кодирующий указанный белок.
SEQ ID NO.1 представляет собой OsXCL-кодирующую полноразмерную кДНК, состоящую из 1062 оснований, где 5' нетранслируемый участок включает 105 оснований, 3' нетранслируемый участок включает 192 основания и кодирующий участок включает 765 оснований (от положения 106 до положения 870), кодирующих белок OsXCL, имеющий аминокислотную последовательность, представленную в SEQ ID NO.2 в Перечне последовательностей. В кодирующем участке доля А составляет 15.16% (116), С составляет 40.65% (311), G составляет 32.29% (247), Т составляет 11.9% (91), А+Т составляют 27.06% (207) и C+G составляют 72.94% (558).
Вышеупомянутые жесткие условия заключаются в следующем: гибридную пленку помещают в прегибридизационный раствор (раствор натрий-фосфатного буфера 0.25 моль/л, рН 7.2, 7% SDS (додецилсульфат натрия)) для прегибридизации при 65°С в течение 30 мин; прегибридизационный раствор удаляют и добавляют гибридизационный раствор (раствор натрий-фосфатного буфера 0.25 моль/л, рН 7.2, 7% SDS, меченый изотопом нуклеотидный фрагмент) для гибридизации при 65°С в течение 12 часов; гибридизационный раствор удаляют и добавляют раствор I для промывки мембран (раствор натрий-фосфатного буфера 20 ммоль/л, рН 7.2, 5% SDS), мембрану дважды промывают при 65°С, каждый раз в течение 30 мин; добавляют раствор II для промывки мембран (раствор натрий-фосфатного буфера 20 ммоль/л, рН 7.2, 1% SDS), мембрану промывают при 65°С в течение 30 мин.
Пары праймеров, используемые для амплификации полноразмерной последовательности вышеописанного гена OsXCL или любого его фрагмента, также входят в объем правовой охраны настоящего изобретения.
Трансгенная клеточная линия, содержащая вышеописанный ген, также находится в рамках настоящего изобретения.
Рекомбинантная линия, содержащая вышеописанный ген, также находится в рамках настоящего изобретения.
Рекомбинантный вектор, содержащий вышеописанный ген, также находится в рамках настоящего изобретения.
Рекомбинантный вектор экспрессии, содержащий ген OsXCL, может быть сконструирован на основе существующих растительных векторов экспрессии. Растительные векторы экспрессии включают бинарные векторы из Agrobacterium и векторы, пригодные для баллистической трансфекции растений и подобные им, такие как рСАМВ1А3301, рСАМВ1А1300, pBI-121, pBin19, pCAMBIA2301, pCAMBIA1301-UbiN, pBY505 или другие производные формы растительных векторов экспрессии. При конструировании рекомбинантного вектора экспрессии с геном OsXCL перед инициацией транскрипции нуклеотидов указанного гена могут быть добавлены любые элементы, выбранные из усилителя, конститутивного промотора, тканеспецифичного промотора или индуцируемого промотора, которые могут использоваться отдельно или в комбинации с другими растительными промоторами, такими как промотор вируса мозаики цветной капусты (CaMV) 35S, промоторы гена убиквитина (pUbi), промоторы гена актина и подобные им.
Кроме того, при конструировании растительного вектора экспрессии с геном согласно настоящему изобретению может быть использован усилитель, в том числе усилитель трансляции или также усилитель транскрипции. Указанные усиливающие участки могут представлять собой стартовые ATG кодоны или стартовые кодоны смежных областей и подобные им, обязательно идентичные рамке считывания кодирующей последовательности для обеспечения корректной трансляции всей последовательности. Существует множество источников регуляторов трансляции и стартовых кодонов как натуральных, так и синтезированных. Участки инициации трансляции могут принадлежать области инициации транскрипции или структурному гену.
Используемый растительный вектор экспрессии может быть преобразован, например, введением гена, экспрессирующегося в растении с образованием влияющего на цвет фермента или светящегося соединения (GUS ген, GFP ген, ген люциферазы и т.п.), маркеров устойчивости к антибиотикам (маркеров устойчивости к гентамицину, канамицину и т.п.) или маркерных генов устойчивости к химикатам (например, гена устойчивости к гербицидам) и подобных им, для удобства идентификации и скрининга трансгенных растительных клеток или трансгенного растения.
В частности, вышеописанный рекомбинантный вектор может представлять собой рекомбинантный вектор, полученный введением вышеописанного гена в сайт множественного клонирования в векторе экспрессии 163-1300;
причем вектор экспрессии 163-1300 был сконструирован лигированием отрезка ДНК с двойным промотором 35S, полученного ферментативным расщеплением pJIT163 посредством KpnI и XhoI и большого фрагмента, полученного ферментативным расщеплением рСАМВ1А1300 посредством KpnI и SalI, для получения рекомбинантного вектора экспрессии.
Еще одной целью настоящего изобретения является обеспечение способа селекции трансгенного растения с увеличенным весом зерен. Способ селекции трансгенного растения с увеличенным весом зерен, предложенный в настоящем изобретении, представляет собой введение вышеописанного гена в целевое растение с получением генетически модифицированного растения с большим весом зерен, чем у целевого растения.
Еще одной целью настоящего изобретения является обеспечение способа селекции трансгенного растения с увеличенной длиной зерен. Способ селекции трансгенного растения с увеличенной длиной зерен, предложенный в настоящем изобретении, представляет собой введение вышеописанного гена в целевое растение с получением генетически модифицированного растения с большей, чем у целевого растения, длиной зерен.
Еще одной целью настоящего изобретения является обеспечение способа селекции трансгенного растения с увеличенным количеством зерен в метелке. Способ селекции трансгенного растения с увеличенным количеством зерен в метелке, предложенный в настоящем изобретении, представляет собой введение вышеописанного гена в целевое растение с получением генетически модифицированного растения с большим количеством зерен в метелке, чем у целевого растения.
Еще одной целью настоящего изобретения является обеспечение способа селекции трансгенного растения со скрученными листьями. Способ селекции трансгенного растения со скрученными листьями, предложенный в настоящем изобретении, представляет собой введение вышеописанного гена в целевое растение с получением генетически модифицированного растения со скрученными листьями.
Вышеописанный ген вводится в целевое растение посредством вышеописанного рекомбинантного вектора. Растительные клетки или ткани могут быть трансформированы при помощи растительного вектора экспрессии, несущего ген OsXCL, предложенный в настоящем изобретении, посредством Ti-плазмиды, Ri-плазмиды, растительного вирусного вектора, стандартных биологических методик, таких как использование генной пушки, введение через пыльцевую трубку, микроинъекции, электротрансформация, введение с использованием Agrobactehum и так далее.
Вышеописанное растение может представлять собой двудольное растение или однодольное растение; однодольное растение предпочтительно представляет собой рис, а двудольное растение может представлять собой Arabidopsis thaliana.
Краткое описание чертежей
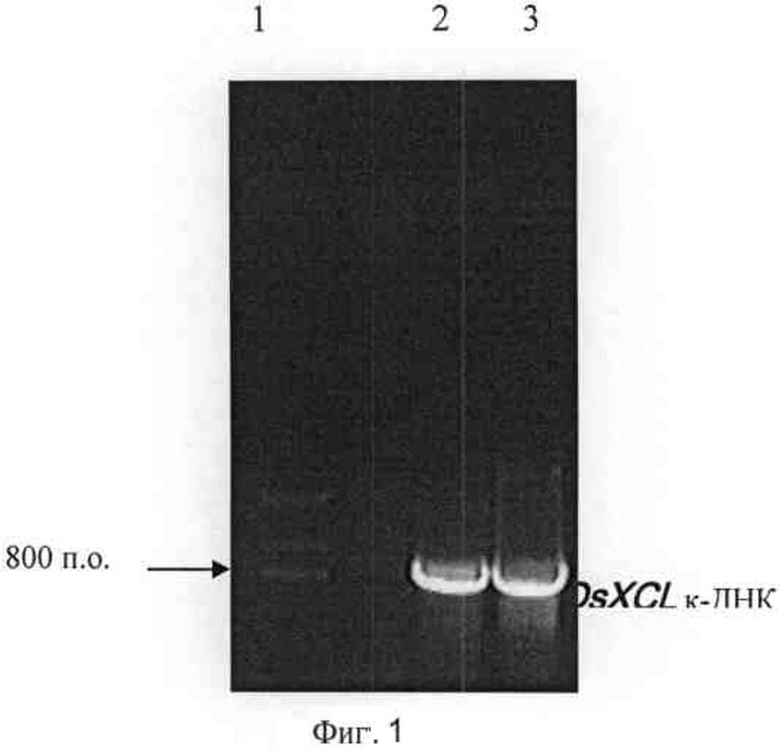
На фигуре 1 показан результат электрофореза в агарозном геле кДНК гена OsXCL, амплифицированной при помощи ПЦР, где полоса 1 представляет собой ДНК-маркер; полосы 2 и 3 представляют собой OsXCL кДНК.
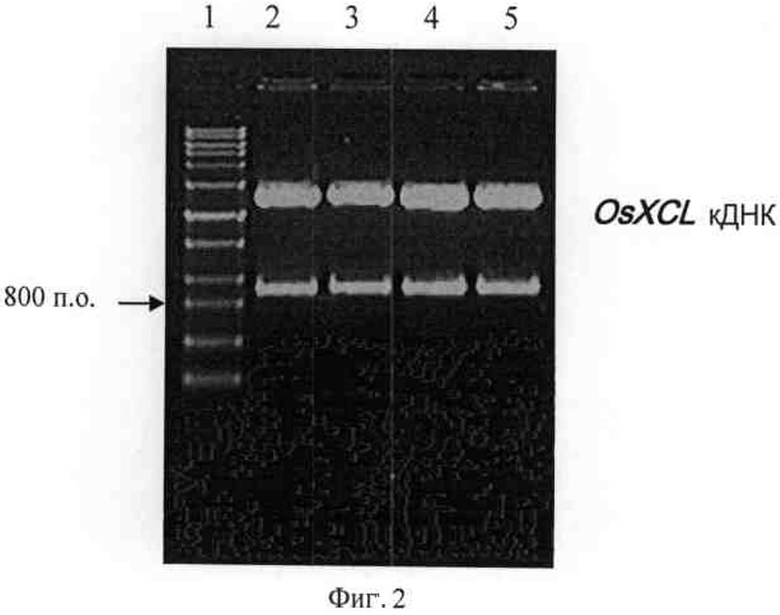
На фигуре 2 представлено подтверждение ферментативного расщепления посредством HindIII и EcoRI после лигирования OsXCL в Т вектор, где полоса 1 представляет собой ДНК-маркер; полосы 2-5 представляют собой результаты двойного ферментативного расщепления клонирующего вектора OsXCL кДНК посредством EcoRI и HindIII.
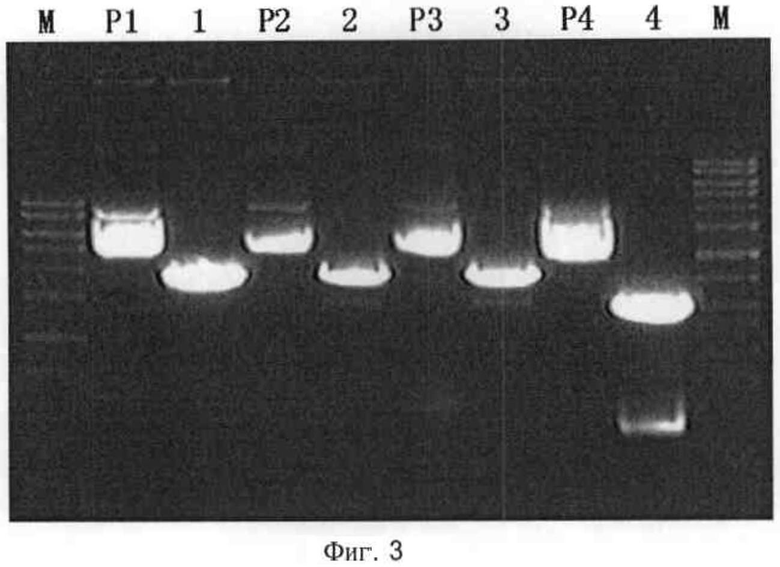
На фигуре 3 представлено подтверждение ферментативного расщепления посредством BamHI после лигирования OsXCL кДНК в Т вектор; Р1, Р2, Р3 и Р4 представляют собой полосы OsXCL кДНК плазмиды до ферментативного расщепления BamHI; 1, 2, 3 и 4 представляют собой полосы OsXCL кДНК плазмиды после ферментативного расщепления BamHI, M представляет собой ДНК-маркер.
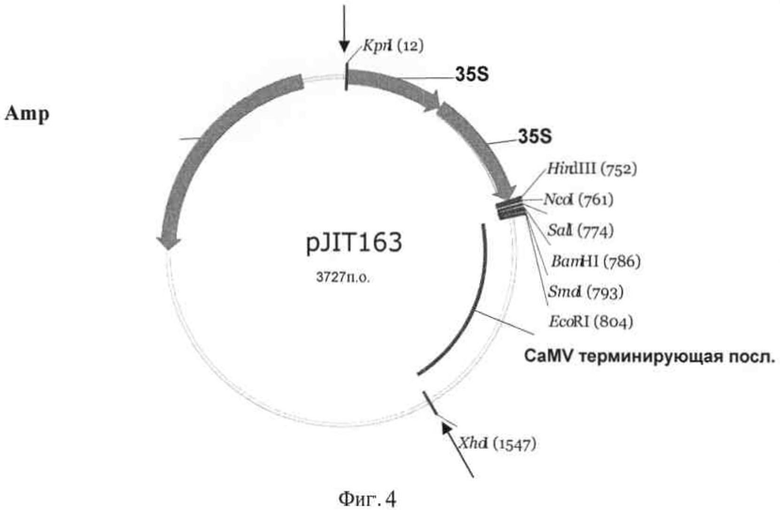
Фигура 4 представляет собой карту pJIT163.
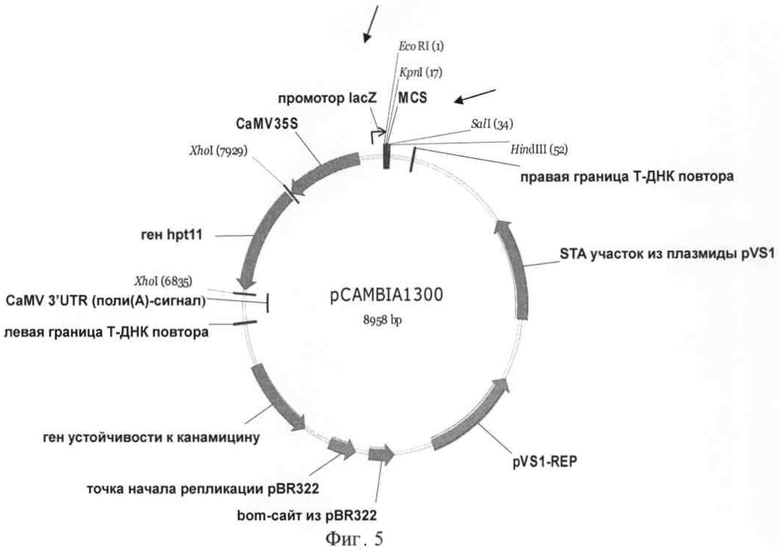
Фигура 5 представляет собой карту pCAMBIA1300.
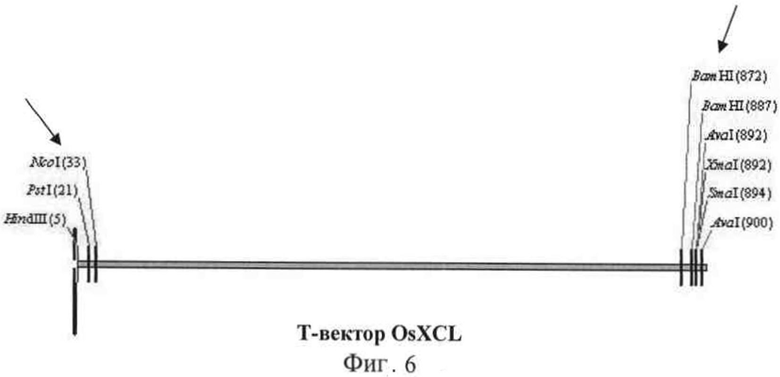
Фигура 6 представляет собой часть карты вектора pMD18-T, включающую OsXCL.
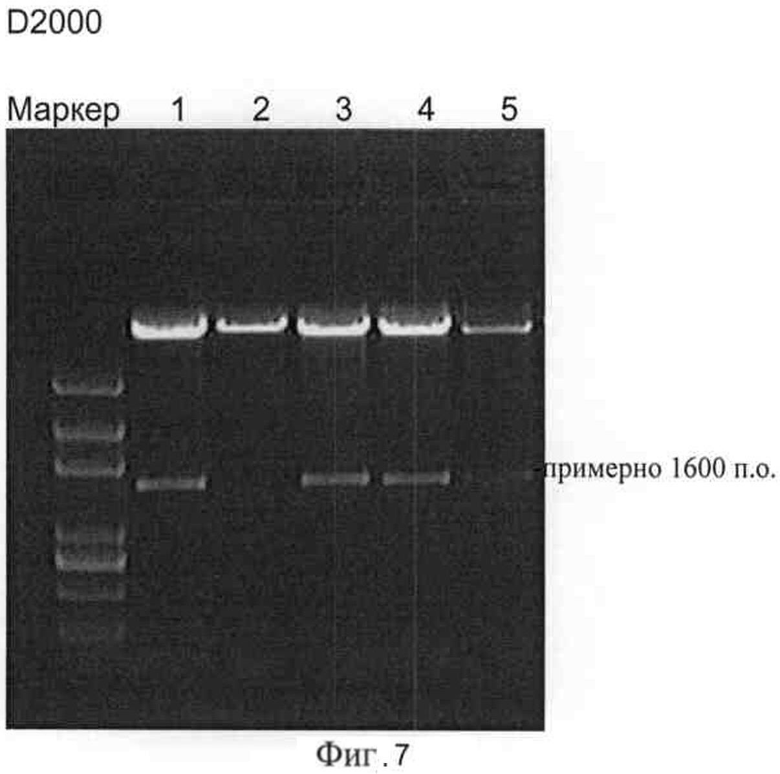
На фигуре 7 представлено подтверждение ферментативного расщепления EcoRI после лигирования OsXCL в вектор экспрессии; полосы 1-5 представляют собой результаты ферментативного расщепления вектора экспрессии OsXCL при помощи EcoRI.
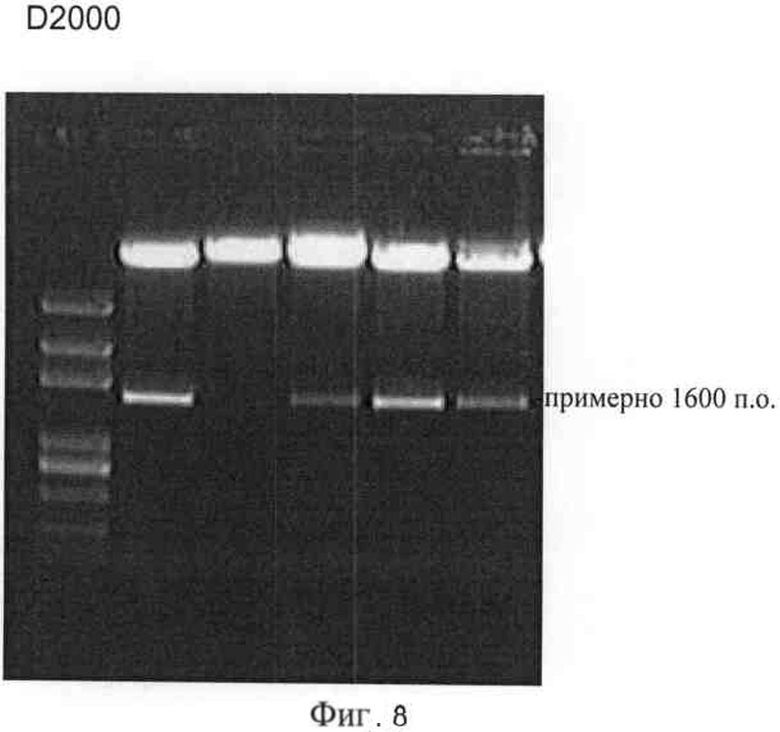
На фигуре 8 представлено подтверждение ферментативного расщепления HindIII после лигирования OsXCL в вектор экспрессии; полосы 1-5 представляют собой расщепленные при помощи фермента HindIII векторы экспрессии OsXCL.
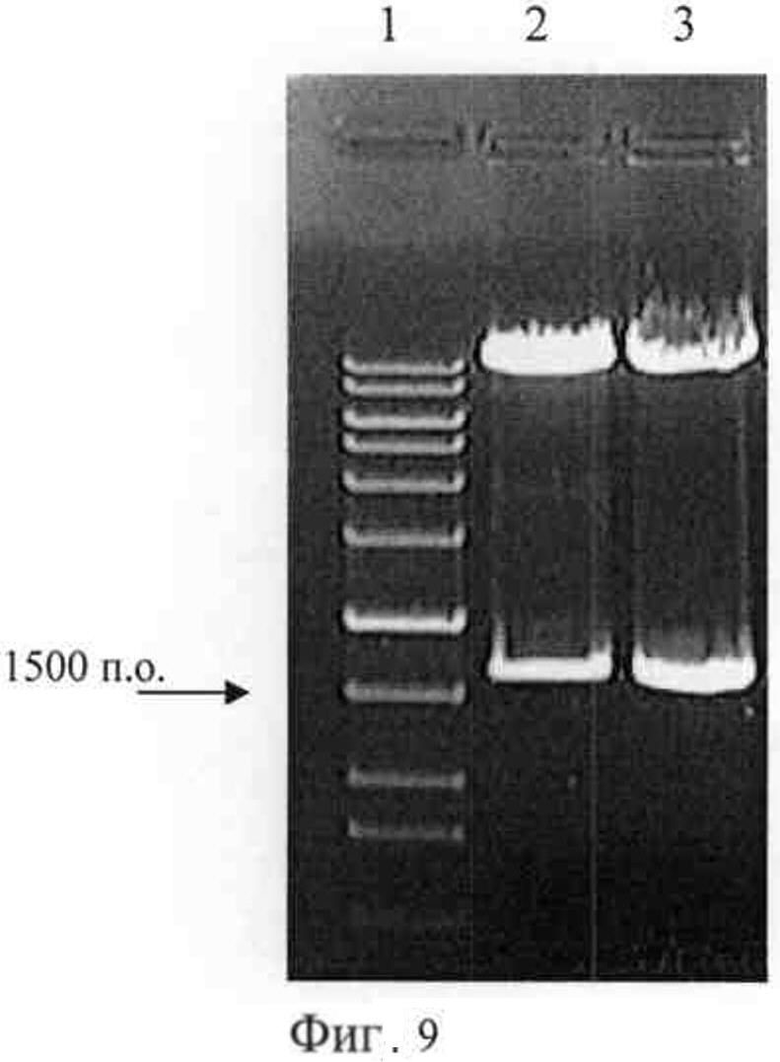
На фигуре 9 представлено подтверждение последовательного ферментативного расщепления посредством EcoRI и HindIII, соответственно, проведенного на плазмиде, выделенной из Agrobacterium; полоса 1 - ДНК-маркер; полоса 2 - результат ферментативного расщепления посредством EcoRI плазмидного вектора экспрессии OsXCL; полоса 3 - результат ферментативного расщепления посредством HindIII плазмидного вектора экспрессии OsXCL.
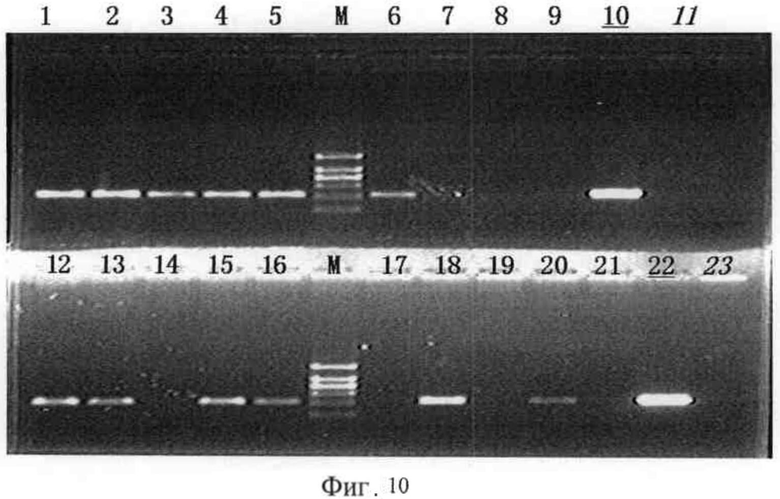
На фигуре 10 представлены результаты ПЦР, проведенной с праймерами на ген устойчивости к гигромицину. На указанной фигуре М представляет собой ДНК-маркер; полосы 1-9 и 12-21 представляют собой результаты ПЦР гена устойчивости к гигромицину, проведенной с геномной ДНК трансгенного по OsXCL риса в качестве матрицы; полосы 10 и 22 - ген фермента, обеспечивающего устойчивость к гигромицину, амплифицированный с плазмидным вектором экспрессии в качестве матрицы, был использован в качестве положительного контроля; полосы 11 и 23 - негативный контроль без матрицы (вода).
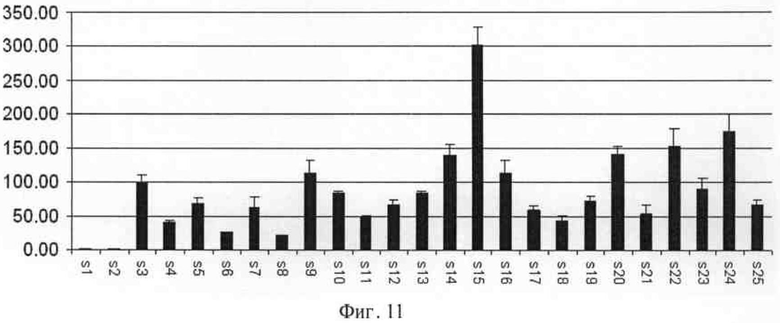
На фигуре 11 представлен анализ относительной экспрессии методом количественной ПЦР в режиме реального времени, проведенной на растениях риса 93-11 поколения Т0, трансформированных геном OsXCL. S1 - контрольные генетически не модифицированные растения риса; S2 - контрольные растения риса с пустым вектором, не содержащим ген OsXCL; S3-S25 - растения риса 93-11 поколения Т0, трансформированные геном OsXCL.
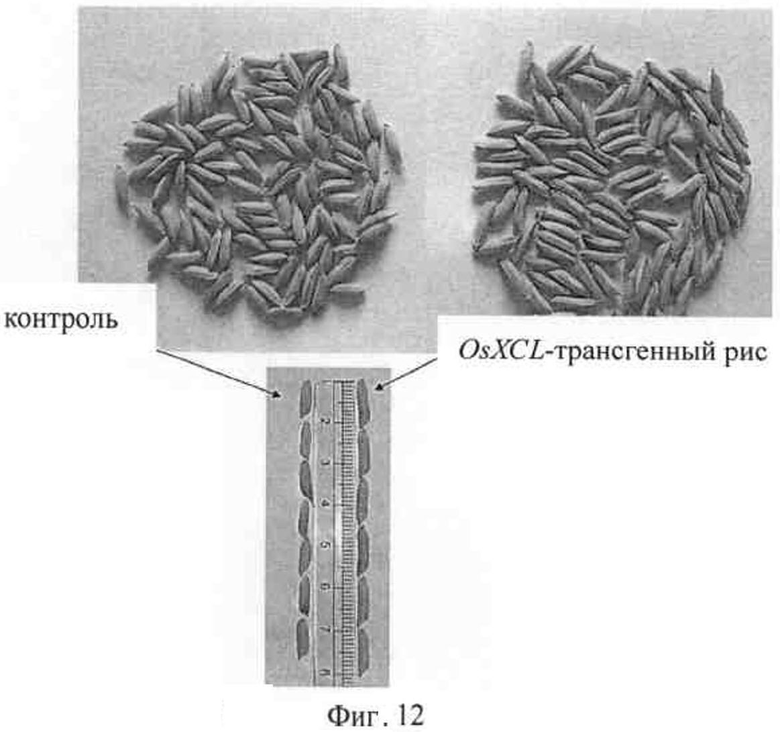
На фигуре 12 представлены снимки зерен OsXCL-трансгенного риса и зерна риса из контрольной группы.
На фигуре 13 представлены снимки OsXCL-трансгенного риса поколения Т0 со скрученными листьями и риса поколения Т2 с основаниями кроющих листьев, закручивающимися на поздних этапах развития.
На фигуре 14 представлен снимок, демонстрирующий увеличение количества зерен в метелке растений поколения Т2 трансгенного риса 9311 с избыточной экспрессией гена OsXCL.
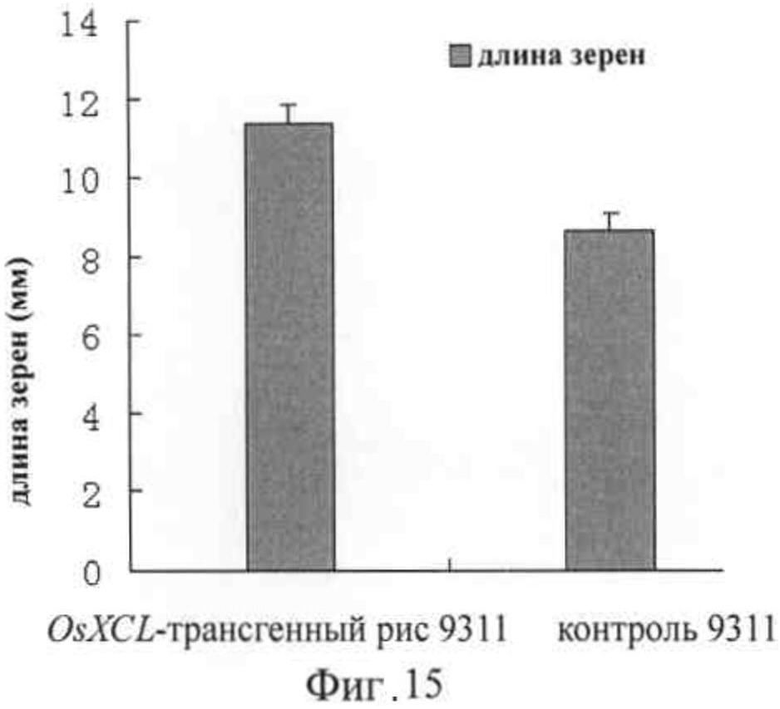
На фигуре 15 представлена диаграмма, демонстрирующая увеличение длины зерен трансгенного риса 9311 с избыточной экспрессией гена OsXCL.
На фигуре 16 представлен снимок трансгенного растения Arabidopsis thaliana с избыточной экспрессией гена OsXCL со значительно увеличенными стручками и скрученными листьями.
Наилучшее техническое выполнение изобретения
Настоящее изобретение описано далее со ссылками на приведенные ниже конкретные
Примеры, которые, тем не менее, не предназначены для ограничения объема настоящего изобретения.
Каждый из способов, представленных в приведенных ниже примерах, представляет собой стандартный метод, если не указано иное.
Пример 1: селекция трансгенного риса с длинными, большими и многочисленными зернами и скрученными листьями
I. Конструирование рекомбинантного вектора экспрессии
1. Клонирование гена OsXCL
Искусственно синтезировали пару праймеров присоединением к 5' концам сайтов ферментативного расщепления NcoI и BamHI, соответственно. Прямой праймер и обратный праймер приведены ниже:
F: 5-CCATGG GAATCCAATCCACTCCACTCCACC-3 (30);
R: 5-GGATCC CTAATAGGCGGTGTGGTGTTGCG-3 (29).
Из РНК, выделенной из риса линии Pei'ai 64S (Китайский Национальный центр гибридизации и селекции риса (Chinese National Center for Rice Hybridization and Breeding), Чанша, Китай) обратной транскрипцией, была получена первая цепь кДНК.
Для амплификации кДНК, соответствующей SEQ ID NO: 1, была проведена ПЦР с вышеописанными прямым и обратным праймерами и кДНК риса Pei'ai 64S в качестве матрицы. Процесс ПЦР начинали с предварительной денатурации при 94°С в течение 5 мин под горячей крышкой (105°С), затем проводили 32 цикла денатурации при 94°С в течение 30 с, отжигали при 56°С в течение 30 с, проводили элонгацию при 72°С в течение 1 минуты и 20 с, завершая финальной элонгацией при 72°С в течение 10 мин и выделением при 22°С.
Использовали следующую систему ПЦР:
Электрофорез в агарозном геле проводили с ТАЕ буфером для электрофореза, полученные фрагменты размером приблизительно 800 п.о. (Фигура 1) были определены как OsXCL.
Указанные отрезки, содержащие OsXCL, были выделены из фрагментов геля с использованием набора от TIANGEN. Выделенные фрагменты встраивали в вектор pMD18-T (ТА Cloning, Jinan TaiTianHe Biotechnology Limited Company); использовали следующую лигирующую систему:
Лигирование продолжали в течение 2 часов, затем трансформировали компетентные клетки Е. coli штамма DH5α, распределяли по чашкам и проводили ампициллиновый скрининг. Отбирали моноклоны, из которых выделяли плазмиду и идентифицировали двойным ферментативным расщеплением HindIII и EcoRI. Ферментативное расщепление служило признаком присутствия отрезков, содержащих OsXCL, длиной около 800 п.о., как показано на фигуре 2.
Плазмида была расщеплена BamHI для подтверждения направления встраивания целевого фрагмента OsXCL в Т-вектор, и в результате, как показано на фигуре 3, так как сайт расщепления BamHI был добавлен в обратный праймер, обратная вставка в Т-вектор дает отрезок размером около 840 п.о.; на фигуре 3 Р1, Р2, Р3 и Р4 соответствуют нерасщепленным плазмидам, длина которых по подсчетам составляет 1 т.п.н. плюс маркер (справа), и 1, 2, 3 и 4 соответствуют результатам расщепления, размеры этих отрезков по подсчетам составляет 1 т.п.н. плюс маркер (слева). Сравнение результатов позволяет определить, что, за исключением плазмиды 4, каждая из плазмид 1, 2 и 3 была разрезана, и целевые фрагменты были встроены прямо (т.о., длина каждого составила около 800 п.о.). Были секвенированы бактериальные препараты, соответствующие плазмидам 1, 2 и 3, и результат секвенирования позволил предположить, что целевой фрагмент OsXCL представлен последовательностью в положениях 50-873, начиная от 5' конца, SEQ ID NO: 1, и ORF (открытая рамка считывания) гена OsXCL представлена последовательностью, полностью идентичной последовательности в положениях 106-870, начиная от 5' конца, SEQ ID NO:1.
2. Конструирование рекомбинантного вектора экспрессии
1) Конструирование вектора экспрессии 163-1300 Вектор pJIT163 (pGreen, http://www.pgreen.ac.uk/), показанный на фиг.4, расщепляли посредством ферментов KpnI и XhoI, и результаты ферментативного расщепления идентифицировали при помощи электрофореза в агарозном геле перед выделением отрезков ДНК с двойными промоторами 35S. Как показано на фиг.5, рСАМВ1А1300 (CambiaLabs, http://www.cambia.org/daisv/bioforge legacv/3725.ht мл) расщепляли ферментами KpnI и SalI и выделяли большие фрагменты. Xhol и Sail являются изокаудомерами. Два выделенных фрагмента лигировали лигазой Т4 в течение ночи для конструирования сложного вектора 163-1300.
2) Конструирование рекомбинантного вектора экспрессии Т-вектор, содержащий OsXCL, как показано на фигуре 6, разрезался ферментами NcoI и BamHI (и в том случае, если BamHI взаимодействовал с сайтом ферментативного расщепления, введенным по положению 872 при создании праймера, и в том случае, если сайт ферментативного расщепления находился на Т-векторе в положении 887, каждый из выделенных фрагментов содержал стоп-кодон для OsXCL ORF). Вектор экспрессии 163-1300 также разрезали двумя указанными ферментами, выделяли и затем лигировали, т.е. ген OsXCL встраивали в вектор экспрессии 163-1300 для получения рекомбинантного вектора экспрессии, обозначаемого как OsXCL-163-1300, который верифицировали последовательным ферментативным расщеплением HindIII и EcoRI, соответственно. Представленные на фигурах 7 и 8 результаты (полосы 1, 2, 3, 4 и 5 каждая соответствуют экспрессионному вектору OsXCL после ферментативного расщепления) подтверждают, что каждая из полос 1, 3, 4 и 5 соответствует целевому отрезку размером около 1600 п.о., содержащей OsXCL.
II. Селекция и определение трансгенного риса с длинными зернами и скрученными листьями
1. Получение трансгенного риса с длинными, крупными многочисленными зернами и скрученными листьями Рекомбинантный вектор экспрессии согласно 1.2 применяли для трансформации штамма Agrobacterium EHA105 (коммерчески доступного у Tiangen Biotech (Пекин) Co., Ltd.) методом замораживания-оттаивания. Плазмиды, выделенные из Agrobacterium, подвергали проверочному ферментативному расщеплению посредством поочередно EcoRI и HindIII, соответственно (Фигура 9). При этом трасформация Agrobacterium методом замораживания-оттаивания включала следующие этапы:
метод замораживания-оттаивания включал следующие этапы: компетентные клетки Agrobacterium штамма EHA105, хранящиеся при температуре -70°С, извлекали и помещали в водяную баню с температурой 0°С для размораживания; добавляли 10-20 мкл плазмидной ДНК pCAMBIA1300-2×CaMV35S-OsMsr1-CaMV35S-Term (около 1-2 мкг) к 200 мл оттаивающих компетентных клеток Agrobacterium, перемешанных стерильным шприцем, и оставляли на несколько минут; смесь помещали в жидкий азот на 1 мин и в водяную баню температурой 37°С на 5 мин, добавляли 700-800 мкл жидкой среды Лурия-Бертани (LB) и затем подвергали вибрации при температуре 28°С и 200 об/мин в течение 4 ч; центрифугировали в течение 30 с при 1000 g, часть супернатанта удаляли, оставляя 100-150 мкл, которые ресуспендировали при помощи шприца и распределяли по чашкам со средой Лурия-Бертани, содержащей 50 мг/л канамицина, 50 мг/л рифампицина и 34 мг/л хлоромицетина; чашки переворачивали и инкубировали при 28°С в течение 2 дней.
Описанную выше верифицированную рекомбинантную Agrobacterium tumefaciens использовали для заражения каллусной ткани риса 93-11 (Китайский Национальный центр гибридизации и селекции риса, Чанша, Китай) путем инфицирования. Затем инфицированный каллус культивировали на селективной среде, содержащей гигромицин (50 мг/л) для получения устойчивых к гигромицину регенерантных растений.
Из листьев, устойчивых к гигромицину регенерантных растений, выделяли геномную ДНК; ее использовали в качестве матрицы для верификации посредством ПЦР со следующими праймерами, созданными на основе гена устойчивости к гигромицину:
pC13-hyg-F: 5'- ACCTGCCTGAAACCGAACTG-3';
рС13-hyg-R: 5'-CTGCTCCATACAAGCCAACC-3'.
Результаты верификации показаны на фигуре 10, целевые отрезки получены в линиях 1, 2, 3, 4, 5, 6, 12, 13, 15, 16, 18 и 20, в общей сложности в 12-ти линиях растений, то есть было получено в общей сложности 12 позитивных по искомому признаку растений в поколении ТО трансгенных растений (гигромициновый ген, тесно связанный с OsXCL, был интегрирован в геном риса).
2. Определение
Описанный выше OsXCL-трансгенный рис перемещали в теплицу для культивации, помещали в мешок, проводили самоопыление и получали семена трансгенного риса.
При этом трансгенный рис, полученный с помощью вектора экспрессии 163-1300, не содержащего гена OsXCL, использовали как контроль с пустым вектором; также в качестве контроля использовали нетрансгенный рис.
1) Количественный ПЦР-анализ
Был проведен количественный ПЦР-анализ OsXCL-трансгенного и нетрансгенного риса с ДНК-секвенирующими праймерами 108-F и 108-R гена OsXCL; результаты показаны на фигуре 11: для OsXCL характерен относительно низкий уровень экспрессии в нетрансгенном рисе 93-11 и значительно более высокий уровень экспрессии в OsXCL-трансгенном рисе.
Для описанной ПЦР с обратной транскрипцией были использованы следующие праймеры:
108-F: 5'-CCGCCATCATCCAAACTGA-3' (Tm 59, ПЦР 56);
108-R: 5'-GGTGACCACGCCCTTCTTC-3' (Tm 59, ПЦР 56).
Система ПЦР с обратной транскрипцией (RT-ПЦР)
2) Наблюдаемые фенотипы и статистика
А. Семена растений поколения ТО OsXCL-трансгенного риса 93-11, контроля с пустым вектором и нетрансгенного риса 93-11 взвешивали, измеряли массу 100 зерен и длину зерен; проводили наблюдения за растениями поколения ТО и подсчитывали количество растений со скрученными листьями.
Этот процесс повторяли три раза; результаты представлены на фигуре 12 и в таблице 2. По сравнению с нетрансгенным рисом 93-11 и контролем с пустым вектором OsXCL-трансгенный рис обладает значительно большей массой 100 зерен и большей длиной зерен. При этом по сравнению с рисом дикого типа масса 100 зерен OsXCL-трансгенного риса выше на 25.1% сырого веса и 23% сухого веса, длина зерен больше на 1/4, а число меловидных зерен меньше (качество риса выше).
По сравнению с нетрансгенным рисом и контролем с пустым вектором, растения поколения ТО OsXCL-трансгенного риса обладают несколько более широкими листьями и значительно более выраженной скрученностью кроющих листьев (Фигура 13). Скрученные листья имеют до 90% растений OsXCL-трансгенного риса. Скручивание начинается с оснований листьев и на поздних стадиях развития распространяется на верхнюю часть листьев.
В. Подсчитывалось количество зерен в метелке у растений поколения Т2 из линий с избыточной экспрессией гена OsXCL и у растений из контрольных линий, трансформированных пустым вектором рСАМВ1А1300-163, и проводились наблюдения за растениями поколения Т2, имеющими скрученные листья.
Этот процесс повторяли три раза. На фигуре 14 и в таблице 3 представлены результаты подсчета количества зерен на метелку. По сравнению с контролем с пустым вектором у трансгенного риса 9311 с избыточной экспрессией гена OsXCL количество зерен в метелках существенно выше.
На фигуре 13 представлены результаты наблюдений за скручиванием листьев. Основания кроющих листьев трансгенного риса 9311 с избыточной экспрессией гена OsXCL закручивались на поздних стадиях развития.
С. Тридцать зерен были отобраны соответственно из семян растений поколения Т3 из линий с избыточной экспрессией гена OsXCL и из семян растений контрольных линий, трансформированных пустым вектором pCAMBIA1300-163, и была измерена длина отобранных зерен.
Этот процесс повторяли три раза; результаты представлены на фигуре 15. У растений из контрольных линий с пустым вектором средняя длина зерна составила 8.62 мм; у растений из линий с избыточной экспрессией гена OsXCL длина зерна составила 11.38 мм, на 24.30% больше, чем у растений из контрольных линий с пустым вектором.
Таким образом, все трансгенные линии растений с избыточной экспрессией гена OsXCL демонстрируют фенотип с увеличенной длиной зерна и весом зерна в поколениях Т0-Т3.
Пример 2: Селекция трансгенного Arabidopsis thaliana
Рекомбинантный вектор экспрессии OsXCL-163-1300 получали согласно способу, описанному в Примере 1, и затем встраивали в геном Arabidopsis thaliana (CoI-0, коммерчески доступный от Arabidopsis Biological Resource Center, ABRC) методом погружения цветочных почек, опосредованным Agrobacterium; скрининг проводили на MS-среде, содержащей гигромицин (50 мг/л), семена растений поколения Т2 непрерывно сортировали на MS-среде, содержащей гигромицин, и отбирали линии растений с расщеплением 3:1 для скрининга в поколении Т3; в том случае, если 100% растений поколения Т3 были в состоянии расти на MS-среде, содержащей гигромицин, эта линия считалась гомозиготной; таким образом, получали трансгенный Arabidopsis thaliana с избыточной экспрессией гена OsXCL.
При этом Arabidopsis thaliana, трансформированный вектором экспрессии 163-1300 без гена OsXCL, использовали как контроль с пустым вектором.
Получали поколение Т3 трансгенного Arabidopsis thaliana с избыточной экспрессией гена OsXCL и контроля с пустым вектором, и подсчитывали количество стручков и оценивали скрученность листьев. Результаты представлены на фигуре 16; трансгенный Arabidopsis thaliana с избыточной экспрессией гена OsXCL обладал значительно увеличенными стручками и закрученными листьями.
Промышленное применение
OsXCL-трансгенный рис, полученный согласно настоящему изобретению, имеет массу 100 зерен до 4.224 г, по сравнению с контролем дикого типа зерна трансгенного риса больше на 25.1% по массе, на 1/4 длиннее и в его метелках содержится на 11% больше зерен. Избыточная экспрессия OsXCL в рисе вызывает скручивание листьев, значительное увеличение длины зерен и массы 1000 зерен, а также повышение качества риса и увеличение количества зерен в метелках. Применение гена OsXCL может способствовать не только увеличению урожайности, но также повышению качества риса; кроме того, это не оказывает негативного влияния на рост и развитие риса. Таким образом, указанный ген предположительно представляет собой идеальный ген для повышения урожайности таких культур, как рис и т.п., посредством биотехнологии и генной инженерии, и будет играть активную роль в обеспечении необходимых уровней производства риса и других культур.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ИЗБИРАТЕЛЬНОЙ РЕГУЛЯЦИИ ЭКСПРЕССИИ БЕЛКА | 2012 |
|
RU2667424C2 |
| ПОСЛЕДОВАТЕЛЬНОСТИ СИНТЕТИЧЕСКИХ НУКЛЕОТИДОВ, КОДИРУЮЩИХ ИНСЕКТИЦИДНЫЙ КРИСТАЛЛИЧЕСКИЙ БЕЛОК, И ИХ ПРИМЕНЕНИЯ | 2020 |
|
RU2820699C2 |
| РЕГУЛИРУЮЩИЙ ВЫСОТУ РАСТЕНИЙ ГЕН И ЕГО ПРИМЕНЕНИЯ | 2008 |
|
RU2458132C2 |
| ИНСЕКТИЦИДНЫЕ БЕЛКИ | 2010 |
|
RU2613778C2 |
| КОДОН-ОПТИМИЗИРОВАННЫЕ СИНТЕТИЧЕСКИЕ НУКЛЕОТИДНЫЕ ПОСЛЕДОВАТЕЛЬНОСТИ, КОДИРУЮЩИЕ БЕЛОК Cry2Ai, И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2799821C2 |
| Белок устойчивости к гербицидам, кодирующий его ген и их применение | 2016 |
|
RU2692553C2 |
| БЕЛОК-ФАКТОР ТРАНСКРИПЦИИ DST С ДОМЕНОМ "ЦИНКОВЫЕ ПАЛЬЦЫ" РИСА И ЕГО ПРИМЕНЕНИЕ ДЛЯ РЕГУЛЯЦИИ УСТОЙЧИВОСТИ К ЗАСУХЕ И К ДЕЙСТВИЮ СОЛЕЙ | 2010 |
|
RU2558249C2 |
| Белок устойчивости к гербицидам, кодирующие его гены и их применение | 2016 |
|
RU2681162C1 |
| РАСТИТЕЛЬНЫЕ КЛЕТКИ И ОРГАНИЗМЫ РАСТЕНИЙ С МОДИФИЦИРОВАННЫМ КЛЕТОЧНЫМ РОСТОМ, РАЗВИТИЕМ И ДИФФЕРЕНЦИРОВКОЙ | 2004 |
|
RU2349642C2 |
| ВЫДЕЛЕНИЕ И ОЧИСТКА БЕЛКА | 2005 |
|
RU2420585C2 |





Изобретение относится к области биохимии, в частности к применению гена, кодирующего белок, который состоит из аминокислотной последовательности, представленной в SEQ ID NO.2, для получения трансгенного риса с длинными, большими и многочисленными зернами и увеличенной урожайностью, увеличенным количеством зерен в метелке и скрученными листьями. Раскрыто применение трансгенной линии клеток риса и рекомбинантного вектора для получения трансгенного риса с длинными, большими и многочисленными зернами и увеличенной урожайностью, увеличенным количеством зерен в метелке и скрученными листьями. Изобретение позволяет эффективно получать трансгенный рис с длинными, большими и многочисленными зернами и увеличенной урожайностью, увеличенным количеством зерен в метелке и скрученными листьями. 3 н. и 2 з.п. ф-лы, 16 ил., 4 табл., 2 пр.
1. Применение гена, кодирующего белок, который состоит из аминокислотной последовательности, представленной в SEQ ID NO.2, для получения трансгенного риса с длинными, большими и многочисленными зернами и увеличенной урожайностью, увеличенным количеством зерен в метелке и скрученными листьями.
2. Применение по п. 1 для получения трансгенного растения, отличающееся тем, что: указанный в п. 1 ген представляет собой 1), 2), 3) или 4):
1) ген, имеющий кодирующую последовательность, соответствующую положениям 106-870 от 5'-конца SEQ ID NO.1;
2) ген, имеющий кодирующую последовательность, соответствующую положениям 50-873 от 5'-конца SEQ ID NO.1;
3) ген, кодирующий белок, который состоит из аминокислотной последовательности, представленной в SEQ ID NO.2;
4) ген, более чем на 80% гомологичный гену, определенному в 1) или 2), и кодирующий белок, который состоит из аминокислотной последовательности, представленной в SEQ ID NO.2.
3. Применение трансгенной линии клеток риса, которая содержит ген, выбранный из:
1) гена, который имеет кодирующую последовательность, соответствующую положениям 106-870 от 5'-конца SEQ ID NO.1;
2) гена, который имеет кодирующую последовательность, соответствующую положениям 50-873 от 5'-конца SEQ ID NO.1;
3) гена, кодирующего белок, который состоит из аминокислотной последовательности, представленной в SEQ ID NO.2;
4) гена, более чем на 80% гомологичного гену, определенному в 1) или 2), и кодирующего белок, который состоит из аминокислотной последовательности,
представленной в SEQ ID NO.2, для получения трансгенного риса с длинными, большими и многочисленными зернами и увеличенной урожайностью, увеличенным количеством зерен в метелке и скрученными листьями.
4. Применение рекомбинантного вектора, содержащего ген, выбранный из:
1) гена, который имеет кодирующую последовательность, соответствующую положениям 106-870 от 5'-конца SEQ ID NO.1;
2) гена, который имеет кодирующую последовательность, соответствующую положениям 50-873 от 5'-конца SEQ ID NO.1;
3) гена, кодирующего белок, который состоит из аминокислотной последовательности, представленной в SEQ ID NO.2;
4) гена, более чем на 80% гомологичного гену, определенному в 1) или 2), и кодирующего белок, который состоит из аминокислотной последовательности, представленной в SEQ ID NO.2,
для получения трансгенного риса с длинными, большими и многочисленными зернами и увеличенной урожайностью, увеличенным количеством зерен в метелке и скрученными листьями.
5. Применение по п. 4, отличающееся тем, что указанный рекомбинантный вектор представляет собой рекомбинантный вектор, полученный встраиванием указанного гена в сайт множественного клонирования в векторе экспрессии 163-1300; причем указанный способ конструирования вектора экспрессии 163-1300 состоит в лигировании отрезка ДНК, содержащего двойной промотор 35S, полученного ферментативным расщеплением pJIT163 с помощью Kpnl и Xhol, большим фрагментом, полученным ферментативным расщеплением pCAMBIA1300 с помощью Kpnl и Sall, с получением рекомбинантного вектора экспрессии.
| US2004123343 А1, 24.06.2004 | |||
| JP2005185101 А, 14.07.2005 | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Способ изготовления электрического изолирующего состава | 1924 |
|
SU4799A1 |
| СПОСОБ УВЕЛИЧЕНИЯ УРОЖАЙНОСТИ РАСТЕНИЯ, СПОСОБ КОНТРОЛИРОВАНИЯ РЕЖИМА ЦВЕТЕНИЯ РАСТЕНИЯ И КОНСТРУКЦИЯ ДНК ДЛЯ ИХ ОСУЩЕСТВЛЕНИЯ | 1998 |
|
RU2241753C2 |
Авторы
Даты
2015-06-10—Публикация
2010-07-08—Подача