ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к антителам против альфа-синуклеина и к способу применения этих антител для лечения синуклеинoпатий. В частности, настоящее изобретение относится к антителам против альфа-синуклеина и их применению при лечении болезни Паркинсона.
УРОВЕНЬ ТЕХНИКИ
Альфа-синуклеин представляет собой небольшой растворимый белок длиной 140 аминокислот, существующий в совершенно разных формах. Альфа-синуклеин в основном обнаруживается в пресинаптических нервных окончаниях, и хотя его точная функция неизвестна, исследователи считают, что он играет центральную роль во многих нейродегенеративных процессах.
В течение последних 15 лет было показано, что альфа-синуклеин играет ключевую роль в патогенезе всех форм болезни Паркинсона. Генетические мутации или мультипликации гена альфа-синуклеина вызывают семейную болезнь Паркинсона с ранним началом (PD). Интересно отметить, что при мультипликации локуса генных семейств патогенный эффект, вне всякого сомнения, зависит от дозы гена. Дупликации генов вызывают болезнь Паркинсона с относительно ранним началом (~ 47 лет), которая характеризуется нормальным течение заболевания, в то время как трипликации генов ассоциируются с очень ранним возрастом возникновения (~ 33 года) и очень быстрым течением заболевания. При всех формах болезни Паркинсона альфа-синуклеин является основной структурной составляющей телец Леви, которые являются ключевым патологическим признаком заболевания.
Патология с тельцами Леви распространяется в течение заболевания, и предполагается, что альфа-синуклеин действует как прионоподобный белок, который осуществляет неправильное свертывание с образованием токсичных олигомеров и агрегатов, которые могут распространяться от пораженных нейронов к неповрежденным нейронам (Olanow C.W et al. Movement Disorders, Vol 28, No. 1, 2013). Существующие в настоящее время методы лечения не способны остановить распространение заболевания и позволяют только облегчать симптомы, связанные с прогрессирующей потерей зависимой от мотонейронов активности. В 2014 году в публикации Tran H.T. et al, Cell Reports 7, 2054-2065, June 26, 2014 было показано, что интраперитонеальное введения моноклонального антитела против неправильно свернутого альфа-синуклеина мышам, которым ранее интрастриатально были инъецированы фибриллы, предварительно сформированные из альфа-синуклеина, уменьшает патологию с тельцами Леви, уменьшает потерю дофаминергических нейронов в черной субстанции и облегчают двигательную недостаточность. В связи с этим, все еще остается потребность в пассивной иммунотерапии, которая позволяла бы достигать терапевтических эффектов при болезни Паркинсона и других синуклеинoпатиях.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение направлено на удовлетворение указанной выше потребности путем создания антител против альфа-синуклеина в соответствии со следующими вариантами осуществления.
Вариант осуществления 1. Антитело или его антигенсвязывающий фрагмент, которое связывается с альфа-синуклеином, где антитело или его антигенсвязывающий фрагмент включает:
a. вариабельную область легкой цепи, включающую CDR-L1, выбранный из SEQ ID NO: 1; CDR-L2, соответствующий SEQ ID NO: 2, и CDR-L3, соответствующий SEQ ID NO: 3; и
b. вариабельную область тяжелой цепи, включающую CDR-H1, соответствующий SEQ ID NO: 4; CDR-H2, выбранный из SEQ ID NO: 5, и CDR-H3, выбранный из SEQ ID NO: 6.
Вариант осуществления 2. Антитело или его антигенсвязывающий фрагмент по варианту осуществления 1, где аминокислотный остаток глицина (Gly; G) в положении 6 применительно к SEQ ID NO: 3 заменяют на аланин (Ala; A).
Вариант осуществления 3. Антитело или его антигенсвязывающий фрагмент по вариантам осуществления 1 или 2, где антитело или его антигенсвязывающий фрагмент связывается с двумя или более аминокислотными остатками альфа-синуклеина между положением 113 и 129 относительно SEQ ID NO: 8, где антитело или его антигенсвязывающий фрагмент связывается, по меньшей мере, с аминокислотными остатками D119, N122 и Y125.
Вариант осуществления 4. Антитело или его антигенсвязывающий фрагмент по любому из предшествующих вариантов осуществления, где антитело или антигенсвязывающий фрагмент предотвращает агрегацию альфа-синуклеина, индуцированную фибриллами альфа-синуклеина.
Вариант осуществления 5. Антитело или его антигенсвязывающий фрагмент по любому из предшествующих вариантов осуществления, где антитело или антигенсвязывающий фрагмент способны связывать альфа-синуклеин в форме мономера и в форме фибрилл.
Вариант осуществления 6. Антитело или его антигенсвязывающий фрагмент по любому из предшествующих вариантов осуществления, которые имеют более высокую аффинность связывания по отношению к альфа-синуклеину в фибриллах, чем по отношению к альфа-синуклеину в форме мономера, характеризующуюся константой диссоциации (KD), которая, по меньшей мере, в 10 раз выше для мономерного альфа-синуклеина, чем для альфа-синуклеина в фибриллах.
Вариант осуществления 7. Антитело или его антигенсвязывающий фрагмент по любому из предшествующих вариантов осуществления, которые имеют константу диссоциации (KD) для альфа-синуклеина в фибриллах 60 пM или ниже.
Вариант осуществления 8. Антитело или его антигенсвязывающий фрагмент по любому из предшествующих вариантов осуществления, где антитело представляет собой химерное, гуманизированное или человеческое антитело.
Вариант осуществления 9. Антитело или его антигенсвязывающий фрагмент по любому из предшествующих вариантов осуществления, где антитело представляет собой полноразмерное антитело.
Вариант осуществления 10. Антитело или его антигенсвязывающий фрагмент по варианту осуществления 9, где полноразмерное антитело выбирают из IgG1, IgG4 или IgG4P.
Вариант осуществления 11. Антитело или его антигенсвязывающий фрагмент по любому из предшествующих вариантов осуществления, где антигенсвязывающий фрагмент выбирают из Fab, Fab', F(ab')2, scFv, dAb или VHH.
Вариант осуществления 12. Антитело или его антигенсвязывающий фрагмент по любому из предшествующих вариантов осуществления, где антитело или его антигенсвязывающий фрагмент включает:
a. вариабельную область легкой цепи, соответствующую SEQ ID NO: 13, и вариабельную область тяжелой цепи, выбранную из SEQ ID NO: 25; или
b. вариабельную область легкой цепи, соответствующую SEQ ID NO: 17, или вариабельную область тяжелой цепи, выбранную из SEQ ID NO: 25; или
c. вариабельную область легкой цепи, соответствующую SEQ ID NO: 21, и вариабельную область тяжелой цепи, выбранную из SEQ ID NO: 25.
Вариант осуществления 13. Антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 1-11, где антитело или его антигенсвязывающий фрагмент включает:
a. легкую цепь, соответствующую SEQ ID NO: 14, и тяжелую цепь, соответствующую SEQ ID NO: 26; или
b. легкую цепь, соответствующую SEQ ID NO: 18, и тяжелую цепь, соответствующую SEQ ID NO: 26; или
c. легкую цепь, соответствующую SEQ ID NO: 22, и тяжелую цепь, соответствующую SEQ ID NO: 26.
Вариант осуществления 14. Выделенный полинуклеотид, кодирующий антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 1-13.
Вариант осуществления 15. Выделенный полинуклеотид по варианту осуществления 14, где полинуклеотид кодирует:
a. вариабельную область легкой цепи, где полинуклеотид:
i. по меньшей мере, на 90% идентичен последовательностям SEQ ID NO: 15, 19 или 23; или
ii. включает SEQ ID NO: 15, или 19 или 23; или
iii. состоит в основном из SEQ ID NO: 15, 19 или 23; или
b. вариабельную область тяжелой цепи, где полинуклеотид:
iv. по меньшей мере, на 90% идентичен последовательности SEQ ID NO: 27; или
v. включает SEQ ID NO: 27; или
vi. состоит в основном из SEQ ID NO: 27; или
c. легкую цепь, где полинуклеотид:
vii. по меньшей мере, на 90% идентичен последовательностям SEQ ID NO: 16, 20 или 24; или
viii. включает SEQ ID NO: 16, 20 или 24; или
ix. состоит в основном из SEQ ID NO: 16, 20 или 24;
d. тяжелую цепь, где полинуклеотид:
x. по меньшей мере, на 90% идентичен последовательности SEQ ID NO: 28; или
xi. включает SEQ ID NO: 28; или
xii. состоит в основном из SEQ ID NO: 28.
Вариант осуществления 16. Клонирующий или экспрессирующий вектор, включающий один или более полинуклеотидов по любому из вариантов осуществления 14 или 15.
Вариант осуществления 17. Клетка-хозяина, включающая:
a. один или более полинуклеотидов по любому из вариантов осуществления 14 или 15 или
b. один или более экспрессирующих векторов по варианту осуществления 16.
Вариант осуществления 18. Способ продуцирования антитела или его антигенсвязывающего фрагмента по любому из вариантов осуществления 1-13, включающий культивирование клеток-хозяина по варианту осуществления 17 при соответствующих условиях для продуцирования антитела или его антигенсвязывающего фрагмента и выделение антитела или его антигенсвязывающего фрагмента.
Вариант осуществления 19. Фармацевтическая композиция, включающая антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 1 и 13 и один или более фармацевтически приемлемых носителей, вспомогательных веществ или разбавителей, где фармацевтическая композиция включает один или более дополнительных активных ингредиентов.
Вариант осуществления 20. Антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 1-13 или фармацевтическая композиция по варианту осуществления 19 для применения в терапии.
Вариант осуществления 21. Антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 1-13 или фармацевтическая композиция по варианту осуществления 19 для применения при лечении одной или более синуклеинoпатий.
Вариант осуществления 22. Антитело или его антигенсвязывающий фрагмент, применяемые по варианту осуществления 21, где синуклеинoпатию выбирают из болезни Паркинсона (PD) (включая идиопатические и наследственные формы болезни Паркинсона), деменции с тельцами Леви (DLB), болезни диффузных телец Леви (DLBD), варианта болезни Альцгеймера с тельцами Леви (LBVAD), смешанного типа болезни Альцгеймера и Паркинсона, множественной системной атрофии (MSA) и нейродегенерации с накоплением железа в головном мозге типа 1 (NBIA-1).
Вариант осуществления 23. Антитело или его антигенсвязывающий фрагмент, применяемые по варианту осуществления 22, где синуклеинoпатия представляет собой болезнь Паркинсона.
Вариант осуществления 24. Способ лечения синуклеинoпатии у пациента, включающий введение указанному пациенту терапевтически эффективного количества антитела или его антигенсвязывающего фрагмента по любому из вариантов осуществления 1 или 13 или фармацевтической композиции по варианту осуществления 19.
Вариант осуществления 25. Способ по варианту осуществления 24, где синуклеинoпатию выбирают из болезни Паркинсона (PD) (включая идиопатические и наследственные формы болезни Паркинсона), деменции с тельцами Леви (DLB), болезни диффузных телец Леви (DLBD), варианта болезни Альцгеймера с тельцами Леви (LBVAD), смешанного типа болезни Альцгеймера и Паркинсона, множественной системной атрофии (MSA) и нейродегенерации с накоплением железа в головном мозге типа 1 (NBIA-1), предпочтительно, из болезни Паркинсона.
Вариант осуществления 26. Антитело или его антигенсвязывающий фрагмент по любому из вариантов осуществления 1-13 или фармацевтическая композиция по варианту осуществления 19 для применения при диагностике синуклеинoпатии, предпочтительно, при диагностике болезни Паркинсона.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фигура 1. (A) Электрофорез в полиакриламидном геле в присутствии додецилсульфата натрия (SDS-PAGE) образцов экспрессии альфа-синуклеина. Альфа-синуклеин с His-меткой (1) и после удаления His-метки с помощью высокоспецифичной цистеиновой протеазы вируса гравировки табака (протеазы TEV) (2), гель-проникающая хроматография на колонке Superdex 75 альфа-синуклеина человека, обработанного протеазой TEV (3). Маркер молекулярной массы белка SeeBluePlus2 (Invitrogen) (M). (B) Электрофорез в полиакриламидном геле в присутствии додецилсульфата натрия (SDS-PAGE) альфа-синуклеина человека, очищенного из надосадочной жидкости среды для экспрессии Expi293 в виде немеченого белка дикого типа. (4) Маркер молекулярной массы белка SeeBluePlus2 (Invitrogen) (M).
Фигура 2. (A) Анализ фибрилл путем проведения исследования методом JC-1 мономера без флуоресценции и фибрилл с максимальной флуоресценцией при 540 нм. (B) Типичный пример спектра случайной спирали мономерного альфа-синуклеина человека (длина волны 1646 см-1) и образования β-складчатого промежуточного слоя в рекомбинантном альфа-синуклеине человека в фибриллах (длина волны 1625-1630 см-1).
Фигура 3. Анализ связывания методом иммуноферментного анализа (ELISA). Анализ связывания методом ELISA (A) мышиного 5811 Fab10HIS с мономером рекомбинантного альфа-синуклеина человека и фибриллами и пептидом PVDPDNEAYE альфа-синуклеина человека и (B) мышиного 5811 IgG1 с мономером рекомбинантного альфа-синуклеина человека и фибриллами.
Фигура 4. (А) Вестерн-блоттинг, показывающий связывание мышиного IgG1 5811 с альфа-синуклеином человека и бета-синуклеином человека. 1 - альфа-синуклеин человека; 2 - альфа-синуклеин человека (фирмы rPeptide); 3 - бета-синуклеин человека (фирмы rPeptide); маркер, MagicMark XP. (B) изменения химического сдвига ЯМР, показывающие ожидаемый эпитоп мышиного Fab 5811 на альфа-синуклеине человека.
Фигура 5. Ингибирование связывания 5811 Fab с иммобилизированным альфа-синуклеином (столбики слева - мономер, и столбики справа-фибриллы, соответственно, для каждого из испытанных пептидов).
Фигура 6. Вестерн-блоттинг аланинового сканирования для характеризации эпитопа. (A) Анализ альфа-синуклеин человека (His-меченого) дикого типа и его однонаправленных аминокислотных мутантов на геле 4-12% Bis/Tris NuPage. Полосы: M, SeeBluePlus2; 1, h a-syn V118A; 2, h a-syn D119A; 3, h a-syn P120A; 4, h a-syn D121A; 5, h a-syn N122A; 6, h a-syn E123A; 7, h a-syn A124S; 8, h a-syn Y125A; 9, h a-syn E126A; 10, h a-syn M127A; 11, h a-syn P128A; 12 и 13 h a-syn дикого типа. Вестерн-блоттинг на поливинилидендифторидных (PVDF) мембранах с использованием (B) 5811 mFab и (C) 5811 mIgG в качестве первых антител. Полосы: M, SeeBluePlus2; 1, h a-syn V118A; 2, h a-syn D119A; 3, h a-syn P120A; 4, h a-syn D121A; 5, h a-syn N122A; 6, h a-syn E123A; 7, h a-syn A124S; 8, h a-syn Y125A; 9, h a-syn E126A; 10, h a-syn M127A; 11, h a-syn P128A; 12 h a-syn дикого типа (His-меченый); 13, MagicMark XP; 14, h a-syn дикого типа (без метки).
Фигура 7. Гуманизация легкой цепи. 5811 обозначает крысиную вариабельную последовательность легкой цепи. 5811gL5, 5811gL8 и 5811gL14 обозначают гуманизированные прививки вариабельной легкой цепи 5811 антитела с использованием гена зародышевой линии IGKV1-39 человека в качестве акцепторного каркасного участка. Гипервариабельные участки (CDR) выделены жирным шрифтом/подчеркнуты. Остаток донора показан жирным шрифтом/курсивом и заштрихован: Y71. Мутация в CDR-L3 для модификации потенциального сайта деамидирования показана жирным шрифтом/подчеркнута и заштрихована: G94A.
Фигура 8. Гуманизация тяжелой цепи. 5811 обозначает крысиную вариабельную последовательность легкой цепи. 5811gH4 обозначают гуманизированную прививку вариабельной тяжелой цепи 5811 антитела с использованием гена зародышевой линии IGHV3-15 человека в качестве акцепторного каркасного участка. Гипервариабельные участки (CDR) выделены жирным шрифтом/подчеркнуты. Остатки донора показаны жирным шрифтом/курсивом и заштрихованы: A49 и A100.
Фигура 9. Иммуногистохимия. Иммунореактивность в срезах головного мозга пациентов с болезнью Паркинсона (A-E) и не страдающих болезнью Паркинсона пациентов (F-H). (A-C) В височной коре пациентов с болезнью Паркинсона, антитело 5811 mIgG1 метило нейропиль и цитоплазму некоторых клеток; иногда наблюдались подобные тельцам Леви структуры (белые стрелки). (D, E) Антитело 5811 mIgG1 метило подобные тельцам Леви характерные компоненты (белые стрелки) в черной субстанции пациентов с болезнью Паркинсона . (F, G) В тканях височной коры не страдающих болезнью Паркинсона пациентов, антитело 5811 mIgG1 также метило нейропиль, но никаких подобных тельцам Леви структур не наблюдалось. (H) Никаких подобных тельцам Леви структур не наблюдалось в черной субстанции не страдающего болезнью Паркинсона пациента; черные стрелки указывают на неспецифическую маркировку, соответствующую нейромеланинсодержащим нейронам и нейрональным волокнам. Масштабная полоска = 50 мкм.
Фигура 10. Анализ агрегации клеток (клеток линии HEK); антитела по настоящему изобретению были способны ингибировать агрегацию альфа-синуклеина, индуцированную альфа-синуклеином в фибриллах, с величиной IC50 ниже 5 нM. Отрезки прямой представляют стандартную ошибку среднего значения при измерении (SEM, N=4, n=12).
Фигура 11. Анализ агрегации клеток (первичные нейроны). Антитела по настоящему изобретению были способны ингибировать агрегацию альфа-синуклеина, индуцированную альфа-синуклеином в фибриллах, на мышиных первичных нейронах, экспрессирующих эндогенные уровни альфа-синуклеина, с величиной IC50 ниже 5 нM. Отрезки прямой представляют стандартную ошибку среднего значения (SEM, N=5, n=17).
Фигура 12. Изображения иммуногистохимических препаратов патологии альфа-синуклеина (стрелки) в различных участках головного мозга трансгенных мышей линии SNCA-OVX, которым инъецировали мышиные предварительно сформированные фибриллы (PFF) альфа-синуклеина.
Фигура 13. Количественная оценка патологии альфа-синуклеина в различных участках головного мозга трансгенных мышей линии SNCA-OVX в коре головного мозга, стриатуме и черном веществе.
Фигура 14. Фармакокинетические профили антител 5811 против альфа-синуклеина у мышей дикого типа.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Далее настоящее изобретение будет описано применительно к конкретным неограничивающим аспектам и вариантам его осуществления и со ссылками на конкретные фигуры и примеры.
Технические термины используются в соответствии с их общепринятым значением, если не указано иное. Если определенным терминам придается конкретное значение, то определения терминов будут даны с учетом условий использования этих терминов.
В случае, когда в настоящем описании и формуле изобретения используется термин "включающий", это не исключает наличие других элементов. Применительно к целям настоящего изобретения, считается, что термин "состоящий из" является предпочтительным вариантом термина "включающий".
При использовании в изобретении существительного в форме единственного числа, подразумевается, что эта форма включает данное существительное и во множественном числе, если специально не указано иное.
Используемые в изобретении термин "лечение" и другие подобные термины относятся к достижению желаемого фармакологического и/или физиологического эффекта. Эффект может быть профилактическим с точки зрения полного или частичного предотвращения заболевания или его симптома, и/или может быть терапевтическим с точки зрения частичного или полного излечения заболевания и или неблагоприятного эффекта, связанного с заболеванием. Таким образом, термин "лечение" охватывает любое лечение заболевания у млекопитающего, в частности, у человека, и включает: (а) предотвращение возникновения заболевания у субъекта, который может быть предрасположен к заболеванию, но у которого еще не было диагностировано наличие этого заболевания; (b) подавление заболевания, то есть купирование его развития; и (с) облегчение заболевания, то есть достижение ремиссии при заболевании.
Термин "терапевтически эффективное количество" относится к количеству антитела против альфа-синуклеина или его антигенсвязывающего фрагмента, которое при введении млекопитающему или другому субъекту с целью лечения заболевания является достаточным для осуществления такого лечения заболевания. Терапевтически эффективное количество будет изменяться в зависимости от конкретно используемого антитела против альфа-синуклеина или его антигенсвязывающего фрагмента, заболевания и его тяжести, а также возраста, массы тела и других показателей субъекта, подвергаемого лечению.
Термин "выделенный" означает в этом изобретении, что антитело, антигенсвязывающий фрагмент или полинуклеотид, в зависимости от конкретного случая, существуют в физической окружающей среде, отличной от той, в которой они могут встречаться в природе.
В настоящем изобретении предлагается антитело или его антигенсвязывающий фрагмент, которые связываются с альфа-синуклеином, где антитело или его антигенсвязывающий фрагмент включает:
a. вариабельную область легкой цепи, включающую CDR-L1, выбранный из SEQ ID NO: 1; CDR-L2, соответствующий SEQ ID NO: 2, и CDR-L3, соответствующий SEQ ID NO: 3; и
b. вариабельную область тяжелой цепи, включающую CDR-H1, соответствующий SEQ ID NO: 4; CDR-H2, выбранный из SEQ ID NO: 5, и CDR-H3, выбранный из SEQ ID NO: 6.
В одном варианте осуществления, аминокислотный остаток глицина (Gly; G) в положении 6 применительно к SEQ ID NO: 3 заменяют на аланин (Ala; A).
Альфа-синуклеин (или alpha syn; a-синуклеин; a-syn или любой другой известный синоним) относится к общепринятому названию этого белка и включает, но этим не ограничивая, варианты альтернативные сплайсинга, мутанты и альфа-синуклеин от других особей (мышей, обезьян, и так далее). Если не указано иное, то в случае, когда имеется в виду или упоминается в явной форме альфа-синуклеин человека, такой альфа-синуклеин включает последовательность, представленную последовательностью SEQ ID NO: 8 или Uniprot P37840.
MDVFMKGLSKAKEGVVAAAEKTKQGVAEAAGKTKEGVLYVGSKTKEGVVHGVATVAEKTKEQVTNVGGAVVTGVTAVAQKTVEGAGSIAAATGFVKKDQLGKNEEGAPQEGILEDMPVDPDNEAYEMPSEEGYQDYEPEA (SEQ ID NO: 8).
Используемый в изобретении термин "антитело" обычно относится к интактным (цельным) антителам, то есть включающим элементы двух тяжелых цепей и двух легких цепей. Антитело может включать, кроме того, дополнительные связывающие домены, например, как в молекуле DVD-Ig, раскрытой в патентном документе WO 2007/024715, или в так называемом (FabFv)2Fc, описанном в патентном документе WO2011/030107. Таким образом, используемое в настоящем изобретении антитело включает двух-, трех- или четырехвалентные полноразмерные антитела.
Антигенсвязывающие фрагменты антител включают одноцепочечные антитела (то есть полноразмерную тяжелую цепь и легкую цепь); Fab, модифицированный Fab, Fab', модифицированный Fab', F(ab')2, Fv, Fab-Fv, Fab-dsFv, однодоменные антитела (например, VH или VL или VHH), scFv, двух-, трех- или четырехвалентные антитела, Bis-scFv, диатела, триотела, триатела, тетратела и эпитопсвязывающие фрагменты любого из приведенных выше антител (смотрите, например, Holliger and Hudson, 2005, Nature Biotech. 23(9):1126-1136; Adair and Lawson, 2005, Drug Design Reviews - Online 2(3), 209-217). Методы создания и получения этих фрагментов антител хорошо известны (смотрите, например, Verma et al., 1998, Journal of Immunological Methods, 216, 165-181). Формат Fab-Fv был впервые раскрыт в патентном документе WO2009/040562, а его стабилизированная дисульфидом версия, Fab-dsFv, была впервые раскрыта в патентном документе WO2010/035012. Другие фрагменты антител для применения в настоящем изобретении включают фрагменты Fab и Fab', описанные в патентных документах International patent applications WO2005/003169, WO2005/003170 и WO2005/003171. Поливалентные антитела могут включать полиспецифичности, например, могут быть биспецифичными, или могут быть моноспецифичными (смотрите, например, патентные документы WO 92/22583 и WO05/113605). Одним таким примером упомянутого последним антитела является Tri-Fab (или TFM), описанное в патентном документе WO92/22583.
Альтернативный антигенсвязывающий фрагмент включает Fab, соединенный с двумя scFvs или dsscFvs, при этом каждый scFv или dsscFv связывает одну и ту же или другую мишень (например, один scFv или dsscFv, связывающий терапевтическую мишень, и один scFv или dsscFv, который увеличивает период полувыведения путем связывания, например, альбумина). Такие фрагменты антител описаны в патентном документе International Patent Application Publication No, WO2015/197772, полное содержание которого включено в настоящее изобретение путем ссылки на него и, в частности, применительно к обсуждению фрагментов антител.
Типичная молекула Fab' включает пару тяжелой и легкой цепей, в которой тяжелая цепь включает вариабельную область VH, константный домен CH1 и природную или модифицированную шарнирную область, и легкая цепь включает вариабельную область VL и константный домен CL. Димеры Fab' по настоящему изобретению образуют F(ab')2, где, например, димеризация может завершаться в шарнирной области.
Антитело или его антигенсвязывающий фрагмент по настоящему изобретению связывается с эпитопом альфа-синуклеина. В рамках настоящего изобретения, термин "эпитоп" используется равнозначно как для конформационных, так и для линейных эпитопов, где конформационный эпитоп состоит из прерывающихся секций первичной аминокислотной последовательности антигена, а линейный эпитоп образован последовательностью, сформированной непрерывными аминокислотами.
Эпитоп может быть идентифицирован известным методом картирования подходящего эпитопа в комбинации с любым одним из антител, предлагаемых в настоящем изобретении. Примеры таких методов включают скрининг пептидов различной длины, полученных их полноразмерного альфа-синуклеина, для связывания с антителом или его фрагментом по настоящему изобретению и идентификацию наименьшего фрагмента, который может специфически связываться с антителом, содержащего последовательность эпитопа, распознаваемого антителом. Пептиды альфа-синуклеина могут быть получены синтетическим путем или гидролитическим расщеплением белка альфа-синуклеина. Пептиды, которые связывают антитело, могут быть идентифицированы, например, методом масс-спектрометрического анализа. В другом примере, для идентификации эпитопа, связанного антителом по настоящему изобретению, могут быть использованы методы спектроскопии ядерного магнитного резонанса или рентгеноструктурного анализа. После идентифицирования, эпитоп может служить для приготовления фрагментов, которые связывают антитело по настоящему изобретению, и, при необходимости, может применяться в качестве иммуногена для получения дополнительных антител, которые связывают тот же самый эпитоп.
В одном варианте осуществления, антитело или его антигенсвязывающий фрагмент по настоящему изобретению связывает два или более аминокислотных остатков альфа-синуклеина между положениями 113 и 129 применительно к SEQ ID NO: 8. В частности, антитело или его антигенсвязывающий фрагмент связывают, по меньшей мере, аминокислотные остатки D119, N122 и Y125 в последовательности SEQ ID NO: 8.
Предпочтительно, чтобы антитело или его антигенсвязывающий фрагмент по настоящему изобретению предотвращали агрегацию альфа-синуклеина, вызываемую фибриллами альфа-синуклеина.
В рамках этого конкретного контекста, термин "предотвращать" (и его различные грамматические варианты) используется в изобретении взаимозаменяемо с термином "ингибировать", и этот термин указывает на то, что антитела по настоящему изобретению обладают действием в отношении агрегации альфа-синуклеина, индуцированной фибриллами альфа-синуклеина. Действие может быть профилактическим, что выражается в полном или частичном предотвращении агрегации; или в полном или частичном уменьшении, то есть блокировании агрегации, с целью предотвращения ее дальнейшего прогрессирования, или в полном или частичном уменьшении возникновения дальнейшей агрегации; или в полном или частичном устранении агрегации, которая уже произошла.
Не привлекая в качестве доказательства какую-либо теорию, тем не менее, можно предположить, что антитело или его антигенсвязывающий фрагмент по настоящему изобретению связывается с альфа-синуклеином:
i) в мономерной форме и предотвращает образование олигомеров и агрегатов альфа-синуклеина; и/или
ii) в олигомерной и фибриллярной форме и предотвращает распространение альфа-синуклеина от одного нейрона к другому нейрону; и/или
iii) в олигомерной и фибриллярной форме и предотвращает агрегацию альфа-синуклеина, вызываемую фибриллами альфа-синуклеина, предпочтительно, агрегацию эндогенного альфа-синуклеина.
Термин "фибриллы", "фибриллярная форма" или "в фибриллах", используемый в изобретении в отношении альфа-синуклеина, обозначает немономерные формы альфа-синуклеина, в том числе олигомеры альфа-синуклеина, которые могут образовывать вещества, распространяющиеся внутри и между структурами головного мозга.
В одном варианте осуществления, антитело или его антигенсвязывающий фрагмент по настоящему изобретению способны связывать альфа-синуклеин в форме мономера и в фибриллах. В одном варианте осуществления, антитело или его антигенсвязывающий фрагмент имеет более высокую аффинность связывания для альфа-синуклеина в фибриллах по сравнению с альфа-синуклеином в виде мономера. Это характеризуется константой диссоциации (KD), величина которой, по меньшей мере, в 10 раз выше для мономерного альфа-синуклеина, чем для альфа-синуклеина в фибриллах.
В одном варианте осуществления, антитело или его антигенсвязывающий фрагмент по настоящему изобретению имеет константу диссоциации (KD) менее 60 пM для мономерного альфа-синуклеина. В другом варианте осуществления, антитело или его антигенсвязывающий фрагмент по настоящему изобретению антитело или его антигенсвязывающий фрагмент по настоящему изобретению имеет константу диссоциации (KD) менее 30 пM для альфа-синуклеина в фибриллах.
Используемый в изобретении термин "KD" относится к константе диссоциации, которую рассчитывают по отношению Kd к Ka (то есть Kd/Ka) и выражают в виде молярной концентрации (M). Kd и Ka обозначают скорость диссоциации и скорость ассоциации, соответственно, для конкретного взаимодействия антиген-антитело (или его антигенсвязывающий фрагмент). Величины KD для антител могут быть определены хорошо известными методами. В качестве метода определения величины KD антитела применяют метод поверхностного плазмонного резонанса, например, на системе Biacore®, описанный в примерах изобретения, с использованием выделенного природного или рекомбинантного альфа-синуклеина, его подходящего гибридного белка/полипептида или его фибриллов. В одном примере, аффинность измеряют с использованием рекомбинантного альфа-синуклеина человека, описанного в примерах изобретения. Для поверхностного плазмонного резонанса, молекулы-мишени иммобилизуют на твердой фазе и подвергают воздействию лиганд в подвижной фазе, движущейся вдоль проточной кюветы. Если происходит связывание лиганда с иммобилизированной мишенью, то изменяется локальный показатель преломления, что приводит к изменению угла поверхностного плазмонного резонанса (SPR), которое может постоянно регистрироваться в реальном масштабе времени путем определения изменений интенсивности отраженного света. Могут быть определены скорости изменения сигнала SPR для расчета кажущихся констант скоростей для фаз ассоциации и диссоциации реакции связывания. Отношение этих величин дает кажущуюся константу равновесия (аффинность) (смотрите, например, публикацию Wolff et al, Cancer Res. 53:2560-65 (1993)).
В одном варианте осуществления, антитело или его антигенсвязывающий фрагмент по настоящему изобретению имеет более высокую аффинность связывания (то есть более низкую величину KD) для альфа-синуклеина в фибриллах по сравнению с альфа-синуклеином в виде мономера. Термин "аффинность" относится к силе взаимодействия между антителом или его антигенсвязывающим фрагментом и альфа-синуклеином.
В одном варианте осуществления, антитело или его антигенсвязывающий фрагмент по настоящему изобретению блокирует или предотвращает или уменьшает агрегацию, вызванную альфа-синуклеином, предпочтительно, вызванную альфа-синуклеином в фибриллах.
В одном варианте осуществления, антитело или его антигенсвязывающий фрагмент по настоящему изобретению имеет величину IC50 менее чем 10 нМ для блокирования агрегации, вызванной альфа-синуклеином в фибриллах, предпочтительно, чтобы антитело или его антигенсвязывающий фрагмент по настоящему изобретению имел величину IC50 менее чем 5 нМ для блокирования агрегации, вызванной альфа-синуклеином в фибриллах.
Используемый в изобретении термин "IC50"относится к половине максимальной ингибирующей концентрации, которая является мерой эффективности вещества, такого как антитела, при ингибировании специфической биологической или биохимической функции, применительно к настоящему изобретению, агрегации, вызванной альфа-синуклеином, предпочтительно, альфа-синуклеином в фибриллах. Величина IC50 представляет собой количественную меру, которая указывает, сколько требуется конкретного вещества для ингибирования на половину данного биологического процесса.
В одном варианте осуществления, антитело или его антигенсвязывающий фрагмент по настоящему изобретению не связывает бета-синуклеин и/или гамма-синуклеин и являются специфичными для альфа-синуклеина.
Используемый в настоящем изобретении термин "специфичное" предназначен для обозначения антитела, которое распознает только тот антиген, к которому оно специфично, или для обозначения антитела, которое обладает значительно более высокой величиной аффинности связывания с антигеном, к которому оно специфично (например, с альфа-синуклеином), по сравнению со связыванием с антигенами, к которым оно неспецифично (с гамма- и бета- синуклеинами), например, по меньшей мере, более высокой величиной аффинности связывания в 5, 6, 7, 8, 9, 10 раз.
Антитела по настоящему изобретению могут быть получены любым общепринятым методом. Полипептид/белок альфа-синуклеина, в том числе гибридные белки, клетки, экспрессирующие (рекомбинантно или природно) полипептид, могут быть использованы для продуцирования антител, которые специфично распознают альфа-синуклеин. Полипептид может быть "созревшим" полипептидом или его биологически активным фрагментом или его производным.
В одном варианте осуществления, полипептид (то есть антиген) представляет собой мономер альфа-синуклеина человека или его фрагмент, предпочтительно, продуцированный, как описано в примерах ниже.
Полипептиды, которые применяют для иммунизации организма-хозяина, могут быть приготовлены хорошо известными способами из полученных методами генетической инженерии клеток-хозяина, включающими экспрессирующие системы, или они могут быть извлечены из природных биологических источников. В настоящем изобретении, термин "полипептиды" включает пептиды, полипептиды и белки. Их используют взаимозаменяемо, если не указано иное. Полипептид альфа-синуклеина или его фрагмент могут, в некоторых случаях, представлять собой часть более крупного белка, такого как гибридный белок, например, слитый с аффинным маркером или подобный.
Антитела, генерируемые против полипептид альфа-синуклеина, могут быть получены, в тех случаях, когда необходима иммунизация животного, путем введения полипептидов животному, предпочтительно, низшему животному, используя хорошо известные и общепринятые протоколы, смотрите, например руководство Handbook of Experimental Immunology, D.M. Weir (ed.), Vol 4, Blackwell Scientific Publishers, Oxford, England, 1986). Могут быть иммунизированы многие теплокровные животные, такие как кролики, мыши, крысы, овцы, коровы, верблюды или свиньи. Однако, обычно наиболее подходящими для этой цели являются мыши, кролики, свинью и крысы.
Моноклональные антитела могут быть приготовлены любым известным методом, таким как гибридомная технология (Kohler & Milstein, 1975, Nature, 256:495-497), триомная технология, гибридомная технология с использованием B-клеток человека (Kozbor et al., 1983, Immunology Today, 4:72) и гибридомная технология с использованием вируса Эпштейна-Барра (Cole et al., Monoclonal antibodies and Cancer Therapy, pp77-96, Alan R Liss, Inc., 1985).
Антитела для применения в изобретении могут быть также генерированы с использованием методов получения антител из одиночных лимфоцитов путем клонирования и экспрессирования кДНК вариабельной области иммуноглобулина, генерированных из одиночных лимфоцитов, выбранных для продуцирования специфических антител, например, методами, описанными в публикации Babcook, J. et al., 1996, Proc. Natl. Acad. Sci. USA 93(15):7843-7848l; в патентных документах WO92/02551; WO2004/051268 и WO2004/106377.
Скрининг антител может быть проведен путем измерения связывания с альфа-синуклеином и/или путем измерения ингибирования альфа-синуклеина в процессе образования фибрилл в присутствии антитела или его фрагмента.
Антитело или его антигенсвязывающий фрагмент по настоящему изобретению включает гипервариабельные участки (CDR), три из тяжелой цепи и три из легкой цепи. Обычно, гипервариабельные участки находятся в каркасном участке и вместе образуют вариабельную область. По соглашению, гипервариабельные участки (CDR) в вариабельных областях тяжелых цепей антитела или его антигенсвязывающего фрагмента обозначают как CDR-H1, CDR-H2 и CDR-H3, и в вариабельных областях легких цепей как CDR-L1, CDR-L2 и CDR-L3. Их нумеруют последовательно в направлении от N-конца к C-концу каждой цепи.
Гипервариабельные участки (CDR) по соглашению нумеруют в соответствии с системой, предложенной Кабатом с соавторами. Эта система изложена в публикации Kabat et al., 1987, in Sequences of Proteins of Immunological Interest, US Department of Health and Human Services, NIH, USA (именуемой далее "Kabat et al. (supra)"). В настоящем изобретении используется эта система нумерации, за исключением тех случаев, когда указана иная система нумерации.
Обозначение остатков по системе Кабата не всегда соответствует линейной нумерации аминокислотных остатков. Реальная линейная аминокислотная последовательность может содержать меньшее число или дополнительное число аминокислот, чем в случае строгого соответствия системе нумерации Кабата, что обусловлено укорочением структурного компонента или вставкой в структурный компонент, будь то каркасный участок или гипервариабельный участок (CDR), основной структуры вариабельного домена. Правильная нумерация остатков по Кабату может быть определена для данного антитела путем использования процедуры выравнивания остатков гомологии в последовательности антитела со "стандартной" последовательностью, пронумерованной по Кабату.
Гипервариабельные участки (CDR) вариабельного домена тяжелой цепи расположены на остатках 31-35 (CDR-H1), остатках 50-65 (CDR-H2) и остатках 95-102 (CDR-H3) в соответствии с системой нумерации Кабата. Однако, согласно публикации Chothia, C. and Lesk, A.M. J. Mol. Biol., 196, 901-917 (1987), петля, эквивалентная CDR-H1, имеет протяженность от остатка 26 до остатка 32. В связи с этим, если не указано иное, то предполагается, что используемый в изобретении "CDR-H1" относится к остаткам 26-35, описанным путем использования комбинации системы нумерации Кабата и топологического определения петли по системе нумерации Chothia.
Гипервариабельные участки (CDR) вариабельного домена легкой цепи расположены на остатках 24-34 (CDR-L1), остатках 50-56 (CDR-L2) и остатках 89-97 (CDR-L3) в соответствии с системой нумерации Кабата.
В одном варианте осуществления, антитело может представлять собой химерное, гуманизированное или человеческое антитело или его фрагмент.
В одном варианте осуществления, антитело или его антигенсвязывающий фрагмент по настоящему изобретению может включать каркасные участки животного, у которого индуцировали антитело. Например, если антитело индуцировали у крысы, оно будет включать гипервариабельные участки (CDR), определяемые и заявленные в изобретении, и каркасные участки крысиного антитела, такого как антитело или его антигенсвязывающий фрагмент, включающие вариабельную область легкой цепи, соответствующей SEQ ID NO: 9 (нуклеотидная последовательность которой показана в SEQ ID NO: 11) и вариабельную область тяжелой цепи, соответствующей SEQ ID NO: 10 (нуклеотидная последовательность которой показана в SEQ ID NO: 12).
Химерные антитела обычно продуцируют с использованием методов рекомбинантных ДНК. ДНК может быть модифицирована путем замены кодирующей последовательности H и L константных областей низшего животного (например, грызуна) на соответствующую кодирующую последовательность L и H цепей человека (Morrison; PNAS 81, 6851 (1984)).
Человеческие антитела включают вариабельные области тяжелых или легких цепей или полноразмерные тяжелые или легкие цепи, которые являются "продуктом" или "получены из" конкретной последовательности зародышевой линии, если вариабельные области или полноразмерные цепи антитела получены из системы, которая использует гены иммуноглобулина зародышевой линии человека. Такие системы включают иммунизацию трансгенной мыши, несущей гены человеческого иммуноглобулина, с помощью представляющего интерес антигена, или скрининг библиотеки генов иммуноглобулина человека методом фагового дисплея с использованием представляющего интерес антигена. Человеческое антитело или его фрагмент, которые являются "продуктом" или "получены из" последовательности иммуноглобулина зародышевой линии человека, могут быть идентифицированы в качестве таковых путем сравнения аминокислотной последовательности антитела человека с аминокислотными последовательностями иммуноглобулинов зародышевой линии человека и выбора последовательности иммуноглобулина зародышевой линии человека, которая наиболее близкая с точки зрения последовательности (то есть, имеет наибольший % идентичности) к последовательности человеческого антитела. Человеческое антитело, которое является "продуктом" или "получено из" конкретной последовательности иммуноглобулина зародышевой линии человека, может содержать аминокислотные различия по сравнению с последовательностью зародышевой линии, например, вследствие естественных соматических мутаций или преднамеренного введения сайт-направленной мутации. Однако выбранное человеческое антитело обычно по своей аминокислотной последовательности на 90% идентично аминокислотной последовательности, кодируемой геном иммуноглобулина зародышевой линии человека, и содержит аминокислотные остатки, которые идентифицируют человеческое антитело как человеческое при сравнении с аминокислотными последовательностями иммуноглобулина зародышевой линии других видов млекопитающих (например, с последовательностями зародышевой линии мыши). В определенных случаях, человеческое антитело по своей аминокислотной последовательности может быть, по меньшей мере, на 60%, 70%, 80%, 90% или, по меньшей мере, на 95%, или даже, по меньшей мере, на 96%, 97%, 98% или 99% идентично аминокислотной последовательности, кодируемой геном иммуноглобулина зародышевой линии. Как правило, человеческое антитело, полученное из конкретной последовательности зародышевой линии человека, будет проявлять не более 10 аминокислотных отличий от аминокислотной последовательности, кодируемой геном иммуноглобулина зародышевой линии человека. В конкретных случаях, человеческое антитело может проявлять не более 5 или даже не более 4, 3, 2 или 1 аминокислотного различия с аминокислотной последовательностью, кодируемой геном иммуноглобулина зародышевой линии.
Человеческие антитела могут быть продуцированы с помощью целого ряда методов, известных специалистам в этой области. Человеческие антитела могут быть получены методом гибридомной технологии с использованием линии клеток миеломы человека или линии клеток гетеромиеломы мыши-человека (Kozbor, J Immunol; (1984) 133:3001; Brodeur, Monoclonal Isolated Antibody Production Techniques and Applications, pp51-63, Marcel Dekker Inc, 1987). Альтернативные методы включают использование фаговых библиотек или трансгенных мышей, в каждом из которых используют репертуары человеческих генов вариабельной области (Winter G; (1994) Annu Rev Immunol 12:433-455, Green LL, (1999) J Immunol Methods 231:1 1-23).
В одном предпочтительном варианте осуществления изобретения, антитело или его антигенсвязывающий фрагмент по изобретению являются гуманизированными.
Используемый в изобретении термин "молекула гуманизированного антитела" относится к молекуле антитела, где тяжелая и/или легкая цепь содержит один или более гипервариабельных участков (CDR) (в том числе, если желательно, один или более модифицированных CDR) от донорского антитела (например, нечеловеческого антитела, такого как мышиное или кроличье моноклональное антитело), привитые в каркасный участок вариабельной области тяжелой и/или легкой цепи акцепторного антитела (например, человеческого антитела). Обзорную информацию можно найти в публикации Vaughan et al, Nature Biotechnology, 16, 535-539, 1998. В одном варианте осуществления, переносят не весь полностью CDR, а только один или более из определяющих специфичность остатков из любого одного из описанных в изобретении выше CDR переносят в каркас человеческого антитела (смотрите, например, Kashmiri et al., 2005, Methods, 36, 25-34). В одном варианте осуществления, только определяющие специфичность остатки из одного или более из описанных в изобретении выше CDR переносят в каркас человеческого антитела. В другом варианте осуществления, только определяющие специфичность остатки из каждого из описанных в изобретении выше CDR переносят в каркас человеческого антитела.
При прививке гипервариабельных участков (CDR), может быть использована любая подходящая последовательность акцепторного каркаса вариабельной области, принимая во внимание класс/тип донорного антитела, из которого получены гипервариабельные участки (CDR), включая каркасные участки мыши, примата и человека.
Соответственно, гуманизированное антитело по настоящему изобретению имеет вариабельный домен, включающий человеческие акцепторные каркасные участки, а также один или более из конкретно предложенных в изобретении гипервариабельных участков (CDR). Поэтому, в одном варианте осуществления предлагается блокирующее гуманизированное антитело, которое связывает альфа-синуклеин, предпочтительно, альфа-синуклеин человека, где вариабельный домен включает человеческие акцепторные каркасные участки и нечеловеческие донорные гипервариабельные участки (CDR).
Примерами человеческих каркасов, которые могут быть использованы в настоящем изобретении, являются KOL, NEWM, REI, EU, TUR, TEI, LAY и POM (Kabat et al., supra). Например, KOL и NEWM могут быть использованы для тяжелой цепи, REI может быть использован для легкой цепи, и EU, LAY и POM могут быть использованы как для тяжелой цепи, так и для легкой цепи. В качестве варианта, могут быть использованы последовательности зародышевой линии человека; они доступны на сайте http://www.imgt.org/.
В гуманизированном антителе или его антигенсвязывающем фрагменте по настоящему изобретению, акцепторные тяжелые и легкие цепи необязательно должны быть получены из одного и того же антитела и могут, если это желательно, включать составные цепи, имеющие каркасные участки, полученные из различных цепей.
Подходящий каркасный участок для легкой цепи гуманизированного антитела по настоящему изобретению получают из гена зародышевой линии IGKV1-39 человека, имеющего SEQ ID NO:29, и нуклеотидная последовательность которого представлена в SEQ ID NO: 31.
Соответственно, в одном варианте осуществления, предлагается гуманизированное антитело или его антигенсвязывающий фрагмент, включающие последовательность, представленную в SEQ ID NO: 1, для CDR-L1, последовательность, представленную в SEQ ID NO: 2, для CDR-L2, и последовательность, представленную в SEQ ID NO: 3 или SEQ ID NO: 7, для CDRL3, где каркасный участок легкой цепи получают из гена зародышевой линии IGKV1-39 человека.
Подходящий каркасный участок для тяжелой цепи гуманизированного антитела или его антигенсвязывающего фрагмента по настоящему изобретению получают из гена зародышевой линии IGHV3-15, имеющего последовательность, представленную в SEQ ID NO: 30, и нуклеотидная последовательность которого представлена SEQ ID NO: 32.
В одном варианте осуществления, предлагается гуманизированное антитело или его антигенсвязывающий фрагмент, включающие последовательность, представленную в SEQ ID NO: 4, для CDR-H1, последовательность, представленную в SEQ ID NO: 5, для CDR-H2, и последовательность, представленную в SEQ ID NO: 6, для CDR-H3, где каркасный участок тяжелой цепи получают из гена зародышевой линии IGHV3-15.
В другом варианте осуществления, предлагается гуманизированное антитело или его антигенсвязывающий фрагмент, включающие:
вариабельную область легкой цепи, включающую CDR-L1, соответствующий последовательности, представленной в SEQ ID NO: 1, CDR-L2, соответствующий последовательности, представленной в SEQ ID NO: 2, и CDR-L3, соответствующий последовательности, представленной в SEQ ID NO: 3 или SEQ ID NO: 7, где каркасный участок легкой цепи получают из гена зародышевой линии IGKV1-39 человека, и
вариабельную область тяжелой цепи, включающую CDR-H1, соответствующий последовательности, представленной в SEQ ID NO: 4, CDR-H2, соответствующий последовательности, представленной в SEQ ID NO: 5, и CDR-H3, соответствующий последовательности, представленной в SEQ ID NO: 6, где каркасный участок тяжелой цепи получают из гена зародышевой линии IGHV3-15.
В гуманизированном антителе или его антигенсвязывающем фрагменте по настоящему изобретению, каркасные участки могут не иметь одну и туже последовательность в качестве последовательностей акцепторного антитела. Например, нетипичные остатки могут быть заменены на более часто встречающиеся остатки для класса или типа акцепторной цепи. В качестве варианта, выбранные остатки в акцепторных каркасных участках могут быть изменены таким образом, что они будут соответствовать остаткам, обнаруживаемым в том же самом положении в донорном антителе (смотрите Reichmann et al., 1998, Nature, 332, 323-324). Такие изменения должны быть сведены к минимуму, необходимому для восстановления аффинности донорного антитела. Протокол для выбора остатков в акцепторные каркасные участки, которые могут быть изменены, описан в патентном документе WO91/09967.
Так, в одном варианте осуществления, 1, 2, 3, 4, 5, 6, 7 или 8 остатков в каркасе заменяют альтернативным аминокислотным остатком.
Соответственно, в одном варианте осуществления, предлагается гуманизированное антитело или его антигенсвязывающий фрагмент, где остаток в положении 71 (Phe (F) 71) вариабельного домена легкой цепи (соответствующей SEQ ID NO: 17 или 18) представляет собой донорный остаток (Tyr (Y) 71), смотрите, например, последовательность, представленную в SEQ ID NO: 13 и 14.
В другом варианте осуществления, предлагается гуманизированное антитело или его антигенсвязывающий фрагмент, где остатки в каждом из положений 49 и 100 (Gly (G) 49 и Thr (T) 100), соответствующие SEQ ID NO: 30 вариабельного домена тяжелой цепи, представляют собой донорные остатки (Ala 49 и Ala 100), смотрите, например, последовательность, представленную в SEQ ID NO: 25 и 26.
В одном варианте осуществления, в изобретении предлагается антитело или его антигенсвязывающий фрагмент, включающие
1. вариабельную область легкой цепи, соответствующую SEQ ID NO: 13, и вариабельную область тяжелой цепи, выбранную из SEQ ID NO: 25; или
2. вариабельную область легкой цепи, соответствующую SEQ ID NO: 17, и вариабельную область тяжелой цепи, выбранную из SEQ ID NO: 25; или
3. вариабельную область легкой цепи, соответствующую SEQ ID NO: 21, и вариабельную область тяжелой цепи, выбранную из SEQ ID NO: 25.
В одном варианте осуществления, в изобретении предлагается антитело или его антигенсвязывающий фрагмент, включающие последовательность, которая на 80% аналогична или идентична раскрытой в изобретении последовательности, например, на 85%, 90%, 91%, 92%, 93%, 94%, 95% 96%, 97%, 98% или 99%, относительно части или полной соответствующей последовательности, например, последовательности вариабельного домена, последовательности CDR, или последовательности вариабельного домена, за исключением CDR. В одном варианте осуществления, соответствующая последовательность представляет собой SEQ ID NO: 25. В одном варианте осуществления, соответствующая последовательность представляет собой SEQ ID NO: 13, SEQ ID NO: 17 или SEQ ID NO: 21.
В одном варианте осуществления, в настоящем изобретении предлагается антитело или его антигенсвязывающий фрагмент, которые связывают альфа-синуклеин человека, включающие легкую цепь, где вариабельный домен легкой цепи включает последовательность, имеющую, по меньшей мере, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95% 96%, 97%, 98% или 99% идентичность или сходство с последовательностью, представленной в SEQ ID NO: 13, SEQ ID NO: 17 или SEQ ID NO: 21, и/или где вариабельный домен тяжелой цепи включает последовательность, имеющую, по меньшей мере, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95% 96%, 97%, 98% или 99% идентичность или сходство с последовательностью, представленной в SEQ ID NO:25.
В одном варианте осуществления, в настоящем изобретении предлагается антитело или его антигенсвязывающий фрагмент, которые связывают альфа-синуклеин человека, где антитело или его антигенсвязывающий фрагмент имеет вариабельный домен легкой цепи, который, по меньшей мере, на 90%, 91%, 92%, 93%, 94%, 95% 96%, 97%, 98% или 99% аналогичен или идентичен последовательности, представленной в SEQ ID NO:13, SEQ ID NO: 17 или SEQ ID NO: 21, но где антитело или его антигенсвязывающий фрагмент имеет последовательность, представленную в SEQ ID NO: 1, для CDR-L1, последовательность, представленную в SEQ ID NO: 2, для CDR-L2, и последовательность, представленную в SEQ ID NO: 3 или SEQ ID NO: 7, для CDR-L3.
В одном варианте осуществления, в настоящем изобретении предлагается антитело или его антигенсвязывающий фрагмент, которые связывают альфа-синуклеин человека, где антитело или его антигенсвязывающий фрагмент имеет вариабельный домен тяжелой цепи, который, по меньшей мере, на 90%, 91%, 92%, 93%, 94%, 95% 96%, 97%, 98% или 99% аналогичен или идентичен последовательности, представленной в SEQ ID NO: 25, но где антитело или его антигенсвязывающий фрагмент имеет последовательность, представленную в SEQ ID NO: 4, для CDR-H1, последовательность, представленную в SEQ ID NO: 5, для CDR-H2, и последовательность, представленную в SEQ ID NO: 6, для CDR-H3.
Используемый в изобретении термин "идентичность" указывает на то, что в любом конкретном положении в выровненных последовательностях, аминокислотный остаток является идентичным для этих последовательностей. Используемый в изобретении термин "сходство" указывает на то, что в любом конкретном положении в выровненных последовательностях, аминокислотный остаток является схожим по типу для этих последовательностей. Например, лейцин может быть заменен на изолейцин или валин. Другие аминокислоты, которые могут часто заменять друг на друга, включают, но этим не ограничивая:
- фенилаланин, тирозин и триптофан (аминокислоты, имеющие ароматические боковые цепи);
- лизин, аргинин и гистидин (аминокислоты, имеющие боковые цепи с основными свойствами);
- аспартат и глутамат (аминокислоты, имеющие боковые цепи с кислотными свойствами);
- аспарагин и глутамин (аминокислоты, имеющие амидные боковые цепи); и
- цистеин и метионин (аминокислоты, имеющие серосодержащие боковые цепи). Степень идентичности и сходства может быть легко рассчитана (смотрите публикации Computational Molecular Biology, Lesk, A.M., ed., Oxford University Press, New York, 1988; Biocomputing. Informatics and Genome Projects, Smith, D.W., ed., Academic Press, New York, 1993; Computer Analysis of Sequence Data, Part 1, Griffin, A.M., and Griffin, H.G., eds., Humana Press, New Jersey, 1994; Sequence Analysis in Molecular Biology, von Heinje, G., Academic Press, 1987, Sequence Analysis Primer, Gribskov, M. and Devereux, J., eds., M Stockton Press, New York, 1991, the BLAST™ software available from NCBI (Altschul, S.F. et al., 1990, J. Mol. Biol. 215:403-410; Gish, W. & States, D.J. 1993, Nature Genet. 3:266-272. Madden, T.L. et al., 1996, Meth. Enzymol. 266:131-141; Altschul, S.F. et al., 1997, Nucleic Acids Res. 25:3389-3402; Zhang, J. & Madden, T.L. 1997, Genome Res. 7:649-656,).
В одном варианте осуществления, антигенсвязывающий фрагмент может представлять собой, но этим не ограничивая, Fab, модифицированный Fab, Fab', модифицированный Fab', F(ab')2, Fv, однодоменные антитела (например, VH или VL или VHH), scFv, dsscFv, двух-, трех- или четырехвалентные антитела, Bis-scFv, диатела, триотела, тетратела и эпитопсвязывающие фрагменты любого из приведенных выше (смотрите, например, публикации Holliger and Hudson, 2005, Nature Biotech. 23(9):1126-1136; Adair and Lawson, 2005, Drug Design Reviews - Online 2(3), 209-217). Методы создания и получения этих фрагментов антител хорошо известны (смотрите, например, публикацию Verma et al., 1998, Journal of Immunological Methods, 216, 165-181). Другие фрагменты антител для применения в настоящем изобретении включают фрагменты Fab и Fab', описанные в патентных документах WO2005/003169, WO2005/003170 и WO2005/003171. Поливалентные антитела могут включать полиспецифичности, например, биспецифичность, или могут быть моноспецифичными (смотрите, например, патентные документы WO 92/22853, WO05/113605, WO2009/040562 и WO2010/035012).
Альтернативный антигенсвязывающий фрагмент включает Fab, связанный с двумя scFvs или dsscFvs, при этом каждый scFv или dsscFv связывает одну и ту же или другую мишень (например, один scFv или dsscFv связывает терапевтическую мишень, и один scFv или dsscFv повышает период полувыведения путем связывания, например, альбумина). Такие фрагменты антител описаны в патентном документе International Patent Application Publication No, WO2015/197772, полное содержание которого включено в настоящее изобретение путем ссылки на него и, в частности, при обсуждении фрагментов антител.
Домены константной области молекулы антитела по настоящему изобретению, если они имеются, могут быть выбраны исходя их предполагаемой функции молекулы антитела, и, в частности, исходя из эффекторных функций, которые могут потребоваться. Например, домены константной области могут представлять собой домены человеческих IgA, IgD, IgE, IgG или IgM. В частности, могут быть использованы домены константной области человеческого IgG, в частности, изотипов IgG1 и IgG3, когда молекулу антитела предполагают использовать в терапевтических целях и требуются эффекторные функции антитела. В качестве варианта, могут быть использованы изотипы IgG2 и IgG4, когда молекулу антитела предполагают использовать в терапевтических целях и не требуются эффекторные функции антитела. Следует иметь в виду, что могут быть также использованы вариации последовательностей этих доменов константной области. Например, могут быть использованы молекулы IgG4, в которых серин в положении 241 был заменен на пролин, как это описано в публикации Angal et al., Molecular Immunology, 1993, 30 (1), 105-108. Для любого специалиста в этой области также является очевидным, что антитела могут подвергаться различным посттрансляционным модификациям. Тип и степень этих модификаций часто зависит от линии клеток-хозяина, используемых для экспрессирования антитела, а также от условий культивирования. Такие модификации могут включать вариации при гликозилировании, окислении метионина, образовании дикетопиперазина, изомеризации аспартата и деамидирование аспарагина. Часто встречающейся модификацией является потеря карбоксиконцевого основного остатка (такого как лизин или аргинин) вследствие действия карбоксипептидаз (как это описано в публикации Harris, RJ. Journal of Chromatography 705:129-134, 1995). Соответственно, C-концевой лизин тяжелой цепи антитела может отсутствовать.
В одном варианте осуществления, C-концевую аминокислоту антитела расщепляют в процессе посттрансляционных модификаций.
В одном варианте осуществления, N-концевую аминокислоту антитела расщепляют в процессе посттрансляционных модификаций.
В другом варианте осуществления, антитело по настоящему изобретению может включать полное антитело, имеющее полноразмерные тяжелые и легкие цепи, или его антигенсвязывающий фрагмент. Например, полноразмерное антитело выбирают из IgG1, IgG4 или IgG4P.
В одном варианте осуществления, антитело или его антигенсвязывающий фрагмент включает:
1. легкую цепь, соответствующую SEQ ID NO: 14, и тяжелую цепь, соответствующую SEQ ID NO: 26; или
2. легкую цепь, соответствующую SEQ ID NO: 18, и тяжелую цепь, соответствующую SEQ ID NO: 26; или
3. легкую цепь, соответствующую SEQ ID NO: 22, и тяжелую цепь, соответствующую SEQ ID NO: 26.
В одном варианте осуществления, предлагается антитело по настоящему изобретению в форме связывающего альфа-синуклеин рекомбинантного белка антитела, который включает фрагмент иммуноглобулина, например, фрагмент Fab или Fab' и одно или два однодоменных антитела (dAb), связанных с ним непосредственно или косвенно, например, описанный в патентных документах WO2009/040562, WO2010035012, WO2011/030107, WO2011/061492 и WO2011/086091, содержание которых включено в настоящее изобретение путем ссылки на них.
В одном варианте осуществления, рекомбинантный белок включает двухдоменные антитела, например, в форме образующейся пары вариабельного домена тяжелой цепи (VH) и вариабельного домена легкой цепи (VL), необязательно связанных с помощью дисульфидной связи.
В одном варианте осуществления, элемент Fab или Fab' рекомбинантного белка имеет такую же или аналогичную специфичность к однодоменному антителу или антителам. В одном варианте осуществления, Fab или Fab' имеют отличную друг от друга специфичность к однодоменному антителу или антителам, то есть рекомбинантный белок является поливалентным. В одном варианте осуществления, поливалентный рекомбинантный белок по настоящему изобретению имеет альбумин-связывающий сайт, например, присутствующая в нем пара VH/VL обеспечивает альбумин-связывающий сайт.
В одном варианте осуществления, антитело или его антигенсвязывающий фрагмент включает вариабельную область легкой цепи, соответствующую SEQ ID NO: 13 или 17 или 21, и вариабельную область тяжелой цепи, выбранную из SEQ ID NO: 25. Например, антитело представляет собой полноразмерное IgG4 антитело, включающее вариабельную область легкой цепи, соответствующую SEQ ID NO: 13 или 17 или 21, и вариабельную область тяжелой цепи, выбранную из SEQ ID NO: 25. В другом примере, антитело представляет собой полноразмерное IgG4 антитело, включающее вариабельную область легкой цепи, соответствующую SEQ ID NO: 14, 18 или 22, и тяжелую цепь, соответствующую SEQ ID NO: 26. В еще одном примере, антигенсвязывающий фрагмент представляет собой Fab', включающий вариабельную область легкой цепи, соответствующую SEQ ID NO: 13, 17 или 21, и вариабельную область тяжелой цепи, выбранную из SEQ ID NO: 25.
В одном предпочтительном варианте осуществления, антитело или его антигенсвязывающий фрагмент или фармацевтическая композиция, включающая антитело или его антигенсвязывающий фрагмент, для применения в терапии представляет собой антитело или его антигенсвязывающий фрагмент, включающие:
a. вариабельную область легкой цепи, включающую CDR-L1, соответствующий SEQ ID NO: 1; CDR-L2, соответствующий SEQ ID NO: 2, и CDR-L3, соответствующий SEQ ID NO: 3 или SEQ ID NO: 7; и вариабельная область тяжелой цепи, включающую CDR-H1, соответствующий SEQ ID NO: 4; CDR-H2, соответствующий SEQ ID NO: 5, и CDR-H3, соответствующий SEQ ID NO: 6; или
b. вариабельную область легкой цепи, соответствующую SEQ ID NO: 13 или SEQ ID NO: 17 или SEQ ID NO: 21, и вариабельную область тяжелой цепи, выбранную из SEQ ID NO: 25; или
c. легкую цепь, соответствующую SEQ ID NO: 14 или SEQ ID NO: 18 или SEQ ID NO: 22, и тяжелую цепь, соответствующую SEQ ID NO: 26;
где антитело или его антигенсвязывающий фрагмент связывается с альфа-синуклеином с эпитопом , включающим, по меньшей мере, остатки D119, N122 и Y125 в последовательности SEQ ID NO: 8.
Еще более предпочтительно, чтобы антитело или его антигенсвязывающий фрагмент не давали перекрестную реакцию с бета-синуклеином и связывали альфа-синуклеин при величине константы диссоциации (KD), по меньшей мере, в 10 раз выше для мономерного альфа-синуклеина по сравнению с альфа-синуклеина в фибриллах.
Биологические молекулы, такие как антитела или фрагменты, содержат кислотные и/или основные функциональные группы, в результате чего на молекуле возникает суммарный положительный или отрицательный заряд. Величина суммарного "регистрируемого" заряда будет зависеть от абсолютной аминокислотной последовательности молекулы, локального окружения заряженных групп в трехмерной структуре и окружающих молекулу условий. Изоэлектрическая точка (pI) представляет собой величину рН, при которой конкретная молекула или ее доступная для растворителя поверхность не несет суммарного электрического заряда. В одном примере, антитело против альфа-синуклеина или его антигенсвязывающий фрагмент по настоящему изобретению могут быть сконструированы таким образом, что они будет иметь соответствующую изоэлектрическую точку. Это позволяет создавать антитела и/или фрагменты с более стабильными свойствами, в частности, с подходящей растворимостью и/или профилем стабильности и/или улучшенными характеристиками очистки.
Соответственно, в одном аспекте, в изобретении предлагается гуманизированное антитело против альфа-синуклеина или его антигенсвязывающий фрагмент, сконструированные таким образом, что они имеют изоэлектрическую точку, отличающуюся от изоэлектрической точки первоначально идентифицированного антитела. Антитело может, например, быть сконструировано путем замены аминокислотного остатка, например, замены аминокислотного остатка с кислотными свойствами, на один или более аминокислотных остатков с основными свойствами. В качестве варианта, могут быть введены аминокислотные остатки с основными свойствами или могут быть удалены аминокислотные остатки с кислотными свойствами. В качестве варианта, если молекула имеет неприемлемо высокую величину рI, то, в случае необходимости, могут быть введены кислотные остатки с целью уменьшения величины рI. Важно, чтобы при манипуляции с величиной рI, уделялось особое внимание сохранению требуемой активности антитела или фрагмента. Таким образом, в одном варианте осуществления, сконструированное антитело или его антигенсвязывающий фрагмент обладает такой же или практически такой же активностью, что и "немодифицированное" антитело или фрагмент.
Для предсказания величины изоэлектрической точки антитела или фрагмента могут быть использованы программы, такие как ** ExPASY http://www.expasy.ch/tools/pi_tool.html и http://www.iut-arles.up.univ-mrs.fr/w3bb/d_abim/compo-p.html.
Следует иметь в виду, что аффинность предлагаемых в настоящем изобретении антител может быть изменена путем использования подходящего известного метода. Поэтому, настоящее изобретение также относится к вариантам молекул антител по настоящему изобретению, которые имеют улучшенную аффинность к альфа-синуклеину, в частности, к альфа-синуклеину человека. Такие варианты могут быть получены путем использования целого ряда протоколов "созревания аффинности", включающих мутирование гипервариабельных участков (CDR) (Yang et al., J. Mol. Biol., 254, 392-403, 1995), перестановку цепей (Marks et al., Bio/Technology, 10, 779-783, 1992), использование мутаторных штаммов E. coli (Low et al., J. Mol. Biol., 250, 359-368, 1996), перестановку ДНК (Patten et al., Curr. Opin. Biotechnol., 8, 724-733, 1997), фаговый дисплей (Thompson et al., J. Mol. Biol., 256, 77-88, 1996) и ПЦР с имитацией полового размножения (Crameri et al., Nature, 391, 288-291, 1998). В публикации Vaughan et al. (supra) обсуждаются эти методы "созревания аффинности".
При необходимости, антитело или его антигенсвязывающий фрагмент по настоящему изобретению может быть конъюгирован с одной или более эффекторной молекулой (молекулами). Следует иметь в виду, что эффекторная молекула может включать одиночную эффекторную молекулу или две или более таких молекул, связанных так, чтобы образовывать одиночный фрагмент, который может быть присоединен к антителам или их антигенсвязывающим фрагментом по настоящему изобретению. Когда требуется получить фрагмент антитела, связанного с эффекторной молекулой, он может быть приготовлен путем использования стандартных химических методик или методик рекомбинантной ДНК, в которых фрагмент антитела связывают либо непосредственно, либо через связывающий агент, с эффекторной молекулой. Методы конъюгирования таких эффекторных молекул с антителами хорошо известны (смотрите публикации Hellstrom et al., Controlled Drug Delivery, 2nd Ed., Robinson et al., eds., 1987, pp. 623-53; Thorpe et al., 1982, Immunol. Rev., 62:119-58 and Dubowchik et al., 1999, Pharmacology and Therapeutics, 83, 67-123). Конкретные химические методики включают, например, методики, описанные в патентных документах WO 93/06231, WO 92/22583, WO 89/00195, WO 89/01476 и WO 03/031581. В качестве варианта, когда эффекторная молекула представляет собой белок или полипептид, связывание может осуществлено путем использования методик рекомбинантной ДНК, например, описанных в патентных документах WO 86/01533 и EP0392745.
Используемый в изобретении термин "эффекторная молекула" включает, например, противоопухолевые средства, лекарственные средства, токсины, биологически активные белки, например, ферменты, другое антитело или фрагменты антител, синтетические или природные полимеры, нуклеиновые кислоты и их фрагменты, например, ДНК, РНК и их фрагменты, радионуклиды, конкретный радиойодид, радиоизотопы, хелаты металлов, наночастицы и репортерные группы, такие как флуоресцентные соединения или соединения, которые могут быть обнаружены методами ЯМР- или ЭПР-спектроскопии.
Примеры эффекторных молекул могут включать цитотоксины или цитотоксические средства, в том числе любое средство, которое является пагубным для клеток (например, приводит к гибели клеток). Примеры включают комбрестатины, доластатины, эпотилоны, стауроспорин, майтанзиноиды, спонгистатины, ризоксин, галихондрины, роридины, гемиастерлины, таксол, цитохалазин B, грамицидин D, этидия бромид, эметин, митомицин, этопозид, тенопозид, винкристин, винбластин, колхицин, доксорубицин, даунорубицин, дигидроксиантрациндион, митоксантрон, митрамицин, актиномицин D, 1-дегидротестостерон, глюкокортикоиды, прокаин, тетракаин, лидокаин, пропранолол и пуромицин и их аналоги или гомологи.
Эффекторные молекулы также включают, но этим не ограничивая, антиметаболиты (например, метотрексат, 6-меркаптопурин, 6-тиогуанин, цитарабин, 5-фторурацил, декарбазин), алкилирующие средства (например, мехлорэтамин, тиотепа, хлорамбуцил, мелфалан, кармустин (BSNU) и ломустин (CCNU), циклофосфамид, бусульфан, дибромманнит, стрептозотоцин, митомицин C и цис-дихлордиамин платины(II) (DDP) цисплатин), антрациклины (например, даунорубицин (раньше назывался дауномицином) и доксорубицин), антибиотики (например, дактиномицин (раньше назывался актиномицином), блеомицин, митрамицин, антрамицин (AMC), калихеамицины или дуокармицины) и антимитотические средства (например, винкристин и винбластин).
Другие эффекторные молекулы могут включать хелатированные радионуклиды, такие как 111In и 90Y, Lu177, висмут213, калифорний252, иридий192 и вольфрам188/рений188; или лекарственные средства, такие как, но этим не ограничивая, алкилфосфохолины, ингибиторы топоизомеразы I, таксоиды и сурамин.
Другие эффекторные молекулы включают белки, пептиды и ферменты. Представляющие интерес ферменты включают, но этим не ограничивая, протеолитические ферменты, гидролазы, лиазы, изомеразы, трансферазы. Представляющие интерес белки, полипептиды и пептиды включают, но этим не ограничивая, иммуноглобулины, токсины, такие как абрин, рицин A, экзотоксин синегнойной палочки или дифтерийный токсин, белок, такой как инсулин, фактор некроза опухолей, α-интерферон, β-интерферон, фактор роста нервов, тромбоцитарный фактор роста или тканевой активатор плазминогена, антитромботическое средство или антиангиогенное средство, например, ангиостатин или эндостатин, или модификатор биологического отклика, такой как лимфокин, интерлейкин-1 (IL-1), интерлейкин-2 (IL-2), гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF), колониестимулирующий фактор гранулоцитов (G-CSF), фактор роста нервов (NGF) или другие фактор роста и иммуноглобулины.
Другие эффекторные молекулы могут включать обнаруживаемые вещества, применяемые, например, при диагностировании. Примеры обнаруживаемых веществ включают различные ферменты, простетические группы, флуоресцентные материалы, люминесцентные материалы, биолюминесцентные материалы, радиоактивные нуклиды, позитронно-активные металлы (для использования в позитронной эмиссионной томографии) и ионы нерадиоактивных парамагнитных металлов. Смотрите в общих чертах патентный документ U.S. Patent No. 4741900 для ионов металлов, которые могут быть конъюгированы с антителами с целью применения в качестве диагностических средств. Подходящие ферменты включают пероксидазу из хрена, щелочную фосфатазу, бета-галактозидазу или ацетилхолинэстеразу; подходящие простетические группы включают стрептавидин, авидин и биотин; подходящие флуоресцентные материалы включают умбеллиферон, флуоресцеин, флуоресцеинизотиоцианат, родамин, дихлортриазиниламин флуоресцина, дансилхлорид и фикоэритрин; подходящие люминесцентные материалы включают люминол; подходящие биолюминесцентные материалы включают люциферазу, люциферин и экворин; и подходящие радиоактивные нуклиды включают 125I, 131I, 111In и 99Tc.
В другом примере, эффекторная молекула может увеличивать период полувыведения антитело in vivo и/или снижать иммуногенность антитела и/или интенсифицировать доставку антитела через эпителиальный барьер в иммунную систему. Примеры подходящих эффекторных молекул этого типа включают полимеры, альбумин, альбумин-связывающие белки или альбумин-связывающие соединения, такие как соединения, описанные в патентном документе WO05/117984.
Если эффекторная молекула является полимером, этот полимер может быть, в большинстве случаев, синтетическим или природным полимером, например, необязательно замещенным линейным или разветвленным полиалкиленовым, полиалкениленовым или полиоксиалкиленовым полимером или разветвленным или неразветвленным полисахаридом, например, гомо- или гетеро- полисахаридом.
Конкретные необязательные заместители, которые могут присутствовать на упомянутых выше синтетических полимерах, включают одну или более гидроксильных, метильных или метоксильных групп.
Конкретные примеры синтетических полимеров включают необязательно замещенный линейный или разветвленный полиэтиленгликоль, полипропиленгликоль, поливиниловый спирт или их производные, в частности, необязательно замещенный полиэтиленгликоль, такой как метоксиполиэтиленгликоль или его производные.
Конкретные природные полимеры включают лактозу, амилозу, декстран, гликоген или их производные.
В одном варианте осуществления, полимер представляет собор альбумин или его фрагмент, такой как сывороточный альбумин человека или его фрагмент.
Предполагается, что используемый в изобретении термин "производные" включает реакционно-способные производные, например, тиол-селективные реакционно-способные группы, такие как малеимиды и другие подобные. Реакционно-способная группа может быть связана непосредственно или через линкерный сегмент с полимером. Следует иметь в виду, что остаток такой группы будет в некоторых случаях формировать часть продукта в форме связывающей группы между фрагментом антитела и полимером.
По желанию, размер полимера может быть изменен, но, как правило, он находится в диапазоне средних молекулярных масс от 500 Да до 50000 Да, например, от 5000 до 40000 Да, например, от 20000 до 40000 Да. Размер полимера может быть, в частности, выбран исходя из предполагаемого применения продукта, например, исходя из способности локализоваться на конкретных тканях, таких как опухоли, или исходя из способности увеличивать период полувыведения из кровотока (более подробная информация приведена в публикации Chapman, 2002, Advanced Drug Delivery Reviews, 54, 531-545). Так, например, если предполагается выведение продукта из кровотока с целью его проникновения в ткань, например, для использования при лечении опухоли, то будет предпочтительным использовать полимер с небольшой молекулярной массой, например, с молекулярной массой приблизительно 5000 Да. В случаях применения, когда продукт остается в кровотоке, может быть предпочтительным использовать полимер с более высокой молекулярной массой, например, с молекулярной массой в диапазоне от 20000 Да до 40000 Да.
Подходящие полимеры включают полиалкиленовый полимер, такой как полиэтиленгликоль или, в частности, метоксиполиэтиленгликоль или его производное, и, в частности, с молекулярной массой в диапазоне от приблизительно 15000 Да до приблизительно 40000 Да.
В одном примере, антитела для применения в настоящем изобретении присоединяют к фрагментам полиэтиленгликоля (PEG). В одном конкретном примере, антитело представляет собой фрагмент антитела, и молекулы PEG могут быть присоединены через любую доступную функциональную группу аминокислоты боковой цепи или концевой аминокислоты, расположенной в фрагменте антитела, например, через любую свободную аминогруппу, иминогруппу, тиольную группу, гидроксильную группу или карбоксильную группу. Такие аминокислоты в фрагменте антитела могут иметь природное происхождение, или они могут быть сконструированы в фрагменте путем использования методов рекомбинантной ДНК (смотрите, например, патентные документы US 5219996; US 5667425; WO98/25971, WO2008/038024). В одном примере, молекула антитела по настоящему изобретению представляет собой модифицированный фрагмент Fab, где модификация заключается в добавлении к C-терминальному концу тяжелой цепи фрагмента одной или более аминокислот для обеспечения возможности присоединения эффекторной молекулы. Соответственно, добавленные аминокислоты образуют модифицированную шарнирную область, содержащую один или более остатков цистеина, к которым эффекторная молекула может быть присоединена. Для присоединения двух или более молекул PEG могут быть использованы несколько сайтов.
Соответственно, молекулы PEG ковалентно связывают через тиольную группу, по меньшей мере, одного остатка цистеина, расположенного в фрагменте антитела. Каждая молекула полимера, присоединенная к модифицированному фрагменту антитела, может быть ковалентно связана с атомом серы остатка цистеина, расположенного в фрагменте. Ковалентное связывание, как правило, будет представлять собой дисульфидную связь или, в частности, связь сера-углерод. В случае, когда в качестве точки присоединения соответствующим образом активированных эффекторных молекул используют тиольную группу, могут быть использованы, например, тиол-селективные производные, такие как малеимиды и производные цистеина. При приготовлении описанных выше полимер-модифицированных фрагментов антител, в качестве исходного материала может быть использован активированный полимер. Активированный полимер может представлять собой любой полимер, содержащий реакционноспособную тиольную группу, такую как α-галогенкарбоновая кислота или эфир, например, иодоацетамид, имид, например, малеимид, винилсульфон или дисульфид. Такие исходные материалы производятся промышленностью (например, фирмой Nektar, ранее называвшейся Shearwater Polymers Inc., Huntsville, AL, USA) или они могут быть приготовлены из выпускаемых промышленностью исходных материалов, используя стандартные химические методики. Конкретные молекулы PEG включают 20K метокси-PEG-амин (выпускаемый фирмой Nektar, ранее называвшейся Shearwater; фирмой Rapp Polymere и фирмой SunBio) и M-PEG-SPA (выпускаемый фирмой Nektar, ранее называвшейся Shearwater).
В одном варианте осуществления, антитело представляет собой модифицированный фрагмент Fab, фрагмент Fab' или diFab, который является пегилированным, то есть, содержит ковалентно присоединенный к нему PEG (полиэтиленгликоль), например, путем использования метода, раскрытого в патентных документах EP 0948544 или EP1090037 [смотрите также публикации "Poly(ethyleneglycol) Chemistry, Biotechnical and Biomedical Applications", 1992, J. Milton Harris (ed), Plenum Press, New York, "Poly(ethyleneglycol) Chemistry and Biological Applications", 1997, J. Milton Harris and S. Zalipsky (eds), American Chemical Society, Washington DC and "Bioconjugation Protein Coupling Techniques for the Biomedical Sciences", 1998, M. Aslam and A. Dent, Grove Publishers, New York; Chapman, A. 2002, Advanced Drug Delivery Reviews 2002, 54:531-545]. В одном примере, PEG присоединен к цистеину в шарнирной области. В одном примере, PEG-модифицированный фрагмент Fab имеет малеимидную группу, ковалентно связанную с одной тиольной группой в модифицированной шарнирной области. Остаток лизина может быть ковалентно связан с малеимидной группой, и к каждой из аминогрупп на остатке лизина может быть присоединен полимер метоксиполиэтиленгликоль, имеющий молекулярную массу приблизительно 20000 Да. Суммарная молекулярная масса PEG, присоединенного к фрагменту Fab, может, поэтому, составлять приблизительно 40000 Да.
Конкретные молекулы PEG включают 2-[3-(N-малеимидо)пропионамидо]этиламид N, N'-бисметоксиполиэтиленгликоль (MW 20000) модифицированный лизин, также известный как PEG2MAL40K (выпускаемый фирмой Nektar, ранее называвшейся Shearwater).
Альтернативные производители PEG линкеров включают фирму NOF, которая поставляют их под маркой GL2-400MA3 (где m в изображенной ниже структуре равно 5) и под маркой GL2-400MA (где m равно 2) и n равно приблизительно 450:
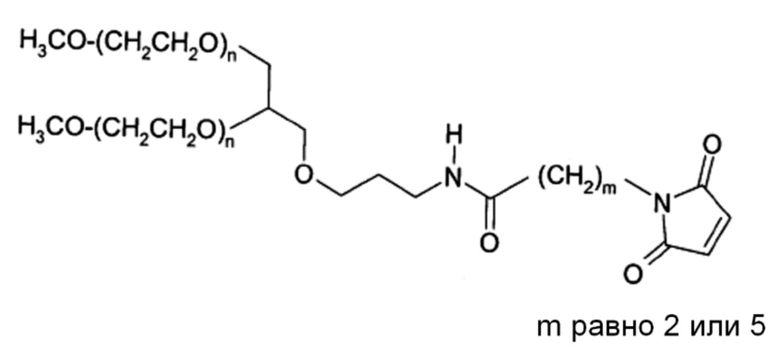 .
.
То есть молекулярная масса каждого PEG составляет приблизительно 20000 Да.
Так, в одном варианте осуществления, PEG представляет собой 2,3-бис(метилполиоксиэтилен-окси)-1-{[3-(6-малеимидо-1-оксо-гексил)амино]пропилокси}гексан (ПЭГ с двумя ветвями, -CH2)3NHCO(CH2)5-MAL, Mw 40000, известный как SUNBRIGHT GL2-400MA3.
Кроме того, альтернативные эффекторные молекулы PEG следующего типа
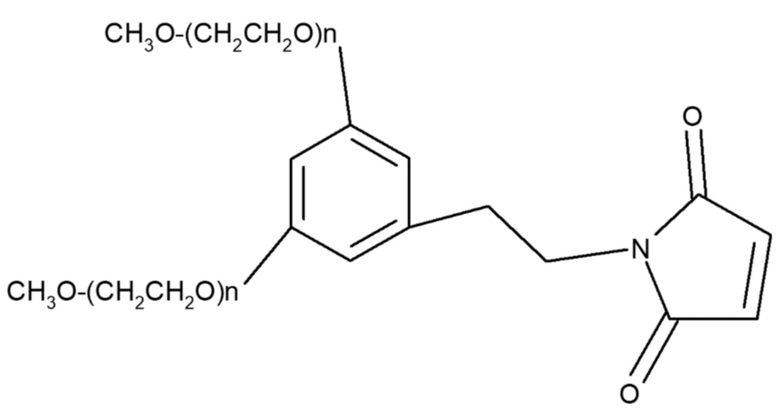
выпускаются фирмами Dr Reddy, NOF и Jenkem.
В одном варианте осуществления, Fab или Fab' по настоящему изобретению конъюгирован с молекулой PEG.
В одном варианте осуществления, предлагается антитело, которое подвергнуто пегилированию (например, с помощью описанного в изобретении PEG), присоединено через аминокислотный остаток цистеина на аминокислоте 226 в цепи или рядом, например, на аминокислоте 226 тяжелой цепи (обозначенной с использованием последовательной нумерации), например, на аминокислоте 224 последовательности SEQ ID NO:26.
В одном варианте осуществления, в настоящем изобретении предлагается молекула Fab'PEG, включающая один или более полимеров PEG, например, 1 или 2 полимера, таких как полимер или полимеры с молекулярной массой 40 кДа.
Молекулы Fab'-PEG по настоящему изобретению могут особенно предпочтительными в том случае, если они имеют период полувыведения, независимый от фрагмента Fc. В одном варианте осуществления, предлагается Fab', конъюгированный с полимером, таким как молекула PEG, молекула крахмала или молекула альбумина. В одном варианте осуществления, предлагается scFv, конъюгированный с полимером, таким как молекула PEG, молекула крахмала или молекула альбумина. В одном варианте осуществления, Fab или Fab' по настоящему изобретению конъюгируют с сывороточным альбумином человека. В одном варианте осуществления, антитело или фрагмент конъюгируют с молекулой крахмала, например, для увеличения периода полувыведения. Методы конъюгирования крахмала с белком описаны в патентном документе US 8017739, содержание которого включено в настоящее изобретение путем ссылки на него.
В настоящем изобретении также предлагается выделенный полинуклеотид, кодирующий антитело или его антигенсвязывающий фрагмент по настоящему изобретению. Выделенный полинуклеотид по настоящему изобретению может включать синтетическую ДНК, например, продуцированную путем химической обработки, кДНК, геномную ДНК или любую их комбинацию.
Для приготовления последовательностей ДНК, кодирующих антитело или его антигенсвязывающий фрагмент по настоящему изобретению могут быть использованы стандартные методы молекулярной биологии. Требуемые последовательности ДНК могут быть синтезированы полностью или частично, используя методы синтез олигонуклеотидов. В соответствующих случаях, могут быть использованы методы сайтнаправленного мутагенеза и полимеразной цепной реакции (PCR).
В одном варианте осуществления, выделенный полинуклеотид по изобретению кодирует:
a. вариабельную область легкой цепи, где полинуклеотид:
i. по меньшей мере, на 90% идентичен последовательности SEQ ID NO: 15 или SEQ ID NO: 19 или SEQ ID NO: 23; или
ii. включает SEQ ID NO: 15 или SEQ ID NO: 19 или SEQ ID NO: 23; или
iii. состоит в основном из SEQ ID NO: 15 или SEQ ID NO: 19 или SEQ ID NO: 23;
b. вариабельную область тяжелой цепи, где полинуклеотид:
i. по меньшей мере, на 90% идентичен последовательности SEQ ID NO: 27; или
ii. включает SEQ ID NO: 27; или
iii. состоит в основном из SEQ ID NO: 27;
c. легкую цепь, где полинуклеотид:
i. по меньшей мере, на 90% идентичен последовательности SEQ ID NO: 16 или SEQ ID NO: 20 или SEQ ID NO: 24; или
ii. включает SEQ ID NO: 16 или SEQ ID NO: 20 или SEQ ID NO: 24; или
iii. состоит в основном из SEQ ID NO: 16 или SEQ ID NO: 20 или SEQ ID NO: 24;
d. тяжелую цепь, где полинуклеотид:
i. по меньшей мере, на 90% идентичен последовательности SEQ ID NO: 28; или
ii. включает SEQ ID NO: 28; или
iii. состоит в основном из SEQ ID NO: 28.
В настоящем изобретении также предлагается клонирующий или экспрессирующий вектор, включающий один или более описанных в изобретении полинуклеотидов. В одном примере, клонирующий или экспрессирующий вектор по настоящему изобретению включает один или более выделенных полинуклеотидов, включающих последовательность, выбранную из SEQ ID NO: 15, 16, 19, 20, 23, 24, 27 или 28.
Общие методы, с помощью которых могут быть сконструированы векторы, методы трансфекции и методы культивирования хорошо известны специалистам в этой области. Подробная информация по этим методам приводится в руководствах “Current Protocols in Molecular Biology”, 1999, F. M. Ausubel (ed), Wiley Interscience, New York and the Maniatis Manual produced by Cold Spring Harbor Publishing.
Кроме того, предлагается клетка-хозяина, включающая один или более выделенных полинуклеотидных последовательностей по изобретению, или один или более клонирующих или экспрессирующих векторов, включающих одну или более выделенных полинуклеотидных последовательностей, кодирующих антитело по настоящему изобретению. Любая подходящая клетка-хозяина/ векторная система может быть использована для экспрессии полинуклеотидных последовательностей, кодирующих антитело или его антигенсвязывающий фрагмент по настоящему изобретению. Могут быть использованы бактериальные, например, E. coli, и другие системы микроорганизмов, или могут быть также использованы экспрессирующие системы на основе эукариотических клеток-хозяина, например, клеток-хозяина млекопитающего. Подходящие клетки-хозяина млекопитающего включают клетки яичника китайского хомячка (CHO), клетки миеломы или гибридомные клетки.
Подходящие типы клеток яичника китайского хомячка (клетки CHO) для применения в настоящем изобретении могут включать клетки CHO и CHO-K1, в том числе клетки dhfr-CHO, такие как клетки CHO-DG44 и клетки CHO-DXB11, которые могут быть использованы с селектируемым маркером DHFR, или клетки CHOK1-SV, которые могут быть использованы с селектируемым маркером глутаминсинтетазы. Другие типы клеток, используемые при экспрессии антител, включают линии лимфоцитарных клеток, например, клетки миеломы NSO и клетки SP2, клетки COS. Клетка-хозяина может быть стабильно трансформирована или трансфицирована с помощью выделенных полинуклеотидных последовательностей или экспрессирующих векторов по настоящему изобретению.
В одном варианте осуществления, клетка-хозяина по настоящему изобретению представляет собой клетку CHO-DG44, стабильно трансфицированную с помощью экспрессирующего вектора, включающего выделенные полинуклеотидные последовательности по настоящему изобретению, предпочтительно, включающего выделенные полинуклеотидные последовательности, соответствующие SEQ ID NO: 15 и 27, или SEQ ID NO: 19 и 27, или SEQ ID NO: 23 и 27, или SEQ ID NO: 16 и 28, или SEQ ID NO: 20 и 28, или SEQ ID NO: 24 и 28.
В настоящем изобретении также предлагается способ продуцирования антитела или его антигенсвязывающего фрагмента по настоящему изобретению, включающий культивирование клетки-хозяина по настоящему изобретению в условиях, подходящих для продуцирования антитела или его антигенсвязывающего фрагмента по изобретению, и выделение антитела или его антигенсвязывающего фрагмента.
Антитело или его антигенсвязывающий фрагмент может включать только тяжелую или легкую полипептидную цепь, и в этом случае требуется только кодирующая последовательность тяжелой или легкой полипептидной цепи для трансфицирования клеток-хозяина. Для продуцирования антител или их антигенсвязывающих фрагментов, включающих как тяжелые цепи, так и легкие цепи, линия клеток может быть трансфицирована с помощью двух векторов, при этом первый вектор кодирует легкую полипептидную цепь, а второй вектор кодирует тяжелую полипептидную цепь. В качестве варианты, может быть использован только один вектор, который включает последовательности, кодирующие легкие и тяжелые полипептидные цепи.
Так, предлагается способ культивирования клетки-хозяина и экспрессирования антитела или его фрагмента, выделение антитела или его фрагмента и необязательно их очистки с получением выделенного антитела или фрагмента. В одном варианте осуществления, способ дополнительно включает стадию конъюгирования эффекторной молекулы с выделенным антителом или фрагментом, например, конъюгирование с полимером PEG, в частности, как это описано в изобретении.
Так, в одном варианте осуществления, предлагается очищенное антитело против альфа-синуклеина или его фрагмент, например, гуманизированное антитело или его фрагмент, в частности, антитело или его фрагмент по изобретению, в практически очищенной форме, в частности, не содержащей или практически несодержащей эндотоксина и/или белка клетки-хозяина или ДНК.
Как правило, предполагается, что выражение "практически несодержащий эндотоксина" относится к содержанию эндотоксина, составляющему 1 эндотоксиновую единицу в 1 миллиграмме полученного антитела или менее, например, 0,5 или 0,1 эндотоксиновой единицы в 1 миллиграмме продукта. Как правило, предполагается, что выражение "практически несодержащий белка клетки-хозяина или ДНК" относится к содержанию белка клетки-хозяина или ДНК, составляющему, в соответствующих случаях, 400 мкг в 1 миллиграмме полученного антитела или менее, например, 100 мкг в 1 миллиграмме или менее, в частности, 20 мкг в 1 миллиграмме.
Так как антитела по настоящему изобретению применяются при лечении, диагностике и/или профилактике патологического состояния, такого как альфа-синуклеинoпатия, в настоящем изобретении также предлагается фармацевтическая или диагностическая композиция, включающая антитело или его антигенсвязывающий фрагмент по настоящему изобретению в комбинации с одним или более из фармацевтически приемлемого носителя, вспомогательного вещества или разбавителя. В одном варианте осуществления, антитело или его антигенсвязывающий фрагмент по настоящему изобретению являются единственным активным ингредиентом. В другом варианте осуществления, антитело или его антигенсвязывающий фрагмент по настоящему изобретению присутствует в комбинации с одним или более дополнительными активными ингредиентами. В качестве варианта, фармацевтические композиции включают антитело или его антигенсвязывающий фрагмент по настоящему изобретению, которые являются единственным активным ингредиентом, и он может быть введен индивидуально пациенту в комбинации (например, одновременно, последовательно или раздельно) с другими средствами, лекарственными средствами или гормонами.
В другом варианте осуществления, фармацевтическая композиция включает антитело или его антигенсвязывающий фрагмент, содержащие вариабельную область легкой цепи последовательности SEQ ID NO: 13 или 17 или 21, и содержащие вариабельную область тяжелой цепи последовательности SEQ ID NO: 25, например, SEQ ID NO: 13 и SEQ ID NO: 25, или SEQ ID NO: 17 и SEQ ID NO: 25, или SEQ ID NO: 21 и SEQ ID NO: 25.
Фармацевтические композиции по изобретению могут быть введены соответствующим образом пациенту для определения требуемого терапевтически эффективного количества. Используемый в изобретении термин "терапевтически эффективное количество" относится к количеству терапевтического средства, необходимому для лечения, облегчения или предотвращения конкретного заболевания или состояния, или для проявления поддающегося обнаружению терапевтического или профилактического эффекта. Для любого антитела, терапевтически эффективное количество может быть оценено на начальном этапе путем проведения исследований либо на культуре клеток, либо на экспериментальных моделях на животных, обычно на грызунах, кроликах, собаках, свиньях или приматах. Экспериментальная модель на животном может также использоваться для определения соответствующего диапазона концентраций и способа введения. Такая информация затем может быть использована для определения подходящих доз и способов введения в случае людей.
Точное терапевтически эффективное количество для человека будет зависеть от тяжести болезненного состояния, общего состояния здоровья субъекта, возраста, массы тела и пола субъекта, режима питания, времени и частоты введения, комбинации (комбинаций) лекарственных средств, чувствительности реакции на лекарственный препарат и толерантности/ответа на проводимую терапию. Это количество может быть определено путем проведения обычных экспериментов, и оно определяется лечащим врачом. Обычно, терапевтически эффективное количество будет составлять от 0,01 мг/кг до 500 мг/кг, например, от 0,1 мг/кг до 200 мг/кг, например, 100 мг/кг. Фармацевтические композиции удобно приготавливать в лекарственных формах с разовой дозой, содержащих заданное количество активного средства по изобретению в разовой дозе.
Фармацевтически приемлемые носители в терапевтических композициях могут дополнительно содержать жидкости, такие как вода, физиологический раствор, глицерин и этанол. Кроме того, в таких композициях могут присутствовать вспомогательные вещества, такие смачивающие средства или эмульгаторы, или буферные вещества для поддержания требуемой величины pH. Такие носители позволяют приготавливать фармацевтические композиции в форме таблеток, пилюль, драже, капсул, жидкостей, гелей, сиропов, пастообразной смеси и суспензий для проглатывания пациентом.
Подходящие формы для введения включают формы, подходящие для парентерального введения, например, путем инъекции или инфузии, например, путем болюсной инъекции или непрерывной инфузии, во внутривенной, ингаляционной или подкожной форме. Когда продукт предназначен для инъекции или инфузии, он может быть приготовлен в форме суспензии, раствора или эмульсии в масляной или водной среде, и он может содержать вспомогательные вещества, такие как суспендирующие средства, консерванты, стабилизаторы и/или диспергирующие средства. В качестве варианта, антитело или его антигенсвязывающий фрагмент по изобретению может быть приготовлено в сухой форме для растворения перед использованием в соответствующей стерильной жидкости. Могут быть также приготовлены твердые формы, подходящие для растворения или суспендирования в жидких средах перед инъекцией.
После приготовления, композиции по изобретению могут быть введены непосредственно субъекту. Соответственно, в изобретении предлагается применение антитела или его антигенсвязывающего фрагмента по изобретению для производства лекарственного препарата.
Субъектами, подвергаемыми лечению, могут быть животные. Предпочтительно, чтобы фармацевтические композиции по настоящему изобретению были адаптированы для введения людям.
В связи с этим, в другом аспекте, в настоящем изобретении предлагается антитело или его антигенсвязывающий фрагмент или фармацевтическая композиция, включающая антитело или его антигенсвязывающий фрагмент, для применения в терапии, и, в частности, для применения при лечении одной или более альфа синуклеинoпатий. В еще одном аспекте, в настоящем изобретении предлагается способ лечения одной или более синуклеинoпатий у пациента, включающий введение указанному пациенту терапевтически эффективного количества антитела или его антигенсвязывающего фрагмента по настоящему изобретению или фармацевтической композиции, включающей антитело или его антигенсвязывающий фрагмент.
В одном варианте осуществления, антитело или его антигенсвязывающий фрагмент или фармацевтическая композиция, включающая антитело или его антигенсвязывающий фрагмент, для применения в терапии представляет собой антитело или его антигенсвязывающий фрагмент, включающие:
a. вариабельную область легкой цепи, включающую CDR-L1, соответствующий SEQ ID NO: 1; CDR-L2, соответствующий SEQ ID NO: 2, и CDR-L3, соответствующий SEQ ID NO: 3 или SEQ ID NO: 7; и вариабельную область тяжелой цепи, включающую CDR-H1, соответствующий SEQ ID NO: 4; CDR-H2, соответствующий SEQ ID NO: 5, и CDR-H3, соответствующий SEQ ID NO: 6; или
b. вариабельную область легкой цепи, соответствующую SEQ ID NO: 13 или SEQ ID NO: 17 или SEQ ID NO: 21, и вариабельную область легкой цепи, выбранную из SEQ ID NO: 25; или
c. легкую цепь, соответствующую SEQ ID NO: 14 или SEQ ID NO: 18 или SEQ ID NO: 22, и тяжелую цепь, соответствующую SEQ ID NO: 26;
где антитело или его антигенсвязывающий фрагмент является гуманизированным и предотвращает агрегацию альфа-синуклеина, индуцированную фибриллами альфа-синуклеина, где антитело или его антигенсвязывающий фрагмент связывает альфа-синуклеин с эпитопом, включающим, по меньшей мере остатки D119, N122 и Y125 последовательности SEQ ID NO: 8, и где антитело или его антигенсвязывающий фрагмент предназначен для применения в терапии. Предпочтительно, чтобы антитело или его антигенсвязывающий фрагмент не давали перекрестную реакцию с бета-синуклеином и связывали альфа-синуклеин с величиной константы диссоциации (KD), по меньшей мере, в 10 раз более высокой для мономерного альфа-синуклеина, чем для альфа-синуклеина в фибриллах.
В другом варианте осуществления, антитело или его антигенсвязывающий фрагмент или фармацевтическая композиция, включающая антитело или его антигенсвязывающий фрагмент, предназначена для применения при лечении одной или более синуклеинoпатий, где антитело или его антигенсвязывающий фрагмент включают:
a. вариабельную область легкой цепи, включающую CDR-L1, соответствующий SEQ ID NO: 1; CDR-L2, соответствующий SEQ ID NO: 2, и CDR-L3, соответствующий SEQ ID NO: 3 или SEQ ID NO: 7; и вариабельную область тяжелой цепи, включающую CDR-H1, соответствующий SEQ ID NO: 4; CDR-H2, соответствующий SEQ ID NO: 5, и CDR-H3, соответствующий SEQ ID NO: 6; или
b. вариабельную область легкой цепи, соответствующую SEQ ID NO: 13 или SEQ ID NO: 17 или SEQ ID NO: 21, вариабельную область тяжелой цепи, выбранную из SEQ ID NO: 25; или
c. легкую цепь, соответствующую SEQ ID NO: 14 или SEQ ID NO: 18 или SEQ ID NO: 22, и тяжелую цепь, соответствующую SEQ ID NO: 26;
где антитело или его антигенсвязывающий фрагмент является гуманизированным и предотвращает агрегацию альфа-синуклеина, индуцированную фибриллами альфа-синуклеина, где антитело или его антигенсвязывающий фрагмент связывает альфа-синуклеин с эпитопом, включающим, по меньшей мере остатки D119, N122 и Y125 последовательности SEQ ID NO: 8. Предпочтительно, чтобы антитело или его антигенсвязывающий фрагмент не давали перекрестную реакцию с бета-синуклеином и связывали альфа-синуклеин с величиной константы диссоциации (KD), по меньшей мере, в 10 раз более высокой для мономерного альфа-синуклеина, чем для альфа-синуклеина в фибриллах.
В другом варианте осуществления, предлагается способ лечения одной или более синуклеинoпатий у пациента, включающий введение указанному пациенту терапевтически эффективного количества антитела или его антигенсвязывающего фрагмента или фармацевтической композиции, включающей антитело или его антигенсвязывающий фрагмент, где антитело или его антигенсвязывающий фрагмент включает:
a. вариабельную область легкой цепи, включающую CDR-L1, соответствующий SEQ ID NO: 1; CDR-L2, соответствующий SEQ ID NO: 2, и CDR-L3, соответствующий SEQ ID NO: 3 или SEQ ID NO: 7; и вариабельную область тяжелой цепи, включающую CDR-H1, соответствующий SEQ ID NO: 4; CDR-H2, соответствующий SEQ ID NO: 5, и CDR-H3, соответствующий SEQ ID NO: 6; или
b. вариабельную область легкой цепи, соответствующую SEQ ID NO: 13 или SEQ ID NO: 17 или SEQ ID NO: 21, вариабельную область тяжелой цепи, выбранную из SEQ ID NO: 25; или
c. легкую цепь, соответствующую SEQ ID NO: 14 или SEQ ID NO: 18 или SEQ ID NO: 22, и тяжелую цепь, соответствующую SEQ ID NO: 26;
где антитело или его антигенсвязывающий фрагмент является гуманизированным и предотвращает агрегацию альфа-синуклеина, индуцированную фибриллами альфа-синуклеина, где антитело или его антигенсвязывающий фрагмент связывает альфа-синуклеин с эпитопом, включающим, по меньшей мере остатки D119, N122 и Y125 последовательности SEQ ID NO: 8. Предпочтительно, чтобы антитело или его антигенсвязывающий фрагмент не давали перекрестную реакцию с бета-синуклеином и связывали альфа-синуклеин с величиной константы диссоциации (KD), по меньшей мере, в 10 раз более высокой для мономерного альфа-синуклеина, чем для альфа-синуклеина в фибриллах.
Альфа-синуклеинoпатии по настоящему изобретению включают, но этим не ограничивая, болезнь Паркинсона (PD) (в том числе идиопатические и наследственные формы болезни Паркинсона), деменцию с тельцами Леви (DLB), болезнь диффузных телец Леви (DLBD), вариант болезни Альцгеймера с тельцами Леви (LBVAD), смешанный тип болезни Альцгеймера и Паркинсона, множественную системную атрофию (MSA) и нейродегенерацию с накоплением железа в головном мозге типа 1 (NBIA-1). Предпочтительно, чтобы альфа-синуклеинoпатия представляла собой болезнь Паркинсона (PD).
В другом варианте осуществления, антитело или его антигенсвязывающий фрагмент или фармацевтическая композиция, включающая антитело или его антигенсвязывающий фрагмент, предназначены для применения при лечении болезни Паркинсона (PD) (в том числе идиопатических и наследственных форм болезни Паркинсона), деменции с тельцами Леви (DLB), болезни диффузных телец Леви (DLBD), варианта болезни Альцгеймера с тельцами Леви (LBVAD), смешанного типа болезни Альцгеймера и Паркинсона, множественной системной атрофии (MSA) и нейродегенерация с накоплением железа в головном мозге типа 1 (NBIA-1), предпочтительно, болезни Паркинсона (PD), где антитело или его антигенсвязывающий фрагмент включает:
a. вариабельную область легкой цепи, включающую CDR-L1, соответствующий SEQ ID NO: 1; CDR-L2, соответствующий SEQ ID NO: 2, и CDR-L3, соответствующий SEQ ID NO: 3 или SEQ ID NO: 7; и вариабельную область тяжелой цепи, включающую CDR-H1, соответствующий SEQ ID NO: 4; CDR-H2, соответствующий SEQ ID NO: 5, и CDR-H3, соответствующий SEQ ID NO: 6; или
b. вариабельную область легкой цепи, включающую SEQ ID NO: 13 или SEQ ID NO: 17 или SEQ ID NO: 21, и вариабельную область тяжелой цепи, выбранную из SEQ ID NO: 25; или
c. легкую цепь, соответствующую SEQ ID NO: 14 или SEQ ID NO: 18 или SEQ ID NO: 22, и тяжелую цепь, соответствующую SEQ ID NO: 26;
где антитело или его антигенсвязывающий фрагмент является гуманизированным и предотвращает агрегацию альфа-синуклеина, индуцированную фибриллами альфа-синуклеина, где, необязательно, антитело или его антигенсвязывающий фрагмент связывает альфа-синуклеин с эпитопом, включающим, по меньшей мере остатки D119, N122 и Y125 последовательности SEQ ID NO: 8, и где антитело или его антигенсвязывающий фрагмент предназначены для применения в терапии. Предпочтительно, чтобы антитело или его антигенсвязывающий фрагмент не давали перекрестную реакцию с бета-синуклеином и связывали альфа-синуклеин с величиной константы диссоциации (KD), по меньшей мере, в 10 раз более высокой для мономерного альфа-синуклеина, чем для альфа-синуклеина в фибриллах.
В другом варианте осуществления, предлагается способ лечения болезни Паркинсона (PD) (в том числе идиопатических и наследственных форм болезни Паркинсона), деменции с тельцами Леви (DLB), болезни диффузных телец Леви (DLBD), варианта болезни Альцгеймера с тельцами Леви (LBVAD), смешанного типа болезни Альцгеймера и Паркинсона, множественной системной атрофии (MSA) и нейродегенерации с накоплением железа в головном мозге типа 1 (NBIA-1), предпочтительно, болезни Паркинсона (PD), у пациента, включающий введение указанному пациенту терапевтически эффективного количества антитела или его антигенсвязывающего фрагмента или фармацевтической композиции, включающей антитело или его антигенсвязывающий фрагмент, где антитело или его антигенсвязывающий фрагмент включает:
a. вариабельную область легкой цепи, включающую CDR-L1, соответствующий SEQ ID NO: 1; CDR-L2, соответствующий SEQ ID NO: 2, и CDR-L3, соответствующий SEQ ID NO: 3 или SEQ ID NO: 7; и вариабельную область тяжелой цепи, включающую CDR-H1, соответствующий SEQ ID NO: 4; CDR-H2, соответствующий SEQ ID NO: 5, и CDR-H3, соответствующий SEQ ID NO: 6; или
b. вариабельную область легкой цепи, соответствующую SEQ ID NO: 13 или SEQ ID NO: 17 или SEQ ID NO: 21, и вариабельную область тяжелой цепи, выбранную из SEQ ID NO: 25; или
c. легкую цепь, соответствующую SEQ ID NO: 14 или SEQ ID NO: 18 или SEQ ID NO: 22, и тяжелую цепь, соответствующую SEQ ID NO: 26;
где антитело или его антигенсвязывающий фрагмент является гуманизированным и предотвращает агрегацию альфа-синуклеина, индуцированную фибриллами альфа-синуклеина, где, необязательно, антитело или его антигенсвязывающий фрагмент связывает альфа-синуклеин с эпитопом, включающим, по меньшей мере остатки D119, N122 и Y125 последовательности SEQ ID NO: 8, и где антитело или его антигенсвязывающий фрагмент предназначены для применения в терапии. Предпочтительно, чтобы антитело или его антигенсвязывающий фрагмент не давали перекрестную реакцию с бета-синуклеином и связывали альфа-синуклеин с величиной константы диссоциации (KD), по меньшей мере, в 10 раз более высокой для мономерного альфа-синуклеина, чем для альфа-синуклеина в фибриллах.
В качестве варианта, В изобретении также предлагается применение антитела или его антигенсвязывающего фрагмента для производства лекарственного препарата для лечения альфа-синуклеинoпатии, где альфа-синуклеинoпатия представляет собой, предпочтительно, болезнь Паркинсона (PD) (в том числе идиопатические и наследственные формы болезни Паркинсона), деменцию с тельцами Леви (DLB), болезнь диффузных телец Леви (DLBD), вариант болезни Альцгеймера с тельцами Леви (LBVAD), смешанный тип болезни Альцгеймера и Паркинсона, множественную системную атрофию (MSA) и нейродегенерацию с накоплением железа в головном мозге типа 1 (NBIA-1), более предпочтительно, болезнь Паркинсона (PD), где антитело или его антигенсвязывающий фрагмент включает:
a. вариабельную область легкой цепи, включающую CDR-L1, соответствующий SEQ ID NO: 1; CDR-L2, соответствующий SEQ ID NO: 2, и CDR-L3, соответствующий SEQ ID NO: 3 или SEQ ID NO: 7; и вариабельную область тяжелой цепи, включающую CDR-H1, соответствующий SEQ ID NO: 4; CDR-H2, соответствующий SEQ ID NO: 5, и CDR-H3, соответствующий SEQ ID NO: 6; или
b. вариабельную область легкой цепи, соответствующую SEQ ID NO: 13 или SEQ ID NO: 17 или SEQ ID NO: 21, и вариабельную область тяжелой цепи, выбранную из SEQ ID NO: 25; или
c. легкую цепь, соответствующую SEQ ID NO: 14 или SEQ ID NO: 18 или SEQ ID NO: 22, и тяжелую цепь, соответствующую SEQ ID NO: 26;
где антитело или его антигенсвязывающий фрагмент является гуманизированным и предотвращает агрегацию альфа-синуклеина, индуцированную фибриллами альфа-синуклеина, где, необязательно, антитело или его антигенсвязывающий фрагмент связывает альфа-синуклеин с эпитопом, включающим, по меньшей мере остатки D119, N122 и Y125 последовательности SEQ ID NO: 8, и где антитело или его антигенсвязывающий фрагмент предназначены для применения в терапии. Предпочтительно, чтобы антитело или его антигенсвязывающий фрагмент не давали перекрестную реакцию с бета-синуклеином и связывали альфа-синуклеин с величиной константы диссоциации (KD), по меньшей мере, в 10 раз более высокой для мономерного альфа-синуклеина, чем для альфа-синуклеина в фибриллах.
Кроме того, частью настоящего изобретения является применение антител против альфа-синуклеина или их антигенсвязывающих фрагментов в качестве диагностических средств или при диагностических исследованиях, например, для диагностирования альфа-синуклеинoпатий, таких как болезнь Паркинсона (PD) (в том числе идиопатические и наследственные формы болезни Паркинсона), деменция с тельцами Леви (DLB), болезнь диффузных телец Леви (DLBD), вариант болезни Альцгеймера с тельцами Леви (LBVAD), смешанный тип болезни Альцгеймера и Паркинсона, множественная системная атрофия (MSA) и нейродегенерация с накоплением железа в головном мозге типа 1 (NBIA-1).
Предпочтительно, чтобы диагностирование можно было проводить на биологических образцах. Термин "биологический образец" охватывает целый ряд типов образцов, взятых у индивидуума, которые могут быть использованы при диагностическом исследовании или мониторинге состояния здоровья. Это определение охватывает спинномозговая жидкость, кровь, например, плазму и сыворотку, и другие образцы жидкостей биологического происхождения, таких как моча и слюна, образцы твердых тканей, такие как биоптат, или тканевые культуры или клетки, полученные из них, и их потомство. Это определение также включает образцы, которые были обработаны тем или иным способом после их получения, таким как обработка с помощью реагентов, солюбилизация или обогащение конкретными компонентами, такими как полинуклеотиды.
Предпочтительно, чтобы диагностическое исследование можно было проводить на биологических образцах, которые находятся вне организма человека или животного. Такое диагностическое исследование называют также исследованием in vitro. Диагностическое исследование in vitro может основываться на методе in vitro обнаружения альфа-синуклеина в биологическом образце, который был взят у индивидуума, включающем стадии i) контактирования биологического образца с описанным в изобретении антителом против альфа-синуклеина или с его антигенсвязывающим фрагментом и ii) обнаружения связывания антитела против альфа-синуклеина или его антигенсвязывающего фрагмента с альфа-синуклеином. Путем сравнения определяемого уровня альфа-синуклеина или присутствия специфической посттрансляционно модифицированной формы альфа-синуклеина с подходящим контролем, могут быть выявлены одна или более альфа-синуклеинoпатий. Такой метод обнаружения может быть соответственно использован для определения того, имеет ли субъект альфа-синуклеинoпатию или подвержен риску развития альфа-синуклеинoпатии, в том числе для определения стадии (тяжести) альфа-синуклеинoпатии.
Поэтому, в настоящем изобретении предлагается антитело или его антигенсвязывающий фрагмент для применения при диагностике альфа-синуклеинoпатий, предпочтительно, при диагностике болезни Паркинсона (PD), где антитело или его антигенсвязывающий фрагмент включает:
a. вариабельную область легкой цепи, включающую CDR-L1, соответствующий SEQ ID NO: 1; CDR-L2, соответствующий SEQ ID NO: 2, и CDR-L3, соответствующий SEQ ID NO: 3 или SEQ ID NO: 7; и вариабельную область тяжелой цепи, включающую CDR-H1, соответствующий SEQ ID NO: 4; CDR-H2, соответствующий SEQ ID NO: 5, и CDR-H3, соответствующий SEQ ID NO: 6; или
b. вариабельную область легкой цепи, соответствующую SEQ ID NO: 13 или SEQ ID NO: 17 или SEQ ID NO: 21, и вариабельную область тяжелой цепи, выбранной из SEQ ID NO: 25; или
c. легкую цепь, соответствующую SEQ ID NO: 14 или SEQ ID NO: 18 или SEQ ID NO: 22, и тяжелую цепь, соответствующую SEQ ID NO: 26;
где, необязательно, антитело или его антигенсвязывающий фрагмент связывает альфа-синуклеин с эпитопом, включающим, по меньшей мере остатки D119, N122 и Y125 последовательности SEQ ID NO: 8.
Последовательности, включенные в настоящее изобретение, представлены в таблице 1.
Таблица 1
P37840
человека
5811
5811
нуклеотид
V-область
Легкая цепь
V-область
нуклеотид
Легкая цепь
нуклеотид
V-область
Легкая цепь
V-область
нуклеотид
Легкая цепь
нуклеотид
V-область
Легкая цепь
V-область
нуклеотид
Легкая цепь
нуклеотид
V-область
Тяжелая цепь
V-область
нуклеотид
Тяжелая цепь
нуклеотид
нуклеотид
нуклеотид
Далее изобретение будет дополнительно описано с помощью примеров со ссылками на варианты осуществления, проиллюстрированные на прилагаемых чертежах.
ПРИМЕРЫ
Пример 1. Экспрессирование мономера альфа-синуклеина и фибриллов человека
Синтезировали ген, кодирующий альфа-синуклеин человека, и субклонировали его в вектор pMH 10His TEV (содержащий промотор CMV) с использованием стандартных методов молекулярной биологии с целью создания вектора, сконструированного для получения альфа-синуклеина с N-концевой меткой 10His-TEV. Полученный вектор трансфицировали в клетки Expi293F с использованием экспрессирующей системы Expi293TM (фирмы Invitrogen) в соответствии с протоколами фирмы-производителя. Белок альфа-синуклеина накапливался в культуральной среде, откуда его извлекали методом аффинной хроматографии с иммобилизованным ионом металла на колонке HisTrap excel (GE Healthcare). Колонку промывали 25 мМ Трис-HCl, 300 мМ NaCl, pH 8,0, и белок элюировали с использованием ступенчатого градиента 500 мМ имидазола в том же буфере. Метку 10His удаляли с использованием протеазы TEV. Затем образец концентрировали и обессоливали, и повторно наносили расщепленный белок в колонку HisTrap excel, и собирали расщепленной альфа-синуклеин в элюате. Альфа-синуклеин дополнительно очищали гель-фильтрацией на колонке HiLoad 26/600 Superdex 75 (GE Healthcare), и удаляли эндотоксин путем пропускания через картридж Proteus NoEndo (Generon). Методом светорассеяние SEC MALS подтверждали, что очищенный альфа-синуклеин является мономерным (фигура 1А).
Дикий тип человеческого альфа-синуклеина (без метки) также экспрессировался в клетках Expi293F. Белок извлекали из культуральной среды методом анионного обмена в колонке HiTrap Q (GE Healthcare). Колонку промывали 20 мМ Трис-HCl, рН 8,0, и белок элюировали с использованием градиента хлорида натрия до 400 мМ. Фракции концентрировали и обессоливали путем пропускания через колонку HiPrep 26/10 (GE Healthcare) и элюировали с помощью 20 мМ трис-HCl, рН 8,0. Затем белок очищали на колонке MonoQ 10/100GL, элюировали с использованием градиента хлорида натрия до 400 мМ в 20 мМ TrisHCl, рН 8,0, и затем проводили гель-фильтрацию на колонке HiLoad 26/600 Superdex 75 (GE Healthcare) с элюированием в PBS pH 7,4 (фигура 1Б).
Этот немеченый мономер альфа-синуклеина дикого типа использовали для приготовления альфа-синуклеина. Фибриллы получали путем непрерывного перемешивания в течение 10 дней очищенного мономера (9-10 мг/мл в PBS pH 7,4) при 1200 об/мин, 37°C в шейкер-инкубаторе Vortemp56 (Labnet). Образование фибрилл оценивали методом анализа JC-1 (Lee et al., Biochem. J. 2009, 418, 311-323) и методом инфракрасной спектроскопии раствора с преобразованием Фурье. Не включенный в фибриллы мономер в растворах оценивали путем ультрацентрифугирования и пропускания через мембрану с отсечением молекул с молекулярной массой 100 кДа с последующим гель-электрофорезом. В дальнейших исследованиях использовали только фибриллы с ответом JC-1> 15, низким количеством растворимого мономера (<5%) и спектром FTIR с основным поглощением между 1625 и 1630 см-1 (фигура 2). Приготовленные фибриллы хранили при -80°С.
Пример 2. Иммунизация и выделение антител
Были осуществлены многочисленные стратегии иммунизации с использованием различных видов животных и иммуногенов. Антитело 5811 получали от самки крысы линии Sprague Dawley (с массой тела > 180 г), иммунизированной путем подкожного введения 50 мкг мономера немеченого альфа-синуклеина дикого типа, экспрессированного, как описано выше (SEQ ID NO: 8).
Крысам делали 3 бустер-инъекции с 21-дневными интервалами, используя неполный адъювант Фрейнда (IFA), отбирая кровь для проведения анализа из хвостовой вены через 14 дней после иммунизации. Терминация происходила через 14 дней после окончательной повторной иммунизации, после чего получали суспензию отдельных клеток селезенки, лимфатического узла, костного мозга и мононуклеарные клетки периферической крови и замораживали в 10% DMSO/FCS при -80°C.
B-клеточная культура
В-клеточные культуры получали с использованием метода, аналогичного методу, описанному в публикации Tickle et al., 2015. J Biomol Screen: 20 (4), 492-497. Вкратце, В-клетки, полученные из лимфатических узлов или спленоцитов иммунизированных животных, культивировали при плотности приблизительно 2000-5000 клеток на лунку в 96-луночных планшетах со штрих-кодом для культивирования клеток тканей с 200 мкл/лунка среды RPMI 1640 (Gibco BRL), дополненной 10% FCS (Sigma Aldrich), 2% HEPES (Sigma Aldrich), 1% L-глутамина (Gibco BRL), 1% раствора пенициллина/стрептомицина (Gibco BRL), 0,1% β-меркаптоэтанола (Gibco BRL), 1% надосадочной жидкости активированных PBMC (BSS) человека и облученными рентгеновскими лучами мутантными клетками мышиной тимомы EL4 (5 × 104/лунка) в течение семи дней при 37°C в атмосфере 5% CO2. Культуры были созданы с использованием В-клеток от всех иммунизированных животных, и в целом было отобрано для исследования приблизительно 1,7 × 109 В-клеток.
Антитело 5811 по настоящему изобретению получали из выделенных из лимфатического узла активированных В-клеток, которые культивировали при плотности приблизительно 2000 клеток на лунку. Лимфатический узел использовали помимо спленоцитов для обнаружения антител, чтобы иметь альтернативный источник В-клеток, из которого можно отбирать и идентифицировать новые антитела. У иммунизированных крыс отбирали приблизительно 3,3 × 108 клеток полноразмерного мономерного альфа-синуклеина человека.
Первичный скрининг
Присутствие специфических антител к альфа-синуклеину человека в надосадочных жидкостях культуры В-клеток определяли методом гомогенного флуоресцентного анализа связывания с использованием микросфер SuperAvidin™ (Bangs Laboratories), покрытых мономером биотинилированного рекомбинантного полноразмерного альфа-синуклеина человека, в качестве источника целевого антигена. Описанный в изобретении рекомбинантный альфа-синуклеин человека биотинилировали с использованием 3-кратного молярного избытка биотина. Небольшой молярный избыток биотина использовали для того, чтобы исключить полную модификацию всех семи остатков лизина, которые находятся в молекуле альфа-синуклеина. Мономер альфа-синуклеина инкубировали в течение ночи при 40°С с биотином, и свободный биотин удаляли на следующий день с использованием спин-обессоливающей колонки Zeba™. Скрининг включал перенос 10 мкл надосадочной жидкости из 96-луночных планшетов со штрих-кодом для тканевых культур в 384-луночные аналитические планшеты со штрих-кодом с черными стенками, содержащие мономер биотинилированного рекомбинантного альфа-синуклеина человека, иммобилизованный на микросферах Superavidin (10 мкл/лунку) с помощью устройства для переноса жидкостей Agilent Bravo. Связывание выявляли с использованием конъюгата Alexafluor647 (Jackson), специфичного к козьему Fcγ фрагменту против крысиного IgG). Планшеты считывали на флуоресцентном цитометре TTP Labtech Mirrorball с целью идентификации лунок, содержащих IgG, специфичных к альфа-синуклеину.
Вторичное сканирование
После проведения первичного скрининга, положительные надосадочные жидкости объединяли на 96-луночных эталонных планшетах со штрих-кодом с использованием робота-дозатора для пипетирования в индивидуальные лунки Beckman Coulter BiomekNXP, и B-клетки в планшетах для культивирования замораживали при -80°C. Затем эталонные планшеты подвергали скринингу методом иммуноферментного анализа (ELISA) с захватом стрептавидином с использованием мономера биотинилированного рекомбинантного альфа-синуклеина человека или фибрилл биотинилированного рекомбинантного альфа-синуклеина человека. Это проводили для идентификации лунок, в которых происходило связывание как мономерного, так и фибриллярного рекомбинантного альфа-синуклеина человека, и для исключения любых ложноположительных лунок, демонстрирующих нецелевое связывание с микросферами Superavidin™. Учитывая нерастворимую природу фибрилл, традиционные протоколы нанесения покрытия в методе ELISA, которые используют с белками в растворе, в данном случае не подходили. Было решено использовать протокол минимального биотинилирования для сохранения фибриллярной структуры и облегчения эффективного покрытия фибрилл на планшете для проведения анализа ELISA, предварительно покрытом стрептавидином.
Генерировали все описанные в настоящем изобретении фибриллы биотинилированного альфа-синуклеина путем объединения мономера биотинилированного рекомбинантного альфа-синуклеина (как описано выше) с 50-кратным избытком немеченого рекомбинантного альфа-синуклеина в PBS. Образование фибрилл подтверждали методом анализа JC1 (Lee et al., Biochem. J. 2009, 418, 311-323).
Биотинилированный мономер или биотинилированные фибриллы в PBS захватывали на 384-луночных планшетах Maxisorp, покрытых стрептавидином, в карбонатном покрывающем буфере (dH2O+0,16% Na2CO3+0,3% NaHCO3.) Планшеты блокировали с помощью 1% масса/объем PEG/PBS и затем инкубировали с 10 мкл/лунку надосадочной жидкости культуры В-клеток (разбавленной 1:1 блокирующим буфером). Добавляли в планшеты вторичный HRP-конъюгированный козий Fcγ фрагмент против крысиного IgG, специфичный конъюгат HRP (Jackson), с последующей визуализацией связывания с помощью субстрата TMB (3,3',5,5'-тетраметилбензидин, фирмы EMD Millipore; 10 мкл/лунка). Измеряли оптическую плотность при 630 нм с использованием считывающего устройства для микропланшетов BioTek Synergy 2. Анализ первичного связывания выявил 83 случая связывания, и после скрининга методом ELISA, было показано, что 29 из этих случаев связывания являются связыванием как мономерного, так и фибриллярного рекомбинантного альфа-синуклеина человека.
Надосадочные жидкости В-клеток, демонстрировавшие наиболее сильные сигналы связывания в анализе ELISA с рекомбинантными фибриллами, отбирали для дальнейшего исследования методом поверхностного плазмонного резонанса с целью идентификации тех клеток, для которых наблюдалась наилучшая скорость диссоциации в случае мономера рекомбинантного альфа-синуклеина человека, фибрилл рекомбинантного альфа-синуклеина человека и фибрилл рекомбинантного альфа-синуклеина мыши. Были исследованы надосадочные жидкости 26 различных В-клеток, в 19 лунках были получены скорости диссоциации (kd) <1 × 10-5 в случае мономера рекомбинантного альфа-синуклеина человека. Из них в 6 лунках были получены величины скорости диссоциации (kd) менее 1 × 10-5 в случае мономера рекомбинантного альфа-синуклеина мыши. Все 19 надосадочных жидкостей были отобраны для выделения вариабельной области.
Выделение вариабельной области
Для того чтобы сделать возможным выделение генов вариабельной области антител из представляющих интерес надосадочных жидкостей, необходимо было провести стадию деконволюции, чтобы можно было идентифицировать антиген-специфические В-клетки в данной лунке, которая содержала гетерогенную популяцию В-клеток. Это достигалось путем использования метода очагов флуоресценции (Clargo et al., 2014. MAbs: 6 (1), 143-159). Вкратце, В-клетки, секретирующие иммуноглобулин, из положительной лунки смешивали с микросферами стрептавидина (New England Biolabs), покрытыми фибриллами биотинилированного рекомбинантного альфа-синуклеина человека (приготовленными с использованием смеси 1:50, как описано выше), и с конечным разведением 1:1200 козьего фрагмента Fc против крысиного IgG, специфичного к конъюгату FITC (Jackson). После инкубации в статических условиях при 37°С в течение 1 часа, антиген-специфические В-клетки можно было идентифицировать по присутствию флуоресцентного ореола, окружающего эти В-клетки. Затем отбирали ряд этих индивидуальных клонов В-клеток, идентифицированных с помощью микроскопа Olympus, с помощью микроманипулятора Eppendorf и помещали в пробирку для проведения ПЦР.
Гены вариабельной области антитела выделяли из отдельных клеток методом ПЦР с обратной транскрипцией, используя праймеры, специфичные к вариабельной области тяжелой и легкой цепей. Проводили два раунда ПЦР с вложенной 2° ПЦР, включающей сайты рестрикции на 3' и 5' концах, позволяющие клонировать вариабельную область в мышиный IgG Fcγ1 или Fab-10HIS (VH) или мышиный каппа (VL) экспрессирующий вектор для млекопитающего. В экспрессирующие векторы были успешно клонированы гены антител против альфа-синуклеина из 9 различных надосадочных жидкостей. Конструкции тяжелой и легкой цепей ко-трансфицировали в клетки Expi-293 с использованием ExpiFectamine 293 (Invitrogen) и экспрессировали в объеме 30 мл в колбе Эрленмейера объемом 125 мл химерные рекомбинантные крысиные-мышиные антитела 5811 mFab или 5811 mIgG1 (включающие крысиные вариабельные области 5811 и мышиные константные области (соответствующие SEQ ID NO: 34 и 35 для IgG и SEQ ID NO: 34 и 36 для Fab). После экспрессирования в течение 5-7 дней, собирали надосадочные жидкости и очищали их методом аффинной хроматографии.
Скрининг методом ELISA промежуточных надосадочных жидкостей
Очищенные крысиные-мышиные химерные антитела затем подвергали дальнейшему скринингу с использованием метода ELISA. Мономер и фибриллы биотинилированного рекомбинантного альфа-синуклеина человека захватывали на 384-луночных планшетах Maxisorp (ThermoScientific/Nunc), покрытых слоем стрептавидина в карбонатном покрывающем буфере (dH2O+0,16% Na2CO3+0,3% NaHCO3). Отдельные планшеты также покрывали слоем биотинилированного пептида, соответствующего остаткам от 117 до 126 альфа-синуклеина человека, соответствующего SEQ ID NO: 8 (пептид PVDPDNEAYE), чтобы проверить, связаны ли промежуточные процессы с этой или другой областью молекулы. Планшеты блокировали с помощью 1% масса/объем PEG/PBS и затем инкубировали с несколькими разведениями очищенной промежуточной надосадочной жидкости. Добавляли в планшеты вторичное HRP-конъюгированное козьи антитело против мышиного IgG Fc (Stratech Scientific Ltd/Jackson ImmunoResearch), и затем проводили визуализацию связывания с субстратом TMB (3,3',5,5'-тетраметилбензидин, фирмы EMD Millipore; 10 мкл/лунка). Оптическую плотность измеряли при 630 нм с использованием считывающего устройства для микропланшетов BioTek Synergy 2. Данные для антитела 5811 в виде IgG Fc-1 (включающего SEQ ID NO: 34 и 35) и в виде Fab (включающего SEQ ID NO: 34 и 36) представлены на фигурах 3А и 3В. Как можно видеть, антитела 5811 демонстрируют связывание как с мономерным, так и с фибриллярным рекомбинантным альфа-синуклеином человека, а также демонстрируют связывание с пептидом PVDPDNEAYE.
Далее проводили характеризацию с целью определения активности, аффинности и авидности, связывания эпитопа и биофизических свойств таких антител. Если специально не указано, что использовалась гуманизированная версия, то эксперименты проводились с крысиными-мышиными химерными антителами (5811 mFab или 5811 mIgG1).
Пример 3. Характеризация антител
Кинетические исследования с использованием системы Biacore
Кинетику взаимодействия исследовали методом поверхностного плазмонного резонанса на приборе Biacore T200. Каждый из трех различных лигандов, включающих мономер рекомбинантного полноразмерного альфа-синуклеина человека, очищенные фибриллы рекомбинантного альфа-синуклеина человека и очищенные фибриллы рекомбинантного альфа-синуклеина мыши, приготовленных, как описано в настоящем изобретении, иммобилизировали на трех разных проточных ячейках на поверхности чипа СМ5 с использованием реакции сочетания амина. Готовили три лиганда в 10 мМ NaAc, pH 3,5 и иммобилизировали их на раздельные поверхности проточной ячейки для достижения уровня иммобилизации около 30 единиц отклика (RU) для мономера альфа-синуклеина, около 40 RU для фибрилл альфа-синуклеина человека и около 300 RU для фибрилл альфа-синуклеина мыши, соответственно, при скорости потока 10 мкл/мин. Буфер HBS-EP + (GE Health Bio-Sciences AB) использовали в качестве подвижного буфера как для иммобилизации лиганда, так и для исследовании кинетики. Затем измеряли связывание моноклонального антитела 5811 mIgG1 против альфа-синуклеина и моноклонального антитела 5811 mFab против трех лигандов. Моноклональные антитела mIgG1 или mFab вводили при 7 различных концентрациях от 800 нМ до 0,195 нМ в 3 проточные ячейки при времени контакта 3 мин и времени диссоциации 30 мин при скорости потока 100 мкл/мин. Поверхность регенерировали путем одной инъекции 50 мМ HCl в течение 90 секунд при скорости потока 10 мкл/мин и еще одной инъекцией 50 мМ HCl в течение 60 секунд при скорости потока 10 мкл/мин. Данные анализировали с использованием программного обеспечения Biacore T200 (версии 3.0) с использованием модели бивалентного аналита с предполагаемым отсутствием общего вклада (RI=0) и глобального Rmax для формата mIgG1, а также модели 1:1 с гибким общим вкладом (локальным RI) и глобальным Rmax.
Кинетические величины для связывания как mIgG1, так и mFab, с иммобилизированными мишенями приведены в таблице 2. Формат mIgG1 продемонстрировал кажущуюся селективную аффинность к фибриллам альфа-синуклеина человека по сравнению с аффинностью к мономеру альфа-синуклеина человека, поскольку константа диссоциации KD более чем в 10 раз ниже для фибрилл человека.
Таблица 2
(1/мс)
(1/с)
(нМ)
(1/мс)
(1/с)
(нМ)
(1/мс)
(1/с)
(нМ)
mFab
mIgG1
Связывание с синуклеином
Связывание антител против альфа-синуклеина человека с бета-синуклеином человека исследовали методом вестерн-блоттинга с использованием бета-синуклеина фирмы rPeptide. 1 мкг синуклеина пропускали на геле 4-12% Bis/Tris и блотировали на мембрану из поливинилиденфторида (PVDF). Мембрану блокировали в PBS с 3% BSA и 0,1% Tween20. Добавляли к блокированному блоту антитело 5811 mIgG1 и инкубировали в течение 1 часа при комнатной температуре, промывали PBS, 0,1% Tween20 и инкубировали в течение 1 часа с конъюгатом вторичное антитело-HRP (конъюгат анти-кроличий H+L HRP, Bethyl, A120- 101P). Блот тщательно промывали в PBS с 0,1% Tween 20, PBS и водой. Хемилюминесценцию измеряли после добавления субстрата вестерн-блоттинга ECL (Pierce). Как показано на фигуре 4 (А), полоска 3, антитело 5811 mIgG1 не связывается с бета-синуклеином человека.
Картирование эпитопа
ЯМР
Альфа-синуклеин человека клонировали в экспрессирующий вектор pET28a таким образом, чтобы белок экспрессировался без каких-либо меток. Конструкцию трансформировали в клетки E.coli BL21 (DE3) (Stratagene), и клетки выращивали в определенной среде с меченной C13 DL-глюкозой и меченым N15 сульфатом аммония в присутствии и в отсутствие оксида дейтерия (D2O). Экспрессию индуцировали при OD 600 нм=1 с помощью 300 мМ IPTG, и культуру инкубировали при 30°C в течение 4 часов. Клетки осаждали и лизировали с помощью трех циклов замораживания-оттаивания в 100 мл буфера для лизиса (20 мМ Tris/HCl, рН 8,0, 25 единиц бензоназы (Merck Millipore), полный коктейль ингибиторов протеаз без EDTA (2 таблетки, Roche) и 10 мг лизоцима ( Сигма)). Лизат осветляли центрифугированием при 18000 об/мин, и очищенный лизат пропускали через фильтр с размером пор 0,22 мкм (Stericup, Millipore). Стерильный лизат загружали в колонку MonoQ 10/100GL (GE Healthcare), приведенную в равновесие с 20 мМ Tris/HCl pH 8,0, 5CV, и белок элюировали с градиентом до 500 мМ NaCl в том же буфере. Дальнейшую очистку наиболее чистых фракций повторяли на колонке MonoQ 10/100GL после 5-кратного разбавления в 20 мМ Tris/HCl, рН 8,0. Самые чистые фракции объединяли, концентрировали с помощью концентрирующей центрифуги MWCO 10 кДа (Centriprep, Millipore), очищали гель-проникающей хроматографией на колонке HiLoad 26/600 Superdex 75 (GE Healthcare) и элюировали в 25 мМ натрий-фосфатном буфере, 100 мМ NaCl (рН 6,4). Фракции из колонки Superdex 75 объединяли, и добавляли азид натрия (конечная концентрация 0,02%) и AEBSF (конечная концентрация 10 мкМ). Конечная концентрация белка составляла приблизительно 5 мг/мл.
Крысиное-мышиное антитело Fab 5811 экспрессировали в CHO SXE в виде His-меченных форм и очищали от надосадочной жидкости методом аффинной хроматографии His-меченых белков, связывая белок с HisTrap Excel (GE Healthcare) из надосадочной жидкости и элюируя его 250 мМ имидазолом в PBS. Элюируемый пул загружали на колонку HiTrap GammaBind Plus Sepharose (GE Healthcare), промывали PBS, и белок элюировали 0,1 М глицин-HCl, pH 2,6, и величину pH доводили до 6 с помощью 0,75 M фосфата натрия, pH 9. Буфер элюируемого белка Fab-His заменяли на буфер для ЯМР (25 мМ фосфата натрия, рН 6,4, 100 мМ NaCl) на колонке для обессоливания HiPrep 26/10. Белковые фракции Fab-His концентрировали, и добавляли ингибиторы протеазы AEBSF (конечная концентрация 10 мкМ) и азид натрия (конечная концентрация 0,02%), затем стерилизовали на фильтре Millex GV с размером пор 0,22 мкм..
Связывание антитела 5811, имеющего VL, соответствующую SEQ ID No: 9, и VH, соответствующую SEQ ID No: 10, с эпитопом определяли методом спектроскопии гетероядерного магнитного резонанса (ЯМР) с использованием Fab-фрагмента антитела.
Базовые отнесения ЯМР-спектра α-синуклеина
Образцы для исследования методом ЯМР обычно имели объем 350 мкл с концентрацией белка 360 мкМ, меченого с помощью 13C/15N, или 430 мкМ, меченого с помощью 2H/13C/15N, альфа-синуклеина человека в ампулах Шигеми диаметром 5 мм. Буфер представлял собой 100 мМ NaCl, 25 мМ фосфата натрия, рН 6,4, 10 мкМ AEBSF, 0,02% NaN3. Все эксперименты регистрировали при 20°С на спектрометре Bruker AVIII с частотой 600 МГц или спектрометре Bruker AVII с частотой 800 МГц, оснащенными зондами с криогенным охлаждением. Последовательные связи между базовыми ЯМР-сигналами остатков в белке, HN(i)-N(i)-N(i±1), устанавливали, используя эксперимент 3D (H)N(CA)NNH (Weisemann et al., 1993 3D Triple-resonance NMR techniques for the sequential assignment of NH and 15N resonances in 15N- and 13C-labelled proteins. J. Biomol. NMR 3), регистрируемые со спектральной шириной 28, 28 и 10 ppm и временем регистрации сигнала 117 (F1) 117 (F2) и 140 (F3) мс при измерениях на 15N, 15N и 1H, соответственно, с 8 сканированиями на инкремент и задержкой релаксации 1,5 секунды. Использовали неоднородную выборку с плотностью выборки 10% (4000 из 40000 гиперкомплексных точек), что давало общее время сбора данных 2,75 дня. Подтверждали последовательные связи, и идентифицировали типы остатков с использованием экспериментов TROSY-HNCA (Grzesiek and Bax, 1992 Improved 3D triple-resonance NMR techniques applied to a 31 kDa protein. J. Magn. Reson. 96, 432-440; Salzmann et.al., 1998. TROSY in triple-resonance experiments: new perspectives for sequential NMR assignment of large proteins. Proc. Natl. Acad. Sci. USA. 95, 13585-90) and TROSY-HNCACB (Wittekind and Mueller, 1993 HNCACB, a High-Sensitivity 3D NMR Experiment to Correlate Amide-Proton and Nitrogen Resonances with the Alpha- and Beta-Carbon Resonances in Proteins. J. Magn. Reson. Ser. B 101, 201-205; Salzmann et.al., 1999. TROSY-type Triple Resonance Experiments for Sequential NMR Assignment of Large Proteins. J. Am. Chem. Soc. 121, 844-848). Эксперимент TROSY-HNCA регистрировали со спектральной шириной 23, 28, 10 ppm и временем регистрации сигнала 12,1 (F1), 21,7 (F2) и 100 (F3) мс при измерениях на 13С, 15N и 1H, соответственно (8 сканирований на инкремент, задержка релаксации 1,5 секунды, общее время сбора данных 1 день), в то время как эксперимент TROSY-HNCACB регистрировали со спектральной шириной 56, 28 и 10 ppm и временем регистрации сигнала 8,2 (F1), 21,7 (F2) и 100 (F3) мс при измерениях на 13С, 15N и 1H, соответственно (8 сканирований на инкремент, задержка релаксации 1,5 с, общее время получения данных 1,7 дня). Базовые отнесения карбонилов получали из спектра TROSY-HNCO (Grzesiek and Bax, 1992 Improved 3D triple-resonance NMR techniques applied to a 31 kDa protein. J. Magn. Reson. 96, 432-440; Salzmann et.al., 1998. TROSY in triple-resonance experiments: new perspectives for sequential NMR assignment of large proteins. Proc. Natl. Acad. Sci. USA. 95, 13585-90), регистрируемого со спектральной шириной 10, 29, 10 ppm и временем регистрации сигнала 80 (F1), 21,7 (F2) и 150 (F3) мс при измерениях на 13С, 15N и 1H, соответственно (8 сканирований на инкремент, задержка релаксации 1,5 с). Использовали неоднородную выборку с плотностью выборки 15% (1208 из 8050 гиперкомплексных точек), что дало общее время сбора данных 19 часов. Спектры ЯМР обрабатывали с использованием системы NMRPipe (Delaglio et al., 1995 NMRPipe: a multidimensional spectral processing system based on UNIX pipes. J. Biomol. NMR 6, 277-93) с линейным предсказанием, используемым для увеличения эффективного времени регистрации сигнала на азоте вплоть до однократного увеличения. Данные неоднородной выборки преобразовывали с использованием гарвардского итерационного метода на основе мягкой пороговой обработки (Hyberts et al., 2012 Application of iterative soft thresholding for fast reconstruction of NMR data non-uniformly sampled with multidimensional Poisson Gap scheduling. J Biomol NMR 52, 315-27) с преобразованием данных до следующего числа Фурье, увеличивая время косвенного сбора данных до 60%. Анализ данных проводили с использованием метода Sparky (Goddard and Kneller, D.G. SPARKY 3. In., University of California, San Francisco), что в результате давало отнесения резонансов амидного протона и азота 133 остатков, соответствующих 99% остатков, исключая остатки пролина и N-концевого метионина. Единственным другим остатком альфа-синуклеина, который не был отнесен, была аспарагиновая кислота в положении 2
Картирование сайта связывания фрагмента антитела 5811Fab
Картирование сайта связывания 5811 проводили с использованием 150 мкМ образца 2Н/13С/15N меченного α-синуклеина человека, содержащего 10% молярный избыток немеченого Fab 5811. Образцы готовили в том же буфере, как описанный выше, для базового отнесения α-синуклеина. Изменения химического сдвига на 1H, 15N и 13C определяли путем сравнения спектра TROSY-HNCO (Grzesiek and Bax, 1992 Improved 3D triple-resonance NMR techniques applied to a 31 kDa protein. J. Magn. Reson. 96, 432-440; Salzmann et.al., 1998. TROSY in triple-resonance experiments: new perspectives for sequential NMR assignment of large proteins. Proc. Natl. Acad. Sci. USA. 95, 13585-90), зарегистрированного для комплекса альфа-синуклеин/Fab, с эквивалентным контрольным спектром, зарегистрированным для свободного альфа-синуклеина. Контрольный эксперимент TROSY-HNCO со свободным альфа-синуклеином регистрировали со спектральной шириной 10, 28 и 10 ppm и временем регистрации сигнала 80 (F1), 21,7 (F2) и 150 (F3) мс при измерениях на 13C, 15N и 1H, соответственно (16 сканирований на инкремент, задержка релаксации 1,4 секунды). Использовали неоднородную выборку (NUS) с плотностью выборки 25% (2013 из 8050 гиперкомплексных точек), что давало общее время сбора данных 2,5 дня. Эксперимент TROSY-HNCO для комплекса α-синуклеин/Fab регистрировали со спектральной шириной 10, 28 и 10 ppm и временем регистрации сигнала 80 (F1), 21,7 (F2) и 80 (F3) мс при измерениях на 13C, 15N и 1H, соответственно (32 сканирования на инкремент, задержка релаксации 1,5 секунды). Использовали неоднородную выборку (NUS) с плотностью выборки 25% (1119 из 4477 гиперкомплексных точек), что давало общее время сбора данных 2,8 дня. Спектры ЯМР обрабатывали с использованием системы NMRPipe (Delaglio et al., 1995 NMRPipe: a multidimensional spectral processing system based on UNIX pipes. J. Biomol. NMR 6, 277-93) с преобразованием данных NUS, выполняемым с использованием многомерной декомпозиции mddnmr (Orekhov and Jaravine, 2011. Analysis of non-uniformly sampled spectra with Multi-Dimensional Decomposition. Prog. Nucl. Magn. Reson. Spectrosc., 59, p 271-292). В процессе преобразования данных, эффективное время регистрации сигнала при измерении на азоте увеличивали вплоть до однократного увеличения.
Изменения химического сдвигов анализировали с использованием методики минимального сдвига (Williamson et al., 1997 Mapping the binding site for matrix metalloproteinase on the N-terminal domain of the tissue inhibitor of metalloproteinases-2 by NMR chemical shift perturbation. Biochemistry 36, 13882-9), практически так же, как было описано ранее (Veverka et al., 2008 Structural characterization of the interaction of mTOR with phosphatidic acid and a novel class of inhibitor: compelling evidence for a central role of the FRB domain in small molecule-mediated regulation of mTOR. Oncogene 27, 585-95), за исключением того, что модифицировали уравнение, используемое для расчета комбинированного изменения химического сдвига (Δδ), с целью включения химического сдвига карбонила, что в результате давало следующее уравнение:
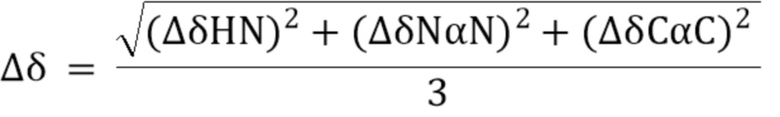
где ΔδHN, ΔδN и ΔδC представляют собой изменения химических сдвигов 1H, 15N и 13C, соответственно. αN и αC соответствуют масштабирующим множителям 0,2 и 0,35, соответственно, используемым для диапазонов изменения химических сдвигов для протона амида, азота и карбонила.
Для идентификации сайтов связывания Fab (эпитопов) на альфа-синуклеине, использовали гистограмму комбинированного минимального сдвига в зависимости от последовательности белка для выявления областей альфа-синуклеина, содержащих значимо возмущенные сигналы. Если размер комбинированного изменения химического сдвига для индивидуальных аминокислот превышал пороговое значение средней величины комбинированного изменения химического сдвига для всех аминокислот плюс одно стандартное отклонение от этого средней величины, то эти остатки отбирали для дальнейшей оценки в качестве возможных контактных остатков в сайте связывания Fab.
Значимо возмущенные остатки идентифицировали в качестве остатков, чей минимальный сдвиг, по меньшей мере, был больше среднего значения плюс одно стандартное отклонение всех рассчитанных сдвигов. Для идентификации остатков, связанных с Fab, применяли четыре различных пороговых значений. Остатки, которые участвуют в сайте связывания, оцениваются с возрастающей точностью как: остатки, чей минимальный сдвиг превышает среднее значение плюс одно стандартное отклонение всех рассчитанных сдвигов (составляющий > 0,025574); остатки, чей минимальный сдвиг превышает среднее значение плюс два стандартных отклонения всех рассчитанных сдвигов (составляющий > 0,042552); остатки, чей минимальный сдвиг превышает среднее значение плюс три стандартных отклонения всех рассчитанных сдвигов (составляющий > 0,059530); остатки, чей минимальный сдвиг превышает среднее значение плюс четыре стандартных отклонения всех рассчитанных сдвигов (составляющий > 0,076508). В этом анализе, остатки пролина не могут быть идентифицированы, так как они не содержат амидного протона.
Поэтому, эпитоп альфа-синуклеина для 5811 Fab определяется с возрастающей точностью как среднее значение плюс одно стандартное отклонение для всех рассчитанных сдвигов: E114, D115, V118, D119, D121, N122, E123, A124, Y125, E126, M127, S129, Q134, D135 и Y136; среднее значение плюс два стандартных отклонения всех рассчитанных сдвигов: V118, D119, D121, N122, Y125, M127, D135 и Y136; среднее значение плюс три стандартных отклонения всех рассчитанных сдвигов: V118, D119, D121, N122, M127, D135 и Y136; отсутствовали остатки, отклонение сдвигов для которых превышало среднее значение плюс четыре стандартных отклонения всех рассчитанных сдвигов
Применяя нумерацию аминокислот, используемую в эталонной последовательности NP_000336.1 Национального центра биотехнологической информации (NCBI), было обнаружено, что 5811 Fab связывает, по меньшей мере, следующие остатки альфа-синуклеина (среднее значение+3 SD) V118, D119, D121, N122, Y125, M127, D135 и Y136. Антитело может также связывать все следующие остатки (среднее значение+1 SD) E114, D115, V118, D119, D121, N122, E123, A124, Y125, E126, M127, S129, Q134, D135 и Y136.
Как показано на фигуре 4B, химический сдвиг ЯМР изменялся на dCN альфа-синуклеина человека после связывания с 5811 mFab. По-видимому, предсказанный эпитоп 5811 mFab включает остатки в аминокислотах 114 и 136 альфа-синуклеина человека (SEQ ID NO: 8)
Картирование пептида
Дальнейшую характеризацию эпитопа, связанного антителом 5811 mFab, проводили с использованием коротких (обычно 9-мерных или 10-мерных) пептидов, представляющих и покрывающих С-концевую область альфа-синуклеина человека. Их использовали в конкурентной схеме анализа поверхностного плазмонного резонанса с целью испытания их способности ингибировать связывание антитела с мономерным альфа-синуклеином или с предварительно образованными фибриллами альфа-синуклеина, иммобилизованными на чипе Biacore. Пептид, демонстрирующий максимальный уровень ингибирования, затем отбирали для исследований по совместной кристаллизации с антителом, для подтверждения строго соответствующего эпитопа.
Пептиды приобретали у фирмы Peptide Protein Research Ltd., Bishop's Waltham, U.K. и синтезировали методом твердофазного химического синтеза с использованием группы Fmoc по методу Атертона и Шеппарда (смотрите публикацию Atherton, E.; Sheppard, R.C. (1989). Solid Phase peptide synthesis: a practical approach. Oxford, England: IRL Press). N и С концы пептидов блокировали ацетильной и амидной группами, соответственно, за исключением случая, когда пептиды представляли N-конец и С-конец α-синуклеина, где аминогруппы и карбоксильные группы, соответственно, оставались свободными. Исходные растворы пептидов готовили в DMSO с содержанием 10 мМ. Полный список пептидов приведен в таблице 3.
Таблица 3
Мономер рекомбинантного альфа-синуклеина человека и предварительно сформированные фибриллы альфа-синуклеина иммобилизировали на чипе СМ5 с использованием прибора Biacore 3000 (GE Healthcare). После активации поверхности карбоксиметилдекстрана путем введения 100 мкл свежеприготовленной смеси 1:1 (по объему) 50 мМ N-гидроксисукцимида и 200 мМ 1-этил-3-(3-диметиламинопропил)карбодиимида при скорости потока 10 мкл/мин HBS-EP (GE Healthcare) в качестве подвижного буфера, инициировали взаимодействие путем пропускания 100 мкл мономера и фибрилл при 5 мкМ в 10 мМ ацетате, рН 5,0, через раздельные проточные ячейки. Референсную проточную ячейку активировали таким же образом, а затем все поверхности проточной ячейки дезактивировали путем импульсного введения 50 мкл 1 М этаноламина ⋅ HCl pH 8,5.
Растворы пептидов готовили в подвижном буфере при 100 мкМ, и готовили холостую пептидную пробу путем разведения DMSO 1 к 100 в подвижном буфере. Приготавливали раствор 5811 mFab при 50,5 нМ в подвижном буфере перед предварительной инкубацией 198 мкл или с 2 мкл холостой пептидной пробы, или с разбавленным пептидом, с получением конечной смеси 50 нМ Fab и 1 мкМ пептида или контроля. Регистрировали сенсограммы для каждого образца путем введения 30 мкл смеси со скоростью 10 мкл/мин и регистрации точки формирования отчета за 5 секунд до окончания введения. Чип регенерировали в конце каждого цикла путем двух введений 10 мкл 40 мМ HCl и одного введения 5 мМ NaOH. Контрольные циклы чередовали с пептидными циклами.
Степень ингибирования каждого пептида рассчитывали как процентное изменение единиц ответа, измеренных в точке формирования отчета, по сравнению со средним значением смежных контрольных циклов.
Уровень ингибирования каждого пептида альфа-синуклеина представлен на фигуре 5. Значительное ингибирование 5811 mFab в отношении либо мономера альфа-синуклеина, либо фибрилл, наблюдалось только для С-концевых пептидов AS113-122, AS115-124, AS117-126 и AS119-128, где уровни ингибирования любой формы α-синуклеина были очень похожи. Самый высокий уровень ингибирования наблюдался для пептида AS117-126 при 81% и 90% для связывания с мономером и фибриллой, соответственно. Общими остатками для четырех указанных выше пептидов являются остатки от 119 до 122, которые, соответственно, составляют часть эпитопа. Поскольку уровень ингибирования в случае пептидов AS113-122 и AS119-128 падает всего на величину от 2 до 5%, остатки от 115 до 118 и от 123 до 124 также должны составлять часть эпитопа.
Результат этого исследования позволил сделать предположение, что эпитоп антитела 5811 включает остатки от 115 до 124 (DMPVDPDNEA).
Сканирование аланина
Получали одноточечные мутанты аминокислоты альфа-синуклеина человека (His-меченого) и экспрессировали в системе Expi293 (Thermo Fisher Scientific) в соответствии с инструкцией фирмы-производителя. Остатки аланина размещали в положениях от 118 до 128, за исключением остатка 124, который уже являлся аланином и который заменяли на серин (таблица 4). Мутантные белки очищали от надосадочных жидкостей, полученных после центрифугирования (4200 об/мин, 2 часа), затем подвергали стерилизующей фильтрации (Stericup, Millipore). Надосадочные жидкости загружали в колонку HisTrap Excel (GE Healthcare), предварительно уравновешенную и промытую 25 мМ фосфатом натрия и 500 мМ NaCl. Связанный белок элюировали градиентом имидазола до 500 мМ в том же буфере. Фракции с представляющим интерес белком идентифицировали методом гель-электрофореза NuPage, объединяли, концентрировали с использованием Centriprep 10 кДа MWCO (Millipore) и проводили замену буфера на колонке PD-10 в PBS. Белковые фракции концентрировали с использованием концентрирующей центрифуги Ultracel 3KDa MWCO (Millipore). Концентрат пропускали через стерилизующий фильтр с размером пор 0,22 мкм (Millex GV, Millipore) и хранили при -20°C. Все мутанты экспрессировались в таком же количестве, что и альфа-синуклеин человека дикого типа (фигура 6А).
Таблица 4
Мутанты альфа-синуклеина человека повергали анализу на геле 4-12% Bis/Tris NuPage, используя 1 микрограмм на белок на полоску, и блотировали на мембрану из PVDF (iBlot mini stack, Thermo Fisher Scientific). Блот блокировали в блокирующем буфере (3% бычьего сывороточного альбумина, 0,1% Tween 20 в забуференном фосфатом физиологическом растворе, PBS) и инкубировали либо с антителом 5811 mFab, либо с антителом 5811 mIgG1. После инкубации в течение 1 часа при комнатной температуре, блот промывали с помощью 0,1% Tween в PBS. Блот инкубировали в течение 1 часа с конъюгатом вторичного идентифицирующего антитела против мышиного IgG Fc HRP (AB5879, Abcam) в блокирующем буфере, промывали и определяли хемилюминесценцию после добавления субстрата для вестерн-блоттинга ECL Western Blotting Substrate (Pierce).
Как показано на фигурах 6B и 6C, 3 мутанта, соответствующих D119A, N122A и Y125A альфа-синуклеина человека, не распознавались антителами 5811 mFab и 5811 mIgG1. Этот анализ позволяет предположить, что эти аминокислоты в альфа-синуклеине человека могут иметь важное значение для связывания антител 5811 mFab и 5811 mIgG1 с альфа-синуклеином человека.
Пример 4. Гуманизация антитела
Крысиное антитело 5811 гуманизировали путем прививки гипервариабельных участков (CDR) из V-области крысы на каркас V-области антитела человеческой зародышевой линии. Для восстановления активности антитела, ряд каркасных остатков из V-области крысы также сохраняли в гуманизированной последовательности. Эти остатки отбирали с использованием протокола, изложенного в патентном документе Adair et al., WO91/ 09967. Выравнивания последовательностей V-области антител крысы (донора) с последовательностями V-области зародышевой линии человека (акцептора) показаны на фигурах 7 и 8 вместе с конструированными гуманизированными последовательностями. Гипервариабельные участки (CDR), привитые от донора к акцепторной последовательности, определены по системе нумерации Кабата (Kabat et al., 1987), за исключением CDR-H1, где используется определение по комбинированной системе нумерации Chothia/Kabat (смотрите патентный документ Adair et al., 1991 Humanized antibodies. WO91/09967).
Гены, кодирующие ряд вариантов последовательностей V-областей тяжелой и легкой цепей, были спроектированы и сконструированы с использованием методики автоматического синтеза фирмы DNA2.0 Inc. Другие варианты V-областей тяжелой и легкой цепей создавали путем модификации генов VH и VK путем олигонуклеотид-направленного мутагенеза, включая, в некоторых случаях, мутации в CDR. Для транзиторной экспрессии в клетках млекопитающих, гены V-области гуманизированной легкой цепи клонировали в экспрессирующий вектор легкой цепи UCB pMhCK, который содержит ДНК, кодирующую константную область цепи Каппа человека (аллотип Km3). Гены V-области гуманизированной тяжелой цепи клонировали в человеческую UCB гамма-4 тяжелую цепь экспрессирующего вектора pMh-4PFL, который содержит ДНК, кодирующую константную область гамма-4 тяжелой цепи человека, со стабилизирующей шарнир мутацией S241P (Angal et al., Mol. Immunol. 1993, 30 (1): 105-8). Химерное антитело крысы-человека 5811 (содержащее SEQ ID NO: 9 и 10) также получали аналогичным образом. Совместная трансфекция полученных векторов тяжелой и легкой цепей в суспензионные культуры клеток Expi293TM осуществляли с использованием реагента для трансфекции ExpiFectamineTM 293 (A14525, ThermoFisher Scientific), и она давала экспрессию гуманизированных, рекомбинантных антител либо в человеческом формате IgG4P, либо в формате Fab-HIS.
Человеческая V-область IGKV1-39 плюс J-область JK1 (IMGT, http://www.imgt.org/) была выбрана в качестве акцептора для гипервариабельных участков (CDR) легкой цепи антитела 5811. Каркасные остатки легкой цепи в прививках gL5, gL8 и gL14 все происходили из гена человеческой зародышевой линии, за исключением остатка 71 (соответствующего SEQ ID No: 13), где был сохранен донорный остаток тирозина (Y71). Остаток 94 в CDRL3 прививки gL14 был мутирован из остатка глицина (G) в остаток аланина (A), таким образом модифицируя потенциальный сайт деамидирования аспарагина.
Человеческая V-область IGHV3-15 плюс JH3 J-область (IMGT, http://www.imgt.org/) была выбрана в качестве акцептора гипервариабельных участков (CDR) тяжелой цепи антитела 5811. Каркасные остатки тяжелой цепи в прививке gH4 все происходили из гена человеческой зародышевой линии, за исключением остатков 49 и 100 (соответствующих SEQ ID No: 25), где сохранялись донорные остатки аланина (A49) и аланина (A100), соответственно.
Экспрессировали варианты цепи гуманизированного антитело и их комбинации, и проводили оценку на предмет их активности относительно исходного антитела, их биофизических свойств и пригодности для последующей обработки.
Как показано в таблице 5, все прививки сохраняли аффинность, ту же самую или аналогичную аффинности исходного крысиного-человеческого антитела, к альфа-синуклеину в фибриллах.
Таблица 5
вариант
(1/мс)
(1/с)
пM
Пример 5. Иммуногистохимическое исследование
Иммуногистохимические исследования были выполнены фирмой Asterand Bioscience (Royston, United Kingdoms). Криосрезы (10 мкм) сначала подвергали процедуре демаскирования антигена с использованием прибора Dako PT Link и растворов для демаскирования EnVision FLEX Target Retrieval Solutions (pH 6) при 97°C в течение 20 минут с автоматическим нагреванием и охлаждением. Все последующие этапы инкубации проводили при комнатной температуре. Криосрезы сушили на воздухе в течение 30 минут, фиксировали в 4% параформальдегиде, приготовленном в 1X PBS, в течение 10 минут, промывали в промывочном буфере Dako EnVision™ FLEX (Dako) и затем загружали в систему для автоматического окрашивания Dako Autostainer Plus. Эндогенную активность пероксидазы блокировали путем инкубации срезов с блоком пероксидазы Dako (Dako) в течение 5 минут. Затем срезы дважды промывали 1X PBS и инкубировали с белковым блоком Dako CSA II (Dako) в течение 10 минут. Раствор белкового блока удаляли струей воздуха, и срезы инкубировали в течение 30 минут с крысиным-мышиным антителом IgG1 5811 (содержащим SEQ ID NO: 34 и 35), разведенным (0,05 мкг/мл) в разбавителе антител Dako (Dako). После инкубации, срезы дважды промывали 1X PBS, затем инкубировали с антимышиным субстратом Dako Flex polymer-HRP (Dako) в течение 20 минут, дважды промывали и затем инкубировали с субстратом диаминобензидина (Dako) в течение 10 минут. Хромогенную реакцию останавливали путем споласкивания предметных стекол дистиллированной водой. После хромогенеза, срезы удаляли из системы для автоматического окрашивания Dako Autostainer Plus и вручную докрашивали гематоксилином, обезвоживали последовательной обработкой этанолом, осветляли в трех сменах ксилола и заливали слоем среды для заливки DPX (Sigma-Aldrich). Получали цифровые изображения окрашенных срезов с использованием системы Aperio ScanScope AT Turbo (Leica Biosystems). Антитело 5811 mIgG1 тестировали на срезах мозга, полученных от пяти разных pS129-альфа-синуклеин-позитивных и трех разных pS129-альфа-синуклеин-негативных доноров (1 срез/донор). Антитело 5811 mIgG1 метило нейропиль и случайные подобные тельцам Леви структуры в височной коре и черной субстанции пациентов с болезнью Паркинсона (фигура 9А-Е). В тканях головного мозга в случае отсутствии болезни Паркинсона антитело 5811 mIgG1 метило нейропиль в височной коре, но в височной коре и черной субстанции не наблюдалось никаких подобных тельцам Леви структур (фигура 9F-H). Эти наблюдения позволяют предположить, что антитело 5811 mIgG1 связывается с нормальным альфа-синуклеином в нейропиле тканей головного мозга пациентов с болезнью Паркинсона и с отсутствием болезни Паркинсона, и, в то же время, оно связывается с патологическим альфа-синуклеином, присутствующим в тельцах Леви только у пациентов с болезнью Паркинсона.
Пример 6. Характеризация гуманизированных антител
Проводили испытания трех Ab5811 гуманизированных IgG4P антител (5811gL5gH4; 5811gL8gH4 5811gL14gH4; последовательности приведены в таблице 1) с целью оценки их биохимических и биофизических характеристик, в том числе термостабильности (Tm), экспериментальной изоэлектрической точки (pI), гидрофобности, растворимости (методом осаждения с помощью PEG), устойчивости к агрегации на границе раздела фаз воздух/жидкость и химической стабильности применительно к предрасположенности к деамидированию Asn93 на CDR-L3 (5811gL14gH4 имеет N(93)A мотив, и оба 5811gL8gH4 и gL5gH4 имеют N(93)G мотив).
Измерения термостабильности (Tm)
Определяли температуру плавления (Tm) или температуру в ключевой момент разворачивания белка с использованием анализа Thermofluor. В этом методе, использовали флуоресцентный краситель SYPRO orange для мониторинга процесса разворачивания белка путем связывания с гидрофобными областями, которые становятся открытыми при повышении температуры.
Реакционная смесь содержала 5 мкл 30x красителя SYPRO® Orange (Invitrogen TM), разбавленного с помощью PBS из 5000X исходного раствора, и 45 мкл исследуемого образца с концентрацией 0,12 мг/мл (в PBS pH 7,4). В четырех параллельных опытах распределяли приблизительно 10 мкл смеси в оптическом 384-луночном планшете для ПЦР, и запускали реакцию на система быстрого ПЦР в реальном времени 7900HT (Applied BiosystemsTM). Нагревательное устройство системы ПЦР устанавливали на диапазон температур от 20°C до 99°C со скоростью повышения температуры 1,1°C/мин. Изменения флуоресценции в лунках контролировали с помощью полупроводникового приемника света. Увеличение интенсивности изображали в виде графической зависимости, и угол наклона касательной к кривой перегиба (перегибов) использовали для расчета величины Tm, как описано ниже. Величину Tm для каждой молекулы антитела получали как в PBS, рН 7,4, так и в 50 мМ ацетата натрия/125 мМ хлорида натрия, рН 5,0, являющихся обычными буферами для предварительной подготовки.
Термическая стабильность для всех трех гуманизированных антител представлена в таблице 6. В PBS pH 7,4, наблюдался один переход и его относили к развертыванию как CH2, так и домена Fab. В 50 мМ ацетата натрия/125 мМ хлорида натрия рН 5,0, наблюдали два перехода. Более низкое значение Tm относили к разворачиванию домена CH2, а второй переход относили к домену Fab. Этот анализ показал, что антитела 5811gL8gH4 и 5811gL5gH4 имеют сравнимую термостабильность с антителом 5811gL14gH4, которое является только чуть менее термически стабильным.
Таблица 6
значение Tm(1)°C
значение Tm(2)°C
pH 7,4
pH 5
Экспериментальное определение изоэлектрической точки (pI)
Экспериментальную величину pI для 5811gL14gH4, 5811gL8gH4 и 5811gL5gH4 получали с использованием системы полной капиллярной визуализации cIEF iCE3 TM (Protein Simple). Образцы готовили путем смешивания следующих компонентов: 30 мкл образца (из исходного раствора 1 мг/мл в воде с чистотой квалификации "для ВЭЖХ"), 35 мкл 1% раствора метилцеллюлозы (Protein Simple), 4 мкл pH 3-10 амфолитов (Pharmalyte), 0,5 мкл 4,65 и 0,5 мкл 9,77 синтетических маркеров pI (ProteinSimple), 12,5 мкл 8М раствора мочевины (Sigma-Aldrich®). Для доведения конечного объема до 100 мкл использовали воду с чистотой квалификации "для ВЭЖХ". Перед анализом, смесь кратковременно встряхивали для обеспечения полного перемешивания и центрифугировали при 10000 об/мин в течение 3 минут для удаления пузырьков воздуха. Образцы фокусировали в течение 1 минуты при 1,5 кВ, затем в течение 5 минут при 3 кВ, и изображения капилляра A280 получали с использованием программного обеспечения ProteinSimple. Полученные электроферограммы сначала анализировали с использованием программного обеспечения iCE3, и проводили отнесения величин pI (линейная зависимость между маркерами pI). Затем откалиброванные электроферограммы интегрировали с использованием программного обеспечения Empower® (Waters).
Экспериментальная величина pI для всех молекул находилась в диапазоне 8,80-9,23 в основном при 9,09. Не было различий в распределении кислых/основных видов, которое было типичным для молекул IgG4P. Экспериментальные величины pI имели высокие значения и, следовательно, могли бы оказывать положительное влияние в процессе производства антител.
Хроматография с гидрофобным взаимодействием (HIC)
Методом хроматографии с гидрофобным взаимодействием (HIC) проводили оценку гуманизированных антител 5811gL14gH4, 5811gL8gH4 и 5811gL5gH4 по проявлению ими гидрофобности. При анализе методом HIC, антитела связываются с гидрофобной стационарной фазой в присутствии высоких концентраций полярных солей и десорбируются в подвижную фазу при уменьшении концентрации соли. Более длительное время удерживания соответствует более высокой гидрофобности.
Образцы антител с концентрацией 2 мг/мл разбавляли 1:2 с помощью 1,6 M сульфата аммония и PBS (pH 7,4). 5 мкг (10 мкл) образца вводили в колонку Dionex ProPac™ HIC-10 (100 мм x 4,6 мм), соединенную последовательно с системой Agilent 1200 binary HPLC с флуоресцентным детектором. Разделение контролировали по собственной флуоресценции (длины волн возбуждения и эмиссии, 280 нм и 340 нм соответственно).
Используя буфер A (0,8 M сульфат аммония 100 мM фосфат pH7.4) и буфер B (100 мM фосфат pH 7,4), проводили анализ образца с использованием градиентного элюирования следующим образом, (i) выдержка в течение 2 минут при 0% B, (ii) линейный градиент от 0 до 100% B в течение 30 минут (0,8 мл/минута) (iii) промывка колонные с помощью 100% B в течение 2 минут и повторное приведение в равновесие при 0% B в течение 10 минут и затем введение следующего образца. Температуру колонки поддерживали при 20°C. Проводили также анализ эталонов, характеризующихся низкой и высокой гидрофобностью, плюс контрольный образец в той же самой выполняемой последовательности с целью нормализации величин времен удерживания. Время удерживания (RT) образца нормализовали относительно эталонов с низкой и высокой гидрофобностью, используя следующие уравнение:
[(Образец (RT) - эталон с низкой гидрофобностью(RT) / Эталон с высокой гидрофобностью(RT) - эталон с низкой гидрофобностью(RT)] x 100
Все три антитела 5811gL14gH4, 5811gL8gH4 и 5811gL5gH4 характеризовались аналогичными нормализованными временами удерживания и аналогичной низкой гидрофобностью, то есть, элюирование из колонки происходило менее чем за 5 минут (смотрите таблицу 7). Низкая гидрофобность оказывает положительное влияние на стабильность (то есть, снижает агрегацию) в процессе производства.
Таблица 7
Измерение растворимости методом осаждения полиэтиленгликолем (PEG).
Коллоидальную устойчивость гуманизированных антител 5811gL14gH4, 5811gL8gH4 и 5811gL5gH4 анализировали с использованием метода осаждения полиэтиленгликолем (PEG). PEG использовали для количественного определения растворимости белка путем увеличения концентрации PEG (масса/объем) и измерения количества белка, остающегося в растворе. Этот анализ служил для имитации влияния высокой концентрации на растворимость без использования традиционных методов измерения концентраций.
Исследовали вызванное с помощью PEG осаждение гуманизированных антител 5811gL14gH4, 5811gL8gH4 и 5811gL5gH4 в присутствии 7-18% PEG-3350 в PBS pH 7,4 и 50 мМ ацетата натрия/125 мМ хлорида натрия pH 5,0. Для образцов антител заменяли буфер, используя диализ, и их концентрацию доводили до 2 мг/мл. Чтобы свести к минимуму неравновесное осаждение, при подготовке проб смешивали 2 х растворы белка и 2 х PEG при объемном соотношении 1:1. После перемешивания, образцы инкубировали при 37°С в течение 30 минут для повторного растворения неравновесных агрегатов. После инкубации в течение ночи при 20°C, образцы центрифугировали в течение 60 минут (4000 g). Аликвоты надосадочной жидкости переносили в половину объема 96-луночных оптических планшетов и измеряли поглощение при 280 нм, используя планшет-ридер BMG Labtech FLUOstar® Omega LVIS A280. Строили графическую зависимость концентраций от процентного содержания PEG, и определяли рассчитанную серединную точку (LogEC50) (полученную из подбора кривой нелинейной регрессии, с переменным наклоном) в качестве меры относительной коллоидной растворимости образцов. В этом анализе, более высокое значение LogEC50 соответствует более высокой коллоидальной устойчивости.
Как показано в таблице 8, не было обнаружено различий в коллоидальной устойчивости между тремя различными антителами. Более высокая коллоидальная устойчивость наблюдалась в ацетатном буфере с pH 5, что иллюстрируется более высоким значением logEC50.
Таблица 8
Влияние стресса на границе фаз воздух-жидкость (анализ на агрегацию)
Этот анализ используют для имитации стресса, которому могут подвергаться антитела в процессе их производства (например, при ультрафильтрации). Белки, такие как антитела, имеют тенденцию разворачиваться при воздействии условий на поверхности раздела фаз воздух-жидкость, на которой наличие гидрофобных поверхностей обусловлено гидрофобной средой (воздухом), а гидрофильных поверхностей обусловлено гидрофильной средой (водой). Перемешивание белковых растворов приводит к образованию обширной поверхности раздела фаз воздух-жидкость, что может инициировать агрегацию.
Образцы гуманизированных антител 5811gL14gH4, 5811gL8gH4 и 5811gL5gH4 в PBS pH 7,4 и 50 мМ ацетата натрия/125 мМ хлорида натрия pH 5,0 подвергали воздействию стресса, создаваемого путем интенсивного перемешивания с использованием термомиксера Eppendorf Thermomixer ComfortTM. Перед перемешиванием, концентрацию доводили до 1 мг/мл с использованием соответствующих коэффициентов экстинкции (1,41 оптическая плотность 280 нм, 1 мг/мл, длина пути 1 см) и оптической плотности при 280 нм, 340 нм и 595 нм, полученных с использованием спектрофотометра Varian Cary® 50-Bio для установления начала отсчета времени считывания. Аликвоту каждого образца помещали в конические пробирки Эппендорфа объемом 1,5 мл с крышками (4 × 250 мкл) и подвергали воздействию жестких условий для испытания на устойчивость к агрегации путем интенсивного перемешивания при 1400 об/мин при 25°C в течение 24 часов. Зависимую от времени агрегацию (помутнение) контролировали путем измерения образцов через 24 часа после перемешивания при 595 нм с использованием спектрофотометра Varian Cary™ 50-Bio. Для каждого образца строили графические зависимости средних величин поглощения от времени.
Молекула антитела 5811gL5gH4 характеризовалась более высокой устойчивостью к агрегации по сравнению с антителами 5811gL14gH4 и 5811gL8gH4. Все антитела характеризовалась более высокой устойчивостью к агрегации в PBS pH 7,4.
Химическая стабильность - исследование воздействия стресса на реакцию деамидирования
Проводили ускоренное исследование воздействия стресса на все три антитела 5811gL5gH4, 5811gL8gH4 и 5811gL14gH4 с целью определения предрасположенности к деамидированию одного идентифицированного в качестве потенциального сайта: Asn(93) в легкой цепи CDR3, где антитело 5811gL14gH4 имеет мотив Asn(93)Ala и оба антитела 5811gL8gH4 и gL5gH4 имеют мотив Asn(93)Gly.
Подвергали три антитела воздействию условий, по поводу которых было известно, что они способствуют деамидированию остатков Asn(N) (50 мМ Tris/125 мМ хлорид натрия, рН 8,0/37°С). Кроме того, также готовили образцы в 50 мМ ацетате натрия/125 мМ хлорид натрия рН 5,0 в качестве контрольного условия для оценки базального деамидирования перед началом воздействия стресса. Конечную концентрацию образца в каждом из буферов доводили до ~ 5 мг/мл, и затем образец разделяли на две аликвоты, где одну хранили при 4°С, а одну при 37°С в течение до 5 недель. Аликвоту удаляли немедленно (T0) и через 2 недели и 5 недель, и хранили при -20°C.
Базальное деамидирование в остатке Asn(93) измеряли на образцах, которые не подвергались воздействию стресса (50 мМ ацетат натрия/125 мМ хлорид натрия, pH 5/4°C), и определяли предрасположенность Asn (93) к деамидированию , используя образцы, подвергавшиеся воздействию стресса 2 недели/pH 8/37°С, генерируя триптический пептид, содержащий соответствующую последовательность. Вкратце, 80 мкг каждого образца восстанавливали с помощью DTT и денатурировали гидрохлоридом гуанидина при 37°С. Затем образцы подвергали алкилированию йодацетамидом при комнатной температуре, и затем проводили замену буфера на 7,5 мМ Tris/1,5 мМ CaCl2, рН 7,9 (центрифужные колонки ZebaTM 7 кДа MWCO, фирмы Thermo Fisher), и приблизительно 3 часа инкубировали с трипсином (1:23 по массе) при 37°С. Протеолиз останавливали путем добавления трифторуксусной кислоты до 0,1% по объему, и образцы хранили при -20°С. При оттаивании, образцы центрифугировали для удаления осадка.
Полученные пептиды разделяли и анализировали на колонке Waters BEH C18, соединенной с масс-спектрометром Thermo Fusion™, работающим в режиме химической ионизации с положительными ионами с использованием зависимого от данных метода фрагментации "орбитальная ловушка ионов-орбитальная ловушка ионов" с индуцированной столкновениями диссоциацией (CID). Данные LC-MS и MS2 анализировали с использованием программ Thermo Xcalibur™ и Pepfinder™. Анализировали соответствующий пептид (LC N93-K102) для оценки процента химической модификации.
Масс-спектрометрическое пептидное картирование показало, что базальный уровень деамидирования Asn (93) был ниже для антитела 5811gL14gH4 по сравнению с антителами 5811gL8gH4 и 5811gL5gH4. Это различие между молекулами не было неожиданным, так как было показано, что, несмотря на сложность предсказания наличия предрасположенности к деамидированию, остатки Asn (N), за которыми следует остаток Gly (G), характеризуются более высокой предрасположенностью к деамидированию, чем остатки, за которыми следует более объемный остаток Ala (A) (Robinson, NE et al., Proc. Natl. Acad. Sci. USA 2001, 98, 4367-4372).
Для всех трех антител, наблюдалась низкая степень деамидирования на Asn(93), а именно, 1,2% - 1,4% в неделю. Разность масс легкой цепи пептида N93-K102 в случае антител 5811gL5gH4 и 5811gL8gH4 включала модификацию -17 Да (вероятно промежуточное соединение сукцинимида) и +1 Да (полностью деамидированный продукт на Asn(93)), в то время как в случае антитела 5811gL14gH4the сукцинимид не обнаруживали (таблица 9).
Таблица 9
Суммарная степень деамидирования была низкой для всех антител, хотя более высокая гетерогенность наблюдалась в случае антител 5811gL5gH4 и 5811gL8gH4.
Пример 7. Исследование клеточной агрегации
Приготавливали в среде для экспрессии Freestyle 293 (Invitrogen TM) клетки линии HEK Freestyle 293F (суспензионную культуру клеток) при плотности 0,7×106 клеток/мл и культивировали до плотности 300×106 клеток/мл. Трансфекцию проводили в соответствии с инструкциями фирмы-производителя, и, вкратце, 600 мкг экспрессирующего вектора pcDNA3.1(+), включающего ген альфа-синуклеина, смешивали в 20 мл среды OptiMEM, одновременно 293-фектин разводили в среде OptiMEM (Invitrogen TM) и инкубировали в течение 5 минут при комнатной температуре. Добавляли разбавленную ДНК, и инкубировали при комнатной температуре в течение 20 минут, а затем добавляли по каплям на клетки (20 мл на колбу). Клетки инкубировали в течение 24 часов при 37°С, 125 об/мин, 8% СО2. Клетки либо сразу же использовали, либо замораживали при концентрации 5 миллионов клеток/мл в FBS+10% DMSO.
Если клетки были предварительно заморожены, то криопробирки оттаивали, и клетки ресуспендировали в среде Freestyle 293, центрифугировали при 500 g в течение 5 минут, надосадочную жидкость сбрасывали, и осадок ресуспендировали в среде Freestyle 293 (Life TechnologiesTM) + Pen/Strep (InvitrogenTM) при плотности 2 × 106 клеток/мл. В 384-луночный планшет (GrainerTM) добавляли 20 мкл суспензионной культуры клеток (всего около 40000 клеток/лунка). В каждую лунку добавляли 150 нМ фибрилл альфа-синуклеина человека (приготовленных, как описано в изобретении в примере 1), а затем для испытания добавляли антитела 5811gL5gH4 IgG4P, 5811 gL8gH4 IgG4P и 5811 gL14gH4 IgG4P (последовательности представлены таблице 1) в PBS (при различных концентрациях). Планшеты инкубировали при 37°C, 5% CO2, 95% влажности в инкубаторе для клеточных культур в течение 2 дней.
В конце второго дня, из всех лунок удаляли среду, и планшет промывали, оставляя в каждой лунке по 20 мкл. Добавляли в каждую лунку приблизительно 50 мкл PBS, и планшеты центрифугировали при 500 g в течение 5 минут. Надосадочную жидкость аспирировали из всех лунок с помощью устройства для промывки планшетов, оставляя в каждой лунке по 20 мкл среды. Добавляли Versene (LonzaTM) (50 мкл/лунку), и планшеты центрифугировали при 500 g в течение 5 минут, надосадочную жидкость аспирировали, оставляя в каждой лунке только по 20 мкл среды. В каждую лунку добавляли 20 мкл 8% формальдегида (16% раствор в воде, Life TechnologiesTM) + 2% Triton Х-100 (VWRTM) в PBS. Планшеты инкубировали при комнатной температуре в течение 15 минут, и затем добавляли 50 мкл буфера FACS, состоящего из HBSS (VWRTM без кальция и магния) + 2% FBS+2 мМ EDTA (Life TechnologiesTM). Планшеты центрифугировали при 2000 g в течение 1 минуты, и надосадочную жидкость аспирировали, оставляя в каждой лунке только по 20 мкл среды. В каждую лунку дополнительно добавляли 20 мкл буфера FACS с антителом против pSer129 альфа-синуклеина (AbCamTM), разведенным 1:300. Планшеты инкубировали в течение 1 часа при комнатной температуре, а затем в каждую лунку добавляли 50 мкл буфера FACS, и повторно центрифугировали при 2000 g в течение 1 минуты. Надосадочную жидкость удаляли, затем добавляли в каждую лунку разведенное 1:500 конъюгированное с Alexafluor647 анти-кроличье вторичное антитело (Life TechnologiesTM) и DAPI (Life TechnologiesTM). Планшеты инкубировали 1 час при комнатной температуре в темноте, и затем добавляли 50 мкл буфера FACS, и планшеты центрифугировали при 2000 g в течение 1 минуты. После промывки, добавляли дополнительное количество буфера FACS, и планшеты были подготовлены для считывания в проточном цитометре (BD FACS Canto II).
Данные проточной цитометрии (FACS) анализировали с использованием программного обеспечения FlowJo. Сначала, проводили селекцию во времени живых отдельных клеток с использованием прямого и бокового рассеяния. Затем, проводили селекцию во времени DAPI+ клеток, и их количество использовали в качестве меры числа живых ядросодержащих отдельных клеток. И наконец, проводили селекцию во времени 129-альфа-синуклеин-положительных (pSer129+) клеток. Процент pSer129+ клеток относительно всех DAPI+ клеток использовали в качестве меры агрегации. Данные нормализовали относительно лунок, обработанных только фибриллами и без антител, и выражены в процентах. Результаты представлены на фигуре 10, которые иллюстрируют способность испытуемых антител ингибировать агрегацию, индуцированную фибриллами альфа-синуклеина в клетках, экспрессирующих альфа-синуклеин. Эти данные подтверждают, что антитела по настоящему изобретению способны блокировать агрегацию, индуцированную фибриллами альфа-синуклеина с величиной IC50 приблизительно 5 нМ или ниже.
Пример 8. Исследование агрегации первичных нейронов
Гиппокампы от эмбрионов мышей линии E17 иссекали в буфере для диссекции (сбалансированный солевой раствор Хенкса (HBSS) без кальция и без магния, 0,6% D-(+)-глюкозы, 20 мМ Hepes). Затем буфер для диссекции удаляли и заменяли раствором для диссоциации (HBSS без кальция и без магния, 0,6% D-(+)-глюкозы, 20 мМ HEPES, 40 единиц измерения папаина, 1 мг/мл дезоксирибонуклеазы, 1 мМ L-цистеина, 0,5 мм ЭДТА). После 30 минут инкубации при 37°С, буфер для диссоциации удаляли, и гиппокампы промывали 3 раза средой для посева (среда Neurobasal™, добавка 2% B27, 1 мМ GlutaMAX, 2,5% FBS, 50 ед/мл пенициллин-стрептомицин). Тканевые сгустки растирали с помощью пипетки объемом 1 мл для получения суспензии отдельных клеток. Клетки разводили до соответствующей концентрации в среде для посева. В каждую лунку 384-луночного планшета, покрытого PDL, высевали около 15000 клеток. Затем клетки выдерживали в инкубаторе для клеточных культур при 37°С, 5% СО2, 95% влажности.
На следующий день, 80% среды заменяли на среду для посева без FBS [среда Neurobasal™, добавка 2% B27, 1 мМ GlutaMAX, 50 ед/мл пенициллин-стрептомицин). Через семь дней после посева, среду удаляли, оставляя в каждой лунке по 20 мкл. В каждую лунку добавляли 100 нМ фибрилл альфа-синуклеина человека (приготовленных, как описано в изобретении в примере 1), затем для испытания добавляли антитела 5811gL5gH4 IgG4P, 5811 gL8gH4 IgG4P и 5811 gL14gH4 IgG4P (последовательности приведены в таблице 1) в PBS (при различных концентрациях). Планшет инкубировали при 37°C, 5% CO2, 95% влажности в инкубаторе для клеточных культур в течение еще 7 дней. Через четырнадцать дней после посева, среду аспирировали из всех лунок, оставляя в лунках по 20 мкл. Каждую лунку промывали с помощью 80 мкл натрий-фосфатного буфера Дульбекко (DPBS). DPBS удаляли, и клетки инкубировали в 40 мкл фиксирующего буфера (DPBS с 4% параформальдегида) на лунку в течение 15 минут. Затем фиксирующий буфер удаляли, и клетки снова промывали с помощью 80 мкл DPBS. DPBS удаляли и заменяли на 40 мкл на лунку буфера для пермеабилизации (DPBS с 0,1% Triton X-100). Через 10 минут буфер для пермеабилизации удаляли, и клетки инкубировали в течение 1 часа в 40 мкл на лунку блокирующего буфера (PBS с 1% BSA и 0,1% Triton X-100). Затем блокирующий буфер удаляли и заменяли 40 мкл на лунку раствора первичного антитела (блокирующий буфер с 0,3% кроличьим антителом против фосфосерин 129-альфа-синуклеинова (AbCamTM ab51253). Раствор антитела инкубировали на клетках в течение 1 часа, затем три раза промывали (90 мкл/каждую, PBS). После последней промывки, PBS удаляли и заменяли на 40 мкл раствора вторичного антитела (0,1% конъюгированного с AlexaFluor647 анти-кроличьего антитела в PBS с 0,2% конъюгированного с AlexaFluor488 антитела против бета-III- тубулина). Раствор вторичного антитела инкубировали на клетках в течение 1 часа, затем удаляли и заменяли на 40 мкл PBS, содержащего 0,3% CellMask BlueTM. После 5 минут инкубации, лунки промывали 3 раза 80 мкл PBS, затем заполняли 50 мкл PBS на лунку, и герметизировали планшет с помощью прозрачной полимерной пленки.
Планшеты визуализировали с помощью устройства для визуализации планшетов Arrayscan (ThermoFisher ScientificTM). Изображения анализировали с использованием программного обеспечения HCS ScanTM той же фирмы-производителя. Плотность нейронов контролировали по сигналу бета-III-тубулина. Разреженные поля зрения или поля зрения с поврежденным слоем нейронных клеток, характеризующиеся значительным уменьшением поверхности сигнала бета-III-тубулина, подлежали исключению. И наконец, поверхность сигнала pSer129 альфа-синуклеина в поле зрения использовали для количественной оценки патологической агрегации альфа-синуклеина.
Считается, что фосфорилирование альфа-синуклеина в сайте S129 играет важную роль при контроле нормальных функций альфа-синуклеина, а также регуляции его агрегации, образования LBs и нейротоксичности. В нормальных состояниях, только небольшая доля альфа-синуклеина конститутивно фосфорилируется в сайте S129 в головном мозге (Fujiwara H, et al. (2002) Nat Cell Biol, 4, 160-164), тогда как в мозге пациентов, страдающих синуклеинопатией, было обнаружено резкое накопление pS129 (Kahle PJ, et al. (2000) Ann N Y Acad Sci, 920, 33-41); Okochi M, et al. (2000) J Biol Chem, 275, 390-397); Anderson JP, et al. (2006) J Biol Chem, 281, 29739-29752).
Данные нормализовали относительно лунок, обработанных только фибриллами и без антител, и выражали в процентах. Как показано на фигуре 11, все три антитела ингибировали агрегацию альфа-синуклеина, индуцированную фибриллами альфа-синуклеина, на первичных нейронах мыши, экспрессирующих эндогенные уровни альфа-синуклеина. Эти данные подтверждают, что антитела 5811gL5gH4 IgG4P, 5811gL8gH4 IgG4P и 5811gL14gH4 IgG4P были способны блокировать агрегацию, индуцированную фибриллами альфа-синуклеина, на первичных нейронах мыши с величиной IC50 ниже 5 нМ.
Пример 9. Оценка in vivo эффективности VR5811
Антитело 5811gL5gH4 IgG4P (включающее SEQ ID NO: 14 и SEQ ID NO: 26 и далее обозначаемое просто как VR5811) испытывали в трансгенной модели мышей, нокаутных по α-синуклеину, экспрессирующих альфа-синуклеин человека (далее называемое SNCA-OVX; Charles River, France).
Мышам SNCA-OVX вводили антитело VR5811 и мышиные предварительно сформированные фибриллы (PFF) (приготовленные, как описано в изобретении в примере 1). Антитело для отрицательного контроля и плацебо также вводили одновременно с антителом сравнения против альфа-синуклеина (антитело сравнения C-term Ab), которое связывает альфа-синуклеин на последних девяти C-концевых остатках. Такое антитело сравнения (которое имеет отличающиеся гипервариабельные участки (CDR) от антител по настоящему изобретению) демонстрировало характеристики связывания, которые были сопоставимы с характеристиками связывания антител по настоящему изобретению. Антитело сравнения C-term Ab обладает такой же аффинностью к альфа-синуклеину, как и антитела по настоящему изобретению, и аналогичными биофизическими свойствами. Оно было также эффективным при предотвращении агрегации альфа-синуклеин при проведении анализов на клетках (таблица 10).
Таблица 10
C-term Ab
Антитела предварительно инкубировали с PFF в течение 30 минут на шейкере при комнатной температуре, затем вводили непосредственно в головной мозг животных. Готовили смеси антитела/PFF в PBS в соотношении 1 мкг PFF/10 мкг антител. В качестве раствора плацебо использовали PBS при pH 7,4. Антитело вводили за 24 часа до комбинированного внутримозгового введения.
Затем антитела интраперитонеально вводили мышам в дозе 30 мг/кг. Вторую интраперитонеальную инъекцию делали через 7 дней после первой инъекции, и затем следовали этой же схеме лечения (одна интраперитонеальная инъекция в неделю в дозе 30 мг/кг для объема введения 10 мл/кг) в течение 11 недель, суммарно 12 инъекций, для мышей линии SNCA-OVX. Мышей случайным образом распределяли по группам лечения лекарственными средствами, а экспериментаторы были в неведении по поводу применяемых лекарственных средств.
Эксперименты на животных проводили в соответствии с руководящими принципами Европейской директивы European Directive 2010/63/EU и бельгийского законодательства. Комитет по этике проведения экспериментов на животных фирмы UCB Biopharma SPRL (LA1220040 и LA2220363) утвердил протокол эксперимента (ASYN-IC-PARKINSON-MO). Масса мышей составляла от 25 до 30 г, а возраст на момент хирургического вмешательства составлял 17 недель. Мышей содержали в клетках (4 мыши на клетку, Macrolon типа 2). Их содержали при поддержании цикла свет/темнота 12:12 с включением света в 06:00. Температуру поддерживали на уровне 20-21°С, а влажность составляла приблизительно 40%. Перед распределением по группам для испытаний, все животные имели свободный доступ к стандартному гранулированному корму и воде. До и после хирургического вмешательства, мышам предоставляли дополнительное питание и создавали более комфортные условия пребывания (Enviro-dri, Pharma Serv). За здоровьем животных ежедневно следил персонал по уходу за животными. Прилагались все усилия для минимизации страдания животных. Умерщвления проводили под наркозом.
Хирургическое вмешательство проводили под общим наркозом с использованием смеси 50 мг/кг кетамина (Nimatek, Eurovet Animal Health B.V.) и 0,5 мг/кг медетомидина (Domitor, Orion Corporation), вводимой интраперитонеально. Кроме того, для облегчения пробуждения после наркоза, вводили 2,5 мг/кг атипамезола (Antisedan, Orion Corporation). Рекомбинантные очищенные фибриллы (PFF) размораживали и обрабатывали ультразвуком при комнатной температуре (Qsonica 500-20 кГц; мощность 65%, 30 импульсов при 1 секунде включения, 1 секунде выключения в течение одной минуты). Затем PFF предварительно смешивали с антителами в течение 30 минут и встряхивали при комнатной температуре в течение 30 минут перед инъекцией в головной мозг. Проводили инфузию раствора (2 мкл) со скоростью 0,2 мкл/мин, и иглу оставляли на месте еще на 2,5 минуты перед ее медленным удалением. Проводили инъецирование с одной и той же стороны в правый стриатум при следующих координатах: AP = + 0,20 мм, ML = -2,00 мм, DV = -3,20 мм.
После анестезии, мышей перфузировали путем транскардиальной перфузии охлажденного льдом 0,9% PBS, содержащим 10 ед/мл гепарина, в течение 9 минут при скорости потока 6 мл/мин через левый желудочек. Правое предсердие вырезали для обеспечения оттока. Затем животных перфузировали путем перфузии охлажденного на льду 4% параформальдегида в PBS в течение 15 минут при скорости потока 6 мл/мин. Проводили фиксацию мозгов в течение ночи в PBS, содержащем 4% параформальдегида при 4°C (день 0). На следующее утро (день +1), 4% параформальдегид отбрасывали, а мозги промывали в холодном PBS и инкубировали в течение ночи. На следующий день (день +2), мозги промывали в PBS в течение, как минимум, 1 часа и переносили в PBS, содержащий 15% сахарозы, и хранили при 4°C до транспортировки.
Изготовление срезов мозга проводили в научно-исследовательской организации Neuroscience Associates (TN, USA). Сначала, мозги обрабатывали в течение ночи 20% глицерином и 2% диметилсульфоксидом для предотвращения артефактов, связанных с замерзанием, и внедряли в желатиновую матрицу с использованием технологии MultiBrain®. После отверждения, блоки быстро замораживали путем погружения в изопентан, охлажденный до -70°C с помощью измельченного сухого льда, и устанавливали на замораживающий столик скользящего микротома AO860. Блоки MultiBrain® секционировали в корональной плоскости с толщиной 40 мкм. Все срезы собирали последовательно в 24 контейнера на блок, которые заполняли раствором Antigen Preserve (49% PBS pH 7,0, 50% этиленгликоль, 1% поливинилпирролидон). Неокрашенные сразу срезы хранили при -20°C.
Свободноплавающие срезы окрашивали иммунохимическим методом с использованием антитела против pSer129альфа-синуклеина (мышиный альфа-синуклеин (pSer129), биотин - (Wako - 010-26481)), разведенного в соотношении 1:30000. Во всех инкубационных растворах из блокирующей сыворотки, в данном случае и в других случаях, использовали буферный раствор Tris-буферизированный физиологический раствор (TBS) с Triton X-100 в качестве среды; все споласкивания проводили с помощью TBS. Эндогенную пероксидазную активность блокировали путем обработки 0,9% перекисью водорода, а неспецифическое связывание блокировали с помощью 1,26% цельной нормальной сывороткой. После споласкивания, срезы окрашивали первичным антителом в течение ночи при комнатной температуре. Раствор носителя для пермеабилизации содержал 0,3% Triton X-100. После споласкивания, срезы инкубировали с комплексом авидин-биотин-HRP (набор Vectastain Elite ABC, фирмы Vector Laboratories, Burlingame, CA) в течение одного часа при комнатной температуре. После споласкивания, срезы обрабатывали тетрагидрохлоридом диаминобензидина (DAB) и 0,0015% перекисью водорода для создания визуально видимого продукта реакции, смонтированного на желатинизированных (заменяемых) предметных стеклах, высушенных на воздухе, слегка окрашенных тионином, обезвоженных в спиртах, осветленных в ксилоле и покрытых слоем среды Permount.
Количественное определение сигнала pSer129 альфа-синуклеина в поле видимости сигнала pSer129 альфа-синуклеина использовали для количественной оценки патологической агрегации альфа-синуклеина в ипсилатеральной стороне стриатума, коре, базолатеральной миндалине и черной субстанции. Границы исследуемых областей (ROI) определяли вручную, и проводили автоматическое количественное определение сигнала pSer129 альфа-синуклеина в различных областях мозга с помощью программного обеспечения VisioPharm 6 (VisioPharm). Для количественной оценки сигнала pSer129 альфа-синуклеина использовался линейный байесовский алгоритм, который позволяет получить величину площади сигнала (площадь маркера в мкм2). Площадь маркера количество отражает патологию pSer129 альфа-синуклеина, которая охватывает различные области мозга. Все количественные оценки получали слепым способом до конца проведения статистического анализа.
Анализ данных проводили по % площади маркера (то есть по соотношению между областью сигнала pSer129 в мкм2 и площадью исследуемой области в мкм2). Процент (%) площади маркера оценивали повторно для нескольких срезов мозга, расположенных ростро-каудально (стриатум: 13-14 срезов от брегмы +1,1 до -0,94; кора: 13-14 срезов от +1,1 до -0,94; базолатеральная миндалина: 6-10 срезов от -0,58 до -2,06; черная субстанция: 6-8 срезов от -2,54 до -3,88), и отдельно для каждого испытуемого объекта рассчитывали площадь под фармакокинетической кривой (AUC).
Для статистического анализа использовали метод однофакторного дисперсионного анализа (ANOVA). Метод ANOVA сопровождали множественными попарными сравнениями между средними значениями без корректировки с учетом множественности (** для р <0,01 и * для р <0,05). Данные преобразовывали в логарифмический вид для удовлетворения критериям нормальности и гомоскедастичности. Графики представляют средние геометрические значения нетрансформированных данных.
Как показано на фигуре 12, антитело VR5811 заметно снижало патологию альфа-синуклеина (то есть pSer129 сигнал альфа-синуклеина) в различных областях мозга, включая стриатум, кору головного мозга, миндалины и черную субстанцию, через 3 месяца после введения фибрилл (PFF) мышам линии SNCA-OVX.
Антитело для отрицательного контроля и антитело для сравнения C-term. не оказывали действия по уменьшению патологии альфа-синуклеина (сигнала pSer129 альфа-синуклеина) по сравнению с подвергаемыми лечению с помощью плацебо мышами, которым вводили те же самые фибриллы (PFF) человека.
На фигуре 13 показано количественное определение альфа-синуклеина, фосфорилированного по Ser129 в каждой из подвергавшихся анализу областей мозга мышей линии SNCA-OVX. Полученные результаты подтверждают, что VR5811 значимо (р <0,05) снижает патологию альфа-синуклеина в различных областях мозга, включая ипсилатеральную сторону стриатума, кору головного мозга и черную субстанцию, по сравнению с тремя контрольными группами (то есть плацебо, 101,4 и антитело для сравнения C-term Ab).
В результате, при проведении испытаний на мышах линии SNCA-OVX, группа, в которой вводили 5811, показала значимое снижение уровня pSer129 α-синуклеина в трех разных структурах, среди которых две являлись дистальными областями от места инъекции (кора головного мозга и черная субстанция).
Это подтверждает, что антитела, обладающие отличительные структурными признаки по настоящему изобретению, способны предотвращать in vivo появление альфа-синуклеина, фосфорилированного по Ser129. Кроме того, результаты показывают, что не все антитела, которые связывают альфа-синуклеин в C-концевой области, эффективны in vivo: антитело сравнения, которое связывается с C-концом альфа-синуклеина с высокой аффинностью и эффективно предотвращает агрегацию альфа-синуклеина в клеточных анализах, не смогло предотвратить фосфорилирование Ser129 in vivo.
Поэтому, антитело или его антигенсвязывающий фрагмент по настоящему изобретению может применяться для лечения альфа синуклеинoпатий, характеризующихся увеличением фосфорилирования Ser129, включая болезнь Паркинсона (PD) (в том числе идиопатические и наследственные формы болезни Паркинсона), деменцию с тельцами Леви (DLB), болезнь диффузных телец Леви (DLBD), вариант болезни Альцгеймера с тельцами Леви (LBVAD), смешанный тип болезни Альцгеймера и Паркинсона, множественную системную атрофию (MSA) и нейродегенерацию с накоплением железа в головном мозге типа 1 (NBIA-1).
Пример 10. Фармакокинетика антитела 5811 у мыши
Самцам мышей линии C57/Bl6 (n=3 на одно лекарственное средство) вводили внутривенно антитело 5811gL14gH4 IgG4P (5811) в форме разовой дозы 2 мг/кг.
Отбирали образцы крови (через 0,083, 1, 4, 8, 24, 72, 120, 168 и 336 часов после инъекций) из хвостовой вены мышей, и выдерживали образцы при комнатной температуре для свертывания крови. Выделяли сыворотку путем центрифугирования, и затем замораживали ее до проведения анализа. Количественное определение антитела 5811 проводили методом жидкостной хроматографии с тандемной масс-спектрометрией (LC-MS/MS). Образцы сыворотки для исследования размораживали и количественно оценивали по калибровочной кривой, приготовленной с использованием антитела 5811, введенного в разных концентрациях в контрольную сыворотку мыши. Перед введением образцов в систему LC-MS/MS, сыворотку денатурировали, восстанавливали и алкилировали, используя ацетонитрил (VWR, UK), TCEP-Трис(2-карбоксиэтил)фосфина гидрохлорид (Sigma, UK) и йодацетамид (Sigma, UK), соответственно. Затем алкилированные образцы растворяли в буфере 100 мМ бикарбоната аммония (Sigma, UK) и дигерировали в течение ночи с использованием фермента трипсина (Promega, UK) при 37°C. Дигерирование останавливали путем добавления муравьиной кислоты к образцам для понижения рН, а затем обессоливали с использованием планшета Waters HLB SPE. Полученный элюент концентрировали с использованием вакуумного испарителя. После того, как образцы были полностью высушены, их растворяли в смеси 95/5 : вода/ацетонитрил, содержащей 0,1% муравьиной кислоты, и вводили в систему LC-MS/MS. Анализ методом LC-MS/MS проводили на системе для высокоэффективной жидкостной хроматографии (HPLC) Schimadzu, соединенной с тройным квадрупольным масс-спектрометром AB Sciex QTrap 6500. Дигерированный образец вводили с помощью автоматического дозатора в колонку для высокоэффективной жидкостной хроматографией с обращенной фазой (колонка Phenomenex Aeris C18 peptide 100 × 2,1 мм, 2,6 мкм), в которой поддерживали температуру 50°C. В течение 6 минут применяли линейный градиент 5-70% ацетонитрила в 0,1% муравьиной кислоте, а затем увеличивали до 95% ацетонитрила в 0,1% муравьиной кислоте в течение 0,8 минут при расходе 0,6 мл/мин. Масс-спектрометр был настроен на проведение мониторинга множественных реакций для обнаружения множественных переходов пептидов 5811 при времени выдержки 50 миллисекунд на переход. Анализ данных проводили с использованием версии программного обеспечения Analyst 1.6.
Эти данные показывают, что антитело 5811 характеризуется очень хорошей фармакокинетикой (таблица 11 и фигура 14) у мышей, что следует из измеренных низких значений клиренса. По-видимому, они превосходят типичный диапазон, на который ссылаются в случае человеческих препаратов IgG, дозируемых мышам (3-16 мл/сутки/кг; Deng et al 2011 mabs 3: 1 61-66).
Таблица 11
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> ЮСБ Биофарма СРЛ
<120> Антитела
<130> PF0129-WO
<150> GB1720970.1
<151> 2017-12-15
<160> 47
<170> PatentIn version 3.5
<210> 1
<211> 11
<212> Белок
<213> Rattus norvegicus
<400> 1
Lys Ala Ser Gln Asn Ile Asn Lys Asn Leu Asp
1 5 10
<210> 2
<211> 7
<212> Белок
<213> Rattus norvegicus
<400> 2
Tyr Ala Asn Asn Leu Gln Thr
5
<210> 3
<211> 8
<212> Белок
<213> Rattus norvegicus
<400> 3
Tyr Gln Tyr Lys Asn Gly Trp Thr
1 5
<210> 4
<211> 10
<212> Белок
<213> Rattus norvegicus
<400> 4
Gly Phe Thr Phe Asn Asn Ala Ala Met Tyr
1 5 10
<210> 5
<211> 19
<212> Белок
<213> Rattus norvegicus
<400> 5
Arg Ile Arg Thr Lys Pro Asn Asn Tyr Ala Thr Ser Tyr Ala Asp Ser
1 5 10 15
Val Lys Gly
<210> 6
<211> 7
<212> Белок
<213> Rattus norvegicus
<400> 6
Asp Tyr Ser Arg Gly Asp Arg
5
<210> 7
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> CDR-L3, вариант 1
<400> 7
Tyr Gln Tyr Lys Asn Ala Trp Thr
1 5
<210> 8
<211> 140
<212> Белок
<213> Homo sapiens
<400> 8
Met Asp Val Phe Met Lys Gly Leu Ser Lys Ala Lys Glu Gly Val Val
1 5 10 15
Ala Ala Ala Glu Lys Thr Lys Gln Gly Val Ala Glu Ala Ala Gly Lys
20 25 30
Thr Lys Glu Gly Val Leu Tyr Val Gly Ser Lys Thr Lys Glu Gly Val
35 40 45
Val His Gly Val Ala Thr Val Ala Glu Lys Thr Lys Glu Gln Val Thr
50 55 60
Asn Val Gly Gly Ala Val Val Thr Gly Val Thr Ala Val Ala Gln Lys
65 70 75 80
Thr Val Glu Gly Ala Gly Ser Ile Ala Ala Ala Thr Gly Phe Val Lys
85 90 95
Lys Asp Gln Leu Gly Lys Asn Glu Glu Gly Ala Pro Gln Glu Gly Ile
100 105 110
Leu Glu Asp Met Pro Val Asp Pro Asp Asn Glu Ala Tyr Glu Met Pro
115 120 125
Ser Glu Glu Gly Tyr Gln Asp Tyr Glu Pro Glu Ala
130 135 140
<210> 9
<211> 106
<212> Белок
<213> Rattus norvegicus
<400> 9
Asn Ile Gln Met Thr Gln Ser Pro Pro Val Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Leu Ser Cys Lys Ala Ser Gln Asn Ile Asn Lys Asn
20 25 30
Leu Asp Trp Tyr Gln Gln Lys His Gly Glu Ala Pro Lys Leu Leu Met
35 40 45
Tyr Tyr Ala Asn Asn Leu Gln Thr Gly Ile Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Tyr Gln Tyr Lys Asn Gly Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 10
<211> 118
<212> Белок
<213> Rattus norvegicus
<400> 10
Glu Met Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Lys Glu
1 5 10 15
Ser Leu Lys Ile Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Asn Ala
20 25 30
Ala Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Arg Thr Lys Pro Asn Asn Tyr Ala Thr Ser Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Met
65 70 75 80
Val Tyr Leu Gln Met Asp Asn Leu Lys Ser Glu Asp Thr Ala Met Tyr
85 90 95
Tyr Cys Thr Ala Asp Tyr Ser Arg Gly Asp Arg Trp Gly Gln Gly Val
100 105 110
Met Val Thr Val Ser Ser
115
<210> 11
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<223> нуклеотиды VL крысы
<400> 11
aacatccaga tgacccagtc tcctccagtc ctgtctgcat ctgtgggaga cagagtcact 60
ctcagctgca aagcaagtca gaacattaat aagaacttag actggtatca gcaaaagcat 120
ggagaagctc caaaactcct gatgtattat gcaaacaatt tacaaacggg catcccatca 180
aggttcagtg gcagtggatc tggaacagat tacacgctca ccatcagcag cctgcagcct 240
gaagatgttg ccacatatta ctgctatcag tataagaatg ggtggacgtt cggtggaggc 300
accaagctgg aactgaaa 318
<210> 12
<211> 354
<212> ДНК
<213> Искусственная последовательность
<220>
<223> нуклеотиды VH крысы
<400> 12
gaaatgcagc tggtggagtc tggtggagga ttggtgcagc ctaaggagtc attgaaaatc 60
tcatgtgcag cctctggatt caccttcaat aatgctgcca tgtactgggt ccgccaggct 120
ccaggaaagg gtctggaatg ggttgctcgc ataagaacta aacctaataa ttatgcaaca 180
tcttatgctg attcagtgaa aggcagattc accatctcca gagatgattc aaaaagcatg 240
gtctacctac aaatggataa cttgaaaagt gaggacacag ccatgtatta ctgtacagca 300
gattactcca gaggtgacag gtggggccaa ggagtcatgg tcacagtctc gagc 354
<210> 13
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<223> V-область gL5 5811
<400> 13
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Ile Asn Lys Asn
20 25 30
Leu Asp Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Asn Asn Leu Gln Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Tyr Gln Tyr Lys Asn Gly Trp Thr
85 90 95
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 14
<211> 213
<212> Белок
<213> Искусственная последовательность
<220>
<223> легкая цепь gL5 5811
<400> 14
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Ile Asn Lys Asn
20 25 30
Leu Asp Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Asn Asn Leu Gln Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Tyr Gln Tyr Lys Asn Gly Trp Thr
85 90 95
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 15
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<223> нуклеотиды V-области gL5 5811
<400> 15
gacatccaga tgacccagag cccgagctcc ctgtccgcat cagtggggga tcgcgtgact 60
attacgtgca aagcctcgca gaacatcaac aagaacctcg actggtatca gcagaagcca 120
ggaaaggcgc ctaagctgct gatctactac gccaacaatc tccagaccgg cgtgccctcg 180
cggttctccg gatctgggtc cggtactgat tacaccctga ccattagctc ccttcaaccg 240
gaggacttcg ccacctatta ctgctaccag tacaagaacg gctggacttt tggacaaggc 300
accaaggtcg aaatcaag 318
<210> 16
<211> 639
<212> ДНК
<213> Искусственная последовательность
<220>
<223> нуклеотиды легкой цепи gL5 5811
<400> 16
gacatccaga tgacccagag cccgagctcc ctgtccgcat cagtggggga tcgcgtgact 60
attacgtgca aagcctcgca gaacatcaac aagaacctcg actggtatca gcagaagcca 120
ggaaaggcgc ctaagctgct gatctactac gccaacaatc tccagaccgg cgtgccctcg 180
cggttctccg gatctgggtc cggtactgat tacaccctga ccattagctc ccttcaaccg 240
gaggacttcg ccacctatta ctgctaccag tacaagaacg gctggacttt tggacaaggc 300
accaaggtcg aaatcaagcg tacggtggcc gctccctccg tgttcatctt cccaccctcc 360
gacgagcagc tgaagtccgg caccgcctcc gtcgtgtgcc tgctgaacaa cttctacccc 420
cgcgaggcca aggtgcagtg gaaggtggac aacgccctgc agtccggcaa ctcccaggaa 480
tccgtcaccg agcaggactc caaggacagc acctactccc tgtcctccac cctgaccctg 540
tccaaggccg actacgagaa gcacaaggtg tacgcctgcg aagtgaccca ccagggcctg 600
tccagccccg tgaccaagtc cttcaaccgg ggcgagtgc 639
<210> 17
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<223> V-область gL8 5811
<400> 17
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Ile Asn Lys Asn
20 25 30
Leu Asp Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Asn Asn Leu Gln Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Tyr Gln Tyr Lys Asn Gly Trp Thr
85 90 95
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 18
<211> 213
<212> Белок
<213> Искусственная последовательность
<220>
<223> легкая цепь gL8 5811
<400> 18
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Ile Asn Lys Asn
20 25 30
Leu Asp Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Asn Asn Leu Gln Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Tyr Gln Tyr Lys Asn Gly Trp Thr
85 90 95
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 19
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<223> нуклеотиды V-области 5811
<400> 19
gacatccaga tgacccagag cccgagctcc ctgtccgcat cagtggggga tcgcgtgact 60
attacgtgca aagcctcgca gaacatcaac aagaacctcg actggtatca gcagaagcca 120
ggaaaggcgc ctaagctgct gatctactac gccaacaatc tccagaccgg cgtgccctcg 180
cggttctccg gatctgggtc cggtactgat ttcaccctga ccattagctc ccttcaaccg 240
gaggacttcg ccacctatta ctgctaccag tacaagaacg gctggacttt tggacaaggc 300
accaaggtcg aaatcaag 318
<210> 20
<211> 639
<212> ДНК
<213> Искусственная последовательность
<220>
<223> нуклеотиды легкой цепи gL8 5811
<400> 20
gacatccaga tgacccagag cccgagctcc ctgtccgcat cagtggggga tcgcgtgact 60
attacgtgca aagcctcgca gaacatcaac aagaacctcg actggtatca gcagaagcca 120
ggaaaggcgc ctaagctgct gatctactac gccaacaatc tccagaccgg cgtgccctcg 180
cggttctccg gatctgggtc cggtactgat ttcaccctga ccattagctc ccttcaaccg 240
gaggacttcg ccacctatta ctgctaccag tacaagaacg gctggacttt tggacaaggc 300
accaaggtcg aaatcaagcg tacggtggcc gctccctccg tgttcatctt cccaccctcc 360
gacgagcagc tgaagtccgg caccgcctcc gtcgtgtgcc tgctgaacaa cttctacccc 420
cgcgaggcca aggtgcagtg gaaggtggac aacgccctgc agtccggcaa ctcccaggaa 480
tccgtcaccg agcaggactc caaggacagc acctactccc tgtcctccac cctgaccctg 540
tccaaggccg actacgagaa gcacaaggtg tacgcctgcg aagtgaccca ccagggcctg 600
tccagccccg tgaccaagtc cttcaaccgg ggcgagtgc 639
<210> 21
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<223> V-область gL14 5811
<400> 21
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Ile Asn Lys Asn
20 25 30
Leu Asp Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Asn Asn Leu Gln Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Tyr Gln Tyr Lys Asn Ala Trp Thr
85 90 95
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 22
<211> 213
<212> Белок
<213> Искусственная последовательность
<220>
<223> легкая цепь gL14 5811
<400> 22
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Ile Asn Lys Asn
20 25 30
Leu Asp Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Asn Asn Leu Gln Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Tyr Gln Tyr Lys Asn Ala Trp Thr
85 90 95
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 23
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<223> нуклеотиды V-области gL14 5811
<400> 23
gacatccaga tgacccagag cccgagctcc ctgtccgcat cagtggggga tcgcgtgact 60
attacgtgca aagcctcgca gaacatcaac aagaacctcg actggtatca gcagaagcca 120
ggaaaggcgc ctaagctgct gatctactac gccaacaatc tccagaccgg cgtgccctcg 180
cggttctccg gatctgggtc cggtactgat ttcaccctga ccattagctc ccttcaaccg 240
gaggacttcg ccacctatta ctgctaccag tacaagaacg cttggacttt tggacaaggc 300
accaaggtcg aaatcaag 318
<210> 24
<211> 639
<212> ДНК
<213> Искусственная последовательность
<220>
<223> нуклеотиды легкой цепи gL14 5811
<400> 24
gacatccaga tgacccagag cccgagctcc ctgtccgcat cagtggggga tcgcgtgact 60
attacgtgca aagcctcgca gaacatcaac aagaacctcg actggtatca gcagaagcca 120
ggaaaggcgc ctaagctgct gatctactac gccaacaatc tccagaccgg cgtgccctcg 180
cggttctccg gatctgggtc cggtactgat ttcaccctga ccattagctc ccttcaaccg 240
gaggacttcg ccacctatta ctgctaccag tacaagaacg cttggacttt tggacaaggc 300
accaaggtcg aaatcaagcg tacggtggcc gctccctccg tgttcatctt cccaccctcc 360
gacgagcagc tgaagtccgg caccgcctcc gtcgtgtgcc tgctgaacaa cttctacccc 420
cgcgaggcca aggtgcagtg gaaggtggac aacgccctgc agtccggcaa ctcccaggaa 480
tccgtcaccg agcaggactc caaggacagc acctactccc tgtcctccac cctgaccctg 540
tccaaggccg actacgagaa gcacaaggtg tacgcctgcg aagtgaccca ccagggcctg 600
tccagccccg tgaccaagtc cttcaaccgg ggcgagtgc 639
<210> 25
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> V-область gH4 5811
<400> 25
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Asn Ala
20 25 30
Ala Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Arg Thr Lys Pro Asn Asn Tyr Ala Thr Ser Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Thr Ala Asp Tyr Ser Arg Gly Asp Arg Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 26
<211> 445
<212> Белок
<213> Искусственная последовательность
<220>
<223> тяжелая цепь gH4 5811
<400> 26
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Asn Ala
20 25 30
Ala Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Arg Thr Lys Pro Asn Asn Tyr Ala Thr Ser Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Thr Ala Asp Tyr Ser Arg Gly Asp Arg Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys
210 215 220
Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu
225 230 235 240
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
245 250 255
Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln
260 265 270
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
275 280 285
Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu
290 295 300
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
305 310 315 320
Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys
325 330 335
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
340 345 350
Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
355 360 365
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
370 375 380
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
385 390 395 400
Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln
405 410 415
Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
420 425 430
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440 445
<210> 27
<211> 354
<212> ДНК
<213> Искусственная последовательность
<220>
<223> нуклотиды V-области gH4 5811
<400> 27
gaagtgcagc ttgtggagag cggaggtgga ctcgtgaagc ctggcggatc tctgcgcctg 60
tcctgcgccg cctcggggtt cacctttaac aatgccgcaa tgtattgggt cagacaggcc 120
ccgggaaagg gtttggaatg ggtggctagg attcggacta agcccaacaa ctacgcgacc 180
tcctacgccg atagcgtgaa gggcagattc accatctccc gggacgactc aaagaacacg 240
ctgtacctcc aaatgaactc cctgaaaacc gaggacaccg ccgtgtacta ctgcaccgcg 300
gactactccc ggggcgatcg ctggggacag gggactatgg tcactgtctc gagt 354
<210> 28
<211> 1335
<212> ДНК
<213> Искусственная последовательность
<220>
<223> нуклеотиды тяжелой цепи gH4 5811
<400> 28
gaagtgcagc ttgtggagag cggaggtgga ctcgtgaagc ctggcggatc tctgcgcctg 60
tcctgcgccg cctcggggtt cacctttaac aatgccgcaa tgtattgggt cagacaggcc 120
ccgggaaagg gtttggaatg ggtggctagg attcggacta agcccaacaa ctacgcgacc 180
tcctacgccg atagcgtgaa gggcagattc accatctccc gggacgactc aaagaacacg 240
ctgtacctcc aaatgaactc cctgaaaacc gaggacaccg ccgtgtacta ctgcaccgcg 300
gactactccc ggggcgatcg ctggggacag gggactatgg tcactgtctc gagtgcctcc 360
accaagggcc cctccgtgtt ccctctggcc ccttgctccc ggtccacctc cgagtctacc 420
gccgctctgg gctgcctggt caaggactac ttccccgagc ccgtgacagt gtcctggaac 480
tctggcgccc tgacctccgg cgtgcacacc ttccctgccg tgctgcagtc ctccggcctg 540
tactccctgt cctccgtcgt gaccgtgccc tcctccagcc tgggcaccaa gacctacacc 600
tgtaacgtgg accacaagcc ctccaacacc aaggtggaca agcgggtgga atctaagtac 660
ggccctccct gccccccctg ccctgcccct gaatttctgg gcggaccttc cgtgttcctg 720
ttccccccaa agcccaagga caccctgatg atctcccgga cccccgaagt gacctgcgtg 780
gtggtggacg tgtcccagga agatcccgag gtccagttca attggtacgt ggacggcgtg 840
gaagtgcaca atgccaagac caagcccaga gaggaacagt tcaactccac ctaccgggtg 900
gtgtccgtgc tgaccgtgct gcaccaggac tggctgaacg gcaaagagta caagtgcaag 960
gtgtccaaca agggcctgcc ctccagcatc gaaaagacca tctccaaggc caagggccag 1020
ccccgcgagc cccaggtgta caccctgccc cctagccagg aagagatgac caagaaccag 1080
gtgtccctga cctgtctggt caagggcttc tacccctccg acattgccgt ggaatgggag 1140
tccaacggcc agcccgagaa caactacaag accacccccc ctgtgctgga cagcgacggc 1200
tccttcttcc tgtactctcg gctgaccgtg gacaagtccc ggtggcagga aggcaacgtc 1260
ttctcctgct ccgtgatgca cgaggccctg cacaaccact acacccagaa gtccctgtcc 1320
ctgagcctgg gcaag 1335
<210> 29
<211> 107
<212> Белок
<213> Homo sapiens
<400> 29
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 30
<211> 116
<212> Белок
<213> Homo sapiens
<400> 30
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Lys Ser Lys Thr Asp Gly Gly Thr Thr Asp Tyr Ala Ala
50 55 60
Pro Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Thr Thr Asp Ala Phe Asp Val Trp Gly Gln Gly Thr Met Val
100 105 110
Thr Val Ser Ser
115
<210> 31
<211> 321
<212> ДНК
<213> Homo sapiens
<400> 31
gacatccaga tgacccagtc tccatcctcc ctgtctgcat ctgtaggaga cagagtcacc 60
atcacttgcc gggcaagtca gagcattagc agctatttaa attggtatca gcagaaacca 120
gggaaagccc ctaagctcct gatctatgct gcatccagtt tgcaaagtgg ggtcccatca 180
aggttcagtg gcagtggatc tgggacagat ttcactctca ccatcagcag tctgcaacct 240
gaagattttg caacttacta ctgtcaacag agttacagta ccccttggac gttcggccaa 300
gggaccaagg tggaaatcaa a 321
<210> 32
<211> 348
<212> ДНК
<213> Homo sapiens
<400> 32
gaggtgcagc tggtggagtc tgggggaggc ttggtaaagc ctggggggtc ccttagactc 60
tcctgtgcag cctctggatt cactttcagt aacgcctgga tgagctgggt ccgccaggct 120
ccagggaagg ggctggagtg ggttggccgt attaaaagca aaactgatgg tgggacaaca 180
gactacgctg cacccgtgaa aggcagattc accatctcaa gagatgattc aaaaaacacg 240
ctgtatctgc aaatgaacag cctgaaaacc gaggacacag ccgtgtatta ctgtaccaca 300
gatgcttttg atgtctgggg ccaagggaca atggtcaccg tctcttca 348
<210> 33
<211> 306
<212> Белок
<213> Искусственная последовательность
<220>
<223> а-syn кролик Fc человек 68-140
<400> 33
Gly Ala Val Val Thr Gly Val Thr Ala Val Ala Gln Lys Thr Val Glu
1 5 10 15
Gly Ala Gly Ser Ile Ala Ala Ala Thr Gly Phe Val Lys Lys Asp Gln
20 25 30
Leu Gly Lys Asn Glu Glu Gly Ala Pro Gln Glu Gly Ile Leu Glu Asp
35 40 45
Met Pro Val Asp Pro Asp Asn Glu Ala Tyr Glu Met Pro Ser Glu Glu
50 55 60
Gly Tyr Gln Asp Tyr Glu Pro Glu Ala Val Glu Lys Thr Val Ala Pro
65 70 75 80
Ser Thr Cys Ser Lys Pro Thr Cys Pro Pro Pro Glu Leu Leu Gly Gly
85 90 95
Pro Ser Val Phe Ile Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
100 105 110
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Asp
115 120 125
Asp Pro Glu Val Gln Phe Thr Trp Tyr Ile Asn Asn Glu Gln Val Arg
130 135 140
Thr Ala Arg Pro Pro Leu Arg Glu Gln Gln Phe Asn Ser Thr Ile Arg
145 150 155 160
Val Val Ser Thr Leu Pro Ile Ala His Gln Asp Trp Leu Arg Gly Lys
165 170 175
Glu Phe Lys Cys Lys Val His Asn Lys Ala Leu Pro Ala Pro Ile Glu
180 185 190
Lys Thr Ile Ser Lys Ala Arg Gly Gln Pro Leu Glu Pro Lys Val Tyr
195 200 205
Thr Met Gly Pro Pro Arg Glu Glu Leu Ser Ser Arg Ser Val Ser Leu
210 215 220
Thr Cys Met Ile Asn Gly Phe Tyr Pro Ser Asp Ile Ser Val Glu Trp
225 230 235 240
Glu Lys Asn Gly Lys Ala Glu Asp Asn Tyr Lys Thr Thr Pro Ala Val
245 250 255
Leu Asp Ser Asp Gly Ser Tyr Phe Leu Tyr Ser Lys Leu Ser Val Pro
260 265 270
Thr Ser Glu Trp Gln Arg Gly Asp Val Phe Thr Cys Ser Val Met His
275 280 285
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Ile Ser Arg Ser Pro
290 295 300
Gly Lys
305
<210> 34
<211> 213
<212> Белок
<213> Искусственная последовательность
<220>
<223> химерная легкая цепь крыса-мышь 5811
<400> 34
Asn Ile Gln Met Thr Gln Ser Pro Pro Val Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Leu Ser Cys Lys Ala Ser Gln Asn Ile Asn Lys Asn
20 25 30
Leu Asp Trp Tyr Gln Gln Lys His Gly Glu Ala Pro Lys Leu Leu Met
35 40 45
Tyr Tyr Ala Asn Asn Leu Gln Thr Gly Ile Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Tyr Gln Tyr Lys Asn Gly Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Leu Lys Arg Thr Asp Ala Ala Pro
100 105 110
Thr Val Ser Ile Phe Pro Pro Ser Ser Glu Gln Leu Thr Ser Gly Gly
115 120 125
Ala Ser Val Val Cys Phe Leu Asn Asn Phe Tyr Pro Lys Asp Ile Asn
130 135 140
Val Lys Trp Lys Ile Asp Gly Ser Glu Arg Gln Asn Gly Val Leu Asn
145 150 155 160
Ser Trp Thr Asp Gln Asp Ser Lys Asp Ser Thr Tyr Ser Met Ser Ser
165 170 175
Thr Leu Thr Leu Thr Lys Asp Glu Tyr Glu Arg His Asn Ser Tyr Thr
180 185 190
Cys Glu Ala Thr His Lys Thr Ser Thr Ser Pro Ile Val Lys Ser Phe
195 200 205
Asn Arg Asn Glu Cys
210
<210> 35
<211> 442
<212> Белок
<213> Искусственная последовательность
<220>
<223> химерная тяжелая цепь крыса-мышь 5811
<400> 35
Glu Met Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Lys Glu
1 5 10 15
Ser Leu Lys Ile Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Asn Ala
20 25 30
Ala Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Arg Thr Lys Pro Asn Asn Tyr Ala Thr Ser Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Met
65 70 75 80
Val Tyr Leu Gln Met Asp Asn Leu Lys Ser Glu Asp Thr Ala Met Tyr
85 90 95
Tyr Cys Thr Ala Asp Tyr Ser Arg Gly Asp Arg Trp Gly Gln Gly Val
100 105 110
Met Val Thr Val Ser Ser Ala Lys Thr Thr Pro Pro Ser Val Tyr Pro
115 120 125
Leu Ala Pro Gly Ser Ala Ala Gln Thr Asn Ser Met Val Thr Leu Gly
130 135 140
Cys Leu Val Lys Gly Tyr Phe Pro Glu Pro Val Thr Val Thr Trp Asn
145 150 155 160
Ser Gly Ser Leu Ser Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Asp Leu Tyr Thr Leu Ser Ser Ser Val Thr Val Pro Ser Ser Thr
180 185 190
Trp Pro Ser Glu Thr Val Thr Cys Asn Val Ala His Pro Ala Ser Ser
195 200 205
Thr Lys Val Asp Lys Lys Ile Val Pro Arg Asp Cys Gly Cys Lys Pro
210 215 220
Cys Ile Cys Thr Val Pro Glu Val Ser Ser Val Phe Ile Phe Pro Pro
225 230 235 240
Lys Pro Lys Asp Val Leu Thr Ile Thr Leu Thr Pro Lys Val Thr Cys
245 250 255
Val Val Val Asp Ile Ser Lys Asp Asp Pro Glu Val Gln Phe Ser Trp
260 265 270
Phe Val Asp Asp Val Glu Val His Thr Ala Gln Thr Gln Pro Arg Glu
275 280 285
Glu Gln Phe Asn Ser Thr Phe Arg Ser Val Ser Glu Leu Pro Ile Met
290 295 300
His Gln Asp Trp Leu Asn Gly Lys Glu Phe Lys Cys Arg Val Asn Ser
305 310 315 320
Ala Ala Phe Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly
325 330 335
Arg Pro Lys Ala Pro Gln Val Tyr Thr Ile Pro Pro Pro Lys Glu Gln
340 345 350
Met Ala Lys Asp Lys Val Ser Leu Thr Cys Met Ile Thr Asp Phe Phe
355 360 365
Pro Glu Asp Ile Thr Val Glu Trp Gln Trp Asn Gly Gln Pro Ala Glu
370 375 380
Asn Tyr Lys Asn Thr Gln Pro Ile Met Asp Thr Asp Gly Ser Tyr Phe
385 390 395 400
Val Tyr Ser Lys Leu Asn Val Gln Lys Ser Asn Trp Glu Ala Gly Asn
405 410 415
Thr Phe Thr Cys Ser Val Leu His Glu Gly Leu His Asn His His Thr
420 425 430
Glu Lys Ser Leu Ser His Ser Pro Gly Lys
435 440
<210> 36
<211> 230
<212> Белок
<213> Искусственная последовательность
<220>
<223> химерная тяжелая цепь крыса-мышь Fab-His 5811
<400> 36
Glu Met Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Lys Glu
1 5 10 15
Ser Leu Lys Ile Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Asn Ala
20 25 30
Ala Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Arg Thr Lys Pro Asn Asn Tyr Ala Thr Ser Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Met
65 70 75 80
Val Tyr Leu Gln Met Asp Asn Leu Lys Ser Glu Asp Thr Ala Met Tyr
85 90 95
Tyr Cys Thr Ala Asp Tyr Ser Arg Gly Asp Arg Trp Gly Gln Gly Val
100 105 110
Met Val Thr Val Ser Ser Ala Lys Thr Thr Pro Pro Ser Val Tyr Pro
115 120 125
Leu Ala Pro Gly Ser Ala Ala Gln Thr Asn Ser Met Val Thr Leu Gly
130 135 140
Cys Leu Val Lys Gly Tyr Phe Pro Glu Pro Val Thr Val Thr Trp Asn
145 150 155 160
Ser Gly Ser Leu Ser Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Asp Leu Tyr Thr Leu Ser Ser Ser Val Thr Val Pro Ser Ser Thr
180 185 190
Trp Pro Ser Glu Thr Val Thr Cys Asn Val Ala His Pro Ala Ser Ser
195 200 205
Thr Lys Val Asp Lys Lys Ile Val Pro Arg Asp Cys His His His His
210 215 220
His His His His His His
225 230
<210> 37
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> C-концевой фрагмент альфа-синклеина
<400> 37
Glu Glu Gly Ala Pro Gln Glu Gly Ile Leu
1 5 10
<210> 38
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> C-концевой фрагмент альфа-синклеина
<400> 38
Gln Glu Gly Ile Leu Glu Asp Met Pro Val
1 5 10
<210> 39
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> C-концевой фрагмент альфа-синклеина
<400> 39
Gly Ile Leu Glu Asp Met Pro Val Asp Pro
1 5 10
<210> 40
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> С-концевой фрагмент альфа-синклеина
<400> 40
Leu Glu Asp Met Pro Val Asp Pro Asp Asn
1 5 10
<210> 41
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> С-концевой фрагмент альфа-синклеина
<400> 41
Asp Met Pro Val Asp Pro Asp Asn Glu Ala
1 5 10
<210> 42
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> С-концевой фрагмент альфа-синклеина
<400> 42
Pro Val Asp Pro Asp Asn Glu Ala Tyr Glu
1 5 10
<210> 43
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> С-концевой фрагмент альфа-синклеина
<400> 43
Asp Pro Asp Asn Glu Ala Tyr Glu Met Pro
1 5 10
<210> 44
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> С-концевой фрагмент альфа-синклеина
<400> 44
Asp Asn Glu Ala Tyr Glu Met Pro Ser Glu
1 5 10
<210> 45
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> С-концевой фрагмент альфа-синклеина
<400> 45
Glu Ala Tyr Glu Met Pro Ser Glu Glu Gly
1 5 10
<210> 46
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> С-концевой фрагмент альфа-синклеина
<400> 46
Tyr Glu Met Pro Ser Glu Glu Gly Tyr Gln
1 5 10
<210> 47
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> С-концевой фрагмент альфа-синклеина
<400> 47
Met Pro Ser Glu Glu Gly Tyr Gln Asp Tyr
1 5 10
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Моноклональные антитела к альфа-синуклеину для предотвращения агрегации тау-белка | 2017 |
|
RU2760334C2 |
| АНТИТЕЛА ПРОТИВ АЛЬФА-СИНУКЛЕИНА | 2018 |
|
RU2787039C2 |
| СРЕДСТВА, ПУТИ ПРИМЕНЕНИЯ И СПОСОБЫ ЛЕЧЕНИЯ СИНУКЛЕОПАТИИ | 2016 |
|
RU2765303C2 |
| ГУМАНИЗИРОВАННЫЕ АНТИТЕЛА, КОТОРЫЕ РАСПОЗНАЮТ АЛЬФА-СИНУКЛЕИН | 2012 |
|
RU2743738C2 |
| АНТИТЕЛА ПРОТИВ ФАКТОРА СВЕРТЫВАНИЯ XI | 2017 |
|
RU2757314C2 |
| АНТИТЕЛО К АЛЬФА-РЕЦЕПТОРУ ИНТЕРЛЕЙКИНА-4 ЧЕЛОВЕКА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2807060C1 |
| КОМБИНАЦИИ АНТИТЕЛ К STAPHYLOCOCCUS AUREUS | 2019 |
|
RU2804815C2 |
| СПОСОБЫ ОБНАРУЖЕНИЯ ФОЛАТНОГО РЕЦЕПТОРА 1 В ОБРАЗЦЕ ПАЦИЕНТА | 2018 |
|
RU2759410C2 |
| ПРОКОАГУЛЯНТНЫЕ АНТИТЕЛА | 2018 |
|
RU2810094C2 |
| АНТИТЕЛО, НАПРАВЛЕННОЕ ПРОТИВ ФАКТОРА СЛИПАНИЯ А (ClfA) S. aureus | 2019 |
|
RU2818805C2 |
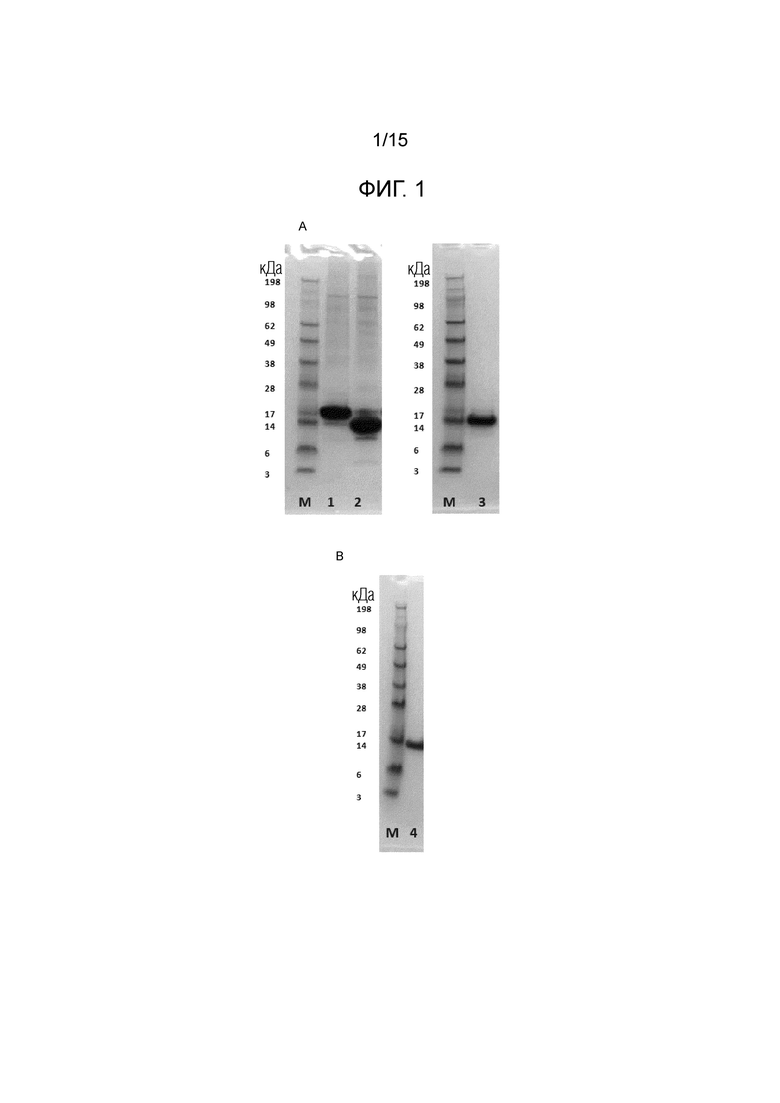
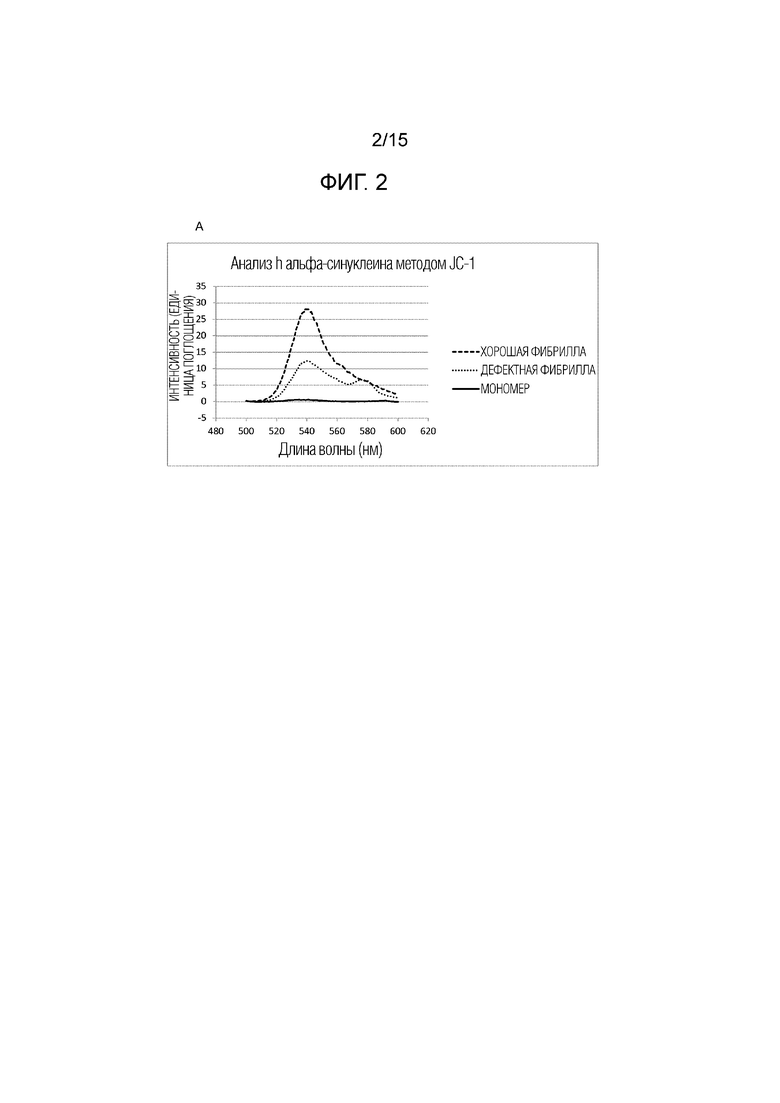
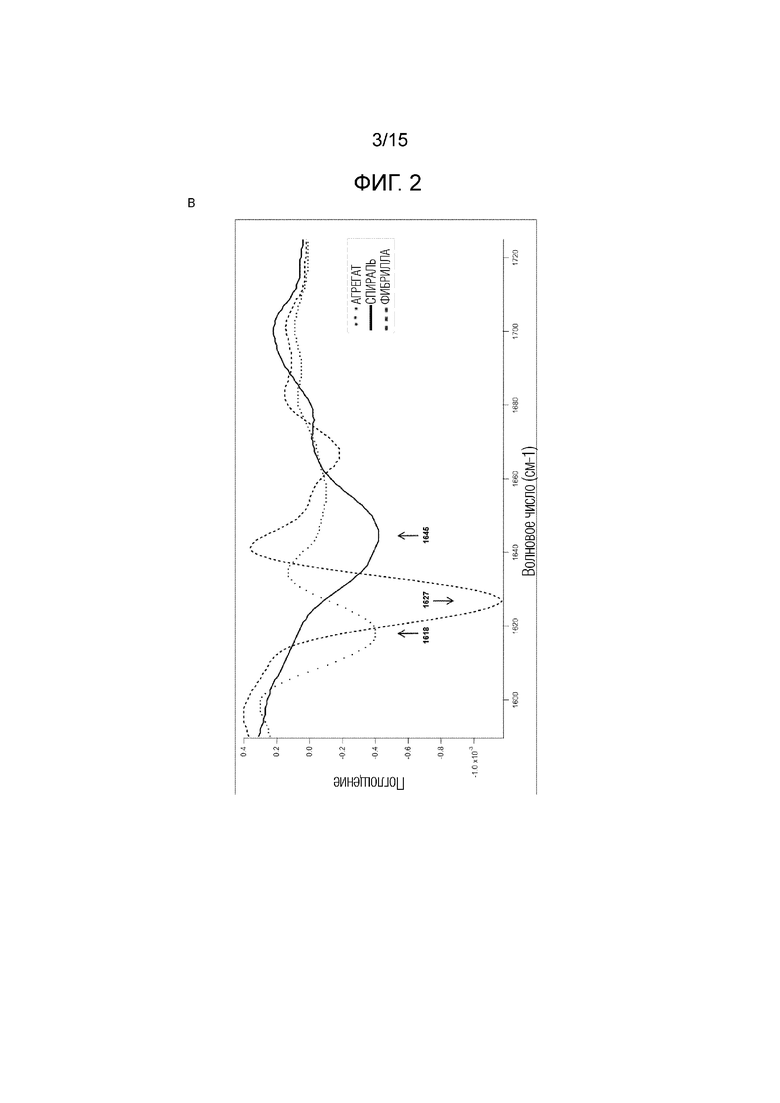
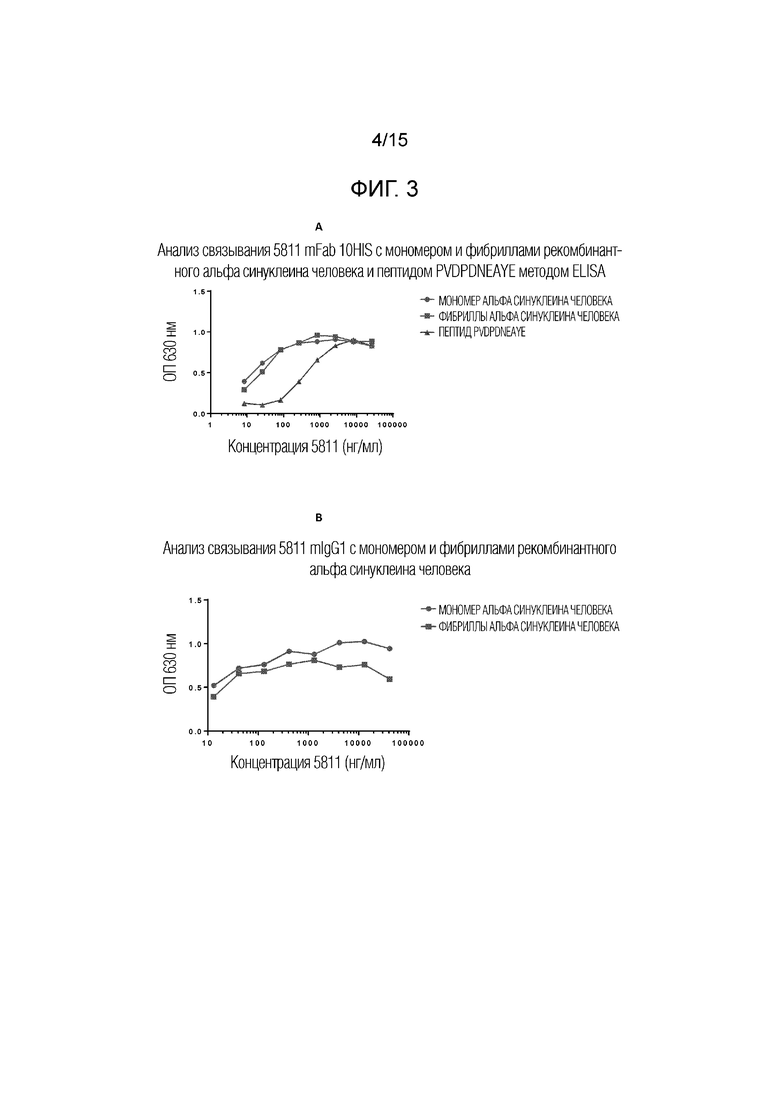
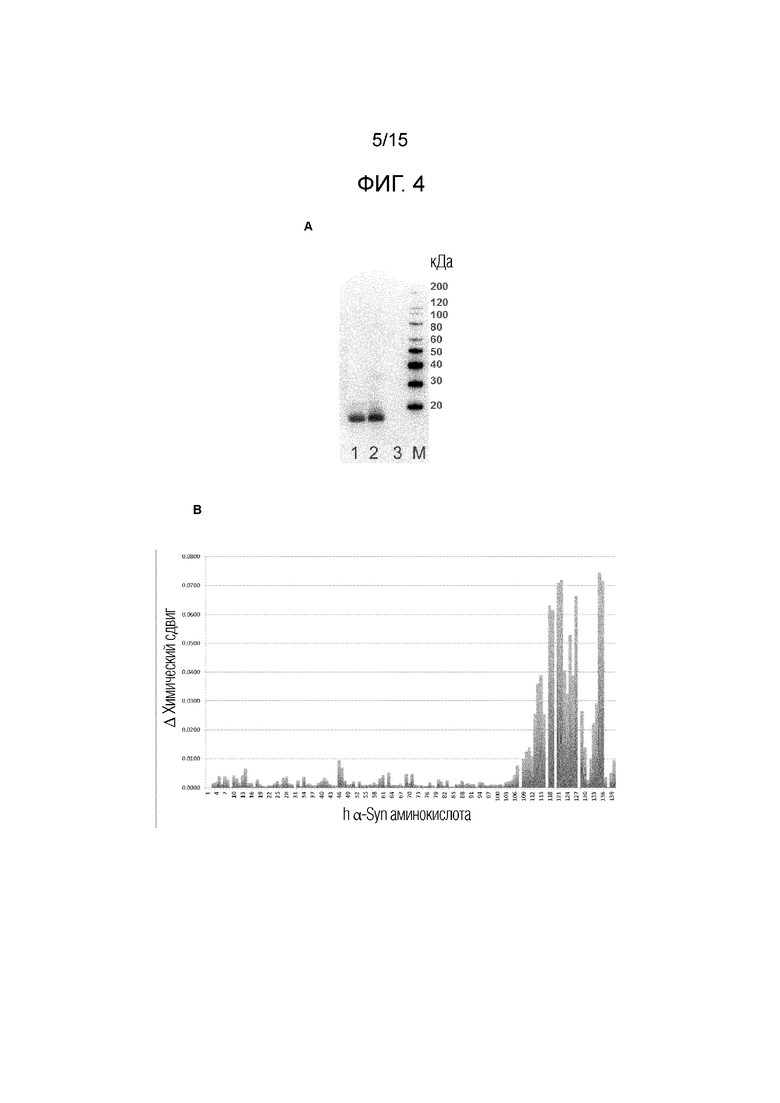
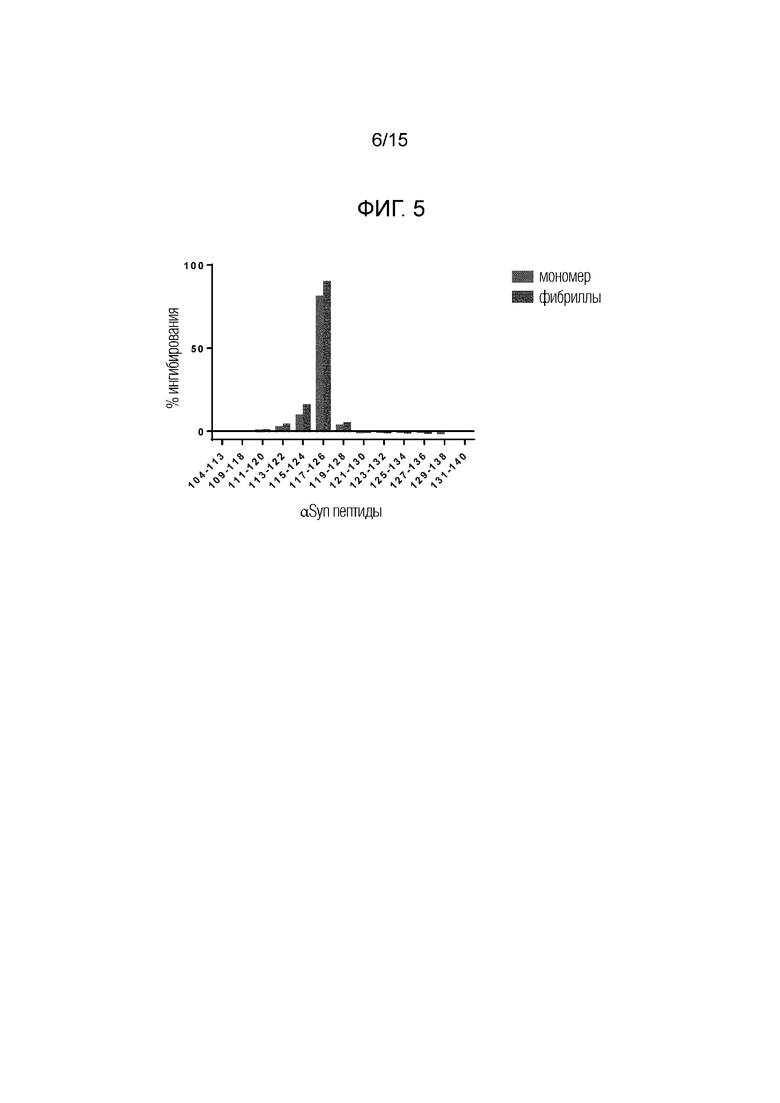
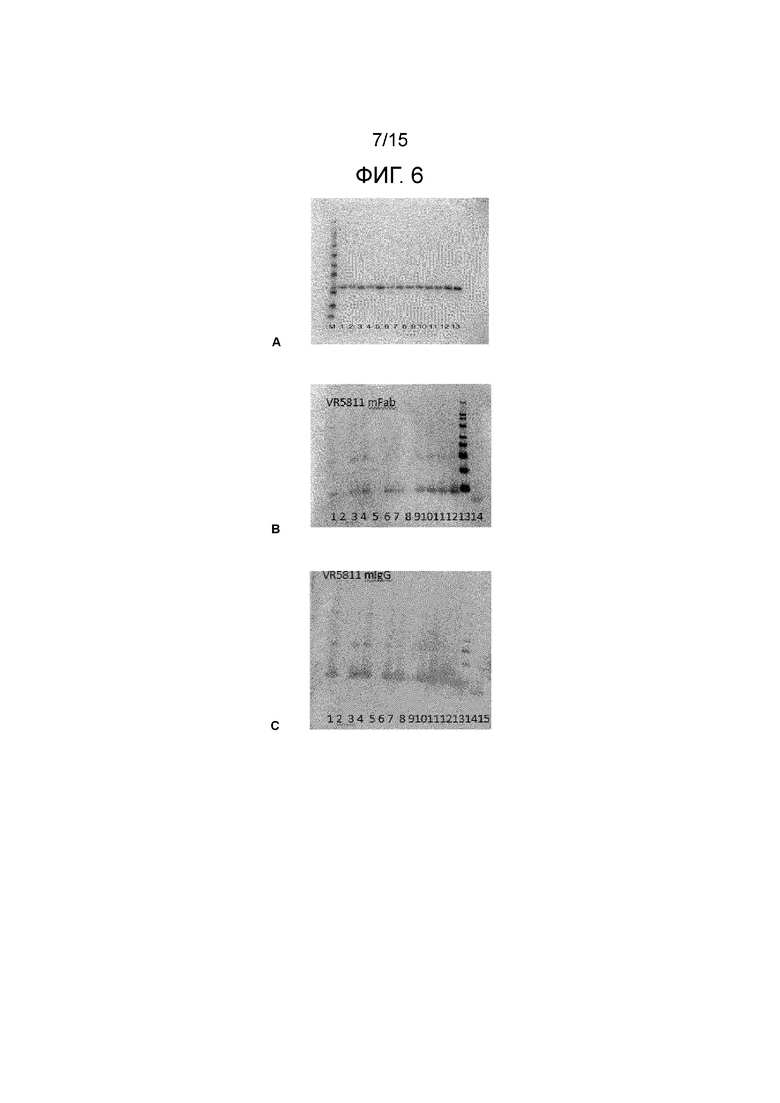
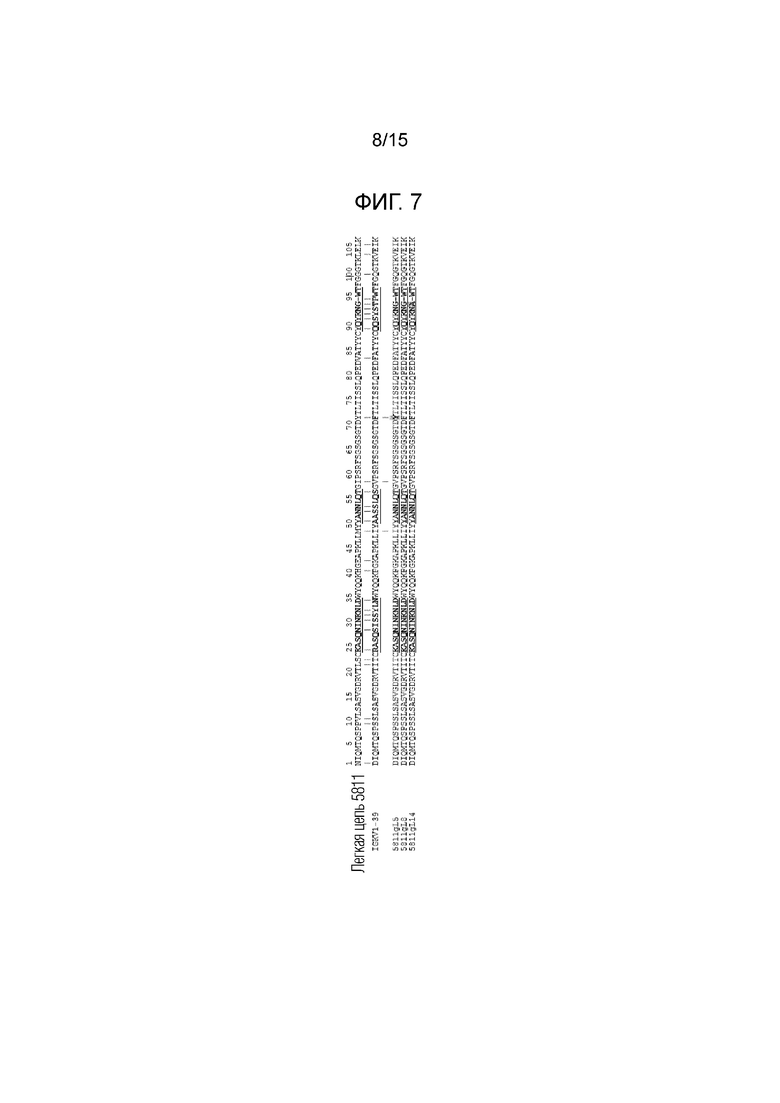


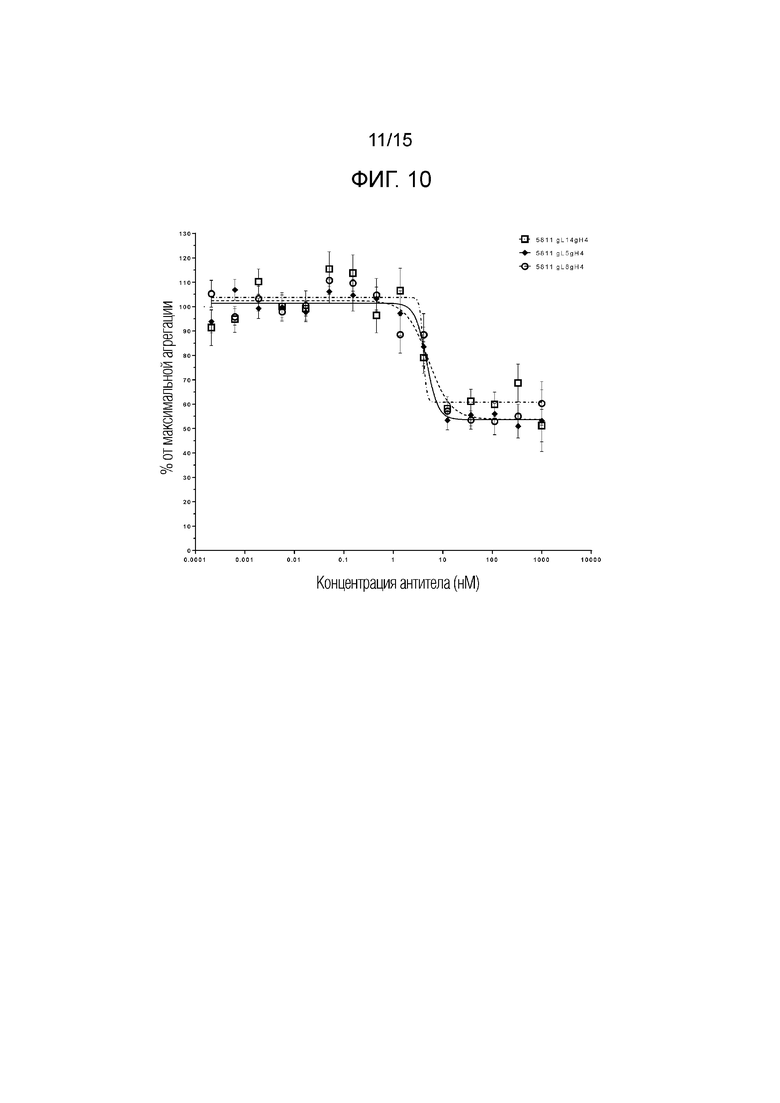
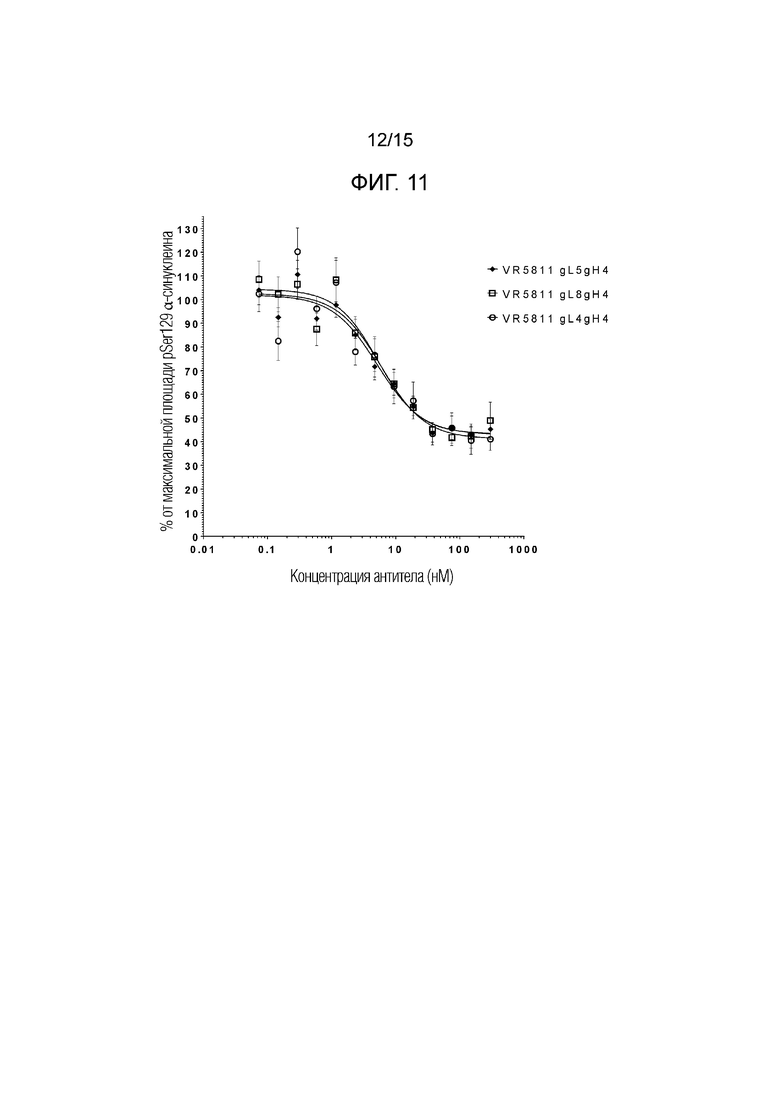

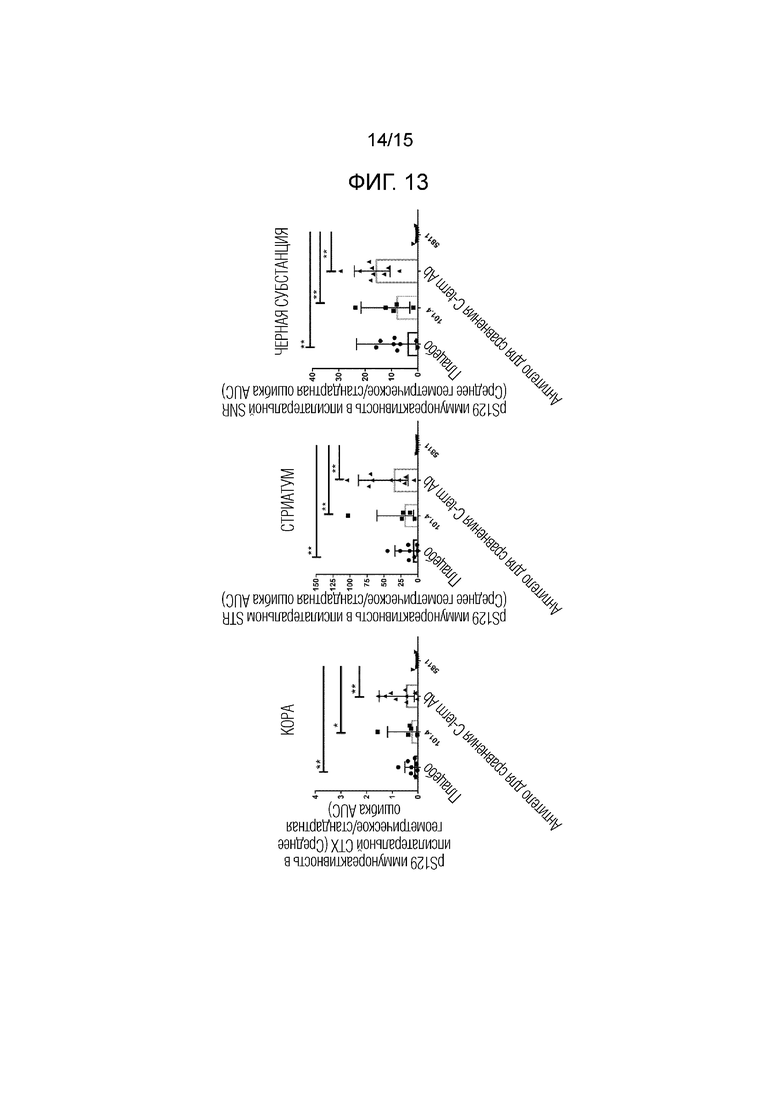
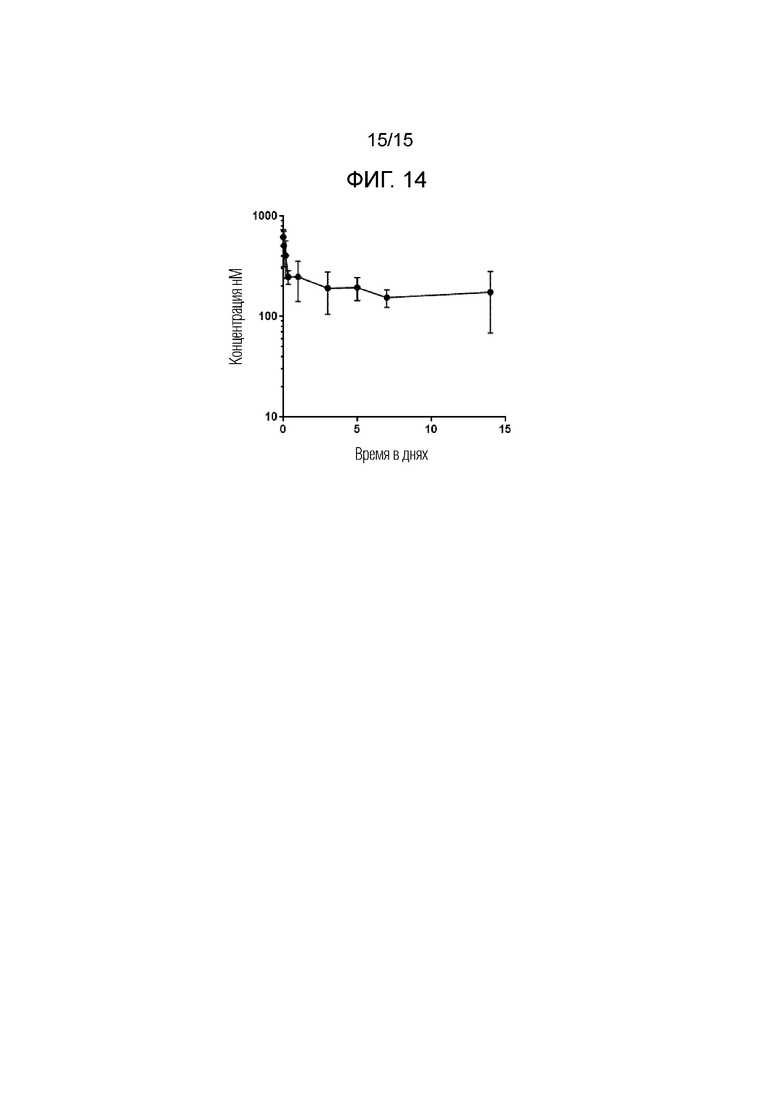
Группа изобретений относится к биотехнологии. В частности, к антителам и их фрагментам, способным связывать альфа-синуклеин в форме мономера и в фибриллах, предотвращая агрегацию альфа-синуклеина, индуцированную фибриллами альфа-синуклеина и способу их получения. Также представлены: выделенный полинуклеотид, кодирующий антитело или его антигенсвязывающий фрагмент, клонирующий вектор и вектор экспрессии, клетка-хозяин для получения антитела и способ лечения болезни Паркинсона (PD) у пациента, включающий введение указанному пациенту терапевтически эффективного количества антитела или его антигенсвязывающего фрагмента. Изобретение используется для лечения альфа-синуклеинoпатий, в том числе болезни Паркинсона. 8 н. и 15 з.п. ф-лы, 11 табл., 14 ил., 10 пр.
1. Антитело или его антигенсвязывающий фрагмент, которые связываются с альфа-синуклеином, где антитело или его антигенсвязывающий фрагмент содержит:
a. вариабельную область легкой цепи, содержащую CDR-L1 с SEQ ID NO:1; CDR-L2 c SEQ ID NO:2 и CDR-L3 c SEQ ID NO:3; и
b. вариабельную область тяжелой цепи, содержащую CDR-H1 с SEQ ID NO:4; CDR-H2 с SEQ ID NO:5 и CDR-H3 с SEQ ID NO:6.
2. Антитело или его антигенсвязывающий фрагмент, которые связываются с альфа-синуклеином, где антитело или его антигенсвязывающий фрагмент содержит:
a. вариабельную область легкой цепи, содержащую CDR-L1 с SEQ ID NO:1; CDR-L2 c SEQ ID NO:2 и CDR-L3 c SEQ ID NO:7; и
b. вариабельную область тяжелой цепи, содержащую CDR-H1 с SEQ ID NO:4; CDR-H2 с SEQ ID NO:5 и CDR-H3 с SEQ ID NO:6.
3. Антитело или его антигенсвязывающий фрагмент по п.1 или 2, где антитело или его антигенсвязывающий фрагмент связывает два или более аминокислотных остатков альфа-синуклеина между положениями 113 и 129 последовательности SEQ ID NO:8,
где антитело или его антигенсвязывающий фрагмент связывает по меньшей мере аминокислотные остатки D119, N122 и Y125 в последовательности SEQ ID NO:8.
4. Антитело или его антигенсвязывающий фрагмент по любому из предшествующих пунктов, где антитело или антигенсвязывающий фрагмент предотвращает агрегацию альфа-синуклеина, индуцированную фибриллами альфа-синуклеина.
5. Антитело или его антигенсвязывающий фрагмент по любому из предшествующих пунктов, где антитело или его антигенсвязывающий фрагмент способны связывать альфа-синуклеин в форме мономера и в форме фибрилл.
6. Антитело или его антигенсвязывающий фрагмент по любому из предшествующих пунктов, которые имеют более высокую аффинность связывания в отношении альфа-синуклеина в форме фибрилл по сравнению с альфа-синуклеином в форме мономера, характеризующуюся константой диссоциации (KD), которая по меньшей мере в 10 раз выше в отношении мономерного альфа-синуклеина, чем в отношении альфа-синуклеина в форме фибрилл.
7. Антитело или его антигенсвязывающий фрагмент по любому из предшествующих пунктов, которые имеют величину (KD) для альфа-синуклеин в фибриллах 60 пM или менее.
8. Антитело или его антигенсвязывающий фрагмент по любому из предшествующих пунктов, где антитело представляет собой химерное, гуманизированное или человеческое антитело.
9. Антитело или его антигенсвязывающий фрагмент по любому из предшествующих пунктов, где антитело представляет собой полноразмерное антитело.
10. Антитело или его антигенсвязывающий фрагмент по п.9, где полноразмерное антитело выбрано из IgG1, IgG4 или IgG4P.
11. Антитело или его антигенсвязывающий фрагмент по любому из предшествующих пунктов, где антигенсвязывающий фрагмент выбран из Fab, Fab’, F(ab’)2, scFv, dAb или VHH.
12. Антитело или его антигенсвязывающий фрагмент по любому из предшествующих пунктов, где антитело или его антигенсвязывающий фрагмент содержит:
a. вариабельную область легкой цепи с SEQ ID NO:13, и
вариабельную область тяжелой цепи с SEQ ID NO:25; или
b. вариабельную область легкой цепи с SEQ ID NO:17, и
вариабельную область тяжелой цепи с SEQ ID NO:25; или
c. вариабельную область легкой цепи с SEQ ID NO:21, и
вариабельную область тяжелой цепи с SEQ ID NO:25.
13. Антитело или его антигенсвязывающий фрагмент по любому из пп.1-11, где антитело или его антигенсвязывающий фрагмент содержит:
a. легкую цепь с SEQ ID NO:14, и
тяжелую цепь с SEQ ID NO:26; или
b. легкую цепь с SEQ ID NO:18, и
тяжелую цепь с SEQ ID NO:26; или
c. легкую цепь с SEQ ID NO:22, и
тяжелую цепь с SEQ ID NO:26.
14. Выделенный полинуклеотид, кодирующий антитело или его антигенсвязывающий фрагмент по любому из пп.1-13.
15. Выделенный полинуклеотид по п.14, где полинуклеотид кодирует:
a. вариабельную область легкой цепи, где полинуклеотид:
i. по меньшей мере, на 90% идентичен последовательности SEQ ID NO:15, 19 или 23; или
ii. содержит SEQ ID NO:15 или 19 или 23; или
iii. состоит в основном из SEQ ID NO:15, 19 или 23; или
b. вариабельную область тяжелой цепи, где полинуклеотид:
i. по меньшей мере, на 90% идентичен последовательности SEQ ID NO:27; или
ii. содержит SEQ ID NO:27; или
iii. состоит в основном из SEQ ID NO:27; или
c. легкую цепь, где полинуклеотид:
i. по меньшей мере, на 90% идентичен последовательности SEQ ID NO:16, 20 или 24; или
ii. содержит SEQ ID NO:16, 20 или 24; или
iii. состоит в основном из SEQ ID NO:16, 20 или 24;
d. тяжелую цепь, где полинуклеотид:
i. по меньшей мере, на 90% идентичен последовательности SEQ ID NO:28; или
ii. содержит SEQ ID NO:28; или
iii. состоит в основном из SEQ ID NO:28.
16. Клонирующий вектор, содержащий один или более полинуклеотидов по любому из пп.14, 15.
17. Вектор экспрессии, содержащий один или более полинуклеотидов по любому из пп.14, 15.
18. Клетка-хозяин для получения антитела по любому из пп.1-13, содержащая:
a. один или более полинуклеотидов по любому из пп.14 или 15 или
b. один или более векторов экспрессии по п.16 или 17.
19. Способ получения антитела или его антигенсвязывающего фрагмента по любому из пп.1-13, включающий
культивирование клетки-хозяина по п.18 в подходящих условиях для получения антитела или его антигенсвязывающего фрагмента и
выделение антитела или его антигенсвязывающего фрагмента.
20. Антитело или его антигенсвязывающий фрагмент по любому из пп.1-13 для применения в терапии.
21. Антитело или его антигенсвязывающий фрагмент по любому из пп.1-13 для применения в терапии болезни Паркинсона (PD).
22. Способ лечения болезни Паркинсона (PD) у пациента, включающий введение указанному пациенту терапевтически эффективного количества антитела или его антигенсвязывающего фрагмента по любому из пп.1-13.
23. Антитело или его антигенсвязывающий фрагмент по любому из пп.1-13 для применения в диагностике болезни Паркинсона.
| EP 3067066 A1, 14.09.2016 | |||
| WO 2011104696 A1, 01.09.2011 | |||
| US 2014241984 A1, 28.08.2014 | |||
| WO 2007012061 A2, 25.01.2007 | |||
| WO 2004041067 A2, 21.05.2004 | |||
| АНТИТЕЛА, СВЯЗЫВАЮЩИЕСЯ С ПРОТОФИБРИЛЛАМИ, И ИХ ПРИМЕНЕНИЕ В МЕТОДАХ ТЕРАПИИ И ДИАГНОСТИКИ БОЛЕЗНИ ПАРКИНСОНА, ДЕМЕНЦИИ, АССОЦИИРОВАННОЙ С ОБРАЗОВАНИЕМ ДИФФУЗНЫХ ТЕЛЕЦ ЛЕВИ, И ДРУГИХ АЛЬФА-СИНУКЛЕИНОПАТИЙ | 2011 |
|
RU2555526C2 |
Авторы
Даты
2023-06-22—Публикация
2018-12-13—Подача